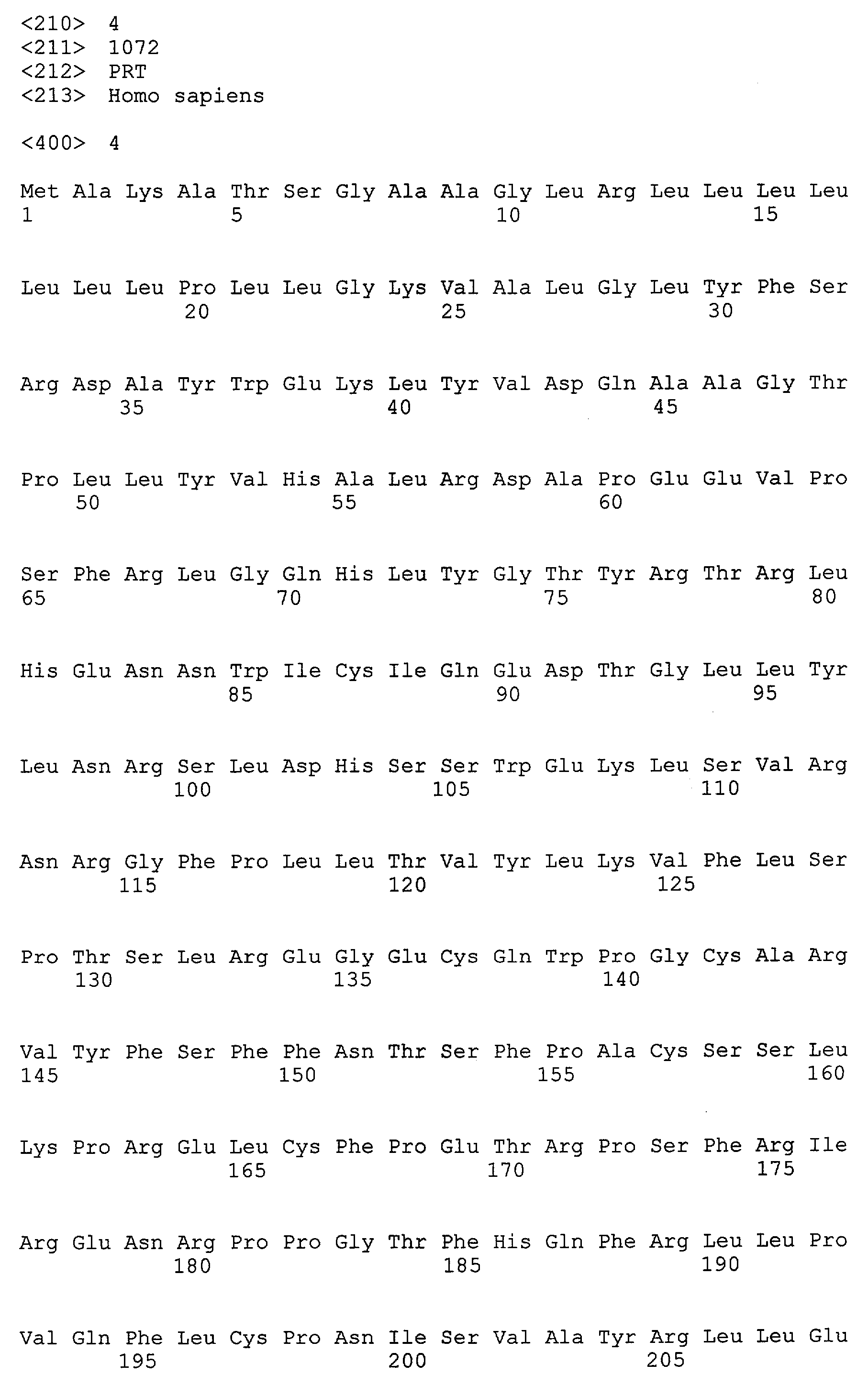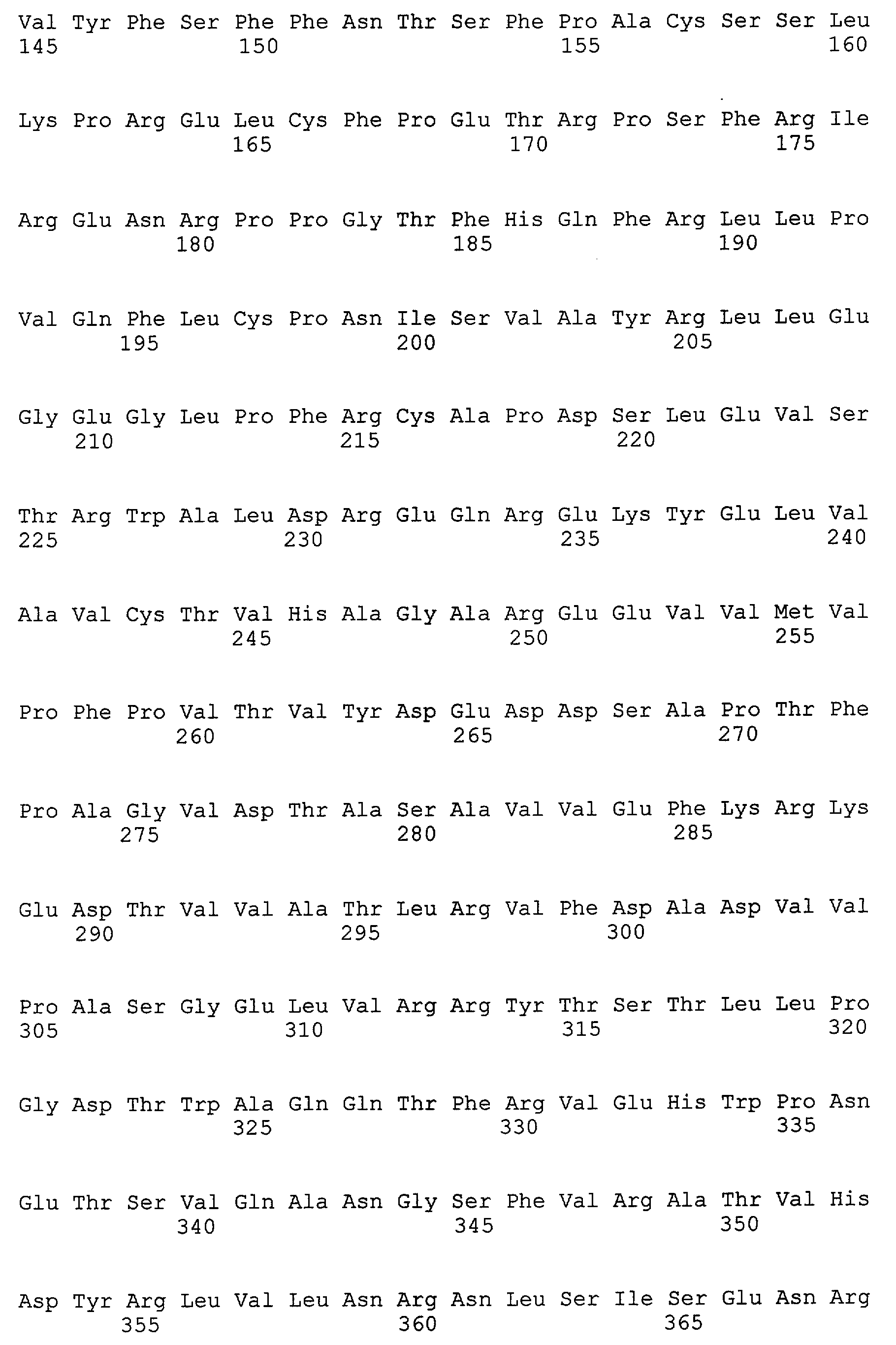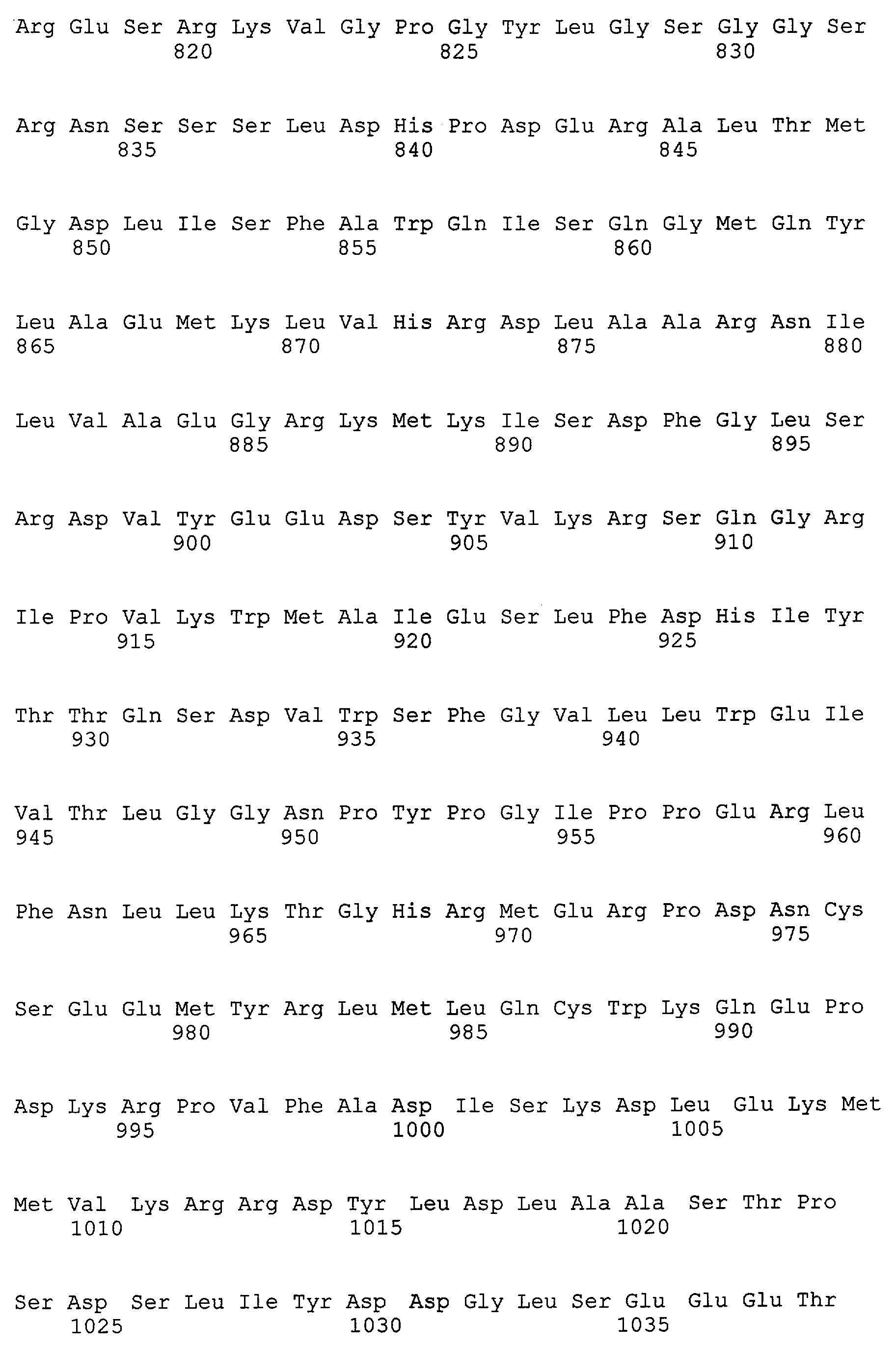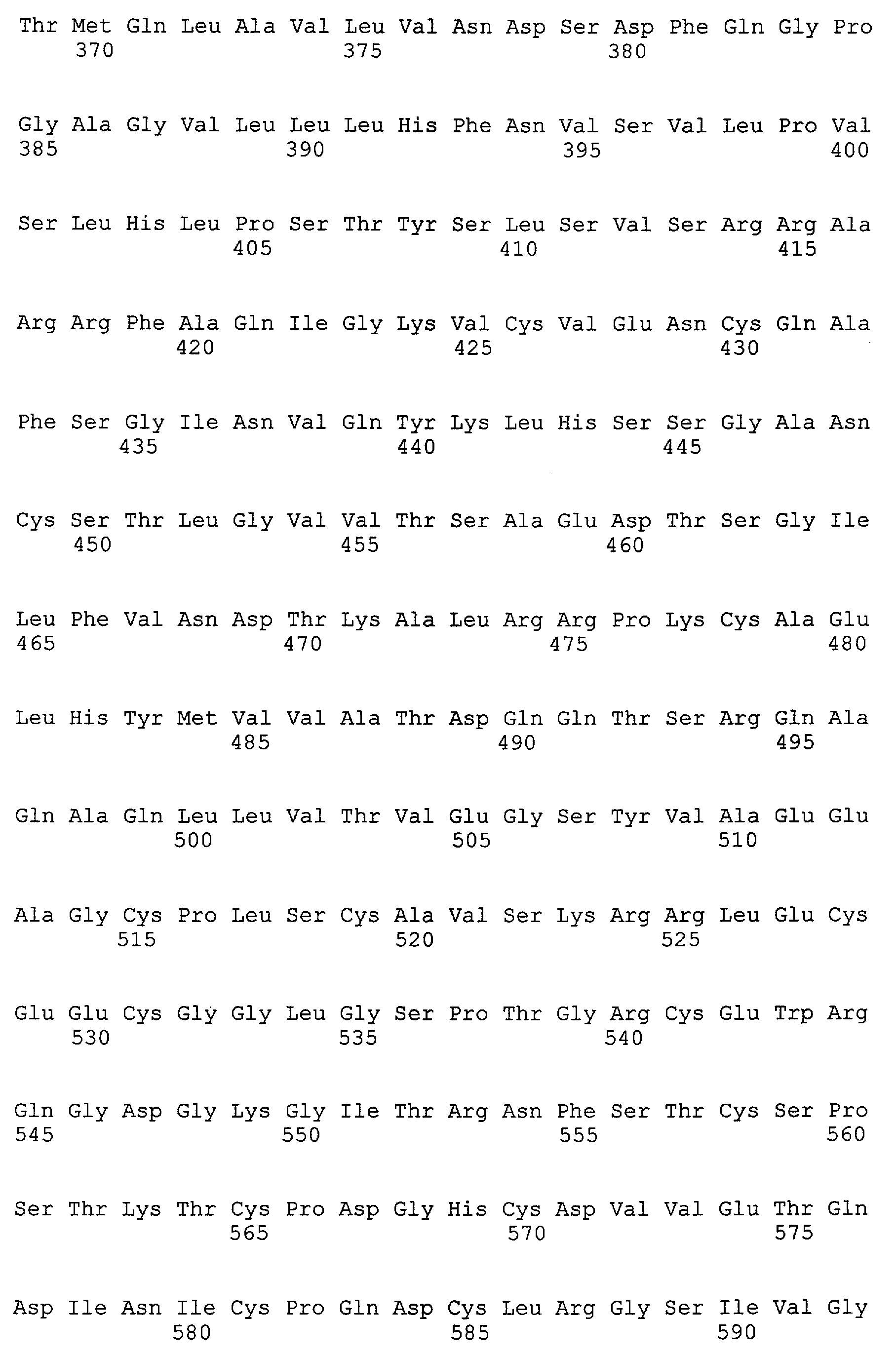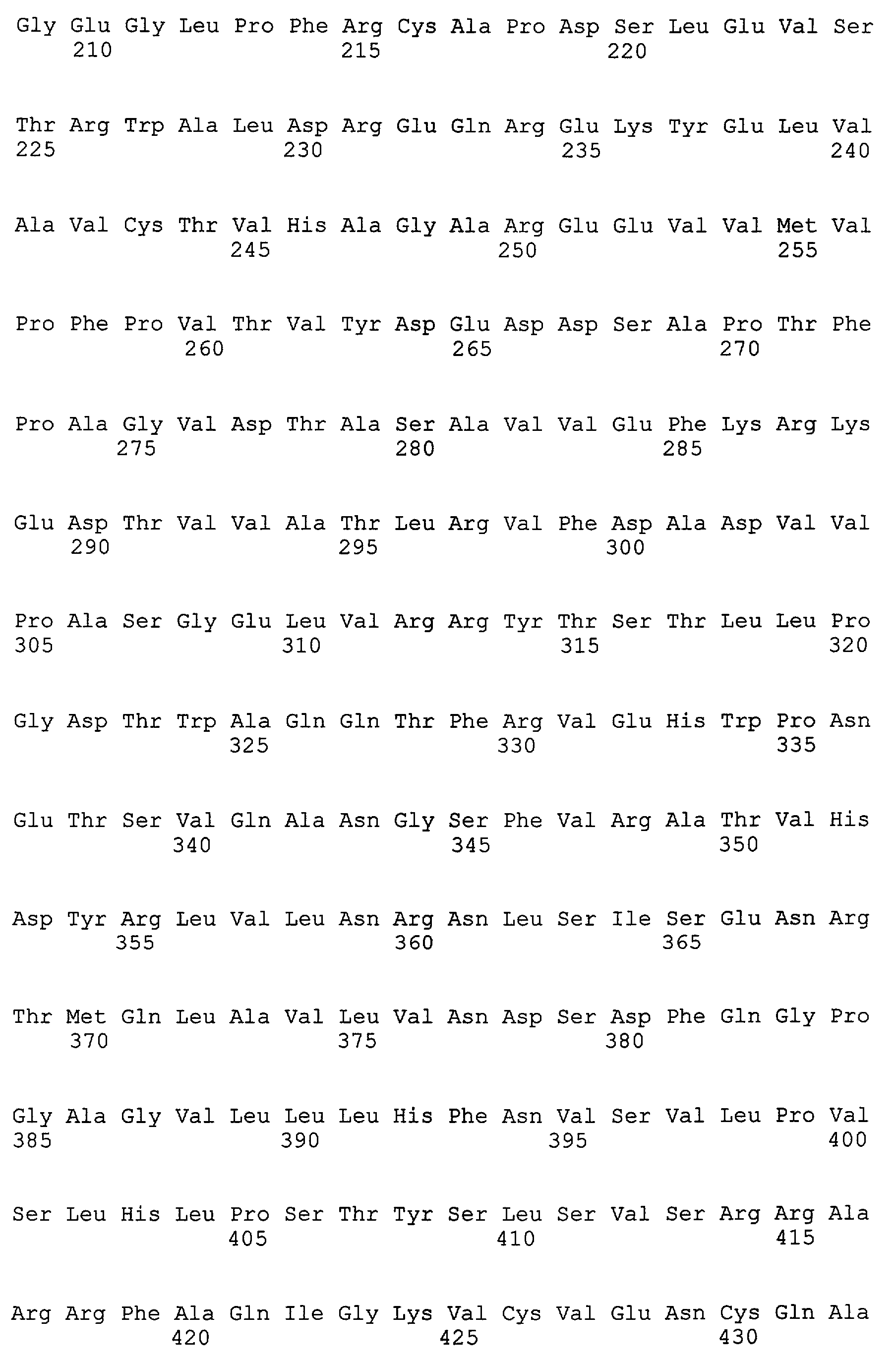Результат интеллектуальной деятельности: ПРОТИВООПУХОЛЕВОЕ СРЕДСТВО ПРОТИВ РАКА ЩИТОВИДНОЙ ЖЕЛЕЗЫ
Вид РИД
Изобретение
Область техники, к которой относится изобретение
Настоящее изобретение относится к терапевтическому средству и способу лечения, по меньшей мере, одного заболевания, выбранного из группы, состоящей из множественной эндокринной неоплазии типа IIA, множественной эндокринной неоплазии типа IIB, семейной медуллярной карциномы щитовидной железы, папиллярной карциномы щитовидной железы, спорадической медуллярной карциномы щитовидной железы, болезни Гиршспрунга, феохромоцитомы, гиперплазии паращитовидной железы и невром слизистой оболочки желудочно-кишечного тракта, включающему введение вещества, которое ингибирует активность киназы RET (далее в данном описании также называемого «веществом, ингибирующим активность киназы RET»), к применению вещества, ингибирующего активность киназы RET, для получения указанного терапевтического средства и к веществу, ингибирующему активность киназы RET, для указанного лечебного средства.
Настоящее изобретение также относится к терапевтическому средству и способу лечения карциномы щитовидной железы, включающему введение вещества, ингибирующего активность киназы RET, к применению вещества, ингибирующего активность киназы RET, для получения указанного терапевтического средства и веществу, ингибирующему активность киназы RET, для указанного терапевтического средства.
Кроме того, настоящее изобретение относится к фармацевтической композиции, включающей вещество, ингибирующее активность киназы RET, для введения в организм, содержащий клетки, экспрессирующие мутантную RET, к способу лечения заболевания, включающему введение в организм, содержащий клетки, экспрессирующие мутантную RET, к применению вещества, ингибирующего активность киназы RET, для получения указанной фармацевтической композиции и к веществу, ингибирующему активность киназы RET, для указанной фармацевтической композиции.
Настоящее изобретение также относится к ингибитору киназы RET.
Кроме того, настоящее изобретение относится к способу прогнозирования действия вещества, ингибирующего активность киназы RET, на пациента с использованием в качестве показателя наличия или отсутствия мутации RET в клетке.
Предпосылки создания изобретения
RET является одной из рецепторных тирозинкиназ и представляет собой молекулу клеточной поверхности, которая передает сигналы для роста и дифференцировки клеток.
Известно, что мутация RET вовлекается в заболевание, такое как множественная эндокринная неоплазия типа IIA, множественная эндокринная неоплазия типа IIB, семейная медуллярная карцинома щитовидной железы, спорадическая медулярная карциномы щитовидной железы, папиллярная карцинома щитовидной железы и болезнь Гиршспрунга(1,2). Предполагается, что вещество, ингибирующее киназу RET, является потенциально эффективным терапевтическим средством в случае таких заболеваний(1,2).
Мутация одного из пяти цистеиновых остатков в кодонах 609, 611, 618, 620 и 634 RET обнаруживается у 93-98% больных множественной эндокринной неоплазией типа IIA, где наиболее часто обнаруживается мутация в кодоне RET 634(3,4).
С другой стороны, у 95% больных множественной эндокринной неоплазией типа IIB обнаруживается мутация RET М918Т (мутация из метионина в тирозин в кодоне 918)(4).
Мутация в одном из кодонов RET 609, 611, 618, 620, 634, 768, 790, 791, 804 и 891 обнаруживается у многих больных семейной медуллярной карциномой щитовидной железы(4).
Известно, что все указанные точечные мутации вызывают константную лиганднезависимую активацию RET(3,4).
Синдром множественной эндокринной неоплазии типа IIA характеризуется медуллярной карциномой щитовидной железы, феохромоцитомой и гиперплазией паращитовидной железы, в то время как синдром множественной эндокринной неоплазии типа IIB ассоциируется с медуллярной карциномой щитовидной железы, феохромоцитомой и невромами слизистой оболочки желудочно-кишечного тракта. Главным симптомом синдрома семейной медуллярной карциномы щитовидной железы является медуллярная карцинома щитовидной железы(5).
Точечная мутация RET соматических клеток обнаруживается у примерно 40% больных спорадической медуллярной карциномой щитовидной железы, хотя мутации обнаруживаются, главным образом, в кодоне 918(6).
Более того, гибридный ген гена RET и другого гена, а именно реаранжировка гена RET, обнаруживается при папиллярной карциноме щитовидной железы из-за хромосомных инверсий или хромосомных транслокаций. Известно, что слитый белок, образованный через реаранжировку гена RET, приводит к лиганднезависимой димеризации и константной активации RET(7).
Болезнь Гиршспрунга характеризуется стойкой констипацией и интестинальной дилатацией у новорожденных, вызванными аномальным нервным сплетением толстой кишки. Известно, что одной из причин болезни Гиршспрунга является мутация RET(8).
Сообщается, что мутация RET вызывает независимую от клеточного каркаса пролиферацию и онкогенез клеток NIH3T3(2).
Сообщается, что ингибирующее киназу RET вещество ZD6474 подавляет независимую от клеточного каркаса пролиферацию в клетках NIH3T3, трансформированных мутантной RET, и ингибирует образование опухоли после инфузии указанных клеток голым мышам(2).
Сообщается, что ингибирующее киназу RET вещество BAY 43-9006 уменьшает размер опухоли на модели с подкожной трансплантацией клеточной линии медуллярной карциномы щитовидной железы человека (ТТ)(9).
Поэтому предполагается, что вещества, ингибирующие киназу RET, индуцируют ингибирование роста клеток, экспрессирующих мутантную RET, и показывают противоопухолевое действие против таких опухолевых клеток. Также оказывается, что вещества, ингибирующие киназу RET, эффективны против заболеваний, вызванных мутацией RET.
Таким образом, ожидается, что вещества, ингибирующие киназу RET, эффективны против множественной эндокринной неоплазии типа IIA, множественной эндокринной неоплазии типа IIB, семейной медуллярной карциномы щитовидной железы, папиллярной карциномы щитовидной железы, спорадической медуллярной карциномы щитовидной железы, болезни Гиршспрунга, феохромоцитомы, гиперплазии паращитовидной железы, невром слизистой оболочки желудочно-кишечного тракта и карциномы щитовидной железы.
4-(3-Хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид и его аналоги известны как вещества, ингибирующие ангиогенез(10-20). Однако сообщения, что 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид и его аналоги обладают активностью ингибирования киназы RET отсутствуют.
Перечень ссылок
(1) Oncogene, 19, 5590-5597, 2000.
(2) Cancer Research, 15, 7284-7290, 2002.
(3) Cancer Research, 66, 1177-1180, 2006.
(4) Journal of Clinical Endocrinology and Metabolism, 88, 5438-5443, 2003.
(5) Journal of Clinical Endocrinology and Metabolism, 89, 4142-4145, 2004.
(6) Journal of Clinical Endocrinology and Metabolism, 89, 5823-5827, 2004.
(7) Endocrinology, 145, 5448-5451, 2004.
(8) Proceedings of the National Academy of Sciences of the United States of America, 102, 8949-8954, 2005.
(9) Journal of the National Cancer Institute, 98, 326-334, 2006.
(10) Международная публикация № 02/32872, брошюра.
(11) Международная публикация № 2004/080462, брошюра.
(12) Международная публикация № 2005/063713, брошюра.
Раскрытие изобретения
Настоящее изобретение осуществлено с учетом обстоятельств, описанных выше, и в свете проблем, которые решает изобретение, относится к терапевтическому средству и способу лечения, по меньшей мере, одного заболевания, выбранного из группы, состоящей из множественной эндокринной неоплазии типа IIA, множественной эндокринной неоплазии типа IIB, семейной медуллярной карциномы щитовидной железы, папиллярной карциномы щитовидной железы, спорадической медуллярной карциномы щитовидной железы, болезни Гиршспрунга, феохромоцитомы, гиперплазии паращитовидной железы и невром слизистой оболочки желудочно-кишечного тракта, а также карциномы щитовидной железы, и к фармацевтической композиции и способу лечения, высокоэффектиному для организмов, включающих клетки, экспрессирующие мутантную RET. Другой проблемой, которую решает изобретение, является ингибитор активности киназы RET. Еще одной проблемой, которую решает изобретение, является способ прогнозирования действия 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамида и его аналогов.
Для того чтобы решить указанные выше проблемы, авторы настоящего изобретения провели исследования и нашли, что 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид обладает активностью ингибирования киназы RET, и что 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид и его аналоги высокоэффективны против, по меньшей мере, одного заболевания, выбранного из группы, состоящей из множественной эндокринной неоплазии типа IIA, множественной эндокринной неоплазии типа IIB, семейной медуллярной карциномы щитовидной железы, папиллярной карциномы щитовидной железы, спорадической медуллярной карциномы щитовидной железы, болезни Гиршспрунга, феохромоцитомы, гиперплазии паращитовидной железы и невром слизистой оболочки желудочно-кишечного тракта, а также карциномы щитовидной железы. Авторы настоящего изобретения также нашли, что 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид и его аналоги высокоэффективны для организмов, включающих клетки, экспрессирующие мутантную RET, и также нашли, что действие 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамида и его аналогов можно прогнозировать, используя в качестве показателя наличие или отсутствие мутации RET в клетке.
Таким образом, настоящее изобретение относится к перечисленному далее.
(1) Терапевтическое средство, включающее вещество, ингибирующее киназу RET, для лечения, по меньшей мере, одного заболевания, выбранного из группы, состоящей из множественной эндокринной неоплазии типа IIA, множественной эндокринной неоплазии типа IIB, семейной медуллярной карциномы щитовидной железы, папиллярной карциномы щитовидной железы, спорадической медуллярной карциномы щитовидной железы, болезни Гиршспрунга, феохромоцитомы, гиперплазии паращитовидной железы и невром слизистой оболочки желудочно-кишечного тракта.
(2) Терапевтическое средство для лечения карциномы щитовидной железы, включающее вещество, ингибирующее киназу RET.
(3) Фармацевтическая композиция, включающая вещество, ингибирующее киназу RET, для введения в организм, содержащий клетки, экспрессирующие мутантную RET.
(4) Способ лечения, по меньшей мере, одного заболевания, выбранного из группы, состоящей из множественной эндокринной неоплазии типа IIA, множественной эндокринной неоплазии типа IIB, семейной медуллярной карциномы щитовидной железы, папиллярной карциномы щитовидной железы, спорадической медуллярной карциномы щитовидной железы, болезни Гиршспрунга, феохромоцитомы, гиперплазии паращитовидной железы и невром слизистой оболочки желудочно-кишечного тракта, включающий введение пациенту эффективного количества вещества, ингибирующего киназу RET.
(5) Способ лечения карциномы щитовидной железы, включающий введение пациенту эффективного количества вещества, ингибирующего киназу RET.
(6) Способ лечения заболевания, включающий введение в организм, содержащий клетки, экспрессирующие мутантную RET, эффективного количества вещества, ингибирующего киназу RET.
(7) Применение вещества, ингибирующего киназу RET, для получения терапевтического средства для лечения, по меньшей мере, одного заболевания, выбранного из группы, состоящей из множественной эндокринной неоплазии типа IIA, множественной эндокринной неоплазии типа IIB, семейной медуллярной карциномы щитовидной железы, папиллярной карциномы щитовидной железы, спорадической медуллярной карциномы щитовидной железы, болезни Гиршспрунга, феохромоцитомы, гиперплазии паращитовидной железы и невром слизистой оболочки желудочно-кишечного тракта.
(8) Применение вещества, ингибирующего киназу RET, для получения терапевтического средства для лечения карциномы щитовидной железы.
(9) Применение вещества, ингибирующего киназу RET, для получения фармацевтической композиции, включающей вещество, ингибирующее киназу RET, для введения в организм, содержащий клетки, экспрессирующие мутантную RET.
(10) Вещество, ингибирующее киназу RET, для терапевтического средства для лечения, по меньшей мере, одного заболевания, выбранного из группы, состоящей из множественной эндокринной неоплазии типа IIA, множественной эндокринной неоплазии типа IIB, семейной медуллярной карциномы щитовидной железы, папиллярной карциномы щитовидной железы, спорадической медуллярной карциномы щитовидной железы, болезни Гиршспрунга, феохромоцитомы, гиперплазии паращитовидной железы и невром слизистой оболочки желудочно-кишечного тракта.
(11) Вещество, ингибирующее киназу RET, для терапевтического средства для лечения карциномы щитовидной железы.
(12) Вещество, ингибирующее киназу RET, для фармацевтической композиции, включающей вещество, ингибирующее киназу RET, для введения в организм, содержащий клетки, экспрессирующие мутантную RET.
(13) Способ прогнозирования того, будет ли пациент высокочувствителен к веществу, ингибирующему киназу RET, включающий использование в качестве показателя наличие или отсутствие в клетке мутации RET.
(14) Способ анализа чувствительности клетки к веществу, ингибирующему киназу RET, включающий определение наличия или отсутствия в клетке мутации RET.
(15) Способ отбора клеток, высокочувствительных к веществу, ингибирующему киназу RET, включающий определение наличия или отсутствия в клетке мутации RET.
(16) Способ отбора пациентов, высокочувствительных к веществу, ингибирующему киназу RET, включающий определение наличия или отсутствия в клетке мутации RET.
(17) Способ классификации пациентов согласно результатам, полученным в анализе чувствительности пациентов к веществу, ингибирующему киназу RET, включающий определение наличия или отсутствия в клетке мутации RET.
(18) Способ отбора пациентов, которым предполагается введение вещества, ингибирующего киназу RET, включающий определение наличия или отсутствия в клетке мутации RET и отбор по результатам определения пациентов, имеющих клетки экспрессирующие мутантную RET.
(19) Способ прогнозирования лечебного действия на пациента вещества, ингибирующего киназу RET, включающий определение наличия или отсутствия в клетке мутации RET.
(20) Способ определения наличия или отсутствия мутации RET в клетках пациента для прогнозирования чувствительности пациента к веществу, ингибирующему киназу RET.
Указанное вещество, ингибирующее киназу RET, может представлять собой соединение, представленное общей формулой (I)
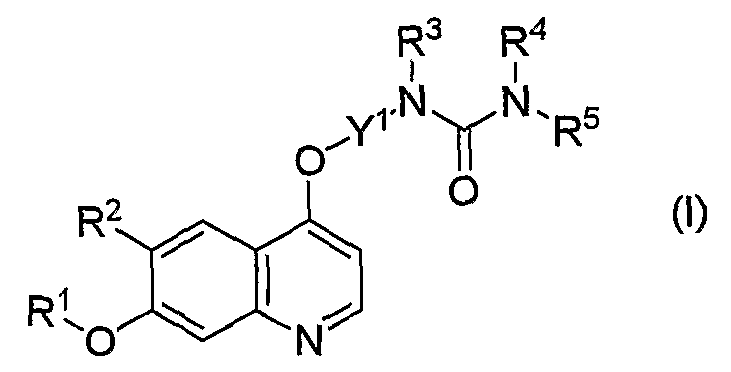
[где R1 представляет собой группу, представленную формулой -V1-V2-V3 (где V1 представляет собой С1-6-алкиленовую группу, которая может иметь заместитель; V2 представляет собой простую связь, атом кислорода, атом серы, карбонильную группу, сульфинильную группу, сульфонильную группу, группу, представленную формулой -CONR6-, группу, представленную формулой -SO2NR6-, группу, представленную формулой -NR6SO2-, группу, представленную формулой -NR6CO-, или группу, представленную формулой -NR6- (где R6 представляет собой атом водорода, С1-6-алкильную группу, которая может иметь заместитель, или С3-8-циклоалкильную группу, которая может иметь заместитель); V3 представляет собой атом водорода, С1-6-алкильную группу, которая может иметь заместитель, С2-6-алкенильную группу, которая может иметь заместитель, С2-6-алкинильную группу, которая может иметь заместитель, С3-8-циклоалкильную группу, которая может иметь заместитель, С6-10-арильную группу, которая может иметь заместитель, 5-10-членную гетероарильную группу, которая может иметь заместитель, или 3-10-членную неароматическую гетероциклическую группу, которая может иметь заместитель);
R2 представляет собой цианогруппу, С1-6-алкоксигруппу, которая может иметь заместитель, карбоксильную группу, С2-7-алкоксикарбонильную группу, которая может иметь заместитель, или группу, представленную формулой -CONVa11Va12 (где Va11 представляет собой атом водорода, С1-6-алкильную группу, которая может иметь заместитель, С2-6-алкенильную группу, которая может иметь заместитель, С2-6-алкинильную группу, которая может иметь заместитель, С3-8-циклоалкильную группу, которая может иметь заместитель, С6-10-арильную группу, которая может иметь заместитель, 5-10-членную гетероарильную группу, которая может иметь заместитель, или 3-10-членную неароматическую гетероциклическую группу, которая может иметь заместитель; Va12 представляет собой атом водорода, С1-6-алкильную группу, которая может иметь заместитель, С2-6-алкенильную группу, которая может иметь заместитель, С2-6-алкинильную группу, которая может иметь заместитель, С3-8-циклоалкильную группу, которая может иметь заместитель, С6-10-арильную группу, которая может иметь заместитель, 5-10-членную гетероарильную группу, которая может иметь заместитель, 3-10-членную неароматическую гетероциклическую группу, которая может иметь заместитель, гидроксильную группу, С1-6-алкоксигруппу, которая может иметь заместитель, или С3-8-циклоалкоксигруппу, которая может иметь заместитель);
Y1 представляет собой группу, представленную формулой
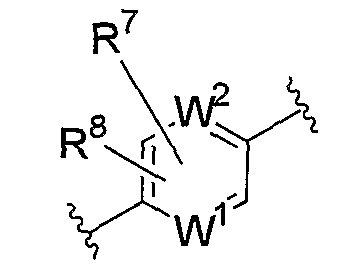 или
или 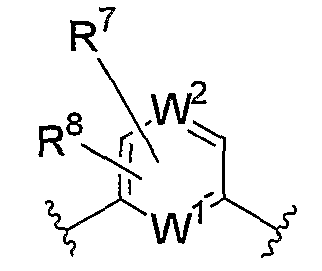
(где R7 и R8, каждый независимо, представляет собой атом водорода, атом галогена, цианогруппу, нитрогруппу, аминогруппу, С1-6-алкильную группу, которая может иметь заместитель, С3-8-циклоалкильную группу, которая может иметь заместитель, С1-6-алкоксигруппу, которая может иметь заместитель, С1-6-алкилтиогруппу, которая может иметь заместитель, формильную группу, С2-7-ацильную группу, которая может иметь заместитель, С2-7-алкоксикарбонильную группу, которая может иметь заместитель, или группу, представленную формулой -CONVd1Vd2 (где Vd1 и Vd2, каждый независимо, представляет собой атом водорода или С1-6-алкильную группу, которая может иметь заместитель); W1 и W2, каждый независимо, представляет собой атом углерода или атом азота, который может иметь заместитель);
R3 и R4, каждый независимо, представляет собой атом водорода, С1-6-алкильную группу, которая может иметь заместитель, С2-6-алкенильную группу, которая может иметь заместитель, С2-6-алкинильную группу, которая может иметь заместитель, С3-8-циклоалкильную группу, которая может иметь заместитель, С2-7-ацильную группу, которая может иметь заместитель, или С2-7-алкоксикарбонильную группу, которая может иметь заместитель; и
R5 представляет собой атом водорода, С1-6-алкильную группу, которая может иметь заместитель, С2-6-алкенильную группу, которая может иметь заместитель, С2-6-алкинильную группу, которая может иметь заместитель, С3-8-циклоалкильную группу, которая может иметь заместитель, С6-10-арильную группу, которая может иметь заместитель, 5-10-членную гетероарильную группу, которая может иметь заместитель, или 3-10-членную неароматическую гетероциклическую группу, которая может иметь заместитель],
его фармакологически приемлемую соль или его сольват.
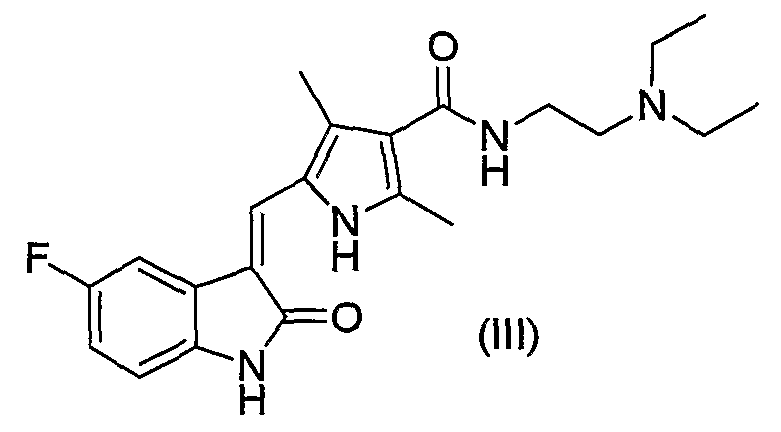
Более того, вещество, ингибирующее киназу RET, также может представлять собой, по меньшей мере, одно соединение, выбранное из группы, состоящей из (2-диэтиламиноэтил)амида 5-(5-фтор-2-оксо-1,2-дигидроиндол-3-илиденметил)-2,4-диметил-1Н-пиррол-3-карбоновой кислоты, N-{2-хлор-4-[(6,7-диметокси-4-хинолил)окси]фенил}-N'-(5-метил-3-изоксазолил)мочевины и 4-[(4-фтор-2-метилиндол-5-ил)окси]-6-метокси-7-[3-(пирролидин-1-ил)пропокси]хиназолина, его фармакологически приемлемую соль или его сольват.
Настоящее изобретение также относится к описанному далее.
(21) Ингибитор киназы RET, включающий соединение, представленное общей формулой (I), его фармакологически приемлемую соль или его сольват.
(22) Ингибитор киназы RET, включающий, по меньшей мере, одно соединение, выбранное из группы, состоящей из
(2-диэтиламиноэтил)амида 5-(5-фтор-2-оксо-1,2-дигидроиндол-3-илиденметил)-2,4-диметил-1Н-пиррол-3-карбоновой кислоты,
N-{2-хлор-4-[(6,7-диметокси-4-хинолил)окси]фенил}-N'-(5-метил-3-изоксазолил)мочевины и
4-[(4-фтор-2-метилиндол-5-ил)окси]-6-метокси-7-[3-(пирролидин-1-ил)пропокси]хиназолина,
его фармакологически приемлемую соль или его сольват.
Предпочтительно, настоящее изобретение также относится к описанному далее.
(23) Терапевтическое средство, включающее 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид, его фармакологически приемлемую соль или его сольват, для лечения, по меньшей мере, одного заболевания, выбранного из группы, состоящей из множественной эндокринной неоплазии типа IIA, множественной эндокринной неоплазии типа IIB, семейной медуллярной карциномы щитовидной железы, папиллярной карциномы щитовидной железы, спорадической медуллярной карциномы щитовидной железы, болезни Гиршспрунга, феохромоцитомы, гиперплазии паращитовидной железы и невром слизистой оболочки желудочно-кишечного тракта.
(24) Терапевтическое средство, включающее 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид, его фармакологически приемлемую соль или его сольват, для лечения карциномы щитовидной железы.
(25) Фармацевтическая композиция, включающая 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид, его фармакологически приемлемую соль или его сольват, для введения в организм, содержащий клетки, экспрессирующие мутантную RET.
(26) Способ лечения, по меньшей мере, одного заболевания, выбранного из группы, состоящей из множественной эндокринной неоплазии типа IIA, множественной эндокринной неоплазии типа IIB, семейной медуллярной карциномы щитовидной железы, папиллярной карциномы щитовидной железы, спорадической медуллярной карциномы щитовидной железы, болезни Гиршспрунга, феохромоцитомы, гиперплазии паращитовидной железы и невром слизистой оболочки желудочно-кишечного тракта, включающий введение пациенту эффективного количества 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамида, его фармакологически приемлемой соли или его сольвата.
(27) Способ лечения карциномы щитовидной железы, включающий введение пациенту эффективного количества 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамида, его фармакологически приемлемой соли или его сольвата.
(28) Способ лечения заболевания, включающий введение в организм, содержащий клетки, экспрессирующие мутантную RET, эффективного количества 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамида, его фармакологически приемлемой соли или его сольвата.
(29) Применение 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамида, его фармакологически приемлемой соли или его сольвата для получения терапевтического средства для лечения, по меньшей мере, одного заболевания, выбранного из группы, состоящей из множественной эндокринной неоплазии типа IIA, множественной эндокринной неоплазии типа IIB, семейной медуллярной карциномы щитовидной железы, папиллярной карциномы щитовидной железы, спорадической медуллярной карциномы щитовидной железы, болезни Гиршспрунга, феохромоцитомы, гиперплазии паращитовидной железы и невром слизистой оболочки желудочно-кишечного тракта.
(30) Применение 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамида, его фармакологически приемлемой соли или его сольвата для получения терапевтического средства для лечения карциномы щитовидной железы.
(31) Применение 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамида, его фармакологически приемлемой соли или его сольвата для получения фармацевтической композиции, включающей вещество, ингибирующее киназу RET, для введения в организм, содержащий клетки, экспрессирующие мутантную RET.
(32) 4-(3-Хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид, его фармакологически приемлемая соль или его сольват для получения терапевтического средства для лечения, по меньшей мере, одного заболевания, выбранного из группы, состоящей из множественной эндокринной неоплазии типа IIA, множественной эндокринной неоплазии типа IIB, семейной медуллярной карциномы щитовидной железы, папиллярной карциномы щитовидной железы, спорадической медуллярной карциномы щитовидной железы, болезни Гиршспрунга, феохромоцитомы, гиперплазии паращитовидной железы и невром слизистой оболочки желудочно-кишечного тракта.
(33) 4-(3-Хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид, его фармакологически приемлемая соль или его сольват для терапевтического средства для лечения карциномы щитовидной железы.
(34) 4-(3-Хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид, его фармакологически приемлемая соль или его сольват для фармацевтической композиции, включающей вещество, ингибирующее киназу RET, для введения в организм, содержащий клетки, экспрессирующие мутантную RET.
(35) Способ прогнозирования того, будет ли пациент высокочувствителен к 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамиду, его фармакологически приемлемой соли или его сольвату, включающий использование в качестве показателя наличие или отсутствие в клетке мутации RET.
(36) Способ анализа чувствительности клетки к 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамиду, его фармакологически приемлемой соли или его сольвату, включающий определение наличия или отсутствия в клетке мутации RET.
(37) Способ отбора клеток, высокочувствительных к 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамиду, его фармакологически приемлемой соли или его сольвату, включающий определение наличия или отсутствия в клетке мутации RET.
(38) Способ отбора пациентов, высокочувствительных к 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамиду, его фармакологически приемлемой соли или его сольвату, включающий определение наличия или отсутствия в клетке мутации RET.
(39) Способ классификации пациентов согласно результатам, полученным в анализе чувствительности пациентов к 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамиду, его фармакологически приемлемой соли или его сольвату, включающий определение наличия или отсутствия в клетке мутации RET.
(40) Способ отбора пациентов, которым предполагается введение 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамида, его фармакологически приемлемой соли или его сольвата, включающий определение наличия или отсутствия в клетке мутации RET и отбор по результатам определения пациентов, имеющих клетки, экспрессирующие мутантную RET.
(41) Способ прогнозирования лечебного действия на пациента 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамида, его фармакологически приемлемой соли или его сольвата, включающий определение наличия или отсутствия в клетке мутации RET.
(42) Способ определения наличия или отсутствия мутации RET в клетках пациента для прогнозирования чувствительности пациента к 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамиду, его фармакологически приемлемой соли или его сольвату.
(43) Ингибитор киназы RET, включающий 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид, его фармакологически приемлемую соль или его сольват.
Настоящее изобретение относится к терапевтическому средству и способу лечения, включающему вещество, ингибирующее киназу RET, по меньшей мере, одного заболевания, выбранного из группы, состоящей из множественной эндокринной неоплазии типа IIA, множественной эндокринной неоплазии типа IIB, семейной медуллярной карциномы щитовидной железы, папиллярной карциномы щитовидной железы, спорадической медуллярной карциномы щитовидной железы, болезни Гиршспрунга, феохромоцитомы, гиперплазии паращитовидной железы и невром слизистой оболочки желудочно-кишечного тракта, применению вещества, ингибирующего киназу RET, для получения указанного терапевтического средства и ингибирующему киназу RET веществу для указанного терапевтического средства.
Настоящее изобретение относится к терапевтическому средству и способу лечения карциномы щитовидной железы, включающему вещество, ингибирующее киназу RET, применению вещества, ингибирующего киназу RET, для получения указанного терапевтического средства и ингибирующему киназу RET веществу для указанного терапевтического средства.
Настоящее изобретение также относится к фармацевтической композиции, включающей вещество, ингибирующее киназу RET, для введения в организм, содержащий клетки, экспрессирующие мутантную RET, способу лечения заболевания, включающему введение в организм, содержащий клетки, экспрессирующие мутантную RET, указанной фармацевтической композиции, применению вещества, ингибирующего киназу RET, для получения указанной фармацевтической композиции и ингибирующему киназу RET веществу для указанной фармацевтической композиции.
Настоящее изобретение также относится к ингибитору киназы RET.
Кроме того, настоящее изобретение относится к способу прогнозирования действия вещества, ингибирующего киназу RET.
Конкретнее, действие вещества, ингибирующего киназу RET, можно прогнозировать, используя в качестве показателя наличие или отсутствие клеток, экспрессирующих мутантную RET.
Так как способом по изобретению можно прогнозировать действие соединения без введения соединения пациенту, становится возможным отбор пациентов, которые, как ожидается, более чувствительны к соединению. Таким образом, становится возможным содействие (вклад в) QOL пациента.
Краткое описание чертежей
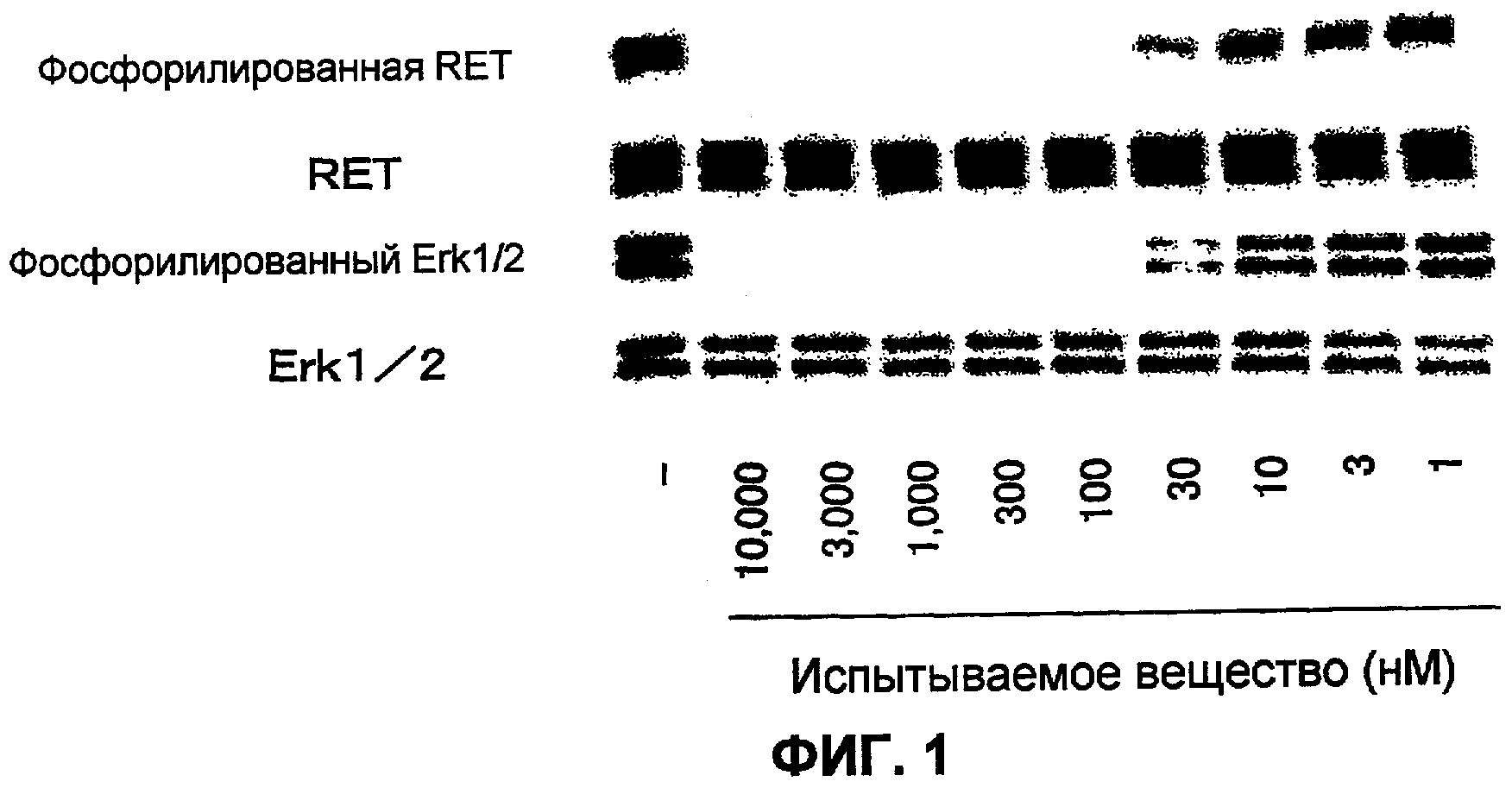
Фиг.1 показывает действие 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамида на активацию киназы RET и Erk1/2 (показатель фосфорилирования) на клеточную линию медуллярной карциномы щитовидной железы человека (ТТ) в культуре. Крайняя левая полоса является определением активации киназы RET и Erk1/2 (показатель фосфорилирования) без добавления испытываемого вещества.
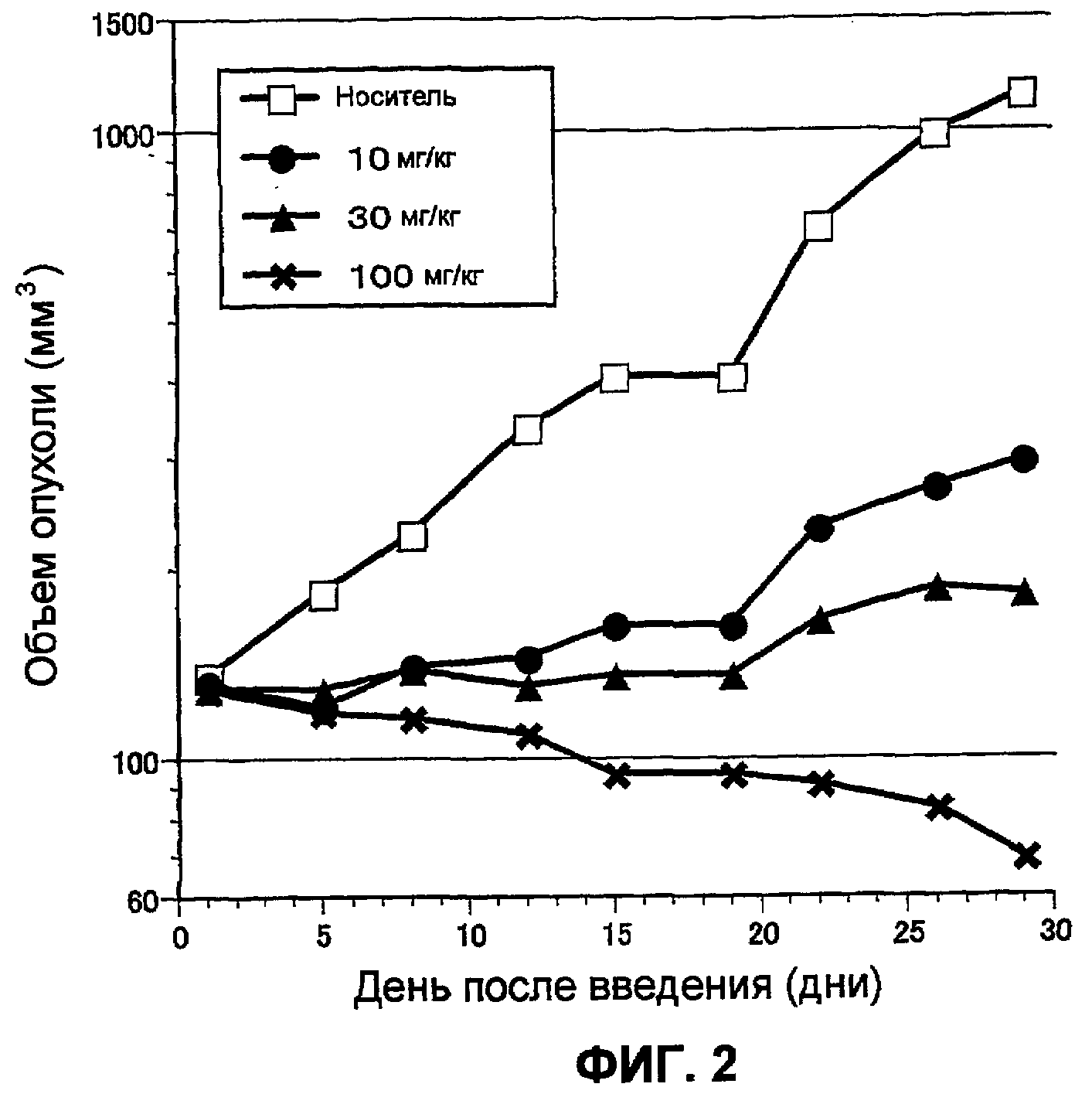
Фиг.2 показывает противоопухолевое действие 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамида на модели с подкожной трансплантацией клеточной линии медуллярной карциномы щитовидной железы человека (ТТ).
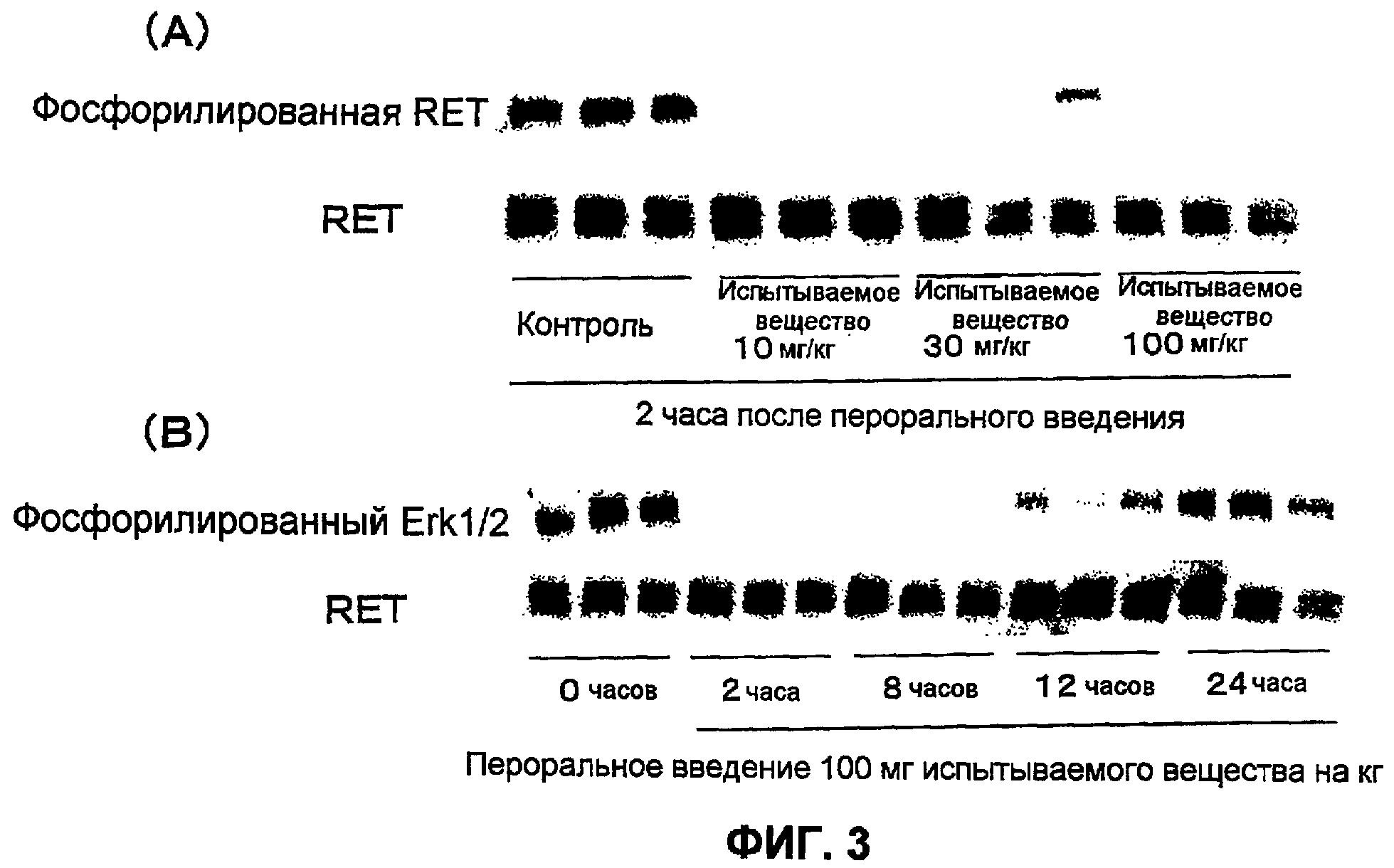
Фиг.3 показывает действие 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамида на киназу RET в опухолевой ткани модели с подкожной трансплантацией клеточной линии медуллярной карциномы щитовидной железы человека (ТТ). (А) показывает действие на фософрилирование RET через 2 часа после перорального введения испытываемого вещества в каждой дозировке (10, 30 или 100 мг/кг), в то время как (В) показывает действие на фософрилирование RET через 2, 8, 12 или 24 часа после перорального введения испытываемого вещества в дозе 100 мг/кг.
Наилучшие способы осуществления изобретения
Далее в данном описании будут описываться воплощения настоящего изобретения. Указанные далее воплощения иллюстрируют настоящее изобретение, но не предназначены для ограничения настоящего изобретения. Настоящее изобретение можно осуществить в различных воплощениях без отхода от объема изобретения.
Документы, заявки на патент с открытой выкладкой, патентные публикации и другие патентные документы, цитированные в данном описании, включены в данное описание в качестве ссылок. Настоящее описание также включает в качестве ссылки предварительную заявку на патент США 60/747570, на приоритет которой притязает настоящая заявка.
1. Терапевтическое средство, фармацевтическая композиция и способ лечения по изобретению
(1) RET
Согласно настоящему изобретению RET представляет собой белок, кодированный протоонкогеном ret, например полипептид, состоящий из аминокислотной последовательности, представленной SEQ ID NO: 2 (GenBank, инвентарный № NM_020975) или SEQ ID NO: 4 (GenBank, инвентарный № NM_020630). Аминокислотные последовательности, представленные SEQ ID NO: 2 и SEQ ID NO: 4, имеют длину 1114 ак и 1072 ак, соответственно.
Протоонкоген ret представляет собой, например, полинуклеотид 181-3522 из нуклеотидной последовательности, представленной SEQ ID NO: 1 (GenBank, инвентарный № NM_020975), или полинуклеотид 181-3396 из нуклеотидной последовательности, представленной SEQ ID NO: 3 (GenBank, инвентарный № NM_020630).
В данном описании указанные RET также могут называться «RET дикого типа».
(2) Мутантная RET
Согласно настоящему изобретению RET представляет собой полипептид, включающий мутантный вариант аминокислотной последовательности RET дикого типа, например аминокислотную последовательность, имеющую одну или несколько аминокислот, делетированных, замененных, добавленных или измененных путем их комбинации в аминокислотной последовательности, представленной SEQ ID NO: 2 или 4. Примеры включают полипептид, обладающий активностью киназы RET. Предпочтительно, мутантная RET может представлять собой, например, полипептид, обладающий активностью киназы RET и включающий аминокислотную последовательность, имеющую одну замененную аминокислоту в аминокислотной последовательности RET дикого типа (например, аминокислотной последовательности, представленной SEQ ID NO: 2 или 4).
В данном описании термин «активность киназы RET» относится к способности RET фосфорилировать тирозиновый остаток собственного или другого белка.
Примеры мутантных RET включают полипептиды, включающие последовательности описанные ниже в (i)-(xix).
(i) Аминокислотная последовательность, имеющая глицин в позиции 321, замененный в аминокислотной последовательности, представленной SEQ ID NO: 2 или 4, на другую аминокислоту, предпочтительно аргинин (Journal of Endocrinology Investigation, 28, 905-909, 2005).
(ii) Аминокислотная последовательность, имеющая глицин в позиции 533, замененный в аминокислотной последовательности, представленной SEQ ID NO: 2 или 4, на другую аминокислоту, предпочтительно цистеин (Journal of Clinical Endocrinology and Metabolism, 88, 5438-5443, 2003).
(iii) Аминокислотная последовательность, имеющая цистеин в позиции 609, замененный в аминокислотной последовательности, представленной SEQ ID NO: 2 или 4, на другую аминокислоту, предпочтительно серин (Clin. Endocrinol., 63, 678-682, 2005).
(iv) Аминокислотная последовательность, имеющая цистеин в позиции 611, замененный в аминокислотной последовательности, представленной SEQ ID NO: 2 или 4, на другую аминокислоту, предпочтительно серин, тирозин или фенилаланин (European Journal of Human Genetics, 11, 364-368, 2003; Journal of Clinical Endocrinology and Metabolism, 86, 1104-1109, 2001).
(v) Аминокислотная последовательность, имеющая цистеин в позиции 618, замененный в аминокислотной последовательности, представленной SEQ ID NO: 2 или 4, на другую аминокислоту, предпочтительно аргинин, серин, глицин или фенилаланин (American Journal of Pathology, 168, 1262-1275, 2006; Journal of Clinical Endocrinology and Metabolism, 86, 1104-1109, 2001).
(vi) Аминокислотная последовательность, имеющая цистеин в позиции 620, замененный в аминокислотной последовательности, представленной SEQ ID NO: 2 или 4, на другую аминокислоту, предпочтительно аргинин или серин (American Journal of Pathology, 168, 1262-1275, 2006; Journal of Clinical Endocrinology and Metabolism, 86, 1104-1109, 2001).
(vii) Аминокислотная последовательность, имеющая цистеин в позиции 630, замененный в аминокислотной последовательности, представленной SEQ ID NO: 2 или 4, на другую аминокислоту, предпочтительно аргинин или тирозин (Thyroid, 15, 668-671, 2005; Biochemical and Biophysical Research Communications, 255, 587-590, 1999).
(viii) Аминокислотная последовательность, имеющая аспарагиновую кислоту в позиции 631, замененную в аминокислотной последовательности, представленной SEQ ID NO: 2 или 4, на другую аминокислоту, предпочтительно тирозин, глицин, аспарагин или аланин (Biochemical and Biophysical Research Communications, 255, 587-590, 1999).
(ix) Аминокислотная последовательность, имеющая цистеин в позиции 634, замененный в аминокислотной последовательности, представленной SEQ ID NO: 2 или 4, на другую аминокислоту, предпочтительно аргинин, глицин, тирозин, фенилаланин, серин или триптофан (Biochemical and Biophysical Research Communications, 255, 587-590, 1999; Journal of Clinical Endocrinology and Metabolism, 86, 1104-1109, 2001; Biochemical and Biophysical Research Communications, 207, 1022-1028, 1995).
(х) Аминокислотная последовательность, имеющая глицин в позиции 691, замененный в аминокислотной последовательности, представленной SEQ ID NO: 2 или 4, на другую аминокислоту, предпочтительно серин (Cancer Research, 66, 1177-1189, 2006).
(xi) Аминокислотная последовательность, имеющая глутаминовую кислоту в позиции 768, замененную в аминокислотной последовательности, представленной SEQ ID NO: 2 или 4, на другую аминокислоту, предпочтительно аспарагиновую кислоту (Clinical Chemistry, 50, 522-529, 2004; Journal of Clinical Endocrinology and Metabolism, 86, 1104-1109, 2001).
(xii) Аминокислотная последовательность, имеющая лейцин в позиции 790, замененный в аминокислотной последовательности, представленной SEQ ID NO: 2 или 4, на другую аминокислоту, предпочтительно фенилаланин (Journal of Clinical Endocrinology and Metabolism, 83, 770-774, 1998; Journal of Clinical Endocrinology and Metabolism, 86, 1104-1109, 2001).
(xiii) Аминокислотная последовательность, имеющая тирозин в позиции 791, замененный в аминокислотной последовательности, представленной SEQ ID NO: 2 или 4, на другую аминокислоту, предпочтительно фенилаланин (Journal of Clinical Endocrinology and Metabolism, 83, 770-774, 1998).
(xiv) Аминокислотная последовательность, имеющая валин в позиции 804, замененный в аминокислотной последовательности, представленной SEQ ID NO: 2 или 4, на другую аминокислоту, предпочтительно метионин (Journal of Clinical Endocrinology and Metabolism, 86, 1104-1109, 2001).
(xv) Аминокислотная последовательность, имеющая тирозин в позиции 806, замененный в аминокислотной последовательности, представленной SEQ ID NO: 2 или 4, на другую аминокислоту, предпочтительно цистеин (Japanese Journal of Cancer Research, 90, 1-5, 1999).
(xvi) Аминокислотная последовательность, имеющая аргинин в позиции 844, замененный в аминокислотной последовательности, представленной SEQ ID NO: 2 или 4, на другую аминокислоту, предпочтительно лейцин (Exp. Clin. Endocrinol. Diabetes, 108, 128-132, 2000).
(xvii) Аминокислотная последовательность, имеющая аланин в позиции 883, замененный в аминокислотной последовательности, представленной SEQ ID NO: 2 или 4, на другую аминокислоту, предпочтительно фенилаланин или тирозин (European Journal of Endocrinology, 142, 573-575, 2000; Journal of Clinical Endocrinology and Metabolism, 89, 5823-5827, 2004).
(xviii) Аминокислотная последовательность, имеющая серин в позиции 891, замененный в аминокислотной последовательности, представленной SEQ ID NO: 2 или 4, на другую аминокислоту, предпочтительно аланин (Journal of Clinical Endocrinology and Metabolism, 89, 5823-5827, 2004).
(xix) Аминокислотная последовательность, имеющая метионин в позиции 918, замененный в аминокислотной последовательности, представленной SEQ ID NO: 2 или 4, на другую аминокислоту, предпочтительно треонин (Clinical Cancer Research, 8, 457-463, 2002).
Кроме того, мутантные RET могут представлять собой RET, включающие, по меньшей мере, одну из замен, указанных выше в (i) - (xix), а именно мутантные RET, включающие сайты мутации, где, по меньшей мере, одна аминокислота, выбранная из группы, состоящей из аминокислот в кодонах 321, 533, 609, 611, 618, 620, 630, 631, 634, 691, 768, 790, 791, 804, 806, 844, 883, 891 и 918, заменена в аминокислотной последовательности, представленной SEQ ID NO: 2 или 4, на другую аминокислоту. Например, полипептид, включающий аминокислотную последовательность, содержащую сайт мутации, где валин в позиции 804 заменен на другую аминокислоту, и сайт мутации, где тирозин в позиции 806 заменен в аминокислотной последовательности, представленной SEQ ID NO: 2, на другую аминокислоту, входит в число мутантных RET. В данном описании число и комбинация указанных выше замен (i)-(xix), включенных в мутантную RET, особо не ограничиваются.
Согласно настоящему изобретению мутантная RET представляет собой, предпочтительно, полипептид, включающий последовательность, представленную выше (iii), (iv), (v), (vi), (ix), (xi), (xii), (xiii), (xiv), (xviii) или (xix), предпочтительнее последовательность, представленную (ix) или (xix).
В данном описании алфавитное обозначение аминокислот отражено в широко используемых трехбуквенных или однобуквенных кодах. Буква, предшествующая числу, показывает однобуквенный код заменяемой аминокислоты, буква, следующая за числом, показывает однобуквенный код аминокислоты, которая заменяет исходную аминокислоту, и число показывает позицию аминокислоты в аминокислотной последовательности. Например, как показано выше в (xix), когда метионин в позиции 918 заменяют на треонин, это можно показать в виде «М918Т».
Более того, число, следующее за кодоном, может показывать позицию аминокислоты в аминокислотной последовательности. Например, определение «аминокислота в кодоне 918» относится к 918-й аминокислоте в аминокислотной последовательности.
Согласно настоящему изобретению мутантная RET может представлять собой полипептид, обладающий активностью киназы RET и кодированный геном, реаранжированным между геном, кодирующим RET дикого типа (далее в данном описании также называемым «геном RET»), и другим геном. Более того, мутантная RET по изобретению представляет собой, например, полипептид, обладающий активностью киназы RET и кодированный полинуклеотидом, где полинуклеотид с нуклеотидной последовательностью, представленной SEQ ID NO: 1 или 3, частично реаранжирован другим геном. Более того, мутантная RET по изобретению представляет собой, например, полипептид, обладающий активностью киназы RET и кодированный полинуклеотидом, в котором полинуклеотид 181-3522 SEQ ID NO: 1 или полинуклеотид 181-3396 SEQ ID NO: 3 реаранжирован другим геном.
В данном описании определение «реаранжировка гена» относится к рекомбинации между генами, которая приводит к новому гену.
Примеры мутантных RET включают полипептиды (i)-(xi), приведенные ниже. Воплощения реаранжировки генов для полипептидов (i)-(xi), приведенных ниже, описаны в литературе, указанной в скобках.
(i) Полипептид, кодированный реаранжированным геном (также называемым «RET/PTC1») между геном RET и геном Н4 (также называемым CCDC6, спираль-спиральный домен, содержащий 6 или D10S170; GenBank, инвентарный № NM_005436) (European Journal of Cancer, 41, 816-821, 2005; Cell, 60, 557-563, 1990).
(ii) Полипептид, кодированный реаранжированным геном (также называемым «RET/PTC2») между геном RET и геном RIα (также называемым PRKARIA, сАМР-зависимый регулятор типа I альфа; GenBank, инвентарный № NM_212471) (Eur. J. Endocrinology, 147, 741-745, 2002).
(iii) Полипептид, кодированный реаранжированным геном (также называемым «RET/PTC3») между геном RET и геном ELEI (также называемым NCOA4, коактиватор ядерного рецептора 4 или RFG; GenBank, инвентарный № NM_005437) (European Journal of Cancer, 41, 816-821, 2005).
(iv) Полипептид, кодированный реаранжированным геном (также называемым «RET/PTC4») между геном RET и геном ELEI (также называемым NCOA4, коактиватор ядерного рецептора 4 или RFG; GenBank, инвентарный № NM_005437) (Oncogene, 13, 1093-1097, 1996).
(v) Полипептид, кодированный реаранжированным геном (также называемым «RET/PTC5») между геном RET и геном RFG5 (также называемым GOLGA5, golgin-84; GenBank, инвентарный № NM_005113) (Cancer Research, 58, 198-203, 1998).
(vi) Полипептид, кодированный реаранжированным геном (также называемым «RET/PTC6») между геном RET и геном hTIF (также называемым TRIM24, содержащий тройной мотив 24 или РТС6; GenBank, инвентарный № NM_003852) (Oncogene, 18, 4388-4393, 1999).
(vii) Полипептид, кодированный реаранжированным геном (также называемым «RET/PTC7») между геном RET и геном RFG7 (также называемым TRIM33, содержащий тройной мотив 33, РТС7; GenBank, инвентарный № NM_033020) (Cancer Research, 60, 2786-2789, 2000).
(viii) Полипептид, кодированный реаранжированным геном (также называемым «RET/PTC8») между геном RET и геном кинектина (также называемым KTN1, кинектин 1; GenBank, инвентарный № NM_182926) (Cancer Research, 60, 7028-7032 2000; Cancer Research, 60, 2786-2789, 2000).
(ix) Полипептид, кодированный реаранжированным геном (также называемым «RET/ELKS») между геном RET и геном ELKS (также называемым RAB6IP2 или взаимодействующий с RAB6 белок 2; GenBank, инвентарный № NM_178037) (Genes Chromosomes Cancer, 25, 97-103, 1999).
(x) Полипептид, кодированный реаранжированным геном (также называемым «RET/PCM-1») между геном RET и геном РСМ-1 (также называемым РСМ1 или перицентриолярное вещество 1; GenBank, инвентарный № NM_006197) (Oncogene, 19, 4236-4242, 2000).
(xi) Полипептид, кодированный реаранжированным геном (также называемым «RFP-RET») между геном RET и геном RFP (также называемым фингерным белком ret; GenBank, инвентарный № NM_006510) (Endocrinology, 145, 5448-5451, 2004).
Наличие или отсутствие мутации RET можно проверить через анализ последовательности гена RET или транскрипта гена RET, т.е. мРНК. Процедура анализа может представлять собой, например, метод обрыва цепи дидезоксинуклеотидом (Sanger et al. (1977), Proc. Natl. Acad. Sci. USA, 74: 5463). Последовательность можно анализировать с использованием подходящего секвенатора ДНК.
С другой стороны, наличие или отсутствие мутации RET можно проанализировать, например, таким методом как гибридизация in situ, анализ методом норзерн-блоттинга, ДНК-микроматрицы, ОФ-ПЦР или SSCP-PCR (анализ конформационного полиморфизма одноцепочечных фрагментов - ПЦР). Указанные методы можно осуществлять согласно обычным процедурам (Clinical Cancer Research, 8, 457-463, 2002).
Наличие или отсутствие мутации RET также можно проанализировать, например, иммунохимическим способом (например, иммуногистохимическим способом, иммунопреципитацией, вестерн-блоттингом, проточной цитометрией, ELISA, РИА и т.д.). Указанные методы можно осуществлять согласно обычным процедурам.
Последовательности праймеров для ПЦР для анализа наличия или отсутствия мутантной RET можно создать согласно обычной процедуре. Например, последовательности праймеров можно создать с использованием экспрессии праймеров (Perkin-Elmer Applied Biosystems).
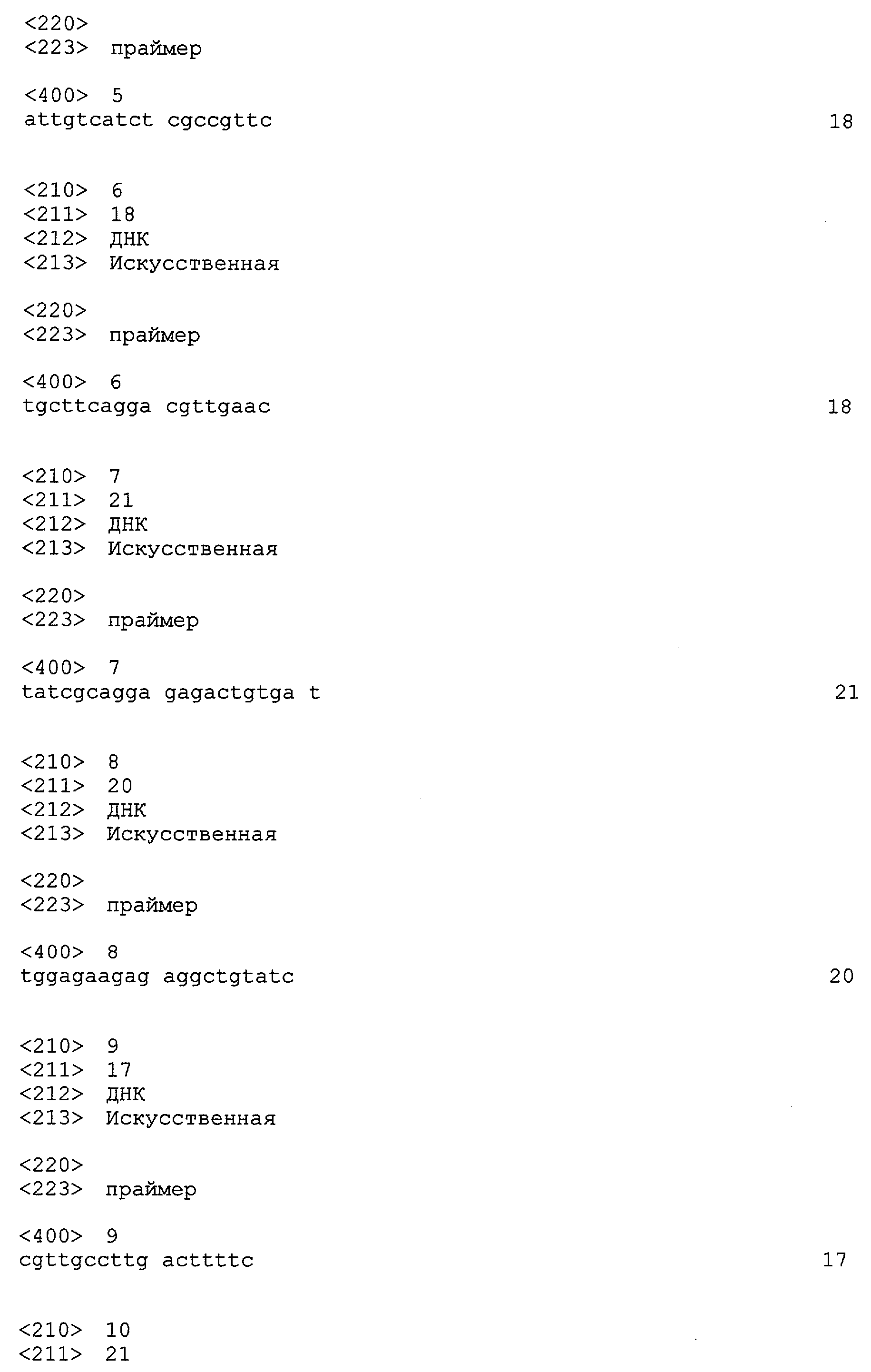
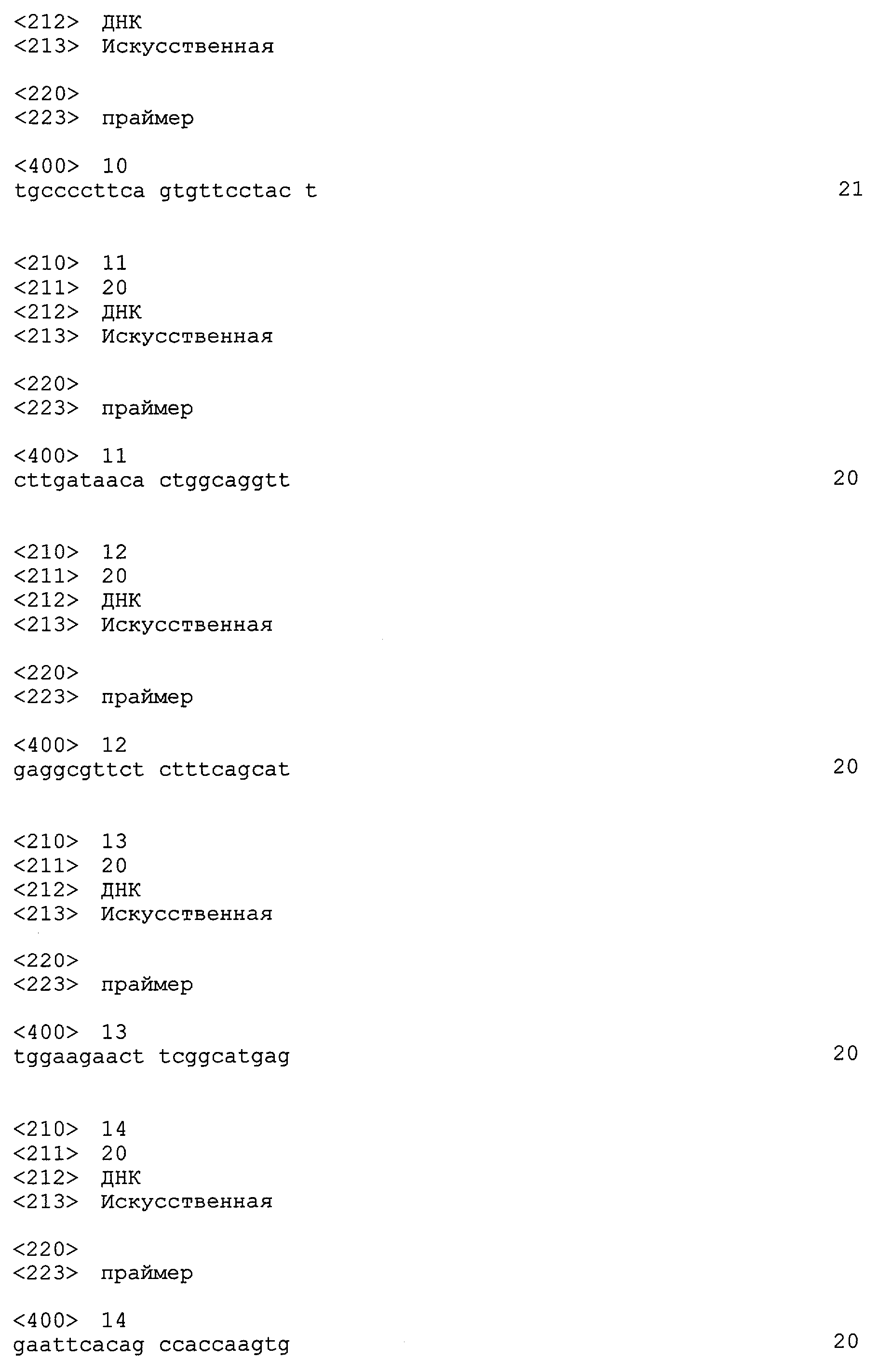
Для того чтобы проанализировать наличие или отсутствие мутантной RET, можно использовать, например, праймеры, указанные в таблице 1. Например, для анализа RET/PTC1 можно использовать полинуклеотиды с последовательностями, представленными SEQ ID NO: 5 и 6.
|
Таблица 1 показывает некоторые примеры праймеров для мутантных RET, предполагаемых для анализа.
Ниже приводятся нуклеотидные последовательности, представленные SEQ ID NOS: 5-20.
SEQ ID NO: 5 ATT GTC ATC TCG CCG TTC
SEQ ID NO: 6 TGC TTC AGG ACG TTG AAC
SEQ ID NO: 7 TAT CGC AGG AGA GAC TGT GAT
SEQ ID NO: 8 TGG AGA AGA GAG GCT GTA TC
SEQ ID NO: 9 CGT TGC CTT GAC TTT TC
SEQ ID NO: 10 TGC CCC TTC AGT GTT CCT ACT
SEQ ID NO: 11 CTT GAT AAC ACT GGC AGG TT
SEQ ID NO: 12 GAG GCG TTC TCT TTC AGC AT
SEQ ID NO: 13 TGG AAG AAC TTC GGC ATG AG
SEQ ID NO: 14 GAA TTC ACA GCC ACC AAG TG
SEQ ID NO: 15 CTA CTT AGC TTT CCA AGT GG
SEQ ID NO: 16 GGG ACA GAC ACC TTT GGA AAT A
SEQ ID NO: 17 GTTGAAGGAGTCCTTGACTG
SEQ ID NO: 18 CTTTCAGCATCTTCACGG
SEQ ID NO: 19 AGTGAAGTTTCTACCATCC
SEQ ID NO: 20 GGCGTTCTCTTTCAGCATCT
(3) Клетки, экспрессирующие мутантные RET
Согласно настоящему изобретению клетки, экспрессирующие мутантные RET, представляют собой, предпочтительно, клетки множественной эндокринной неоплазии типа IIA, множественной эндокринной неоплазии типа IIB, семейной медуллярной карциномы щитовидной железы, папиллярной карциномы щитовидной железы, спорадической медуллярной карциномы щитовидной железы, болезни Гиршспрунга, феохромоцитомы, гиперплазии паращитовидной железы или невром слизистой оболочки желудочно-кишечного тракта. С другой стороны, клетки, экспрессирующие мутантные RET, согласно настоящему изобретению, представляют собой, предпочтительно, клетки карциномы щитовидной железы.
(4) Ингибирующее киназу RET вещество по изобретению
В данном описании термин «атом галогена» относится к атому фтора, атому хлора, атому брома или атому йода.
Предпочтительные примеры «атома галогена» включают атом фтора и атом хлора.
В данном описании термин «С1-6-алкильная группа» относится к линейной или разветвленной алкильной группе с числом атомов углерода 1-6, причем конкретными примерами являются метильная группа, этильная группа, 1-пропильная группа (н-пропильная группа), 2-пропильная группа (изопропильная группа), 2-метил-1-пропильная группа (изобутильная группа), 2-метил-2-пропильная группа (трет-бутильная группа), 1-бутильная группа (н-бутильная группа), 2-бутильная группа (втор-бутильная группа), 1-пентильная группа, 2-пентильная группа, 3-пентильная группа, 2-метил-1-бутильная группа, 3-метил-1-бутильная группа, 2-метил-2-бутильная группа, 3-метил-2-бутильная группа, 2,2-диметил-1-пропильная группа, 1-гексильная группа, 2-гексильная группа, 3-гексильная группа, 2-метил-1-пентильная группа, 3-метил-1-пентильная группа, 4-метил-1-пентильная группа, 2-метил-2-пентильная группа, 3-метил-2-пентильная группа, 4-метил-2-пентильная группа, 2-метил-3-пентильная группа, 3-метил-3-пентильная группа, 2,3-диметил-1-бутильная группа, 3,3-диметил-1-бутильная группа, 2,2-диметил-1-бутильная группа, 2-этил-1-бутильная группа, 3,3-диметил-2-бутильная группа и 2,3-диметил-2-бутильная группа.
Предпочтительные примеры «С1-6-алкильной группы» включают метильную группу, этильную группу, 1-пропильную группу, 2-пропильную группу, 2-метил-1-пропильную группу, 2-метил-2-пропильную группу, 1-бутильную группу и 2-бутильную группу.
В данном описании термин «С1-6-алкиленовая группа» относится к двухвалентной группе, образованной от указанной выше «С1-6-алкильной группы» удалением из нее одного атома водорода, и конкретные примеры включают метиленовую группу, 1,2-этиленовую группу, 1,1-этиленовую группу, 1,3-пропиленовую группу, тетраметиленовую группу, пентаметиленовую группу и гексаметиленовую группу.
В данном описании термин «С2-6-алкенильная группа» относится к линейной или разветвленной алкенильной группе с одной двойной связью и числом атомов углерода 2-6, и конкретные примеры включают этенильную группу (винильную группу), 1-пропенильную группу, 2-пропенильную группу (аллильную группу), 1-бутенильную группу, 2-бутенильную группу, 3-бутенильную группу, пентенильную группу и гексенильную группу.
В данном описании термин «С2-6-алкинильная группа» относится к линейной или разветвленной алкинильной группе с одной тройной связью и числом атомов углерода 2-6, и конкретные примеры включают этинильную группу, 1-пропинильную группу, 2-пропинильную группу, 1-бутинильную группу, 2-бутинильную группу, 3-бутинильную группу, пентинильную группу и гексинильную группу.
В данном описании термин «С3-8-циклоалкильная группа» относится к моноциклической или бициклической насыщенной алифатической углеводородной группе с числом атомов углерода 3-8, и конкретные примеры включают циклопропильную группу, циклобутильную группу, циклопентильную группу, циклогексильную группу, циклогептильную группу, циклооктильную группу, бицикло[2.1.0]пентильную группу, бицикло[3.1.0]гексильную группу, бицикло[2.1.1]гексильную группу, бицикло[4.1.0]гептильную группу, бицикло[2.2.2]гептильную группу (норборнильную группу), бицикло[3.3.0]октильную группу, бицикло[3.2.1]октильную группу и бицикло[2.2.2]октильную группу.
Предпочтительные примеры «С3-8-циклоалкильной группы» включают циклопропильную группу, циклобутильную группу и циклопентильную группу.
В данном описании термин «С6-10-арильная группа» относится к ароматической углеводородной циклической группе с числом атомов углерода 6-10, и конкретные примеры включают фенильную группу, 1-нафтильную группу, 2-нафтильную группу, инденильную группу и азуленильную группу.
Предпочтительным примером «С6-10-арильной группы» является фенильная группа.
В данном описании термин «гетероатом» относится к атому азота, атому кислорода или атому серы.
В данном описании термин «5-10-членная гетероарильная группа» относится к ароматической циклической группе с 5-10 атомами, образующими цикл, включающими 1-5 гетероатомов, и конкретные примеры включают фурильную группу, тиенильную группу, пирролильную группу, имидазолильную группу, триазолильную группу, тетразолильную группу, тиазолильную группу, пиразолильную группу, оксазолильную группу, изоксазолильную группу, изотиазолильную группу, фуразанильную группу, тиадиазолильную группу, оксадиазолильную группу, пиридильную группу, пиразинильную группу, пиридазинильную группу, пиримидинильную группу, триазинильную группу, пуринильную группу, птеридильную группу, хинолинильную группу, изохинолинильную группу, нафтиридинильную группу, хиноксалинильную группу, циннолинильную группу, хиназолинильную группу, фталазинильную группу, имидазопиридильную группу, имидазотиазолильную группу, имидазооксазолильную группу, бензотиазолильную группу, бензооксазолильную группу, бензимидазолильную группу, индолильную группу, изоиндолильную группу, индазолильную группу, пирролопиридильную группу, тиенопиридильную группу, фуропиридильную группу, бензотиадиазолильную группу, бензооксадиазолильную группу, пиридопиримидинильную группу, бензофурильную группу, бензотиенильную группу и тиенофурильную группу.
Предпочтительные примеры «5-10-членной гетероарильной группы» включают фурильную группу, тиенильную группу, пирролильную группу, имидазолильную группу, тиазолильную группу, пиразолильную группу, оксазолильную группу, изоксазолильную группу, изотиазолильную группу, пиридильную группу и пиримидинильную группу.
В данном описании термин «3-10-членная неароматическая гетероциклическая группа»
(а) имеет 3-10 атомов, образующих цикл;
(b) имеет 1-2 гетероатома, входящих в число атомов, образующих цикл;
(с) может включать 1-2 двойные связи в цикле;
(d) может иметь 1-3 карбонильные группы, сульфинильные группы или сульфонильные группы в цикле; и
(е) представляет собой неароматическую моноциклическую или бициклическую группу, где в случае, когда атом азота входит в число атомов, образующих цикл, атом азота может иметь свободную связь.
Конкретными примерами являются азиридинильная группа, азетидинильная группа, пирролидинильная группа, пиперидинильная группа, азепанильная группа, азоканильная группа, пиперазинильная группа, диазепанильная группа, диазоканильная группа, диазабицикло[2.2.1]гептильная группа, морфолинильная группа, тиоморфолинильная группа, 1,1-диоксотиоморфолинильная группа, оксиранильная группа, оксетанильная группа, тетрагидрофуранильная группа, диоксоранильная группа, тетрагидропиранильная группа, диоксанильная группа, тетрагидротиенильная группа, тетрагидротиопиранильная группа, оксазолидинильная группа и тиазолидинильная группа.
Предпочтительными примерами «3-10-членной неароматической гетероциклической группы» являются азиридинильная группа, азетидинильная группа, пирролидинильная группа, пиперидинильная группа, азепанильная группа, пиперазинильная группа, диазепанильная группа, морфолинильная группа, тиоморфолинильная группа, 1,1-диоксотиоморфолинильная группа, тетрагидрофуранильная группа и тетрагидропиранильная группа.
В данном описании термин «С1-6-алкоксигруппа» относится к группе, в которой атом кислорода связан с концевой «С1-6-алкильной группой», имеющей значения, указанные выше, и конкретными примерами являются метоксигруппа, этоксигруппа, 1-пропоксигруппа (н-пропоксигруппа), 2-пропоксигруппа (изопропоксигруппа), 2-метил-1-пропоксигруппа (изобутоксигруппа), 2-метил-2-пропоксигруппа (трет-бутоксигруппа), 1-бутоксигруппа (н-бутоксигруппа), 2-бутоксигруппа (втор-бутоксигруппа), 1-пентилоксигруппа, 2-пентилоксигруппа, 3-пентилоксигруппа, 1-метил-1-бутоксигруппа, 3-метил-1-бутоксигруппа, 2-метил-2-бутоксигруппа, 3-метил-2-бутоксигруппа, 2,2-диметил-1-пропоксигруппа, 1-гексилоксигруппа, 2-гексилоксигруппа, 3-гексилоксигруппа, 2-метил-1-пентилоксигруппа, 3-метил-1-пентилоксигруппа, 4-метил-1-пентилоксигруппа, 2-метил-2-пентилоксигруппа, 3-метил-2-пентилоксигруппа, 4-метил-2-пентилоксигруппа, 2-метил-3-пентилоксигруппа, 3-метил-3-пентилоксигруппа, 2,3-диметил-1-бутоксигруппа, 3,3-диметил-1-бутоксигруппа, 2,2-диметил-1-бутоксигруппа, 2-этил-1-бутоксигруппа, 3,3-диметил-2-бутоксигруппа и 2,3-диметил-2-бутоксигруппа.
Предпочтительными примерами «С1-6-алкоксигруппы» являются метоксигруппа, этоксигруппа, 1-пропоксигруппа, 2-пропоксигруппа, 2-метил-1-пропоксигруппа, 2-метил-2-пропоксигруппа, 1-бутоксигруппа и 2-бутоксигруппа.
В данном описании термин «С1-6-алкилтиогруппа» относится к группе, в которой атом серы связан с концевой «С1-6-алкильной группой», имеющей значения, указанные выше, и конкретными примерами являются метилтиогруппа, этилтиогруппа, 1-пропилтиогруппа (н-пропилтиогруппа), 2-пропилтиогруппа (изопропилтиогруппа), 2-метил-1-пропилтиогруппа (изобутилтиогруппа), 2-метил-2-пропилтиогруппа (трет-бутилтиогруппа), 1-бутилтиогруппа (н-бутилтиогруппа), 2-бутилтиогруппа (втор-бутилтиогруппа), 1-пентилтиогруппа, 2-пентилтиогруппа, 3-пентилтиогруппа, 2-метил-1-бутилтиогруппа, 3-метил-1-бутилтиогруппа, 2-метил-2-бутилтиогруппа, 3-метил-2-бутилтиогруппа, 2,2-диметил-1-пропилтиогруппа, 1-гексилтиогруппа, 2-гексилтиогруппа, 3-гексилтиогруппа, 2-метил-1-пентилтиогруппа, 3-метил-1-пентилтиогруппа, 4-метил-1-пентилтиогруппа, 2-метил-2-пентилтиогруппа, 3-метил-2-пентилтиогруппа, 4-метил-2-пентилтиогруппа, 2-метил-3-пентилтиогруппа, 3-метил-3-пентилтиогруппа, 2,3-диметил-1-бутилтиогруппа, 3,3-диметил-1-бутилтиогруппа, 2,2-диметил-1-бутилтиогруппа, 2-этил-1-бутилтиогруппа, 3,3-диметил-2-бутилтиогруппа и 2,3-диметил-2-бутилтиогруппа.
Предпочтительными примерами «С1-6-алкилтиогруппы» являются метилтиогруппа, этилтиогруппа, 1-пропилтиогруппа (н-пропилтиогруппа), 2-пропилтиогруппа (изопропилтиогруппа), 2-метил-1-пропилтиогруппа (изобутилтиогруппа), 2-метил-2-пропилтиогруппа (трет-бутилтиогруппа), 1-бутилтиогруппа (н-бутилтиогруппа) и 2-бутилтиогруппа (втор-бутилтиогруппа).
В данном описании термин «С3-8-циклоалкоксигруппа» относится к группе, в которой атом кислорода связан с концевой «С3-8-циклоалкильной группой», имеющей значения, указанные выше, и конкретными примерами являются циклопропоксигруппа, циклобутоксигруппа, циклопентилоксигруппа, циклогексилоксигруппа, циклогептилоксигруппа, циклооктилоксигруппа, бицикло[2.1.0]пентилоксигруппа, бицикло[3.1.0]гексилоксигруппа, бицикло[2.1.1]гексилоксигруппа, бицикло[4.1.0]гептилоксигруппа, бицикло[2.2.1]гептилоксигруппа (норборнилоксигруппа), бицикло[3.3.0]октилоксигруппа, бицикло[3.2.1]октилоксигруппа и бицикло[2.2.2]октилоксигруппа.
Предпочтительными примерами «С3-8-циклоалкоксигруппы» являются циклопропоксигруппа, циклобутоксигруппа и циклопентилоксигруппа.
В данном описании термин «моно-С1-6-алкиламиногруппа» относится к группе, в которой атом водорода в аминогруппе заменен «С1-6-алкильной группой», имеющей значения, указанные выше, и конкретными примерами являются метиламиногруппа, этиламиногруппа, 1-пропиламиногруппа (н-пропиламиногруппа), 2-пропиламиногруппа (изопропиламиногруппа), 2-метил-1-пропиламиногруппа (изобутиламиногруппа), 2-метил-2-пропиламиногруппа (трет-бутиламиногруппа), 1-бутиламиногруппа (н-бутиламиногруппа), 2-бутиламиногруппа (втор-бутиламиногруппа), 1-пентиламиногруппа, 2-пентиламиногруппа, 3-пентиламиногруппа, 2-метил-1-бутиламиногруппа, 3-метил-1-бутиламиногруппа, 2-метил-2-бутиламиногруппа, 3-метил-2-бутиламиногруппа, 2,2-диметил-1-пропиламиногруппа, 1-гексиламиногруппа, 2-гексиламиногруппа, 3-гексиламиногруппа, 2-метил-1-пентиламиногруппа, 3-метил-1-пентиламиногруппа, 4-метил-1-пентиламиногруппа, 2-метил-2-пентиламиногруппа, 3-метил-2-пентиламиногруппа, 4-метил-2-пентиламиногруппа, 2-метил-3-пентиламиногруппа, 3-метил-3-пентиламиногруппа, 2,3-диметил-1-бутиламиногруппа, 3,3-диметил-1-бутиламиногруппа, 2,2-диметил-1-бутиламиногруппа, 2-этил-1-бутиламиногруппа, 3,3-диметил-2-бутиламиногруппа и 2,3-диметил-2-бутиламиногруппа.
В данном описании термин «ди-С1-6-алкиламиногруппа» относится к группе, в которой два атома водорода в аминогруппе заменены идентичными или различными «С1-6-алкильными группами», имеющими значения, указанные выше, и конкретными примерами являются N,N-диметиламиногруппа, N,N-диэтиламиногруппа, N,N-ди-н-пропиламиногруппа, N,N-диизопропиламиногруппа, N,N-ди-н-бутиламиногруппа, N,N-диизобутиламиногруппа, N,N-ди-втор-бутиламиногруппа, N,N-ди-трет-бутиламиногруппа, N-этил-N-метиламиногруппа, N-н-пропил-N-метиламиногруппа, N-изопропил-N-метиламиногруппа, N-н-бутил-N-метиламиногруппа, N-изобутил-N-метиламиногруппа, N-втор-бутил-N-метиламиногруппа и N-трет-бутил-N-метиламиногруппа.
В данном описании термин «С2-7-ацильная группа» относится к карбонильной группе, связанной с «С1-6-алкильной группой», имеющей значения, указанные выше, и конкретными примерами являются ацетильная группа, пропионильная группа, изопропионильная группа, бутирильная группа, изобутирильная группа, валерильная группа, изовалерильная группа и пивалоильная группа.
В данном описании термин «С2-7-алкоксикарбонильная группа» относится к карбонильной группе, связанной с «С1-6-алкоксигруппой», имеющей значения, указанные выше, и конкретными примерами являются метоксикарбонильная группа, этоксикарбонильная группа, 1-пропоксикарбонильная группа, 2-пропоксикарбонильная группа и 2-метил-2-пропоксикарбонильная группа.
В данном описании выражение «который может иметь заместитель» означает, что могут иметься один или несколько заместителей в замещаемых положениях в любом сочетании, и конкретные примеры заместителя включают атом галогена, гидроксильную группу, тиольную группу, нитрогруппу, цианогруппу, формильную группу, карбоксильную группу, аминогруппу, силильную группу, метансульфонильную группу, С1-6-алкильную группу, С2-6-алкенильную группу, С2-6-алкинильную группу, С3-8-циклоалкильную группу, С6-10-арильную группу, 5-10-членную гетероарильную группу, 3-10-членную неароматическую гетероциклическую группу, С1-6-алкоксигруппу, С1-6-алкилтиогруппу, С3-8-циклоалкоксигруппу, моно-С1-6-алкиламиногруппу, ди-С1-6-алкиламиногруппу, С2-7-ацильную группу и С2-7-алкоксикарбонильную группу. В данном случае С1-6-алкильная группа, С2-6-алкенильная группа, С2-6-алкинильная группа, С3-8-циклоалкильная группа, С6-10-арильная группа, 5-10-членная гетероарильная группа, 3-10-членная неароматическая гетероциклическая группа, С1-6-алкоксигруппа, С1-6-алкилтиогруппа, С3-8-циклоалкоксигруппа, моно-С1-6-алкиламиногруппа, ди-С1-6-алкиламиногруппа, С2-7-ацильная группа и С2-7-алкоксикарбонильная группа, каждая независимо, может иметь 1-3 группы, выбранных из группы, состоящей из заместителей, перечисленных далее.
Заместители
Атом галогена, гидроксильная группа, тиольная группа, нитрогруппа, цианогруппа, С1-6-алкильная группа, С3-8-циклоалкильная группа, С2-6-алкенильная группа, С2-6-алкинильная группа, С6-10-арильная группа, 5-10-членная гетероарильная группа, 3-10-членная неароматическая гетероциклическая группа, С1-6-алкоксигруппа и С1-6-алкилтиогруппа.
Согласно настоящему изобретению вещество, ингибирующее киназу RET, может представлять собой, например, соединение, представленное общей формулой (I)

(i) R1
R1 представляет собой группу, представленную формулой -V1-V2-V3 (где V1 представляет собой С1-6-алкиленовую группу, которая может иметь заместитель; V2 представляет собой простую связь, атом кислорода, атом серы, карбонильную группу, сульфинильную группу, сульфонильную группу, группу, представленную формулой -CONR6-, группу, представленную формулой -SO2NR6-, группу, представленную формулой -NR6SO2-, группу, представленную формулой -NR6CO-, или группу, представленную формулой -NR6- (где R6 представляет собой атом водорода, С1-6-алкильную группу, которая может иметь заместитель, или С3-8-циклоалкильную группу, которая может иметь заместитель); V3 представляет собой атом водорода, С1-6-алкильную группу, которая может иметь заместитель, С2-6-алкенильную группу, которая может иметь заместитель, С2-6-алкинильную группу, которая может иметь заместитель, С3-8-циклоалкильную группу, которая может иметь заместитель, С6-10-арильную группу, которая может иметь заместитель, 5-10-членную гетероарильную группу, которая может иметь заместитель, или 3-10-членную неароматическую гетероциклическую группу, которая может иметь заместитель).
Предпочтительным примером R1 является С1-6-алкильная группа. В данном случае R1 может иметь заместитель, выбранный из 3-10-членной неароматической гетероциклической группы, которая может содержать С1-6-алкильную группу, гидроксильную группу, С1-6-алкоксигруппу, аминогруппу, моно-С1-6-алкиламиногруппу и ди-С1-6-алкиламиногруппу.
Более предпочтительные примеры R1 включают метильную группу и группу, представленную одной из формул
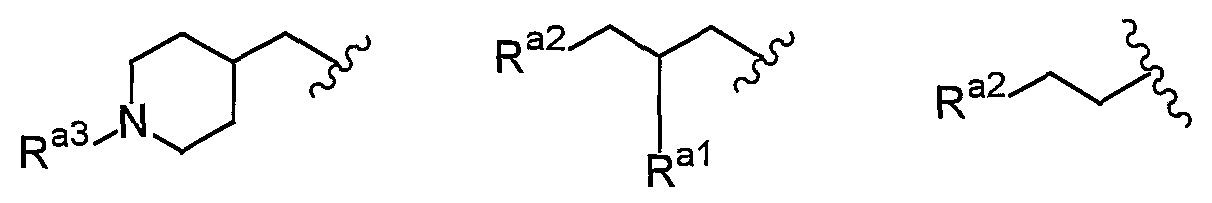
(где Ra3 представляет собой метильную группу; Ra1 представляет собой атом водорода или гидроксильную группу; Ra2 представляет собой метоксигруппу, этоксигруппу, 1-пирролидинильную группу, 1-пиперидинильную группу, 4-морофолинильную группу, диметиламиногруппу или диэтиламиногруппу).
Еще более предпочтительные примеры R1 включают метильную группу и 2-метоксиэтильную группу.
(ii) R2
R2 представляет собой цианогруппу, С1-6-алкоксигруппу, которая может иметь заместитель, карбоксильную группу, С2-7-алкоксикарбонильную группу, которая может иметь заместитель, или группу, представленную формулой -CONVa11Va12 (где Va11 представляет собой атом водорода, С1-6-алкильную группу, которая может иметь заместитель, С2-6-алкенильную группу, которая может иметь заместитель, С2-6-алкинильную группу, которая может иметь заместитель, С3-8-циклоалкильную группу, которая может иметь заместитель, С6-10-арильную группу, которая может иметь заместитель, 5-10-членную гетероарильную группу, которая может иметь заместитель, или 3-10-членную неароматическую гетероциклическую группу, которая может иметь заместитель; Va12 представляет собой атом водорода, С1-6-алкильную группу, которая может иметь заместитель, С2-6-алкенильную группу, которая может иметь заместитель, С2-6-алкинильную группу, которая может иметь заместитель, С3-8-циклоалкильную группу, которая может иметь заместитель, С6-10-арильную группу, которая может иметь заместитель, 5-10-членную гетероарильную группу, которая может иметь заместитель, 3-10-членную неароматическую гетероциклическую группу, которая может иметь заместитель, гидроксильную группу, С1-6-алкоксигруппу, которая может иметь заместитель, или С3-8-циклоалкоксигруппу, которая может иметь заместитель).
Предпочтительные примеры R2 включают цианогруппу или группу, представленную формулой -CONVa11Va12 (где Va11 и Va12 имеют значения, указанные выше).
Более предпочтительные примеры R2 включают цианогруппу или группу, представленную формулой -CONHVa16 (где Va16 представляет собой атом водорода, С1-6-алкильную группу, С3-8-циклоалкильную группу, С1-6-алкоксигруппу или С3-8-циклоалкоксигруппу, где Va16 может иметь, по меньшей мере, один заместитель, выбранный из атома галогена, цианогруппы, гидроксильной группы и С1-6-алкоксигруппы).
Еще более предпочтительным примером R2 является группа, представленная формулой -CONHVa17 (где Va17 представляет собой атом водорода, С1-6-алкильную группу или С1-6-алкоксигруппу).
Наиболее предпочтительным примером R2 является группа, представленная формулой -CONHVa18 (где Va18 представляет собой атом водорода, метильную группу или метоксигруппу).
(iii) Y1
Y1 представляет собой группу, представленную формулой
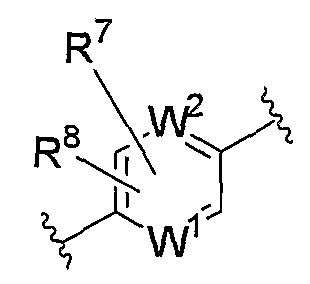 или
или 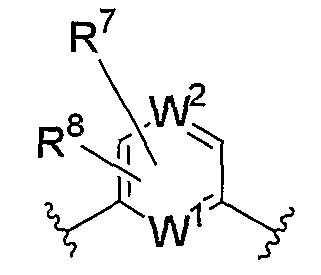
где R7 и R8, каждый независимо, представляет собой атом водорода, атом галогена, цианогруппу, нитрогруппу, аминогруппу, С1-6-алкильную группу, которая может иметь заместитель, С3-8-циклоалкильную группу, которая может иметь заместитель, С1-6-алкоксигруппу, которая может иметь заместитель, С1-6-алкилтиогруппу, которая может иметь заместитель, С2-7-ацильную группу, которая может иметь заместитель, С2-7-алкоксикарбонильную группу, которая может иметь заместитель, или группу, представленную формулой -CONVd1Vd2 (где Vd1 и Vd2, каждый независимо, представляет собой атом водорода или С1-6-алкильную группу, которая может иметь заместитель; и
W1 и W2, каждый независимо, представляет собой атом углерода или атом азота, который может иметь заместитель.
Предпочтительным примером Y1 является группа, представленная формулой
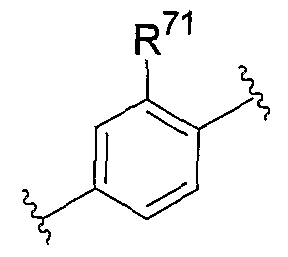
(где R71 представляет собой атом водорода или атом галогена).
(iv) R3 и R4
R3 и R4, каждый независимо, представляет собой атом водорода, С1-6-алкильную группу, которая может иметь заместитель, С2-6-алкенильную группу, которая может иметь заместитель, С2-6-алкинильную группу, которая может иметь заместитель, С3-8-циклоалкильную группу, которая может иметь заместитель, С2-7-ацильную группу, которая может иметь заместитель, или С2-7-алкоксикарбонильную группу, которая может иметь заместитель.
Предпочтительным примером R3 и R4 является атом водорода.
(v) R5
R5 представляет собой атом водорода, С1-6-алкильную группу, которая может иметь заместитель, С2-6-алкенильную группу, которая может иметь заместитель, С2-6-алкинильную группу, которая может иметь заместитель, С3-8-циклоалкильную группу, которая может иметь заместитель, С6-10-арильную группу, которая может иметь заместитель, 5-10-членную гетероарильную группу, которая может иметь заместитель, или 3-10-членную неароматическую гетероциклическую группу, которая может иметь заместитель.
Предпочтительные примеры R5 включают атом водорода, С1-6-алкильную группу, которая может иметь заместитель, С2-6-алкенильную группу, которая может иметь заместитель, С2-6-алкинильную группу, которая может иметь заместитель, С3-8-циклоалкильную группу, которая может иметь заместитель, С6-10-арильную группу, которая может иметь заместитель, или 3-10-членную неароматическую гетероциклическую группу, которая может иметь заместитель.
Более предпочтительные примеры R5 включают атом водорода, С1-6-алкильную группу, С3-8-циклоалкильную группу и С6-10-арильную группу (где R5 может иметь, по меньшей мере, один заместитель, выбранный из группы, состоящей из атома галогена и метансульфонильной группы).
Более предпочтительные примеры R5 включают метильную группу, этильную группу или циклопропильную группу.
Кроме того, предпочтительными примерами соединения, представленного общей формулой (I), являются
N-(4-(6-циано-7-(2-метоксиэтокси)-4-хинолил)окси-2-фторфенил)-N'-(4-фторфенил)мочевина;
N-(2-хлор-4-((6-циано-7-((1-метил-4-пиперидил)метокси)-4-хинолил)окси)фенил)-N'-циклопропилмочевина;
N-(4-((6-циано-7-(((2R)-3-(диэтиламино)-2-гидроксипропил)окси)-4-хинолил)окси)фенил)-N'-(4-фторфенил)мочевина;
N-(4-((6-циано-7-(((2R)-2-гидрокси-3-(1-пирролидино)пропил)окси)-4-хинолил)окси)фенил)-N'-(4-фторфенил)мочевина;
4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид;
4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-(2-метоксиэтокси)-6-хинолинкарбоксамид;
N6-циклопропил-4-(3-хлор-4-(((циклопропиламино)карбонил)амино)фенокси)-7-метокси-6-хинолинкарбоксамид;
N6-(2-метоксиэтокси)-4-(3-хлор-4-(((циклопропиламино)карбонил)амино)фенокси)-7-метокси-6-хинолинкарбоксамид;
N6-(2-фторэтил)-4-(3-хлор-4-(((циклопропиламино)карбонил)амино)фенокси)-7-метокси-6-хинолинкарбоксамид;
N6-метокси-4-(3-хлор-4-(((циклопропиламино)карбонил)амино)фенокси)-7-метокси-6-хинолинкарбоксамид;
N6-метил-4-(3-хлор-4-(((циклопропиламино)карбонил)амино)фенокси)-7-метокси-6-хинолинкарбоксамид;
N6-этил-4-(3-хлор-4-(((циклопропиламино)карбонил)амино)фенокси)-7-метокси-6-хинолинкарбоксамид;
4-(3-фтор-4-(циклопропиламинокарбонил)аминофенокси)-7-(2-метоксиэтокси)-6-хинолинкарбоксамид;
4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-(2-гидроксиэтокси)-6-хинолинкарбоксамид;
4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-((2S)-2,3-дигидроксипропил)окси)-6-хинолинкарбоксамид;
4-(3-хлор-4-(метиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид;
4-(3-хлор-4-(этиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид;
N6-метокси-4-(3-хлор-4-(((этиламино)карбонил)амино)фенокси)-7-метокси-6-хинолинкарбоксамид;
4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-(2-этоксиэтокси)-6-хинолинкарбоксамид;
4-(4-((циклопропиламино)карбонил)аминофенокси)-7-(2-метоксиэтокси)-6-хинолинкарбоксамид;
N-(2-фтор-4-((6-карбамоил-7-метокси-4-хинолил)окси)фенил)-N'-циклопропилмочевина;
N6-(2-гидроксиэтил)-4-(3-хлор-4-(((циклопропиламино)карбонил)амино)фенокси)-7-метокси-6-хинолинкарбоксамид;
4-(3-хлор-4-(1-пропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид;
4-(3-хлор-4-(цис-2-фторциклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид;
N6-метил-4-(3-хлор-4-(((циклопропиламино)карбонил)амино)фенокси)-7-(2-метоксиэтокси)-6-хинолинкарбоксамид;
N6-метил-4-(3-хлор-4-(((этиламино)карбонил)амино)фенокси)-7-метокси-6-хинолинкарбоксамид;
4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-(2-(4-морфолино)этокси)-6-хинолинкарбоксамид;
4-(3-хлор-4-(2-фторэтиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид;
N6-((2R)-тетрагидро-2-фуранилметил)-4-(3-хлор-4-(((метиламино)карбонил)амино)фенокси)-7-метокси-6-хинолинкарбоксамид;
4-(3-фтор-4-(этиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид;
4-(3-хлор-4-(((циклопропиламино)карбонил)амино)фенокси)-7-((2R)-2-гидрокси-3-(1-пирролидино)пропокси)-6-хинолинкарбоксамид;
N6-метил-4-(3-хлор-4-(((метиламино)карбонил)амино)фенокси)-7-((2R)-3-диэтиламино-2-гидроксипропокси)-6-хинолинкарбоксамид;
N6-метил-4-(3-хлор-4-(((этиламино)карбонил)амино)фенокси)-7-((2R)-3-диэтиламино-2-гидроксипропокси)-6-хинолинкарбоксамид;
N6-метил-4-(3-хлор-4-(((метиламино)карбонил)амино)фенокси)-7-((2R)-2-гидрокси-3-(1-пирролидино)пропокси)-6-хинолинкарбоксамид;
N6-метил-4-(3-хлор-4-(((этиламино)карбонил)амино)фенокси)-7-((2R)-2-гидрокси-3-(1-пирролидино)пропокси)-6-хинолинкарбоксамид;
N6-метил-4-(3-хлор-4-(((метиламино)карбонил)амино)фенокси)-7-((1-метил-4-пиперидил)метокси)-6-хинолинкарбоксамид;
N6-метил-4-(3-хлор-4-(((этиламино)карбонил)амино)фенокси)-7-((1-метил-4-пиперидил)метокси)-6-хинолинкарбоксамид;
N-(4-(6-циано-7-(2-метоксиэтокси)-4-хинолил)окси-2-фторфенил)-N'-циклопропилмочевина;
N-(4-(6-циано-7-(3-(4-морфолино)пропокси)-4-хинолил)оксифенил)-N'-(3-метилсульфонил)фенил)мочевина;
4-(4-((циклопропиламино)карбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид;
4-(3-фтор-4-((2-фторэтиламино)карбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид;
N6-(2-этоксиэтил)-4-(3-хлор-4-(((метиламино)карбонил)амино)фенокси)-7-метокси-6-хинолинкарбоксамид;
(2-цианоэтил)амид 4-(4-(3-этилуреидо)-3-фторфенокси)-7-метоксихинолин-6-карбоновой кислоты и
N-(4-(6-(2-цианоэтил)карбамоил-7-метокси-4-хинолил)окси-2-фторфенил)-N'-циклопропилмочевина.
Более предпочтительными примерами соединений, представленных общей формулой (I), являются
4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид;
4-(3-хлор-4-(этиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид;
N6-метокси-4-(3-хлор-4-(((циклопропиламино)карбонил)амино)фенокси)-7-метокси-6-хинолинкарбоксамид;
4-(3-хлор-4-(метиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид и
N6-метокси-4-(3-хлор-4-(((этиламино)карбонил)амино)фенокси)-7-метокси-6-хинолинкарбоксамид.
Еще более предпочтительным примером соединений, представленных общей формулой (I), является 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид (см. формулу (II)).
Наиболее предпочтительным примером вещества, ингибирующего киназу RET, является метансульфонат 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамида.
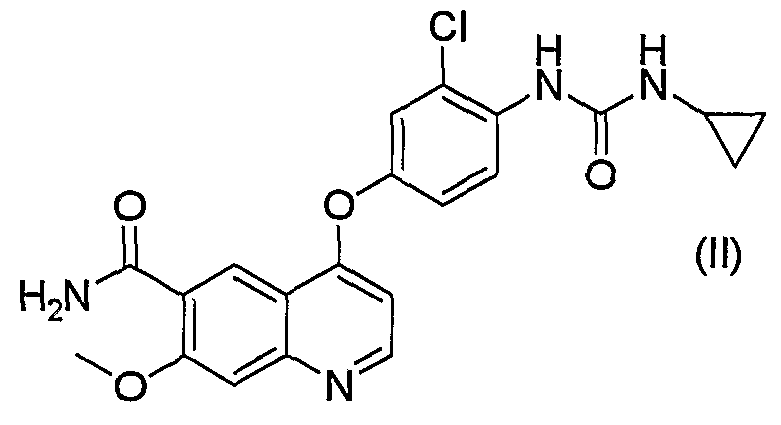
Соединение, представленное общей формулой (I), можно получить известными способами, например способами, описанными в брошюре международной публикации № 02/32872 (WO 02/32872) и брошюре международной публикации № 2005/063713 (WO 2005/063713).
Кроме того, ингибирующим киназу RET веществом по изобретению является, например, (2-диэтиламиноэтил)амид 5-(5-фтор-2-оксо-1,2-дигидроиндол-3-илиденметил)-2,4-диметил-1Н-пиррол-3-карбоновой кислоты (далее в настоящем описании называемый также “SU11248”, Clinical Cancer Research, 9, 327-337, 2003; Journal of Medicinal Chemistry, 46: 1116-9, 2003; WO 01/060814 (см. формулу (III))
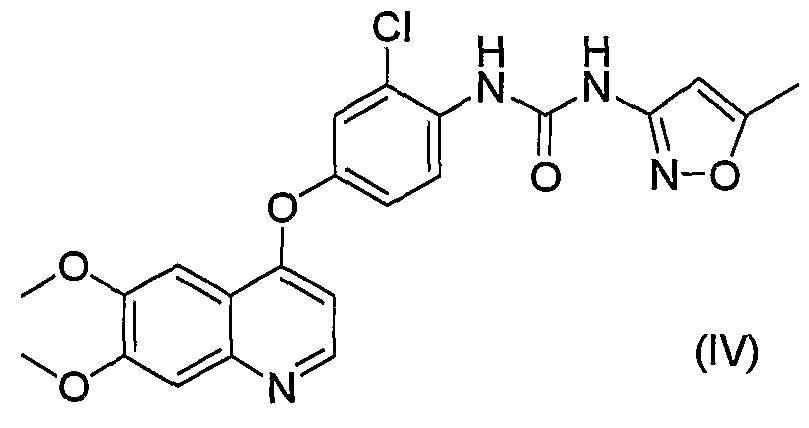
N-{2-хлор-4-[(6,7-диметокси-4-хинолил)окси]фенил}-N'-(5-метил-3-изоксазолил)мочевина (далее в настоящем описании называемая также “KRN951”; WO 02/088110) (см. формулу (IV))
 и
и
4-[(4-фтор-2-метилиндол-5-ил)окси]-6-метокси-7-[3-(пирролидин-1-ил)пропокси]хиназолин (далее в настоящем описании называемый также “AZD2171”; Cancer Research, 65: 4389-400, 2005; WO 00/47212) (см. формулу (V))
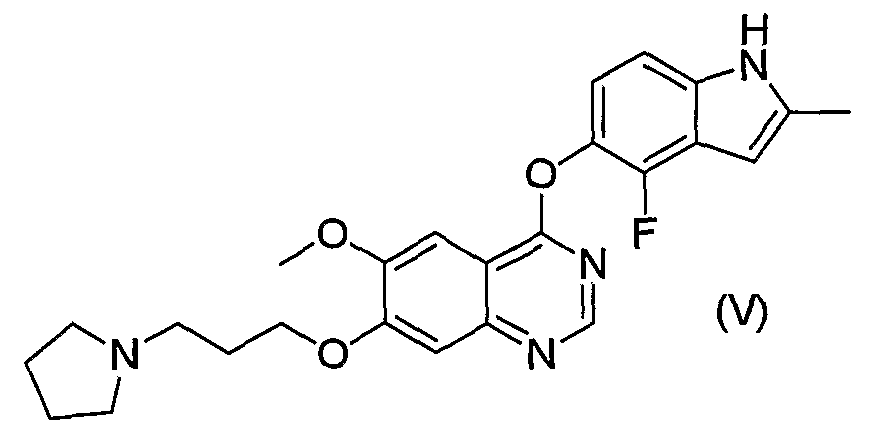
SU11248, KRN951 и AZD2171 можно получить согласно известным способам. Их можно получить, например, согласно способам, описанным в соответствующей литературе.
Согласно настоящему изобретению вещество, ингибирующее киназу RET, может образовывать фармакологически приемлемую соль с кислотой или основанием. Согласно настоящему изобретению вещество, ингибирующее киназу RET, также включает такие фармакологические приемлемые соли. Примеры солей, образованных с кислотами, включают соли неорганических кислот, такие как гидрохлориды, гидробромиды, сульфаты и фосфаты, и соли органических кислот, таких как муравьиная кислота, молочная кислота, янтарная кислота, фумаровая кислота, малеиновая кислота, лимонная кислота, винная кислота, стеариновая кислота, бензойная кислота, метансульфоновая кислота, бензолсульфоновая кислота, п-толуолсульфоновая кислота и трифторуксусная кислота. Примеры солей, образованных с основаниями, включают соли щелочных металлов, такие как натриевые соли и калиевые соли, соли щелочноземельных металлов, такие как кальциевые и магниевые соли, соли оргнаических оснований, таких как триметиламин, триэтиламин, пиридин, пиколин, дициклогексиламин, N,N'-дибензилэтилендиамин, аргинин и лизин, и аммониевые соли.
Кроме того, согласно настоящему изобретению вещество, ингибирующее киназу RET, также включает сольваты и энантиомеры указанных соединений, если они существуют. Примеры сольватов включают гидраты и негидраты, предпочтительно гидраты. Примеры растворителей включают воду, спирты (например, метанол, этанол, н-пропанол) и диметилформамид.
Кроме того, согласно настоящему изобретению вещество, ингибирующее киназу RET, может быть кристаллическим или аморфным. Если существует кристаллический полиморф, он может представлять собой отдельный полиморф или смесь полиморфов в любой кристаллической форме.
Согласно настоящему изобретению вещество, ингибирующее киназу RET, включает ингибирующие киназу RET вещества, поддающиеся метаболизму, такому как окисление, восстановление, гидролиз и конъюгация in vivo. Ингибирующее киназу RET вещество по изобретению также включает соединения, которые генерируют вещество, ингибирующее киназу RET, претерпевая метаболизм, такой как окисление, восстановление и гидролиз in vivo.
Ингибирующее киназу RET вещество по изобретению обладает активностью ингибирования активности киназы RET (далее в данном описании также называемой «активностью ингибирования киназы RET»). Ингибирующая способность вещества по изобретению, ингибирующего киназу RET, не ограничивается до тех пор, пока оно ингибирует активность киназы RET. Примеры способов определения активности ингибирования киназы RET вещества, ингибирующего киназу RET, включают анализ клеточной свободной киназы, вестерн-блоттинг, анализ клеточного роста и анализ жизнеспособности. Примеры анализа клеточного роста включают способ с поглощением меченного тритием тимидина, способ МТТ, способ ХТТ (набор 8 для подсчета клеток (Dojindo Laboratories)), способ с AlamarBlue, способ с нейтральным красным, способ с BrdU, окрашивание Ki167 и окрашивание PCNA. Примеры анализа жизнеспособности включают окрашивание TUNNEL, детекцию расщепления каспазой-3 и детекцию расщепления PARP. Указанные способы можно осуществить согласно обычным методам (Blood, 2005, 105, 2941-2948; Molecular Cancer Therapeutics, 2005, 4, 787-798).
Далее в данном описании будет описан способ определения активности ингибирования киназы RET.
Активность ингибирования киназы RET можно определить анализом клеточной свободной киназы.
RET можно получить средствами генной инженерии согласно обычному способу. Например, согласно способу с бакуловирусной экспрессирующей системой человеческий рекомбинантный слитый белок GST, человеческий рекомбинантный слитый белок с гистидиновой меткой или подобный белок можно экспрессировать в клетках насекомого (Spodoptera frugiperda 9 (Sf9)). Затем экспрессированный рекомбинантный белок можно очистить аффинной хроматографией (например, на агарозе GSH (Sigma) или на агарозе Ni-NTH (Qiagen)). Чистоту и идентификацию белка можно подтвердить SDS-PAGE, окрашиванием серебром и вестерн-блоттингом с использованием антител, специфических к RET.
Анализ клеточной свободной киназы можно осуществить следующим образом.
Сначала в каждую лунку планшета (например, 96-луночного, 384-луночного и т.д.) можно последовательно добавить смешанный раствор, включающий 20 мкл стандартного реакционного раствора, 5 мкл раствора АТФ, 5 мкл раствора испытываемого вещества, и смешанный раствор, включающий 10 мкл раствора, содержащего 50 нг рекомбинантного белка RET, и 10 мкл раствора, содержащего 125 нг биотинилированного поли(Glu, Tyr)4:1.
Такой реакционный раствор киназы (50 мкл) может содержать 60 мМ HEPES-NaOH (pH 7,5), 3 мМ MgCl2, 3 мМ MnCl2, 3 мкМ ортованадата Na, 1,2 мМ DTT, 50 мкг/мл ПЭГ20000 и 1 мкМ АТФ. В данном случае можно использовать АТФ, меченный радиоактивным изотопом, такой как [γ-32P]-АТФ или [γ-33P]-АТФ.
Реакционный раствор можно инкубировать на протяжении определенного времени, и затем для обрыва реакции можно добавить 50 мкл 2% (об./об.) раствора Н3РО4.
Каждую лунку можно подвергнуть соответствующей процедуре промывки.
Активность ингибирования киназы RET можно оценить, определяя количество включенного АТФ. Когда используют АТФ, меченный радиоактивным изотопом, количество включенного АТФ можно оценить, определяя сцинтилляционным счетчиком радиоактивность, захваченную на планшете.
Согласно данному способу можно оценить ингибирующую активность соединения в отношении киназы RET.
(5) Терапевтическое средство, фармацевтическая композиция и способ лечения
Терапевтическое средство по изобретению, включающее вещество, ингибирующее киназу RET, представляет собой средство для лечения, по меньшей мере, одного заболевания, выбранного из группы, состоящей из множественной эндокринной неоплазии типа IIA, множественной эндокринной неоплазии типа IIB, семейной медуллярной карциномы щитовидной железы, папиллярной карциномы щитовидной железы, спорадической медуллярной карциномы щитовидной железы, болезни Гиршспрунга, феохромоцитомы, гиперплазии паращитовидной железы и невром слизистой оболочки желудочно-кишечного тракта. Кроме того, терапевтическое средство по изобретению, включающее вещество, ингибирующее киназу RET, представляет собой средство для лечения карциномы щитовидной железы. Предпочтительно, терапевтическое средство по изобретению используют в случае заболевания, включающего клетки, экспрессирующие мутантную RET.
Терапевтическое средство по изобретению можно вводить живому организму, т.е. млекопитающему (например, человеку, крысе, кролику, овце, свинье, корове, кошке, собаке, обезьяне и т.д.), которому требуется лечение от заболевания.
Фармацевтическая композиция по изобретению включает вещество, ингибирующее киназу RET, для введения в организм, содержащий клетки, экспрессирующие мутантную RET.
Фармацевтическую композицию по изобретению можно использовать в качестве терапевтического средства для лечения заболевания с экспрессией мутантной RET. Примеры заболеваний с экспрессией мутантной RET включают множественную эндокринную неоплазию типа IIA, множественную эндокринную неоплазию типа IIB, семейную медуллярную карциному щитовидной железы, папиллярную карциному щитовидной железы, спорадическую медуллярную карциному щитовидной железы, болезнь Гиршспрунга, феохромоцитому, гиперплазию паращитовидной железы и невромы слизистой оболочки желудочно-кишечного тракта.
Фармацевтическую композицию по изобретению можно вводить живому организму, т.е. млекопитающему (например, человеку, крысе, кролику, овце, свинье, корове, кошке, собаке, обезьяне и т.д.). Согласно настоящему изобретению указанный живой организм включает клетки, экспрессирующие мутантную RET.
Согласно настоящему изобретению терапевтическое средство включает средство для улучшения прогноза рака, средство для предупреждения рецидива рака или подобное средство. Терапевтическое средство для лечения рака или опухоли включает противоопухолевое средство, средство для подавления метастазиса рака или подобное средство.
Эффект лечения можно подтвердить, наблюдая рентгеновское изображение, СТ или подобное, гистопатологическим диагнозом биопсии или по показанию маркера заболевания.
Когда используют терапевтическое средство или фармацевтическую композицию по изобретению, заданная доза вещества, ингибирующего киназу RET, различается в зависимости от степени симптомов, возраста, пола, массы и различия в чувствительности пациента, способа введения, времени введения, интервала при введении, характера, рецептуры и типа фармацевтического препарата и типа активного элемента. Как правило, но без ограничения, дозировка вещества, ингибирующего киназу RET, составляет 0,1-1000 мг/сутки, предпочтительно 0,5-100 мг/сутки, предпочтительнее 1-30 мг/сутки, для взрослого индивидуума (масса 60 кг), которую можно вводить один-три раза в сутки.
Хотя терапевтическое средство или фармацевтическая композиция по изобретению, включающие в качестве активного элемента вещество, ингибирующее киназу RET, можно использовать одни, как правило, их смешивают с соответствующими добавками и получают в форме препарата.
Примерами таких добавок являются эксципиенты, связующие вещества, смазывающие вещества, вещества, способствующие рассыпанию, красители, корригенты, эмульгаторы, поверхностно-активные вещества, солюбилизаторы, суспендирующие вещества, вещества, придающие тоничность, буферы, антисептики, антиоксиданты, стабилизаторы, промоторы абсорбции и подобные вещества, которые обычно используют для лекарственных средств. При необходимости их можно использовать в сочетании. Примеры таких добавок приводятся далее.
Эксципиенты: лактоза, сахароза, глюкоза, кукурузный крахмал, маннит, сорбит, крахмал, альфа-крахмал, декстрин, кристаллическая целлюлоза, легкий диоксид кремния, силикат алюминия, силикат кальция, алюмометасиликат магния и гидрофосфат кальция.
Связующие вещества: например, поливиниловый спирт, метилцеллюлоза, этилцеллюлоза, аравийская камедь, трагакант, желатин, шеллак, гидроксипропилметилцеллюлоза, гидроксипропилцеллюлоза, натрийкарбоксиметилцеллюлоза, поливинилпирролидон и макроголь.
Смазывающие вещества: стеарат магния, стеарат кальция, стеарилфумарат натрия, тальк, полиэтиленгликоль и коллоидный диоксид кремния.
Вещества, способствующие рассыпанию: кристаллическая целлюлоза, агар, желатин, карбонат кальция, гидрокарбонат натрия, цитрат кальция, декстрин, пектин, гидроксипропилцеллюлоза с низкой степенью замещения, карбоксиметилцеллюлоза, кальцийкарбоксиметилцеллюлоза, натрийкроскармелоза, карбоксиметилированный крахмал и карбоксиметилированный натрийкрахмал.
Красители: оксид железа, желтый оксид железа, кармин, жженый сахар, бета-каротин, оксид титана, тальк, фосфат рибофлавиннатрия, желтый алюминиевый краситель и т.п., которые одобрены в медицине как добавки.
Корригенты: порошок какао, ментол, ароматический порошок, масло из перечной мяты, камфора и порошок корицы.
Эмульгаторы или поверхностно-активные вещества: стеарилтриэтаноламин, лаурилсульфат натрия, лауриламинопропионат, лецитин, моностеарат глицерина, эфир жирной кислоты и сахарозы и эфир жирной кислоты и глицерина.
Солюбилизаторы: полиэтиленгликоль, пропиленгликоль, бензилбензоат, этанол, холестерин, триэтаноламин, карбонат натрия, цитрат натрия, полисорбат 80 и амид никотиновой кислоты.
Суспендирующие вещества: кроме указанных выше поверхностно-активных веществ, гидрофильные полимеры, такие как поливиниловый спирт, поливинилпирролидон, метилцеллюлоза, гидроксиметилцеллюлоза, гидроксиэтилцеллюлоза и гидроксипропилцеллюлоза.
Вещества, придающие тоничность: глюкоза, хлорид натрия, маннит и сорбит.
Буферы: буферы, полученные из фосфата, ацетата, карбоната и цитрата.
Антисептики: метилпарабен, пропилпарабен, хлорбутанол, бензиловый спирт, фенетиловый спирт, дегидроуксусная кислота и сорбиновая кислота.
Антиоксиданты: гидросульфаты, аскорбиновая кислота и альфа-токоферол.
Стабилизаторы: стабилизаторы, обычно используемые в медицине.
Промоторы абсорбции: промоторы абсорбции, обычно используемые в медицине.
При необходимости также можно добавлять такие компоненты, как витамины и аминокислоты.
Примеры препаратов включают пероральные препараты, такие как таблетки, порошки, гранулы, мелкие гранулы, капсулы, сиропы, лепешки и препараты для ингаляции; препараты для наружного применения, такие как суппозитории, мази, глазная мазь, припарки, глазные капли, капли в нос, ушные капли, пэтчи и лосьоны и препараты для инъекции.
Пероральные препараты, указанные выше, можно получить, комбинируя, соответственно, добавки, указанные выше. При необходимости на поверхности указанных выше препаратов могут быть нанесены покрытия.
Препараты для наружного применения, указанные выше, можно получить, комбинируя, соответственно, добавки, указанные выше, в частности эксципиенты, связующие вещества, корригенты, эмульгаторы, поверхностно-активные вещества, солюбилизаторы, суспендирующие вещества, вещества, придающие тоничность, антисептики, антиоксиданты, стабилизаторы и промоторы абсорбции.
Препараты для инъекций, указанные выше, можно получить, комбинируя, соответственно, добавки, указанные выше, в частности эмульгаторы, поверхностно-активные вещества, солюбилизаторы, суспендирующие вещества, вещества, придающие тоничность, буферы, антисептики, антиоксиданты, стабилизаторы и промоторы абсорбции. Препараты для инъекций можно использовать такими способами, как инфузия, внутримышечная инъекция, подкожная инъекция, интрадермальная инъекция и внутривенная инъекция.
Настоящее изобретение относится к способу лечения, по меньшей мере, одного заболевания, выбранного из группы, состоящей из множественной эндокринной неоплазии типа IIA, множественной эндокринной неоплазии типа IIB, семейной медуллярной карциномы щитовидной железы, папиллярной карциномы щитовидной железы, спорадической медуллярной карциномы щитовидной железы, болезни Гиршспрунга, феохромоцитомы, гиперплазии паращитовидной железы и невром слизистой оболочки желудочно-кишечного тракта, причем способ включает введение пациенту эффективного количества вещества, ингибирующего киназу RET. Настоящее изобретение также относится к способу лечения карциномы щитовидной железы, включающему введение пациенту эффективного количества вещества, ингибирующего киназу RET.
Настоящее изобретение также относится к способу лечения заболевания, включающему введение эффективного количества вещества, ингибирующего киназу RET, в организм, содержащий клетки, экспрессирующие мутантную RET. Согласно настоящему изобретению указанное заболевание представляет собой, предпочтительно, по меньшей мере, одно заболевание, выбранное из группы, состоящей из множественной эндокринной неоплазии типа IIA, множественной эндокринной неоплазии типа IIB, семейной медуллярной карциномы щитовидной железы, папиллярной карциномы щитовидной железы, спорадической медуллярной карциномы щитовидной железы, болезни Гиршспрунга, феохромоцитомы, гиперплазии паращитовидной железы и невром слизистой оболочки желудочно-кишечного тракта.
Согласно способу лечения по изобретению путь и способ введения вещества, ингибирующего киназу RET, особо не ограничиваются, и можно обратиться к приведенному выше описанию терапевтического средства или фармацевтической композиции.
Настоящее изобретение относится к применению вещества, ингибирующего киназу RET, для получения терапевтического средства для лечения, по меньшей мере, одного заболевания, выбранного из группы, состоящей из множественной эндокринной неоплазии типа IIA, множественной эндокринной неоплазии типа IIB, семейной медуллярной карциномы щитовидной железы, папиллярной карциномы щитовидной железы, спорадической медуллярной карциномы щитовидной железы, болезни Гиршспрунга, феохромоцитомы, гиперплазии паращитовидной железы и невром слизистой оболочки желудочно-кишечного тракта. Настоящее изобретение также относится к применению вещества, ингибирующего киназу RET, для получения терапевтического средства для лечения карциномы щитовидной железы.
Настоящее изобретение также относится к применению вещества, ингибирующего киназу RET, для получения фармацевтической композиции, включающей вещество, ингибирующее киназу RET, для введения в организм, содержащий клетки, экспрессирующие мутантную RET. В случае применения по изобретению фармацевтическая композиция эффективна в качестве средства для лечения, по меньшей мере, одного заболевания, выбранного из группы, состоящей из множественной эндокринной неоплазии типа IIA, множественной эндокринной неоплазии типа IIB, семейной медуллярной карциномы щитовидной железы, папиллярной карциномы щитовидной железы, спорадической медуллярной карциномы щитовидной железы, болезни Гиршспрунга, феохромоцитомы, гиперплазии паращитовидной железы и невром слизистой оболочки желудочно-кишечного тракта.
Настоящее изобретение относится к веществу, ингибирующему киназу RET, для терапевтического средства для лечения, по меньшей мере, одного заболевания, выбранного из группы, состоящей из множественной эндокринной неоплазии типа IIA, множественной эндокринной неоплазии типа IIB, семейной медуллярной карциномы щитовидной железы, папиллярной карциномы щитовидной железы, спорадической медуллярной карциномы щитовидной железы, болезни Гиршспрунга, феохромоцитомы, гиперплазии паращитовидной железы и невром слизистой оболочки желудочно-кишечного тракта. Кроме того, настоящее изобретение относится к веществу, ингибирующему киназу RET, для терапевтического средства для лечения карциномы щитовидной железы.
Кроме того, настоящее изобретение относится к веществу, ингибирующему киназу RET, для фармацевтической композиции, включающей вещество, ингибирующее киназу RET, для введения в организм, содержащий клетки, экспрессирующие мутантную RET. Согласно настоящему изобретению фармацевтическая композиция применима в качестве терапевтического средства для лечения, по меньшей мере, одного заболевания, выбранного из группы, состоящей из множественной эндокринной неоплазии типа IIA, множественной эндокринной неоплазии типа IIB, семейной медуллярной карциномы щитовидной железы, папиллярной карциномы щитовидной железы, спорадической медуллярной карциномы щитовидной железы, болезни Гиршспрунга, феохромоцитомы, гиперплазии паращитовидной железы и невром слизистой оболочки желудочно-кишечного тракта.
Настоящее изобретение также относится к ингибитору киназы RET, включающему соединение, представленное общей формулой (I), его фармацевтически приемлемую соль или его сольват.
Соединение, представленное общей формулой (I), таковое, как описанное выше, и представляет собой, предпочтительно, 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид.
Настоящее изобретение также относится к ингибитору киназы RET, включающему, по меньшей мере, одно соединение, выбранное из группы, состоящей из
(2-диэтиламиноэтил)амида 5-(5-фтор-2-оксо-1,2-дигидроиндол-3-илиденметил)-2,4-диметил-1Н-пиррол-3-карбоновой кислоты (SU11248),
N-{2-хлор-4-[(6,7-диметокси-4-хинолил)окси]фенил}-N'-(5-метил-3-изоксазолил)мочевины (KRN951) и
4-[(4-фтор-2-метилиндол-5-ил)окси]-6-метокси-7-[3-(пирролидин-1-ил)пропокси]хиназолина (AZD2171),
его фармакологически приемлемую соль или его сольват.
Ингибирующую активность в отношении киназы RET ингибитора киназы RET по изобретению можно определить так, как описано выше.
Соединение можно использовать или одно, или в смеси с соответствующими добавками, указанными выше, и получить в виде препарата как ингибитора киназы RET по изобретению.
Что касается применения и дозировки ингибитора киназы RET по изобретению, можно обратиться к приведенному выше описанию терапевтического средства или фармацевтической композиции.
Настоящее изобретение также относится к применению, по меньшей мере, одного соединения, выбранного из группы, состоящей из соединения, представленного общей формулой (I), SU11248, KRN951 и AZD2171, его фармакологически приемлемой соли или его сольвата, для получения ингибитора киназы RET.
Настоящее изобретение также относится к способу ингибирования киназы RET, по меньшей мере, одним соединением, выбранным из группы, состоящей из соединения, представленного общей формулой (I), SU11248, KRN951 и AZD2171, его фармакологически приемлемой соли или его сольвата. Согласно способу по изобретению, применение и дозировка соединения особо не ограничиваются, и можно обратиться к приведенному выше описанию терапевтического средства или фармацевтической композиции.
2. Способ прогнозирования чувствительности
Настоящее изобретение относится к способу прогнозирования того, будет ли или нет пациент высокочувствителен к ингибирующему киназу RET веществу по изобретению, с использованием в качестве показателя наличия или отсутствия мутации RET в клетке. Терапевтическое действие вещества, ингибирующего киназу RET, более перспективно для пациентов, высокочувствительных к веществу, ингибирующему киназу RET.
Согласно способу по изобретению пациент, предпочтительно, является пациентом, страдающим от, по меньшей мере, одного заболевания, выбранного из группы, состоящей из множественной эндокринной неоплазии типа IIA, множественной эндокринной неоплазии типа IIB, семейной медуллярной карциномы щитовидной железы, папиллярной карциномы щитовидной железы, спорадической медуллярной карциномы щитовидной железы, болезни Гиршспрунга, феохромоцитомы, гиперплазии паращитовидной железы и невром слизистой оболочки желудочно-кишечного тракта.
(1) Стадия определения наличия или отсутствия мутации RET в клетке
На данной стадии клетки, предпочтительно, берут у пациента. Клетки можно получить, например, извлечением их из организма пациента хирургической процедурой (например, биопсией и т.д.). Предпочтительно используют клетки крови в случае заболеваний, вызванных генетическими изменениями, таких как множественная эндокринная неоплазия типа IIA, множественная эндокринная неоплазия типа IIB, семейная медуллярная карцинома щитовидной железы, папиллярная карцинома щитовидной железы, спорадическая медуллярная карцинома щитовидной железы, болезнь Гиршспрунга, феохромоцитома, гиперплазия паращитовидной железы и невромы слизистой оболочки желудочно-кишечного тракта.
Наличие или отсутствие мутации RET в клетке можно определить согласно способу, описанному выше.
(2) Стадия прогнозирования того, будет ли или нет пациент высокочувствителен к веществу, ингибирующему киназу RET
На данной стадии прогнозировать будет ли или нет пациент высокочувствителен к веществу, ингибирующему киназу RET, можно, предпочтительно, с использованием в качестве показателя наличие или отсутствие мутации RET в клетке, определенное в (1). Конкретно, когда установлено, что клетки экспрессируют мутантную RET, пациента считают высокочувствительным к веществу, ингибирующему киназу RET.
Другим аспектом изобретения является способ анализа чувствительности клеток к веществу, ингибирующему киназу RET, с использованием в качестве показателя результата, полученного в (1). Конкретно, когда на основании результатов в (1) клетки являются экспрессирующими мутантную RET, такие клетки считают более чувствительными к веществу, ингибирующему киназу RET, в сравнении с клетками, неэкспрессирующими мутантную RET.
Еще одним аспектом изобретения является способ отбора клеток или пациентов, высокочувствительных к веществу, ингибирующему киназу RET, с использованием в качестве показателя результата, полученного в (1). Конкретно, когда клетки являются экспрессирующими мутантную RET, что определено из результатов, полученных в (1), такие клетки или пациенты, имеющие такие клетки, считаются высокочувствительными к веществу, ингибирующему киназу RET. Таким образом, такие клетки или таких пациентов можно отобрать как клетки или пациентов, которые высокочувствительны к веществу, ингибирующему киназу RET.
Еще одним аспектом изобретения является способ классификации пациентов через анализ чувствительности к веществу, ингибирующему киназу RET, с использованием в качестве показателя результата, полученного в (1). Конкретно, согласно способу по изобретению, чувствительность пациентов к веществу, ингибирующему киназу RET, анализируют, основываясь на результатах определения в (1), как описано выше, и пациентов, имеющих клетки, представляющие интерес, можно классифицировать по таким результатам. Например, пациентов можно отнести к группе, включающей клетки, экспрессирующие мутантную RET, и группе без таких клеток. С другой стороны, пациентов можно разделить на группу пациентов, высокочувствительных к веществу, ингибирующему киназу RET, и группу остальных пациентов.
Еще одним аспектом изобретения является способ отбора пациентов для введения вещества, ингибирующего киназу RET, включающий отбор пациентов, имеющих клетки, экспрессирующие мутантную RET, на основании результатов определения в (1). Пациенты, имеющие клетки, экспрессирующие мутантную RET, могут являться предполагаемой мишенью для введения вещества, ингибирующего киназу RET.
Еще одним аспектом изобретения является способ прогнозирования терапевтического действия на пациента вещества, ингибирующего киназу RET, основанный на результатах определения в (1). Согласно способу по изобретению, когда клетки являются экспрессирующими мутантную RET, что определено из результатов, полученных в (1), клетки считают высокочувствительными к веществу, ингибирующему киназу RET, и, таким образом, прогнозируется, что терапевтическое действие такого ингибирующего киназу RET вещества на клетки или пациента, имеющего такие клетки, будет высоким.
Настоящее изобретение также относится к способу определения наличия или отсутствия мутации RET в клетках, полученных от пациента, для прогнозирования уровня чувствительности пациента к веществу, ингибирующему киназу RET. Такой способ определения представляет собой такой способ, какой описан выше в (1).
Определение наличия или отсутствия мутации RET в клетках позволяет прогнозировать уровень чувствительности пациента к веществу, ингибирующему киназу RET.
На данной стадии, хотя вещество, ингибирующее киназу RET, представляет собой соединение, описанное выше, оно, предпочтительно, представляет собой 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид, его фармацевтически приемлемую соль или его сольват.
Способ по изобретению можно использовать для прогнозирования уровня эффективности вещества, ингибирующего киназу RET, в отношении пациента до введения пациенту вещества, ингибирующего киназу RET. Следовательно, для осуществления лечения заболевания можно отобрать пациентов, которые, как ожидается, более чувствительны к веществу, ингибирующему киназу RET. Таким образом, настоящее изобретения является высокоэффективным в клиническом отношении.
Настоящее изобретение относится к набору для анализа для определения наличия или отсутствия мутации RET, используемого в способе по изобретению. Набор для анализа по изобретению включает используемые для определения реагенты, указанные выше. Набор для анализа по изобретению дает возможность прогнозировать, будет ли или не будет пациент высокочувствительным к веществу, ингибирующему киназу RET.
Настоящее изобретение также относится к применению набора для анализа для прогнозирования, указанного выше.
Далее настоящее изобретение будет поясняться конкретными примерами, хотя изобретение не должно ими ограничиваться.
Пример 1
Определение активности ингибирования киназы RET вещества, ингибирующего киназу RET
Активность ингибирования киназы RET испытываемого вещества по просьбе авторов изобретения определяли в ProQinase (Freiburg, Германия, GmbH). Точнее, активность ингибирования киназы RET можно определить как описано далее.
1. Экспрессия и очистка RET
RET экспрессируют в виде человеческого рекомбинантного слитого белка GST (называемого далее в данном описании также «рекомбинантный белок RET») в клетках насекомого (Spodoptera frugiperda 9 (Sf9)) согласно способу с бакуловирусной экспрессирующей системой. Экспрессированный рекомбинантный белок RET очищают аффинной хроматографией с использованием GSH-агарозы (Sigma) или Ni-NTH-агарозы (Qiagen). Чистоту и идентификацию белка можно подтвердить SDS-PAGE, окрашиванием серебром и вестерн-блоттиногом с использованием антител, специфических к RET.
2. Определение ингибирующей активности в отношении активности киназы RET
Сначала в каждую лунку сенсибилизированного стрептавидином 96-луночного планшета FlashPlate (Perkin Elmer/NEM) последовательно добавляют 20 мкл стандартного реакционного раствора, 5 мкл раствора АТФ (разбавленного Н2О), 5 мкл раствора испытываемого вещества (10% водный раствор в диметилсульфоксиде) и смешанный раствор, включающий 10 мкл раствора, содержащего 50 нг рекомбинантного белка RET, и 10 мкл раствора, содержащего 125 нг биотинилированного поли(Glu, Tyr)4:1. Такой реакционный раствор киназы (50 мкл) содержит 60 мМ HEPES-NaOH (pH 7,5), 3 мМ MgCl2, 3 мМ MnCl2, 3 мкМ ортованадата Na, 1,2 мМ DTT, 50 мкг/мл ПЭГ20000 и 1 мкМ [γ-33P]-АТФ.
В качестве испытываемого вещества используют 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид (метансульфонат), 6-[2-(метилкарбамоил)фенилсульфанил]-3-E-[2-(пиридин-2-ил)этенил]индазол (также называемый далее в данном описании “AG013736”), SU11248, KRN951 или AZD2171.
4-(3-Хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид получают согласно описанию в брошюре международной публикации № 02/32872 (WO 02/32872) и брошюре международной публикации № 2005/063713 (WO 2005/063713).
AG013736 получают на основании описания в брошюре международной публикации № 01/002369 (WO 01/002369). SU11248 получают на основании описания в брошюре международной публикации № 01/060814 (WO 01/060814). KRN951 получают на основании описания в брошюре международной публикации № 02/088110 (WO 02/088110). AZD2171 получают на основании описания в брошюре международной публикации № 00/47212 (WO 00/47212).
Затем реакционный раствор инкубируют при 30оС в течение 80 минут, после чего для обрыва реакции добавляют 50 мкл 2% (об./об.) раствора Н3РО4.
Дважды промывают и аспирируют 96-луночный планшет 200 мкл 0,9% (мас./об.) раствора NaCl.
Количество внедрившегося 33Pi можно оценить, определяя радиоактивность на планшете сцинтилляционным счетчиком для микропланшетов (от Microbeta, Wallac).
Манипуляцию осуществляют с помощью роботизированной системы BeckmanCoulter/Sagian.
Концентрацию испытываемого вещества, необходимую для ингибирования активности киназы RET на 50% (IC50), вычисляют с использованием удельной радиоактивности 33P при различных концентрациях (10 точек в интервале от 10 мкМ до 0,0003 мкМ) с программой Prism 3.03 (Windows, Graphpad, San Diego, California, USA).
В данном случае величину, полученную в случае, когда добавляют один поли(Glu, Tyr)4:1 (без добавления рекомбинантного белка RET), принимают за 0%, в то время как величину, полученную в случае, когда добавляют рекомбинантный белок RET и субстрат поли(Glu, Tyr)4:1 (без добавления испытываемого соединения), принимают за 100%.
Киназную активность в присутствии испытываемого соединения в каждой концентрации оценивают в виде процента величины, полученной путем вычитания величины 0% из значения радиоактивности, от величины, полученной путем вычитания величины 0% из величины 100%. На основании полученного процента (%) вычисляют концентрацию испытываемого соединения, необходимую для ингибирования киназной активности на 50% (IC50).
В результате обнаружено, что 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид обладает активностью ингибирования киназы RET (IC50=35 нМ). Кроме того, также обнаружено, что активностью ингибирования киназы RET обладают SU11248, KRN951 и AZD2171 (IC50=64, 92 и 75 нМ, соответственно). AG013736 имеет IC50 5600 нМ. Кроме того, испытываемые вещества различаются по уровню активности ингибирования киназы RET.
Пример 2
Действие вещества, ингибирующего киназу RET, на лиганднезависимое фосфорилирование RET в клеточной линии медуллярной карциномы щитовидной железы человека (ТТ)
1. Получение клеточного экстракта
Клеточную линию медуллярной карциномы щитовидной железы человека (ТТ, закупают у АТСС) суспендируют в среде RPMI1640, содержащей 15% FBS (закупают у Sigma). ТТ представляет собой клеточную линию, экспрессирующую RET, в которой цистеин в кодоне 634 в аминокислотной последовательности RET дикого типа мутирован триптофаном (Biochemical and Biophysical Research Communications, 207, 1022-1028, 1995). По два мл полученной клеточной суспензии на лунку (4×105 клеток/мл) добавляют в 6-луночный планшет для клеточных культур (закупают у FALCON) и культивируют в инкубаторе с 5% СО2 (37°C) в течение ночи. После культивирования из каждой лунки удаляют супернатант и добавляют 1,8 мл среды RPMI1640, содержащей 15% FBS. Затем добавляют 0,2 мл раствора испытываемого вещества 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамида (метансульфоната) в диметилсульфоксиде (разведенного в среде RPMI1640, содержащей 15% FBS) и проводят культивирование в инкубаторе с 5% СО2 (37°C) в течение часа. Удаляют супернатант из каждой лунки, затем лунки промывают 400 мкл PBS и добавляют 100 мкл буфера для солюбилизации (50 мМ Hepes (рН 7,4), 150 мМ NaCl, 10% (об./об.) глицерина, 1% тритона Х-100, 1,5 мМ MgCl2, 1 мМ ЭДТК (рН 8,0), 100 мМ NaF, 1 мМ PMSF, 10 мкг/мл апротинина, 50 мкг/мл лейпептина, 1 мкг/мл пепстатина А и 1 мМ Na3VO4). Клетки в полученном растворе собирают сребком и обрабатывают при 15000 об/мин и 4°C в течение 15 минут. К супернатанту добавляют буфер SDS и подвергают обработке при 94°C в течение 5 минут для солюбилизации белка, который затем получают в виде клеточного экстракта в концентрации 20 мкг/10 мкл.
2. Электрофорез и вестерн-блоттинг
Клеточный экстракт (20 мкг/10 мкл) подвергают электрофорезу в градиенте 4-20% полиакриламидного геля (закупают у Daiichi Pure Chemicals) и затем переносят на PVDF мембрану (закупают у Amersham Pharmacia Biotech) обычным методом. Затем перенесенную мембрану подвергают иммуноблоттингу с использованием антител против RET (анти-RET, закупают у Cell Signaling), антител против фосфорилированной RET (анти-фосфоRET, закупают у Cell Signaling), антител против Erk1/2 (анти-Erk1/2, закупают у Cell Signaling) или антител против фосфорилированного Erk1/2 (анти-фосфо-Erk1/2, закупают у Cell Signaling) в качестве первичных антител и антител против кроличьего IgG, меченных пероксидазой из хрена (антитела против кроличьего IgG, связанные с HRP (закупают у Cell Signaling)), в качестве вторичных антител. Мембрану промывают и затем обрабатывают Super Signal (закупают у PIERCE) для получения окрашивания.
Активность аутофосфорилирования RET (%) каждой полосы определяют, оценивая поглощение в лунке с добавленным испытываемого вещества без клеточного экстракта как 100% активность аутофосфорилирования RET. Активность аутофосфорилирования RET (%) определяют, изменяя ступенчато концентрацию испытываемого вещества, для вычисления концентрации испытываемого вещества, необходимой для ингибирования активности аутофосфорилирования RET на 50% (IC50).
В результате 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид ингибирует фосфорилирование RET в зависимости от концентрации (IC50=27 нМ) (фиг.1). Кроме того, также обнаружено, что 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид ингибирует фосфорилирование одной из следующих по ходу метаболизма (downstream) молекул RET Erk1/2, которая ассоциируется с сигналом клеточного роста, в концентрации, схожей с концентрацией в случае киназы RET (фигура 1).
Пример 3
Действие вещества, ингибирующего киназу RET, на рост клеток клеточной линии медуллярной карциномы щитовидной железы человека (ТТ)
Клеточную линию медуллярной карциномы щитовидной железы человека (ТТ, закупают у АТСС) суспендируют в среде RPMI1640, содержащей 15% FBS (закупают у Sigma). По 0,1 мл полученной клеточной суспензии на лунку (3×104 клеток/мл) добавляют в 96-луночный планшет для клеточных культур (закупают у NUNC) и культивируют в инкубаторе с 5% СО2 (37°C) в течение ночи. После культивирования в каждую лунку добавляют 0,1 мл раствора испытываемого вещества 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамида (метансульфоната), разведенного в среде RPMI1640, содержащей 15% FBS, и затем проводят культивирование в инкубаторе с 5% СО2 (37°C) в течение 10 суток. После культивирования в каждую лунку добавляют 10 мкл раствора 1 из набора для подсчета клеток (закупают у DOJINDO), обрабатывают в инкубаторе с 5% СО2 (37°C) для появления окраски и измеряют поглощение в каждой лунке с помощью планшет-ридера МТР-500 (Corona Electric) при длине волны измерения 415 нм и эталонной длине волны 660 нм. Процент (%) поглощения в каждой лунке с испытываемым веществом определяют, сравнивая с поглощением в лунке без испытываемого вещества, на основании чего вычисляют концентрацию испытываемого вещества, необходимую для ингибирования роста клеток на 50% (IC50).
В результате обнаружено, что 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид имеет ингибирующую активность в отношении роста клеток клеточной линии медуллярной карциномы щитовидной железы человека (ТТ) IC50=78 нМ.
Пример 4
Противоопухолевое действие вещества, ингибирующего киназу RET, на модели с подкожной трансплантацией клеточной линии медуллярной карциномы щитовидной железы человека (ТТ)
Клеточную линию медуллярной карциномы щитовидной железы человека (ТТ, закупают у АТСС) культивируют при 37°C в среде RPMI1640 (содержащей 15% FBS) в инкубаторе с 5% диоксида углерода до 80% слияния и клетки собирают с трипсином-ЭДТК согласно общему способу. Клетки суспендируют в фосфатном буфере и получают клеточную суспензию 1×108 клеток/мл. По 0,1 мл каждой полученной клеточной суспензии подкожно трансплантируют в бок голым мышам (закупают у Charles River).
Как только после трансплантации объем опухоли достигает приблизительно 100-200 мм3, вводят перорально испытываемое вещество 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид (метансульфонат) по 10 мг/кг, 30 мг/кг или 100 мг/кг один раз в сутки в течение четырех недель. Измеряют большую и малую оси опухолей циркулем Digimatic (Mitsutoyo) и вычисляют объемы опухолей согласно следующей формуле:
объем опухоли (TV) = большая ось опухоли (мм) × (малая ось опухоли)2 (мм2)/2.
В результате обнаруживают, что на модели с подкожной трансплантацией клеточной линии медуллярной карциномы щитовидной железы человека (ТТ) 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид оказывает противоопухолевое действие, зависящее от дозы (фиг.2).
Пример 5
Действие вещества, ингибирующего киназу RET, на фосфорилирование RET у модели с подкожной трансплантацией клеточной линии медуллярной карциномы щитовидной железы человека (ТТ)
Клеточную линию медуллярной карциномы щитовидной железы человека (ТТ, закупают у АТСС) культивируют при 37°C в среде RPMI1640 (содержащей 15% FBS) в инкубаторе с 5% диоксида углерода до 80% слияния и клетки собирают с трипсином-ЭДТК согласно общему способу. Клетки суспендируют в фосфатном буфере и получают клеточную суспензию 1×108 клеток/мл. По 0,1 мл каждой полученной клеточной суспензии подкожно трансплантируют в бок голым мышам (закупают у Charles River).
Как только после трансплантации объем опухоли достигает приблизительно 100-200 мм3, вводят перорально испытываемое вещество 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид (метансульфонат) по 10 мг/кг, 30 мг/кг или 100 мг/кг. Опухоли резецируют через 2, 8, 12 или 24 часа после введения, добавляют к ним буфер для солюбилизации (50 мМ Hepes (рН 7,4), 150 мМ NaCl, 10% (об./об.) глицерина, 1% тритона Х-100, 1,5 мМ MgCl2, 1 мМ ЭДТК (рН 8,0), 100 мМ NaF, 1 мМ PMSF, 10 мкг/мл апротинина, 50 мкг/мл лейпептина, 1 мкг/мл пепстатина А и 1 мМ Na3VO4), 25 мМ β-глицерофосфата и коктейль II ингибитора фосфатазы (Sigma) и гомогенизируют. После обработки при 15000 об/мин и 4°C в течение 15 минут и добавления к супернатанту буфера SDS проводят обработку при 94°C в течение 5 минут для солюбилизации белка и получают клеточный экстракт в концентрации 20 мкг/10 мкл. Клеточный экстракт подвергают электрофорезу и иммуноблоттингу таким же способом, как в примере 2.
В результате обнаруживают, что 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамид проявляет активность ингибирования аутофосфорилирования RET в зависимости от дозы на модели с подкожной трансплантацией клеточной линии медуллярной карциномы щитовидной железы человека (ТТ) (фиг.3).
Из полученных результатов видно, что предполагается, что ингибирующее киназу RET вещество по изобретению является более эффективным в отношении организмов, включающих клетки, экспрессирующие мутантную RET. Также показано, что ингибирующее киназу RET вещество по изобретению применимо в качестве терапевтического средства для лечения, по меньшей мере, одного заболевания, выбранного из группы, состоящей из множественной эндокринной неоплазии типа IIA, множественной эндокринной неоплазии типа IIB, семейной медуллярной карциномы щитовидной железы, папиллярной карциномы щитовидной железы, спорадической медуллярной карциномы щитовидной железы, болезни Гиршспрунга, феохромоцитомы, гиперплазии паращитовидной железы и невром слизистой оболочки желудочно-кишечного тракта, а также карциномы щитовидной железы.
Ссылочный пример
Далее в данном описании в качестве ссылочного примера будет описан способ получения композиции с одним из веществ, ингибирующих киназу RET, - 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамидом.
Получение фармацевтической композиции
(1) Таблетки с 1 мг
Смешивают 24 г кристаллического (С) метансульфоната 4-(3-хлор-4-(циклопропиламинокарбонил)аминофенокси)-7-метокси-6-хинолинкарбоксамида (далее в данном описании также называемым «кристаллы (С)»), который получен согласно способу, описанному в примере 7 в WO 2005/063713, и 192 г легкого безводного диоксида кремния (вещество, препятствующее желатинизации, продается под торговым наименованием аэросил (зарегистрированный торговый знак) 200, Nippon Aerosil) в 20-л смесителе (Super Mixer), затем добавляют еще 1236 г D-маннита (эксципиент, Towa-Kasei), 720 г кристаллической целлюлозы (эксципиент, продается под торговым наименованием авесил РН101, Asahi Kasei) и 72 г гидроксипропилцеллюлозы (связующее вещество, продается под торговым наименованием НРС-L, Nippon Soda) и все перемешивают. Затем добавляют подходящее количество безводного этанола для получения гранул, содержащих кристаллы (С). Гранулированную массу сушат в стеллажной сушилке (60°C) и затем регулируют размер частиц с использованием мельницы Power Mill, и получают гранулы. Вместе с гранулами 120 г натрийкроскармелозы (вещество, способствующее рассыпанию, продается под торговым наименованием Ac-Di-Sol, FMC International Inc.) и 36 г стеарилфумарата натрия (смазывающее вещество, JPS Pharma LP) помещают в 20-л барабанный смеситель, все перемешивают, массу формуют на таблетировочной машине и получают таблетки общей массой 100 мг на таблетку. Затем на таблетки наносят покрытие с использованием в качестве раствора для покрытия водного 10% раствора желтого опадри (OPADRY 03F42069 YELLOW, Colorcon Japan) с помощью машины для нанесения покрытия на таблетки и получают посредством этого таблетки с покрытием общей массой 105 мг на таблетку.
(2) Таблетки с 10 мг
Смешивают 60 г кристаллов (С) и 192 г легкого безводного диоксида кремния (вещество, препятствующее желатинизации, продается под торговым наименованием аэросил (зарегистрированный торговый знак) 200, Nippon Aerosil) в 20-л смесителе (Super Mixer), затем добавляют еще 1200 г D-маннита (эксципиент, Towa-Kasei), 720 г кристаллической целлюлозы (эксципиент, продается под торговым наименованием авесил РН101, Asahi Kasei) и 72 г гидроксипропилцеллюлозы (связующее вещество, продается под торговым наименованием НРС-L, Nippon Soda) и все перемешивают. Затем добавляют подходящее количество безводного этанола для получения гранул, содержащих кристаллы (С). Гранулированную массу сушат в стеллажной сушилке (60°C) и затем регулируют размер частиц с использованием мельницы Power Mill, и получают гранулы. Вместе с гранулами 120 г натрийкроскармелозы (вещество, способствующее рассыпанию, продается под торговым наименованием Ac-Di-Sol, FMC International Inc.) и 36 г стеарилфумарата натрия (смазывающее вещество, JPS Pharma LP) помещают в 20-л барабанный смеситель, все перемешивают, массу формуют на таблетировочной машине и получают таблетки общей массой 400 мг на таблетку. Затем на таблетки наносят покрытие с использованием в качестве раствора для покрытия водного 10% раствора желтого опадри (OPADRY 03F42069 YELLOW, Colorcon Japan) с помощью машины для нанесения покрытия на таблетки и получают посредством этого таблетки с покрытием общей массой 411 мг на таблетку.
(3) Таблетки со 100 мг
Смешивают 31,4 г кристаллов (С) и 4 г легкого безводного диоксида кремния (вещество, препятствующее желатинизации, продается под торговым наименованием аэросил (зарегистрированный торговый знак) 200, Nippon Aerosil) в 1-л смесителе (Super Mixer), затем добавляют еще 40,1 г безводного гидрофосфата кальция (эксципиент, Kyowa Chemical Industry), 10 г гидроксипропилцеллюлозы с низкой степенью замещения (связующее вещество, продается под торговым наименованием L-HPC (LH-21), Shin-Etsu Chemical) и 3 г гидроксипропилцеллюлозы (связующее вещество, продается под торговым наименованием НРС-L, Nippon Soda) и все перемешивают. Затем добавляют подходящее количество безводного этанола для получения гранул, содержащих кристаллы (С). Гранулированную массу сушат в стеллажной сушилке (60°C) и затем гранулируют с использованием мельницы Power Mill, и получают гранулы. Смешивают с гранулами 10 г натрийкроскармелозы (вещество, способствующее рассыпанию, продается под торговым наименованием Ac-Di-Sol, FMC International Inc.) и 1,5 г стеарилфумарата натрия (смазывающее вещество, JPS Pharma LP), массу формуют на таблетировочной машине и получают таблетки общей массой 400 мг на таблетку.
Промышленная применимость
Настоящее изобретение относится к включающим вещество, ингибирующее киназу RET, терапевтическому средству и способу лечения, по меньшей мере, одного заболевания, выбранного из группы, состоящей из множественной эндокринной неоплазии типа IIA, множественной эндокринной неоплазии типа IIB, семейной медуллярной карциномы щитовидной железы, папиллярной карциномы щитовидной железы, спорадической медуллярной карциномы щитовидной железы, болезни Гиршспрунга, феохромоцитомы, гиперплазии паращитовидной железы и невром слизистой оболочки желудочно-кишечного тракта, применению вещества, ингибирующего киназу RET, для получения указанного терапевтического средства и веществу, ингибирующему киназу RET, для указанного терапевтического средства.
Настоящее изобретение также относится к включающим вещество, ингибирующее киназу RET, терапевтическому средству и способу лечения карциномы щитовидной железы, применению вещества, ингибирующего киназу RET, для получения указанного терапевтического средства и веществу, ингибирующему киназу RET, для указанного терапевтического средства.
Кроме того, настоящее изобретение относится к фармацевтической композиции, включающей вещество, ингибирующее киназу RET, для введения в организм, содержащий клетки, экспрессирующие мутантную RET, способу лечения заболевания, включающему введение указанной фармацевтической композиции в организм, содержащий клетки, экспрессирующие мутантную RET, применению вещества, ингибирующего киназу RET, для получения указанной фармацевтической композиции и веществу, ингибирующему киназу RET, для указанной фармацевтической композиции.
Настоящее изобретение также относится к ингибитору киназы RET.
Кроме того, настоящее изобретение относится к способу прогнозирования действия вещества, ингибирующего киназу RET.
Конкретнее, действие вещества, ингибирующего киназу RET, можно прогнозировать с использованием в качестве показателя наличия или отсутствия в клетке мутации RET.
Так как способ по изобретению позволяет прогнозировать действие соединения без введения соединения пациенту, становится возможным отбор пациентов, которые, как предполагается, более чувствительны к соединению. Таким образом, становится возможным вклад в QOL пациента.
В тексте на естественном языке дается перечень последовательностей праймеров SEQ ID NOS: 5-20.