Результат интеллектуальной деятельности: СПОСОБ ИЗГОТОВЛЕНИЯ СЕНСОРОВ ДЛЯ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ САХАРОВ И ГИДРОКСИКИСЛОТ
Вид РИД
Изобретение
Область техники
Группа изобретений относится к аналитической химии, электроанализу, биохимии, электрохимическим сенсорам, тест-системам, методам лабораторной медицинской диагностики, методам анализа объектов пищевой промышленности и медицинских препаратов.
Уровень техники
Сахара и многие органические гидроксикислоты являются широко распространенными соединениями в природе, участниками метаболических процессов в организмах. Такие соединения встречаются в живых системах как в свободном виде, так и в связанном с биомолекулами, в составе клеточных стенок. Мониторинг концентрации этих соединений или их производных в физиологических жидкостях необходим для целей медицинской диагностики и лабораторных исследований. Среди методов определения биологических объектов, а также цельных макромолекул и клеток широко распространены биосенсоры [Карякин А.А., Корякина Е.Е., Проблемы аналитической химии. Т.12: Биохимические методы анализа, «Наука», 2010, с. 93-138]. Сенсоры на основе синтетических рецепторов при достаточно высокой чувствительности обладают некоторыми преимуществами по сравнению с биосенсорами, а именно, они электрохимически и химически стабильны на воздухе при комнатной температуре, методы их получения просты и не затратны, сенсор возможно регенерировать и использовать многократно [Artificial Receptors for Chemical Sensors, edited by V.M. Mirsky and A.K. Yatsimirsky, WILEY-VCH, 2011].
Фенилборные кислоты, способные селективно и обратимо связываться с сахарами (моно-, о лито- и полисахариды) и гидроксикислотами, а также некоторыми гликопротеинами с образованием устойчивых циклических боронатных эфиров, будучи включенными в структуру проводящих полимеров, например полианилина, служат высокоэффективными синтетическим материалами для создания электрохимических сенсоров для определения концентраций сахаров и оксикислот [Springsteen, G., Wang, B., Tetrahedron, V.58, 26, 2002, pp.5291-5300(10)].
Электроды, модифицированные проводящими полимерами, находят широкое применение в анализе в качестве сенсоров. Все известные подходы, использующие проводящие свойства полимеров для регистрации аналитического сигнала основаны на снижении проводимости чувствительного полимерного слоя, что не позволяет различать сигнал, обусловленный специфическими взаимодействиями с аналитом на фоне неспецифических процессов, которые также всегда приводят к снижению проводимости. [Santos A., Davis J.J., Bueno P.R., Fundamentals and Applications of Impedimetric and Redox Capacitive Biosensors, J. Analytical & Bioanalytical Techniques, 2015, S7.016; Ma, Y., Yang, X., J, Electroanalytical Chemistry, 2005, V. 580, p.348-352; Plesu, N., Kellenberger, A., Taranu, I., Taranu, В.О., Popa, I., Reactive and Functional Polymers, 2013, 73, 772-778; Liu, S.; Bakovic, L.; Chen, A., J. Electroanalitical Chemistry, 2006, V. 591, p.210-216.]
В ряде исследований описываются различные сенсоры на основе синтетических рецепторов, где аналитический сигнал регистрируют методом спектроскопии электрохимического импеданса в присутствии медиаторов. Как правило, такие системы применяются для биосенсоров, а не химических сенсоров.
В патенте Вадгама и др. [«Sensor employing impedance measurements», US 6300123 B1] раскрыто использование электродов, модифицированных проводящими полимерами, а аналитическим сигналом служит изменение полного импеданса системы. Однако, невозможно однозначно обуславливать изменение такого параметра системы как полный ее импеданс специфическим взаимодействиями с анализируемыми объектами, т.к. причинами такого изменения могут являться и второстепенные конкурирующие процессы. Указанная разработка относится к сфере биосенсоров, то есть взаимодействие аналита происходит не с самим полимером непосредственно, как синтетическим рецептором, а иммобилизованным биологическим элементом распознавания. Применение биологических элементов распознавания, несмотря на их несомненные достоинства: высокая чувствительность и селективность, ограничено их низкой стабильностью, необходимостью обеспечения определенных условий хранения и эксплуатации во избежание быстрой потери активности, а также слишком высокой аффиностью, приводящей лишь к однократной возможности проведения анализа с помощью отдельного сенсора, что исключает использование таких устройств в целях постоянного мониторинга или анализа в потоке в течение времени.
При модификации поверхности электрода проводящими поли(анилинборными кислотами), было показано, что в результате электрохимической полимеризации получается самодопированный полимер, электроактивный в нейтральных средах, как описано в патенте US 20070093644 («Switchable self-doped polyaniline»). Авторами показано изменение степени допирования полимера при связывании с сахарами, что подтверждается данными ИК- и 11В ЯМР-спектроскопии. Однако в указанной работе не проводились исследования непосредственно проводимости полимеров аминофенилборных кислот.
В патенте Фройнда и др. [«Sensors and sensing methods for detecting analytes based on changes in pKa of a sensing polymer», US 6797152], выбранного в качестве прототипа, описано применение сенсоров на основе поли(3-аминофенилборной кислоты), полученной посредством электрохимической полимеризации, для определения концентрации сахаров потенциометрическим методом. Аналитическим сигналом служит скачок потенциала, объясняемый авторами изменением рКа полимера в результате взаимодействия с аналитом. Чувствительность потенциометрического метода нельзя считать удовлетворительной для проведения анализа реальных объектов, кроме того, описанный способ не позволяет дифференцировать специфические взаимодействия функциональных групп полимера с аналитами от неспецифических, так как изменение рКа полимера может происходить по различным причинам, включая сдвиг рН фонового раствора, что не позволяет говорить о достоверных результатах анализа. В указанном патенте также нет сведений о том, обладает ли полученное сенсорное полимерное покрытие проводимостью. В заявленном изобретении, в отличие от указанного аналога, для определения концентрации аналитов используют высокочувствительный метод спектроскопии импеданса, а аналитический сигнал регистрируют в виде увеличения проводимости проводящего полимера аминофенилборной кислоты, что позволяет, в отличие от аналога, дифференцировать специфические взаимодействия с аналитами на фоне неспецифических.
Раскрытие изобретения
Задачей заявляемой группы изобретений является разработка способа получения электрохимического сенсора на основе синтетического полимерного материала и методики для достоверного определения концентрации сахаров и гидроксикислот с высокой точностью с использованием полученного сенсора.
Поставленная задача решается способом изготовления сенсора для определения концентрации сахаров и гидроксикислот в водных средах, включающим синтез поли(аминофенилборной кислоты) на поверхности электрода путем электрополимеризации, протекающий с постоянным увеличением скорости окисления аминофенилборной кислоты при фиксированном потенциале, с получением проводящего полимера, характеризующегося свойством уменьшения сопротивления при взаимодействии с сахарами и гидроксикислотами.
Предпочтительно в качестве аминофенилборной кислоты использовать 3-аминофенилборную кислоту, при этом синтез проводить в кислой среде в присутствии фторид-ионов.
Предпочтительно в качестве аминофенилборной кислоты использовать 2-аминофенилборную кислоту, при этом синтез ведут в кислоте, нормальность которой больше 0.1.
Поставленная задача также решается способом определения концентрации сахаров или гидроксикислот в водных средах с использованием полученного сенсора, путем его погружения в исследуемую среду, регистрацию спектра импеданса методом спектроскопии электрохимического импеданса и определением из него сопротивления R поли(аминофенилборной кислоты), с последующим определением количественного содержания искомого компонента по калибровочной кривой, предварительно полученной для сахара или гидроксикислоты.
Предпочтительно для получения калибровочной кривой сенсор помещают в буферный раствор, регистрируют методом спектроскопии электрохимического импеданса спектр и определяют из него сопротивление R полимера при введении пробы в буферный раствор, по процентному изменению сопротивления полимера в растворе, содержащем анализируемые соединения, относительно сопротивления в растворе, не содержащем аналитов, строят калибровочную кривую, представляющую собой нелинейную убывающую зависимость относительного сопротивления полимера от концентрации аналита.
Техническим результатом данной группы технических решений является то, что аналитический сигнал полученного сенсора направлен в сторону увеличения, а не ухудшения проводимости полимерной пленки, что позволяет наиболее селективно по сравнению с известными способами регистрировать только специфические взаимодействия с аналитами, исключая вклады побочных процессов (деградация полимера) и конкурирующих реакций, которые всегда приводят к потере проводимости. Селективность обеспечивается проводящими свойствами полимеров, синтезированных на поверхности электродов, а именно способностью полученных полимеров к увеличению проводимости в результате взаимодействия функциональных групп полимера с аналитами. Направленность отклика в сторону увеличения проводимости позволяет отличить полезный сигнал от мешающего, дифференцируя специфические взаимодействия на фоне неспецифических. Эффект увеличения проводимости полимерного покрытия в результате взаимодействия с аналитами достигается при электрохимическом синтезе поли(анилинборных кислот) в условиях, способствующих формированию на поверхности электрода проводящего полимерного покрытия полианилиновой структуры, а также при регистрации сопротивления полимера в отсутствии и присутствии аналита высокочувствительным методом спектроскопии электрохимического импеданса.
Таким образом, с помощью сенсоров на основе проводящих полимеров аминофенилборных кислот возможно проводить селективное количественное определение сахаров или гидроксикислот в анализируемых объектах с высокой точностью. Методом спектроскопии электрохимического импеданса регистрируют обратимое увеличение проводимости полимерного покрытия на поверхности электрода в результате быстрой и обратимой реакции протекающей в нейтральной среде между борными группами полимера, осажденного на электроде, с сахарами и гидроксикислотами, находящимися в растворе. Заявляется способ получения сенсора на основе поли(аминофенилборной кислоты) и способ его использования для определении концентрации аналитов по увеличению проводимости полимерного покрытия, регистрируемого методом спектроскопии электрохимического импеданса.
Краткое описание чертежей
Изобретение поясняется чертежами.
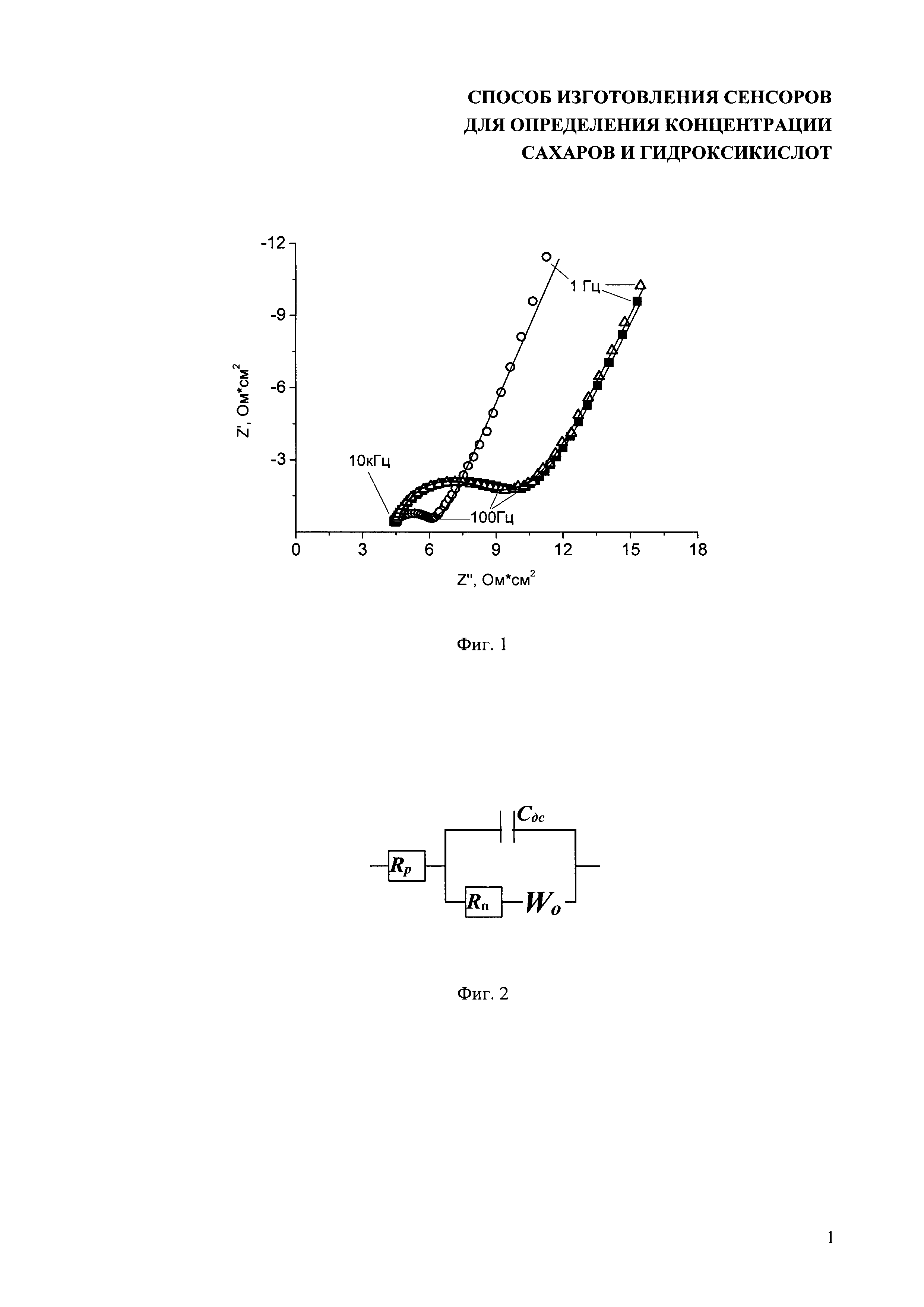
На фиг. 1 показаны спектры электрохимического импеданса стеклоуглеродных электродов, модифицированных поли(АФБК): в буферном растворе, не содержащем аналит (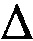 ), в присутствии аналита (
), в присутствии аналита ( ), в исходном буферном растворе после проведения анализа (
), в исходном буферном растворе после проведения анализа ( ); результат аппроксимации в соответствии с эквивалентной электрической схемой (
); результат аппроксимации в соответствии с эквивалентной электрической схемой ( ).
).
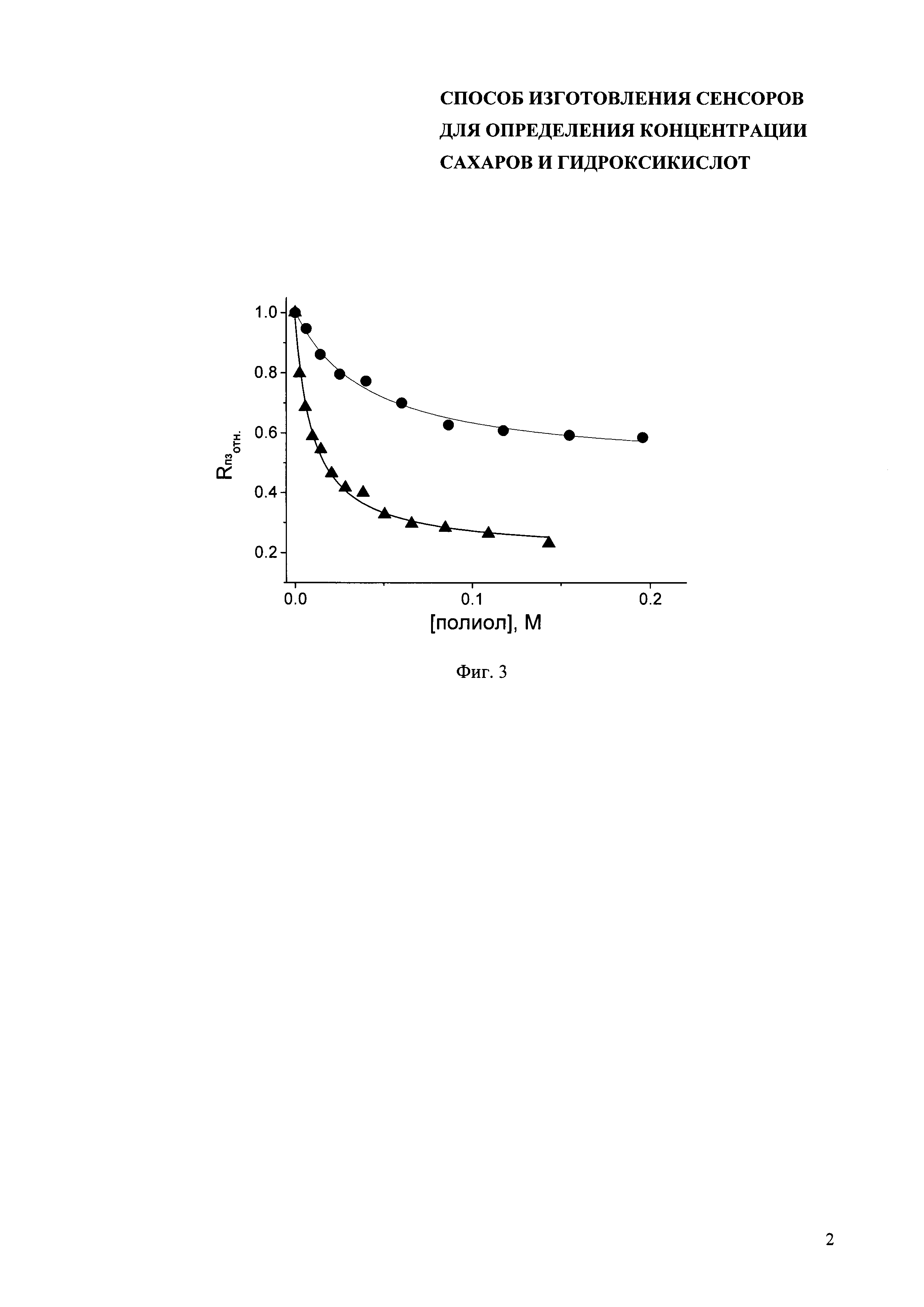
На фиг. 2 представлена эквивалентная электрическая схема с диффузионным импедансом, где Rр - сопротивление фонового раствора, Rп - сопротивление переносу заряда в полимерной пленке (в рассматриваемой системе эквивалентно сопротивлению полимера на поверхности электрода), Сдс - емкость двойного электрического слоя, W0 - диффузионный импеданс в случае отражающих граничных условий.
На фиг. 3 представлены градуировочные зависимости сенсоров на основе поли(АФБК): фруктоза ( ), лактат (
), лактат ( ), в 50 мМ фосфатном буферном растворе рН 7.0 для сахара и рН 6.0 для гидроксикислоты.
), в 50 мМ фосфатном буферном растворе рН 7.0 для сахара и рН 6.0 для гидроксикислоты.
Осуществление изобретения
Сенсоры для определения концентрации сахаров или гидроксикислот изготавливают, модифицируя поверхность электродов проводящими полимерами аминофенилборных кислот. Синтез проводящих полимеров на поверхности электродов проводят в электрохимической ячейке путем погружения рабочего как макро-, так и микроэлектрода любой конструкции: планарные, торцевые, взаимопроникающие и т.д. из различных материалов: золото, стеклоуглерод, графит и т.д. [Electropolymerization: Concepts, Materials and Applications, ed. by S. Cosnier and A. Karyakin, 2010, WILEY-VCH, 280 pp.] в ростовую смесь, находящуюся в ячейке, подключении электродов ячейки к прибору (потенциостат/гальваностат) и запуска выбранного электрохимического режима с заданными параметрами. Оптимальным условиям электрохимического синтеза проводящего полимера из аминофенилборных кислот отвечает полимеризация из раствора мономера в кислой среде в потенциодинамическом, гальваностатическом, потенциостатическом и т.п. режимах [Electrochemical methods. Fundamentals and applications, Bard A. J., Faulkner L.R. 2001, John Wiley & Sons, Inc.] при значениях тока или потенциала, не допускающих переокисление полимера, ведущее к потере проводимости [Electropolymerization: Concepts, Materials and Applications, ed.by S. Cosnier and A. Karyakin, 2010, WILEY-VCH, 280 pp.]. Электрополимеризацию 3-аминофенилборной кислоты (3-АФБК) (0.01-0.1М) проводят в растворе, содержащем 0.01-2.0Н кислоту и пятикратный избыток фторида по отношению к аминофенилборной кислоте. Электрополимеризацию 2-аминофенилборной кислоты (2-АФБК) (0.1-1.0М) проводят в растворе 0.05-1.0 М H2SO4. Во избежание переокисления полимера, ведущего к деградации и потере проводимости, стоит избегать высоких анодных потенциалов. О формировании проводящего покрытия на поверхности электрода судят по росту тока при фиксированном потенциале в анодной области 0.6-1 В, соответствующем процессу окисления молекул мономера.
В качестве источника фторид ионов могут быть использованы соли плавиковой кислоты, растворимые в водной среде, содержащие в качестве катиона, как ион металла, так и органический катион.
В качестве кислот для осуществления способа могут быть использованы водорастворимые карбоновые кислоты, содержащие гидроксильную группу в α- или β-положении.
Проводимость полученных на поверхности электрода полимерных пленок затем исследуют методом спектроскопии электрохимического импеданса в буферных растворах с различными значениями рН (5.0÷8.0). Спектры электрохимического импеданса регистрируют в диапазоне частот от 20 кГц до 1 Гц с амплитудой наложенного напряжения 5 мВ. Диапазон частот можно расширить в зависимости от толщины полимерной пленки на поверхности электрода. Спектры импеданса представляют собой трехмерные графики зависимостей мнимой и действительной частей импеданса от частоты. Для последующего анализа и определения проводимости полимеров аминофенилборных кислот удобно представить выходные данные (спектры) в координатах Найквиста, в виде проекции на плоскость при фиксированных частотах, как на фиг. 1.
Аппроксимацию полученных спектров импеданса проводят в соответствии с эквивалентной электрической схемой с диффузионным импедансом (фиг. 2), наиболее применимой для описания проводящих полимерных пленок, иммобилизованных на поверхности электродов в фоновом электролите в отсутствии медиатора [Inzelt G.,  G.G. Electropolymerization, Wiley-VCH, 2010, p.51-76]. Эквивалентная схема состоит из последовательно соединенных резистора Rp и конденсатора Сдс, с параллельно подключенным вторым резистором Rп и не имеющим электрического аналога элементом W0, соответствующем диффузии при отражающих граничных условиях. При введении аналита в ячейку, содержащую фоновый буферный раствор, диаметр высокочастотного полукруга, соответствующий сопротивлению переносу заряда в полимерной пленке (Rп на электрической схеме) уменьшается. Уменьшение величины этого сопротивления свидетельствует об увеличении проводимости полимерной пленки при взаимодействии полимера с аналитами. Наблюдаемый отклик системы, приводящий к увеличению проводимости полимерной пленки, является полностью обратимым, что также представлено на фиг. 1. После регистрации уменьшения проводимости в присутствии аналита раствор заменяют на исходный буферный раствор, не содержащий аналита, и сопротивление полимера возвращается к исходному значению, а спектр импеданса, в свою очередь, к своему первоначальному виду.
G.G. Electropolymerization, Wiley-VCH, 2010, p.51-76]. Эквивалентная схема состоит из последовательно соединенных резистора Rp и конденсатора Сдс, с параллельно подключенным вторым резистором Rп и не имеющим электрического аналога элементом W0, соответствующем диффузии при отражающих граничных условиях. При введении аналита в ячейку, содержащую фоновый буферный раствор, диаметр высокочастотного полукруга, соответствующий сопротивлению переносу заряда в полимерной пленке (Rп на электрической схеме) уменьшается. Уменьшение величины этого сопротивления свидетельствует об увеличении проводимости полимерной пленки при взаимодействии полимера с аналитами. Наблюдаемый отклик системы, приводящий к увеличению проводимости полимерной пленки, является полностью обратимым, что также представлено на фиг. 1. После регистрации уменьшения проводимости в присутствии аналита раствор заменяют на исходный буферный раствор, не содержащий аналита, и сопротивление полимера возвращается к исходному значению, а спектр импеданса, в свою очередь, к своему первоначальному виду.
Для количественной оценки использовали метод калибровочного графика. Градуировочные кривые представляют собой нелинейные убывающие зависимости относительного изменения сопротивления от концентрации аналита, которые хорошо описываются уравнением формулы (1). Используя калибровочные зависимости, определяют неизвестную концентрацию аналита в образце по увеличению проводимости полимера в растворе образца. Новый подход к проведению аналитического определения концентраций сахаридов и гидроксикислот в жидких средах, основанный на обратимом увеличении проводимости полимерного чувствительного слоя сенсора в результате взаимодействия с определяемыми соединениями, позволяет по направлению отклика сенсора надежно дифференцировать полезный сигнал специфических взаимодействий от фонового, сопровождающегося увеличением сопротивления и обусловленного неспецифическими взаимодействиями.
На фиг. 3 приведены примеры зависимостей нормированного сопротивления от концентрации сахаров (фруктоза, глюкоза) и соли гидроксикислоты (лактат калия). Калибровочный график представляет собой убывающую функцию: сопротивление падает при увеличении концентрации сахара или гидроксикислоты. Полученные зависимости позволяют определить соответствующие наблюдаемые константы связывания аналитов с борными группами полимера, используя уравнение (1):

где С - концентрация аналита, Rотн - относительное сопротивление полимера, a и b - параметры аппроксимации, k - наблюдаемая константа связывания полимера с аналитом. Сплошной линией на фиг. 3 показан результат аппроксимации экспериментальных данных.
Градуировочные зависимости сенсора на основе поли(анилинборных кислот) представляют собой убывающую функцию относительного сопротивления переноса заряда от концентрации аналита. Таким образом, возможно по увеличению проводимости полимерной пленки на поверхности электрода определить неизвестную концентрацию сахари да или гидроксикислоты в образце.
Сенсором на основе поли(анилинборных кислот), полученным заявляемым способом можно определять любые соединения классов сахара и гидроксикислоты. Более того, были получены данные и при определении веществ и биомолекул, включающих структурные фрагменты, присущие данным классам.
Пример 1
Сенсор для определения концентрации сахаров и гидроксикислот на основе проводящего полимера, полученного полимеризацией 3-аминофенилборной кислоты в потенциодинамическом режиме.
Электрополимеризацию 3-аминофенилборной кислоты (3-АФБК) (0.04М) проводили в трехэлектродной электрохимической ячейке с разделенным пространством рабочего электрода, электрода сравнения и вспомогательного электрода в режиме циклической вольтамперометрии из раствора, содержащего 0.04М H2SO4 и 0.2М NaF, на стеклоуглеродном рабочем электроде в диапазоне потенциалов от 0.0 В до 0.9 В относительно хлоридсеребряного электрода сравнения со скоростью развертки 40 мВ/с в течение 10 циклов.
Для регистрации спектров электрохимического импеданса электродов модифицированных проводящей поли(аминофенилборной кислотой) использовали трехэлектродную ячейку с разделенным пространством рабочего электрода и электрода сравнения. В качестве вспомогательного электрода использовали платиновую сетку цилиндрической формы, коаксиальную рабочему электроду. Спектры электрохимического импеданса электродов модифицированных проводящей поли(аминофенилборной кислотой) регистрировали в до достижения стабильного спектра (импеданс на одной и той же частоте в двух последовательно записанных спектрах совпадает с максимальным отклонением в 2-3%) в 50 мМ фосфатном буферном растворе (KH2PO4, K2HPO4), рН 7.0, содержащем 0.1М KCl, в диапазоне частот от 10 кГц до 1 Гц, амплитуда наложенного напряжения составляла 5 мВ. Конечный (стабильный) спектр импеданса представлен в координатах Найквиста, то есть в виде зависимостей мнимой составляющей импеданса системы от действительной (точки типа треугольник на фиг. 1): Затем в ячейку вводили водный раствор фруктозы (конечная концентрация в ячейке 20 мМ) и снова регистрировали спектры импеданса до достижения стабильного спектра (полного совпадения двух последующих спектров в пределах 2% отклонения). Спектр также представляли в координатах Найквиста (точки типа круг на фиг. 1). Затем, после проведения определения, буферный раствор в ячейке, содержащий фруктозу, заменили на исходный буферный раствор, не содержащий сахара, и снова записывали спектры импеданса. Конечный спектр представлен на фиг. 1 точками типа квадрат. Видно, что спектр импеданса, записанный после проведения определения фруктозы, возвращается к своему первоначальному виду, что говорит об обратимости процесса связывания сахара с полимерной пленкой.
Аппроксимацию полученных спектров импеданса проводили в соответствии с эквивалентной электрической схемой с диффузионным импедансом (фиг. 2). На фиг. 1 точками представлены экспериментальные данные, а прямые - есть результат их аппроксимации по приведенной схеме. Можно заключить, что данный способ обработки экспериментальных данных является наиболее подходящим, так как ошибка аппроксимации чрезвычайно мала (не превышает 4%). Исходя из результатов аппроксимации, для всех полученных спектров были рассчитаны значения элементов приведенной эквивалентной схемы. Практический интерес представляют значения сопротивления переносу заряда в полимерной пленке (Rп на схеме на фиг. 2), соответствующие диаметру высокочастотного полукруга на спектрах импеданса, представленных в координатах Найквиста на фиг. 1. Значения сопротивлений с учетом погрешностей аппроксимации приведены в табл. 1. На рисунке видно, что также подтверждается рассчитанными значениями Rп, что при введении аналита в ячейку, содержащую фосфатный буферный раствор, диаметр высокочастотного полукруга, соответствующий сопротивлению полимера (Rп) уменьшается, что свидетельствует об увеличении проводимости полимерной пленки в результате взаимодействия полимера с аналитом. Возврат спектра (и соответственно значений Rп) к первоначальному виду после проведения анализа говорит о том, что отклик системы, приводящий к увеличению проводимости полимерной пленки, является полностью обратимым.

Пример 2
Определение концентрации сахаров и гидроксикислот с помощью сенсора на основе проводящего полимера, полученного полимеризацией 3-аминофенилборной кислоты.
Синтез полимерного покрытия на поверхности электрода и регистрацию спектров импеданса в буферном растворе проводили, как описано в примере 1. После записи спектра импеданса в исходном буферном растворе в ячейке последовательно увеличивали концентрацию сахара. Регистрировали спектры импеданса при каждой концентрации, аппроксимировали и рассчитывали сопротивление полимера, как описано в примере 1. Затем строили концентрационные зависимости относительного сопротивления полимера (отношение сопротивления, рассчитанного при данной концентрации сахара к исходному сопротивлению в буферном растворе в отсутствии сахара). На фиг. 3 обозначенные точками приведены зависимости такого нормированного сопротивления от концентрации сахаров (фруктоза, глюкоза) и соли гидроксикислоты (лактат калия). Калибровочная зависимость представляет собой убывающую функцию: сопротивление падает при увеличении концентрации сахара или гидроксикислоты. Полученные зависимости аппроксимировали в соответствии с приведенным уравнением (1):
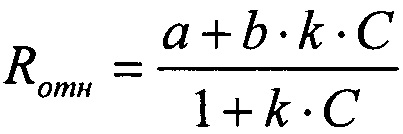 ,
,
где С - концентрация аналита, Rотн - относительное сопротивление полимера, a и b - параметры аппроксимации, k - наблюдаемая константа связывания полимера с аналитом.
Сплошной линией на фиг. 3 показан результат аппроксимации экспериментальных данных. Результат аппроксимации позволяет определить соответствующие наблюдаемые константы связывания сахаров и гидроксикислот с борными группами полимера. Рассчитанные константы приведены в табл. 2.

Пример 3
Сенсор для определения концентрации сахаров и гидроксикислот на основе проводящего полимера, полученного полимеризацией 3-аминофенилборной кислоты в гальваностатическом режиме.
Электроосаждение 3-аминофенилбороновой кислоты проводили в ячейке с тремя разделенными пространствами электродов, заполненной раствором фонового электролита: 0.1 М H2SO4, 0.2 М NaF. Пространство рабочего электрода заполняли раствором мономера 3-АФБК (40 мМ) в фоновом электролите. Электрополимеризацию осуществляли в гальваностатическом режиме при плотностях тока 0.1-0.6 мА/см2. Далее, как описано в примере 1 и 2.
Пример 4
Сенсор для определения концентрации сахаров и гидроксикислот на основе проводящего полимера, полученного полимеризацией 2-аминофенилборной кислоты в потенциодинамическом режиме.
Электрополимеризацию 2-аминофенилборной кислоты (2-АФБК) (0.1М) проводили в трехэлектродной электрохимической ячейке в режиме циклической вольтамперометрии из раствора, содержащего 1.0 М H2SO4, на стеклоуглеродном дисковом рабочем электроде в диапазоне потенциалов от 0.0 В до 0.98 В относительно хлоридсеребряного электрода сравнения со скоростью развертки 40 мВ/с в течение 30 циклов. Далее, как описано в примере 1. Концентрационные зависимости получали аналогично описанному в примере 2. Рассчитанные константы связывания представлены в таблице 3.

Аналогичные калибровочные зависимости были получены и определены константы связывания как для упомянутых сахаров и гидроксикислот при других значениях рН в диапазоне от 5.5 до 8.0, так и для других сахаров и гидроксикислот в указанном диапазоне рН. По величине сопротивления поли(аминофенилборной кислоты) в анализируемом растворе сахара или гидроксикислоты определяют неизвестную концентрацию в образце, используя калибровочные зависимости, предварительно полученные для сенсора.
Таким образом, преимуществом заявленного сенсора на основе синтетического полимерного материала является точность и достоверность определения сахаров и гидроксикислот. Регистрируемый методом спектроскопии импеданса эффект увеличения проводимости полимерной пленки на поверхности электрода обусловлен исключительно специфическими взаимодействиями полимера с аналитом. При проведении определения по заявленной методике исключено влияние побочных процессов и конкурирующих реакций, которые всегда приводят к обратному эффекту снижения проводимости полимерной пленки.
Сенсоры на основе поли(аминофенилборной кислоты) могут быть востребованы для определения концентрации диолов, полиолов, моно- и полисахаридов, гидроксикислот, гликозилированных биомолекул в различных объектах (модельные растворы, физиологические жидкости, медицинские препараты, пищевые объекты) в целях лабораторной медицинской диагностики, биохимического анализа, контроля качества медицинских препаратов и объектов пищевой промышленности.