Результат интеллектуальной деятельности: Способ оценки суммарного показателя анеуплоидии и пролиферативной активности опухолевых клеток немелкоклеточного рака легкого и рака яичников с использованием специфического красителя ДНК нового поколения DRAQ7
Вид РИД
Изобретение
Изобретение относится к области медицины, а именно к способам оценки плоидности и пролиферативной активности опухоли при немелкоклеточном раке легкого и раке яичников.
Плоидность опухолей является одним из важных прогностических показателей злокачественных опухолей, как и пролиферативная активность опухоли, оцениваемая по доли клеток, находящихся в S-фазе клеточного цикла.
Анеуплоидия опухоли коррелирует с низкой выживаемостью больных тиреоидной карциномой [Pinto А.Е., Silva G., Banito A., Leite V., Soares J. Aneuploidy and high S-phase as biomarkers of poor clinical outcome in poorly differentiated and anaplastic thyroid carcinoma. Oncology Reports 2008, Vol. 20, p. 913-919], а также с агрессивностью течения заболевания и увеличивается на поздних стадиях колоректального рака и рака желудка [Risques R.-A., Moreno V., Marcuello E., Petriz J., Cancelas J. A., Sancho F.J., Torregrosa  .,
.,  G., Peinado M.A. Redefining the significance of aneuploidy in the prognostic assessment of colorectal cancer. Laboratory investigation 2001, Vol. 81, № 3, p. 307; Tsujimoto H., Sugihara H., Hagiwara A., Hattori T. Amplification of growth factor receptor genes and DNA ploidy pattern in the progression of gastric cancer. Virchows Arch 1997, Vol. 31, p. 383-389]. Показатели лучшей общей и безрецидивной выживаемости выше у пациентов с диплоидными злокачественными опухолями молочной железы [Cornelisse C.J., van de Velde C.J.H, Caspers R.J.C., Moolenaar A.J., Hemans J. DNA ploidy and survival in breast cancer patients. Cytometry 1987, Vol. 8, p. 225-234]. В анеуплоидных злокачественных опухолях молочной железы достоверно повышается количество клеток, находящихся в S-фазе клеточного цикла [M.-L. Jourdan, Ferrero-Pous М., Spyratos F., Romain S., Martin P.-M., Chassevent A. Flow cytometric S-phase fraction measurement in breast carcinoma: influence of software and histogram resolution. Cytometry 2002, Vol. 48, p. 66-70]. У больных раком молочной железы с анеуплоидными опухолями вне зависимости от стадии болезни чаще проявляются рецидивы и метастазы, по сравнению с диплоидными опухолями [Николаева Т.Г. Проточная ДНК-цитометрия в прогнозировании течения опухолевого процесса при некоторых злокачественных новообразованиях человека: Автореф. дис. докт. биол. наук: 14.00.14 / Николаева Т.Г. - Москва, 2003. - 44 с.].
G., Peinado M.A. Redefining the significance of aneuploidy in the prognostic assessment of colorectal cancer. Laboratory investigation 2001, Vol. 81, № 3, p. 307; Tsujimoto H., Sugihara H., Hagiwara A., Hattori T. Amplification of growth factor receptor genes and DNA ploidy pattern in the progression of gastric cancer. Virchows Arch 1997, Vol. 31, p. 383-389]. Показатели лучшей общей и безрецидивной выживаемости выше у пациентов с диплоидными злокачественными опухолями молочной железы [Cornelisse C.J., van de Velde C.J.H, Caspers R.J.C., Moolenaar A.J., Hemans J. DNA ploidy and survival in breast cancer patients. Cytometry 1987, Vol. 8, p. 225-234]. В анеуплоидных злокачественных опухолях молочной железы достоверно повышается количество клеток, находящихся в S-фазе клеточного цикла [M.-L. Jourdan, Ferrero-Pous М., Spyratos F., Romain S., Martin P.-M., Chassevent A. Flow cytometric S-phase fraction measurement in breast carcinoma: influence of software and histogram resolution. Cytometry 2002, Vol. 48, p. 66-70]. У больных раком молочной железы с анеуплоидными опухолями вне зависимости от стадии болезни чаще проявляются рецидивы и метастазы, по сравнению с диплоидными опухолями [Николаева Т.Г. Проточная ДНК-цитометрия в прогнозировании течения опухолевого процесса при некоторых злокачественных новообразованиях человека: Автореф. дис. докт. биол. наук: 14.00.14 / Николаева Т.Г. - Москва, 2003. - 44 с.].
Низкая доля фракции клеток в S-фазе строго коррелирует с лучшей безрецидивной и общей выживаемостью больных раком молочной железы [O'Reilly S.M., Camplejohn R.S., Barnes D.M., Millis R.R., Allen D., Rubens R.D., Richards M.A. DNA index, S-phase fraction, histological grade and prognosis in breast cancer. Br.J. Cancer 1990, Vol. 61, p. 671-674]. Высокая доля фракции клеток в S-фазе в диплоидных опухолях коррелирует с высокой стадией опухолевого процесса, низкой безрецидивной выживаемостью и с низкой общей выживаемостью больных раком молочной железы [Romero Н., Schneider J., Burgos J., Bilbao J., Rodriguez-Escudero F.J. S-phase fraction identifies high-risk subgroups among DNA-diploid breast cancers. Breast Cancer Res Treat. 1996, Vol., 38, №3, p. 265-275].
Известен способ оценки плоидности опухоли и доли клеток, находящихся в S-фазе клеточного цикла, с помощью проточной цитофлуориметрии [Портной С.М. Рак молочной железы (факторы прогноза и лечение). Дисс. д.м.н. / Портной С.М. - Москва, 1997. - 306 с.].
Образец опухолевой ткани, полученный во время операции, измельчают бритвой в чашке Петри в объеме 0,5 мл профильтрованного через 0,45 мкм миллипоровый фильтр Трис-НСl-буфера (рН=7,4) или 0,9% раствора NaCl до получения клеточной суспензии. Клеточную суспензию тщательно перемешивают в течение 3 минут автоматической пипеткой до получения однородной взвеси клеток, затем фильтруют в градуированную центрифужную пробирку сначала через редкий фильтр (поры 500-600 мкм), затем через стандартный нейлоновый фильтр с диаметром пор 100-130 мкм. Далее суспензия фиксируется (если нужно отсрочить проведение исследования) или сразу после окрашивания исследуется на проточном анализаторе. Фиксацию клеток осуществляют двумя методами: к 1-1,5 мл клеточной суспензии добавляют по капле 9 мл холодной (4°С) смеси этанол-ацетон (1:1), все время тщательно пипетируя клеточную взвесь во избежание слипания клеток; по другой методике к 0,5-1,0 мл клеточной суспензии добавляют по капле 96% этанол, при этом суспензия постоянно пипетируется с помощью автоматической пипетки. Концентрация спирта в суспензии постепенно увеличивается до 70%. Пробирки плотно закрывают резиновыми пробками или пленкой Parafilm "М" и после 48-часовой фиксации при 20°С клетки могут быть подвергнуты окраске.
Окрашивание ДНК осуществляется акридиновым оранжевым либо смесью бромид этидия + митромицин.
Индекс плоидности вычисляют как соотношение интенсивности флуоресценции пика G0/G1 опухолевых клеток к интенсивности флуоресценции пика G0/G1 диплоидного стандарта. По соотношениям площадей: пика G0/G1, S-фазы и фаз G2/M вычисляется процентное распределение опухолевых клеток по фазам клеточного цикла. Сумма долей клеток, находящихся в S-фазе и фазах G2/M, обозначается как индекс пролиферативной активности.
Недостатки способа:
Данный способ требует значительных временных затрат с применением фиксации опухолевого материала - более 48 часов. Исследование же плоидности и пролиферативной активности опухоли указанным способом без фиксации малоприменим в клинической практике в связи с необходимостью исследования материала сразу же после операции, что даже при незначительном увеличении определенного времени работы с живыми клетками часто приводит к повреждению клеток.
Вследствие того, что акридиновый оранжевый и бромид этидия кроме ДНК связываются и с РНК, усложняется аналитический этап: применение ферментов, требующих тестирование их активности; увеличение количества этапов анализа и контролей. Это приводит к увеличению процента неинформативных гистограмм и неправильной диагностике анеуплоидии или высокой пролиферативной активности опухоли.
Использование нескольких красителей нуклеиновых кислот, что увеличивает количество этапов и усложняет процедуру анализа.
Существующие алгоритмы математической обработки данных результатов окрашивания ДНК не унифицированы и не позволяют получить сопоставимые межлабораторные результаты анализа фаз клеточного цикла отдельно от анеуплоидных клеток. Использование даже одной программы в разных лабораториях может привести к различному диагнозу при исследовании плоидности и пролиферативной активности одной и той же опухоли.
Расчет раздельно трех показателей по гистограмме распределения клеток по окрашиванию ДНК приводит к усложнению анализа, из-за чего значительно повышается процент ошибки определения количества клеток в разных фазах клеточного цикла и анеуплоидных клеток.
Недостатком также является отсутствие анализа показателя, включающего суммарную фракцию клеток, ассоциированных с плохим прогнозом.
Задачей изобретения является создание нового способа оценки плоидности опухоли и чувствительности к химиотерапии в ткани немелкоклеточного рака легкого и рака яичников с помощью интегрального показателя анеуплоидии и пролиферативной активности опухоли, позволяющего количественно оценивать объединенную фракцию клеток, определяющих прогноз заболевания: анеуплоидные клетки и клетки в М, S и G2 фазах клеточного цикла независимо от плоидности опухоли.
Технический результат изобретения заключается в том, что заявляемый способ позволяет оценить прогноз течения и чувствительности к химиотерапии на основе интегрального показателя - количественного анализа в опухолевой ткани суммарной фракции клеток, определяющих прогноз заболевания: анеуплоидные клетки и клетки в М, S и G2 фазах клеточного цикла, а также оценить чувствительность опухоли к химиотерапии. Способ требует небольших временных затрат - около 1,5 часов и небольшое количество манипуляций. Изначальная фиксация операционного образца только в 4% растворе формальдегида обеспечивает безошибочное проведение преданалитического этапа. В результате достигается высокий процент «информативных» гистограмм. Расчет одного показателя вместо трех упрощает анализ, делает его строго количественным и позволяет сравнивать данные разных лабораторий, что приводит к улучшению межлабораторной воспроизводимости результатов. Задача решается тем, что:
Образец опухоли фиксируют в 4% растворе формальдегида, готовят одноклеточную суспензию, окрашивают специфическим красителем ДНК нового поколения DRAQ7, проводят анализ на проточном цитофлуориметре, строят гистограммы распределения клеток по интенсивности окрашивания ДНК в программе WinMDI 2.9, расставляют маркеры, отделяющие пики диплоидных клеток в G0/G1 фазах клеточного цикла от анеуплоидных и клеток в М, S и G2 фазах цикла, делят количество анеуплоидных клеток и клеток в М, S и G2 фазах клеточного цикла на суммарное число клеток, рассчитывают суммарный показатель процента клеток, ассоциированных с неблагоприятным прогнозом. Превышение интегральным показателем 30% указывает на неблагоприятный прогноз заболевания и резистентность опухоли к химиотерапии, значение суммарного показателя менее 30% указывает на благоприятный прогноз и чувствительность опухоли к химиотерапии.
Способ осуществляется следующим образом.
Приготовление одноклеточной суспензии из операционных образцов
Образец опухолевой ткани помещали в 4% раствор формальдегида в фосфатном буфере рН=7,4. Фиксированную опухолевую ткань разрезали ножницами на мелкие кусочки объемом менее 1 мм3 в чашке Петри и добавляли в полученную кашицу раствор Версена. Затем инкубировали в течение 30 мин в термостате при t= +37°C. После инкубации содержимое чашки Петри гомогенизировали в цилиндрическом стеклянном гомогенизаторе и переносили в пробирку объемом 50 мл, доводя фосфатным буфером рН=7,4 объем жидкости до 40 мл. Далее проводили фильтрацию суспензии с помощью фильтра с диаметром пор 40 мкм, центрифугировали в течение 10 мин при 3 тыс. об/мин. Надосадочную жидкость удаляли пипеткой, а осадок ресуспендировали в 3-7 мл раствора фосфатного буфера рН=7,4. Количество клеток в полученной суспензии подсчитывали в камере Горяева.
Окрашивание клеток специфическим красителем ДНК DRAQ7 для определения плоидности и количества клеток в М, S и G2 фазах клеточного цикла
Окрашивание проводили в 100 мкл одноклеточной суспензии с концентрацией 400 тыс. клеток/мл. Для отмывания клеток от формальдегида к суспензии клеток в пробирке для проточного цитофлуориметра добавляли фосфатный буферный раствор рН=7,4 до 3 мл. Затем центрифугировали в течение 5 мин со скоростью 3 тыс. об/мин, отбирали надосадочную жидкость, оставляя 100 мкл раствора и перемешивали пипетированием. После этого добавляли краситель ДНК DRAQ7 до конечной концентрации 5 мкМ и перемешивали встряхиванием. Инкубировали в течение 5 мин при комнатной температуре.
Измерение флуоресценции проводили на проточном цитофлуориметре при λех=633 нм, λем=755 нм и более. Число анализируемых событий - 10 тыс. Анализ гистограмм проводили с помощью программы WinMDI 2.9.
Расчет интегрального показателя анеуплоидии и пролиферативной активности опухоли
Для оценки интегрального показателя анеуплоидии и пролиферативной активности клеток проводили анализ гистограммы распределения клеток по интенсивности окрашивания опухолевых клеток специфическим красителем ДНК DRAQ7. При этом на гистограмме устанавливали маркеры, отделяющие пик, соответствующий диплоидным клеткам в G0/G1 фазах клеточного цикла от остальных - анеуплоидных и клеток в М, S и G2 фазах цикла независимо от плоидности. Это позволило разделить опухолевые клетки на две части, имеющие разное прогностическое значение, и подсчитать их количество. Путем деления количества анеуплоидных клеток и клеток в М, S и G2 фазах клеточного цикла на общее число клеток рассчитывали интегральный показатель клеток, ассоциированных с неблагоприятным прогнозом заболевания. Порог интегрального показателя принимали за 30%, так как при таком значении достигается значительное статистически достоверное разделение по прогнозу (р<0,05, по критерию Стьюдента для групп с нормальным распределением и по критерию Манна-Уитни для групп с ненормальным распределением признака).
Расчет интегрального показателя анеуплоидии и пролиферативной активности
I=M2/M1×100%,
где I - интегральный показатель анеуплоидии и пролиферативной активности клеток,
M1 - суммарное количество опухолевых клеток,
М2 - количество клеток в фазах М, S и G2 фазах цикла независимо от плоидности.
Значение порога рассчитывается с помощью статистической обработки всех полученных значений процента клеток в М, S и G2 фазах цикла независимо от плоидности и определения медианы.
Формула расчета порога интегрального показателя анеуплоидии и пролиферативной активности клеток для ряда данных, содержащих нечетное количество значений
MI=x N+1/2
где I - интегральный показатель анеуплоидии и пролиферативной активности клеток,
MI - значение порога, разделяющего низкий и высокий уровни I,
N - номер значений I в ряду, отсортированного по увеличению значений,
х N+1/2 - значение показателя интегрального показателя анеуплоидии и пролиферативной активности клеток с номером N+1/2.
Формула расчета порога интегрального показателя анеуплоидии и пролиферативной активности клеток для ряда данных, содержащих четное количество значений
MI=xN/2+x N/2+1/2
где I - интегральный показатель анеуплоидии и пролиферативной активности клеток,
MI - значение порога, разделяющего низкий и высокий уровни I,
N - номер значений I в ряду, отсортированного по увеличению значений,
х N/2 - значение показателя интегрального показателя анеуплоидии и пролиферативной активности клеток с номером N2,
х N+1/2 - значение показателя интегрального показателя анеуплоидии и пролиферативной активности клеток с номером N+1/2.
Превышение интегрального показателя 30% указывало на неблагоприятный прогноз заболевания и позволяет диагностировать опухоли, имеющие агрессивное течение (плоскоклеточный рак легкого). Значения интегрального показателя менее 30% позволяло диагностировать опухоли с более благоприятным прогнозом (аденокарциномы легкого).
Изобретение иллюстрируется фиг. 1-4.
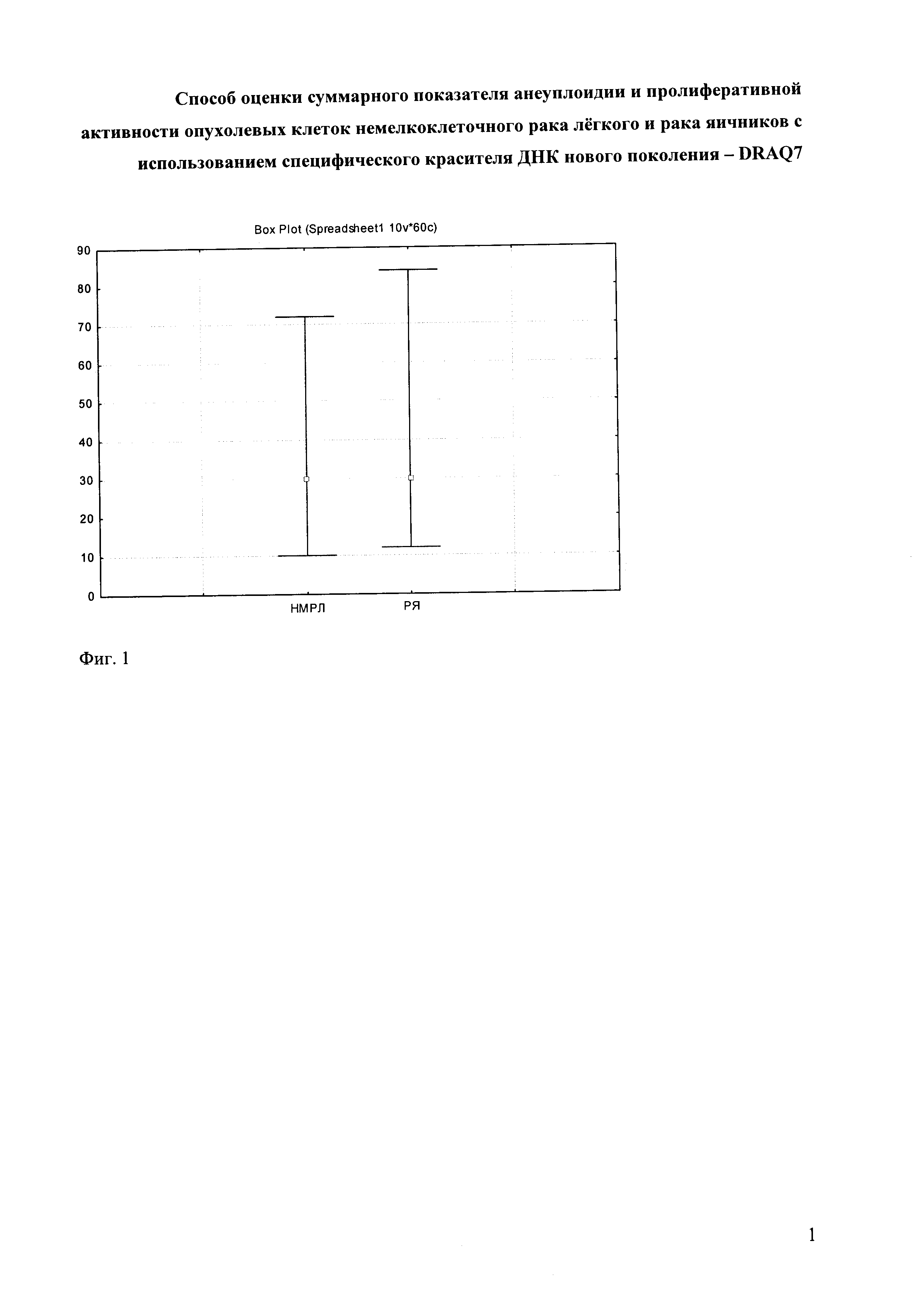
На фиг. 1 представлено распределение всех значений интегрального показателя анеуплоидии и пролиферативной активности клеток в тканях немелкоклеточного рака легкого (НМРЛ) и рака яичников (РЯ). Горизонтальные линии отделяют минимальные и максимальные значения показателя I, а выделенное квадратом значение 30% является порогом, разделяющим низкий и высокий уровни.
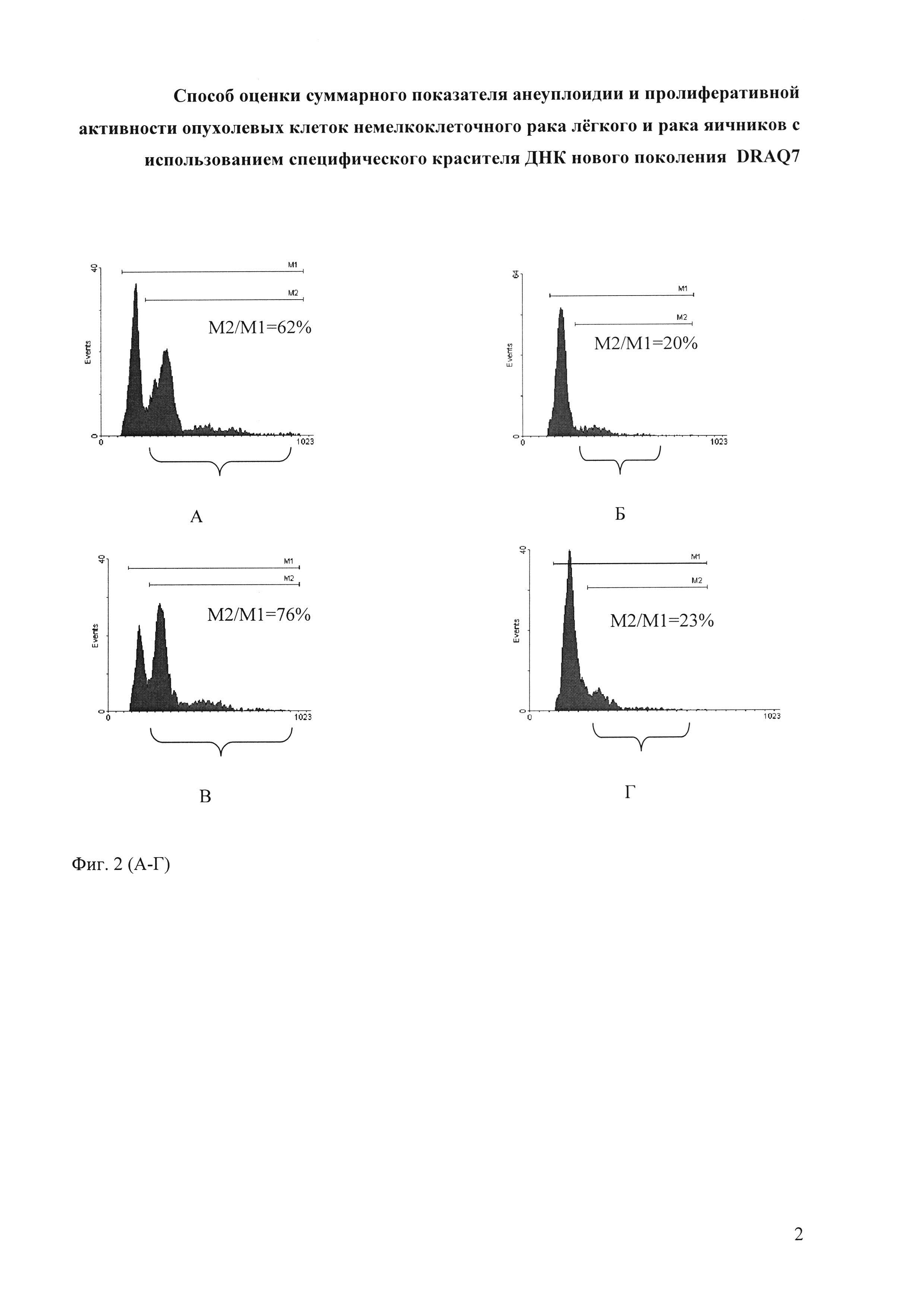
На фиг. 2 (А-Г) представлены гистограммы распределения интенсивности окрашивания ДНК. На фиг. 2 (А-Г) по оси абсцисс - интенсивность окрашивания ДНК, по оси ординат - количество клеток. Фигурной скобкой выделены клетки, составляющие интегральный показатель анеуплоидных клеток и клеток в М, S и G2 фазах цикла независимо от плоидности. На фиг. 2 (А-Б) - пример оценки интегрального показателя в немелкоклеточном раке легкого, на фиг. 2 (В-Г) - в раке яичников. Маркер M1 - общее количество клеток, М2 количество клеток, составляющих интегральный показатель, который рассчитывается путем деления М2 на M1. На фиг. 2 (А) интегральный показатель I=62%; на фиг. 2 (Б) интегральный показатель I=20%; на фиг. 2 (В) интегральный показатель I=76%; на фиг. 2 (Г) интегральный показатель I=23%.
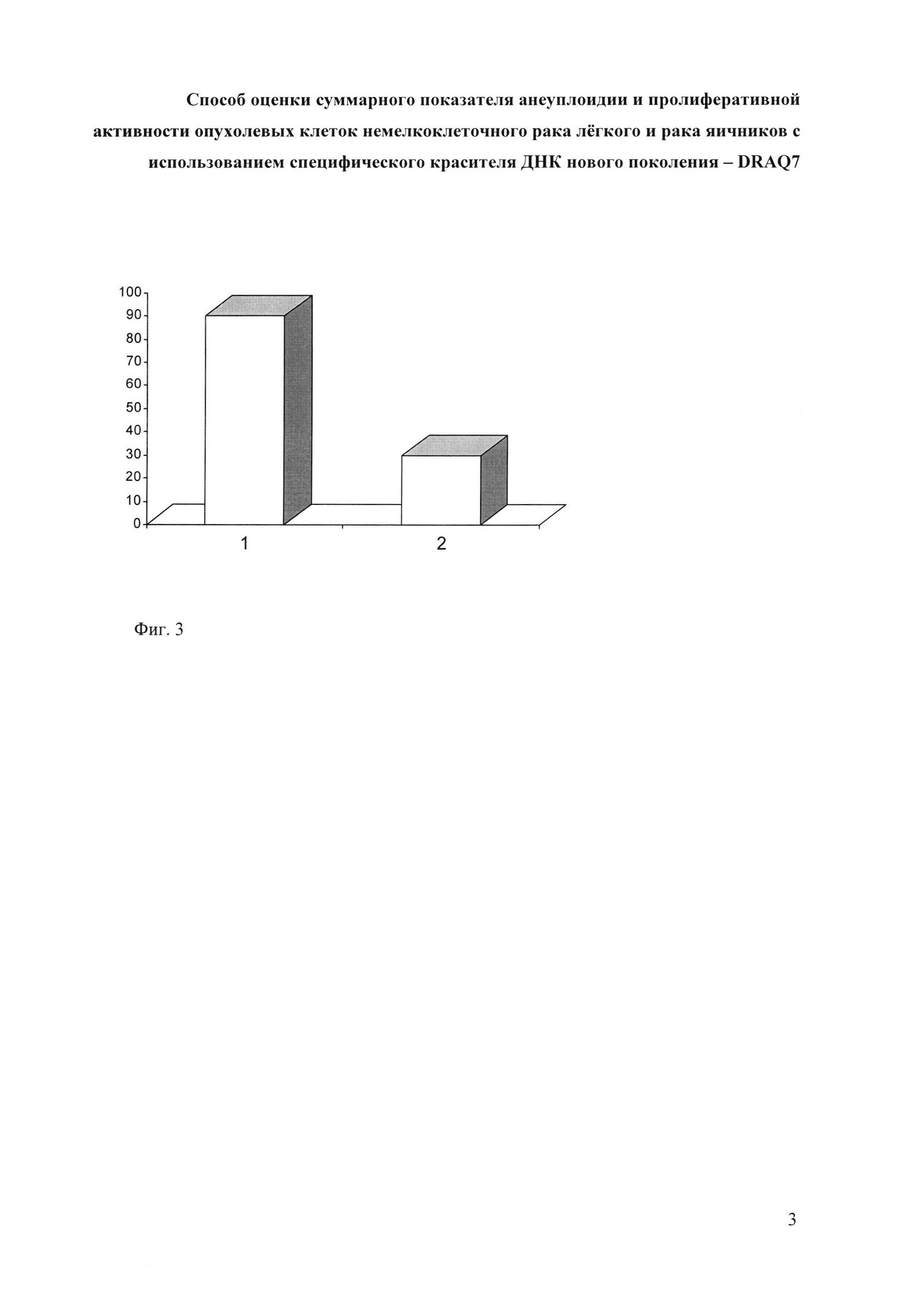
На фиг. 3 представлена частота встречаемости низкого значения интегрального показателя анеуплоидии и пролиферативной активности опухоли (значение показателя менее 30%) в чувствительных (1) и резистентных (2) к терапии, включающей карбоплатин и паклитаксел, случаев серозной аденокарциномы рака яичников. На фиг. 3 по оси абсцисс - группы больных раком яичников чувствительных (1) n=30 и резистентных (2) n=30 к терапии, включающей карбоплатин и паклитаксел, по оси ординат - частота встречаемости низкого (значение показателя менее 30%) значения интегрального показателя анеуплоидии и пролиферативной активности опухоли. Показано, что в группе чувствительных опухолей процент низких значений интегрального показателя значительно превышает значение этого параметра в группе резистентных опухолей (90,0% и 30,0% соответственно, р=0,01).
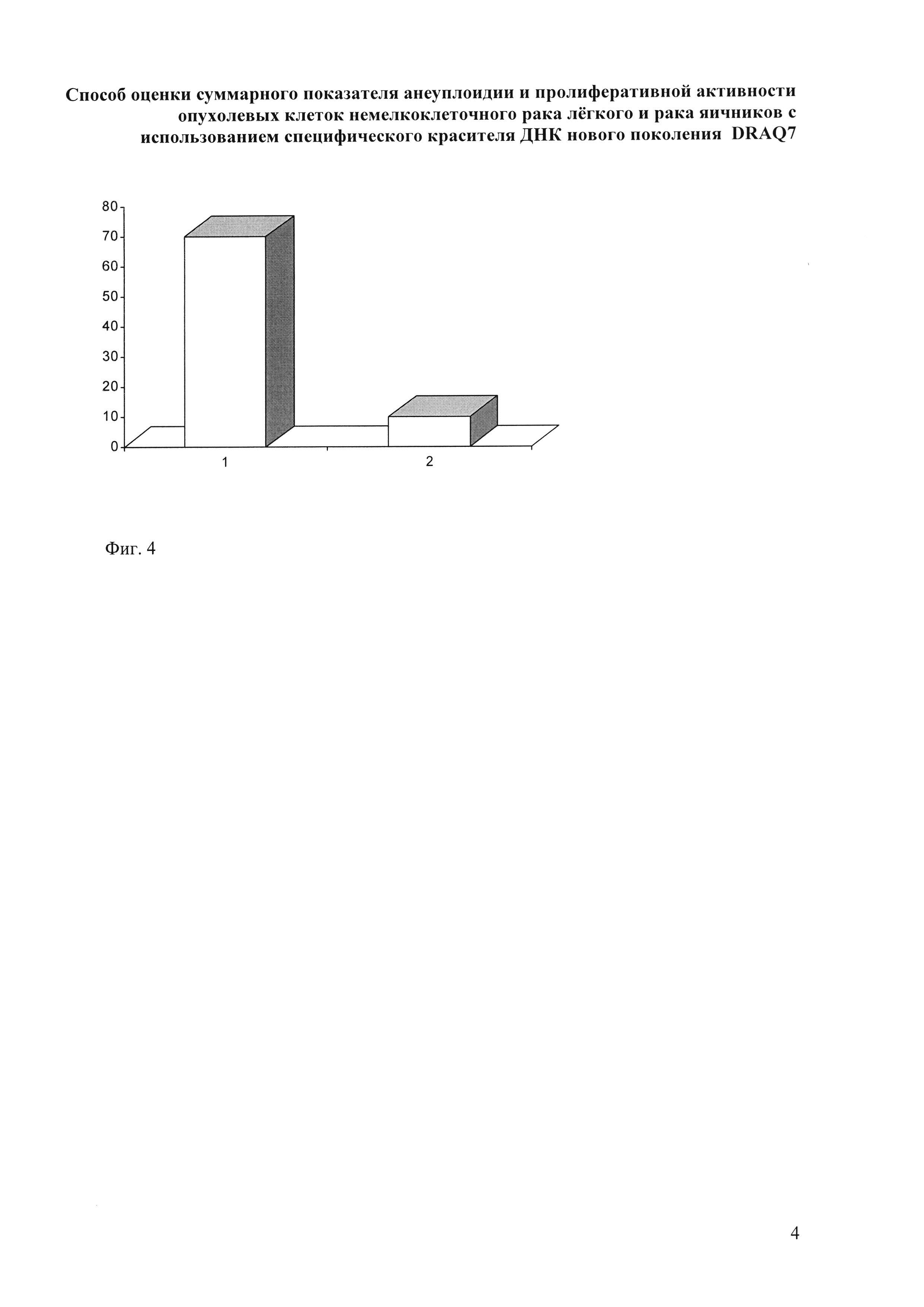
На фиг. 4 представлена частота встречаемости низкого значения интегрального показателя анеуплоидии и пролиферативной активности опухоли (значение показателя менее 30%) в различных по прогнозу типах немелкоклеточного рака легкого - аденокарциноме и плоскоклеточном раке. На фиг. 4 по оси абсцисс - гистологические типы рака легкого: аденокарцинома (1) n=30 и плоскоклеточный рак (2) n=30; по оси ординат - процент встречаемости низкого (значение показателя менее 30%) значения интегрального показателя анеуплоидии и пролиферативной активности опухоли. Показано, что низкие значения интегрального показателя значительно чаще встречаются в аденокарциноме (70,0%) по сравнению с плоскоклеточным раком легкого (10,0%) с достоверностью р=0,02.