Результат интеллектуальной деятельности: СПОСОБ ПОДГОТОВКИ КРИОКОНСЕРВИРОВАННЫХ ТРОМБОЦИТОВ ДЛЯ ТРАНСФУЗИИ
Вид РИД
Изобретение
Область, к которой относится изобретение
Изобретение относится к области медицины, а именно производственной и клинической трансфузиологии, и может быть использовано для заготовки тромбоцитов длительного хранения (до 24 месяцев), пригодных к трансфузии.
Уровень техники
Известен способ подготовки криоконсервировнных тромбоцитов для трансфузии, описанный в технологии криоконсервирования тромбоцитов в присутствии 10% ДМСО, предусматривающий отмывание тромбоцитов от ДМСО и разведение плазмой тромбоцитов после размораживания [Khuri S.F., Healey N., MacGregor H. et al. Comparison of the effects of transfusions of cryopreserved and liquid-preserved platelets on hemostasis and blood loss after cardiopulmonary bypass J Thorac Cardiovasc Surg 1999; 117: 172-84]. Однако данный способ не предусматривает оценку концентрации ДМСО в замороженных тромбоцитах, что часто приводит к значительному увеличению содержания в концентрате размороженных тромбоцитов активированных клеток.
Наиболее близким к заявляемому решению является способ подготовки криоконсервированных тромбоцитов для трансфузии, описанный в технологии криоконсервирования тромбоцитов с ДМСО и хранения клеток при -80°С [С. Robert Valery, Gina Rango, and Shukri Khuri Freezing human platelets with 6 percent dimethyl sulfoxide with removal of the supernatant solution before freezing and storage at -80°C without postthaw processing II Transfusion 2005; 45: 1890-1898]. Размораживание тромбоцитов проводится в водяной бане (Thermogenesis), при температуре 36°С в течение 5 минут. Размороженную суспензию тромбоцитов разводят 10-20 мл 0,9% раствора NaCl с целью уменьшения общей концентрации клеток, увеличения объема ТК, а также для уменьшения концентрации ДМСО в дозе размороженных тромбоцитов. Проверку качества тромбоцитов после размораживания криоконсервированных тромбоцитов (КТ) проводят по следующим параметрам: количество тромбоцитов (109/мл); рН, величину R-периода на тромбоэластограмме, агрегационную активность тромбоцитов (индукторы - 50 мкг/мл арахидоновой кислоты и 2 мкМ/л АДФ); продукцию тромбоксана В2 после стимуляции 50 мкг/мл арахидоновой кислоты и 2 мкМ/л АДФ; содержание аннексин-положительных тромбоцитов. Трансфузию размороженных КТ проводят через фильтр диаметром 170 микрон.
Однако данный способ подготовки КТ для трансфузии не предусматривает определение концентрации ДМСО в размороженном ТК; использует параметры агрегометрии, тромбоэластографии и проточной цитометрии, которые не отражают структурную целостность тромбоцитов, что не позволяет оценить сохранность (в %) биологически полноценных клеток в КТ после размораживания, что не позволяет произвести адекватный расчет требуемого количества тромбоцитов для конкретного пациента; для разведения размороженных тромбоцитов используется 0,9% раствор NaCl, не обладающий буферными свойствами, что приводит к закислению среды (рН=6.5-6.6) и повышает риск повреждения тромбоцитов; разведение размороженных ТК 0,9% раствором NaCl снижает конечную концентрацию ДМСО в ТК только до 3%, что является недостаточным для достижения концентрации, нетоксичной для тромбоцитов человека (0,5%); размороженная доза ТК обладает очень высокой осмолярностью (800-860 мОсмоль/л при физиологической норме 300-380 мОсмоль/л) и повышает риск развития у пациентов посттрансфузионных реакций.
Раскрытие изобретения
Задачей изобретения является разработка способа подготовки КТ для трансфузии, обеспечивающего получение безопасного гемокомпонента с высоким содержанием биологически полноценных тромбоцитов и его хранение при температуре 20-24°С в течение 4 часов без угрозы потери структурной или функциональной полноценности тромбоцитов.
Техническим результатом, на достижение которого направлено заявленное изобретение, является повышение качества получаемых после размораживания криоконсервированных тромбоцитов за счет комплекса используемых технологических операций, параметров и режимов, позволяющих сохранить гораздо большее число биологически полноценных тромбоцитов (в 1,5-1,8 раза по сравнению с технологией по прототипу), хранить размороженные ТК при комнатной температуре в течение 4 часов без угрозы потери структурной или функциональной полноценности тромбоцитов, получить осмолярность дозы ТК, соответствующей физиологической норме, не вызывающей развития у пациентов посттрансфузионных реакций.
Поставленная задача решается тем, что способ подготовки криоконсервированных тромбоцитов для трансфузии включает следующие этапы:
- размораживание контейнеров, содержащих замороженные тромбоциты, нагреванием при температуре от 37 до 40°С в течение от 2 до 4 минут;
- определение концентрации ДМСО в размороженных криоконсервированных тромбоцитах;
- определение объема плазмы или ресуспендирующего раствора, необходимого для введения в размороженные криоконсервированные тромбоциты для получения конечной концентрации ДМСО не более 0,5%, с последующим ресуспендированием размороженных тромбоцитов данным объемом плазмы, совместимой по системе АВО, или ресуспендирующим раствором при постоянном перемешивании в течение 8-12 минут со скоростью подачи плазмы или раствора 1-3 мл в минуту;
- хранение размороженных тромбоцитов до трансфузии не более 4 часов при температуре от 20 до 24°С и постоянном перемешивании.
Концентрацию ДМСО, как правило, определяют в аликвоте размороженных криоконсервированных тромбоцитов методом газовой хроматографии. Для этого может быть использован газовый хроматограф Shimadzu GC-17A (Япония) с пламенно-ионизационным детектором и автосамплером.
В качестве ресуспендирующего раствора могут быть использованы SSP, SSP+. В зависимости от концентрации ДМСО в криоконсервированные тромбоциты вводят плазму или ресуспендирующий раствор в соотношении от 1:9 до 1:19.
Перед ресуспендированием размороженные тромбоциты из контейнера, в котором они хранились в замороженном состоянии, переводят в аэрируемый контейнер из ПВХ с фталатным пластификатором, например контейнер для получения, транспортировки и хранения тромбоцитов: 994CF-E № ФСЗ 2011/09569, 2011-04-18 от Дельрус (Россия); производитель: Haemonetics Corporation (США).
После размораживания тромбоцитов оценивают их качество по следующим параметрам: объем от 180 до 220 мл, сохранность тромбоцитов не менее 75% от исходного (определенного перед замораживанием), сохранность тромбоцитов с гранулами и тромбоцитов с адгезивной активностью не менее 50% от исходного. Перед трансфузией конкретному пациенту производят расчет дозы размороженных тромбоцитов исходя из его антропометрических характеристик по следующей формуле: (2×1011 тромбоцитов на 1 м2 поверхности тела пациента или 0,7×1011 тромбоцитов на 10 кг веса пациента).
При этом после размораживания измеряют следующие параметры тромбоцитов: количество тромбоцитов, количество тромбоцитов с гранулами и количество адгезивно активных тромбоцитов. Данную информацию наносят на контейнер для последующего выбора контейнера с необходимыми параметрами для трансфузии конкретному пациенту в зависимости от его антропометрических характеристик.
Таким образом, поставленная задача решается за счет внедрения в процедуру метода количественного определения ДМСО в размороженных КТ; режимов размораживания и ресуспендирования КТ плазмой до концентрации тромбоцитов от 1,0×109/мл до 1,5×109/мл и снижения концентрации ДМСО до значения менее 0,5%, использования методов анализа структурной целостности и функциональной активности тромбоцитов и оценки сохранности биологически полноценных тромбоцитов после размораживания КТ.
Определение количества ДМСО в размороженных КТ необходимо для расчета объема плазмы, используемой для ресуспендирования тромбоцитов, для снижения концентрации ДМСО до 0,5% и ниже. Количество ДМСО определяется газохроматографическим методом. На этапе пробоподготовки 100 мкл тромбоцитарной массы ресуспендируют 900 мкл метанола и 50 мкл 0,02% метанольного внутреннего стандарта диметилформамида, перемешивают на орбитальном шейкере 10 минут с частотой 120 об/мин. Центрифугируют при 3000 об/мин в течение 10 минут, декантируют надосадочную жидкость и помещают в виалу для проведения исследования на газовом хроматографе Agilent 6850 с пламенно-ионизационным детектором, испарителем для режимов работы со сбросом/без сброса и автоматическим дозатором. Колонка - HP-FFAP, 25 метров, диаметр - 0,32 мм, толщина фазы - 0,5 нм. Температура испарителя - 200°С, режим работы с постоянным давлением - 45 кПa, 1 мкл образца вводится с сбросом 1/15. Температурный режим печи - 70°С начальная температура, плато 3 мин, подъем температуры со скоростью 15°С/мин до 180°С, плато 10 мин. Температура детектора - 280°С, поток водорода - 40 мл/мин, поток воздуха - 300 мл/мин. Время удерживания диметилсульфоксида составляет 11,05 мин, диметилформамида - 8,12 мин.
Для оценки качества клеток в ТК на разных этапах криоконсервирования может быть использован разработанный ранее способ оценки морфофункционального статуса тромбоцитов человека [Патент РФ на изобретение №2485502 «Способ оценки морфофункционального статуса тромбоцитов человека», авторы Хубутия М.Ш., Макаров М.С., Хватов В.Б., Высочин И.В., Кобзева Е.Н., Боровкова Н.В., Конюшко О.И., 20.06.2013], основанный на витальном (прижизненном) окрашивании тромбоцитов флуорохромным красителем на основе трипафлавина и акридинового оранжевого с последующим их анализом во флуоресцентном микроскопе. Данный метод позволяет параллельно оценить структурную целостность и функциональную активность тромбоцитов независимо от их концентрации в пробе, в том числе - в бесплазменной среде. Таким образом, используя данный метод, появляется возможность оценить общее содержание биологически полноценных тромбоцитов в исследуемом ТК (109/мл), а также оценить сохранность таких клеток после разных процедур криоконсервирования. Проведенные исследования показывают, что биологически полноценными (с нормальной структурой и функциями) являются лишь те тромбоциты, в которых при витальном окрашивании отчетливо выявляются гранулы - не менее 3 гранул диаметром более 300 мкм на клетку во флуоресцентном микроскопе, яркость свечения клетки - не менее 40 фут-кандел (Макаров М.С., Кобзева Е.Н., Высочин И.В., Боровкова Н.В., Хватов В.Б. Морфофункциональный анализ тромбоцитов человека с помощью витального окрашивания // Бюллетень экспериментальной биологии и медицины. - 2013. - №9. - С. 388-391). Следовательно, оценка содержания тромбоцитов с гранулами может быть использована для контроля качества клеток ТК до и после криоконсервирования.
При экспозиции богатой тромбоцитами плазмы (БоТП) с ДМСО в конечной концентрации от 0,5 до 20% при комнатной температуре было установлено, что в процессе контакта с ДМСО биологическая полноценность клеток БоТП снижается, параллельно с этим уменьшается содержание тромбоцитов с гранулами (табл. 1). Так, при 0,5% ДМСО содержание тромбоцитов с гранулами в БоТП практически не менялось в течение 2 часов при комнатной температуре, через 4 часа снижалось на 7-10%, через 20 часов - на 70%. При концентрации ДМСО от 1 до 20% динамика снижения числа тромбоцитов с гранулами была сходной в течение первых двух часов: через 1 час потеря тромбоцитов с гранулами составила 10-20%, через 2 часа - 40-50%, через 4 часа - от 60 до 80%, через 20 часов тромбоциты с гранулами в БоТП полностью отсутствовали. Еще более выраженной динамика снижения тромбоцитов с гранулами была при 10-20% ДМСО: через 2 часа потеря тромбоцитов с гранулами составила 55-65%, через 4 часа - 90-99%. Стоит особо отметить, что при концентрации ДМСО 5% и выше адгезивная активность тромбоцитов с гранулами падает гораздо быстрее, чем их содержание. Этот эффект становится выражен уже при концентрации ДМСО 2% и выше. При использовании 5% ДМСО после 30 мин экспозиции адгезивная активность тромбоцитов снижалась в среднем 2 раза (табл. 2). Таким образом, уже через 30 мин экспозиции БоТП с 5% ДМСО при комнатной температуре в среднем 50% тромбоцитов с гранулами не проявляли функциональной активности. Это указывает на то, что время контакта тромбоцитов с 5% ДМСО при комнатной температуре должно быть минимизировано. С другой стороны, при концентрации 0,3-0,5% ДМСО биологическая полноценность тромбоцитов практически не нарушается в течение нескольких часов. Следовательно, разведение размороженных ДМСО-содержащих ТК до концентрации 0,3-0,5% ДМСО позволит сохранить их структурную и функциональную полноценность в течение 4-6 часов после разморозки.


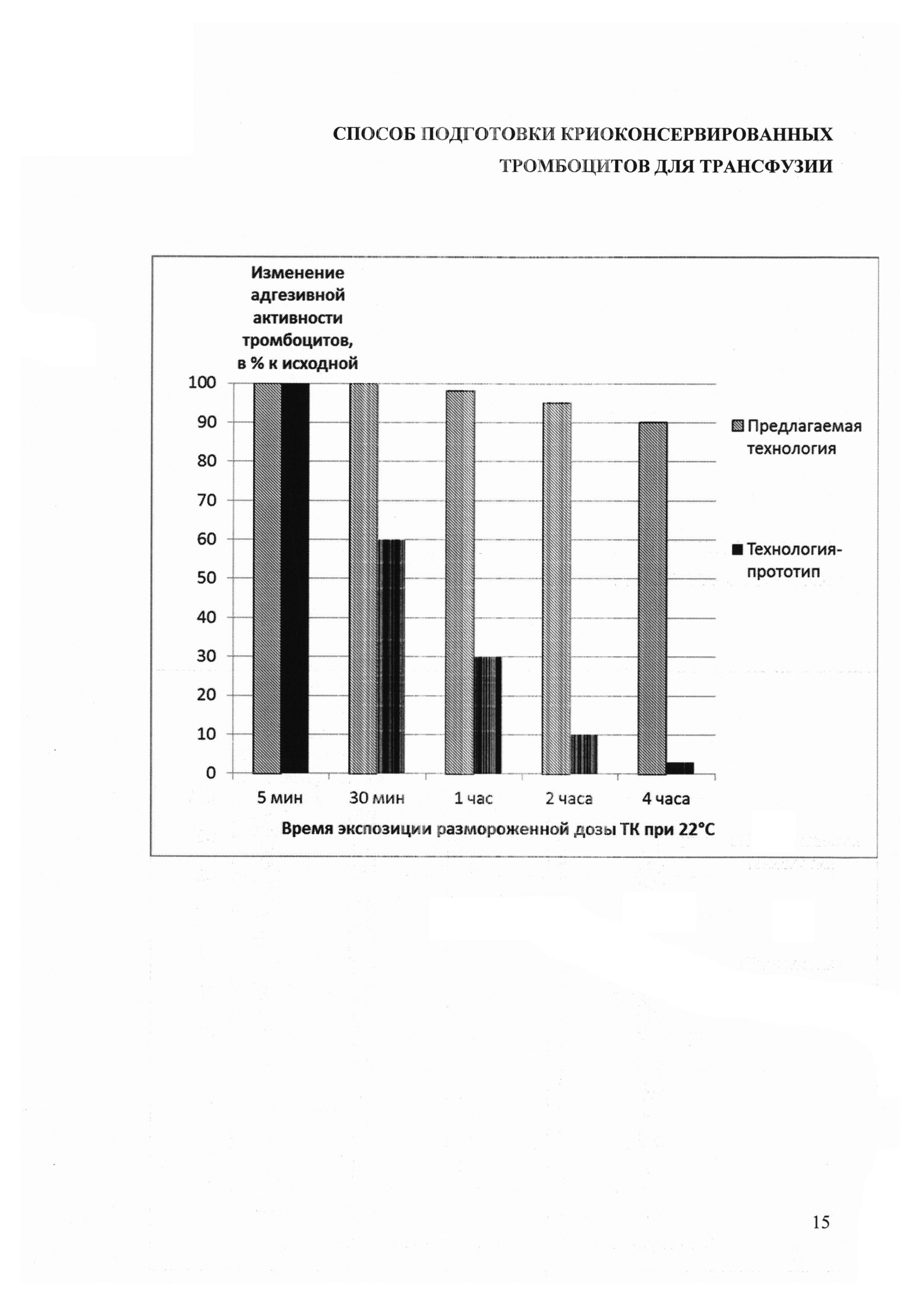
Результаты сравнения качества тромбоцитов в размороженных КТ, полученных с помощью технологии-прототипа и с помощью заявляемого способа, представлены в Таблице 3. Для оценки эффективности криоконсервирования решено было определять сохранность тромбоцитов с гранулами и сохранность их адгезивной активности. Было установлено, что заявляемый способ позволяет сохранить гораздо большее число биологически полноценных тромбоцитов (в 1,5-1,8 раза), чем технология-прототип. Размороженные КТ разводили плазмой. Объем размороженной плазмы составлял 90-100 мл, что позволяло развести КТ в 10 раз, снижая концентрацию ДМСО в ней до 0,4-0,6%. В то же время в прототипе концентрация ДМСО составляет 2,5-3%, осмолярность - более 800 мОсмоль/л, что является токсичным для тромбоцитов человека, при этом для дилюции КТ используется 0,9% раствор хлорида натрия, не обладающий буферными свойствами и не препятствующий закислению среды. В результате хранение размороженных ТК, полученных по технологии-прототипу, сопровождается выраженным снижением структурной и функциональной полноценности тромбоцитов. Так, через 1 час хранения в размороженных КТ адгезивная активность клеток снижается на 70%, через 2 часа - на 90%, через 4 часа - на 95-98% (рис. 1). Это указывает на неэффективность хранения ТК (в прототипе) при температуре от 20 до 24°С. Напротив, при разведении КТ плазмой (предлагаемая технология) адгезивная активность тромбоцитов снижается через 4 часа лишь на 10% (рис. 1). Таким образом, появляется возможность хранения размороженных КТ при комнатной температуре в течение 4 часов без угрозы потери структурной или функциональной полноценности тромбоцитов. Осмолярность полученной дозы КТ составляет 360-380 мОсмоль/л, что соответствует физиологической норме и не вызывает развития у пациентов посттрансфузионных реакций.

Краткое описание чертежей
Изобретение поясняется чертежами, где на фиг. 1 изображена динамика изменения адгезивной активности тромбоцитов в размороженных ТК, приготовленных с использованием технологии-прототипа и предложенной нами технологии.
Осуществление изобретения
Процесс подготовки криоконсервированных тромбоцитов для трансфузии включает следующие этапы:
1. Определение концентрации ДМСО.
Концентрацию ДМСО в криоконсервированных тромбоцитах определяют методом газовой хроматографии. Для хроматографирования применяют капиллярную колонку НР-FFAP фирмы Agilent Technologies (США) с полярной фазой (100% полиэтиленгликоль). Аликвоту криоконсервированных тромбоцитов в количестве 100 мл разводят 900 мкл метанола и 50 мкл метанольного раствора диметилформамида. Полученную смесь центрифугируют при 3000 об/мин в течение 10 минут. Надосадок декантируют и переносят в количестве 1 мкл в хроматограф. Количественный анализ проводили по методу внутреннего стандарта, в качестве которого использовали диметилформамид. Для построения калибровочного графика зависимости площади пика ДМСО от его концентрации готовят контрольные смеси ТК с ДМСО в конечной концентрации последнего: 1,51; 3,02; 6,05; 30,25; 60,5 и 121 мкг/мл. Калибровочный график, составляемый по результатам анализа контрольных смесей, представляет собой прямую линию во всем диапазоне используемых концентраций. Концентрацию ДМСО в криоконсервированных тромбоцитах пересчитывают в % с учетом объема замороженных тромбоцитов и далее учитывают при расчете объема раствора для ресуспендирования тромбоцитов.
2. Размораживание тромбоцитов.
Замороженные тромбоциты, нагревают в программном размораживателе плазмы (например, Barkey Plasmatherm) при температуре от 37 до 40°С в течение от 2 до 4 минут.
3. Ресуспендирование размороженных тромбоцитов.
Плазму или разводящий раствор SAGM добавляют к размороженным тромбоцитам в соотношении от 1:9 до 1:19 при постоянном перемешивании в течение 10 минут. Объем разводящего раствора или плазмы зависит от концентрации ДМСО в исходных криоконсервированных тромбоцитах и рассчитывается для достижения конечной концентрации ДМСО в размороженных тромбоцитах не более 0,5%.
4. Хранение размороженных тромбоцитов.
Хранят размороженные тромбоциты при температуре от 20 до 24°С и постоянном перемешивании не более 4 часов до трансфузии.
Пример 1.
Для приготовления КТ к трансфузии использовали две равные части замороженного гемокомпонента: КТ №1 (прототип) и КТ №2 (разработка). Параметры качества криоконсервированных тромбоцитов представлены в таблице 4.

Анализ результатов размороженных КТ показал, что предложенная технология криоконсервирования тромбоцитов по сравнению с прототипом обеспечивает значимо большую сохранность жизнеспособных клеток в размороженных ТК. Так, через 10 минут после размораживания криоконсервированных по предложенной технологии тромбоцитов содержание жизнеспособных клеток было больше, чем в прототипе в 2,5-3 раза, через 4 часа хранения при комнатной температуре - в 40 раз.
Пример 2.
Больной А, 65 лет
Диагноз: Расслаивающаяся аневризма грудного отдела аорты 2 типа.
Операция с использованием аппарата искусственного кровообращения (АИК) - протезирование грудного отдела аорты.
Состояние больного после операции. Кровопотеря за две операции - 2300 мл. После операции в течение первых суток сохраняется геморрагическое отделяемое по дренажам. Тромбоцитопения (концентрация тромбоцитов в крови больного) 59×109. Лейкопения (концентрация лейкоцитов в крови 3,5 тыс./мкл), анемия (гемоглобин 71 г/л и гематокрит 19,5%). Доля тромбоцитов с гранулами - 5%, адгезивная активность тромбоцитов - 3%, что говорит о выраженной тромбоцитопении и высоком риске кровотечения.
Тактика лечения. С учетом наличия у больного тромбоцитопении и выраженного геморрагического синдрома, развившихся после интраоперационной массивной кровопотери, для коррекции клеточного звена гемостаза проведена лечебная трансфузия тромбоцитного концентрата, размороженного после 9 месяцев криохранения и карантинизации.
Характеристика КТ. Общий объем - 200 мл, общее количество тромбоцитов - 2,4×1011, содержание тромбоцитов с гранулами - 0,84×1011, адгезивная активность тромбоцитов - 0,72×1011. Трансфузия - лечебная с учетом группы крови и фенотипа О (I) положительный.
Эффективность трансфузии.
После переливания ТК геморрагический синдром купирован. В крови больного концентрация тромбоцитов повысилась до 77×109/л через 1 час, и до 102×109/л через 24 часа после переливания ТК. Скорректированный прирост тромбоцитов составил через 1 час 16; через 24 часа - 38×109/л, что говорит о высокой эффективности трансфузии ТК. Больной экстубирован, моча светлая, геморрагический синдром купирован.