Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ КУЛЬТУРЫ МЕЗЕНХИМНЫХ СТВОЛОВЫХ КЛЕТОК ЧЕЛОВЕКА ИЗ ПЕРИВАСКУЛЯРНОГО ПРОСТРАНСТВА ВЕНЫ ПУПОЧНОГО КАНАТИКА
Вид РИД
Изобретение
Изобретение относится к области клеточной биологии и биотехнологии, а именно к клеточным технологиям, в частности к способам получения мезенхимных стволовых клеток человека, применяемых в регенеративной терапии.
Мезенхимные стромальные (стволовые) клетки (МСК) - это мультипотентные клетки, происходящие из мезодермального зародышевого листка, обладающие способностью к самоподдержанию популяции и дифференцировке в клетки мезенхимного ряда: хондроциты, остеоциты, адипоциты. Существуют методы дифференцировки МСК в клетки, которые в организме формируются из других зародышевых листков: эпителиоциты, нейроноподобные клетки. МСК оказывают иммуномодулирующие действие, выделяют ангиогенные факторы, а также способны к миграции к месту повреждения. Кроме того, МСК способны дифференцироваться в клетки поврежденных тканей, способствуя, таким образом, восстановлению функциональной целостности органа или ткани. Подобные свойства позволяют рассматривать МСК как перспективный инструмент регенеративной терапии, основанной на клеточных технологиях.
Пуповина, в частности Вартонов студень и периваскулярное пространство сосудов, а также пуповинная кровь и плацента, обычно утилизируемые после родов, представляют собой удобные источники получения МСК, поскольку в них содержится большое количество МСК в пересчете на 1 грамм ткани, и количество получаемой ткани велико по сравнению с остальными источниками. Кроме этого, клетки из этих источников обладают более высоким пролиферативным потенциалом по сравнению с МСК жировой ткани и костного мозга взрослого человека, что позволяет сократить время экспансии, то есть наращивания клеток без утраты дифференцировочного потенциала в условиях in vitro. Подобная экспансия необходима в большинстве случаев, т.к. для большинства терапевтических и хирургических процедур с использованием МСК ни один источник получения МСК не позволяет получить клетки в количестве, достаточном для взрослого пациента, то есть 20-80 млн в зависимости от массы тела пациента и проводимой процедуры.
В пуповине обнаружено пять зон, из которых возможно выделить МСК:
1. 20-50% свежевыделенной мононуклеарной фракции пуповинной крови;
2. субэндотелиальный слой пупочной вены;
3. внешние слои (периваскулярное пространство) пуповинных сосудов;
4. интраваскулярное пространство;
5. субамниотическое пространство.
МСК, выделенные из разных зон пупочного канатика, являются отдельными популяциями с одинаковым иммунофенотипом, но различной пролиферативной активностью и дифференцировочной способностью, обзор этих данных сделан в статье: Conconi М.Т., Di Liddo R., Tommasini M., Calore C., Parnigotto P.P. Phenotype and differentiation potential of stromal populations obtained from various zones of human umbilical cord: an overview // The Open Tissue Eng Regen Med J. - 2011. - V. 4. - P. 6-20. МСК периваскулярного пространства характеризуются высокой скоростью роста популяции in vitro и высоким уровнем экспрессии панцитокератина и CD146 [Carvalho М., Teixeira F.G., Reis R.L., Sousa N., Salgado AJ. Mesenchymal stem cells in the umbilical cord: phenotypic characterization, secretome and applications in central nervous system regenerative medicine // Current stem cell research & therapy. - 2011. - V. 6. - №. 3. - P. 221-228]. Кроме того, МСК из этих двух регионов отличаются по уровню продукции IL-6 и Flt3 [Xu М., Zhang В., Liu Y., Zhang J., Sheng H., Shi R., Chen H. The immunologic and hematopoietic profiles of mesenchymal stem cells derived from different sections of human umbilical cord // Acta biochimica et biophysica Sinica. - 2014. - C. 100].
В статье: Ennis J., Sarugaser R., Gomez A., Baksh D., Davies J.E. Isolation, characterization, and differentiation of human umbilical cord perivascular cells (HUCPVCs) // Methods in cell biology. - 2008. - V. 86. - P. 121-136 показана возможность получения МСК из периваскулярного пространства пупочной вены.
Известен способ получения культуры МСК из периваскулярного пространства пупочного канатика, описанный в: Sarugaser R., Lickorish D., Baksh D., Hosseini M.M., Davies J.E. Human umbilical cord perivascular (HUCPV) cells: a source of mesenchymal progenitors // Stem Cells. - 2005. - V. 23. - №2. З. 220-229. Способ заключается в том, что сосуды - вену и обе артерии - пупочного канатика поочередно вырезают из Вартонова студня, сшивают концы каждого сосуда друг с другом, чтобы образовалась замкнутая петля, и инкубируют в 0,1% растворе коллагеназы в течение 18-24 часов. Затем петли вынимают, раствор центрифугируют, осадок несколько раз промывают и культивируют стандартным способом. Вышеописанный способ очень трудоемкий, включает в себя сложные процедуры препарирования сосудов из Вартонова студня и длительную 24-часовую ферментативную обработку. Это делает вышеописанный способ непригодным для применения в терапевтических целях для большого количества пациентов, особенно при необходимости быстрого получения МСК. Жизнеспособность выделенных клеток низка в результате длительной 24-часовой ферментативной обработки.
В статье: Айзенштадт А.А., Иванова Н.А., Багаева В.В., Смолянинов А.Б., Самойлович М.П., Климович В.Б. Внутриклеточные иммуноглобулины в линиях Namalva и U266 при сокультивировании с мезенхимными клетками // Цитология - 2014. - Т. 56. - №2. - С. 117-121 описан способ получения МСК из периваскулярного пространства пупочного канатика, позволяющий сократить время обработки пупочного канатика с 16-26 ч до 1,5 ч. Этот способ заключается в том, что в пупочную вену цельного неизмельченного фрагмента канатика (10-30 см) вводят 0,2% раствор коллагеназы IV типа, закрывают с обоих концов клеммами и выдерживают в течение 60 мин при температуре 37°С. После инкубации, пупочную вену промывают фосфатно-солевым буфером и полученную при промывке жидкость центрифугируют. Осадок переносят в селективную среду и культивируют несколько пассажей в культуральных емкостях, приспособленных для культивирования адгезивных клеток.
Полученные клетки обладают иммунофенотипом МСК и способны дифференцироваться в остео-, хондро- и адипогенном направлении. Вышеописанный способ существенно сокращает время получения культуры МСК за счет исключения этапа препарирования сосудов пуповины и сокращения времени обработки коллагеназой. Однако недостатками метода являются: а) низкий выход клеток - 1 млн клеток на 10 см длины канатика после первого пассажа; б) загрязнение выделяемых МСК клетками других типов, в-основном, эндотелиоцитами; в) низкая сохранность МСК в результате длительного 1-часового инкубирования в растворе коллагеназы, а вследствие этого - их низкая пролиферативная активность; г) большое время эксплантации МСК в культуру (5 дней). Эти недостатки делают вышеописанный способ малопригодным для коммерческого использования. Данный способ является наиболее близким к заявляемому изобретению и выбран в качестве прототипа.
Задачей настоящего изобретения является создание способа получения культуры МСК из периваскулярного пространства пупочного канатика, обеспечивающего уменьшение времени получения культуры МСК, повышение выхода и сохранности получаемых клеток, повышение чистоты культуры МСК.
Поставленная задача решается тем, что в способе получения культуры МСК из периваскулярного пространства пупочного канатика вырезают фрагмент упомянутого пупочного канатика, заполняют вену упомянутого канатика раствором 0,2% коллагеназы, закрывают оба конца упомянутого пупочного канатика и выдерживают в течение по меньшей мере 20 минут, но не более 40 минут при температуре 37°С, после этого упомянутую вену промывают сбалансированным солевым раствором, вену заполняют новой порцией упомянутого раствора коллагеназы, закрывают оба конца упомянутого пупочного канатика и выдерживают в течение по меньшей мере 30 минут, но не более 60 минут при температуре 37°С, после этого упомянутую вену промывают сбалансированным солевым раствором, полученную при промывке жидкость центрифугируют. Полученный осадок культивируют известным способом с использованием селективных сред.
В отличие от прототипа в заявляемом способе получения культуры МСК проводят два цикла инкубации в растворе коллагеназы. После первого инкубирования пупочных канатиков в 0,2% растворе коллагеназы, которая заполняет только просвет пупочной вены, часть внеклеточного матрикса стенки пупочной вены разрушается. Таким образом, в растворе, собранном из пупочной вены, содержатся в основном клетки из зон 1-2. То есть кроме МСК в этой порции встречается значительное количество эндотелиоцитов, клеток крови, гематопоэтических стволовых клеток и т.д. После второй инкубации в получаемой фракции содержатся преимущественно клетки 3-4 зон, а мукополисахариды Вартонова студня (зона 5) чаще всего отсутствуют. В результате последующей промывки удаляются излишки коллагеназы, таким образом, большая часть клеток сохраняется от ее повреждающего воздействия. При осуществлении настоящего способа увеличивается доля МСК в препарате выделенных клеток, уменьшается общее время получения культуры клеток, увеличивается сохранность клеток и чистота клеточной культуры, увеличивается доля активно пролиферирующих МСК периваскулярного пространства и уменьшается доля медленнорастущих МСК Вартонова студня, вплоть до их полного отсутствия. МСК культуры, полученной при осуществлении настоящего способа, сохраняют свою жизнеспособность и пролиферативный потенциал.
При необходимости обе фракции после первой и второй обработки коллагеназами культивируют раздельно на селективных средах с использованием адгезивного пластика, а полученные культуры МСК объединяют для использования в целях регенеративной терапии.
Описанная в заявляемом способе последовательность операций обработки полученного фрагмента пупочного канатика, выбранные режимы и вещества, используемые при этом, обеспечивают решение поставленной задачи.
Изобретение иллюстрируется следующими графическими материалами.
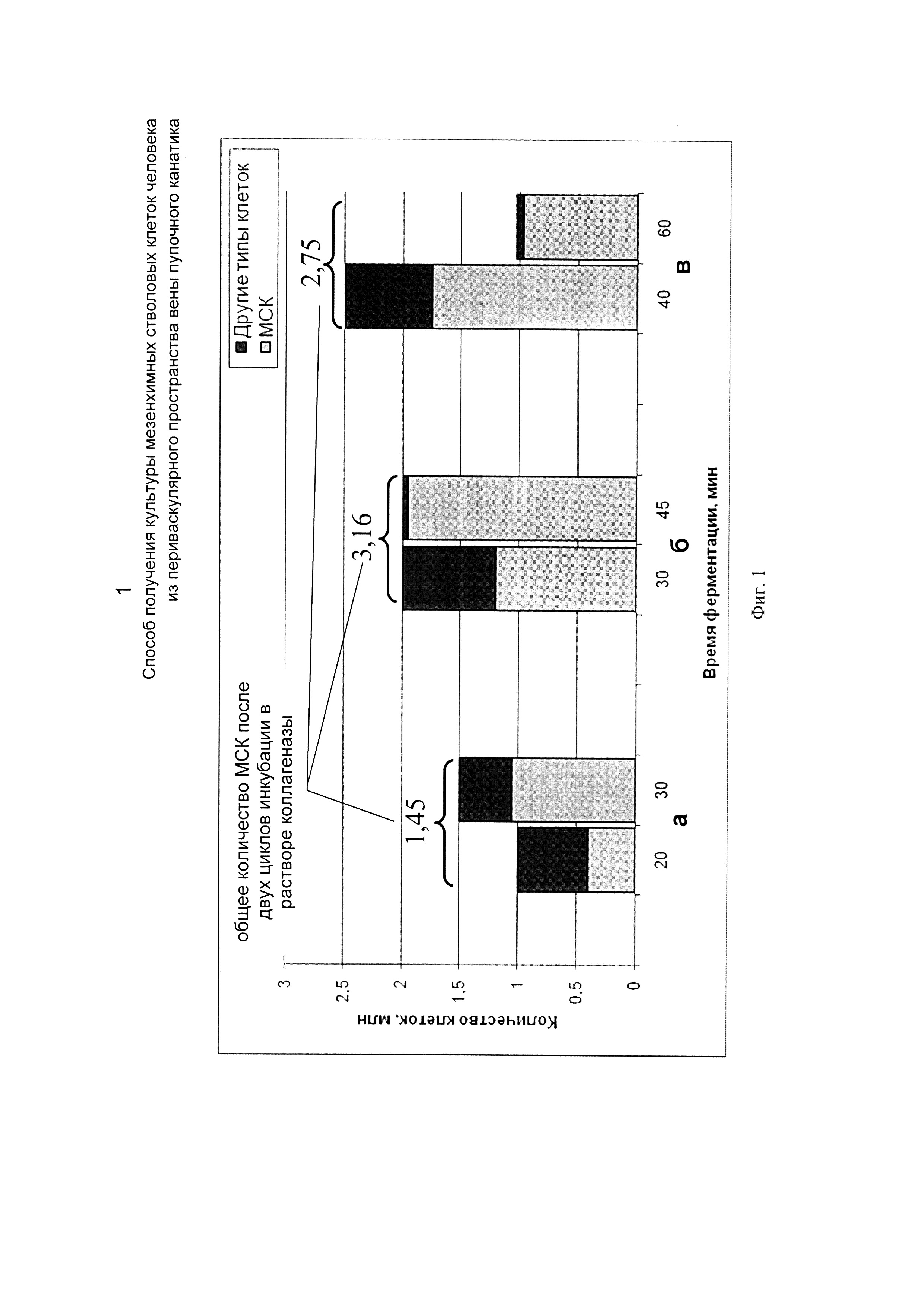
На Фиг. 1 представлено количество получаемых МСК и клеток других типов после первого пассажа в зависимости от длительности первого и второго выдерживания в 0,2% растворе коллагеназы.
На Фиг. 1а представлено количество МСК и клеток других типов, полученных способом, описанным в примере 1.
На Фиг. 1б представлено количество МСК и клеток других типов, полученных способом, описанным в примере 2.
На Фиг. 1в представлено количество МСК и клеток других типов, полученных способом, описанным в примере 3.
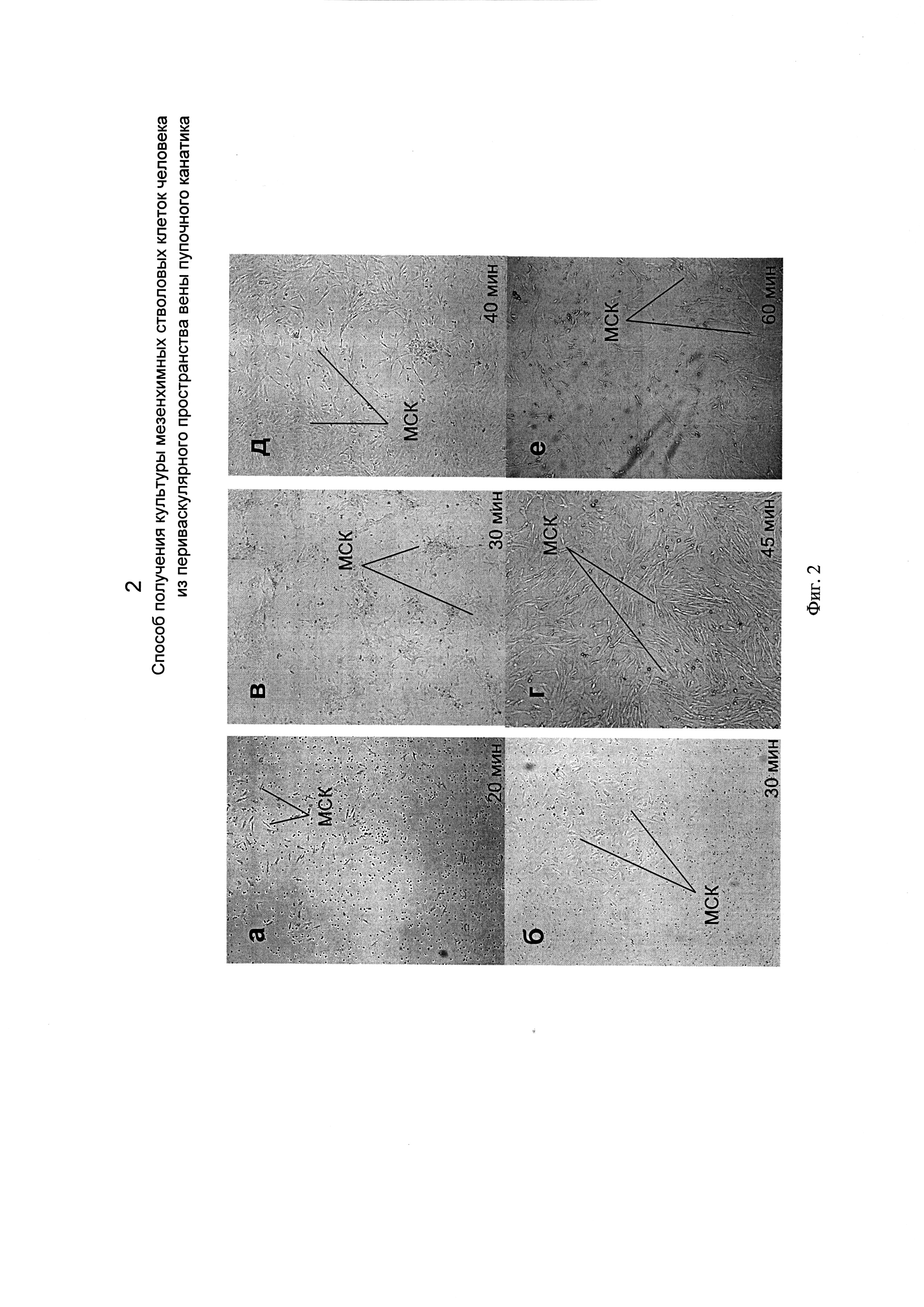
На Фиг. 2 представлены полученные с помощью микроскопа изображения культур клеток, полученных при различной длительности первого и второго выдерживания в 0,2% растворе коллагеназы.
На Фиг. 2а представлено полученное с помощью микроскопа изображение культуры клеток, полученной после первого выдерживания в 0,2% растворе коллагеназы в течение 20 минут, как описано в примере 1.
На Фиг. 2б представлено полученное с помощью микроскопа изображение культуры клеток, полученной после второго выдерживания в 0,2% растворе коллагеназы в течение 30 минут, как описано в примере 1.
На Фиг. 2в представлено полученное с помощью микроскопа изображение культуры клеток, полученной после первого выдерживания в 0,2% растворе коллагеназы в течение 30 минут, как описано в примере 2.
На Фиг. 2г представлено полученное с помощью микроскопа изображение культуры клеток, полученной после второго выдерживания в 0,2% растворе коллагеназы в течение 45 минут, как описано в примере 2.
На Фиг. 2д представлено полученное с помощью микроскопа изображение культуры клеток, полученной после первого выдерживания в 0,2% растворе коллагеназы в течение 40 минут, как описано в примере 3.
На Фиг. 2е представлено полученное с помощью микроскопа изображение культуры клеток, полученной после второго выдерживания в 0,2% растворе коллагеназы в течение 60 минут, как описано в примере 3.
Изображения получены с помощью микроскопа биологического для лабораторных исследований (микроскоп серии Axiovert 40 со штативом Axiovert 40 CFL) и фотокамеры для микроскопа (Progress СТ 3 Carl Zeiss, ФРГ).
Способ осуществляли следующим образом.
Пример 1. Полученный стандартным способом пупочный канатик помещали в сосуд, содержащий достаточное количество «гепариновой воды» (5 мл гепарина на 200 мл физиологического раствора), с добавлением антибиотика, после этого транспортировали его в лабораторию. Тщательно промывали пупочную вену сбалансированным солевым раствором, например раствором Версена, с помощью шприца. Затем промывали пупочную вену 0,2% раствором коллагеназы I и IV типа (1:1) в PBS с помощью шприца. Клеммировали пупочный канатик с одной стороны, затем наполняли пупочную вену вышеупомянутым раствором коллагеназы. Клеммировали пупочный канатик с противоположной стороны. Клеммированный образец помещали в чашку Петри и выдерживали в шейкере-инкубаторе, например, ES-20 (Biosan, Латвия), при температуре 37°С и слабом помешивании в течение 20 минут. После этого упомянутый раствор коллагеназы собирали и тщательно промывали пупочную вену сбалансированным солевым раствором, например раствором PBS. Раствор коллагеназы и солевой раствор после промывок собирали и центрифугировали, например, на центрифуге СМ-6М (Elmi, Латвия), 7 минут при 1100 об/мин. Удаляли супернатант, осадок помещали в культуральный флакон площадью 75 см2, в который предварительно было добавлено 10-15 мл полной культуральной среды, например, среды МЕМ-α/ Advanced Stem Cell Media (HyClone, Германия) с добавлением 20% фетальной коровьей сыворотки для МСК или заменителя сыворотки Advanced Supplement for Stem Cells (HyClone, Германия). Помещали флаконы в СО2-инкубатор, например, BBD 6220 (Thermo, Германия), для прикрепления фракции МСК к пластику, время экспозиции 3-5 суток в зависимости от состояния клеток. Полученную первую фракцию МСК использовали для сравнения. Вторично промывали пупочную вену упомянутым раствором коллагеназы с помощью шприца. Клеммировали пупочный канатик с одной стороны, затем наполняли пупочную вену упомянутым раствором коллагеназы. Клеммировали пупочный канатик с противоположной стороны. Клеммированный образец помещали в чашку Петри и выдерживали в упомянутом шейкере-инкубаторе при температуре 37°С и слабом помешивании в течение 30 минут. После выдерживания упомянутый раствор коллагеназы собирали и тщательно промывали пупочную вену упомянутым сбалансированным солевым раствором. Раствор коллагеназы и солевой раствор после промывок собирали и центрифугировали на упомянутой центрифуге 7 минут при 1100 об/мин. Удаляли супернатант, осадок помещали в культуральный флакон площадью 75 см2, в который предварительно было добавлено 10-15 мл полной упомянутой культуральной среды. Помещали флаконы в упомянутый СО2-инкубатор для прикрепления фракции МСК к пластику, время экспозиции 3-5 суток в зависимости от состояния клеток. Далее МСК культивировали известным способом культивирования МСК.
Пример 2. Получение культуры МСК проводили по схеме, приведенной в примере №1, отличающейся тем, что первое выдерживание в упомянутом растворе коллагеназы проводили в течение 30 минут, а второе выдерживание в упомянутом растворе коллагеназы проводили в течение 45 минут.
Пример 3. Получение культуры МСК проводили по схеме, приведенной в примере №1, отличающейся тем, что первое выдерживание в упомянутом растворе коллагеназы проводили в течение 40 минут, а второе выдерживание в упомянутом растворе коллагеназы проводили в течение 60 минут.
Заявитель просит рассмотреть представленные материалы заявки «Способ получения культуры мезенхимных стволовых клеток человека из периваскулярного пространства вены пупочного канатика» на предмет выдачи патента РФ на изобретение.