Результат интеллектуальной деятельности: Способ получения биологически активных веществ в клеточной культуре Conium maculatum L. (болиголова пятнистого)
Вид РИД
Изобретение
Изобретение относится к биотехнологии, в частности к культивированию клеточных культур лекарственных растений, и может быть использовано в фармацевтической промышленности при получении фуранокумаринов и ациклических тритерпеноидов из клеточной культуры болиголова пятнистого. Наряду с другими биологически активными веществами эти соединения входят в состав болиголова пятнистого. Фуранокумарины оказывают фотосенсибилизирующее (Кузнецова Г.А. Природные кумарины и фурокумарины / Г.А. Кузнецова. - Л.: Наука, 1967. - 248 с.), сосудорасширяющее, бактериостатическое и антигрибковое действие. Так же они обладают противосвертывающей, противоопухолевой активностью, гипогликемизирующим свойством (снижают уровень сахара в крови) (Коновалова О.Ю. Биологические активные вещества лекарственных растений / О.Ю. Коновалова, и др. - М.: Издательско-полиграфический центр «Киевский университет», 2008. - 352 с.).
Ациклические тритерпеноиды, в частности сквален, обладают антиоксидантными свойствами (защищают от перекисного окисления липидов), способностью снижать уровень холестерина, оказывают иммуностимулирующее действие, используются в качестве дополнительной терапии при различных формах рака (Gregory S. Squalene And Its Potential Clinical Uses / S. Gregory, N.D. Kelly // Alternative Medicine Review. - 1999. - Vo.l 4. - №1. P 29-36.). Сквален является цитопротективным средством против вызванной химиотерапией токсичности (Das В. Squalene Selectively Protects Mouse Bone Marrow Progenitors Against Cisplatin and Carboplatin-Induced Cytotoxicity In Vivo Without Protecting Tumor Growth / B. Das, et al. // Neoplasia. - 2008. - Vol 10. - №10. P 1105-1119).
Известен способ получения биологически активных веществ из биомассы культивируемых клеток растений (патент РФ 2039817, опубл. 20.07.1995, МПК C12N 5/04), включающий выращивание клеточной биомассы, ее разрушение, отделение жидкой фракции, концентрирование биологически активных веществ в жидкой фракции и сушку концентрата до получения целевого продукта, отличающийся тем, что выращенную биомассу при разрушении подвергают тепловой обработке при 80-130°С в течение 5-60 мин. Недостатком данного способа является сложность технологического процесса, также для его осуществления необходимо дополнительное оборудование.
Известен способ получения стефарина сульфата в культуре клеток растения стефания гладкая (патент РФ 2399666, опубл. 20.09.2010, МПК C12N 5/04). Клетки растения стефания гладкая культивируют на жидкой питательной среде при перемешивании и аэрации воздухом в темноте. Добавление в питательную среду в конце экспоненциальной фазы роста культуры метилового эфира жасмоновой кислоты и олеиновой кислоты повышает выход стефарина сульфата, который является субстанцией для получения медицинского препарата стефаглабрина сульфата.
Известен способ получения алкалоидов (патент РФ 2394100, опубл. 10.07.2010, МПК C12N 5/04), который предусматривает выращивание культуры ткани Rauwolfia serpentina Benth (раувольфии змеиной) штамм К-27 на питательной среде заданного состава в присутствии мелафена (меламиновой соли бис(оксиметил)фосфиновой кислоты) 10-17 пассажей
при концентрации мелафена 1⋅10-3 г/л. После чего полученную культуру ткани Rauwolfia serpentina Benth пересаживают на питательную среду того же состава, но содержащую сверхмалые концентрации мелафена 1⋅10-10-1⋅10-15 г/л, преимущественно при 1⋅10-13 г/л, и выращивают на этой среде в течение 1 пассажа не более 50 суток.
Недостатками известных аналогов является их направленность на культивирование определенных видов растений: стефании гладкой, раувольфии змеиной, а также получение других групп БАВ (биологически активные вещества). Исходя из этого данные способы не подходят для культивирования и получения БАВ из клеточной культуры болиголова пятнистого.
Культивирование стефании производится на жидких средах с добавлением метилового эфира жасмоновой кислоты и олеиновой кислоты, выращивание культуры болиголова пятнистого идет на твердых питательных средах, без добавления иных стимуляторов, кроме гормонов.
Для получения алкалоидов культуры ткани Rauwolfia serpentina Bent дополнительно в среду для культивирования добавляют мелафен, что усложняет технологию культивирования и приготовления питательной среды и увеличивает ее стоимость.
Наиболее близким к заявляемому техническому решению по технической сущности и достигаемому техническому результату является способ получения биологически активных веществ в клеточной культуре Atragene speciosa Weinm. (княжик сибирский) (патент РФ 2428473, опубл. 10.09.2011, МПК C12N 5/04).
Клетки растения Atragene speciosa Weinm. (княжик сибирский) культивируют на среде МС при освещении белым светом интенсивностью (2-4)×103 лк с фотопериодом 12-14 час при концентрации 2,4-D (2,4-дихлорфеноксиуксусной кислоты) 0,6-1,2 мг/л, 6-БАП (6-бензиламинопурин) 0,2-0,6 мг/л, мезоинозита 100-125 мг/л. Введение дополнительно в питательную среду фитогормона 24-эпибрассинолида увеличивает процентное содержание целевого продукта в клетках. Описанный способ принят за прототип изобретения. Недостатками прототипа является более сложная технология выращивания культуры, при которой используется свет определенной интенсивности, для этого необходимо определенное оборудование. Также для увеличения процентного содержание целевого продукта в среду добавляют 24-эпибрассинолид, что увеличивает ее стоимость. Данный способ подходит для регуляции содержания веществ с адаптогенной и ноотропной активностью княжика сибирского, в то время как предлагаемый способ направлен на получение активных веществ болиголова пятнистого. Для выращивания одной из линий культуры болиголова пятнистого в качестве стимуляторов роста используется 2,4-D, как и в прототипе. Однако для культуры болиголова пятнистого необходима более низкая концентрация стимулятора в отличие от прототипа.
Болиголов пятнистый (Conium maculatum L.) - растение семейства зонтичные, содержит значительное количество различных биологически активных веществ, в том числе фуранокумаринов и ациклических тритерпеноидов. Болиголов обладает болеутоляющим, успокаивающим, противосудорожным, противовоспалительным и очень сильным иммуностимулирующим действием, благодаря чему включен в большинство сборов трав для лечения практически всех заболеваний, особенно онкологических.
Задачей настоящего изобретения является разработка способа получения биологически активных веществ в клеточной культуре болиголова пятнистого, перспективной в качестве возможного источника БАВ лекарственного действия.
Для решения поставленной задачи разработан способ, включающий культивирование на питательной среде МС в присутствии 6-БАП, сбор биомассы и выделение биологически активных веществ, отличающийся тем, что культивирование ведут при 26±1°С, влажности 70%, в темноте, 6-БАП вводят в питательную среду при концентрации 1 - 0,1 мг/л совместно с 2,4-D при концентрации в диапазоне 1 - 0,5 мг/л или совместно с НУК (α-нафтилуксусной) кислотой при концентрации в диапазоне 3 - 0,5 мг/л, а биологически активные вещества выделяют путем кислого и щелочного хлороформного извлечения.
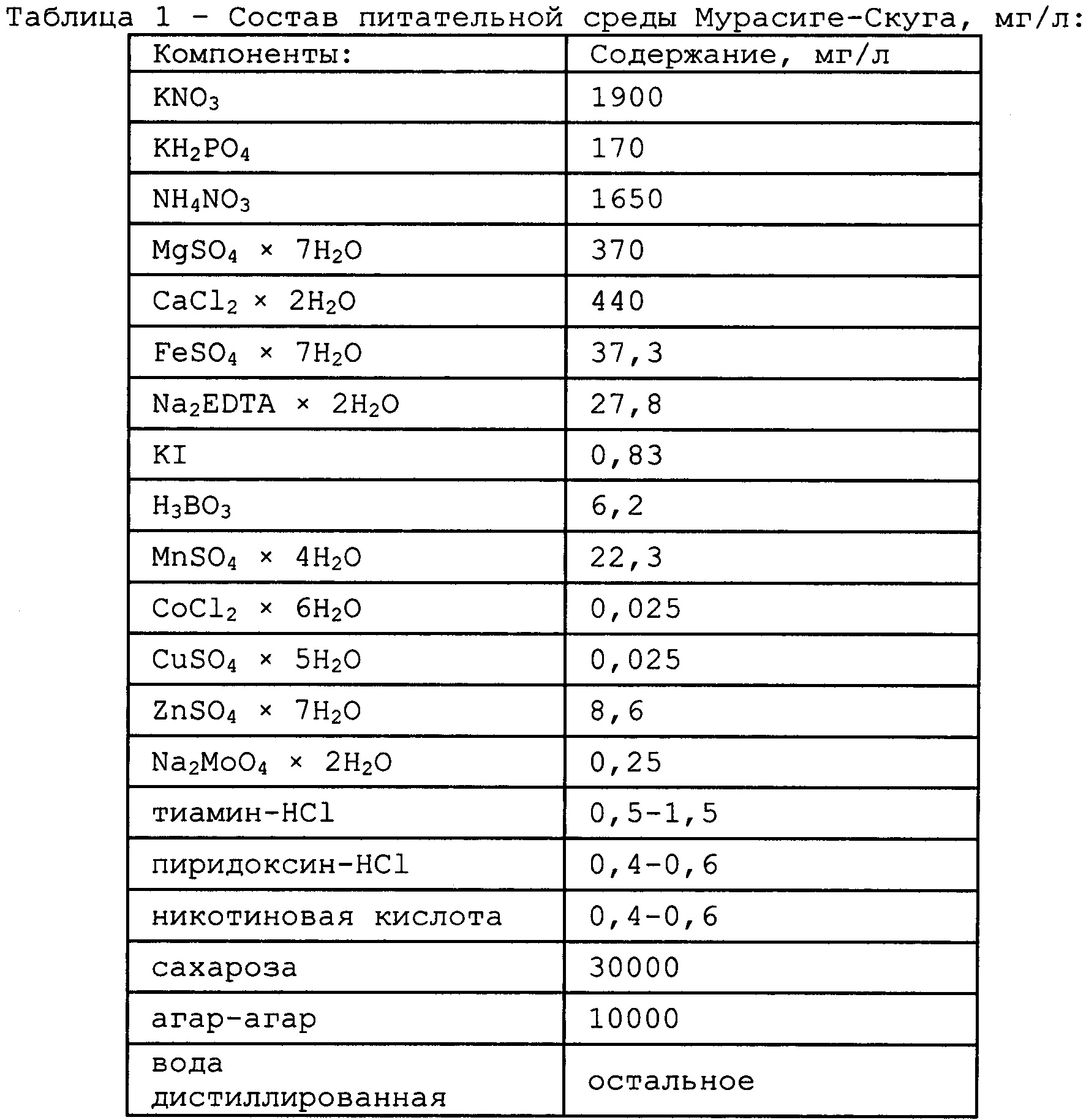
Питательная среда Мурасиге-Скуга содержит компоненты в количественном соотношении, представленном в таблице 1.
Сбор биомассы осуществляют на 30 сутки культивирования, культуру отделяют от питательной среды, измельчают в фарфоровой ступке до однородного состояния. Из полученной массы получают водный экстракт, подкисляют насыщенным раствором винной кислоты до получения рН 2 и проводят извлечение хлороформом (кислое извлечение содержит фуранокумарины), затем водный раствор подщелачивают раствором натрия гидроксида до рН 10 и вновь извлекают хлороформом (щелочное извлечение содержит ациклические тритерпеноиды).
Прирост сырой биомассы оценивают по общепринятому показателю - ростовому индексу, определяя средние значения начальной и конечной биомассы. Сухую массу определяют, высушивая клетки при температуре 55-60°С до воздушно-сухого состояния.
Ростовой индекс по массе сырого вещества первой линии каллусной культуры Conium maculatum составляет - 7,58, второй линии - 6,04. Продуктивность каллусной культуры Conium maculatum на 1 литр среды составила для первой линии - 446 г/л, для второй линии - 379 г/л.
Содержание фуранокумаринов в культуре клеток Conium maculatum L линии первой составляет 1,14% и линии второй 2,07%, выращенной по изобретению, значительно выше, чем их количество в надземной части интактного растения (0,13-0,17%). Содержание каллусной культуре Conium maculatum L ациклических тритерпеноидов в первой линии составляет 1,15%, во второй линии 0,43%, что также превышает содержание ациклических тритерпеноидов в надземной части интактного растения (0,17-0,19%). Полученные данные позволяют говорить об эффективности заявленного способа регуляции содержания фуранокумаринов и ациклических тритерпеноидов в клеточной культуре Conium maculatum L и перспективности его применения в промышленных масштабах.
Достигаемый технический результат заключается в получении требуемого объема биомассы каллусной культуры, который содержит БАВ - фуранокумарины и ациклические тритерпеноиды.
Пример 1. Биомассу каллусной культуры болиголова пятнистого получают путем выращивания на питательной среде МС с добавлением 1,5 мг/л 2-4 D и 1 - мг/л 6-БАП.
Для приготовления питательной среды готовят концентрат макросолей (KNO3 - 1900 мг/л, NH4NO3 - 1650 мг/л, MgSO4×7H2O 370 мг/л, KH2PO4 - 170 мг/л), при этом каждую из макросолей растворяют последовательно в небольшом количестве воды, а затем объем доводят до 1 л. Аналогично готовят концентраты микросолей (H3BO3 - 6,2 мг/л, MnSO4×4H2O - 32,3 мг/л, ZnSO4×7H2O - 8,6 мг/л, Na2MoO4×2H2O - 0,25 мг/л, KI - 0,83 мг/л, CuSO4×5H2O - 0,025 мг/л, CoCl2×6H2O - 0,025 мг/л), Fe-хелата (FeSO4×7H2O - 37,3 мг/л, Na2EDTA×2H2O - 27,8 мг/л), CaCl2×2H2O, витаминов (пиридоксин-HCl - 0,4-0,6 мг/л, тиамин-HCl - 0,5-1,5 мг/л, никотиновая кислота-HCl - 0,4-0,6 мг/л). Макро- и микросоли, Fe-хелат, CaCl2×2H2O, витамины в виде концентратов смешивают в небольшом количестве воды. Раствор доводят дистиллированной водой до 1 л. В колбы на 500 мл насыпают по 3 г агара, по 9 г сахарозы, среду разливают по 300 мл, закрывают фольгой и стерилизуют в автоклаве 20 мин при 1,0 атм. Чашки Петри, сосуды для культивирования, пинцеты и скальпель стерилизуют в течение 2,5 часа в сухожаровом шкафу при 160°С. Затем стерильную питательную среду в условиях ламинарного бокса размещают по культуральным сосудам.
В условиях ламинарного бокса в стерильную питательную среду добавляют 2,4-D (1 мг/л) и 6-БАП (1 мг/л) и размещают ее по культуральным сосудам.
Ткань высаживают в возрасте 30 суток. Культивирование каллусной культуры проводят при 26±1°С, влажности - 70%, в темноте.
После накопления необходимого количества биомассы на 30 сутки производят отделение ткани от питательной среды и выделение комплекса биологически активных веществ.
Навеску каллусной ткани (100 г) растирают в фарфоровой ступке до кашеобразного состояния, помещают в химический стакан, приливают 120 мл дистиллированной воды, добавляют по каплям насыщенный раствор винной кислоты до получения рН 2 и оставляют на 2 часа, полученное извлечение фильтруют через бумажный фильтр.
Получение кислого хлороформного извлечения. Для выделения фуранокумаринов полученный водный раствор помещают в делительную воронку, приливают 40 мл хлороформа и экстрагируют в течение минуты. Хлороформное извлечение отделяют и повторяют экстракцию еще два раза, добавляя по 30 и 25 мл хлороформа. Полученное кислое извлечение фильтруют через фильтр с безводным натрия сульфатом и выпаривают до сухого остатка. Сухой остаток растворяют в 1,5 мл хлороформа.
Получение щелочного хлороформного извлечения. Для выделения ациклических тритерпеноидов водный остаток подщелачивают раствором 10% NaOH до рН 10, помещают в делительную воронку, добавляют 40 мл хлороформа и экстрагируют в течение минуты. Хлороформное извлечение отделяют и повторяют экстракцию еще три раза, добавляя по 40 и 30 (дважды) мл хлороформа. Готовое щелочное извлечение фильтруют через фильтр с безводным натрия сульфатом и выпаривают до сухого остатка. Сухой остаток растворяют в 1,5 мл хлороформа.
Анализ БАВ кислого и щелочного хлороформного извлечения из каллусной культуры проводят методом хромато-масс-спектрометрии (ГХ/МС) на приборе Trace DSQ (Thermoelectron corp., США), с программным обеспечением Xcalibur 1.4. В работе используют колонку TR-5MS (30 м·0,25 мм·0,25 мкм).
Пример 2. Биомассу каллусной культуры болиголова пятнистого получают путем выращивания на питательной среде МС с добавлением 0,5 мг/л 2-4 D и 0,1 - мг/л 6-БАП.
Для приготовления питательной среды готовят концентрат макросолей (KNO3 - 1900 мг/л, NH4NO3 - 1650 мг/л, MgSO4×7H2O 370 мг/л, KH2PO4 - 170 мг/л), при этом каждую из макросолей растворяют последовательно в небольшом количестве воды, а затем объем доводят до 1 л. Аналогично готовят концентраты микросолей (H3BO3 - 6,2 мг/л, MnSO4×4H2O - 32,3 мг/л, ZnSO4×7H2O - 8,6 мг/л, Na2MoO4×2H2O - 0,25 мг/л, KI - 0,83 мг/л, CuSO4×5H2O - 0,025 мг/л, CoCl2×6H2O - 0,025 мг/л), Fe-хелата (FeSO4×7H2O - 37,3 мг/л, Na2EDTA×2H2O - 27,8 мг/л), CaCl2×2H2O, витаминов (пиридоксин-HCl - 0,4-0,6 мг/л, тиамин-HCl - 0,5-1,5 мг/л, никотиновая кислота-HCl - 0,4-0,6 мг/л). Макро- и микросоли, Fe-хелат, CaCl2×2H2O, витамины в виде концентратов смешивают в небольшом количестве воды. Раствор доводят дистиллированной водой до 1 л. В колбы на 500 мл насыпают по 3 г агара, по 9 г сахарозы, среду разливают по 300 мл, закрывают фольгой и стерилизуют в автоклаве 20 мин при 1,0 атм. Чашки Петри, сосуды для культивирования, пинцеты и скальпель стерилизуют в течение 2,5 часа в сухожаровом шкафу при 160°С. Затем стерильную питательную среду в условиях ламинарного бокса размещают по культуральным сосудам.
В условиях ламинарного бокса в стерильную питательную среду добавляют 2,4-D (1 мг/л) и 6-БАП (1 мг/л) и размещают ее по культуральным сосудам.
Ткань высаживают в возрасте 30 суток. Культивирование каллусной культуры проводят при 26±1°С, влажности - 70%, в темноте.
После накопления необходимого количества биомассы на 30 сутки производят отделение ткани от питательной среды и выделение комплекса биологически активных веществ.
Навеску каллусной ткани (100 г) растирают в фарфоровой ступке до кашеобразного состояния, помещают в химический стакан, приливают 120 мл дистиллированной воды, добавляют по каплям насыщенный раствор винной кислоты до получения рН 2 и оставляют на 2 часа, полученное извлечение фильтруют через бумажный фильтр.
Получение кислого хлороформного извлечения. Для выделения фуранокумаринов полученный водный раствор помещают в делительную воронку, приливают 40 мл хлороформа и экстрагируют в течение минуты. Хлороформное извлечение отделяют и повторяют экстракцию еще два раза, добавляя по 30 и 25 мл хлороформа. Полученное кислое извлечение фильтруют через фильтр с безводным натрия сульфатом и выпаривают до сухого остатка. Сухой остаток растворяют в 1,5 мл хлороформа.
Получение щелочного хлороформного извлечения. Для выделения ациклических тритерпеноидов водный остаток подщелачивают раствором 10% NaOH до рН 10, помещают в делительную воронку, добавляют 40 мл хлороформа и экстрагируют в течение минуты. Хлороформное извлечение отделяют и повторяют экстракцию еще три раза, добавляя по 40 и 30 (дважды) мл хлороформа. Готовое щелочное извлечение фильтруют через фильтр с безводным натрия сульфатом и выпаривают до сухого остатка. Сухой остаток растворяют в 1,5 мл хлороформа.
Анализ БАВ кислого и щелочного хлороформного извлечения из каллусной культуры проводят методом хромато-масс-спектрометрии (ГХ/МС) на приборе Trace DSQ (Thermoelectron corp., США), с программным обеспечением Xcalibur 1.4. В работе используют колонку TR-5MS (30 м·0,25 мм·0,25 мкм).
Пример 3. Биомассу каллусной культуры болиголова пятнистого получают путем выращивания на питательной среде МС с добавлением 3 мг/л НУК и 1 - мг/л 6-БАП.
Для приготовления питательной среды готовят концентрат макросолей (KNO3 - 1900 мг/л, NH4NO3 - 1650 мг/л, MgSO4×7H2O 370 мг/л, KH2PO4 - 170 мг/л), при этом каждую из макросолей растворяют последовательно в небольшом количестве воды, а затем объем доводят до 1 л. Аналогично готовят концентраты микросолей (H3BO3 - 6,2 мг/л, MnSO4×4H2O - 32,3 мг/л, ZnSO4×7H2O - 8,6 мг/л, Na2MoO4×2H2O - 0,25 мг/л, KI - 0,83 мг/л, CuSO4×5H2O - 0,025 мг/л, CoCl2×6H2O - 0,025 мг/л), Fe-хелата (FeSO4×7H2O - 37,3 мг/л, Na2EDTA×2H2O - 27,8 мг/л), CaCl2×2H2O, витаминов (пиридоксин-HCl - 0,4-0,6 мг/л, тиамин-HCl - 0,5-1,5 мг/л, никотиновая кислота-HCl - 0,4-0,6 мг/л). Макро- и микросоли, Fe-хелат, CaCl2×2H2O, витамины в виде концентратов смешивают в небольшом количестве воды. Раствор доводят дистиллированной водой до 1 л. В колбы на 500 мл насыпают по 3 г агара, по 9 г сахарозы, среду разливают по 300 мл, закрывают фольгой и стерилизуют в автоклаве 20 мин при 1,0 атм. Чашки Петри, сосуды для культивирования, пинцеты и скальпель стерилизуют в течение 2,5 часа в сухожаровом шкафу при 160°С. Затем стерильную питательную среду в условиях ламинарного бокса размещают по культуральным сосудам.
В условиях ламинарного бокса в стерильную питательную среду добавляют 2,4-D (1 мг/л) и 6-БАП (1 мг/л) и размещают ее по культуральным сосудам.
Ткань высаживают в возрасте 30 суток. Культивирование каллусной культуры проводят при 26±1°С, влажности - 70%, в темноте.
После накопления необходимого количества биомассы на 30 сутки производят отделение ткани от питательной среды и выделение комплекса биологически активных веществ.
Навеску каллусной ткани (100 г) растирают в фарфоровой ступке до кашеобразного состояния, помещают в химический стакан, приливают 120 мл дистиллированной воды, добавляют по каплям насыщенный раствор винной кислоты до получения рН 2 и оставляют на 2 часа, полученное извлечение фильтруют через бумажный фильтр.
Получение кислого хлороформного извлечения. Для выделения фуранокумаринов полученный водный раствор помещают в делительную воронку, приливают 40 мл хлороформа и экстрагируют в течение минуты. Хлороформное извлечение отделяют и повторяют экстракцию еще два раза, добавляя по 30 и 25 мл хлороформа. Полученное кислое извлечение фильтруют через фильтр с безводным натрия сульфатом и выпаривают до сухого остатка. Сухой остаток растворяют в 1,5 мл хлороформа.
Получение щелочного хлороформного извлечения. Для выделения ациклических тритерпеноидов водный остаток подщелачивают раствором 10% NaOH до рН 10, помещают в делительную воронку, добавляют 40 мл хлороформа и экстрагируют в течение минуты. Хлороформное извлечение отделяют и повторяют экстракцию еще три раза, добавляя по 40 и 30 (дважды) мл хлороформа. Готовое щелочное извлечение фильтруют через фильтр с безводным натрия сульфатом и выпаривают до сухого остатка. Сухой остаток растворяют в 1,5 мл хлороформа.
Анализ БАВ кислого и щелочного хлороформного извлечения из каллусной культуры проводят методом хромато-масс-спектрометрии (ГХ/МС) на приборе Trace DSQ (Thermoelectron corp., США), с программным обеспечением Xcalibur 1.4. В работе используют колонку TR-5MS (30 м·0,25 мм·0,25 мкм).
Пример 4. Биомассу каллусной культуры болиголова пятнистого получают путем выращивания на питательной среде МС с добавлением 3 мг/л НУК и 0,1 - мг/л БАП.
Для приготовления питательной среды готовят концентрат макросолей (KNO3 - 1900 мг/л, NH4NO3 - 1650 мг/л, MgSO4×7H2O 370 мг/л, KH2PO4 - 170 мг/л), при этом каждую из макросолей растворяют последовательно в небольшом количестве воды, а затем объем доводят до 1 л. Аналогично готовят концентраты микросолей (H3BO3 - 6,2 мг/л, MnSO4×4H2O - 32,3 мг/л, ZnSO4×7H2O - 8,6 мг/л, Na2MoO4×2H2O - 0,25 мг/л, KI - 0,83 мг/л, CuSO4×5H2O - 0,025 мг/л, CoCl2×6H2O - 0,025 мг/л), Fe-хелата (FeSO4×7H2O - 37,3 мг/л, Na2EDTA×2H2O - 27,8 мг/л), CaCl2×2H2O, витаминов (пиридоксин-HCl - 0,4-0,6 мг/л, тиамин-HCl - 0,5-1,5 мг/л, никотиновая кислота-HCl - 0,4-0,6 мг/л). Макро- и микросоли, Fe-хелат, CaCl2×2H2O, витамины в виде концентратов смешивают в небольшом количестве воды. Раствор доводят дистиллированной водой до 1 л. В колбы на 500 мл насыпают по 3 г агара, по 9 г сахарозы, среду разливают по 300 мл, закрывают фольгой и стерилизуют в автоклаве 20 мин при 1,0 атм. Чашки Петри, сосуды для культивирования, пинцеты и скальпель стерилизуют в течение 2,5 часа в сухожаровом шкафу при 160°С. Затем стерильную питательную среду в условиях ламинарного бокса размещают по культуральным сосудам.
В условиях ламинарного бокса в стерильную питательную среду добавляют 2,4-D (1 мг/л) и 6-БАП (1 мг/л) и размещают ее по культуральным сосудам.
Ткань высаживают в возрасте 30 суток. Культивирование каллусной культуры проводят при 26±1°С, влажности - 70%, в темноте.
После накопления необходимого количества биомассы на 30 сутки производят отделение ткани от питательной среды и выделение комплекса биологически активных веществ.
Навеску каллусной ткани (100 г) растирают в фарфоровой ступке до кашеобразного состояния, помещают в химический стакан, приливают 120 мл дистиллированной воды, добавляют по каплям насыщенный раствор винной кислоты до получения рН 2 и оставляют на 2 часа, полученное извлечение фильтруют через бумажный фильтр.
Получение кислого хлороформного извлечения. Для выделения фуранокумаринов полученный водный раствор помещают в делительную воронку, приливают 40 мл хлороформа и экстрагируют в течение минуты. Хлороформное извлечение отделяют и повторяют экстракцию еще два раза, добавляя по 30 и 25 мл хлороформа. Полученное кислое извлечение фильтруют через фильтр с безводным натрия сульфатом и выпаривают до сухого остатка. Сухой остаток растворяют в 1,5 мл хлороформа.
Получение щелочного хлороформного извлечения. Для выделения ациклических тритерпеноидов водный остаток подщелачивают раствором 10% NaOH до рН 10, помещают в делительную воронку, добавляют 40 мл хлороформа и экстрагируют в течение минуты. Хлороформное извлечение отделяют и повторяют экстракцию еще три раза, добавляя по 40 и 30 (дважды) мл хлороформа. Готовое щелочное извлечение фильтруют через фильтр с безводным натрия сульфатом и выпаривают до сухого остатка. Сухой остаток растворяют в 1,5 мл хлороформа.
Анализ БАВ кислого и щелочного хлороформного извлечения из каллусной культуры проводят методом хромато-масс-спектрометрии (ГХ/МС) на приборе Trace DSQ (Thermoelectron corp., США), с программным обеспечением Xcalibur 1.4. В работе используют колонку TR-5MS (30 м·0,25 мм·0,25 мкм).
Технический результат достигается благодаря использованию разработанного способа получения БАВ - фуранокумаринов и ациклических тритерпеноидов, из каллусной культуры Conium maculatum L., что позволит расширить арсенал средств биотехнологического происхождения с повышением терапевтического эффекта.

