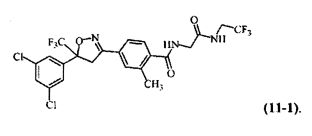
Результат интеллектуальной деятельности: ИЗОКСАЗОЛИНОВЫЕ КОМПОЗИЦИИ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ПРОТИВОПАРАЗИТАРНЫХ СРЕДСТВ
Вид РИД
Изобретение
Перекрестная ссылка на родственные заявки на патент
По данной заявке испрашивается приоритет на основании предварительной заявки на патент США 61/080444 (поданной 14 июля 2008); предварительной заявки на патент США 60/956448 (поданной 17 августа 2007); заявки на Европейский патент 07016152.6 (поданной 17 августа 2007) и заявки на Европейский патент 07150309.8 (поданной 21 декабря 2007). Все указанные заявки на патент включены в данное описание посредством ссылок.
Область техники, к которой относится изобретение
Изобретение относится к способам борьбы с заражением паразитами животных и окружающей их среды и, в особенности, к способам применения изоксазолинов для борьбы с паразитами у животных или в окружающей их среде, а также лечения паразитарных заболеваний у животных. Изоксазолины включают 4-(изоксазолинил)бензамиды (конкретно, замещенные 4-(5-(галогенметил)-5-фенилизоксазолин-3-ил)бензамиды) и 4-(изоксазолинил)бензотиоамиды (конкретно, замещенные 4-(5-(галогенметил)-5-фенилизоксазолин-3-ил)бензотиоамиды). Настоящее изобретение также относится к композициям, содержащим изоксазолины, для применения в таких способах, к применению изоксазолинов для осуществления таких способов, и наборам, содержащим изоксазолины, для осуществления таких способов. Настоящее изобретение также относится к применению изоксазолинов в качестве лекарственных средств, в частности лекарственных средств, которые можно использовать в вышеуказанных способах.
Предпосылки создания изобретения
Известен ряд вредителей и паразитов, которые заражают теплокровных животных. Такие вредители и паразиты могут доставлять большие неприятности как животным, так и их владельцам. Например, фактически все домашние и сельскохозяйственные животные могут быть поражены эктопаразитами, такими как иксодовые клещи, клещи, вши и блохи. Эктопаразиты имеют склонность раздражать животных, а также могут вызывать клиническое заболевание и вредные субклинические состояния или сами по себе, или посредством внесения переносимых переносчиками патогенов. На сегодняшний день разработаны различные способы обработки для борьбы с эктопаразитами у теплокровных животных. Тем не менее, остается потребность в композициях (и способах их применения), которые являются биодоступными, могут обеспечить контактную или системную активность, потенциально эффективны, начинают быстро действовать, имеют длительный период действия и/или являются безопасными для животных-реципиентов и/или их владельцев людей. Настоящее изобретение направлено на удовлетворение такой потребности.
Сущность изобретения
В основном, настоящее изобретение относится к изоксазолиновым композициям (в частности, композициям с 4-(изоксазолинил)бензамидами (также известным как, например, композиции с «амидом 4-(4,5-дигидроизоксазол-3-ил)бензойной кислоты») и композициям с 4-(изоксазолинил)бензотиоамидами (также известным как, например, композиции с «4-(4,5-дигидроизоксазол-3-ил)бензотиоамидом»)) и их применению для борьбы с эктопаразитами у теплокровных животных. В соответствии с настоящим изобретением, обнаружено, что такие композиции, как правило, показывают желаемую биодоступность и могут обеспечить контактную и/или системную активность. Многие композиции также обеспечивают профили безопасности, желаемые для теплокровных животных-реципиентов и/или их владельцев. Кроме того, обнаружено, что одно введение таких композиций, как правило, обеспечивает возможную активность против одного или нескольких эктопаразитов, причем в то же время имеется тенденция к обеспечению быстрого начала действия, длительной активности и/или нужных профилей безопасности.
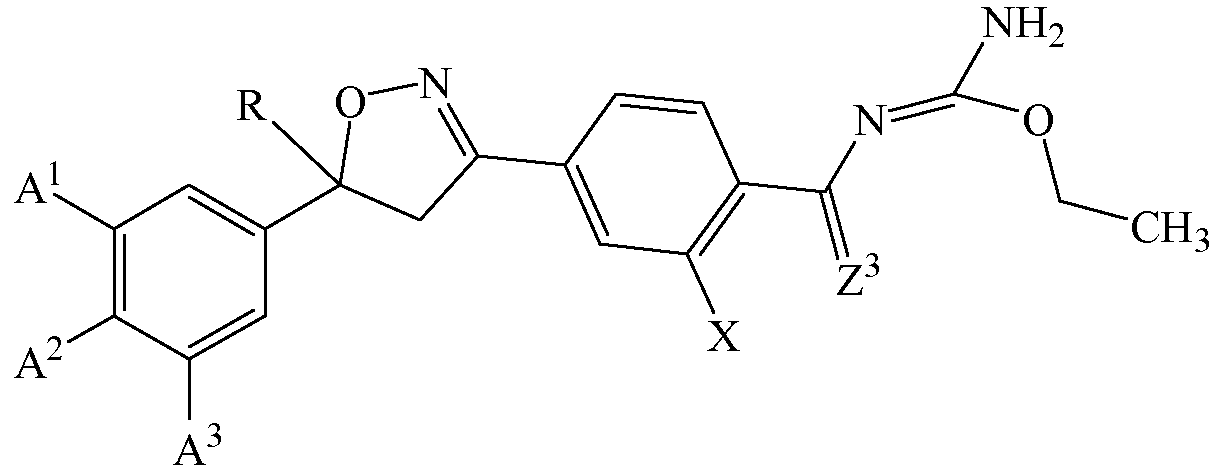
Поэтому настоящее изобретение относится, в частности, к способу борьбы с заражением животного эктопаразитами. Способ включает введение животному изоксазолина, соли изоксазолина или сольвата изоксазолина или его соли. Изоксазолин имеет структурную формулу (I)
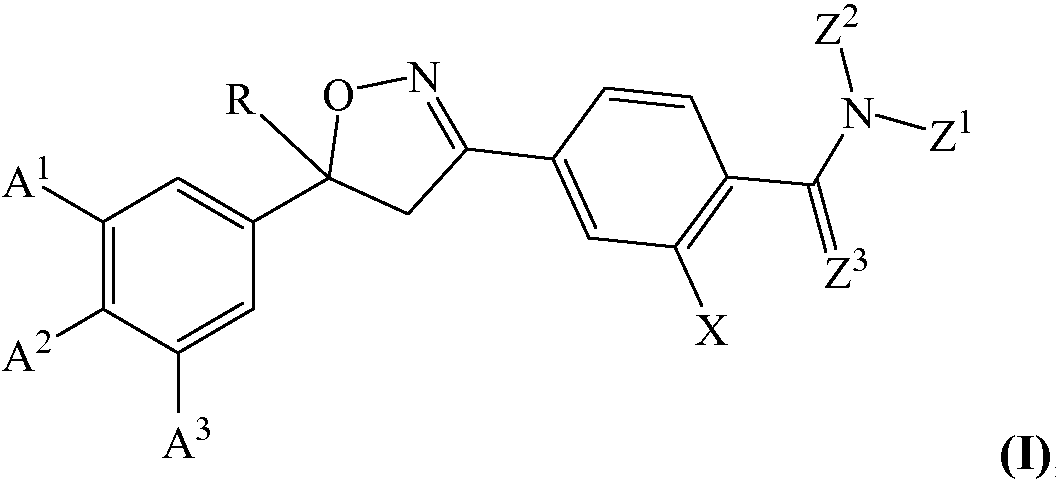
где один из А1 и А2 выбирают из группы, состоящей из галогена и галогенметила;
один из А1 и А2 выбирают из группы, состоящей из водорода, галогена и галогенметила;
А3 выбирают из группы, состоящей из водорода, галогена и галогенметила;
R представляет собой галогенметил;
Х выбирают из группы, состоящей из водорода, галогена, метила, галогенметила, этила и галогенэтила.
В некоторых вариантах осуществления Z1 и Z2 являются независимыми заместителями. В таких вариантах осуществления
Z1 выбирают независимо из группы, состоящей из водорода, метила, галогенэтила, галогенпропила, галогенбутила, метоксиметила, галогенметоксиметила, этоксиметила, галогенэтоксиметила, пропоксиметила, этиламинокарбонилметила, этиламинокарбонилэтила, диметоксиэтила, пропиниламинокарбонилметила, N-фенил-N-метиламино, галогенэтиламинокарбонилметила, галогенэтиламинокарбонилэтила, тетрагидрофурила, метиламинокарбонилметила, (N,N-диметиламино)карбонилметила, пропиламинокарбонилметила, циклопропиламинокарбонилметила, пропениламинокарбонилметила, галогенэтиламинокарбонилциклопропила,



 и
и 
Когда Z1 является иным, чем водород, Z2 выбирают из группы, состоящей из водорода, этила, метоксиметила, галогенметоксиметила, этоксиметила, галогенэтоксиметила, пропоксиметила, метилкарбонила, этилкарбонила, пропилкарбонила, циклопропилкарбонила, метоксикарбонила, метоксиметилкарбонила, аминокарбонила, этиламинокарбонилметила, этиламинокарбонилэтила, диметоксиэтила, пропиниламинокарбонилметила, галогенэтиламинокарбонилметила и галогенэтиламинокарбонилэтила.
Когда Z1 представляет собой водород, Z2 выбирают из группы, состоящей из метилкарбонила, этилкарбонила, пропилкарбонила, циклопропилкарбонила, метоксикарбонила, метоксиметилкарбонила и аминокарбонила.
В других вариантах осуществления Z1 и Z2 вместе образуют заместитель, выбранный из группы, состоящей из
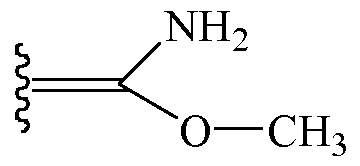 и
и 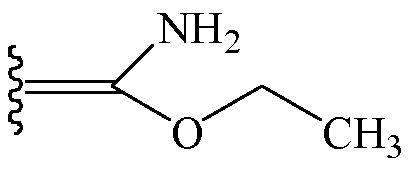
Z3 выбирают из группы, состоящей из О и S.
ZA выбирают из группы, состоящей из водорода, галогена и циано.
Настоящее изобретение также относится, в частности, к способу лечения паразитарных заболеваний у животного. Такой способ включает введение животному вышеописанного изоксазолина, его соли или сольвата.
Настоящее изобретение также относится, в частности, к способу борьбы с заражением эктопаразитами в окружающей среде, которую занимает (периодически или постоянно) животное (например, домашнее животное, такое как кошка или собака). Такой способ включает введение животному вышеописанного изоксазолина, его соли или сольвата.
Настоящее изобретение также относится, в частности, к применению вышеописанного изоксазолина, его соли или сольвата в качестве лекарственного средства.
Настоящее изобретение также относится, в частности, к применению вышеописанного изоксазолина, его соли или сольвата для получения лекарственного средства для лечения паразитарных заболеваний у животного.
Настоящее изобретение также относится, в частности, к вышеописанному изоксазолину, его соли или сольвату для лечения паразитарных заболеваний у животного.
Настоящее изобретение также относится, в частности, к паразитицидной композиции для применения к животному. Композиция содержит вышеописанный изоксазолин, его соль или сольват в количестве, которое эффективно для борьбы с заражением эктопаразитами, когда композицию вводят животному. Композиция также содержит эксципиент (т.е. она содержит по меньшей мере один эксципиент).
Настоящее изобретение также относится, в частности, к терапевтическому набору. Набор содержит вышеописанный изоксазолин, его соль или сольват и дополнительный компонент. Дополнительный компонент может представлять собой, например, диагностический инструмент, инструкции по введению, прибор для введения, эксципиент или другой активный ингредиент или памятку.
Другие преимущества изобретения будут очевидны для специалистов в данной области по прочтению данного описания.
Краткое описание чертежа
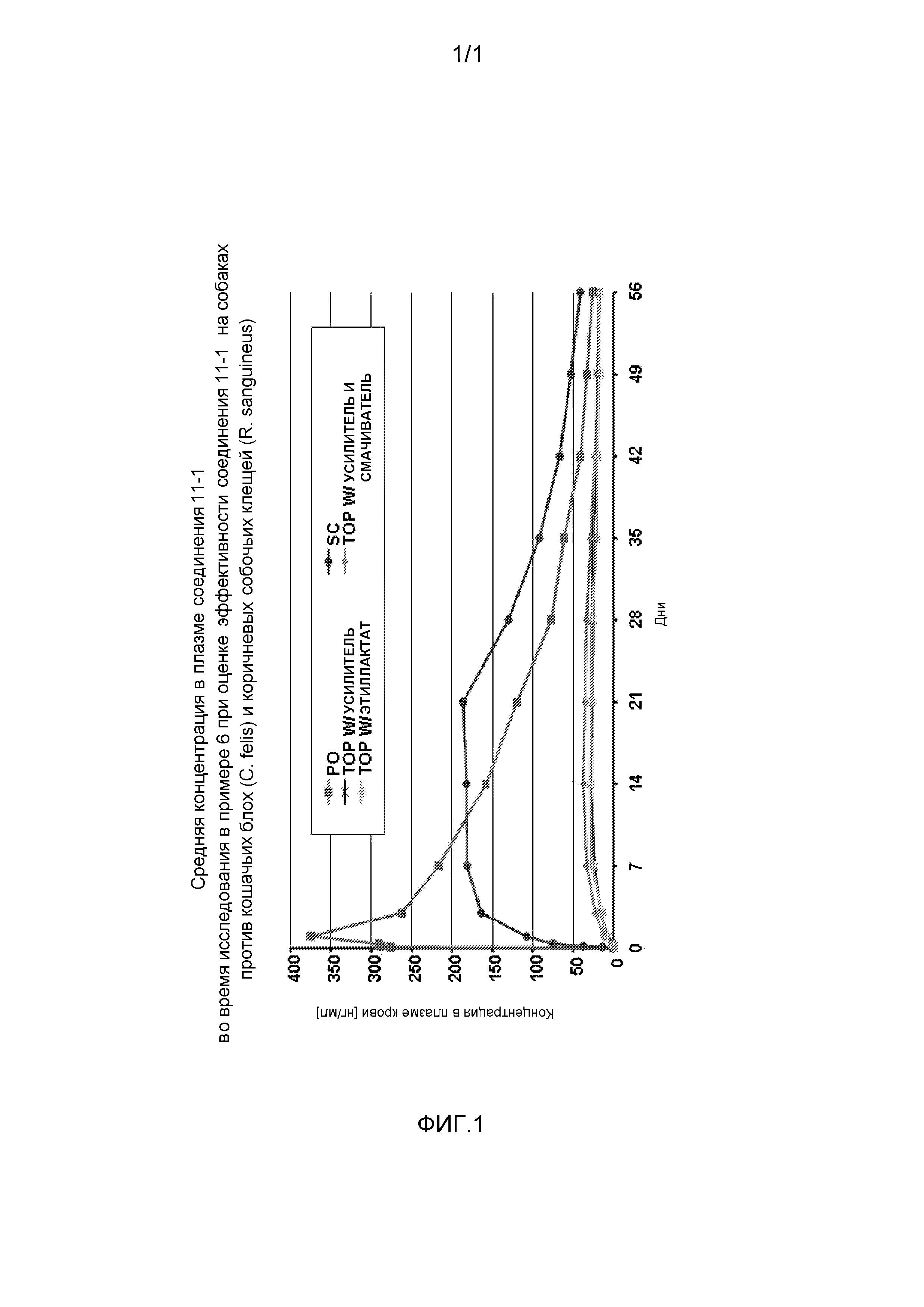
На фиг.1 показана средняя концентрация в плазме соединения 11-1 в исследовании в примере 6, в котором на собаках оценивается эффективность соединения 11-1 против кошачьих блох (Ctenocephalides felis) и коричневых собачьих иксодовых клещей (Rhipicephalus sanguineus). На фиг.1 данные «РО» относятся к группе А (1 мг/кг массы тела соединения 11-1 в форме таблетки для перорального введения); данные «SC» относятся к группе В (1 мг/кг массы тела соединения 11-1 в форме раствора для инъекции для подкожного введения); данные «TOP W/УСИЛИТЕЛЬ» относятся к группе С (1 мг/кг массы тела соединения 11-1 в форме раствора для местного применения, содержащего усилитель абсорбции); данные «TOP W/УСИЛИТЕЛЬ И СМАЧИВАТЕЛЬ» относятся к группе D (1 мг/кг массы тела соединения 11-1 в форме раствора для местного применения, содержащего усилитель абсорбции и смачиватель); и данные «TOP W/ЭТИЛЛАКТАТ» относятся к группе Е (1 мг/кг массы тела соединения 11-1 в форме раствора для местного применения, содержащего в качестве растворителя этиллактат).
Подробное описание предпочтительных вариантов осуществления
Подробное описание предпочтительных вариантов осуществления предназначено только для ознакомления специалистов в данной области с изобретением, его принципами и его практическим применением, так что другие специалисты в данной области смогут адаптировать и применять изобретение в его многочисленных формах, какие могут наилучшим образом подходить для требований практического применения. Данное подробное описание и конкретные примеры в нем, показывающие предпочтительные варианты осуществления настоящего изобретения, предназначены только для целей пояснения. Поэтому настоящее изобретение не ограничивается предпочтительными вариантами осуществления, описанными в данном описании, и может модифицироваться различным образом.
I. Изоксазолины
В основном, изоксазолины, используемые согласно настоящему изобретению, включают соединения формулы (I)

Предпочтительные соединения формулы (I) включают варианты осуществления, указанные ниже.
А. Предпочтительные варианты осуществления А1 и А2
Один из А1 и А2 выбирают из группы, состоящей из галогена и галогенметила. Другой из А1 и А2 выбирают из группы, состоящей из водорода, галогена и галогенметила.
В некоторых вариантах осуществления А1 представляет собой галоген. В некоторых таких вариантах осуществления А1 представляет собой бром. В других вариантах осуществления А1 представляет собой хлор.
В некоторых вариантах осуществления А1 представляет собой галогенметил. В некоторых таких вариантах осуществления А1 представляет собой трифторметил.
В некоторых вариантах осуществления А2 представляет собой водород.
В некоторых вариантах осуществления А2 представляет собой галоген. В некоторых таких вариантах осуществления А2 представляет собой фтор. В других вариантах осуществления А2 представляет собой хлор.
В. Предпочтительные варианты осуществления А3
А3 выбирают из группы, состоящей из водорода, галогена и галогенметила.
В некоторых вариантах осуществления А3 представляет собой водород.
В некоторых вариантах осуществления А3 представляет собой галоген. В некоторых таких вариантах осуществления А3 представляет собой хлор. В других вариантах осуществления А3 представляет собой бром.
В некоторых вариантах осуществления А3 представляет собой галогенметил. В некоторых таких вариантах осуществления А3 представляет собой трифторметил.
С. Предпочтительные варианты осуществления R
R представляет собой галогенметил. В некоторых вариантах осуществления R представляет собой монохлорметил. В других вариантах осуществления R представляет собой трифторметил. В еще других вариантах осуществления R представляет собой монохлордифторметил.
D. Предпочтительные варианты осуществления Х
Х выбирают из группы, состоящей из водорода, галогена, метила, галогенметила, этила и галогенэтила. В некоторых вариантах осуществления Х представляет собой водород. В других вариантах осуществления Х представляет собой бром. В других вариантах осуществления Х представляет собой йод. В других вариантах осуществления Х представляет собой хлор. В других вариантах осуществления Х представляет собой метил. В других вариантах осуществления Х представляет собой этил. В других вариантах осуществления Х представляет собой трифторметил.
Е. Предпочтительные варианты осуществления Z1 и Z2
В некоторых вариантах осуществления Z1 и Z2 являются независимыми заместителями. В таких вариантах осуществления Z1 выбирают из группы, состоящей из водорода, метила, галогенэтила, галогенпропила, галогенбутила, метоксиметила, галогенметоксиметила, этоксиметила, галогенэтоксиметила, пропоксиметила, этиламинокарбонилметила, этиламинокарбонилэтила, диметоксиэтила, пропиниламинокарбонилметила, N-фенил-N-метиламино, галогенэтиламинокарбонилметила, галогенэтиламинокарбонилэтила, тетрагидрофурила, метиламинокарбонилметила, (N,N-диметиламино)карбонилметила, пропиламинокарбонилметила, циклопропиламинокарбонилметила, пропениламинокарбонилметила, галогенэтиламинокарбонилциклопропила,
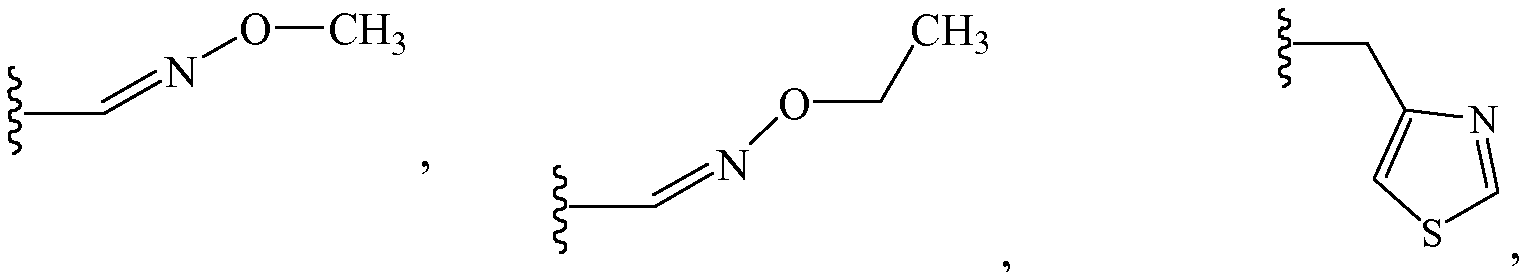
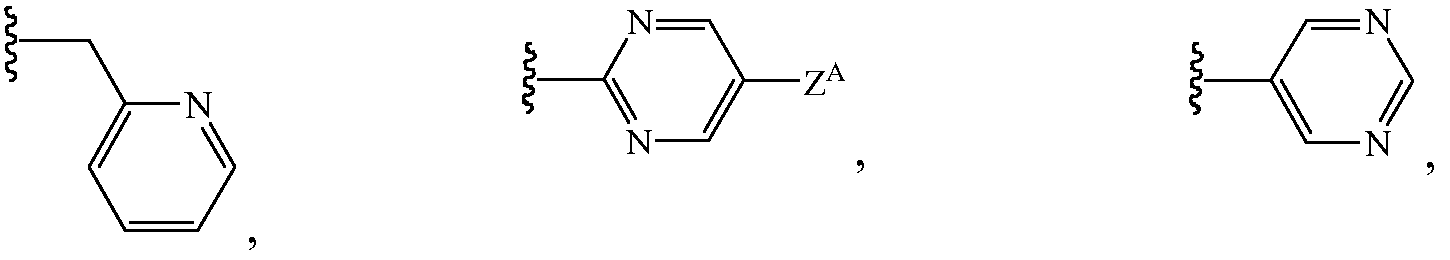
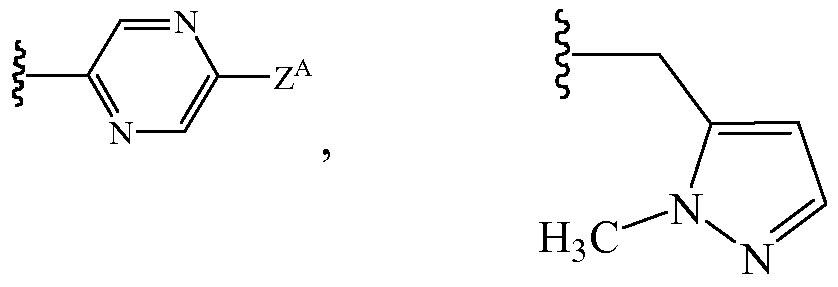 и
и 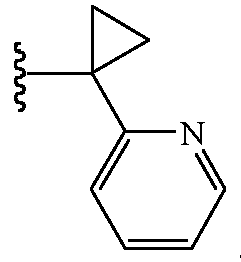
В некоторых таких вариантах осуществления Z1 выбирают из группы, состоящей из водорода, метила, 2,2,2-трифторэтила, метоксиметила, этоксиметила, (2,2,2-трифторэтокси)метила, изопропоксиметила, этиламинокарбонилметила, 2,2-диметоксиэтила, 2-пропиниламинокарбонилметила, N-фенил-N-метиламино, (2,2,2-трифторэтил)аминокарбонилметила, 1-[(2,2,2-трифторэтил)аминокарбонил]этила, тетрагидрофурила, метиламинокарбонилметила, (N,N-диметиламино)карбонилметила, изопропиламинокарбонилметила, циклопропиламинокарбонилметила, (2-пропенил)аминокарбонилметила, (2,2,2-трифторэтил)аминокарбонилциклопропила, (2-фторэтил)аминокарбонилметила, (2-хлорэтил)аминокарбонилметила, 1-(этиламинокарбонил)этила,
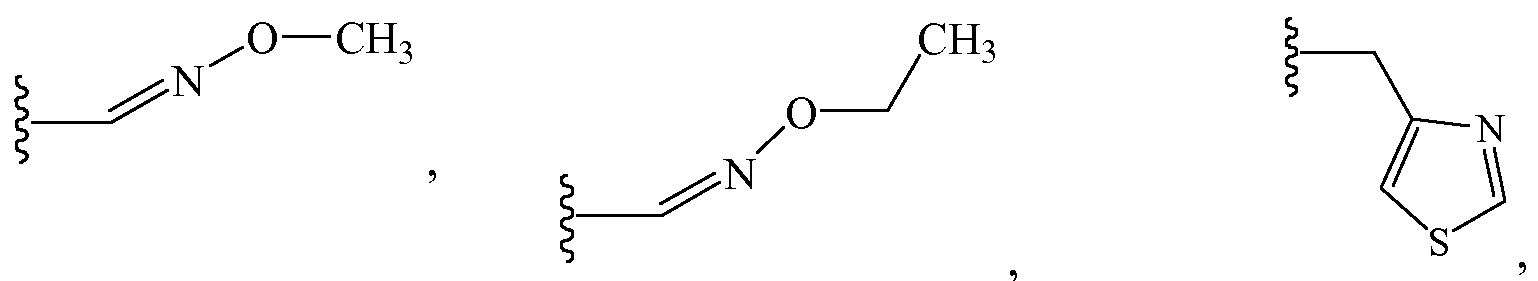
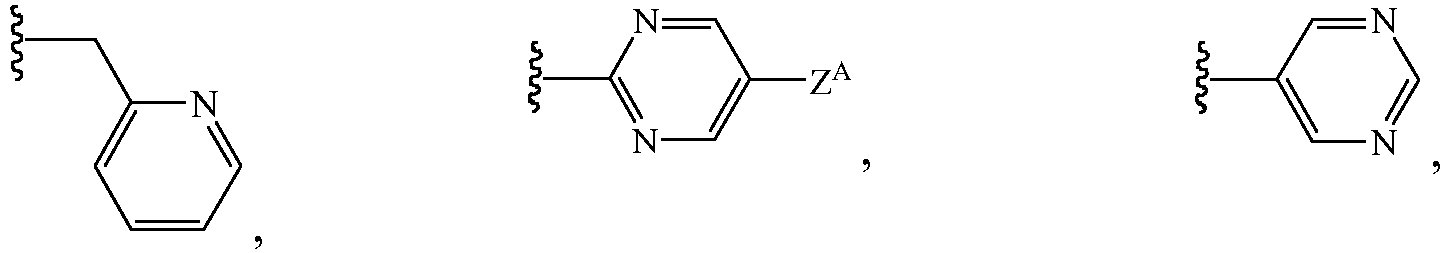
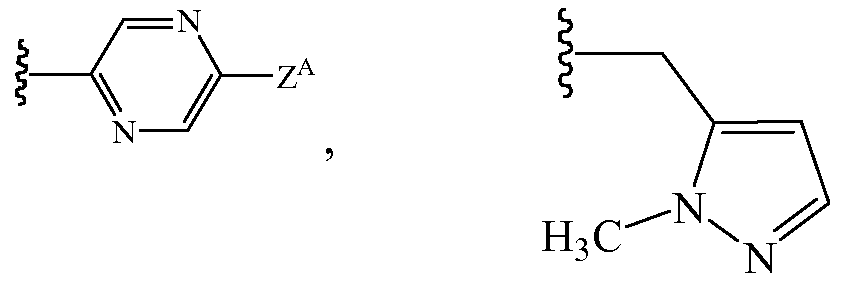 и
и 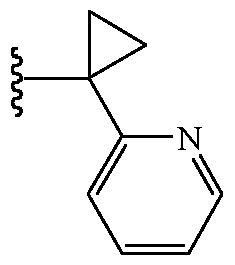
В других вариантах осуществления Z1 выбирают из группы, состоящей из водорода, метила, галогенэтила, галогенпропила, галогенбутила, метоксиметила, галогенметоксиметила, этоксиметила, галогенэтоксиметила, пропоксиметила, этиламинокарбонилметила, этиламинокарбонилэтила, диметоксиэтила, пропиниламинокарбонилметила, N-фенил-N-метиламино, галогенэтиламинокарбонилметила, галогенэтиламинокарбонилэтила, тетрагидрофурила, метиламинокарбонилметила, (N,N-диметиламино)карбонилметила, пропиламинокарбонилметила, циклопропиламинокарбонилметила, пропениламинокарбонилметила, галогенэтиламинокарбонилциклопропила,
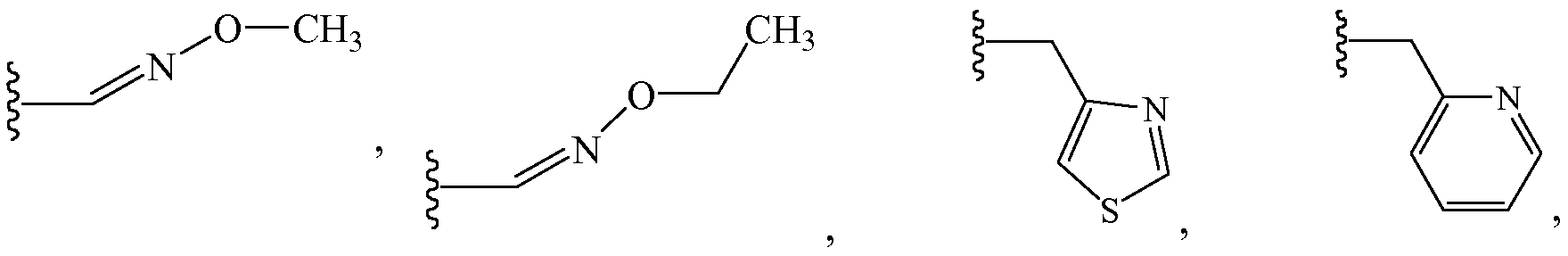
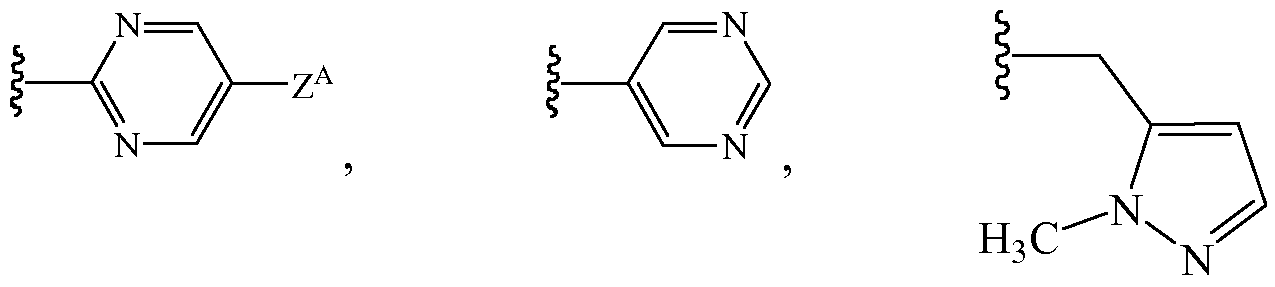 и
и 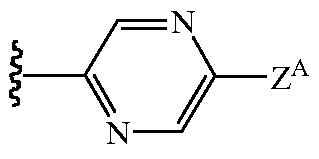
В других вариантах осуществления Z1 выбирают из группы, состоящей из водорода, метила, 2,2,2-трифторэтила, метоксиметила, этоксиметила, (2,2,2-трифторэтокси)метила, изопропоксиметила, этиламинокарбонилметила, 2,2-диметоксиэтила, 2-пропиниламинокарбонилметила, N-фенил-N-метиламино, (2,2,2-трифторэтил)аминокарбонилметила, 1-[(2,2,2-трифторэтил)аминокарбонил]этила, тетрагидрофурила, метиламинокарбонилметила, (N,N-диметиламино)карбонилметила, изопропиламинокарбонилметила, циклопропиламинокарбонилметила, (2-пропенил)аминокарбонилметила, (2,2,2-трифторэтил)аминокарбонилциклопропила, (2-фторэтил)аминокарбонилметила, (2-хлорэтил)аминокарбонилметила, 1-(этиламинокарбонил)этила,

 и
и 
В других вариантах осуществления Z1 выбирают из группы, состоящей из водорода, метила, 2,2,2-трифторэтила, метоксиметила, этоксиметила, (2,2,2-трифторэтокси)метила, изопропоксиметила, этиламинокарбонилметила, 2,2-диметоксиэтила, 2-пропиниламинокарбонилметила, N-фенил-N-метиламино, (2,2,2-трифторэтил)аминокарбонилметила, 1-[(2,2,2-трифторэтил)аминокарбонил]этила, тетрагидрофурила,
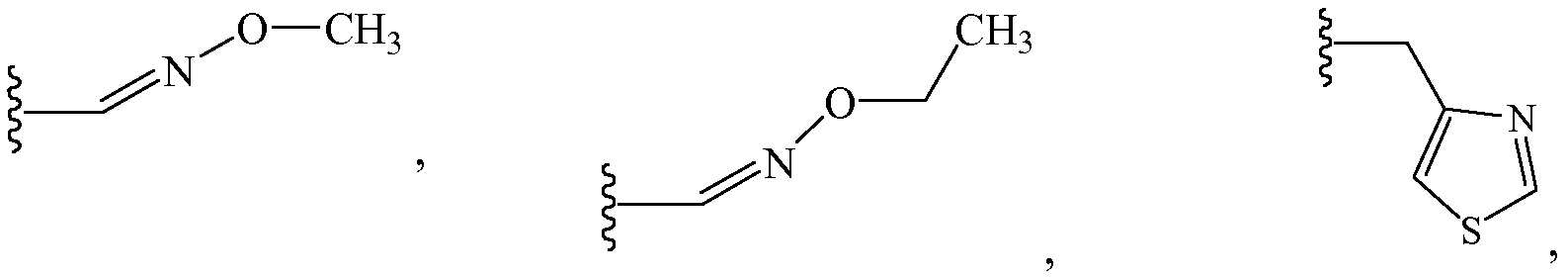
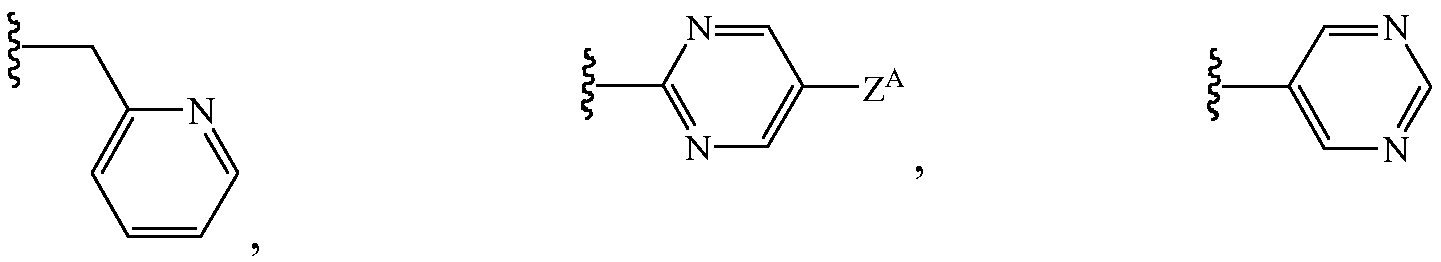 и
и 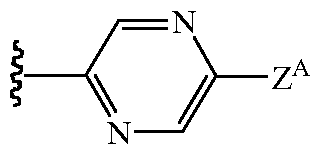
В других вариантах осуществления Z1 выбирают из группы, состоящей из водорода, метила, метоксиметила, этоксиметила, (2,2,2-трифторэтокси)метила, изопропоксиметила, этиламинокарбонилметила, 2,2-диметоксиэтила, 2-пропиниламинокарбонилметила, N-фенил-N-метиламино, (2,2,2-трифторэтил)аминокарбонилметила, 1-[(2,2,2-трифторэтил)аминокарбонил]этила, тетрагидрофурила,

 и
и 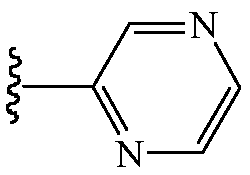
В других вариантах осуществления Z1 выбирают из группы, состоящей из водорода, метила, метоксиметила, этоксиметила, (2,2,2-трифторэтокси)метила, изопропоксиметила, этиламинокарбонилметила, 2-пропиниламинокарбонилметила, (2,2,2-трифторэтил)аминокарбонилметила, тетрагидрофурила,

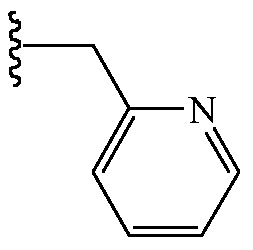 и
и 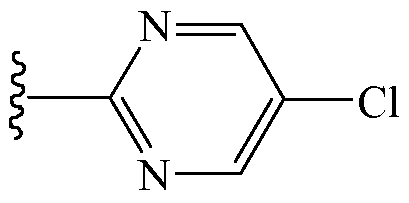
В других вариантах осуществления Z1 выбирают из группы, состоящей из водорода, метоксиметила, этоксиметила, (2,2,2-трифторэтокси)метила, этиламинокарбонилметила, 2,2-диметоксиэтила, 2-пропиниламинокарбонилметила, N-фенил-N-метиламино, (2,2,2-трифторэтил)аминокарбонилметила, 1-[(2,2,2-трифторэтил)аминокарбонил]этила, тетрагидрофурила,

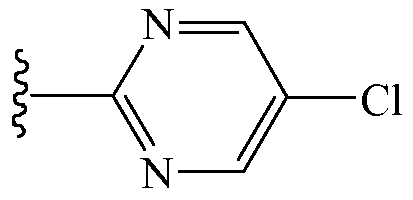 и
и 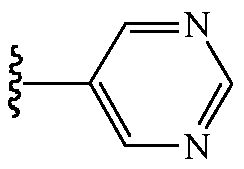
В других вариантах осуществления Z1 выбирают из группы, состоящей из N-фенил-N-метиламино,
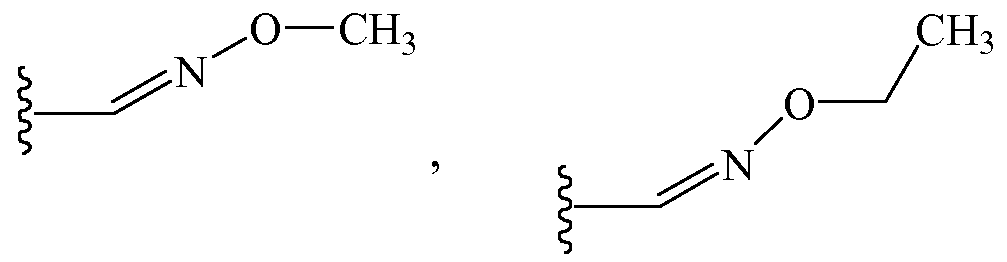 и
и 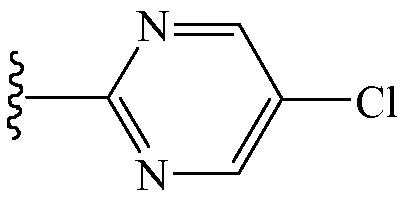
В других вариантах осуществления Z1 выбирают из группы, состоящей из водорода, (2,2,2-трифторэтокси)метила,
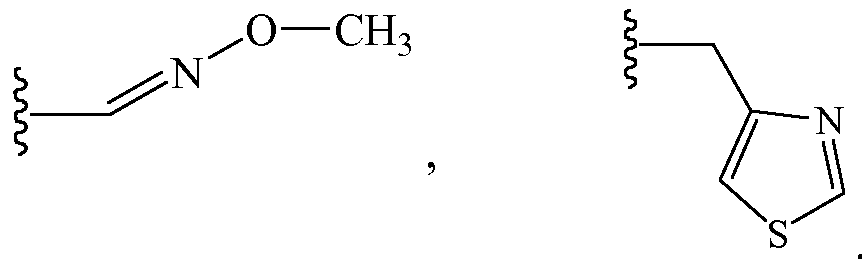 и
и 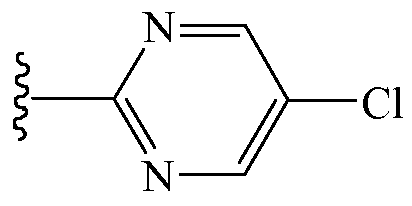
В других вариантах осуществления Z1 выбирают из группы, состоящей из водорода, (2,2,2-трифторэтокси)метила, этиламинокарбонилметила, 2-пропиниламинокарбонилметила, N-фенил-N-метиламино, (2,2,2-трифторэтил)аминокарбонилметила, 1-[(2,2,2-трифторэтил)аминокарбонил]этила, тетрагидрофурила,
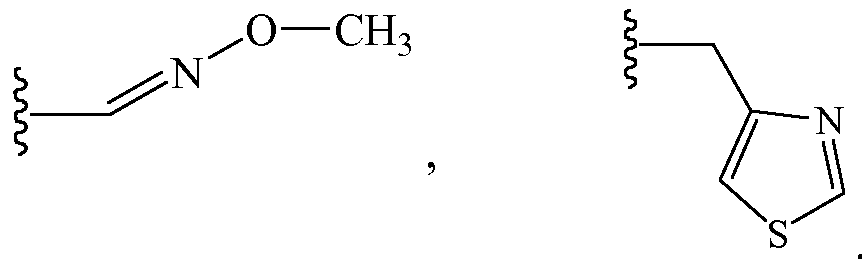 и
и 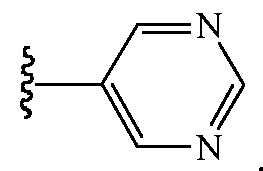
В других вариантах осуществления Z1 выбирают из группы, состоящей из 1-[(2,2,2-трифторэтил)аминокарбонил]этила, метиламинокарбонилметила, (N,N-диметиламино)карбонилметила, изопропиламинокарбонилметила, циклопропиламинокарбонилметила, (2-пропенил)аминокарбонилметила, (2,2,2-трифторэтил)аминокарбонилциклопропила, (2-фторэтил)аминокарбонилметила, (2-хлорэтил)аминокарбонилметила, 1-(этиламинокарбонил)этила,
 и
и 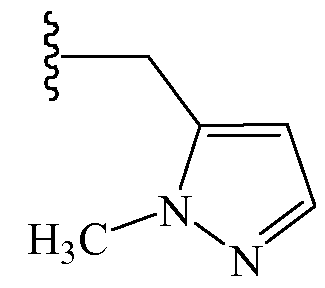
В других вариантах осуществления Z1 выбирают из группы, состоящей из этиламинокарбонилметила, 2-пропиниламинокарбонилметила, (2,2,2-трифторэтил)аминокарбонилметила, тетрагидрофурила,
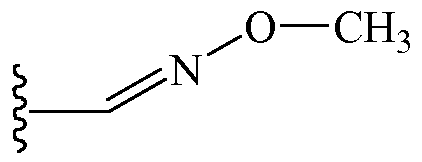 и
и 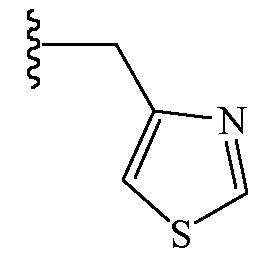
В других вариантах осуществления Z1 выбирают из группы, состоящей из метоксиметила, этоксиметила, этиламинокарбонилметила, 2-пропиниламинокарбонилметила, (2,2,2-трифторэтил)аминокарбонилметила, тетрагидрофурила,
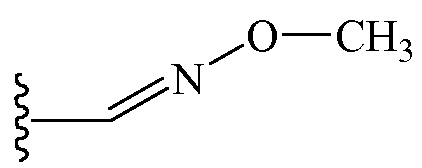 и
и 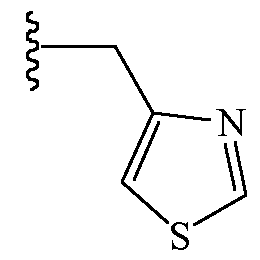
В других вариантах осуществления Z1 выбирают из группы, состоящей из метоксиметила, этоксиметила и тетрагидрофурила.
В других таких вариантах осуществления Z1 представляет собой
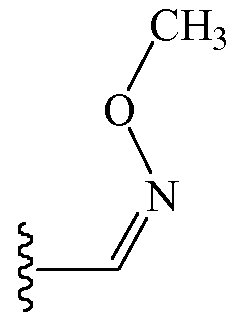
В других вариантах осуществления Z1 представляет собой галогенэтиламинокарбонилметил. В некоторых таких вариантах осуществления Z1 представляет собой (2,2,2-трифторэтил)аминокарбонилметил.
Когда Z1 представляет собой водород, Z2 выбирают из группы, состоящей из метилкарбонила, этилкарбонила, пропилкарбонила, циклопропилкарбонила, метоксикарбонила, метоксиметилкарбонила и аминокарбонила. В некоторых таких вариантах осуществления Z2 представляет собой метоксикарбонил. В других вариантах осуществления Z2 представляет собой аминокарбонил.
Когда Z1 представляет собой независимый заместитель иной, чем водород, Z2 выбирают из группы, состоящей из водорода, этила, метоксиметила, галогенметоксиметила, этоксиметила, галогенэтоксиметила, пропоксиметила, метилкарбонила, этилкарбонила, пропилкарбонила, циклопропилкарбонила, метоксикарбонила, метоксиметилкарбонила, аминокарбонила, этиламинокарбонилметила, этиламинокарбонилэтила, диметоксиэтила, пропиниламинокарбонилметила, галогенэтиламинокарбонилметила и галогенэтиламинокарбонилэтила.
В некоторых вариантах осуществления, когда Z1 представляет собой независимый заместитель иной, чем водород, Z2 выбирают из группы, состоящей из водорода, этила, метоксиметила, галогенметоксиметила, этоксиметила, галогенэтоксиметила, пропоксиметила, метилкарбонила, этилкарбонила, пропилкарбонила, циклопропилкарбонила, метоксикарбонила, метоксиметилкарбонила, аминокарбонила, этиламинокарбонилметила, этиламинокарбонилэтила, диметоксиэтила, пропиниламинокарбонилметила, галогенэтиламинокарбонилметила и галогенэтиламинокарбонилэтила.
В некоторых вариантах осуществления, когда Z1 представляет собой независимый заместитель иной, чем водород, Z2 представляет собой водород.
В некоторых вариантах осуществления, когда Z1 представляет собой независимый заместитель иной, чем водород, Z2 представляет собой этил.
В некоторых вариантах осуществления, когда Z1 представляет собой независимый заместитель иной, чем водород, Z2 представляет собой метоксиметил.
В некоторых вариантах осуществления, когда Z1 представляет собой независимый заместитель иной, чем водород, Z2 представляет собой метилкарбонил.
В некоторых вариантах осуществления, когда Z1 представляет собой независимый заместитель иной, чем водород, Z2 представляет собой этилкарбонил.
В некоторых вариантах осуществления, когда Z1 представляет собой независимый заместитель иной, чем водород, Z2 представляет собой изопропилкарбонил.
В некоторых вариантах осуществления, когда Z1 представляет собой независимый заместитель иной, чем водород, Z2 представляет собой циклопропилкарбонил.
В некоторых вариантах осуществления, когда Z1 представляет собой независимый заместитель иной, чем водород, Z2 представляет собой метоксикарбонил.
В некоторых вариантах осуществления, когда Z1 представляет собой независимый заместитель иной, чем водород, Z2 представляет собой метоксиметилкарбонил.
В некоторых вариантах осуществления, когда Z1 представляет собой независимый заместитель иной, чем водород, Z2 выбирают из группы, состоящей из водорода, метилкарбонила и этилкарбонила.
В некоторых вариантах осуществления Z1 и Z2 вместе образуют один заместитель, отличный от независимых заместителей. В таких вариантах осуществления Z1 и Z2 вместе образуют структуру
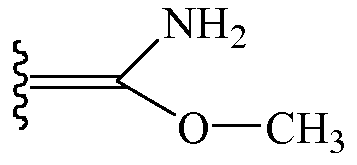
В таких вариантах осуществления изоксазолин соответствует структуре
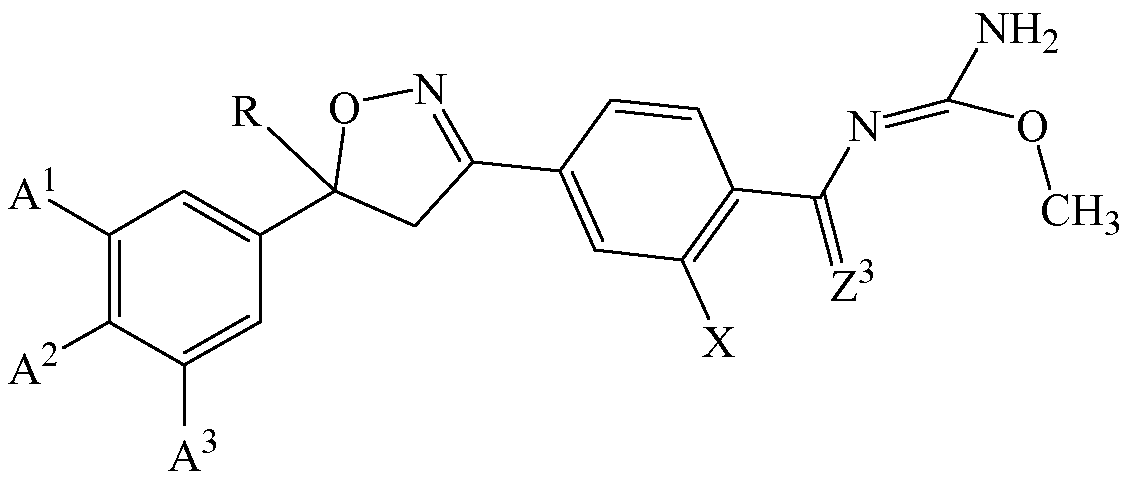
В некоторых вариантах осуществления Z1 и Z2 вместе образуют один заместитель, отличный от независимых заместителей. В таких вариантах осуществления Z1 и Z2 вместе образуют структуру
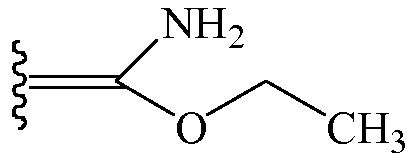
В таких вариантах осуществления изоксазолин соответствует структуре
F. Предпочтительные варианты осуществления Z3
В некоторых вариантах осуществления Z3 представляет собой О (т.е. атом кислорода). В других вариантах осуществления Z3 представляет собой S (т.е. атом серы).
G. Предпочтительные варианты осуществления ZA
ZA выбирают из группы, состоящей из водорода, галогена и циано. В некоторых таких вариантах осуществления ZA представляет собой водород. В других вариантах осуществления ZA представляет собой бром. В других вариантах осуществления ZA представляет собой хлор. В других вариантах осуществления ZA представляет собой циано.
Н. Иллюстративные комбинации заместителей
Приведенные ниже комбинации заместителей являются просто иллюстративными и не имеют какого-либо особого предпочтения.
Н1. Иллюстративная комбинация заместителей № 1
В некоторых вариантах осуществления А1 и А3 выбирают независимо из группы, состоящей из галогена и галогенметила, и А2 представляет собой водород. В некоторых таких вариантах осуществления, например, каждый из А1 и А3 представляет собой хлор, так что изоксазолин имеет структурную формулу
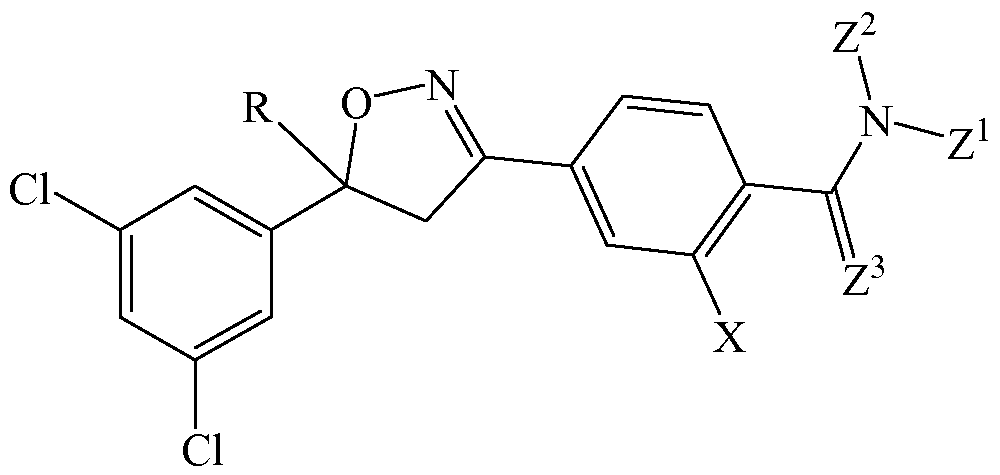
Н2. Иллюстративная комбинация заместителей № 2
В некоторых вариантах осуществления Z1 и Z2 либо представляют собой независимые заместители, либо вместе образуют один заместитель следующим образом:
когда Z1 и Z2 представляют собой независимые заместители,
Z1 выбирают независимо из группы, состоящей из водорода, метила, галогенэтила, галогенпропила, галогенбутила, метоксиметила, галогенметоксиметила, этоксиметила, галогенэтоксиметила, пропоксиметила, этиламинокарбонилметила, этиламинокарбонилэтила, диметоксиэтила, пропиниламинокарбонилметила, N-фенил-N-метиламино, галогенэтиламинокарбонилметила, галогенэтиламинокарбонилэтила, тетрагидрофурила,
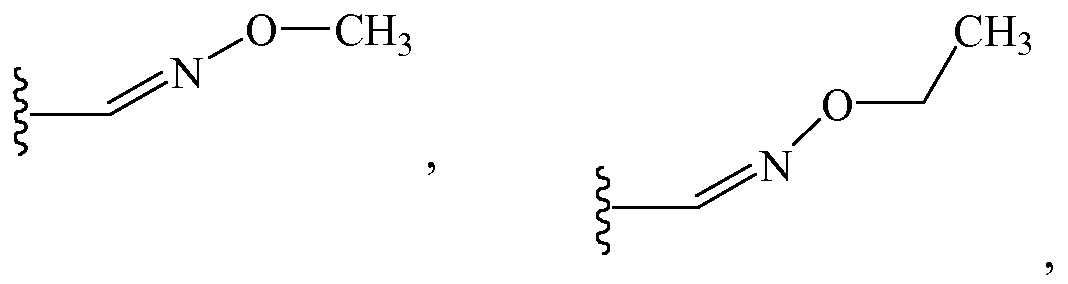

 и
и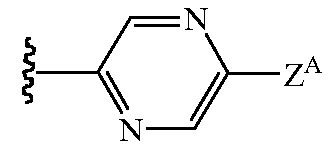 ;
;
когда Z1 представляет собой водород, и Z2 выбирают из группы, состоящей из метилкарбонила, этилкарбонила, пропилкарбонила, циклопропилкарбонила, метоксикарбонила, метоксиметилкарбонила и аминокарбонила;
когда Z1 является иным, чем водород, и Z2 выбирают независимо из группы, состоящей из водорода, этила, метоксиметила, галогенметоксиметила, этоксиметила, галогенэтоксиметила, пропоксиметила, метилкарбонила, этилкарбонила, пропилкарбонила, циклопропилкарбонила, метоксикарбонила, метоксиметилкарбонила, аминокарбонила, этиламинокарбонилметила, этиламинокарбонилэтила, диметоксиэтила, пропиниламинокарбонилметила, галогенэтиламинокарбонилметила и галогенэтиламинокарбонилэтила;
когда Z1 и Z2 вместе образуют один заместитель, они образуют

Н3. Иллюстративная комбинация заместителей № 3
В некоторых вариантах осуществления заместители в формуле (I) имеют значения, указанные ниже.
А1 выбирают из группы, состоящей из хлора, брома и трифторметила.
А2 выбирают из группы, состоящей из водорода, хлора и фтора.
А3 выбирают из группы, состоящей из хлора, брома и трифторметила.
R выбирают из группы, состоящей из монохлорметила, трифторметила и монохлордифторметила.
Х выбирают из группы, состоящей из водорода, брома, йода, хлора, метила, этила и трифторметила.
Z3 представляет собой О.
ZA выбирают из группы, состоящей из водорода, брома, хлора и циано.
В некоторых таких вариантах осуществления Z1 и Z2 являются независимыми заместителями, так что
Z1 выбирают из группы, состоящей из водорода, метила, 2,2,2-трифторэтила, метоксиметила, этоксиметила, (2,2,2-трифторэтокси)метила, изопропоксиметила, этиламинокарбонилметила, 2,2-диметоксиэтила, 2-пропиниламинокарбонилметила, N-фенил-N-метиламино, (2,2,2-трифторэтил)аминокарбонилметила, 1-[(2,2,2-трифторэтил)аминокарбонил]этила, тетрагидрофурила,
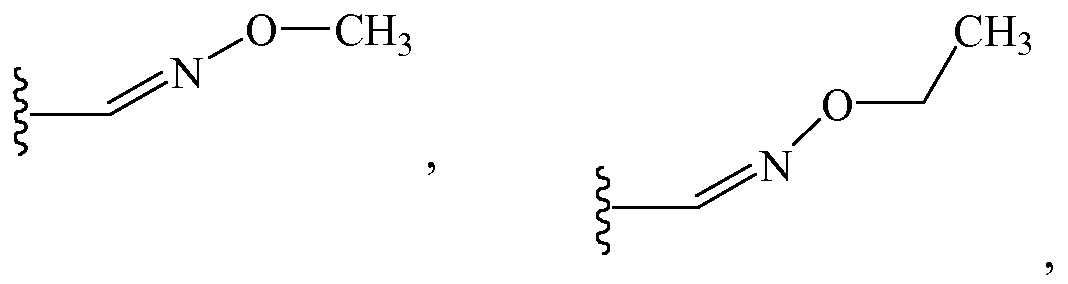


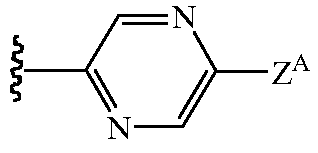 и
и 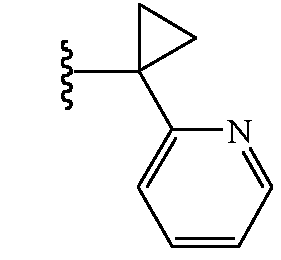 ;
;
когда Z1 представляет собой водород, Z2 выбирают из группы, состоящей из метоксикарбонила и аминокарбонила;
когда Z1 является иным, чем водород, Z2 выбирают из группы, состоящей из водорода, этила, метоксиметила, метилкарбонила, этилкарбонила, изопропилкарбонила, циклопропилкарбонила, метоксикарбонила и метоксиметилкарбонила.
В других таких вариантах осуществления Z1 и Z2 вместе образуют

Н4. Иллюстративная комбинация заместителей № 4
В некоторых вариантах осуществления Z1 и Z2 либо представляют собой независимые заместители, либо образуют вместе один заместитель следующим образом:
когда Z1 и Z2 представляют собой независимые заместители,
Z1 выбирают из группы, состоящей из водорода, метила, 2,2,2-трифторэтила, метоксиметила, этоксиметила, (2,2,2-трифторэтокси)метила, изопропоксиметила, этиламинокарбонилметила, 2,2-диметоксиэтила, 2-пропиниламинокарбонилметила, N-фенил-N-метиламино, (2,2,2-трифторэтил)аминокарбонилметила, 1-[(2,2,2-трифторэтил)аминокарбонил]этила, тетрагидрофурила,
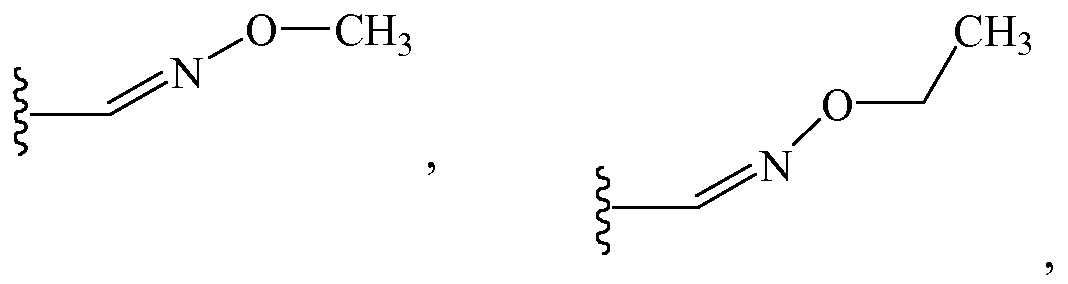

 и
и  ;
;
когда Z1 представляет собой водород, Z2 выбирают из группы, состоящей из метоксикарбонила и аминокарбонила;
когда Z1 является иным, чем водород, Z2 выбирают из группы, состоящей из водорода, этила, метоксиметила, метилкарбонила, этилкарбонила, изопропилкарбонила, циклопропилкарбонила, метоксикарбонила и метоксиметилкарбонила;
когда Z1 и Z2 вместе образуют один заместитель, они образуют

Примеры изоксазолинов, охваченных такими вариантами осуществления, включают следующие структуры:
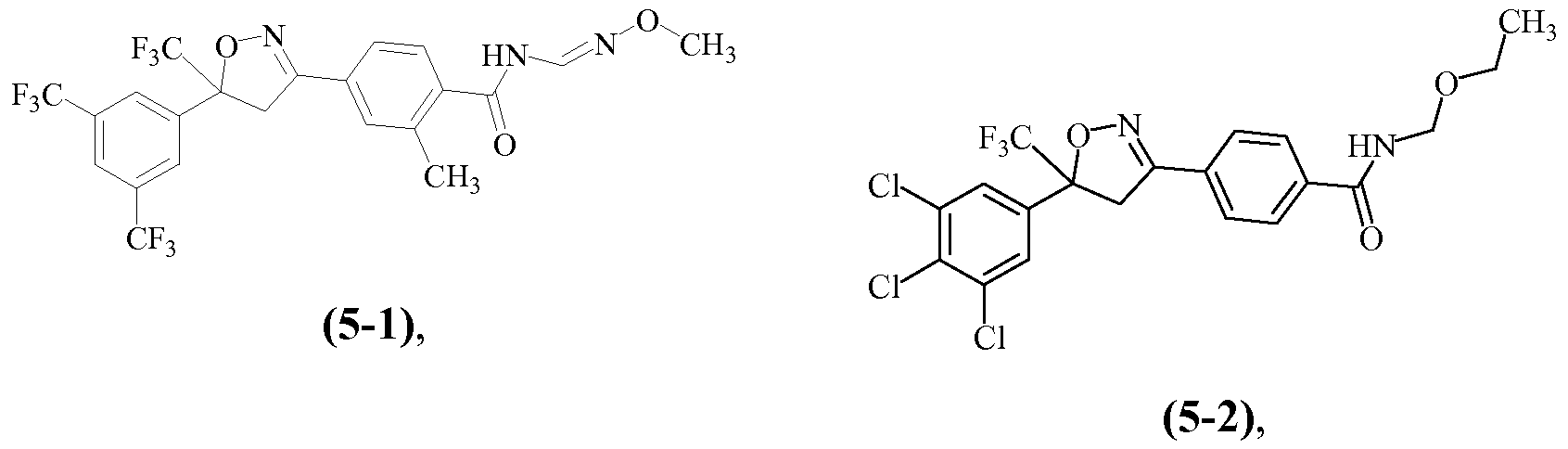
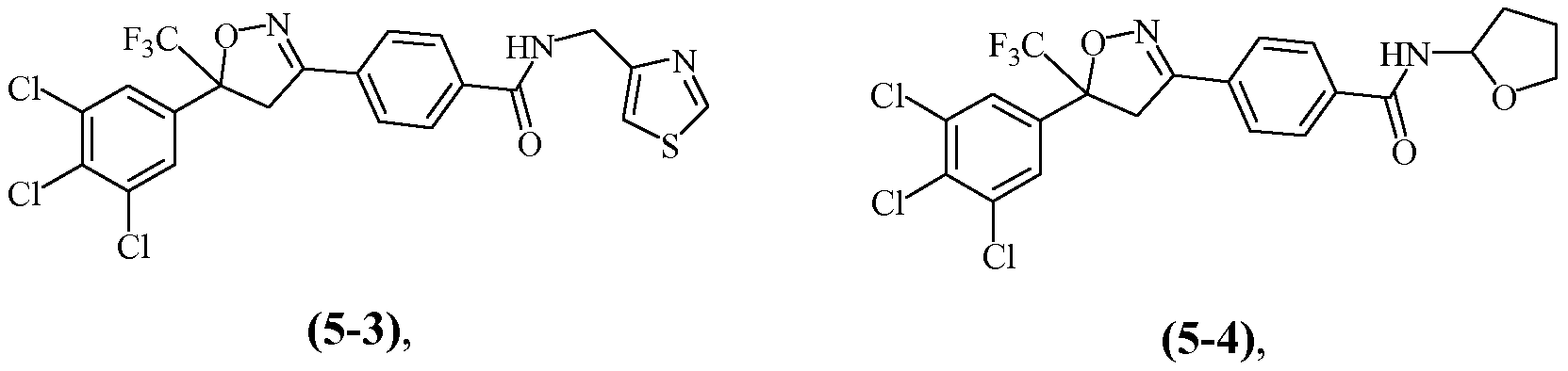
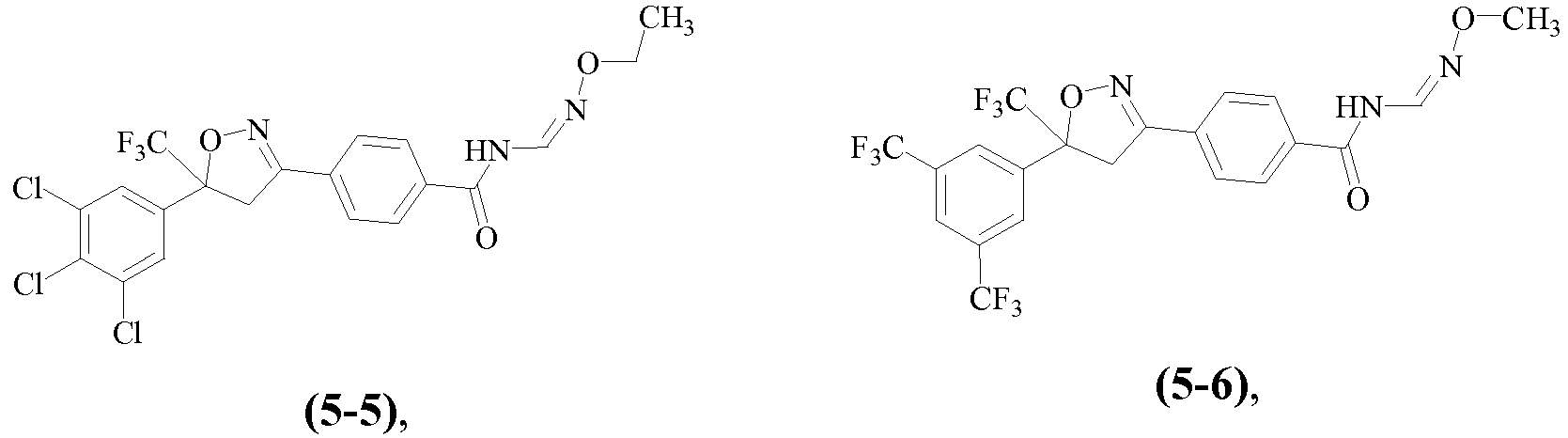
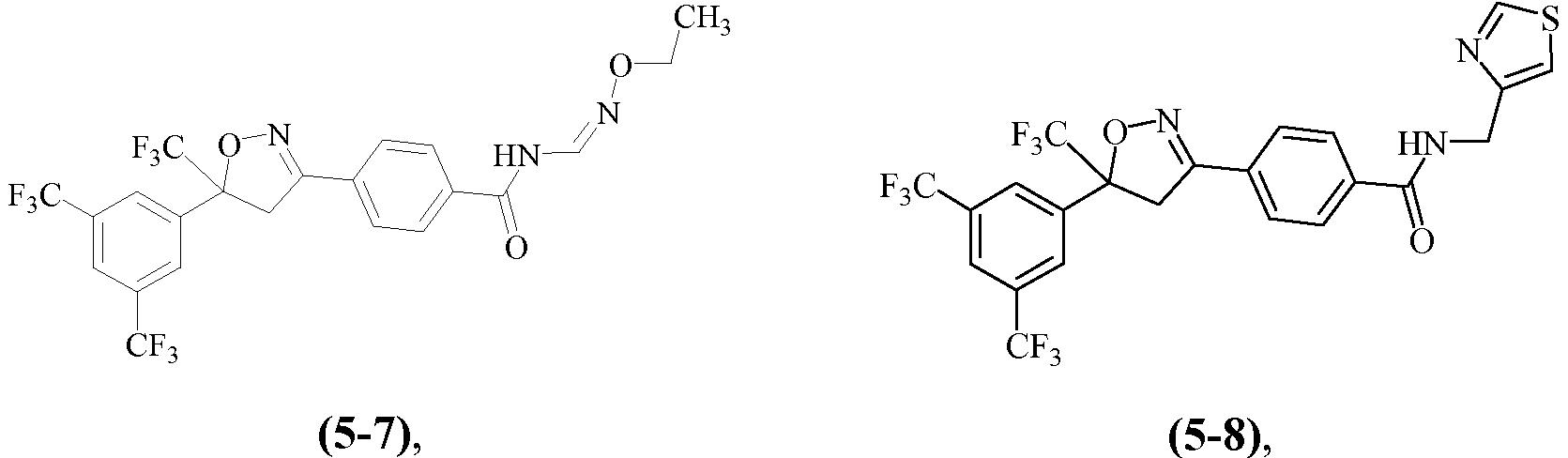
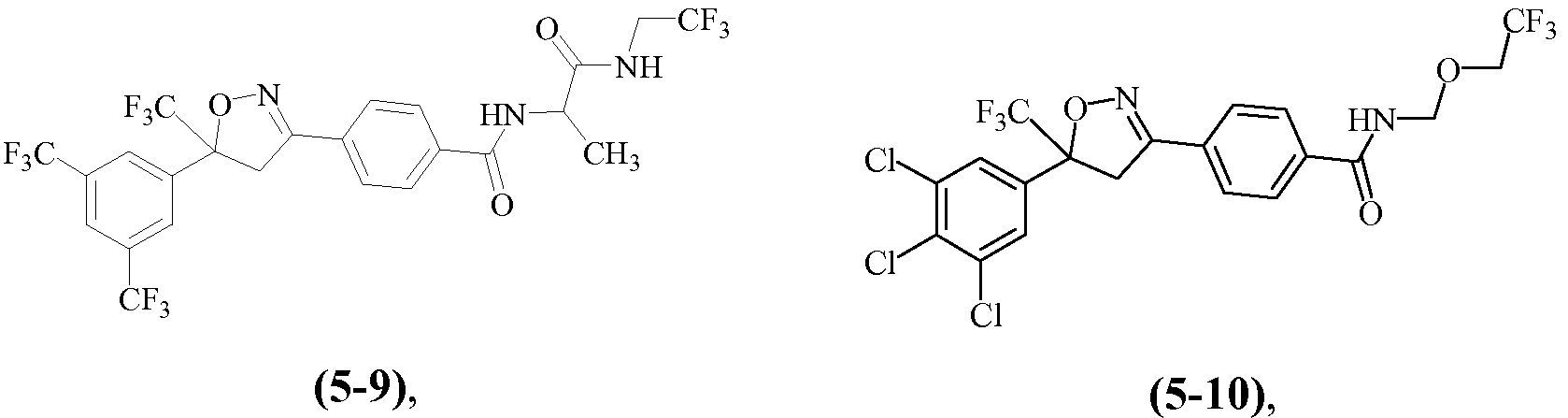
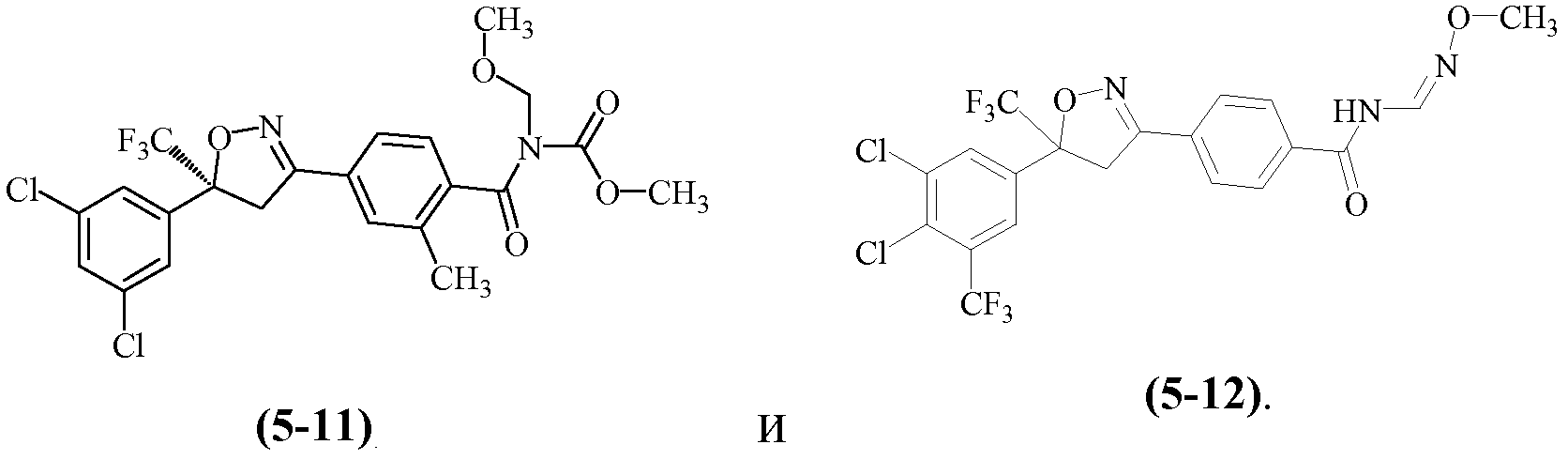
Н5. Иллюстративная комбинация заместителей № 5
В некоторых вариантах осуществления изоксазолины формулы (I) имеют значения, указанные ниже.
Изоксазолин соответствует структуре
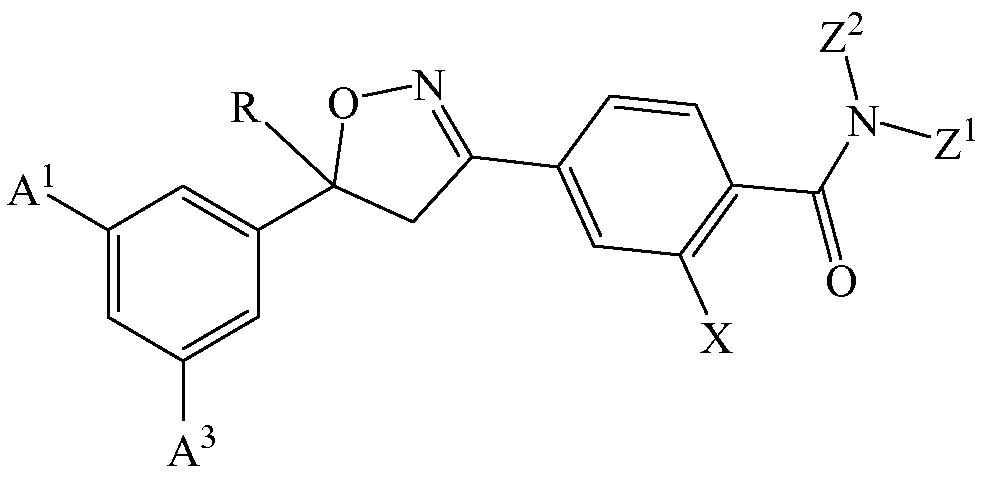
А1 выбирают из группы, состоящей из хлора и брома.
А3 выбирают из группы, состоящей из хлора и брома.
Х выбирают из группы, состоящей из водорода, брома, йода, хлора, метила, этила и трифторметила.
В некоторых таких вариантах осуществления Z1 и Z2 представляют собой независимые заместители, так что
Z1 выбирают из группы, состоящей из водорода, метила, 2,2,2-трифторэтила, метоксиметила, этоксиметила, (2,2,2-трифторэтокси)метила, изопропоксиметила, этиламинокарбонилметила, 2,2-диметоксиэтила, 2-пропиниламинокарбонилметила, N-фенил-N-метиламино, (2,2,2-трифторэтил)аминокарбонилметила, 1-[(2,2,2-трифторэтил)аминокарбонил]этила, тетрагидрофурила,
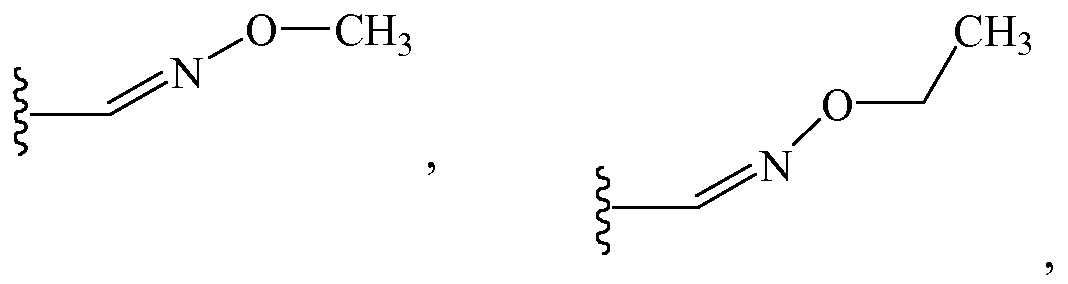

 и
и  ;
;
когда Z1 представляет собой водород, Z2 выбирают из группы, состоящей из метоксикарбонила и аминокарбонила;
когда Z1 является иным, чем водород, Z2 выбирают из группы, состоящей из водорода, этила, метоксиметила, метилкарбонила, этилкарбонила, изопропилкарбонила, циклопропилкарбонила, метоксикарбонила и метоксиметилкарбонила.
В других таких вариантах осуществления Z1 и Z2 вместе образуют

Примеры изоксазолинов, охваченных такими вариантами осуществления, включают следующие структуры:
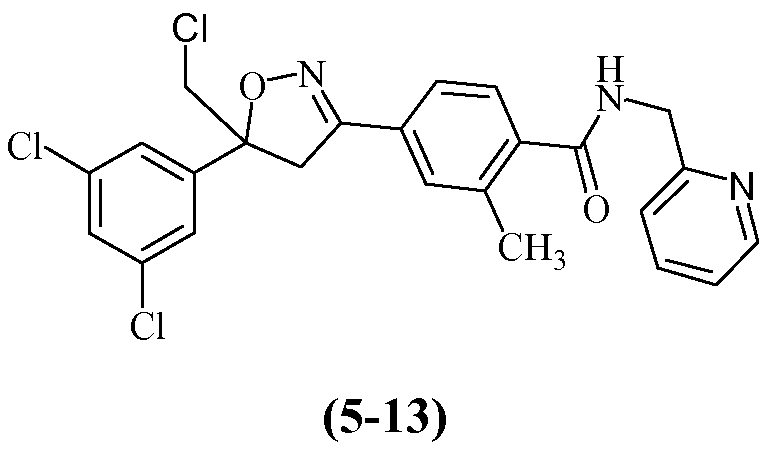 и
и 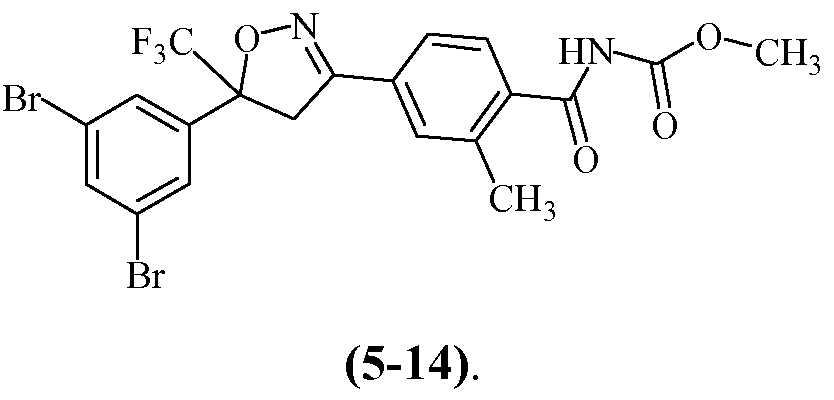
Еще другие примеры, охваченные такими вариантами осуществления, включают следующие структуры:
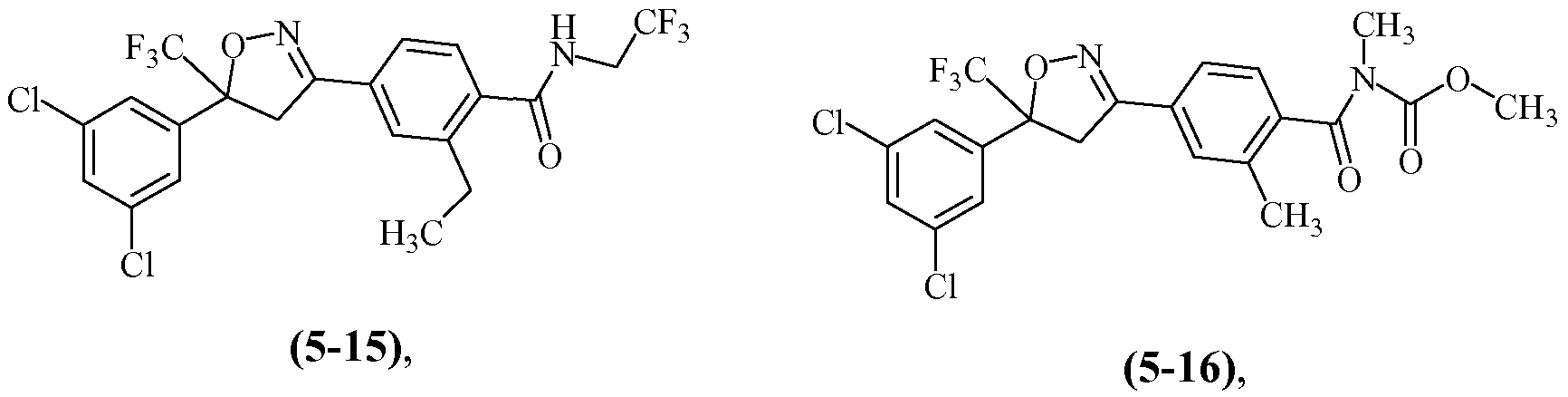
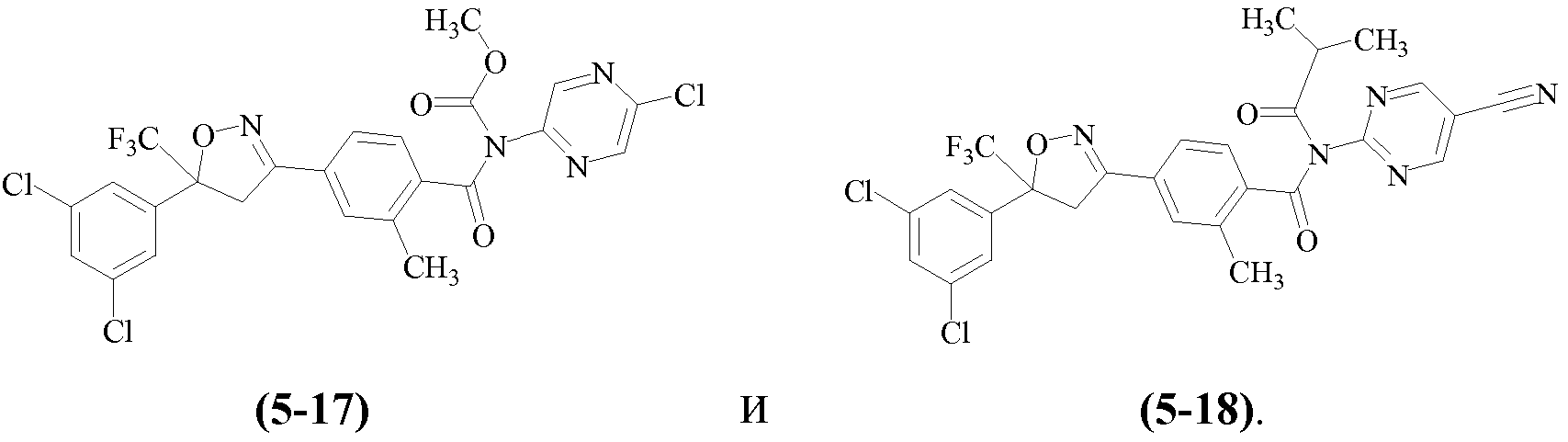
Н6. Иллюстративная комбинация заместителей № 6
В некоторых вариантах осуществления заместители в формуле (I) имеют значения, указанные ниже.
А1 и А3 выбирают независимо из группы, состоящей из хлора, брома и трифторметила.
А2 выбирают из группы, состоящей из водорода, хлора и фтора.
R выбирают из группы, состоящей из трифторметила и монохлордифторметила.
Х выбирают из группы, состоящей из водорода, брома, йода, хлора, метила и трифторметила.
Z3 представляет собой О.
ZA выбирают из группы, состоящей из брома, хлора и циано.
В некоторых таких вариантах осуществления Z1 и Z2 являются независимыми заместителями, так что
Z1 выбирают из группы, состоящей из водорода, метила, метоксиметила, этоксиметила, (2,2,2-трифторэтокси)метила, изопропоксиметила, этиламинокарбонилметила, 2,2-диметоксиэтила, 2-пропиниламинокарбонилметила, N-фенил-N-метиламино, (2,2,2-трифторэтил)аминокарбонилметила, 1-[(2,2,2-трифторэтил)аминокарбонил]этила, тетрагидрофурила,
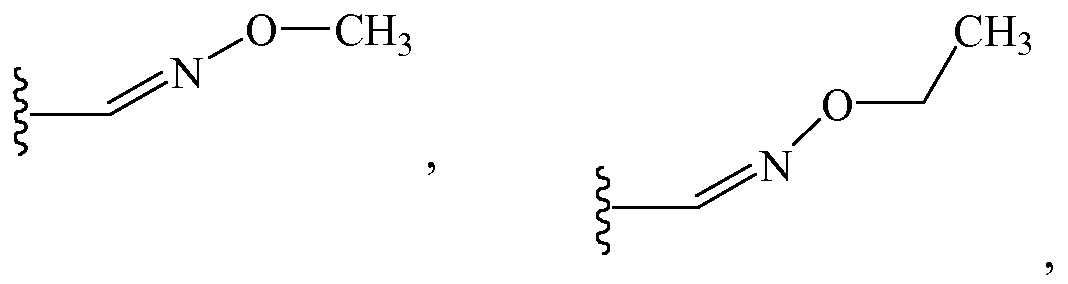

 и
и 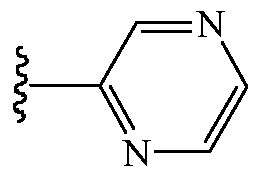 ;
;
когда Z1 представляет собой водород, Z2 представляет собой аминокарбонил;
когда Z1 является иным, чем водород, Z2 выбирают из группы, состоящей из водорода, этила, метоксиметила, метилкарбонила, этилкарбонила, изопропилкарбонила, циклопропилкарбонила, метоксикарбонила и метоксиметилкарбонила;
когда Z1 представляет собой водород, Z2 представляет собой аминокарбонил.
В других таких вариантах осуществления Z1 и Z2 вместе образуют

Согласно настоящему изобретению обнаружено, что изоксазолины таких вариантов осуществления имеют склонность проявлять особенно благоприятное подавление блох in vivo в пределах 24 и 48 часов после заражения. См., например, пример 3 ниже.
Примеры изоксазолинов, охваченных такими вариантами осуществления, включают следующие структуры:
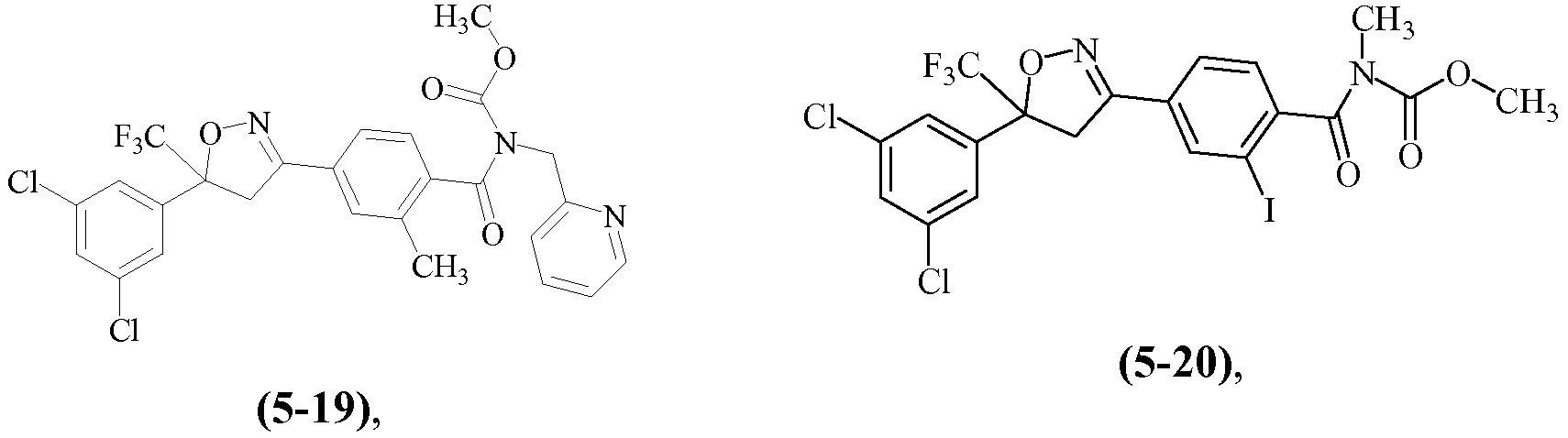
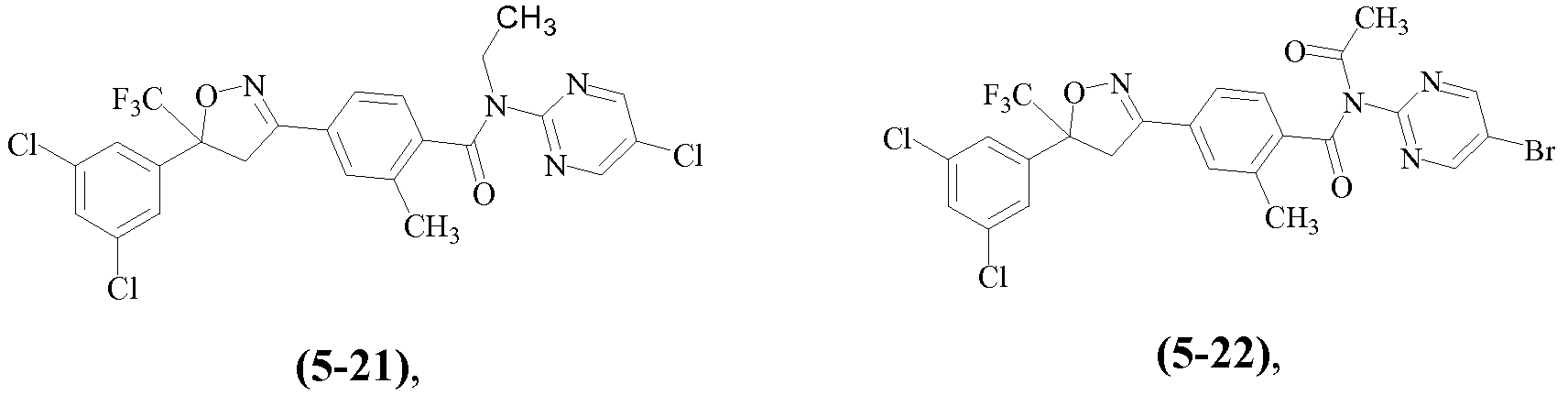
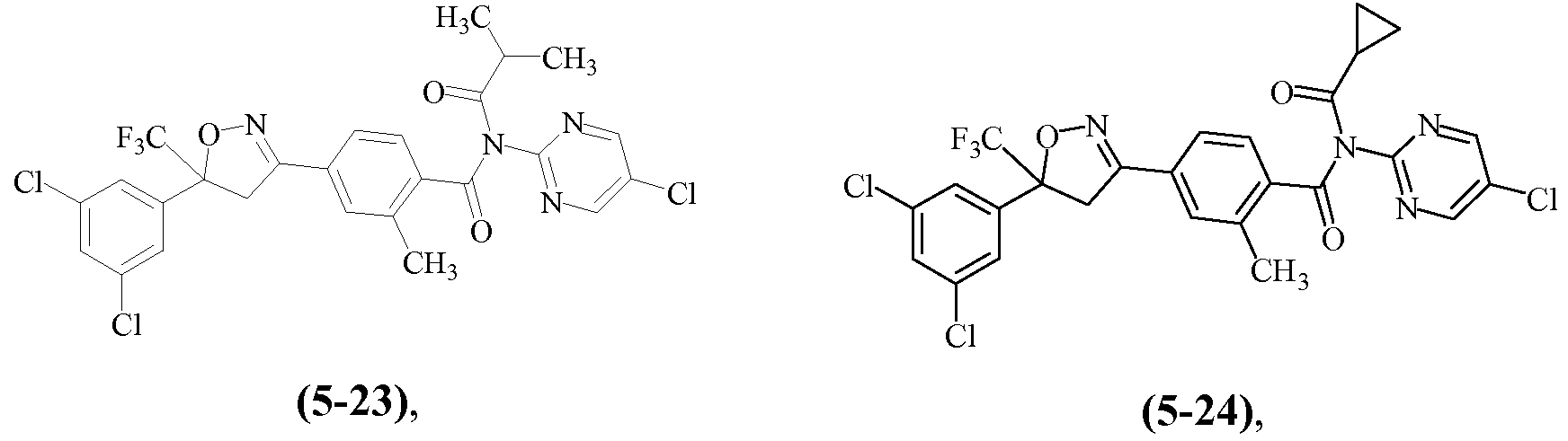
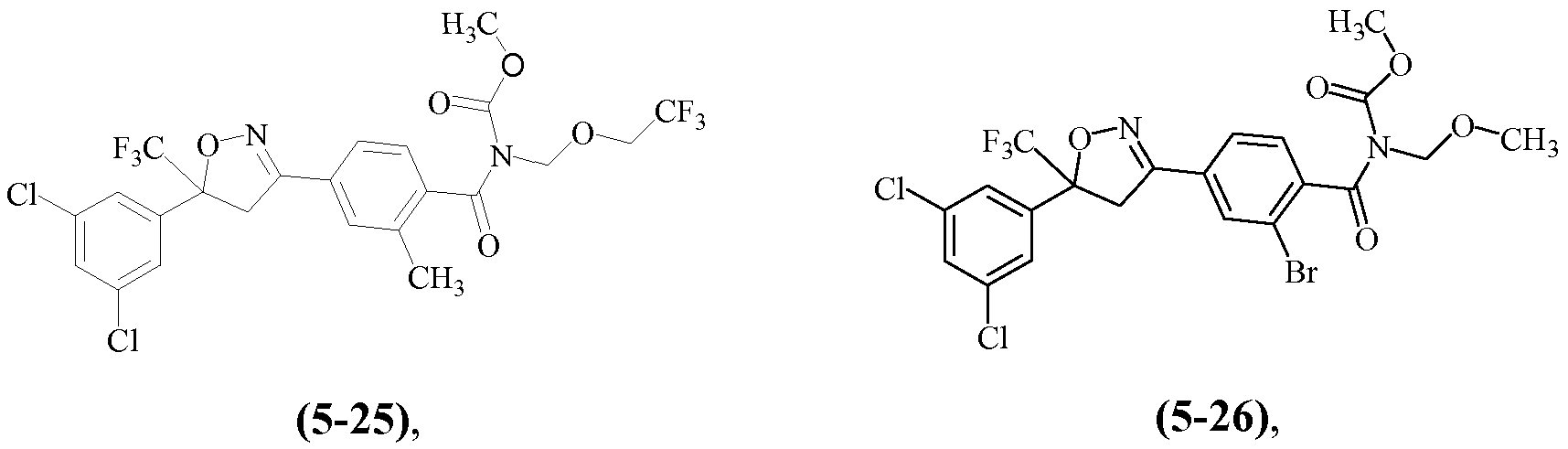
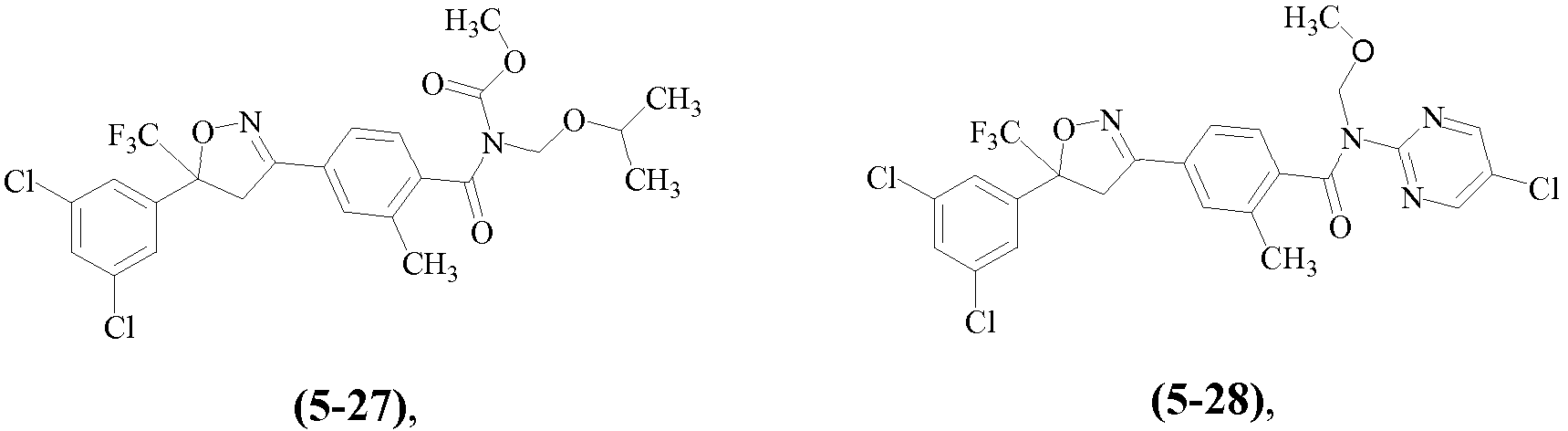
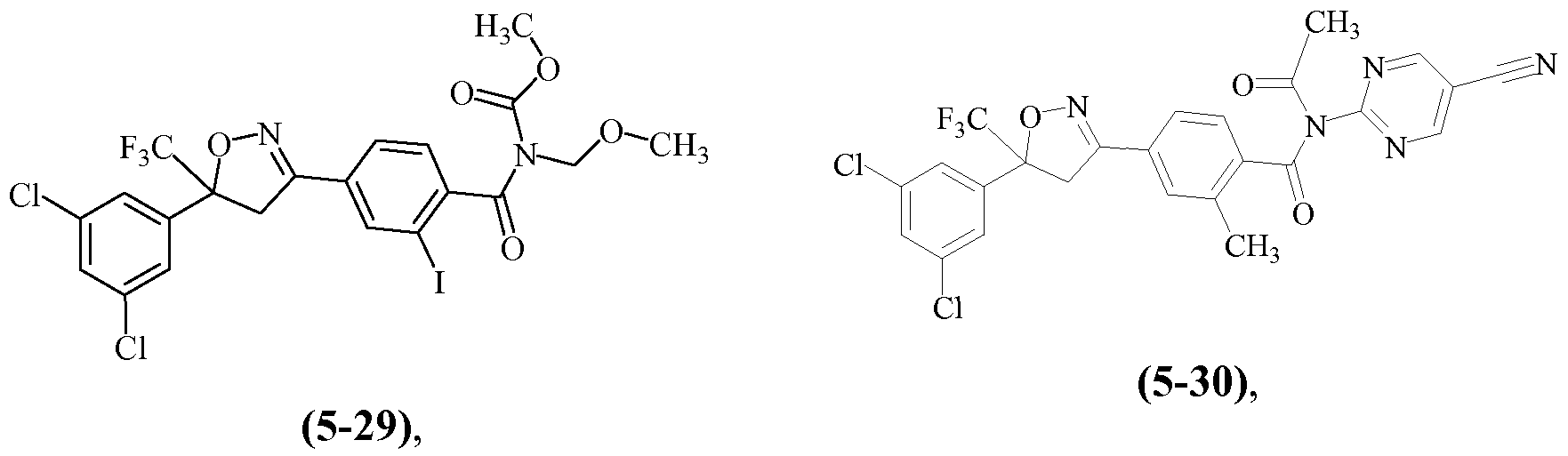
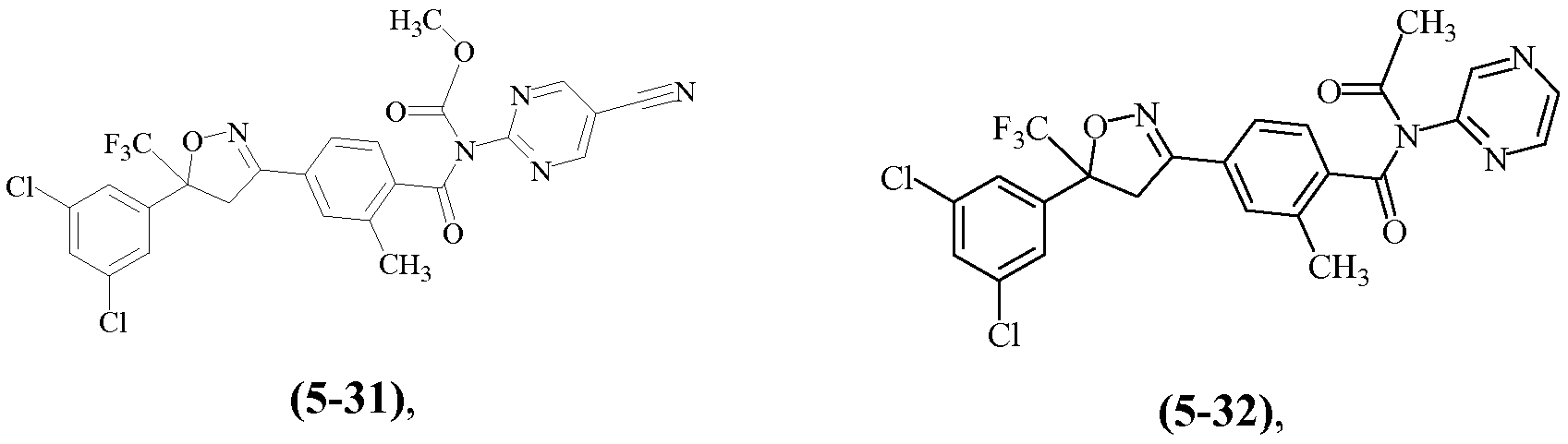
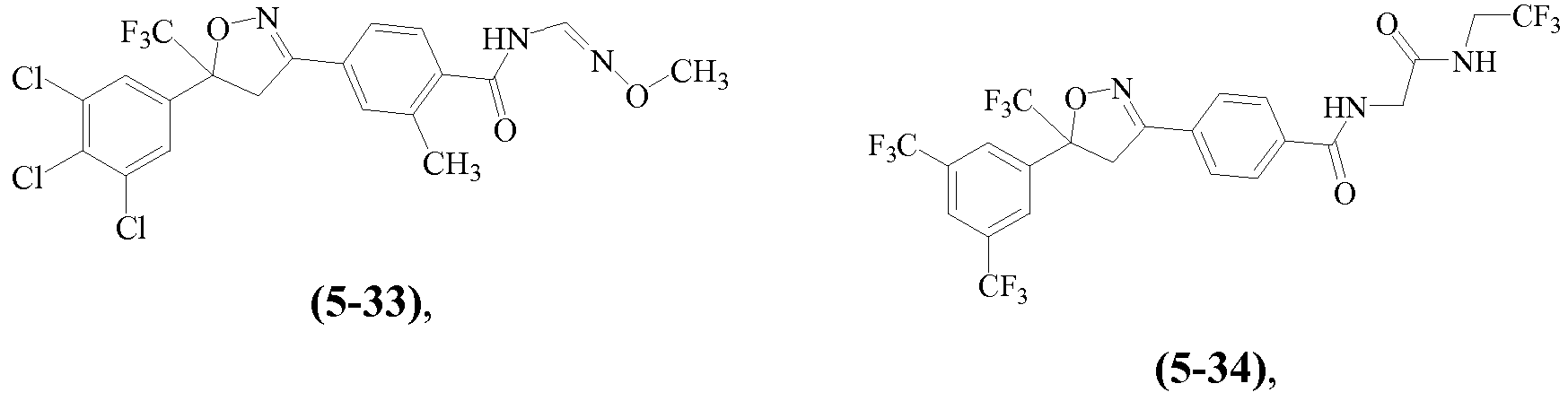
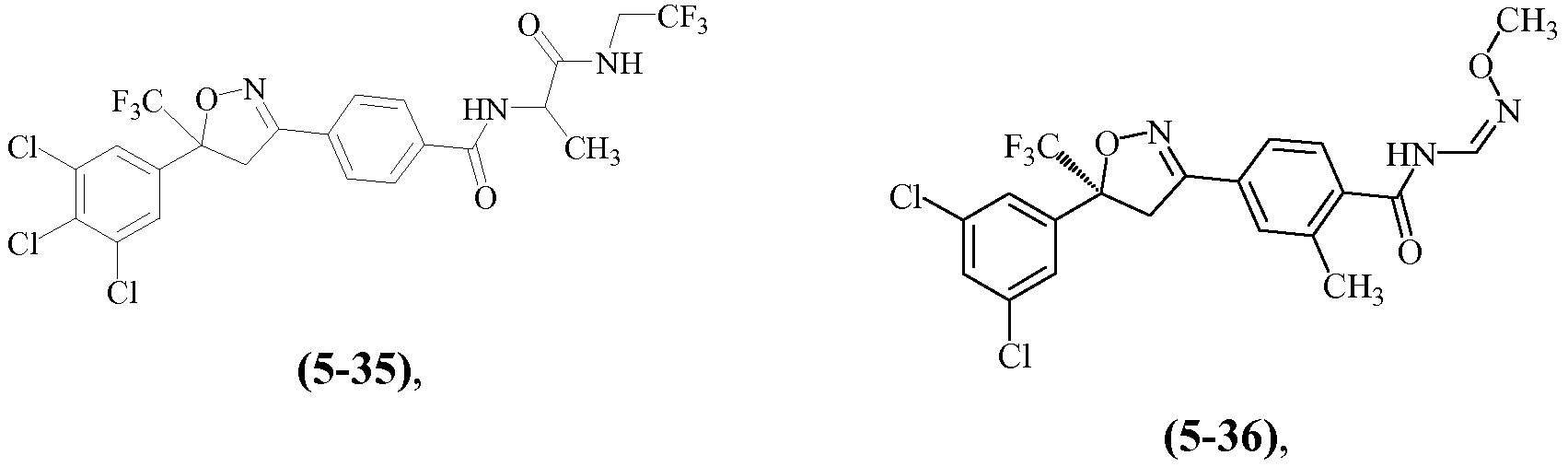
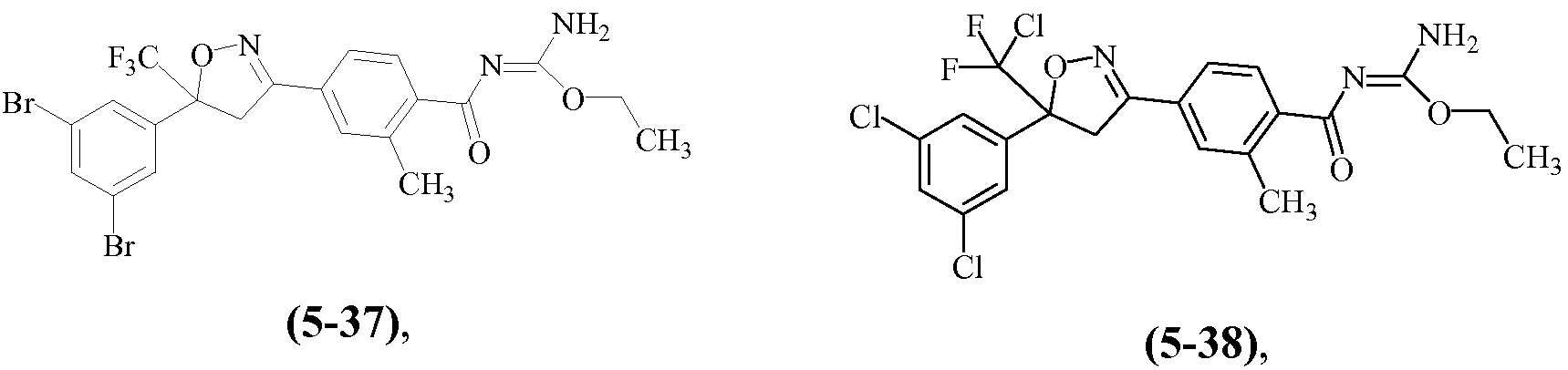
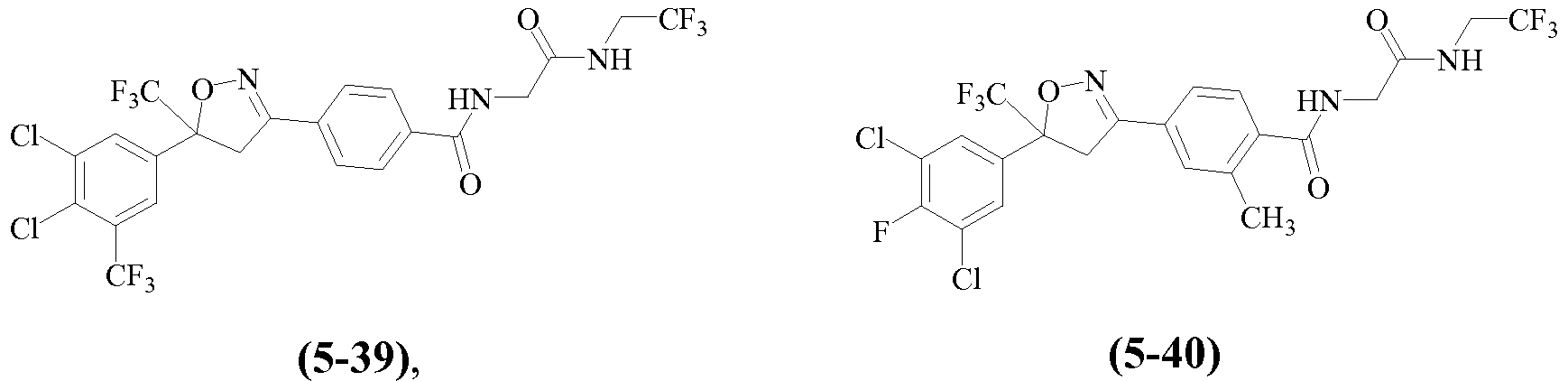 и
и 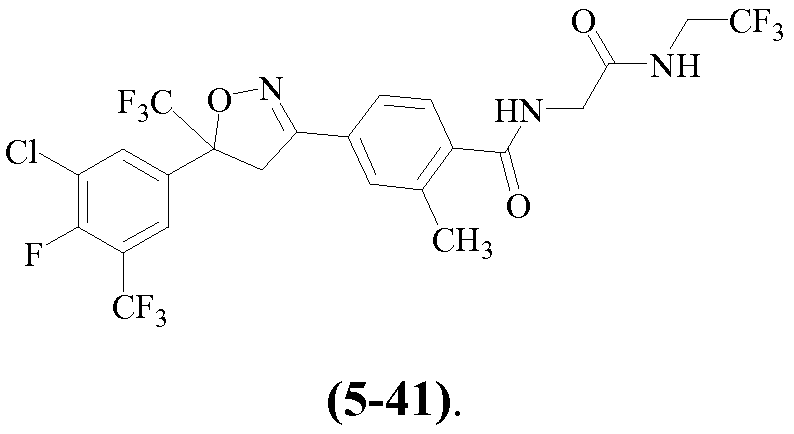
Еще другие примеры, охваченные такими вариантами осуществления, включают следующие структуры:
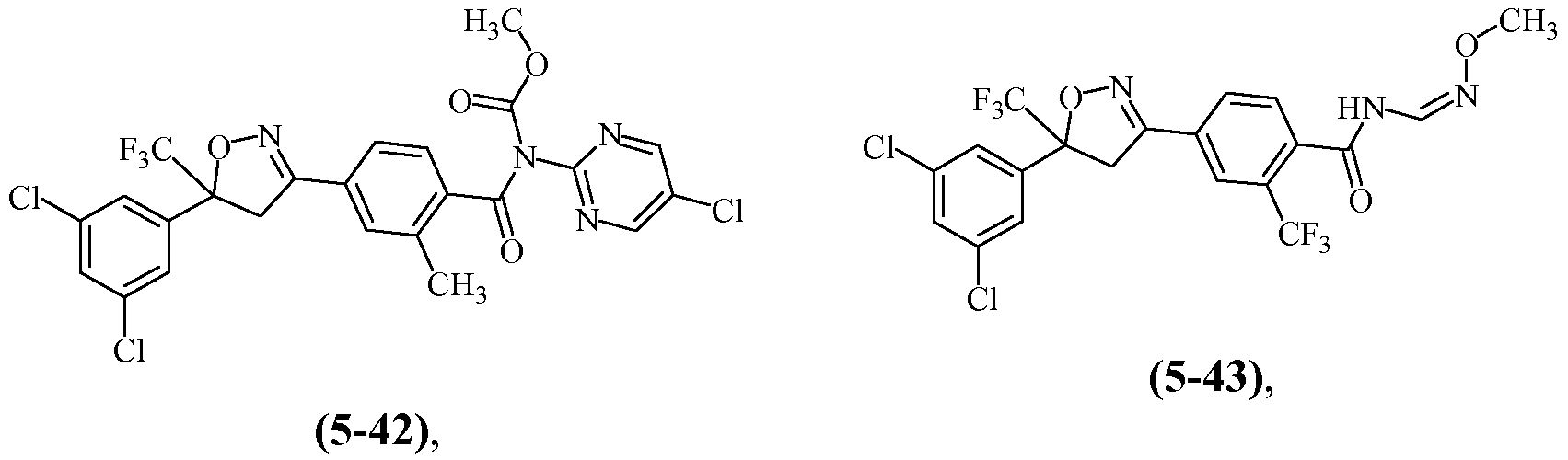
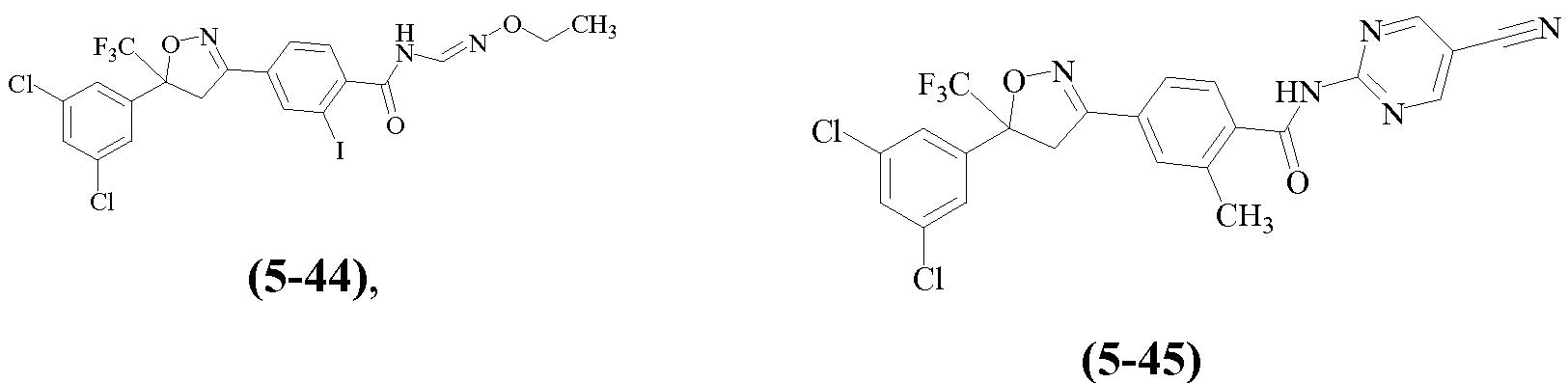 и
и 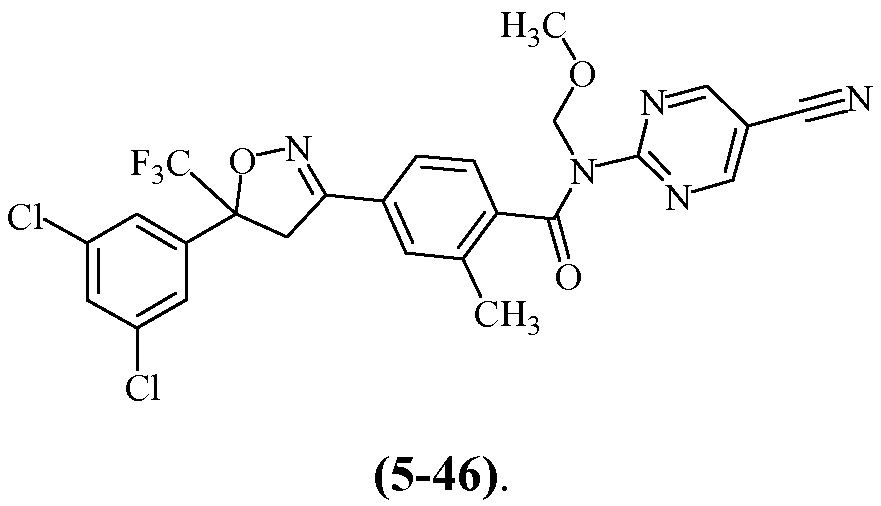
Н7. Иллюстративная комбинация заместителей № 7
В некоторых вариантах осуществления изоксазолин формулы (I) определен, как указано ниже.
Изоксазолин соответствует структуре
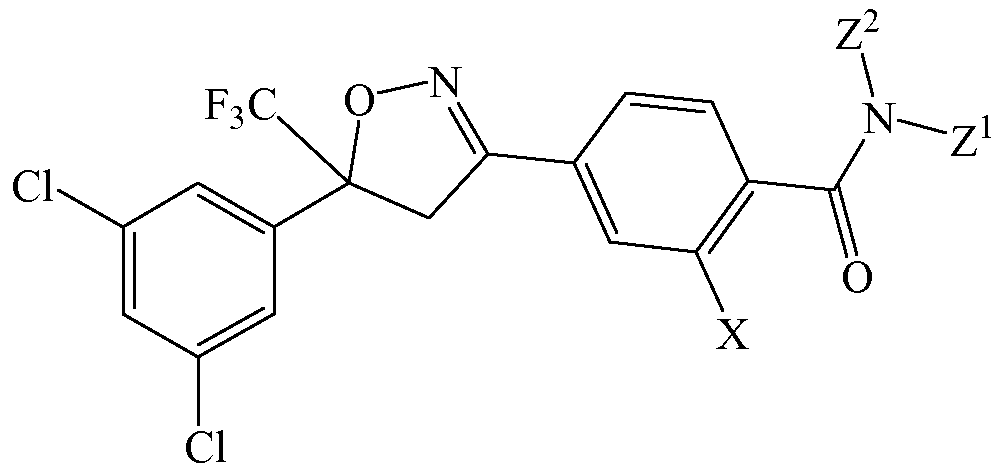
Х выбирают из группы, состоящей из хлора и метила.
Z1 выбирают из группы, состоящей из N-фенил-N-метиламино,
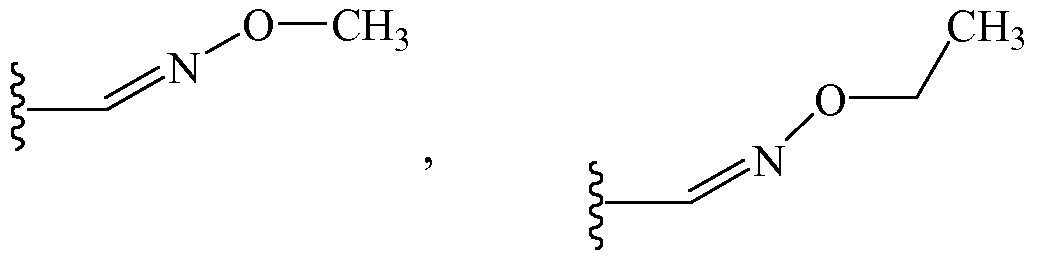 и
и 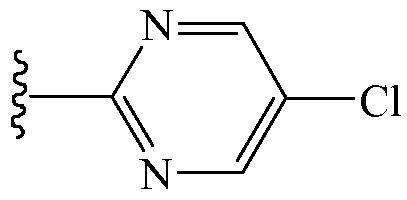
Z2 выбирают из группы, состоящей из водорода, этилкарбонила, метоксикарбонила и метоксиметилкарбонила.
Согласно настоящему изобретению обнаружено, что изоксазолины таких вариантов осуществления имеют склонность проявлять особенно благоприятное подавление блох in vivo в пределах 24 и 48 часов после заражения. См., например, пример 3 ниже.
Примеры изоксазолинов, охваченных такими вариантами осуществления, включают следующие структуры:
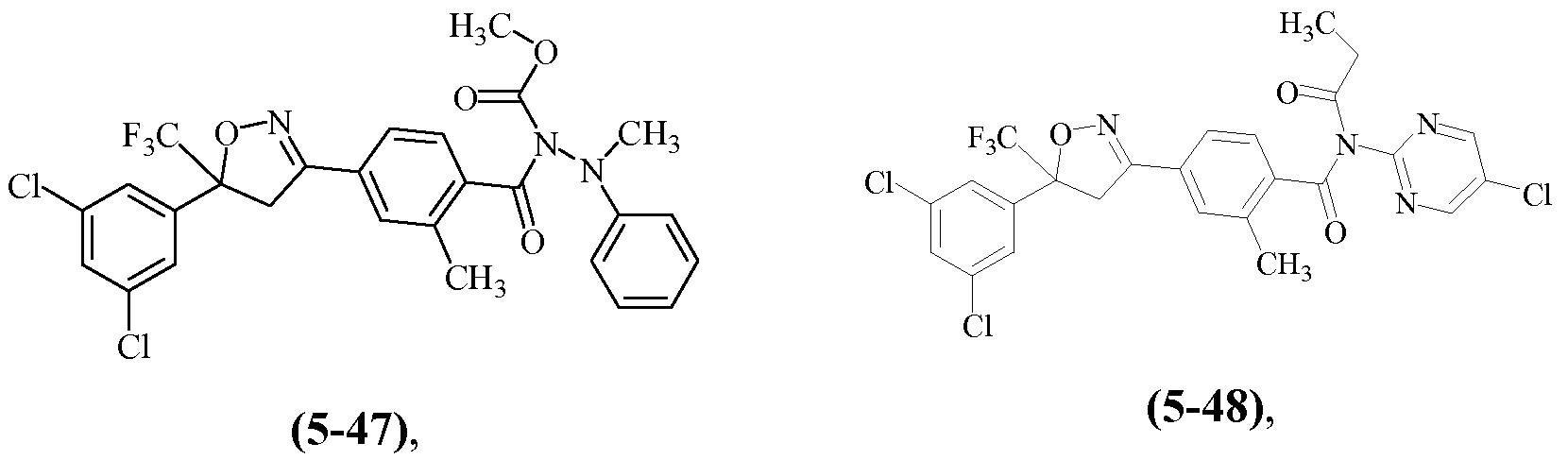
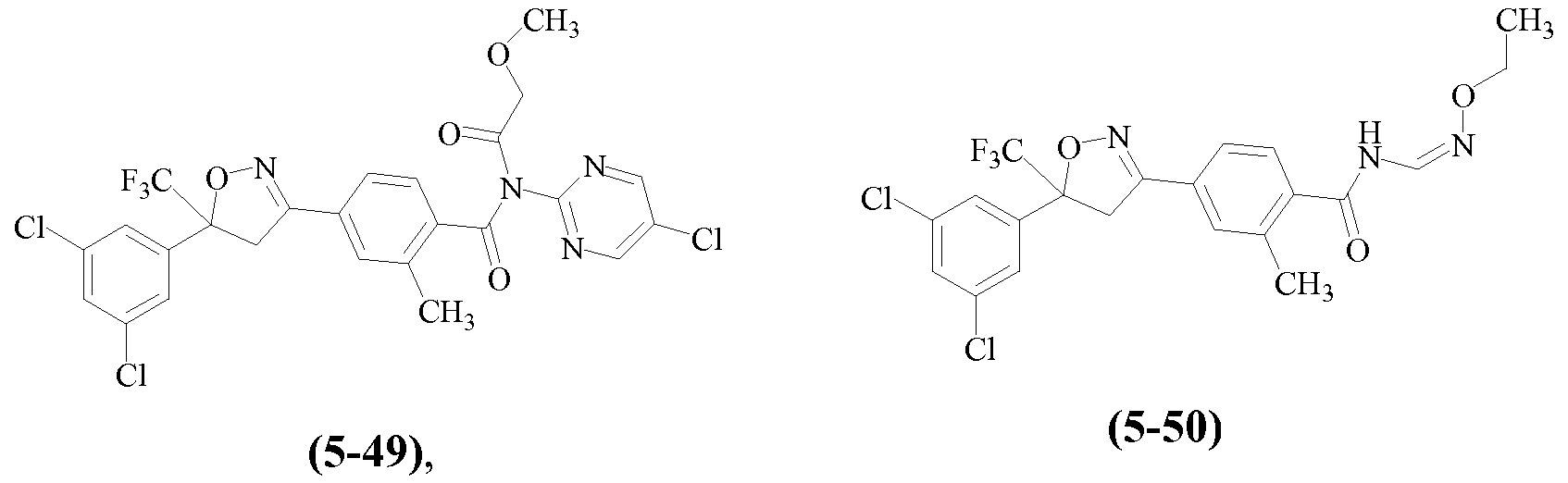 и
и 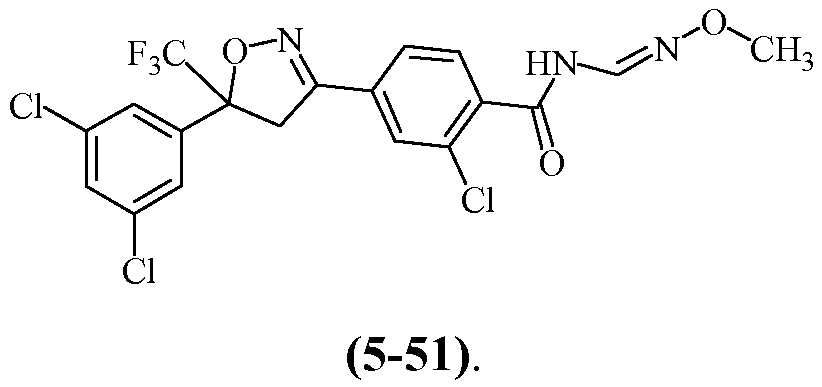
Н8. Иллюстративная комбинация заместителей № 8
В некоторых вариантах осуществления изоксазолин формулы (I) определен, как указано ниже.
Изоксазолин соответствует структуре
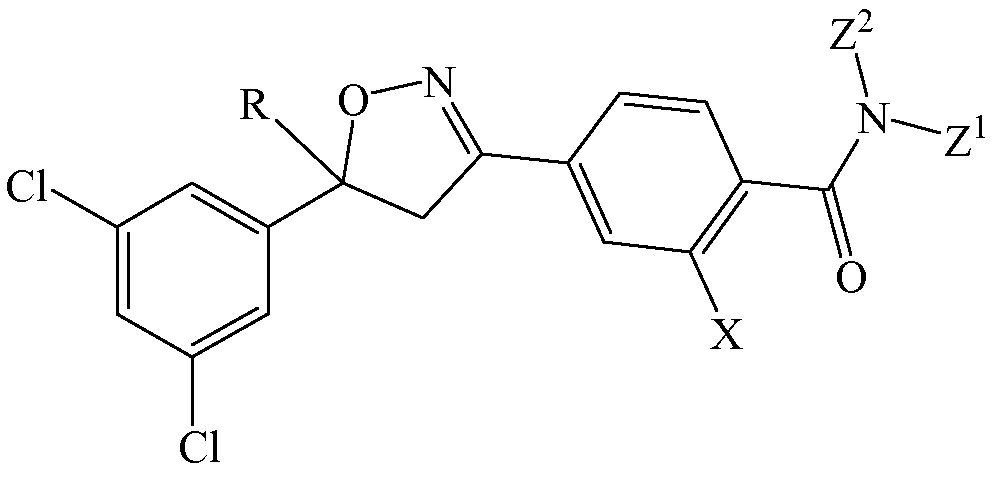
R выбирают из группы, состоящей из трифторметила и монохлордифторметила.
Х выбирают из группы, состоящей из йода и метила.
Z1 выбирают из группы, состоящей из водорода, метоксиметила, этоксиметила, (2,2,2-трифторэтокси)метила, этиламинокарбонилметила, 2,2-диметоксиэтила, 2-пропиниламинокарбонилметила, N-фенил-N-метиламино, (2,2,2-трифторэтил)аминокарбонилметила, 1-[(2,2,2-трифторэтил)аминокарбонил]этила, тетрагидрофурила,

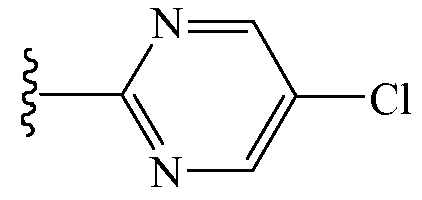 и
и 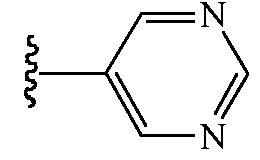
Когда Z1 представляет собой водород, Z2 представляет собой аминокарбонил.
Когда Z1 является иным, чем водород, Z2 выбирают из группы, состоящей из водорода, метилкарбонила, этилкарбонила и метоксикарбонила.
Согласно настоящему изобретению обнаружено, что изоксазолины таких вариантов осуществления имеют склонность проявлять особенно благоприятные результаты in vivo в отношении подавления блох в пределах 24 и 48 часов после заражения и иксодовых клещей в течение по меньшей мере 8 суток. См., например, примеры 3 и 4 ниже.
Примеры изоксазолинов, охваченных такими вариантами осуществления, включают следующие структуры:
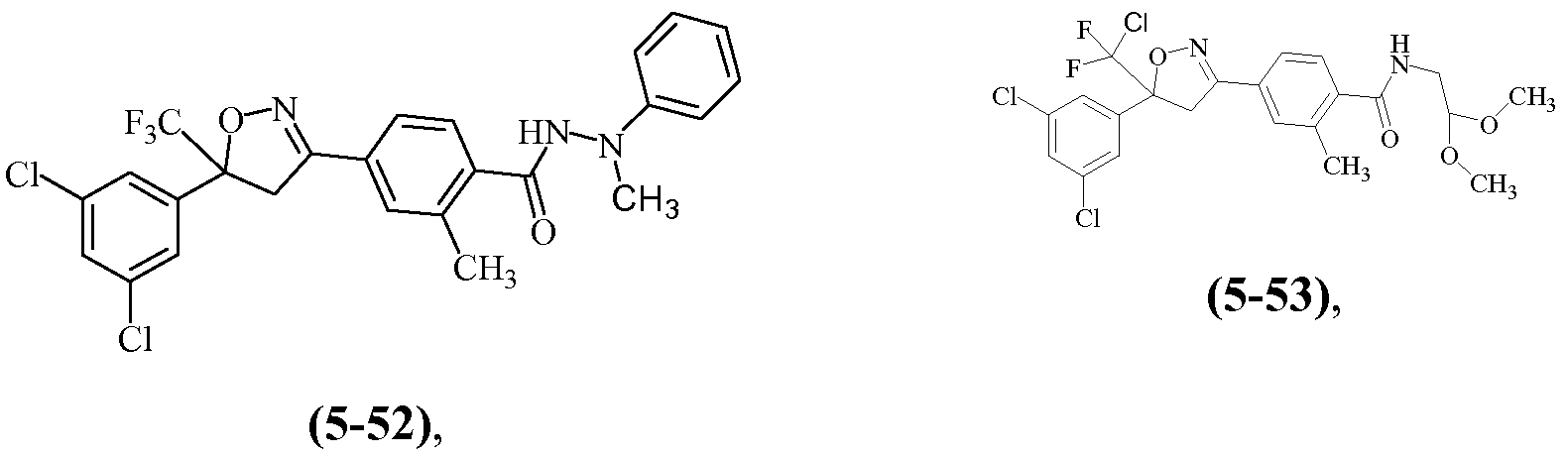
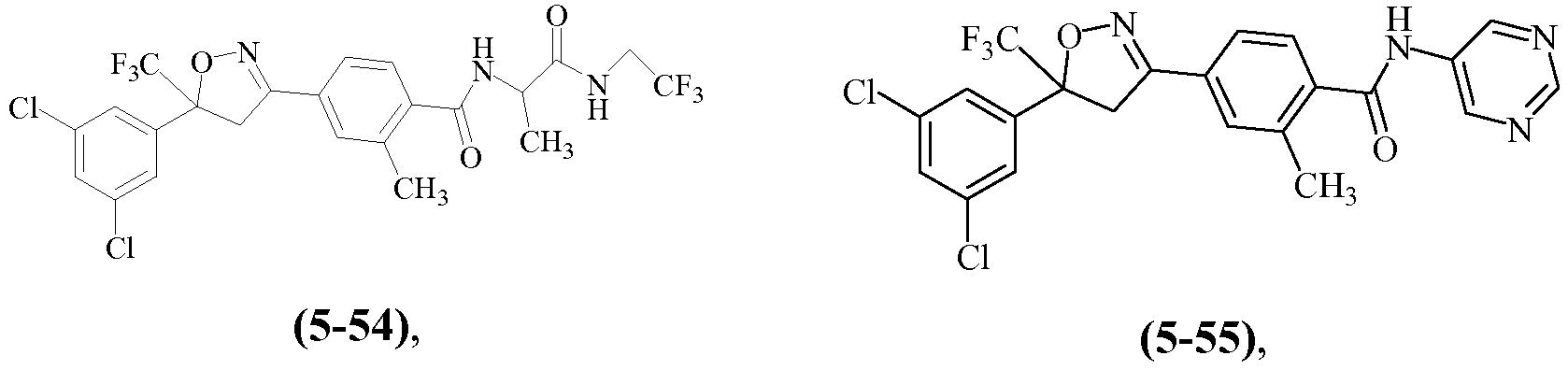
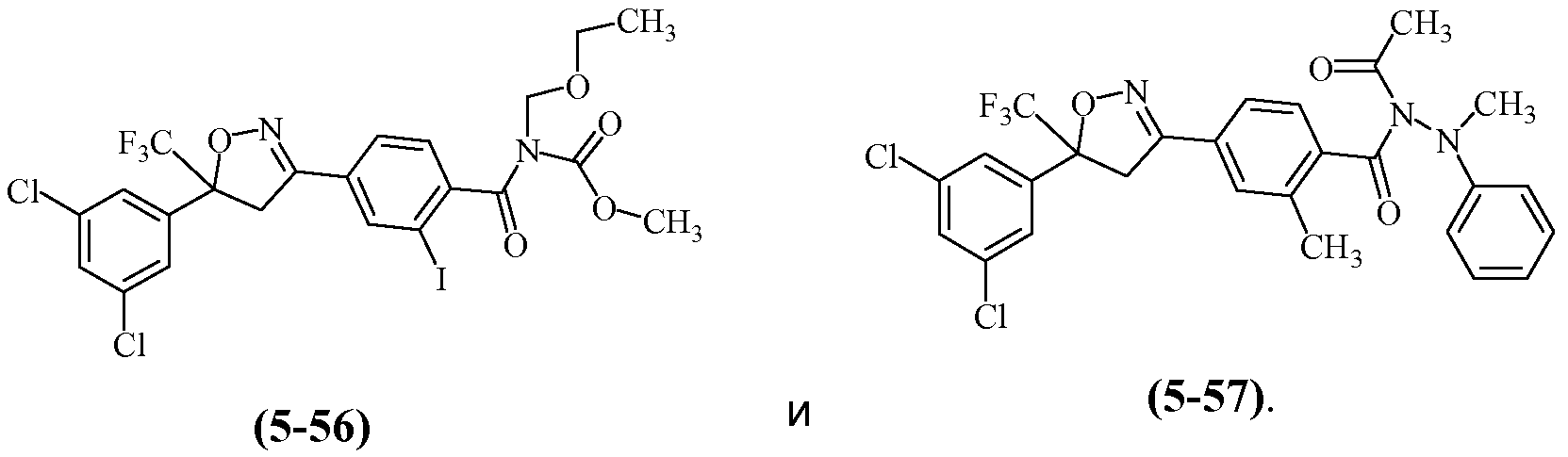
Н9. Иллюстративная комбинация заместителей № 9
В некоторых вариантах осуществления изоксазолин формулы (I) определен, как указано ниже.
Изоксазолин соответствует структуре
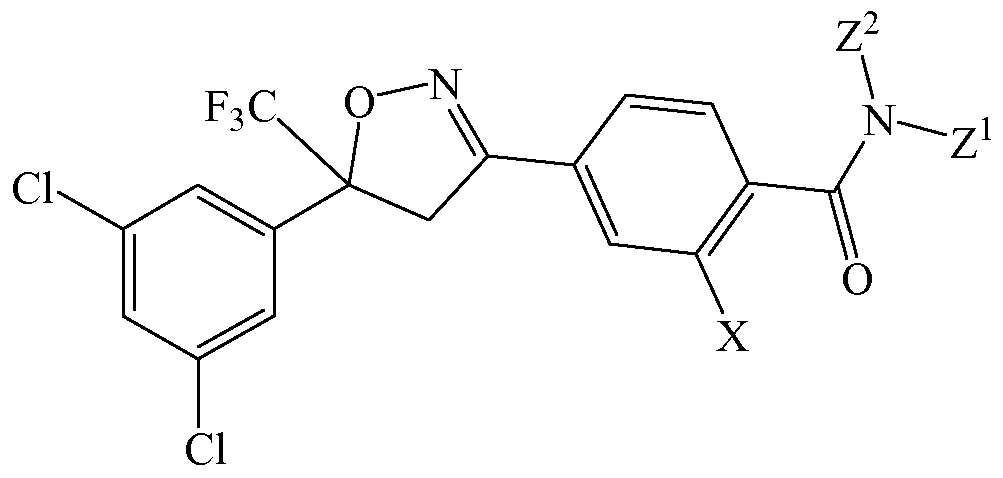
Х выбирают из группы, состоящей из йода и метила.
Z1 выбирают из группы, состоящей из водорода, (2,2,2-трифторэтокси)метила, этиламинокарбонилметила, 2-пропиниламинокарбонилметила, N-фенил-N-метиламино, (2,2,2-трифторэтил)аминокарбонилметила, 1-[(2,2,2-трифторэтил)аминокарбонил]этила, тетрагидрофурила,
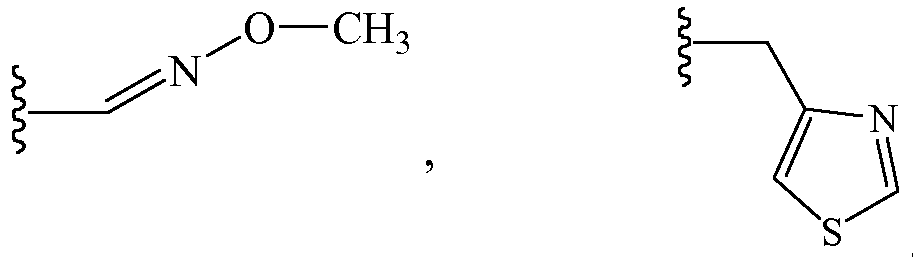 и
и 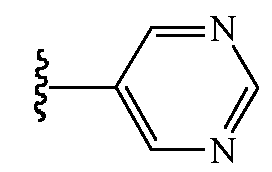
Когда Z1 представляет собой водород, Z2 представляет собой аминокарбонил.
Когда Z1 является иным, чем водород, Z2 выбирают из группы, состоящей из водорода и этилкарбонила.
Согласно настоящему изобретению обнаружено, что изоксазолины таких вариантов осуществления также имеют склонность проявлять особенно благоприятные результаты in vivo в отношении подавления как блох в пределах 24 и 48 часов, так и иксодовых клещей в течение по меньшей мере 8 суток. См., например, примеры 3 и 4 ниже.
Н10. Иллюстративная комбинация заместителей № 10
В некоторых вариантах осуществления изоксазолин формулы (I) определен, как указано ниже.
Изоксазолин соответствует структуре
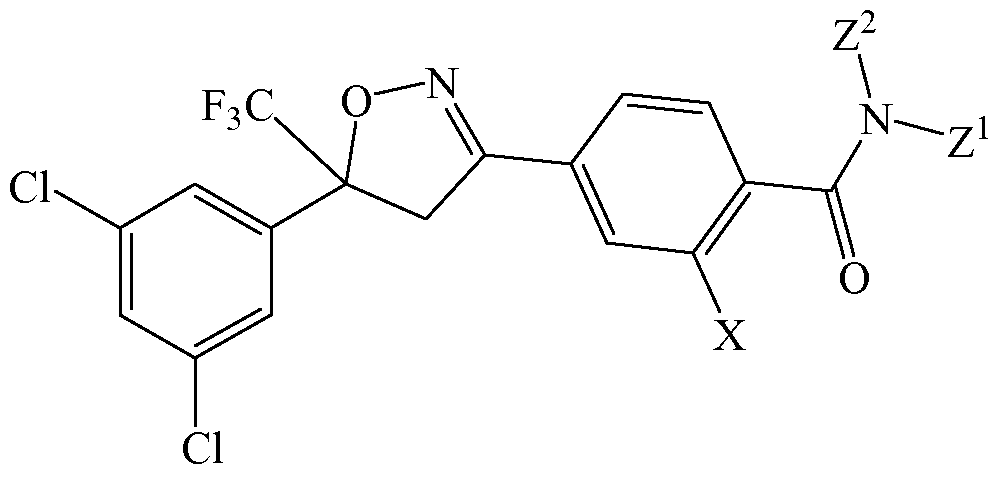
Х выбирают из группы, состоящей из йода и метила.
Z1 выбирают из группы, состоящей из водорода, (2,2,2-трифторэтокси)метила,
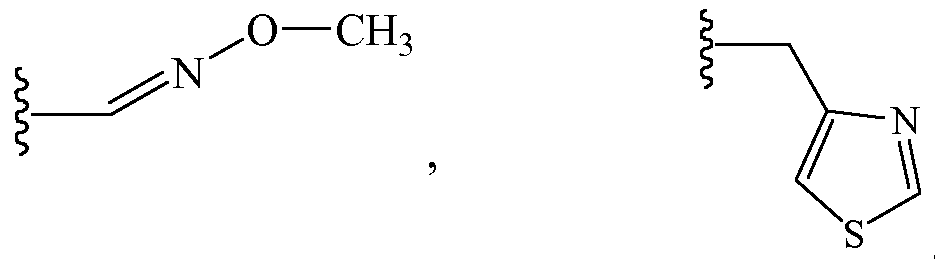 и
и 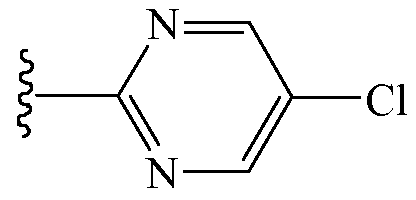
Когда Z1 представляет собой водород, Z2 представляет собой аминокарбонил.
Когда Z1 является иным, чем водород, Z2 выбирают из группы, состоящей из водорода, метилкарбонила и этилкарбонила.
Согласно настоящему изобретению обнаружено, что изоксазолины таких вариантов осуществления имеют склонность проявлять особенно благоприятные результаты in vivo в отношении подавления блох в пределах 24 и 48 часов после заражения и иксодовых клещей в течение по меньшей мере 8 суток. См., например, примеры 3 и 4 ниже.
Примеры изоксазолинов, охваченных такими вариантами осуществления, включают следующие структуры:
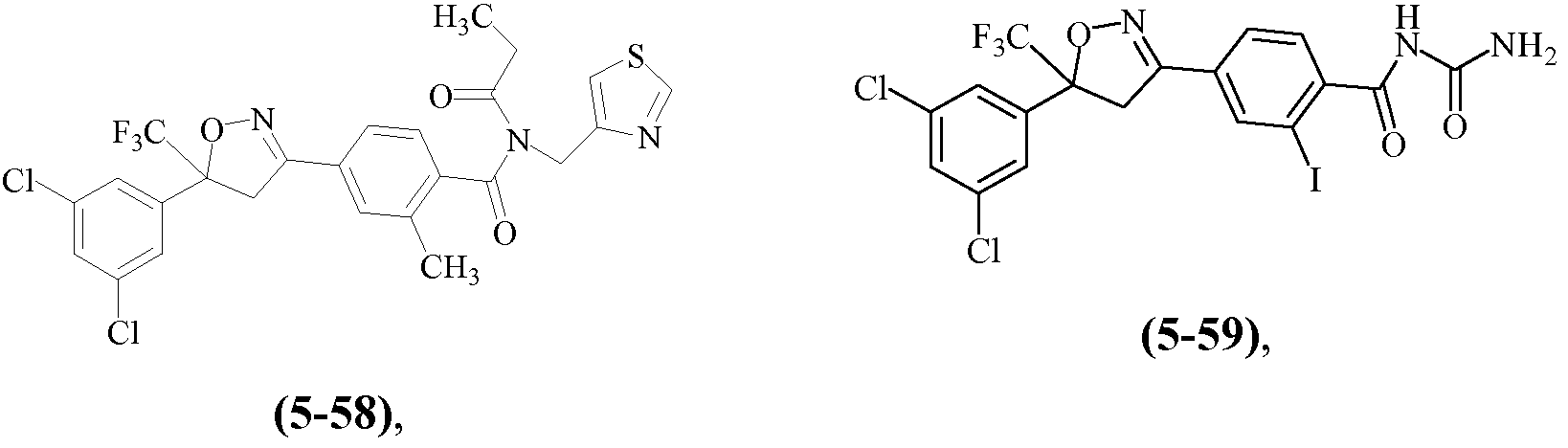
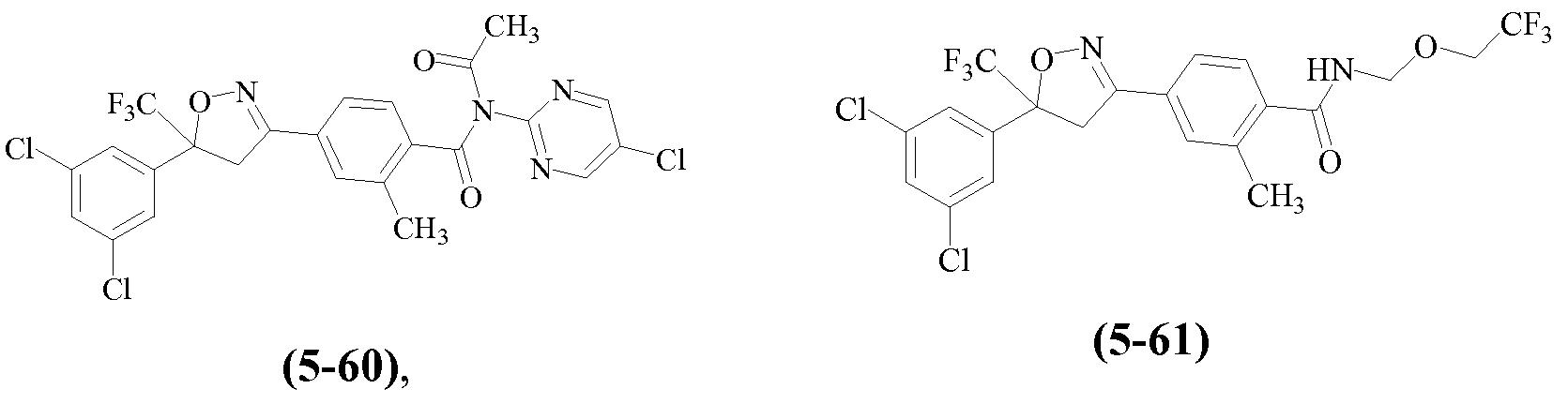 и
и 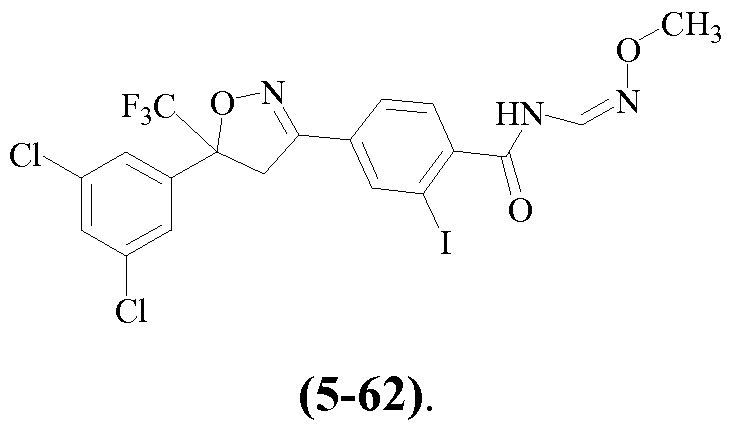
Н11. Иллюстративная комбинация заместителей № 11
В некоторых вариантах осуществления изоксазолин формулы (I) определен, как указано ниже.
Изоксазолин соответствует структуре
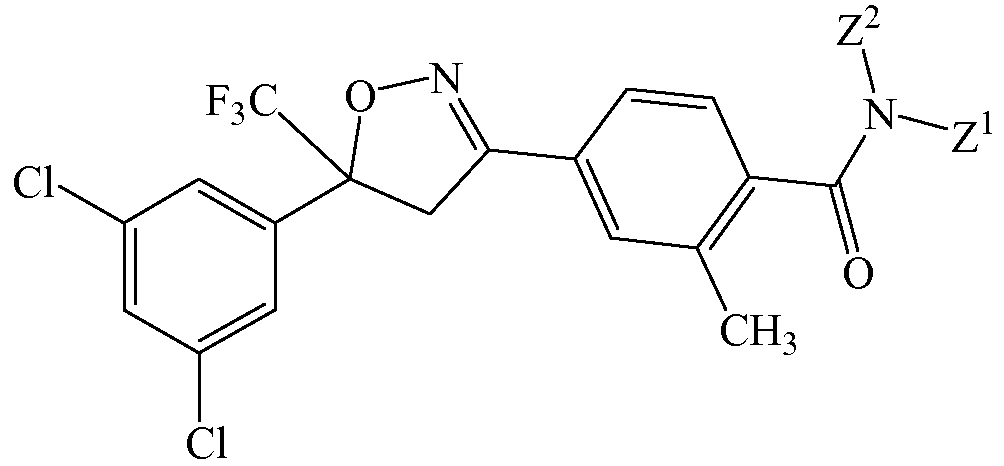
Z1 выбирают из группы, состоящей из метоксиметила, этоксиметила и тетрагидрофурила.
Z2 выбирают из группы, состоящей из водорода и метоксикарбонила.
Согласно настоящему изобретению обнаружено, что изоксазолины таких вариантов осуществления имеют склонность проявлять особенно благоприятные результаты in vivo в отношении подавления блох в пределах 24 и 48 часов после заражения и иксодовых клещей в течение по меньшей мере 8 суток. См., например, примеры 3 и 4 ниже.
Примеры изоксазолинов, охваченных такими вариантами осуществления, включают следующие структуры:
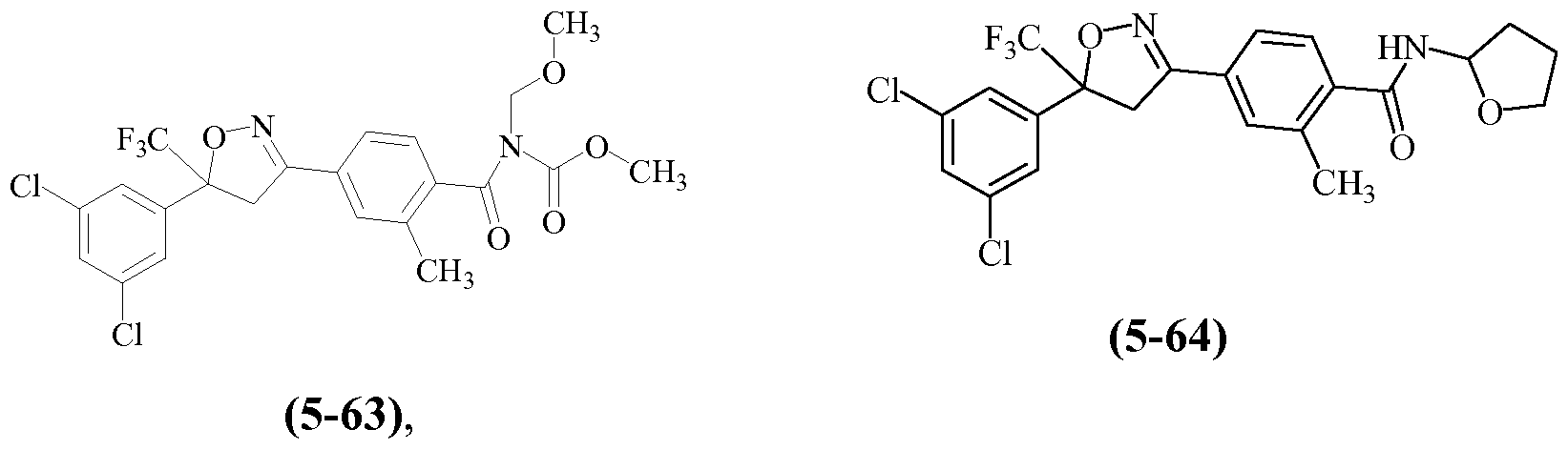 и
и 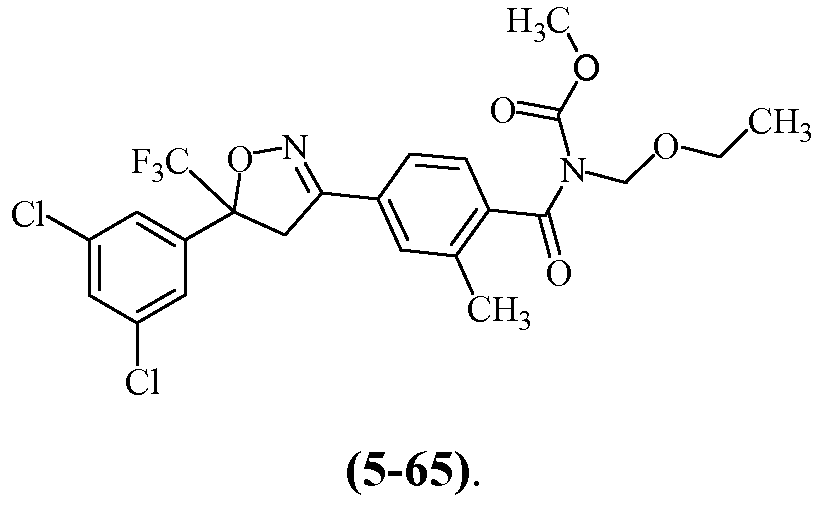
Н12. Иллюстративная комбинация заместителей № 12
В некоторых вариантах осуществления изоксазолин формулы (I) определен, как указано ниже.
Изоксазолин соответствует структуре
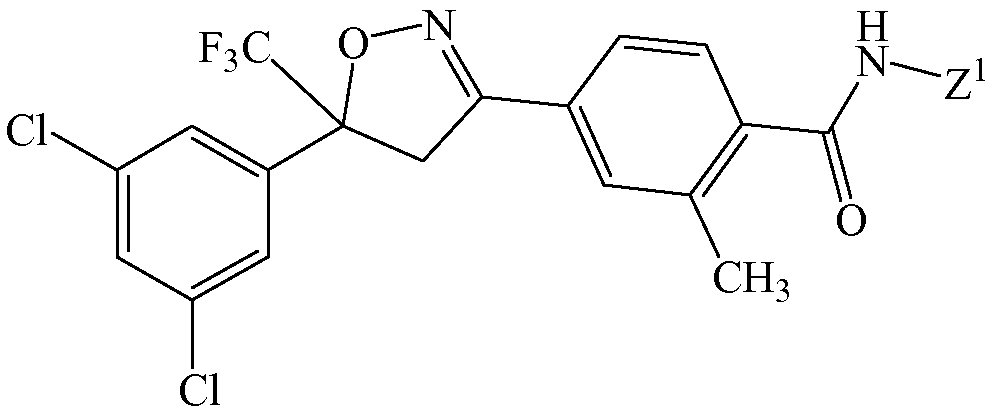
Z1 выбирают из группы, состоящей из этиламинокарбонилметила, 2-пропиниламинокарбонилметила, (2,2,2-трифторэтил)аминокарбонилметила, тетрагидрофурила,
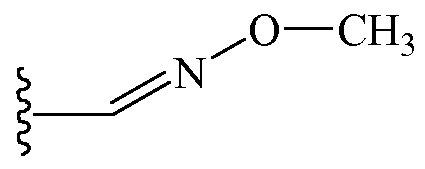 и
и 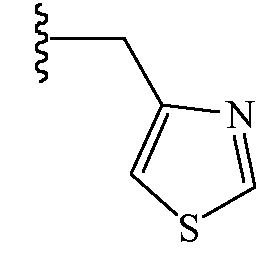
Согласно настоящему изобретению обнаружено, что изоксазолины таких вариантов осуществления имеют склонность проявлять особенно благоприятные результаты in vivo в отношении подавления блох в пределах 1, 24 и 48 часов после заражения и иксодовых клещей в течение по меньшей мере 8 суток. См., например, примеры 3 и 4 ниже.
Примеры изоксазолинов, охваченных такими вариантами осуществления, включают следующие структуры:
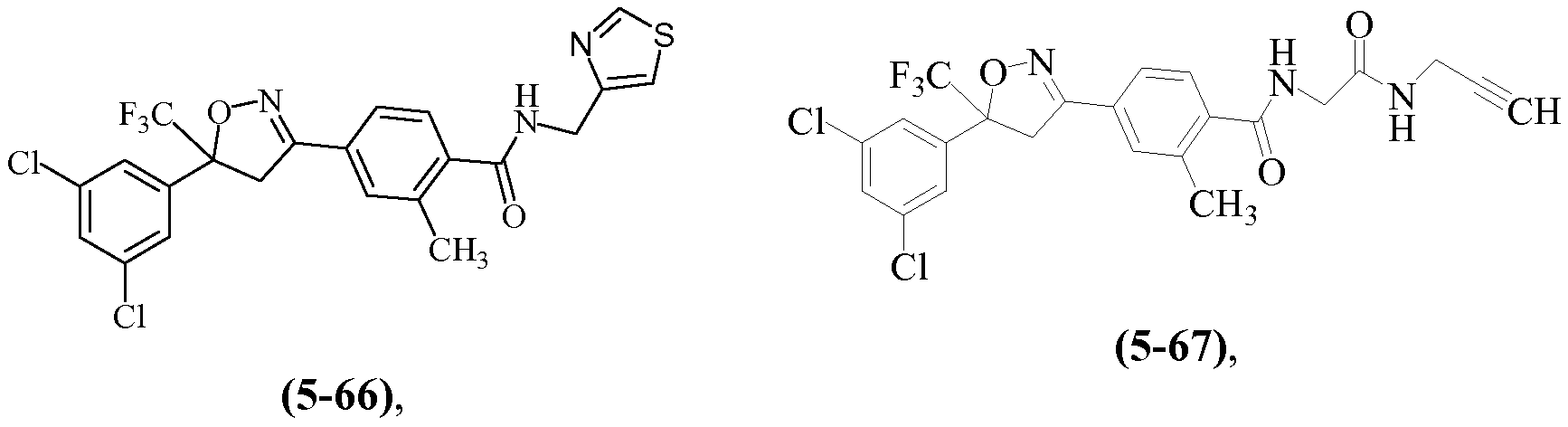
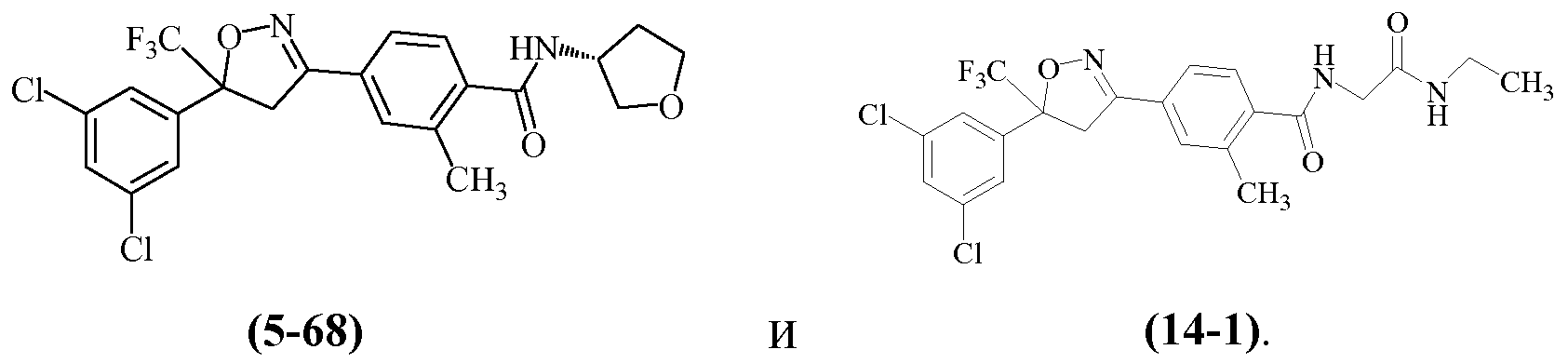
Другие изоксазолины, охваченные такими вариантами осуществления, включают структуру
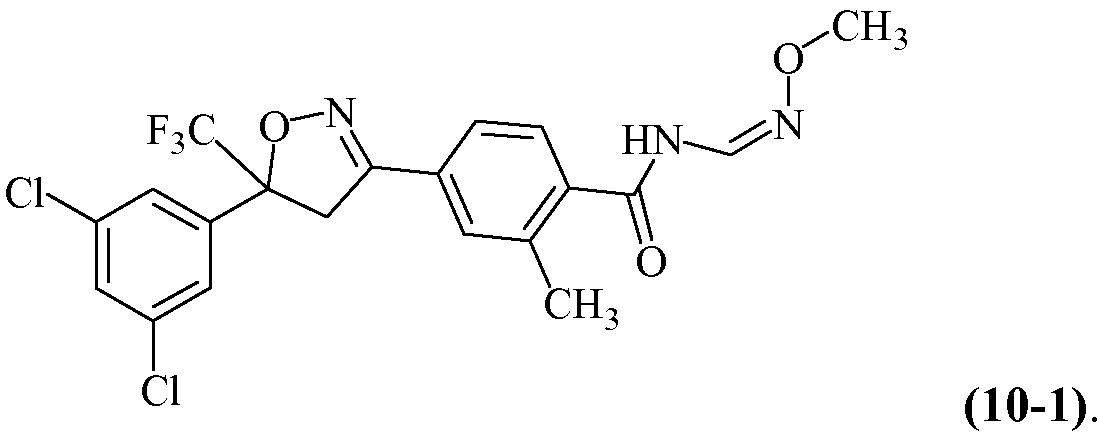
Химическое название такого изоксазолина (Z)-4-[5-(3,5-дихлорфенил)-5-трифторметил-4,5-дигидроизоксазол-3-ил]-N-[(метоксиимино)метил]-2-метилбензамид. Его можно найти, например, в CAS RN [928789-76-8].
Еще другие изоксазолины, охваченные такими вариантами осуществления, включают структуру
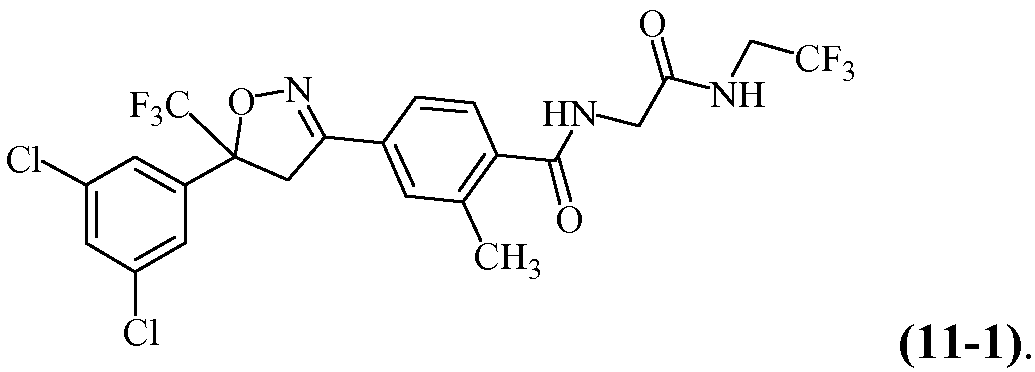
Химическое название такого изоксазолина 4-[5-(3,5-дихлорфенил)-5-трифторметил-4,5-дигидроизоксазол-3-ил]-2-метил-N-[(2,2,2-трифторэтилкарбамоил)метил]бензамид. Его можно найти, например, в CAS RN [864731-61-3]. Согласно настоящему изобретению обнаружено, что соединение 11-1 проявляет особенно благоприятные результаты in vivo в отношении длительности подавления блох с использованием различных способов введения, включая местное, пероральное или подкожное. См., например, пример 5 ниже.
Н13. Иллюстративная комбинация заместителей № 13
В некоторых вариантах осуществления изоксазолин формулы (I) определен, как указано ниже.
Изоксазолин имеет структурную формулу (I)
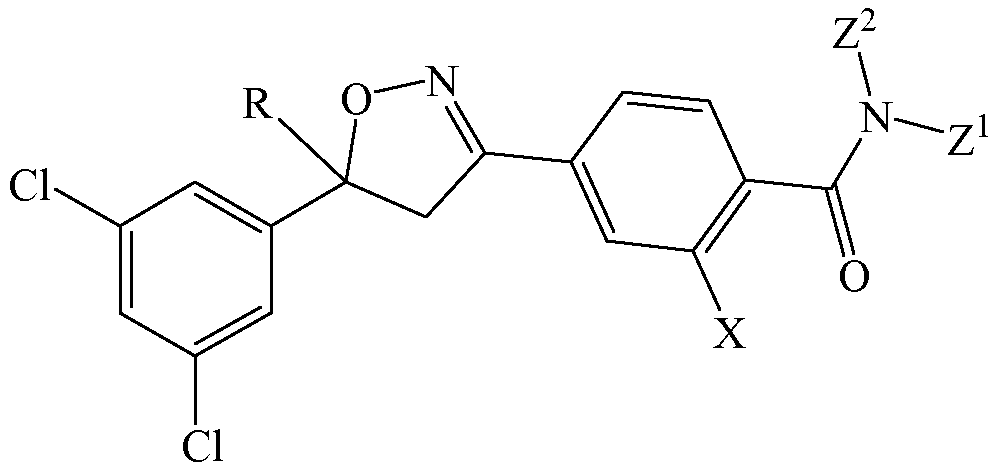
R выбирают из группы, состоящей из монохлорметила и трифторметила.
Х выбирают из группы, состоящей из йода и метила.
Z1 выбирают из группы, состоящей из водорода, метоксиметила, этоксиметила, (2,2,2-трифторэтокси)метила, изопропоксиметила, этиламинокарбонилметила, 2-пропиниламинокарбонилметила, (2,2,2-трифторэтил)аминокарбонилметила, тетрагидрофурила,
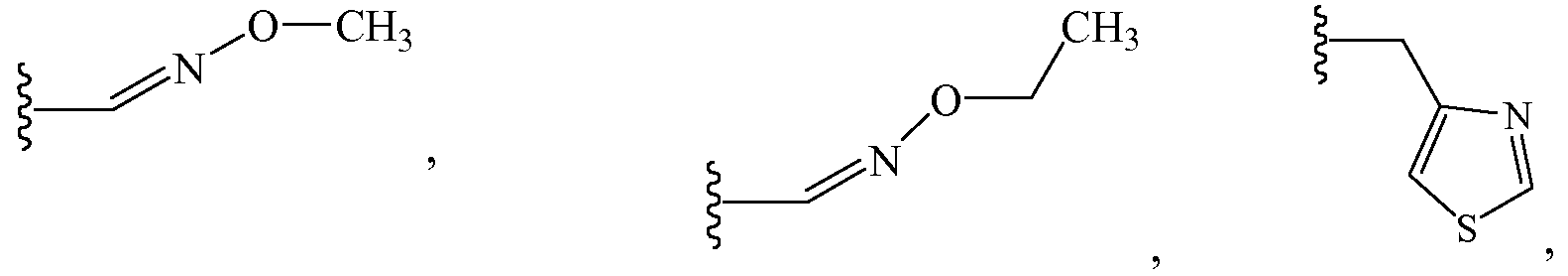
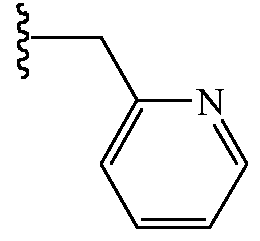 и
и 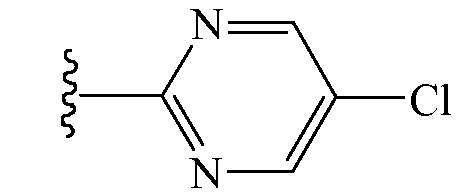
Когда Z1 представляет собой водород, Z2 представляет собой аминокарбонил.
Когда Z1 является иным, чем водород, Z2 выбирают из группы, состоящей из водорода, метилкарбонила, этилкарбонила и метоксикарбонила, за исключением того, что
Н14. Иллюстративная комбинация заместителей № 14
В некоторых вариантах осуществления изоксазолин формулы (I) определен, как указано ниже.
Изоксазолин соответствует структуре
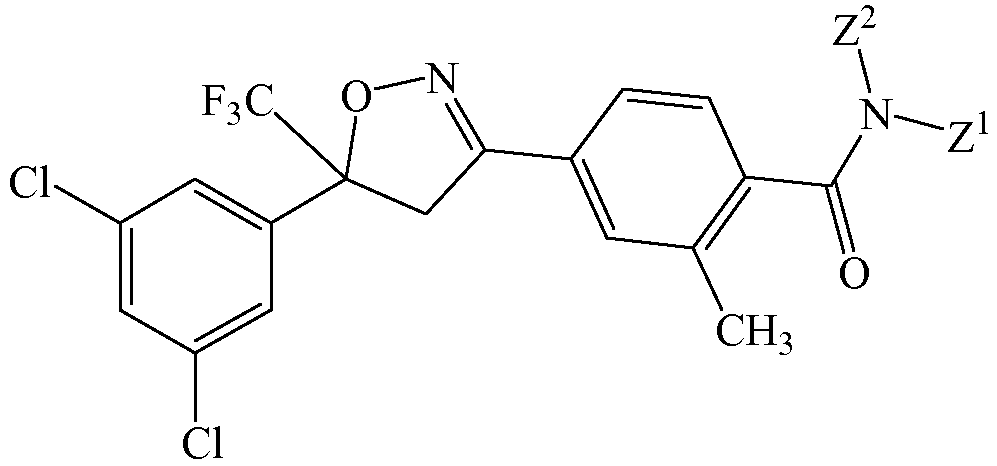
Z1 выбирают из группы, состоящей из метоксиметила, этоксиметила, этиламинокарбонилметила, 2-пропиниламинокарбонилметила, (2,2,2-трифторэтил)аминокарбонилметила, тетрагидрофурила,
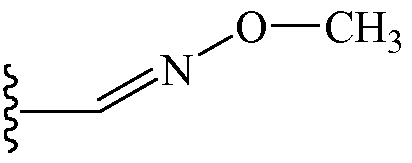 и
и 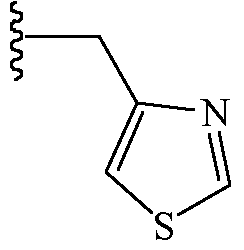
Z2 выбирают из группы, состоящей из водорода и метоксикарбонила.
Н15. Иллюстративная комбинация заместителей № 15
В некоторых вариантах осуществления изоксазолин формулы (I) определен, как указано ниже.
Изоксазолин соответствует структуре
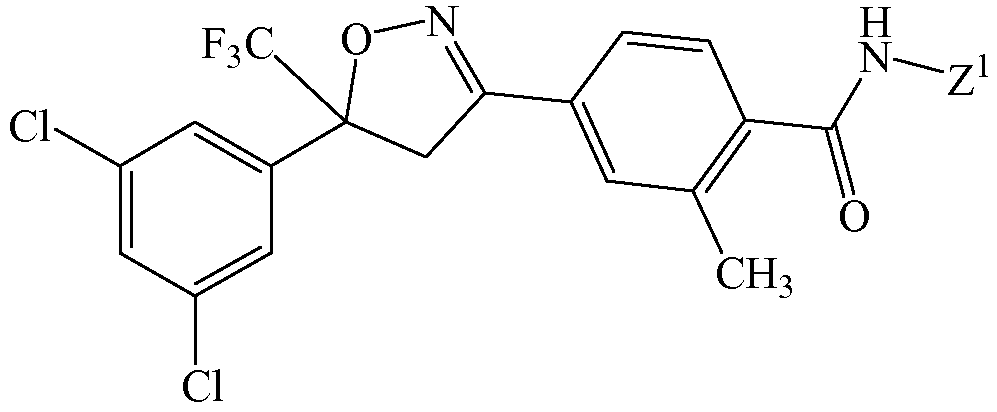
Z1 выбирают из группы, состоящей из этиламинокарбонилметила, 2-пропиниламинокарбонилметила, (2,2,2-трифторэтил)аминокарбонилметила, тетрагидрофурила,
 и
и 
Согласно настоящему изобретению обнаружено, что изоксазолины таких вариантов осуществления имеют склонность проявлять особенно благоприятные результаты in vivo в отношении подавления блох в пределах 1, 24 и 48 часов после заражения. См., например, пример 3 ниже.
Пример изоксазолинов, охваченных такими вариантами осуществления, включает следующую структуру:
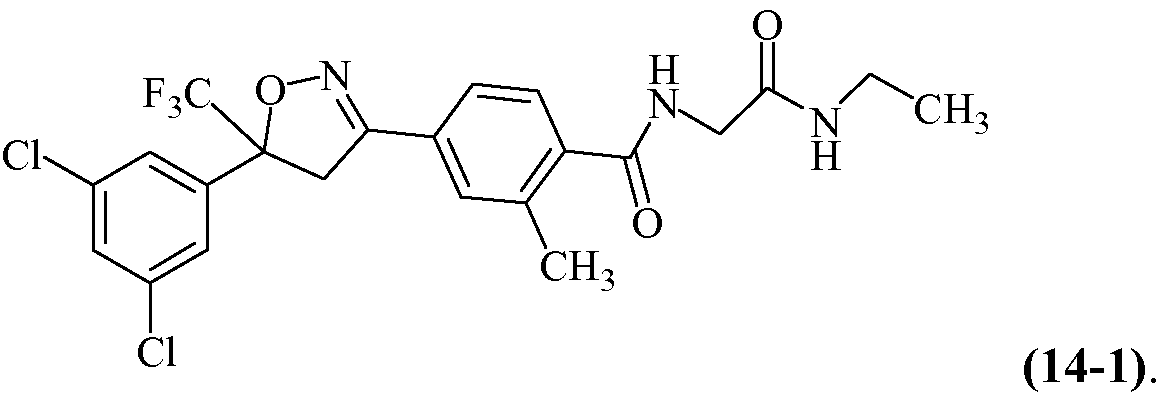
Н16. Иллюстративная комбинация заместителей № 16
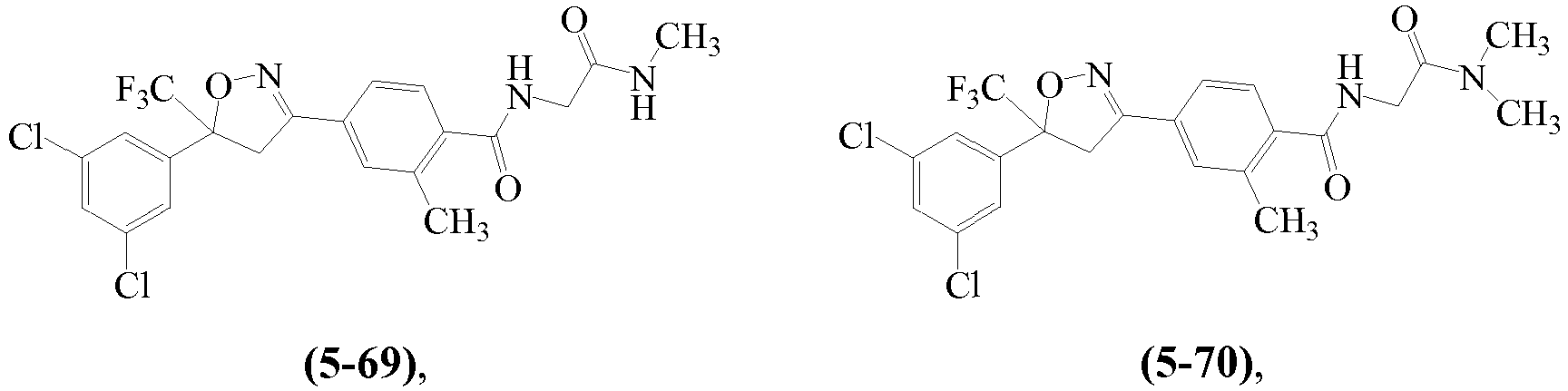
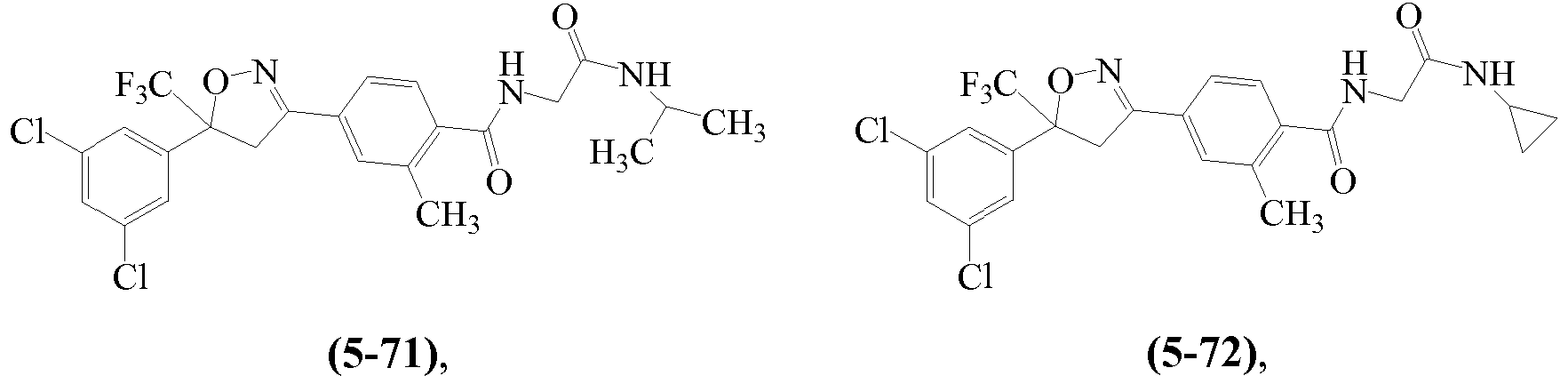
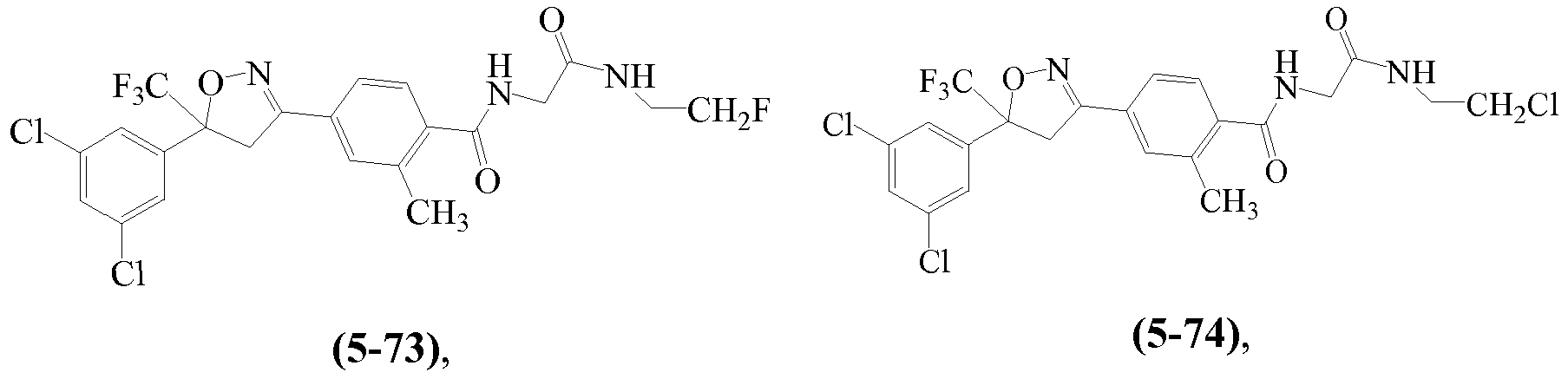
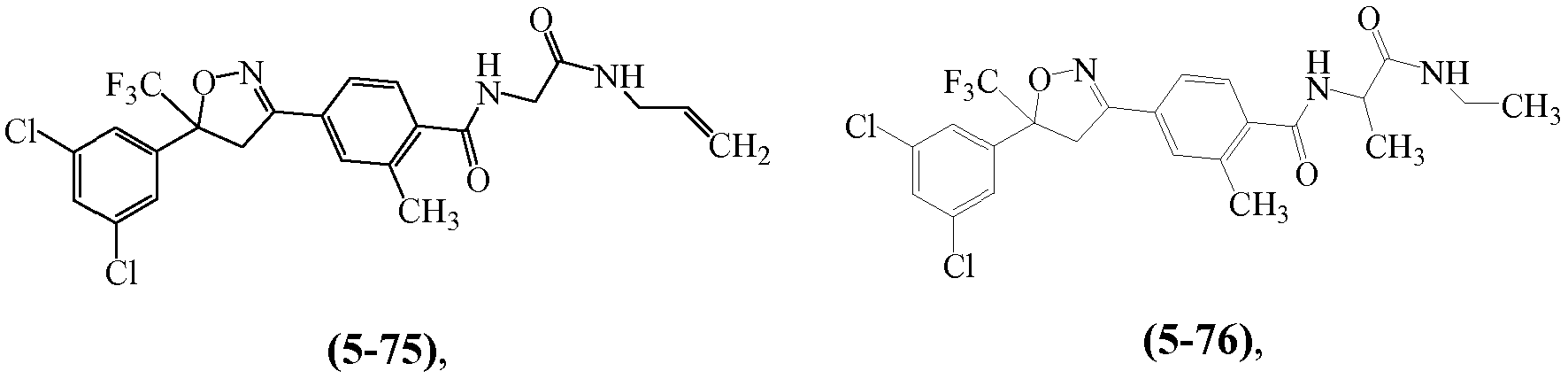
В некоторых вариантах осуществления изоксазолин соответствует структуре
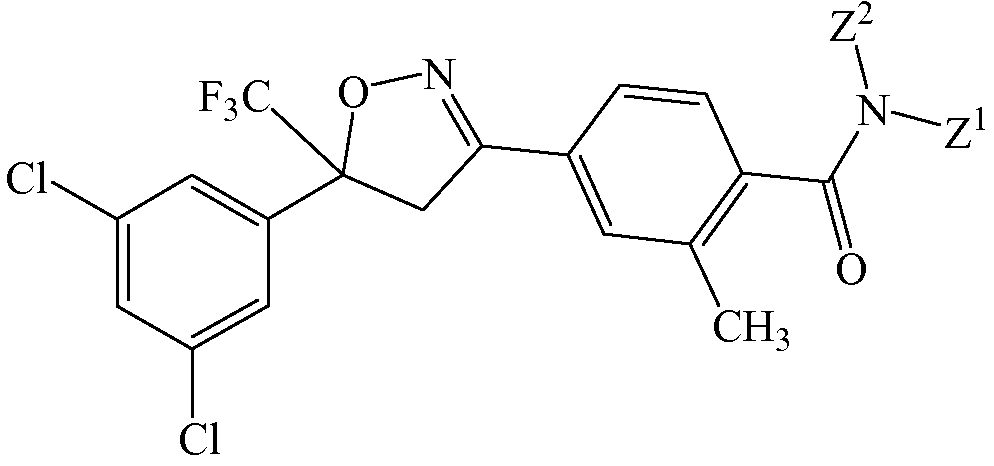
В таких вариантах осуществления Z1 и Z2 либо являются независимыми заместителями, либо вместе образуют один заместитель.
Когда Z1 и Z2 являются независимыми заместителями,
Z1 выбирают из группы, состоящей из 1-[(2,2,2-трифторэтил)аминокарбонил]этила, метиламинокарбонилметила, (N,N-диметиламино)карбонилметила, изопропиламинокарбонилметила, циклопропиламинокарбонилметила, (2-пропенил)аминокарбонилметила, (2,2,2-трифторэтил)аминокарбонилциклопропила, (2-фторэтил)аминокарбонилметила, (2-хлорэтил)аминокарбонилметила, 1-(этиламинокарбонил)этила,
 и
и 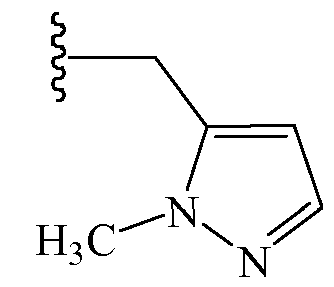 ; и
; и
Z2 выбирают из группы, состоящей из водорода, метилкарбонила и этилкарбонила.
Когда Z1 и Z2 вместе образуют один заместитель, они образуют
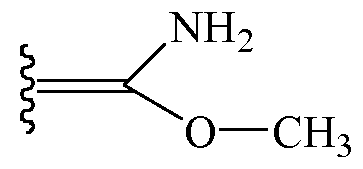
Примеры изоксазолинов, охваченных такими вариантами осуществления, включают следующие структуры:
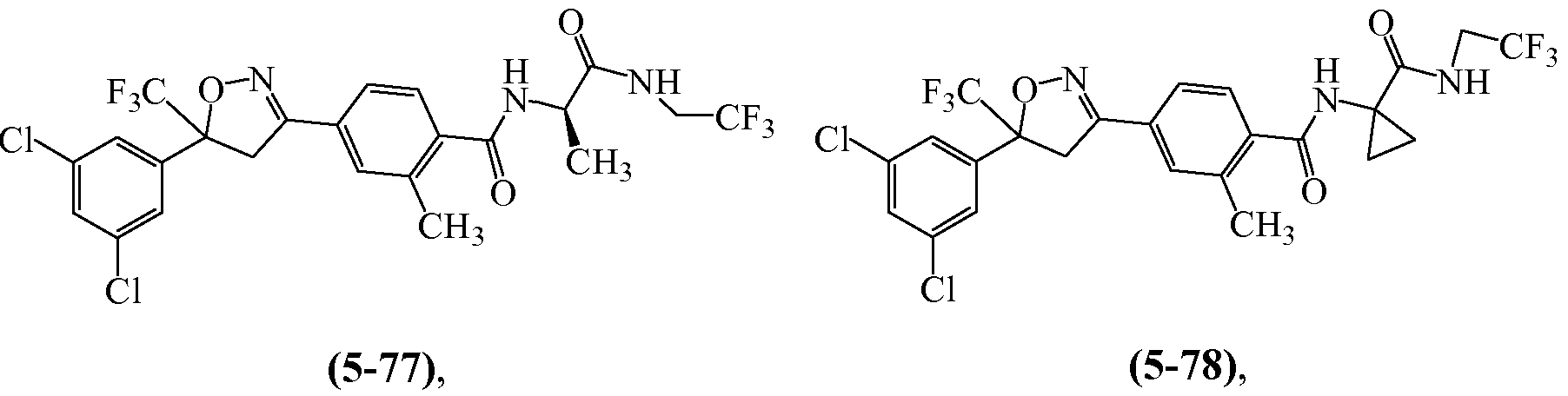
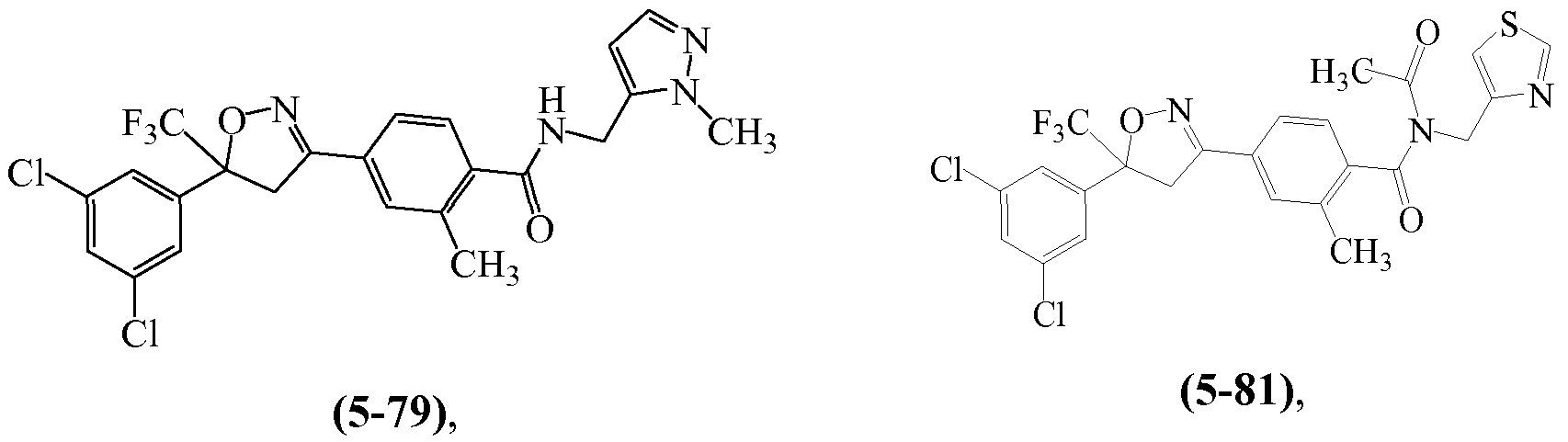
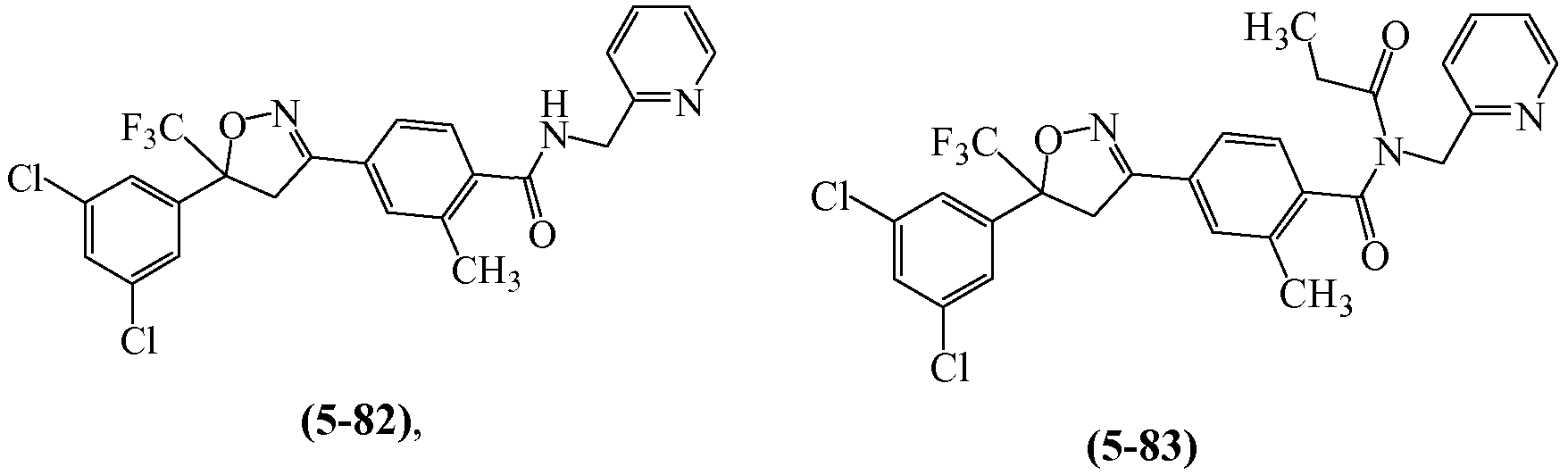 и
и 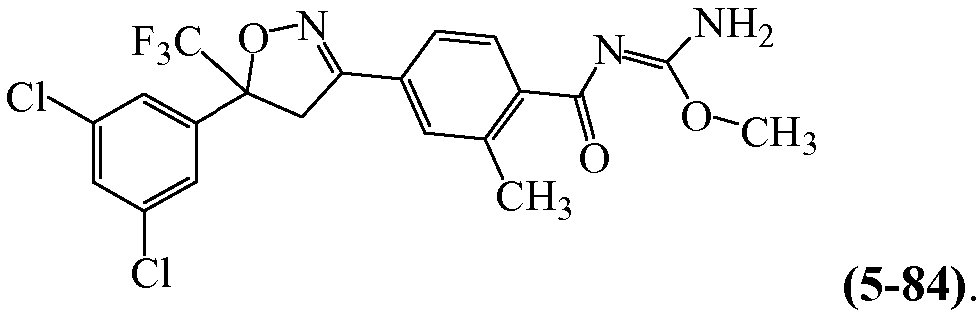
Н17. Иллюстративная комбинация заместителей № 17
В некоторых вариантах осуществления изоксазолин соответствует структуре
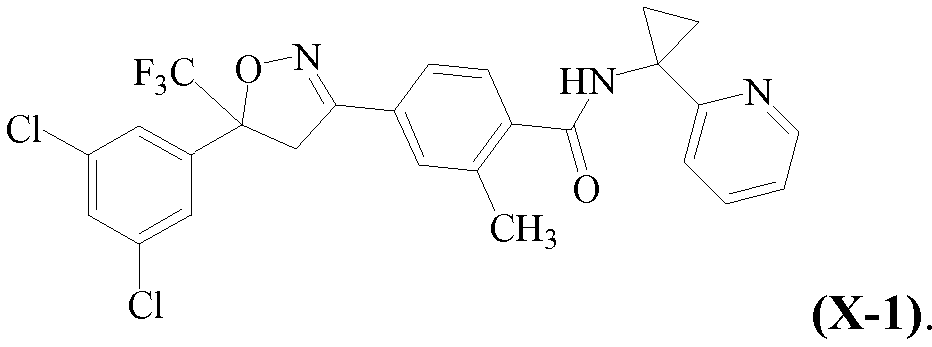
Н18. Иллюстративная комбинация заместителей № 18
В некоторых вариантах осуществления изоксазолин соответствует структуре
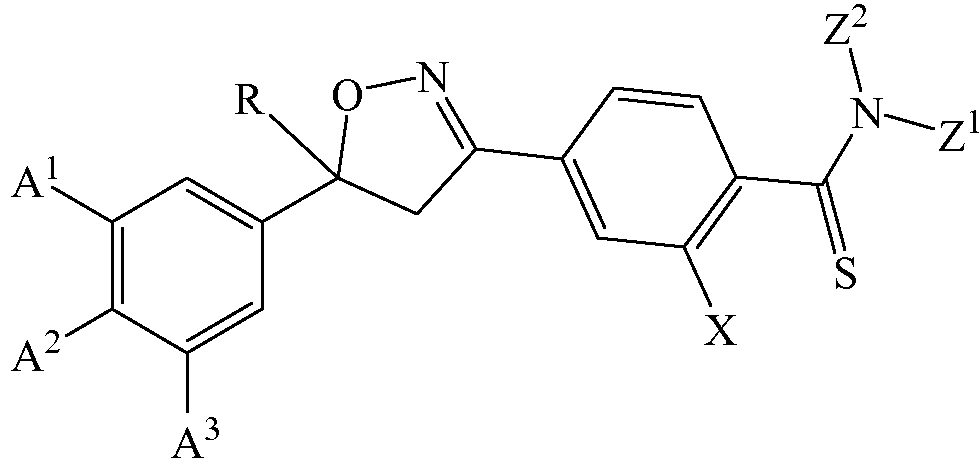
Примеры изоксазолинов, охваченных такими вариантами осуществления, включают следующее соединение:
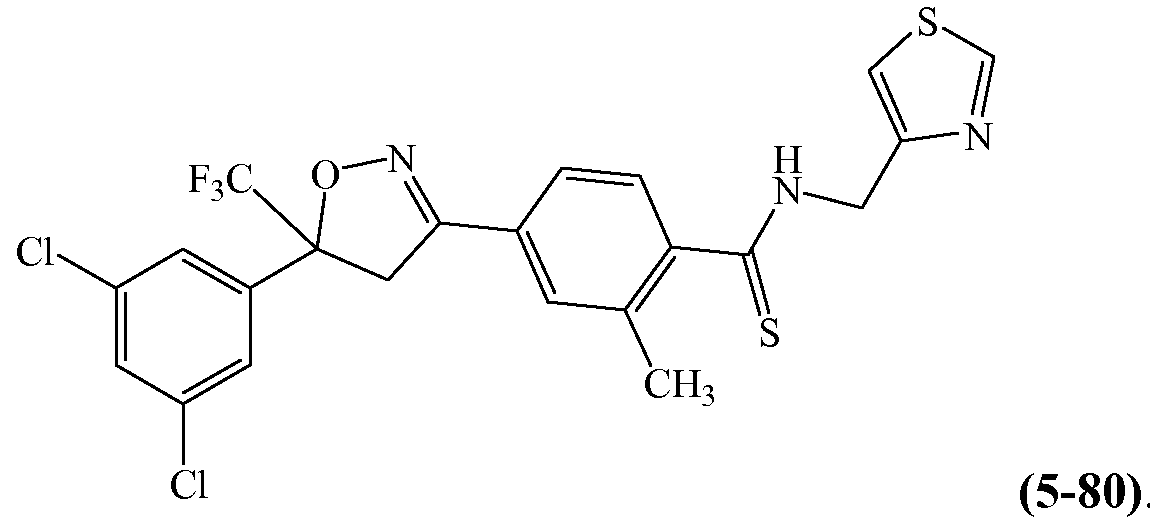
I. Изомеры
Изоксазолины, используемые в настоящем изобретении, как правило, могут иметь две или больше конформационных структур. Минимум, например, все изоксазолины включают хиральный (или асимметричный) атом углерода в положении 5 изоксазолинового кольца. В некоторых вариантах осуществления, например, хиральный атом углерода имеет левостороннюю (или «S» или «левую») конфигурацию. Такие изоксазолины включают изоксазолины, имеющие следующую структуру:
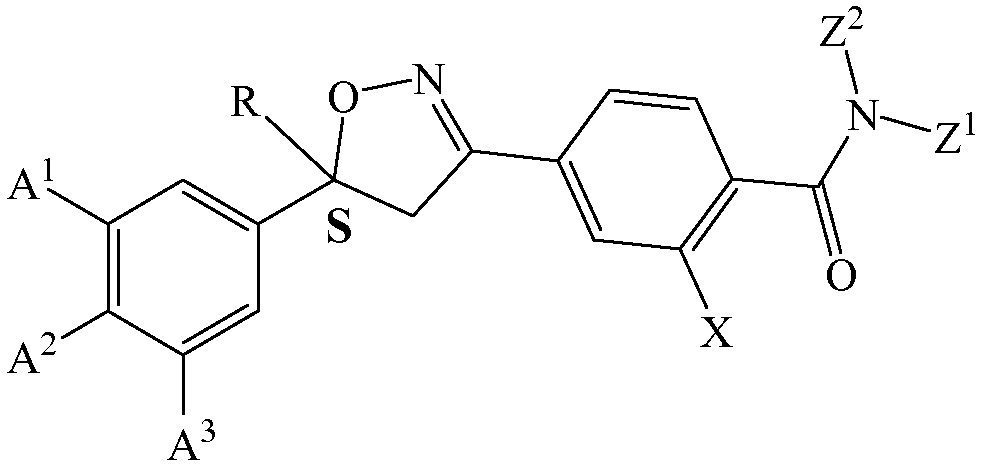
В некоторых таких вариантах осуществления, например, изоксазолины соответствуют структуре
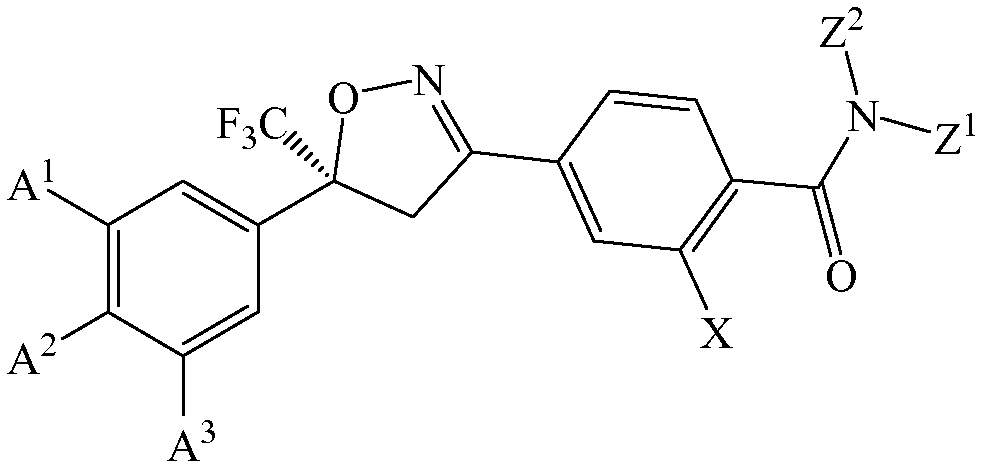
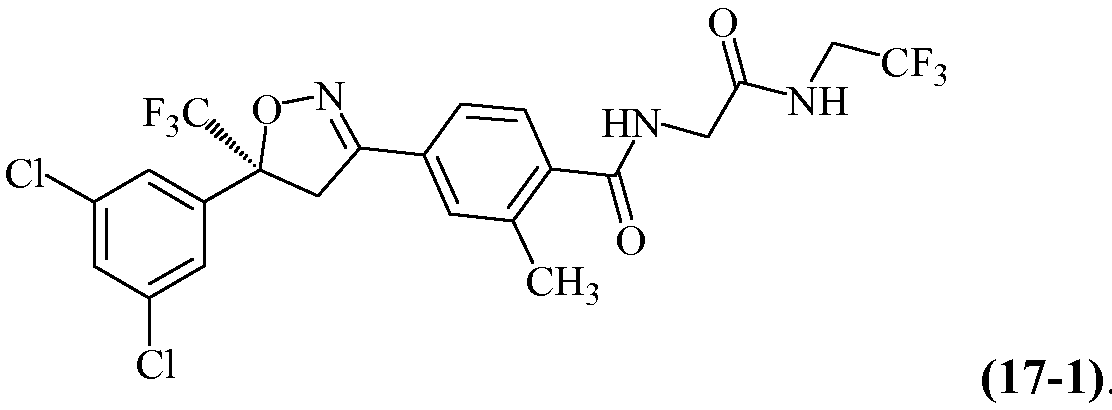
Примером такого соединения является
В других вариантах осуществления хиральный атом углерода имеет правостороннюю (или «R» или «правую») конфигурацию. Такие изоксазолины включают изоксазолины, соответствующие следующей структуре:
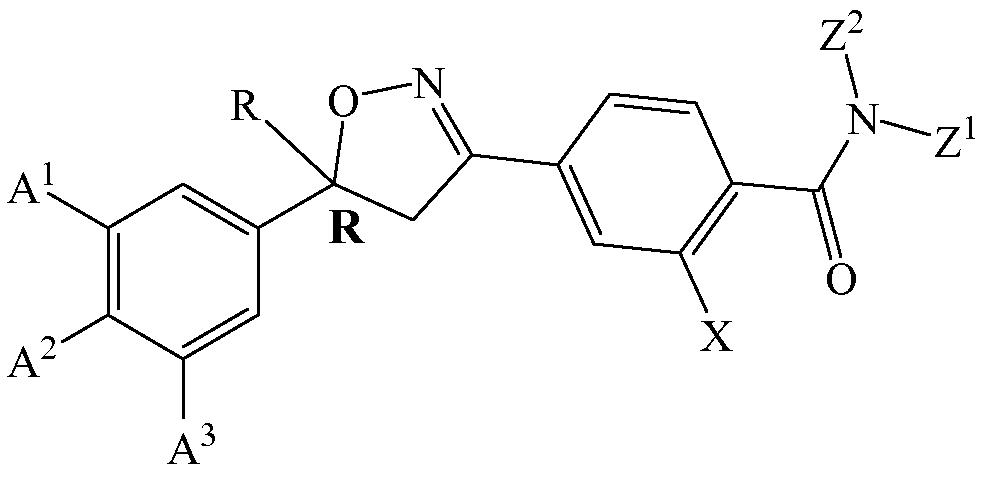
Примером такого соединения является
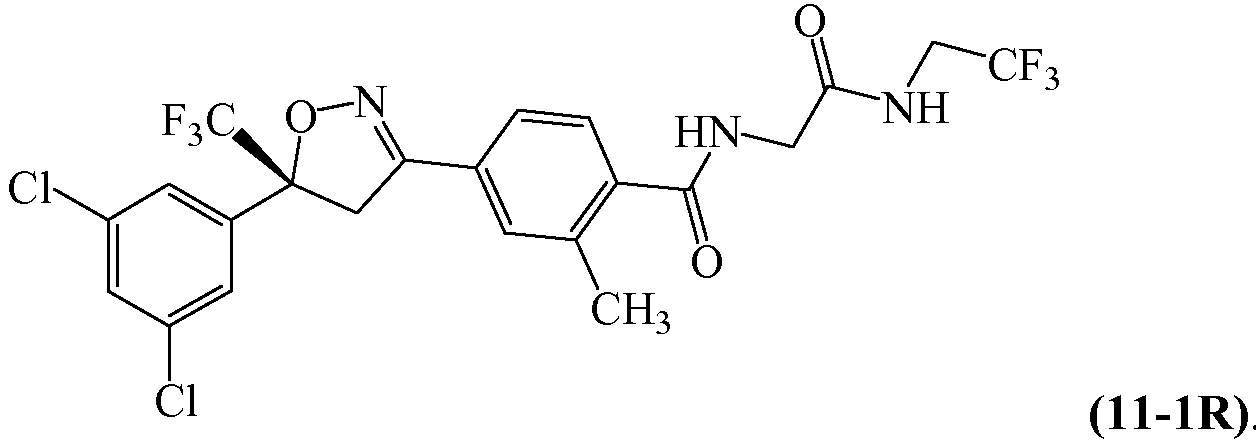
Изоксазолины могут иметь дополнительно другие конформационные изомеры, такие как, например, заместители с цис или транс двойной связью.
Конкретный изомер часто может быть выделен из соответствующей рацемической смеси (или ее соли) с использованием, например, методов хиральной высокоэффективной жидкостной хроматографии (ВЭЖХ). Такой метод поясняется ниже в примере 7 для выделения R- и S-изомеров рацемического соединения 11-1. В некоторых случаях, когда изомер трудно выделить, выделяют более растворимое производное изомера из рацемической смеси соответствующих производных (или их солей) и затем преобразовывают в изомер. Альтернативно, конкретный изомер часто может быть синтезирован непосредственно из, например, оптически чистого исходного вещества.
В некоторых вариантах осуществления в фармацевтической композиции в настоящем изобретении используют отношение одного энантиомера (например, соединения 17-1) к другому энантиомеру (например, соединению 11-1R) большее, чем 1:1. В некоторых случаях, например, отношение больше, чем примерно 70:30, больше, чем примерно 85:15, больше, чем примерно 90:10, больше, чем примерно 95:5, больше, чем примерно 98:2 или больше, чем примерно 99:1.
В некоторых вариантах осуществления концентрация одного энантиомера (например, соединения 17-1) в композиции (или более конкретно предварительной композиции) больше, чем примерно 50% (по массе). В некоторых таких вариантах осуществления, например, концентрация больше чем примерно 70% (по массе), больше чем примерно 85% (по массе), больше чем примерно 90% (по массе), больше чем примерно 95% (по массе), больше чем примерно 98% (по массе), больше чем примерно 99% (по массе) или больше чем примерно 99,5% (по массе).
Если не указано иное, предполагается, что структура изоксазолина, которая не показывает определенную конформацию, охватывает композиции всех возможных конформационных изомеров изоксазолина, а также композиции, содержащие не все (например, только один) возможные конформационные изомеры.
J. Соли изоксазолинов
Как отмечалось выше, многие изоксазолины, используемые в настоящем изобретении, могут находиться в форме соли. Соль может быть преимущественной из-за одного или нескольких ее физических свойств, таких как фармацевтическая стабильность при различных температурах и влажности; кристаллических свойств и/или желаемой растворимости в воде, масле или других растворителях. Аддитивные соли кислот и оснований обычно могут быть получены, например, путем смешивания соединения с кислотой или основанием, соответственно, с использованием различных способов, известных в данной области. Как правило, когда предполагается введение соли in vivo (т.е. животному) преимущественно для терапевтического воздействия, соль, предпочтительно, является фармацевтически приемлемой.
В некоторых случаях аддитивная соль основания изоксазолина формулы (I) может быть получена взаимодействием изоксазолина с приблизительно стехиометрическим количеством неорганического или органического основания, как правило, сильного неорганического или органического основания. Примеры аддитивных солей основания могут включать, например, соли металлов и органические соли. Соли металлов, в частности, включают соли щелочных металлов (группы Ia, например, лития, натрия или калия), соли щелочноземельных металлов (группы IIa, например, бария, кальция и магния), соли тяжелых металлов (например, цинка и железа) и другие физиологически приемлемые соли металлов. Такие соли можно получить с кальцием, литием, магнием, калием, натрием и цинком. Например, изоксазолин в форме свободной кислоты может быть смешан с гидроксидом натрия, с образованием такой аддитивной соли основания.
В некоторых случаях кислотно-аддитивная соль изоксазолина формулы (I) может быть получена взаимодействием изоксазолина с приблизительно стехиометрическим количеством неорганической или органической кислоты. Примеры предполагаемых неорганических кислот для получения фармацевтически приемлемых солей включают хлористоводородную, бромистоводородную, йодистоводородную, азотную, угольную, серную и фосфорную кислоту. Примеры обычно подходящих органических кислот для получения фармацевтически приемлемых солей, как правило, включают, например, органические кислоты алифатического, циклоалифатического, ароматического, аралифатического, гетероциклического, карбонового и сульфонового классов. Конкретные примеры органических кислот включают холевую, сорбиновую, лауриновую, уксусную, трифторуксусную, муравьиную, пропионовую, янтарную, гликолевую, глюконовую, диглюконовую, молочную, яблочную, винную кислоту, лимонную, аскорбиновую, глюкуроновую, малеиновую, фумаровую, пировиноградную, аспарагиновую, глутаминовую кислоту, арилкарбоновую кислоту (например, бензойную), антраниловую кислоту, метансульфоновую кислоту, стеариновую, салициловую, п-гидроксибензойную, фенилуксусную, миндальную, эмбоновую (памовую) кислоту, алкилсульфоновую (например, этансульфоновую) кислоту, арилсульфоновую (например, бензолсульфоновую) кислоту, пантотеновую, 2-гидроксиэтансульфоновую, сульфаниловую, циклогексиламиносульфоновую, -гидроксимасляную, галактаровую, галактуроновую, адипиновую, альгиновую, масляную, камфорную, камфорсульфоновую, циклопентанпропионовую кислоту, додецелсульфоновую кислоту, гликогептановую, глицерофосфорную, гептановую, гексановую, никотиновую, 2-нафталинсульфоновую, щавелевую, пальминовую, пектиновую, 3-фенилпропионовую, пикриновую, пивалиновую, тиоциановую, п-толуолсульфоновую и ундекановую кислоту.
В некоторых случаях органическая соль изоксазолина формулы (I) может быть получена, например, кватернизацией азотсодержащий основной группы изоксазолина таким агентом, как (С1-С6)галогенид (например, метил-, этил-, пропил- и бутилхлорид, бромид или йодид), диалкилсульфат (например, диметил-, диэтил-, дибутил- или диамилсульфат), длинноцепочечные галогениды (например, децил-, лаурил-, миристил- и стеарилхлорид, бромид и йодид), арилалкилгалогенид (например, бензил- и фенетилбромид) и подобными агентами.
Следует иметь в виду, что противоион кислоты или основания может быть, в некоторых случаях, оптически активным (например, соли D-лактат и L-лизина) или рацемическим (например, соли DL-тартрат и DL-аргинина).
К. Сольваты изоксазолинов
В некоторых случаях изоксазолины формулы (I) находятся в форме стабильных комплексов с молекулами растворителя, которые остаются неизменными после того, как не вошедшие в комплекс молекулы растворителя удалены из соединений. Такие комплексы, как правило, относят к «сольватам». В некоторых случаях сольваты можно выделить, например, когда одна или несколько молекул растворителя внедрены в кристаллическую решетку кристаллического твердого вещества. Термин «сольват» охватывает сольваты как в фазе раствора, так и сольваты, которые можно выделить. Примеры подходящих сольватов включают этанолаты, метанолаты и т.п. «Гидрат» представляет собой сольват, в котором молекулой растворителя является молекула воды. Предполагается, что сольват, используемый in vivo, предпочтительно является фармацевтически приемлемым.
L. Пролекарства изоксазолинов
Предполагается, что пролекарства изоксазолинов формулы (I) можно использовать со способами настоящего изобретения. Используемый в данном описании термин «пролекарство» относится к соединению, которое при применении (например, in vivo) может преобразовываться за счет метаболизма или других процессов (например, гидролиза) в изоксазолин формулы (I). В некоторых вариантах осуществления доставка изоксазолина в форме пролекарства является улучшенной доставкой изоксазолина за счет улучшения физико-химических или фармакокинетических свойств, например, за счет усиления системной абсорбции, замедления клиренса или замедления разрушения in vivo.
II. Получение изоксазолинов формулы (I)
Способы получения изоксазолинов известны в данной области. Способы получения различных изоксазолинов формулы (I), например, обсуждаются в публикации патента США US2007/0066617 (включенной в данное описание посредством ссылки), в публикации международной патентной заявки № WO2007/026965 (включенной в данное описание посредством ссылки) и публикации заявки на патент Японии № JP2007/308471 (включенной в данное описание посредством ссылки). Например, в публикации патента США US2007/0066617 обсуждается получение соединения 11-1 в примере 21 на странице 72, получение соединения 5-19 в примере 28 на страницах 74-75, получение соединения 5-61 в примере 30 на страницах 76-77 и получение соединения 5-64 в примере 34 на страницах 77-78; в публикации международной заявки № WO2007/026965 обсуждается получение соединения 5-16 в примере 21 на странице 317, получение соединения 5-25 в примере 22 на страницах 317-318, получение соединения 5-49 в примере 12 на странице 312, получение соединения 5-60 в примере 11 на страницах 311-312 и получение соединения 10-1 в примере 32 на страницах 321-322; и в публикации заявки на патент Японии № JP2007/308471 обсуждается получение соединения 5-45 в примере 38 на странице 381. Кроме того, способы получения различных изоксазолинов также обсуждаются, например, в публикации международной патентной заявки № WO2005/085216 (включенной в данное описание посредством ссылки), международной заявке № РСТ/JP/2008/054096 (включенной в данное описание посредством ссылки), публикации европейской патентной заявки № ЕР1932836 (включенной в данное описание посредством ссылки) и публикации заявки на патент Японии № JP2008/133242 (включенной в данное описание посредством ссылки). Другие изоксазолины формулы (I) можно получить с использованием, например, способов, проиллюстрированных в указанных ссылках, или одних или в комбинации с другими методами, известными в данной области.
III. Способы лечения с использованием композиции настоящего изобретения
Изоксазолины формулы (I), как правило, можно использовать для борьбы с эктопаразитами у животных и, в свою очередь, заболеваниями, непосредственно вызванными такими эктопаразитами, и/или заболеваниями, вызванными патогенами, переносимыми такими эктопаразитами. Предполагается, что композицию можно использовать для лечения ряда животных, в особенности, теплокровных животных. Такие теплокровные животные включают, например, млекопитающих. Млекопитающие включают, например, людей. Другие млекопитающие включают, например, сельскохозяйственных животных или скот (например, свиней, коров, овец, коз и т.д.), лабораторных животных (например, мышей, крыс, малых песчанок и т.д.), домашних животных (например, собак, кошек, лошадей), пушных зверей (например, норок, лис, шиншилл, кроликов и т.д.) и диких животных и животных в зоопарках (например, буйволов, оленей и т.д.). В некоторых вариантах осуществления композиции используют для лечения собак (таких как, например, чистопородные домашние собаки и/или дворняжки, выставочные собаки, ездовые собаки, пастушьи собаки, охотничьи собаки, сторожевые собаки, полицейские собаки, беговые собаки и/или лабораторные собаки). В других вариантах осуществления композиции используют для лечения кошек (например, домашних кошек). Предполагается, что композиции также подходят для лечения немлекопитающих, таких как птицы (например, индейки, куры, гуси, утки, попугаи и т.д.). Также предполагается, что такие композиции могут подходить для лечения холоднокровных животных, таких как, например, рыбы (например, лосось, радужная форель, koi и т.д.).
Согласно настоящему изобретению обнаружено, что изоксазолины формулы (I) имеют особое значение для борьбы с эктопаразитами, т.е. членистоногими, которые являются вредоносными или распространяют заболевания, или действуют как переносчики заболеваний у теплокровных животных. Изоксазолины, как правило, благоприятны для борьбы с паразитами на различных стадиях их жизни, включая стадии яйца, нимфы, личинки, молодую и взрослую стадии. Эктопаразиты (как правило, насекомые и клещи-вредители) включают перечисленных ниже.
А. Жалящие насекомые. К ним относятся, например, мигрирующие личинки двукрылых, таких как, например, виды Hypoderma у крупного рогатого скота, Gastrophilus у лошадей и вид Cuterbra у грызунов; жалящие мухи, такие как, например, кровососущие взрослые мухи (например, жигалка коровья малая (Haematobia irritans), оводы лошадиные (виды Tabanus), оводы обыкновенные (Stomoxys calcitrans), мошки (виды Simulium), оленьи слепни (виды Chrysops), кровососки (Melophagus ovinus), мухи цеце (виды Clossina); паразитические личинки мух, таких как, например, носоглоточных оводов (Oestrus ovis и виды Cuterebra), мясных синих мух (виды Phaencicia), личинки мясной мухи (Cochiliomyia hominivorax), личинки скота (виды Hypoderma) и волосатые черви; и комары, такие как, например, виды Culex, виды Anopheles и виды Aedes.
B. Клещи. К ним относятся
i) виды Mesostigmata, такие как мезостигматиды, которые включают куриных клещей (Dermanyssus gallinae);
ii) виды Astigmata, такие как чесоточные или конские клещи, которые включают виды Sarcoptidae (например, Sarcoptes scabiei); и зудни чесоточные, которые включают виды Psoroptidae (например, Chorioptes bovis и Psoroptes ovis);
iii) виды Prostigmata, такие как клещи, которые включают виды Trombiculidae (например, североамериканские тромбикулиды Trombicula alfreddugesi);
iv) демодексы.
С. Иксодовые клещи. К ним относятся, например, клещи с мягким покровом, такие как виды Argasidae (например, виды Argas и виды Orniyhodoros); и клещи с твердым покровом, такие как виды Ixodidae (например, Ixodes ricinus Rhipicephalus sanguineus, виды Haemaphysalis, Dermacentor reticulates, Dermacentor variabilis, Amblyomma americanum и виды Boophilus).
D. Вши. К ним относятся, например, жалящие вши, такие как виды Menopon и виды Bovicola; и сосущие вши, такие как виды Haematopinus, виды Linognathus и виды Solenopotes.
Е. Блохи. К ним относятся, например, виды Ctenocephalides, такие как блохи собачьи (Ctenocephalides canis) и блохи кошачьи (Ctenocephalides felis); виды Xenopsylla, такие как блохи крысиные южные (Xenopsylla cheopis); виды Pulex, такие как блохи обыкновенные (Pulex irritans); блохи ежей обыкновенных (Archaeopsylla erinacei) и птичьи блохи (Ceratophyllus gallinae).
F. Клопы настоящие полужесткокрылые. К ним относятся, например, Cimcidae или обыкновенный постельный клоп (Cimex lectularius) и виды Triatominae, такие как триатомидные клопы (также известные как триатомиды) (например, Rhodnius prolixus и виды Triatoma).
Термин «заражение» относится к присутствию паразитов в количестве, которое создает риск нарушения или вреда здоровью людей или животных. Они могут присутствовать в окружающей среде (например, в подстилке для животного) или на коже или в шерсти животного и т.д. Если не указано иное, когда заражение имеется в организме животного (например, в крови или других внутренних тканях), предполагается, что термин «заражение» является синонимом термину «инфекция»? как его обычно понимают в данной области.
Выражение «борьба с заражением эктопаразитами» означает уменьшение числа или уничтожение паразитов в организме и/или на животном. Этого можно достичь, например, убивая, отгоняя, удаляя, лишая действенности, замедляя, устраняя, ослабляя или сводя к минимуму активность паразита. Борьба с эктопаразитами может быть борьбой с применением инсектицидов или акарицидов. Действие изоксазолинов может представлять собой действие на яйца, личинки, нимфы, взрослых насекомых или их комбинацией. Кроме того, действие может само проявляться непосредственно в уничтожении паразитов или сразу или по истечении некоторого времени (например, когда происходит линька или путем разрушения яиц). Альтернативно (или дополнительно), действие может само проявиться непосредственно, например, в уменьшении числа отложенных яиц и/или в скорости вылупливания.
Как правило, количество изоксазолина, которое является достаточным для «борьбы» или является «эффективным» против паразита-мишени, представляет собой количество, достаточное для уменьшения числа или уничтожения паразитов в организме и/или на животном и/или для частичного или полного подавления развития паразитарного заражения в организме и/или на животном. Когда изоксазолин вводят системно, эффективное количество, как правило, составляет количество, которое дает в ткани и/или крови концентрации, как правило, токсичные, когда заглатываются паразитом-мишенью.
Специалист в данной области обычно сможет определить «эффективную» дозу, например, наблюдая или детектируя изменения в клиническом состоянии или поведении животного-хозяина, а также наблюдая или детектируя соответствующие изменения числа паразитов после такой обработки. Как правило, доза считается эффективной для борьбы с паразитом-мишенью, когда она достаточна для того, чтобы вызвать снижение имеющегося или возможного количества паразита-мишени по меньшей мере примерно на 5%. В некоторых таких случаях, например, доза считается эффективной, когда она достаточна для того, чтобы вызвать снижение имеющегося или возможного количества паразита-мишени по меньшей мере примерно на 10% (или по меньшей мере примерно на 30%, по меньшей мере примерно на 50%, по меньшей мере примерно на 60%, по меньшей мере примерно на 75%, по меньшей мере примерно на 95% или по меньшей мере примерно на 99%).
Оптимальная дозировка в основном зависит от множества факторов, включающих, например, определенный изоксазолин, идентичность любого(ых) другого(их) активного(ых) ингредиента(ов), который(е) вводят животному-реципиенту, способ введения, тип и тяжесть состояния и патогена-мишени, тип (например, вид и порода), возраст, размер, пол, питание, активность и состояние предполагаемого животного-реципиента и фармакологические соображения, такие как активность, эффективность, фармакокинетический и токсикологический профили изоксазолина и другого(их) активного(ых) ингредиента(ов), который(е) вводят животному-реципиенту. До известной степени многие активные ингредиенты вводят для комбинированного действия на паразита-мишень или состояние, количество каждого ингредиента, составляющего «эффективное количество», является количеством, которое при объединении с другими активными ингредиентами вызывает желаемое действие.
Изоксазолины формулы (I) можно вводить несколько раз для отдельной обработки. Предполагается, что такие многодозовые обработки включают несколько доз в сутки в течение одного или нескольких дней, ежесуточные дозы в течение нескольких дней и/или дозы, вводимые через два или больше дней. Однако в некоторых вариантах осуществления настоящего изобретения однократную дозу вводят для эффективной борьбы с паразитом-мишенью на протяжении длительного периода, такого как, например, по меньшей мере примерно одну неделю. В некоторых таких вариантах осуществления, например, однократная доза является эффективной для борьбы с паразитом-мишенью в течение по меньшей мере примерно 2 недель, по меньшей мере примерно 3 недель, по меньшей мере примерно 1 месяца, по меньшей мере примерно 2 месяцев, по меньшей мере примерно 3 месяцев, по меньшей мере примерно 4 месяцев или по меньшей мере примерно 6 месяцев. Соответственно, в некоторых вариантах осуществления частота обработок может являться, например, еженедельной, раз в две недели, раз в полгода или даже более редкой (например, раз в год). Длительность периодов, на протяжении которых изоксазолины формулы (I) имеют склонность быть эффективными против различных эктопаразитов при системном введении, является неожиданностью. Это, в частности, справедливо, так как обнаружено, что такую длительную активность можно получить во многих случаях с использованием низких доз, которые нетоксичны для животных-реципиентов, при отсутствии требования применения средств, регулирующих высвобождение. Не ограничиваясь какой-либо теорией, предполагается, что такой длительный период активности дают изоксазолины с особенно высокой токсичностью, когда поглощаются паразитом-мишенью.
Для многих животных-реципиентов дозу изоксазолина и композиции выбирают такую, чтобы поддерживать сывороточный уровень изоксазолина по меньшей мере примерно 1 нг/мл (например, 1-50 нг/мл). Как правило, количество изоксазолина, вводимое животному-реципиенту, составляет примерно от 0,001 до примерно 200 мг/кг массы тела. В некоторых вариантах осуществления вводят, например, примерно от 0,01 до примерно 200 мг/кг массы тела. В других вариантах осуществления вводят, например, примерно от 0,001 до примерно 100 мг/кг массы тела. В некоторых таких вариантах осуществления вводят, например, примерно от 0,01 до примерно 100 мг/кг массы тела. В других таких вариантах осуществления вводят, например, примерно от 1 до примерно 30 мг/кг массы тела. Бóльшие дозировки склонны обеспечивать бóльшую длительность активности.
Предполагается, что длительность активности изоксазолина можно увеличить как раз также (или сделав более сообразным) использованием композиции или дозированной формы с регулируемым высвобождением. Например, изоксазолин можно вводить в микросферах, гранулах или имплантатах (например, подкожных имплантатах), которые высвобождают изоксазолин, например, путем диффузии и/или эрозии. Применение такой дозированной формы, содержащей примерно от 1 и до примерно 50 мг/кг массы тела (или примерно от 10 до примерно 30 мг/кг массы тела, как, например, 20 мг/кг массы тела) изоксазолина, может создать возможность для соответствующей активности, длящейся на протяжении нескольких месяцев или дольше (например, года).
В некоторых вариантах осуществления настоящего изобретения изоксазолин формулы (I) вводят для лечения паразитозов у животного (или применяют для получения лекарственного средства для лечения паразитозов у животного). Термин «паразитоз» включает паталогические состояния и заболевания, связанные с или вызванные одним или несколькими эктопаразитами непосредственно, такие как, например, анемия и блошиный аллергический дерматит. Он также включает паталогические состояния или заболевания, связанные с или вызванные одним или несколькими патогенами, переносимыми переносчиками, такие как, например, болезнь Лайма, эрлихиоз (в частности, собачий эрлихиоз) и клещевой тиф Скалистых гор, переносимый иксодовыми клещами. Выражение «лечение паразитозов» означает частичное или полное подавление развития паразитозов у животного, восприимчивого к паразитозам, ослабление или полное устранение симптомов паразитозов у животного с паразитозом и/или частичное или полное излечение паразитоза у животного с паразитозом. Как правило, лечения паразитозов достигают путем введения изоксазолина формулы (I) для борьбы с заражением эктопаразитами.
Настоящее изобретение также относится к способам лечения, в которых по меньшей мере вспомогательной задачей борьбы с эктопаразитами в организме и/или на животном должна быть борьба с заражением эктопаразитами в окружающей среде, в которой находится (периодически или постоянно) животное. В некоторых таких вариантах осуществления, например, животным является домашнее животное (например, кошка или собака). Окружающая среда может представлять собой, например, дом или другое жилище, комнату, загон, стойло или другие помещения для содержания, подстилку и т.д.
Термины «вводить» и «введение» относятся к доставке изоксазолина формулы (I), соли изоксазолина, сольвата изоксазолина или его соли или пролекарства изоксазолина. В некоторых вариантах осуществления настоящего изобретения желательна системная доставка. «Системная доставка» представляет собой доставку в место, отдаленное от места, в котором обитает по меньшей мере часть паразитов. При системной доставке по меньшей мере часть изоксазолина достигает паразита-мишени через кровоток животного-реципиента, другие жидкости организма (лимфатическую жидкость) и/или ткани (например, кожу или жировую ткань). Как правило, паразит поглощает изоксазолин вместе с кровью животного-реципиента, другими жидкостями организма и/или тканью. Системного введения можно достичь в нескольких формах.
В некоторых вариантах осуществления изоксазолиновую композицию вводят системно пероральным путем в единичной дозированной форме, такой как, например, мягкая или твердая капсула, пилюля, порошок, гранулы, таблетка (например, жевательная таблетка), паста, раствор, суспензия (водная или неводная), эмульсия (масло в воде или вода в масле), эликсир, сироп, болюс, большая доза или в корме или питьевой воде для животного-реципиента. Когда композицию вводят с кормом животного, она может скармливаться, например, в виде нормального корма или в виде обработки для жевания. Альтернативно (или дополнительно), она может, например, быть тщательно распределена в постоянном корме животного-реципиента, насыпана на него сверху или использована в форме гранул или жидкости, которые добавляют в готовый корм. Когда композицию вводят в форме кормовой добавки, может быть удобно получить «премикс», в котором композицию распределяют в жидком или твердом носителе. Такой «премикс», в свою очередь, диспергируют в корме животного с использованием, например, обычного смесителя. Когда композицию вводят в питьевой воде животного-реципиента или в виде пропитывающей жидкости, может быть удобным использование композиции в виде раствора или суспензии. Такая композиция может представлять собой, например, концентрированную суспензию, которую смешивают с водой, или сухой препарат, который подмешивают и суспендируют в воде. В обоих случаях предпочтительно иметь изоксазолин в тонко измельченной форме.
Альтернативно (или дополнительно), изоксазолиновую композицию можно вводить местно с использованием трансдермальной композиции (т.е. композиции, которая проникает через кожу). Альтернативно (или дополнительно), композицию можно системно вводить местно через слизистую оболочку. Конкретные композиции для местного введения и введения через слизистую включают, например, примочки, капли, растворы, спреи, муссы, шампуни, порошки, гели, гидрогели, лосьоны, растворы, кремы, мази, порошки-дусты, повязки, пенки, пленки, пэтчи, повязки на конечности, ошейники, ушные метки, облатки, спонжи, волокна, бандажи и микроэмульсии. Способы с примочками и каплями включают, например, нанесение изоксазолиновой композиции на определенный участок кожи или шерстного покрова, такой как на шее или боку животного. Этого можно достичь, например, используя тампон или каплю раствора для примочек или капли к относительно небольшой площади кожи или шерстного покрова животного-реципиента (т.е., как правило, не более чем к 10% кожи или шерстного покрова животного-реципиента). В некоторых вариантах осуществления изоксазолин распределяют от места нанесения на большие площади шерсти из-за смачивающих свойств компонентов в композиции и движений животного, при этом он в то же время параллельно абсорбируется через кожу и распространяется через жидкости организма и/или ткани животного-реципиента.
Альтернативно (или дополнительно), изоксазолиновую композицию может быть системно введена парентерально, например, внутримышечной инъекцией, внтуривенной инъекцией, покожной инъекцией, через имплантат (например, подкожный имплантат), инфузией, болюсной инъекцией и т.д. В некоторых таких вариантах осуществления парентеральная дозированная форма обеспечивает животное-реципиента примерно от 0,01 до примерно 200 мг/кг массы тела изоксазолина.
Другие предполагаемые способы введения включают, например, ректальный и вагинальный способы и ингаляцию (например, тонким распылением или аэрозолем).
IV. Фармацевтические композиции
Настоящее изобретение также относится к фармацевтическим композициям (или лекарственным средствам), содержащим изоксазолин формулы (I), соль изоксазолина, сольват изоксазолина или его соль или пролекарство изоксазолина. Композиции также могут (и, как правило, будут) содержать один или несколько фармацевтически приемлемых эксципиентов.
Фармацевтические композиции по настоящему изобретению можно получить, например, способами, известными в данной области. Такие способы включают, например, различные известные способы смешивания, растворения, грануляции, эмульгирования, инкапсулирования, захвата и лиофилизации. Оптимальная композиция зависит, например, от способа введения.
Твердые дозированные формы могут быть получены, например, тщательным, до однородного состояния, смешиванием изоксазолина с наполнителями, связующими веществами, лубрикантами, глидантами, дезинтегрантами, корригентами (например, подслащивающими веществами), буферами, консервантами, красителями или пигментами фармацевтической категории и веществами, регулирующими высвобождение.
Пероральные дозированные формы, иные, чем твердые, можно получить, смешивая изоксазолин, например, с одним или несколькими растворителями, загустителями, поверхностно-активными веществами, консервантами, стабилизаторами, смолами, наполнителями, связующими веществами, лубрикантами, глидантами, дезинтегрантами, сорастворителями, подслащивающими веществами, корригентами, отдушками, буферами, суспендирующими веществами и красителями или пигментами фармацевтической категории.
Предполагаемые связующие вещества включают, например, желатин, аравийскую камедь и карбоксиметилцеллюлозу.
Предполагаемые лубриканты включают, например, стеарат магния, стеариновую кислоту и тальк.
Предполагаемые дезинтегранты включают, например, кукурузный крахмал, альгиновую кислоту, натрийкарбоксиметилцеллюлозу и натрийкроскармелозу.
Предполагаемые буферы включают, например, цитрат натрия и карбонат и бикарбонат магния и кальция.
Предполагаемые растворители включают, например, воду, вазелин, животные жиры, растительные масла, минеральное масло и синтетическое масло. Также могут быть включены физиологический раствор или гликоли (например, этиленгликоль, пропиленгликоль или полиэтиленгликоль). Растворитель, предпочтительно, имеет обоснованные химические свойства и количество, чтобы изоксазолин оставался в растворе при температурах, при которых композицию хранят и используют.
Предполагаемые загустители включают, например, полиэтилен, метилцеллюлозу, натрийкарбоксиметилцеллюлозу, гидроксипропилметилцеллюлозу, гидроксипропилцеллюлозу, альгинат натрия, карбомер, повидон, аравийскую камедь, гуаровую камедь, ксантановую камедь, трагакант, метилцеллюлозу, алюмосиликат магния, полимеры винилкарбоновых кислот, каррагенан, гидроксиэтилцеллюлозу, лапонит, водорастворимые соли эфиров целлюлозы, природные смолы, коллоидный алюмосиликат магния или тонко измельченный диоксид кремния, гомополимеры акриловой кислоты, сшитые простым эфиром пентаэритрита или простым эфиром сахарозы, и карбомеры.
Предполагаемые поверхностно-активные включают, например, оксиэтилированные эфиры жирных кислот и сорбитана, полиоксиэтиленмоноалкиловые эфиры, моноэфиры сахарозы, сложные и простые эфиры ланолина, соли алкилсульфатов и натриевые, калиевые и аммониевые соли жирных кислот.
Предполагаемые консерванты включают, например, фенол, алкиловые эфиры пара-гидроксибензойной кислоты (например, метил-п-гидроксибензоат (или «метилпарабен») и пропил-п-гидроксибензоат (или «пропилпарабен»)), сорбиновую кислоту, о-фенилфенолбензойную кислоту и ее соли, хлорбутанол, бензиловый спирт, тимеросал, фенилмеркурацетат и -нитрат, нитромерсол, бензалконийхлорид и цетилпиридинийхлорид.
Предполагаемые стабилизаторы включают, например, хелатообразователи и антиоксиданты.
Твердые дозированные формы также могут включать, например, один или несколько эксципиентов, регулирующих высвобождение изоксазолина. Например, предполагается, что изоксазолин можно диспергировать, например, в гидроксипропилметилцеллюлозе. Некоторые пероральные дозированные формы (например, таблетки и пилюли) также можно получить с энтеросолюбильными покрытиями.
Местного введения можно достичь с использованием, например, концентрированного раствора, суспензии (водной или неводной), эмульсии (вода в масле или масло в воде) или микроэмульсии, содержащих изоксазолин, растворенный, суспендированный или эмульгированный в фармацевтически приемлемой жидкой среде. В таких вариантах осуществления, как правило, но необязательно, может присутствовать ингибитор кристаллизации.
Когда жидкую композицию используют местно на коже, ее можно вводить, например, наливанием, намазыванием, растиранием, пульверизацией, разбрызгиванием, окунанием, обмыванием и мытьем. Композицию для наливания или капания, например, можно наливать или разбрызгивать на ограниченном участке на коже (обычно не более чем примерно на 10% кожи). В некоторых таких вариантах осуществления композиция допускает или облегчает проникновение изоксазолина через кожу и действие в других частях организма (например, во всем организме). Такую композицию для наливания или капания можно получить путем растворения, суспендирования или эмульгирования изоксазолина в подходящем соответствующем коже растворителе или смеси растворителей. Также могут быть включены другие эксципиенты, такие как, например, поверхностно-активное вещество, краситель, антиоксидант, стабилизатор, адгезив и т.д. Предполагаемые растворители включают, например, воду, спирт, гликоль, полиэтиленгликоль, полипропиленгликоль, глицерин, бензиловый спирт, фенилэтиловый спирт, феноксиэтиловый спирт, этилацетат, бутилацетат, бензилбензоат, монометиловый эфир дипропиленгликоля, монобутиловый эфир диэтиленгликоля, ацетон, метилэтилкетон, ароматические и/или алифатические углеводороды, растительное или синтетическое масло, ДМФА, жидкий парафин, силикон, диметилацетамид, N-метилпирролидон или 2,2-диметил-4-оксиметилен-1,3-диоксолан.
В некоторых вариантах осуществления местнодействующая (для местного применения) композиция (в частности, композиция для наливания или капания) включает носитель, который промотирует абсорбцию или проникновение изоксазолина через кожу в кровоток, другие жидкости организма (лимфу) и/или ткань организма (жировую ткань). Примеры усилителей дермальной пенетрации включают, например, диметилсульфоксид, изопропилмиристат, пеларгонат дипропиленгликоля, силиконовое масло, алифатические сложные эфиры, триглицериды и жирные спирты.
Местнодействующие композиции также (или альтернативно) могут включать, например, одно или несколько веществ, повышающих смачивающую способность. Такие вещества действуют как носители, которые способствуют распространению активного ингредиента по шерсти или коже животного-реципиента. К ним могут относиться, например, изопропилмеристат, пеларгонат дипропиленгликоля, силиконовые масла, эфиры жирных кислот, триглицериды и/или жирные спирты. Также могут быть подходящими различные комбинации веществ, повышающих смачивающую способность, с маслом/растворителем, такие как, например, масляные растворы, спиртовые растворы и изопропанольные растворы (например, растворы 2-октилдодеканола или олеилового спирта), растворы эфиров монокарбоновых кислот (таких как, например, изопропилмиристат, изопропилпальмитат, лауриловый эфир щавелевой кислоты, олеиловый эфир олеиновой кислоты, дециловый эфир олеиновой кислоты, гексиллаурат, олеилолеат, децилолеат и эфиры насыщенных жирных спиртов с углеродной цепью в 12-18 атомов углерода капроновой кислоты), растворы эфиров дикарбоновых кислот (например, дибутилфталата, диизопропилизофталата, диизопропилового эфира адипиновой кислоты и ди-н-бутиладипата) или растворы эфиров алифатических кислот (например, гликолевых). Когда композиция содержит вещество, повышающее смачивающую способность, также может иметь преимущество включение в нее диспергирующего вещества, такого как, например, пирролидин-1-он, N-алкилпирролидон-2-он, ацетон, полиэтиленгликоль или его простой или сложный эфир, пропиленгликоль или синтетические триглицериды.
Когда композиция имеет, например, форму мази, предполагается, что изоксазолин может быть смешан, например, или с парафиновой или смешивающейся с водой основой мази. Когда композиция имеет форму крема, предполагается, что изоксазолин может быть введен в состав с основой крема «масло в воде». В некоторых случаях водная фаза кремовой основы включает, например по меньшей мере примерно 30% (мас./мас.) многоосновного спирта, такого как пропиленгликоль, бутан-1,3-диол, маннит, сорбит, глицерин, полиэтиленгликоль или их смесь.
Препараты для инъекции можно получить, например, согласно способам, известным в данной области, с использованием подходящих растворителей, солюбилизаторов, стабилизаторов, диспергаторов, смачивающих агентов и/или суспендирующих агентов. Предполагаемые материалы-носители включают, например, воду, этанол, бутанол, бензиловый спирт, глицерин, 1,3-бутанол, раствор Рингера, изотонический раствор хлорида натрия, смесь нелетучих масел (например, синтетических моно- или диглицеридов), растительное масло (например, кукурузное масло), декстрозу, маннит, жирные кислоты (например, олеиновую кислоту), диметилацетамид, поверхностно-активные вещества (например, ионогенные и неионогенные поверхностно-активные вещества), N-метилпирролидон, пропиленгликоль и/или полиэтиленгликоли (например, ПЭГ 400). Предполагаемые солюбилизаторы включают, например, поливинилпирролидон, оксиэтилированное касторовое масло, оксиэтилированный сложный эфир сорбитана и т.п. Предполагаемые стабилизаторы включают, например, бензиловый спирт, трихлорбутанол, эфир п-гидроксибензойной кислоты, н-бутанол и т.п.
В некоторых вариантах осуществления парентеральную композицию получают, например, из стерильных порошков или гранул с одним или несколькими материалами-носителями, указанных выше для других композиций. Изоксазолин, например, растворяют или суспендируют в жидкости, такой как вода, полиэтиленгликоль, пропиленгликоль, этанол, кукурузное масло, хлопковое масло, арахисовое масло, сезамовое масло, бензиловый спирт, раствор хлорида натрия и/или различные буферные растворы. При необходимости можно отрегулировать рН подходящей кислотой или основанием, или буфером.
Для ректального введения можно использовать суппозиторий. Суппозиторий может быть получен, например, смешиванием изоксазолина с подходящим не вызывающим раздражения эксципиентом, который является твердым при обычной температуре, но становится жидким при ректальной температуре, и поэтому будет плавиться в прямой кишке, высвобождая лекарственное средство. Предполагаемые эксципиенты включают, например, масло какао, синтетические моно-, ди- и триглицериды, жирные кислоты и/или полиэтиленгликоли.
При желании обычно в композицию могут быть добавлены другие инертные ингредиенты. Для иллюстрации предполагается, что они могут включать, например, лактозу, маннит, сорбит, карбонат кальция, карбонат натрия, тризамещенный фосфат кальция, дизамещенный фосфат кальция, фосфат натрия, каолин, сжимаемый сахар, крахмал, сульфат кальция, декстро- или микрокристаллическую целлюлозу, коллоидный диоксид кремния, натрийкрахмалгликолят, кросповидон, трагакант, гидроксипропилцеллюлозу, крахмал, набухающий в холодной воде, повидон, этилцеллюлозу, гидроксипропилметиллцеллюлозу и метилцеллюлозу.
Общее обсуждение, касающееся получения лекарственных средств и различных эксципиентов, можно найти, например, у Gennaro A.R. et al., eds., в Remington: The Science and Practice of Pharmacy (Lippincott Williams & Wilkins, 20th Ed., 2000). Еще одно обсуждение, касающееся получения лекарственных средств и различных эксципиентов, можно найти, например, у Liberman H.A. et al., eds., в Pharmaceutical Dosage Forms (Marcel Deeker, New York, N.Y., 1980).
Концентрация изоксазолина формулы (I) (или любой соли изоксазолина, сольвата изоксазолина или его соли или пролекарства изоксазолина) в композиции может изменяться в широких пределах в зависимости, например, от способа введения. Как правило, концентрация составляет примерно от 1 до примерно 70% (по массе). В некоторых таких вариантах осуществления, например, концентрация составляет примерно от 1 до примерно 50% (по массе) или примерно от 10 до примерно 50% (по массе). В других вариантах осуществления концентрация составляет примерно от 35 до примерно 65% (по массе), примерно от 40 до примерно 60% (по массе), примерно от 45 до примерно 55% (по массе) или примерно 50% (по массе).
V. Примеры предполагаемой комбинированной терапии
Способы по настоящему изобретению охватывают способы, в которых изоксазолин является единственным активным ингредиентом, вводимым животному-реципиенту. Однако предполагается, что способы также охватывают комбинированную терапию, при которой изоксазолин вводят в комбинации с одним или несколькими другими активными ингредиентами. Другой(ие) активный(е) ингредиент(ы) может(могут) представлять собой один или несколько других изоксазолинов. Альтернативно (или дополнительно), другой(ие) активный(е) ингредиент(ы) может(могут) представлять собой одно или несколько соединений, которые не являются изоксазолинами. Другой(ие) активный(е) ингредиент(ы) может(могут) предназначаться для тех же самых и/или других патогенов и состояний.
Предполагаемый(е) активный(е) ингредиент(ы), который(е) можно вводить в комбинации с изоксазолином, включает(ют), например, антигельминтные средства, инсектициды и акарициды, регуляторы роста насекомых и аналоги ювенильных гормонов, противовоспалительные средства, антибактериальные средства, гормоны, дерматологические препараты (например, антисептики и дезинфицирующие средства) и иммунобиологические средства (например, вакцины и антисыворотки) для предупреждения заболеваний.
Антигельминтные средства включают, например, авермектины (например, ивермектин, моксидектин и милбемицин), бензимидазолы (например, фенбендазол, альбендазол и триклабендазол), салициланилиды (например, клозантел и оксиклозанид), замещенные фенолы (например, нитроксинил), пиримидины (например, пирантел), имидазотиазолы (например, левамизол), циклооктадепсипептиды (например, эмодепсид) и тетрагидропиримидины (например, празиквантел). Антигельминтные средства также включают, например, производные аминоацетонитрила, такие как, например, производные, описанные Kaminsky R. et al., в «А new class of anthelmintics effective against drug-resistant nematodes», Nature, vol.452, pp. 176-180 (March 13, 2008); и в публикации международных патентных заявок №№ WO2006/050887 и WO2005/044784.
В некоторых вариантах осуществления изоксазолины вводят в комбинации (и в некоторых случаях в одной и той же композиции) с одним или несколькими эндэктоцидными паразитицидами макроциклическими лактонами. Имеется тенденция применения таких паразитицидов против, например, широкого спектра эндопаразитов и эктопаразитов у млекопитающих.
Одним из особенно рассматриваемых паразитоцидов макроциклических лактонов является ивермектин. Ивермектин представляет собой полусинтетическое производное авермектина, которое, как правило, получают в виде смеси по меньшей мере 80% 22,23-дигидроавермектина В1а и менее 20% 22,23-дигидроавермектина B1b. Ивермектин раскрыт в патенте США 4199569. Ивермектин используют в качестве противопаразитарного средства для лечения различных паразитарных заболеваний с середины 1980-х годов.
Другие паразитоциды макроциклические лактоны включают, например:
А. Абамектин. Данное соединение, например, идентифицируют в патенте США 4310519 как авермектин В1а/B1b. Абамектин содержит по меньшей мере 80% авермектина В1а и не более 20% авермектина B1b.
В. Дорамектин. Данное соединение известно как 25-циклогексилавермектин В1. Его строение и получение обсуждаются, например, в патенте США 5089480.
С. Моксидектин. Данное соединение обсуждаются, например, в патенте США 4916154.
D. Селамектин. Данное соединение также известно как моносахарид 25-циклогексил-25-де(1-метилпропил)-5-дезокси-22,23-дигидро-5-(гидроксиимино)авермектина В1.
Е. Милбемицин. Данное соединение также известно как В41. Его выделяют из культуральной жидкости продуцирующего милбемицин штамма Streptomyces. Микроорганизм, условия ферментации и методы выделения обсуждаются, например, в патентах США 3950360 и 3984564.
F. Эмамектин. Данное соединение также известно как 4”-дезокси-4”-эпиметиламиноавермектин В1. Его получение обсуждается, например, в патентах США 5288710 и 5399717. Он представляет собой смесь двух гомологов 4”-дезокси-4”-эпиметиламиноавермектина В1а и 4”-дезокси-4”-эпиметиламиноавермектина B1b. Как правило, используют соль эмамектина. Неограничивающие примеры таких солей обсуждаются в патенте США 5288710, в котором описаны соли, полученные с бензойной кислотой, замещенной бензойной кислотой, бензолсульфоновой кислотой, лимонной кислотой, фосфорной кислотой, винной кислотой и малеиновой кислотой. Особенно обсуждаемой солью является бензоат эмамектина.
G. Эприномектин. Данное соединение также известно как 4”-эпиацетиламино-4”-дезоксиавермектин В1. Он разработан для применения для крупного рогатого скота всех классов и возрастных групп. Он был первым авермектином, показавшим широкий спектр активности против как эндо-, так и экзопаразитов, при этом одновременно оставаясь в мясе и молоке в минимальном количестве. Он, как правило, имеет дополнительное преимущество высокой силы при местной доставке.
Инсектициды и акарициды включают, например, ацефат, ацетампирид, ацетопрол, амитраз, амидофлумет, авермектин, азадирахтин, азинфосметил, бифентрин, бифеназат, бипрофезин, бистрифлурон, карбофуран, картап, хлорфенапир, хлорфлуазурон, хлорантранилпрол, хлорпирифос, хлорпирифосметил, хлормафенозид, клотианидин, цифлутиин, β-цифлутрин, цигалотрин, γ-цигалотрин, λ-цигалотрин, циперметрин, циромазин, дельтаметрин, диафентиурон, диазинон, диэлдрин, дифлубензурон, димефлутрин, диметоат, динотефуран, диофенолан, эмамектин, эндосульфан, эсфенвалерат, этипрол, фенотиокарб, феноксикарб, фенпропатрин, фенвалерат, фипронил, флоникамид, флубендиамид, флуцитринат, тау-флувалинат, флуфенерим, флуфеноксурон, фонофос, галофенозид, гексафлумурон, гидраметилнон, имидаклоприд, индоксакарб, изофенфос, луфенурон, малатион, метафлумизон, метальдегид, метамидофос, метидатион, метопрен, метоксихлор, метофлутрин, монокротофос, метоксифенозид, нитенпирам, нитиазин, новалурон, новифлумурон, оксамил, паратион, паратиориметил, перметрин, форат, фозалон, фосмет, фосфамидори, пиримикарб, профенофос, профлутрин, протрифенбут, пиметрозин, пирафлупрол, пиретрин, пиридалил, пирифлухиназон, пирипрол, пирипроксифен, ротенон, рианодин, спинеторам, спинозад, спиродиклофен, спиромезифен, спиротетрамат, сульпрофос, тебуфенозид, тефлубензурон, тефлутрин, тербофос, тетрахлорвинфос, тиаклоприд, тиаметоксам, тиодикарб, тиосультапнатрий, толфенпирад, тралометрин, триазамат, трихлорфон и трифлумурон. Общие ссылки, в которых обсуждаются противопаразитарные средства, такие как инсектициды и акарициды, включают, например, The Pesticide Manual. 13th Edition, C.D.S. Tomlin, Ed., British Crop Protection Council, Farnham, Surrey, U.K. (2003).
В некоторых предполагаемых вариантах осуществления изоксазолин вводят с производными пиридилметиламина, такими как, например, производные пиридилметиламина, обсуждаемые в Европейской патентной заявке ЕР0539588 или в публикации международной патентной заявки WO2007/115643.
В некоторых предполагаемых вариантах осуществления изоксазолин вводят с нодулиспориновыми (nodulisporic) кислотами и их производными, такими как, например, соединения, обсуждаемые в патентах США 5399582, 5945317, 5962499, 5834260, 6221894 или 5595991 или публикации международной заявки 1996/29073.
Регуляторы роста насекомых включают, например, агридин, диофенолан, феноксикарб, гидропрен, кинопрен, метопрен, пирипроксифен, тетрагидроазадирахтин, хлорфлуазурон, циромазин, дифлубензурон, флуазурон, флуциклоксурон, флуфеноксурон, гексафлумурон, ифенурон, тебуфенозид и трифлумурон. Указанные соединения склонны обеспечивать как начальный, так и длительный контроль за паразитами на всех стадиях развития насекомого, включая яйца, на животном, а также в среде, окружающей животного.
Другие антипаразитарные соединения, предполагаемые для применения в комбинированной терапии с изоксазолином, включают, например, соединения имидазо[1,2-b]пиридазина, обсуждаемые в публикации заявки на патент США № 2005-0182059; соединения 1-(4-моно- и дигалогенметилсульфонилфенил)-2-ациламино-3-фторпропанола, обсуждаемые в патенте США 7361689; соединения простого эфира оксима трифторметансульфонанилида, обсуждаемые в патенте США 7312248; соединения н-[(фенилокси)фенил]-1,1,1-трифторметансульфонамида и н-[(фенилсульфанил)фенил]-1,1,1-трифторметансульфонамида, обсуждаемые в публикации заявки на патент США 2006-0281695; и соединения 2-фенил-3-(1Н-пиррол-2-ил)акрилонитрила, обсуждаемые в публикации заявки на патент США 2006/0128779.
Противовоспалительные средства включают, например, кортикостероиды, которые, в свою очередь, включают, например, дипропионат беклометазона, дипропионат бетаметазона, валерат бетаметазона, будезонид, циклезонид, дефлазакорт, дексаметазон, флуоцинолона ацетонид, пропионат флутиказона, фуроат флутиказона, лотепреднол, этабонат, мометазон и фуроат мометазона, метилпреднизолон, преднизолон, преднизон, рофлепонид и ацетонид триамцинолона. Противовоспалительные средства также включают, например, одно или несколько нестероидных противовоспалительных лекарственных средств («NSAID»). NSAID включают, например, салицилаты, арилалкановые кислоты, 2-арилпропионовые кислоты (или «профены»), N-арилантраниловые кислоты, производные пиразолидина, оксикамы, ингибиторы СОХ-2, сульфонанилиды и ликофелон. Противовоспалительные ингредиенты также могут включать, например, антигистамины. Антигистамины включают, например, агонисты рецептора Н1, агонисты рецептора Н2, агонисты рецептора Н3, агонисты рецептора Н4, стабилизаторы тучных клеток и витамин С.
В предполагаемой комбинированной терапии изоксазолин формулы (I) можно вводить до, одновременно и/или после другого(их) активного(ых) ингредиента(ов). Кроме того, изоксазолин можно вводить в той же композиции, что и другой(ие) активный(ые) ингредиент(ы), и/или в отдельных композициях другого(их) активного(ых) ингредиента(ов). Кроме того, изоксазолин и другой(ие) активный(ые) ингредиент(ы) можно вводить одним и тем же и/или различными способами введения.
Когда изоксазолин вводят в комбинированной терапии, массовое отношение активных ингредиентов может изменяться в широких пределах. Факторы, влияющие на такое отношение, включают, например, определенный изоксазолин, идентичность другого(их) активного(ых) ингредиента(ов), вводимого(ых) в комбинированной терапии, способ(ы) введения изоксазолина и другого(их) активного(ых) ингредиента(ов), состояние мишени и патогена, тип (например, вид и породу), возраст, размер, пол, питание, активность и состояние предполагаемого реципиента, и фармакологические соображения, такие как активность, эффективность, фармакокинетический и токсикологический профили изоксазолина и другого(их) активного(ых) ингредиента(ов). В некоторых предполагаемых вариантах осуществления, например, массовое отношение изоксазолина к другому(им) активному(ым) ингредиенту(ам) составляет, например, примерно от 1:3000 до примерно 3000:1. В некоторых таких случаях массовое отношение составляет примерно от 1:300 до примерно 300:1. В других таких случаях массовое отношение составляет примерно от 1:30 до примерно 30:1.
Предполагается, что кроме других активных ингредиентов изоксазолин можно вводить с одним или несколькими другими соединениями, которые благоприятно влияют на активность (например, усиливают или пролонгируют) (или другие свойства, такие как безопасность) изоксазолина. Например, предполагается, что изоксазолин можно вводить с одним или несколькими синергически действующими лекарственными средствами, такими как, например, пиперонилбутоксид (РВО) и трифенилфосфат (ТРР). Другие синергически действующие лекарственные средства включают, например, N-(2-этилгексил)-8,9,10-тринорборн-5-ен-2,3-дикарбоксамид (также известный как «ENT 8184» или «MGK 264») и вербутин (также известный как «МВ-599»). Обсуждение, относящееся к инсектицидным синергически действующим лекарственным средствам, можно найти, например, в The Pesticide Manual, 13th Edition, цитировано выше.
VI. Терапевтические наборы
Настоящее изобретение также относится к наборам, которые подходят, например, для применения при осуществлении способов лечения, описанных выше. Как правило, такой набор будет включать терапевтически эффективное количество изоксазолина формулы (I) и другой(ие) компонент(ы). Другой(ие) компонент(ы) может(могут) представлять собой, например, одну или несколько из следующих позиций: диагностический инструмент, инструкции по введению композиции, прибор для введения композиции, контейнер, включающий эксципиент или другой активный ингредиент, смешиваемый или вводимый в комбинации с композицией, или памятку (например, ярлык, наклеиваемый на календарь для того, чтобы напомнить владельцу животного время введения следующей дозы композиции).
Примеры
Приведенные ниже примеры являются только пояснительными и не ограничивают настоящее изобретение каким-либо образом. Номера соединений, указанные в приведенных примерах, относятся к номерам структур соединений в приведенном выше подробном описании и в формуле изобретения, приведенной ниже.
Пример 1. Эффективность соединений 10-1 и 11-1 против кошачьих блох (Ctenocephalides felis)
Взрослых блох (2-30) кормят на искусственных мембранах кровью с добавлением соединения 10-1, соединения 11-1 или положительного контроля (фипронил) в концентрации 100, 10 или 1 ч/млн. Эффективность против блох оценивают через 48 час непрерывного кормления, сравнивая число погибших и поврежденных блох с числом питавшихся блох. Эффективность против блох составляет 100% для соединения 10-1, соединения 11-1 и фипронила при концентрации 100, 10 и 1 ч/млн.
Пример 2. Исследования на животной модели для соединения 11-1
Целью таких исследований является оценка эффективности соединения 11-1 против различных паразитов. Паразиты указаны в таблице ниже.
|
А. Эффективность против блох на мышах
Мышей делят на группы по три и обрабатывают местно 100 ч/млн массы тела, перорально 10 мг/кг массы тела или подкожно 10 мг/кг массы тела соединения 11-1, фипронила (положительный контроль) или не обрабатывают (отрицательный контроль). На данных мышей воздействуют седативным средством и заражают их взрослыми блохами (C. felis) через 1, 3, 6 и 24 часа после обработки. Блох снимают с мышей приблизительно после 30-минутного кормления. Оценку подавления блох (% погибших и поврежденных блох) проводят через 1 и 24 часа после каждого заражения. Результаты приведены в таблице 1.
|
Как правило, с соединением 11-1 обнаруживают только несколько поврежденных блох относительно погибших блох. Однако с фипронилом погибших и поврежденных блох, как правило, находят в равных количествах. Какого-либо побочного действия с соединением 11-1 или фипронилом во время данного эксперимента не наблюдают.
В. Эффективность против клещей на мышах
Все мыши, использованные в исследовании, заражены M. musculinus на всех стадиях развития паразита по меньшей мере со средней степенью заражения («++»). Мышей делят на группы по три и обрабатывают местно 100 ч/млн массы тела, перорально 10 мг/кг массы тела или подкожно 10 мг/кг массы тела соединения 11-1, фипронила (положительный контроль) или не обрабатывают (отрицательный контроль). Затем такую обработку повторяют через 7 дней. Степень заражения на мышь («+» = низкая степень заражения, «++» = средняя степень заражения, «+++» = высокая степень заражения) оценивают повторно в дни 1, 6, 9, 13 и 23. Эффективность определяют как снижение степени заражения на обработанных мышах относительно группы отрицательного контроля. Результаты приведены в таблице 2.
|
Какого побочного действия с соединением 11-1 или фипронилом во время исследования эффективности против клещей не наблюдают.
С. Эффективность против клещей с мягким покровом (аргазиды) и постельных клопов на морских свинках
Шесть морских свинок обрабатывают перорально, подкожно или интраперитонеально 10 мг/кг массы тела соединения 11-1 или фипронила (положительный контроль). Морских свинок локально совместно заражают ювенильными клещами с мягким покровом (О. moubata) и постельными клопами (С. lectularius) непосредственно перед обработкой и в различные моменты времени после обработки между днями 2 и 50. Собирают десять насытившихся клещей/клопов, и оценивают процент погибших особей на вид через 24 часа после каждого заражения.
В случае морских свинок, обработанных соединением 11-1, клещи и постельные клопы погибают в течение 1-5 часов после заражения до дня 29 и в течение 8-24 час после дня 29. В случае морских свинок, обработанных фипронилом, клещи и постельные клопы погибают в течение 1-7 часов после заражения до дня 29 и в течение 8-24 час после дня 29. Результаты по эффективности в отношении клещей приведены в таблице 3.
|
Результаты по эффективности в отношении постельных клопов приведены в таблице 4.
|
Какого-либо побочного действия с соединением 11-1 или фипронилом во время данного исследования не наблюдают. Хотя морская свинка, обработанная перорально соединением 11-1 (т.е. животное №1), погибла после дня 31, ее гибель произошла без клинических симптомов и не рассматривается как связанная с обработкой, так как произошла через достаточно длительное время после обработки.
D. Эффективность против клещей с твердым покровом (ixodide) на морских свинках
Морских свинок делят на группы по три. Каждую группу подвергают одной из указанных ниже обработок или соединением 11-1, или фипронилом (положительный контроль), или не подвергают обработке (отрицательный контроль).
Исследование 1
1. Местное введение 100 ч/млн частей массы тела погружением животного.
2. Пероральное введение 10 мг/кг массы тела.
3. Подкожное введение 10 мг/кг массы тела.
4. Без обработки (отрицательный контроль).
Исследование 2
1. Местное введение 100 ч/млн массы тела погружением животного.
2. Пероральное введение 2,5 мг/кг массы тела.
3. Подкожное введение 2,5 мг/кг массы тела.
4. Без обработки (отрицательный контроль).
Накануне обработки всех морских свинок заражают 100 жизнеспособных молодых («нимфа») клещей с твердым покровом (коричневые собачьи клещи, R. sanguineus). Насытившихся отвалившихся нимф считают (eN) со дня 4 по день 8 для вычисления эффективности обработок по следующей формуле:

В дополнение, собранных клещей оценивают на линьку на следующей стадии.
На первой стадии собирают 32 насытившиеся нимфы R. sanguineus с животных необработанной группы отрицательного контроля. И на второй стадии с животных необработанной группы отрицательного контроля собирают 75 насытившихся нимф R. sanguineus. На следующей стадии наблюдают линьку для групп отрицательного контроля обеих стадий. Напротив, нимф какой-либо группы, обработанной соединением 11-1 или фипронилом, ни в каком исследовании не собирают. Таким образом, подавление насытившихся нимф в случае как соединения 11-1, так и фипронила составляет 100%. Какого-либо побочного действия с соединением 11-1 или фипронилом во время любого исследования не наблюдают.
Пример 3. Эффективность различных изоксазолинов против кошачьих блох (Ctenocephalides felis) на мышах
В данном эксперименте мышей произвольно распределяют в группу обработки или группу отрицательного контроля (без обработки). Каждая группа состоит из трех мышей. Мышам в группах обработки вводят перорально по 20 мг/кг массы тела различных изоксазолинов, растворенных в 7% ДМФА-премиксе и 93% дистиллированной воды (вода для инъекций). Наносимый объем при таких обработках составляет 0,1 мл/г массы тела. Через час после обработки на каждую мышь воздействуют седативным средством и, как правило, заражают (по всему телу) 30 жизнеспособными взрослыми блохами (С. felis). Для того чтобы этого достичь, мышей под действием седативного средства помещают непосредственно в банку для заражения паразитами, и блох помещают непосредственно на шерсть. Приблизительно через 30 минут насыщения блох собирают с мышей. Оценки подавления и летальности проводят через 1 час, 24 часа и 48 часов после каждого заражения. Эффективность вычисляют как процент подавленных блох в обработанных группах относительно группы отрицательного контроля.
(Мс-Mt)
Эффективность в отношении блох (%)=--------×100.
Мс
Результаты по эффективности приведены в таблице 5. Все обработки, показанные в таблице 5, хорошо переносятся мышами.
|
|
|
Пример 4. Эффективность различных изоксазолинов против коричневых собачьих клещей (Rhipicephalus sanguineus) на морских свинках
В данном эксперименте морских свинок произвольно распределяют в группу обработки или группу отрицательного контроля (без обработки). Каждая группа состоит из трех морских свинок. В день ноль каждую морскую свинку заражают 100 жизнеспособных нимф R. sanguineus. В день 1 морским свинкам в группах обработки перорально вводят 10 мг/кг массы тела различных изоксазолинов, растворенных в 7% ДМФА-премиксе и 93% дистиллированной воды (вода для инъекций). Насытившихся отвалившихся нимф считают (eN) со дня 4 по день 8 для вычисления эффективности изоксазолинов по следующей формуле:

В дополнение, собранных клещей оценивают на линьку на следующей стадии. Результаты по эффективности приведены в таблице 6. Какого-либо побочного действия с каким-либо из испытываемых соединений, представленных в таблице 6, во время исследования не наблюдают.
|
Пример 5. Эффективность соединения 11-1 против кошачьих блох (С. felis) и коричневых собачьих клещей (R. sanguineus) на собаках
В день ноль одну группу из 4 биглей обрабатывают перорально желатиновыми капсулами, содержащими 20 мг/кг массы тела соединения 11-1. Другую группу из 4 биглей обрабатывают местно мытьем 2 л раствора, содержащего 200 ч/млн массы тела соединения 11-1, растворенного в ДМФА-премиксе/водопроводной воде (1:100, по объему). Наконец, группу из 3 биглей оставляют необработанной в качестве отрицательного контроля. За два дня до обработки в день ноль всех биглей заражают приблизительно 80 голодными взрослыми блохами (С. felis) и приблизительно 60 голодными коричневыми собачьими клещами (R. sanguineus). Паразитарную нагрузку на каждого бигля оценивают в день 2 (приблизительно через 48 час после обработки), удаляя и подсчитывая блох и клещей. Блох и клещей классифицируют по жизнеспособности (блохи: погибшие или живые; клещи: погибшие или живые и насытившиеся или ненасытившиеся). Эффективность вычисляют из среднего числа живых блох и клещей в обработанной группе (Mt) относительно среднего числа живых блох и клещей в необработанной контрольной группе (Мс) с использованием следующей формулы:

Соединение 11-1 показывает эффективность в отношении блох и клещей 100% после пероральной и местной обработки. Какого-либо побочного действия во время данного исследования не наблюдают.
Пример 6. Дополнительное исследование эффективности соединения 11-1 против кошачьих блох (С. felis) и коричневых собачьих клещей (R. sanguineus) на собаках
Биглей произвольно распределяют в 5 групп обработки по 4 животных в каждой и в одну контрольную группу без обработки из 3 животных. Собак в группах обработки обрабатывают в день ноль, как показано в таблице 7.
|
Собак заражают приблизительно 80 блохами (С. felis) и 60 коричневыми собачьими клещами (R. sanguineus) в дни -2, 7, 14, 21, 28, 35, 42 и 49. Блох и клещей считают в день 2 (приблизительно 48 час после обработки), а также в дни 9, 16, 23, 30, 37, 44 и 51 (приблизительно 48 час после каждой обработки после повторного заражения) для оценки инсектицидной и акарицидной активности в обработанных группах. В группе В проводят дополнительное заражение блохами и клещами в день 56 с соответствующим подсчетом блох и клещей в день 58. Кроме подсчета блох и клещей берут образцы крови перед обработками, а также приблизительно через 2 часа, 4 час, 8 час, 24 часа и 72 часа после обработки в день ноль и затем один раз в каждый из дней 7, 14, 21, 28, 35, 42, 49 и 56. Концентрацию соединения 11-1 в плазме крови анализируют ВЭЖХ/МС/МС. LOQ такого способа составляет 5 нг/мл. В таблице 8 показана наблюдаемая эффективность против клещей.
|
В таблице 9 показана наблюдаемая эффективность против блох.
|
Наблюдаемая средняя концентрация соединения 11-1 в плазме на протяжении исследования показана на фиг.1. На фиг.1 данные «РО» относятся к группе А, данные «SC» относятся к группе B, данные «TOP W/УСИЛИТЕЛЬ» относятся к группе C данные «TOP W/УСИЛИТЕЛЬ И СМАЧИВАТЕЛЬ» относятся к группе D, и данные «TOP W/ЭТИЛЛАКТАТА» относятся к группе E. Результаты для группы F на фиг.1 не приведены, поскольку задано, что указанной группе соединение 11-1 не вводят.
Пример 7. Выделение R- и S-изомеров соединения 11-1
Соединение 11-1 (260 мг) растворяют в смеси н-гексан/этанол 1:1 (13 мл) при 40°С. Разделяют 80% полученного раствора на аликвоты по 400 мкл на системе полупрепаративной жидкостной хроматографии, снабженной колонкой Diacel Chiralpack® AD-H длиной 250 мм, диаметром 10 мм и с частицами размером 5 мкм. Подвижная фаза состоит из смеси н-гексан/этанол 8:2. Используют скорость потока 4 мл/мин. Хиральные фракции обоих энантиомеров собирают и упаривают в вакууме. Чистоту собранных фракций контролируют аналитической хиральной хроматографией с использованием колонки Diacel Chiralpack® AD-H (250 мм×4,6 мм, 5 мкм) и УФ-детекции при 254 нм. Для обоих энантиомеров определяют, что чистота превышает 99%. Такой метод дает 88 мг соединения 17-1 (S-энантиомер), который имеет оптическое вращение [α]D 23 +63,97° (этанол, с=2,97 мг/мл); и 80 мг соединения 11-1R (R-энантиомер), который имеет оптическое вращение [α]D 23 -61,07° (этанол, с=3,93 мг/мл).
Слова «включать», «включает» и «включение» следует интерпретировать включительно, а не исключительно. Предполагается, что такая интерпретация аналогична интерпретации указанных слов, которая приводится в Законе о патентах Соединенных Штатов.
Термин «фармацевтически приемлемый» используется как прилагательное для обозначения соответствия определяемого существительного использованию в фармацевтическом продукте. Когда его используют, например, для описания соли, эксципиента или сольвата, он характеризует соль, эксципиент или сольват как совместимые с другими ингредиентами композиции и не вредоносные для предполагаемого животного-реципиента до степени, при которой вредоносное(ые) действие(я) превышает(ют) благоприятное(ые) действие(я) соли, эксципиента или сольвата.
Все ссылки, цитированные в данном описании, включены в данное описание посредством ссылок.
Приведенное выше подробное описание предпочтительных вариантов осуществления предназначено только для ознакомления специалистов в данной области с изобретением, его принципами и его практическим применением, так что специалисты в данной области смогут адаптировать и применять изобретение в его многочисленных формах, которые могут наилучшим образом подходить для определенного применения. Поэтому настоящее изобретение не ограничивается описанными выше вариантами осуществления и может широко варьироваться.