Результат интеллектуальной деятельности: ЛИПОСОМЫ С ЛИПИДАМИ, ИМЕЮЩИМИ ПРЕИМУЩЕСТВЕННОЕ ЗНАЧЕНИЕ РКА, ДЛЯ ДОСТАВКИ РНК
Вид РИД
Изобретение
Данная заявка заявляет приоритет предварительных заявок на патент США 61/361830 (поданной 6 июля 2010) и 61/378837 (поданной 31 августа 2010), полное содержание обеих заявок включено в данный документ для сведения для всех целей.
Область техники, к которой относится изобретение
Данное изобретение относится к области невирусной доставки РНК для иммунизации.
Уровень техники
В течение нескольких лет доставка нуклеиновых кислот для иммунизации животных является целью научных исследований. Тестировались различные подходы, при применении ДНК или РНК, такие как доставка с использованием вирусных и невирусных носителей (даже доставка без носителя в «голой» вакцине) реплицирующихся или нереплицирующихся векторов или вирусных, или невирусных векторов.
Остается потребность в дополнительных и улучшенных нуклеиновокислотных вакцинах.
Раскрытие изобретения
Согласно изобретению РНК, кодирующую иммуноген, доставляют в липосоме в целях иммунизации. Липосома включает липиды, которые имеют значение pKa в пределах от 5,0 до 7,6. В идеальном варианте липид со значением pKa в данных пределах содержит третичный амин; такие липиды ведут себя иначе по сравнению с липидами, такими как DOTAP или DC-Chol, которые содержат группу четвертичного амина. При физиологических значениях рН амины с pKa в пределах от 5,0 до 7,6 имеют нейтральный или пониженный поверхностный заряд, в то время как липид, такой как DOTAP, является сильно катионным. Заявители настоящего изобретения установили, что липосомы, образованные липидами с четвертичным амином (например, DOTAP), являются менее подходящими для доставки иммуноген-кодирующей РНК, чем липосомы, образованные липидами с третичным амином (например, DLinDMA).
Таким образом, изобретение относится к липосоме, имеющей липидный бислой, инкапсулирующий водное ядро, где (i) липидный бислой содержит липид, имеющий значение pKa от 5,0 до 7,6, и предпочтительно содержащий третичный амин, и (ii) водное ядро включает РНК, которая кодирует иммуноген. Такие липосомы подходят для доставки в условиях in vivo РНК в клетку позвоночных животных и, таким образом, они пригодны в качестве компонентов в фармацевтических композициях для иммунизации субъектов против вирусных заболеваний.
Изобретение также относится к способу получения РНК-содержащей липосомы, включающему стадии: (а) смешивание РНК с липидом при рН, который ниже pKa липида, но который выше 4,5, с образованием липосомы, в которой инкапсулирована РНК; и (b) повышение рН полученной липосома-содержащей смеси до значения, которое выше pKa липида.
Липосома
В изобретении используются липосомы, в которых инкапсулирована РНК, кодирующая иммуноген. Таким образом, РНК отделена (как и в природном вирусе) от внешней среды липидным бислоем липосомы, и было установлено, что такое инкапсулирование защищает РНК от расщепления РНКазой. Липосомы могут включать некоторое количество внешней РНК (например, на их поверхности), но, по меньшей мере, половина РНК (и в идеальном варианте вся РНК) инкапсулирована в ядре липосомы. Инкапсулирование в липосомах отличается, например, от комплексов липид/РНК, раскрытых в источнике 1.
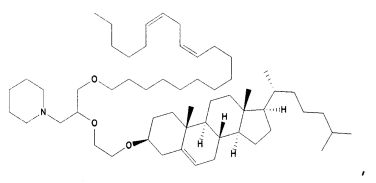
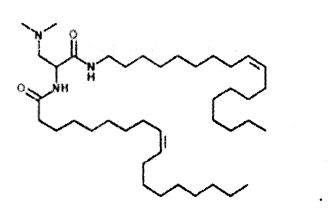
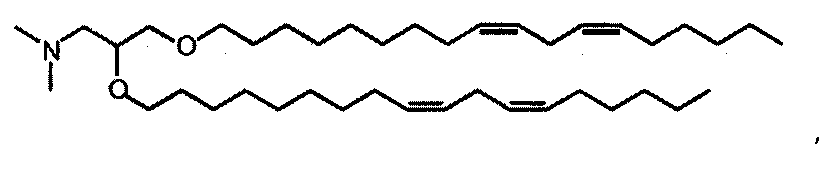
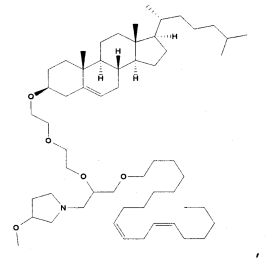
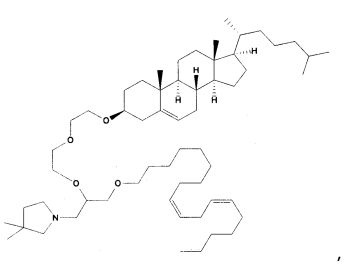
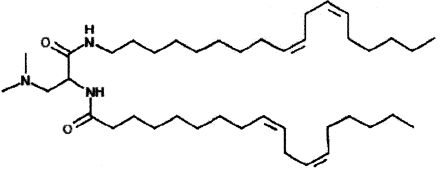
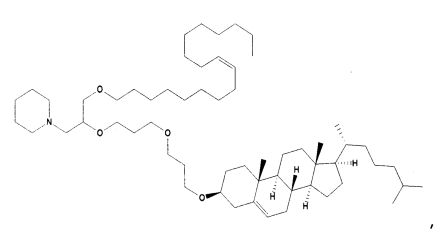
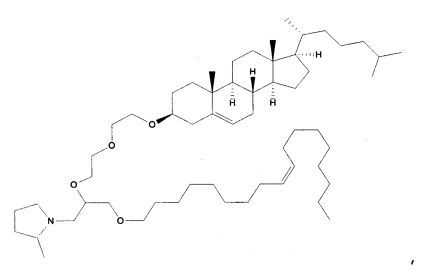
Различные амфифильные липиды могут образовать бислои в водной среде с инкапсулированием РНК-содержащего водного ядра в виде липосомы. Такие липиды содержат анионную, катионную или цвитерионную гидрофильную «головку». Липосомы по изобретению содержат липид, имеющий значение pKa в пределах от 5,0 до 7,6, и предпочтительные липиды с pKa в этих пределах содержат третичный амин. Например, они могут содержать 1,2-дилинолеилокси-N,N-диметил-3-аминопропан (DLinDMA; pKa 5,8) и/или 1,2-дилиноленилокси-N,N-диметил-3-аминопропан (DLenDMA). Другим подходящим липидом, содержащим третичный амин, является 1,2-диолеилокси-N,N-диметил-3-аминопропан (DODMA). Смотри фиг.3 и источник 2. Также можно использовать некоторые аминолипиды из источника 3, а также некоторые аминолипиды из источника 4. Дополнительные подходящие липиды с третичными аминами в их «головках» раскрыты в источнике 5, полное содержание которого включено в данный документ для сведения.
Липосомы по изобретению также можно получить из одного липида или из смеси липидов, при условии, что, по меньшей мере, один из липидов имеет значение pKa в пределах от 5,0 до 7,6 (и предпочтительно содержит третичный амин). В данных пределах значений pKa предпочтительные липиды имеют pKa от 5,5 до 6,7, например, в пределах от 5,6 до 6,8, от 5,6 до 6,3, от 5,6 до 6,0, от 5,5 до 6,2 или от 5,7 до 5,9. pKa представляет рН, при котором 50% липидов заряжено, находясь в середине между точкой, при которой липиды полностью заряжены, и точкой, при которой липиды полностью не заряжены. Этот показатель можно определить различными путями, но предпочтительно с использованием способа, раскрытого ниже в разделе под заголовком «Определение pKa». Как правило, pKa следует определять для одного липида в большей степени, чем для липида в контексте смеси, которая также включает другие липиды (например, отлично от того, как описано в источнике 6, который в большей степени относится к pKa SNALP, чем для отдельных липидов).
Когда липосому по изобретению получают из смеси липидов, то предпочтительно, чтобы относительное количество липидов, которые имеют pKa в требуемых пределах, составляло 20-80% от общего содержания липидов в смеси, например, находилось в пределах 30-70% или 40-60%. Например, ниже показаны подходящие липосомы, в которых 40% или 60% от общего содержания липидов представлял липид с pKa в требуемых пределах. Остальная часть может представлять, например, холестерин (например, в смеси может находиться 35-50% холестерина) и/или DMG (необязательно ПЭГилированного), и/или DSPC. Такие смеси используются ниже. Такие % значения являются моль процентами.
Липосома может содержать амфифильный липид, в котором гидрофильный фрагмент ПЭГилирован (т.е. модифицирован ковалентным присоединением полиэтиленгликоля). Такая модификация может повысить стабильность и предупредить неспецифическую адсорбцию липосом. Например, липиды можно конъюгировать с ПЭГом с использованием методов, которые раскрыты в источниках 6 и 7. ПЭГ обеспечивает липосомы с оболочкой, которая придает ей благоприятные фармакокинетические свойства. Сочетание эффективного инкапсулирования РНК (в частности, самореплицирующейся РНК), катионного липида, имеющего значение pKa в пределах 5,0-7,6 и ПЭГилированной поверхности обеспечивают эффективную доставку к многочисленным типам клеток (включая иммунные и неиммунные клетки), тем самым вызывая более сильный и лучший иммунный ответ по сравнению с тем, когда используются четвертичные амины без ПЭГилирования. Можно использовать ПЭГ молекулярной массы, например, 0,5-8 kDa.
Липиды, используемые по изобретению, могут быть насыщенными или ненасыщенными. Применение, по меньшей мере, одного ненасыщенного липида для получения липосом является предпочтительным. На фиг.3 показано три подходящих ненасыщенных липида. Если ненасыщенный липид имеет два «хвоста», то оба «хвоста» могут быть ненасыщенными, или он может иметь один насыщенный «хвост» или ненасыщенный «хвост».
В примерах используется смесь DSPC, DLinDMA, PEG-DMG и холестерина. Независимым аспектом изобретения является липосома, содержащая DSPC, DLinDMA, ПЭГ-DMG и холестерин. Такая липосома предпочтительно инкапсулирует РНК, такую как самореплицирующаяся РНК, например, кодирующая иммуноген.
Липосомальные частицы обычно разделяют на три группы: мультиламеллярные везикулы (MLV); небольшие униламеллярные везикулы (SUV) и крупные униламеллярные везикулы (LUV). MLV имеют многочисленные бислои в каждой везикуле, образуя несколько отдельных водных компартментов. SUV и LUV имеют один бислой, инкапсулирующий водное ядро; как правило, SUV имеют диаметр ≤50 нм, и LUV имеют диаметр >50 нм. В идеальном варианте липосомальные частицы по изобретению являются LUV с диаметром в пределах 50-220 нм. Для композиции, содержащей популяцию LUV с различными диаметрами, имеются следующие условия: (i) по меньшей мере, 80% по количеству должно иметь диаметры в пределах 20-220 нм, (ii) в идеальном варианте средний диаметр (Zav по интенсивности) в популяции находится в пределах 40-200 нм и/или (iii) диаметры должны иметь показатель полидисперсности <2. Полагают, что комплексы липосома/РНК из источника 1 имеют диаметр в пределах 600-800 нм, и для них характерна высокая полидисперсность. Липосома должна быть по существу сферической.
Способы приготовления подходящих липосом являются хорошо известными в данной области, например, смотри источники 8-10. Один подходящий способ описан в источнике 11, и он включает смешивание (i) этанольного раствора липидов, (ii) водного раствора нуклеиновой кислоты и (iii) буфера с последующим перемешиванием, уравновешиванием, разведением и выделением. Предпочтительные липосомы по изобретению получают данным способом смешивания.
Способ смешивания
Как уже указывалось выше, изобретение относится к способу получения РНК-содержащей липосомы, включающему стадии: (а) смешивания РНК с липидом при рН, который ниже значения pKa липида, но выше 4,5; затем (b) повышение рН до значения, которое выше pKa липида.
Таким образом, катионный липид положительно заряжен во время образования липосомы на стадии (а), но затем изменение рН означает, что большинство (или все) положительно заряженные группы становятся нейтральными. Такой способ является преимущественным для приготовления липосом по изобретению, и избегая достичь рН ниже 4,5 на стадии (а), повышается стабильность инкапсулированной РНК.
Значения рН на стадии (а) находятся выше 4,5, и в идеальном варианте выше 4,8. Используя рН в пределах от 5,0 до 6,0 или в пределах 5,0 до 5,5, можно получить подходящие липосомы.
Повышенное значение рН на стадии (b) выше значения pKa липида. В идеальном варианте рН повышают до рН ниже 9 и предпочтительно ниже 8. В зависимости от pKa липида рН на стадии (b) можно, таким образом, повысить до пределов 6-8, например, до рН, равного 6,5±0,3. Повышения рН на стадии (b) можно достичь переносом липосом в подходящий буфер, например, забуференный фосфатом физиологический раствор. В идеальном варианте повышение рН на стадии (b) моно провести после образования липосом.
РНК, используемая на стадии (а), может находиться в водном растворе, который смешивают с органическим раствором липида (например, этанольным раствором, как описано в источнике (11)). Затем смесь разводят с получением липосом, после чего рН можно повысить на стадии (b).
РНК
Изобретение является подходящим для доставки в условиях in vivo РНК, которая кодирует иммуноген. РНК транслируется неиммунными клетками в месте доставки, приводя к экспрессии иммуногена, и она также стимулирует иммунные клетки к секреции интерферонов I и/или провоспалительных цитокинов, которые обеспечивают местный адъювантный эффект. Неиммунные клетки также могут секретировать интерфероны типа I и/или провоспалительные цитокины в ответ на РНК.
РНК является плюс-цепочечной и, таким образом, может транслироваться неиммунными клетками без необходимости в каких-либо промежуточных стадиях репликации, таких как обратная транскрипция. Она также может связываться с рецепторами TLR7, которые экспрессируются иммунными клетками, тем самым инициируя адъювантный эффект.
Предпочтительные плюс-цепочечные РНК являются самореплицирующимися молекулами. Молекула самореплицирующейся РНК (репликон), когда доставляется в клетки позвоночных животных даже без каких-либо белков, приводит к продукции многочисленных дочерних РНК транскрипцией из нее самой (посредством антисмысловой копии, которую она генерирует из себя самой). Таким образом, молекула самореплицирующейся РНК обычно представляет плюс-цепочечную молекулу, которая может непосредственно транслироваться после доставки в клетку, и такая трансляция обеспечивает РНК-зависимую РНК-полимеразу, которая затем продуцирует антисмысловые и смысловые транскрипты из доставленной РНК. Таким образом, доставленная РНК приводит к продукции многочисленных дочерних копий РНК. Такие дочерние РНК, а также коллинеарные субгеномные транскрипты, могут транслировать самих себя с обеспечением экспрессии in situ кодированного иммуногена, или могут транскрибироваться с обеспечением дополнительных транскриптов с тем же смыслом, что и доставленная РНК, которые транслируются с обеспечением экспрессии in situ иммуногена. В целом результаты данной последовательности транскрипций представляют высокую амплификацию копий введенных РНК-репликонов и, таким образом, кодированный иммуноген становится основным полипептидным продуктом клеток.
Как показано ниже, для РНК не требуется самореплицирующейся активности для обеспечения адъювантного эффекта, хотя, она может повысить секрецию цитокинов после трансфекции. Самореплицирующаяся активность является особенно пригодной для достижения высокого уровня экспрессии иммуногена неиммунными клетками. Она также может повысить апоптоз неиммунных клеток.
Одной подходящей системой для достижения саморепликации является применение РНК-репликона на основе альфа-вируса. Такие плюс-цепочечные репликоны транслируются после доставки в клетку с получением репликазы (или репликазы-транскриптазы). Репликаза транслируется в виде полипротеина, который саморасщепляется с обеспечением комплекса репликации, который продуцирует геномные минус-цепочечные копии плюс-цепочечной доставленной РНК. Такие минус-цепочечные транскрипты могут транскрибировать их самих с образованием дополнительных копий плюс-цепочечной исходной РНК и также могут генерировать субгеномный транскрипт, который кодирует иммуноген. Трансляция субгеномного транскрипта, таким образом, приводит к экспрессии in situ иммуногена инфицированной клеткой. В подходящих репликонах на основе альфа-вирусов можно использовать репликазу из вируса Синдбис, вируса леса Семлики, вируса восточного энцефалита лошадей, вируса венесуэльского энцефалита лошадей и т.д. В репликонах могут использоваться последовательности мутантных вирусов или вирусов дикого типа, например, аттенуированный мутант TC83 VEEV [12].
Таким образом, предпочтительная молекула самореплицирующейся РНК кодирует (i) РНК-зависимую РНК-полимеразу, которая может транскрибировать РНК из молекулы самореплицирующейся РНК, и (ii) иммуноген. Полимераза может представлять репликазу альфа-вируса, например, включающую один или более альфа-вирусных белков nsP1, nsP2, nsP3 и nsP4.
Несмотря на то, что геномы природных альфа-вирусов кодируют структурные белки вирионов в дополнении к неструктурному полибелку репликазы, предпочтительно, чтобы молекула самореплицирующейся РНК по изобретению не кодировала структурные белки альфавирусов. Таким образом, предпочтительная самореплицирующаяся РНК может приводить к продукции копий геномной РНК ее самой в клетке, но не продуцировать РНК-содержащие вирионы. Отсутствие способности продуцировать такие вирионы означает, что в отличие от альфа-вируса дикого типа, молекула самореплицирующейся РНК не может сохранять себя в инфекционной форме. Структурные белки альфа-вируса, которые необходимы для сохранения в вирусах дикого типа, отсутствуют из самореплицирующихся РНК по изобретению и их место занято геном(и), кодирующими интересующих иммуноген, так, что субгеномный транскрипт кодирует иммуноген в большей степени, чем структурные белки альфа-вирусного вириона.
Таким образом, молекула самореплицирующейся РНК, подходящая для изобретения, может иметь две открытых рамки считывания. Первая (5') открытая рамка считывания кодирует репликазу; вторая (3') открытая рамка считывания кодирует иммуноген. В некоторых вариантах осуществления РНК может иметь дополнительные (например, даунстрим) открытые рамки считывания, например, для кодирования дополнительных иммуногенов (смотри ниже) или для кодирования вспомогательных полипептидов.
Молекула самореплицирующейся РНК может содержать 5'-последовательность, которая совместима с кодированной репликазой.
Молекулы самореплицирующейся РНК могут иметь различную длину, но, как правило, их длина составляет 5000-25000 нуклеотидов, например, 8000-15000 нуклеотидов или 9000-12000 нуклеотидов. Таким образом, РНК длиннее, чем длина, наблюдаемая в системе siPHK доставки.
Молекула РНК, подходящая для изобретения, может содержать 5'-кэп (например, 7-метилгуанозин). Такая кэп-структура может повышать трансляцию РНК in vitro.
5'-нуклеотид молекулы РНК, подходящей для изобретения, содержит 5'-трифосфатную группу. В кэпированной РНК она может быть связана с 7-метилгуанозином посредством 5'-5' мостика. 5'-трифосфат может повышать связывание с RIG-I и, таким образом, стимулировать адъювантные эффекты.
Молекула РНК может содержать 3'-поли-А-хвост. Она также может содержать последовательность распознавания поли-А-полимеразы (например, AAUAAA) около 3'-конца.
Молекула РНК, подходящая для изобретения, как правило, является одноцепочечной. Одноцепочечные РНК обычно инициируют адъювантный эффект посредством связывания с TLR7, TLR8, РНК-геликазами и/или PKR. Доставленная в двухцепочечной форме РНК (dsPHK) может связываться c TLR3, и этот рецептор также может запускаться dsPHK, которая образуется во время репликации одноцепочечной РНК или находится во вторичной структуре одноцепочечной РНК.
Молекулу РНК, подходящую для изобретения, можно соответственно получить транскрипцией в условиях in vitro (IVT). При IVT можно использовать матрицу (кДНК), полученную и размноженную в плазмидной форме в бактериях, или получить синтетически (например, методами генной инженерии, синтезом гена и/или полимеразной цепной реакцией (ПЦР)). Например, ДНК-зависимую РНК-полимеразу (такую как РНК-полимеразы бактериофага Т7, Т3 или SP6) можно использовать для транскрибирования РНК с ДНК-матрицы. Можно использовать соответствующие реакции кэпирования и поли-А-добавления, в зависимости от того, что требуется (хотя, поли-А-хвост репликона обычно кодирован в ДНК-матрице). Такие РНК-полимеразы могут иметь строгие требования для транскрибированного 5'-нуклеотида(в), и в некоторых вариантах осуществления такие требования должны соответствовать требованиям кодированной репликазы для гарантии того, что транскрибированная IVT РНК может эффективно функционировать в качестве субстрата для ее самокодированной репликазы.
Как обсуждается в источнике 13, самореплицирующаяся РНК может содержать (в дополнении к 5'-кэпированной структуре) один или более модифицированных азотистых оснований. Таким образом, РНК может включать m5C (5-метилцитидин), m5U (метилуридин), m6A (N6-метиладенозин), s2U (2-тиоуридин), Um (2'-О-метилуридин), m1A (1-метиладенозин); m2A (2-метиладенозин); Am (2'-О-метиладенозин); ms2m6A (2-метилтио-N6-метиладенозин); i6A (N6-изопентениладенозин); ms2i6A (2-метилтио-N6-изопентениладенозин); io6A (N6-(цис-гидроксиизопентенил)аденозин); ms2io6A (2-метилтио-N6-(цис-гидроксиизопентенил)аденозин); g6A (N6-глицинилкарбамоиладенозин); t6A (N6-треонилкарбамоиладенозин); ms2t6A (2-метилтио-N6-треонилкарбамоиладенозин); m6t6A (N6-метил-N6-треонилкарбамоиладенозин); hn6A (N6-гидроксинорвалилкарбамоиладенозин); ms2hn6A (2-метилтио-N6-гидроксинорвалилкарбамоиладенозин); Ar(p) (2'-О-рибозиладенозин (фосфат)); I (инозин); m11 (1-метилинозин); m'Im (1,2'-О-диметилинозин); m3C (3-метилцитидин); Cm (2Т-О-метилцитидин); s2C (2-тиоцитидин); ас4С (N4-ацетилцитидин); f5C (5-фоннилцитидин); m5Cm (5,2-О-диметилцитидин); ac4Cm (N4-ацетил-2ТО-метилцитидин); k2C (лизидин); m1G (1-метилгуанозин); m2G (N2-метилгуанозин); m7G (7-метилгуанозин); Gm (2'-О-метилгуанозин); m22G (N2,N2-диметилгуанозин); m2Gm (N2,2'-O-диметилгуанозин); m22Gm (N2,N2,2'-O-триметилгуанозин); Gr(p)(2'-O-рибозилгуанозин (фосфат)); yW (вибутозин); o2yW (пероксивибутозин); OHyW (гидроксивибутозин); OHyW* (немодифицированный гидроксивибутозин); imG (виозин); mimG (метилгуанозин); Q (квеозин); oQ (эпоксиквеозин); galQ (галтактозилквеозин); manQ (маннозилквеозин); preQ (7-циано-7-деазагуанозин); preQi (7-аминометил-7-деазагуанозин); G (археозин); D (дигидроуридин); m5Um (5,2'-О-диметилуридин); s4U (4-тиоуридин); m5s2U (5-метил-2-тиоуридин); s2Um (2-тио-2'-О-метилуридин); acp3U (3-(3-амино-3-карбоксипропил)уридин); ho5U (5-гидроксиуридин); mo5U (5-метоксиуридин); cmo5U (уридин-5-оксиуксусную кислоту); mcmo5U (метиловый эфир уридин-5-оксиуксусной кислоты); chm5U (5-(карбоксигидроксиметил)уридин)); mchm5U (метиловый эфир 5-(карбоксигидроксиметил)уридина)); mcm5U (5-метоксикарбонилметилуридин); mcm5Um (S-метоксикарбонилметил-2-О-метилуридин); mcm5s2U (5-метоксикарбонилметил-2-тиоуридин); nm5s2U (5-аминометил-2-тиоуридин); mnm5U (5-метиламинометилуридин); mnm5s2U (5-метиламинометил-2-тиоуридин); mnm5se2U (5-метиламинометил-2-селеноуридин); ncm5U (5-карбамоилметилуридин); ncn5Um (5-карбамоилметилуридин); ncm5Um (5-карбамоилметил-2'-О-метилуридин); cmnm5U (5-карбоксиметиламинометилуридин); cnmm5Um (5-карбоксиметиламинометил-2-L-О-метилуридин); cmnm5s2U (5-карбоксиметиламинометил-2-тиоуридин); m62A (N6,N6-диметиладенозин); Tm (2'-О-метилинозин); m4C (N4-метилцитидин); m4Cm (N4,2-O-диметилцитидин); hm5C (5-гидроксиметилцитидин); m3U (3-метилуридин); cm5U (5-карбоксиметилуридин); m6Am (N6,T-O-диметиладенозин); rn62Am (N6,N6,О-2-триметиладенозин); m2'7G (N2,7-диметилгуанозин); m2'2'7G (N2,N2,7-триметилгуанозин); m3Um (3,2Т-О-диметилуридин); m5D (5-метилдигидроуридин); f5Cm (5-формил-2'-О-метилцитидин); m1Gm (1,2'-О-диметилгуанозин); m'Am (1,2-О-диметиладенозин)иринометилуридин); tm5s2U (S-тауринометил-2-тиоуридин); imG-14 (4-деметилгуанозин); imG2 (изогуанозин) или ас6А (N6-ацетиладенозин), гипоксантин, инозин, 8-оксоаденин, его 7-замещенные производные, дигидроурацил, псевдоурацил, 2-тиоурацил, 4-тиоурацил, 5-аминоурацил, 5-(С1-С6)алкилурацил, 5-метилурацил, 5-(С2-С6)алкенилурацил, 5-(С2-С6)алкинилурацил, 5-(гидроксиметил)урацил, 5-хлорурацил, 5-фторурацил, 5-бромурацил, 5-гидроксицитозин, 5-(С1-С6)алкилцитозин, 5-метилцитозин, 5-(С2-С6)алкенилцитозин, 5-(С2-С6)алкинилцитозин, 5-хлорцитозин, 5-фторцитозин, 5-бромцитозин, N2-диметилгуанин, 7-деазагуанин, 8-азагуанин, 7-деаза-7-замещенный гуанин, 7-деаза-7-(С2-С6)алкинилгуанин, 7-деаза-8-замещенный гуанин, 8-гидроксигуанин, 6-тиогуанин, 8-оксогуанин, 2-аминопурин, 2-амино-6-хлорпурин, 2,4-диаминопурин, 2,6-диаминопурин, 8-азапурин, замещенный 7-деазапурин, 7-деаза-7-замещенный пурин, 7-деаза-8-замещенный пурин или абазический нуклеотид. Например, самореплицирующаяся РНК может содержать одно или более модифицированных пиримидиновых азотистых оснований, таких как остатки псевдоуридина и/или 5-метилцитозина. Однако в некоторых вариантах осуществления РНК включает немодифицированные азотистые основания, и может включать немодифицированные нуклеотиды, т.е. все нуклеотиды в РНК являются обычными А, С, G и U рибонуклеотидами (за исключением 5'-кэпированной структуры, которая может содержать 7'-метилгуанозин). В других вариантах осуществления РНК может включать 5'-кэп, содержащий 7'-метилгуанозин, и первые 1, 2 или 3 5'-рибонуклеотида могут быть метилированными в 2'-положении рибозы.
В идеальном варианте РНК, используемая в изобретении, включает только фосфодиэфирные связи между нуклеотидами, но в некоторых вариантах осуществления она может содержать фосфорамидатные, фосфоротиоатные и/или метилфосфонатные связи.
В идеальном варианте липосома включает менее 10 различных видов РНК, например, 5, 4, 3 или 2 различных вида; наиболее предпочтительно липосома включает один вид РНК, т.е. молекулы РНК в липосоме имеют одинаковую последовательность и длину.
Количество РНК на липосому может варьировать. Как правило, число отдельных молекул самореплицирующихся РНК на липосому составляет ≤50, например, <20, <10, <5 или 1-4 на липосому.
Иммуноген
Молекулы РНК, используемые в изобретении, кодируют полипептидный иммуноген. После введения в липосомах РНК транслируется в условиях in vivo, и иммуноген может вызывать иммунный ответ у реципиента. Иммуноген может вызывать иммунный ответ против бактерии, вируса, гриба или паразита (или в некоторых вариантах осуществления против аллергена, и в других вариантах осуществления против опухолевого антигена). Иммунный ответ может включать ответную продукцию антител (обычно представляющих собой IgG) и/или опосредованный клетками иммунный ответ. Полипептидный иммуноген, как правило, будет вызывать иммунный ответ, в результате которого распознается соответствующий бактериальный, вирусный, грибковый или паразитарный (или аллерген или опухолевый) полипептид, но в некоторых вариантах осуществления полипептид может функционировать в качестве мимотопа для индукции иммунного ответа, который распознает бактериальный, вирусный, грибковый или паразитарный сахарид. Как правило, иммуноген является поверхностным полипептидом, например, адгезином, гемагглютинином, гликопротеином оболочки, гликопротеином шипов и т.д.
Молекулы самореплицирующейся РНК могут кодировать единичный полипептидный иммуноген или многочисленные полипептиды. Многочисленные иммуногены могут находиться в виде одного полипептидного иммуногена (слитого полипептида) или в виде отдельных полипептидов. Если иммуногены экспрессируются в виде отдельных полипептидов, то тогда один или более из них может обеспечиваться с апстрим IRE или дополнительным вирусным промоторным элементом. Альтернативно многочисленные иммуногены могут экспрессироваться из полипротеина, который кодирует отдельные иммуногены, слитые с короткой аутокаталитический протеазой (например, белок 2А вируса ящура), или в виде интеинов.
В отличие от источников 1 и 14, РНК кодирует иммуноген. Во избежание разночтений изобретение не включает РНК, которая кодирует люциферазу светляков или которая кодирует слитый белок β-галактозидазу E. coli, или которая кодирует зеленый флуоресцентный белок (GFP). Также РНК не является общей мышиной РНК тимуса.
В некоторых вариантах осуществления иммуноген вызывает иммунный ответ против одной из следующих бактерий:
Nesseria meningitides: подходящие иммуногены включают, не ограничиваясь этим, мембранные белки, такие как адгезины, аутотранспортеры, токсины, белки захвата железа и белок, связывающийся с фактором Н.
Streptococcus pneumoniae: подходящие полипептидные иммуногены описаны в источнике 16. Они включают, не ограничиваясь этим, субъединицу фимбрии RrgB, предшественник бета-N-ацетилгексозаминидазы (spr0057), spr0096, общий стресс-белок GSP-781 (spr2021, SP2216), серин-треониновую протеинкиназу StkP (SP1732) и поверхностный адгезин PsaA пневмококков.
Streptococcus pyogenes: подходящие иммуногены включают, не ограничиваясь этим, полипептиды раскрытые в источниках 17 и 18.
Moraxella catarrhalis.
Bordetella pertussis: подходящие столбнячные иммуногены включают, не ограничиваясь этим, столбнячный токсин или токсоид (РТ), нитчатый гемагглютинин (FHA), пертактин и агглютиногены 2 и 3.
Staphylococcus aureus: подходящие иммуногены включают, не ограничиваясь этим, полипептиды, раскрытые в источнике 19, такие как гемолизин, esxA, esxB, феррихром-связывающий белок (sta006) и/или липопротеин sta011.
Clostridium tetani: типичным иммуногеном является столбнячный токсоид.
Cornynebacterium diphtheriae: типичным иммуногеном является дифтерийный токсоид.
Haemophilus influenzae: подходящие иммуногены включают, не ограничиваясь этим, полипептиды, раскрытые в источниках 20 и 21.
Pseudomonas aeruginosa.
Streptococcus agalactiae: подходящие иммуногены включают, не ограничиваясь этим, полипептиды раскрытые в источнике 17.
Chlamydia trachomatis: подходящие иммуногены включают, не ограничиваясь этим, PepA, LcrE, ArtJ, DnaK, CT398, OmpH-подобный, AtoS, CT547, Eno, HtrA и MurG (например, смотри раскрытые в источнике 22. LcrE [23] и HtrA [24] являются двумя предпочтительными иммуногенами.
Chlamydia pneumoniae: подходящие иммуногены включают, не ограничиваясь этим, полипептиды раскрытые в источнике 25.
Helicobacter pylori: подходящие иммуногены включают, не ограничиваясь этим, CagA, VacA, NAP и/или уреазу [26].
Escherichia coli: подходящие иммуногены включают, не ограничиваясь этим, иммуногены, полученные из энтеротоксигенных E. coli (ETEC), энтероаггрегативных E. coli (EAggEC), диффузноадгезирующих E. coli (DAEC), энтеропатогенных E. coli (EPEC), внекишечных патогенных E. coli (ExPEC) и/или энтерогеморрагических E. coli (EHEC). Штаммы ExPEC включают уропатогенные E. coli (UPEC) и менингит/сепсис-ассоциированные E. coli (MNEC). Подходящие полипептидные иммуногены раскрыты в источниках 27 и 28. Подходящие иммуногены MNEC раскрыты в источнике 29. Подходящим иммуногеном для некоторых типов E. coli является AcfD [30].
Bacillus anthracis
Yersinia pestis: подходящие иммуногены включают, не ограничиваясь этим, полипептиды раскрытые в источниках 31 и 32.
Staphylococccus epidermis
Clostridium perfringens или Clostridium botulinums
Leggionella pneumophila
Coxiella burnetii
Brucella, такие как B. abortis, B. canis, B. melitensis, B. neotomae, B. ovis, B. suis, B. Pinnipediae.
Francisella, такие как F. novicida, F. philomiragia, F. tularensis
Neisseria gonorrhoeae
Treponema pallidum
Haemophilus ducreyi
Enterococcus faecalis или Enterococcus faecium
Staphylococcus saprophyticus
Yersinia enterocolitica
Mycobacterium tuberculosis
Rickettsia
Listeria monocytogenes
Vibrio cholerae
Salmonella typhi
Borrelia burgdorferi
Porphyrominas gingivalis
Klebsiella
В некоторых вариантах осуществления иммуноген вызывает иммунный ответ против одного из следующих вирусов:
Ортомиксовирус: подходящие иммуногены могут происходить из вируса гриппа А, В и С, такие как гемагглютинин, нейраминидаза или матричные белки М2. В том случае, когда иммуноген представляет собой гемагглютинин вируса гриппа А, то он может происходить из любого субтипа, например, Н1, Н2, Н3, Н4, Н5, Н6, Н7, Н8, Н9, Н10, Н11, Н12, Н13, Н14, Н15 или Н16.
Парамиксовирусы: вирусные иммуногены включают, не ограничиваясь этим, полученные из пневмовирусов (например, респираторный синцитиальный вирус, RSV), рубулавирусов (например, вирус свинки), парамиксовирусов (например, вирус парагриппа), метапневмовирусов и морбилливирусов (например, кори).
Поксвирус: вирусные иммуногены включают, не ограничиваясь этим, полученные из ортопоксвируса, такого как Variola vera, включая, не ограничиваясь этим, Variola major и Variola minor.
Пикорнавирус: вирусные иммуногены включают, не ограничиваясь этим, полученные из пикорнавирусов, таких как энтеровирусы, риновирусы, гепарнавирусы, кардиовирусы и афтоловирусы. В одном варианте осуществления энтеровирус является полиовирусом, например, полиовирусом типа 1, типа 2 и/или типа 3. В еще одном варианте осуществления энтеровирус представляет энтеровирус EV71. В еще одном варианте осуществления энтеровирус представляет вирус Коксаки А или В.
Буньявирус: вирусные иммуногены включают, не ограничиваясь этим, полученные из ортобуньявируса, такого как вирус калифорнийского энцефалита, флебовируса, такого как вирус лихорадки долины Рифт, или наировируса, такого как вирус геморрагической лихорадки Крым-Конго.
Гепарнавирус: вирусные иммуногены включают, не ограничиваясь этим, полученные из гепарнавируса, такого как вирус гепатита А (HAV).
Филовирус: вирусные иммуногены включают, не ограничиваясь этим, полученные из филовируса, такого как вирус Эбола (включая подтипы вируса Эбола заирский, побережья Ивори, рестонский или суданский) или вирус Марбурга.
Тогавирус: вирусные иммуногены включают, не ограничиваясь этим, полученные из тогавируса, такого как рубивирус, альфа-вирус или артеривирус. Они включают вирус краснухи. rubella
Флавивирус: вирусные иммуногены включают, не ограничиваясь этим, полученные из флавивируса, такого как вирус клещевого энцефалита (TBE), вирус Денге (тип 1, 2, 3 или 4), вирус желтой лихорадки, вирус японского энцефалита, вирус болезни кьясанурского леса, вирус энцефалита Западного Нила, вирус энцефалита Сент-Луис, вирус русского весеннего-летнего энцефалита, вирус энцефалита Повассан.
Пестивирус: вирусные иммуногены включают, не ограничиваясь этим, полученные из пестивирусов, вызывающих вирусную диарею крупного рогатого скота (BVDV), классическую лихорадку свиней (CSFV) или пограничную болезнь (BDV).
Гепаднавирус: вирусные иммуногены включают, не ограничиваясь этим, полученные из гепаднавируса, такого как вирус гепатита В. Композиция может включать поверхностный антиген вирус гепатита В (HBsAg).
Другие вирусы гепатита: композиция может включать иммуноген из вируса гепатита С, вируса гепатита-дельта, вируса гепатита Е или вируса гепатита G.
Рабдовирус: вирусные иммуногены включают, не ограничиваясь этим, полученные из рабдовирусов, таких как лиссавирус (например, вирус бешенства) и везикуловирус (VSV).
Калицивирус: вирусные иммуногены включают, не ограничиваясь этим, полученные из калицивируса, такого как вирус Норуолк (Norovirus) и Норуолк-подобные вирусы, такие как вирус Гавайи и вирус Снежных Гор.
Коронавирус: вирусные иммуногены включают, не ограничиваясь этим, полученные из коронавируса SARS, вируса инфекционного бронхита птиц (IBV), вируса гепатита мышей (MHV) и вируса трансмиссивного гастроэнтерита свиней (TGEV). Иммуноген коронавируса может быть полипептидом шипов.
Ретровирус: вирусные иммуногены включают, не ограничиваясь этим, полученные из онковируса, лентивируса (например, HIV-1 или HIV-2) или спумавируса.
Реовирус: вирусные иммуногены включают, не ограничиваясь этим, полученные из ортореовируса, ротавируса, орбивируса или колтивируса.
Парвовирус: вирусные иммуногены включают, не ограничиваясь этим, полученные из парвовируса B19.
Герпесвирус: вирусные иммуногены включают, не ограничиваясь этим, полученные из герпесвирусов человека, таких как, например, приводимые только в качестве примера, вирус герпеса простого (HSV) (например, HSV типов 1 и 2), вирус опоясывающего лишая (VZV), вирус Эпштейна-Барра (EBV), цитомегаловирус (CMV), герпесвирус человека типа 6 (HHV6), герпесвирус человека типа 7 (HHV7) и герпесвирус человека типа 8 (HHV8).
Паповавирусы: вирусные иммуногены включают, не ограничиваясь этим, полученные из папилломавирусов и полиомавирусов. Папилломавирус (человека) может представлять серотип 1, 2, 3, 4, 5, 6, 8, 11, 13, 16, 18, 31, 33, 35, 39, 41, 42, 47, 51, 57, 58, 63 или 65, например, одного или более серотипов 6, 11, 16 и/или 18.
Аденовирус: вирусные иммуногены включают, не ограничиваясь этим, полученные из аденовируса серотипа 36 (Ad-36).
В некоторых вариантах осуществления иммуноген вызывает иммунный ответ против вируса, который заражает рыб, такого как вирус инфекционной анемии лососевых (ISAV), вирус болезни поджелудочной железы лососевых (SPDV), вирус инфекционного некроза поджелудочной железы (IPNV), возбудитель вирусной болезни канального сома (CCV), вирус лимфоцистиса рыб (FLDV), вирус инфекционного гематопоэтического некроза (IHNV), кои-герпесвирус, вирус, подобный пикорнавирусам у лососевых (также известный, как вирус, подобный пикорнавирусам у атлантического лосося), вирус пресноводного лосося (LSV), ротавирус атлантического лосося (ASR), вирус земляничной форели (TSD), вирус папилломатоза лосося кижуча (CSTV) или вирус геморрагической септицемии (VHSV).
Грибковые иммуногены могут быть получены из Dermatophytres, включая: Epidermophyton floccusum, Microsporum audouini, Microsporum canis, Microsporum distorum, Microsporum equinum, Microsporum gypsum, Microsporum nanum, Trichophyton concetricum, Trichophyton equinum, Trichophyton gallinae, Trichophyton gypseum, Trichophyton megnini, Trichophyton mentagrophytes, Trichophyton quinckeanum, Trichophyton rubrum, Trichophyton schoeleini, Trichophyton tonsurans, Trichophyton verrucosum, Trichophyton verrucosum var. album, var. discoides, var. ochraceum, Trichophyton violaceum и/или Trichophyton faviforme; или из Aspergillus fumigatus, Aspergillus flavus, Aspergillus niger, Aspergillus nidulans, Aspergillus terreus, Aspergillus sydowi, Aspergillus flavatus, Aspergillus glaucus, Blastoschizomyces capitatus, Candida albicans, Candida enolase, Candida tropicalis, Candida glabrata, Candida krusei, Candida parapsilosis, Candida stellatoidea, Candida kusei, Candida parakwsei, Candida lusitaniae, Candida pseudotropicalis, Candida guilliermondi, Cladosporium carrionii, Coccidiodes immitis, Blastomyces dermatidis, Cryptococcus neoformans, Geotrichum clavatum, Histoplasma capsulatum, Klebsiella pneumoniae, Microsporidia, Encephalitozoon spp., Septata interstinalis и Enterocytozoon bieneusi; реже Brachiola sp., Microsporidium sp., Nosema sp., Pleistophora sp., Trachipleistophora sp., Vittaforma sp., Paracoccidioides brasiliensis, Pneumocystis carinii, Pythiumn insidiosum, Pityrosporum ovale, Sacharomyces cerevisae, Sacharomyces boulardii, Sacharomyces pombe, Scedosporium apiosperum, Sporothrix schenckii, Trichosporon beigelii, Toxoplasma gondii, Penicillium marneffei, Malassezia spp., Fonsecaea spp., Wangiella spp., Sporothrix spp., Basidiobolus spp., Conidiobolus spp., Rhizopus spp., Mucor spp., Absidia spp., Mortierella spp., Cunninghamella spp., Saksenaea spp., Alternaria spp., Curvularia spp., Helminthosporium spp., Fusarium spp., Aspergillus spp., Penicillium spp., Monolinia spp., Rhizoctonia spp., Paecilomyces spp., Pithomyces spp. и Cladosporium spp.
В некоторых вариантах осуществления иммуноген вызывает иммунный ответ против паразита из рода Plasmodium, такого как P. falciparum, P. vivax, P. malariae или P. ovale. Таким образом, изобретение можно использовать для иммунизации против малярии. В некоторых вариантах осуществления иммуноген вызывает иммунный ответ против паразита семейства Caligidae, в частности, родов Lepeophtheirus и Caligus, например, это морская вошь, такая как Lepeophtheirus salmonis и Caligus rogercresseyi.
В некоторых вариантах осуществления иммуноген вызывает иммунный ответ против: аллергенов пыльцы (аллергенов пыльцы деревьев, травянистых растений, сорных растений и злаковых трав); аллергенов насекомых или клещей (воздушных аллергенов, аллергенов слюны и яда, например, аллергенов клещей, аллергенов тараканов и мошек, аллергенов яда отряда перепончатокрылых); аллергенов волос и перхоти животных (например, собак, кошек, лошади, крысы мыши и т.д.) и пищевых аллергенов (например, глиадин). Важными аллергенами пыльцы деревьев, злаковых трав и травянистых растений являются аллергены, которые происходят от растений таксономических отрядов Fagales, Oleales, Pinales и Platanaceae, включая, не ограничиваясь этим, березу (Betula), ольху (Alnus), лещина (Corylus), граб (Carpinus) и оливковое дерево (Olea), кедр (Cryptomeria и Juniperus), плоское дерево (Platanus), отряд Poales, включая злаковые травы родов Lolium, Phleum, Poa, Cynodon, Dactylis, Holcus, Phalaris, Secale и Sorghum, отрядов Asteralis и Urticales, включая травянистые растения родов Ambrosia, Artemisia и Parietaria. Другими важными воздушными аллергенами являются аллергены клещей домашней пыли рода Dermatophagoides и Euroglyphus, амбарных клещей, например, Lepidoglyphys, Glycyphagus и Tyrophagus, аллергены тараканов, мошек и блох, например, Blatella, Periplaneta, Chironomus и Ctenocepphalides, и аллергены млекопитающих, таких как кошка, собака и лошадь, аллергены ядов, включая аллергены жалящих или кусающих насекомых, такие как аллергены таксономического отряда перепончатокрылых, включая пчел (Apidae), ос (Vespidea) и муравьев (Formicoidae).
В некоторых вариантах осуществления иммуноген является опухолевым антигеном, выбранным из: (а) антигенов злокачественной опухоли семенников, таких как полипептиды семейства NY-ESO-1, SSX2, SCP1, а также полипептиды семейства RAGE, BAGE, GAGE и MAGE, например, GAGE-1, GAGE-2, MAGE-1, MAGE-2, MAGE-3, MAGE-4, MAGE-5, MAGE-6 и MAGE-12 (которые можно использовать, например, при вакцинации против меланомы, опухолей легких, головы и шеи, NSCLC, молочной железы, органов желудочно-кишечного тракта и мочевого пузыря); (b) мутированных антигенов, например, р53 (ассоциированного с различными солидными опухолями, например, злокачественными опухолями ободочной и прямой кишки, легких, головы и шеи), p21/Ras (ассоциированного, например, с меланомой, раком поджелудочной железы и колоректальным раком), CDK4 (ассоциированного с меланомой), MUM1 (ассоциированного, например, с меланомой), каспазы-8 (ассоциированной, например, со злокачественными опухолями головы и шеи), CIA 0205 (ассоциированного, например, с раком мочевого пузыря), HLA-A2-R1701, бета-катенина (ассоциированного, например, с меланомой), TCR (ассоциированного, например, с Т-клеточной неходжкинской лимфомой), BCR-abl (ассоциированного, например, с хроническим миелогенным лейкозом), триосефосфатизомеразы, KIA 0205, CDC-27 и LDLR-FUT; (c) сверхэкспрессированных антигенов, например, галектина 4 (ассоциированного, например, с колоректальным раком), галектина 9 (ассоциированного, например, с болезнью Ходжкина), протеиназы 3 (ассоциированной, например, с хроническим миелоидным лейкозом), WT 1 (ассоциированного, например, с различными лейкозами), карбоангидразы (ассоциированной, например, с раком почек), альдолазы А (ассоциированной, например, с раком легких), PRAME (ассоциированного, например, с меланомой), HER-2/neu (ассоциированного, например, с раком молочной железы, ободочной кишки, легких и яичников), маммоглобина, альфа-фетопротеина (ассоциированного, например, с гепатомой), KSA (ассоциированного, например, с колоректальным раком), гастрина (ассоциированного, например, с раком поджелудочной железы и желудка), каталитического компонента теломеразы MUC-1 (ассоциированного, например, с раком молочной железы и яичников), G-250 (ассоциированного, например, с почечно-клеточной карциномой), р53 (ассоциированного, например, с раком молочной железы, ободочной кишки) и карциноэмбрионального антигена (ассоциированного, например, с раком молочной железы, раком легких и раком органов желудочно-кишечного тракта, таким как колоректальный рак); (d) общих антигенов, например, антигенов меланомы-дифференцировки меланоцитов, таких как MART-1/Melan A, gp100, MC1R, рецептор меланоцит-стимулирующего гормона, тирозиназы, связанного с тирозиназой белка-1/TRP1 и связанного с тирозиназой белка-2/TRP2 (ассоциированных, например, с меланомой); (е) ассоциированных с предстательной железой антигенов, таких как PAP, PSA, PSMA, PSH-1, PSM-P1, PSM-P2, ассоциированных, например, с раком предстательной железы; (f) иммуноглобулиновых идиотипов (ассоциированных, например, с миеломой и В-клеточными лимфомами). В некоторых вариантах осуществления опухолевые иммуногены включают, не ограничиваясь этим, p15, Hom/Mel-40, H-Ras, E2A-PRL, H4-RET, IGH-IGK, MYL-RAR, антигены вируса Эпштейна-Барра, EBNA, антигены папилломавируса (HPV), включая Е6 иЕ7, антигены вируса гепатита В и С, антигены Т-лимфотропного вируса, TSP-180, p185erbB2, p180erb-3, c-met, mn-23H1, TAG-72-4, CA 19-9, CA 72-4, CAM 17.1, NuMa, K-ras, p16, TAGE, PSCA, CT7, 43-9F, 5T4, 791 Tgp72, beta-HCG, BCA225, BTAA, CA 125, CA 15-3 (CA 27.29\BCAA), CA 195, CA 242, CA-50, CAM43, CD68\KP1, CO-029, FGF-5, Ga733 (EpCAM), HTgp-175, M344, MA-50, MG7-Ag, MOV18, NB/70K, NY-CO-1, RCAS1, SDCCAG16, TA-90 (Mac-2-связывающий белок/циклофилин С-ассоциированный белок), TAAL6, TAG72, TLP, TPS и тому подобное.
Фармацевтические композиции
Липосомы по изобретению являются подходящими в качестве компонентов в фармацевтических композициях для иммунизации субъектов против различных заболеваний. Как правило, такие композиции включают фармацевтически приемлемый носитель в дополнении к липосомам. Подробное обсуждение фармацевтически приемлемых носителей приводится в источнике 33.
Фармацевтическая композиция по изобретению может включать один или более небольших молекул иммунопотенциаторов. Например, композиция может содержать агонист TLR2 (например, Pam3CSK4), агонист TLR4 (например, аминоалкилглюкозаминид фосфат, такой как Е6020), агонист TLR4 (например, имиквимод), агонист TLR8 (например, резиквимод) и/или агонист TLR9 (например, IC31). В идеальном варианте любой такой агонист имеет молекулярную массу <2000 Da. В том случае, если РНК инкапсулирована, то в некоторых вариантах осуществления агонист(ы) также инкапсулируют с РНК, но в других вариантах осуществления они остаются неинкапсулированными. В тех случаях, когда РНК адсорбирована на частице, то в некоторых вариантах осуществления такой агонист(ы) также адсорбируется с РНК, но в других вариантах осуществления он не адсорбирован.
Фармацевтические композиции по изобретению могут содержать липосомы в обыкновенной воде (например, в вожже для инъекций) или в буфере, например, фосфатном буфере, Трис-буфере, боратном буфере, сукцинатном буфере, гистидиновом буфере или цитратном буфере. Как правило, соли буфера будут находиться в количестве в пределах 5-20 мМ.
Фармацевтические композиции по изобретению могут иметь рН в пределах от 5,0 до 9,5, например, от 6,0 до 8,0.
Композиции по изобретению могут содержать соли натрия (например, хлорида натрия) для обеспечения эффективного осмотического давления раствора. Концентрация NaCl 10±2 мг/мл является типичной, например, примерно 9 мг/мл.
Композиции по изобретению могут содержать вещества, образующие хелатные комплексы с ионами металлов. Они могут пролонгировать стабильность РНК посредством удаления ионов, ускоряющих гидролиз фосфодиэфирных связей. Таким образом, композиция может содержать одно или более из ЭДТА, ЭГТА, BAPTA, пентетовой кислоты и т.д. Такие хелатообразующие вещества, как правило, находятся в количестве 10-500 мкМ, например, 0,1 мМ. Цитрат, такой как цитрат натрия, также может функционировать в качестве хелатообразующего агента, одновременно преимущественно обеспечивая также буферную активность.
Фармацевтические композиции по изобретению могут иметь осмолярность в пределах от 200 мОсм/кг до 400 мОсм/кг, в пределах 240-360 мОсм/кг или в пределах 290-310 мОсм/кг.
Фармацевтические композиции по изобретению могут содержать один или более консервантов, таких как тиомерсал или 2-феноксиэтанол. Предпочтительными являются не содержащие ртути композиции, и можно приготовить не содержащие консервантов вакцины.
Фармацевтические композиции по изобретению предпочтительно являются стерильными.
Фармацевтические композиции по изобретению предпочтительно являются непирогенными, например, содержащими <1 ЕЭ (единиц эндотоксина, стандартный показатель) на дозу, и предпочтительно <0,1 ЕЭ.
Фармацевтические композиции по изобретению предпочтительно не содержат глютен.
Фармацевтические композиции по изобретению можно приготовить в форме разовой дозы. В некоторых вариантах осуществления разовая доза может иметь объем в пределах 0,1-1,0 мл, например, примерно 0,5 мл.
Композиции можно приготовить в виде инъекционных препаратов, или в виде растворов или суспензий. Композицию можно приготовить для пульмонарного введения, например, с помощью ингалятора, с использованием мелкодисперсного спрея. Можно приготовить композиции для интраназального, внутриушного или внутриглазного введения, например, в виде спрея или капель. Типичными являются инъекционные препараты для внутримышечного введения.
Композиции могут включать иммунологически эффективное количество липосом, а также любые другие компоненты, которые требуются. Выражение «иммунологически эффективное количество» означает, что введение такого количества индивидууму, в одной дозе или в виде части серий доз, эффективно для лечения или профилактики. Такое количество варьирует в зависимости от состояния здоровья и физического состояния индивидуума, который подвергается лечению, возраста, таксономической группы индивидуума, который подвергается лечению (например, примат, отличный от человека, примат и т.д.), способности иммунной системы индивидуума продуцировать антитела, степени требуемой защиты, формуляции вакцины, оценки медицинской ситуации лечащим врачом и других имеющих отношении факторов. Полагается, что количество будет находиться в относительно широких пределах, которые можно определить обычными исследованиями. Содержание липосомы и РНК в композициях по изобретению, как правило, будет выражаться в единицах количества РНК на дозу. Предпочтительная доза составляет ≤100 мкг РНК (например, в пределах 10-100 мкг, например, примерно 10 мкг, 25 мкг, 50 мкг, 75 мкг или 100 мкг), но экспрессия может наблюдаться при значительно более низких количествах, ≤1 мкг/дозу, ≤100 нг/дозу, ≤10 нг/дозу, ≤1 нг/дозу и т.д.
Изобретение также относится к устройству для доставки (например, шприцу, распылителю, пульверизатору, дермальному пластырю и т.д.), содержащему фармацевтическую композицию по изобретению. Такое устройство можно использовать для введения композиции субъекту позвоночному животному.
Липосомы по изобретению не содержат рибосом.
Способы лечения и медицинские применения
В противоположность частицам, раскрытым в источнике 14, липосомы и фармацевтические композиции по изобретению являются пригодными в условиях in vivo для индукции иммунного ответа против интересующего иммуногена.
Изобретение относится к способу индукции иммунного ответа у позвоночного животного, включающему стадию введения эффективного количества липосомы и фармацевтической композиции по изобретению. Иммунный ответ предпочтительно является протективным и предпочтительно включает антитела и/или опосредованный клетками иммунитет. Способ может индуцировать бустер-эффект.
Также изобретение относится к липосоме и фармацевтической композиции по изобретению для применения в способе индукции иммунного ответа у позвоночного животного.
Также изобретение относится к применению липосомы по изобретению в производстве лекарственного препарата для индукции иммунного ответа у позвоночного животного.
Посредством индукции иммунного ответа у позвоночного животного с данными применениями и способами позвоночное животное может быть защищено против различных заболеваний и/или инфекций, например, против бактериальных и/или вирусных заболеваний, которые обсуждались выше. Липосомы и композиции являются иммуногенными, и более предпочтительно представляют вакцинные композиции. Вакцины по изобретению могут быть профилактическими (т.е. профилактировать инфекцию) или терапевтическими (т.е. лечить инфекцию), но обычно они являются профилактическими.
Позвоночное животное предпочтительно является млекопитающим, таким как человек или крупное сельскохозяйственное животное (например, лошади, крупный рогатый скот, олень, козы, свиньи). В том случае, когда вакцина предназначена для профилактического применения, то человек предпочтительно является ребенком (например, ребенком ясельного возраста или младенцем), или подростком; когда вакцина рассчитана для терапевтического применения, то человек предпочтительно представляет подростка или взрослого человека. Вакцину, предназначенную для детей, также можно вводить взрослым, например, для оценки безопасности, установления дозировки, иммуногенности и т.д.
Вакцины, приготовленные по изобретению, можно использовать для лечения детей и взрослых. Таким образом, человек-пациент может находиться в возрасте моложе 1 года, моложе 5 лет, в возрасте 1-5 лет, 5-15 лет, 15-55 лет или, по меньшей мере, 55 лет. Предпочтительными пациентами для введения вакцин являются пожилые люди (например, в возрасте ≥50 лет, ≥60 лет и предпочтительно ≥65 лет), молодые люди (например, в возрасте ≤5 лет), пациенты больниц, работники учреждений здравоохранения, военные и полицейские, беременные женщины, пациенты с хроническими болезнями или люди с иммунодефицитными состояниями. Однако вакцины подходят не только для этих групп, их можно использовать более широко для других групп населения.
Композиции по изобретению, как правило, вводят непосредственно пациенту. Прямую доставку можно осуществить парентеральной инъекцией (например, подкожно, внутрибрюшинно, внутривенно, внутримышечно, внутрикожно или в интерстициальное пространство ткани; в отличие от источника 1, внутриязычная инъекция не используется широко в настоящем изобретении). Альтернативные пути введения включают ректальный, пероральный (например, таблетки, спрей), буккальный, сублингвальный, интравагинальный, местный, трансдермальный или чрезкожный, интраназальный, внутриглазной, внутриушной, пульмонарный или другие мукозальные пути введения. Внутрикожное и внутримышечное введение является двумя предпочтительными путями. Инъекцию можно проводить с использованием иглы (например, гиподермической иглы), но альтернативно можно проводить безыгольную инъекцию. Типичная доза при внутримышечном введении составляет 0,5 мл.
Изобретение можно использовать для индукции системного и/или мукозального иммунитета, предпочтительно для индукции повышенного системного и/или мукозального иммунитета.
Дозировка может представлять однодозовую схему или мультидозовую схему. Мультидозы можно использовать в схеме первичной иммунизации и/или схеме повторной иммунизации. В мультидозовой схеме различные дозы можно вводить одним и тем же или различными путями, например, первую дозу - парентеральным путем и повторную дозу - через слизистую, первую дозу - через слизистую и повторную дозу - парентеральным путем и т.д. Как правило, мультидозы вводят, по меньшей мере, с интервалом 1 неделю (например, примерно 2 недели, примерно 3 недели, примерно 3 недели, примерно 4 недели, примерно 6 недель, примерно 8 недель, примерно 10 недель, примерно 12 недель, примерно 16 недель и т.д.). В одном варианте осуществления мультидозы можно вводить через примерно 6 недель, 10 недель и 14 недель после рождения, например, в возрасте 6 недель, 10 недель и 14 недель, как это часто применяют в расширенной программе иммунизации Всемирной Организации Здравоохранения («EPI»). В альтернативном варианте осуществления две основные дозы вводят с интервалом примерно два месяца, например, с интервалом примерно 7, 8 или 9 недель, с последующим введением одной или более повторных доз примерно через период времени от 6 месяцев до 1 года после второй основной дозы, например, примерно через 6, 8, 10 или 12 месяцев после второй основной дозы. В дополнительном варианте осуществления три основных дозы вводят с интервалом примерно два месяца, например, с интервалом примерно 7, 8 или 9 недель, с последующим введением одной или более повторных доз через период времени от 6 месяцев до 1 года после третьей основной дозы, например, примерно через 6, 8, 10 или 12 месяцев после третьей основной дозы.
Общая информация
В практике настоящего изобретения будут применяться, если не указано иначе, обычные методы химии, биохимии, молекулярной биологии, иммунологии и фармакологии, известные в данной области. Такие методы подробно описаны в литературе. Смотри, например, источники 34-40 и т.д.
Термин «содержащий» означает «включающий», а также «состоящий», например, композиция, «содержащая» Х, может исключительно состоять из Х, или может содержать некоторые дополнительные компоненты, например, Х+Y.
Термин «примерно» по отношению к цифровому значению x является необязательным и означает, например, х±10%.
Выражение «по существу» не исключает «полностью», например, композиция, которая «по существу не содержит» Y, может полностью не содержать Y. Когда это необходимо, то выражение «по существу» можно исключить из определения по изобретению.
Обращения к терминам заряд, катионы, анионы, цвитеррионы и т.д., используются при рН 7.
TLR3 представляет Toll-подобный рецептор 3. Это единичный мембранный рецептор, который играет ключевую роль в системе врожденного иммунитета. Известные агонисты TLR3 включают поли(I:C). «TLR3» является принятым по номенклатуре HGNC названием гена, кодирующего данный рецептор, и его уникальным номером HGNC ID является HGNC:11849. Последовательность RefSeq для гена TLR3 человека представляет GI:2459625.
TLR7 представляет Toll-подобный рецептор 7. Это единичный мембранный рецептор, который играет ключевую роль в системе врожденного иммунитета. Известные агонисты TLR7 включают, например, имиквимод. «TLR7» является принятым по номенклатуре HGNC названием гена, кодирующего данный рецептор, и его уникальным номером HGNC ID является HGNC:15631. Последовательность RefSeq гена TLR7 человека представляет GI:67944638.
TLR8 представляет Toll-подобный рецептор 8. Это единичный мембранный рецептор, который играет ключевую роль системе врожденного иммунитета. Известные агонисты TLR7 включают, например, резиквимод. «TLR8» является принятым по номенклатуре HGNC названием гена, кодирующего данный рецептор, и его уникальным номером HGNC ID является HGNC:15632. Последовательность RefSeq гена TLR8 человека представляет GI:20302165.
Семейство RIG-I-подобных рецепторов («RLR») включает различные РНК-геликазы, которые играют ключевую роль системе врожденного иммунитета [41]. RLR-1 (также известный, как RIG-I или ген I, индуцируемый ретиноевой кислотой) имеет два домена рекрутирования каспазы около его N-конца. Принятым по номенклатуре HGNC названием гена, кодирующего геликазу RLR-1, является «DDX58» (для DEAD (Asp-Glu-Ala-Asp) box полипептида 58), и его уникальным номером HGNC ID является HGNC:19102. Последовательность RefSeq гена RLR-1 человека представляет GI:77732514. RLR-2 (также известный, как MDA5 или ассоциированный с дифференцировкой меланомы ген 5) также имеет два домена рекрутирования каспазы около его N-конца. Принятым по номенклатуре HGNC названием гена, кодирующего геликазу RLR-2, является «IFIH1» (для домена 1 индуцированной интерфероном геликазы С), и его уникальный номер HGNC ID представляет HGNC:18873. Последовательность RefSeq гена RLR-2 человека представляет GI:27886567. RLR-3 (также известный, как LGP2 или лаборатория генетики и физиологии 2) не имеет доменов рекрутирования каспазы. Принятым по номенклатуре HGNC названием гена, кодирующего геликазу RLR-3, является «DHX58» (для DHX (Asp-Glu-Х-His) box полипептида 58), и его уникальным номером HGNC ID является HGNC:29517. Последовательность RefSeq гена RLR-3 человека представляет GI:149408121.
PKR представляет зависимую от двухцепочечной РНК протеинкиназу. Она играет ключевую роль в системе врожденного иммунитета. «EIF2AK2» (для эукариотического фактора инициации трансляции 2-альфа киназы 2) является принятым по номенклатуре HGNC названием гена, кодирующего данный фермент, и его уникальный номер HGNC ID представляет HGNC:9437. Последовательность RefSeq гена PKR человека представляет GI:208431825.
КРАТКОЕ ОПИСАНИЕ ФИГУР
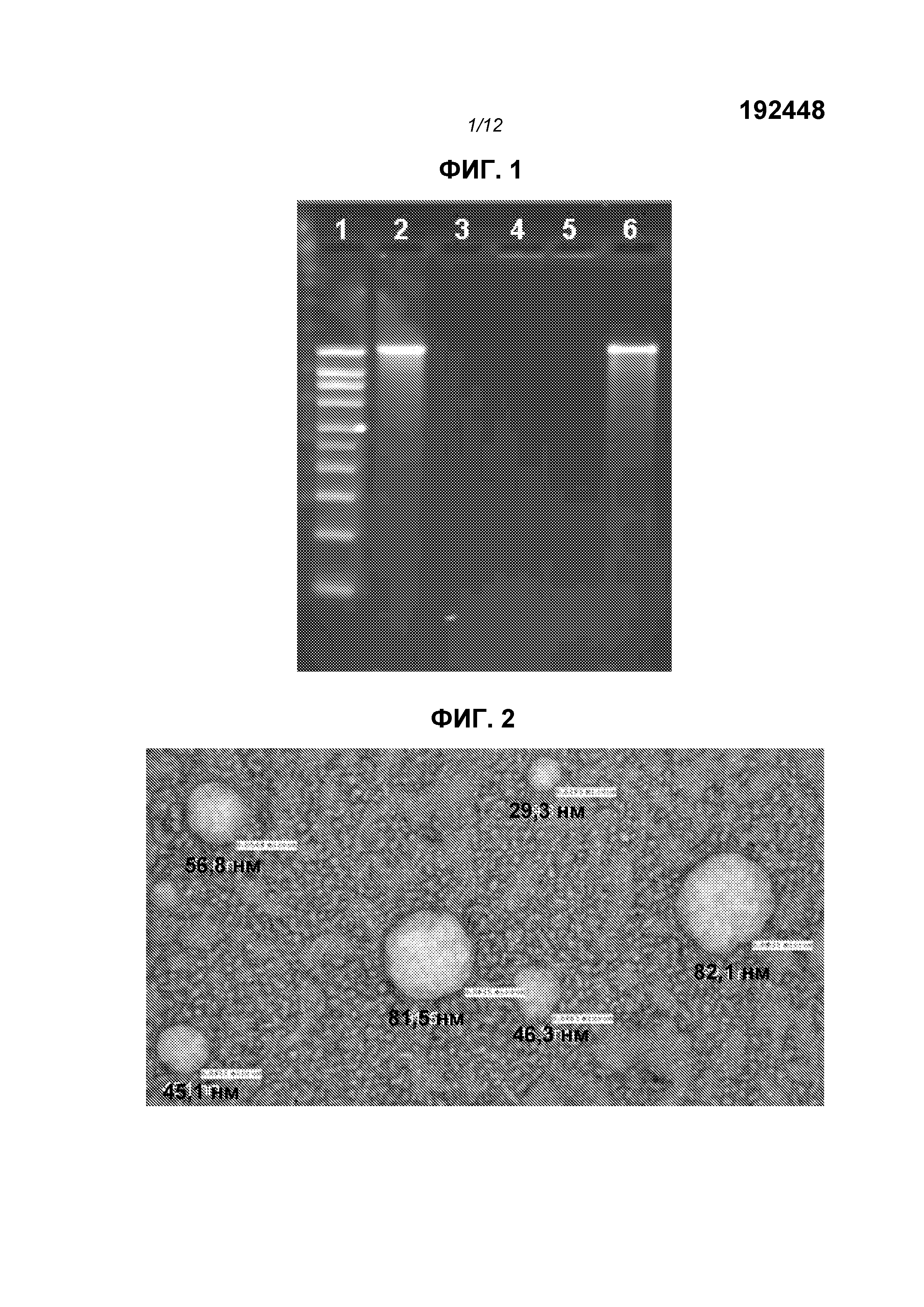
На фиг.1 показан гель с окрашенной РНК. Дорожки показывают (1) маркеры (2) «голый» репликон (3) репликон после обработки РНКазой (4) репликон, инкапсулированный в липосоме (5) липосома после обработки РНКазой (6) липосома, обработанная РНКазой, затем подвергнутая экстракции смесью фенол/хлороформ.
Фиг.2 представляет электронную микрофотографию липосом.
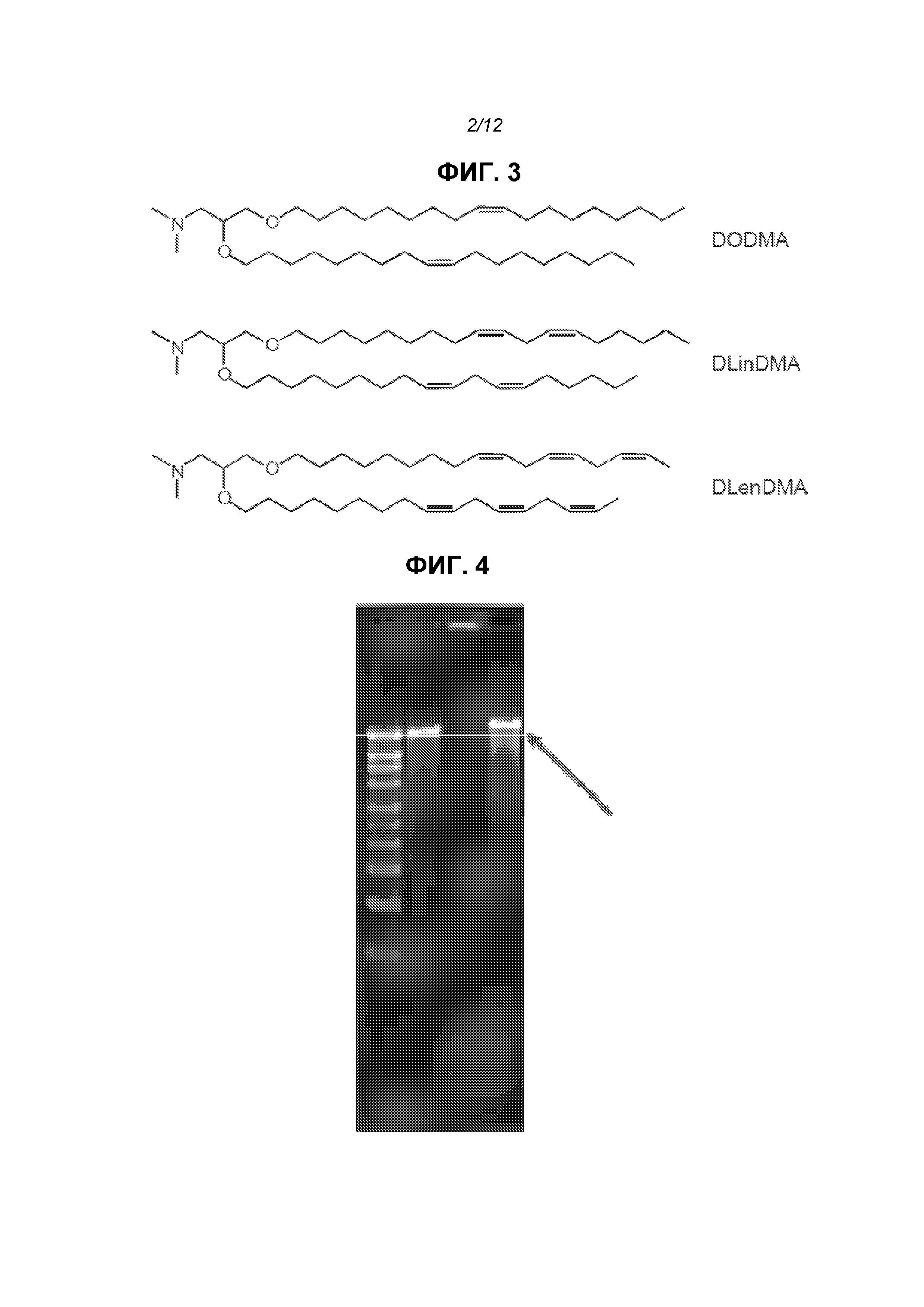
На фиг.3 приведены структуры DLinDMA, DLenDMA и DODMA.
На фиг.4 показан гель с окрашенной РНК. Дорожки показывают (1) маркеры (2) «голый» репликон (3) репликон, инкапсулированный в липосому (4) липосома, обработанная РНКазой, затем подвергнутая экстракции смесью фенол/хлороформ.
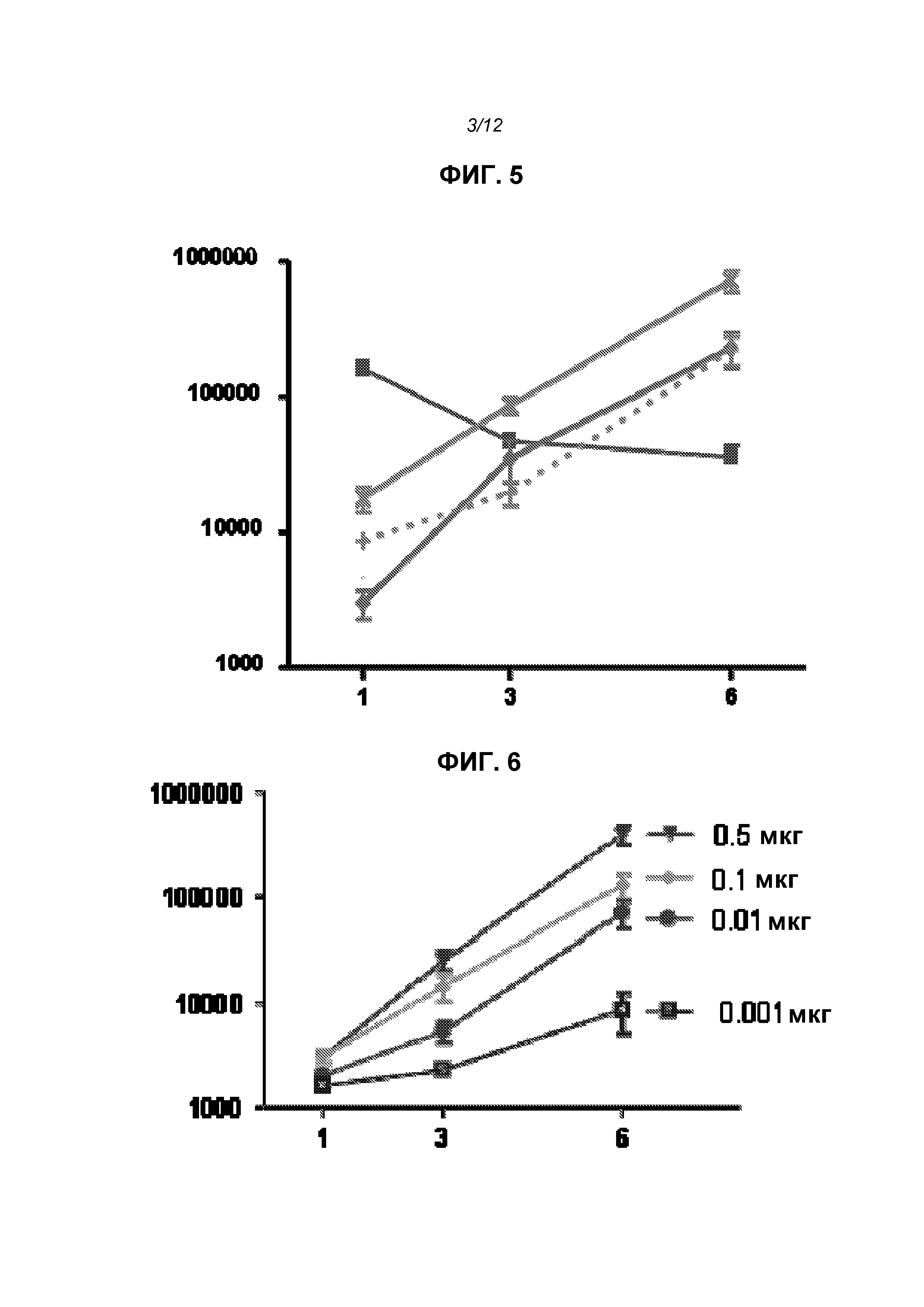
На фиг.5 показана экспрессия белка на сутки 1; 3 и 6 после доставки РНК в виде упакованного в вирион репликона (прямоугольники) в виде «голой» РНК (ромбы) или в липосомах (+=0,1 мкг, х=1 мкг).
На фиг.6 показана экспрессия белка на сутки 1; 3 и 6 после доставки инкапсулированной в липосому РНК в четырех различных дозах.
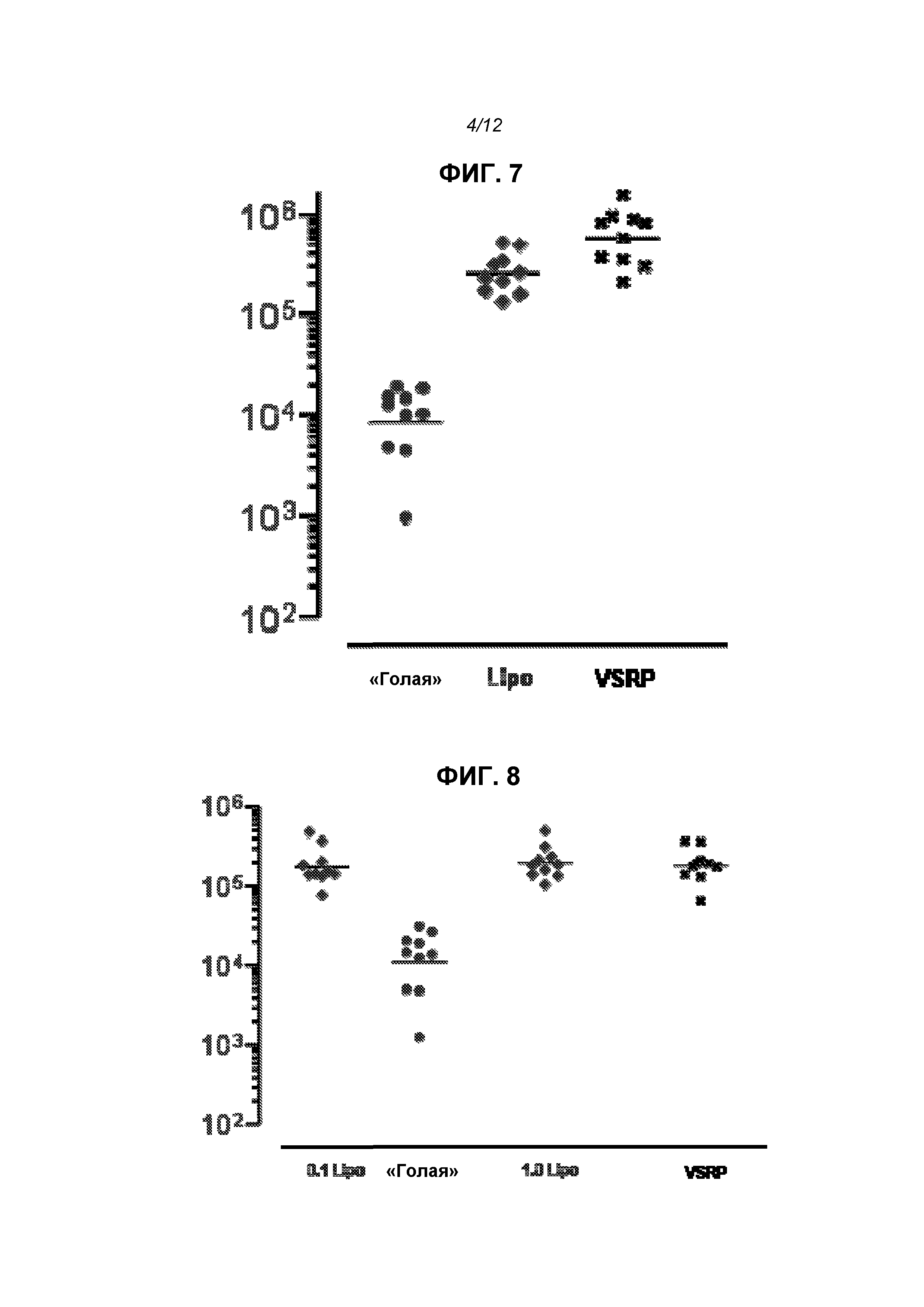
На фиг.7 показаны титры анти-F-IgG у животных, получивших упакованный в вирион репликон (VRP или VSRP), 1 мкг «голой» РНК и 1 мкг инкапсулированной в липосому РНК.
На фиг.8 показаны титры анти-F-IgG у животных, получивших VRP, 1 мкг «голой» РНК и 0,1 г или 1 мкг инкапсулированной в липосому РНК.
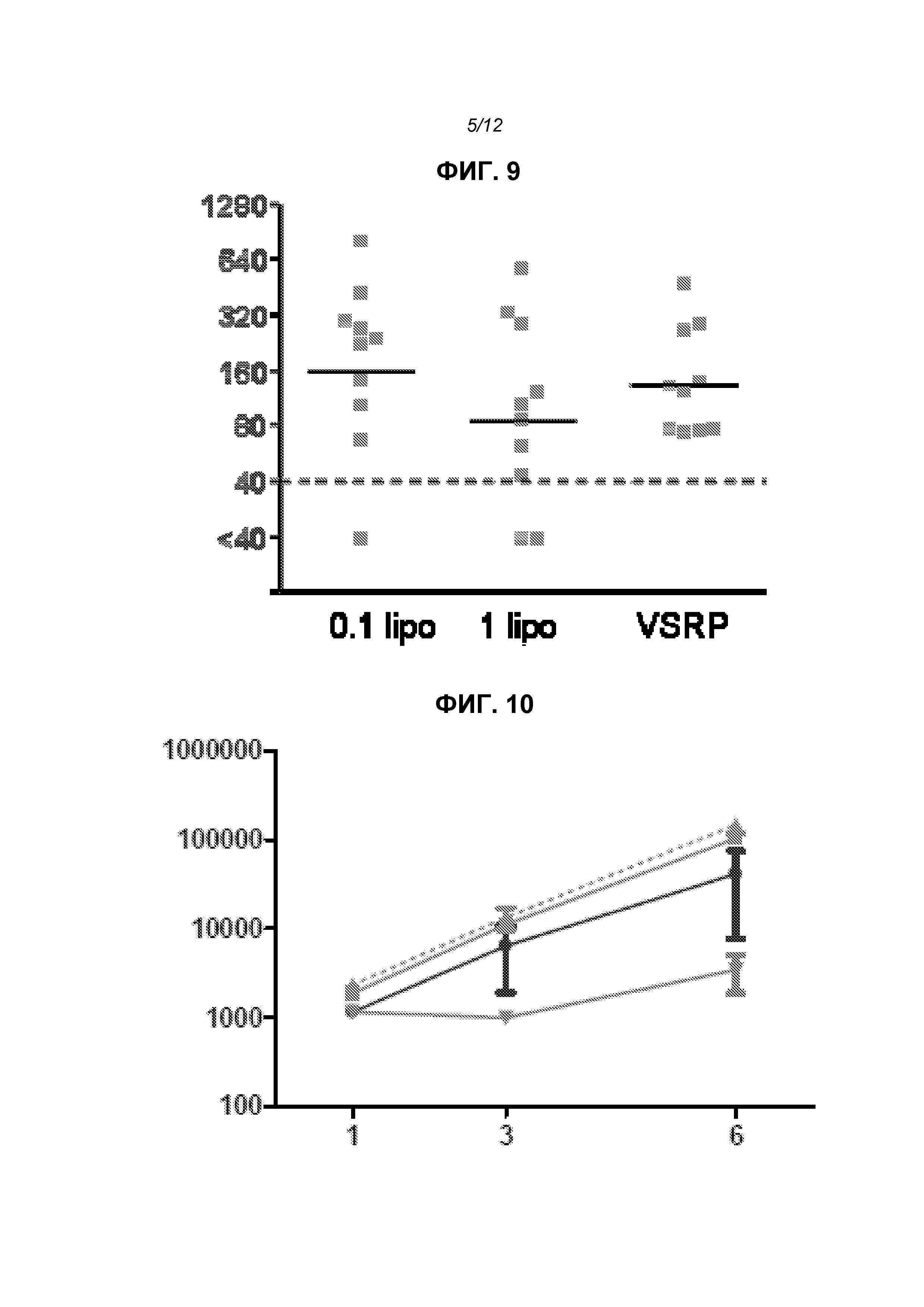
На фиг.9 показаны титры нейтрализующих антител у животных, получивших VRP или 0,1 г или 1 мкг инкапсулированной в липосому РНК.
На фиг.10 показаны уровни экспрессии после доставки репликона в виде «голой» РНК (кружки), инкапсулированной в липосому РНК (треугольники и прямоугольники) или в виде липоплекс (перевернутые треугольники).
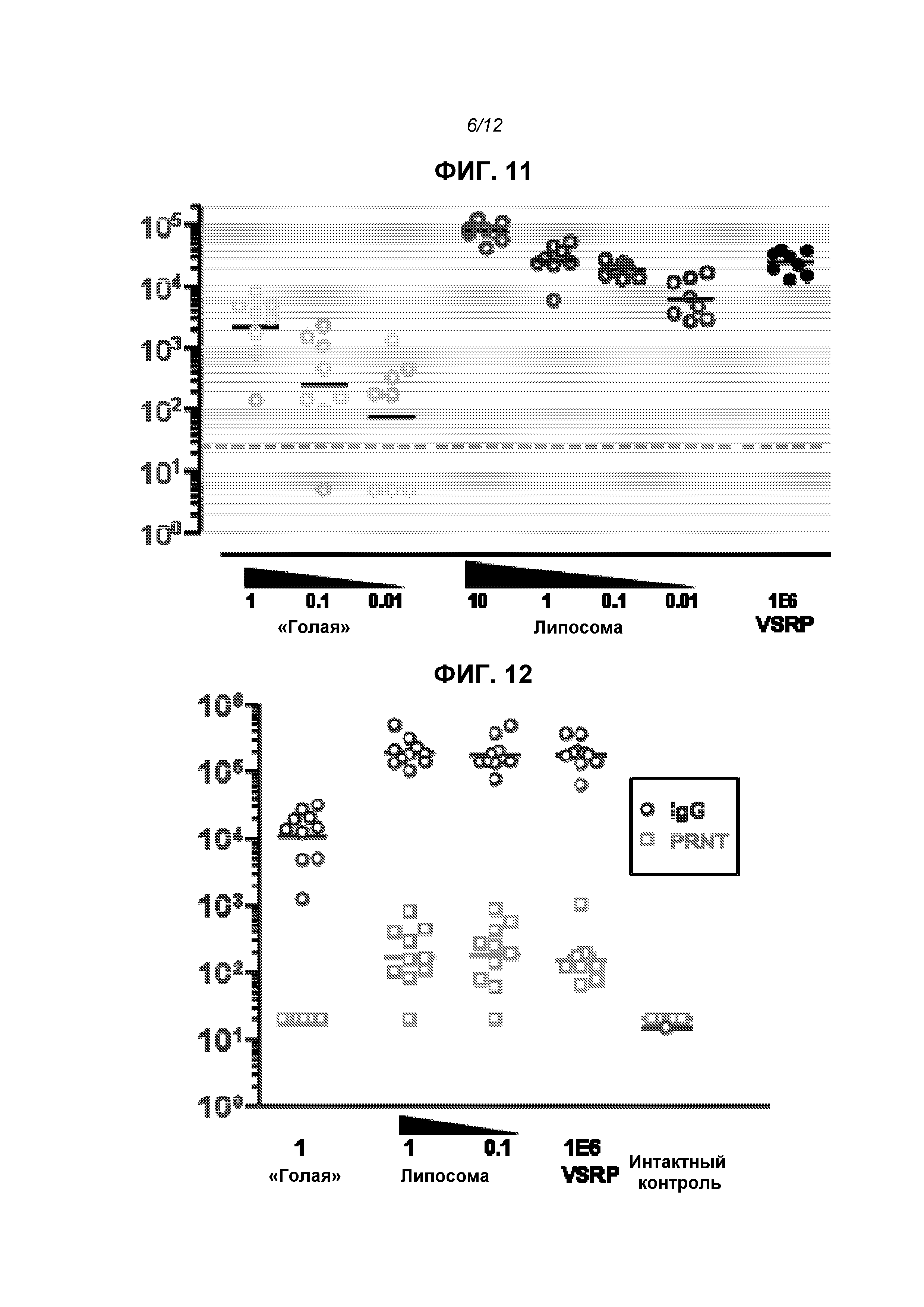
На фиг.11 показаны титры F-специфического IgG (через 2 недели после второй дозы) после доставки репликона в виде «голой» РНК (0,01-1 мкг), инкапсулированной в липосому РНК (0,01-10 мкг) или упакованной в виде вириона (VRP, 106 инфекционных единиц или МЕ).
На фиг.12 показаны титры F-специфического IgG (кружки) и титры PRNT (прямоугольники) после доставки репликона в виде «голой» РНК (1 мкг), инкапсулированной в липосому РНК (0,1 или 1 мкг) или упакованной в виде вириона (VRP, 106 МЕ). Также представлены титры у интактных мышей. Сплошные линии являются геометрическими средними значениями.
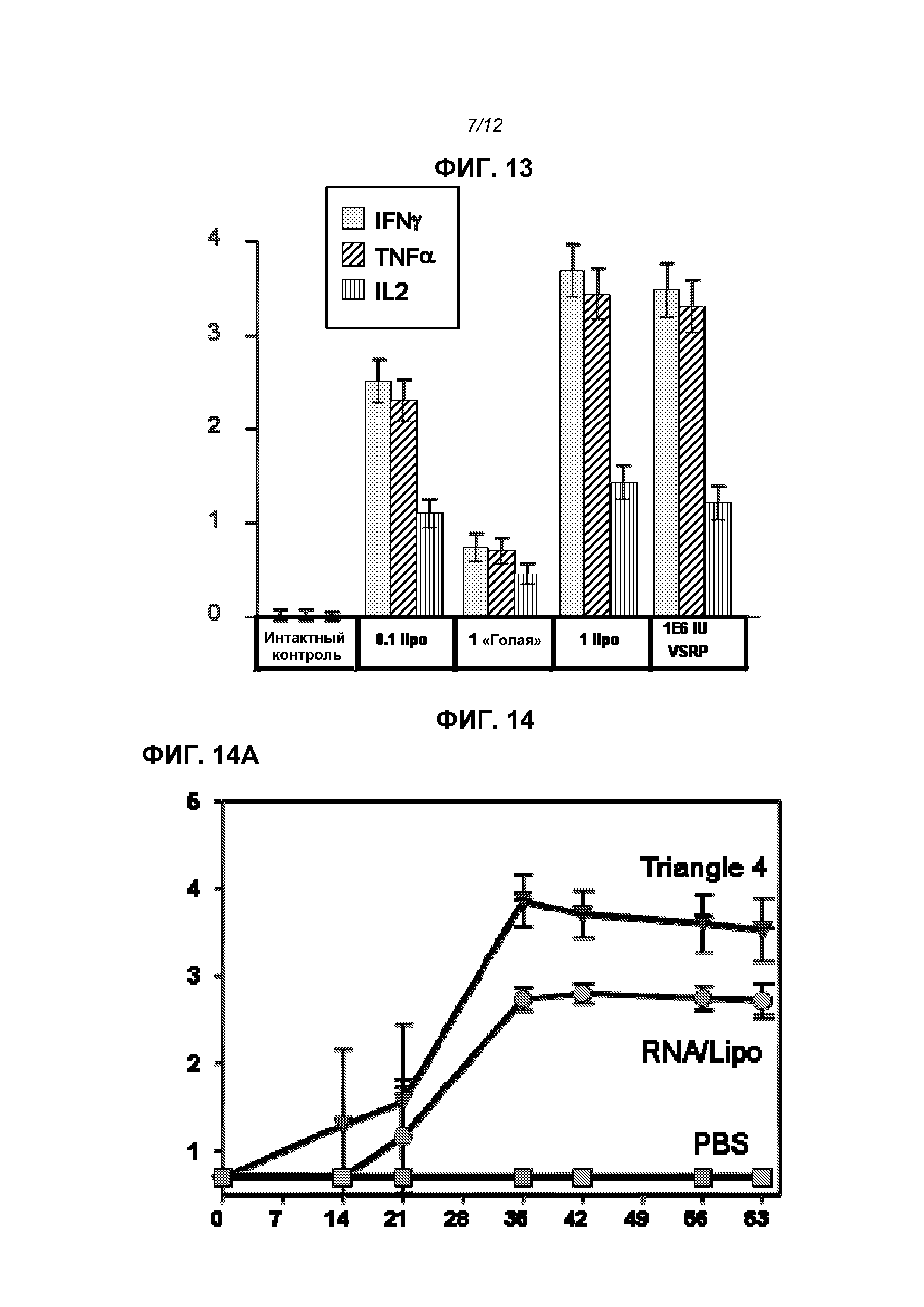
На фиг.13 показана внутриклеточная продукция цитокинов после повторной стимуляции синтетическими пептидами, представляющими основные эпитопы в белке F, 4 недели после второй дозы. На оси Y приведен % цитокина+ CD8+CD4-.
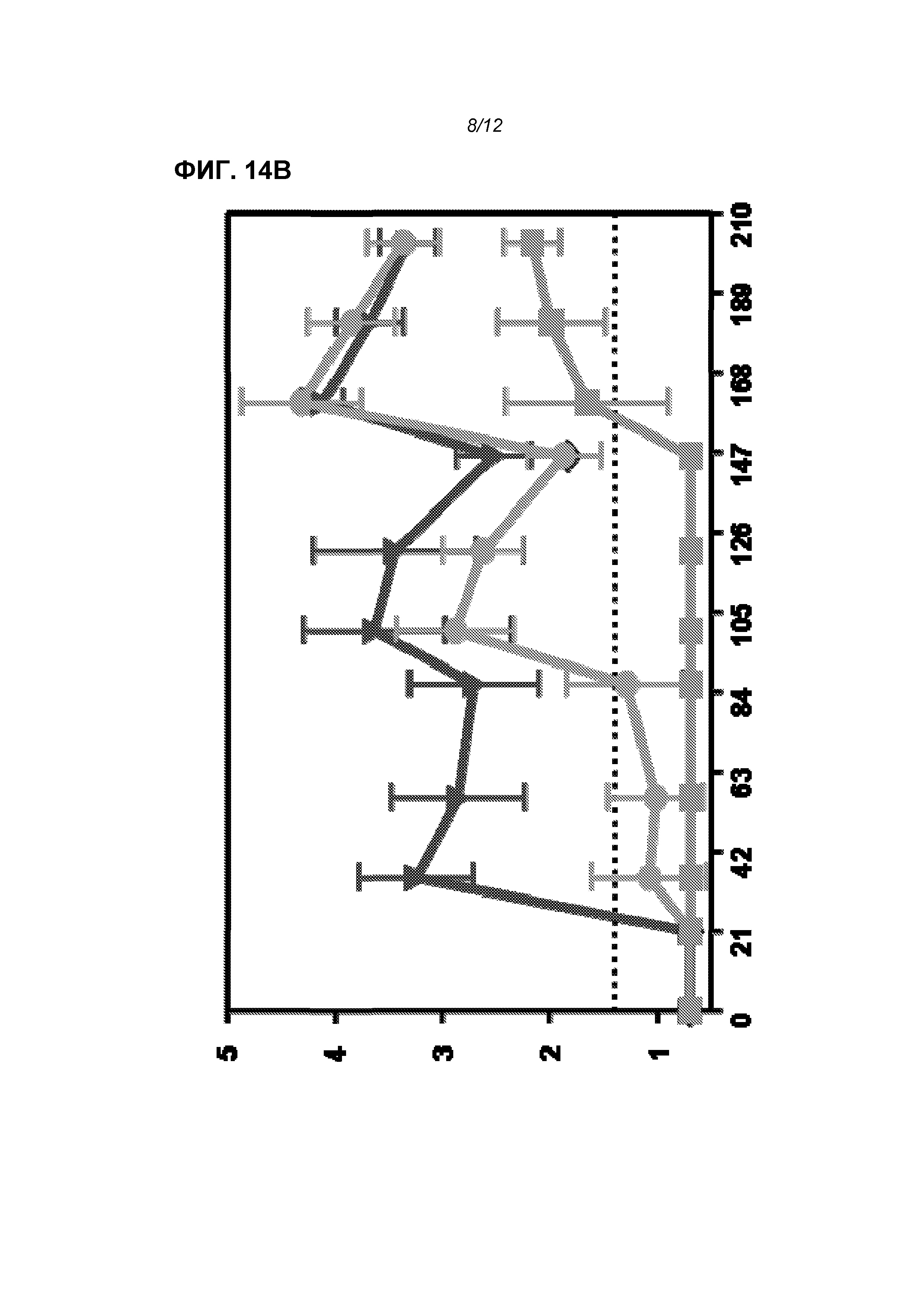
На фиг.14 показаны титры F-специфического IgG (log10 средних значений титров) в течение 63 суток (фиг.14А) и 210 суток (фиг.14В) после иммунизации телят. Три линии легко распознаются на 63 сутки и снизу вверх означают: отрицательный контроль PBS, доставленная в липосомах РНК и продукт «Triangle 2».
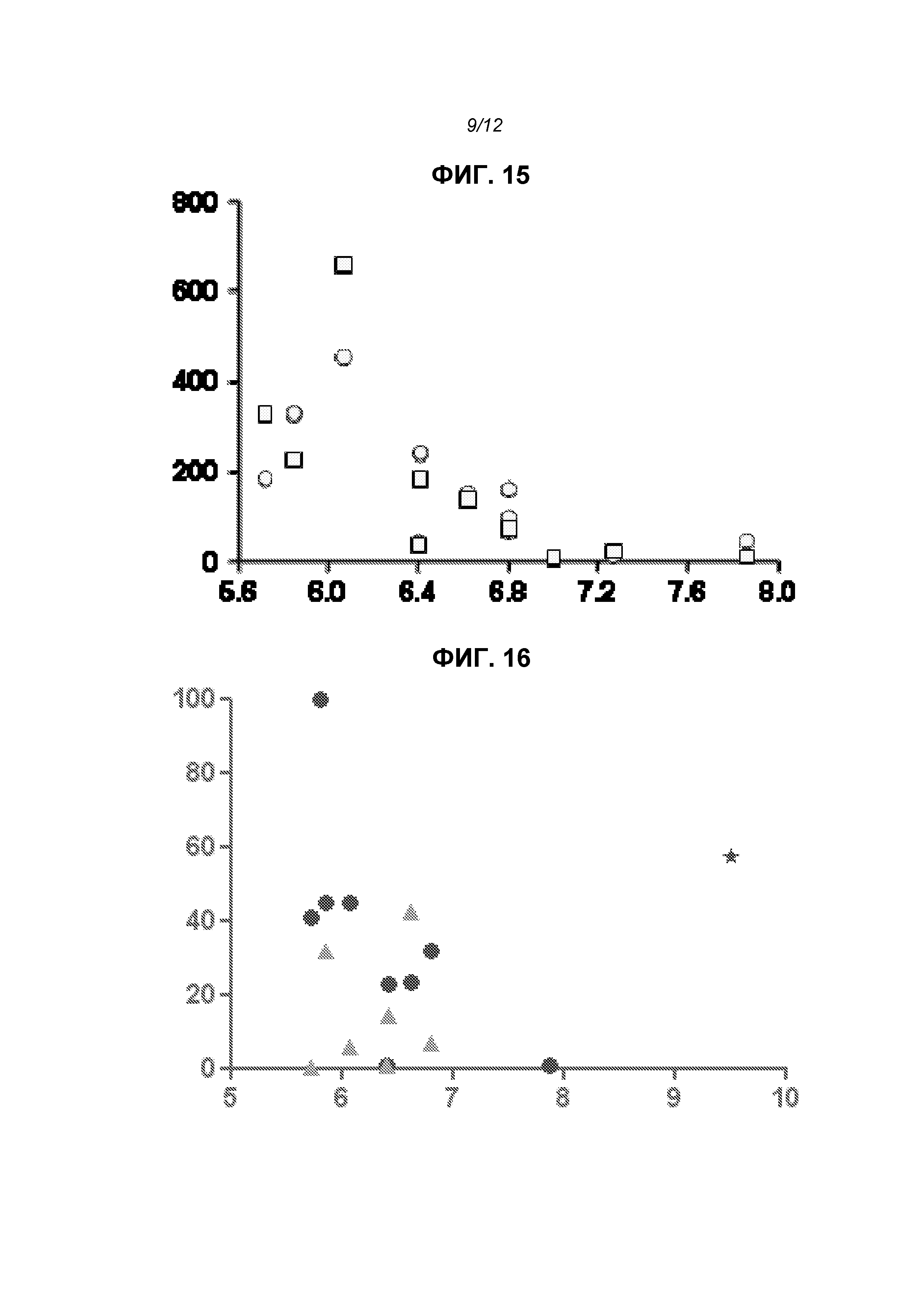
На фиг.15 показана зависимость экспрессии SEAP (относительная интенсивность) на сутки 6 против pKa липидов, использованных в липосомах. Кружки показывают значения для липосом с DSPC и прямоугольники - для липосом без DSPC; в некоторых случаях прямоугольники и кружки перекрываются, оставляя видимыми только прямоугольники для данного значения pKa.
На фиг.16 показана экспрессия титров анти-F-IgG (относительно RV01, 100%) через две недели после первой дозы репликона, кодирующего F-белок. Строили график зависимости титров от pKa аналогично тому, как на фиг.15. Звездочки показывают RV02, в которых использовали катионный липид, имеющий pKa выше, чем другие липиды. Треугольники показывают данные для липосом с отсутствием DSPC; кружки - для липосом, которые содержали DSPC.
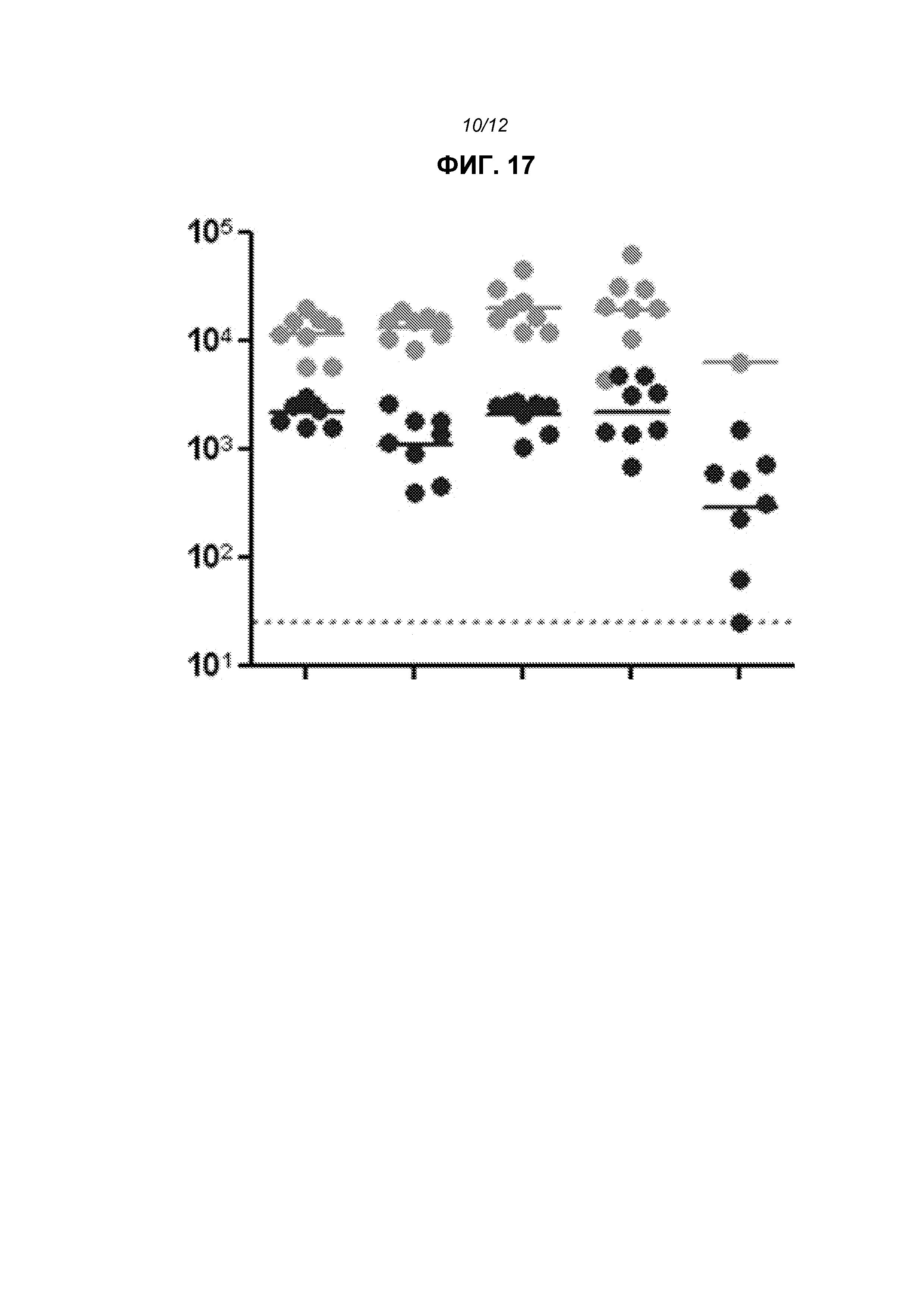
На фиг.17 показаны общие титры IgG после доставки репликона в липосомах с использованием, слева направо, RV01, RV16, RV17, RV18 или RV19. Линии показывают средние значения. Верхняя линия в каждом случае 2wp2 (т.е. через 2 недели после второй дозы), в то время как нижняя линия представляет 2wp1.
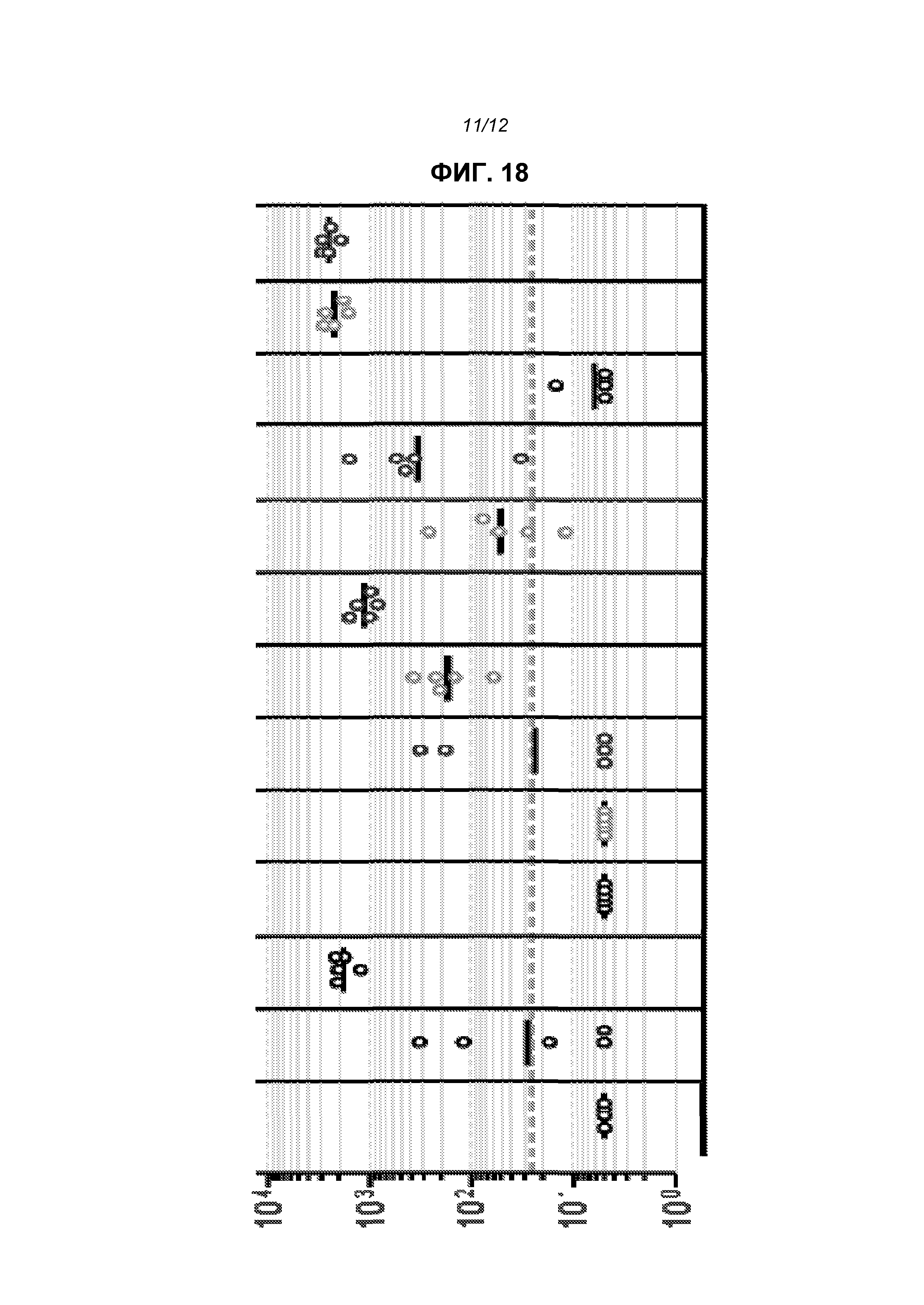
На фиг.18 показаны титры IgG в 13 группах мышей. Каждый кружок означает отдельную мышь, и сплошные линии показывают геометрические средние значения. Прерывистая горизонтальная линия представляет предел определения теста. 13 групп, слева направо, представляют от А до М, как показано ниже.
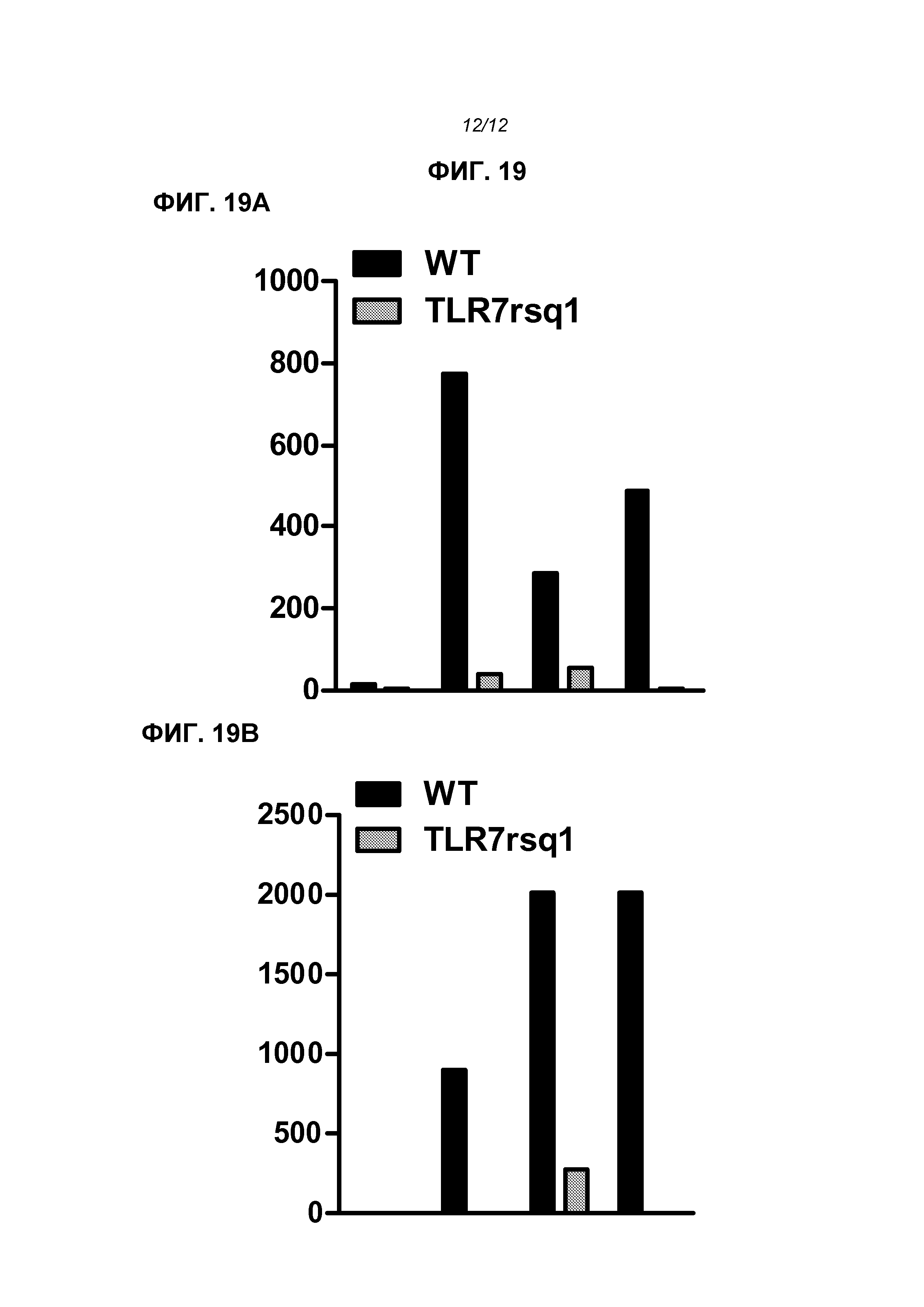
На фиг.19 показано (А) IL-6 и (В) IFNα (пкг/мл), продуцированные pDC. Имеются 4 пары столбцов, слева направо: контроль; иммунизированные РНК+DOTAP; иммунизированные РНК+липофектамин и иммунизированные РНК в липосомах. В каждой паре черный столбец представляет мышей дикого типа, серый - мутанта rsq1.
СПОСОБЫ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
РНК-репликоны
Ниже используются различные репликоны. В целом они основаны на рекомбинантном геноме альфа-вируса с неструктурными белками из вируса венесуэльского энцефалита лошадей (VEEV), сигналом упаковки из вируса Синдбис и 3' UTR из вируса Синдбис или мутанта VEEV. Репликон имеет длину примерно 10 т.п.н. и содержит поли-А-хвост.
Плазмидная ДНК, кодирующая репликоны альфа-вируса (имеющая название: pT7-mVEEV-FL.RSVF или A317; pT7-mVEEV-SEAP или A306; pSP6-VCR-GFP или A50), служила в качестве матрицы для синтеза РНК в условиях in vitro. Репликоны содержат генетические элементы альфа-вируса, необходимые для репликации РНК, но в них отсутствуют элементы, кодирующие продукты гена, необходимые для сборки частиц; структурные белки замещены интересующим белком (репортером, таким как SEAP или GFP, или иммуногеном, таким как полноразмерный RSV F-белок) и, таким образом, репликоны не способны индуцировать генерацию инфекционных частиц. Промотор бактериофага (Т7 или SP6) апстрим кДНК альфа-вируса облегчает синтез РНК-репликона в условиях in vitro, и рибозим вируса гепатита дельта (HDV) сразу же даунстрим поли(А)-хвоста генерирует правильный 3'-конец посредством его саморасщепляющей активности.
После линеаризации плазмидной ДНК даунстрим от рибозима HDV с использованием подходящей рестриктазы, синтезировали «прерванные» транскрипты в условиях in vitro с использованием ДНК-зависимой РНК-полимеразы бактерифага Т7 или SP6. Транскрипции проводили в течение 2 ч при 37°С в присутствии 7,5 мМ (РНК-полимеразы Т7) или 5 мМ (РНК-полимеразы SP6) каждого из нуклеозидтрифосфатов (ATP, CTP, GTP и UTP), следуя инструкциям, предоставленным изготовителем (Ambion). После транскрипции ДНК-матрицу расщепляли ДНКазой TURBO (Ambion). РНК-репликон преципитировали LiCl и восстанавливали в воде, не содержащей нуклеаз. После транскрипции некэпированную РНК кэпировали с использованием Vaccinia Capping Enzyme (VCE) с использованием системы ScriptCap m7G Capping System (Epicentre Biotechnologies), как описано в инструкции для пользователя; репликоны, кэпированные таким образом, представлены с приставкой «v», например, vA317 является репликоном A317, кэпированным VCE. После транскрипции кэпированную РНК преципитировали LiCl и восстанавливали в воде, не содержащей нуклеаз. Концентрацию образцов РНК анализировали по определению OD260nm. Целостность транскриптов in vitro подтверждали электрофорезом в агарозном геле в денатурирующих условиях.
Липосомальное инкапсулирование
РНК инкапсулировали в липосомах, приготовленных способом, описанным в источниках 11 и 42. Липосомы готовили из 10% DSPC (цвиттерионный), 40% DLinDMA (катионный), 48% холестерина и 2% конъюгированного с ПЭГом DMG (ПЭГ 2 kDa). Данные относительные количества относятся к моль % к всей липосоме.
DLinDMA (1,2-дилинолеилокси-N,N-диметил-3-аминопропан) синтезировали с использованием метода, описанного в источнике 6. DSPC (1,2-диастероил-sn-глицеро-3-фосфохолин) получали от Genzyme. Холестерин получали от Sigma-Aldrich. Конъюгированный с ПЭГом DMG (1,2-димиристоил-sn-глицеро-3-фосфоэтаноламин-N-[метокси(полиэтиленгликоль] аммониевая соль), DOTAP (1,2-диолеоил-3-триметиламмоний пропан хлорид) и DC-chol (3β-[N-(N',N'-диметиламиноэтан)карбамоил]холестерин гидрохлорид) получали от Avanti Polar Lipids.
Вкратце, липиды растворяли в этаноле (2 мл), РНК-репликон растворяли в буфере (2 мл, 100 мМ цитрата натрия, рН 6) и растворы смешивали с 2 мл буфера с последующим уравновешиванием в течение 1 ч. Смесь разбавляли 6 мл буфера, затем фильтровали. Полученный продукт содержал липосомы, с эффективностью инкапсулирования примерно 95%.
Например, в одном конкретном способе готовили свежие маточные растворы в этаноле. Взвешивали 37 мг DLinDMA, 11,8 мг DSPC, 27,8 мг холестерина и 8,07 мг ПЭГ-DMG и растворяли в 7,55 мл этанола. Свежеприготовленный маточный раствор липидов осторожно качали при 37°С примерно в течение 15 мин с получением гомогенной смеси. Затем 755 мкл маточного раствора добавляли к 1,245 мл этанола с получением рабочего маточного раствора липидов объемом 2 мл. Это количество липидов использовали для получения липосом с 250 мкг РНК. Также готовили 2 мл рабочего раствора РНК из маточного раствора с концентрацией ≈1 мкг/мкл в 100 мМ цитратном буфере (рН 6). Три стеклянных сосуда емкостью 20 мл (с магнитной мешалкой) промывали раствором RNase Away (Molecular BioProducts) и промывали избытком воды MilliQ перед использованием для инактивации РНКаз в сосудах. Один из сосудов использовали для рабочего раствора РНК и другие для сбора смесей липида и РНК (как описано ниже). Рабочие растворы липидов и РНК нагревали при 37°С в течение 10 мин перед загрузкой в шприцы 3cc «Луер Лок». В другой шприц 3cc вносили 2 мл цитратного буфера (рН 6). Шприцы, содержащие РНК и липиды, подсоединяли к Т-смесителю (PEEKTM 500 мкм ID junction, Idex health Science), используя трубку из FEP (фторированный этилен-пропилен; все использованные FEP-трубки имели внутренний диаметр 2 мм и внешний диаметр 3 мм). Выходное отверстие Т-смесителя также представляло трубку из FEP. Третий шприц, содержащий цитратный буфер, соединяли с отдельным участком FEP-трубки. Затем содержимое всех шприцов приводилось в движение со скоростью 7 мл/мин с использованием шприцевого насоса. Выходные отверстия трубок располагались для сбора смесей в стеклянном сосуде емкостью 20 мл (с одновременным перемешиванием). Затем извлекали магнитные мешалки, и смеси этанол/водный раствор давали уравновеситься при комнатной температуре в течение 1 ч. 4 мл смеси загружали в шприц 5 сс, который был соединен с участком FEP-трубки, и в другой шприц 5 сс, соединенный с таким же по длине участком FEP-трубки, загружали равное количество 100 мМ цитратного буфера (рН 6). Содержимое двух шприцов приводили в движение со скоростью 7 мл/мин с использованием шприцевого насоса и конечную смесь собирали в стеклянном сосуде емкостью 20 мл (с одновременным перемешиванием). Затем смесь, собранную на второй стадии сбора (липосомы) пропускали через мембрану Mustang Q (анионообменная подложка, которая связывает и удаляет анионные молекулы, производства Pall Corporation). Перед использованием данной мембраны для липосом через нее последовательно пропускали 4 мл 1М NaOH, 4 мл 1М NaCl и 10 мл 100 мМ цитратного буфера (рН 6). Липосомы подогревали в течение 10 мин при 37°С до пропускания через мембрану. Затем липосомы концентрировали до 2 мл и диализовали против 10-15 объемов IX PBS с использованием тангенциального проточного фильтрования перед извлечением конечного продукта. Систему TFF и фильтрационные мембраны из полых волокон получали от Spectrum Labs (Rancho Dominguez) и использовали согласно указаниям изготовителя. Использовали полисульфоновые фильтрационные мембраны из полых волокон с отсечением по молекулярной массе 100 kD и площадью поверхности 8 см2. Для экспериментов in vitro и in vivo композиции разбавляли до требуемой концентрации РНК с использованием IX PBS.
На фиг.2 показан пример электронной микрофотографии липосом, приготовленных данными способами. Эти липосомы содержат инкапсулированную РНК, кодирующую полноразмерный антиген RSV F. Результаты динамического рассеяния света одной партии показывали, что средний диаметр равен 141 нм (по интенсивности) или 78 нм (по числу).
Определяли процент инкапсулированной РНК и концентрацию РНК с использованием набора Quant-iT RiboGreen RNA reagent (Invitrogen), следуя инструкциям изготовителя. Стандарт рибосомальной РНК, включенный в набор, использовали для построения калибровочной кривой. Липосомы разводили 10× или 100× буфером 1X TE (из набора) перед добавлением красителя. Отдельно липосомы разводили 10× или 100× буфером 1X TE, содержащим 0,5% Тритона Х до добавления красителя (для разрушения липосом и, таким образом, анализа общей фракции РНК). Затем добавляли равное количество красителя в каждый раствор и затем ≈180 мкл каждого раствора, после добавления красителя, вносили в двух параллелях в 96-луночный планшет для культивирования тканей. Определяли флуоресценцию (длина волны возбуждения 485 нм, длина волны эмиссии 528 нм) на ридере для планшетов. Все композиции липосом дозировали in vivo по инкапсулированному количеству РНК.
Было показано, что липосомы защищали РНК от расщепления РНКазой. В опытах использовали 3,8 mAU РНКазы А на мкг РНК, инкубировали в течение 30 мин при комнатной температуре. РНКазу инактивировали протеиназой К при 55°С в течение 10 мин. Затем добавляли смесь образца добавляли 1:1 об/об к смеси фенол:хлороформ:изоамиловый спирт 25:24:1 об/об/об для экстракции РНК из липидов в водную фазу. Образцы смешивали на вортексе в течение нескольких секунд и затем помещали в центрифугу на 15 мин при 12k RPM. Водную фазу (содержащую РНК) удаляли и использовали для анализа РНК. Перед загрузкой (400 нг РНК на лунку) все образцы инкубировали с красителем, содержащим формальдегид, денатурировали в течение 10 мин при 65°С и охлаждали до комнатной температуры. Использовали маркеры Ambion Millennium для приближения к молекулярной массе РНК-конструкции. Электрофорез в геле проводили при 90 В. Гель окрашивали с использованием красителя 0,1% SYBR gold согласно инструкциям изготовителя в воде при качании при комнатной температуре в течение 1 ч. На фиг.1 показано, что РНКаза полностью расщепляет РНК в отсутствии инкапсулирования (дорожка 3). РНК не детектируется после инкапсулирования (дорожка 4), и отсутствовали изменения, если липосомы обрабатывали РНКазой (дорожка 4). После обработки РНКазой липосомы подвергали экстракции фенолом, видна нерасщепленная РНК (дорожка 6). Даже после 1 недели при 4°С РНК детектировали без какой-либо фрагментации (фиг.4, стрелка). Экспрессия белка in vivo не изменялась через 6 недель выдерживания при 4°С и одного цикла замораживания-оттаивания. Таким образом, инкапсулированная в липосоме РНК является стабильной.
Для оценки экспрессии РНК in vivo репортерный фермент (SEAP; секретированная щелочная фосфатаза) кодировали в репликон в большей степени, чем в иммуноген. Определяли уровни экспрессии в сыворотке крови, разведенной 1:4 в буфере для разведения 1X Phospa-Light, с использованием хемилюминесцентного субстрата щелочной фосфатазы. 8-10-недельным мышам BALB/c (5 животных/на группу) вводили внутримышечно на сутки 0 по 0,50 мкл на конечность в дозе 0,1 мкг или 1 мкг РНК. Этот же вектор также вводили без липосом (в 1X PBS, не содержащем РНКазу) в дозе 1 мкг. Также тестировали упакованные в вирион репликоны. Упакованные в вирион репликоны, использованные в данном случае (далее относится к «VRP»), получали с использованием способов, описанных в источнике 43, где альфа-вирусный репликон был получен из мутантного VEEV или химеры, полученной из генома VEEV, сконструированного с включением 3' UTR вируса Синдбис и сигнала упаковки вируса Синдбис (PS), упакованных совместной электропорацией в клетки BHK с дефектными хэлперными РНК, кодирующими гены капсида вируса Синдбис и гликопротеина.
Как показано на фиг.5, инкапсулирование повышало уровни SEAP примерно на ½ log при дозе 1 мкг, и на 6 сутки экспрессия после введения 0,1 мкг инкапсулированной дозы совпадала с уровнями, наблюдаемыми для 1 мкг неинкапсулированной дозы. На 3 сутки уровни экспрессии превышали таковые, достигаемые с VRP (прямоугольники). Таким образом, экспрессия возрастала, когда РНК формулировали в липосомы по сравнению с контрольной «голой» РНК, даже в 10 раз более низкой дозе. Экспрессия также была выше по сравнению с контролем VRP, но кинетика экспрессии была очень различной (смотри фиг.5). Доставка РНК электропорацией приводила к повышенной экспрессии по сравнению с «голой» РНК, но эти уровни были ниже по сравнению с липосомами.
Для оценки того, насколько эффект, наблюдаемый в группах с липосомами, имел место только за счет компонентов липосомы или был непосредственно связан с инкапсулированием, репликон вводили в инкапсулированной форме (с двумя различными протоколами выделения, 0,1 мкг РНК) или смешивали с липосомами после их приготовления (неинкапсулированный «липоплекс», 0,1 мкг РНК), или в виде «голой» РНК (1 мкг). На фиг.10 показано, что липоплекс давал наиболее низкие уровни экспрессии, свидетельствуя о том, что инкапсулирование является важным для обеспечения высокой экспрессии.
Опыты in vivo с использованием доставки в липосомах подтвердили эти установленные факты. Мышам вводили различные комбинации (i) самореплицирующийся РНК-репликон, кодирующий полноразмерный RSV F-белок, (ii) самореплицирующийся РНК-репликон, кодирующий GFP, (iii) РНК-репликон, кодирующий GFP, с нокаутом в nsP4, что элиминировало саморепликацию, (iv) полноразмерный RSV F-белок. 13 групп мышей в целом получали:
|
|
Результаты, приведенные на фиг.18, показывают, что для ответной продукции F-специфического IgG требуется инкапсулирование в липосоме в большей степени, чем только совместная доставка с пустыми липосомами (сравните группы С&D). Сравнение данных по группам K, L и М показывает, что РНК обеспечивает адъювантный эффект против совместно доставленного белка, и данный эффект имел место как с реплицирующейся, так и нереплицирующейся РНК.
Дальнейшие опыты с SEAP показали наличие четкой зависимости доза-ответ в условиях in vivo для экспрессии, регистрируемой после доставки, по меньшей мере, 1 нг РНК (фиг.6). Результаты дальнейших экспериментов по сравнению экспрессии от инкапсулированного и «голого» репликонов указывали, что действие 0,01 мкг инкапсулированной РНК эквивалентно действию 1 мкг «голой» РНК. Инкапсулированное вещество в дозе 0,5 мкг РНК приводило к более высокой 12-кратной экспрессии на 6 сутки; в дозе 0,1 мкг - к 24-кратной экспрессии на 6 сутки.
Проводили анализ не только средних значений по группе, но также исследовали отдельных животных. В то время, как несколько животных не были респондерами на «голые» репликоны, инкапсулирование элиминировало наличие таких нон-респондеров.
В дальнейших опытах DLinDMA заменяли на DOTAP. Несмотря на то, что липосомы с DOTAP приводили к лучшей экспрессии по сравнению с «голым» репликоном, их эффект был ниже по сравнению с липосомами, содержащими DLinDMA (на 1 сутки различие составило 2-3 раза). В то время как DOTAP содержит четвертичный амин, и, таким образом, имеет положительный заряд в точке доставки, DLinDMA содержит третичный амин.
Для оценки иммуногенности in vivo конструировали репликон для экспрессии полноразмерного F-белка из респираторного синцитиального вируса (RSV). Его вводили «голым» (1 мкг), инкапсулированным в липосомы (0,1 или 1 мкг) или упакованным в вирионы (106 МЕ; «VRP») на сутки 0 и 21. На фиг.7 приведены титры анти-F-IgG через 2 недели после второй дозы, и липосомы четко повышали иммуногенность. На фиг.8 показаны титры еще через 2 недели, на этой временной точке отсутствовала статистически достоверная разница между группами с инкапсулированной РНК в дозе 0,1 мкг, инкапсулированной РНК в дозе 1 мкг или VRP. Титры нейтрализации (определено в виде 60% снижения бляшкообразования, «PRNT60») не различались статистически значимым образом в данных трех группах через 2 недели после второй дозы (фиг.9). На фиг.12 показаны титры IgG и PRNT через 4 недели после второй дозы.
Данные на фиг.13 подтверждают, что РНК индуцирует сильный ответ CD8 Т-клеток.
В дальнейших опытах сравнивали титры F-специфического IgG у мышей, получавших VRP, 0,1 мкг инкапсулированной в липосомы РНК или 1 мкг инкапсулированной в липосомы РНК. Соотношения титров (VRP:липосома) на различные периоды времени после второй дозы были следующими:
|
Таким образом, инкапсулированная в липосомы РНК индуцировала по существу такой же иммунный ответ, что и введение вирионов.
В дальнейших опытах была показана более высокая ответная продукция F-специфического IgG с дозой 10 мкг, эквивалентные ответы на дозы 1 мкг и 0,1 мкг, и более низкий ответ на дозировку 0,01 мкг. На фиг.11 показаны титры IgG у мышей, получавших репликон в «голой» форме при введении в трех различных дозах, в липосомах в 4 различных дозах или VRP (106 МЕ). Ответ, наблюдаемый с 1 мкг инкапсулированной в липосомы РНК не отличался статистически достоверно (ANOVA) по сравнению с VRP, но был установлен достоверно более высокий ответ на 10 мкг инкапсулированной в липосомы РНК (Р<0,05) по сравнению с обеими группами.
Результаты дополнительного опыта подтвердили, что 0,1 мкг инкапсулированной в липосомы РНК обеспечивало более высокую ответную продукцию анти-F-IgG (через 15 суток после второй дозы) по сравнению с 0,1 мкг доставленной ДНК, и первая была более иммуногенной по сравнению с 20 мкг плазмидной ДНК, кодирующей F-антиген, доставленной электропорацией (ElgenTM DNA Delivery System, Inovio).
Проводили дополнительное исследование на хлопковых крысах (Sigmodon hispidis) вместо мышей. Инкапсулирование в липосомы в дозе 1 мкг приводило к повышению титров F-специфического IgG в 8,3 раза по сравнению с «голой» РНК и к повышению титров PRNT в 9,5 раз. Уровень ответной продукции антител был эквивалентным ответу, индуцированному 5×106 МЕ VRP. «Голая» и инкапсулированная в липосомы РНК были способны защитить хлопковых крыс от заражения RSV (1×105 бляшкообразующих единиц), снижая вирусную нагрузку в легких, по меньшей мере, в 3,5 log. Инкапсулирование усиливало снижение примерно в 2 раза.
Опыт на крупных животных проводил на крупном рогатом скоте. Коров иммунизировали 66 мкг репликона, кодирующего полноразмерный RSV F-белок на сутки 0 и 21, формулированного в липосомах. Один PBS использовали а качестве отрицательного контроля, а официально разрешенную вакцину использовали в качестве положительного контроля («Triangle» 4 производства Fort Dodge, содержащую убитый вирус). На фиг.14 показаны титры F-специфического IgG в течение 63-суточного периода, начиная от первой иммунизации. РНК-репликон был иммуногенным у коров, хотя, он индуцировал более низкие титры по сравнению официально разрешенной вакциной. У всех вакцинированных коров детектировали наличие F-специфических антител после второй дозы, и титры были очень стабильными в период 2-6 недель после введения второй дозы (и были особенно стабильными для РНК-вакцины).
Механизм действия
Дендритные клетки, генерированные из костного мозга (pDC), получали от мышей дикого типа или мышей мутантного штамма «Resq» (rsq1). Мутантный штамм содержит точечную мутацию в аминоконце рецептора TLR7, что элиминирует сигнальный путь TLR7, не оказывая влияние на связывание лиганда [44]. Клетки стимулировали РНК-репликоном, формулированным с DOTAP, липофектамином 2000 и внутри липосомы. Как показано на фиг.16, IL-6 и INFα продуцировались клетками мышей дикого типа, но данный ответ почти полностью отсутствовал у мутантных мышей. Эти результаты свидетельствуют о том, что TLR7 необходим для распознавания РНК в иммунных клетках, и что инкапсулированные в липосомах репликоны могут стимулировать иммунные клетки к секреции высоких уровней интерферонов и провоспалительных цитокинов.
Определение pKa
pKa липида определяют в воде при обычной температуре и давлении с использованием следующего метода:
- Готовят 2 мМ раствор липида в этаноле взвешиванием липида и растворением в этаноле. Готовят 0,3 мМ раствор флуоресцентного зонда толуолнитросульфоновой кислоты (TNS) в смеси этанол:метанол 9:1 посредством приготовления вначале 3 мМ раствора TNS в метаноле и затем разведением до 0,3 мМ этанолом.
- Готовят водный буфер, содержащий фосфат натрия, цитрат натрия, ацетат натрия и хлорид натрия в концентрациях соответственно 20 мМ, 25 мМ, 20 мМ и 150 мМ. Буфер разделяют на восемь частей и рН доводят 12н HCl или 6н NaOH до 4,44-4,52, 5,27, 6,15-6,21, 6,57, 7,10-7,20, 7,72-7,80, 8,27-8,33 и 10,47-11,12. Смешивают 400 мкл 2 мМ раствора липида и 800 мкл 0,3 мМ раствора TNS.
- 7,5 мкл смеси зонд/липид добавляют к 242,5 мкл буфера в 1 мл в 96-луночном планшете. Так поступают со всеми восьмью буферами. После перемешивания 100 мкл каждой смеси зонд/липид/буфер переносят в 250 мкл в черный 96-луночный планшет с прозрачным дном (например, модель COSTAR 3904, Corning). Удобным способом осуществления такого перемешивания является применение высокопропускного манипулятора для жидкостей Tecan Genesis RSP150 и программного обеспечения Gemini Software.
- Анализируют флуоресценцию каждой смеси зонд/липид/буфер (например, на спектрофотометре SpectraMax M5 и программном обеспечении SoftMax pro 5,2) при длине волны возбуждения 322 нм и длине волны эмиссии 431 нм (аутопорог при 420 нм).
- После анализа вычитают фоновую флуоресценцию пустой лунки в 96-луночном планшете из флуоресценции смеси зонд/липид/буфер. Затем значения флуоресценции нормализуют к значению при наиболее низком рН. Затем строят график зависимости нормализованной флуоресценции против рН и получают линию наилучшей подгонки.
- Находят точку на линии наилучшей подгонки, при которой интенсивность нормализованной флуоресценции равна, 0,5. Находят рН, соответствующий нормализованной интенсивности флуоресценции, равной 0,5, и принимают это значение за pKa липида.
Данный метод дает значение pKa, равное 5,8, для DLinDMA. Значения pKa, анализированные данным методом, для катионных липидов из источника 5 приведены ниже.
Инкапсулирование в липосомах с использованием альтернативных катионных липидов
В качестве альтернативны для DLinDMA использовали катионные липиды из источника 5. Данные липиды можно синтезировать, как описано в источнике 5.
Липосомы, полученные выше, с использованием DLinDMA относятся ниже к серии «RV01». DLinDMA заменяли на различные катионные липиды в сериях «RV02»-«RV12», как описано ниже. Получали два различных типа каждой липосомы с использованием 2% ПЭГ2000-DMG с (01) 40% катионного липида, 10% DSPC и 48% холестерина или (02) 60% катионного липида и 38% холестерина. Таким образом, сравнение липосом (01) и (02) показывает эффект нейтрального цвиттерионного липида.
Липосомы RV02 готовили с использованием следующего катионного липида (pKa>9, без третичного амина):
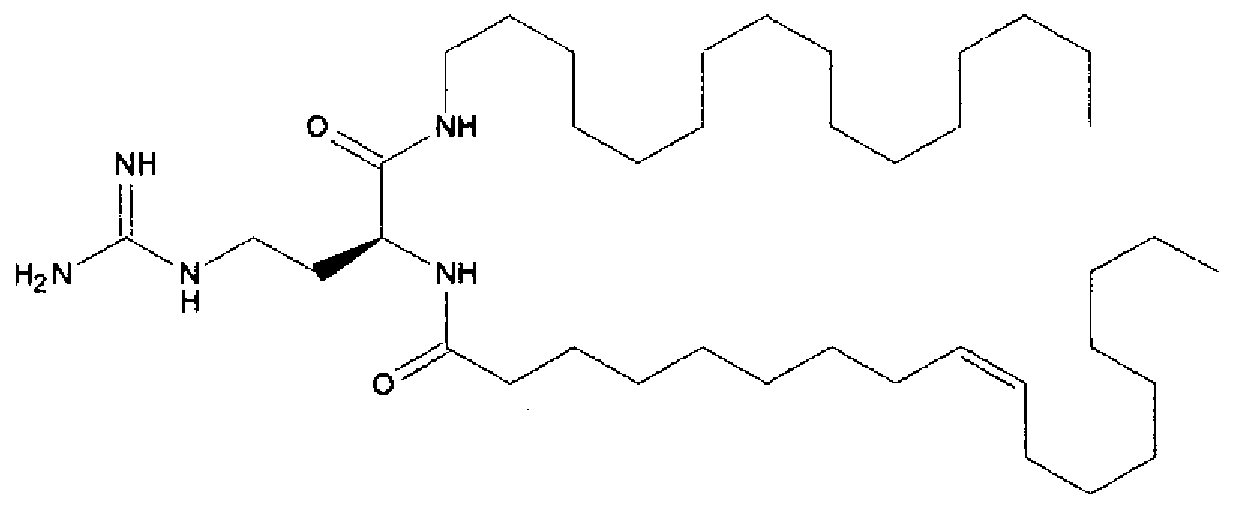
Липосомы RV03 готовили с использованием следующего катионного липида (pKa 6,4):
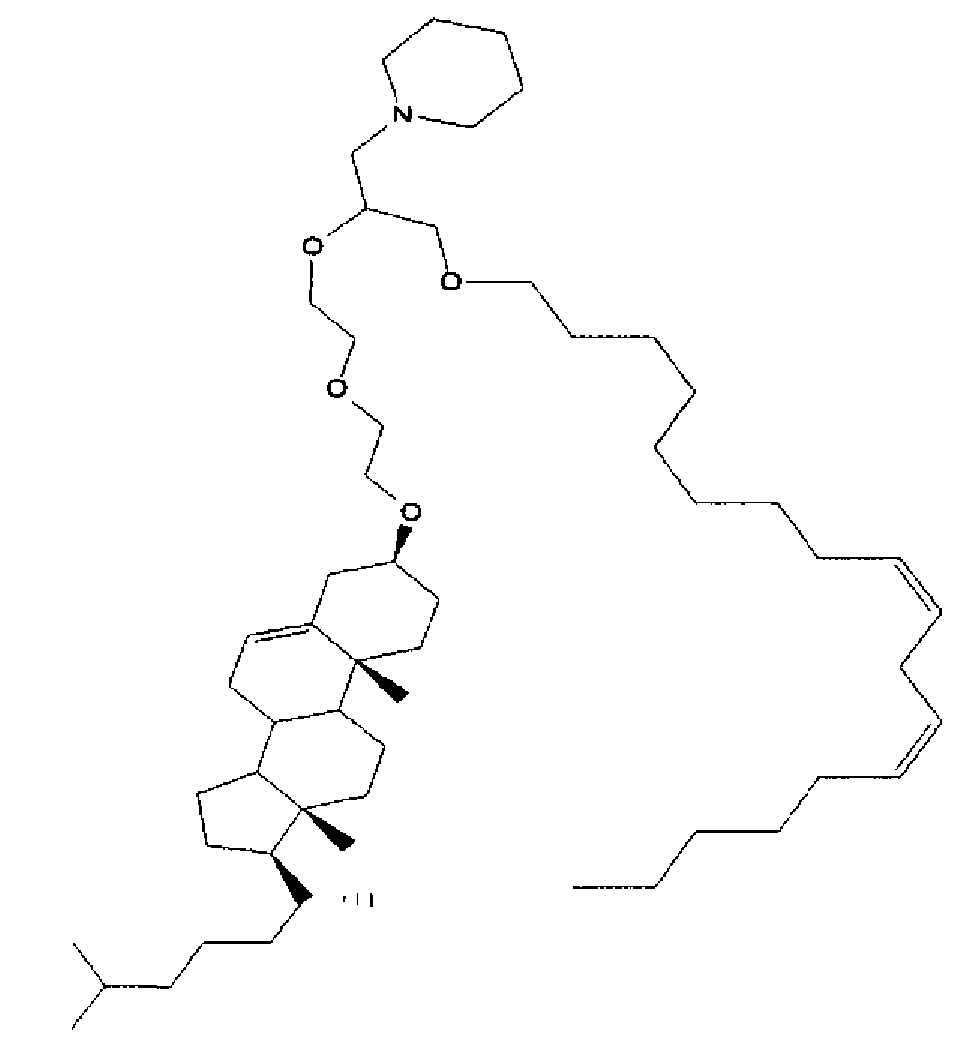
Липосомы RV04 готовили с использованием следующего катионного липида (pKa 6,62):
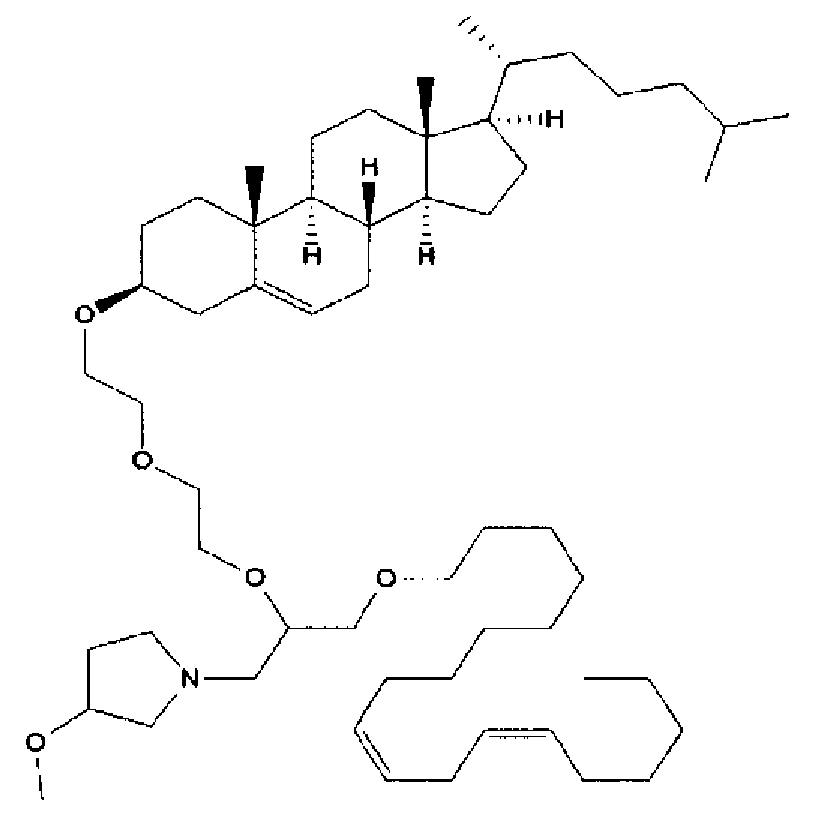
Липосомы RV05 готовили с использованием следующего катионного липида (pKa 5,85):
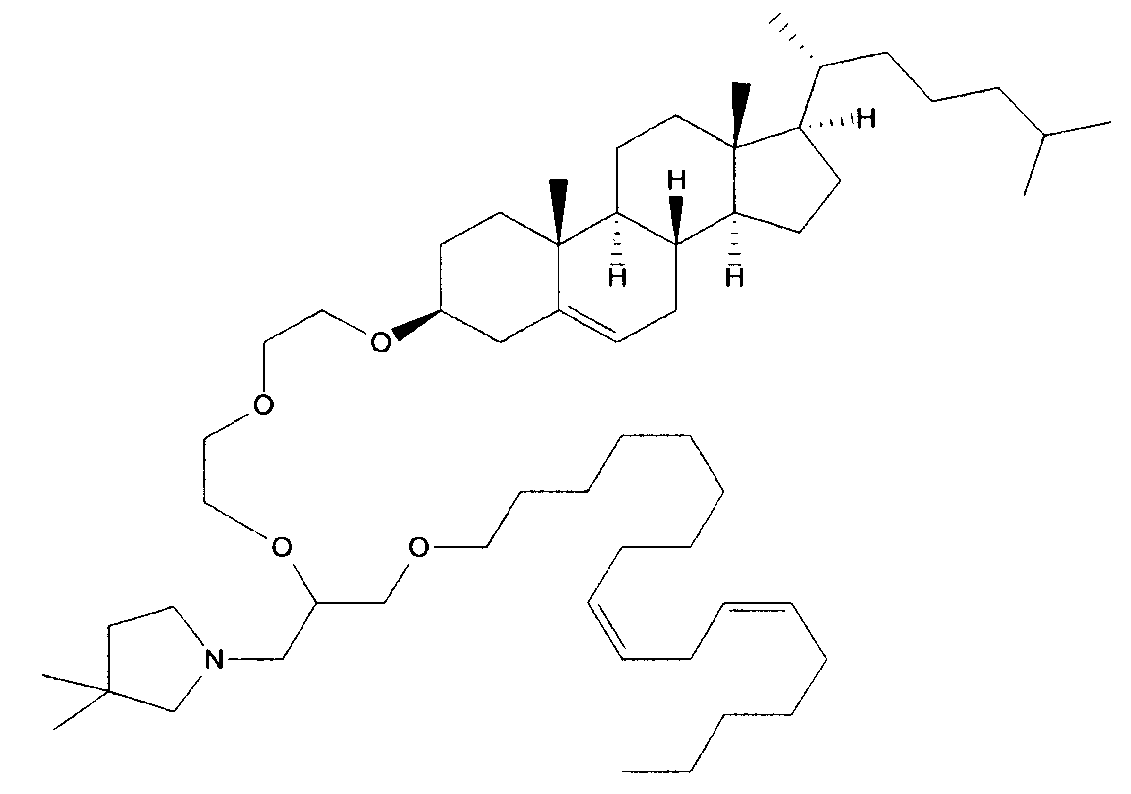
Липосомы RV06 готовили с использованием следующего катионного липида (pKa 7,27):
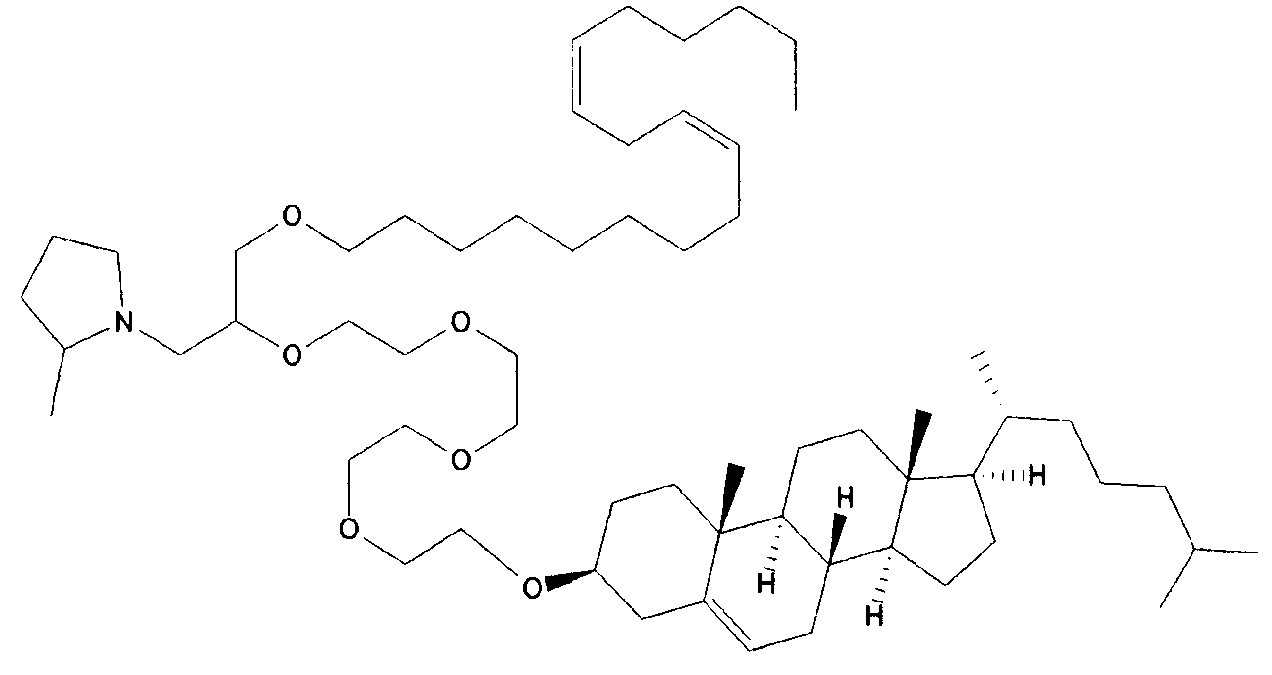
Липосомы RV07 готовили с использованием следующего катионного липида (pKa 6,8):
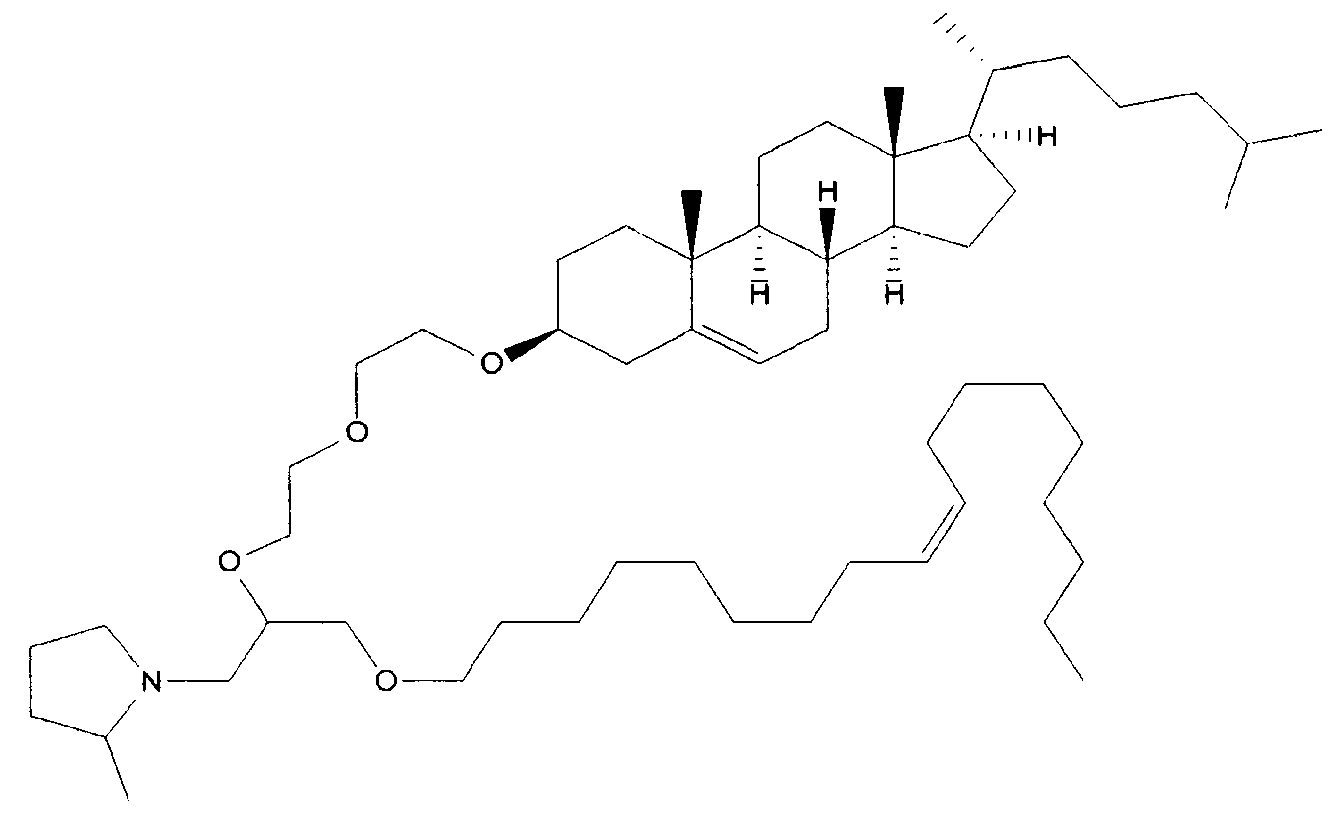
Липосомы RV08 готовили с использованием следующего катионного липида (pKa 5,72):
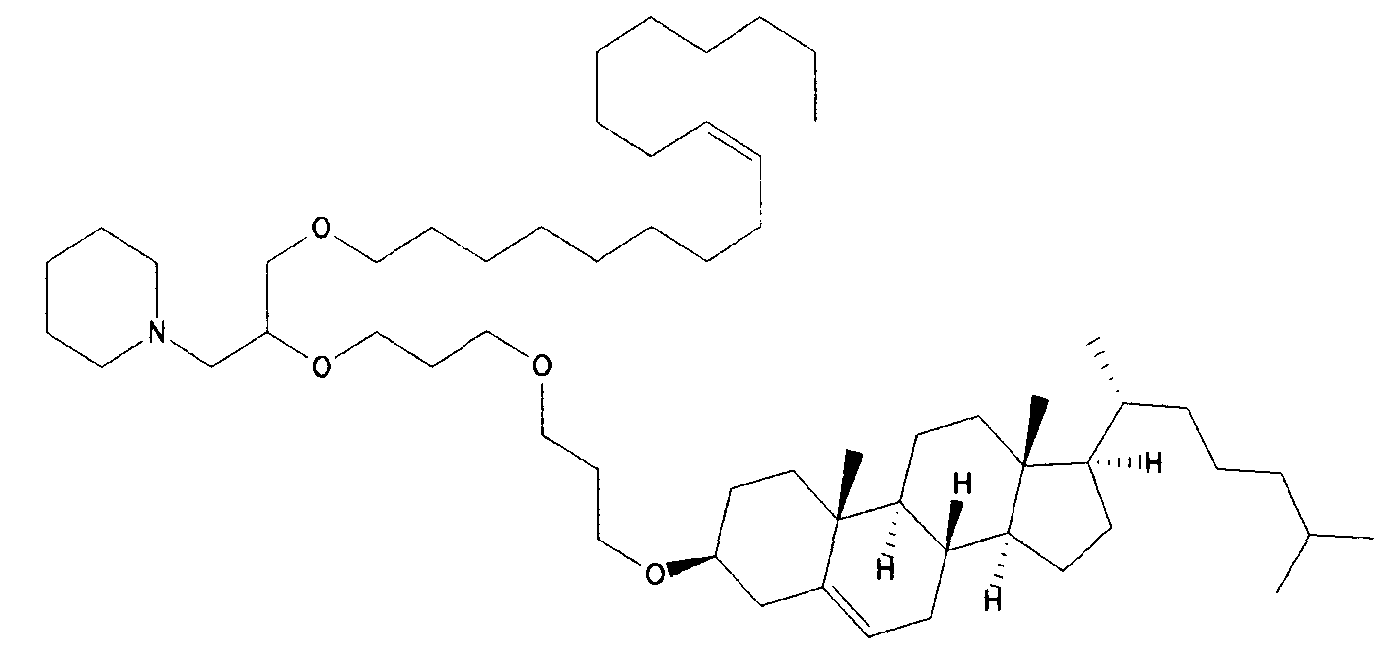
Липосомы RV09 готовили с использованием следующего катионного липида (pKa 6,07):
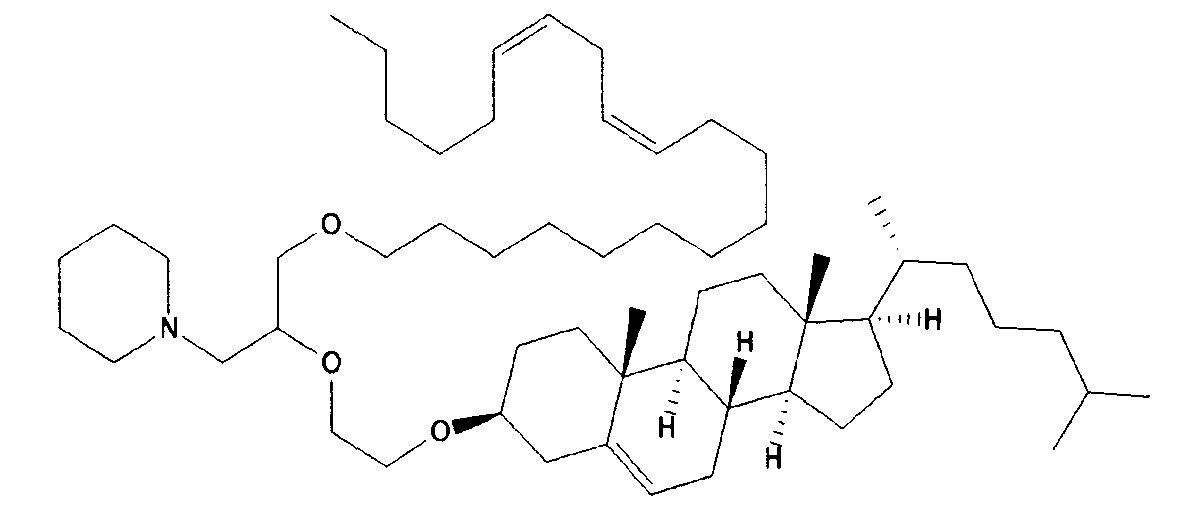
Липосомы RV10 готовили с использованием следующего катионного липида (pKa 7,86):
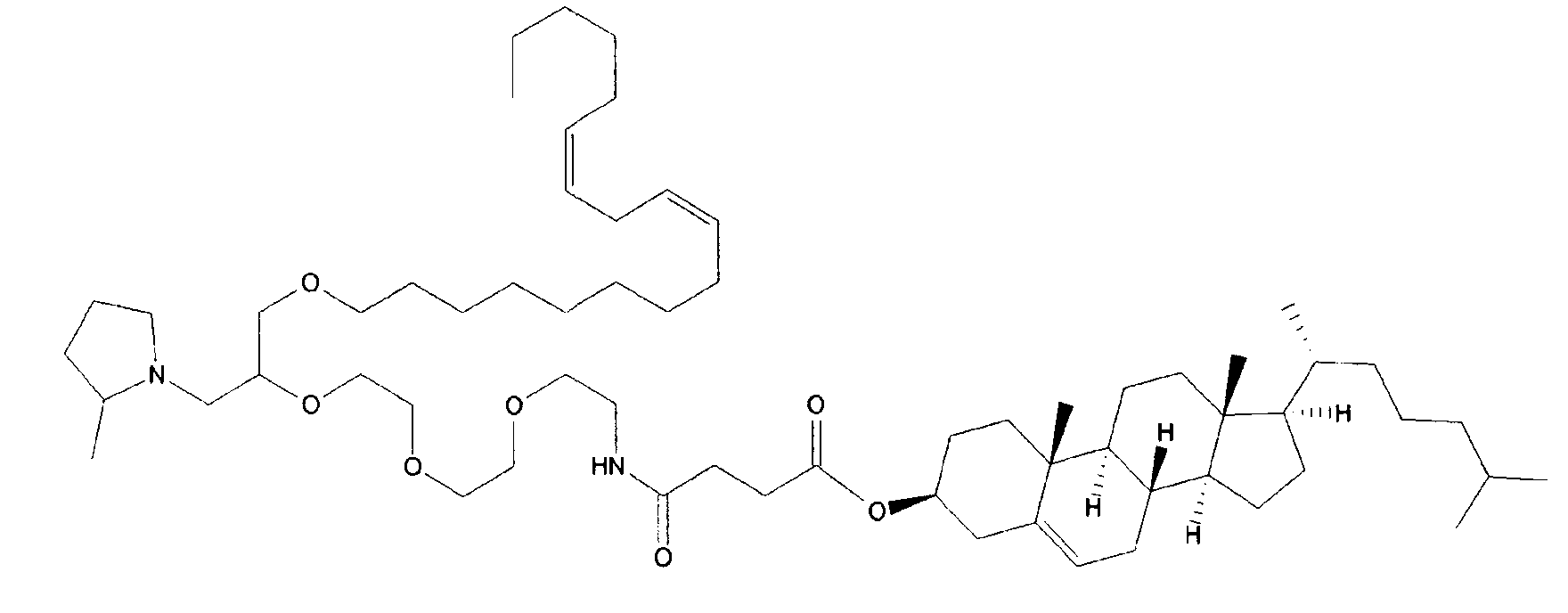
Липосомы RV11 готовили с использованием следующего катионного липида (pKa 6,41):
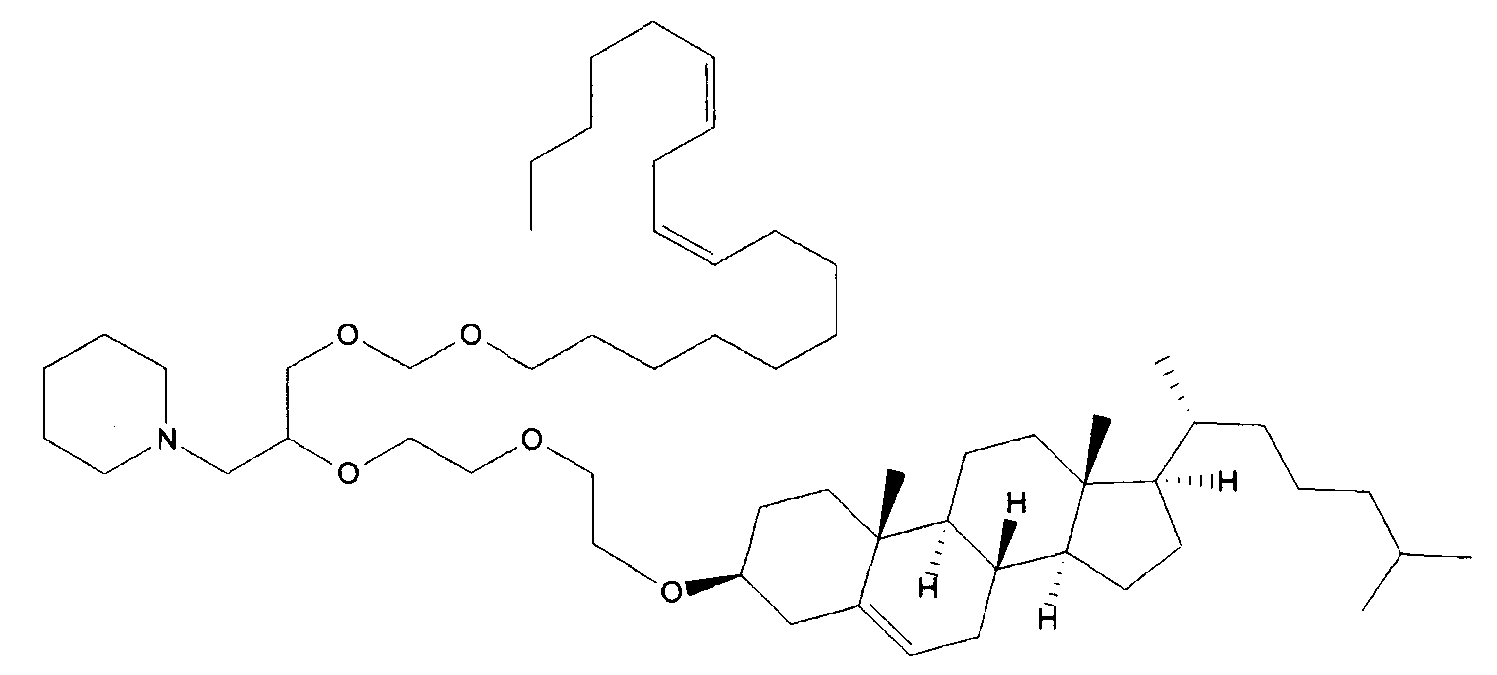
Липосомы RV12 готовили с использованием следующего катионного липида (pKa 7):
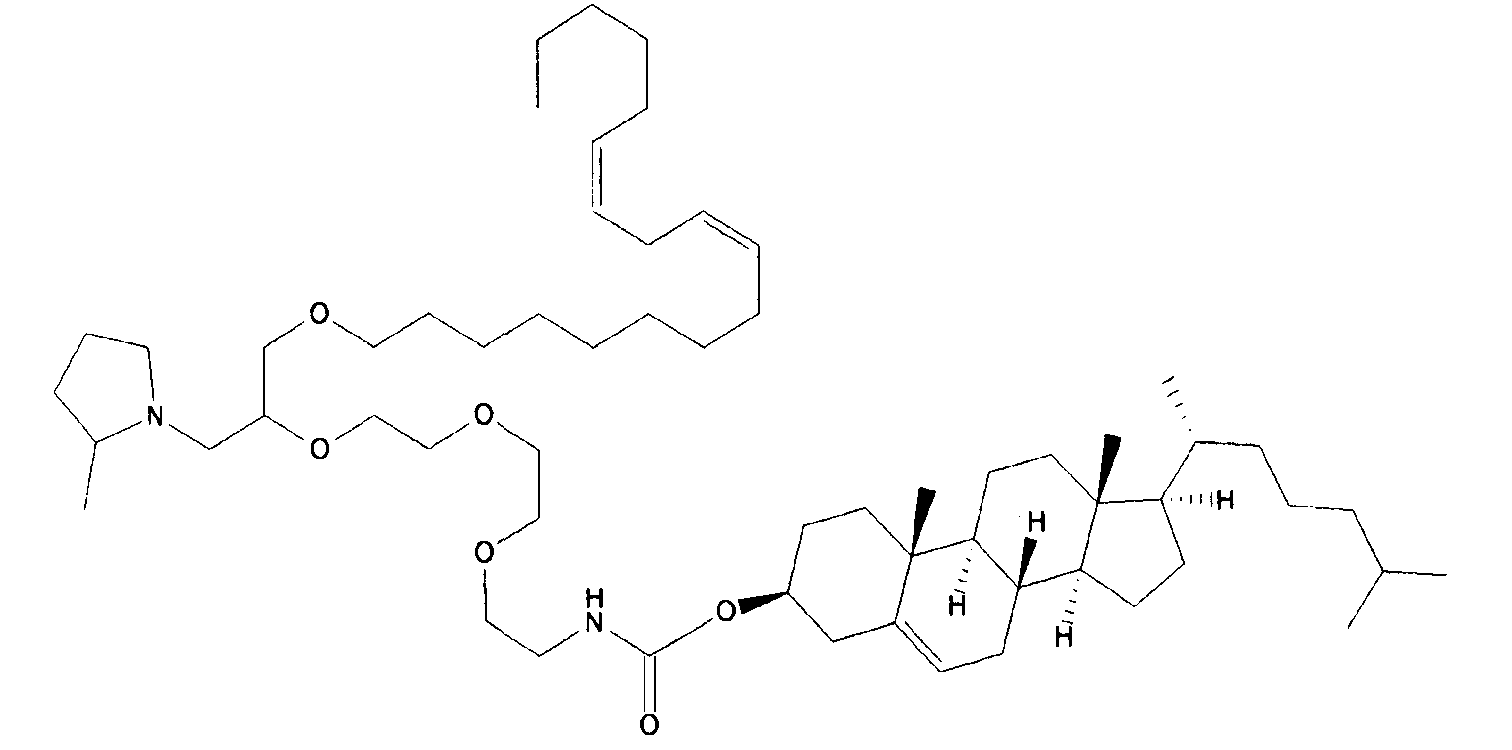
Липосомы RV16 готовили с использованием следующего катионного липида (pKa 6,1) [45]:
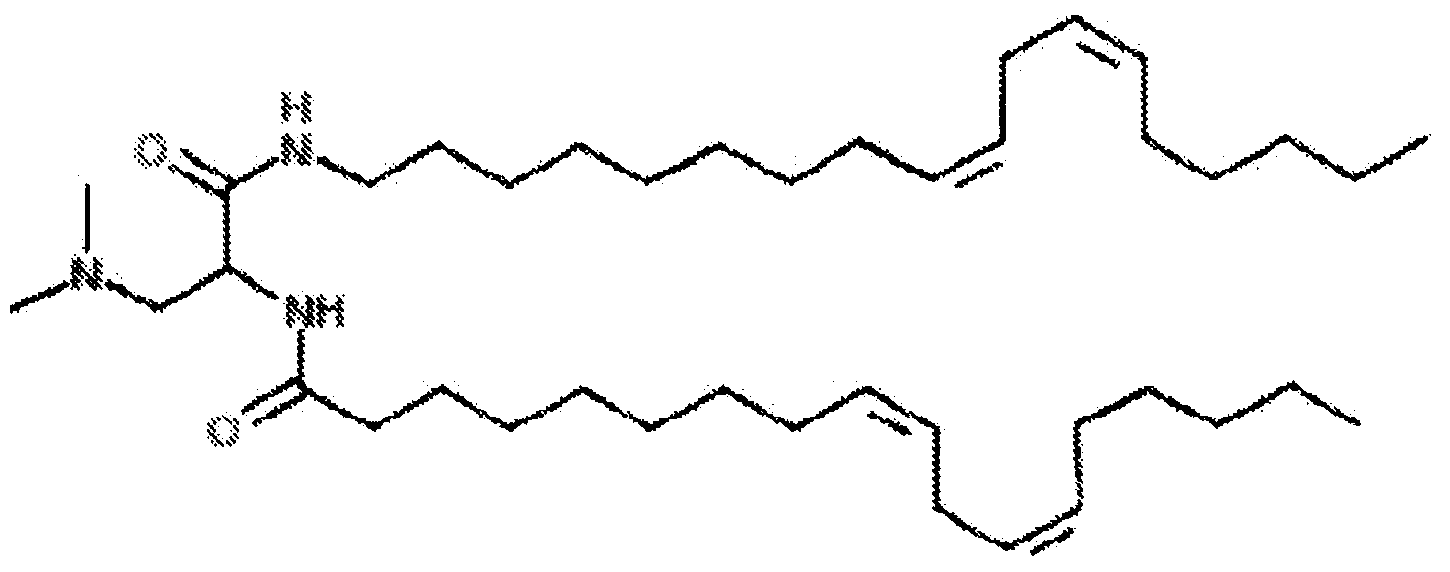
Липосомы RV17 готовили с использованием следующего катионного липида (pKa 7,27):
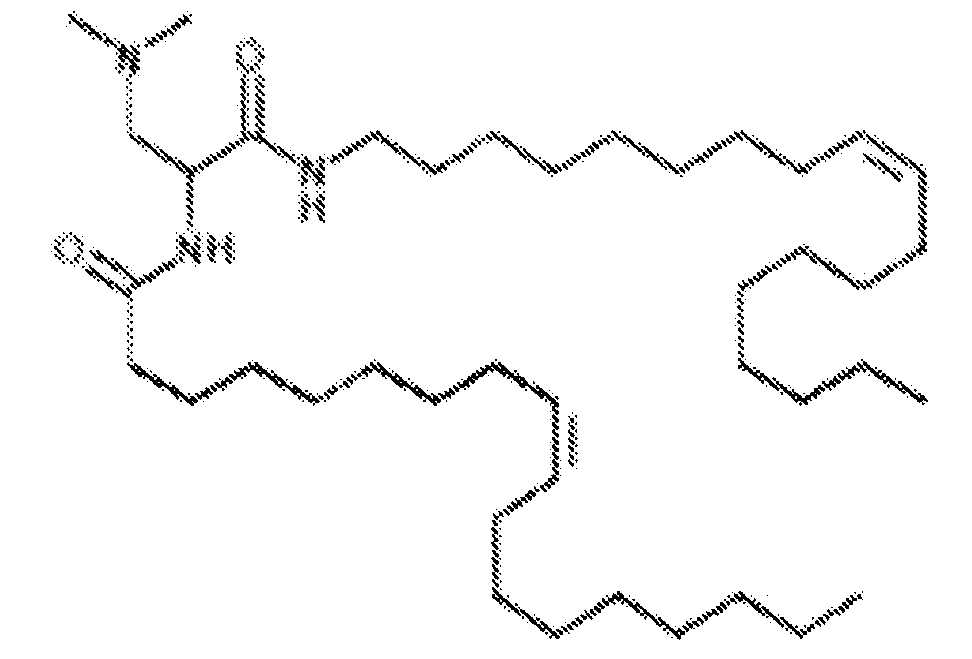
Липосомы RV18 готовили с использованием DODMA. Липосомы RV19 получали с использованием DOTMA, и липосомы RV13 готовили с использованием DOTAP, оба липида содержали «головку» из четвертичного амина.
Липосомы характеризовали и тестировали с использованием репортера SEAP, описанного выше. В следующей таблице приведены размеры липосом (Z средний размер и индекс полидисперности), % инкапсулирования РНК в каждой липосоме, вместе с активностью SEAP, детектированной на 1 и 6 сутки после инъекции. Активность SEAP выражена относительно липосом «RV01(02)», приготовленных из DlinDMA, холестерина и ПЭГ-DMG:
|
На фиг.15 приведены графики зависимости уровней SEAP от pKa катионных липидов на 6 сутки. Наилучшие результаты были получены, когда липид имел значение pKa в пределах от 5,6 до 6,8, и в идеальном варианте от 5,6 до 6,3.
Данные липосомы также использовали для доставки репликона, кодирующего полноразмерный RSV F-белок. Строили график зависимости общих титров IgG к F-белку против pKa через две недели после введения первой дозы (2wp1), который приведен на фиг.16. Наилучшие результаты были получены при pKa, когда катионный липид имеет pKa в пределах 5,7-5,9, но только значение pKa не в достаточной мере гарантирует высокий титр IgG, например, липид должен поддерживать образование липосомы.
Иммуногенность RSV
Проводили дальнейшую работу с самореплицирующимся репликоном (vA317), кодирующим RSV F-белок. Мышей BALB/c, 4-8 животных на группу, вакцинировали билатерально внутримышечно (50 мкл на конечность) на сутки 0 и 21 одним репликоном (1 мкг) или репликоном, формулированным в липосомы с липидами RV01 или RV02 (смотри выше; pKa равен 5,8 или 5,85) или с RV013. Липосомы RV01 содержали 40% DLinDMA, 10% DSPC, 48% холестерина и 2% ПЭГ-DMG, но с различными количествами РНК. Липосомы RV05(01) содержали 40% катионного липида, 48% холестерина, 10% DSPC и 2% ПЭГ-DMG; липосомы RV05(02) содержали 60% катионного липида, 38% холестерина и 2% ПЭГ-DMG. Липосомы RV13 содержали 40% DOTAP, 10% DPE, 48% холестерина, 10% DSPC и 2% ПЭГ-DMG. В целях сравнения «голую» плазмидную ДНК (20 мкг), экспрессирующую тот же антиген RSV-F, доставляли либо с использованием электропорации, либо в липосомах RV01(10) (0,1 мкг ДНК). Четыре мыши использовали в качестве интактной контрольной группы.
Липосомы готовили способом (А) или (В). В способе (А) готовили свежие маточные растворы липидов в этаноле. Взвешивали 37 мг катионного липида, 11,8 мг DSPC, 27,8 мг холестерина и 8,07 мг ПЭГ-DMG, и растворяли в 7,55 мл этанола. Свежеприготовленный маточный раствор липидов осторожно качали при 37°С примерно в течение 15 мин с получением гомогенной смеси. Затем 226,7 мкл маточного раствора добавляли к 1,773 мл этанола с получением рабочего маточного раствора липидов объемом 2 мл. Это количество липидов использовали для приготовления липосом с 75 мкг РНК с получением соотношения азота к фосфору, равного 8:1 (за исключением липосом RV01(08) и RV01(09), для которых данное соотношение изменяли на 4:1 или 16:1). Также готовили 2 мл рабочего раствора РНК (или для RV01(10) ДНК) из маточного раствора с концентрацией ≈1 мкг/мкл в 100 мМ цитратном буфере (рН 6). Три стеклянных сосуда емкостью 20 мл (с магнитной мешалкой) промывали раствором RNase Away (Molecular BioProducts) и промывали избытком воды MilliQ перед использованием для инактивации РНКаз в сосудах. Один из сосудов использовали для рабочего раствора РНК и другие для сбора смесей липида и РНК (как описано ниже). Рабочие растворы липидов и РНК нагревали при 37°С в течение 10 мин перед загрузкой в шприцы 3cc «Луер Лок». В другой шприц 3cc вносили 2 мл цитратного буфера (рН 6). Шприцы, содержащие РНК и липиды, подсоединяли к Т-смесителю (PEEKTM 500 мкм ID junction, Idex health Science), используя трубку из FEP. Выходное отверстие Т-смесителя также представляло трубку из FEP. Третий шприц, содержащий цитратный буфер, соединяли с отдельным участком FEP-трубки. Затем содержимое всех шприцов приводилось в движение со скоростью 7 мл/мин с использованием шприцевого насоса. Выходные отверстия трубок располагались для сбора смесей в стеклянном сосуде емкостью 20 мл (с одновременным перемешиванием). Затем извлекали магнитные мешалки, и смеси этанол/водный раствор давали уравновеситься при комнатной температуре в течение 1 ч. Затем смесь загружали в шприц 5 сс, который был соединен с участком FEP-трубки, и в другой шприц 5 сс, соединенный с таким же по длине участком FEP-трубки, загружали равное количество 100 мМ цитратного буфера (рН 6). Содержимое двух шприцов приводили в движение со скоростью 7 мл/мин с использованием шприцевого насоса и конечную смесь собирали в стеклянном сосуде емкостью 20 мл (с одновременным перемешиванием). Затем липосомы концентрировали до 2 мл и диализовали против 10-15 объемов IX PBS с использованием TFF перед извлечением конечного продукта. Систему для TFF и и фильтрационные мембраны из полых волокон получали от Spectrum Labs и использовали согласно указаниям изготовителя. Использовали полисульфоновые (PES) фильтрационные мембраны из полых волокон (код P-C1-100E-100-01N) с отсечением по молекулярной массе 100 kD и площадью поверхности 20 см2. Для экспериментов in vitro и in vivo композиции разбавляли до требуемой концентрации РНК с использованием IX PBS.
Способ приготовления (В) отличался двояким образом от способа (А). Вначале после сбора в стеклянном сосуде емкостью 20 мл, но до концентрирования TFF, смесь пропускали через мембрану Mustang Q (анионообменная подложка, которая связывает и удаляет анионные молекулы, производства Pall Corporation Ann Arbor, MI, США). Данную мембрану вначале промывали 4 мл 1 М NaOH, 4 мл 1 М NaCl и 10 мл 100 мМ цитратного буфера (рН 6), и липосомы подогревали в течение 10 мин при 37°С до фильтрования. Второе отличие: фильтрационная мембрана из полых волокон представляла собой полисульфон (код PN: Х1АВ-100-20Р).
Средний диаметр частиц Z, индекс полидисперности и эффективность инкапсулирования липосом были следующими:
|
Сыворотки крови собирали для анализа антител на сутки 14; 36 и 49. Образцы селезенки отбирали у мышей на сутки 49 для анализа Т-клеток.
Сывороточные титры F-специфического IgG (GMT) были следующими:
|
Относительное количество Т-клеток, которые являются цитокин-позитивными и специфическими для пептида RSV F51-66, являются следующими, показаны только цифровые данные, которые статистически достоверно выше нуля:
|
Таким образом, липосомальные композиции достоверно повышали иммуногенность по сравнению с «голыми» контрольными РНК, судя по повышенным титрам F-специфического IgG и относительному количеству отдельных популяций Т-клеток. Плазмидная ДНК, формулированная в липосомах, или доставленная «голой» с использованием электропорации, была менее иммуногенной по сравнению с самореплицирующейся РНК, формулированной в липосомы.
РНК-вакцины RV01 и RV05 были более иммуногенными по сравнению с вакциной RV13 (DOTAP). Данные композиции имели сравнимые физические характеристики и были сформулированы с одной и той же самореплицирующейся РНК, но они содержали разные катионные липиды. Липиды в RV01 и RV05 содержат третичный амин в «головке» и имеют значение pKa примерно 5,8, и также включают ненасыщенные алкильные хвосты. Липид в RV13 содержит ненасыщенные алкильные «хвосты», но в его «головке» имеется четвертичный амин, и он является сильно катионным. На основании этих результатов можно предположить, что липиды с третичными аминами со значениями pKa в пределах от 5,0 до 7,6 превосходят по своим свойствам липиды, такие как DOTAP, которые являются высоко катионными, при использовании в липосомальной системе для доставки РНК.
Дополнительные альтернативы DLinDMA
Катионный липид в липосомах RV01 (DLinDMA) замещали RV16, RV17, RV18 или RV19. Общие титры IgG приведены на фиг.17. Наиболее низкие результаты были получены с RV19, т.е. с DOTMA, содержащим четвертичный амин.
Экспрессия в BHK
Липосомы с различными липидами инкубировали с клетками ВНК в течение ночи и оценивали на их способность экспрессировать белок. По сравнению с фоновым уровнем экспрессия белка с липидом RV05 повышалась в 18 раз при добавлении в липосому 10% 1,2-дифитаноил-sn-глицеро-3-фосфоэтаноламина (DPyPE), в 10 раз при добавлении 10% 18:2 (цис) фосфатидилхолина, и в 900 раз при замене на RV01.
Иммуногенность RSV на различных штаммах мышей
Репликон «vA142» кодирует полноразмерный поверхностный слитый (F) гликопротеин дикого типа RSV, но с делецированным слитым белком, и 3'-конец сформирован рибозим-опосредованным отщеплением.
Мышей BALB/c вакцинировали билатерально внутримышечно (50 мкл на конечность) на сутки 0 и 22. Животных разделяли на 8 опытных групп (5 животных в группе) и интактную контрольную группу (2 животных):
мышам группы 1 вводили «голый» репликон (1 мкг);
мышам группы 2 вводили 1 мкг репликона при введении в липосомах «RV01(37)» с 40% DLinDMA, 10% DSPC, 48% Chol, 2% конъюгированного с ПЭГом DMG;
мышам группы 3 вводили то же самое, что и мышам группы 2, но вводили в дозе 0,1 мкг РНК;
мышам группы 4 вводили 1 мкг репликона в липосомах «RV17(10)» (40% RV17 (смотри выше), 10% DSPC, 49,5% холестерина, 0,5% ПЭГ-DMG);
мышам группы 5 вводили 1 мкг репликона в липосомах «RV05(11)» (40% липид RV17, 30% PE 18:2 (DLoPE, 28% холестерина, 2% ПЭГ-DMG);
мышам группы 6 вводили 0,1 мкг репликона в липосомах «RV17(10)»;
мышам группы 7 вводили 5 мкг субъединицы белка RSV-F с адъювантом гидроксидом алюминия;
мыши группы 8 были интактными контрольными (2 животных).
Собирали сыворотки крови для анализа антител на сутки 14; 35 и 49. GMT F-специфического IgG были следующими:
|
На сутки 35 титры (GMT) F-специфических IgG1 и IgG2 были следующими:
|
Титры сывороточных нейтрализующих RSV антител на сутки 35 и 49 были следующими (данные представляют титры нейтрализации по 60% снижению бляшек для объединенных сывороток от 2-5 мышей, 1 пул на группу):
|
Образцы селезенки отбирали на сутки 49 для анализа Т-клеток. Средние значения относительной доли чистых F-специфических цитокин-позитивных Т-клеток (CD4+ или CD8+) были следующими, показаны только цифровые данные, которые статистически достоверно выше нуля (специфические для пептидов RSV F51-66, F164-178, F309-323 для CD4+ или для пептидов F85-93 и F249-258 для CD8+):
|
Мышей C57BL/6 иммунизировали аналогично, но мыши 9-й группы получали VRP (1×106 МЕ), экспрессирующие полноразмерный слитый поверхностный гликопротеин дикого типа RSV (слитый пептид делеции).
Собирали сыворотки крови для анализа антител на сутки 14; 35 и 49. Титры (GMT) F-специфического IgG были следующими:
|
На сутки 35 титры (GMT) F-специфических IgG1 и IgG2 были следующими:
|
Титры сывороточных нейтрализующих RSV антител на сутки 35 и 49 были следующими (данные представляют титры нейтрализации по 60% снижению бляшек для объединенных сывороток от 2-5 мышей, 1 пул на группу):
|
Образцы селезенки отбирали на сутки 49 для анализа Т-клеток. Средние значения относительной доли чистых F-специфических цитокин-позитивных Т-клеток (CD8+) были следующими, показаны только цифровые данные, которые статистически достоверно выше нуля (специфические для пептидов RSV F85-93 и F249-258):
|
|
Девять групп мышей C3H/HeN иммунизировали аналогично. Титры (GMT) F-специфического IgG были следующими:
|
На сутки 35 титры (GMT) F-специфических IgG1 и IgG2 были следующими:
|
Титры сывороточных нейтрализующих антител RSV на сутки 35 и 49 были следующими:
|
Таким образом, три разных липида (RV01, RV05, RV17; pKa 5,8, 5,85, 6,1) тестировали на трех различных штаммах инбредных мышей. На всех 3 штаммах RV01 был более эффективным по сравнению с RV17; для мышей штаммов BALB/c и С3Н RV05 был менее эффективным по сравнению с RV01 или RV17, но был более эффективным на штамме В6. Однако во всех случаях липосомы были более эффективными, чем две катионные наноэмульсии, которые тестировались параллельно.
Иммуногенность CMV
Липосомы RV01 с DLinDMA в качестве катионного липида использовали для доставки РНК-репликонов, кодирующих гликопротеины цитомегаловируса (CMV). Репликон «vA160» кодирует полноразмерные гликопротеины Н и L (gH/gL), в то время как «vA322» кодирует растворимую форму (gHsol/gL). Два белка находятся под контролем отдельных субгеномных промоторов в одном репликоне; совместное введение двух отдельных векторов, из которых один кодирует gH, и другой кодирует gL, не давало хороших результатов.
Мышей BALB/c, 10 животных на группу, вакцинировали билатерально внутримышечно (50 мкл на конечность) на сутки 0; 21 и 42 VRP, экспрессирующими gH/gL (1×106 МЕ), VRP, экспрессирующими gHsol/gL (1×106 МЕ), и PBS в качестве контроля. Две опытные группы получали 1 мкг репликона vA160 или vA322, формулированного в липосомах (40% DLinDMA, 10% DSPC, 48% Chol, 2% ПЭГ-DMG; липосомы были приготовлены способом (А), как обсуждалось выше, но партией размером 150 мкг РНК).
Липосомы vA160 имели диаметр Zav 168 нм, pdI 0,144, и эффективность инкапсулирования равнялась 87,4%. Липосомы vA322 имели диаметр Zav 162 нм, pdI 0,131 и с 90% инкапсулированием.
Репликоны были способны экспрессировать два белка из одного вектора.
Собирали сыворотки для иммунологического анализа на сутки 63 (3wp3). Титры нейтрализации CMV (обратная величина разбавлению сыворотки, которая дает 50% снижение числа позитивных на вирус очагов на лунку по сравнению с контролем) были следующими:
|
Таким образом, РНК, экспрессирующая полноразмерную или растворимую форму комплекса CMV gH/gL, индуцировала высокие титры нейтрализующих антител при тестировании на эпителиальных клетках. Средние титры, индуцированные инкапсулированными в липосомы РНК, были, по меньшей мере, такими же высокими, как для соответствующих VRP.
Очевидно, понятно, что изобретение описано только с помощью примера, и могут быть сделаны модификации, не отступая от объема и сущности изобретения.
СПИСОК ИСТОЧНИКОВ ЛИТЕРАТУРЫ
[I] Johanning etal. (1995) Nucleic Acids Res 23:1495-1501. [2] WO2005/121348.
[3] WO2008/137758.
[4] WO2009/086558.
[5] WO2011/076807.
[6] Heyes etal. (2005) JControlled Release 107:276-87.
[7] WO2005/121348.
[8] Liposomes: Methods and Protocols, Volume 1: Pharmaceutical Nanocarriers: Methods an Protocols, (ed. Weissig). Humana Press, 2009. ISBN 160327359X.
[9] Liposome Technology, volumes I, II & III. (ed. Gregoriadis). Informa Healthcare, 2006.
[10] Functional Polymer Colloids and Microparticles volume 4 (Microspheres, microcapsules & liposomes). (eds. Arshady & Guyot). Citus Books, 2002.
[11] Jeffs et al. (2005) Pharmaceutical Research 22 (3):362-372.
[12] WO2005/113782.
[13] WO2011/005799.
[14] El Ouahabi et al. (1996)FEBSLetts 380:108-12.
[15] Giuliani et al. (2006)Proc Natl Acad Sci USA 103(29): 10834-9.
[16] WO2009/016515.
[17] WO02/34771.
[18] WO2005/032582.
[19] WO2010/119343.
[20] WO2006/110413.
[21] WO2005/111066.
[22] WO2005/002619.
[23] WO2006/138004.
[24] WO2009/109860.
[25] WO02/02606.
[26] WO03/018054.
[27] WO2006/091517.
[28] WO2008/020330.
[29] WO2006/089264.
[30] WO2009/104092.
[31] WO2009/031043.
[32] WO2007/049155.
[33] Gennaro (2000) Remington: The Science and Practice of Pharmacy. 20th edition, ISBN: 0683306472.
[34] Methods In Enzymology (S. Colowick and N. Kaplan, eds., Academic Press, Inc.)
[35] Handbook of Experimental Immunology, Vols. I-IV (D.M. Weir and C.C. Blackwell, eds, 1986, Blackwell Scientific Publications)
[36] Sambrook et al. (2001) Molecular Cloning: A Laboratory Manual, 3rd edition (Cold Spring Harbor Laboratory Press).
[37] Handbook of Surface and Colloidal Chemistry (Birdi, K.S. ed., CRC Press, 1997)
[38] Ausubel et al. (eds) (2002) Short protocols in molecular biology, 5th edition (Current Protocols).
[39] Molecular Biology Techniques: An Intensive Laboratory Course, (Ream et al, eds., 1998, Academic Press)
[40] PCR (Introduction to Biotechniques Series), 2nd ed. (Newton & Graham eds., 1997, Springer Verlag)
[41] Yoneyama & Fujita (2007) Cytokine & Growth Factor Reviews 18:545-51.
[42] Maurer et al. (2001) Biophysical Journal, 80: 2310-2326.
[43] Perri et al. (2003) J Virol 77:10394-10403.
[44] Iavarone et al. (2011) J Immunol 186;4213-22.
[45] WO2011/057020.