Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ КОНЦЕНТРАТА ТРОМБИНА
Вид РИД
Изобретение
Изобретение относится к области фармацевтической промышленности, а именно к биотехнологии получения гемостатических препаратов.
Тромбин - естественный компонент свертывающей системы крови, образующийся в организме из неактивной формы фермента, протромбина, при ферментативной активации последнего тромбопластином.
Промышленное получение препаратов тромбина из плазмы крови связано с его клиническим применением в качестве основного гемостатика. В терапии тромбин используется как самостоятельное средство или чаще вместе с фибриногеном в виде фибринового клея.
Фибриновый клей является высокоэффективным местным гемостатическим средством, используемым в современной хирургии. Основные компоненты клея - фибриноген, фактор свертывания XIII и тромбин выделяются из донорской плазмы. При нанесении на раневую поверхность фибриновый клей полимеризуется с образованием эластичной фибриновой пленки белого цвета. Этот процесс повторяет основные стадии физиологического процесса свертывания крови и позволяет останавливать диффузные кровотечения, склеивать и фиксировать ткани, а также ускорять заживление ран.
Препараты очищенного тромбина производят как из плазмы донорской крови человека, так и методами генной инженерии.
В качестве начальной стадии производства препаратов - производных донорской плазмы, в том числе и тромбинсодержащих, обычно используется метод криофракционирования свежезамороженной плазмы донорской крови, за которым обычно следует несколько ступеней хроматографического фракцинирования. Сырьем для получения концентрата тромбина обычно служит так называемый концентрат протромбинового комплекса (РСС), получаемый из криосупернатанта (КСН) плазмы донорской крови. В состав РСС входят витамин К-зависимые факторы свертывания: FII (протромбин), FVII, FIX, FX, протеины С и S и т.д.
PPSB выделяют из КСН методами хроматографического фракционирования или осаждения. Метод хроматографического фракционирования, разработанный в 1960-х годах и наиболее распространенный в настоящее время, заключается во взаимодействии КСН со слабым анионообменном сорбентом.
Поскольку тромбин находится в плазме в неактивной форме, в виде протромбина, следующей стадией получения после первичной очистки является активация FII-содержащих фракций плазмы.
Существует несколько способов активации. Первый метод - активация протромбина в составе РСС тромбопластином, обычно в присутствии хлорида кальция. Этот липопротеин активирует фактор VII, который в свою очередь активизирует фактор X, превращающий протромбин в тромбин. Недостатком этого метода является то, что тромбопластин обычно получают методом грубой очистки из гомогенизированных мозга, легких и тканей кишечника. Данный метод не может быть использован для производства тромбина человека, поскольку качество получаемого продукта очень зависит от сырья, обладающего большим риском перекрестной вирусной контаминации.
Вторым методом активации является использование компонентов яда кобры. Однако, как было обнаружено, расщепление некоторыми видами ядов происходит по положениям внутри протромбина, отличным от естественного активатора - фактора Ха. Поэтому применение этого метода является также опасным и неприменимым для производства препаратов для клинического использования.
Третий метод предполагает проведение активации в условиях близких к физиологическим: протромбин активируется в присутствии факторов IX, X, VII, фосфолипидов и ионов кальция. Получаемый таким образом тромбин часто является нестабильным и требует внесения белков-стабилизаторов, полиолов и/или сахаров.
После активации тромбинсодержащий раствор подвергается финальной очистке. Помимо распространенных методов фракционирования на ионообменных и гель-фильтрационных сорбентах, тромбин также может быть очищен при помощи гепарин-, бензамидин-аффинных сорбентов, а также с помощью хроматографии гидрофобных взаимодействий, с использованием сорбента с пришитыми фенильными группам. Кроме того, существуют работы, описывающие использование для очистки тромбина металл-хелатную хроматографии с иммобилизованными ионами металлов.
Поскольку тромбин человека получают из донорской плазмы, существует риск контаминации тромбина различными вирусами. Поэтому все препараты тромбина, предназначенные для клинического использования, должны быть подвергнуты вирусной инактивации. Для тромбина это обычно сольвент-детергентная обработка и/или пастеризация и стерилизующая фильтрация.
В таблице 1 приведены примеры методов получения тромбина, не использующих для активации компоненты биологического происхождения.
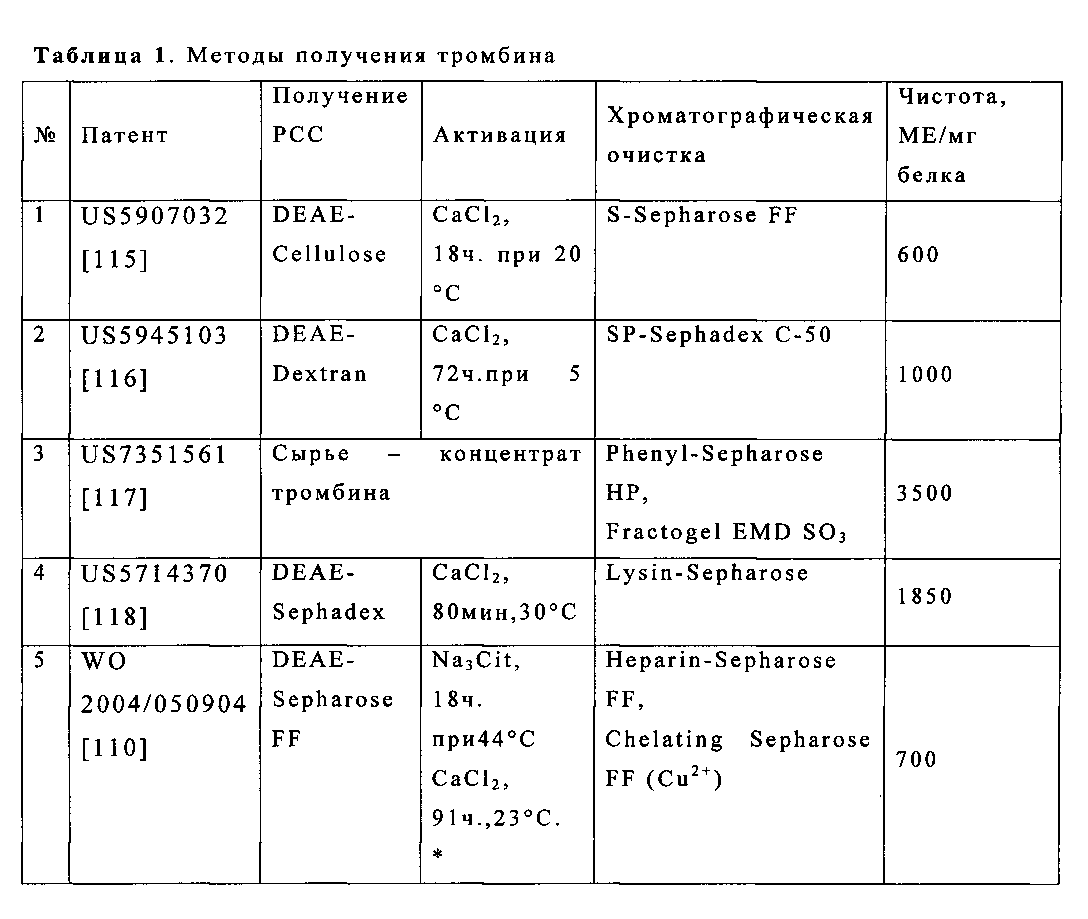
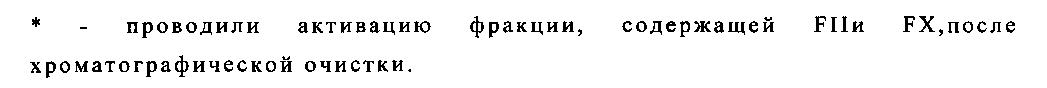
Был предложен также метод получения тромбина с активацией на сорбенте. В этом методе РСС, очищенный на DEAE-SepharoseCL6B, наносили на сорбент DEAE-Sepharose или Fractogel EMDSO3 в термостатируемой хроматографической колонке и заполняли буферным раствором, содержащим СаСl2. Активация происходила в закрытой колонке при 20°С в течение 64 часов. После чего активированный тромбин элюировали стартовым буфером, а протромбин, не подвергшийся активации, оставался при этом адсорбированным на сорбенте. Чистота полученного тромбина на обоих сорбентах составила >2000 МЕ/мг.
Целью настоящего изобретения является разработка способа промышленного производства стабильного препарата высокоочищенного тромбина.
Разработку технологии получения высокоочищенного тромбина проводили в лабораторных условиях с последующей оптимизацией выбранной методики, а затем масштабировали в условиях опытного производства.
Сырьем для получения тромбина является свежезамороженная плазма донорской крови.
Процесс получения тромбина из плазмы донорской крови включает следующие стадии:
1. криофракционирование СЗП;
2. выделение протромбинового комплекса на анионообменном сорбенте;
3. активация протромбина в составе протромбинового комплекса с получением тромбина;
4. вирусная инактивация сольвент-детергентным методом;
5. очистка полученного тромбина на катионообменном сорбенте.
На стадии криофракционирования СЗП методом контролируемого оттаивания и центрифугирования разделяют на 2 фракции: криопреципитат (КП) и криосупернатант (КСН). Отделяемый КП используют как сырье для получения концентратов FVIII и фибриногена.
Из полученного КСН после корректировки рН и ионной силы выделяют концентрат протромбинового комплекса (PPSB).
В качестве анионообменного сорбента на стадии выделения PPSB возможно использование слабых анионообменников, содержащих DEAE-группы, предпочтительно сорбентов на основе модифицированной агарозы, предпочтительно сорбента DEAE-Sepharose Fast Flow.
Выделение PPSB проводят с использованием Трис-цитратных буферных растворов с рН 7.8 в ступенчатом градиенте ионной силы, создаваемом повышением концентрации NaCl в стартовом буферном растворе. Линейная скорость процесса составляет 80-90 см/ч.
Выход протромбина во фракции PPSB составляет не менее 90%.
Активацию PPSB проводят в условиях, близких к физиологическим. Активатором протромбина выступает раствор СаСl2. Концентрацию ионов кальция Са2+ рассчитывают с учетом количества цитрата в буферном растворе так, чтобы концентрация свободных ионов кальция Са2+ составила 2-20 ммоль/л. рН раствора поддерживают на уровне 7,0. Процесс активации длится около 24 часов при температуре 23°С. Выход по тромбину составляет не менее 90%.
Полученный раствор тромбина до начала стадии хроматографической очистки подвергают вирусной инактивации SD-обработкой с использованием 0,3% раствора три-n-буфтилфосфата (ТnВР) и 1% раствора Triton Х-100 в течение 6 часов при комнатной температуре при значениия рН от 6,5 до 7,8.
Очистку вирус-инактивированного раствора тромбина проводят катионообменной хроматографией, предпочтительно с использованием ионообменника Fractogel EMD-SO3. Хроматографическую очистку проводят с использованием Трис-НСl-буферных растворов с рН от 6,5 до 7,8 в ступенчатом градиенте ионной силы, создаваемом повышением концентрации NaCl в стартовом буферном растворе. Линейная скорость процесса составляет 80-90 см/ч.
Целевая фракция очищенного тромбина имеет удельную активность не менее 2000 МЕ/мг общего белка.
Выход тромбина на ступени хроматографической очистки составляет не менее 90%.
В полученный раствор тромбина добавляют человеческий альбумин в качестве стабилизатора, стерильно фильтруют, разливают по флаконам и лиофилизируют.
Общий выход тромбина из 1 л СЗП составляет не менее 90%.
Ниже представлен конкретный пример осуществления изобретения.
Пример 1.
1. 30 л свежезамороженной плазмы доноров с активностью протромбина, равной 0,7-1МЕ/мл*, размораживали в реакторе при температуре -0,5°С и выделяли криосупернатант (КСН) центрифугированием на проточной центрифуге при скорости 18000 об/мин и 3°С. При этом потери протромбина составили менее 10%.
2. Хроматографическое фракционирование 30 л КСН проводили на колонне диаметром 200 мм, заполненной сорбентом DEAE Sepharose Fast Flow, с использованием трис-цитратных буферных растворов рН 7,2 повышением концентрации хлорида натрия в стартовом буферном растворе от 0,08М до 0,22М. Потери протромбина на стадии нанесения КСН и промывки стартовым буферным раствором не превысили 1% от исходного содержания. Фракцию, содержащую протромбин, элюировали в объеме около 1 л буферным раствором, содержащим 0,22М хлорида натрия. Выход протромбина составил не менее 90%.
3. Активацию тромбина проводили при комнатной температуре при перемешивании, используя в качестве активирующего агента СаСl2. Сырьем для активации служит полученная на предыдущей стадии фракция, содержащая протромбин с активностью около 20 МЕ/мл*, в которую добавляли хлорид кальция в виде 0,5 М раствора до концентрации свободных ионов Са2+, равной 8 ммоль/л. Время активации составляло 24 часа. После активации полученную смесь центрифугировали 10-15 мин при 4000 об/мин. В этих условиях порядка 90-95% протромбина трансформируется в тромбин.
4. Вирусную инактивацию раствора тромбина проводили сольвент-детергентным методом, добавляя Тритон Х-100 до конечной концентрации 1% и три-n-бутилфосфат до конечной концентрации 0,3% при рН 6,8.
5. Хроматографическую очистку тромбин-содержащей фракции проводили на колонке, заполненной ионообменным сорбентом Fractogel EMD-SO3 с использованием Трис-НСl буферных растворов, рН 6,5, повышением концентрации ионов натрия в стартовом буферном растворе. Концентрация хлорида натрия в стартовом растворе составляла 100 ммоль/л. После нанесения образца проводили промывку 10 объемами стартового буферного раствора для удаления несвязанных белков и реагентов, используемых для вирусной инактивации. Далее проводили промывку сорбента буферными растворами с промежуточной ионной силой. На этой ступени потери тромбина не превышали 1% от исходного количества. Элюцию тромбина осуществляли повышением концентрации ионов натрия до 1000 мМоль/л. Выход тромбина* на стадии хроматографической очистки составлял не менее 90%. Удельная активность очищенного тромбина превышала 2000МЕ/мг белка**.
6. В полученный раствор тромбина добавляют человеческий альбумин в качестве стабилизатора, стерильно фильтруют, разливают по флаконам и лиофилизируют.
* Определение протромбинового времени проводили с использованием тромбопластин-кальциевого реагента и субстрат-дефицитной плазмы по протромбину
** Концентрацию тромбина определяли коагулометрически по времени свертывания при добавлении к образцу стандартного раствора фибриногена.
*** Концентрацию общего белка определяли по методу Бредфорда.
Способ выделения очищенного концентрата тромбина, избавленного от вирусов, характеризующегося большим выходом, чистотой и высокой стабильностью, заключающийся в криофракционировании исходного сырья, представленного свежезамороженной плазмой донорской крови человека, выделении протромбинового комплекса на анионообменном сорбенте DEAE Sepharose Fast Flow, активации протромбина раствором CaCl в составе протромбинового комплекса с получением тромбина, вирусной инактивации сольвент-детергентным методом и очистке полученного тромбина на катионообменном сорбенте Fractogel EMD-SO, отличающийся тем, что количество раствора CaCl, выступающего в качестве активатора протромбина, рассчитывается с учетом взаимодействия CaCl с цитратом натрия, который входит в состав буфера, используемого при выделении протромбинового комплекса на анионобменном сорбенте, так, чтобы концентрация свободных ионов Са в растворе на стадии активации составляла от 2 до 20 ммоль/л.
