Результат интеллектуальной деятельности: СПОСОБ МОДЕЛИРОВАНИЯ ЦЕРЕБРАЛЬНОГО СОСУДИСТОГО СПАЗМА ПРИ НЕТРАВМАТИЧЕСКОМ СУБАРАХНОИДАЛЬНОМ КРОВОИЗЛИЯНИИ IN VIVO
Вид РИД
Изобретение
Область техники, к которой относится изобретение
Изобретение относится к области медицины, а именно нейрохирургии, патологической анатомии, и может быть использовано для изучения сосудистого спазма при нетравматических субарахноидальных кровоизлияниях в эксперименте и проведения исследований терапевтической эффективности препаратов для профилактики и лечения сосудистого спазма.
Уровень техники
Из уровня техники известен способ моделирования нетравматического субарахноидального кровоизлияния у крыс (Solomon R.A., Antunes J.L., Chen R.Y., Bland L., Chien S.: Decrease in cerebral blood flow in rat after experimental subarachnoid hemorrhage: a new animal model. Stroke 16:58-64, 1985). При данной методике авторы производили однократное пункционное введение свежей артериальной аутокрови в затылочную цистерну крысы и проводили последующую оценку церебральной перфузии в сроки до 2 часов.
Однако в известном способе производится однократное введение крови в затылочную цистерну, что позволяет наблюдать изменение церебрального кровотока в острую фазу спазма. В то же время при однократном способе введения изменения в отсроченном периоде эксперимента практически отсутствуют. Указанная модель не позволяет изучать терапевтическую эффективность препаратов, специфичных к белкам крови человека.
Из уровня техники известен также способ моделирования нетравматического субарахноидального кровоизлияния у крыс (Bederson J.B., Germano I.M., Guarino L.: Cortical blood flow and cerebral perfusion pressure in a new noncraniotomy model of subarachnoid hemorrhage in the rat. Stroke 26:1086-1092, 1995). При данной методике авторы осуществляли эндоваскулярную перфорацию внутренней сонной артерии у крысы и оценивали изменения церебрального кровотока в первые 24 часа от эксперимента.
Однако известный способ также не позволяет наблюдать отсроченные изменения сосудистого спазма и изучать терапевтическую эффективность препаратов, специфичных к белкам крови человека.
Одним из наиболее близких способов моделирования нетравматического субарахноидального кровоизлияния у крыс является метод двухкратного введения крови (Meguro Т., Clower B.R., Carpenter R., Parent A.D., Zhang J.H. Improved rat model for cerebral vasospasm studies. Neurol Res Oct 2001; 23(7):761-6). При данной методике авторы выполняли двухкратное введение свежей артериальной аутокрови в затылочную цистерну крысы с интервалом 48 часов между введениями и оценивали морфологические изменения интракраниальных сосудов в сроки до 7 суток.
Однако при всех перечисленных методиках невозможно апробировать профилактическое и лечебное воздействие препаратов, имеющих сродство к белкам крови человека, например, фибринолитическим препаратам группы рекомбинантной стафилокиназы, которые эффективны только у некоторых видов животных и человека, но неэффективны у крыс (Species Reactivity to Staphylokinase. Exp Biol Med (Maywood) June 1949 71:261-263, Lijnen H.R., De Cock F., Matsuo O. & Collen D. Comparative fibrinolytic and fibrinogenolytic properties of staphylokinase and streptokinase in plasma of different species in vitro. Fibrinolysis 6, 33-37 (1992)).
Раскрытие изобретения
Задачей изобретения является создание удобной, доступной биологической модели для изучения способов профилактики и лечения церебрального сосудистого спазма при нетравматических субарахноидальных кровоизлияниях с использованием препаратов, специфичных к белкам крови человека (например, препараты группы рекомбинантной стафилокиназы).
Техническим результатом, на достижение которого направлено заявленное изобретение, является воспроизведение морфологических изменений интракраниальных сосудов при сосудистом спазме у лабораторных белых крыс, наиболее близких к таковым у человека, обеспечивающих адекватное изучение терапевтической эффективности препаратов, специфичных к белкам крови человека.
Поставленная задача решается тем, что способ моделирования церебрального сосудистого спазма при нетравматическом субарахноидальном кровоизлиянии в эксперименте включает введение в затылочную цистерну крысы крови, при этом вводят свежую человеческую венозную кровь, причем перед введением выполняют пункцию или дренирование затылочной цистерны с выведением спинномозговой жидкости.
Пункцию и введение крови выполняют под контролем частоты и глубины дыхания животного. Выведение спинномозговой жидкости из субарахноидального пространства крысы осуществляют в объеме от 0,05 до 0,2 мл в течение 3-7 мин. Введение человеческой крови в затылочную цистерну осуществляют в объеме от 0,05 до 0,25 мл в течение 5-10 мин.
В одном из вариантов выполнения изобретения возможно повторное введение крови в затылочную цистерну через время, обеспечивающее постоянное присутствие крови с момента первого введения, необходимое для развития церебрального сосудистого спазма. Указанное время составляет 24-48 ч.
После введения крови выполняют послойное ушивание раны, включающее ушивание затылочной мембраны.
В одном из вариантов исполнения при введении крови в затылочную цистерну выполняют одновременную сенсибилизацию животного путем внутривенного введения человеческой крови в объеме, не приводящем к нарушению витальных функций у крысы. Указанный объем составляет 0,5-2 мл.
Перед введением крови выполняют гепаринизацию средств введения.
Для исключения агглютинации человеческих эритроцитов агглютининами крыс перед экспериментом у 10 произвольных животных была проведена оценка групповой принадлежности по системе АВО и резус-фактор с использованием цоликлонов и проведением пробы на индивидуальную совместимость со всеми группами человеческой крови. Помимо этого, перед каждым введением человеческой крови проводили пробу на индивидуальную совместимость. Агглютинации между сывороткой крысы и эритроцитами человека не наблюдали ни в одном случае, что позволяет предположить, что человеческие эритроциты не агглютинируют под воздействием плазмы крови крыс.
При сравнительной эффективности интрацистернального введения препаратов рекомбинантной стафилокиназы с последующим наружным дренированием цереброспинальной жидкости на модели с использованием свежей аутокрови у крыс нами были получены данные, говорящие об отсутствии фибринолитической активности как местно (в затылочной цистерне), так и системно (влияние на параметры гемостаза).
По предварительным данным интрацистернальное применение препаратов рекомбинантной стафилокиназы на модели введения человеческой крови в затылочную цистерну на 3-4-е сутки эксперимента с последующим наружным дренирование цереброспинальной жидкости в объеме, не приводящем к нарушению витальных функций крысы (0,3-1,5 мл спинномозговой жидкости в сутки), снижает выраженность морфологических изменений при сосудистом спазме как в стенке интракраниальных сосудов, так и в ткани мозга.
Краткое описание чертежей
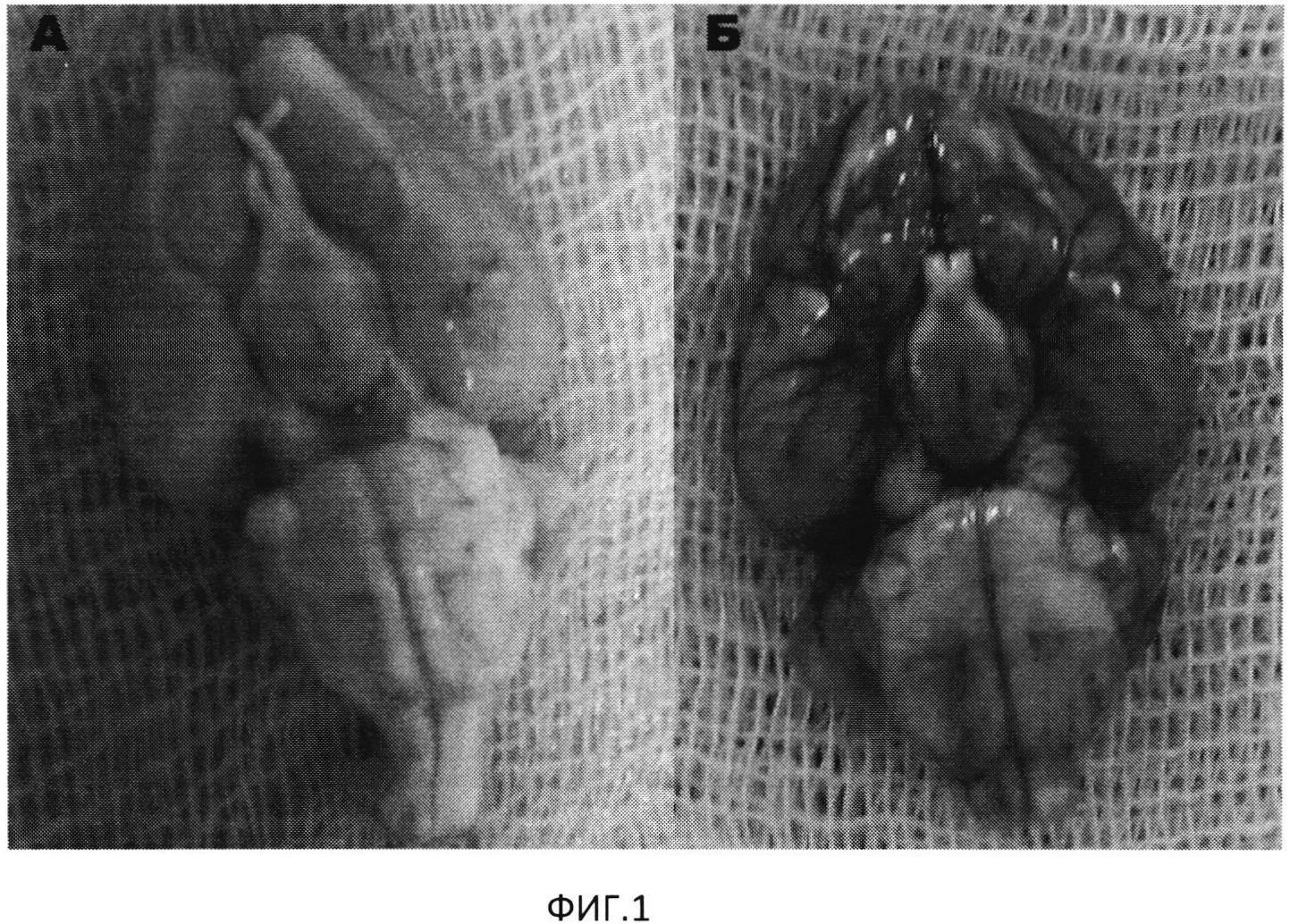
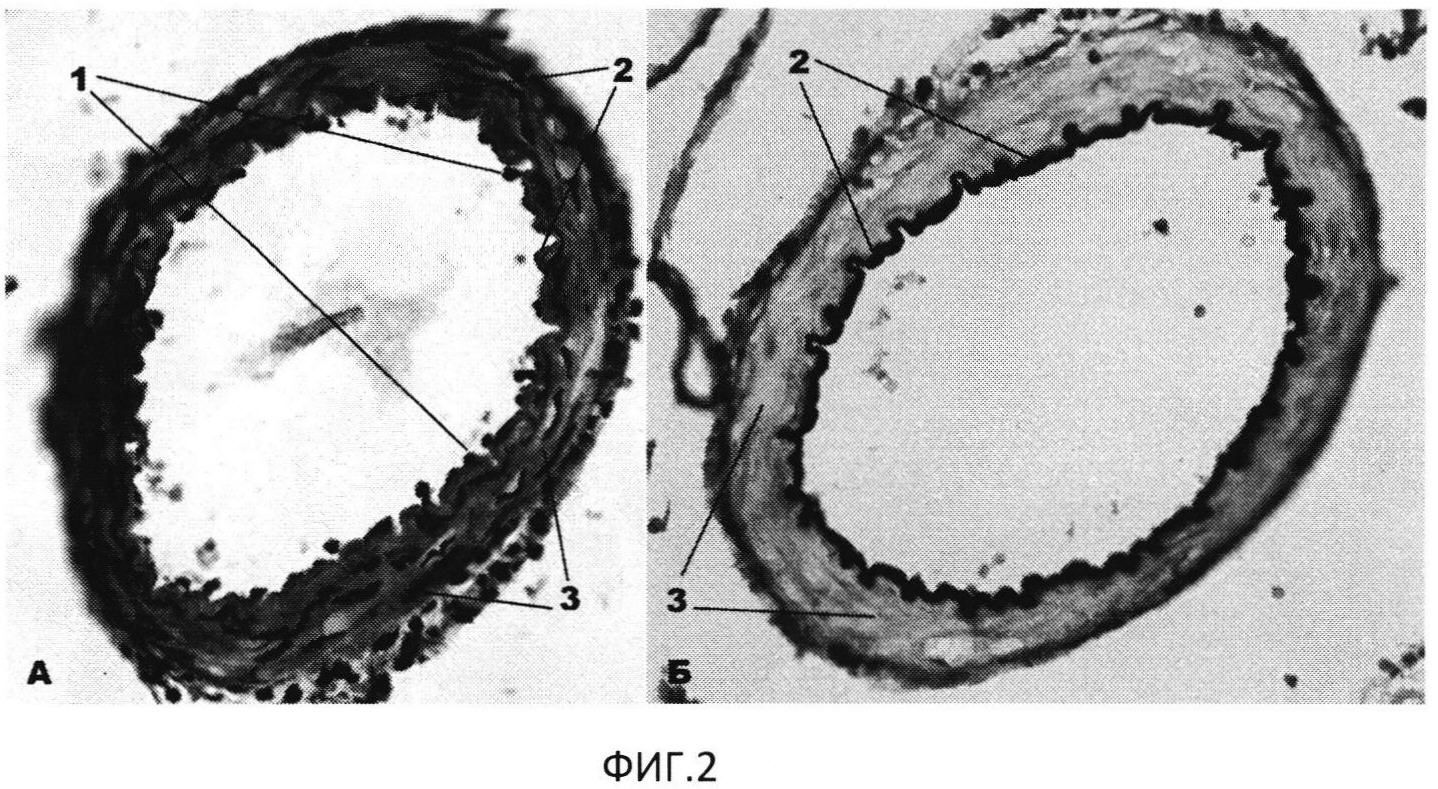
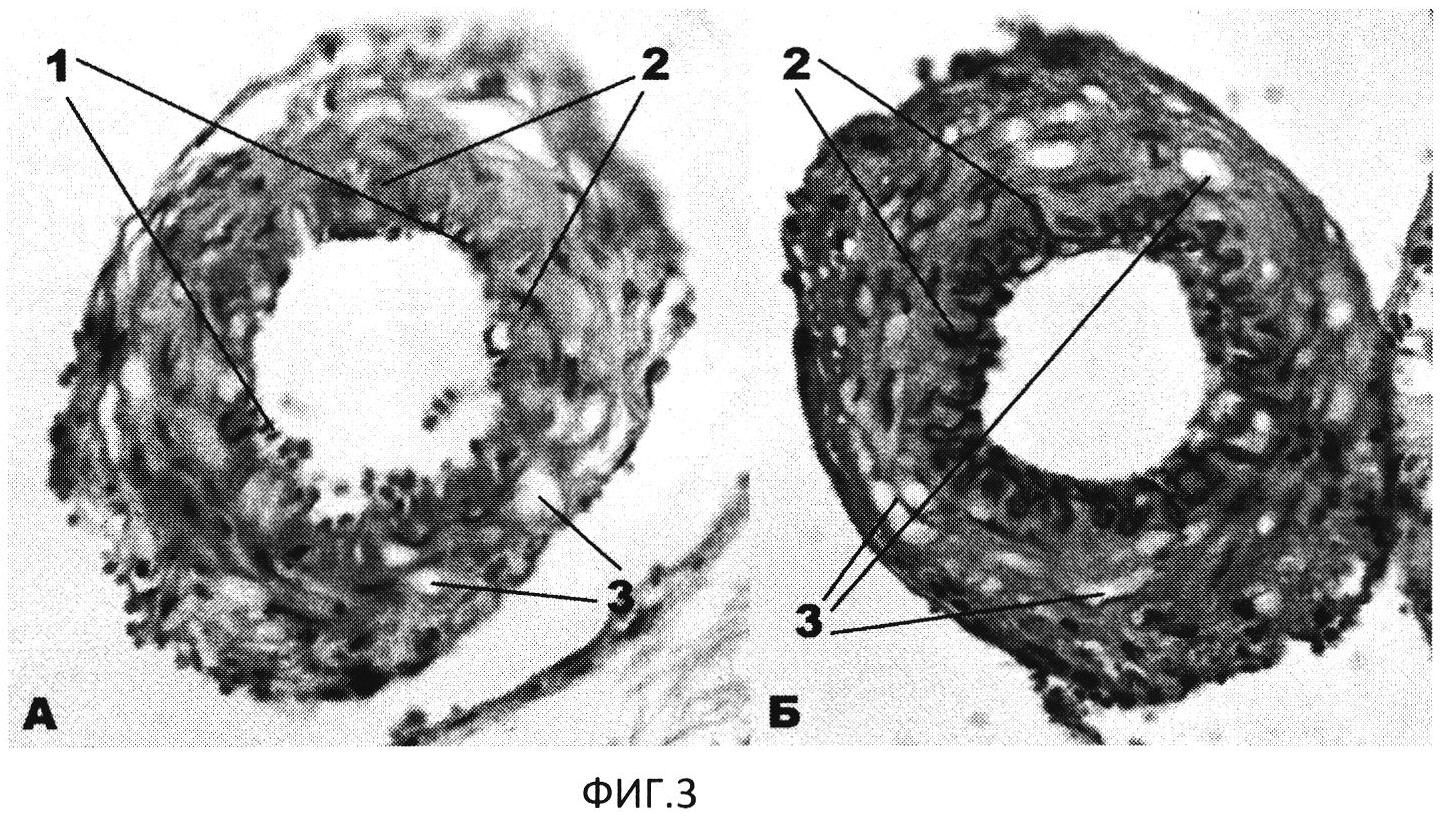
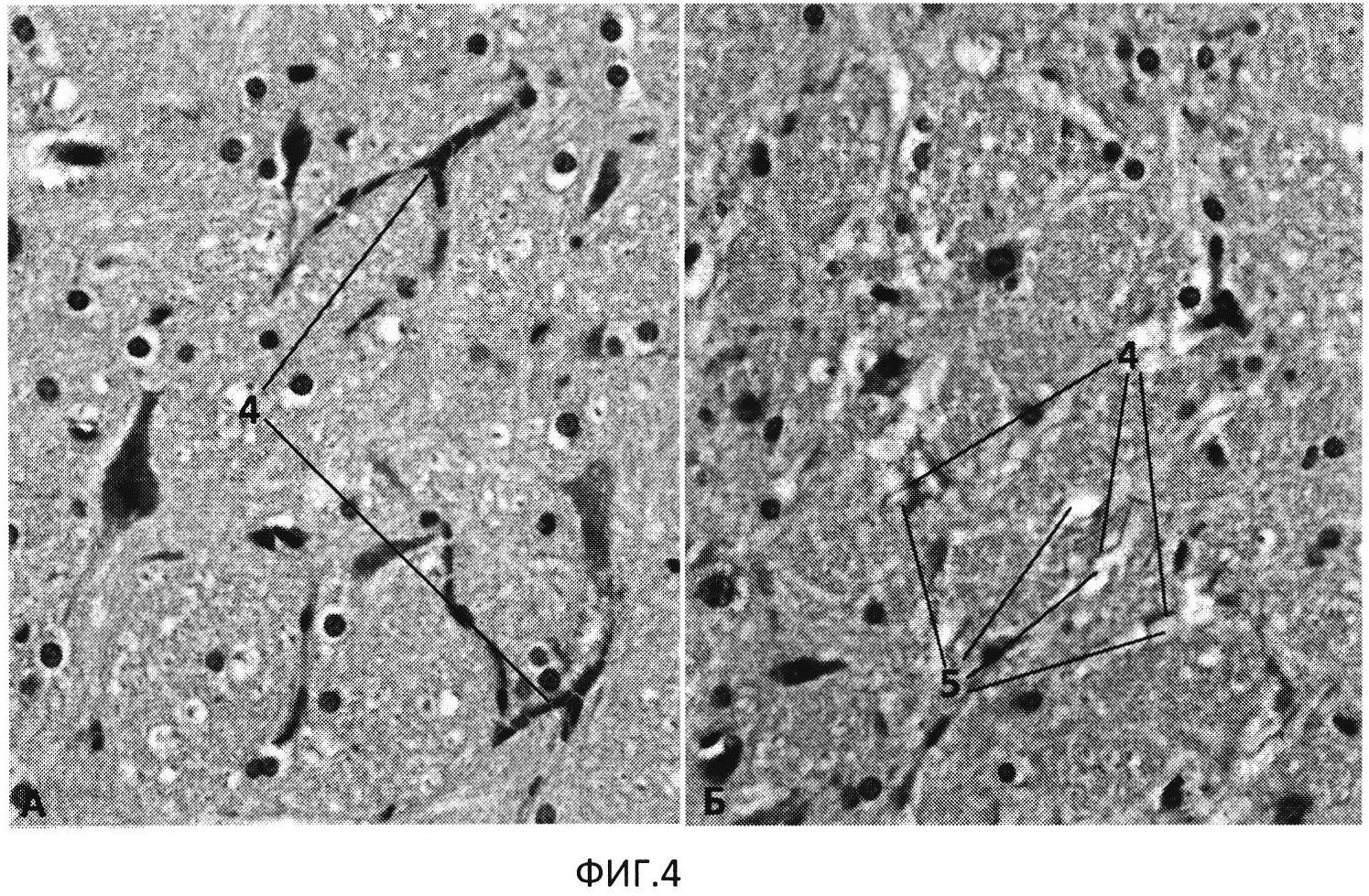
Изобретение поясняется фотографиями изображения объекта исследования в эксперименте, где на фиг. 1 показана верификация САК: А - мозг интактного животного; Б - мозг изъят через 30 мин после введения 0,25 мл аутокрови в затылочную цистерну; на фиг. 2 - верхняя треть основной артерии (увеличение ×400), контроль, А - окраска гематоксилином и эозином, Б - окраска по Грамм-Вейгерту, на изображениях позициями обозначены: 1 - ядра эндотелиоцитов, 2 - ВЭМ, 3 - ГМК. Соответствует нормальному строению верхней трети основной артерии крысы; на фиг. 3 показана верхняя треть основной артерии на 5-е сутки после двухкратного введения крови (увеличение ×400), А - окраска гематоксилином и эозином, Б - окраска по Lie, на изображениях позициями обозначены: 1 - ядра эндотелиоцитов, 2 - ВЭМ, 3 - ГМК (имеются признаки вакуолизации цитоплазмы). Отмечается резкое сужение просвета сосуда, значительное утолщение стенки артерии, сближение ядер эндотелиоцитов. ВЭМ имеет выраженно извитые контуры, в цитоплазме ГМК - распространенная гидропическая дистрофия; на фиг. 4 представлено изображение верхних отделов моста крысы (окраска по Lie, увеличение ×1000), А - 3-и сутки после введения крови, Б - 7-е сутки после введения крови, на изображениях позициями обозначены: 4 - капилляры с сохраненным током крови (на фиг. А - полнокровные, на фиг. Б - со спавшимся просветом), 5 - зоны выраженного периваскулярного отека.
Осуществление изобретения
Ниже представлено подробное описание осуществления изобретения и результаты морфологических исследований полученной модели церебрального сосудистого спазма при двукратном введении в затылочную цистерну крысы свежей человеческой венозной крови. При этом данное подробное описание не ограничивает заявляемое изобретение, т.к. в эксперименте был получен заявленный результат и при однократном введении крови.
1. Анестезия
Обезболивание животных осуществляли по следующей методике.
Крысу помещали в замкнутую емкость, на дне которой уложена гигроскопичная вата, пропитанная диэтиловым эфиром. Через 1-2 мин крыса засыпала. После этого выполняли премедикацию для потенцирования основного наркоза: внутримышечно в область бедра инсулиновым шприцем вводили следующие препараты: дроперидол - 0,3 мг/кг массы тела (0,03 мл 0,25% раствора), димедрол 1,2 мг/кг массы тела (0,03 мл 1% раствора), атропин - 0,012 мг/кг массы тела (0,03 мл 0,1% раствора). Через 15 мин после премедикации в область бедра другой лапки крысы вводили следующие препараты: «золетил 100» - 24 мг/кг массы тела (0,06 мл раствора), ксилазин - 3,2 мг/кг массы тела (0,04 мл 2% раствора). Как правило, крыса засыпала в течение 5-15 мин. Оценку глубины анестезии проводили по выраженности корнеального рефлекса. При необходимости через 20 мин добавляли 0,02-0,04 мл «золетил 100».
2. Техника операции
Введение крови в затылочную цистерну (выполняли на 1-е и 2-е сутки эксперимента с интервалом между введениями 24 часа). Животное фиксировали на операционном столике и брили область операции. После обработки кожи растворами антисептиков выполняли срединный разрез от области затылочного возвышения до остистого отростка VI-VII шейного позвонков. Мышцы шеи для снижения кровоточивости и потенцирования наркоза инфильтрировали комбинированным местным анестетиком «Ультракаин ДС 1:200000» (артикаина гидрохлорид 40 мг/мл + эпинефрина гидрохлорид 6 мг/мл) в разведении с физиологическим раствором 1:5. Далее мышцы в месте их прикрепления к черепу отсекали и скелетировали чешую затылочной кости, атлантоокципитальную мембрану и дугу I шейного позвонка. Выполняли пункцию затылочной цистерны с выведением 0,05-0,2 мл спинномозговой жидкости в течение 3-7 мин под контролем частоты и глубины дыхания животного. После этого в затылочную цистерну в течение 5-10 мин вводили 0,05-0,2 мл свежей человеческой венозной крови под контролем частоты и глубины дыхания животного. Для того чтобы большая часть крови скапливалась в области базальных цистерн, животное оставляли на 20 мин с опущенным на 20°-30° головным концом. После этого рану послойно ушивали. При необходимости компенсации кровопотери подкожно вводили смесь 5% раствора глюкозы и 0,9% раствора хлорида натрия объемом до 5-10 мл.
3. Оценка неврологического статуса
Оценку неврологического статуса проводили 1 раз в сутки в течение 7 дней после введения крови по методике, предложенной J.B. Bederson с соавт. (1986) [Bederson J.B., Pitts L.H., Tsuji M., Nishimura M.C., Davis R.L., Bartkowski H.: Rat middle cerebral artery occlusion: Evaluation of the model and development of a neurologic examination. Stroke 17:472-476, 1986] по 4-балльной шкале:
0 баллов - отсутствие неврологических нарушений
1 балл - крыса малоподвижна, вяло реагирует на прикосновение. Очаговая неврологическая симптоматика отсутствует
2 балла - имеется изолированный парез одной конечности (при приподнимании животного за хвост активность движений в одной из конечностей снижена)
3 балла - имеется односторонний гемипарез (при подталкивании животного в бок оно заваливается на пораженную сторону)
4 балла - имеется односторонняя гемиплегия (животное не может активно передвигаться, при движении вперед отмечается выраженное отклонение в пораженную сторону - движение по кругу).
По нашим данным изменения неврологического статуса наблюдались в течение первых суток после любого вмешательства под наркозом до 1 балла и не были связаны с проявлением сосудистого спазма
4. Морфологическое исследование
Перед изъятием головного мозга животное усыпляли смесью препаратов «золетил 100» (0,4 мл), ксилазина гидрохлорид (0,3 мл 2% р-ра) и рокурония бромида (0,1 мл 1% р-ра). По имевшемуся разрезу рану вскрывали. Выполняли декапитацию на уровне III-IV шейного позвонков, вскрывали черепную коробку и, по возможности не травмируя твердую и мягкую мозговую оболочки, извлекали препарат головного мозга вместе с верхнешейным отделом спинного мозга. Далее препарат помещали на 24 ч в 5% р-р формалина и заливали в парафин. Для морфологического исследования использовали срезы на уровне верхней трети базилярной артерии.
Окраску парафиновых срезов осуществляли следующими способами:
- Обзорная: гематоксилином и эозином,
- Для оценки состояния эластических волокон стенки артерии: по Грамм-Вейгерту (определение морфологического типа стенки базилярной артерии),
- Для оценки состояния сократительного аппарата гладкомышечных клеток (миофибрилл): по Lie.
Описание микропрепаратов проводили на светооптическом микроскопе Leica DM 1000 при увеличении 400-1000 раз, микрофотосъемку выполняли на цифровой камере Leica ЕС 3.
Были получены прямые качественные признаки церебрального сосудистого спазма в виде характерных морфологических изменений интракраниальных сосудов и ишемических изменений ткани мозга.
При исследовании верхней трети базилярной артерии у крыс после двухкратного введения аутокрови в затылочную цистерну были выявлены следующие изменения:
4-е сутки - морфологически прослеживались признаки умеренного спадения просвета сосуда без значительного утолщения стенки основной артерии и изменений внутренней эластической мембраны (ВЭМ). При окрасках по Lie и MSB выявлялись признаки гиперконтрактурных изменений гладкомышечных клеток (ГМК).
5-е сутки - отмечали утолщение стенки сосуда, подчеркнутую извитость эластической мембраны с углублением ее складок, сужением межскладочных промежутков, сближением эндотелиоцитов с выступающими в просвет ядрами, ориентированными по верхушкам сладок ВЭМ. При гистохимической реакции (окраска по Lie) в цитоплазме ГМК появлялись признаки дистрофических изменений от очаговой до распространенной гидропической дистрофии цитоплазмы в виде перинуклеарной и внутриклеточной вакуолизации, а также признаки внутриклеточной фуксинофилии цитоплазмы, указывающие на гиперконтрактурные изменения сократительных миофибрилл.
6-е и 7-е сутки - отмечали умеренное спадение просвета сосуда с распространенными дистрофическими изменениями цитоплазмы ГМК, как проявления остаточных признаков нарушения сократительной способности миоцитов при разрешении спазма.
Помимо этого, были выявлены признаки нарушения капиллярного кровотока в ткани мозга крысы, что является прямым признаком ишемии мозга на микроциркуляторном уровне.
Предложенный способ может быть использован для апробации методов профилактики и лечения церебрального сосудистого спазма в эксперименте, в том числе при интратекальном введении препаратов и использовании препаратов, имеющих сродство к белкам крови человека.