Результат интеллектуальной деятельности: СПОСОБ ЭПИДЕМИОЛОГИЧЕСКОГО РАЙОНИРОВАНИЯ ПО КОМПЛЕКСУ ПОКАЗАТЕЛЕЙ С ПРОИЗВОЛЬНОЙ ПРОСТРАНСТВЕННОЙ ТОЧНОСТЬЮ ДЛЯ СИСТЕМЫ ПОДДЕРЖКИ ПРИНЯТИЯ УПРАВЛЕНЧЕСКИХ РЕШЕНИЙ
Вид РИД
Изобретение
Изобретение относится к области медицины, в частности эпидемиологии, и может быть использовано для оценки эпидемиологической ситуации и планирования санитарно-профилактических и противоэпидемических мероприятий.
Эпидемиологическое районирование осуществляется с целью дифференциации территорий по степени риска осложнения эпидемиологической обстановки.
В основу районирования закладываются критерии оценки и сравнения территорий по одному или нескольким показателям.
Известен способ эпидемиологического районирования территории, заключающийся в подсчете заболеваемости по административным территориям, позволяющий ранжировать районы и определять приоритетность в проведении мероприятий эпидемиологического надзора [1]. Однако использование в данном способе районирования только одной характеристики - заболеваемости (или абсолютного числа больных), взятой за основу районирования территории, делает оценку эпидемиологического риска лишенной временных и групповых параметров, а также не учитывает влияния факторов риска. Кроме того, границы природных очагов инфекционных болезней чаще всего не совпадают с границами административных районов, что делает районирование малоинформативным.
Известен способ эпидемиологического районирования путем анализа нескольких значимых эпидемиологических показателей для описания административных районов. Мера значимости эпидемиологических показателей определяется экспертным путем, а именно эксперт на основании бальной оценки определяет значимость отдельных показателей, исходя из собственного опыта [2, 3]. При выборе показателей для проведения районирования в настоящее время параметр «число больных» является наиболее емким интегральным выражением эпидемиологического риска на территории, однако корректное использование данного параметра возможно при условии сопоставимости сравниваемых участков территории по площади и численности проживающего населения. В качестве показателя, определяющего экспозицию факторов риска, используется число лет регистрации больных в данном административном районе или на данном участке территории. При таком подходе подсчитывается сумма лет, в которых был зарегистрирован, по крайней мере, один больной.
Недостатком такого способа районирования является субъективность экспертной оценки в отношении значимости отдельных показателей и, как следствие, низкой повторяемости метода при использовании мнения других экспертов. В данном случае эксперту приходится сравнивать разнохарактерные величины. Например, определять, что при ранжировании территорий по риску возникновения острых кишечных инфекций доля домовладений, не имеющих канализации, в два раза важнее, чем доля населения, не имеющего доступ к центральному водоснабжению. Кроме того, неравнозначность административных территорий по площади, числу проживающего населения, ландшафтной структуре и плотности населения приводит к потере значимой информации при расчете средних (агрегированных) показателей и невозможности корректного сравнения районов.
Кроме того, данный способ характеризуется низкой разрешающей способностью в наиболее значимом диапазоне значений высокого эпидемиологического риска ввиду ограниченной точности способа определения экспозиции, поскольку за одинаковое число лет регистрации для множества участков территории с различным и при этом высоким эпидемиологическим статусом этот показатель оказывается одинаковым (максимальным).
Задачей изобретения является создание способа, позволяющего объективно ранжировать исследуемую территорию по степени эпидемиологического риска.
Технический результат заключается в повышении информативности, объективности оценки эпидемиологического риска и точности эпидемиологического районирования.
Технический результат достигается тем, что электронную карту выбранной территории покрывают сеткой из равных по площади ячеек в форме правильных шестиугольников, на полученную основу путем пространственного соединения агрегируется информация по эпидемиологически значимым показателям, при этом данные записываются в атрибутивную таблицу ячеек с последующей их обработкой и расчетом дополнительных показателей: число больных, совокупная длительность эпидемического периода, численность населения, показатель темпа роста числа больных, далее ячейки со схожими значениями объединяют в кластеры, для каждого кластера рассчитывают степень эпидемиологического риска: максимальный, средний, низкий; с последующим построением карты эпидемиологического риска и районированием территории путем объединения кластеров.
Способ осуществляют следующим образом.
На первом этапе территорию покрывают сеткой из равных по площади ячеек с размером, сопоставимым со средним населенным пунктом. Преимущества покрытий территории полигонами одинакового размера состоят в наглядности, большей пространственной точности, возможности использовать абсолютные показатели эпидемиологического риска и возможности варьирования размерами стандартных участков.
Выбор оптимальных параметров регулярного покрытия для эффективного районирования территории по эпидемиологическому риску состоит в обосновании площади стандартного участка и его формы. Традиционным способом такого дробления территории на стандартные участки можно считать деление на квадратные районы, линии которых проходят вдоль параллелей и меридианов, каждый из которых при необходимости повышения точности делится на четыре равных сектора.
Данный способ деления удобен своей простотой и даже может быть реализован без применения компьютерной техники. Однако, с точки зрения пространственного анализа, квадратная сетка обладает двумя существенными недостатками. Во-первых, площадь таких стандартных участков не одинакова на разных широтах, поскольку по мере удаления от экватора к полюсам участки приобретают трапециевидную форму и площадь их уменьшается. Во-вторых, центральные точки квадратных ячеек находятся на разных расстояниях от центров соседних ячеек.
Данные особенности квадратной сетки важны с точки зрения пространственного анализа, поскольку способствуют искажению при учете объектов или явлений, географически расположенных диагонально по отношению к сетке.
С точки зрения пространственного анализа, оптимальной формой покрытия для учета окружения точечного объекта является окружность. Однако сплошное регулярное покрытие с использованием окружности имеет зоны двойного пересечения, что искажает учет населенных пунктов и больных, расположенных в этой зоне.
В связи с этим предложено использование максимально приближенной к окружности и при этом лишенной недостатков квадратной сетки, форма сплошного регулярного покрытия, состоящая из правильных шестиугольников.
При построении слоя правильных шестиугольников определяющим параметром является длина ребра, которая определяет площадь фигуры. Выбор длины ребра осуществляется исходя из преобладающих условий заражения по выборочному анализу карт эпидемиологического обследования и может составлять от 2-5 км для одного субъекта Российской Федерации, до 15-30 км при районировании в общенациональном масштабе и от 30 км и более для глобальных покрытий.
На следующем этапе путем пространственного соединения в географической информационной системе (ГИС) на полученную основу агрегируется информация по населенным пунктам и больным, при этом данные записываются в поля атрибутивной таблицы шестиугольников. Данная таблица подвергается предварительной обработке с целью получения показателей для кластеризации. Число больных получается суммированием всех больных, зарегистрированных в пределах данного шестиугольника. Совокупная длительность эпидемического периода также определяется для каждого шестиугольника путем обработки дат заболевания больных. Численность населения вычисляется как сумма жителей всех населенных пунктов, располагающихся в пределах ячейки. Показатель темпа роста числа больных рассчитывается как отношение значения числа больных за последний год наблюдения к среднемноголетнему показателю (среднее арифметическое за пять лет, в которые не входит последний год).
После описанной обработки таблица принимает законченный вид, при этом в строках обозначаются уникальные идентификаторы шестиугольников, а в столбцах указано число больных, совокупная длительность эпидемического периода, численность населения и темпы роста больных по данному участку.
Ячейки территории с указанными атрибутами являются объектами кластеризации на 3 однородные группы, характеризующиеся различной степенью эпидемиологического риска. Основная идея и назначение кластерного анализа состоит в классификации (дифференцировании) выборки объектов на подмножества, называемые кластерами, так, чтобы каждый кластер состоял из схожих объектов, а объекты разных кластеров существенно отличались.
Сходство территорий по совокупности признаков в составе кластера определяется в ходе многомерной статистической процедуры. Принципиальным преимуществом кластерного анализа является независимость результатов кластеризации от субъективного мнения эксперта относительно принадлежности тех или иных территорий к определенным категориям риска.
Эпидемиологическая интерпретация значимости полученных кластеров осуществляется по средним величинам показателей и состоит в том, что участки территории, представляющие максимальный риск, относят к первой группе ячеек, представляющей максимальный эпидемиологический риск для населения в силу длительной экспозиции факторов риска по отношению к большому числу жителей. Кластер, характеризующийся средним эпидемиологическим риском, относят ко второй группе, а в третью группу - ячейки с низким эпидемиологическим риском.
На следующем этапе осуществляется построение карты эпидемиологического риска, т.е. полученные новые данные об эпидемиологическом статусе стандартных участков визуализируются при помощи ГИС, что является результатом соответствующего этапа районирования.
Способ эпидемиологического районирования апробирован на примере Астраханской области.
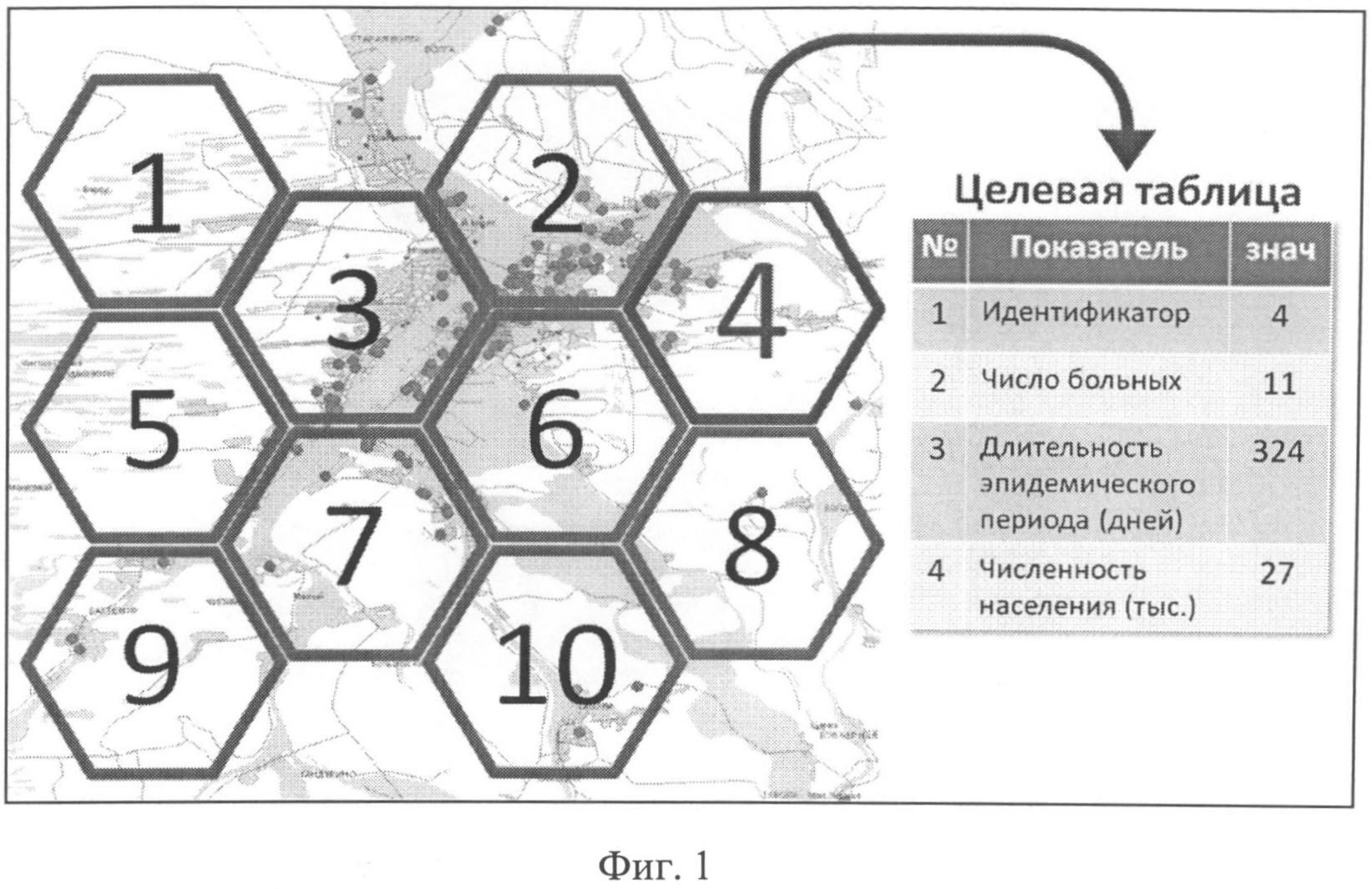
Для эпидемиологического районирования территории Астраханской области в отношении эпидемических проявлений Астраханской пятнистой лихорадки карта Астраханской области при помощи ГИС поделена на 12670 стандартных участков в форме правильных шестиугольников площадью - 5,9 км2 и длиной ребра 1,5 км. На полученную основу агрегируется информация по населенным пунктам и больным путем пространственного соединения. Данные о численности населения, числе больных и о длительности эпидемического периода записываются в атрибутивные поля таблицы шестиугольников. Агрегация данных по каждому стандартному участку и запись полученных значений в целевую таблицу представлены на фиг.1.
Таблица, полученная в результате агрегации данных, подвергается предварительной обработке с целью получения показателей для кластеризации. Число больных получается суммированием всех больных, зарегистрированных в пределах данного шестигранника. Совокупная длительность эпидемического периода также определяется для каждого шестигранника путем обработки дат заболевания больных. Численность населения вычисляется как сумма жителей всех населенных пунктов, располагающихся в пределах стандартного участка.
После описанной обработки таблица принимает законченный вид, при этом в строках обозначаются уникальные идентификаторы шестиугольников, а в столбцах указано число больных, совокупная длительность эпидемического периода и численность населения. По результатам предварительной обработки из 12670 стандартных участков заболеваемость отмечается в 223, именно по ним и была проведена кластеризация. В результате кластеризации 223 шестиугольников выделены три однородные группы, характеризующиеся различной степенью эпидемиологического риска. Характеристика кластеров представлена в табл.1. Согласно таблице к первому кластеру отнесено 9 стандартных участков со средним удельным числом больных 45±5 (среднее ± стандарт. ошиб.), средней совокупной длительностью эпидемического периода 618±41 и численностью постоянно проживающего населения более трех тысяч человек на один участок.
Ко второму кластеру отнесено 26 стандартных участков. Данный кластер характеризовался средним числом больных 18±1 на участок, средней совокупной длительностью эпидемического периода 320±14 дней и численностью населения от одной до трех тысяч человек.
В третий кластер вошло 188 стандартных участков, в каждом из которых зарегистрировано в среднем 3±0,2 больных, средняя совокупная длительностью эпидемического периода составила 28±3, а численность жителей не превышала одну тысячу человек.
Эпидемиологическая интерпретация значимости полученных кластеров состоит в том, что участки территории, относящиеся к первому кластеру, представляют максимальный эпидемиологический риск для населения в силу длительной экспозиции факторов риска по отношению к большому числу жителей. Второй кластер характеризуется средним эпидемиологическим риском, а третий - низким. Остальные 12447 стандартных участков, на территории которых заболеваемость АПЛ ранее не регистрировалась, были охарактеризованы как минимально опасные.
Завершающий этап эпидемиологического районирования заключается в визуализации при помощи ГИС полученных в результате кластеризации данных. Оценивая профили полученных кластеров, следует отметить, что максимальный эпидемиологический риск выявляется для территории, составляющей всего 0,07% от общей площади Астраханской области. На фиг.2 представлена карта эпидемиологического районирования территории Астраханской области, иллюстрирующая искомые районы с максимальным, средним и низким эпидемиологическим риском.
Таким образом, предложенный метод эпидемиологического районирования на основе кластеризации ячеек, характеризуется высокой пространственной точностью за счет использования большого числа ячеек вместо административных районов. Карты эпидемиологического риска, полученные методом кластеризации ячеек, демонстрируют прогностическую ценность, поскольку учитывают тенденцию к росту или падению заболеваемости. Эпидемиологическое районирование по комплексу показателей, осуществляемое при помощи кластеризации, обладает объективной основой, что определяет ее преимущество по отношению к балльной оценке риска, при которой определяющее значение имеет мнение эксперта.
Предложенный метод районирования на основе указанных преимуществ улучшает процесс принятия управленческих решений в области определения объемов и приоритетных территорий для проведения профилактических и противоэпидемических мероприятий.
Литература
1. Беляков В.Д. Современные аспекты изучения эпидемического процесса применительно к зоонозным природно-очаговым инфекциям // Вестн. АМН СССР. - 1980. - №10. - С.15-19.
2. Прохоров Б.Б. Медико-экологическое районирование и региональный прогноз здоровья населения России. М.: Изд-во МНЭПУ. 1996. - 72 с.
3. Трофимов A.M., Заботин Я.И., Панасюк М.В., Рубцов В.А. Количественные методы районирования и классификации. - Казань: изд-во Казанск. ун-та. - 1985. - 120 с.
|