Результат интеллектуальной деятельности: НАБОР ОЛИГОНУКЛЕОТИДНЫХ ПРАЙМЕРОВ И ФЛУОРЕСЦЕНТНО-МЕЧЕНОГО ЗОНДА ДЛЯ ИДЕНТИФИКАЦИИ Burkholderia pseudomallei
Вид РИД
Изобретение
Изобретение относится к биотехнологии, молекулярной биологии и может быть использовано в медицине для выявления генетического материала возбудителя мелиоидоза Burkholderia pseudomallei в пробах как для диагностики в практическом здравоохранении и службе Роспотребнадзора, так и для научных исследований.
В списке инфекционных заболеваний мелиоидоз занимает место особо опасной инфекции (ООИ) с ареалом распространения в тропических и субтропических регионах мира. В основном это страны юго-восточной Азии: Малайзия, Сингапур, Таиланд, а также северные регионы Австралии. Возбудитель В. pseudomallei - аэробная грамотрицательная неферментирующая бактерия. В настоящее время проблема мелиоидоза приобрела значение не только для традиционно эндемичных районов, но и для стран, где заболевание ранее не регистрировалось (Западная Европа и Северная Америка). Это связано с расширением торгово-экономических, транспортных, культурных взаимоотношений между странами мира и развитием туризма. Распространение и укоренение возбудителя в «новых» районах его обитания возможно также и за счет завоза больных животных, зараженной почвы, воды, пищевых продуктов. Клинические проявления мелиоидоза разнообразны с возможностью перехода латентного и хронического в острое состояние. Отсутствие настороженности медицинского персонала определяет сложность при установлении диагноза в неэндемичных регионах, в частности в России.
Метод полимеразной цепной реакции является прямым методом выявления ДНК возбудителя мелиоидоза и обладает высокой специфичностью и чувствительностью. В основе реакции лежит механизм репликации, который характеризуется внутриклеточным удвоением молекул ДНК ферментом ДНК-полимеразой. Выбор специфического фрагмента ДНК и подбор праймеров играет важнейшую роль в специфичности проведения амплификации, что сказывается на качестве проведения диагностики исследуемых микроорганизмов.
Внедрение в лабораторную диагностику метода ПЦР в режиме реального времени с флуоресцентной детекцией позволяет проводить выявление продуктов амплификации в процессе реакции и вести количественный учет ДНК. В одной пробирке протекает и детектируется реакция с использованием зондов, меченных различными флуоресцентными красителями, при помощи которых становится возможным автоматическая регистрация и интерпретация полученных результатов. Подобный подход дает возможность отказаться от стадии электрофореза, что ведет к резкому уменьшению вероятности контаминации исследуемых проб продуктами амплификации, а также позволяет снизить требования, предъявляемые к ПЦР-лаборатории.
Известно использование зондов для идентификации возбудителей сапа и мелиоидоза с флуоресцентной детекцией на основе последовательностей генов 23S рРНК, BTTS, bfl (патент РФ 2435861, МПК С12Р 19/30, С12Q 1/68, опубл. 10.12.2011, Бюл. №34. Ткаченко Г.А., Савченко С.С., Зинченко О.В., Антонов В.А., Алексеева В.В.; патент РФ 2439159, МПК С12Р 19/30, опубл. 10.01.2012, Бюл. №1. Ткаченко Г.А., Савченко С.С., Зинченко О.В., Антонов В.А., Алексеева В.В.; патент РФ 2435860, МПК С12Р 19/30, C12Q 1/68, опубл. 10.12.2011, Бюл. №34. Ткаченко Г.А., Савченко С.С., Зинченко О.В., Антонов В.А., Алексеева В.В.).
В 2012 году опубликована статья Абрамова Д.Д., Воробьева А.А., Кузнецовского Д.А., Чухланцева Н.В. Праймеры и зонд, входящие в тест-систему, идентифицируют возбудителей мелиоидоза и сапа, но не дифференцируют друг от друга [Разработка и испытания молекулярно-биологической тест-системы для выявления ДНК патогенных видов буркхолдерий методом ПЦР в реальном времени // Молекулярная медицина. - 2012. - №3. - стр.16-22].
Наиболее близким аналогом являются специфичные праймеры, опубликованные в статье Janse I. с соавторами, входящие в тест-систему для дифференциации патогенных буркхольдерий на основе мультиплексной ПЦР. В качестве ДНК-мишени для идентификации возбудителя мелиоидоза использован ген psu [Janse I, Hamidjaja RA, Hendriks AC, van Rotterdam BJ. Multiplex qPCR for reliable detection and differentiation of Burkholderia mallei and Burkholderia pseudomallei. BMC Infect Dis. 2013 Feb 14; 13:86. dot: 10.1186/1471-2334-13-86].
Однако в настоящее время в России для ПЦР-диагностики существуют наборы реагентов, которые идентифицируют возбудителей мелиоидоза и сапа, но не дифференцируют их между собой.
Целью настоящего изобретения является разработка высокоспецифичных олигонуклеотидных праймеров и флуоресцентно-меченого зонда для идентификации возбудителя мелиоидоза, а также для дифференциации его от возбудителя сапа методом полимеразной цепной реакции с флуоресцентной детекцией.
Цель достигается конструированием видоспецифичных олигонуклеотидов для идентификации мелиоидоза и дифференциации его от возбудителя сапа, обладающих активностью прямого и обратного праймеров в реакции амплификации, имеющих следующую структуру:
5′-TGCATTCGGCCTTCAACATTCCA-3′-Bps-gp68-f
5′-CGGATCGCGCCATCTTGCTAC-3′-Bps-gp68-r
Флуоресцентная детекция реализуется при помощи сконструированного видоспецифичного олигонуклеотидного зонда с комплементарными концевыми последовательностями по типу «молекулярного маяка»:
Bps-gp68-Pr 5′(TAMRA)-TGCGCTTCATGATTGTCGGTGCGCA-(BHQ2)3′,
где TAMRA - тетраметилкарбоксиродамин, флуоресцентный краситель, длина волны поглощения которого составляет 546 нм, а длина волны флуоресценции - 576 нм. BHQ2 - гаситель флуоресценции с диапазоном гашения 550-650 нм.
Характеристика олигонуклеотидных праймеров, зонда и ДНК-мишени для гибридизации.
Основываясь на данных, представленных в базе GenBank NCBI (National Center for Biotechnology Information, США), для идентификации ДНК возбудителя мелиоидоза и дифференциации его от возбудителя сапа были подобраны праймеры, обозначенные Bps-gp68-f/Bps-gp68-r, и зонд Bps-gp68-Pr, комплементарные участку гена, кодирующего белок gp68 B. pseudomallei из региона RimL (ацетилтрансферазы, включающие N-ацетилазы рибосомальных белков). Расчетная длина специфического фрагмента составляла 221 п.н.
В качестве положительного контроля эксперименты проводили на типовом штамме В. pseudomallei 100, используя для выделения ДНК обеззараженные суспензии микроорганизма в концентрациях от 1×109 м.к./мл до 1×101 м.к./мл. Апробация праймеров была осуществлена на наборе штаммов возбудителей мелиоидоза и сапа коллекционного центра ФКУЗ Волгоградский научно-исследовательский противочумный институт Роспотребнадзора.
Чувствительность реакции амплификации с флуоресцентной детекцией в режиме реального времени с праймерами Bps-gp68-f/Bps-gp68-r и зондом Bps-gp68-Pr оценивалась при исследовании проб ДНК, выделенных из десятикратных разведений чистых культур возбудителей мелиоидоза, и составила 1×104 м.к./мл.
Примеры конкретного выполнения.
Пример 1. Методика конструирования олигонуклеотидных праймеров и флуоресцентно-меченого олигонуклеотидного зонда для идентификации ДНК возбудителей мелиоидоза методом ПНР в режиме реального времени.
На основе анализа in silico нуклеотидных последовательностей возбудителей мелиоидоза, присутствующих в базах данных (EMBL, Genbank, DDBJ), для конструирования прямого Bps-gp68-f и обратного Bps-gp68-r праймеров был выбран участок генома В. pseudomallei размером 486 п.н. (GenBank NCBI, GeneID: 126221798), кодирующий белок gp68 и входящий в состав RimL региона (ацетилтрансферазы, включающие N-ацетилазы рибосомальных белков). Расчетная длина предполагаемого ампликона, фланкируемого предлагаемыми праймерами, - 221 п.н. (табл.1).
Сконструирован флуоресцентно-меченый зонд Bps-gp68-Pr размером 25 п.н., обладающий комплементарностью к продукту реакции амплификации с праймерами Bps-gp68-f/Bps-gp68-r, меченный с 5′-конца флуоресцентным красителем TAMRA и с 3′-конца - гасителем флуоресценции BHQ2. Концевые последовательности зонда гибридизуются между собой и образуют «шпильку» по принципу «молекулярного маяка».
При подборе праймеров и зонда руководствовались общими требованиями к олигонуклеотидным затравкам, используемым в ПНР. С помощью компьютерных программ была проанализирована структура выбранных пар праймеров и зондов (образование димеров, шпилек и других вторичных структур) и показана их теоретическая пригодность для успешной инициации реакции амплификации и гибридизации.
Праймеры Bps-gp68-f/Bps-gp68-r и зонд Bps-gp68-Pr были проанализированы с использованием компьютерной программы BLAST на web-сервере Национального Центра Биотехнологической Информации (NCBI) (http://www.ncbi.nlm.nih.gov/BLAST/) для установления гомологии между ними и нуклеотидными последовательностями близкородственных буркхольдерий, в том числе с В. mallei и других гетерологичных микроорганизмов, присутствующих в базах данных (EMBL, GenBank, DDBJ, Pathema). На момент проведения компьютерного анализа гомологии выявлено не было.
Пример 2. Амплификация и детекция специфических фрагментов ДНК с помощью разработанных праймеров Bps-gp68-f/Bps-gp68-r и флуоресцентно-меченого зонда Bps-gp68-Pr для идентификации возбудителя мелиоидоза методом ПНР в режиме реального времени.
В состав реакционной смеси помимо анализируемой ДНК входили разработанные комплементарные специфическому фрагменту ДНК В. pseudomallei олигонуклеотидный зонд Bps-gp68-Pr, прямой Bps-gp68-f и обратный Bps-gp68-r праймеры, а также дезоксирибонуклеозидтрифосфаты, буферный раствор и фермент Taq-F-полимераза (ФБУН ЦНИИ Эпидемиологии Роспотребнадзора). Амплификацию продолжительностью 45 циклов проводили в объеме 25 мкл. В качестве отрицательного контрольного образца в реакционную смесь добавляли ТЕ-буфер.
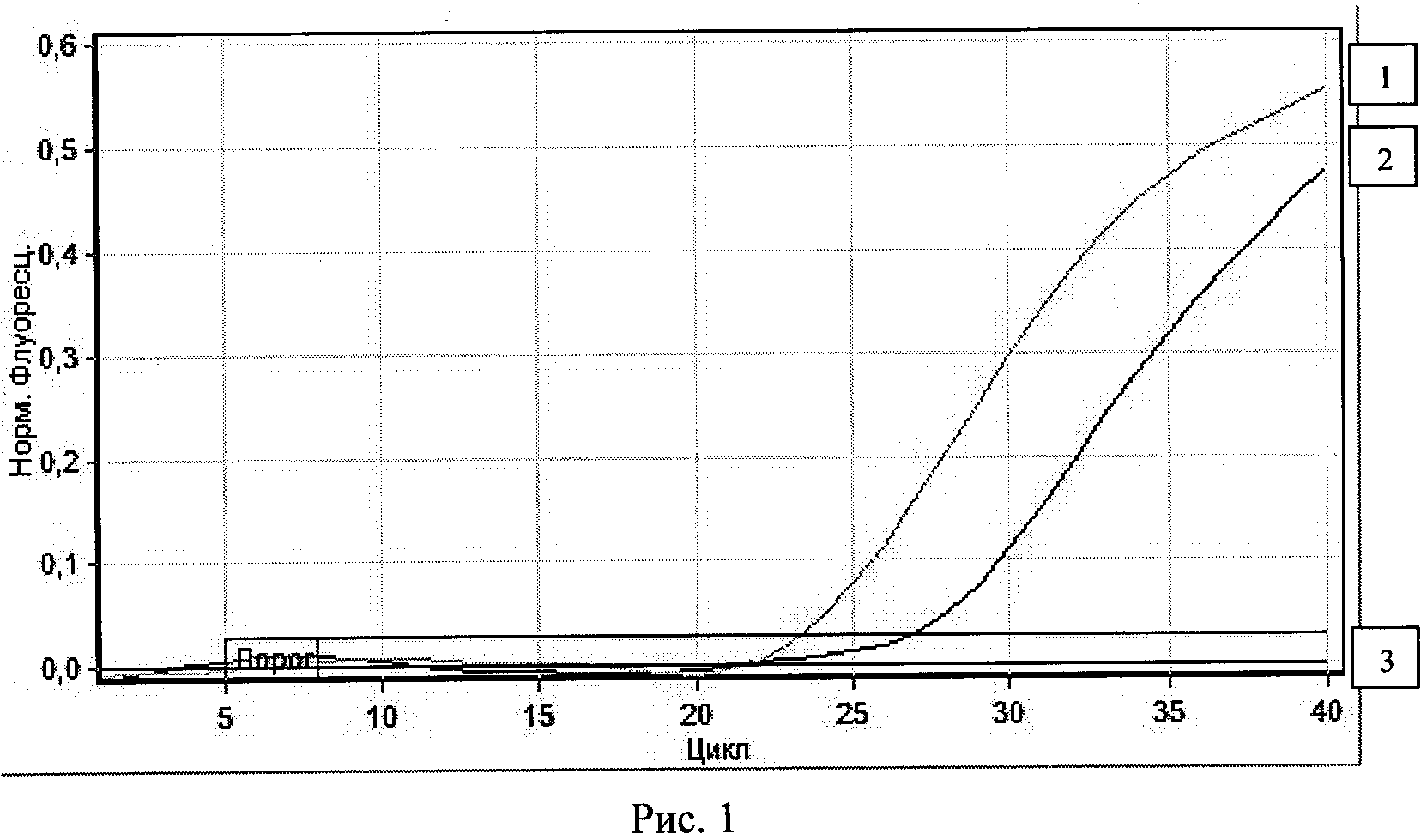
Анализ продуктов ПЦР осуществляли в режиме реального времени на приборе «Rotor-Gene 6000» («Corbett Research», Австралия). Регистрацию результатов проводили в табличной и графической форме. Результат амплификации каждого штамма В. pseudomallei считался положительным, в случае если кривая накопления флуоресценции по каналу детекции пересекала пороговую линию на участке характерного экспоненциального подъема флуоресценции, на цикле, не превышающем граничное значение порогового цикла реакции (Ct) в соответствующей графе в таблице результатов (рис.1). Рисунок 1 отображает график нарастания флуоресцентных кривых, полученных при амплификации ДНК штаммов возбудителя мелиоидоза с праймерами Bps-gp68-f /Bps-gp68-r и зондом Bps-gp68-Pr (изображены кривые 1 - В. pseudomallei 100 в концентрации 105 м.к./мл; 2 - В. pseudomallei 100 в концентрации 104 м.к./мл, 3 - отрицательный контроль и кривые накопления флуоресценции проб В. pseudomallei в концентрации меньше 103 м.к./мл, не пересекающие пороговую линию).
Пример 3. Определение чувствительности и специфичности реакции амплификации с помощью разработанных олигонуклеотидных праймеров Bps-gp68-f/Bps-gp68-r и флуоресцентно-меченого зонда Bps-gp68-Pr для идентификации ДНК возбудителя мелиоидоза и дифференциации его от возбудителя сапа.
Чувствительность реакции амплификации с разработанными специфичными праймерами Bps-gp68-f/Bps-gp68-r и флуоресцентно-меченым зондом Bps-gp68-Pr оценивалась при исследовании проб ДНК, выделенных из бактериальных взвесей клеток В. pseudomallei. Штаммы буркхольдерий выращивали на плотных питательных средах в течение 1-2 суток. Готовили бактериальные взвеси клеток в 4 мл 0,15 М раствора натрия хлорида в концентрации 1×09 м.к./мл по отраслевому стандартному образцу мутности ГИСК им. Л.А. Тарасевича (ОСО 42-28-85 П) и разводили таким образом, чтобы концентрации возбудителей сапа составляла от 1×109 до 1×101 м.к./мл.
Учитывая, что возбудитель мелиоидоза относится к агентам II группы патогенности, пробоподготовку и обеззараживание материала для проведения ПЦР осуществляли согласно МУ 1.3.2569-09 «Организация работы лабораторий, использующих методы амплификации нуклеиновых кислот при работе с материалом, содержащим микроорганизмы I-IV групп патогенности» и МУ 4.2.2787-10 «Лабораторная диагностика мелиоидоза». Обеззараживание исследуемых проб проводили добавлением раствора мертиолята натрия до конечной концентрации 0,01% и прогреванием в течение 30 мин при температуре 56°С. Выделение ДНК из чистых культур буркхольдерий, близкородственных и гетерологичных микроорганизмов проводили путем нуклеосорбции и лизиса клеток гуанидинтиоцианатом с помощью набора «ДНК-сорб-В» (ФБУН ЦНИИ Эпидемиологии Роспотребнадзора) в соответствии с инструкцией по применению.
Специфичность разработанных праймеров Bps-gp68-f/Bps-gp68-r и флуоресцентно-меченого зонда Bps-gp68-Pr оценена на коллекции из 84 штаммов, из которых 48 штаммов В. pseudomallei и 36 штаммов гетерологичных микроорганизмов (14 штаммов В. mallei, 10 штаммов В. cepacia, 5 штаммов В. thailandensis и по 1 штамму Pseudomonas aeruginosa, Pseudomonas fluorescens, Pseudomonas putida, Francisella tularensis, Yersinia pestis, Bacillus anthracis, Echerichia coli). Оценка специфичности показала отсутствие перекрестных реакций с близкородственными гетерологичными штаммами, в том числе с ДНК В. mallei, и наличие специфической амплификации со всеми штаммами В. pseudomallei.
Чувствительность тест-системы оценивали на десятикратных разведениях бактериальных взвесей штаммов В. pseudomallei. В амплификационную смесь добавляли по 10 мкл ДНК, выделенной из разведений от 1×105 до 1×101 м.к./мл. Анализ результатов показал, что с помощью разработанных праймеров Bps-gp68-f/Bps-gp68-r и флуоресцентно-меченого зонда Bps-gp68-Pr обнаруживают ДНК возбудителя мелиоидоза при концентрации в пробе 1×104 м.к./мл.
Таким образом, разработанные праймеры Bps-gp68-f/Bps-gp68-r и флуоресцентно-меченый зонд Bps-gp68-Pr могут быть использованы для обнаружения ДНК возбудителя мелиоидоза и позволяют в короткий срок с высокой чувствительностью и специфичностью детектировать возбудителя мелиоидоза и дифференцировать его от возбудителя сапа в пробах чистых культур и биологическом материале.
Набор олигонуклеотидных праймеров и флуоресцентно-меченого зонда для идентификации Burkholderia pseudomallei и дифференциации от возбудителя сапа методом полимеразной цепной реакции с флуоресцентной детекцией, комплементарных участку гена, кодирующего белок gp68 В. pseudomallei из региона RimL ацетилтрансферазы, включая N-ацетилазы рибосомальных белков, обладающие активностью прямого и обратного праймеров в реакции амплификации, и зонда с комплементарными концевыми последовательностями по типу «молекулярного маяка», обеспечивающего флуоресцентную детекцию, имеющие следующую структуру:5′-TGCATTCGGCCTTCAACATTCCA-3′-Bps-gp68-ƒ5′-CGGATCGCGCCATCTTGCTAC-3′-Bps-gp68-r5′(TAMRA)-TGCGCTTCATGATTGTCGGTGCGCA-(BHQ2)3′-Bps-gp68-Pr,где TAMRA - тетраметилкарбоксиродамин, флуоресцентный краситель, длина волны поглощения которого составляет 546 нм, а длина волны флуоресценции - 576 нм; BHQ2 - гаситель флуоресценции с диапазоном гашения 550-650 нм.