Результат интеллектуальной деятельности: СПОСОБ ОПРЕДЕЛЕНИЯ ВОДЫ В КООРДИНАЦИОННЫХ СОЕДИНЕНИЯХ
Вид РИД
Изобретение
Изобретение относится к способам качественного и количественного определения воды во внутренней сфере координационных соединений (КС) и может найти применение в координационной химии и фармации.
Наиболее эффективным природным средством детоксикации организма человека от вредного воздействия радионуклидов, тяжелых и токсичных металлов являются пектины, способные за счет различных функциональных групп и атомов кислорода образовывать с ионами металлов КС - пектинаты металлов (Комиссаренко С.Н., Спиридонов В.Н. Пектины - их свойства и применение. Растит. ресурсы, 1998, т.34, вып.1, с.111-119). Наряду с ионами металлов и пектином, очень большую роль в построении КС играют молекулы воды, существенно влияющие на строение и состав КС. Это связано с тем, что появление пектина в реакционной среде, содержащей гидратированные катионы металла, приводит к полному или частичному замещению молекул воды: вода может остаться в координационном ионе, т.е. быть, наряду с пектином, лигандом в КС, может перейти во внешнюю сферу КС или быть капиллярно связанной (адсорбированной). Определение положения молекул воды в КС необходимо для установления структуры и состава КС, а также обоснования терапевтических дозировок лекарственных средств.
Из немногочисленных способов определения воды в КС можно отметить следующие.
Описан полярографический способ исследования структуры КС, основанный на электролизе веществ, восстанавливающихся на катоде или окисляющихся на аноде, в т.ч. воды (Желиговская Н.Н., Черняев И.И. Химия комплексных соединений, М., ВШ, 1966, с.291-298). Однако данный способ не позволяет определить положение молекул воды: входят ли они в состав КС или являются капиллярно связанными. Кроме того, на электродах окислительно-восстановительные свойства, помимо воды, проявляют другие структурные компоненты КС.
Более информативным является исследование строения КС по ИК-спектрам поглощения, характер которых и положение характеристических частот позволяют предположить тип связи «металл - лиганд». Описан способ определения структурных компонентов твердых пектинов, пектинатов металлов в виде пленок путем регистрации ИК-спектров в токе паров D2O при фиксированной температуре и области поглощения в пределах 700-3800 см-1 (Филиппов М.П. Инфракрасные спектры пектина и его производных. Изв. АН МССР, 1976, №4, с.80-87). Этим способом идентифицируют молекулы воды, в том числе ассоциированные межмолекулярными водородными связями, по трем типам колебаний: два типа (валентные колебания) сопровождаются периодическим изменением длин связей (проявляются в виде полос поглощения 3652 см-1 и 3756 см-1), третий тип (деформационные колебания) - периодическим изменением угла связи (в виде полосы 1515 см-1). В результате координации лигандов к ионам металлов свойства симметрии молекул и характер колебаний в общем сохраняются, хотя молекулы, ставшие лигандами в КС, претерпевают некоторые изменения, что сказывается на типах и частотах колебаний (Желиговская Н.Н., 1966, … с.319-320). Однако эти изменения не позволяют дифференцировать молекулы воды в определенных сферах (внутренней или внешней) КС и, кроме того, могут быть обусловлены и другим лигандом (пектином), комплексообразователем (ионом металла). Таким образом, основным недостатком данного способа является ориентировочность определения молекул воды в КС по относительным изменениям типов и частот колебаний и относительной прочности связи, поэтому о составе КС можно судить только предположительно.
Описан способ определения структуры пектината натрия, полученного в виде пленки длиной 5 мк и массой 10 мг, по ИК-спектру, зарегистрированному в токе паров D2O в вакууме в области 700-3800 см-1 (Куриленко О.Д., Фабуляк Я.Г., Климович В.М. IЧ-спектроскопiя при адсорбцiï води яблучним пектином i його натриєвою сiллю. Доповiдi Академiï наук Украïнськоï РСР, серiя Б: Геологiя, геофiзика, хiмiя та бiологiя, Киïв, Наукова думка, 1975, №4, с.332-334). Сравнением с яблочным пектином устанавливают различные структурные особенности пектината натрия: связи между ионами натрия и атомами кислорода гидроксильных групп (появление полос поглощения 3200 см-1 и 3500 см-1); ионизацию гидроксильных групп и гидролиз эфирных групп (снижение интенсивности полос в области 1000-1100 см-1); исчезновение свободных карбоксильных групп (отсутствие полосы 1740 см-1) и появление ионизированных карбоксильных групп (обнаружение полос 1615 см-1 и 1420 см-1; смену конформации пиранозного цикла из «кресла» в «ванну» (исчезновение полосы 925 см-1 и появление полосы 820 см-1). Из-за невозможности определения молекул воды в КС по этим данным, далее проводят дегидратацию образцов (в условиях вакуума Р=10-5 мм рт.ст. и температуры 185°С) с последующей количественной обработкой пленок водой для определения ее участия в образовании пектината натрия. По ИК-спектру подготовленного подобным образом пектината натрия предположительно устанавливают наличие в нем трех форм воды: заполняющей внутренние полости, образованные пиранозными циклами (полоса 2190 см-1); связанной ионизированными карбоксильными группами (полоса 2750 см-1) и связанной гидроксильными группами (полоса 3440 см-1), в отличие от пектина, где второй формой воды является вода, связанная карбоксильными группами (полоса 2650 см-1). Более высокая интенсивность всех указанных полос поглощения в спектре пектината натрия по сравнению с пектином свидетельствует о его большей способности к адсорбции воды. Ступенчато отделяя воду из обоих образцов путем обработки их хлористым тионилом, устанавливают наличие обычной, быстро выделяемой, воды (полоса 3440 см-1) и более прочно связанной воды (полоса 2190 см-1).
Данный способ определения воды в структуре КС наиболее близок к заявляемому и выбран за прототип.
Недостатками указанного способа являются:
1) высушивание образцов при температуре 185°С, даже в вакууме, способствует удалению молекул, как адсорбционной, так и координационной воды, что не позволяет их обнаружить по ИК-спектру;
2) последующая обработка дегидратированных образцов определенными количествами воды может не привести к включению молекул воды в КС и тогда заключение об отсутствии координационной воды в КС до дегидратации будет неправомерным;
3) дифференциация воды по принципу «обычной, быстро выделяемой» и «более прочно связанной» носит относительный характер и не позволяет определить принадлежность к КС, тем более конкретизировать положение молекул воды в КС;
4) неоднозначность идентификации молекул воды по ИК-спектрам: отнесение как к разным полосам поглощения (3440 см-1, 2650 см-1, 2190 см-1, 3500-3000 см-1, 1800-1600 см-1), так и «накладка», например, ионизированных карбоксильных групп (1800-1600 см-1);
5) в связи с вышесказанным, невозможность установления, как качественного, так и количественного состава КС;
6) трудоемкость получения пленок образцов, необходимость создания вакуума для дегидратации.
Цель изобретения - идентификация и количественное определение воды во внутренней сфере КС для установления состава (формулы) КС.
Поставленная цель достигается тремя стадиями анализа КС в сопоставлении с исходными веществами.
I. Сначала определяют наличие «высокотемпературной» воды, для чего образцы в твердом состоянии анализируют в вариантах дифференциального термического (ДТА), дифференциального термогравиметрического (ДТГА), термогравиметрического (ТГА) анализа в интервале температур 20÷1000°С при скорости нагревания веществ 10 град/мин.
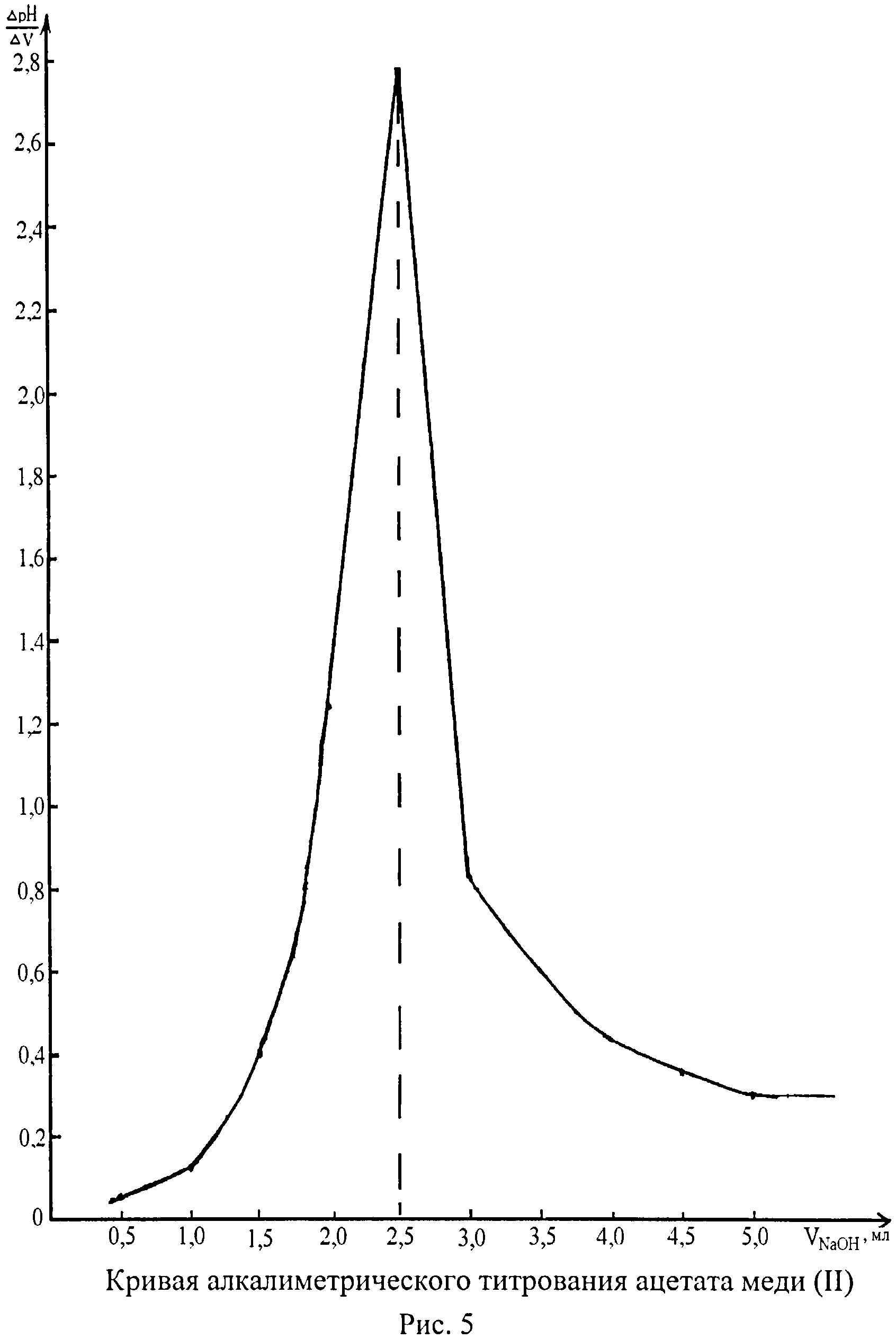
II. Затем определяют возможность образования гидроксосоединения при алкалиметрическом титровании образцов (т.е. проявление ими кислотных свойств) с потенциометрической фиксацией значения рН в точке эквивалентности. Для этого 0,1-0,3% водные растворы, приготовленные из высушенных при температуре 120°С в течение 8 час образцов, титруют 0,1 моль/л раствором гидроксида натрия и определяют точку эквивалентности на кривой титрования дифференциальным способом в графической системе «(ΔрН/ΔV)-VТИТРАНТА».
III. Далее, при установлении наличия «высокотемпературной» воды (температура дегидратации >150°С) по термическим кривым и выявлении образования гидроксосоединения по кривой алкалиметрического титрования (рН в точке эквивалентности <5), что свидетельствует о присутствии «внутрисферной» воды, определяют ее содержание и формулу КС: для высушенных при 120°С в течение 8 час образцов по термогравиграмме в графической системе «Количество удаленной воды, ммоль - Температура дегидратации, °С», определяют содержание внутрикоординационной воды и рассчитывают молярный состав (формулу) КС.
При низкой скорости нагревания веществ (2 град/мин) в ходе записи термических кривых может произойти структурная перестройка КС, связанная с переходом молекул воды в координационную сферу комплексного иона (Координационная химия редкоземельных элементов. Под ред. Спицына В.И., Мартыненко Л.И., М., МГУ, 1979, 254 с.), поэтому в заявляемом способе снятие термических кривых проводят при высокой скорости нагревания веществ (10 град/мин).
Предлагаемый способ анализа можно охарактеризовать на примере КС - пектинатов металлов (II), полученных в твердом состоянии (осадки) известным способом путем смешивания 0,1 моль/л раствора ацетата металла (II) и 0,25% раствора пектина в соотношении 1:10 (Лакатош Б., Майзель Ю., Варью М. Способ получения комплекса иона металла с олиго- или полигалактуроновыми кислотами. Пат. СССР 886750, МКИ С07Н 23/00, опубл. 30.11.81).
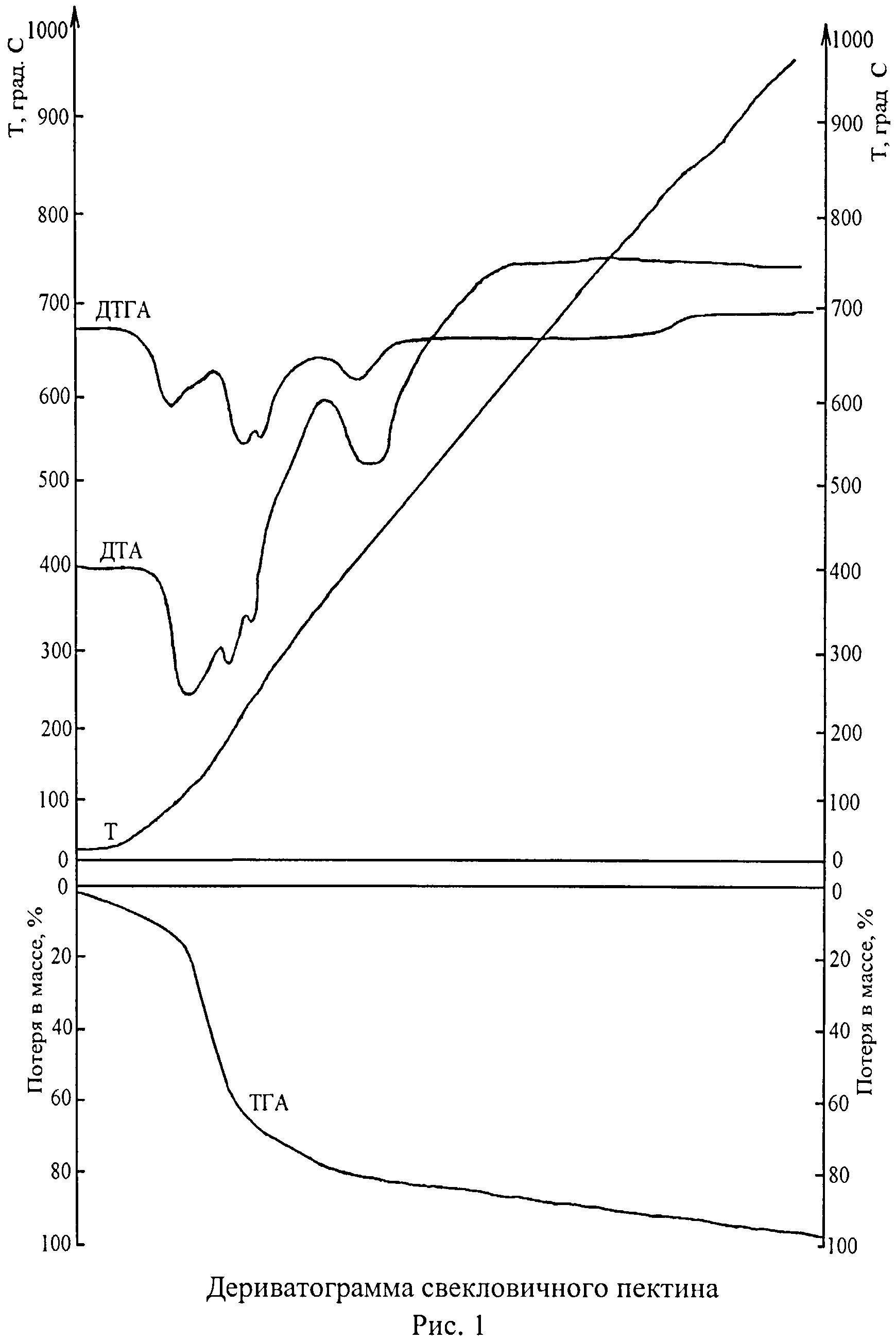
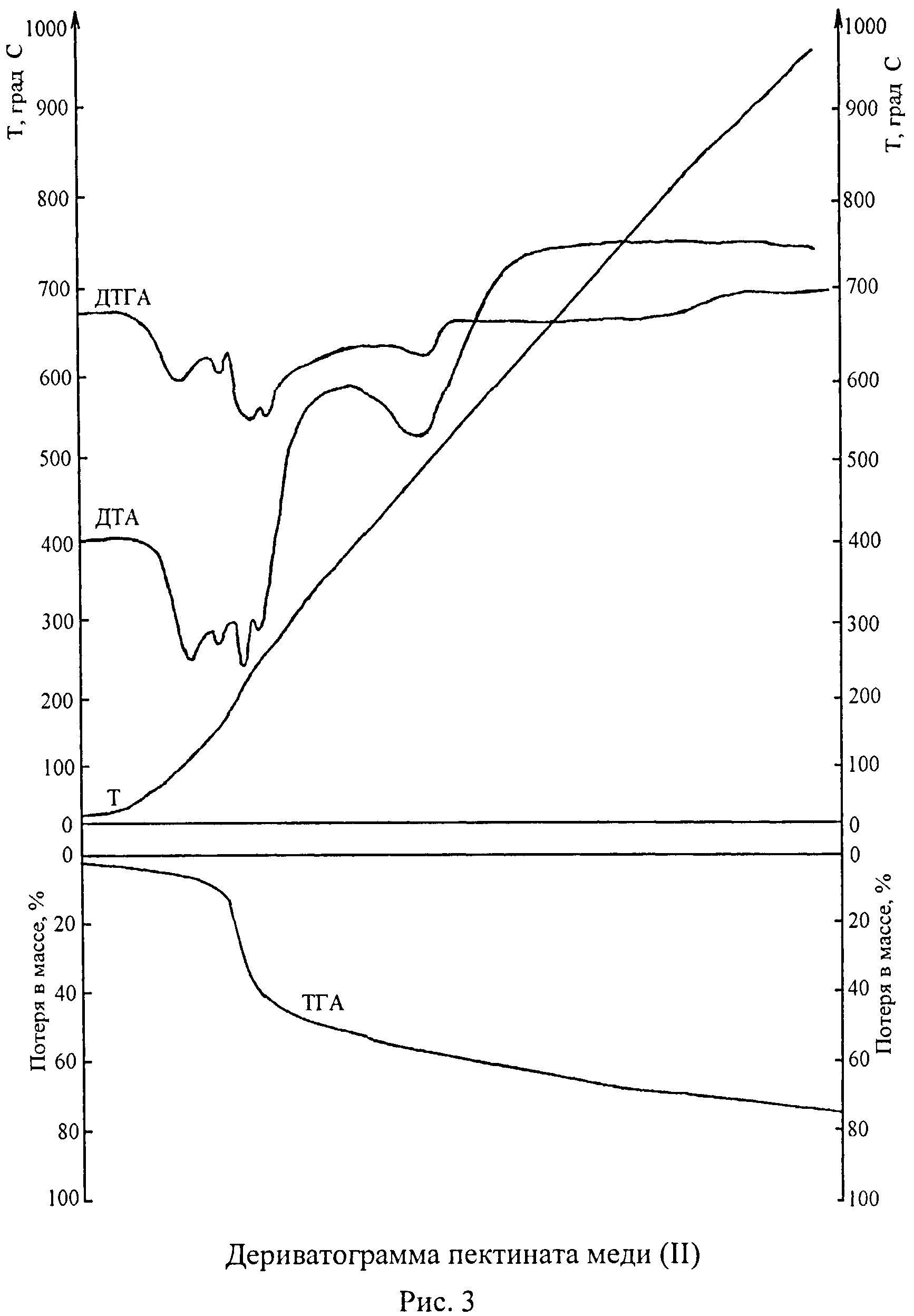
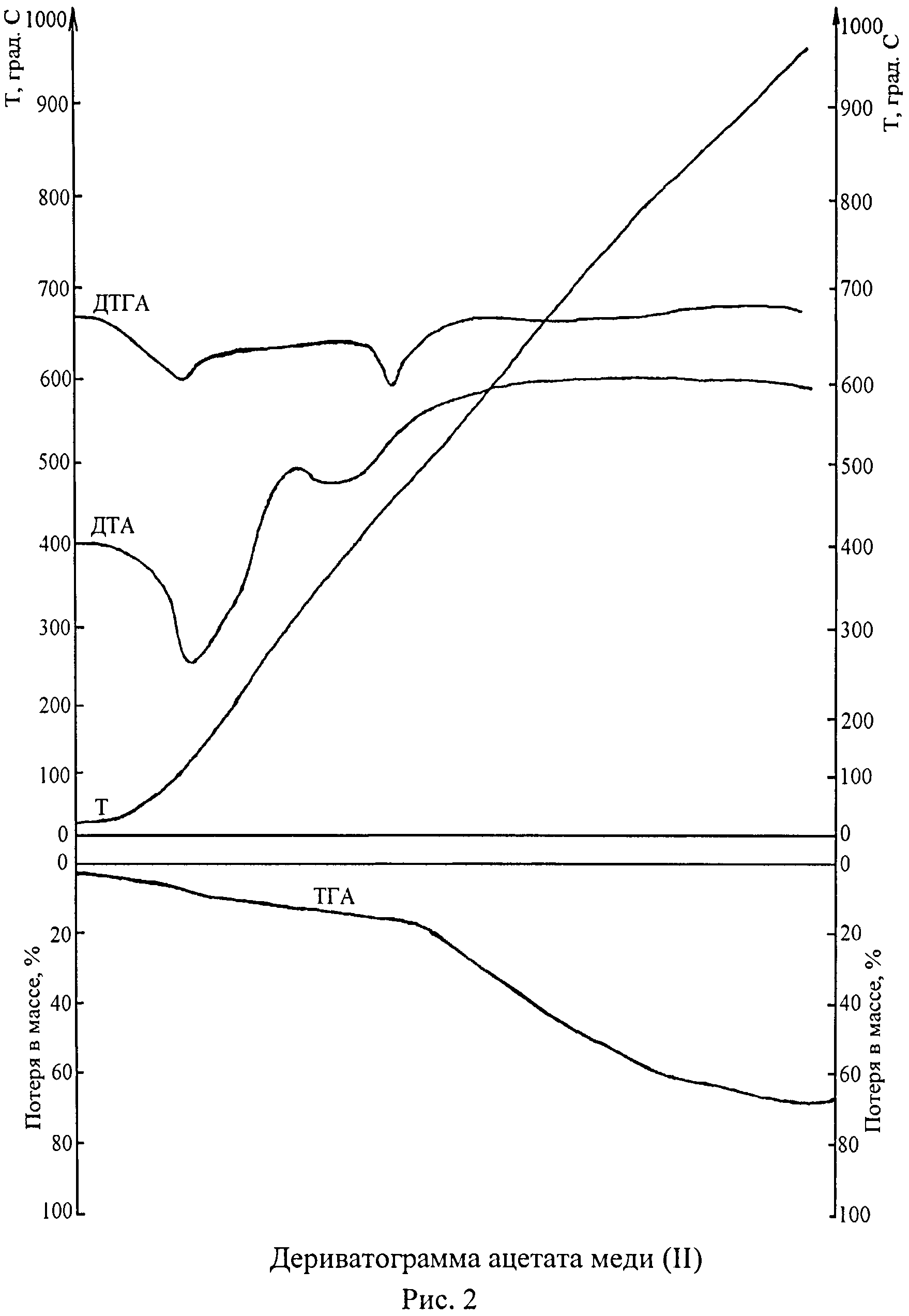
Для получения пектината меди (II) использованы свекловичный пектин и ацетат меди (II), их дериватограммы приведены на рисунках 1, 2, 3, характеристика дериватограмм - в таблице 1. Сравнительный анализ термических кривых исходных веществ и пектината показывает, что первый эндотермический эффект на кривой ДТГА наблюдается при температурах: 80-105°С для пектина, 110-115°С для ацетата меди (II), 90-115°С для пектината меди (II). Учитывая содержание влаги в образцах (17,2%, 9,0%, 7,4% соответственно), данный эффект относится к потере капиллярно связанной (адсорбированной) воды. Этому же эффекту соответствует на кривой ДТА эндотермический пик: при 100-115°С для пектина, 115-120°С для ацетата меди (II), 115-120°С для пектината меди (II). Значительное различие между анализируемыми образцами отмечается при температуре 150-165°С и 155-160°С на кривых ДТГА и ДТА соответственно: у пектината меди (II) наблюдается эндотермический эффект, не обнаруженный для исходных веществ. Можно предположить, что данный эффект относится также к потере воды пектинатом меди (II), т.е. для пектина и ацетата меди (II) процесс дегидратации является одноступенчатым: молекулы воды отщепляются в одну стадию при температуре 80-115°С и 110-120°С, а для пектината меди (II) - двухступенчатым: при 90-120°С и 150-165°С. Другие наблюдаемые эффекты (тоже эндотермические) обусловлены деструкцией органической части пектина и пектината меди (II): по карбоксильным группам (190-230°С), гликозидным связям (230-270°С). Последующее повышение температуры ведет к полному разложению всех веществ.
Таким образом, анализ термических кривых показывает, что все исследуемые вещества содержат воду, отщепляющуюся при более низкой температуре (что характерно для адсорбционной воды), и только пектинат меди (II) содержит еще и «высокотемпературный» (150-165°С) компонент, предположительно молекулы координационной воды.
Для подтверждения или опровержения этого предположения сначала из исследуемых веществ удаляют адсорбционную воду. По данным дериватограмм, верхний предел интервала температур, соответствующих дегидратации адсорбционной воды из различных образцов, составил 120°С, поэтому влияние продолжительности высушивания на потерю адсорбционной воды устанавливают при указанной температуре (таблица 2). Как следует из таблицы 2, для всех исследуемых веществ оптимальной продолжительностью высушивания, при которой достигается практически полное удаление адсорбционной воды, является 8 час.
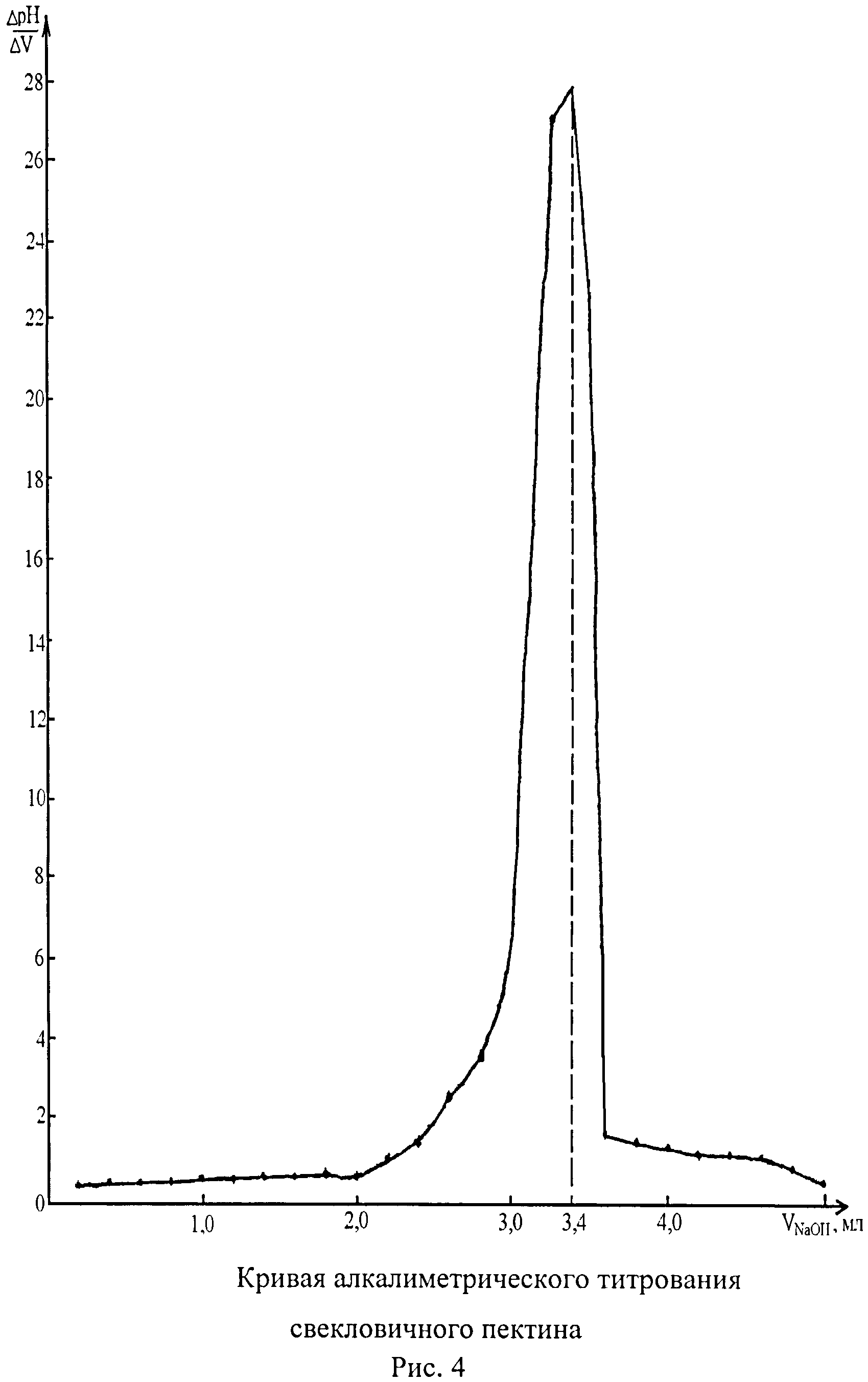
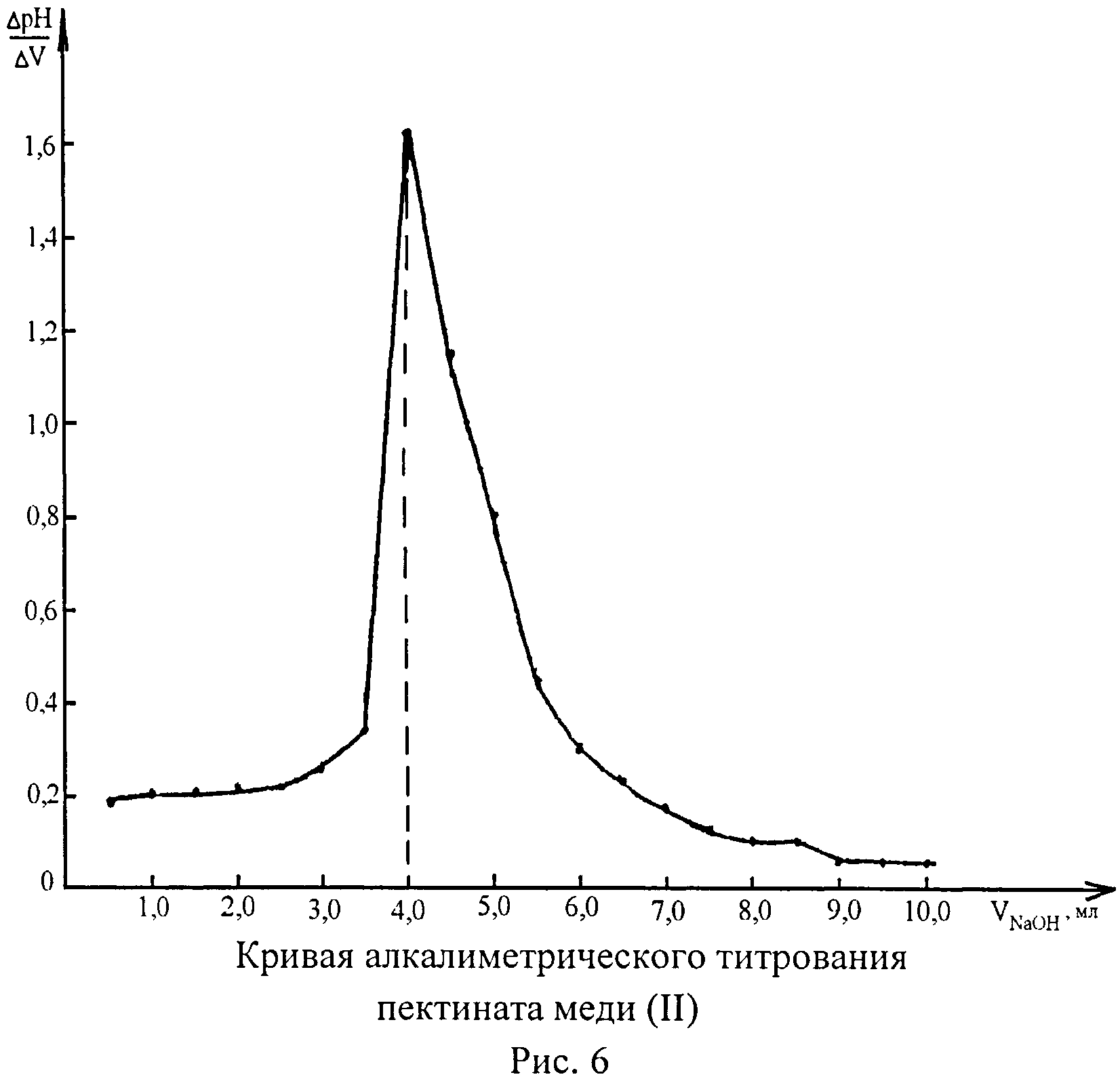
Далее дегидратированные от адсорбционной воды при температуре 120°С в течение 8 час образцы подвергают алкалиметрическому титрованию 0,1 моль/л раствором гидроксида натрия с потенциометрической фиксацией точки эквивалентности на рН-метре марки «рН-340» при использовании в качестве электрода сравнения хлорсеребряного электрода, в качестве индикаторного - стеклянного электрода. Для надежного определения точки эквивалентности используют дифференциальный способ (Пономарев В.Д. Аналитическая химия. М., ВШ, 1982, ч. 2. с.219-228) путем построения графической зависимости «(ΔрН/ΔV)-VТИТРАНТА». Кривые алкалиметрического титрования приведены на рисунках 4, 5, 6. Из представленных данных следует, что рН в точке эквивалентности при титровании пектината меди (II) составляет 4,87, в то время как при титровании пектина - 9,14, ацетата меди (II) - 6,42. Эти результаты свидетельствуют о том, что ни при титровании пектина, ни при титровании ацетата меди (II) не наступает точка эквивалентности в кислой среде, в отличие от пектината меди (II), что доказывает образование пектинатом меди (II) гидроксосоединения. Установленная величина рН в точке эквивалентности (4,87) значительно ниже рН, как для пектина, так и для ацетата меди (II), и не может рассматриваться даже как промежуточная. Следовательно, гидроксокомплекс в пектинате меди (II) образуют только молекулы воды, усиление кислотных свойств которых (согласно Желиговской Н.Н., 1966, с.139, 142) происходит в результате координации с комплексообразователем (ионом металла).
Таким образом, выявление двух фактов в пектинате меди (II): наличие «высокотемпературного» компонента (150-165°С) и проявление кислотных свойств при взаимодействии со щелочью с образованием гидроксосоединения (рН в точке эквивалентности 4,87), доказывают присутствие молекул воды во внутренней координационной сфере пектината меди (II).
Два интервала температур дегидратации у пектината меди (II) можно объяснить различной длиной и, соответственно, прочностью связей, образуемых ионами меди (II) (проявляющих сильное поляризующее действие) с молекулами воды, находящимися внутри координационной сферы и вне ее.
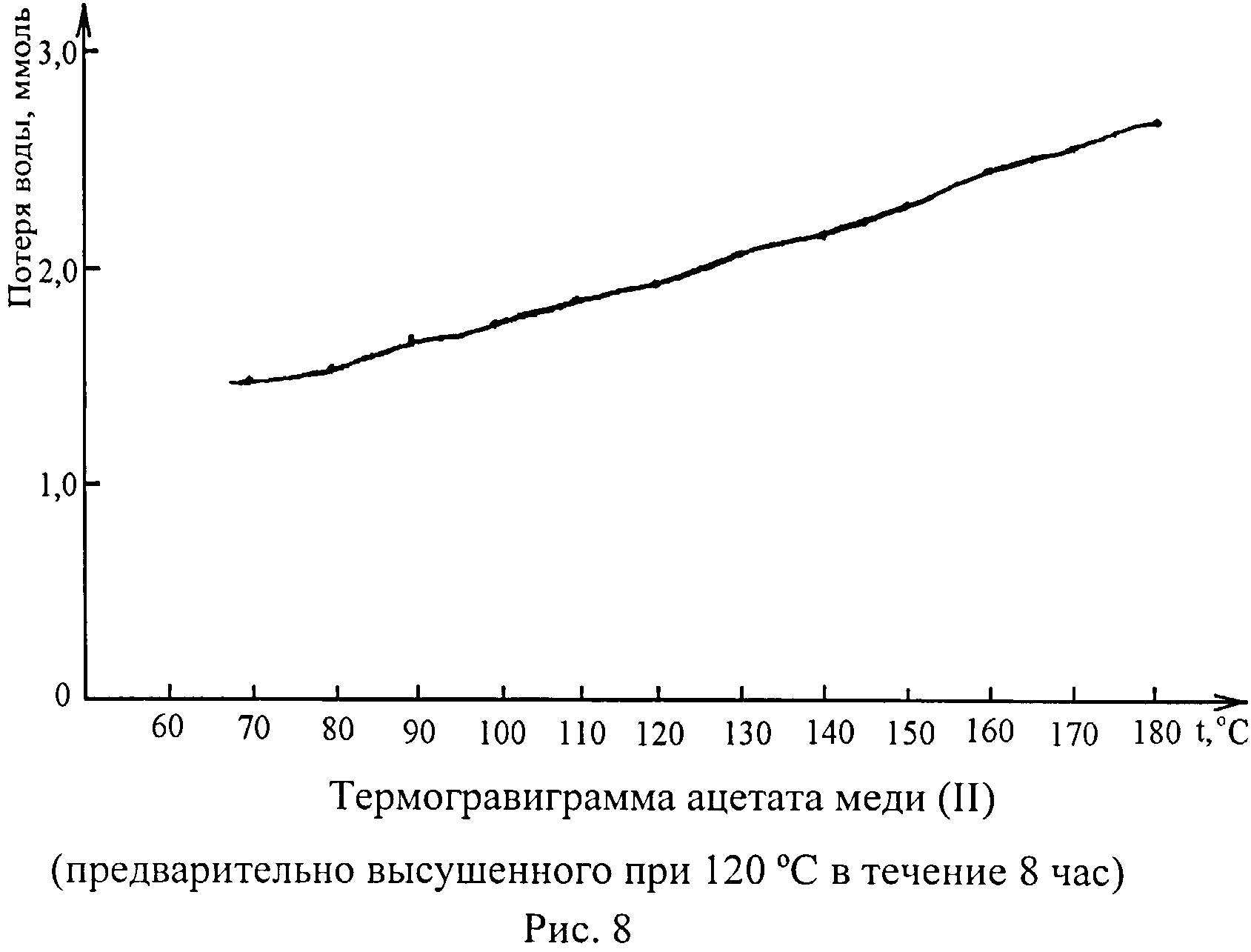
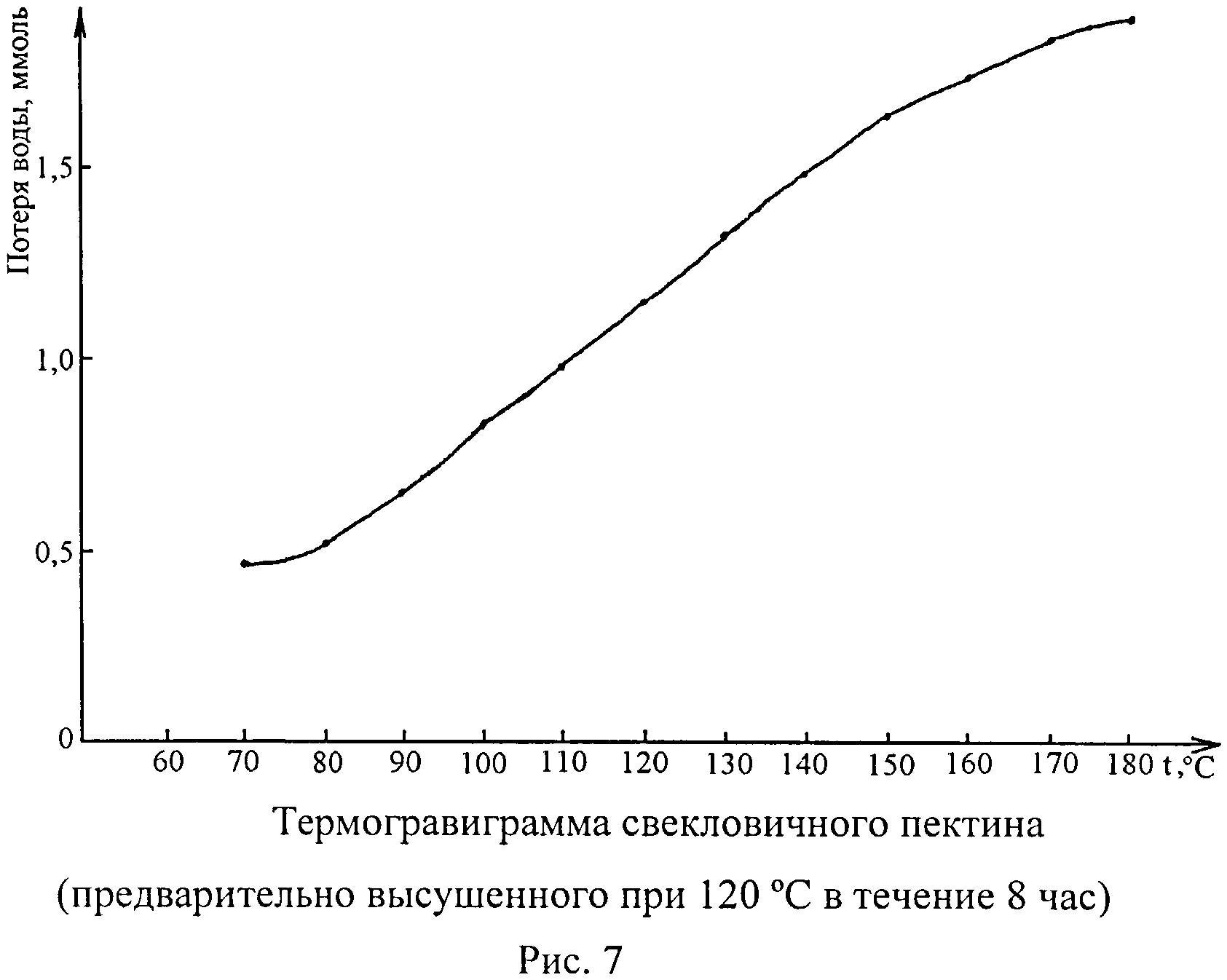
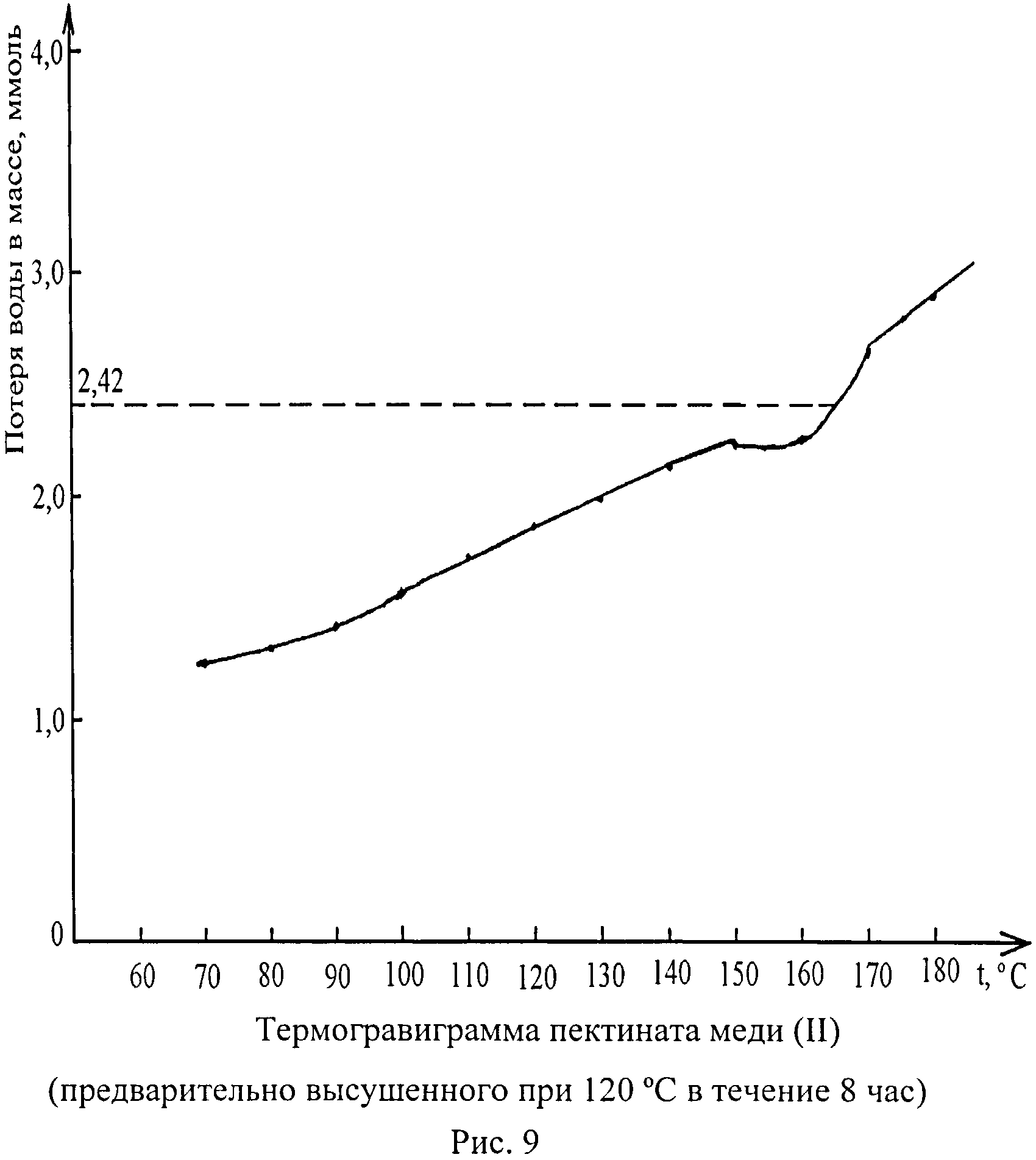
Установив в высушенном при температуре 120°С в течение 8 час пектинате меди (II) наличие молекул «внутрисферной» воды, определяют ее количество по термогравиграмме, построенной в графической системе «Количество удаленной воды, ммоль - Температура дегидратации, °С», в сопоставлении с исходными веществами (рисунки 7, 8, 9). В отличие от пектина (рисунок 7) и ацетата меди (II) (рисунок 8), на термогравиграмме пектината меди (II) (рисунок 9) выявлена «площадка», соответствующая координационной воде. Определив по термогравиграмме ее количество (при температуре 150-165°С) во взятой навеске пектината меди (II) и учитывая молярное соотношение других компонентов КС - ионов меди (II) и мономеров пектина (остатков галактуроновой кислоты (L)), равное 1:2 (или их массовое соотношение 15,46%:84,54%) (Кайшева Н.Ш. Научные основы применения полиуронидов в фармации. Пятигорск, ПятГФА, 2003, 194 с.), рассчитывают количественный состав внутренней сферы, выражающийся формулой [Cu(H2O)2L2]. Эти результаты позволяют считать, что при взаимодействии пектина с ионом меди (II) происходит частичное замещение молекул воды в гидратной оболочке иона меди (II) на мономеры пектина.
Аналогично определению воды в пектинате меди (II), заявляемым способом определяют воду и в других КС.
Предлагаемый способ определения внутрикоординационной воды в КС поясняется следующими примерами конкретного выполнения.
Пример 1. Для получения пектината меди (II) смешивают 100 мл 0,1 моль/л раствора ацетата меди (II) и 1000 мл 0,25% раствора свекловичного пектина, выделившийся осадок зеленого цвета через 2 часа отфильтровывают через бумажный фильтр «красная лента», промывают на фильтре водой до нейтральной реакции промывных вод, высушивают при температуре 70±5°С в течение 3 час.
Анализ осуществляют в 3 стадии.
I. Выявление «высокотемпературного» компонента
Образцы массой около 0,5 г (точная навеска): свекловичный пектин - 0,60802 г, ацетат меди (II) - 0,52315 г, пектинат меди (II) - 0,58683 г подвергают термическому анализу на дериватографе марки «Q-1500» фирмы MOM (Венгрия) с применением различных вариантов: ДТА, ДТГА, ТГА. Дериватограммы записывают в интервале температур 20÷1000°С в динамической атмосфере воздуха при скорости нагревания веществ 10 град/мин, скорости движения бумаги 5 мм/мин, используя в качестве эталона оксид алюминия. Полученные дериватограммы (рисунки 1, 2, 3) сравнивают между собой, особенно отмечая тепловые эффекты в области температур 80-180°С на кривых ДТГА, ДТА. Первый эффект (эндотермический) аналогичен для всех трех веществ, он наблюдается в области температур 80-115°С на кривых ДТГА и 100-120°С на кривых ДТА. Этому эффекту на кривых ТГА соответствует потеря в массе: 17,2% для пектина (рисунок 1), 9,0% для ацетата меди (II) (рисунок 2), 7,4% для пектината меди (II) (рисунок 3), которая относится к потере адсорбционной воды. Данное заключение основано на результатах определения влаги в образцах: после высушивания при температуре 120°С в течение 8 час масса образцов составила: свекловичный пектин - 0,50344 г (потеря влаги 17,2%), ацетат меди (II) - 0,47607 г (потеря влаги 9,0%), пектинат меди (II) - 0,54340 г (потеря влаги 7,4%). В отличие от пектина (рисунок 1) и ацетата меди (II) (рисунок 2), для пектината меди (II) (рисунок 3) обнаружен еще эндотермический эффект при температуре 150-165°С (кривая ДТГА), 155-160°С (кривая ДТА) («высокотемпературный» компонент).
II. Выявление образования гидроксосоединения Из образцов, освобожденных от адсорбционной воды путем высушивания при температуре 120°С в течение 8 час, готовят водные растворы объемом 50 мл с концентрацией: 0,2% раствор свекловичного пектина, 0,1% раствор ацетата меди (II), 0,3% раствор (суспензия) пектината меди (II). Полученные растворы титруют 0,1 моль/л раствором гидроксида натрия на рН-метре марки «рН-340»; в качестве индикаторного электрода используют стеклянный электрод, в качестве электрода сравнения - хлорсеребряный. Результаты титрования растворов исследуемых веществ приведены в таблице 3. Дифференциальным способом (Пономарев В.Д., 1982) в графической системе «(ΔрН/ΔV)-VNaOH, мл» устанавливают точку эквивалентности (рисунки 4, 5, 6). Из представленных данных следует, что при титровании пектина точка эквивалентности наступает при рН 9,14 (соответствует объему титранта 3,4 мл при (ΔрН/ΔV)=28,70), при титровании ацетата меди (II) - рН 6,42 (соответствует объему титранта 2,5 мл при (ΔрН/ΔV)=2,78), а при титровании пектината меди (II) - рН 4,87 (соответствует объему титранта 4,0 мл при (ΔрН/ΔV)=1,62). Следовательно, только пектинат меди (II) при алкалиметрическом титровании имеет точку эквивалентности в кислой среде, что доказывает проявление им кислотных свойств с образованием гидроксосоединения. Для ацетата меди (II) точка эквивалентности наблюдается практически в нейтральной среде, для пектина - в щелочной среде.
Таким образом, выявление по термическим кривым «высокотемпературного» компонента (150-165°С) в пектинате меди (II) и проявление им кислотных свойств с образованием гидроксосоединения в кислой среде (рН 4,87) доказывает наличие молекул воды во внутренней сфере КС, чего не наблюдается для исходных веществ.
III. Определение содержания внутрикоординационной воды и количественного состава пектината меди (II)
Для высушенных при температуре 120°С в течение 8 час исследуемых образцов пересчитывают содержание удаленной воды из % (данные ТГА) в ммоль (таблица 4), после чего строят графическую зависимость «Количество удаленной воды, ммоль - дегидратации, °С» (рисунки 7, 8, 9). Как и ранее (I и II стадии анализа), присутствие внутрикоординационной воды не отмечено ни для пектина (рисунок 7), ни для ацетата меди (II) (рисунок 8). У пектината меди (II) на термогравиграмме (рисунок 9) отчетливо наблюдается «площадка», соответствующая внутрикоординационной воде (температура дегидратации 150-165°С). Согласно рисунку 9, количество этой воды равно 2,42 ммоль (или 0,04356 г). Вычитая из массы высушенного при температуре 120°С в течение 8 час пектината меди (II) (0,54340 г) массу внутрикоординационной воды (0,04356 г), находят массу фрагмента меди (II) с пектином, т.е. 0,49984 г.Учитывая молярное соотношение в пектинате меди (II) иона меди (II) и остатков галактуроновой кислоты (мономера пектина) 1:2 или их массовое соотношение 15,4б%:84,54% (Кайшева Н.Ш., 2003), рассчитывают содержание иона меди (II) - 0,07728 г или 1,217 ммоль и содержание остатков галактуроновой кислоты (молярная масса 175 г/моль) - 0,42256 г или 2,415 ммоль.
Таким образом, состав пектината меди (II), освобожденного от адсорбционной воды, выражается следующими соотношениями ион меди (II): галактуроновая кислота (L): координационная вода:
по массе (в г) - 0,07728:0,42256:0,04356;
по количеству (в ммоль) - 1,217:2,415:2,420 или 1:2:2,
т.е. пектинат меди (II) имеет формулу: [CuL2(H2O)2].
Пример 2. Получение пектината свинца (II) осуществляют аналогично получению пектината меди (II), как указано в примере 1, используя вместо ацетата меди (II) ацетат свинца (II). Пектинат свинца (II) имеет светло-коричневую окраску.
I. Выявление «высокотемпературного» компонента Образцы массой около 0,5 г (точная навеска): свекловичный пектин - 0,57942 г, ацетат свинца (II) - 0,53274 г, пектинат свинца (II) - 0,56358 г подвергают термическому анализу в условиях, аналогичных примеру 1. Характеристика дериватограмм исследуемых образцов приведена в таблице 5. Для всех исследуемых образцов наблюдается эндотермический эффект в области температур 80-115°С на кривых ДТГА и 100-120°С на кривых ДТА. Этому эффекту на кривых ТГА соответствует потеря в массе: 17,2% для пектина, 13,5% для ацетата свинца (II), 9,4% для пектината свинца (II), которая относится к потере адсорбционной воды. Данный вывод подтверждается результатами определения влаги в образцах: после высушивания при температуре 120°С в течение 8 час масса образцов составила: свекловичный пектин - 0,47976 г (потеря влаги 17,2%), ацетат свинца (II) - 0,46082 г (потеря влаги 13,5%), пектинат свинца (II) - 0,51060 г (потеря влаги 9,4%). В отличие от пектина и ацетата свинца (II), для пектината свинца (II) обнаружен «высокотемпературный» компонент, которому соответствует эндотермический эффект при температуре 150-160°С (кривая ДТГА), 150-158°С (кривая ДТА).
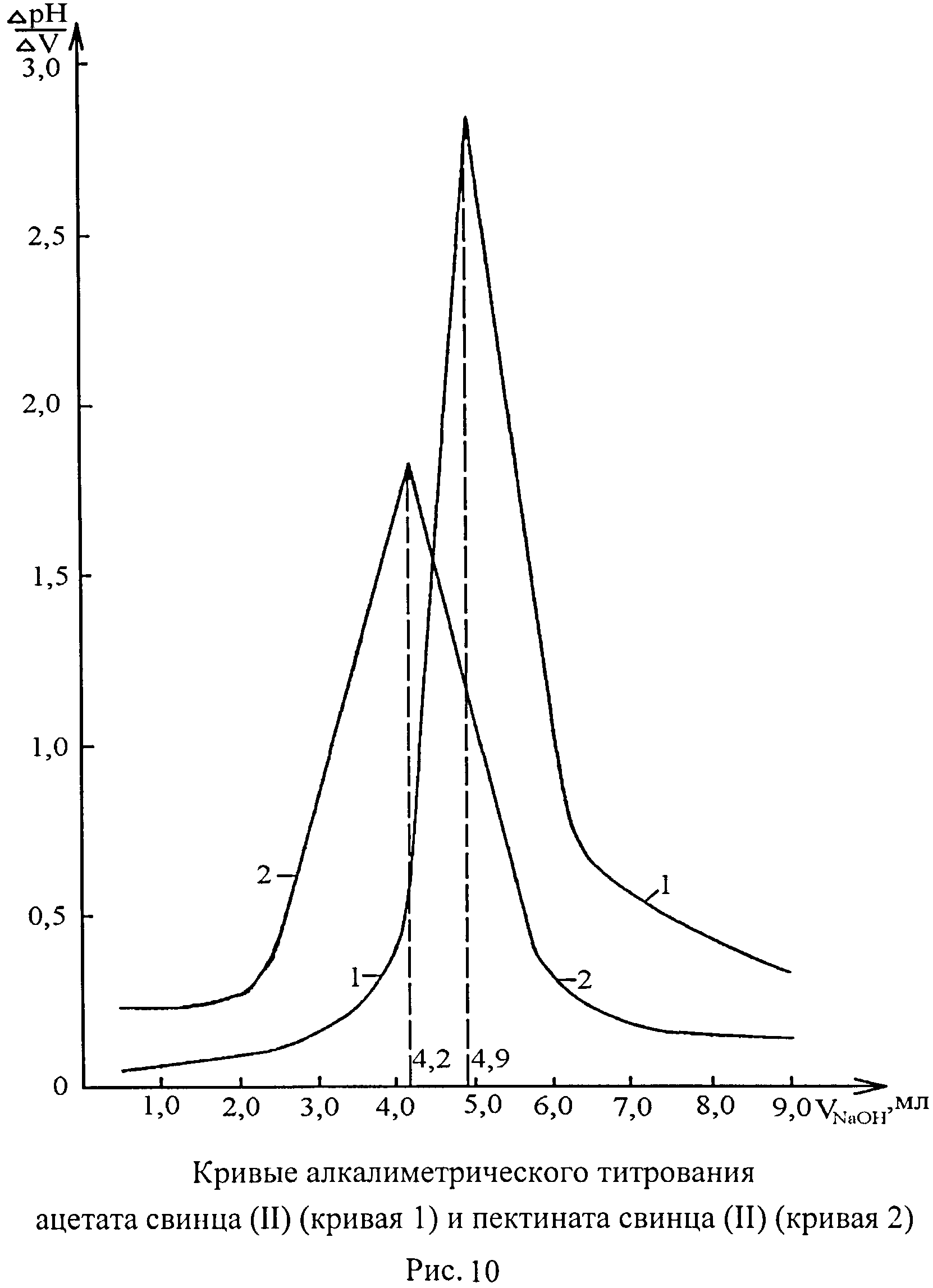
II. Выявление образования гидроксосоединения Поле высушивания при температуре 120°С в течение 8 час исследуемых образцов, готовят их водные растворы объемом 50 мл с концентрацией: 0,2% раствор свекловичного пектина, 0,2% раствор ацетата свинца (II), 0,3% раствор (суспензия) пектината свинца (II). Полученные растворы титруют 0,1 моль/л раствором гидроксида натрия в условиях, аналогичных примеру 1. Кривые алкалиметрического титрования ацетата свинца (II) и пектината свинца (II) представлены на рисунке 10. Если при титровании пектина (рисунок 4) точка эквивалентности наступает при рН 9,14, а при титровании ацетата свинца (II) (рисунок 10, кривая 1) - рН 7,84 (объем титранта 4,9 мл при (ΔрН/ΔV)=2,84), то при титровании пектината свинца (II) (рисунок 10, кривая 2) - рН 4,95 (объем титранта 4,2 мл при (ΔpH/ΔV)=1,83). Следовательно, только пектинат свинца (II) при алкалиметрическом титровании имеет точку эквивалентности в кислой среде, что свидетельствует о проявлении им кислотных свойств с образованием гидроксосоединения. В отличие от пектината свинца (II), исходные вещества имеют точку эквивалентности в щелочной среде.
Таким образом, выявление по термическим кривым «высокотемпературного» компонента (150-160°С) в пектинате свинца (II) и проявление им кислотных свойств с образованием гидроксосоединения в кислой среде (рН 4,95) доказывает наличие молекул воды во внутренней сфере КС, чего не наблюдается для исходных веществ.
III. Определение содержания внутрикоординационной воды и количественного состава пектината свинца (II)
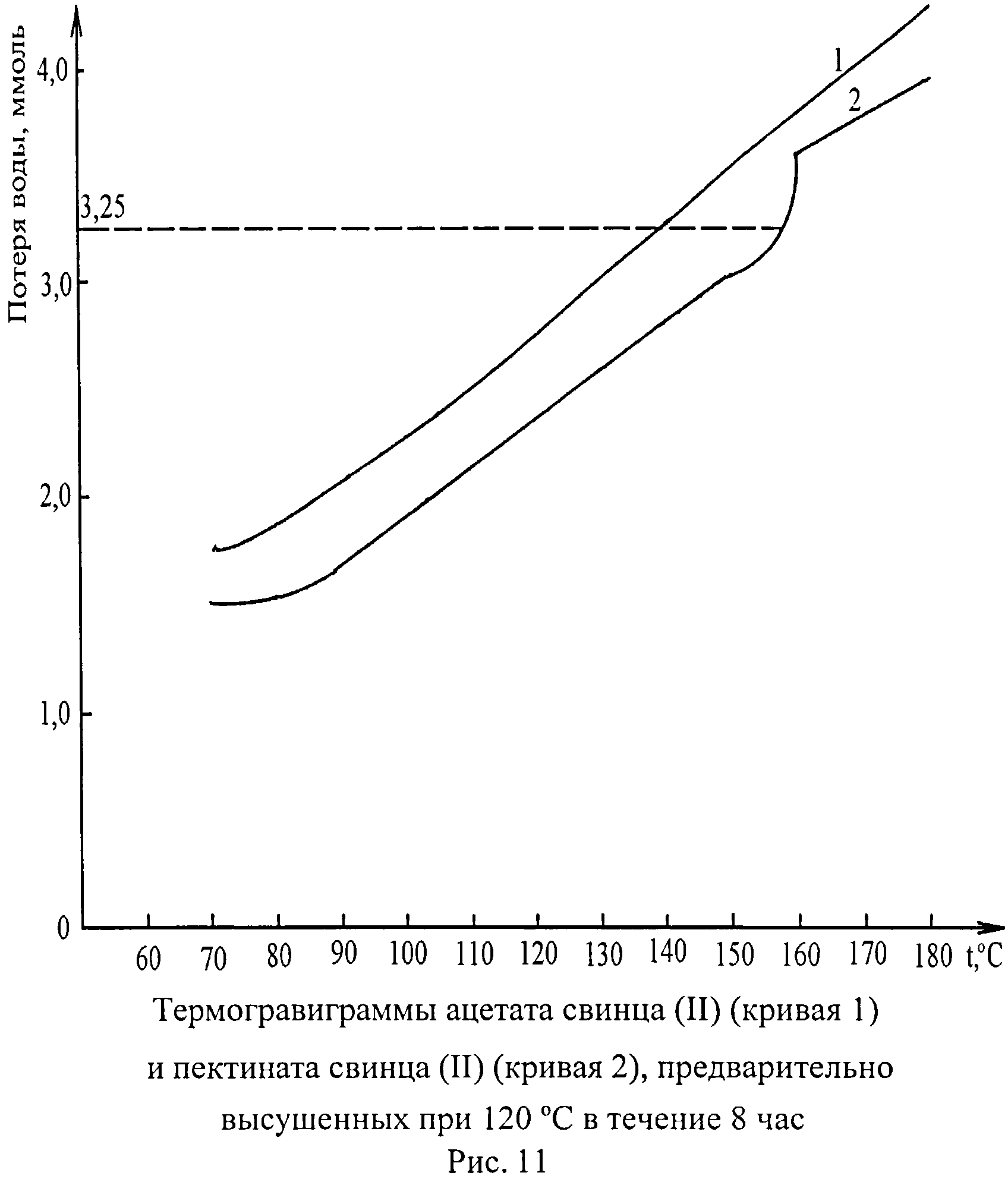
Для высушенных при температуре 120°С в течение 8 час исследуемых образцов по данным ТГА определяют содержание удаленной воды в ммоль и строят термогравиграмму в системе «Количество удаленной воды, ммоль - TДЕГИДРАТАЦИИ, °С» (рисунок 11). Как и на предыдущих стадиях анализа, ни для пектина (рисунок 7), ни для ацетата свинца (II) (рисунок 11, кривая 1) не отмечено присутствие внутрикоординационной воды. В отличие от них, у пектината свинца (II) на термогравиграмме (рисунок 11, кривая 2) обнаружена «площадка», соответствующая внутрикоординационной воде (температура дегидратации 150-160°С). Согласно рисунку 11 (кривая 2), количество этой воды равно 3,25 ммоль (или 0,05850 г).
Вычитая из массы высушенного при температуре 120°С в течение 8 час пектината свинца (II) (0,51060 г) массу внутрикоординационной воды (0,05850 г), находят массу фрагмента свинца (II) с пектином, т.е. 0,45210 г. Учитывая молярное соотношение в пектинате свинца (II) иона свинца (II) и остатков галактуроновой кислоты (мономера пектина) 1:2 или их массовое соотношение 37,19%:62,81% (Кайшева Н.Ш., 2003), рассчитывают содержание иона свинца (II) -0,16814 г или 0,811 ммоль и содержание остатков галактуроновой кислоты (молярная масса 175 г/моль) - 0,28396 г или 1,623 ммоль.
Таким образом, состав пектината свинца (II), освобожденного от адсорбционной воды, выражается следующими соотношениями ион свинца (II): галактуроновая кислота (L): координационная вода:
по массе (в г)- 0,16814:0,28396:0,05850;
по количеству (в ммоль) - 0,811:1,623:3,25 или 1:2:4,
т.е. пектинат свинца (II) имеет формулу: [PbL2(H2O)4].
Таким образом, предлагаемый способ обеспечивает следующий положительный эффект:
1) достоверную идентификацию молекул воды во внутренней сфере КС
Это обеспечивается тем, что сначала определяют температуру, характерную для удаления адсорбционной воды (природу воды, как адсорбционной, подтверждают содержанием влаги в образце) и удаления внутрикоординационной воды (с характерной температурой дегидратации ≥150°С), затем при соответствующей температуре удаляют адсорбционную воду, оставляя в КС внутрикоординационную воду. Подтверждением наличия воды как лиганда в КС является образование при алкалиметрическом титровании гидроксосоединения в кислой среде, что обусловлено усилением кислотных свойств молекул внутрикоординационной воды за счет сильного поляризующего действия на них катионов металлов. Если бы молекулы воды не были бы связаны с ионом металла во внутренней сфере, а находились бы вне ее, то поляризующее действие на них иона металла проявлялось бы слабо и не наблюдались бы их кислотные свойства при взаимодействии со щелочью, приводящие к образованию гидроксокомплекса. Таким образом, в предлагаемом способе идентификация молекул воды, как внутрисферной, осуществляется по двум признакам: температуре дегидратации ≥150°С (на термических кривых) и значению рН<5,0 в точке эквивалентности при алкалиметрическом титровании. Эти признаки не характерны другим структурным компонентам КС.
2) количественное определение внутрикоординационной воды в КС
Это обеспечивается тем, что по характерным «площадкам», свойственным для внутрикоординационной воды, на термогравиграммах определяют количество этой воды во взятой навеске КС;
3) выведение формулы КС
Установленное количество внутрикоординационной воды в определенной навеске КС с учетом содержания других компонентов позволяет вывести формулу (молярный состав) КС. Знание формулы КС имеет огромное теоретическое значение в координационной химии при исследовании структуры КС и практическое значение в фармации при определении терапевтических доз лекарственных средств.
4) заявляемый способ отличается хорошей воспроизводимостью и сопоставимостью результатов определения, а также упрощенностью, как с точки зрения подготовки образцов к анализу (не требуется изготовления пленок), так и с точки зрения условий анализа (не требуется создания вакуума).
|
|
|
|
|