Результат интеллектуальной деятельности: ЗАМЕЩЕННЫЕ (2R,3R,5R)-3-ГИДРОКСИ-(5-ПИРИМИДИН-1-ИЛ)ТЕТРАГИДРОФУРАН-2-ИЛМЕТИЛ АРИЛ ФОСФОРАМИДАТЫ
Вид РИД
Изобретение
Настоящее изобретение относится к новым замещенным эфирам фосфорамидной кислоты и их использованию в качестве средства для лечения вирусных заболеваний. Эти соединения являются ингибиторами репликации РНК-зависимой вирусной РНК и являются полезными в качестве ингибиторов полимеразы NS5B вируса гепатита C и для лечения гепатита С. Вирус гепатита С, наряду с другими важными патогенами человека, такими как вирус желтой лихорадки, вирус West Nile, вирус Денги (Dengue) и вирус гепатита GBV-C, относится к Флавивирусам (genus Flaviviridae).
Известно, что NS5B представляет собой белок вируса гепатита [Vincent Soriano et al., Hepatitis C therapy with HCV NS5B polymerase inhibitors, Expert Opinion on Pharmacotherapy, June 2013, Vol.14, No.9, Pages 1161-1170]. Разработка антивирусных лекарственных средств для вируса гепатита C (ВГС) идет все более быстрым темпом. Среди ингибиторов полимеразы ВГС, софосбувир позиционируется как уникальный компаньон для рибавирина в качестве терапии для большинства генотипов ВГС 2 или 3.
Современное лечение хронического гепатита C, основанное на комбинации пегилированного интерферона и рибавирина, является эффективеным только у 50% больных. Специальная таргетная противовирусная терапия представляет собой перспективный подход к искоренению инфекции. Обзор [Legrand-Abravanel F, Nicot F, Izopet J. New NS5B polymerase inhibitors for hepatitis C. Expert Opin Investig Drugs. 2010 Aug; 19(8):963-75] уделяет основное внимание прогрессу в отношении развития ингибиторов полимеразы вируса гепатита C, которые прошли клинические исследования в последние годы. Нуклеоз(т)идные аналоги нацелены на активный центр полимеразы ВГС и действует как агенты, обрывающие цепь. Они обладают высокой активностью в отношении всех генотипов. Ненуклеозидные ингибиторы достигают ингибирования полимеразы за счет связывания с одним из, по меньшей мере, четырех аллостерических энзимных сайтов. Большинство из них имеют генотип-специфическую активность и они могут быстро выбирать резистентные штаммы если репликации ВГС не полностью подавлена. Тем не менее, они предоставляют дополнительные возможности для лечения инфицированных пациентов. Ингибиторы NS5B полимеразы будут являться неотъемлемой частью более эффективной анти-ВГС терапии в комбинации с интерфероном или с другими противовирусными агентами прямого действия.
В последнее десятилетие, интенсивные усилия были сосредоточены на открытии обоих: нуклеоз(т)идных и ненуклеозидных ингибиторов полимеразы NS5B ВГС. Эти усилия привели к некоторым перспективным агентам, проходящим стадию клинического исследования. Обзор [Watkins WJ, Ray AS, Chong LS. HCV NS5B polymerase inhibitors. Curr Opin Drug Discov Devel. 2010 Jul; 13(4):441-65] прослеживает историю оптимизации химических серий, которые привели к развитию клинических кандидатов, и обобщает последние исследования в этой области с акцентом на клинической эффективности и влиянии на будущие комбинированные исследования.
Примерами лекарственных кандидатов могут служить нуклеозидные ингибиторы полимеразы NS5B ВГС: PSI-7977 фирмы Фармасет (США) и NM283 (Valopicitabine) фирмы Айденикс (США) и др. [М.J. Sofia, D. Bao, W. Chang, J. Du, D. Nagarathnam, S. Rachakonda, P.G. Reddy, B.S. Ross, P. Wang, H.-R. Zhang, S. Bansal, C. Espiritu, М. Keilman, A.М. Lam, H.М.М. Steuer, Congrong Niu, М.J. Otto, P.A. Furman. Discovery of a β-D-20-Deoxy-20-r-fluoro-20-β-C-methyluridine Nucleotide Prodrug (PSI-7977) for the Treatment of Hepatitis С Virus. J. Med. Chem. 2010, 53, 7202-7218; Pat. US 7964580 B2; Pat US 8334270 B2.].
До настоящего времени гепатит C является серьезной проблемой здравоохранения. Он приводит к хроническому заболеванию печени, переходящему к циррозу печени и гепатоцеллюлярной карциноме.
В этой связи поиск новых высокоэффективных противофлавивирусных лекарственных препаратов в настоящее время по-прежнему является одним из основных направлений создания новых фармакологических средств для лечения широкого и разнообразного круга вирусных инфекций, в том числе ВГС. Поэтому до настоящего времени является актуальным синтез новых соединений и использование их в качестве противовирусных активных компонентов для фармацевтических композиций и лекарственных средств, в том числе ВГС.
Ниже приведены определения терминов, которые использованы в описании этого изобретения:
«Алкил» означает алифатическую углеводородную линейную или разветвленную группу с 1-12 атомами углерода в цепи. Разветвленная означает, что алкильная цепь имеет один или несколько «низших алкильных» заместителей. Алкил может иметь один или несколько одинаковых или различных заместителей («алкильных заместителей») включая галоген, алкенилокси, циклоалкил, арил, гетероарил, гетероциклил, ароил, циано, гидрокси, алкокси, карбокси, алкинилокси, аралкокси, арилокси, арилоксикарбонил, алкилтио, гетероарилтио, аралкилтио, арилсульфонил, алкилсульфонилгетероаралкилокси, аннелированный гетероарилциклоалкенил, аннелированный гетероарилциклоалкил, аннелированный гетероарилгетероцикленил, аннелированный гетероарил гетероциклил, аннелированный арилциклоалкенил, аннелированный арилциклоалкил, аннелированный арилгетероцикленил, аннелированный арилгетероциклил, алкоксикарбонил, аралкоксикарбонил, гетероаралкилоксикарбонил или Rk aRk+1 aN-, Rk aRk+1 aNC(=O)-, Rk aRk+1 aNC(=S)-, Rk aRk+1 aNSO2-, где Rk a и Rk+1 a независимо друг от друга представляют собой «заместители амино группы», значение которых определено в данном разделе, например, атом водорода, алкил, арил, аралкил, гетероаралкил, гетероциклил или гетероарил, или Rk a и Rk+1 a вместе с атомом N, с которым они связаны, образуют через Rk a и Rk+1 a 4-7 членный гетероциклил или гетеоцикленил. Предпочтительными алкильными группами являются метил, трифторметил, циклопропилметил, циклопентилметил, этил, н-пропил, изо-пропил, н-бутил, трет-бутил, н-пентил, 3-пентил, метоксиэтил, карбоксиметил, метоксикарбонилметил, этоксикарбонилметил, бензилоксикарбонилметил и пиридилметилоксикарбонилметил. Предпочтительными «алкильными заместителями» являются циклоалкил, арил, гетероарил, гетероциклил, гидрокси, алкокси, алкоксикарбонил, аралкокси, арилокси, алкилтио, гетероарилтио, аралкилтио, алкилсульфонил, арилсульфонил, алкоксикарбонил, аралкоксикарбонил, гетероаралкилоксикарбонил или Rk aRk+1 aN-, Rk aRk+1 aNC(=O)-, аннелированный арилгетероцикленил, аннелированный арилгетероциклил.
«Алкилокси (алкокси)» означает CnH2n+1O- группу, в которой алкил определен в данном разделе. Предпочтительным алкилокси группами являются метокси, этокси, н-пропокси, изо-пропокси и н-бутокси.
«Арил» означает ароматическую моноциклическую или полициклическую систему, включающую от 6 до 14 атомов углерода, преимуществено от 6 до 10 атомов углерода. Арил может содержать один или более «заместителей циклической системы», которые могут быть одинаковыми или разными. Представителями арильных групп являются фенил, замещенный фенил, нафтил, и замещенный нафтил. Арил может быть анелирован с неароматической циклической системой или гетероциклом.
«Арилокси» означает арил-O- группу, в которой значение арил определено в данном разделе.
Представителями арилокси групп являются фенокси и 2-нафтилокси.
«Гидрат» означает стехиометрические или нестехиометрические композиции соединений или их солей с водой.
«Заместитель» означает химический радикал, который присоединяется к скэффолду (фрагменту), например, «заместитель алкильный», «заместитель аминогруппы», «заместитель карбамоильный», «заместитель циклической системы».
«Активный компонент» (лекарственное вещество, лекарственная субстанция, drug-substance) означает физиологически активное вещество синтетического или иного (биотехнологического, растительного, животного, микробного и прочего) происхождения, обладающее фармакологической активностью и являющееся активным началом фармацевтической композиции, используемой для производства и изготовления лекарственного препарата (средства).
«Лекарственное средство (препарат)» - вещество (или смесь веществ в виде фармацевтической композиции) в виде таблеток, капсул, инъекций, мазей и других готовых форм, предназначенное для восстановления, исправления или изменения физиологических функций у человека и животных, а также для лечения и профилактики болезней, диагностики, анестезии, контрацепции, косметологии и прочего.
«Низший алкил» означает линейный или разветвленный алкил с 1-4 атомами углерода.
«Терапевтический коктейль» представляет одновременно администрируемую комбинацию двух и более лекарственных препаратов, обладающих различным механизмом фармакологического действия и направленных на различные биомишени, участвующие в патогенезе заболевания.
«Фармацевтическая композиция» обозначает композицию, включающую в себя соединение формулы 1 или 2 и, по крайней мере, один из компонентов, выбранных из группы, состоящей из фармацевтически приемлемых и фармакологически совместимых наполнителей, растворителей, разбавителей, носителей, вспомогательных, распределяющих и воспринимающих средств, средств доставки, таких как консерванты, стабилизаторы, наполнители, измельчители, увлажнители, эмульгаторы, суспендирующие агенты, загустители, подсластители, отдушки, ароматизаторы, антибактериальные агенты, фунгициды, лубриканты, регуляторы пролонгированной доставки, выбор и соотношение которых зависит от природы и способа назначения и дозировки. Примерами суспендирующих агентов являются этоксилированный изостеариловый спирт, полиоксиэтилен, сорбитол и сорбитовый эфир, микрокристаллическая целлюлоза, метагидроксид алюминия, бентонит, агар-агар и трагакант, а также смеси этих веществ. Защита от действия микроорганизмов может быть обеспечена с помощью разнообразных антибактериальных и противогрибковых агентов, например, таких как, парабены, хлорбутанол, сорбиновая кислота и подобные им соединения. Композиция может включать также изотонические агенты, например, сахара, хлористый натрий и им подобные. Пролонгированное действие композиции может быть обеспечено с помощью агентов, замедляющих абсорбцию активного начала, например, моностеарат алюминия и желатин. Примерами подходящих носителей, растворителей, разбавителей и средств доставки являются вода, этанол, полиспирты, а также их смеси, растительные масла (такие, как оливковое масло) и инъекционные органические сложные эфиры (такие, как этилолеат). Примерами наполнителей являются лактоза, молочный сахар, цитрат натрия, карбонат кальция, фосфат кальция и им подобные. Примерами измельчителей и распределяющих средств являются крахмал, алгиновая кислота и ее соли, силикаты. Примерами лубрикантов являются стеарат магния, лаурилсульфат натрия, тальк, а также полиэтиленгликоль с высоким молекулярным весом. Фармацевтическая композиция для перорального, сублингвального, трансдермального, внутримышечного, внутривенного, подкожного, местного или ректального введения активного начала, одного или в комбинации с другим активным началом, может быть введена животным и людям в стандартной форме введения, или в виде смеси с традиционными фармацевтическими носителями. Пригодные стандартные формы введения включают пероральные формы, такие как таблетки, желатиновые капсулы, пилюли, порошки, гранулы, жевательные резинки и пероральные растворы или суспензии, сублингвальные и трансбуккальные формы введения, аэрозоли, имплантаты, местные, трансдермальные, подкожные, внутримышечные, внутривенные, интраназальные или внутриглазные формы введения и ректальные формы введения.
«Фармацевтически приемлемая соль» означает относительно нетоксичные органические и неорганические соли кислот и оснований, заявленных в настоящем изобретении. Эти соли могут быть получены in situ в процессе синтеза, выделения или очистки соединений или приготовлены специально. В частности, соли оснований могут быть получены специально, исходя из очищенного свободного основания заявленного соединения и подходящей органической или неорганической кислоты. Примерами полученных таким образом солей являются гидрохлориды, гидробромиды, сульфаты, бисульфаты, фосфаты, нитраты, ацетаты, оксалаты, валериаты, олеаты, пальмитаты, стеараты, лаураты, бораты, бензоаты, лактаты, тозилаты, цитраты, малеаты, фумараты, сукцинаты, тартраты, мезилаты, малонаты, салицилаты, пропионаты, этансульфонаты, бензолсульфонаты, сульфаматы и им подобные (Подробное описание свойств таких солей дано в Berge S.M., et al., "Pharmaceutical Salts" J. Pharm. Sci. 1977, 66: 1-19). Соли заявленных кислот также могут быть специально получены реакцией очищенной кислоты с подходящим основанием, при этом могут быть синтезированы соли металлов и аминов. К металлическим относятся соли натрия, калия, кальция, бария, цинка, магния, лития и алюминия, наиболее желательными из которых являются соли натрия и калия. Подходящими неорганическими основаниями, из которых могут быть получены соли металлов, являются гидроксид, карбонат, бикарбонат и гидрид натрия, гидроксид, карбонат и бикарбонат калия, гидроксид лития, гидроксид кальция, гидроксид магния, гидроксид цинка. В качестве органических оснований, из которых могут быть получены соли заявленных кислот, выбраны амины и аминокислоты, обладающие достаточной основностью, чтобы образовать устойчивую соль, и пригодные для использования в медицинских целях (в частности, они должны обладать низкой токсичностью). К таким аминам относятся аммиак, метиламин, диметиламин, триметиламин, этиламин, диэтиламин, триэтиламин, бензиламин, дибензиламин, дициклогексиламин, пиперазин, этилпиперидин, трис(гидроксиметил)аминометан и подобные им. Кроме того, для солеобразования могут быть использованы гидроокиси тетраалкиламмония, например, такие как, холин, тетраметиламмоний, тетраэтиламмоний и им подобные. В качестве аминокислот могут быть использованы основные аминокислоты -лизин, орнитин и аргинин.
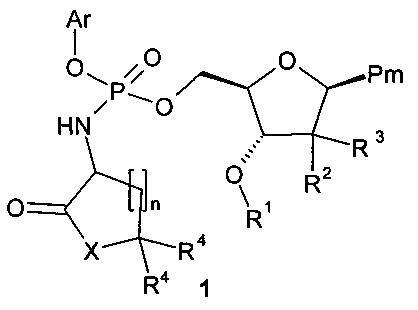
Предметом настоящего изобретения являются соединения, представляющие собой новые замещенные эфиры амидофосфорной кислоты - (2R,3R,5R)-3-гидрокси-(5-пиримидин-1-1-ил)тетрагидрофуран-2-илметил арил фосфорамидат общей формулы 1, или их стереоизомеры, или фармацевтически приемлемые соли,
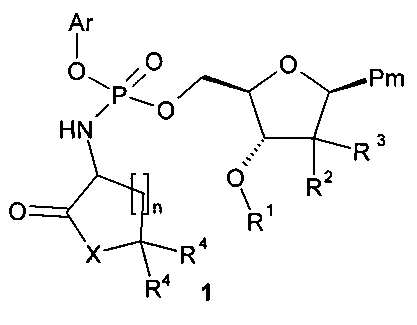
где:
R1 представляет собой водород, (СН3)2[(СН3)3С]Si, C2-C6ацил, необязательно замещенный бензилоксигруппой, NR5R6 группой, в которой R5 и R6 представляют собой независимо водород или С1-С4 алкил; 1-пиррол-2-илкарбонил, пиперидин-3-илкарбонил или пиперидин-4-илкарбонил;
R2 и R3 представляют собой F или R2 представляет собой F или ОН и R3 представляет собой СН3;
R4 представляет собой водород или метил;
Ar представляет собой фенил, пиридил или нафтил, где фенил, пиридил или нафтил являются необязательно замещенными по крайней мере одним из: С1-3алкил, С2-4алкенил, С2-4алкинил, С1-3алкокси, F, Сl, Br, I, нитро, циано, -N(C1-3алкил)2;
Pm представляет собой 2,4-диоксо-3,4-дигидро-2Н-пиримидин-1-ил или 4-(4-амино-2-оксо-2Н-пиримидин-1-ил), в которых амино группа является необязательно замещенной 1-пиррол-2-илкарбонилом, пиперидин-3-илкарбонилом, пиперидин-4-илкарбонилом или радикалом C(O)R8, где R8 представляет собой C1-C4алкил, необязательно замещенный NR6R7 группой, где R6 и R7 представляют собой независимо водород или С1-С4алкил; C1-3алкокси, необязательно замещенную фенилом;
X представляет собой О или N-R9, где R9 представляет собой C1-C4алкил, необязательно замещенный ОН или ОСН3;
n=1,2 или 3.
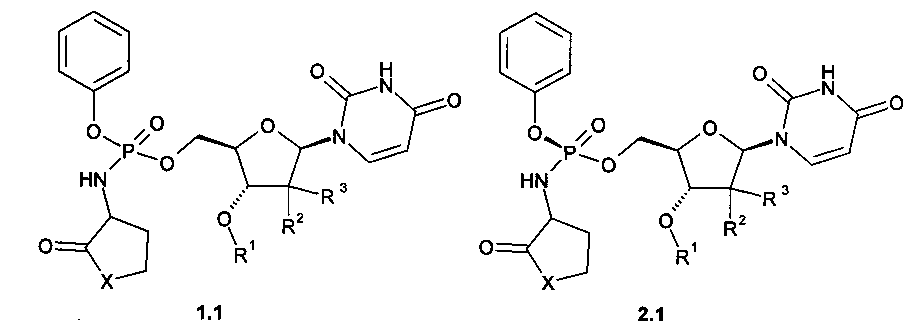
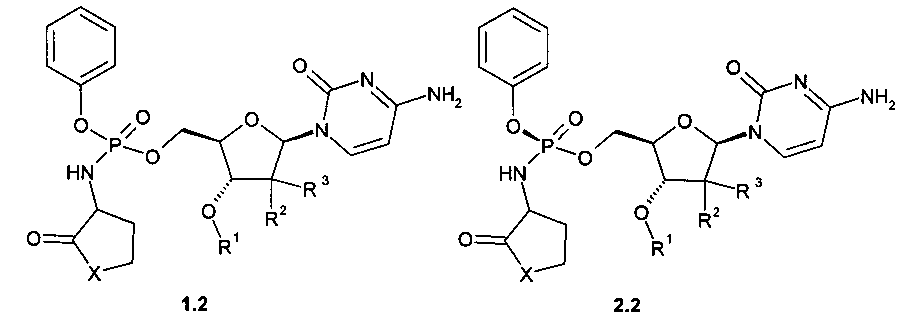
Предпочтительными новыми замещенными эфирами амидофосфорной кислоты являются соединения общей формулы 1.1 или общей формулы 2.1, или их стереоизомер, или фармацевтически приемлемая соль,
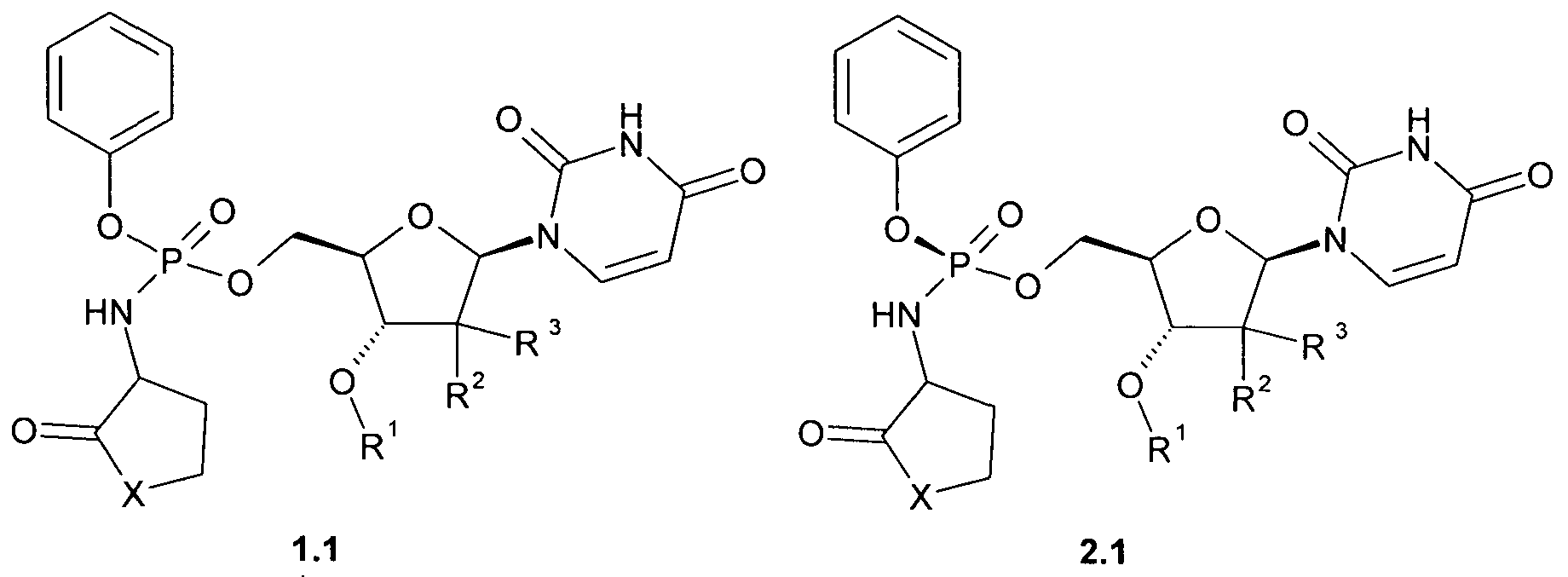
где R1, R2, R3 и Х имеют вышеуказанное значение.
Предпочтительными новыми замещенными эфирами амидофосфорной кислоты являются соединения общей формулы 1.2 или общей формулы 2.2, или их стереоизомер, или фармацевтически приемлемая соль,
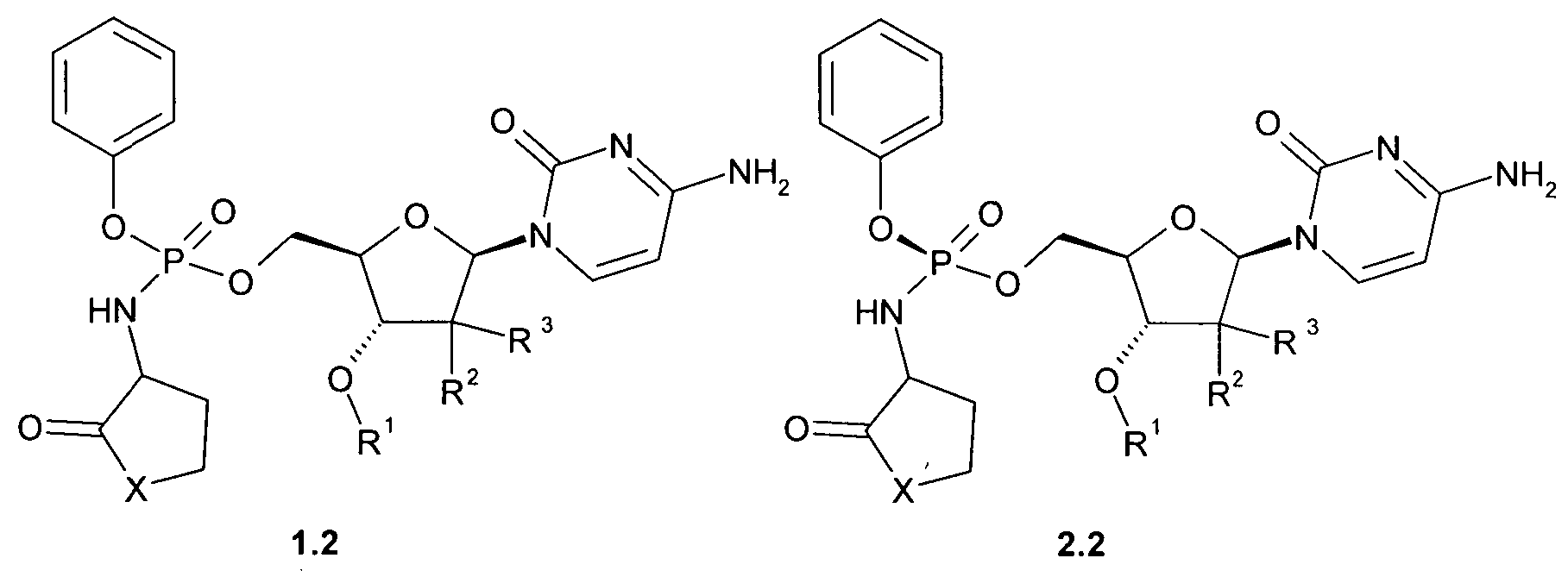
где R1, R2, R3 и X имеют вышеуказанное значение.
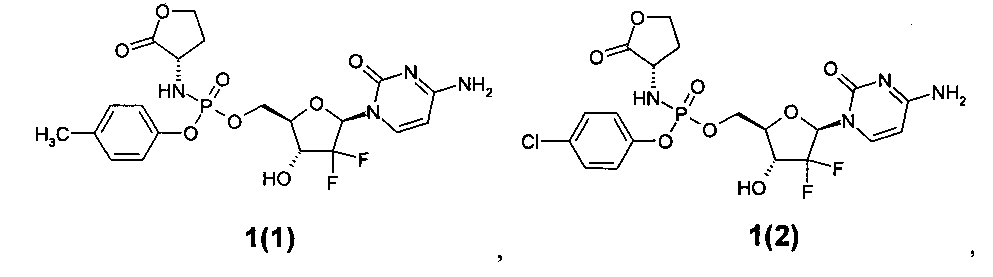
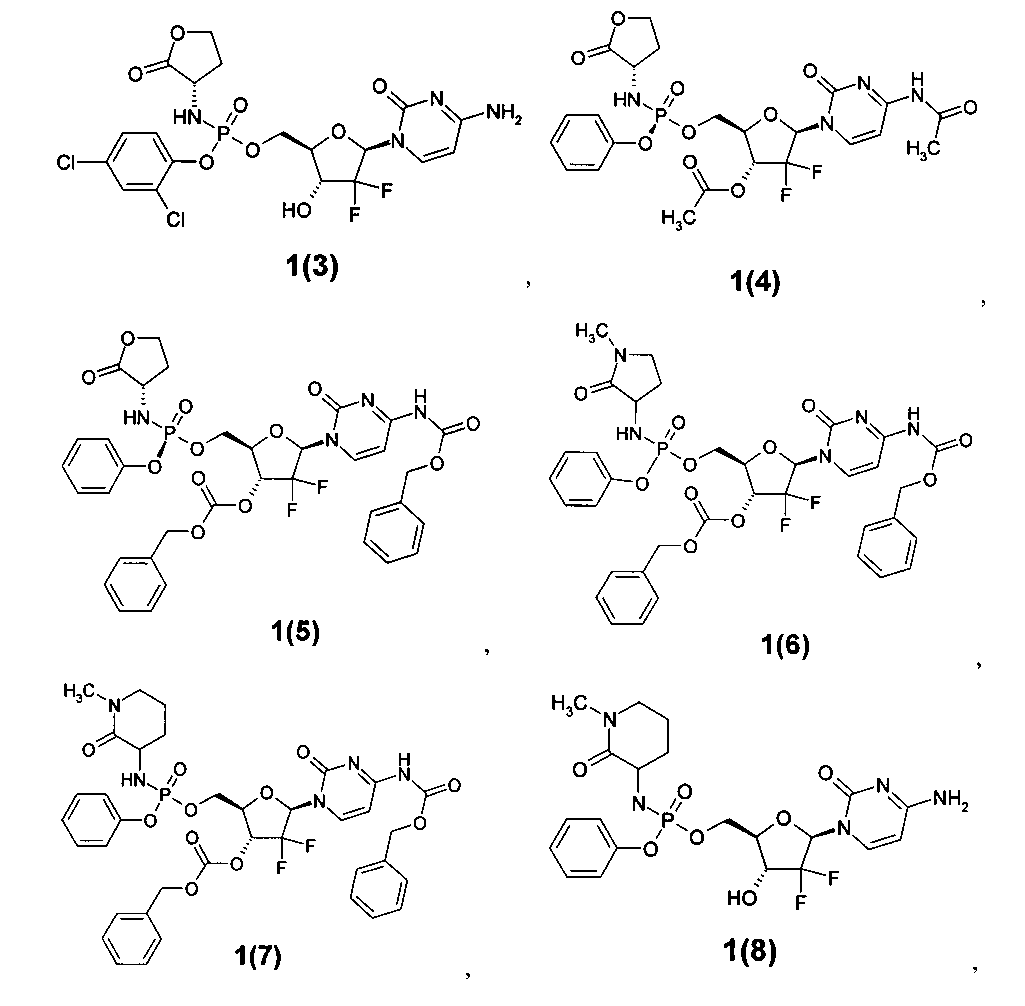
Более предпочтительными новыми замещенными эфирами амидофосфорной кислоты являются соединения общей формулы 1, выбранные из группы, включающей: ((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил п-толил (S)-2-оксо-тетрагидрофуран-3-ил-фосфорамидат 1(1),
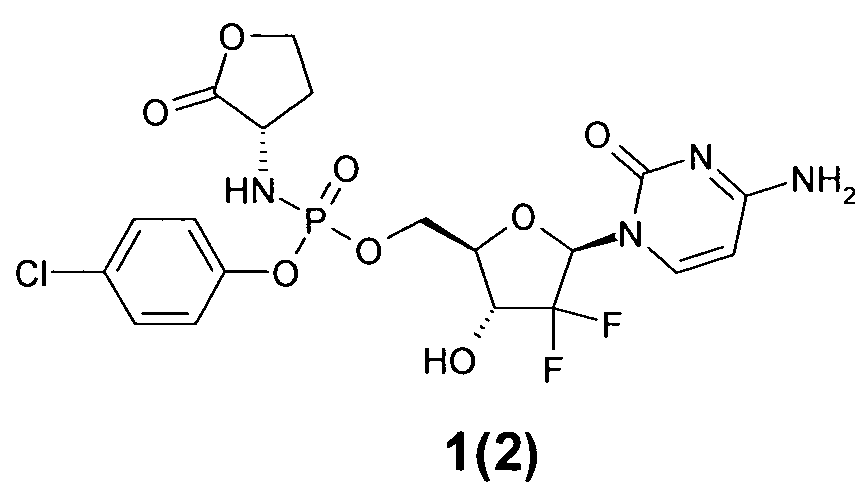
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил 4-хлорфенил (S)-2-оксо-тетрагидрофуран-3-ил-фосфорамидат 1(2),
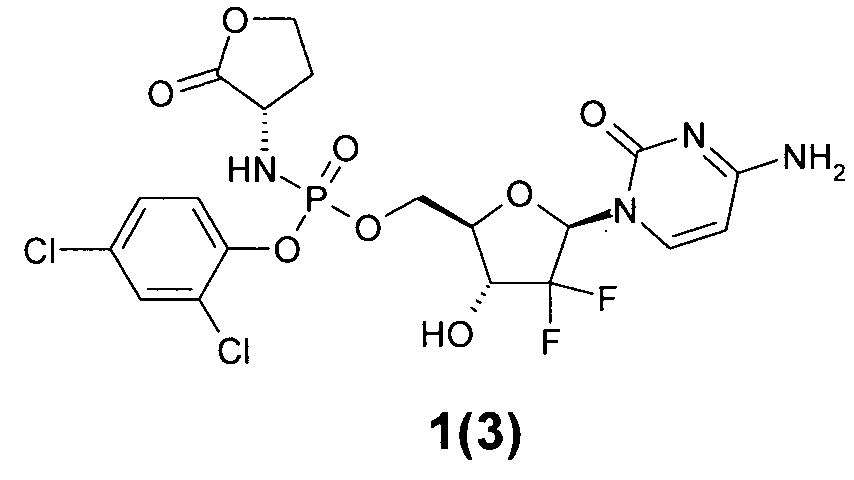
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил 2,4-дихлорфенил (S)-2-оксо-тетрагидрофуран-3-ил-фосфорамидат 1(3),
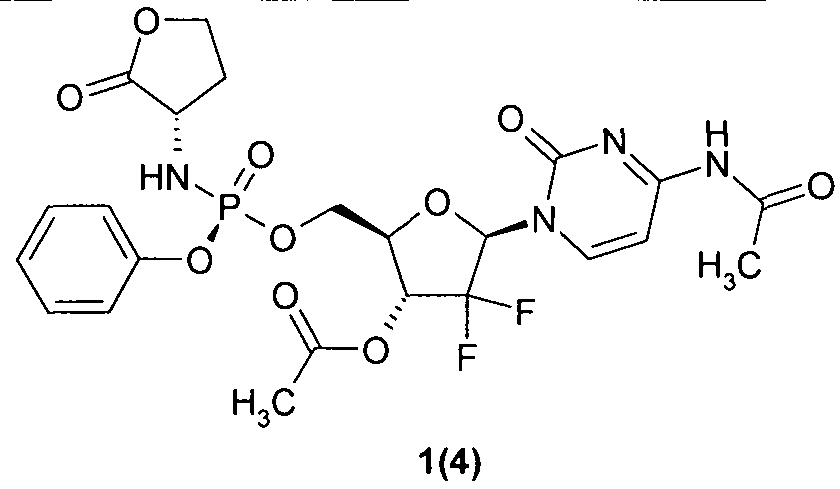
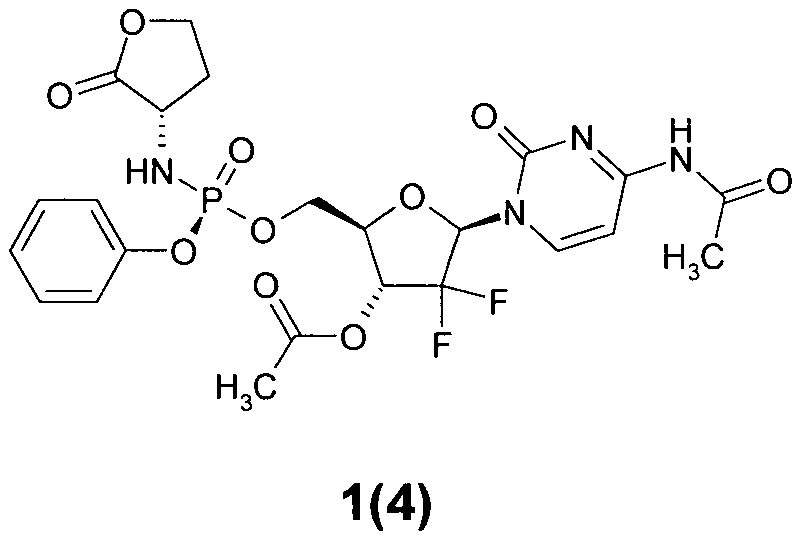
(2R,3R,5R)-5-(4-ацетамидо-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-2-(((S)-(S)-2-оксотетрагидрофуран-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-3-ил ацетат 1(4),
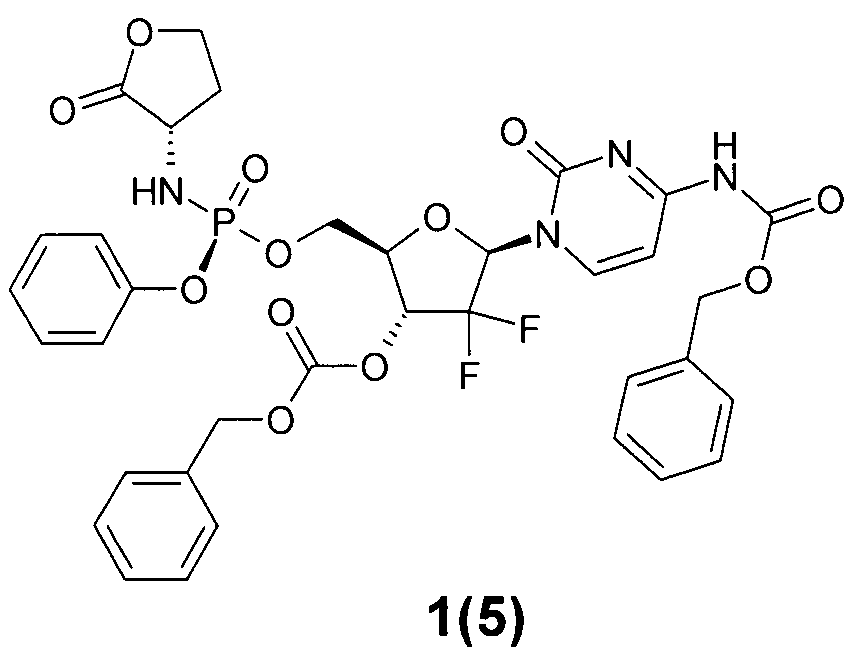
бензил 1-(2R,4R,5R)-4-(бензилоксикарбонилокси)-3,3-дифтор-5-(((S)-((S)-(2-оксотетрагидрофуран-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-2-ил)-2-оксо-1,2-дигидропиримидин-4-илкарбамат 1(5),
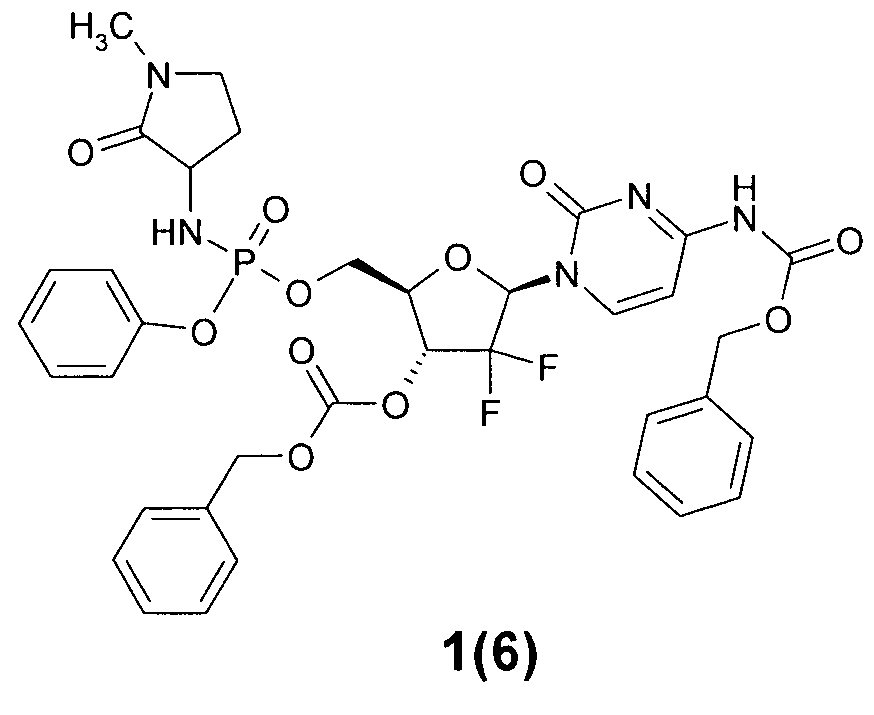
бензил 1-((2R,4R,5R)-4-(бензилоксикарбонилокси)-3,3-дифтор-5-(((1-метил-2-оксопирролидин-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-2-ил)-2-оксо-1,2-дигидропиримидин-4-илкарбамат 1(6),
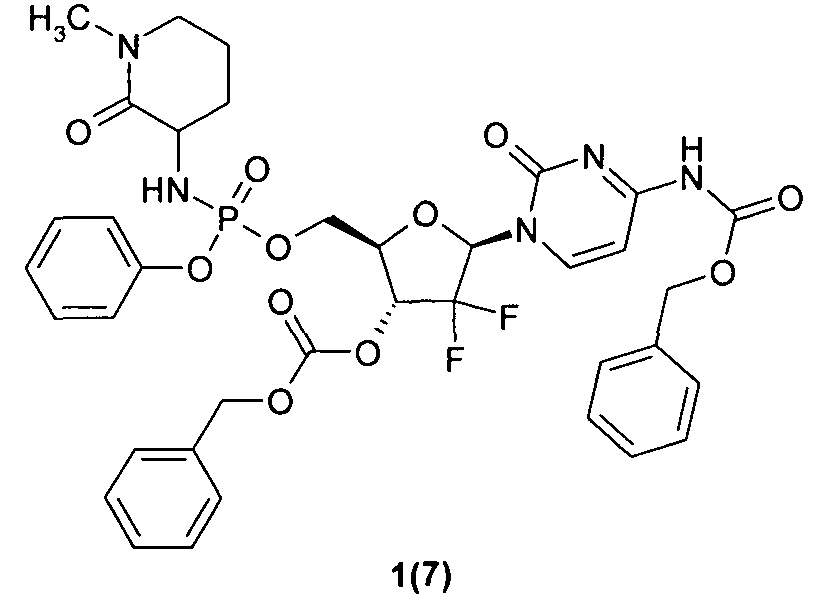
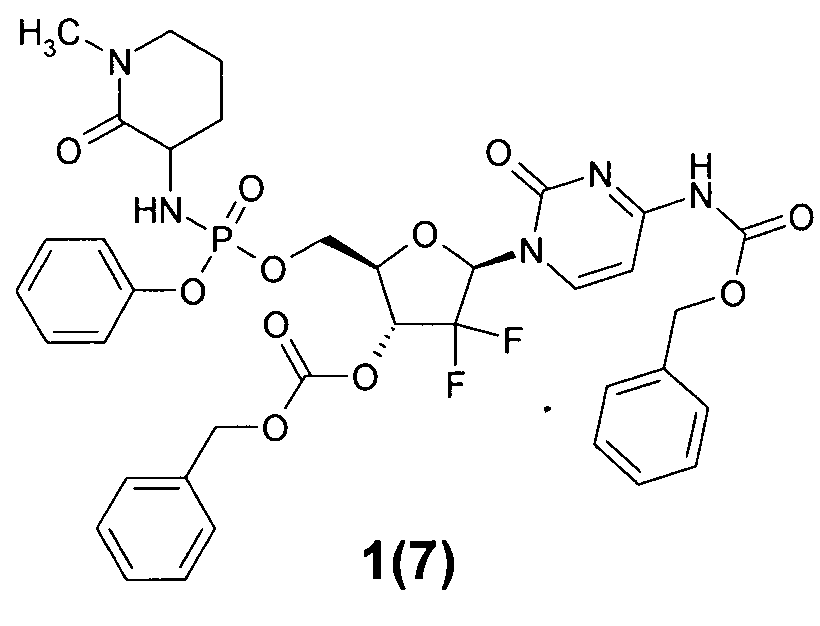
бензил 1-((2R,4R,5R)-4-(бензилоксикарбонилокси)-3,3-дифтор-5-(((1-метил-2-оксопиперидин-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-2-ил)-2-оксо-1,2-дигидропиримидин-4-илкарбамат 1(7),
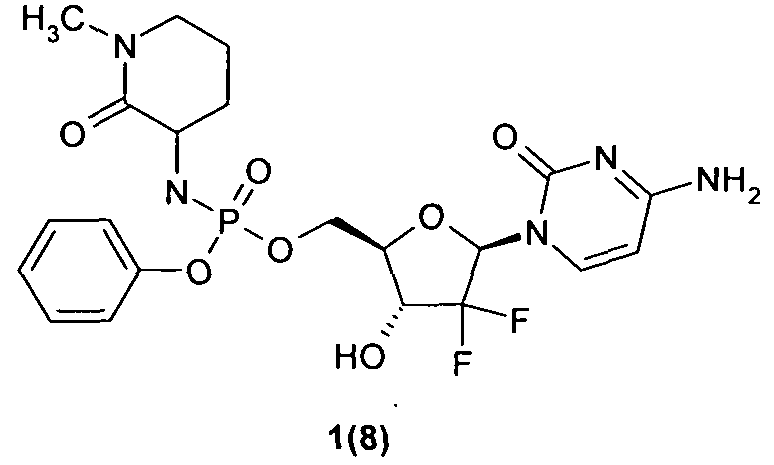
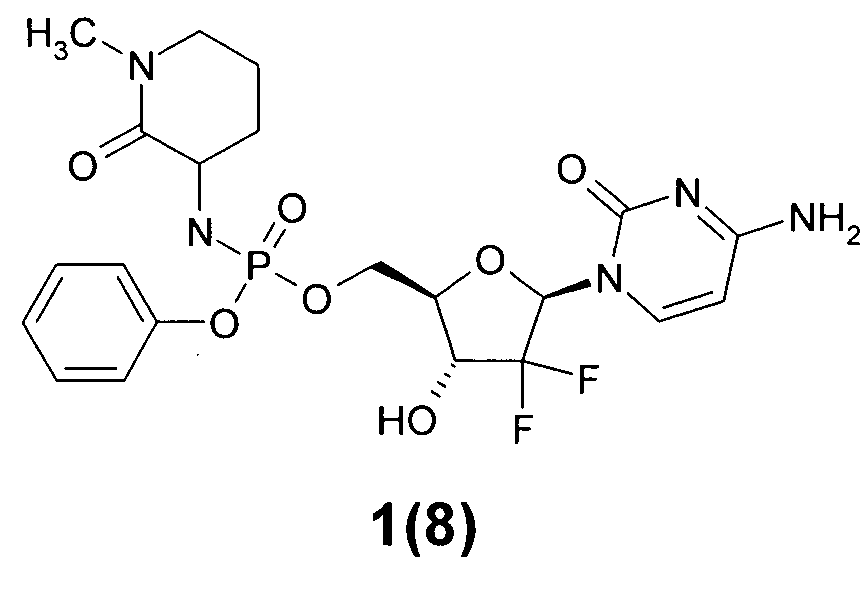
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопиперидин-3-илфосфорамидат 1(8),
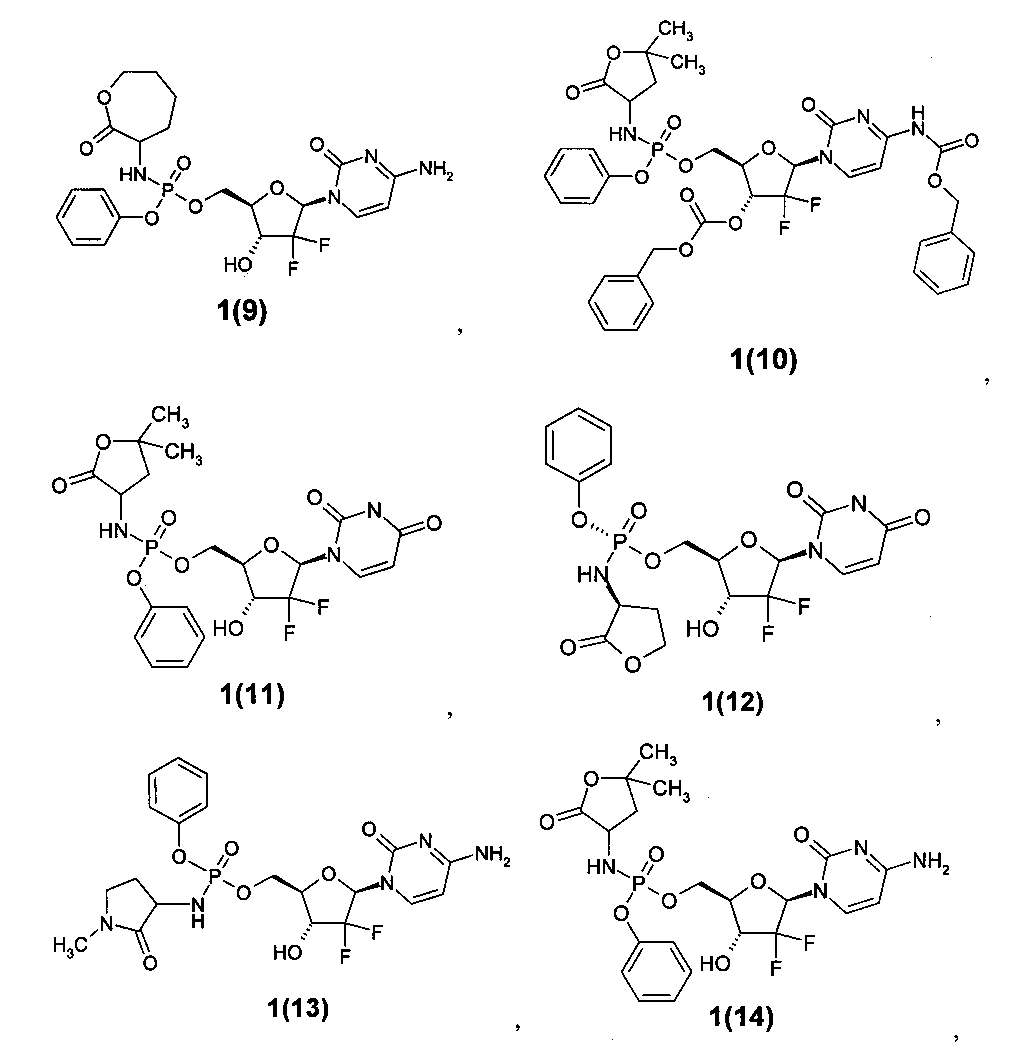
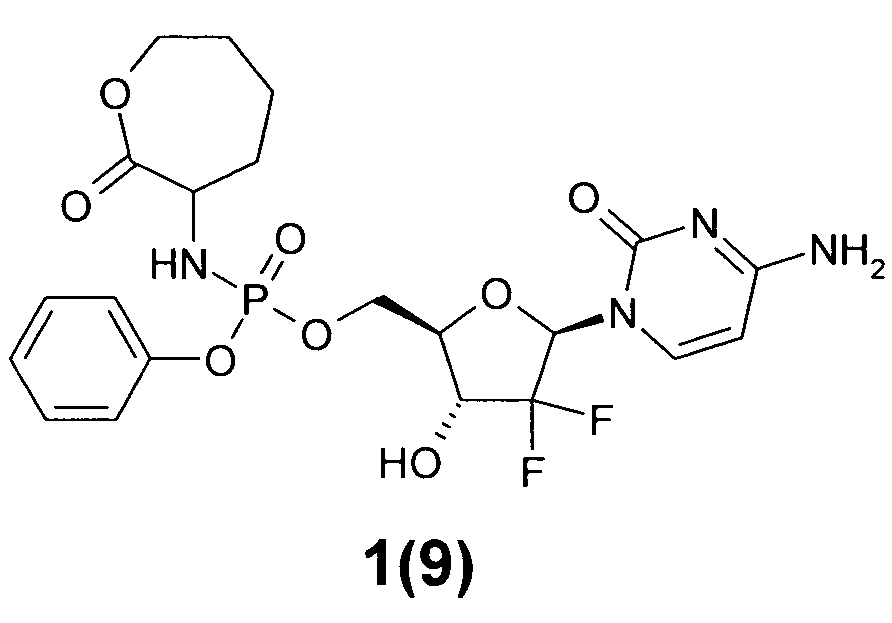
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 2-оксооксепан-3-ил-фосфорамидат 1(9),
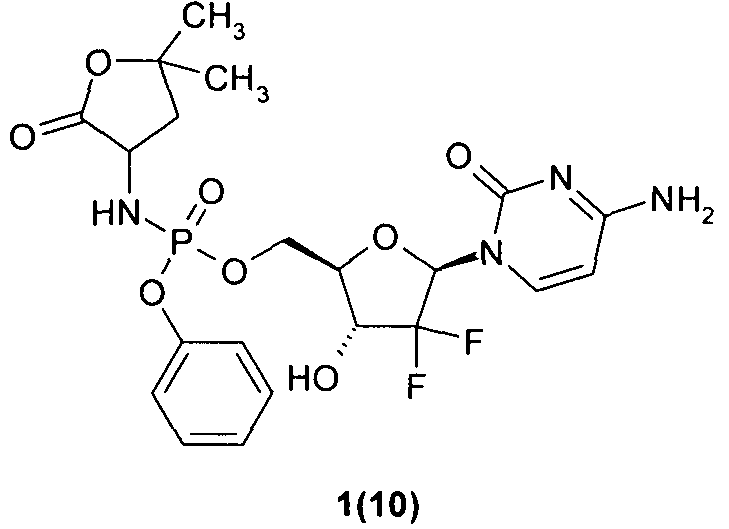
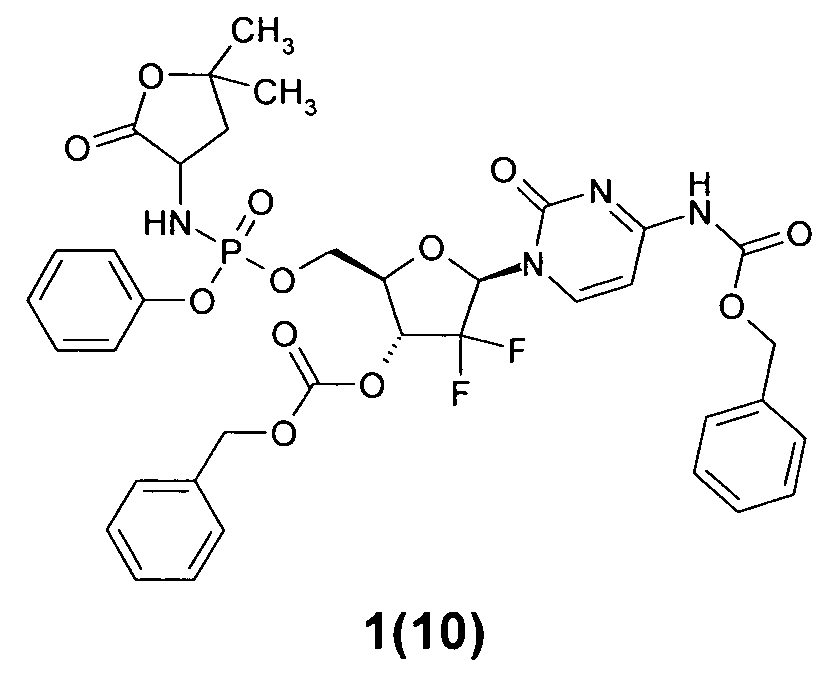
бензил 1-((2R,4R,5R)-4-(бензилоксикарбонилокси)-5-(((5,5-диметил-2-оксотетрагидрофуран-3-иламино)(фенокси)фосфорилокси)метил)-3,3-дифтортетрагидрофуран-2-ил)-2-оксо-1,2-дигидропиримидин-4-илкарбамат 1(10),
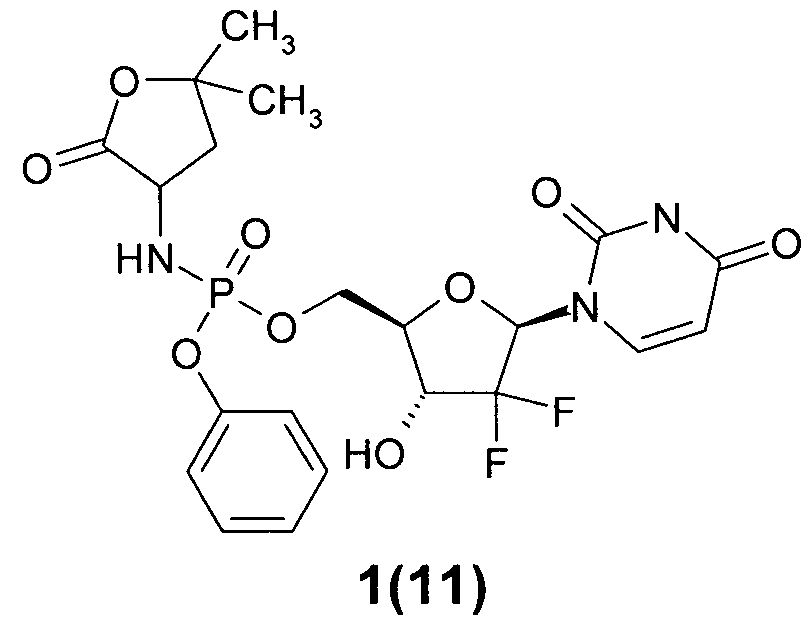
((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 5,5-диметил-2-оксотетрагидрофуран-3-илфосфорамидат 1(11),
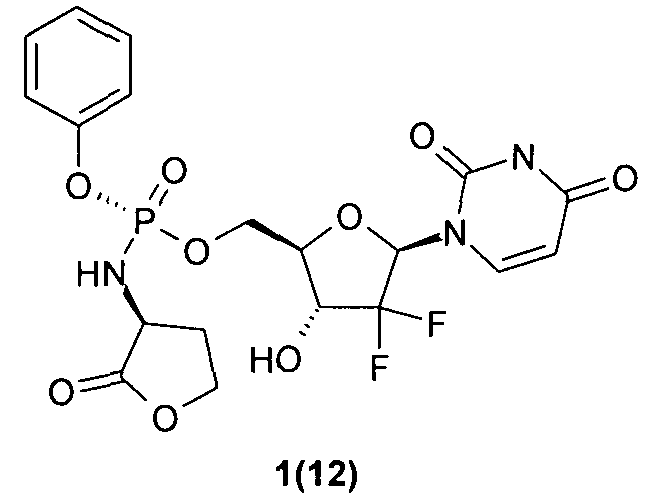
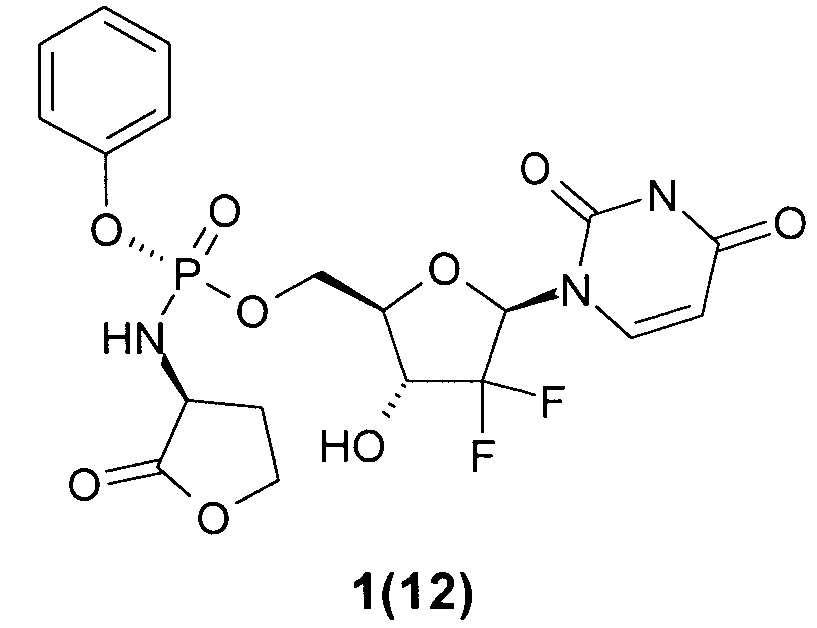
(R)-((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил ((S)-2-оксотетрагидрофуран-3-ил)фосфорамидат 1(12),
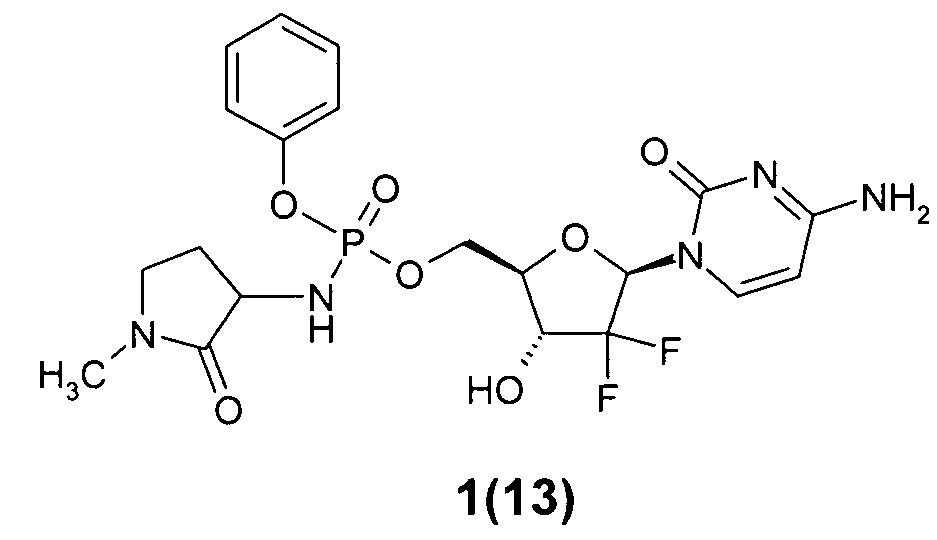
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопирролидин-3-илфосфорамидат 1(13),
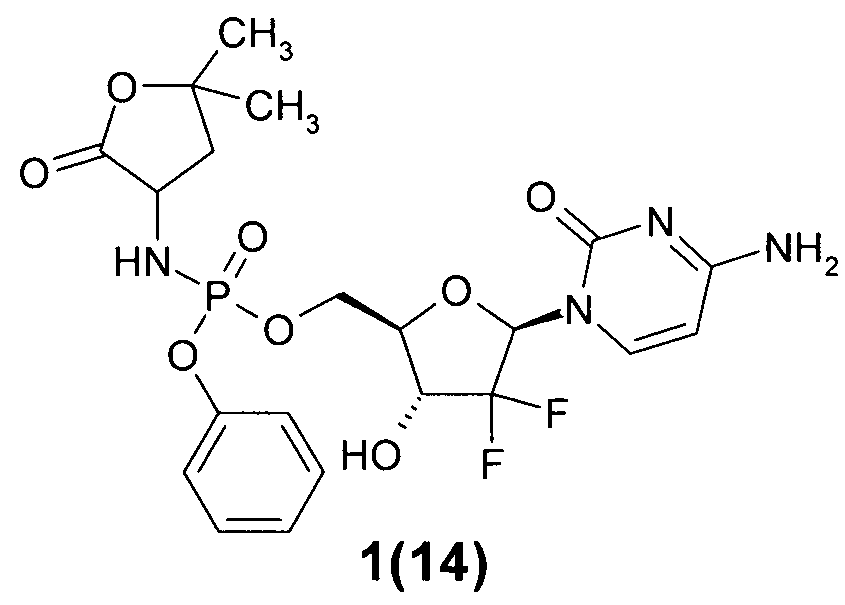
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 5,5-диметил-2-оксотетрагидрофуран-3-илфосфорамидат 1(14),
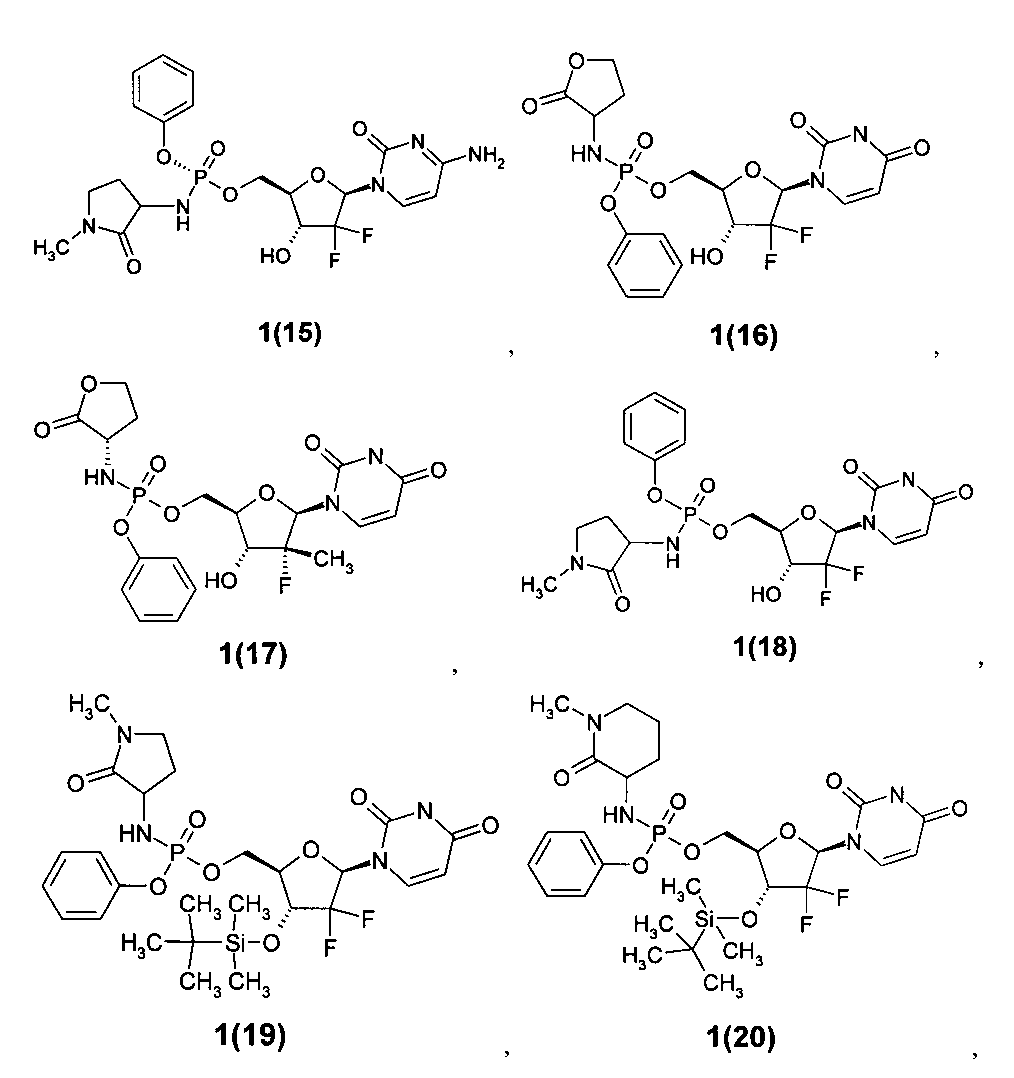
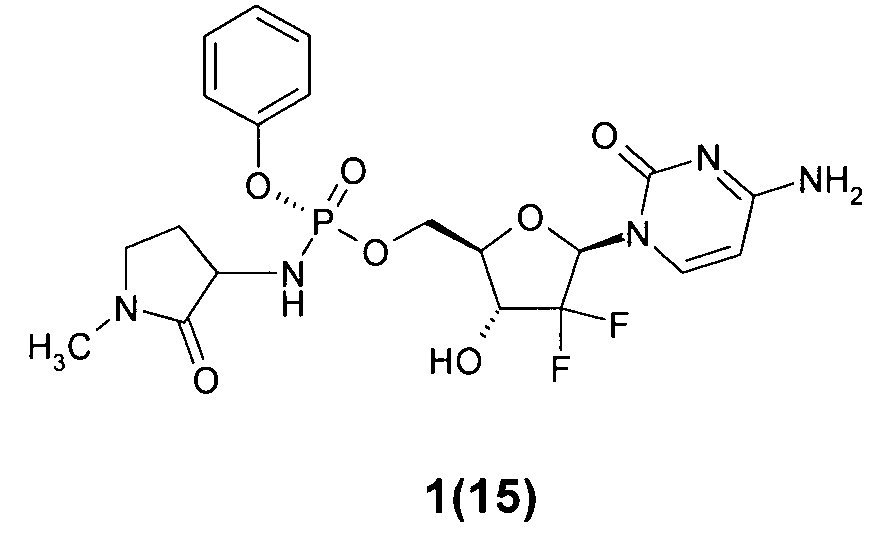
(R)-((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопирролидин-3-илфосфорамидат 1(15),
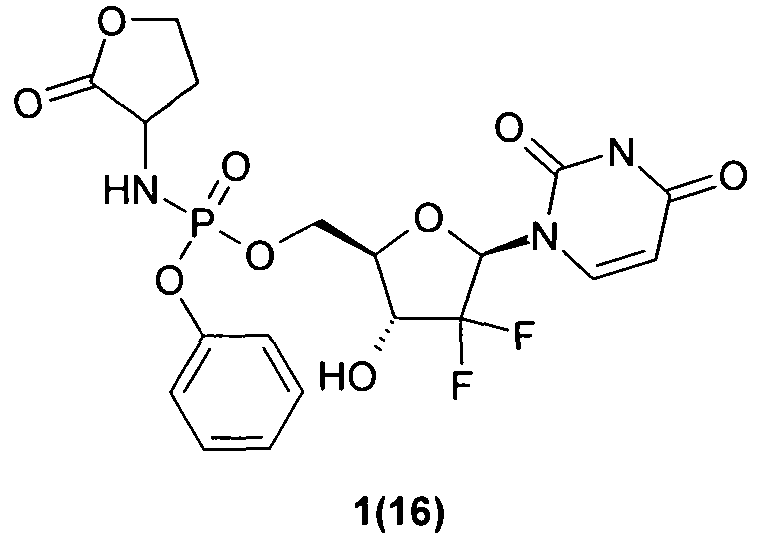
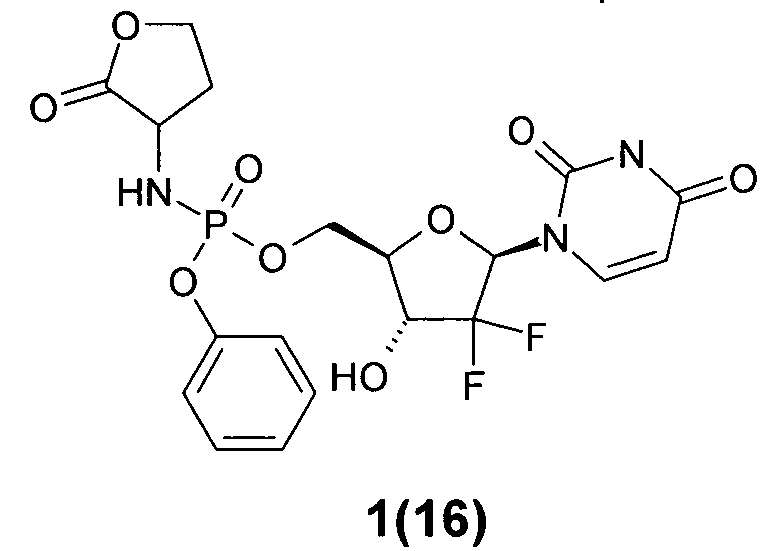
((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 2-оксотетрагидрофуран-3-илфосфорамидат 1(16),
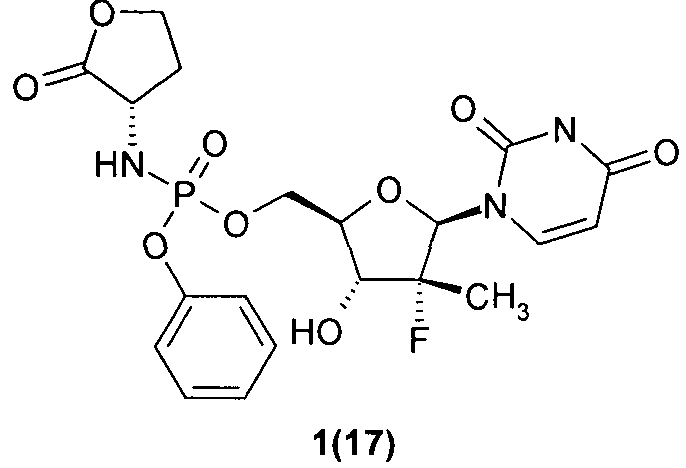
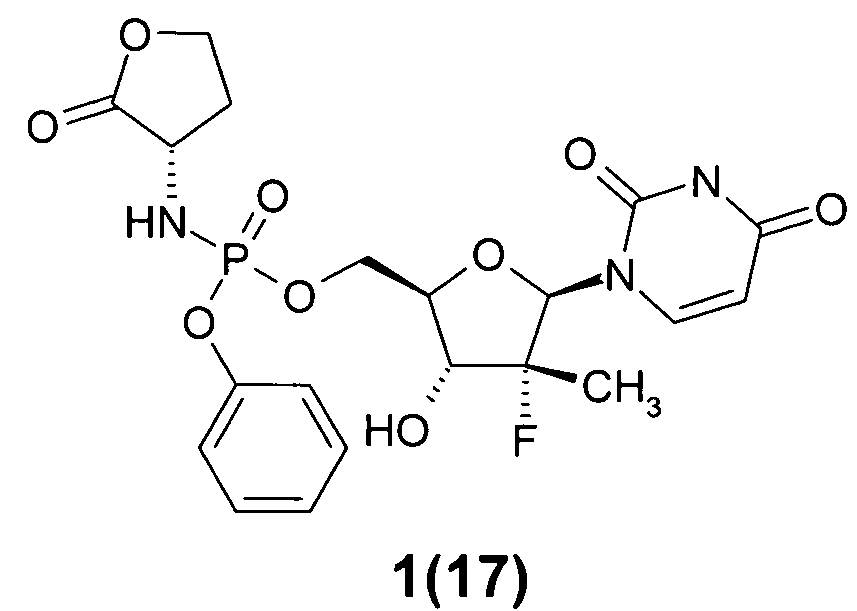
((2R,3R,4R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4-фтор-3-гидрокси-4-метилтетрагидрофуран-2-ил)метил фенил (S)-2-оксотетрагидрофуран-3-илфосфорамидат 1(17)
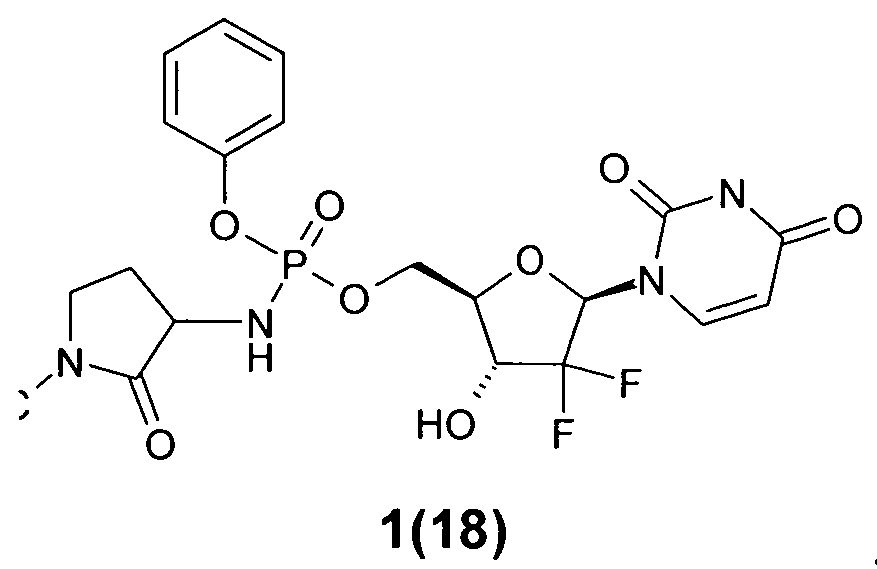
((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопирролидин-3-илфосфорамидат 1(18),
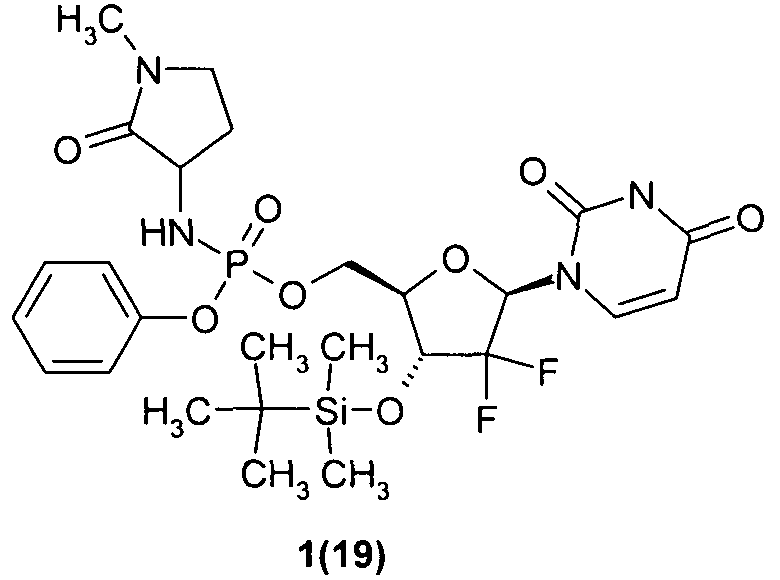
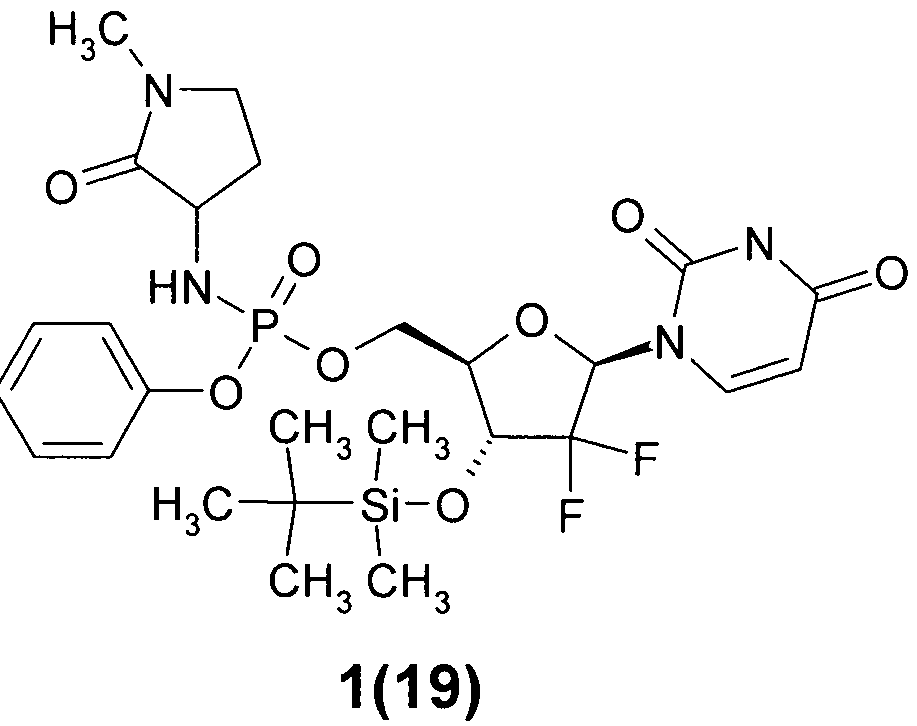
((2R,3R,5R)-3-(трет-бутилдиметилсилилокси)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтортетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопирролидин-3-илфосфорамидат 1(19),
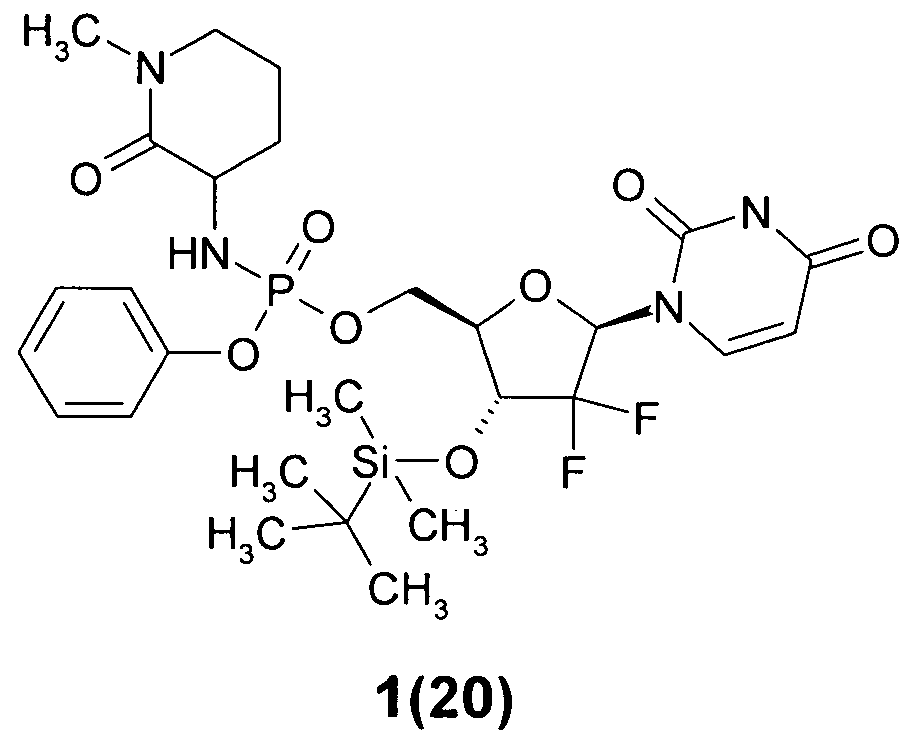
((2R,3R,5R)-3-(трет-бутилдиметилсилилокси)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтортетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопиперидин-3-илфосфорамидат 1(20),
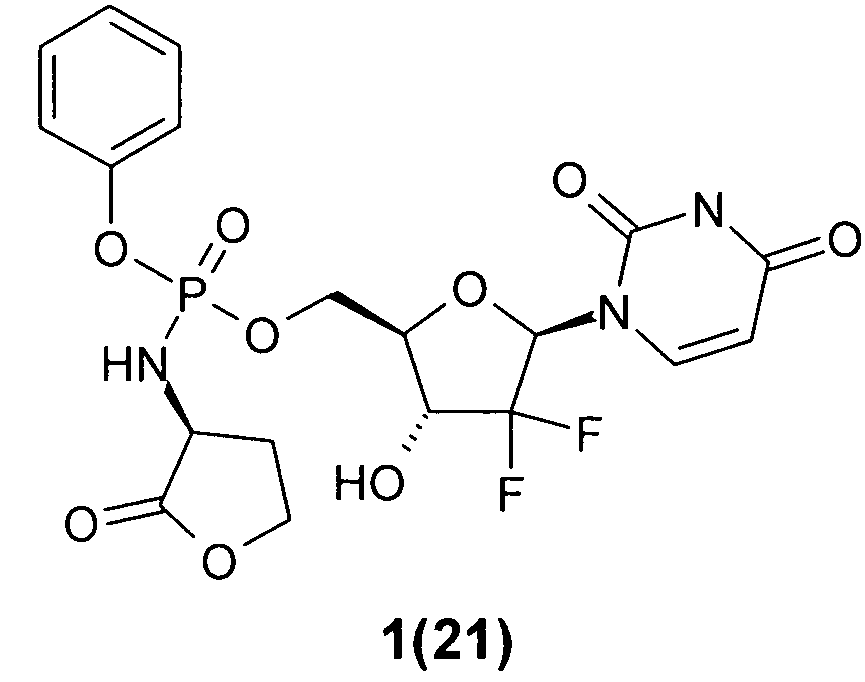
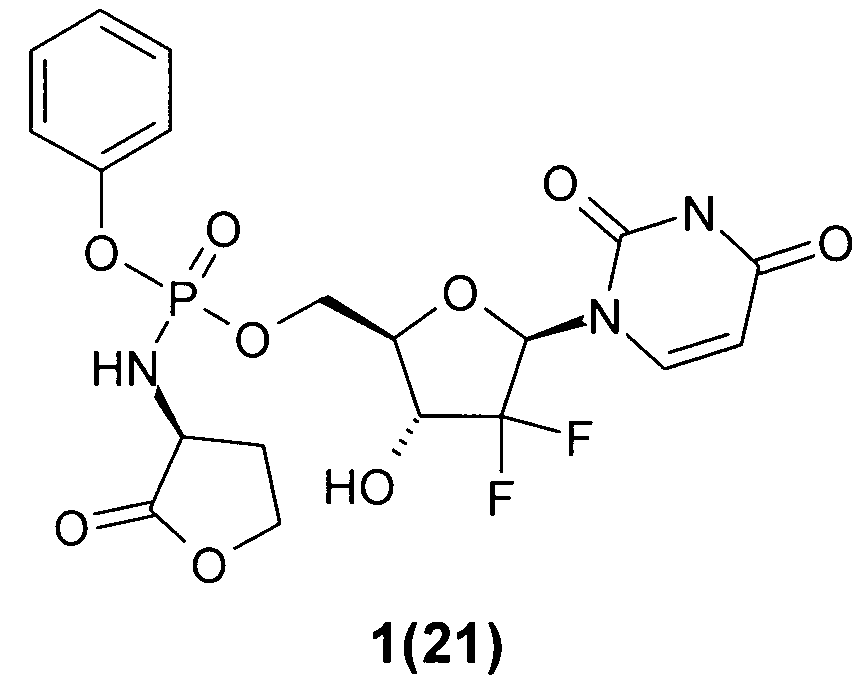
((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил (R)-2-оксотетрагидрофуран-3-илфосфорамидат 1(21)
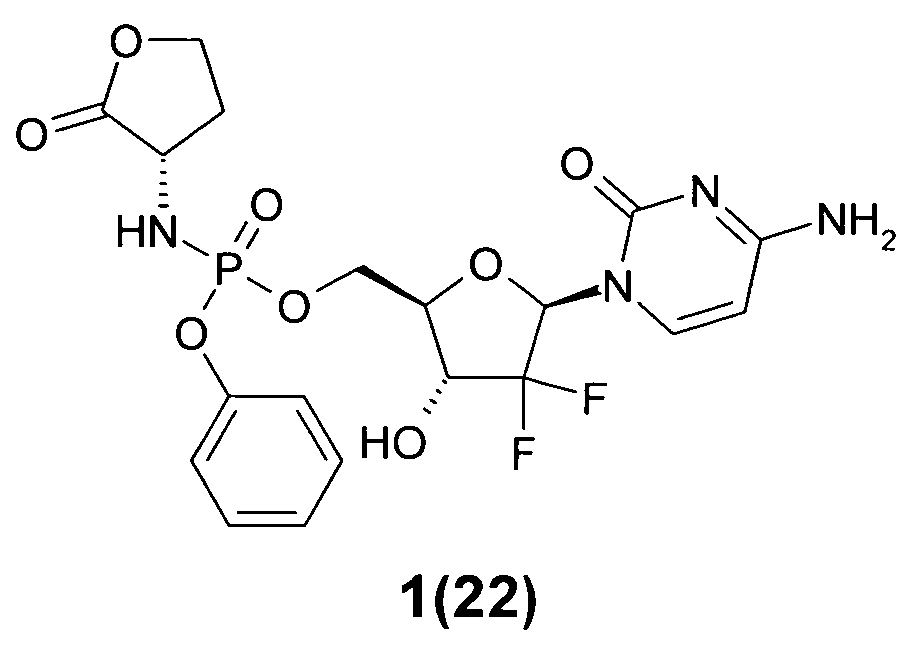
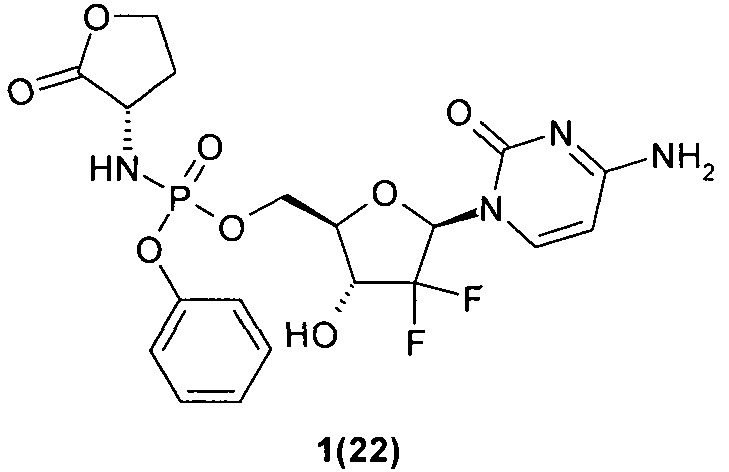
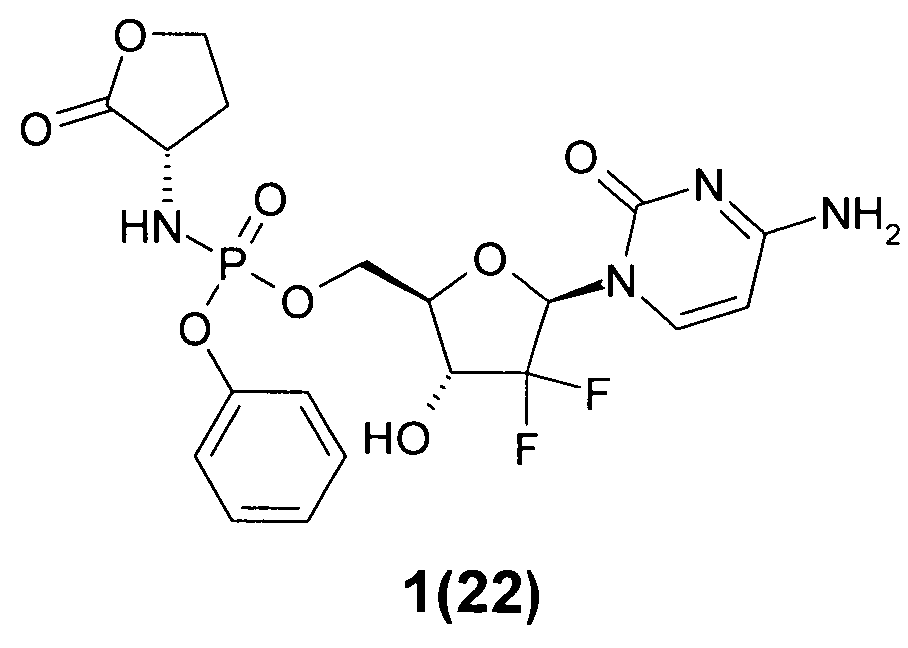
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил (S)-2-оксотетрагидрофуран-3-илфосфорамидат 1(22),
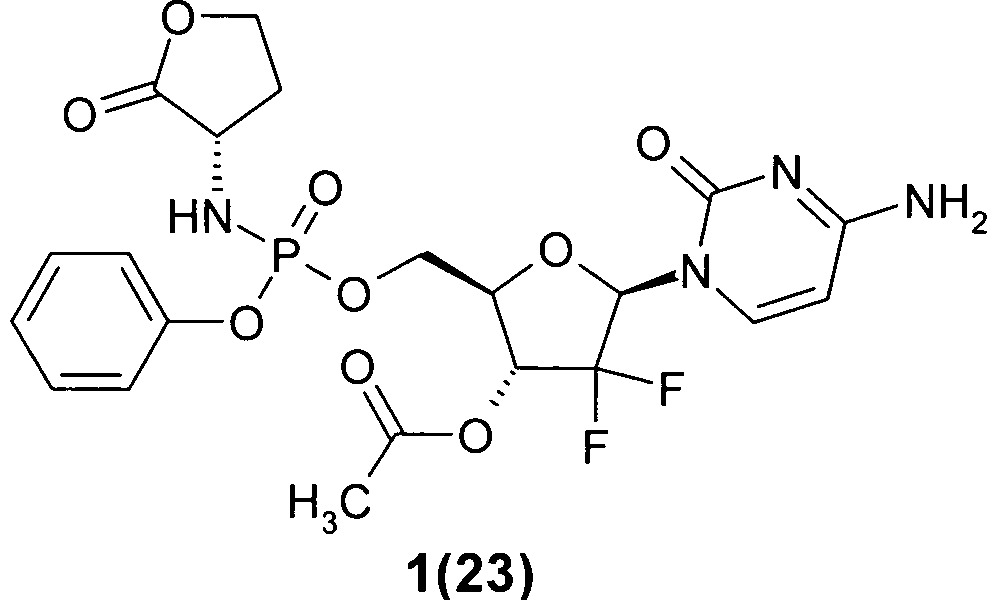
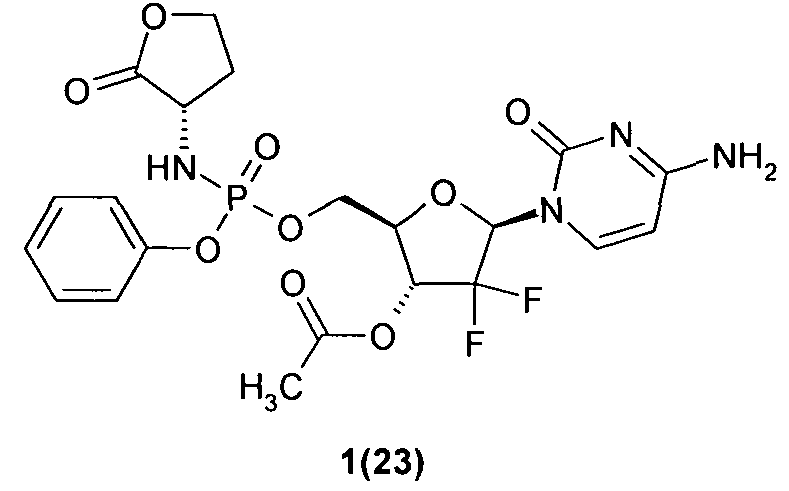
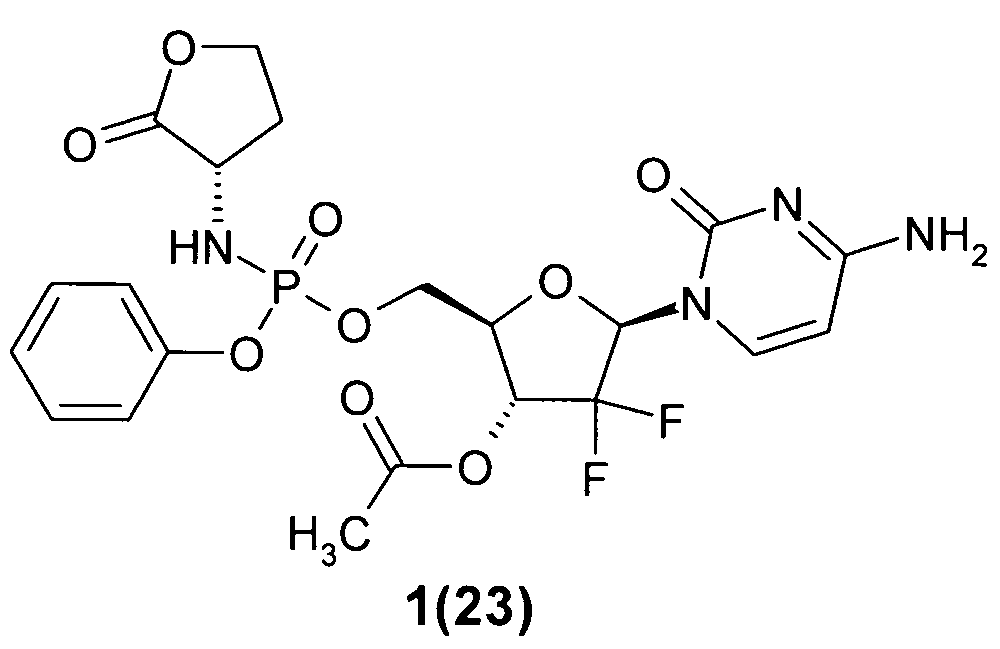
(2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-2-((((S)-2-оксотетрагидрофуран-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-3-ил ацетат 1(23),
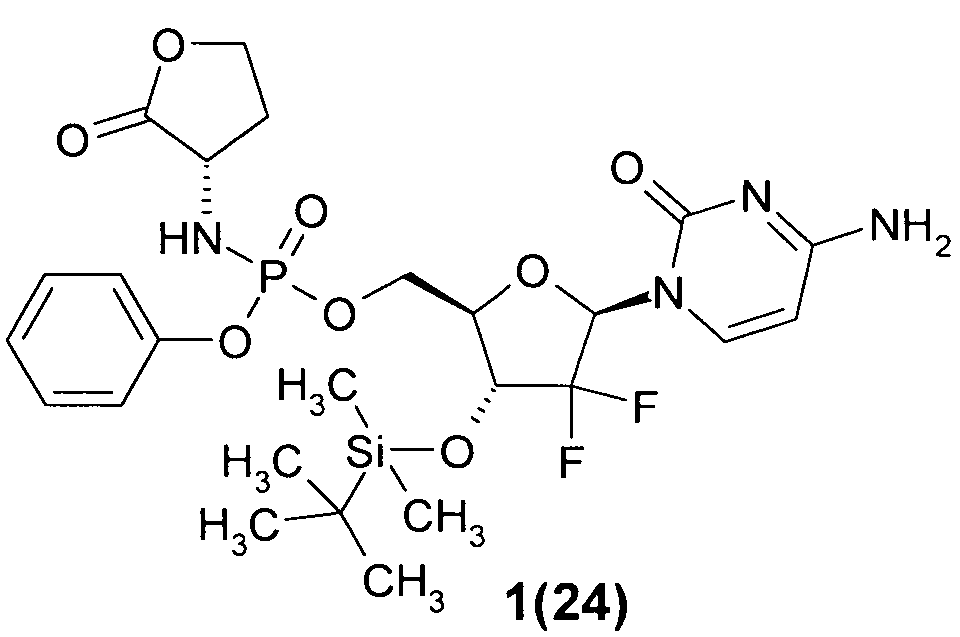
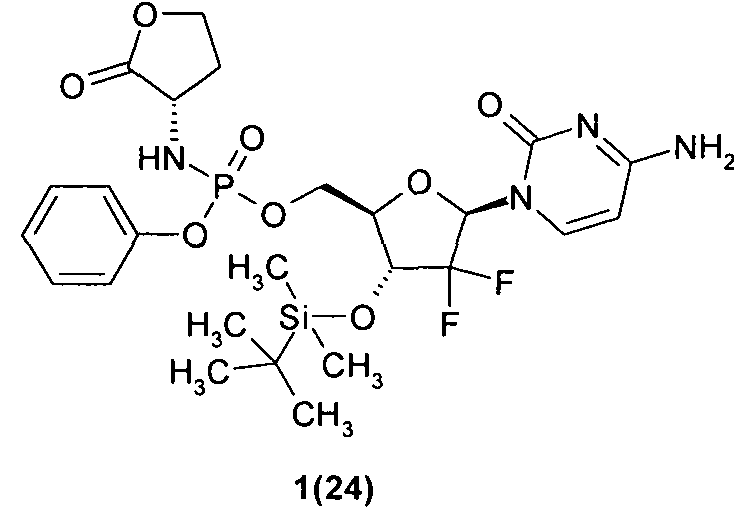
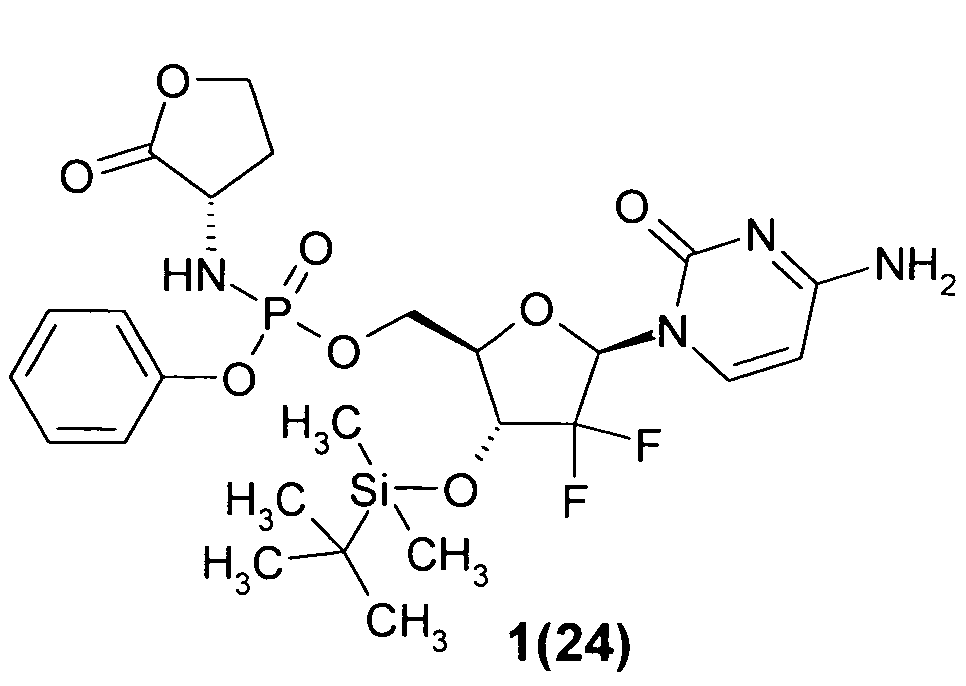
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-3-(трет-бутилдиметилсилилокси)-4,4-дифтортетрагидрофуран-2-ил)метил фенил (S)-2-оксотетрагидрофуран-3-илфосфорамидат 1(24),
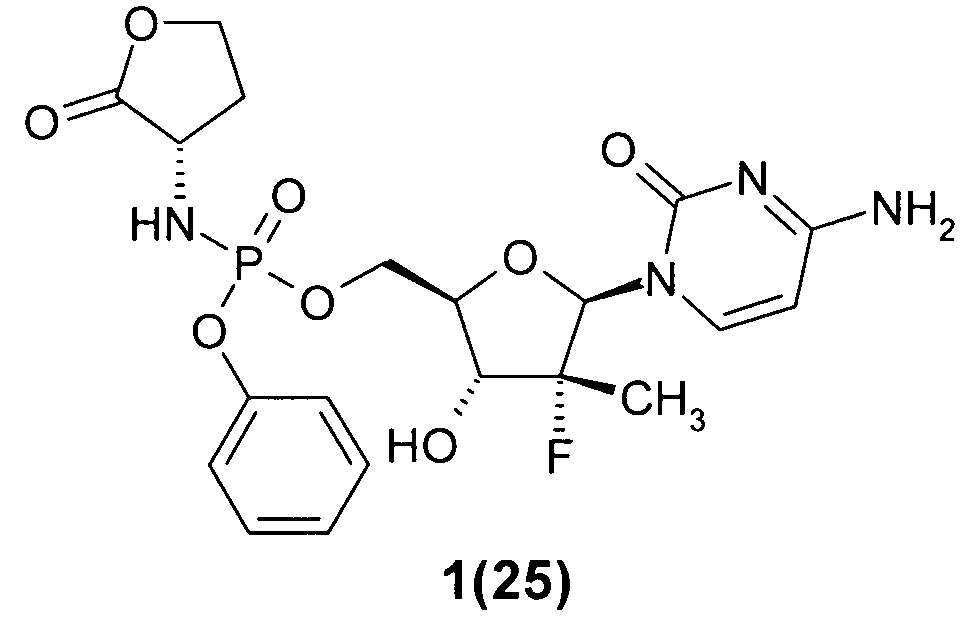
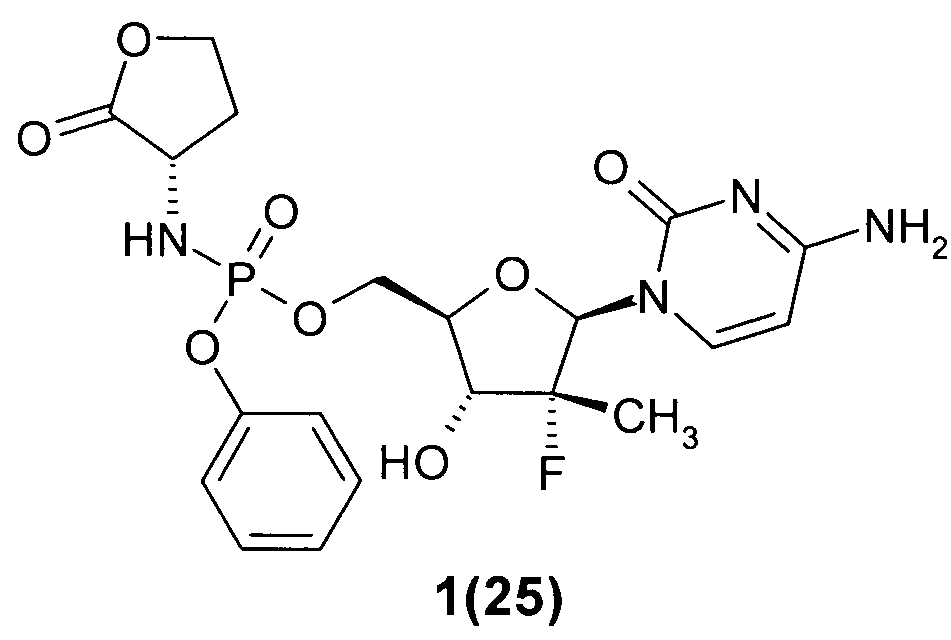
((2R,3R,4R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4-фтор-3-гидрокси-4-метилтетрагидрофуран-2-ил)метил фенил (S)-2-оксотетрагидрофуран-3-илфосфорамидат 1(25),
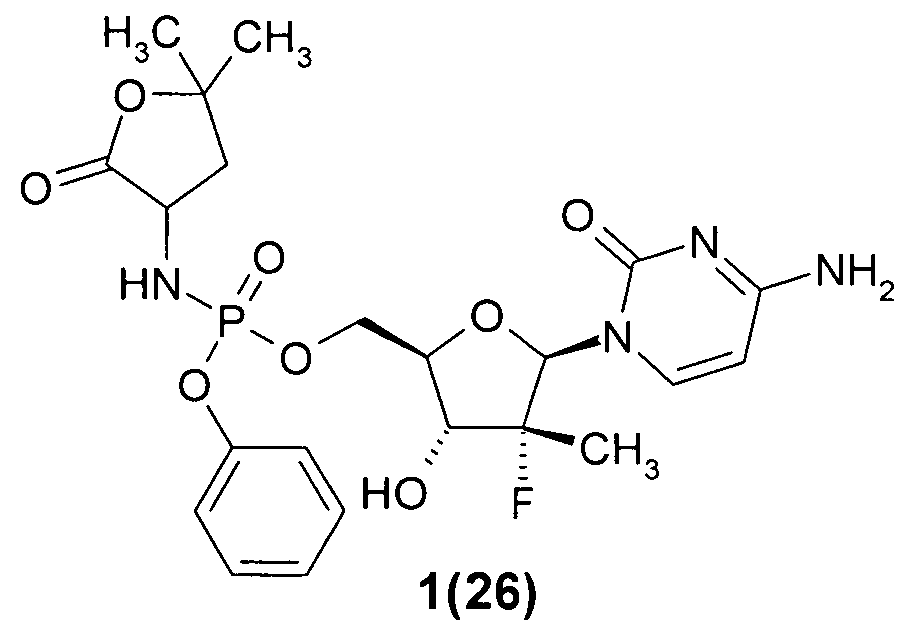
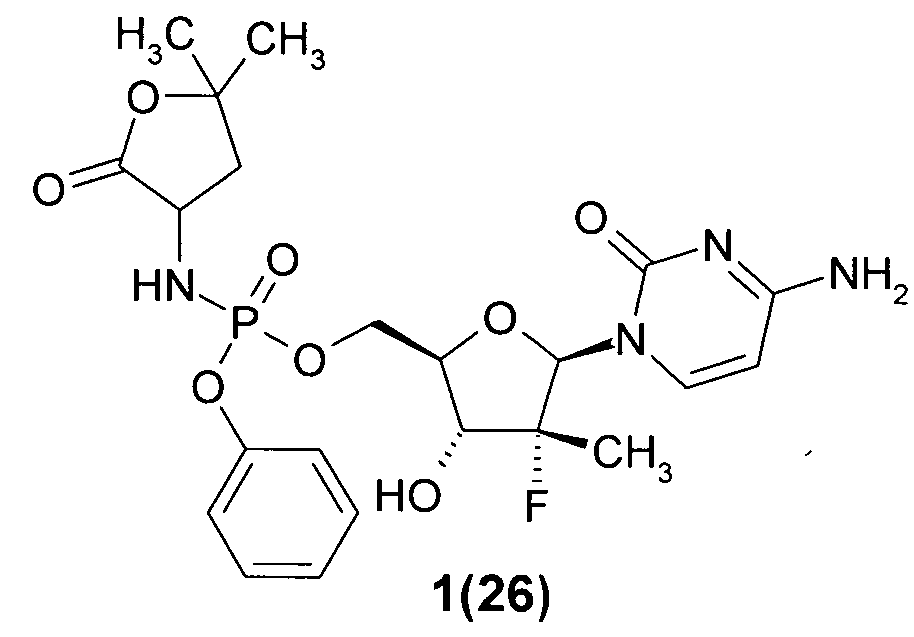
((2R,3R,4R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4-фтор-3-гидрокси-4-метилтетрагидрофуран-2-ил)метил фенил 5,5-диметил-2-оксотетрагидрофуран-3-илфосфорамидат 1(26),
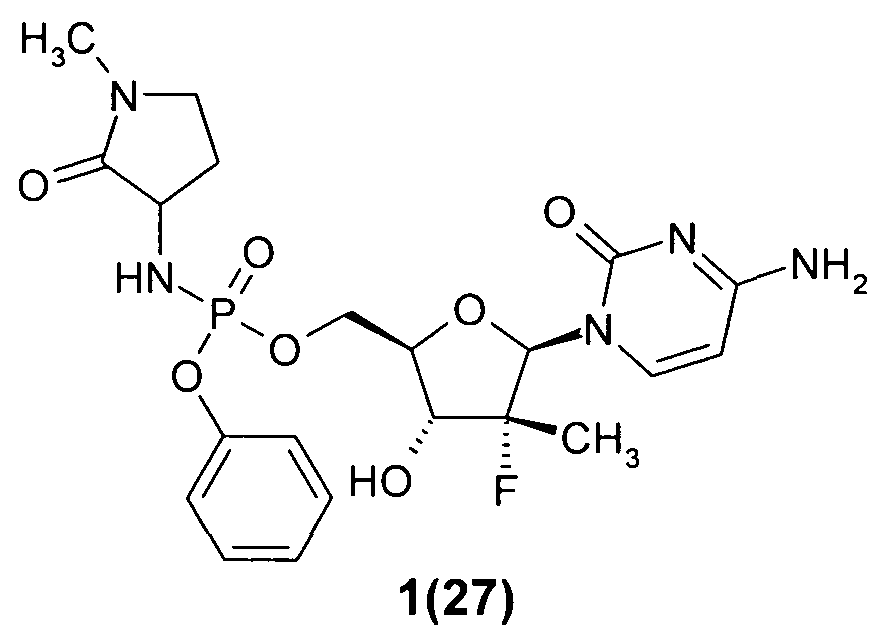
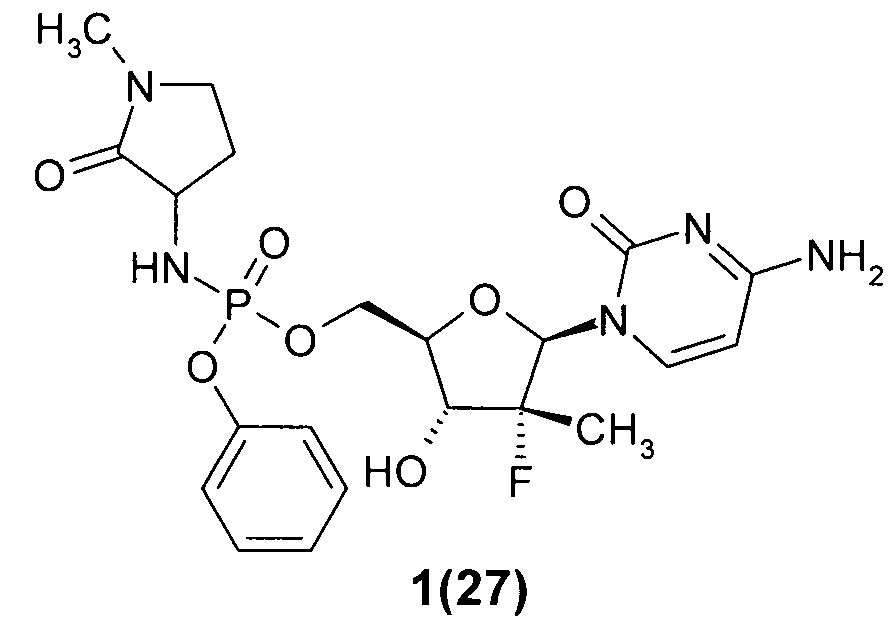
((2R,3R,4R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4-фтор-3-гидрокси-4-метилтетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопирролидин-3-илфосфорамидат 1(27),
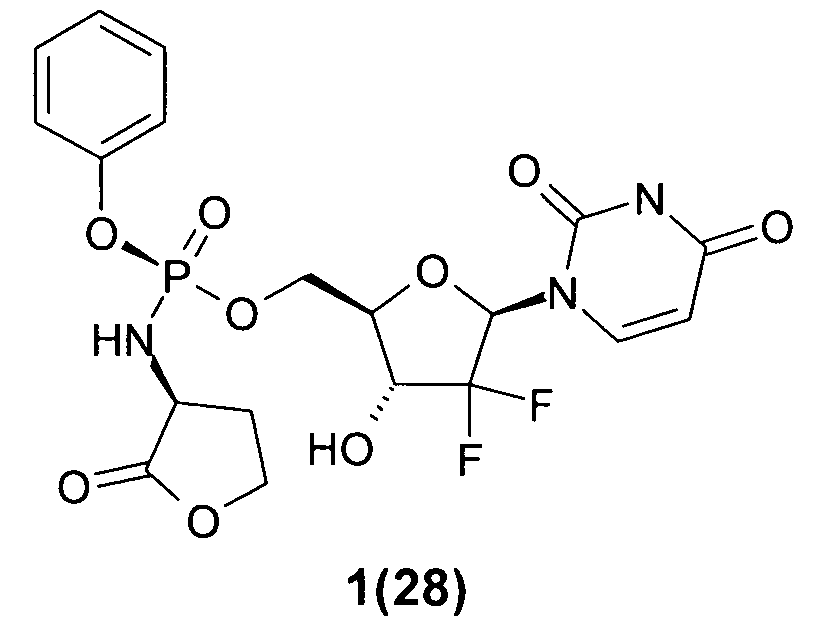
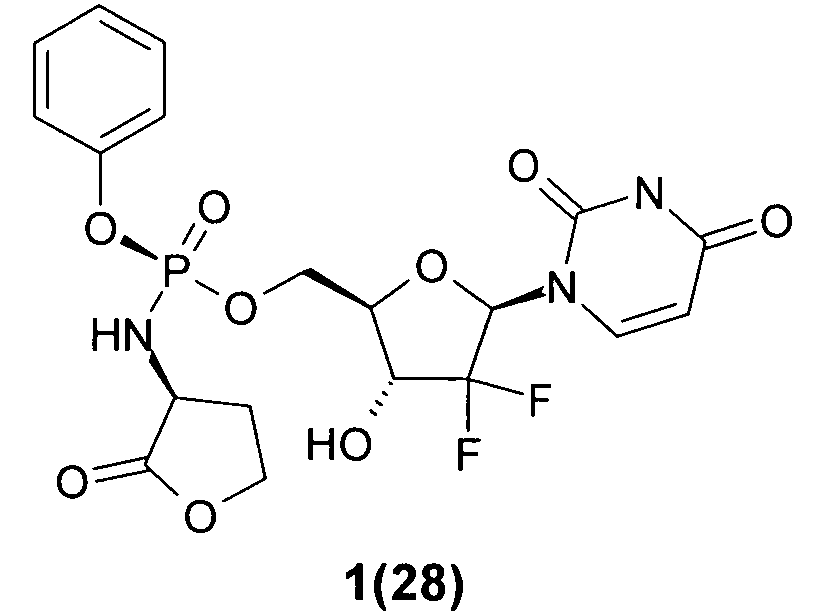
(S)-((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)- 4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил ((R)-2-оксотетрагидрофуран-3-ил)фосфорамидат 1(28),
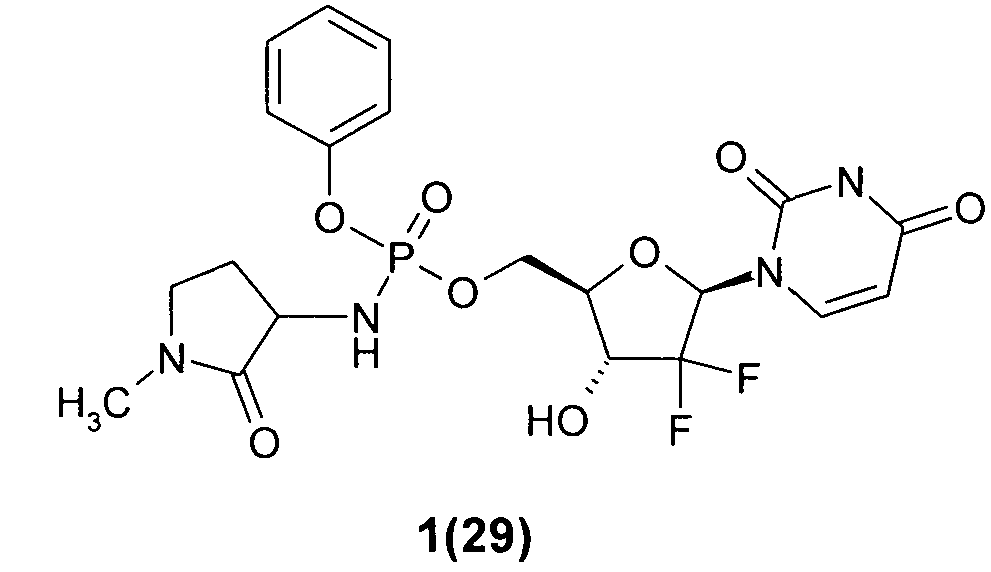
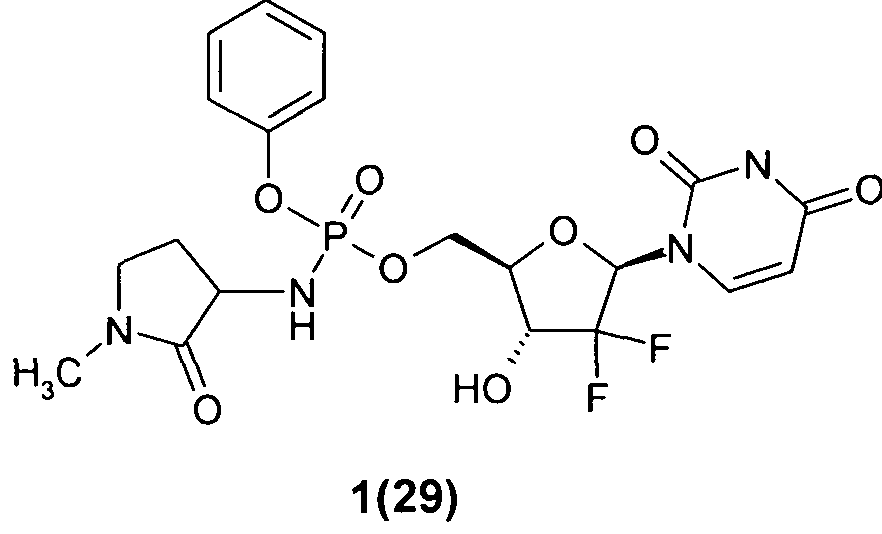
((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопирролидин-3-илфосфорамидат 1(29), и
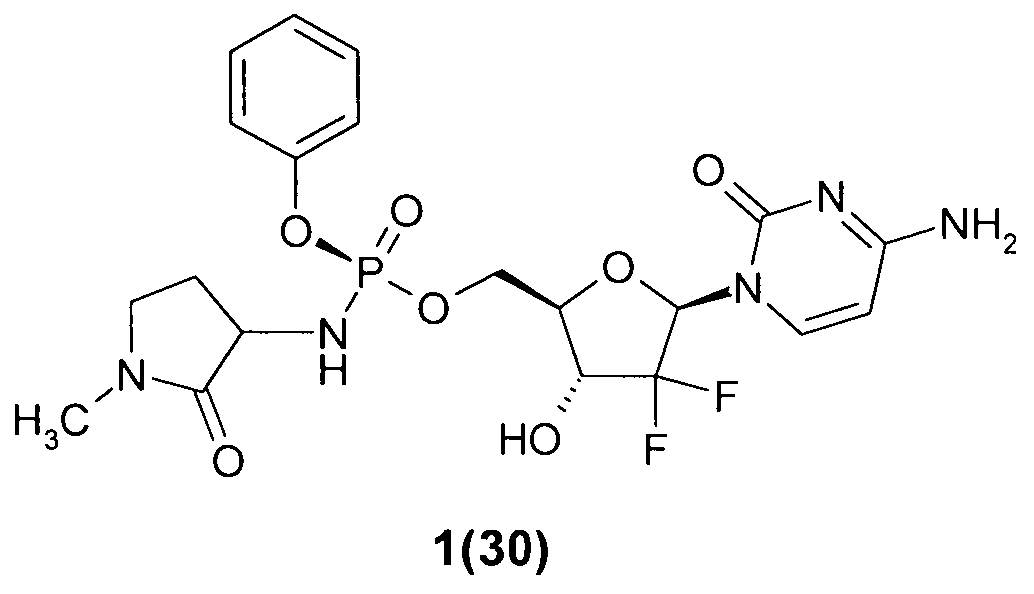
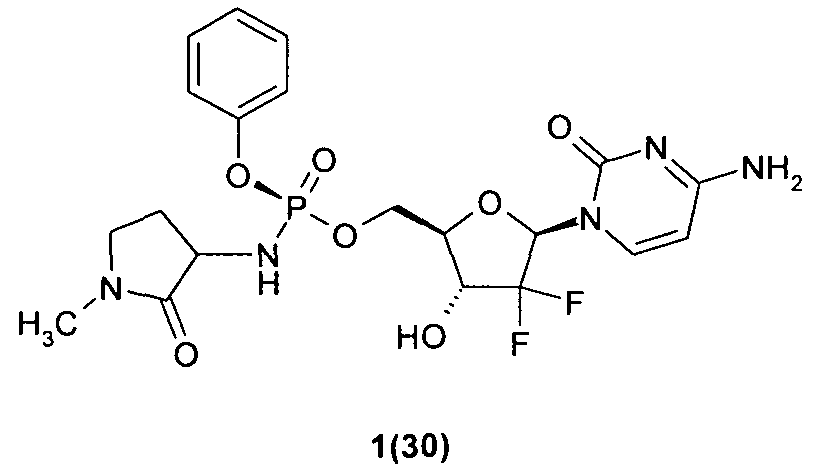
(S)-((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопирролидин-3-илфосфорамидат
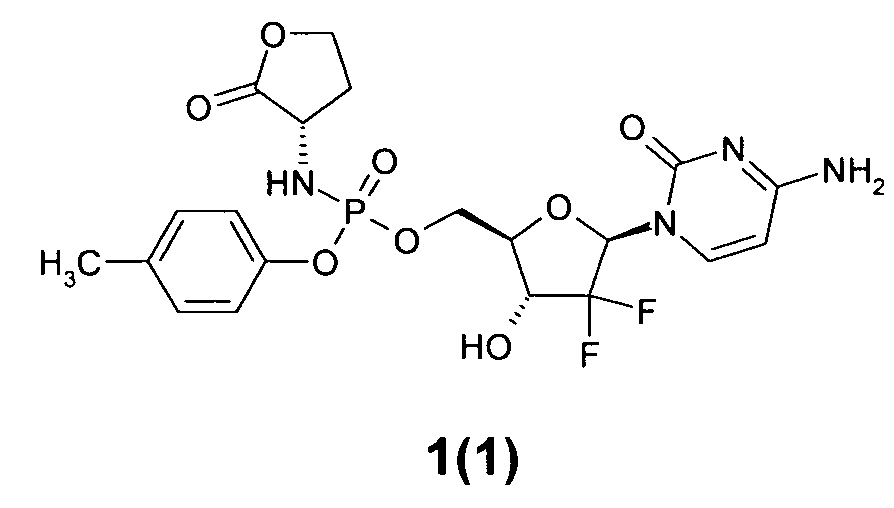 ,
,  ,
,
 ,
,  ,
,
 ,
,  ,
,
 ,
, 
 ,
,  ,
,
 ,
,  ,
,
 ,
,  ,
,
 ,
,  ,
,
 ,
,  ,
,
 ,
,  ,
,
 ,
,  ,
,
 ,
,  ,
,
 ,
,  ,
,
 ,
,  ,
,
 , и
, и 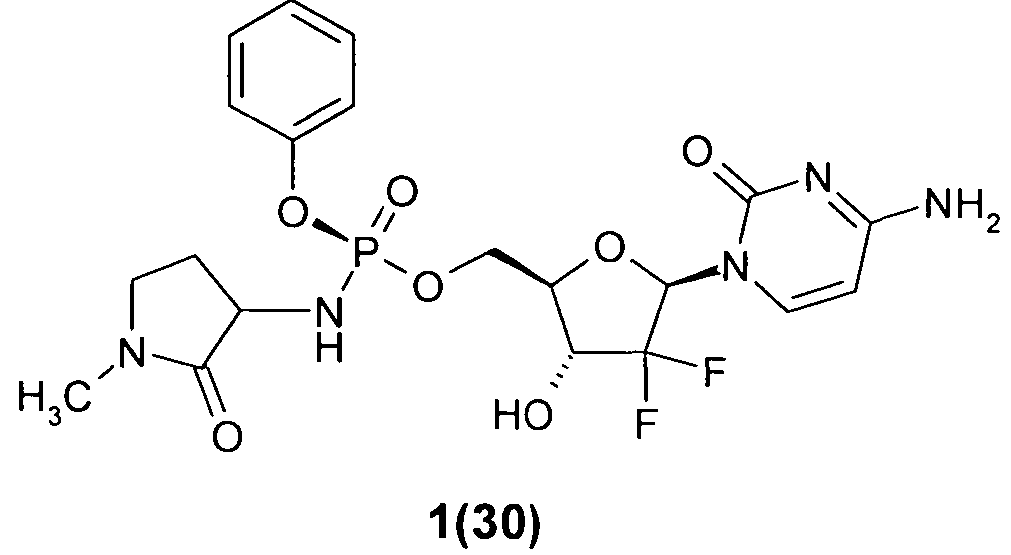
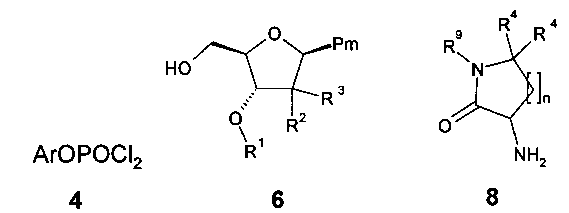
Предметом настоящего изобретения является способ получения соединения формулы 1 или его стереоизомера взаимодействием соединения формулы 6 с соединением формулы 4 и последующим смешиванием с амином формулы 8,
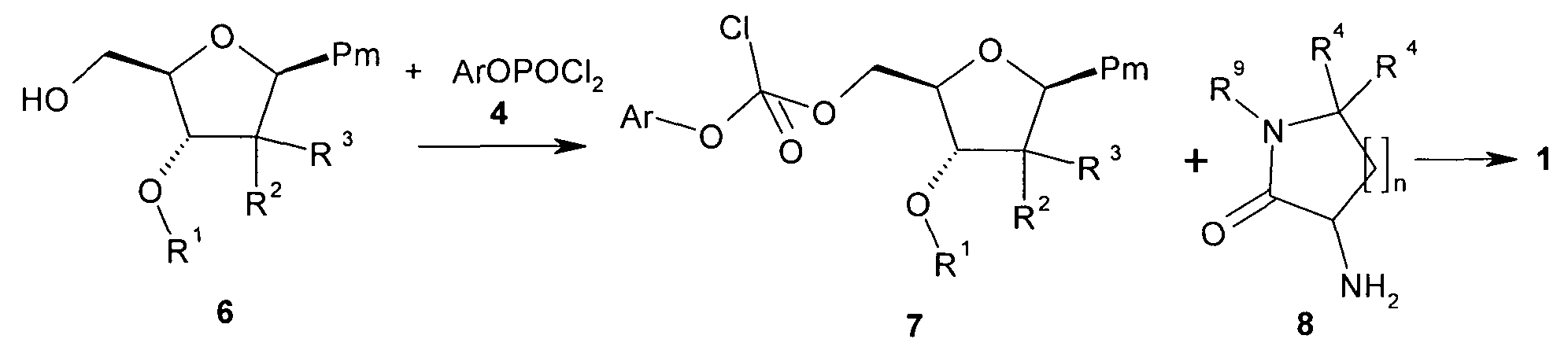
где Ar, n, R1, R2, R3, R4, R9, и Pm имеют вышеуказанное значение.
Предметом настоящего изобретения является способ получения соединения формулы 1 или его стереоизомера, где R1 представляет собой ацил, ацилированием соединения формулы 1, где R1 представляет собой водород.
Предметом настоящего изобретения является способ получения соединения общей формулы 1 или его стереоизомера, где R1 представляет собой диметил-трет-бутилдиметилсилил, смешиванием диметил-трет-бутилдиметилсилил хлорида с соединением формулы 1, где R1 представляет собой водород.
Предметом настоящего изобретения является способ получения соединения общей формулы 1 или его стереоизомера, взаимодействием амина формулы 3 с соединением общей формулы 4 и последующим смешиванием с соединением формулы 6,
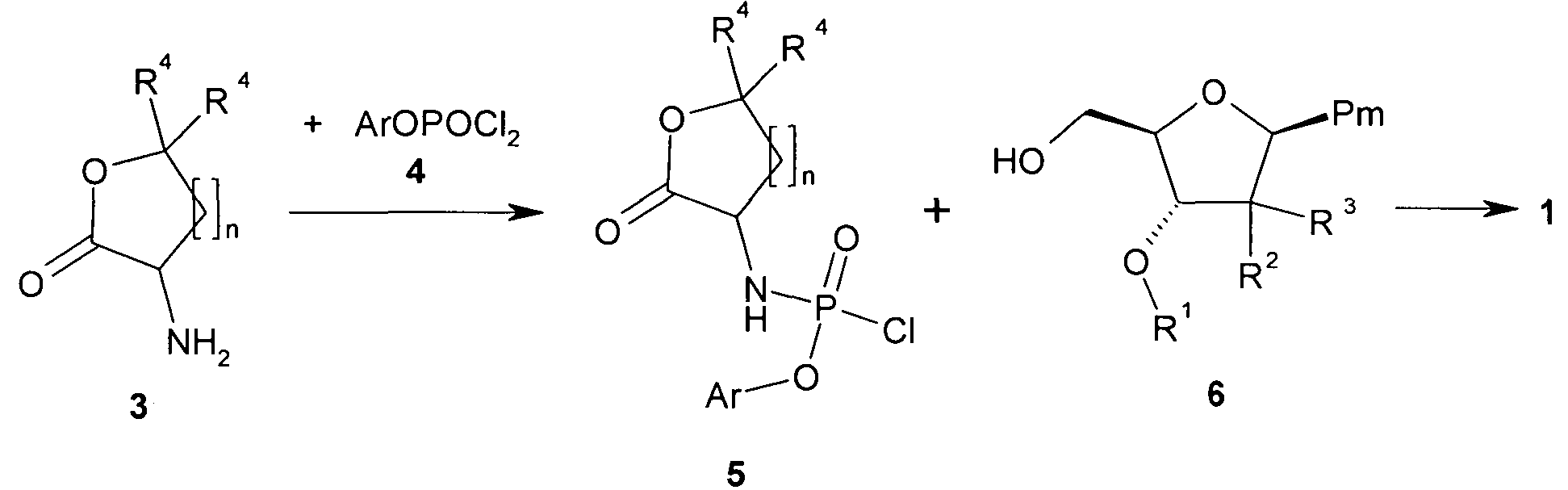
где Ar, n, R1, R2, R3, R4, и Pm имеют вышеуказанное значение.
Разделение рацемических смесей соединения общей формулы 1 на стереоизомеры проводится либо кристаллизацией и/или LC, или выполняется путем кристаллизации и/или HPLC.
Исходные соединения, которые использовались в приведенном выше процессе получения нового замещенного эфира амидофосфорной кислоты, представленного общей формулой 1, его стереоизомера, фармацевтически приемлемой соли, являются коммерчески доступными соединениями или они могут быть легко получены известными из литературы методами. Качество соединений контролируют при помощи LCMS и ЯМР спектров.
Для определения противовирусной активности замещенных эфиров амидофосфорной кислоты общей формулы 1 (тест соединений) используют ВГС репликонный анализ. В качестве тестовой клеточной линии, используемой в ВГС репликонном анализе, берут линию клеток гепатомы человека Huh7, содержащую репликон ВГС (генотип 1b, штамм Con1). Клетки высеивают в 96-луночные планшеты плотностью 7.5×103 клеток на лунку в 50 мкл питательной среды. Основные растворы тестируемых соединений готовят непосредственно перед использованием в питательной среде ДМЕМ (DMEM IX, Cellgro; кат. # 10-013-CV) в виде двухкратных 2Х стоков. Всего готовят 11 серий 3-кратных разведений тестовых соединений из двухкратных 2Х стоков в питательной среде с диапазоном конечной концентрации 20 нМ - 0.2 пМ. По крайней мере, через 4 часа после того, как клетки были посеяны, инициируют обработку соединениями путем добавления к каждой плашке по 50 мкл определенного разведения соединения. Конечная концентрация тестируемых соединений составляет от 10 нМ до 0.1 пМ после разбавления 1:1 имеющейся питательной средой. Конечная концентрация ДМСО составляет 0.5%. Клетки и ингибиторы инкубируют в течение трех дней при 37°C/5% CO2. Среду удаляют из плашек посредством аккуратного постукивания. Клетки фиксируют добавлением 100 мкл смеси ацетон/метанол (1:1) на 1 минуту, потом трижды промывают буфферным раствором PBS, и после этого блокируют добавлением 150 мкл/лунка 10% фетальной телячьей сыворотки (FBS) в растворе PBS на 1 час при комнатной температуре. Клетки трижды промывают буфферным раствором PBS, и инкубируют с антителами к кор-антигену гепатита С mAb 100 мкл/лунка (Affinity BioReagents; кат. # МА1-080, 1 мг/мл сток был разведен 1:4000 в 10% FBS-PBS) в течение 2 часов при 37°C. Клетки промывают 3 раза раствором PBS и инкубируют с антителами козы к иммуноглобулинам мыши (HRP-Goat Anti-Mouse antibody) в количестве 100 мкл/лунка (разведение 1:3,500 в 10% FBS-PBS) в течение 1 часа при 37°C. Клетки промывают 3 раза раствором PBS и выдерживают с ОПД раствором - 100 мкл/лунка (1 ОПД таблетка + 12 мл цитрат/фосфатный буфер + 5 мкл 30% H2O2 на планшет) в течение 30 минут в темноте при комнатной температуре. Реакцию останавливают добавлением 2 н. H2SO4 в количестве 100 мкл/лунка, и измеряют оптическую плотность при А490 Х на многоканальной спектрофотометре Victor3 V 1420 (Perkin Elmer). Значения EC50 для каждого тестируемого соединения рассчитывают на основании уравнений наилучшего соответствия при помощи программы XLFit.
Цитотоксичность тестируемых соединений исследуют в опытах на культуре линии клеток гепатомы человека Huh7. Количество живых клеток определяют при помощи набора ATPLite (Perkin-Elmer, Boston, USA), в соответствии с инструкциями производителя. Клетки высеивают в 96-луночные черные микроплаты с прозрачным дном плотностью 7.5×103 клеток на лунку в 50 мкл среды. Через 18 часов была инициирована обработка соединениями путем добавления к каждой плашке по 50 мкл определенного разведения соединения. Каждое разведение соединения тестируют в трех параллельных экспериментах. Клетки и ингибиторы инкубируют в течение 96 часов при 37°C/5% CO2. Планшеты промывают дважды фосфатно-солевым буфером PBS (0.2 мл/лунка), и затем лизируют клетки добавлением 0.05 мл/лунка клеточного буфера (все указанные реактивы входят в комплект набора ATPLite). После инкубирования в течение 5 минут на вращающейся платформе добавляют 0.05 мл/лунка буфер субстрата. После инкубирования в течение еще 5 минут выдерживают планшет в темноте в течение 10 минут и измеряют люминесценцию на приборе TopCount NXT (Packard, Perkin Elmer). Величину EC50 для всех тестируемых соединений определяют при помощи программы XLfit 4.1.
Результаты этих исследований показывают, что новые замещенные эфиры амидофосфорной кислоты общей формулы 1 являются мощными ингибиторами ВГС in vitro с низкой цитотоксичностью.
Ингибирующая активность (EC50) в условиях ВГС репликонного анализа некоторых новых замещенных эфиров амидофосфорной кислоты общей формулы 1 представлена в таблице 1. Как видно из таблицы 1 новые NS5B ингибиторы общей формулы 1 обладают микромолярной цитотоксичностью (CC50) и наномолярной активностью (EC50), которая, как правило, заметно выше активности известного ингибитора PSI-7851 [EC50=75 нМ. Е. Murakami, Т. Tolstykh, H. Вао, С. Niu, H.M. Micolochick Steuer, D. Bao, W. Chang, C. Espiritu, S. Bansal, A.M. Lam, M.J. Otto, M.J. Sofia, P.A. Furman. Mechanism of Activation of PSI-7851 and Its Diastereoisomer PSI-7977. J. Biol. Chem., 285(45), 34337-34347 (2010)].
|
|
|
|
Предметом настоящего изобретения является использование замещенного эфира амидофосфорной кислоты общей формулы 1, или его стереоизомера, или его фармацевтически приемлемой соли, в качестве активного компонента, который обладает свойствами нуклеозидных ингибиторов РНК-полимеразы NS5B вируса гепатита C,
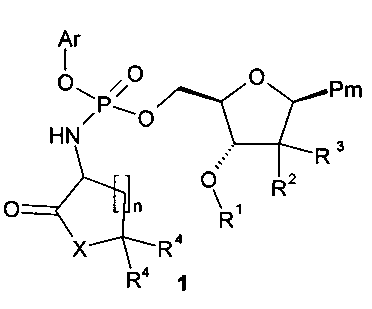
где:
R1 представляет собой водород, (СН3)2[(СН3)3С]Si, С2-С6ацил, необязательно замещенный бензилоксигруппой, NR5R6 группой, в которой R5 и R6 представляют собой независимо водород или C1-C4алкил; 1-пиррол-2-илкарбонил, пиперидин-3-илкарбонил или пиперидин-4-илкарбонил;
R2 и R3 представляют собой F или R2 представляет собой F или ОН и R3 представляет собой СН3;
R4 представляет собой водород или метил;
Ar представляет собой фенил, пиридил или нафтил, где фенил, пиридил или нафтил являются необязательно замещенными по крайней мере одним из: С1-3алкил, С2-4алкенил, С2-4алкинил, C1-3алкокси, F, Cl, Br, I, нитро, циано, -N(C1-3алкил)2;
Pm представляет собой 2,4-диоксо-3,4-дигидро-2Н-пиримидин-1-ил или 4-(4-амино-2-оксо-2Н-пиримидин-1-ил), в которых амино группа является необязательно замещенной 1-пиррол-2-илкарбонилом, пиперидин-3-илкарбонилом, пиперидин-4-илкарбонилом или радикалом C(O)R8, где R8 представляет собой С1-С4алкил, необязательно замещенный NR6R7 группой, где R6 и R7 представляют собой независимо водород или С1-С4алкил; С1-3алкокси, необязательно замещенную фенилом;
X представляет собой О или N-R9, где R9 представляет собой С1-С4алкил, необязательно замещенный ОН или ОСН3;
n=1, 2 или 3.
Согласно данному изобретению более предпочтительным является использование соединения, представленного общей формулой 1, или его стереоизомера, или его фармацевтически приемлемой соли, выбранного из:
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил п-толил (S)-2-оксо-тетрагидрофуран-3-ил-фосфорамидат 1(1),
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил 4-хлорфенил (S)-2-оксо-тетрагидрофуран-3-ил-фосфорамидат 1(2),
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил 2,4-дихлорфенил (S)-2-оксо-тетрагидрофуран-3-ил-фосфорамидат 1(3),
(2R,3R,5R)-5-(4-ацетамидо-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-2-(((S)-(S)-2-оксотетрагидрофуран-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-3-ил ацетат 1(4),
бензил 1-(2R,4R,5R)-4-(бензилоксикарбонилокси)-3,3-дифтор-5-(((S)-((S)-(2-оксотетрагидрофуран-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-2-ил)-2-оксо-1,2-дигидропиримидин-4-илкарбамат 1(5),
бензил 1-((2R,4R,5R)-4-(бензилоксикарбонилокси)-3,3-дифтор-5-(((1-метил-2-оксопирролидин-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-2-ил)-2-оксо-1,2-дигидропиримидин-4-илкарбамат 1(6),
бензил 1-((2R,4R,5R)-4-(бензилоксикарбонилокси)-3,3-дифтор-5-(((1-метил-2-оксопиперидин-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-2-ил)-2-оксо-1,2-дигидропиримидин-4-илкарбамат 1(7),
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопиперидин-3-илфосфорамидат 1(8),
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 2-оксооксепан-3-ил-фосфорамидат 1(9),
бензил 1-((2R,4R,5R)-4-(бензилоксикарбонилокси)-5-(((5,5-диметил-2-оксотетрагидрофуран-3-иламино)(фенокси)фосфорилокси)метил)-3,3-дифтортетрагидрофуран-2-ил)-2-оксо-1,2-дигидропиримидин-4-илкарбамат 1(10),
((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 5,5-диметил-2-оксотетрагидрофуран-3-илфосфорамидат 1(11),
(R)-((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)- 4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил ((S)-2-оксотетрагидрофуран-3-ил)фосфорамидат 1(12),
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопирролидин-3-илфосфорамидат 1(13),
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 5,5-диметил-2-оксотетрагидрофуран-3-илфосфорамидат 1(14),
(R)-((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопирролидин-3-илфосфорамидат 1(15),
((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 2-оксотетрагидрофуран-3-илфосфорамидат 1(16),
((2R,3R,4R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4-фтор-3-гидрокси-4-метилтетрагидрофуран-2-ил)метил фенил (S)-2-оксотетрагидрофуран-3-илфосфорамидат 1(17)
((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопирролидин-3-илфосфорамидат 1(18),
((2R,3R,5R)-3-(трет-бутилдиметилсилилокси)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтортетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопирролидин-3-илфосфорамидат 1(19),
((2R,3R,5R)-3-(трет-бутилдиметилсилилокси)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтортетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопиперидин-3-илфосфорамидат 1(20),
((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил (R)-2-оксотетрагидрофуран-3-илфосфорамидат 1(21)
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил (S)-2-оксотетрагидрофуран-3-илфосфорамидат 1(22),
(2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-2-((((S)-2-оксотетрагидрофуран-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-3-ил ацетат 1(23),
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-3-(трет-бутилдиметилсилилокси)-4,4-дифтортетрагидрофуран-2-ил)метил фенил (S)-2-оксотетрагидрофуран-3-илфосфорамидат 1(24),
((2R,3R,4R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4-фтор-3-гидрокси-4-метилтетрагидрофуран-2-ил)метил фенил (S)-2-оксотетрагидрофуран-3-илфосфорамидат 1(25),
((2R,3R,4R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4-фтор-3-гидрокси-4-метилтетрагидрофуран-2-ил)метил фенил 5,5-диметил-2-оксотетрагидрофуран-3-илфосфорамидат 1(26),
((2R,3R,4R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4-фтор-3-гидрокси-4-метилтетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопирролидин-3-илфосфорамидат 1(27),
(S)-((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)- 4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил ((R)-2-оксотетрагидрофуран-3-ил)фосфорамидат 1(28),
((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопирролидин-3-илфосфорамидат 1(29), и
(S)-((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопирролидин-3-илфосфорамидат 1(30).
Предметом настоящего изобретения является фармацевтическая композиция для профилактики и/или лечения вирусных инфекций, включая гепатит С, содержащая активный компонент в терапевтически эффективном количестве, представленный общей формулой 1, или его стереоизомером, или его фармацевтически приемлемой солью, и фармацевтически приемлемый эксципиент, выбранный из наполнителя, носителя, растворителя,
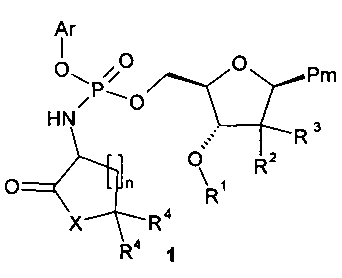
где:
R1 представляет собой водород, (СН3)2[(СН3)3С]Si C2-C6ацил, необязательно замещенный бензилоксигруппой, NR5R6 группой, в которой R5 и R6 представляют собой независимо водород или С1-С4алкил; 1-пиррол-2-илкарбонил, пиперидин-3-илкарбонил или пиперидин-4-илкарбонил;
R2 и R3 представляют собой F или R2 представляет собой F или ОН и R3 представляет собой СН3;
R4 представляет собой водород или метил;
Ar представляет собой фенил, пиридил или нафтил, где фенил, пиридил или нафтил являются необязательно замещенными по крайней мере одним из: С1-3алкил, С2-4алкенил, С2-4алкинил, C1-3алкокси, F, Cl, Br, I, нитро, циано, -N(C1-3алкил)2;
Pm представляет собой 2,4-диоксо-3,4-дигидро-2Н-пиримидин-1-ил или 4-(4-амино-2-оксо-2Н-пиримидин-1-ил), в которых амино группа является необязательно замещенной 1-пиррол-2-илкарбонилом, пиперидин-3-илкарбонилом, пиперидин-4-илкарбонилом или радикалом C(O)R8, где R8 представляет собой C1-C4алкил, необязательно замещенный NR6R7 группой, где R6 и R7 представляют собой независимо водород или С1-С4алкил; C1-3алкокси, необязательно замещенную фенилом;
X представляет собой О или N-R9, где R9 представляет собой С1-С4алкил, необязательно замещенный ОН или ОСН3;
n=1, 2 или 3.
Согласно данному изобретению более предпочтительной является фармацевтическая композиция, содержащая активный компонент в терапевтически эффективном количестве, представленный общей формулой 1, или его стереоизомером, или его фармацевтически приемлемой солью, и фармацевтически приемлемый эксципиент, выбранный из наполнителя, носителя, растворителя, где замещенный эфир амидофосфорной кислоты общей формулы 1 выбран из:
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил п-толил (S)-2-оксо-тетрагидрофуран-3-ил-фосфорамидат 1(1),
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил 4-хлорфенил (S)-2-оксо-тетрагидрофуран-3-ил-фосфорамидат 1(2),
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил 2,4-дихлорфенил (S)-2-оксо-тетрагидрофуран-3-ил-фосфорамидат 1(3),
(2R,3R,5R)-5-(4-ацетамидо-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-2-(((S)-(S)-2-оксотетрагидрофуран-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-3-ил ацетат 1(4),
бензил 1-(2R,4R,5R)-4-(бензилоксикарбонилокси)-3,3-дифтор-5-(((S)-((S)-(2-оксотетрагидрофуран-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-2-ил)-2-оксо-1,2-дигидропиримидин-4-илкарбамат 1(5),
бензил 1-((2R,4R,5R)-4-(бензилоксикарбонилокси)-3,3-дифтор-5-(((1-метил-2-оксопирролидин-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-2-ил)-2-оксо-1,2-дигидропиримидин-4-илкарбамат 1(6),
бензил 1-((2R,4R,5R)-4-(бензилоксикарбонилокси)-3,3-дифтор-5-(((1-метил-2-оксопиперидин-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-2-ил)-2-оксо-1,2-дигидропиримидин-4-илкарбамат 1(7),
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопиперидин-3-илфосфорамидат 1(8),
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 2-оксооксепан-3-ил-фосфорамидат 1(9),
бензил 1-((2R,4R,5R)-4-(бензилоксикарбонилокси)-5-(((5,5-диметил-2-оксотетрагидрофуран-3-иламино)(фенокси)фосфорилокси)метил)-3,3-дифтортетрагидрофуран-2-ил)-2-оксо-1,2-дигидропиримидин-4-илкарбамат 1(10),
((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 5,5-диметил-2-оксотетрагидрофуран-3-илфосфорамидат 1(11),
(R)-((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)- 4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил ((S)-2-оксотетрагидрофуран-3-ил)фосфорамидат 1(12),
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопирролидин-3-илфосфорамидат 1(13),
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 5,5-диметил-2-оксотетрагидрофураи-3-илфосфорамидат 1(14),
(R)-((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопирролидин-3-илфосфорамидат 1(15),
((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 2-оксотетрагидрофуран-3-илфосфорамидат 1(16),
((2R,3R,4R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4-фтор-3-гидрокси-4-метилтетрагидрофуран-2-ил)метил фенил (S)-2-оксотетрагидрофуран-3-илфосфорамидат 1(17)
((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопирролидин-3-илфосфорамидат 1(18),
((2R,3R,5R)-3-(трет-бутилдиметилсилилокси)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтортетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопирролидин-3-илфосфорамидат 1(19),
((2R,3R,5R)-3-(трет-бутилдиметилсилилокси)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтортетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопиперидин-3-илфосфорамидат 1(20),
((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил (R)-2-оксотетрагидрофуран-3-илфосфорамидат 1(21)
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил (S)-2-оксотетрагидрофуран-3-илфосфорамидат 1(22),
(2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-2-((((S)-2-оксотетрагидрофуран-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-3-ил ацетат 1(23),
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-3-(трет-бутилдиметилсилилокси)-4,4-дифтортетрагидрофуран-2-ил)метил фенил (S)-2-оксотетрагидрофуран-3-илфосфорамидат 1(24),
((2R,3R,4R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4-фтор-3-гидрокси-4-метилтетрагидрофуран-2-ил)метил фенил (S)-2-оксотетрагидрофуран-3-илфосфорамидат 1(25),
((2R,3R,4R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4-фтор-3-гидрокси-4-метилтетрагидрофуран-2-ил)метил фенил 5,5-диметил-2-оксотетрагидрофуран-3-илфосфорамидат 1(26),
((2R,3R,4R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4-фтор-3-гидрокси-4-метилтетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопирролидин-3-илфосфорамидат 1(27),
(S)-((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)- 4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил ((R)-2-оксотетрагидрофуран-3-ил)фосфорамидат 1(28),
((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 1 -метил-2-оксопирролидин-3-илфосфорамидат 1(29), и
(S)-((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 1 -метил-2-оксопирролидин-3-илфосфорамидат 1(30).
Более предпочтительная фармацевтическая композиция может также добавочно содержать, по крайней мере, одну лекарственную субстанцию, выбранное из группы, включающей: ингибитор инозин 5-монофосфат дегидрогеназы, ингибитор протеазы NS3 гепатита С, ингибитор протеазы NS3/4A гепатита С и ингибитор РНК-полимеразы NS5A.
Предметом настоящего изобретения является лекарственное средство для профилактики и лечения вирусных инфекций, включая гепатит С, в форме таблеток, капсул, инъекций, мазей, ректальных суспензий и гелей, помещенных в фармацевтически приемлемую упаковку, содержащее в терапевтически эффективном количестве активный компонент, представляющий собой соединения общей формулы 1, или новую фармацевтическую композицию.
Предметом настоящего изобретения является способ профилактики и лечения заболеваний, вызванных вирусом гепатита С, заключающийся во введении в терапевтически эффективном количестве активного компонента, представляющего собой соединения общей формулы 1, или новой фармацевтической композиции субъекту, нуждающемуся в этом,
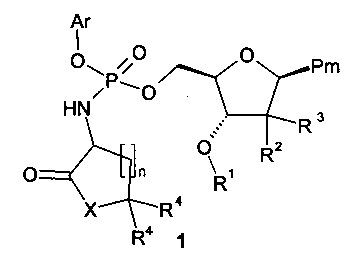
где:
R1 представляет собой водород, (СН3)2[(СН3)3С]Si, C2-C6ацил, необязательно замещенный бензилоксигруппой, NR5R6 группой, в которой R5 и R6 представляют собой независимо водород или С1-С4алкил; 1-пиррол-2-илкарбонил, пиперидин-3-илкарбонил или пиперидин-4-илкарбонил;
R2 и R3 представляют собой F или R2 представляет собой F или ОН и R3 представляет собой CH3;
R4 представляет собой водород или метил;
Ar представляет собой фенил, пиридил или нафтил, где фенил, пиридил или нафтил являются необязательно замещенными по крайней мере одним из: C1-3алкил, C2-4алкенил, C2-4алкинил, C1-3алкокси, F, Cl, Br, I, нитро, циано, -N(C1-3алкил)2;
Pm представляет собой 2,4-диоксо-3,4-дигидро-2Н-пиримидин-1-ил или 4-(4-амино-2-оксо-2Н-пиримидин-1-ил), в которых амино группа является необязательно замещенной 1-пиррол-2-илкарбонилом, пиперидин-3-илкарбонилом, пиперидин-4-илкарбонилом или радикалом C(O)R8, где R8 представляет собой C1-C4алкил, необязательно замещенный NR6R7 группой, где R6 и R7 представляют собой независимо водород или C1-C4алкил; C1-3алкокси, необязательно замещенную фенилом;
Х представляет собой О или N-R9, где R9 представляет собой C1-C4алкил, необязательно замещенный ОН или OCH3;
n=1, 2 или 3.
Согласно данному изобретению более предпочтительным является способ профилактики и лечения заболеваний, заключающийся во введении в терапевтически эффективном количестве активного компонента, представляющего собой соединения общей формулы 1, или новой фармацевтической композиции субъекту, нуждающемуся в этом, где соединения общей формулы 1 выбраны из:
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил п-толил (S)-2-оксо-тетрагидрофуран-3-ил-фосфорамидат 1(1),
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил 4-хлорфенил (S)-2-оксо-тетрагидрофуран-3-ил-фосфорамидат 1(2),
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил 2,4-дихлорфенил (S)-2-оксо-тетрагидрофуран-3-ил-фосфорамидат 1(3),
(2R,3R,5R)-5-(4-ацетамидо-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-2-(((S)-(S)-2-оксотетрагидрофуран-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-3-ил ацетат 1(4),
бензил 1-(2R,4R,5R)-4-(бензилоксикарбонилокси)-3,3-дифтор-5-(((S)-((S)-(2-оксотетрагидрофуран-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-2-ил)-2-оксо-1,2-дигидропиримидин-4-илкарбамат 1(5),
бензил 1-((2R,4R,5R)-4-(бензилоксикарбонилокси)-3,3-дифтор-5-(((1-метил-2-оксопирролидин-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-2-ил)-2-оксо-1,2-дигидропиримидин-4-илкарбамат 1(6),
бензил 1-((2R,4R,5R)-4-(бензилоксикарбонилокси)-3,3-дифтор-5-(((1-метил-2-оксопиперидин-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-2-ил)-2-оксо-1,2-дигидропиримидин-4-илкарбамат 1(7),
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопиперидин-3-илфосфорамидат 1(8),
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 2-оксооксепан-3-ил-фосфорамидат 1(9),
бензил 1-((2R,4R,5R)-4-(бензилоксикарбонилокси)-5-(((5,5-диметил-2-оксотетрагидрофуран-3-иламино)(фенокси)фосфорилокси)метил)-3,3-дифтортетрагидрофуран-2-ил)-2-оксо-1,2-дигидропиримидин-4-илкарбамат 1(10),
((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 5,5-диметил-2-оксотетрагидрофуран-3-илфосфорамидат 1(11),
(R)-((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)- 4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил ((S)-2-оксотетрагидрофуран-3-ил)фосфорамидат 1(12),
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопирролидин-3-илфосфорамидат 1(13),
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 5,5-диметил-2-оксотетрагидрофуран-3-илфосфорамидат 1(14),
(R)-((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопирролидин-3-илфосфорамидат 1(15),
((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 2-оксотетрагидрофуран-3-илфосфорамидат 1(16),
((2R,3R,4R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4-фтор-3-гидрокси-4-метилтетрагидрофуран-2-ил)метил фенил (S)-2-оксотетрагидрофуран-3-илфосфорамидат 1(17)
((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопирролидин-3-илфосфорамидат 1(18),
((2R,3R,5R)-3-(трет-бутилдиметилсилилокси)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтортетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопирролидин-3-илфосфорамидат 1(19),
((2R,3R,5R)-3-(трет-бутилдиметилсилилокси)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтортетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопиперидин-3-илфосфорамидат 1(20),
((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил (R)-2-оксотетрагидрофуран-3-илфосфорамидат 1(21)
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил (S)-2-оксотетрагидрофуран-3-илфосфорамидат 1(22),
(2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-2-((((S)-2-оксотетрагидрофуран-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-3-ил ацетат 1(23),
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-3-(трет-бутилдиметилсилилокси)-4,4-дифтортетрагидрофуран-2-ил)метил фенил (S)-2-оксотетрагидрофуран-3-илфосфорамидат 1(24),
((2R,3R,4R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4-фтор-3-гидрокси-4-метилтетрагидрофуран-2-ил)метил фенил (S)-2-оксотетрагидрофуран-3-илфосфорамидат 1(25),
((2R,3R,4R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4-фтор-3-гидрокси-4-метилтетрагидрофуран-2-ил)метил фенил 5,5-диметил-2-оксотетрагидрофуран-3-илфосфорамидат 1(26),
((2R,3R,4R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4-фтор-3-гидрокси-4-метилтетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопирролидин-3-илфосфорамидат 1(27),
(S)-((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил ((R)-2-оксотетрагидрофуран-3-ил)фосфорамидат 1(28),
((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопирролидин-3-илфосфорамидат 1(29), и
(S)-((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопирролидин-3-илфосфорамидат 1(30).
Клиническая дозировка фармацевтической композиции, содержащей в качестве активного компонента, по крайней мере, один замещенный эфир амидофосфорной кислоты общей формулы 1, или его стереоизомер, или фармацевтически приемлемую соль, может быть корректирована в зависимости от: терапевтической эффективности и биодоступности активных ингредиентов в организме пациента, скорости их обмена и выведения из организма, а также в зависимости от возраста, пола и тяжести симптомов пациента, при этом суточная доза у взрослых обычно составляет 10~500 мг. Поэтому во время приготовления фармацевтических композиций по настоящему изобретению в виде единиц дозировки необходимо учитывать вышеназванную эффективную дозировку, при этом каждая единица дозировки препарата должна содержать 10~500 мг замещенного эфира амидофосфорной кислоты общей формулы 1, или его стереоизомера, или фармацевтически приемлемой соли.
В соответствии с указаниями врача или фармацевта данные препараты могут приниматься несколько раз в течение определенных промежутков времени (предпочтительно - от одного до шести раз).
Предметом настоящего изобретения является метод ингибирования РНК-полимеразы NS5B гепатита C, включающий контактирование РНК-полимеразы NS5B гепатита C с соединениями общей формулы 1, 1.1, 1.2, 2.1 или 2.2, или их стереоизомерами, или фармацевтически приемлемыми солями.
Предметом настоящего изобретения является также терапевтический коктейль для профилактики и лечения людей и животных, инфецированных флававирусами, в том числе вирусом гепатита C, включающий в качестве одного из компонентов фармакологически эффективное количество замещенного эфира амидофосфорной кислоты общей формулы 1, или его стереоизомер, или фармацевтически приемлемую соль, или фармацевтическую композицию, содержащую замещенный эфир амидофосфорной кислоты общей формулы 1, или его стереоизомер, или фармацевтически приемлемую соль.
Терапевтические коктейли для профилактики и лечения указанных выше флававирусных заболеваний, в том числе гепатита C, наряду с лекарственными средствами по данному изобретению, могут включать другие активные компоненты, такие как: ингибиторы инозин-5-монофосфат дегидрогеназы, например, Рибавирин (разрешен) и Рибамидин; ингибиторы NS3 протеазы гепатита C, например, Телапревир и Боцепревир; ингибиторы РНК-полимеразы NS5A, например, VX222, R7128, PF-868554, ANA598; ингибиторы альфа-глюкозидазы, например, аминоуглевод Селгозивир; а также агонисты TLR-рецепторов, гепатопротекторы, циклоспорины, различные белки (например, интерфероны), антитела, вакцины и т.д.
Для комбинированной терапии любые классы агентов, которые могут оказаться полезными будучи объединены с соединениями настоящего изобретения, включают, например, нуклеозидные и ненуклеозидные ингибиторы полимеразы гепатита C, ингибиторы протеазы, ингибиторы геликазы, NS4A ингибиторы и медицинские агенты, которые функционально ингибируют внутренний рибосомный сайт вхождения (IRES), a также другие медикаменты, которые ингибируют прикрепление клетки или вхождение вируса, трансляцию РНК гепатита C, реплакацию или созревание ВГС, или выделение вируса.
Специфические соединения в этих классах и полезные в этом изобретении включают, но не ограничиваются, макроциклические, гетероциклические и линейные ингибиторы протеазы ВГС, такие как Телапревир (VX-950), Боцепревир (SCH-503034), Нарлопревир. (SCH-900518), ITMN-191 (R-7227), TMC-435350 (a.k.a. TMC-435), MK-7009, BI-201335, BI-2061 (Силупревир), BMS-650032, АСН-1625, АСЫ-1095 (ингибитор сопутствующего фактора протеазы ВГС NS4A), VX-500, VX-813, PHX-1766, PHX2054, IDX-136, IDX-316, АВТ-450 ЕР-013420 (и родственные), и ингибиторы нуклеозидной полимеразы (репликазы) ВГС, полезные в данном изобретении, включают, но не ограничиваются, R7128, PSI-7851, IDX-184, IDX-102, R1479, UNX-08189, PSI-6130, PSI-938 и PSI-879 и различные другие нуклеозиды и нуклеотидные аналоги и ингибиторы ВГС, включающие, (но не ограничивающиеся) происходящие от 2'-C-метил модифицированных нуклеозидов и нуклеотидов; и 7'-деаза модифицированных нуклеозидов и нуклеотидов. Ингибиторы ненуклеозидной полимеразы (репликазы) ВГС, полезные в данном изобретении, включают, но не ограничиваются, HCV-796, HCV-371, VCH-759, VCH-916, VCH-222, ANA-598, МК-3281, АВТ-333, АВТ-072, PF-00868554, BI-207127, GS-9190, A-837093, JKT-109, GL-59728 и GL-60667.
Кроме того, ингибиторы NS5B настоящего изобретения могут быть использованы в комбинации с антагонистами циклофиллина и имунофиллина (например, без ограничений DEBIO соединения, NM-811, а также циклоспорин и его производные), ингибиторами киназ, ингибиторами белков теплового шока (напр. HSP90, HSP70), другими иммуномодуляторными агентами, которые могут включать без ограничения интерфероны (альфа-, бета-, омега-, гамма-, ламбда- или синтетические), такие как: Intron A™, Roferon-А™, Canferon-А300™, Advaferon™, Infergen™, Humoferon™, Sumiferon MP™, Alfaferon™, IFN-β™, Feron™, и подобные, интерфероновые соединения, дериватизированные полиэтиленгликолем (пегилированные), такие как: PEG интерферон-α-2а (Pegasys™), PEG интерферон-α-2b (PEGIntron™), пегилированный IFN-α-con 1 и подобные; пролонгированные формулы и производные интерфероновых соединений, такие как: альбумин-конденсированный интерферон, Albuferon™, Locteron™, и подобные; интерфероны с различными типами контролируемой доставки (напр, ITCA-638, омега-интерферон, доставляемый подкожной системой доставки DUROS); соединения, которые стимулируют синтез интерферона в клетках, такие как Resiquimod и подобные; интерлейкины; соединения, которые улучшают развитие отклика тип 1 хелпер Т клетки, такие как: SCV-07 и подобные; TOLL- подобные агонисты рецепторов, такие как: CpG-10101 (эффект), Isotorabine, ANA773 и подобные; Thymosin α-1, ANA-245 и ANA-246, гистамин дигидрохлорид, Propagermanium; Tetrachlorodecaoxide; Ampligen; IMP-321; K.RN-7000; антитела, такие как: Civacir, XTL-6865 и подобные и профилактические и терапевтические вакцины такие как: Inno Vac, HCV E1E2/MF59 и подобные. В добавление, любой из вышеописанных методов, включающий введение NS5B ингибитора, агониста рецептора интерферона типа 1 (напр. IFN-α) и агониста рецептора интерферона типа П (напр. IFN-γ), могут быть усилены введением эффективного количества TNF-α антагониста. Типичные, но не ограниченные, TNF-α антагонисты, которые подходят для использования в такой комбинированной терапии, включают ENBREL™ и HLJMIRA™.
В дополнение, NS5B ингибиторы настоящего изобретения могут быть использованы в комбинации с антипротозоанами и другими антивирусами, считающимися эффективными при лечении ВГС инфекции, такими как: пролекарство Nitazoxanide. Nitazoxanide может быть использован как агент в комбинации с соединениями, раскрытыми в этом изобретении, а также в комбинации с другими агентами, полезными при лечении ВГС инфекции, такими как: Peginterferon alfa-2a и Ribavarin (напр. Rossignol, JF и Keeffe, ЕВ, Future Microbiol. 3:539-545, 2008).
NS5B ингибиторы настоящего изобретения могут быть также использованы в комбинации с альтернативными формами интерферонов и пегилированных интерферонов, Рибавирином или его аналогами (напр. Tarabavarin, Levovirion), микроРНК, маловредными РНК соединениями (напр. SIRPLEX-140-N и подобные), аналогами нуклеотидов или нуклеозидов, иммуноглобулинами, гепатопротекторами, противовоспалительными агентами и другими ингибиторами NS5A. Ингибиторы других мишеней в жизненном цикле ВГС включают ингибиторы NS3 геликазы; ингибиторы NS4A ко-фактора, ингибиторы антисмысловых олигонуклеотидов такие как: ISIS-14803, AVI-4065 и подобные; вектор-зашифрованную короткую «шпильку» РНК (shRNA); специфические рибозимы ВГС, такие как: Heptazyme, RPI, 139199 и подобные; ингибиторы вхождения, такие как: НереХ-С, HuMax-НерС и подобные; ингибиторы альфа-глюкозидазы, такие как: Celgosivir, UT-231B и подобные; KPE-02003002 и BIVN 401 и IMPDH ингибиторы. Другие показательные соединения - ингибиторы ВГС включают ингибиторы, раскрытые в известных научных и патентных публикациях.
Дополнительно, комбинации, например, Рибавирина и интеферона могут быть введены как комбинированная терапия с, по крайней мере, одним замещенным эфиром амидофосфорной кислоты общей формулы 1, или его стереоизомером, или фармацевтически приемлемой солью. Настоящее изобретение не ограничивается вышеуказанными классами или соединениями и рассматривает известные и новые соединения и комбинации биологически активных агентов. Имеется в виду, что комбинированные терапии настоящего изобретения включают любые химически совместимые комбинации соединений этой патентоспособной группы с другими соединениями патентоспособной группы или другими соединениями вне патентоспособной группы, а также комбинация не исключает антивирусную активность соединения этой патентоспособной группы или антивирусную активность самой фармацевтической композиции.
Комбинированная терапия может быть последовательной, т.е. лечение сначала одним агентом, а затем другим (например, когда каждый этап лечения подразумевает другое соединение настоящего изобретения или когда один этап лечения включает соединение настоящего изобретения, а другой - подразумевает один или более биологически активных агентов) или может быть лечение с обоими агентами одновременно. Последовательная терапия может включать существенное время после завершения первой стадии терапии и до начала второй стадии терапии. Лечение обоими агентами в одно и то же время может осуществляться в одной ежедневной дозе или в разных дозах. Комбинированная терапия не нуждается в ограничении двумя агентами и может включать три или более агентов. Дозы для одновременной и последовательной комбинированной терапии будут зависеть от всасывания, распределения, скоростей обмена веществ и выведения компонентов комбинированной терапии, а также других факторов, хорошо известных специалисту. Размер дозы будет также изменяться в зависимости от тяжести состояния, которое нужно облегчить. Для каждого особого субъекта специфическая схема приема доз и расписание могут быть отрегулированы по времени в соответствии с потребностью индивидуума и профессиональным суждением лица, которое лечит или наблюдает за лечением методом комбинированной терапии.
Представленные ниже примеры иллюстрируют, но не ограничивают данное изобретение.
Пример 1. Общий способ получения соединения общей формулы 1
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил (S)-2-оксотетрагидрофуран-3-илфосфорамидат 1.2(1).
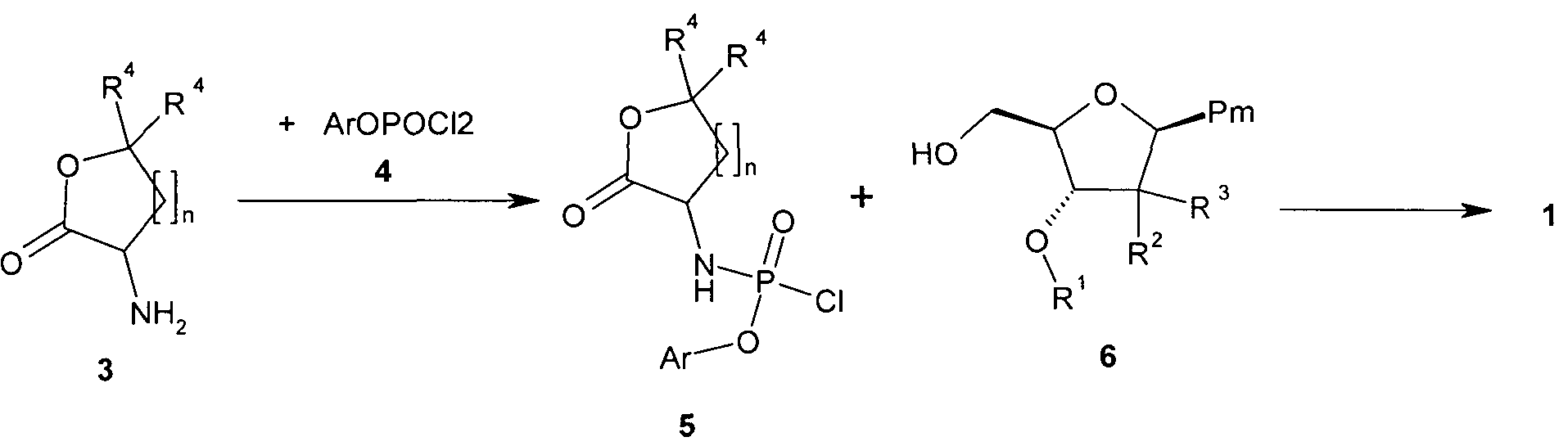
Смешивают 2.18 ммоль (300 мг) амина 3 с 2.18 ммоль арил дихлорфосфатом 4 в 15 мл дихлорметана и охлаждают в атмосфере аргона до -70°C. К полученной смеси добавляют раствор 0.6 мл триэтиламина (4.36 ммоль) в 3 мл дихлорметана и перемешивают реакционную смесь в течение 30 минут при -70°C. Удаляют охлаждение и дают реакционной смеси нагреться до комнатной температуры. Дихлорметан упаривают, остаток добавляют к эфиру, фильтруют, получают осадок, который промывают эфиром. Фильтрат упаривают и остаток хроматографируют на силикагеле, используя элюент этилацетат-гексан 1:1, 2:1. Получают арил амидохлорфосфат 5. Растворяют арил амидохлорфосфат 5 (2.9 ммоль), замещенный 1-((2R,4S,5R)-4-гидрокси-5-(гидроксиметил)тетрагидрофуран-2-ил)пиримидин-2,4(1Н,3H)-дион 6(1) (2.9 ммоль)или замещенный 4-амино-1-((2R,4S,5R)-4-гидрокси-5-(гидроксиметил)тетрагидрофуран-2-ил)пиримидин-2(1Н)-он 6(2) (2.9 ммоль) и 433 мл (2.9 ммоль) DBU в 20 мл ацетонитрила и кипятят реакционную смесь в течение 16 часов. Реакционную смесь охлаждают, разбавляют этилацетатом и промывают водой. Органический слой сушат над Na2SO4 и упаривают в вакууме. Очистку продукта осуществляют с использованием метода HPLC без кислоты в подвижной фазе. Получают соединение общей формулы 1, включающее:
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил п-толил (S)-2-оксо-тетрагидрофуран-3-ил-фосфорамидат 1(1), LC-MS (ESI) [М+Н]+ 517;
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил 4-хлорфенил (S)-2-оксо-тетрагидрофуран-3-ил-фосфорамидат 1(2), LC-MS (ESI) [М+Н]+ 537;
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил 2,4-дихлорфенил (S)-2-оксо-тетрагидрофуран-3-ил-фосфорамидат 1(3), LC-MS (ESI) [М+Н]+ 572;
бензил 1-(2R,4R,5R)-4-(бензилоксикарбонилокси)-3,3-дифтор-5-(((S)-((S)-(2-оксотетрагидрофуран-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-2-ил)-2-оксо-1,2-дигидропиримидин-4-илкарбамат 1(5), LC-MS (ESI) [М+Н]+ 771. 1H ЯМР (DMSO-d6, 400 МГц) δ 11.04 (с, 1Н), 8.02 (д, J=7.6 Гц, 1Н), 7.39 (м, 13Н), 7.23 (м, 2Н), 7.18 (м, 1Н), 7.13 (д, J=7.2 Гц, 1Н), 6.35 (т, J=8.6 Гц, 1 Н), 6.15 (дд, J1=12.4 Гц, J2=10.4 Гц, 1Н), 5.38 (м, 1Н), 5.24 (АВ sys, J=12.0 Гц, 2Н), 5.21 (с, 2Н), 4.58 (м, 1Н), 4.51 (м, 1Н), 4.43 (м, 1Н), 4.27 (м, 2Н), 4.15 (м, 1Н), 2.36 (м, 1Н), 2.01 (м, 1Н);
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 2-оксооксепан-3-ил-фосфорамидат 1(9), LC-MS (ESI) [M+H]+ 531;
((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 5,5-диметил-2-оксотетрагидрофуран-3-илфосфорамидат 1(11), LC-MS (ESI) [M+H]+ 532;
((2R,3R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 2-оксотетрагидрофуран-3-илфосфорамидат 1(16), LC-MS (ESI) [M+H]+ 504;
((2R,3R,4R,5R)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4-фтор-3-гидрокси-4-метилтетрагидрофуран-2-ил)метил фенил (S)-2-оксотетрагидрофуран-3-илфосфорамидат 1(17), LC-MS (ESI) [М+Н]+ 500, 1H ЯМР (DMSO-d6, 400 МГц) δ 11.47 (с, 1Н), 7.55 (д, J=7.6 Гц, 1Н), 7.39 (м, 2Н), 7.26 (м, 2Н), 7.19 (м, 1Н), 6.13 (м, 1Н), 6.03 (м, 1Н), 5.89 (м, 1Н), 5.58 (м, 1Н), 4.30 (м, 5Н), 4.05 (м, 1H), 3.83 (br м, 1Н), 2.33 (м, 1Н), 2.00 (м, 1Н), 1.25 (м, 3H);
((2R,3R,5R)-3-(трет-бутилдиметилсилилокси)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтортетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопирролидин-3-илфосфорамидат 1(19), LC-MS (ESI) [М+Н]+631;
((2R,3R,5R)-5-(2,4-диoкco-3,4-дигидpoпиpимидин-l(2H)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил (R)-2-oкcoтeтpaгидpoфypaн-3-илфocфopaмидaт 1(21), LC-MS (ESI) [М+Н]+504, 1Н ЯМР (DMSO-d6, 400 МГц) δ 11.61 (с, 1Н), 7.55 (м, 1Н), 7.38 (м, 2Н), 7.23 (м, 3Н), 6.50 (br м, 1H), 6.13 (м, 2Н), 5.65 (м, 1Н), 4.25 (м, 7Н), 2.34 (м, 1Н), 2.00 (м, 1H);
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-
гидрокситетрагидрофуран-2-ил)метил фенил (S)-2-оксотетрагидрофуран-3-илфосфорамидат 1(22), LC-MS (ESI) [М+Н]+503, 1Н ЯМР (DMSO-d6, 400 МГц): δ 7,70 (д, J=7,2 Гц, 1Н), 7,40 (м, 4Н), 7,25 (м, 3Н), 6,38 (м, 1Н), 6,22 (м, 1Н), 5,80 (д.д, J1=7,6 Гц, J2=2,8 Гц, 1Н), 5,20 (б.с, 1Н), 5,05 (м, 1H), 4,28 (м, 2Н), 3,58-4,22 (м, 4Н), 2,40 (м, 1Н), 2,04 (м, 1Н);
((2R,3R,5R)-5-(2,4-диoкco-3,4-дигидpoпиpимидин-l(2H)-ил)-3,4-дигидpoкcи-4-метилтетрагидрофуран-2-ил)метил фенил (S)-2-оксотетрагидрофуран-3-илфосфорамидат, LC-MS (ESI) [М+Н]+498;
((2R,3R,5R)-5-(4-aминo-2-oкcoпиpимидин-l(2H)-ил)-4,4-дифтop-3-гидрокситетрагидрофуран-2-ил)метил пиридин-2-ил(S)-2-оксо-тетрагидрофуран-3-ил-фосфорамидат, LC-MS (ESI) [М+Н]+504;
((2R,3R,5R)-5-(4-aминo-2-oкcoпиpимидин-l(2H)-ил)-4,4-дифтop-3-гидрокситетрагидрофуран-2-ил)метил нафталин-1-ил(S)-2-оксо-тетрагидрофуран-3-ил-фосфорамидат, LC-MS (ESI) [М+Н]+553;
((2R,3R,5R)-5-(4-aминo-2-oкcoпиpимидин-l(2H)-ил)-4,4-дифтop-3-гидрокситетрагидрофуран-2-ил)метил 4-винилфенил(S)-2-оксо-тетрагидрофуран-3-ил-фосфорамидат, LC-MS (ESI) [М+Н]+529;
((2R,3R,5R)-5-(4-aминo-2-oкcoпиpимидин-l(2H)-ил)-4,4-дифтop-3-гидрокситетрагидрофуран-2-ил)метил 3-этинилфенил(S)-2-оксо-тетрагидрофуран-3-ил-фосфорамидат, LC-MS (ESI) [М+Н]+527;
((2R,3R,5R)-5-(4-aминo-2-oкcoпиpимидин-l(2H)-ил)-4,4-дифтop-3-гидрокситетрагидрофуран-2-ил)метил3-метоксифенил(S)-2-оксо-тетрагидрофуран-3-ил-фосфорамидат, LC-MS (ESI) [М+Н]+533;
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил 4-нитрофенил (S)-2-оксо-тетрагидрофуран-3-ил-фосфорамидат, LC-MS (ESI) [М+Н]+548;
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил 4-цианофенил (S)-2-оксо-тетрагидрофуран-3-ил-фосфорамидат, LC-MS (ESI) [М+Н]+528;
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1 (2Н)-ил)-4,4-дифтор-3-
гидрокситетрагидрофуран-2-ил)метил 4-(диметиламино)фенил (8)-2-оксо-тетрагидрофуран-3-ил-фосфорамидат, LC-MS (ESI) [М+Н]+546.
Пример 2. Общий способ получения соединений общей формулы 1
К раствору 0.8 ммоль арил фосфордихлоридат 4 в 5 мл MeCN по каплям добавляют раствор 0.67 ммоль спирта 6 и N-метилимидазола (55 мг, 0.67 ммоль) в 4 мл MeCN при -10°C и смесь перемешивают при -10°C в течение 5 ч. После чего добавляют раствор 0.8 ммоль амина гидрохлорида 8 и N-метилимидазола (131 мг, 1.6 ммоль) в 10 мл DCM и перемешивают смесь при комнатной температуре в течение 12 ч. Смесь упаривают в вакууме. Очистку продукта осуществляют используя метод HPLC без кислоты в подвижной фазе. Получают соединения общей формулы 1,1.1 and 1.2, включающие: бензил 1-((2R,3R,5R)-4-(бензилоксикарбонилокси)-3,3-дифтор-5-(((1-метил-2-оксопирролидин-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-2-ил)-2-оксо-1,2-дигидропиримидин-4-илкарбамат 1(6), LC-MS (ESI) [М+Н]+784;
бензил 1-((2R,3R,5R)-4-(бензилоксикарбонилокси)-3,3-дифтор-5-(((1-метил-2-оксопиперидин-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-2-ил)-2-оксо-1,2-дигидропиримидин-4-илкарбамат 1(7), LC-MS (ESI) [М+Н]+798;
((2R,3R,5R)-3-(трет-бутилдиметилсилилокси)-5-(2,4-диоксо-3,4-дигидропиримидин-1(2Н)-ил)-4,4-дифтортетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопиперидин-3-илфосфорамидат 1(20), LC-MS (ESI) [М+Н]+645;
((2R,3R,5R)-5-(4-(1-пиррол-2-илкарбониламино)-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-(1-пиррол-2-илкарбонилокси)тетрагидрофуран-2-ил)метил фенил 2-оксо-тетрагидрофуран-3-ил-фосфорамидат, LC-MS (ESI) [М+Н]+689;
бензил 1-((2R,3R,5R)-4-(бензилоксикарбонилокси)-3,3-дифтор-5-(((1-гидроксиметил-2-
оксопирролидин-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-2-ил)-2-оксо-1,2-дигидропиримидин-4-илкарбамат, LC-MS (ESI) [М+Н]+800;
бензил1-((2R,3R,5R)-4-(бензилоксикарбонилокси)-3,3-дифтор-5-(((1-метоксиметил-2-
оксопирролидин-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-2-ил)-2-оксо-1,2-дигидропиримидин-4-илкарбамат, LC-MS (ESI) [М+Н]+814.
Пример 3. (2R,3R,5R)-5-(4-Ацетамидо-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-2-(((S)-(S)-2-оксотетрагидрофуран-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-3-ил ацетат 1(4) и (2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-2-((((S)-2-оксотетрагидрофуран-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-3-ил ацетат 1(23). К раствору соединения 1(22) (100 мг, 0.2 ммоль) в 2 мл пиридина добавляют Ac2O (41 мг, 0.4 ммоль) и смесь перемешивают в течение 12 ч. Раствор упаривают в вакууме, остаток растворяют в DCM, промывают водой, сушат над Na2SO4, упаривают в вакууме и разделяют методом HPLC без кислоты. Получают соединение 1(23), LC-MS (ESI) [М+Н]+545, 1Н ЯМР (DMSO-d6, 400 МГц) δ 7.44 (м, 5Н), 7.23 (м, 3Н), 6.18 (м, 2Н), 5.74, 5.79 (2д, J=7А Гц, 1Н), 5.38 (brm, 1Н), 4.40 (м, 3Н), 4.26 (м, 2Н), 4.15 (м, 2Н), 2.35 (м, 1H), 2.14, 2.15 (2 с, 3Н), 2.01 (м, 1Н) и соединение 1(4), LC-MS (ESI) [М+Н]+587, 1Н ЯМР (DMSO-d6, 400 МГц) δ 11.05 (с, 1Н), 7.93, 8.04 (2д, J=7.6 Гц, 1Н), 7.38 (м, 2Н), 7.23 (м, 5Н), 6.34 (м, 1H), 6.17 (м, 1Н), 5.42 (м, 1Н), 4.45 (м, 3Н), 4.27 (м, 2Н), 4.16 (м, 2Н), 2.35 (м, 1Н), 2.15, 2.16 (2 с, 3Н), 2.12 (с, 3Н), 2.01 (м, 1Н);
Аналогичным способом из соответствующих исходных соединений получают ((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-(метиламиноэтилкарбонилокси)тетрагидрофуран-2-ил)метил фенил (S)-2-оксо-тетрагидрофуран-3-ил-фосфорамидат, LC-MS (ESI) [М+Н]+588;
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-(пиперидин-3-илкарбонилокси)тетрагидрофуран-2-ил)метил фенил (S)-2-оксо-тетрагидрофуран-3^ил-фосфорамидат, LC-MS (ESI) [М+Н]+614;
((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-(пиперидин-4-илкарбонилокси)тетрагидрофуран-2-ил)метил фенил (S)-2-оксо-тетрагидрофуран-3-ил-фосфорамидат, LC-MS (ESI) [М+Н]+614;
((2R,3R,5R)-5-(4-(метиламиноэтилкарбониламино)-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-(метиламиноэтилкарбонилокси)тетрагидрофуран-2-ил)метил фенил (S)-2-оксо-тетрагидрофуран-3-ил-фосфорамидат, LC-MS (ESI) [М+Н]+673.
Пример 4. ((2R,3R,5R)-5-(4-Амино-2-оксопиримидин-1(2Н)-ил)-3-(трет-бутилдиметилсилилокси)-4,4-дифтортетрагидрофуран-2-ил)метил фенил (S)-2-оксотетрагидрофуран-3-илфосфорамидат 1(24). К раствору соединения 1(22) (112 мг, 0.22 ммоль) в 1 мл пиридина добавляют TBDMSCl (84 мг, 56 ммоль) и смесь перемешивают при 50°C в течение 48 ч. Раствор упаривают в вакууме, остаток растворяют в DCM, промывают водой, сушат над Na2SO4, упаривают в вакууме и очищают хроматографированием на SiO2 (элюент MeCN: i-PrOH=10:1). Получают соединение 1(24), LC-MS (ESI) [М+Н]+617, 1Н ЯМР (DMSO-d6, 400 МГц) δ 7.50 (м, 1Н), 7.40 (м, 4Н), 7.22 (м, 3Н), 6.20 (м, 1Н), 6.12 (м, 1Н), 5.78 (м, 1H), 4.38 (м, 2Н), 4.26 (м, 3Н), 4.12 (м, 2Н), 2.33 (м, 1Н), 0.88 (с, 9Н), 0.10 (с, 3Н), 0.09 (с, 3Н).
Пример 5. Бензил l-((2R,4R,5R)-4-(бензилоксикарбонилокси)-5-(((5,5-диметил-2-оксотетрагидрофуран-3-иламино)(фенокси)фосфорилокси)метил)-3,3-дифтортетрагидрофуран-2-ил)-2-оксо-1,2-дигидропиримидин-4-илкарбамат 1(10) и ((2R,3R,5R)-5-(4-aминo-2-oкcoпиpимидин-l(2H)-ил)-4,4-дифтop-3-гидрокситетрагидрофуран-2-ил)метил фенил 5,5-диметил-2-оксотетрагидрофуран-3-илфосфорамидат 1(14) получают в соответствии со следующей схемой.
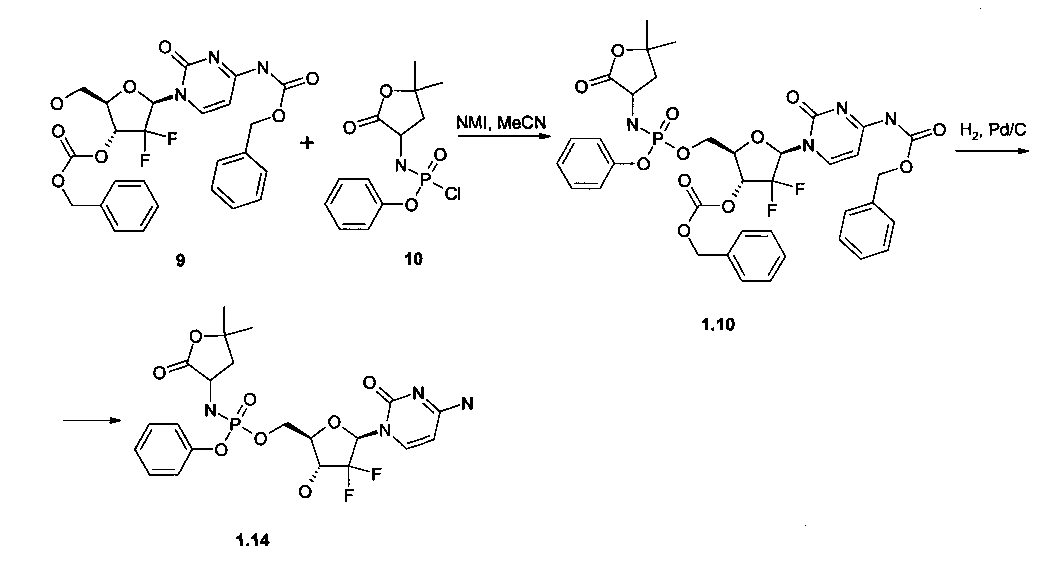
Раствор 673 мг (1.27 ммоль) бис-CBZ-гемцитабина 9, 500 мг (1.65 ммоль) фенил 5,5-диметил-2-оксо-тетрагидрофуран-3-илфосфорамидохлоридата 10 и 135 мг (1.65 ммоль) N-метилимидазола в 20 мл сухого MeCN кипятят в течение 48 ч. Смесь упаривают в вакууме, растворяют в 40 мл DCM, промывают дважды водой, сушат над Na2SO4 и упаривают в вакууме. Остаток растворяют в смеси 1:1 CHCl3/Ме2СО и фильтруют через слой 2 см SiO2, упаривают в вакууме. Получают соединение 1(10), LC-MS [М+Н]+799, которое гидрируют в 25 мл i-PrOH над 100 мг 10% Pd/C. HPLC разделение проводят без кислоты и получают соединение 1(14), LC-MS (ESI) [М+Н]+531, 1Н ЯМР (DMSO-d6, 400 МГц) δ 7.48 (м, 1Н), 7.39 (м, 4Н), 7.23 (м, 3Н), 6.43 (м, 1Н), 6.14 (м, 2Н), 5.75 (м, 1Н), 4.35 (м, 3Н), 4.19 (м, 1Н), 4.05 (м, 1Н), 2.33 (м, 1Н), 1.85 (м, 1Н), 1.35 (с, 3Н), 1.31 (с, 3Н).
Пример 6. ((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил (S)-2-оксотетрагидрофуран-3-илфосфорамидат 1(22). Раствор 2 г (2.6 ммоль) соединения 1(5) гидрируют в 150 мл изопропанола над 200 мг 10% Pd/C. После завершения реакции (LC-MS контроль) смесь фильтруют через целит, упаривают в вакууме и очищают хроматографированием на колонке с SiO2 (элюент MeCN: t-BuOH=5:1), получают соединение 1(22), LC-MS (ESI) [М+Н]+503, 1Н ЯМР (DMSO-d6, 400 МГц) δ 7.44, 7.49 (2д, J=7.6 Гц, 1H), 7.39 (м, 4Н), 7.23 (м, 3Н), 6.40, 6.44 (2д, J=6.0 Гц, 1Н), 6.14 (м, 2H), 5.73, 5.77 (2д, J=7.6 Гц, 1Н), 4.42 (м, 1H), 4.35 (м, 1Н), 4.27 (м, 2Н), 4.17 (м, 2Н), 4.05 (м, 1Н), 2,35 (м, 1Н), 2,01 (м, 1Н).
Пример 7. ((2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-3-гидрокситетрагидрофуран-2-ил)метил фенил 1 -метил-2-оксопирролидин-3-илфосфорамидат 1(13), его (S)- 1(15) и (R)-изомер 1(30). Раствор соединения 1(6) (108 мг, 0.14 ммоль) гидрируют в 20 мл диоксана над 100 мг 10% Pd/C и получают соединение 1(13), LC-MS (ESI) [М+Н]+516. 1Н ЯМР (DMSO-d6, 400 МГцz) δ 7.47 (м, 2Н), 7.37 (м, 3Н), 7.27 (м, 2Н), 7.19 (м, 1Н), 6.42 (м, 1Н), 6.18 (м, 1Н), 5.89 (м, 1Н), 5.75 (м, 1H), 4.32 (м, 3Н), 4.05 (м, 1Н), 3.82 (м, 1Н), 3.20 (м, 2Н), 2.73 (с, 3Н), 2.19 (м, 1Н), 1.67 (м, 1Н). HPLC разделение без кислоты дает быстро движущийся изомер, предположительно (R)-изомер 1(30), LC-MS (ESI) [М+Н]+516, и медленно движущийся изомер, предположительно (8)-изомер 1(15), LC-MS (ESI) [М+Н]+516.
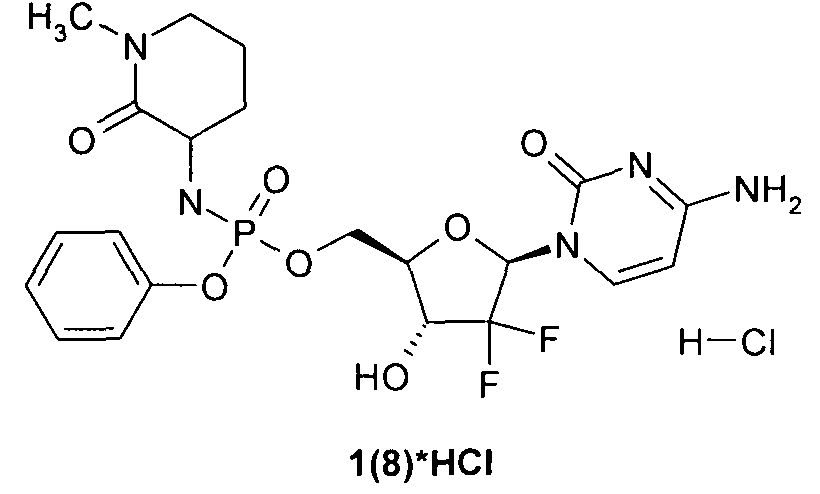
Пример 8. ((2R,3R,5R)-5-(4-aминo-2-oкcoпиpимидин-l(2H)-ил)-4,4-дифтop-3-гидрокситетрагидрофуран-2-ил)метил фенил 1-метил-2-оксопиперидин-3-илфосфорамидат 1(8). Раствор соединения 1(7) (194 мг, 0.24 ммоль) гидрируют в 20 мл этанола над 100 мг 10% Pd/C. HPLC разделение без кислоты дает соединение 1(8), LC-MS (ESI) [М+Н]+530. Соединение 1(8) растворяют в небольшом количестве метанола и добавляют эквивалентное количество 0,2 М хлористого водорода в метаноле. Растворитель отгоняют, полученный продукт промывают эфиром и сушат в вакууме. Выход гидрохлорида 1(8)*HCl 90%.
Пример 9. Получение фармацевтической композиции в форме таблеток. Смешивают 1600 мг крахмала, 1600 мг измельченной лактозы, 400 мг талька и 1000 мг (2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-2-((((8)-2-оксотетрагидрофуран-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-3-ил ацетат 1(23). Полученный брусок измельчают в гранулы и просеивают через сита, собирая гранулы размером 14-16 меш. Полученные гранулы таблетируют в подходящую форму таблетки весом 560 мг каждая.
Пример 10. Получение фармацевтической композиции в форме капсул. Тщательно смешивают (2R,3R,5R)-5-(4-aминo-2-oкcoпиpимидин-l(2H)-ил)-4,4-дифтop-2-((((S)-2-оксотетрагидрофуран-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-3-ил ацетат 1(23) с порошком лактозы в соотношении 2:1. Полученную порошкообразную смесь упаковывают по 300 мг в желатиновые капсулы подходящего размера.
Пример 11. Получение фармацевтической композиции в форме инъекционных композиций для внутримышечных, внутрибрюшинных или подкожных инъекций. Смешивают 500 мг смешивают (2R,3R,5R)-5-(4-амино-2-оксопиримидин-1(2Н)-ил)-4,4-дифтор-2-((((S)-2-оксотетрагидрофуран-3-иламино)(фенокси)фосфорилокси)метил)тетрагидрофуран-3-ил ацетат 1(23) с 300 мг хлорбутанола, 2 мл пропиленгликоля и 100 мл инъекционной воды. Полученный раствор фильтруют и помещают по 1 мл в ампулы, которые запаивают.