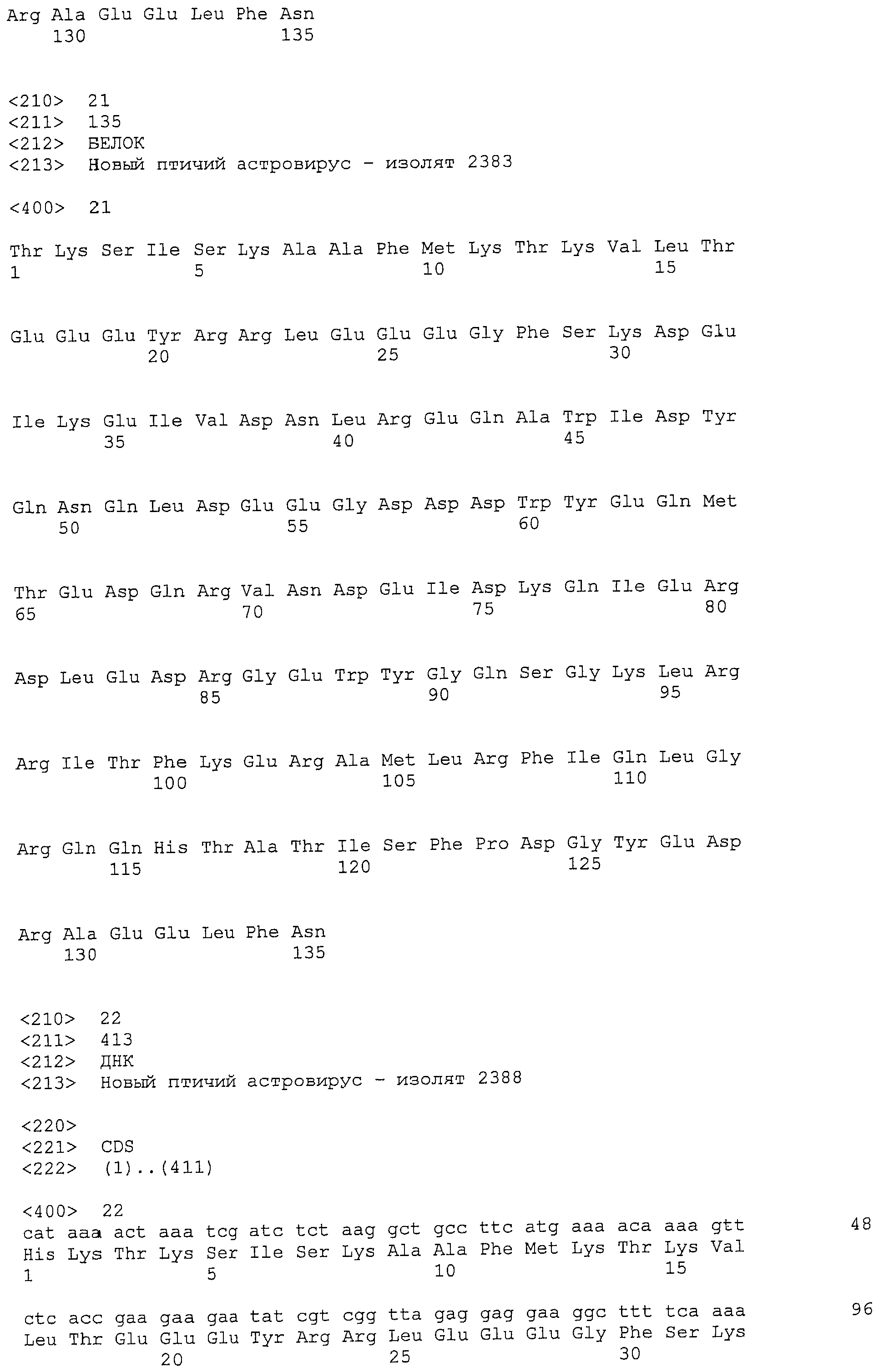Результат интеллектуальной деятельности: НОВЫЙ ПТИЧИЙ АСТРОВИРУС
Вид РИД
Изобретение
Настоящее изобретение относится к области ветеринарии, вирусологии и иммунологии. В частности, настоящее изобретение относится к новому птичьему астровирусу; к антителам и их фрагментам, направленным против нового птичьего астровируса; к антигенным препаратам, белкам и ДНК-молекулам нового птичьего астровируса; к вакцинам на основе нового птичьего астровируса или к их антигенным препаратам, белку или ДНК; к способам получения таких вакцин и к диагностическим наборам.
Астровирусы представляют собой небольшие круглые вирусы без оболочки, имеющие одноцепочечный РНК-геном с положительной смысловой цепью. Большинство астровирусов вызывают энтериты определенного типа, ассоциирующиеся с диареей, рвотой, малабсорбцией, общим недомоганием и задержкой роста. Инфицирование человека или животных этим вирусом может приводить к летальному исходу и плохо поддается лечению, например, у молодых и пожилых индивидуумов или у индивидуумов с ослабленной иммунной системой. См.: Matsui and Greenberg (in: Fields virology, 3rd ed., 1996, ed.: B. Fields et al., ISBN: 781702534, chapter 26), и Moser and Schultz-Cherry (2005, Viral Immunology, vol. 18, p. 4-10).
Кроме того, тяжесть патологии, вызываемой астровирусом, может варьироваться в зависимости от вирулентности самих астровирусов различных типов или штаммов. Поэтому, существует мнение, что некоторые астровирусы действуют как вторичные патогены, которые сами по себе вызывают лишь субклиническое заболевание, а все клинические симптомы заболевания проявляются лишь в том случае, если другой причиной данного заболевания является какой-либо иной патоген.
Механизм, посредством которого развивается иммунитет против инфекции астровирусом, также пока еще точно не изучен, но, вероятно, существуют вирус-нейтрализующие антитела, которые, очевидно, играют определенную роль в осуществлении защиты и создании иммунологической памяти, однако, вероятно, они являются не только эффекторами иммунных ответов против астровирусной инфекции. См. M. Koci (2005, Viral Immunology, vol. 18, p. 11-16).
Астровирусы распространены по всему миру и были выделены у широкого ряда животных. В свою очередь, из видов астровирусов, инфицирующих некоторых животных-мишеней, описаны лишь несколько серотипов. Таксономически, семейство астровирусов подразделяется на два основных рода: астровирусы млекопитающих: мамастровирус, и птичьи астровирусы: авастровирусы. В настоящее время известно, что род авастровирусов включает официально известные виды: вирусы 1 и 2 птичьего нефрита (ANV1,2) (куриные), и астровирусы индейки 1 и 2 (TAstV1,2).
Некоторые другие птичьи астровирусы были выделены у уток, кур, страусов и индеек. Так, например, куриный астровирус 2 (CAstV2) был описан Baxendale и Mebatsion (2004, Avian pathology, vol. 33, p. 364-370; и в Международной патентной заявке WO 2004/027053), а Todd и др. описали вирус CAstV3 (WO 2007/077464), который является близкородственным вирусу CAstV2. Эти астровирусы пока еще не были официально классифицированы, как сообщалось в публикации Koci и Schulz-Cherry (2002, Avian Pathology vol. 31, p. 213-227).
Астровирусы обладают очень высокой стабильностью в условиях окружающей среды, например, они могут сохранять резистентность к общим липидам-растворителям и к детергентам, обладают устойчивостью к значениям рН широкого ряда и являются сравнительно термостабильными. Эти их свойства, наряду с высокой инфекционностью и способностью легко передаваться по фекально-пероральному пути передачи инфекции, позволяют объяснить, почему астровирусы или антитела против астровирусов могут присутствовать у такого большого числа людей и животных во всем мире.
В настоящее время, по мере получения новых экспериментальных данных, классификация этих небольших РНК-вирусов и названия, присваиваемые этим вирусам, часто меняются. Так, например, утиный астровирус (DAstV) раньше был классифицирован как пикорнавирус, а первоначально он назывался вирусом утиного гепатита типа II, так как такой вирус вызывает гепатит. Аналогичным образом, ANV1 раньше был описан как пикорнавирус, а в частности, энтеровирус, но затем он был переклассифицирован в авастровирус (Imada et al., 2000, J. of Virology, vol. 74, p. 8487-8493). ANV1 также называется куриным астровирусом 1 (CAstV1) и вызывает нефрит.
Переклассификация этих вирусов была произведена после получения новой информации о последовательности и организации генома этого вируса. В частности, что касается астровирусов, то было обнаружено, что информация о физических, электронно-микроскопических и биохимических свойствах данных вирусов в большинстве случаев является недостаточной для идентификации астровирусов от других так называемых «небольших круглых вирусов» или «вирусов, подобных энтеровирусам», таких как пикорнавирус, калицивирус или Hepeviridae (вирусов, подобных вирусу гепатита Е), или даже от оболочечных РНК-вирусов, таких как реовирусы, ротавирусы или коронавирусы, которые вызывают заболевания, симптомы которых очень напоминают симптомы заболеваний, вызываемых астровирусами. Это обусловлено тем, что данные о таких свойствах могут варьироваться в зависимости от применяемого метода и от используемых условий. Поэтому, в настоящее время пока еще недостаточно данных для получения точной информации.
С другой стороны, данные о молекулярно-биологических свойствах, таких как генотипирование, в комбинации с данными об иммунологических свойствах, подробно описаны в литературе и могут быть воспроизведены на уровне, достаточном для отнесения данного микроорганизма к конкретной таксономической группе (Van Regenmortel et al., 2000, in: Virus Taxonomy, 7th report of the ICTV, Academic press, New York). Поэтому, в идеальном случае, такие данные получают путем осуществления секвенирования нуклеотидов, а также путем проведения анализов с помощью полимеразной цепной реакции (ПЦР) и анализов по серологическому типированию.
РНК-геном вируса Astroviridae имеет размер приблизительно 7 т.п.н., а организация генома этого вируса является типичной для вирусов данного семейства, см.: Jiang et al. (1993, PNAS-USA, vol. 90, p. 10539-10543) и Koci et al. (2000, J. of Virology, vol. 74, p. 6173-6177). В соответствии с общепринятым мнением, этот геном включает три явно распознаваемых открытых рамок считывания (ОРС) в направлении 5'→3':
ОРС1а: имеет размер приблизительно 3 т.п.н. и кодирует неструктурный белок, имеющий мотив сериновой протеазы.
OPC1b: имеет размер приблизительно 1,5 т.п.н., частично перекрывается с OPC1a и кодирует неструктурную РНК-зависимую РНК-полимеразу.
ОРС2: кодирует структурные вирусные белки посредством субгеномной РНК размером приблизительно 2 т.п.н. Перед сборкой вируса, экспрессируемый полипротеин, вероятно, расщепляется на более мелкие части и содержит другие капсидные или оболочечные белки.
Из трех ОРС, OPC1b имеет наиболее консервативную нуклеотидную последовательность по сравнению с нуклеотидными последовательностями астровируса, которые являются общеизвестными, а ОРС2 представляет собой ОРС, последовательность которой является наиболее вариабельной.
Начиная с 1987 года и до сегодняшнего дня, при выращивании домашней птицы на фермах в Нидерландах, в Германии и в Объединенных Арабских Эмиратах, у этих птиц обнаруживались некоторые конкретные патологические состояния, а именно, у кур и индеек наблюдалась диарея, снижение степени метаболизма корма и снижение роста, а также патологии, ассоциированные с распуханием и болезненностью суставов и сухожилий ног. Такие патологии были обнаружены у птиц-бройлеров, племенных птиц и птиц-несушек различного возраста, и у различных сельскохозяйственных видов без какой-либо явной взаимосвязи.
В первую неделю и в последующие несколько месяцев у птиц наблюдалась хромота. У этих птиц наблюдалось распухание скакательных (заплюсневых) суставов и сухожилий сгибательной плюсны нижних конечностей, причем, на обоих участках наблюдался избыток прозрачной слегка вязкой жидкости и обнаруживались симптомы артрита. У этих птиц наблюдалось снижение уровня метаболизма корма и снижение скорости роста, что, наиболее вероятно, является результатом нарушения двигательной системы. В худших случаях, птицы были уже неспособны двигаться, а поэтому больше не могли подходить к корму или питью, что приводило к их гибели. Такие поражения конечностей наиболее часто наблюдались у птиц высокопродуктивной породы типа бройлеров, однако, экономический ущерб оставался значительным и в отношении птиц всех видов.
Еще большую проблему представляла диарея, которая наблюдалась, главным образом, у более молодых птиц, а также у птиц, несущих яйца. Симптомы варьировались от нарушения пищеварения до истинного энтерита и приводили к снижению уровня метаболизма пищи, к замедлению роста или даже к потере веса, к ухудшению яйценоскости («откладывания яиц»); к увеличению числа яиц плохого качества и к гибели птиц.
На некоторых фермах такие проблемы наблюдались в течение нескольких лет, что приводило к постоянному низкому показателю продуктивности без всяких видимых причин.
После исследований post mortem, в некоторых случаях, помимо тонкого кишечника и сустав лап были также обнаружены поражения и в других частях тела, такие как эрозия преджелудка или увеличение печени.
Для выявления причин развития этих симптомов были исследованы аспекты лечения и кормления, однако, какой-либо взаимосвязи с патологическими нарушениями, наблюдаемыми в этих случаях, не обнаруживалось. Кроме того, были исследованы патогены, которые могут быть ответственны, в частности, за реовирусную инфекцию, поскольку хорошо известно, что этот вирус вызывает малабсорбцию и поражения суставов. Однако, несмотря на проведение ряда анализов, во многих случаях, реовирус не был обнаружен.
Были также исследованы, рутинным способом или в частном порядке, некоторые другие патогены, которые, как известно, вызывают аналогичные симптомы, например, такие патогены, как Salmonella, Mycoplasma, Haemophilus и Pasteurella; и вирусы, такие как аденовирус, вирус инфекционного бронхита (IBV), вирус ньюкаслской болезни (NDV), вирус инфекционного бурсита (IBDV), возбудитель синдрома кладки яиц (EDS) и вирус птичьего гриппа (AIV).
До настоящего времени, несмотря на тяжесть указанных поражений и на проблемы, связанные со здоровьем животных и экономическим ущербом от снижения продаж домашней птицы, какого-либо этиологического фактора, вызывающего поражения конечностей и тонкого кишечника, не было обнаружено.
Следовательно, крайне необходимо идентифицировать фактор, связанный с наблюдаемыми симптомами заболеваний, и получить вакцины и диагностические средства, что позволило бы предупреждать эти заболевания и выявить их возбудитель.
Новый вирус неожиданно был обнаружен у кур и индеек, страдающих кишечными заболеваниями и нарушением двигательной системы. Этот вирус может быть выделен из суставов и сухожилий, а также из различных внутренних органов больных птиц различного возраста, вида и происхождения. Выделенный вирус, в свою очередь, индуцировал аналогичные симптомы заболевания после инфицирования здоровых тестируемых животных, и этот вирус мог быть снова выделен у больных тестируемых животных и проанализирован в соответствии с постулатами Коха.
Этот новый вирус может быть использован для разработки диагностических анализов и вакцин в целях обнаружения и уничтожения вируса, а также для лечения патологических состояний, вызываемых этим вирусом у домашней птицы, а в частности, заболеваний суставов, сухожилий и желудочно-кишечного тракта.
Новый вирус был проанализирован различными способами и неожиданно был идентифицирован как астровирус. Поскольку, этот вирус присутствует преимущественно у кур и индеек, он был предварительно классифицирован как птичий астровирус.
Наряду со многими другими свойствами этого нового вируса было установлено, что он не имеет оболочки, на что указывают результаты двух последовательных экстракций хлороформом, после которых экстрагированный образец вируса был еще способен вызывать специфическое патогенное действие в яйцах кур SPF с развивающимся эмбрионом.
На присутствие РНК-генома в новом вирусе указывает тот факт, что нуклеиновая кислота, подходящая для последующего анализа, могла быть получена только после экстракции РНК и ОТ-ПЦР, но не после выделения ДНК и проведения стандартной ПЦР.
Неожиданно было обнаружено, что наиболее близкородственными (уже различаемыми) являются вирусы типа ANV1, а поэтому новые птичьи астровирусы, описанные в настоящей заявке, представляет собой новую группу вирусов птичьего нефрита, предварительно классифицированных как вирусы ANV3.
Однако, авторами настоящего изобретения был неожиданно обнаружен ряд признаков, по которым можно отличить новые птичьи астровирусы, описанные в настоящей заявке, от вирусов ANV1 и других (астро-)вирусов, и однозначно охарактеризовать различные изоляты нового птичьего астровируса как изоляты, принадлежащие к новой и отдельной группе таких вирусов.
Главным отличительным свойством этих вирусов является присутствие специфической нуклеотидной последовательности, которая может быть идентифицирована путем проведения анализа нуклеотидной последовательности и ПЦР-анализа.
Были также обнаружены отдельные патологические симптомы, индуцированные в результате инфицирования эмбрионов. Специфические иммунологические различия были выявлены путем серотипирования с помощью VN- или IFT-анализов. Все эти анализы описаны ниже в разделе «Экспериментальные результаты» и «Подробное описание».
Настоящее изобретение относится к выделенному новому птичьему астровирусу, имеющему геномную область с открытой рамкой считывания (OPC) 1a, и отличающемуся тем, что ОРС1а указанного птичьего астровируса, при ее сравнении с ОРС1а вируса птичьего нефрита 1, содержит вставку из 12 нуклеотидов, где указанная вставка расположена между нуклеотидами, соответствующими нуклеотидам 2485 и 2486 последовательности SEQ ID NO: 1.
Предпочтительными «птичьими» организмами является домашняя птица, а более предпочтительно, птицы, выбранные из группы, состоящей из кур, индеек, уток и гусей. Наиболее предпочтительными являются куры.
Термин «астровирус» указывает на взаимосвязь группы новых вирусов согласно изобретению с вирусами, которые в настоящее время описаны и классифицированы как вирусы, принадлежащие к таксономическому семейству Astrovirideae. Однако, для специалиста в этой области очевидно, что таксономическая классификация может со временем меняться, поскольку появляющиеся новые данные могут привести к пересмотру классификации и созданию новых или других таксономических групп. Однако, поскольку такой пересмотр не изменяет свойств вируса согласно изобретению, а изменяет только его классификацию, то такие переклассифицированные организмы входят в объем настоящего изобретения.
В частности, настоящее изобретение охватывает все вирусы, входящие в подклассы птичьих астровирусов согласно изобретению, а именно, в подвиды, штаммы, изоляты, генотипы, серотипы, варианты или подтипы и т.п.
Поэтому, в соответствии с настоящим изобретением, «асторвирус» представляет собой вирус, имеющий отличительные признаки вируса, классифицированного как астровирус. Такие отличительные признаки относятся, например, к молекулярным, биохимическим и биологическим признакам, а именно, что такие вирусы имеют одноцепочечный РНК-геном с положительной смысловой цепью, содержащий ОРС, идентифицируемые как 1a, 1b и 2; представляют собой вирион без оболочки размером примерно 28-30 нм; и вызывают энтерит.
Термин «геномная область» означает часть генетического материала нового астровируса согласно изобретению. Такая область состоит из нуклеиновой кислоты, а в случае нового птичьего астровируса согласно изобретению, такой нуклеиновой кислотой является РНК.
Геном нового птичьего астровируса согласно изобретению содержит, как и все другие астровирусы, области, распознаваемые как ОРС1а, 1b и 2, и области, соответствующие этим ОРС.
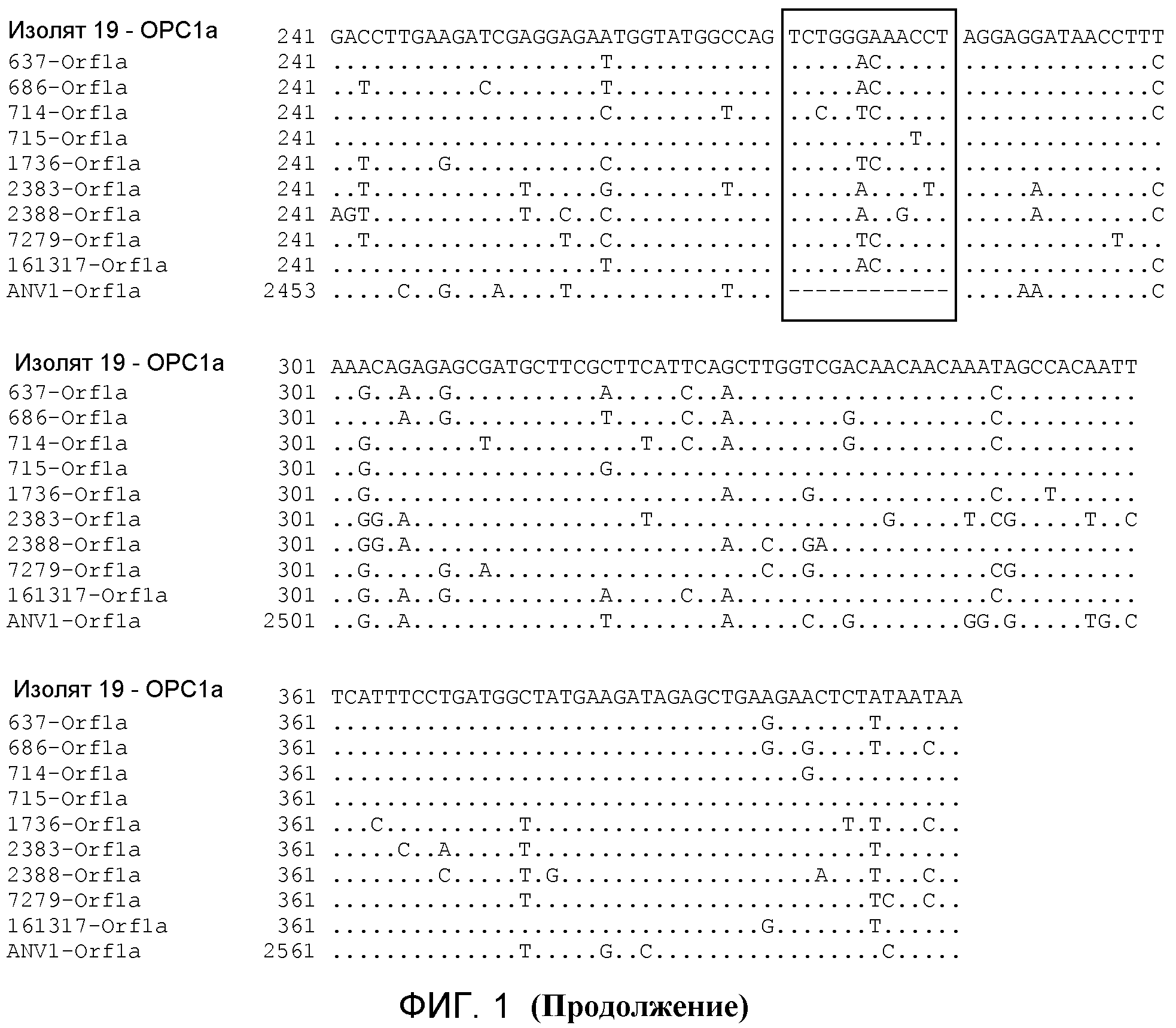
Однако неожиданно было обнаружено, что новый птичий астровирус имеет в своей геномной области ОРС1а некоторые нуклеотиды, которые отсутствуют в ОРС1а ANV1 или астровируса (птичьего) любого другого типа. Эти нуклеотиды присутствуют в форме линейных и непрерывных фрагментов из 12 нуклеотидов и, по сравнению с последовательностью ОРС1а ANV1, они представляют собой вставку в этой области. «Вставка» из 12 нуклеотидов присутствует в ОРС1а всех изолятов, тестируемух групп новых птичьих астровирусов, описанных в настоящей заявке.
Локализация вставки из 12 нуклеотидов, присутствующей в ОРС1а изолятов новых птичьих астровирусов, описанных в настоящей заявке, указана посредством ссылки на нумерацию, приведенную для геномной последовательности известного штамма ANV1, который был описан Imada et al. (2000, J. of Virology, vol. 74, p. 8487-8493). кДНК-последовательность геномной последовательности этого штамма ANV1 также имеется в Интернете в базе данных нуклеотидов Американского национального института здравоохранения, известной как GenBank, под регистрационным номером AB033998, и представлена в настоящей заявке как SEQ ID NO: 1.
Во всех изолятах новых птичьих астровирусов согласно изобретению, вставка из 12 нуклеотидов в ОРС1а была расположена между нуклеотидами, соответствующими нуклеотидам 2485 и 2486 последовательности SEQ ID NO: 1.
В настоящее время неизвестно, может ли вставка из 12 нуклеотидов в ОРС1а нового птичьего астровируса согласно изобретению, которая отсутствует в ОРС1а ANV1, влиять на поведение этого нового птичьего астровируса, а также неизвестно, каким образом такая вставка влияет на поведение данного астровируса. Не ограничиваясь какой-либо теорией, авторы настоящего изобретения лишь предполагают, что факт существования вставки из 12 нуклеотидов, и, тем самым, из 4 триплетов, которые сохраняют трансляционную рамку ОРС1а в интактной форме, позволяет кодируемым 4 дополнительным аминокислотам включаться в неструктурные белки, экспрессируемые из ОРС1а. Существует очень большая вероятность того, что такая вставка будет влиять на патобиологическое поведение вирусов, например, на их вирулентность и способность вызывать заболевание тонкой кишки, а также ног, суставов и сухожилий.
Тем не менее тот факт, что эти 12 нуклеотидов присутствуют в геномной области OPC1a описанных здесь новых птичьих астровирусов, но не в ОРС1а ANV1 или других (птичьих) астровирусов, указывает на возможность получения позитивного генетического маркера для этой новой группы вирусов.
Как хорошо известно специалистам в данной области, генетическим маркером является особенность генетического материала организма, то есть, область, расположенная в некоторых геномных участках, которая может быть использована для выявления определенного различия или для корреляции, и может быть детектирована техническими методами. Если, как и в данном случае, такая особенность наблюдается у идентифицируемой группы, то она представляет собой «позитивный» генетический маркер для этой группы.
Указанная нуклеотидная последовательность вставки из 12 нуклеотидов, которая характеризует новый птичий астровирус согласно изобретению, может не идентифицироваться во всех изолятах нового птичьего астровируса, описанного в настоящей заявке, однако, ее размер и локализация являются идентичными. Консенсусная последовательность данной нуклеотидной последовательности вставки из 12 нуклеотидов, представляет собой:
5'-TCYGGDMARYYT-3', и обозначена здесь как SEQ ID NO: 2.
Поэтому, в своем предпочтительном варианте, настоящее изобретение отличается тем, что вставка из 12 нуклеотидов имеет последовательность нуклеиновой кислоты, представленную в SEQ ID NO: 2.
Специалисту в данной области известно, что последовательность SEQ ID NO: 2 представляет собой так называемую «денатурированную» праймерную последовательность, где указаны положения (в данном случае, Y, D, M и R), в которых может присутствовать один из ряда нуклеотидов. Одним из кодов, часто используемых для указания денатурированных оснований, является код ИЮПАК (IUPAC) (опубликованный в Biochem. J., 1985, vol. 229, p. 281-286), где: R=G или A; Y=T или C; M=A или C; K=G или T; S=G или C; W=A или T; H=A, C, или T; B=G, T или C; V=G, C или A; D=G, A или T; и N=G, A, T или C.
Что касается нового описанного здесь птичьего астровируса, то присутствие этого детектируемого генетического маркера позволяет идентифицировать новый вирус и его новую группу путем детектирования, например, посредством секвенирования ДНК или ПЦР.
Секвенирование ДНК представляет собой хорошо известный метод, а стандартные протоколы и оборудование, например, для проведения высокоскоростного автоматического секвенирования, широко применяются специалистами в данной области. Наиболее часто используемыми протоколами являются протоколы, в которых применяется «циклическое секвенирование» на основе ПЦР с последующим проведением электрофореза с высокой степенью достоверности.
Что касается секвенирования нуклеиновых кислот РНК-вирусов, таких как астровирусы, то исследование нуклеиновой кислоты необходимо осуществлять в форме ДНК-копии (кДНК), поскольку пока еще невозможно проводить секвенирование РНК. Для получения кДНК существует множество стандартных протоколов и коммерчески доступных наборов. В таких протоколах используется фермент обратная транскриптаза. Для инициации процедуры копирования обычно используется праймер.
Примером подходящего праймера для проведения реакции с обратной транскриптазой является ДНК-олигонуклеотид, представленный здесь как SEQ ID NO: 3 и имеющий последовательность: 5'-TCG WTS CTA CYC-3'. Этот праймер указан авторами настоящего изобретения как праймер 17.
Указанный праймер гибридизуется с отдаленной 3'-областью генома многих птичьих астровирусов, начиная с нуклеотида, соответствующего нуклеотиду 6731 SEQ ID NO: 1, и такая гибридизация происходит в обратном направлении.
На фигуре 1 проиллюстрировано выравнивание множества последовательностей кДНК фрагмента ОРС1а полученных из выбранного числа изолятов птичьих астровирусов согласно изобретению. Такие последовательности выравнивают с соответствующей частью генома эталонного вируса ANV1, представленного в SEQ ID NO:1. Как хорошо видно из участка, очерченного рамкой, все изоляты имеют область из 12 нуклеотидов, которая отсутствует в ОРС1а ANV1. Последовательности SEQ ID NO кДНК ОРС1а изолятов птичьего астровируса согласно изобретению представлены в таблице 1.
Аналогичным образом, на фигуре 2 проиллюстрировано выравнивание множества предполагаемых аминокислотных последовательностей, полученных путем компьютерной трансляции последовательностей кДНК, перечисленных на фигуре 1. Как видно из участка, очерченного рамкой, белок, кодируемый ОРС1а птичьих астровирусов согласно изобретению, содержит 4 аминокислоты, которые отсутствуют в белке, кодируемом ОРС1а вируса ANV1. SEQ ID NO транслированной последовательности ОРС1а изолятов птичьего астровируса согласно изобретению перечислены в таблице 1.
Что касается изолятов птичьих астровирусов согласно изобретению, то большое число природных изолятов было взято в течение определенного периода времени у кур и индеек, страдающих заболеваниями ног и/или тонкого кишечника, описанными выше. Было проанализировано множество изолятов из числа изолятов, входящих в новую группу птичьих астровирусов согласно изобретению, описанных в настоящей заявке. Однако для определения нового птичьего астровируса в рамках природных изменений, имеющихся в этой группе, в настоящей заявке представлен весь набор только проанализированных изолятов.
В таблице 1 приводится описание изолятов птичьего астровируса согласно изобретению, указанных в настоящей заявке. В таблице 1 также приводится список SEQ ID NO кДНК и предполагаемых последовательностей белка, происходящих от ОРС1 а, 1b и 2 данного набора изолятов.
|
|
Изолят птичьих астровирусов согласно изобретению может быть получен от птиц, страдающих заболеваниями тонкого кишечника или ног, путем взятия образца из одного или нескольких органов, либо из суставов или сухожилий ног. Образцы, если это необходимо, могут быть гомогенизированы, и, например, смешаны с соответствующим буферным раствором, предпочтительно содержащим антибиотики.
Для амплификации вирусного титра таких изолятов могут быть использованы различные субстраты, такие как птичьи клеточные линии или птичьи яйца с развивающимся эмбрионом. При использовании яиц, суспензия может быть инокулирована в птичьи яйца с развивающимся эмбрионом и культивирована в этих яйцах. Могут быть проведены различные способы инокуляции, такие как инокуляция на хорио-аллантоисной оболочке (CAM) или в желточный мешок или в полости с аллантоисной жидкостью. Первые несколько раундов инокуляции, предпочтительно, проводят в желточном мешке, а остальные раунды (если это необходимо) могут быть проведены в аллантоисной жидкости. Могут быть использованы примерно 5-7-дневные куриные яйца SPF (свободные от специфических контаминантов) с развивающимся эмбрионом. Все эти методы хорошо известны специалистам в данной области, а куриные яйца SPF соответствующего качества и возраста являются коммерчески доступными и поставляются, например, фирмами Spafas® или Lohmann®.
После инкубирования в течение 2-7 дней в соответствующих условиях могут быть собраны эмбрионы, хорио-аллантоисные оболочки (CAM) или (предпочтительно) аллантоисная жидкость. При необходимости, могут быть проведены дополнительные раунды амплификации на яйцах путем инокуляции в желточный мешок или в аллантоисную жидкость. И наконец, может быть собрана аллантоисная жидкость, содержащая большое количество птичьего астровируса согласно изобретению.
Для ПЦР-секвенирования обеих цепей репрезентативной части ОРС1а могут быть использованы нижеследующие праймеры:
SEQ ID NO: 28: 5'-AAA GGK AAG ACD AAG ARR RAC MG-3', и
SEQ ID NO: 29: 5'-TCG CCT TCT GGA AGG TCT TCA-3'.
Авторами настоящего изобретения эти секвенирующие праймеры были названы праймерами F-II и R-II-3, соответственно. SEQ ID NO: 28 гибридизуется начиная с нуклеотидов, соответствующих нуклеотиду 2171 и далее нуклеотидам ANV1 (SEQ ID NO:1); SEQ ID NO: 29 гибридизуется с нуклеотидами, начинающимися с нуклеотида 2640 последовательности SEQ ID NO:1, и такая гибридизация происходит в обратном направлении (см. таблицу 4). Таким образом, геномная область ОРС1а птичьего астровируса согласно изобретению, содержащая 12 нуклеотидов, отсутствующих в ANV1, покрывается частью ОРС1а, которая является секвенированной.
Для компьютерного анализа определенных последовательностей ДНК, эти последовательности усекают так, чтобы они не содержали денатурированных последовательностей от самих праймеров. Кроме того, для достижения репрезентативного выравнивания необходимо, чтобы сравниваемые последовательности имели одинаковую длину. Кроме того, выравнивание осуществляют так, чтобы оно покрывало всю длину усеченных последовательностей.
Так, например, в случае использования праймеров SEQ ID NO: 28 и 29, длина сравниваемой последовательности составляет примерно 400-425 нуклеотидов.
Стандартной компьютерной программой для таких манипуляций и выравниваний является программа Clone Manager™ (Scientific and Educational software™), и альтернативно, доступными программами являются программы, имеющиеся в Интернете: «ClustalW» для множественного выравнивания и «Translate» для трансляций, причем, обе эти программы имеются на сайте www.expasy.org; или программы «Blast», имеющиеся на сайте www.ncbi.nlm.nih.gov. Предпочтительно, используются параметры весовых коэффициентов по умолчанию.
Для многих изолятов птичьего астровируса согласно изобретению, секвенирование кДНК проводят с использованием праймеров SEQ ID NO: 28 и 29. Набор отобранных усеченных нуклеотидных последовательностей представлен здесь последовательностями SEQ ID NO: 4, 10, 12, 14, 16, 18, 20, 22, 24 и 26, указанными в таблице 1.
Эти последовательности сопоставляли друг с другом с использованием в качестве эталона последовательности одного изолята, выделенного у курицы и обозначенного как 161319, где указанный изолят был назван авторами настоящего изобретения «изолятом 19». Кроме того, проводили выравнивание нескольких последовательностей ДНК соответствующих частей ОРС1а от других астровирусов, имеющихся в базе данных GenBank, например, ANV1 (AB033998, SEQ ID NO: 1), индюшачьего астровируса 1 (TAstV1) (Y15936), индюшачьего астровируса 2 (AF206663), овечьего астровируса (Y15937), астровируса норки (AY179509) и человеческого астровируса (Z25771); а дефисы между ними означают соответствующие регистрационные номера GenBank.
Из этих последовательностей ОРС1а других астровирусов, только последовательность в ANV1, а в частности, часть, соответствующая нуклеотидам 2213-2607 SEQ ID NO:1, имеет последовательность, идентичность которой является значимой, что означает, что процент идентичности нуклеотидных последовательностей значительно превышает 50%. Что касается остальных других астровирусов, то только TAstV1 (GenBank рег. №: Y15936) имеет детектируемую, но почти незначимую идентичность последовательностей в части нуклеотидов 2450-2856. Эти последовательности представлены в таблице 2.
|
|
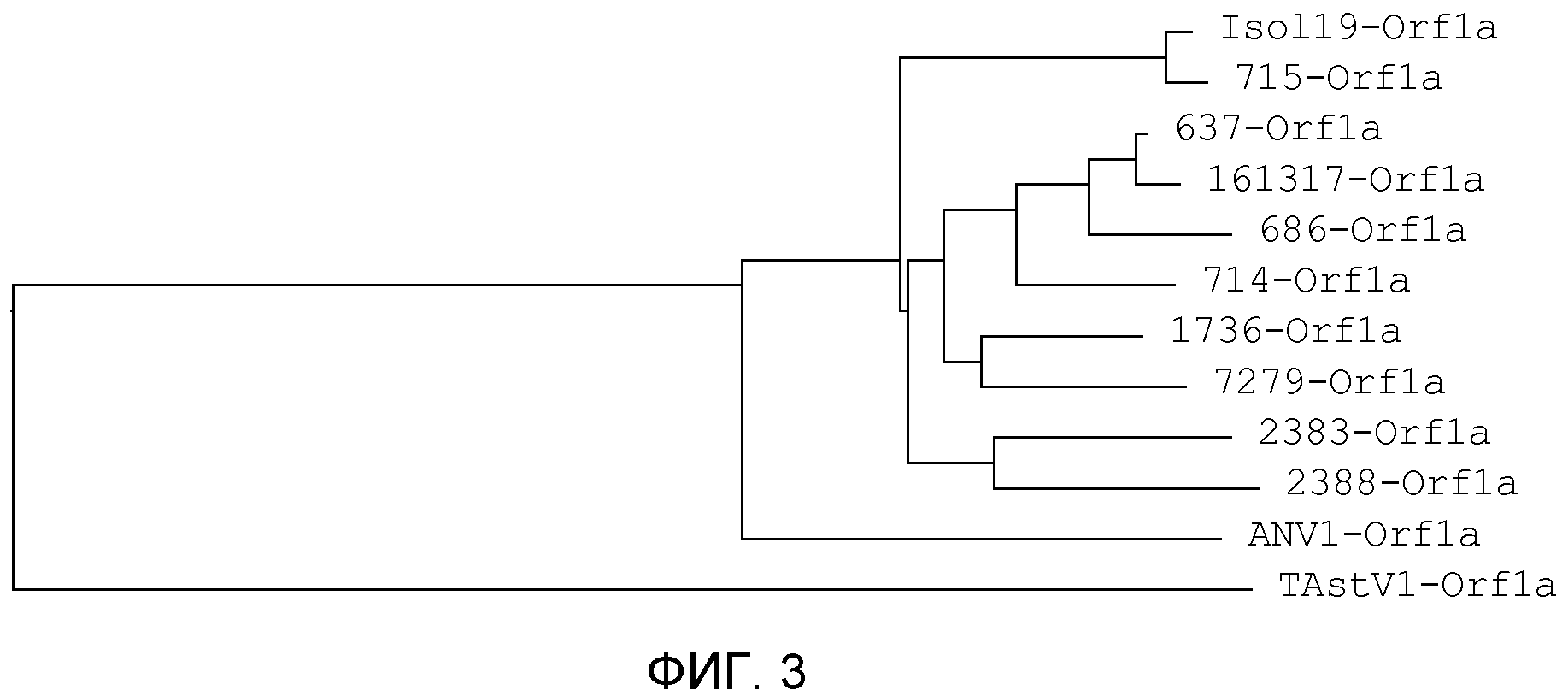
Дендрографическое дерево, построенное на основании результатов выравнивания этих нуклеотидных последовательностей, представлено на фигуре 3.
Таким образом, было неожиданно обнаружено, что группа новых птичьих астровирусов согласно изобретению отличается от всех других астровирусов, как птичьих, так и вирусов млекопитающих, то есть, их нуклеотидные последовательности, при сравнении областей последовательностей ОРС1а ДНК, соответствующих SEQ ID NO:4, имеют идентичность 88% или более.
Поэтому, в своем предпочтительном варианте, настоящее изобретение относится к птичьему астровирусу согласно изобретению, отличающемуся тем, что ОРС1а указанного птичьего астровируса содержит область, имеющую нуклеотидную последовательность, которая по меньшей мере на 88% идентична последовательности SEQ ID NO:4.
Более предпочтительно, настоящее изобретение относится к птичьему астровирусу согласно изобретению, отличающемуся тем, что ОРС1а указанного птичьего астровируса содержит область, имеющую нуклеотидную последовательность, которая по меньшей мере на 89%, а более предпочтительно, на 90, 91, 92, 93, 94, 95, 96, 97, 98, 99 или 100 %, в порядке предпочтительности, идентична последовательности SEQ ID NO: 4.
В других предпочтительных вариантах изобретения, для характеризации птичьего астровируса согласно изобретению, помимо SEQ ID NO:4, может служить любая из нуклеотидных последовательностей части ОРС1а, описанных в SEQ ID NO: 10, 12, 14, 16, 18, 20, 22, 24 и 26.
Аналогично множественному выравниванию нуклеотидных последовательностей ОРС1а, представленных в таблице 2, может быть осуществлено выравнивание предполагаемых аминокислотных последовательностей, кодируемых усеченными последовательностями нуклеиновой кислоты, представленными в таблице 2, а именно, SEQ ID NO: 4, 10, 12, 14, 16, 18, 20, 22, 24 и 26. Полученные аминокислотные последовательности, транслированные с помощью компьютера, представлены здесь как SEQ ID NO: 5, 11, 13, 15, 17, 19, 21, 23, 25 и 27. Сравниваемой последовательностью является SEQ ID NO: 5, то есть, предполагаемая аминокислотная последовательность части ОРС1а изолята 19. Выравнивание было также проведено с помощью программы Align+, в которой применяется выравнивание по всей длине SEQ ID NO: 5. Результаты представлены в таблице 3.
|
Выравнивание аминокислот подробно проиллюстрировано на фигуре 2.
Результат анализов этой аминокислотной последовательности был сравнимым с результатами, представленными в таблице 2, то есть, аминокислотные последовательности изолятов птичьего астровируса согласно изобретению были более родственными по отношению друг к другу, чем по отношению к другим птичьим астровирусам. Проценты идентичности аминокислотных последовательностей различных изолятов птичьего астровируса согласно изобретению с последовательностью SEQ ID NO:5 составляют 93-99%, тогда как идентичность с вирусом ANV1 является более низкой и составляет 88%.
Поэтому, в своем предпочтительном варианте, настоящее изобретение относится к птичьему астровирусу согласно изобретению, отличающемуся тем, что ОРС1а указанного птичьего астровируса кодирует аминокислотную последовательность, включающую область, имеющую аминокислотную последовательность, которая по меньшей мере на 93% идентична последовательности SEQ ID NO: 5.
Более предпочтительно, настоящее изобретение относится к птичьему астровирусу согласно изобретению, отличающемуся тем, что ОРС1а указанного птичьего астровируса кодирует аминокислотную последовательность, включающую область, имеющую аминокислотную последовательность, которая по меньшей мере на 94%, а более предпочтительно, на 95, 96, 97, 98, 99 или 100%, в порядке предпочтительности, идентична последовательности SEQ ID NO: 5.
В других предпочтительных вариантах изобретения, для характеризации птичьего астровируса согласно изобретению, помимо SEQ ID NO:5, может служить любая из предполагаемых транслированных нуклеотидных последовательностей части ОРС1а, описанных в SEQ ID NO: 11, 13, 15, 17, 19, 21, 23, 25 и 27.
Помимо секвенирования и выравнивания нуклеотидов может быть идентифицирован позитивный генетический маркер птичьих астровирусов согласно изобретению путем проведения ПЦР-теста для детектирования присутствия 12 нуклеотидов в области ОРС1а птичьих астровирусов согласно изобретению, которые отсутствуют в ОРС1а ANV1, например, в образцах, взятых у птиц с заболеванием тонкой кишки или нарушением двигательной способности.
Поэтому, в другом предпочтительном варианте изобретения, птичий астровирус согласно изобретению отличается тем, что из ОРС1а указанного птичьего астровируса может быть продуцирован ПЦР-продукт примерно из 260 нуклеотидов в ПЦР-анализе с использованием набора праймеров, представленных в SEQ ID NO: 30 и 31.
Были использованы следующие ПЦР-праймеры:
SEQ ID NO: 30: 5'-GTY CTY ACC GAR GAR GAR TAY C-3'
SEQ ID NO: 31: 5'-AAD GTT ATY CTC CTA RGB TKH C-3'
Эти праймеры были названы авторами настоящего изобретения «праймерами 29 и 30», соответственно.
Эти праймеры гибридизуются с нуклеотидами, соответствующими нуклеотиду ANV1 (SEQ ID NO:1) № 2252 и далее, и с нуклеотидом № 2499, и такая гибридизация происходит в обратном направлении.
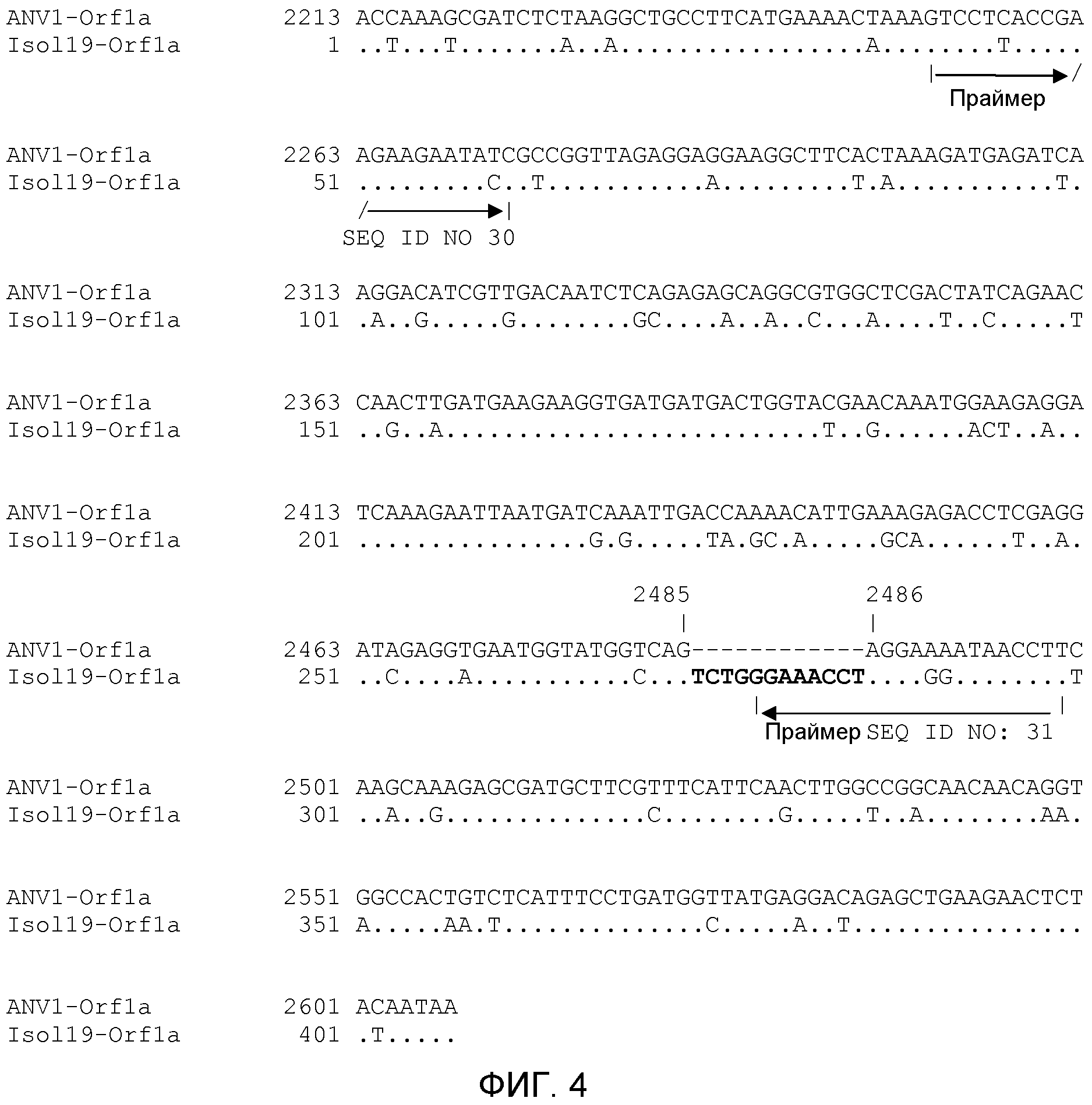
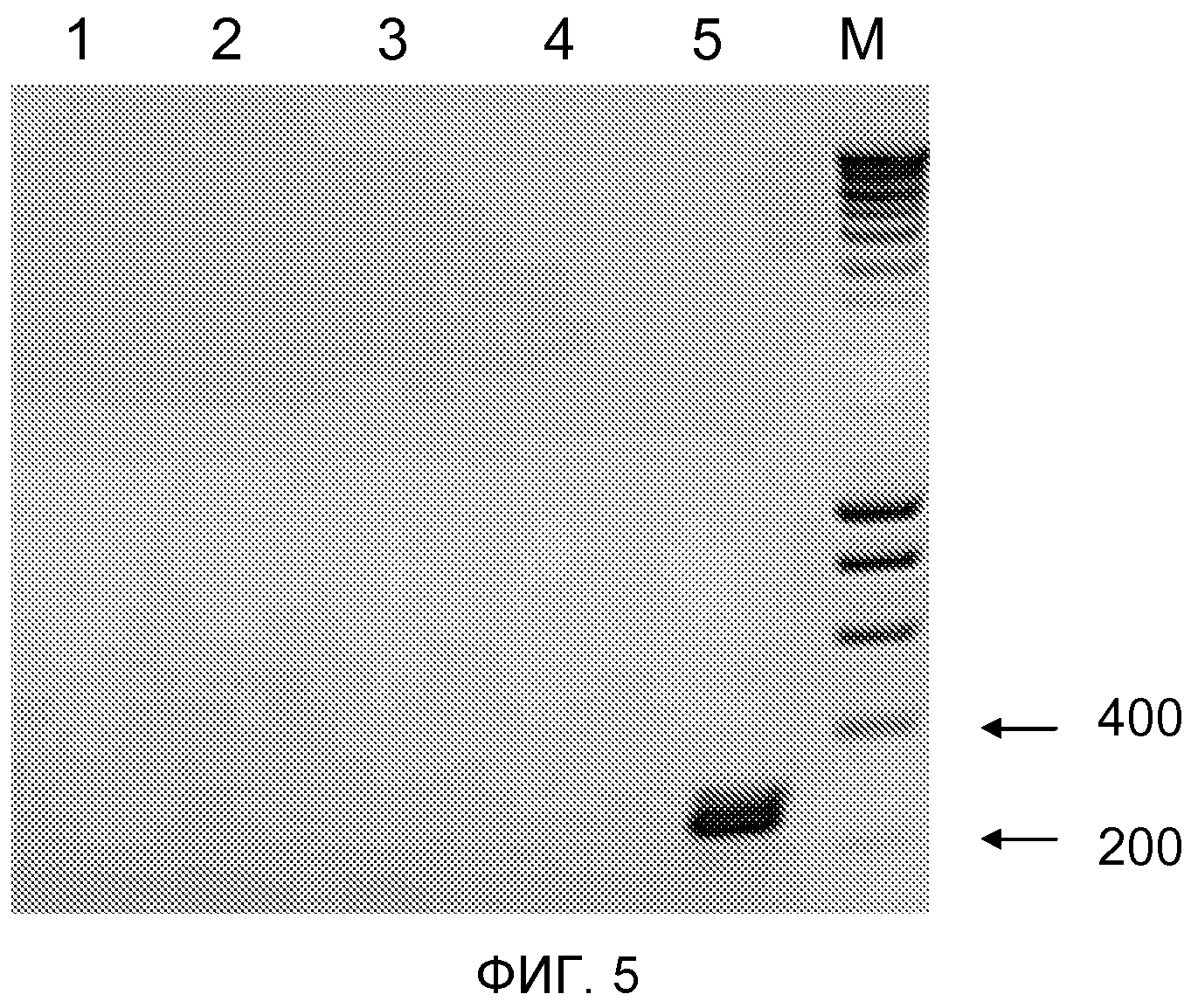
Продуцированный ПЦР-продукт был визуализирован на геле в виде полосы приблизительно из 260 нуклеотидов (в эту полосу включена длина самих праймеров). Эта полоса продуцировалась только в том случае, если исходный продукт содержал ДНК, включающую область ОРС1а птичьих астровирусов согласно изобретению, поскольку только эти последовательности содержат 12 нуклеотидов, которые отсутствуют в ОРС1а ANV1. Графическое представление специфического связывания праймеров SEQ ID No: 30 и 31, по отношению к локализации области из 12 нуклеотидов, проиллюстрировано на фигуре 4.
В таких ПЦР-анализах, специфичность и чувствительность определяют с помощью специфической ПЦР используемых праймеров, а в частности, по последовательности и длине праймеров. Оптимизация селективности и чувствительности может быть затем достигнута путем адаптации условий проведения реакции и условий проведения циклов, таких как температура и продолжительность стадий проведения реакции, хорошо известных специалистам в данной области.
Эти и другие методы, применяемые в молекулярной биологии, более подробно объяснены в стандартных руководствах, таких как руководство Sambrook & Russell: "Molecular cloning: a laboratory manual" (2001, Cold Spring Harbour Laboratory Press; ISBN: 0879695773); Ausubel et al., in: Current Protocols in Molecular Biology (J. Wiley and Sons Inc, NY, 2003, ISBN: 047150338X); C. Dieffenbach & G. Dveksler: "PCR primers: a laboratory manual" (CSHL Press, ISBN 0879696540); и "PCR protocols", by: J. Bartlett and D. Stirling (Humana press, ISBN: 0896036421).
В основном, ПЦР-реакцию, проводимую с использованием праймеров SEQ ID No: 30 и 31, объединяют с ОТ-реакцией, а затем непосредственно проводят ОТ-реакцию, необходимую для продуцирования кДНК, после чего проводят объединенный ОТ-ПЦР-анализ, описанный в примерах.
ОТ-ПЦР-анализ, описанный в настоящей заявке, был применен авторами настоящего изобретения на ряде образцов, при этом, позитивные результаты были получены для образцов изолятов нового птичьего астровируса согласно изобретению, а «позитивным» ПЦР-результатом является визуализация продукта реакции, содержащего приблизительно 260 пар нуклеотидов и полученного после электрофореза, по сравнению с соответствующими позитивными и негативными результатами, полученными для контрольных образцов. Однако, в соответствии с этим было обнаружено, что ОТ-ПЦР-образцы, полученные от родственных птичьих астровирусов ANV1 и куриного астровируса 2 (CAstV2), дали отрицательный результат в ПЦР, проводимой с использованием праймеров SEQ ID No: 30 и 31.
Примеры таких результатов ПЦР-теста проиллюстрированы на фигуре 5, где представлена фотография агарозного геля, который был окрашен этидий-бромидом и облучен УФ-светом, и на котором ПЦР-продукты были подвергнуты ПЦР с использованием праймеров SEQ ID No: 30 и 31. Только образец изолята 19 обнаруживал положительную реакцию, тогда как образцы, содержащие ANV1 или CAstV2, давали отрицательный результат как и негативный контроль.
Неожиданно было обнаружено, что очень заметный и ярко выраженный патологический эффект наблюдался после инфицирования птичьих яиц с развивающимся эмбрионом птичьим астровирусом согласно изобретению и инкубирования этих яиц с указанным астровирусом, а именно, у пораженного эмбриона наблюдалось окрашивание ног и кончиков крыльев в ярко-красный цвет. Такой эффект никогда не наблюдался и не был описан ранее. Кроме того, у инфицированного эмбриона наблюдались и другие, но менее выраженные признаки, а именно, генерализованное окрашивание в светло-красный цвет, отек брюшной полости и значительное увеличение печени, которая приобретала темно-красную/пурпурную окраску.
Такая специфическая патология наблюдалась приблизительно через 2-7 дней после инфицирования куриных яиц SPF с развивающимся эмбрионом, и почти всегда приводила к гибели эмбриона в зависимости от титра инокулированного вируса.
Для сравнения, одновременно была проведена инокуляция вирусом ANV1 яиц с развивающимся эмбрионом с использованием аналогичных условий теста. ANV1 также индуцировал распухание печени, но в этом случае, печень имела даже еще более темную окраску, а весь эмбрион был темно-красного цвета. Однако, ANV1 никогда не индуцировал специфическое окрашивание ног и кончиков крыльев в ярко-красный цвет, как это наблюдалось для изолятов птичьего астровируса согласно изобретению.
Поэтому, в другом предпочтительном варианте изобретения, птичий астровирус согласно изобретению отличается тем, что он обладает способностью индуцировать окрашивание ног и кончиков крыльев куриных эмбрионов в красный цвет после инокуляции куриных яиц SPF с развивающимся эмбрионом в возрасте примерно 5-7 дней с последующим их инкубированием в течение 2-7 дней или даже в течение более длительного периода времени, если это необходимо.
Как описано выше, куриные яйца SPF с развивающимся эмбрионом и оборудование для их инкубирования являются коммерчески доступными. Обычно, инкубирование куриных яиц с развивающимся эмбрионом осуществляют примерно при 35-39°C в инкубаторах с повышенной влажностью.
Инокуляция может быть осуществлена любым стандартным способом, например, в хорио-аллантоисную оболочку (CAM), в желточный мешок или в аллантоисную жидкость.
Как известно специалистам, специфическое окрашивание ног и кончиков крыльев в ярко-красный цвет не будет заметным в тех случаях, когда, например, количество вируса, который был инокулирован, является крайне низким (не позволяющим выделить этот вирус) или очень высоким (вызывающим гибель еще до окрашивания); или в тех случаях, когда эмбрионы не имеют достаточно высокое качество, позволяющее осуществлять репликацию вируса. В общих чертах, специфическое окрашивание в ярко-красный цвет может наблюдаться после инокуляции примерно от 10 до 106 EID50/яйцо (EID50 = доза, инфицирующая 50% яиц).
Один конкретный изолят птичьих астровирусов согласно изобретению, названный изолятом 19, был дополнительно очищен и амплифицирован в целях его использования в качестве эталонного образца, а затем он был депонирован. Этот изолят был очищен путем лимитирующего разведения на клетках печени куриного эмбриона (CEL). Каждый раз, наивысшее разведение, еще индуцирующее цитопатический эффект (сре) на клетках CEL, пересевали. Затем этот очищенный вирус амплифицировали путем проведения трех раундов амплификации вируса в аллантоисной полости куриных яиц SPF с развивающимся эмбрионом. Аллантоисную жидкость собирали и хранили в замороженном виде. Этот очищенный вирус титровали на куриных яйцах SPF с развивающимся эмбрионом, в результате чего было обнаружено, что титр вируса составлял 6,1 log10 EID50/мл. Этот материал выдерживали в лиофилизованном виде в стандартном стабилизирующем буфере и хранили при -20°С. Затем подтверждали его стерильность. После этого, образцы данного вирусного материала депонировали в Национальной коллекции культур микроорганизмов (CNCM) Института Пастера, в Париже, Франция, под депозитарным номером: CNCM I-3895 23 января 2008.
Поэтому, в другом предпочтительном варианте изобретения, птичьим астровирусом согласно изобретению является вирус, депонированный под номером: CNCM I-3895 в Национальной коллекции культур микроорганизмов Института Пастера, в Париже, Франция.
Хотя образцом, который был очищен, амплифицирован и депонирован, является изолят, названный «изолятом 19», однако, любой из изолятов птичьего астровируса согласно изобретению, описанный в таблице 1, может служить в качестве эталонного образца для новой группы птичьих астровирусов согласно изобретению.
Для культивирования in vitro и для тестирования птичьих астровирусов согласно изобретению могут быть использованы несколько систем культивирования, например, преимущественно используются (птичьи) клеточные линии, такие как первичные клетки, подобные клеткам CEL или клеткам почек куриного эмбриона (CEK). Метод получения клеточных культур CEL или CEK из куриных яиц SPF с развивающимся эмбрионом хорошо известен специалистам в данной области.
Клетки CEK являются особенно подходящими для мониторинга размножения вируса и определения количества вируса и его жизнеспособности. Даже если цитопатический эффект (cpe), который продуцирует птичий астровирус согласно изобретению на этих клетках, является атипичным, то инфицированные клетки могут четко наблюдаться как округлые клетки, образующие завитки, выступающие из монослоя, а затем подвергающиеся лизису.
Поэтому, анализы на титрование вируса могут быть проведены путем постепенных разведений вирусных образцов, и последующей оценки наивысшего разведения вируса, еще продуцирующего цитопатический эффект (cpe). Титр вируса может быть затем выражен как доза, инфицирующая 50% тканевой культуры (TCID50) на миллилитр, как было вычислено методом Спирмана-Кербера (описанным в работе D. Finney: Statistical method in biological assay, C. Griffin & Co., Londen, ISBN 0195205677). Все эти методы хорошо известны специалистам.
Таким образом, вирус может быть культивирован в колбах для культивирования тканей или в микротитрационных планшетах для проведения ряда тестов и для других применений. Обычно, сначала желательно адаптировать выделенные из среды вирусы для их культивирования in vitro на клетках путем проведения нескольких пассажей на этих клетках, с последующим их использованием в тестах на присутствие вируса или для титрования вируса.
Альтернативно, тесты и титрование могут быть осуществлены в яйцах с развивающимся эмбрионом, а предпочтительно, в куриных яйцах SPF. Так, например, титрование вируса может быть осуществлено путем инокуляции образцов вируса, разведенных в возрастающей концентрации, в желточный мешок 6-дневных куриных яиц SPF с развивающимся эмбрионом. После подсчета числа инфицированных или погибших эмбрионов, полученный титр тестируемого образца может быть выражен в EID50 на миллилитр, например, методом Спирмана-Кербера (см. выше).
Способность депонированного вируса вызывать патологию у вылупившихся из яиц цыплят и индюшат была подтверждена в лабораторных условиях в ряде экспериментальных тестов, проводимых на курах. Инокуляцию проводили различными путями: внутримышечно, перорально и офтальмически. У нескольких из инокулированных кур наблюдалось развитие тяжелых признаков заболевания, тогда как у ложноинфицированных кур таких симптомов не наблюдалось. Наблюдаемыми симптомами были гибель, общая депрессия и диарея, варьирующаяся от слабой до сильной. После гистопатологического анализа были обнаружены нефрит и энтерит. Какого-либо заболевания ног или суставов не наблюдалось, однако, такие симптомы и не могли наблюдаться, поскольку куры, используемые в этих экспериментах, были слишком молодыми (3-6 недель), и/или не имели тяжелых патологий (куры-несушки SPF), достаточных для проявления таких симптомов.
Нуклеотидная последовательность других областей генома депонированного вируса, таких как OPC1b и ОРС2, представлена здесь для дополнительной характеризации. Соответствующие нуклеотидные и предполагаемые аминокислотные последовательности представлены здесь как SEQ ID No: 5-8, смотри таблицу 1.
Различные праймеры, которые были использованы для определения этих других нуклеотидных последовательностей, представлены здесь как SEQ ID No: 32-34, и описаны в таблице 4; причем, для удобства, в данную таблицу также включены другие ПЦР-праймеры и секвенирующие праймеры, описанные в настоящей заявке.
|
Другим методом получения дополнительной информации о птичьих астровирусах согласно изобретению, в котором в качестве эталона используется образец депонированного вируса, является определение иммунологических признаков этого вируса путем серотипирования, а предпочтительно, с помощью VN- или IFT-анализов.
Во всех тестах было подтверждено, что новый птичий астровирус по своим иммунологическим свойствам отличается от других птичьих вирусов, поскольку он не может быть нейтрализован и специфически не связывается с антителами против ряда других птичьих вирусов, таких как реовирус, аденовирус домашней птицы (типа 1, 2, 4, 5 и 8), вирус инфекционного бронхита, вирус ньюкаслской болезни, вирус инфекционного бурсита, птичий энтеровирус (изоляты 1821/9 и FP3), вирус, вызывающий синдром кладки яиц и вирус птичьего гриппа. Это относится также к антителам, специфичным к птичьим астровирусам ANV1 или CAstV2, однако, эти сыворотки эффективно нейтрализуют их донорные вирусы ANV1 и CAstV2 в разведении до 1:640 или 1:10240, соответственно.
Однако, образец изолята 19 депонированного вируса эффективно и селективно нейтрализуется куриной антисывороткой, вырабатываемой против изолята 19 у кур SPF, которые были экспериментально инфицированы изолятом 19 данного вируса. После бустер-инокуляций может быть получена специфическая антисыворотка. Данные, полученные в этом анализе и используемые для нейтрализации вируса, могут быть применены в целях предупреждения развития патологии у эмбрионов посредством нейтрализации.
Результаты таких иммунологических экспериментов, в которых антитела распознают и нейтрализуют только птичий астровирус согласно изобретению, продемонстрировали, что эти вирусы принадлежат к новому и уникальному вирусному серотипу.
Такая информация может быть положена в основу осуществления, например, другого предпочтительного варианта изобретения, где указанный птичий астровирус согласно изобретению отличается тем, что указанный птичий астровирус может быть нейтрализован в анализе на нейтрализацию вируса антителами, направленными против образца астровируса, депонированного под номером CNCM I-3895 в Национальной коллекции культур микроорганизмов (CNCM) Института Пастера, в Париже, Франция.
Также может быть осуществлен альтернативный способ получения антител с использованием депонированного вируса согласно изобретению. Так, например, образец вируса, который исследуется на присутствие (происхождение от) птичьего астровируса согласно изобретению, может быть сам использован для индуцирования антител, которые, в свою очередь, могут быть протестированы на их способность связываться с птичьим астровирусом согласно изобретению или даже нейтрализовать этот астровирус. Обычно такие антитела тестируют на образце депонированного вируса согласно изобретению.
Для этих целей, тестируемый вирус или его часть или препарат на его основе, могут быть инокулированы животному. Животным, используемым для вырабатывания таких антител, в принципе, может быть любое животное, но предпочтительными являются мыши, крысы, кролики, хомячки, козы или куры. Антитела, продуцируемые таким способом, могут быть протестированы на связывание с птичьим астровирусом согласно изобретению или на нейтрализацию этого астровируса, который, например, может быть получен после запроса на выдачу образца депонированного вируса согласно изобретению из CNCM. Этот вирус может быть культивирован, например, на яйцах, на клетках CEK или CEL, или на других субстратах, и наконец, инкубирован с антителом, вырабатываемом образцом тестируемого вируса. Детектирование связывания антитела может быть осуществлено, например, с помощью IFT- или VN-анализа.
Таким образом, настоящее изобретение относится к способу идентификации и характеризации «живого» и инактивированного вируса, либо фракции или препарата этого вируса, являющегося птичьим астровирусом согласно изобретению или происходящего от птичьего астровируса согласно изобретению.
Поэтому, в другом своем предпочтительном варианте, настоящее изобретение относится к птичьему астровирусу согласно изобретению, отличающемуся тем, что указанный вирус обладает способностью индуцировать антитела, которые могут нейтрализовать образец депонированного астровируса согласно изобретению в VN-анализе.
Протоколы для проведения VN-анализов хорошо известны специалистам и входят в компетенцию среднего специалиста в данной области. Преимущества и подробное описание VN-анализов приводятся выше.
Как показали результаты иммунологических анализов, проводимых с использованием антител против птичьего астровируса согласно изобретению, настоящее изобретение также относится к антителу, которое может связываться с птичьим астровирусом согласно изобретению и может нейтрализовать указанный астровирус.
Поэтому, другим аспектом настоящего изобретения является антитело или его фрагмент, которые могут нейтрализовать птичий астровирус согласно изобретению в анализе на нейтрализацию вируса.
Такие антитела согласно изобретению могут быть получены и продуцированы различными способами, хорошо известными и доступными для специалиста в данной области. Так, например, такие антитела могут быть получены у экспериментальных животных путем (повторной) инокуляции, описанной выше.
Альтернативно, антитела могут быть продуцированы иммортализованными B-лимфоцитами с помощью гибридомной технологии. Современные усовершенствованные методы осуществления классической гибридомной технологии позволяют повышать эффективность и продуктивность этой технологии, например, путем увеличения количества необходимых клеток селезенки перед их слиянием посредством позитивного отбора (пэннинга) с последующим их размножением в культуре, содержащей смесь цитокинов. Кроме того, эта техника слияния может быть улучшена путем замены классического слияния с использованием полиэтиленгликоля на электрослияние.
В другом альтернативном способе, антитела могут быть получены методами молекулярной биологии и экспрессированы в рекомбинантных экспрессионных системах. Методы молекулярной биологии позволяют адаптировать такие антитела для лучшего соответствия уникальных свойств антител против обрабатываемых видов мишеней, или сконструировать антитела, несущие две связывающие области с различными специфичностями. Разработка экспрессионных систем позволяет создать широкомасштабные экспрессионные системы, такие как экспрессионные системы в растениях.
Рекомбинантные экспрессионные системы также хорошо известны специалистам, и в таких системах, например, используются клетки бактерий (например, Escherichia coli, Salmonella, Bacillus, Caulobacter и т.п.), дрожжей (например, Saccharomyces), насекомых (Spodoptera, Trichoplusia), млекопитающих (например, яичника китайского хомячка) или растений (табака, картофеля и т.п.). Эти клетки могут быть трансформированы экспрессионной конструкцией, несущей экспрессируемую гетерологичную последовательность. Известны также комбинированные системы, в которых используется рекомбинантный микроорганизм, содержащий экспрессируемую нуклеиновую кислоту, где указанный микроорганизм может быть культивирован на клетках in vitro для продуцирования нужного белка в нужном масштабе. Одним из примеров является экспрессионная система бакуловирусов/клеток насекомых. И наконец, для бесклеточной экспрессии соответствующей рекомбинантной молекулы ДНК используются так называемые бесклеточные экспрессионные системы, которые являются коммерчески доступными.
Термин «антитело или его фрагмент» означает полноразмерную молекулу иммуноглобулина или ее части, входящие в объем определения антитела согласно изобретению. Фрагментами антител согласно изобретению являются молекулы белка, которые еще могут связываться с эпитопом птичьего астровируса согласно изобретению. Примерами являются Fab-, scFv-, Fv-, dAb- или Fd-фрагменты, хорошо известные специалистам.
Такие фрагменты могут быть получены из интактных антител, например, путем химического или ферментативного расщепления. Альтернативно, такие фрагменты могут быть, например, получены из рекомбинантной экспрессионной системы, например, системы фагового представления.
Как хорошо известно специалистам, связывание антитела или его фрагмента с вирусом включает распознавание ими эпитопов на вирусной частице. В большинстве случаев, такие эпитопы образованы линейными или трехмерными конформациями молекул, представленных на вирусной частице. В результате, препараты вирусов или их частей могут связываться с антителами или их фрагментами согласно изобретению, при условии, что эти препараты или их части еще содержат и представляют нужные эпитопы в нужной форме. В случае птичьего астровируса согласно изобретению, вирусный белок, наиболее часто презентируемый иммунной системе, представляет собой капсидный белок, кодируемый ОРС2.
Для специалиста в данной области также очевидно, что если антитело согласно изобретению было получено путем инокуляции животного, то полученной сывороткой животного является поликлональная антисыворотка, что означает, что указанная антисыворотка содержит смесь антител, которые могут связываться с эпитопами широкого ряда. На практике, это означает множество взаимодействий, которые позволяют эффективно связывать препараты или фрагменты вирусного белка, даже, когда они могут не содержать или соответствующим образом не презентировать все эпитопы, которые обычно являются доступными на интактной частице «живого» вируса.
Альтернативно, антителом согласно изобретению может быть моноклональное антитело, например, антитело, продуцируемое с помощью гибридомной технологии, либо антителом согласно изобретению может быть фрагмент антитела, такой как Fab-фрагмент. В этом случае, антитело или его фрагмент обладают гораздо меньшей способностью распознавать различные эпитопы, поскольку обычно они специфически связываются только с одним эпитопом. Следовательно, если этот конкретный эпитоп не присутствует или не представлен на вирусном фрагменте или препарате, то он вообще не может связываться с таким моноклональным антителом или с его фрагментом.
Антитела согласно изобретению могут быть использованы в различных целях, а именно, для характеризации птичьего астровируса согласно изобретению, для диагностики, для лечения и/или для гарантии качества.
Настоящее изобретение относится к продуцированию птичьего астровируса согласно изобретению в промышленном масштабе. Это может быть достигнуто путем культивирования указанного вируса на клетках-хозяевах в системах in vivo или in vitro. Системы in vitro содержат первичные или иммортализованные клеточные линии. Примерами первичных клеток являются клетки CEK или CEL. Примером иммортализованной клеточной линии является клеточная линия LMH (Kawaguchi et al., Cancer Res., vol. 47, p. 4460-4464). Примерами систем in vivo являются культуры, полученные путем культивирования в птичьих яйцах с эмбрионом или в организме инокулированных птиц. В частности, культуры, полученные на клетках или яйцах, могут быть масштабированы, например, клеточные культуры могут содержаться в контейнерах различных размеров, таких как колбы, роллер-флаконы или даже ферментеры. Методы и оборудование, применяемые в технологии культивирования клеток в любом масштабе, хорошо известны специалистам и могут быть легко получены у коммерческих поставщиков.
Поэтому, в другом своем аспекте, настоящее изобретение относится к клетке-хозяину, инфицированной птичьим астровирусом согласно изобретению.
Кроме того, настоящее изобретение относится к способу продуцирования птичьего астровируса согласно изобретению, где указанный способ включает размножение птичьего астровируса согласно изобретению в соответствующей системе и сбор вирусного материала.
Описанные здесь свойства птичьего астровируса согласно изобретению относятся не только к указанным птичьим астровирусам в интактной и компетентной по репликации форме. Как очевидно для специалиста в данной области, настоящее изобретение относится к препаратам этого вируса во многих различных формах. Такими препаратами являются, например, препараты, в которых птичий астровирус согласно изобретению был инактивирован, либо препараты, в которых такой вирус был фракционирован одним или несколькими способами, а именно, (био-)химическими или физическими способами, например, путем экстракции, лизиса, расщепления, гомогенизации или обработки ультразвуком.
Методы инактивации вируса хорошо известны специалистам, и, например, включают химическую или физическую инактивацию, такую как инактивация формалином, бета-этанолимином или бета-пропиолактоном, а также нагревание или облучение УФ- или рентгеновскими лучами или радиоактивное облучение.
Методы фракционирования также известны большинству специалистов, и такими методами являются, например, экстракция или лизис детергентом, таким как Triton® X-100; гидролиз трипсином; гомогенизация путем замораживания-оттаивания, либо обработка под давлением во френч-прессе или обработка ультразвуком.
Исходным материалом для получения таких препаратов может быть очищенный («живой» или инактивированный) птичий астровирус согласно изобретению, а также клетки-хозяева согласно изобретению или клеточная культура или ее часть, содержащие клетку-хозяина или птичий астровирус согласно изобретению. Так, например, такой частью клеточной культуры может быть супернатант или осадок центрифугированной клеточной культуры. Следует также отметить, что эти клеточные культуры или их части могут быть сами превращены в препараты, такие как экстракт, лизат, гидролизат, гомогенат или препарат, обработанный ультразвуком, как описано выше.
Такие препараты птичьего астровируса согласно изобретению содержат один или несколько антигенов и эпитопов птичьего астровируса согласно изобретению.
Поэтому, в другом своем аспекте, настоящее изобретение относится к антигенному препарату, получаемому из птичьего астровируса согласно изобретению.
Антигенный препарат согласно изобретению может быть связан с антителами согласно изобретению или их фрагментами, либо он сам может быть использован для индуцирования связывания или нейтрализации антител или их частей. Такой препарат может преимущественно применяться для получения вакцин и в целях диагностики, как описано ниже.
Антигенными препаратами согласно изобретению являются, например, белки птичьего астровируса согласно изобретению или части таких белков. Эти белки или их части могут быть получены путем их выделения из указанного вируса. Однако, эти белки или их части могут быть продуцированы стандартными методами экспрессии рекомбинантных ДНК с использованием нуклеиновых кислот от птичьего астровируса согласно изобретению. Так, например, могут быть использованы последовательности нуклеиновой кислоты части областей ОРС1а, описанных в любой одной из SEQ ID NO: 4, 10, 12, 14, 16, 18, 20, 22, 24 или 26, поскольку описанные последовательности кДНК являются родственными, то есть, они имеют нуклеотидную последовательность, которая по меньшей мере на 88% идентична последовательности SEQ ID NO: 4.
Поэтому, в другом своем аспекте, настоящее изобретение относится к молекуле ДНК, содержащей область, имеющую нуклеотидную последовательность, которая на 88% идентична последовательности SEQ ID NO: 4.
Могут быть также использованы нуклеиновые кислоты OPC1b или ОРС2, описанные в SEQ ID NO: 6 или 8.
Такие последовательности нуклеиновой кислоты и фрагменты кДНК могут быть клонированы и экспрессированы с использованием техники рекомбинантных ДНК, известной специалистам, например, путем субклонирования молекулы ДНК для ее последующей модификации. Указанная рекомбинантная молекула кДНК (recDNA) может представлять собой вектор, такой как бактериальная плазмида. При этом, предпочтительно, чтобы нуклеиновая кислота птичьего астровируса согласно изобретению была функционально присоединена к последовательности, регулирующей экспрессию, такой как промотор, что позволяет осуществлять ее экспрессию в соответствующей клетке-хозяине или экспрессионной системе. Альтернативно, нуклеиновая кислота, кДНК или рекомбинантная молекула ДНК может быть введена в живые рекомбинантные микроорганизмы-носители, такие как бактерия или вирус.
Аналогичным образом, в другом своем аспекте, настоящее изобретение относится к белку, полученному исходя из предполагаемых аминокислотных последовательностей, описанных в SEQ ID NO: 5, 11, 13, 15, 17, 19, 21, 23, 25 и 27 и родственных им последовательностей, и содержащему область, имеющую аминокислотную последовательность, которая по меньшей мере на 93% идентична последовательности SEQ ID NO: 5.
Эти варианты настоящего изобретения могут иметь широкое практическое и преимущественное применение в разработке вакцин и диагностических средств, описанных ниже.
Вакцина может быть получена из живых или инактивированных микробных патогенов, таких как вирусы, или из фрагментов таких микроорганизмов. Указанные микроорганизмы обычно получают в промышленном масштабе в небольших или больших объемах путем инкубирования на клетках, органах или тканях, в яйцах с развивающимся эмбрионом или в организме животных-хозяев. После сбора суспензии, содержащей указанный микроорганизм, такую суспензию приготавливают в виде вакцины с последующей упаковкой конечного продукта. После широкого тестирования на качество, количество и стерильность, такие вакцинные продукты могут быть представлены на продажу.
Общие методы и концепции, обсуждаемые в области вакцинологии, хорошо известны специалистам и описаны, например, в инструкциях Регуляторных органов, а также в руководствах, таких как, «Veterinary vaccinology» (P. Pastoret et al. ed., 1997, Elsevier, Amsterdam, ISBN: 0444819681) и «Remington: the science and practice of pharmacy» (2000, Lippincot, USA, ISBN: 683306472).
Вакцинные препараты хорошо известны специалистам и представляют собой фармацевтическую композицию, содержащую иммуногенное соединение в фармацевтически приемлемом носителе. Иммуногенным соединением являются живые или инактивированные микроорганизмы или их субъединицы, способные индуцировать активацию иммунной системы-мишени.
Неожиданно было обнаружено, что птичий астровирус согласно изобретению и антигенные препараты, клетки-хозяева, антитела, нуклеиновые кислоты, белки, а также методы их получения, культивирования, идентификации и количественной оценки могут быть применены для приготовления вакцин и в целях диагностики. Такие вакцины служат для защиты животного-мишени от инфицирования птичьим астровирусом, либо для снижения репликации указанного вируса или ослабления симптомов заболевания, которое он вызывает. Такие диагностические анализы позволяют детектировать вирус или его антигены, например, в образцах, взятых от животного, или в вирусных препаратах.
Вакцины и диагностические средства, взятые в комбинации, позволяют идентифицировать птичий астровирус согласно изобретению, осуществлять защиту от указанного астровируса и/или предотвращать заболевание, вызываемое таким астровирусом.
Емкость вакцины была продемонстрирована в экспериментах на животных, в которых курам был инокулирован птичий астровирус согласно изобретению. Такая инокуляция приводила к продуцированию в высокой степени специфических антител. Кроме того, было продемонстрировано, что эти антитела способны специфически нейтрализовывать птичий астровирус согласно изобретению. Как хорошо известно специалистам, индуцирование нейтрализующих антител является важной ступенью в разработке эффективных и иммунопротективных вакцин.
Повторная инокуляция тестируемых животных не только приводила к повышению уровня продуцируемых антител, но также служила в качестве контрольного заражения, которое позволяло определить степень толерантности и выносливости большого числа птиц в данном тесте.
Таким образом, птичий астровирус согласно изобретению или его часть могут быть приготовлены в виде соответствующей фармацевтической композиции и использованы для вакцинации птиц.
Специалист в данной области может дополнительно оптимизировать данную вакцину, например, путем тонкой коррекции эффективности и безопасности вакцины в целях обеспечения достаточной защиты от реакции вакцинации на приемлемом уровне. Это может быть осуществлено путем выбора дозы вакцины или использования вакцины в другой форме или композиции, либо выбора других компонентов вакцины (например, стабилизатора или адъюванта), либо путем ее введения другим способом.
Так, например, в настоящем изобретении могут быть использованы хорошо известные варианты вакцины на основе нового птичьего астровируса в форме «живого» или инактивированного вируса; при этом, если используется антигенный препарат и/или белок согласно изобретению, то такой вакциной может быть субъединичная вакцина; если используется антитело согласно изобретению или его фрагмент, то такая вакцина может быть получена в форме пассивной вакцины, а если используется молекула ДНК согласно изобретению, то такая вакцина может быть получена в форме ДНК-вакцины.
Поэтому, в другом своем аспекте, настоящее изобретение относится к вакцине, включающей птичий астровирус, антитело или его фрагмент, антигенный препарат, молекулу ДНК или белок согласно изобретению и фармацевтически приемлемый носитель.
Аналогичным образом, в других своих аспектах, настоящее изобретение относится к соединению или к композиции, используемых в вакцине для домашней птицы, где указанным соединением или композицией являются птичий астровирус, антитело или его фрагмент, антигенный препарат, молекула ДНК или белок согласно изобретению.
В другом своем аспекте, настоящее изобретение относится к соединению или к композиции, применяемым в целях приготовления вакцины для домашней птицы, где указанным соединением или композицией является птичий астровирус, антитело или его фрагмент, антигенный препарат, молекула ДНК или белок согласно изобретению.
В другом своем аспекте, настоящее изобретение относится к способу приготовления вакцины для домашней птицы, где указанное соединение или композицию смешивают с подходящим фармацевтическим носителем, и где указанным соединением или указанной композицией является птичий астровирус, антитело или его фрагмент, антигенный препарат, молекула ДНК или белок согласно изобретению.
«Фармацевтически приемлемым носителем» может быть, например, стерильная вода, физиологический раствор или буфер, подходящий для этой цели. В более сложных формах, указанный носитель может содержать другие соединения, такие как адъювант, дополнительный антиген, цитокин и т.п.
Вакцина согласно изобретению может быть использована как для профилактического, так и для терапевтического лечения.
Термин «вакцина» подразумевает присутствие иммунологически эффективного количества птичьего астровируса согласно изобретению и присутствие фармацевтически приемлемого носителя.
Определение «иммунологически эффективное количество» вакцины согласно изобретению зависит от желаемого эффекта и от свойств птичьего астровируса и организма-мишени. Такое эффективное количество может быть определено самим специалистом рутинным способом, например, путем мониторинга иммунологического ответа после вакцинации или после провокационного заражения, например, путем мониторинга клинических признаков заболевания организма-мишени, серологических параметров или путем повторного выделения патогена, и сравнения с ответами, наблюдаемыми у невакцинированных животных.
Использование очень больших количеств птичьего астровируса, антигенного препарата, антитела или его фрагмента, молекулы ДНК или белка согласно изобретению в вакцине, хотя и является очень эффективным с иммунологической точки зрения, но мало привлекательно с экономической точки зрения. Предпочтительное количество любого из этих соединений или любой из этих композиций согласно изобретению, содержащихся в вакцине согласно изобретению, составляет от 0,1 до 90% от конечного объема вакцины. Более предпочтительно, такое количество, в порядке предпочтительности, составляет 1-50%, 1-25% и 1-10%.
В случае инактивированных или субъединичных вакцин, соединение или композиция согласно изобретению могут быть выражены в ELISA-единицах. Количества ELISA-единиц, которые являются эффективными, должны быть определены по отношению к ELISA-единице стандартизированного образца, дающего определенную эффективность.
В случае «живой» вакцины согласно изобретению, количество б.о.е. (бляшкообразующих единиц), количество к.о.е. (колониеобразующих единиц), TCID50, EID50 или ELD50 (доза, которая является летальной для 50% эмбрионов) может быть использовано в зависимости от конкретно применяемого стандартного способа количественной оценки дозы вакцины на основе птичьего астровируса. Так, например, предпочтительно, доза вакцины, полученной на основе «живого» птичьего астровируса, может составлять в пределах от 1 до 106 EID50 на дозу вакцины, более предпочтительно, в пределах от 10 до 105 EID50/дозу, а еще более предпочтительно, от 102 до 104 EID50/дозу.
В своем предпочтительном варианте, настоящее изобретение относится к вакцине согласно изобретению, в которой птичий астровирус согласно изобретению присутствует в «живой» форме.
По существу, «живые» вакцины обладают преимущественными свойствами, заключающимися в том, что поскольку микроорганизм реплицируется сам, то в данном случае требуется лишь незначительное количество инокулята. Кроме того, такие вакцины в основном индуцируют стойкий и эффективный иммунный ответ с адекватной иммунологической памятью.
Как известно специалистам в данной области, «живые» вакцины могут быть использованы в качестве аттенуированных «живых» вакцин, в которых вакцинный вирус обладает пониженной вирулентностью или патогенностью по сравнению с исходным вирусным изолятом. Методы аттенуирования вируса известны специалистам и включают, например, непрерывный пассаж в организме животных или поверх клеточных культур; химическое аттенуирование или аттенуирование методами молекулярной биологии.
В своем альтернативном предпочтительном варианте, настоящее изобретение относится к вакцине согласно изобретению, в которой птичий астровирус согласно изобретению является инактивированным.
Методы и материалы для инактивации вируса описаны выше. Такие инактивированные вакцины, по существу, имеют то преимущество, что они являются более безопасными, чем «живые» вакцины, поскольку при их применении, хозяин не подвергается какому-либо риску заражения патогенным реплицирующимся вирусом, таким как «живой» птичий астровирус.
В другом предпочтительном варианте изобретения, вакцина согласно изобретению также содержит адъювант.
Адъювантом является иммуностимулирующее вещество, усиливающее неспецифический иммунный ответ у хозяина. Специалистам известно множество различных адъювантов. Примерами наиболее часто используемых адъювантов являются мурамилдипептиды, липополисахариды, некоторые глюканы или гликаны, Карбопол®, гидроксид алюминия (Al(OH)3). Эти адъюванты могут быть объединены с различными эмульсиями, такими как эмульсии типа «вода в масле» (вода/масло), эмульсии типа «масло в воде» и двойные эмульсии типа «вода/масло/вода». Масляными адъювантами, подходящими для использования в маслянистых эмульсиях, являются, например, минеральные масла или масла, преобразующиеся в процессе метаболизма. Минеральными маслами являются, например, Bayol®, Marcol® и Drakeol®, а маслами, преобразующимися в процессе метаболизма, являются, например, растительные масла, такие как арахисовое масло и соевое масло, или масла животного происхождения, такие как сквален рыбьего жира. Альтернативно, преимущественно используется солюбилизат витамина E (токоферол), описанный в EP 382271.
Наиболее подходящими эмульсиями типа «масло в воде» являются, например, эмульсии, составляющие 5-50% масс./масс. водной фазы и 95-50% масс./масс. масляного адъюванта, а более предпочтительно, 20-50% масс./масс. водной фазы и 80-50% масс./масс. масляного адъюванта.
Количество добавляемого адъюванта зависит от природы самого адъюванта и от информации о его количествах, полученных производителем.
Хотя в соответствии с общей практикой, адъюванты используются в комбинации с инактивированными вакцинами, однако, было также показано, что использование адъюванта в комбинации с некоторыми живыми вакцинами может давать определенное преимущество. Поэтому, этот вариант также входит в объем настоящего изобретения.
В другом предпочтительном варианте изобретения, вакцина согласно изобретению также включает стабилизатор.
Стабилизатор может быть добавлен в вакцину согласно изобретению, например, для ее защиты от деструкции, для увеличения срока хранения или для повышения эффективности лиофилизации. Подходящими стабилизаторами являются, среди прочих, SPGA (Bovarnik et al., 1950, J. Bacteriology, vol. 59, p. 509), сепарированное молоко, желатин, альбумин бычьей сыворотки, углеводы, например, сорбит, маннит, трегалоза, крахмал, сахароза, декстран или глюкоза, белки, такие как альбумин или казеин или продукты их разложения, буферы, такие как фосфаты щелочного металла, и полиамины, такие как спермин.
Также могут быть добавлены консерванты, такие как тимеросал, мертиолят или гентамицин.
Кроме того, вакцина может содержать одно или несколько подходящих поверхностно-активных соединений или эмульгаторов, например, Span® или Tween®.
Вакцина может также содержать так называемый «носитель». Носителем является соединение, к которому присоединяется, но кавалентно не связывается с ним, полипептид или белок согласно изобретению. Такими носителями являются, inter alia, биомикрокапсулы, микроальгинаты, липосомы и макрозоли, которые известны специалистам. Особой формой такого носителя является иммуностимулирующий комплекс (ISCOM).
Само собой разумеется, что в объем настоящего изобретения входит смесь других стабилизаторов, носителей, разбавителей, эмульсий и т.п. с вакцинами согласно изобретению. Такие добавки описаны в общеизвестных руководствах, таких как «Remington» и «Veterinary Vaccinology» (см. выше).
Наиболее эффективным является приготовление вакцины согласно изобретению в виде комбинированной вакцины, поскольку, в этом случае, множество иммунологических агентов может быть введено сразу, что позволяет снизить затраты времени и средств, а также минимизировать дискомфорт, связанный с вакцинацией животных-мишеней.
Такие комбинированные вакцины получают путем объединения вакцины согласно изобретению с другим антигенным соединением, таким как (живой или инактивированный) вирус, бактерия, паразит или их части, такие как белок, углевод или нуклеиновая кислота, способная кодировать антиген. Поскольку вакцина согласно изобретению предназначена для птиц-мишеней, то предпочтительно использовать комбинацию с дополнительным антигеном, которым является другой патоген домашней птицы, или который происходит от этого патогена.
Поэтому, в другом предпочтительном варианте изобретения, вакцина согласно изобретению содержит по меньшей мере один дополнительный антиген, происходящий от микроорганизма, который является патогенным для домашней птицы.
Многие птичьи патогены являются известными, однако, некоторыми из наиболее релевантных, с ветеринарной и экономической точки зрения, являются следующие патогены:
- вирусы: вирус инфекционного бронхита, вирус ньюкаслской болезни, вирус птичьего гриппа, аденовирус, вирус синдрома снижения яйценоскости, вирус инфекционного бурсита (то есть, гумборовирус), вирус анемии кур, вирус птичьего энцефаломиелита, вирус оспы домашней птицы, вирус ринотрахеита индеек, вирус утиных бляшек (утиный вирусный энтерит), вирус оспы голубей, вирус, вызывающий болезнь Марека, вирус птичьего лейкоза, вирус инфекционного ларинготрахеита, птичий пневмовирус и реовирус;
- бактерии: Escherichia coli, Salmonella spec, Ornitobacterium rhinitracheale, Haemophilis paragallinarum, Pasteurella multocida, Erysipelothrix rhusiopathiae, Erysipelas spec, Mycoplasma spec и Clostridium sp.;
- паразиты: Eimeria;
- грибы: например, Aspergillus, и т.п.
В вакцине согласно изобретению, также подходящей является комбинация из двух или более птичьих астровирусов согласно изобретению, используемая, например, для получения комбинированной вакцины, которая является более эффективной против вариантов птичьих астровирусов согласно изобретению широкого ряда. Примерами птичьих астровирусов, которые могут быть использованы для получения комбинированной вакцины, являются изоляты, описанные в таблице 1.
Вакцина согласно изобретению может быть получена в любой форме, подходящей для введения домашней птице и для введения соответствующим способом в целях достижения нужного эффекта.
Получение вакцины согласно изобретению осуществляют способом, хорошо известным специалистам. Предпочтительно, вакцину согласно изобретению готовят в форме, подходящей для инъекции, такой как суспензия, раствор, дисперсия, эмульсия и т.п. Обычно, такие вакцины изготавливают в стерильных условиях.
Вакцина может быть введена многими способами, известными специалистам. Если вакцины согласно изобретению являются инактивированными, то они могут быть введены путем инъекции; если вакцины являются «живыми», то их предпочтительно, вводят методом объемного введения, например, вместе с пищей, спреем или с водой для питья.
В идеальном случае, протокол введения вакцины согласно изобретению включают в существующие схемы вакцинации другими вакцинами.
Предпочтительной мишенью для вакцины согласно изобретению являются птицы. Более предпочтительно, такие мишени выбирают из группы, состоящей из кур, индеек, уток и гусей. Наиболее предпочтительной мишенью являются куры.
Схема введения доз вакцины согласно изобретению в организм-мишень предусматривает введение одной или множества доз, которые могут быть введены одновременно или последовательно, способом, подходящим для данного вакцинного препарата, и в таких количествах, которые являются иммунологически эффективными.
Возраст, вес, пол, иммунологический статус и другие параметры птицы-мишени не имеют решающего значения, хотя, очевидно, что предпочтительными для вакцинации являются здоровые птицы, и чем раньше проводится такая вакцинация, тем лучше с точки зрения предупреждения от инфекций, вносимых окружающей средой. Поэтому, например, домашняя птица может быть вакцинирована в день ее вылупления, или даже раньше, еще in ovo за 3-4 дня до ее вылупления, например, на 18-й день развития эмбриона, для кур, или на 24-й день развития эмбриона, для индеек.
Из соображений стабильности или экономии, вакцина согласно изобретению может быть подвергнута лиофилизации. Обычно, это способствует более длительному сроку хранения при температуре выше 0°С, например, при 4°С. Процедура лиофилизации хорошо известна специалистам, а оборудование для лиофилизации в различных масштабах является коммерчески доступным.
Поэтому, в предпочтительном варианте изобретения, вакцину согласно изобретению получают в лиофилизованной форме.
Для разведения лиофилизованной вакцинной композиции, ее суспендируют в фармацевтически приемлемом разбавителе. Таким разбавителем может быть, например, просто стерильная вода или физиологический раствор, такой как (забуференный фосфатом) физиологический раствор, либо такой разбавитель может уже содержать адъювантное соединение, такое как токоферол, описанный в EP 382271. В своей более сложной форме, лиофилизованная вакцина может быть суспендирована в эмульсии, например, как описано в EP 1140152.
Поэтому, в другом своем предпочтительном варианте, настоящее изобретение относится к вакцинной композиции, которая может быть получена путем разведения лиофилизованной вакцины согласно изобретению.
Помимо различных применений соединений и композиций согласно изобретению в вакцинах, эти соединения и композиции могут быть использованы в диагностике, для детектирования вируса согласно изобретению или его антигенов или нуклеиновых кислот, например, в образцах, взятых у животных или в вирусных препаратах.
Результаты такого применения были также продемонстрированы в экспериментах по серотипированию, проводимых с помощью IFT- и VN-анализа, описанных выше, где антисыворотку против депонированного птичьего астровируса согласно изобретению использовали для идентификации вирусов, входящих в объем настоящего изобретения (изолятов, описанных в таблице 1), и вирусов, не входящих в объем изобретения (среди многих других вирусов: ANV1, CAstV2, Reovirus и т.п.). Аналогичным образом, описанные ПЦР-эксперименты продемонстрировали возможность применения такого способа для селективной идентификации птичьего астровируса согласно изобретению.
Для специалиста в данной области очевидно, что этот метод применим не только к антителам согласно изобретению, но также и к другим соединениям и композициям согласно изобретению. В таких диагностических анализах применяются, например: антитела или их фрагменты согласно изобретению для тестирования на антиген; либо антиген (вирус, антигенный препарат или белок согласно изобретению) для тестирования на антитела против этого антигена; либо нуклеиновая кислота (РНК вируса или молекула ДНК согласно изобретению) для осуществления гибридизации или ПЦР-анализов.
Поэтому, в другом своем аспекте, настоящее изобретение относится к диагностическому набору, содержащему птичий астровирус, антигенный препарат, антитело или его фрагмент, молекулу ДНК или белок согласно изобретению.
Термин «диагностический набор» включает элементы, относящиеся к упаковке для коммерческих продаж, содержащей, например, ряд компонентов и приспособлений одноразового применения для осуществления диагностического теста и инструкцию в виде брошюры; где все эти элементы присутствуют в упаковке в коммерчески приемлемой форме.
Такой диагностический набор, например, содержит материалы, необходимые для проведения ELISA с использованием антител. В таком тесте, например, лунки ELISA-планшета сенсибилизируют птичьим астровирусом согласно изобретению и получают набор для ELISA, проводимого в целях детектирования антител против птичьего астровируса согласно изобретению или его препаратов и белков. После инокуляции тест-образца, в лунки добавляют меченные антитела, реагирующие с иммуноглобулинами тест-образца (если они присутствуют). Затем проводят цветную реакцию, которая позволяет выявить присутствие специфических антител в тест-образце.
Аналогичным образом, может быть получен набор ELISA для детектирования антигена, содержащий, например, микротитрационные планшеты, сенсибилизированные вирусом, антигенным препаратом или белком согласно изобретению.
Схема проведения таких иммуноанализов может варьироваться. Так, например, иммуноанализ может быть проведен на основе конкурентного, но не прямого, связывания. Кроме того, в таких тестах, вместо твердого носителя, имеющегося в данном устройстве, может также использоваться материал в виде частиц или клеточный материал. Детектирование комплекса «антитело - антиген», образующегося в процессе проведения теста, может включать использование меченных антител, где указанными метками могут быть, например, ферменты или флуоресцентные молекулы, хемилюминесцентные молекулы, радиоактивные молекулы или молекулы красителей.
Предпочтительно, в настоящее время, вакцины и диагностические средства согласно изобретению могут быть использованы в комбинации друг с другом для разработки метода уничтожения птичьего астровируса согласно изобретению в некоторых регионах или у некоторых популяций животных.
ОПИСАНИЕ ФИГУР
На фигуре 1 представлено множественное выравнивание последовательностей кДНК части ОРС1а, взятых из выбранного ряда изолятов птичьих астровирусов согласно изобретению. Эталонной является последовательность изолята 19. Внешним эталоном является соответствующая часть последовательности кДНК генома эталонного вируса ANV1 (SEQ ID NO:1). Область в рамке обозначает область из 12 нуклеотидов, которые отсутствуют в ОРС1а вируса ANV1.
На фигуре 2 представлено множественное выравнивание предполагаемых аминокислотных последовательностей, полученных с помощью компьютерной трансляции последовательностей кДНК, показанных на фигуре 1. Область в рамке обозначает область из 4 аминокислот, которые отсутствуют в белке, кодируемом ОРС1а ANV1.
На фигуре 3 показано дендрографическое дерево результатов выравнивания нуклеотидных последовательностей, представленных на фигуре 1.
На фигуре 4 дано графическое представление областей гибридизации праймеров SEQ ID NO: 30 и 31 по отношению к локализации области из 12 нуклеотидов (представленной жирным шрифтом), которая является уникальной для птичьих астровирусов согласно изобретению.
На фигуре 5 приводится фотография окрашенного этидийбромидом и облученного УФ-светом агарозного геля, на котором был проведен электрофорез продуктов ПЦР-анализа с использованием праймеров SEQ ID NO: 30 и 31 на ряде образцов кДНК. Предполагаемый продукт позитивной ПЦР, то есть, полоса размером приблизительно 260 пар нуклеотидов, был явно заметен только на дорожке 5. Предыдущие ОТ-реакции проводили с использованием праймера SEQ ID NO: 3.
Дорожка 1: Негативный контроль (без кДНК в ПЦР-реакции)
Дорожка 2: Гомогенат печени от неинфицированных кур
Дорожка 3: ANV1; изолят, полученный в Германии в 1991 г., амплифицированный 1 x CAM, 4x желточный мешок, собранная аллантоисная жидкость.
Дорожка 4: CAstV2, происходящий от вируса, депонированного в CNCM под номером CNCM I-2932, аллантоисная жидкость.
Дорожка 5: Изолят 19 птичьего астровируса согласно изобретению, аллантоисная жидкость.
M: дорожка маркера размера ДНК: полосы размером 200, 400, 600, 800, 1000 п.н. и т.п..
Настоящее изобретение более подробно описано со ссылками на нижеследующие неограничивающие примеры.
ПРИМЕРЫ
ПРИМЕР 1: Выделение птичьего астровируса из природных образцов
Многие изоляты птичьего астровируса согласно изобретению были выделены у кур и индеек на различных фермах в Нидерландах и Германии. Типичным примером является изолят образца № 161319 («изолят 19»), подробно описанный в настоящей заявке.
Изолят 19 астровируса был выделен из пула трахей, взятых у 4 кур-несушек в возрасте 36 недель на ферме в Голландии, у которых наблюдалось снижение потребления корма, снижение яйценоскости и увеличение числа яиц второго сорта. Эти куры, в основном, страдали расстройством пищеварения, диареей и нарушением двигательных функций.
Собранную ткань (0,5-1,0 г) трахей от 4 птиц смешивали примерно с 10 мл «среды для ополаскивания» (содержащей 500 мл HBSS [основного солевого раствора Хэнкса] + 2 мл натрий-содержащего бензилпенициллина (1000000 МЕ/мл) + 8 мл стрептомицина (250 мг/мл) + 0,5 мл фунгизона (2000 мкг/мл) + 2 мл NaHCO3, 7,5%) и гомогенизировали с использованием гомогенизатора Stomacher в течение 2 минут. Суспензию центрифугировали в течение 15 минут при 2000×g и при температуре 2-8°C. Затем супернатант фильтровали на 450 нм-фильтре.
Полученную жидкость инокулировали в аллантоисную полость четырех 8-9-дневных куриных яиц SPF с развивающимся эмбрионом (1 мл на яйцо), в желток четырех 5-6-дневных куриных яиц SPF с развивающимся эмбрионом (1 мл на яйцо), и в CAM четырех 9-дневных куриных яиц SPF с развивающимся эмбрионом (0,5 мл на яйцо) и инкубировали при 36,5-38,5°C и при влажности 40-55%. Эти яйца ежедневно просвечивали. Гибель эмбриона в первый день инокуляции рассматривалась как нехарактерная.
Эмбрионы яиц с инокулированным желточным мешком не обнаруживали каких-либо аномалий через 7 дней после инокуляции (p.i.). Тем не менее, желточную жидкость собирали и использовали для второго пассажа.
4 мл собранной желточной жидкости от первого пассажа (1 мл на яйцо) смешивали с 0,5 мл «среды для пассажа» (содержащей 90 мл HBSS + 2 мл натрий-содержащего бензилпенициллина (1000000 МЕ/мл) + 8 мл стрептомицина (250 мг/мл) + 0,5 мл фунгизона (2000 мкг/мл) + 2 мл NaHCO3, 7,5%). 1 мл этой смеси на яйцо инокулировали в желток пяти 5-дневных яиц SPF с развивающимся эмбрионом и инкубировали при 36,5-38,5°C и при влажности 40-55%. Эти яйца ежедневно просвечивали.
На шестой день после инокуляции, один эмбрион погиб и у него наблюдалось покраснение тела. Аллантоисную жидкость этого яйца тестировали на реовирус в анализе на преципитацию в агаровом геле (AGP); и этот анализ дал отрицательный результат на реовирус.
Примерно 4-5 мл желтка из этого яйца с аномальным эмбрионом собирали и использовали для последующих пассажей, проводимых так же, как и второй пассаж.
В третьем пассаже, на пятый день после инокуляции, три эмбриона погибли, и у двух из этих эмбрионов наблюдалось покраснение тела. Собранная аллантоисная жидкость показала отрицательный результат в анализе AGP на реовирус и на аденовирус типа 1.
В последующих пассажах, титр изолята повышался, поскольку гибель эмбрионов или обнаружение симптомов заболевания происходило уже после инокуляции. В 6-ом и 7-ом пассажах, типичная ярко-красная окраска ног и кончиков крыльев становилась заметной.
В соответствии с этим, аллантоисная жидкость была негативной в HA- или AGP-тестах на IBDV, реовирус, аденовирус, NDV, AIV и IBV. ПЦР-анализ на IBDV также дал отрицательные результаты.
Собранные CAM и аллантоисные жидкости хранили в замороженном виде при -80°C и использовали для последующей характеризации.
ПРИМЕР 2: Выделение вирусной РНК:
Выделение полноразмерной вирусной РНК осуществляли с использованием мини-набора для вирусной РНК QIAamp® Viral RNA (QiaGen™) в соответствии с инструкциями производителей. Вкратце: 140 мкл вируссодержащей жидкости, такой как аллантоисная жидкость, или гомогенат ткани или эмбрионов (обычно в количествах 5-50% масс./об.) смешивали с ранее полученным буфером для экстракции и РНК-носителем. Эту смесь инкубировали при комнатной температуре в течение 10 минут. Затем добавляли чистый этанол (96-100%), смешивали, и смесь наносили на центрифужную колонку QIAamp Mini (в 2 мл-пробирку для сбора образцов). Смесь центрифугировали в течение 1 минуты при 6000×g. Вещество проходящего потока отбрасывали. Колонку промывали промывочным буфером, содержащим чистый этанол. И наконец, колонку элюировали 60 мкл элюирующего буфера. Обычно, сразу после выделения РНК получали кДНК с помощью ОТ-реакции.
Присутствие РНК астровируса подтверждали путем проведения стандартного гель-электрофореза РНК на агарозном/формамидном геле.
ПРИМЕР 3: Получение кДНК с помощью ОТ-реакции:
Синтез первой цепи кДНК осуществляли с использованием сфер Amersham-Pharmacia™ Ready-To-Go® You-Prime First-Strand Beads в соответствии с инструкциями производителей. Вкратце: 29 мкл элюированной РНК, полученной после выделения полноразмерной вирусной РНК, денатурировали в течение 10 минут при 65°C и 2 минут на льду. В пробирку, содержащую две сферы, добавляли полученную РНК и 4 мкл 10 мкМ праймера 17 (SEQ ID NO: 3) до конечного объема 33 мкл. Эту смесь инкубировали в течение 1 минуты при комнатной температуре, осторожно перемешивали путем пипетирования и инкубировали в течение 1 часа при 37°С. кДНК хранили в замороженном виде при температуре ниже -20°С вплоть до ее использования.
ПРИМЕР 4: ПЦР-реакции
Для приготовления двухцепочечной (дц) ДНК из кДНК, полученной с помощью ОТ-реакции, проводили ПЦР. ПЦР также использовали в качестве детектирующего анализа диагностического типа в целях идентификации, а в частности, для того, чтобы определить, присутствует ли птичий астровирус согласно изобретению в данном образце.
Ингредиенты для ПЦР были получены от HT Biotechnolgy™ Ltd., и такими ингредиентами являются: буфер Supertaq® (10 × конц.), используемый в 1 × конц.; Supertaq® плюс фермент полимераза (5 ед./мкл), используемые в концентрации 1 ед/мкл, и preMixed dNTP (10 мМ), используемые в концентрации 2 мМ. Эти ингредиенты смешивали в дистиллированной воде, не содержащей РНКазы.
Используемые праймеры перечислены в таблице 4. Праймеры были синтезированы Invitrogen™, Нидерланды; маточный раствор праймеров получали в буфере TE (pH 8,0) при 100 мкМ; а рабочий маточный раствор получали в разведении 10 мкМ для непосредственного использования.
Для проведения стандартной ПЦР использовали следующие ингредиенты: 27 мкл воды Aqua dest., 5 мкл 10 × Supertaq плюс буфер; 1 мкл (равный 1 единице) Supertaq плюс фермент; 5 мкл 2 мМ смеси dNTP; 5 мкл каждого прямого и обратного праймера (при 10 мкМ); и наконец, 2 мкл кДНК, полученной из ОТ-реакционной смеси; где общий объем составлял 50 мкл.
Типичные реакции, например, реакцию амплификации ОРС1а с использованием праймеров F-II и R-II-3 (SEQ ID NO: 28, 29), или OPC1b с использованием праймеров 20 и 21 (SEQ ID NO: 32, 33) проводили в следующих условиях:
- 1 минута при 95°C,
- 40 циклов: 30 секунд при 94°C; 1 минута при 48°C; и 40 секунд при 72°C,
- 10 минут при 72°C
- выдерживание при 20°C.
NB: все температуры ПЦР приводятся с точностью примерно ±1°C
В процессе оптимизации были проведены некоторые изменения: вместо 40 циклов было проведено 45 циклов, а также были изменены температуры отжига и время проведения стадий цикла, а именно, были использованы температуры 46-53°C при продолжительности стадии 30 секунд или 1 минуты.
При специфическом детектировании птичьего астровируса согласно изобретению с помощью праймеров 29 и 30 (SEQ ID NO: 30, 31), для проведения фазы циклов применяли следующие оптимальные условия: 45 циклов, со стадией отжига 30 секунд при 51°C. Другие условия были такими же, как и условия для реакции с использованием праймеров 20/21.
ПЦР-реакции для циклов реакций секвенирования проводили, в основном, в других условиях, а именно, 25 циклов: 10 секунд при 96°C; 5 секунд при 50°C; и 2 минуты при 60°С, см. ниже.
ПРИМЕР 5: Анализ ДНК, проводимый путем электрофореза в агарозном геле, очистка ДНК и ее субклонирование
Электрофорез в агарозном геле проводили в целях детектирования и визуализации полученных ПЦР-продуктов. Этот электрофорез проводили также для очистки ПЦР-продуктов путем их вырезания и экстракции, что позволяло осуществлять секвенирование или субклонирование выделенных ПЦР-продуктов.
Вкратце, 0,8% агарозных гелей (с низким уровнем электро-эндоосмоса) заливали в буфер TAE (pH 8,0), содержащий примерно 50 мкл 0,5 мг/мл раствора этидийбромида на 100 мл раствора агарозы. Образец ПЦР-продукта смешивали 1:10 со стандартным буфером для загрузки образца (глицерин/ДСН/бромфеноловый синий). Обычно включали дорожку маркеров с использованием SmartLadder® от Eurogentec™. Электрофорез при погружении в буфер TAE обычно проводили в течение 1 часа при напряжении 100 В для геля размером 20×20×1 см, или до тех пор, пока синяя окраска не достигала краев агара. Визуализацию проводили при УФ-облучении. Гели фотографировали цифровой камерой.
Электрофорез в агаровом геле также проводили в целях оценки концентрации ДНК в вырезанной и очищенной полосе, и в данном случае, образец пропускали по ряду дорожек, содержащих различные количества «лэддера» ДНК-маркеров.
Очистку специфических полос ПЦР-продуктов из агарозного геля проводили с использованием набора для гель-экстракции QIAquick® (QiaGen™) в соответствии с инструкциями производителей, а также с использованием либо микроцентрифуги, либо распределительного вакуумного устройства QIAvac®.
Полосы ДНК, вырезанные и выделенные из агарозного геля, субклонировали в бактериальные плазмиды, используемые для других целей, таких как клонирование, секвенирование, экспрессия или анализ методом гибридизации-детектирования. Фрагменты ДНК клонировали в плазмиду pCR2.1 с использованием вектора TOPO-TA® и набора для клонирования TOPO-TA® (Invitrogen™) в соответствии с инструкциями производителей.
ПРИМЕР 6: Секвенирование ДНК:
Секвенирование ДНК осуществляли путем проведения стандартных циклов ПЦР-секвенирования с использованием готовой реакционной смеси красителей для обрыва цепи (Big Dye® Terminator) (ABI Prism™) на автоматическом секвенаторе ABI Prism™ 310, в соответствии с инструкциями производителей.
Обычно в реакции секвенирования использовали 20-70 нг ДНК (очищенного ПЦР-продукта или фрагмента, клонированного в вектор), 8 мкл готовой реакционной смеси красителей для обрыва цепи (Big Dye® Terminator), 1 мкл 10 мкМ праймера в дистиллированной воде до получения общего объема 20 мкл. Обычно, для секвенирования использовали те же праймеры, которые были использованы в ПЦР для получения продукта двухцепочечной из кДНК.
ПЦР-секвенирование проводили в 25 циклов: 10 секунд при 96°C, 5 секунд при 50°C и 2 минуты при 60°C.
После проведения ПЦР, образцы очищали с использованием центрифужных колонок DyeEx® (QiaGen™) для удаления красителей для обрыва цепи в соответствии с инструкциями производителей, а также с использованием пробирок Эппендорфа® и микроцентрифуги. Конечный элюат ресуспендировали 1:2 до конечного объема 40 мкл с использованием дистиллированной воды.
Затем, определение последовательности осуществляли путем ее анализа на генетическом анализаторе ABI Prism® 310 с помощью программы для сбора данных (Data Collection, версии 1.0.4) и компьютерной программы для анализа последовательностей (Sequence Analysis, версии 3).
Анализ последовательностей проводили с использованием ряда программ, а в основном, с использованием программ Sequencher® (Gene Codes™), и Clone Manager® (Sci. Ed. Software™). Начало и конец последовательности усекали для удаления транскрибируемых нуклеотидов, которые были введены используемыми денатурированными ПЦР-праймерами.
Последовательности ДНК, указанные здесь в SEQ ID NO: 4-26 (четные номера), представляли собой консенсусные последовательности, полученные в результате проведения множества реакций секвенирования. В большинстве случаев, с использованием прямого и обратного секвенирующих праймеров были также определены последовательности для обеих цепей ДНК, и только последовательность SEQ ID NO: 8 была определена для одной цепи. Средняя избыточность составляла примерно 4 x на нуклеотид.
ПРИМЕР 7: Титрование астровируса на куриных яйцах с развивающимся эмбрионом
Суспензию с серийным 10-кратным разведением астровируса инокулировали в желточный мешок 6-дневных куриных яиц SPF с развивающимся эмбрионом с помощью 1"-иглы калибра 23G. Затем яйца инкубировали в инкубаторе в течение семи дней при 37°C.
Эти яйца ежедневно просвечивали. Случаи гибели эмбрионов в течение 24 часов после инокуляции рассматривались как неспецифические, а поэтому яйца, содержащие рано погибшие эмбрионы, отбрасывали и исключали из подсчета титра инфекционности.
Эмбрионы, погибшие в течение 2-7 дней после инокуляции, обследовали на присутствие поражений, характерных для инфекций, вызываемых астровирусом согласно изобретению, а именно, если ноги и кончики крыльев у погибших эмбрионов приобретали ярко-красную окраску, и если у них обнаруживалась увеличенная печень темно-красного цвета. Инфекционный титр вычисляли с помощью компьютерной программы методом Спирмена и Кербера, и выражали в ELD50 на мл.
ПРИМЕР 8: Продуцирование астровируса на куриных яйцах SPF с развивающимся эмбрионом
9-дневные куриные яйца SPF с развивающимся эмбрионом инокулировали 105 ELD50 астровируса на яйцо в желточный мешок 1½”-иглой калибра 22G. Затем эти яйца инкубировали при 37°C в инкубаторе.
После 24-часового инкубирования, яйца просвечивали. Гибель эмбрионов, которая происходила в течение 24 часов, рассматривалась как неспецифическая, и такие яйца исключали из эксперимента.
После 48-часового инкубирования, аллантоисную жидкость всех оставшихся яиц собирали. Аллантоисную жидкость хранили в замороженном виде при температуре ниже -60°C.
Титр инфекционности определяли путем титрования на куриных яйцах с развивающимся эмбрионом или на клетках, как описано выше.
ПРИМЕР 9: Получение первичных клеток:
Клетки CEL получали от 14-16-дневных куриных яиц SPF с развивающимся эмбрионом путем выделения печени из эмбриона. Эту печень промывали PBS/феноловым красным и инкубировали в течение 8-10 минут при комнатной температуре в растворе, содержащем трипсин в PBS. Супернатант собирали через 100 мкм-марлю. Эту процедуру повторяли более двух раз, а затем клетки собирали путем центрифугирования и ресуспендировали в подходящей обогащенной культуральной среде, содержащий 5% фетальную телячью сыворотку (FCS).
Клетки CEK получали аналогичным образом с использованием почек от куриных эмбрионов SPF в возрасте примерно 18 дней. Полученные почки осторожно очищали, промывали и один раз трипсинизировали в течение 20 минут при комнатной температуре. Затем, клетки CEK фильтровали и помещали в культуральную среду + FCS.
ПРИМЕР 10: Анализ IFT:
Для оценки перекрестной видовой специфичности некоторых антисывороток, а также для титрования вируса проводили иммунофлуоресцентные тесты (IFT). Обычно IFT осуществляли на первичных клетках в микротитрационных планшетах.
Если для IFT использовали клетки CEK, то эти клетки высевали в лунки 96-луночных микротитрационных планшетов при плотности 105 клеток/100 мкл. Клетки находились в стандартной обогащенной культуральной среде, содержащей 2% FCS и антибиотики, и были инкубированы при 37°C в атмосфере 5% CO2. На следующий день, эти клетки были инокулированы вирусом.
Для титрования были использованы серийные разведения вируса. Затем планшеты инкубировали в течение еще 2 дней. После этого супернатант удаляли, и клетки фиксировали чистым этанолом при -70°C. Эти планшеты хранили при -20°C вплоть до их использования. Для визуализации вируса, используемого для титрования, планшеты окрашивали специфической антисывороткой. Поэтому планшеты доводили до комнатной температуры, а затем отмывали спиртом и промывали PBS. Разведение антивирусной сыворотки проводили при концентрации, которая, как известно, давала хорошую флуоресценцию, но не слишком высокое фоновое излучение. Затем в планшеты добавляли первую антисыворотку и инкубировали в течение 1 часа при 37°C в атмосфере с повышенной влажностью. Эти планшеты 3 раза промывали PBS. Затем получали конъюгат со «вторым» антителом, а именно конъюгат «козье антитело против куриных IgG-ФИТЦ» (Nordic™). После этого, планшеты подвергали необходимому разведению и снова инкубировали в течение 1 часа при 37°С. После такого инкубирования, планшеты снова 3 раза промывали PBS, а затем дабавляли смесь PBS:глицерин в отношении 1:1. После этого планшеты помещали на хранение в темноте при 4°C, а затем оценивали под флуоресцентным микроскопом. Позитивный сигнал означал детекцию специфической флуоресценции, коррелирующим с уровнем цитопатического эффекта в клеточном слое.
Для характеризации сыворотки и проведения тестов на перекрестную реакцию между различными видами, микротитриционные планшеты приготавливали аналогичным образом с использованием клеток CEK или CEL. На следующий день клетки инфицировали различными тестируемыми вирусами, например, изолятами астровируса согласно изобретению, ANV1 и CAstV2, а также другими птичьими патогенами, а именно, реовирусом, IBV, NDV, FPV, аденовирусом, AIV и т.п. Количество вируса было фиксированным, либо вирусы подвергали разведению, если это было необходимо. Планшеты инкубировали в течение 2-3 дней.
Для определения способности некоторых антисывороток связываться с различными вирусами, эти сыворотки инкубировали на планшетах, и сигнал усиливали путем инкубирования с конъюгатом. Для оптимизации отношения сигналов «связывание - фон», ряд разведений антисывороток в PBS был протестирован при различных разведениях различных вирусов.
ПРИМЕР 11: Инфицирование кур астровирусом
Птичий астровирус согласно изобретению был протестирован на курах в экспериментальной схеме для воспроизведения симптомов заболевания, наблюдаемых в природе, и для повторного выделения микроорганизма у этих повторно инфицированных птиц. Это было осуществлено для удовлетворения требованиям постулатов Коха в целях подтверждения того факта, что тестируемый изолят является патогенным и вирулентным микроорганизмом и этиологическим инфицирующим фактором, вызывающим симптомы, наблюдаемые в природе.
Кроме того, куры были повторно инфицированы для оценки эффективности вакцинации живым инокулятом, проводимой путем последующих контрольных заражений.
И наконец, у экспериментально инфицированных кур выделяли всю сыворотку для получения специфической поликлональной антисыворотки против астровируса-инокулята.
Для этих целей, трех-недельные куры-несушки SPF обоих полов, принадлежащие к породе белый леггорн, помещали в изолятор с отрицательным давлением. Затем птиц произвольно распределяли по экспериментальным группам, и индивидуально метили двумя полосками на крыльях. Птицы получали стандартный корм и питьевую воду ad libitum.
Через определенные интервалы времени, а также на день 0, у птиц брали экспериментальные пробы крови для определения их иммунного статуса. Затем 15 кур инокулировали тремя способами, а именно, 0,2 миллилитрами путем офтальмического и внутримышечного введения, а также 0,5 миллилитрами путем перорального введения, при дозе 105 EID50/0,2 мл, и 105,4 EID50/0,5 мл. Инокулят представлял собой депонированный изолят 19 астровируса, ресуспендированный в воде для инъекций. 5 кур, помещенных в тот же самый изолятор, не инокулировали, и такие куры служили в качестве контроля и являлись объектом наблюдения. Этих птиц ежедневно осматривали на присутствие клинических признаков заболевания и для определения смертности.
На 20-й день после инокуляции (p.i.), ряд кур умерщвляли путем кровопускания и подвергали гистопатологическому анализу post-mortum. На 23-й день p.i., другим курам (предварительно инокулированным) повторно вводили аналогичную дозу инокулята. Еще через 23 дня эксперимент завершали, и оставшихся живых птиц умерщвляли путем кровопускания и анализировали.
Некоторые птицы с самого начала не были инокулированы, но содержались в тех же самых изоляторах, как и инокулированные/инфицированные птицы, и эти птицы, как и ожидалось, становились инфицированным путем горизонтального распространения астровируса.
ПРИМЕР 11a: Результаты гистопатологического анализа:
В испытаниях, проводимых на животных, были получены следующие результаты гистопатологического анализа: 2 курицы погибали, а у 5 кур, из которые 3 были контрольными, наблюдалась диарея. После гистопатологического анализа, уже на 7-й день p.i., у некоторых птиц наблюдалась патология почек и желудочно-кишечного тракта различной степени тяжести. Почки были поражены тяжелым интерстициальным нефритом и дегенерацией канальцев, которые являются наиболее ярко выраженными признаками заболевания. В тимусе и в бурсе наблюдался лимфоцитолиз, в поджелудочной железе наблюдался апоптоз и атрофия ацинуса, а в двенадцатиперстной кишке обнаруживались ослабленные и сросшиеся ворсинки.
Горизонтальное инфицирование инокулированных контрольных кур указывало на вирулентность и инфекционность инокулята астровируса.
ПРИМЕР 11b: Результаты ПЦР
Образцы почек всех кур тестировали с помощью ПЦР на признаки птичьего астровируса согласно изобретению. После гомогенизации и выделения РНК получали OT-образцы. Полученные образцы тестировали с помощью ПЦР с использованием праймеров SEQ ID NO: 30 и 31. Все образцы инфицированных животных были протестированы как позитивные, на что указывало присутствие специфической полосы размером 260 п.н., которая является показателем наличия птичьего астровируса согласно изобретению. Был включен соответствующий позитивный и негативный контроли.
Было продемонстрировано, что этиологическим фактором смертности и патогеном, ответственным за наблюдаемые гистопатологические признаки, является птичий астровирус согласно изобретению. Наблюдаемые симптомы, такие как нефрит и диарея, соответствуют симптомам, наблюдаемым в природе. Симптомы поражения ног не могли быть репродуцированы, поскольку используемые птицы, по всей вероятности, имели очень слабый скелет, а поэтому имели такие же симптомы, и/или условия содержания кур SPF в изоляторе не могли в достаточной степени имитировать множественное инфекционное давление у птиц, наблюдаемых в природе.
ПРИМЕР 11c: Результаты VN-анализа:
Фиксированные количества изолята 19 астровируса инкубировали с куриной антисыворотков на дни 0, 20 и 46 после инокуляции (p.i.) в течение 1 часа при 37°С. Затем эти вирусные образцы инокулировали в 6-дневные яйца SPF с развивающимся эмбрионом, и инкубировали в течение нескольких дней. Через 4 дня после инокуляции яиц, эмбрионы, зараженные вирусом и обработанные сывороткой на день 0, погибали, и у них обраруживались типичные признаки инфицирования птичьим астровирусом согласно изобретению.
Однако, вирус, инкубированный с сывороткой, взятой на 20-й день или на 46-й день, не поражал эмбрионы. Это указывало на то, что изолят 19 вируса может быть эффективно нейтрализован специфической куриной антисывороткой.
Кроме того, это подтверждает то, что эффективная антисыворотка с VN-способностью может быть индуцирована у кур после их инокуляции живым птичьим астровирусом согласно изобретению.
ПРИМЕР 11d: Результаты IFT-анализа:
Результаты IFT-анализов на перекрестную раекцию, проводимые с использованием куриной поликлональной антисыворотки, показали, что антисыворотка против изолята 19 не распознавала какой-либо вирус, не являющийся изолятом птичьего астровируса согласно изобретению.
Аналогичным образом, антисыворотка, специфичная к ANV1 или CAstV2, в равной степени распознавала лишь конкретный вирус, против которого она направлена. Также важно отметить, что ни сыворотка против ANV1, ни сыворотка против ChAstV2 не связывались с вирусным изолятом птичьего астровируса согласно изобретению. Это также относится к самым высоким тестируемым количествам антитела (образцам с наименьшим разведением).
Кроме того, ни одна из антисывороток против других птичьих патогенов, а в основном, направленных против реовирусов, не могла связываться с вирусными изолятами птичьего астровируса согласно изобретению или наоборот.
Это указывает на то, что птичий астровирус согласно изобретению принадлежит к своей собственной новой и уникальной серологической группе, что, таким образом, объясняет наличие идентифицированных уникальных молекулярно-биологических отличительных признаков.
Планшеты с клетками CEK инфицировали изолятом 19 астровируса 3-го пассажа с серийными 10-кратными разведениями вируса. Через два дня, планшеты фиксировали и окрашивали различными антисыворотками:
- пулом сыворотки против изолята 19 на 33-й день после инокуляции, 1:20 в PBS,
- антисывороткой против ANV1 (штамма SE-027/2), полученной у кур; 1:20 в PBS (ANV1 представляет собой изолят ANV1, который был получен в Германии и который, после секвенирования ДНК специфических областей, оказался наиболее близкородственным сравниваемой последовательности ANV1 от GenBank, используемой в настоящей заявке).
- антисывороткой против CAstV2 (штамма TS9L), полученной у кур, 1:500 в PBS (CAstV1 происходил от образца, который был депонирован в CNCM в Париже, Франция, под депозитарным номером I-2932).
- негативным контролем, только PBS.
После конъюгирования с козьим антителом против куриных IgG, планшеты считывали.
|
ПРИМЕР 12: Дополнительные испытания по вакцинации
Инактивированная вакцина:
Индеек и кур вакцинировали вакциной инактивированного астровируса согласно изобретению с адъювантом для оптимизации дозы антигена.
Изолят 19 астровируса культивировали на клетках CEL? как описано выше? и инактивировали с использованием бета-пропиолактона (BPL) с регулируемой температурой и регулируемыми значениями рН в соответствии со стандартными протоколами. Инактивированный астровирус гомогенизировали в стандартной эмульсии типа «вода в масле», состоящей из легких фракций минерального масла и соответствующих эмульгаторов в соответствии со стандартными протоколами.
Индейки и куры содержались в изолированных клетках: 120 двухнедельных индеек стандартного типа произвольно распределяли по 6 отдельным группам (группы 1-6) так, чтобы каждая группа содержала 20 птиц. В возрасте трех недель, индеек в группах 1-4 внутримышечно вакцинировали вакцинной эмульсией типа «вода в масле», содержащей изолят 19 инактивированного астровируса. Индеек группы 5 подкожно вакцинировали той же самой вакцинной эмульсией типа «вода в масле», а индеек группы 6 не вакцинировали и использовали в качестве контроля.
Аналогичным образом, 180 однодневных кур-несушек SPF произвольно распределяли по 9 отдельным группам (группы 7-15) так, чтобы каждая группа содержала 20 кур. В возрасте трех недель, кур в группах 7-10 внутримышечно вакцинировали вакцинной эмульсией типа «вода в масле», содержащей инактивированный астровирус типа 3. Кур группы 11-14 подкожно вакцинировали той же самой вакциной, а кур группы 15 не вакцинировали и использовали в качестве контроля.
Перед началом эксперимента и через 4, 8 и 12 недель после вакцинации, у всех индеек и кур брали пробы крови. Сыворотку оценивали на присутствие антител против астровируса согласно изобретению и его титров с помощью IFT-анализа на клетках CEL или VN-анализа.
Этот протокол может быть легко модифицирован так, чтобы он включал, если это необходимо, исследования на сохранение иммунитета, проводимые, например, путем содержания вакцинированных птиц в изоляторах в течение еще 6-12 месяцев с последующим провокационным заражением астровирусом согласно изобретению.
«Живая» вакцина:
Кур вакцинировали дозой «живого» астровируса согласно изобретению, а затем они были подвергнуты провокационному заражению астровирусом для оптимизации способа применения вакцины на основе «живого» астровируса.
100 однодневных коммерчески доступных MDA+ (антитело-положительных по материнской линии) племенных кур распределяли по 5 отдельным группам, так, чтобы каждая группа содержала 20 кур. Однодневных цыплят в группах 1-4 вакцинировали изолятом 19 взятого из аллантоисной жидкости «живого» астровируса путем закапывания в глаза, введения в распыляемом растворе из крупных частиц, введения в аэрозольном спрее или с питьевой водой. Цыплят в группе 5 не инокулировали, и эти цыплята служили в качестве невакцинированного контроля. Через 4 недели после вакцинации, всех кур подвергали контрольному заражению астровирусом согласно изобретению. В течение трех недель после контрольного заражения, всех кур ежедневно обследовали на наличие клинических признаков, характерных для астровирусной инфекции, и/или на смертность. Через 21 день после контрольного заражения, всех оставшихся кур умерщвляли и подвергали гистопатологическому анализу.