Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ ГЛИКОЛЕВОЙ КИСЛОТЫ
Вид РИД
Изобретение
Гликолевая кислота находит широкое применение в различных отраслях промышленности: пищевой, кожевенной, нефтегазовой, обрабатывающей, текстильной, строительной и т.д. Данная кислота обладает рядом важных свойств, обусловливающих ее широкое практическое применение в медицине: она используется в качестве мономера для получения биоразлагаемых гомополимеров и сополимеров с заданными свойствами, используемых, главным образом, в медицине в качестве саморассасывающихся имплантантов. Полимеры на основе гликолевой кислоты могут применяться в качестве барьерных материалов, препятствующих проникновению кислорода. Кроме того, гликолевая кислота используется в косметологической практике для нормализации процессов обмена и кожной микроциркуляции.
Известным способом получения гликолевой кислоты, реализованным в промышленности, является способ карбонилирования формальдегида [Пат. 2152852 США, МПК C07C 59/00. Process for manufacture of glycolic acid / Loder D.J.; заявитель и патентообладатель du Pont, США. - опубл. 04.04.39. - 4 с.]. Данный способ получения кислоты основан на взаимодействии угарного газа с формальдегидом (или его полимерами - параформальдегидом, триоксаном или их смесью) и водой при высоких давлениях и температуре в присутствии катализаторов. В качестве катализаторов используются сильные кислоты и их соли: фтористоводородная, хлористоводородная, серная, фосфорная, трифторид бора; сульфат калия, фосфат натрия и т.д. Процесс проводится при температуре 110-200°C и давлениях порядка 600-700 атм. Данный способ получения гликолевой кислоты сопряжен со значительным износом оборудования, обусловленным высокими температурами и агрессивностью среды, поэтому целевой продукт получается загрязненным примесями металлов, что требует дополнительной стадии очистки. Выход гликолевой кислоты составляет 20-60% мас. Наряду с целевым продуктом получаемый раствор содержит примеси формальдегида, муравьиной кислоты и уксусной кислот, простые и сложные эфиры гликолевой кислоты. Остро стоит вопрос с удалением катализатора - кислоты.
Известен способ получения гликолевой кислоты омылением уксусной кислоты [Пат. 5723662 США, МПК C07C 59/00. Process for preparing a particularly pure glycolic acid / Ebmeyer F. et al.; заявитель и патентообладатель Hoechst Aktiengesellschaft, Германия. - опубл. 03.03.98. - 3 с.]. В данном способе нейтрализацию хлоруксусной кислоты проводят двукратным избытком щелочи NaOH или KOH при температуре от 100 до 160°C и избыточном давлении до 10 атм, затем при завершении реакции проводят фильтрацию раствора для отделения хлорида щелочного металла. После омыления и фильтрации в реакционной массе остаются лишь следовые количества хлоруксусной кислоты. В патенте [Пат. 5723662 США, МПК C07C 59/00. Process for preparing a particularly pure glycolic acid / Ebmeyer F. et al.; заявитель и патентообладатель Hoechst Aktiengesellschaft, Германия. - опубл. 03.03.98. - 3 с.] предлагается для окончательной очистки маточный раствор подвергать электродиализу при температуре 20-40°C и напряжении от 0,5 до 2,5 В на ячеечную пару при концентрации гликолевой кислоты от 40 до 60% мас. Омыление осуществляется с избытком гидроксида щелочного металла от 2 до 8% мас., что позволяет провести более глубокую очистку методом классического электродиализа. Однако такая очистка приводит не только к удалению хлорида щелочного металла, но и к потерям целевого продукта и его разбавлению из-за процессов диффузии воды из камер концентрирования в камеры с очищаемым раствором.
Также известен способ получения гликолевой кислоты гидролизом циангидрина. Циангидрин получают реакцией формальдегида с синильной кислотой согласно [Пат. 2153064 США, МПК C07C 59/00. Process for the preparation of glycolic acid / Lanon A.T.; заявитель и патентообладатель du Pont, США. - опубл. 04.04.39. - 5 с.]. В качестве катализатора используются соединения щелочных металлов - гидроксиды, галогениды, сульфиты, кислые сульфиты, сульфаты, формиаты и другие. Из них наибольшей каталитической активностью обладают гидроксиды. Процесс проводится при температуре от 45 до 60°C и давлении от 0,1 до 0,8 МПа. После получения циангидрин сразу подвергают гидролизу, что связано с быстрой его деструкцией при температурах выше 10°C.
Оптимальными условиями проведения кислотного гидролиза циангидрина являются рН в пределах от 1,8 до 2,0, температура от 50 до 80°C и давление от 0,1 до 0,8 МПа. В качестве катализатора могут быть выбраны как минеральные кислоты (серная, соляная, азотная, фосфорная) с выходами до 100%, так и органические (малеиновая кислота) с выходами от 30-70%. Как правило, в качестве минеральной кислоты используют серную или фосфорную. В патенте [Пат. 3867440 США, МПК C07C 59/06. Process for the preparation of glycolic acid / Kobetz P.; заявитель и патентообладатель Ethyl Corporation, США. - опубл. 18.02.75. - 4 с.] кислотный гидролиз циангидрина проводят в присутствии кислоты, имеющей pKa 1,5-2,5, например Н3РО3 или H2SO3, и температуре 75-175°C. Время проведения процесса составляет от 3 до 30 часов (в зависимости от температуры). Продуктами служат оксикислоты и их амиды.
Проведение щелочного гидролиза циангидрина осуществляется при повышенном давлении и температуре. В качестве щелочного агента может выступать: гидроксид натрия, гидроксид калия и гидроксид лития. Гидроксиды натрия и калия являются более предпочтительными. Гидролиз проходит за достаточно короткое время от 0,5 до 5 ч, при температуре от 50 до 80°C и давлении от 0,1 до 0,8 МПа. Продукт получается в виде аммонийной соли. В японском патенте [Пат. 2008156300 Япония, МПК C07C 51/02, C08G 63/06, C07C 59/06, C12P 7/42. Method for producing glycolic acid / Makoto О.; заявитель и патентообладатель Asahi Kasei Chemicals Corporation, Япония. - опубл. 07.09.12. - 15 c.] проблема получения гликолевой кислоты из гликолята аммония решается осаждением гликолята кальция из раствора гликолята аммония. Растворимость гликолята аммония составляет 520 г/100 г воды (83,9% мас.) при 25°C, в то время как растворимость гликолята кальция - 1,5 г/100 г воды (1,5% мас.) при 28°C. Далее гликолят кальция растворяют в серной кислоте с получением осадка CaSO4×2Н2О. Однако серная кислота при высокой концентрации выступает в роли окислителя, а образующаяся гликолевая кислота может выступать в роли восстановителя. Образующийся осадок CaSO4×2H2O очень мелкодисперсный и легко проходит через фильтр. Растворимость CaSO4×2H2O составляет 2,06 г/100 г воды при 20°C. Использование мелкопористых фильтров будет приводить к увеличению времени, затрачиваемого на фильтрование, и забиванию фильтров, делая весь процесс неэффективным. Проведение процесса высаживания крупнокристаллического осадка α-CaSO4×½4H2O требует нагревания реакционной смеси до температуры выше 66°С, что будет приводить к значительным энергетическим затратам и окислению образующейся гликолевой кислоты. К тому же растворимость α-CaSO4×½2H2O составляет 7,9 г/100 г воды при 20°С.
В последнее время широкое распространение получил метод ферментативного гидролиза циангидрина под действием фермента нитрилазы [Пат. 7638617 США, МПК C07H 21/04, C12N 1/20, С12Р 7/40. Enzymatic production of glycolic acid / DiCosimo R.; заявитель и патентообладатель du Pont, США.- опубл. 29.12.09. - 70 с.]. Основные недостатки ферментативного получения гликолевой кислоты в том, что необходимо использовать достаточно чистый циангидрин, к примеру высокая примесь формальдегида может значительно повлиять на ход реакции и активность энзима. Также дезактивацию энзима вызывает небольшой процент альдегидов, получаемых в ходе побочных реакций.
Процесс проводят при температуре от 5 до 10°С, в течение 4-15 ч. Для повышения выхода и уменьшения побочных продуктов при работе с бактериями применяется кратковременное повышение температуры, при котором разрушаются нитрилгидратазы и амидазы и сохраняется рабочий фермент. Основной недостаток метода - трудоемкость проведения и значительное загрязнение продукта.
Кроме того, известен способ получения гликолевой кислоты окислением этиленгликоля кислородом в смеси с азотом на неорганических гетерогенных катализаторах, содержащих соединения платины или палладия с висмутом. Однако процессы сопряжены с неполной конверсией этиленгликоля, что дает сложную смесь продуктов, содержащую кроме гликолевой кислоты еще и примеси альдегидов, эфиров и исходного сырья.
Известен способ получения гликолевой кислоты путем каталитической этерификации этиленгликоля. Процесс получения включает в себя получение метилгликолята путем взаимодействия этиленгликоля с метиловым спиртом и воздухом в присутствии катализатора на основе благородных металлов при температуре 50-150°С в течение 10-180 минут. Второй стадией является гидролиз метилгликолята с получением гликолевой кислоты [Пат. 7005536 США, МПК С07С 69/66. Method for producing diol derivatives / Hayashi T. et al.; заявитель и патентообладатель Nippon Shokubai Co., Ltd., Япония. - опубл. 28.02.06. - 23 с.]. Данный процесс характеризуется невысокой селективностью по целевому продукту и высокой стоимостью золотосодержащих катализаторов. К тому же в процессе реакции этерификации образуется не только метилгликолят, но и эфиры щавелевой кислоты, имеющие близкую температуру кипения. Температура кипений метилгликолята составляет 151°С, а диметилоксалата 164°С, поэтому они не могут быть разделены простой перегонкой.
Известны способы получения гликолевой кислоты по способу Канниццаро, путем внутримолекулярного диспропорционирования. Процесс проводят в двух вариантах.
1. Способ получения гликолевой кислоты путем внутримолекулярного диспропорционирования глиоксаля в присутствии неорганических катализаторов, таких как хлорид, нитрат, сульфат или гидроксид алюминия [Takashi О. et al. Theoretical study of Al(III)-catalyzed conversion of glyoxal to glycolic acid: dual activated 1,2-hydride shift mechanism by protonated Al(ОН)3 species // Chem. Commun., 2009. - Vol. 45. - Iss. 19. - P. 2688-2690]. Процесс проводят в инертной атмосфере, при использовании 15% раствора глиоксаля, повышенном давлении и температуре порядка 165°С, при этом достигается практически полная конверсия исходного сырья. Количество катализатора, необходимое для протекания процесса, составляет до 1% (мол.). К недостаткам процесса относится трудность отделения катализатора и образование смолистых примесей.
2. Способ получения гликолевой кислоты путем внутримолекулярного диспропорционирования глиоксаля в концентрированных водных или водно-спиртовых растворах щелочи. В результате данной реакции образуется гликолят (соль гликолевой кислоты) соответствующего щелочного или щелочноземельного металла. Реакцию проводят при охлаждении, чтобы уменьшить выход побочных продуктов реакции (продукты побочных реакций конденсации и осмоления), обуславливающих цветность раствора. Катализаторами данной реакции являются различные металлы (например, серебро, никель, медь) и их оксиды. Наличие примесей в глиоксале, таких как гликолевый альдегид, формальдегид и т.д., имеющих атомы водорода в α-положении, приводит к протеканию преимущественно реакций альдольной конденсации, а не реакции Канниццаро. В [Органические реакции: в 14 т. / гл. ред. Р. Адамс. - М.: Госуд. изд-во иностр. лит., 1950. - Т. 2. - 532 с.] предлагается проводить реакцию Канниццаро между альдегидами, неимеющими атомы водорода в α-положении, в частности глиоксалем, при комнатной температуре в 50% водно-спиртовом растворе щелочи с выходом, непревышающим 60%. Данный способ выбран в качестве прототипа. В патенте [Пат. 8106238 США, МПК С07С 59/00. Method for producing glycolic acid / Hinago H. et al.; заявитель и патентообладатель Asahi Kasei Chemicals Corporation, Япония. - опубл. 31.01.12. - 9 c.] и [Salomaa P. The kinetics of the Cannizzaro Reaction of Glyoxal // Acta Chem. Scand., 1951. - Vol. 10. - №. 2. - P. 311-319] отмечается, что реакция Канниццаро является реакцией диспропорционирования и поэтому ее протекание сопряжено с образованием большого количества побочных продуктов, затрудняющих получение чистой гликолевой кислоты.
Новая техническая задача, на решение которой направлено настоящее изобретение, состоит в создании более эффективного способа получения гликолевой кислоты из глиоксаля с более высоким выходом по сравнению с прототипом.
Для решения поставленной задачи по получению гликолевой кислоты целесообразно проводить реакцию Канниццаро в водной среде при минимальных концентрациях щелочи от 0,5 до 6,5 моль/л, чтобы свести к минимуму выход побочных продуктов реакции. Одним из отличительных признаков заявляемого способа является то, что уменьшению выхода побочных продуктов реакции внутри молекулярного диспропорционирования глиоксаля способствует охлаждение реакционной смеси до температуры от 0 до 10°C и ее постоянное перемешивание при незначительном избытке щелочи (мольное отношение глиоксаля к щелочи составляет от 1:1,05 до 1:1,1). Данный избыток способствует полному превращению глиоксаля в гликолят натрия и обеспечивает меньшее омическое сопротивление в электродиализаторе-синтезаторе при конверсии гликолята натрия в гликолевую кислоту, что уменьшает тепловыделение и избавляет от необходимости использования охлаждения электродного, солевого и щелочного растворов. Отсутствие необходимости использовать теплообменники при конверсии гликолята натрия в гликолевую кислоту методом электродиализа с биполярными мембранами упрощает технологический процесс и уменьшает стоимость целевого продукта.
Реакция внутримолекулярного диспропорционирования глиоксаля проводится в водном растворе щелочи при таких концентрациях 0,5-0,65 моль/л, чтобы уменьшить выход побочных реакций осмоления глиоксаля:
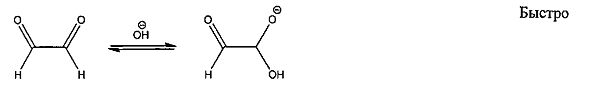
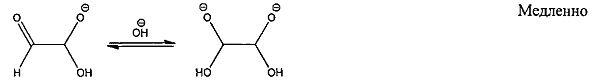
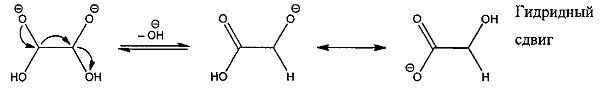
Процесс получения гликолята натрия связан с постепенным прибавлением 40% мас. водного раствора глиоксаля в 0,5-0,65 моль/л водный раствор щелочи при непрерывном перемешивании реакционной массы. Температура, при которой проводится реакция, не должна превышать 0-10°C. При таких условиях теоретический выход соли составляет 100%. Для обеспечения высокой чистоты продукта целесообразно использовать в процессе синтеза воду с удельным сопротивлением, составляющим 12-15 Мом×см.
Перед проведением конверсии гликолята натрия в гликолевую кислоту методом электродиализа с биполярными мембранами необходимо удалить продукты осмоления сорбцией на активированных углях марки ОУ-А, 207ЕА, 607Е или AGC, которые добавляют из расчета 1-5% мас. в пересчете на получаемый гликолят натрия. Раствор гликолята натрия пропускают через колонку, заполненную активированным углем, 3-5 раз со скоростью 2-4 м/сек. При вымывании частичек активированного угля необходимо отфильтровать раствор соли.
Свежеприготовленный раствор гликолята натрия, предварительно очищенный с использованием гранулированного активированного угля, подвергается безреагентной конверсии в гликолевую кислоту методом электродиализа с использованием биполярных мембран.
Электродиализатор-синтезатор (далее ЭДС) включает в себя пять элементарных двухкамерных ячеек с рабочей площадью каждой мембраны 1 дм2 и общей полезной площадью мембран 1 м2. Предпочтение двухкамерной элементарной ячейке ЭДС было отдано по причине образования гликолевой кислоты (pKa=3,83) в процессе конверсии гликолята натрия. Использование трехкамерной элементарной ячейки, образованной чередующимися биполярной, катионо- и анионообменной мембраной, не оправдано, так как при уменьшении концентрации гликолята натрия в солевой камере и увеличении концентрации гликолевой кислоты в кислотной камере аппарата будет уменьшаться проводимость соответствующих растворов и, как следствие, расти сопротивление. Рост сопротивления приведет к увеличению выделения джоулева тепла и, как следствие, к уменьшению выхода по току кислоты.
Процесс конверсии гликолята натрия с концентрацией 0,65 моль/л проводится при плотности тока j=1 А/дм2 в течении 10 часов. При этом начальная проводимость раствора гликолята натрия составляла 26,5, а конечная - 2,2 мСм/см. Изменение рН фиксируется в интервале от 8,3 до 1,8 в начальный и конечный момент времени соответственно. Такой режим позволяет добиться 100% конверсии гликолята натрия в гликолевую кислоту. В предлагаемом нами способе из-за особенности проведения процесса электродиализной конверсии гликолята натрия в гликолевую кислоту достигается 100% конверсии соли в кислоту. Выход по току кислоты составляет 75%, при этом на получение 1 кг чистой кислоты потребуется затратить 0,31 кВт×ч электричества. При данной плотности тока производительность ЭДС составляет 0,468 кг кислоты в час с 1 м2 эффективной поверхности мембран.
Полученную гликолевую кислоту с концентрацией 0,457-0,772 моль/л (3,43-5,39% мас.) конверсией гликолята натрия методом электродиализа с биполярными мембранами подвергают концентрированию методом вакуумного ротационного испарения до концентрации товарного продукта 70% мас. водного раствора. Применение такого метода позволяет проводить концентрирование гликолевой кислоты при температуре 50°C без образования продуктов осмоления, которые загрязняют и уменьшают выход целевого продукта. Воду отгоняют при давлении до 50 мм рт.ст., которого достаточно для эффективного удаления воды (температура кипения воды при 50 мм рт.ст. составляет 44°C).
После получения 70% мас. водного раствора гликолевой кислоты для получения кристаллов целевого продукта необходимо имеющийся водный раствор охладить до температуры не более 10°C. Для ускорения процесса кристаллизации целесообразно внести заранее подготовленные затравочные кристаллы гликолевой кислоты. Масса затравочных кристаллов должна составлять от 0,01 до 1% мас. в зависимости от концентрации мономерной формы кислоты в растворе. Чем больше концентрация олигомеров (не менее 5% мас.) гликолевой кислоты в исходном 70% мас. водном растворе, тем больше необходимо добавлять затравочных кристаллов. При отсутствии затравочных кристаллов можно использовать перемешивание для ускорения процесса кристаллообразования. Интенсивность перемешивания должна быть такой, чтобы скорость кристаллообразования в несколько раз превышала скорость зародышеобразования кристаллов гликолевой кислоты.
Выпавшие кристаллы кислоты отфильтровываются и сушатся на фильтре при комнатной температуре в атмосфере инертного газа. Полученные кристаллы остаются химически стабильными в плоть до температуры 50°C и относительной влажности 85-95%. Выход продукта составляет 47-53% от теоретически возможного. Полученные кристаллы при этом содержат не менее 99,5% мас. основного компонента. Выше указанной температуры преобладают процессы олигомеризации.
Осуществление способа поясняется примерами.
ПРИМЕР 1
Для получения гликолята натрия в реакторе с верхнеприводной мешалкой готовят с использованием воды, имеющей сопротивление не менее 12-15 Мом·см, раствор едкого натра с концентрацией 0,579 моль/л в объеме 10 литров. При температуре не более 10°C и постоянном перемешивании прикапывают 305,3 г водного раствора глиоксаля с концентрацией 40% мас. После проведения реакции получается 0,5 моль/л раствор гликолята натрия, содержащий непрореагировавшую щелочь с концентрацией 0,053 моль/л. Выход составляет 95% от теоретически возможного.
Полученный раствор гликолята натрия с концентрацией 0,5 моль/л очищают от продуктов осмоления сорбцией на активированном угле, который добавляют из расчета 1-5% мас. в пересчете на получаемый гликолят натрия. Целесообразно использовать активированные угли марок 207ЕА, 607Е или AGC, которые имеют зольность менее 1%, в/в и развитую поверхность 1150-1500 м2. Раствор гликолята натрия пропускают через колонку, заполненную активированным углем, 3-5 раз. Для увеличения эффективности очистки гликолята натрия диаметр колонки должен быть меньше ее высоты не менее чем в 100 раз. При вымывании частичек активированного угля необходимо отфильтровать раствор соли.
Очищенный от примесей раствор гликолята натрия объемом 10 литров с концентрацией 0,5 моль/л подвергают безреагентной конверсии в гликолевую кислоту методом электродиализа с биполярными мембранами, в качестве которых используются гомогенные биполярные мембраны, а в качестве катионообменных - гетерогенные мембраны МК-40. Раствор соли с удельной проводимостью 23,2 мСм/см подается в кислотно-солевые камеры электродиализатора синтезатора. На электроды из платинированного титана подается такое напряжение, которое обеспечивает плотность тока не менее 1 А/дм2. Процесс конверсии соли в кислоту осуществляется до того момента, когда удельная проводимость раствора кислоты в кислотно-солевом тракте не достигнет минимального значения 2,23 мСм/см и не будет уменьшаться в течение 10-15 минут. Результаты ВЭЖХ-анализа свидетельствуют о 100% конверсии соли в кислоту.
Полученная гликолевая кислота объемом 9,65 литров имеет концентрацию 0,457 моль/л (88,2% от теоретически возможного). Уменьшение объема раствора, циркулирующего в кислотно-солевых камерах ЭДС, вероятно, обусловлено электроосмотическим переносом молекул растворителя в щелочные камеры. Небольшой радиус катиона натрия обуславливает наличие крепко связанной с ним сольватной оболочки. Частично уменьшить перенос растворителя из кислотно-солевых камер можно, создав избыточное давление в щелочных камерах ЭДС, чтобы создались такие условия, при которых осмотический перенос через мембрану компенсировал бы электроосмотический. Разность давления между трактами должна составлять 10-60 кПа. Потенциометрическое титрование раствора щелочи из щелочного тракта показало, что наблюдается перенос гликолят анионов через гомогенную биполярную мембрану в щелочные камеры ЭДС. Об этом свидетельствовало наличие второго максимума на дифференциальной кривой потенциометрического титрования.
В процессе конверсии гликолята натрия выход по току для кислоты составляет 68,8%. При этом на получение 1 кг кислоты затрачивается 0,323 кВт·ч электроэнергии, а производительность составляет 195,3 г кислоты в час с 1 м2 эффективной площади мембран.
Далее раствор гликолевой кислоты объемом 10,3 литров с концентрацией 0,457 моль/л подвергают концентрированию методом вакуумного ротационного испарения до концентрации товарного 70% мас.
Полученный водный раствор гликолевой кислоты с концентрацией 70% мас. загружают в реактор, подключенный к термокриостату, и охлаждают до температуры не более 10°C. Для ускорения процесса кристаллизации целесообразно внести заранее подготовленные затравочные кристаллы гликолевой кислоты. Масса затравочных кристаллов должна составлять не мене 0,05% мас. в зависимости от концентрации мономерной формы кислоты в растворе. Чем больше концентрация олигомеров гликолевой кислоты в исходном 70% мас. (не менее 5 но не более 7% мас.) водном растворе, тем больше необходимо добавлять затравочных кристаллов. Для ускорения процесса кристаллообразования кристаллизацию необходимо вести при постоянном перемешивании. Выпавшие кристаллы отфильтровывают, затем 2-3 раза промывают маточным раствором и сушат на фильтре при комнатной температуре в атмосфере инертного газа. Полученные кристаллы остаются химически стабильными в плоть до температуры 50°C при относительной влажности 85-95%. Выход продукта составляет 168,25 г, что соответствует 47% от теоретически возможного. Полученные кристаллы, по данным ВЭЖХ-анализа, при этом содержат не менее 99,5% мас. основного компонента.
ПРИМЕР 2
Для получения гликолята натрия в реакторе с верхнеприводной мешалкой готовят с использованием деионизованной воды, имеющей сопротивление не менее 12-15 Мом·см, раствор едкого натра с концентрацией 0,737 моль/л в объеме 50 литров. При температуре не более 5°С и постоянном перемешивании прикапывают 1994 г водного раствора глиоксаля с концентрацией 40% мас. После проведения реакции получается 0,65 моль/л раствор гликолята натрия, содержащий непрореагировавшую щелочь с концентрацией 0,067 моль/л. Выход гликолята натрия составляет 97% от теоретически возможного.
Полученный раствор гликолята натрия с концентрацией 0,65 моль/л очищают от продуктов осмоления сорбцией на активированном угле, который добавляют из расчета 1-5% мас. в пересчете на получаемый гликолят натрия. Целесообразно использовать активированные угли марок 207ЕА, 607Е или AGC, которые имеют зольность менее 1%, в/в и развитую поверхность 1150-1500 м2. Раствор гликолята натрия пропускают через колонку, заполненную активированным углем, 3-5 раз. Для увеличения эффективности очистки гликолята натрия диаметр колонки должен быть меньше ее высоты не менее чем в 100 раз. При вымывании частичек активирорванного угля необходимо отфильтровать раствор соли.
Очищенный от примесей раствор гликолята натрия объемом 50 литров с концентрацией 0,65 моль/л подвергают безреагентной конверсии в гликолевую кислоту методом электродиализа с биполярными мембранами, в качестве которых используются гомогенные биполярные мембраны, а в качестве катионообменных - гетерогенные мембраны МК-40. Раствор соли с удельной проводимостью 26,0 мСм/см подается в кислотно-солевые камеры электродиализатора синтезатора. На электроды из платинированного титана подается такое напряжение, которое обеспечивает плотность тока не менее 1,5 А/дм2. Процесс конверсии соли в кислоту осуществляется до того момента, когда удельная проводимость раствора кислоты в кислотно-солевом тракте не достигнет минимального значения 2,47 мСм/см и не будет уменьшаться в течение 12-15 минут.
Полученная гликолевая кислота объемом 47 литров имеет концентрацию 0,647 моль/л (93,57% от теоретически возможного). Уменьшение объема раствора, циркулирующего в кислотно-солевых камерах ЭДС, вероятно, обусловлено электроосмотическим переносом молекул растворителя в щелочные камеры. Небольшой радиус катиона натрия обуславливает наличие крепко связанной с ним сольватной оболочки. Частично уменьшить перенос растворителя из кислотно-солевых камер можно, создав избыточное давление в щелочных камерах ЭДС, чтобы создались такие условий, при которых осмотический перенос через мембрану компенсировал бы электроосмотический. Разность давления между трактами должно составлять 10-60 кПа. Потенциометрическое титрование раствора щелочи из щелочного тракта показало, что наблюдается перенос гликолят анионов через гомогенную биполярную мембрану в щелочные камеры ЭДС. Об этом свидетельствовало наличие второго максимума на дифференциальной кривой потенциометрического титрования.
В процессе конверсии гликолята натрия выход по току для кислоты составляет 75,23%. При этом на получение 1 кг кислоты затрачивается 0,310 кВт·ч электроэнергии, а производительность составляет 213,7 г кислоты в час с 1 м2 эффективной площади мембран.
Далее раствор гликолевой кислоты объемом 47 литров с концентрацией 0,647 моль/л подвергают концентрированию методом вакуумного ротационного испарения до концентрации товарного 70% мас.
Полученный водный раствор гликолевой кислоты с концентрацией 70% мас. загружают в реактор, подключенный к термокриостату, и охлаждают до температуры не более 7°С. Для ускорения процесса кристаллизации целесообразно внести заранее подготовленные затравочные кристаллы гликолевой кислоты. Масса затравочных кристаллов должна составлять не мене 0,03% мас. в зависимости от концентрации мономерной формы кислоты в растворе. Чем больше концентрация олигомеров гликолевой кислоты в исходном 70% мас. (не менее 5, но не более 7% мас.) водном растворе, тем больше необходимо добавлять затравочных кристаллов. Для ускорения процесса кристаллообразования кристаллизацию необходимо вести при постоянном перемешивании. Выпавшие кристаллы отфильтровывают, затем 2-3 раза промывают маточным раствором и сушат на фильтре при комнатной температуре в атмосфере инертного газа. Полученные кристаллы остаются химически стабильными в плоть до температуры 50°С при относительной влажности 85-95%. Выход продукта составляет 1156,3 г, что соответствует 50% от теоретически возможного. Полученные кристаллы, по данным ВЭЖХ-анализа, при этом содержат не менее 99,4% мас. основного компонента.
ПРИМЕР 3
Для получения гликолята натрия в реакторе с верхнеприводной мешалкой готовят с использованием деионизованной воды, имеющей сопротивление не менее 12-15 Мом·см, раствор едкого натра с концентрацией 0,842 моль/л в объеме 100 литров. При температуре не более 3°С и постоянном перемешивании прикапывают 4440 г водного раствора глиоксаля с концентрацией 40% мас. После проведения реакции получается 0,75 моль/л раствор гликолята натрия, содержащий непрореагировашую щелочь с концентрацией 0,077 моль/л. Выход гликолята натрия составляет 98% от теоретически возможного.
Полученный раствор гликолята натрия с концентрацией 0,75 моль/л очищают от продуктов осмоления сорбцией на активированном угле, который добавляют из расчета 1-5% мас. в пересчете на получаемый гликолят натрия. Целесообразно использовать активированные угли марок 207ЕА, 607Е или AGC, которые имеют зольность менее 1%, в/в и развитую поверхность 1150-1500 м2. Раствор гликолята натрия пропускают через колонку, заполненную активированным углем 3-5 раз. Для увеличения эффективности очистки гликолята натрия диаметр колонки должен быть меньше ее высоты не менее чем в 100 раз. При вымывании частичек активированного угля необходимо отфильтровать раствор соли.
Очищенный от примесей раствор гликолята натрия объемом 100 литров с концентрацией 0,75 моль/л подвергают безреагентной конверсии в гликолевую кислоту методом электродиализа с биполярными мембранами, в качестве которых используются гомогенные биполярные мембраны, а в качестве катионообменных - гетерогенные мембраны МК-40. Раствор соли с удельной проводимостью 29,7 мСм/см подается в кислотно-солевые камеры электродиализатора синтезатора. На электроды из платинированного титана подается такое напряжение, которое обеспечивает плотность тока не менее 1,5 А/дм2. Процесс конверсии соли в кислоту осуществляется до того момента, когда удельной проводимостью раствора кислоты в кислотно-солевом тракте не достигнет минимального значения 2,7 мСм/см и не будет уменьшаться в течении 11-14 минут. Результаты ВЭЖХ-анализа свидетельствуют о 100% конверсии соли в кислоту.
Полученная гликолевая кислота объемом 93 литра имеет концентрацию 0,722 моль/л (89,53% от теоретически возможного). Уменьшение объема раствора, циркулирующего в кислотно-солевых камерах ЭДС, вероятно, обусловлено электроосмотическим переносом молекул растворителя в щелочные камеры. Небольшой радиус катиона натрия обуславливает наличие крепко связанной с ним сольватной оболочки. Частично уменьшить перенос растворителя из кислотно-солевых камер можно, создав избыточное давление в щелочных камерах ЭДС, чтобы создались такие условия, при которых осмотический перенос через мембрану компенсировал бы электроосмотический. Разность давления между трактами должно составлять 10-60 кПа. Потенциометрическое титрование раствора щелочи из щелочного тракта показало, что наблюдается перенос гликолят анионов через гомогенную биполярную мембрану в щелочные камеры ЭДС. Об этом свидетельствовало наличие второго максимума на дифференциальной кривой потенциометрического титрования.
В процессе конверсии гликолята натрия выход по току для кислоты составляет 71,98%. При этом на получение 1 кг кислоты затрачивается 0,310 кВт·ч электроэнергии, а производительность составляет 254,57 г кислоты в час с 1 м2 эффективной площади мембран.
Далее раствор гликолевой кислоты объемом 93 литров с концентрацией 0,722 моль/л подвергают концентрированию методом вакуумного ротационного испарения до концентрации товарного 70% мас.
Полученный водный раствор гликолевой кислоты с концентрацией 70% мас. загружают в реактор, подключенный к термокриостату, и охлаждают до температуры не более 3°C. Для ускорения процесса кристаллизации целесообразно внести заранее подготовленные затравочные кристаллы гликолевой кислоты. Масса затравочных кристаллов должна составлять не мене 0,01% мас. в зависимости от концентрации мономерной формы кислоты в растворе. Чем больше концентрация олигомеров гликолевой кислоты в исходном 70% мас. (не менее 5, но не более 7% мас.) водном растворе, тем больше необходимо добавлять затравочных кристаллов. Для ускорения процесса кристаллообразования кристаллизацию необходимо вести при постоянном перемешивании. Выпавшие кристаллы отфильтровывают, затем 2-3 раза промывают маточным раствором и сушат на фильтре при комнатной температуре в атмосфере инертного газа. Полученные кристаллы остаются химически стабильными в плоть до температуры 50°С при относительной влажности 85-95%. Выход продукта составляет 2706,42 г, что соответствует 53% от теоретически возможного. Полученные кристаллы, по данным ВЭЖХ-анализа, при этом содержат не менее 99,4% мас. основного компонента.
Способ получения гликолевой кислоты, включающий получение водного раствора гликолята натрия из глиоксаля и едкого натра взаимодействием глиоксаля и натриевой щелочи с мольным отношением 1:1,05-1,1 при температуре от 0 до 10С при непрерывном добавлении глиоксаля, очистку полученного раствора от продуктов осмоления сорбцией на активированном угле, затем переработку раствора в гликолевую кислоту методом электродиализа с использованием биполярных мембран и концентрирование раствора гликолевой кислоты.
