Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ ФТОРИДА ВОДОРОДА
Вид РИД
Изобретение
Изобретение относится к неорганической химии, а именно к способам получения фторида водорода, который получают из газообразных и летучих фторидов или отходов, содержащих фториды.
К таким фторидам относят фториды металлов, например гексафториды вольфрама, молибдена, селена, урана, теллура и т.п., и неметаллов, например углерода, азота, серы и т.п. Это вещества, которые являются газообразными при нормальных условиях (температуре 0°C и давлении 101 кПа), или имеют давление паров при температуре 0°C не менее 1 кПа («летучие»).
Известен способ получения фторида водорода (HF) и двуокиси кремния путем гидролиза тетрафторида кремния в пламени при 1150-1650°C [Патент США №4036938, кл. C01B 7/22, оп.19.07.1977].
Фторид водорода при этом получают в виде водного раствора плавиковой кислоты, для обезвоживания которой используют концентрированную серную кислоту, что очень усложняет технологию получения фторида водорода.
Описан [патент США5752158, НКИ США 423/488, оп.12.05.1998] одностадийный способ получения газообразного HF и твердого оксида урана из гексафторида урана UF6. Поток реагентов, включающий UF6, перемешивают с кислородом, а второй поток подают в виде смеси водородсодержащего газа и кислородсодержащего газа. Эти газовые потоки реагентов подают вместе в реактор при температуре 700°-1000°C, обеспечивающей превращение UF6 в пламени в легко разделяемые продукты - твердый оксид урана и газообразный фторид водорода.
Полученный твердый оксид урана отделяют от газообразного фторида водорода осаждением.
Этот способ разработан для превращения урансодержащего сырья в оксиды. Однако нагрев до 700-1000°C потока, содержащего газообразный или летучий фторид, может привести к его термическому разложению с образованием конденсированных соединений, которые, выпадая из потока, не поступят в зону реакции. Если же до указанной температуры нагревается кислород-водородная смесь, то процесс становится взрывоопасным.
Таким образом, существует проблема получения фторида водорода из летучих и газообразных фторидов, без их предварительного нагрева до высоких температур.
Наиболее близким по технической сущности является способ получения фторида водорода при переработке фторидов металлов или фторида кремния [патент РФ 2061649, МПК6 C01B 7/19, C01B 13/22, оп.10.06.1996].
Способ включает пирогидролиз фторида металла или кремния, взаимодействие полученной пылепарогазовой смеси с углеводородом при температуре не ниже 400°C и выделение целевых продуктов - соответствующего оксида и фторида водорода. В качестве углеводорода используют природный газ или пропан, а количество углеводорода берут из расчета 1,2-1,4 грамм-атом углерода на 1 моль разлагаемой воды. Предлагаемым способом получают практически безводный фторид водорода и тонкодисперсные порошки оксидов металлов или кремния с хорошим выходом.
В качестве углеводорода используют природный газ или пропан.
При этом углеводород подают в соотношении 1,2-1,4 грамм-атома углерода на 1 моль воды. При взаимодействии с углеводородом, содержащимся в пыле-парогазовой смеси, полученной при пирогидролизе фторида, имеют место следующие реакции:
H2O+CH4→CO+3H2 (с природным газом, основной частью которого является метан C4),
3H2O+C3H8→3CO+7H2 (с пропаном C3H8).
Способ осуществляют следующим образом.
В качестве высокотемпературного теплоносителя, содержащего пары воды, используют плазменный поток водяного пара.
Установка включает плазмотроны мощностью по 50 кВт, реакционную камеру, питатель для подачи в реакционную камеру перерабатываемого фторида, камеру взаимодействия с углеводородом пылепарогазовой смеси, полученной в результате пирогидролиза фторида, пылеуловитель для выделения оксидов, конденсатор фторида водорода и систему утилизации отходящих газов.
После стадии пирогидролиза фторида получают пыле-парогазовую смесь, содержащую фторид водорода, соответствующий оксид и непрореагировавший, водяной пар, который берут в избытке. Эту смесь направляют на взаимодействие с углеводородом, которое осуществляют при температуре не ниже 400°C.
Для получения практически безводного фторида водорода по этому способу берут углеводород из расчета 1,2-1,4 грамм-атома углерода (т.е. 1,2-1,4 моль природного газа в пересчете на метан или 0,4-0,47 моль пропана) на 1 моль разлагаемой воды.
После взаимодействия смеси с углеводородом из нее выделяют соответствующий оксид, фторид водорода и воду. Оксид углерода и элементный водород, как и продукты взаимодействия углеводорода с водой, направляют в газовую горелку для сжигания в потоке воздуха. Из конденсатора конденсат направляют на анализ для определения содержания в нем HF и H2O.
На опытной установке этим способом перерабатывали фториды кремния, алюминия, железа, циркония и урана.
Однако описанный способ не позволяет перерабатывать фториды, не склонные к гидролизу, например тетрафторид углерода. Кроме того, для испарения и нагрева пара до температуры не ниже 400°C используется дорогостоящее оборудование - плазмотрон, требующее очень значительных затрат электрической энергии.
Задачей, стоящей перед авторами предлагаемого изобретения, была разработка способа получения фторида водорода из широкого диапазона исходных фторидов - как из летучих, так и из газообразных.
Кроме получения фторида водорода в способе должна быть предусмотрена возможность утилизации отходов разных фторидов и переработки их в менее токсичные оксиды.
Кроме того, при переработке твердых летучих фторидов, желательно получение наноразмерных оксидов соответствующих элементов.
Сущность предлагаемого изобретения состоит в том, что фторид водорода получают, проводя взаимодействие газообразных или летучих фторидов с кислородсодержащим и водородсодержащим веществами в режиме горения при температуре 1000-4000°C, при соотношении 1 моль фторида к 1-5 моль водорода и 0,05-4 моль кислорода; при этом в качестве кислородсодержащего вещества (окислителя) используют кислород, воздух, закись азота, и другие кислородсодержащие газы, а в качестве водородсодержащего вещества (горючего) используют водород, аммиак, газообразные углеводороды, например, метан, этан, пропан, бутан, или их смеси.
Соотношение в системе фторид элемента - кислородсодержащее вещество (окислитель) - водородсодержащее вещество (горючее) выбирают так, чтобы температура продуктов реакции лежала в диапазоне 1000-4000°C. Для этого соотношение поддерживают в следующем диапазоне: на 1 моль фторида элемента подают 1-5 моль водородсодержащего вещества в пересчете на молекулярный водород и 0,05-4 моль кислородсодержащего вещества в пересчете на молекулярный кислород.
Целью является достижение не менее 50% конверсии фторида элемента, при минимальном количестве образующейся в процессе воды - обычно она составляет не более 30% по отношению к фториду водорода.
В аспекте данного изобретения к фторидам относят фториды металлов, например гексафториды вольфрама, молибдена, селена, урана, теллура и т.п., и неметаллов, например углерода, азота, серы и т.п., которые являются газообразными соединениями при нормальных условиях (температуре 0°C и давлении 101 кПа), или имеющим давление паров при температуре 0°C не менее 1 кПа.
Ниже приведены схемы реакций процесса получения фторида водорода из фторида элемента при использовании в качестве пары кислородсодержащее вещество-водородсодержащее вещество (окислитель-горючее) пар водород-кислород и аммиак-кислород:
MFx+yH2+zO2→MOk+xHF+mH2O+MFn,
где М - элемент, х≥1, y≥0,5х, z≥0,5k, k≥0, m→0, n→0;
или:
MFx+yNH3+zO2→MOk+xHF+mH2O+nMF,
где M - элемент, х≥1, y≥0,33x, z≥0,5k, k≥0, m→0, n→0.
Здесь m→0, n→0 означают, что взаимодействие желательно проводить таким образом, чтобы как можно более сократить содержание воды и фторидов элементов в потоке продуктов.
Температура такого взаимодействия зависит от соотношения значений x, y и z и обычно ее поддерживают в интервале 1000-4000°С в зависимости от термодинамической устойчивости исходного фторида элемента.
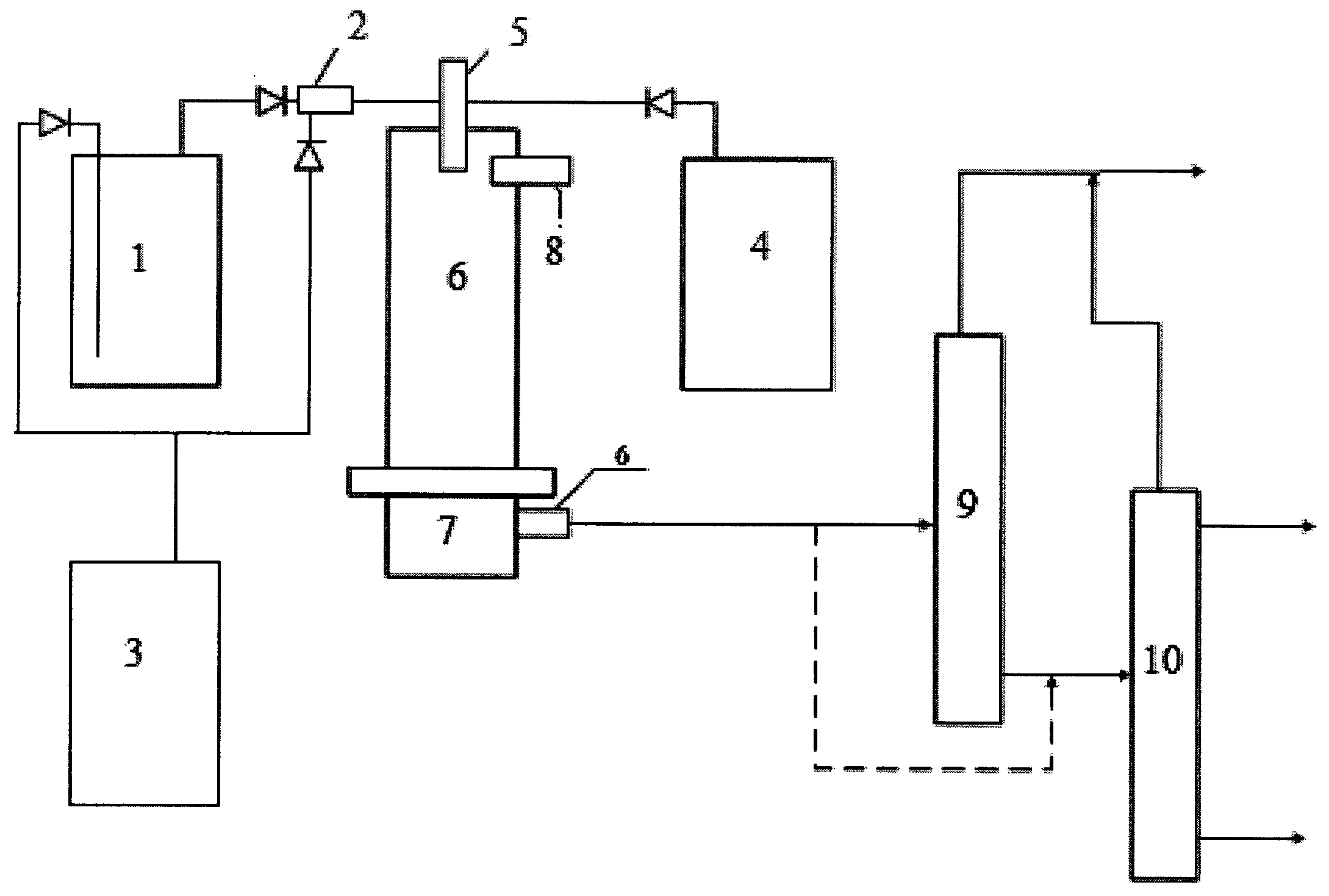
Общая принципиальная схема экспериментальной установки получения фторида водорода из газообразных и летучих фторидов элементов приведена на Фигуре, где:
1 - емкость с газообразным или летучим фторидом,
2 - смеситель газообразного фторида (и кислородсодержащего окислителя)
3 - емкость для кислородсодержащего вещества;
4 - емкость для водородсодержащего вещества,
5 - двухкомпонентная форсунка,
6 - пламенный реактор,
7 - емкость для сбора конденсированного оксида,
8 - приемный бункер с фильтром для очистки газового потока от порошкообразных веществ,
9 - отдувочная колонна для конденсации фторида водорода и воды,
10 - ректификационная колонна для разделения фторида водорода и воды.
Процесс проводят следующим образом.
Из расходной емкости 1 в смеситель 2 подают газообразный или летучий фторид, а из расходной емкости 3 - кислородсодержащее вещество (окислитель). Если в емкости 1 находится летучий фторид в конденсированном состоянии, то часть или весь поток окислителя из емкости 3 подают в смеситель 2 через расходную емкость 1. В расходной емкости 4 содержится водородсодержащее вещество.
Из смесителя 2 и емкости 4 газы поступают в реактор 6 через двухкомпонентную форсунку 5.
В пламенном реакторе 6 смонтированы двухкомпонентная, коаксиальная форсунка 5 для подачи основных компонентов и форсунка (на Фигуре не указана) для инициирования и поддержания устойчивого процесса горения с помощью дежурного факела, которая работает на самовоспламеняющейся паре, например аммиак-фтор. Для инициирования и поддержания устойчивого горения могут быть применены и другие устройства, например, запальная свеча.
При осуществлении способа в зону горения реактора 6, стенки которого термостатированы при температуре, исключающей конденсацию воды и фторида водорода, обычно не выше 150°C, подают водородсодержащее вещество (топливо) и смесь кислородсодержащего вещества (окислителя) и летучего или газообразного фторида элемента через форсунку 5.
Составом продуктов процесса горения управляют, изменяя соотношение потоков веществ на входе в реактор, температуру (в диапазоне 1000-4000°C) и давление (от 1 до 1000 кПа) в зоне реакции так, чтобы добиться возможно более высокой регенерации фтора при минимальном выходе воды, обычно не превышающем 30% от выхода фторида водорода.
На выходе из реактора получают фторид водорода, воду и газообразный или конденсированный оксид элемента.
Конденсированный оксид элемента или элемент разделяют с газовым потоком осаждением в приемном бункере 8, используя для очистки газового потока, например металлокерамический фильтр (не показан).
Из газового потока конденсируют фторид водорода и воду в отдувочной колонне 9. Поток инертных газов рассеивают после санитарной очистки.
Смесь фторида водорода и воды разделяют ректификацией с получением безводного фторида водорода и 38% плавиковой кислоты в ректификационной колонне 10.
В случае получения твердых оксидов элементов со стадии пламенного горения, они представляют собой мелкодисперсный порошок с наноразмерными гранулами.
Ниже приведены примеры конкретной реализации процесса.
Пример 1
В двухкомпонентную коаксиальную форсунку 5 наружным диаметром 10 мм, смонтированную в верхней по потоку части цилиндрического реактора 6, вводят по кольцевому каналу водород, который подают из емкости 4 объемом 40 литров с расходом 10 моль в час, поддерживая расход на заданном уровне с помощью редукторной схемы. В эту же форсунку по осевому каналу вводят заранее приготовленную смесь кислорода и тетрафторида углерода из емкости 1 с расходами 5.2 и 5 моль в час соответственно. Избыток кислорода задают, чтобы избежать образования моноокиси углерода. Температура обоих потоков газа составляет 15-20°С. В реакторе типа "туннельная горелка", который изготовлен из нержавеющей стали и имеет внутренний диаметр 40 мм и длину 1 м, поддерживают давление 110-120 кПа и температуру стенки 150°С. Воспламенение смеси осуществляют дежурным факелом через форсунку для инициирования горения.
Из реактора выводят газовый поток, который состоит из диоксида углерода, фторида водорода и кислорода, расходы которых составляют 5, 20 и 0.4 моль в час соответственно. Фторид водорода конденсируют в отдувочной колонне 9 при температуре минус 50°С и собирают в кубе колонны. Смесь диоксида углерода и кислорода очищают от следов фторида водорода в емкости(не показана) с помощью химического поглотителя известкового и рассеивают.
Пример 2
В реакторе (см. пример 1) форсунка смонтирована так, что поток газа вводится в реактор тангенциально, т.е. реактор представляет собой циклонную камеру. Параметры по расходу компонентов, температуре и давлению поддерживают такими же, как и в примере 1. Выходной поток состоит из диоксида углерода, фторида водорода и кислорода с расходами 5, 20 и 0,2 моль в час соответственно. Фторид водорода конденсируют в колонне 9. Смесь диоксида углерода и кислорода очищают от следов фторида водорода и рассеивают.
Пример 3
В реактор той же конструкции, что и в примере 1, с использованием той же коаксиальной форсунки, что и в примере 1, вводят по коаксиальному каналу форсунки аммиак, а по осевому каналу смесь тетрафторида углерода и кислорода. Расходы аммиака, тетрафторида углерода и кислорода составляют 7,5 и 5,5 моль в час. Аммиак дозируют из расходной емкости, где он находится в газообразном состоянии, с помощью редукторной схемы. Расход аммиака измеряют манометром. Расход смеси тетрафторида углерода и кислорода поддерживают также, как в примере 1.
В реакторе поддерживают давление 110-120 кПа и температуру стенки 150°С. Воспламенение смеси осуществляют дежурным факелом.
Из реактора выводят газовый поток, который состоит из диоксида углерода, фторида водорода, воды, кислорода и азота, расходы которых составляют 5, 20, 0.5, 0.25 и 3.5 моль в час соответственно. Фторид водорода и воду конденсируют в отдувочной колонне 9 при температуре минус 50°С и собирают в кубе колонны. Смесь диоксида углерода и кислорода очищают от следов фторида водорода с помощью химического поглотителя известкового и рассеивают.
Смесь фторида водорода и воды ректификуют в ректификационной колонне 10 и получают безводный фторид водорода и азеотропную смесь воды и фторида водорода с содержанием последнего 38%.
Пример 4
В реактор (пример 1) с помощью вышеописанной форсунки по коаксиальному каналу вводят водород с расходом 3,2 моль/час, и по осевому каналу смесь закиси азота и трифторид азота с расходами 0,2 и 2 моль в час соответственно.
На выходе из реактора получают азот в количестве 1,2 моль/час, фторид водорода в количестве 6 моль/час и воду в количестве 0,2 моль/час. Фторид водорода и воду конденсируют, смесь ректификуют с получением безводного фторида водорода и 38% плавиковой кислоты также, как в примере 2. Азот после санитарной очистки рассеивают в атмосфере.
Пример 5
В реактор (пример 1) с помощью вышеописанной форсунки по коаксиальному каналу вводят водород с расходом 6,2 моль/час, и по осевому каналу смесь кислорода и гексафторида вольфрама с расходами 3,6 и 2 моль в час соответственно. Газообразную смесь кислорода и гексафторида вольфрама получают продувая кислород через емкость с твердым гексафторидом вольфрама, нанесенным на стенки емкости, термостатированной при 0°C. Давление в реакторе и температуру его стенок задают такими же, как и в предыдущих примерах
На выходе из реактора получают порошкообразный триоксид вольфрама в количестве 2 моль/час, фторид водорода в количестве 12 моль/час, воду в количестве 0,2 моль в час и кислород в количестве 0,5 моль/час.
Порошкообразный триоксид вольфрама отделяют осаждением в емкости 8 и фильтрованием газового потока с помощью металлокерамического фильтра.
Фторид водород и воду конденсируют, и эту смесь ректификуют с получением безводного фторида водорода и плавиковой кислоты с содержанием фторида водорода 38%.
Кислород после санитарной очистки рассеивают в атмосфере. Другие примеры применения способа приведены в таблице 1.
Диапазон изменения мольных соотношений фторид-водородсодержащее топливо-кислородсодержащий окислитель - 1-1:5-0,05:4.
В Таблице представлены параметры проведения опытов (примеры 1-17) и полученные результаты.
Таким образом, решена задача, стоявшая перед авторами предлагаемого изобретения: разработан способ получения фторида водорода из широкого диапазона исходных фторидов - как из летучих, так и из газообразных. Этот способ позволяет, кроме получения фторида водорода, утилизировать разнообразные отходы фторидов и перерабатывать их в менее токсичные оксиды. В случае переработки твердых летучих фторидов способ позволит получать наноразмерные оксиды соответствующих элементов.
|
|