Результат интеллектуальной деятельности: ЕМКОСТЬ ДЛЯ ЛЕКАРСТВЕННОГО СРЕДСТВА АЭРОЗОЛЬНОГО ПРИМЕНЕНИЯ
Вид РИД
Изобретение
Область техники
Изобретение относится устройствам, обеспечивающим использование лекарственных средств в виде аэрозолей.
Уровень техники
Потребность в эффективной терапии пациентов привела к разработке различных технологий введения лекарственных препаратов. Одним из традиционных способов является оральный ввод лекарственных препаратов в форме таблетки, капсулы, эликсира и т.п. В некоторых случаях, однако, оральный ввод может оказаться нежелательным. Например, многие лекарственные препараты могут разлагаться в пищеварительном тракте еще до того, как они смогут быть эффективно поглощены в организме. Ввод лекарств ингаляцией, когда распыленный лекарственный препарат вдыхается пациентом через рот или нос для введения препарата в дыхательные пути пациента, является особенно эффективным и(или) желательным альтернативным способом. Например, при одном способе ингаляции, распыленный лекарственный препарат обеспечивает локальное терапевтическое воздействие на часть дыхательных путей, например, легких, для лечения заболеваний, например, астмы, эмфиземы и кистозного фиброза. При другом способе ингаляции лекарственный препарат вводится глубоко в легкие пациента, где возможен его переход в кровоток. Существуют ингаляторные устройства многих типов, включая устройства, в которых выполняется распыление лекарственных препаратов в форме сухого порошка.
В ингаляционном устройстве одного типа выполняется распыление препарата, например, действующего вещества или фармацевтического препарата, хранящегося в капсуле. Например, доза или часть дозы порошкового лекарственного препарата может храниться в капсуле, а капсула может быть вставлена в распылительное устройство, обеспечивающее распыление лекарственного препарата. После того, как капсула вставлена в распылительное устройство, она вскрывается для обеспечения доступа к лекарственному препарату. Для вскрытия капсулы ее можно, например, проткнуть, разрезать или разорвать. Когда капсула надлежащим образом вскрыта, и когда приложена энергия для распыления, лекарственный препарат распыляется с тем, чтобы его мог вдохнуть пользователь, и доза распыленного лекарственного препарата могла быть введена в дыхательные пути пациента.
Неправильное использование распылительного устройства может, однако, привести к тому, что количество введенного лекарственного препарата будет меньше необходимого. Например, если перед распылением капсула открыта ненадлежащим образом или не полностью, количество лекарственного препарата может оказаться уменьшенным, либо поток распыленного лекарственного препарата может оказаться недостаточным для введения пользователю необходимого количества, например, лечебной дозы. Влияние неправильного вскрытия может усиливаться, когда пользователь не может или не хочет визуально контролировать вскрытие капсулы. В этом случае пользователь может по незнанию вдохнуть лекарственный препарат в количестве меньше необходимого. Кроме того, использование заостренных элементов для вскрытия капсулы приводит к отверстиям в капсуле, имеющим нестабильные параметры, что в свою очередь, может привести к нестабильности результатов введения распыленного лекарства.
Известные капсулы фармацевтической категории часто имеют стенки неоднородной толщины, зачастую толщина по концам делается больше по соображениям механической прочности. В таких капсулах толщина стенок на концах может различаться и может варьироваться от капсулы к капсуле (также и в больших партиях), либо может отличаться от одного конца капсулы к другому, либо то и другое.
Поэтому желательно создать емкость/контейнер для лекарственного препарата аэрозольного применения, обеспечивающий его простое и стабильное вскрытие, с надежным получением повторяющихся доз. Также желательно обеспечить такое вскрытие без разработки специальных режущих или колющих элементов. Также желательно обеспечить такое вскрытие для капсул различного состава, например, из полимерных соединений, и для широкого диапазона условий хранения емкости, например, в отношении температуры и влажности.
Раскрытие изобретения
Эти потребности удовлетворены в предлагаемых вариантах осуществления настоящего изобретения.
Так, варианты осуществления настоящего изобретения включают использование прокалываемых емкостей, приспособленных для помещения в них лекарственных средств (далее - препаратов) аэрозольного применения, и включающие одну или более областей с однородной толщиной стенки и(или) однородным интервалом толщин стенки, в то время как по меньшей мере одна из этих областей с однородной толщиной стенки, и(или) однородным интервалом толщин стенки включают место для прокалывания. Также предлагаются препараты аэрозольного применения для ингаляции и системы для распыления препаратов для ингаляции. Другие признаки и преимущества вариантов осуществления настоящего изобретения будут приведены далее в описании изобретения, и частью будут очевидны из описания, либо по результатам осуществления изобретения.
Согласно другой особенности изобретения, система распыления включает распылительное устройство, включающее камеру, приспособленную для установки в нее емкости. Система распыления также включает емкость с лекарственным препаратом, часть стенки которой надежно вскрывается, когда прокалывающие или протыкающие средства прикладывают к ней заданную прокалывающую силу.
Согласно другой особенности изобретения, способ распыления лекарственного препарата включает подготовку распылительного устройства, включающего камеру; подготовку емкости с лекарственным препаратом, стенка которой имеет одну или более областей однородной толщины в пределах примерно от 100 до 235 мкм; приложение прокалывающей силы к одной или более областям емкости однородной толщины для создания в них одного или более отверстий; распыление лекарственного препарата в камере.
Согласно другой особенности изобретения, распылительное устройство включает капсулу, стенка которой имеет по существу однородную толщину примерно от 100 до 235 мкм, корпус, образующий камеру, имеющую одно или более отверстий для впуска воздуха, размеры которой позволяют установить в нее капсулу, содержащую лекарственный препарат аэрозольного применения; расположенный в корпусе прокалывающий механизм, включающий прокалывающий элемент, имеющий передний конец, образующий режущую кромку, обеспечивающую эффективное прорезывание стенки капсулы по существу однородной толщины для создания отверстия в капсуле; и концевую секцию, связанную с корпусом, размеры и форма которой обеспечивают ее введение в рот или нос пользователя с тем, чтобы пользователь мог сделать вдох через концевую секцию для ингаляции распыленным лекарственным препаратом, который находился в капсуле, сквозь отверстие, созданное в капсуле.
Согласно другой особенности изобретения способ распыления лекарственного препарата включает подготовку капсулы, имеющей стенку по существу однородной толщины примерно от 100 до 235 мкм, и содержащей лекарственный препарат аэрозольного применения; продвижение вперед прокалывающего элемента, передний конец которого образует режущую кромку, сквозь стенку капсулы по существу однородной толщины для создания отверстия в капсуле, без отделения от капсулы части стенки капсулы; распыление лекарственного препарата продуванием воздуха сквозь камеру; и введение распыленного лекарственного препарата в дыхательные пути пользователя во время проведения пользователем ингаляции.
Согласно другим особенностям изобретения капсула имеет стенку с по существу однородной толщиной примерно от 100 до 235 мкм, при этом предусматривается использование капсулы, содержащей лекарственный препарат аэрозольного применения, с ингаляционным устройством, имеющим элемент для вскрытия капсул, с заостренным передним концом и затупленным задним концом, для повышения эффективности прокалывания капсулы.
Согласно другой особенности изобретения система распыления включает капсулу, имеющую стенку по существу однородной толщины примерно от 100 до 235 мкм, и корпус, образующий камеру, имеющую одно или более отверстий для впуска воздуха, размеры которой позволяют поместить в нее капсулу, приспособленную для размещения в ней лекарственного препарата аэрозольного применения; расположенный в корпусе прокалывающий механизм, включающий прокалывающий элемент, имеющий передний конец, образующий режущую кромку, обеспечивающую эффективное прорезывание стенки капсулы для создания отверстия в капсуле, и задний край, поверхность которого не имеет режущей формы и не прорезает стенки капсулы, когда задний край вводится в отверстие, созданное передним концом; и концевую секцию, связанную с корпусом, размеры и форма которой обеспечивают ее введение в рот или нос пользователя с тем, чтобы пользователь мог сделать вдох через концевую секцию для ингаляции распыленным лекарственным препаратом, который находился в капсуле, сквозь отверстие, созданное в капсуле.
Варианты осуществления настоящего изобретения включают капсулы, приспособленные для помещения в них препаратов аэрозольного применения, и имеющие куполообразные верхнюю и нижнюю части, в которых верхняя или нижняя части, или обе вместе, имеют стенки с областью однородной толщины, и в которых верхняя или нижняя части или обе вместе, имеют место для прокалывания.
Согласно другой особенности изобретения способ распыления лекарственного препарата включает подготовку капсулы, имеющей стенку по существу однородной толщины примерно от 100 до 235 мкм, и содержащей лекарственный препарат аэрозольного применения; продвижение вперед прокалывающего элемента сквозь стенку капсулы по существу однородной толщины примерно от 100 до 235 мкм для создания отверстия в капсуле, который включает передний конец, на котором сформирована режущая кромка, и задний край, поверхность которого не имеет режущей формы, и которая не прорезает стенку капсулы, когда задний конец вводится в отверстие, созданное передним концом, и при создании которого не происходило отделения от капсулы части стенки капсулы; распыление лекарственного препарата продуванием воздуха сквозь камеру; и введение распыленного лекарственного препарата в дыхательные пути пользователя во время проведения пользователем ингаляции.
Согласно другим особенностям изобретения подготавливается емкость, обеспечивающая его надежное и (воспроизводимое) вскрытие, и множество таких емкостей, обеспечивающих их надежное и воспроизводимое вскрытие, без использования специально разработанных режущих или прокалывающих элементов, например, режущего наконечника.
Согласно другим особенностям подготавливается капсула, имеющая одну или более областей стенки с однородной толщиной и(или) однородным интервалом толщины стенки, вместе с пассивным ингалятором сухого порошка, включающим один или более прокалывающих элемента, конструкция и конфигурация которых обеспечивает прокалывание капсулы вблизи по меньшей мере одной из областей капсулы с однородной толщиной стенки и(или) однородного интервала толщины стенки.
Согласно другим особенностям подготавливается капсула, имеющая одну или более областей стенки с однородной толщиной и(или) однородным интервалом толщины стенки, вместе с активным ингалятором сухого порошка, включающим один или более прокалывающих элемента, конструкция и конфигурация которых обеспечивает прокалывание капсулы вблизи по меньшей мере одной из областей капсулы с однородной толщиной стенки и(или) однородного интервала толщины стенки.
Согласно другим особенностям подготавливается набор, включающий по меньшей мере одну капсулу, имеющую одну или более областей стенки с однородной толщиной и(или) однородным интервалом толщины стенки, и ингалятор сухого порошка, включающий один или более прокалывающих элемента, конструкция и конфигурация которых обеспечивает прокалывание капсулы вблизи по меньшей мере одной из областей капсулы с однородной толщиной стенки и (или) однородного интервала толщины стенки.
Согласно другим особенностям подготавливается набор, включающий по меньшей мере одну капсулу, имеющую одну или более областей стенки с однородной толщиной и(или) однородным интервалом толщины стенки, и пассивный ингалятор сухого порошка, включающий один или более прокалывающих элемента, конструкция и конфигурация которых обеспечивает прокалывание капсулы вблизи по меньшей мере одной из областей капсулы с однородной толщиной стенки и (или) однородного интервала толщины стенки.
Краткое описание чертежей
Приведенные признаки, особенности и преимущества настоящего изобретения будут лучше поняты в виду приведенного далее описания, приложенной формулы и сопроводительных чертежей, иллюстрирующих примеры признаков изобретения. Следует, однако, понимать, что каждый из признаков присущ изобретению вообще, а не только в отношении конкретных чертежей, и изобретение включает любые комбинации таких признаков. На чертежах:
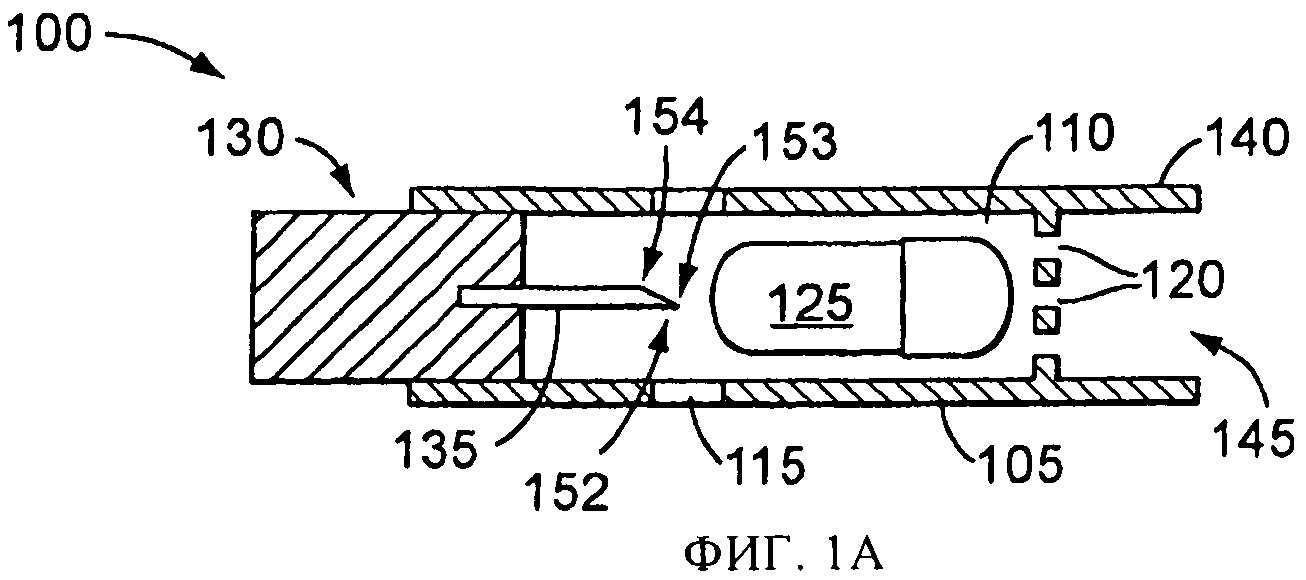
на фиг.1А схематически представлен в сечении вид сбоку распылительного устройства и емкости в начальном положении;
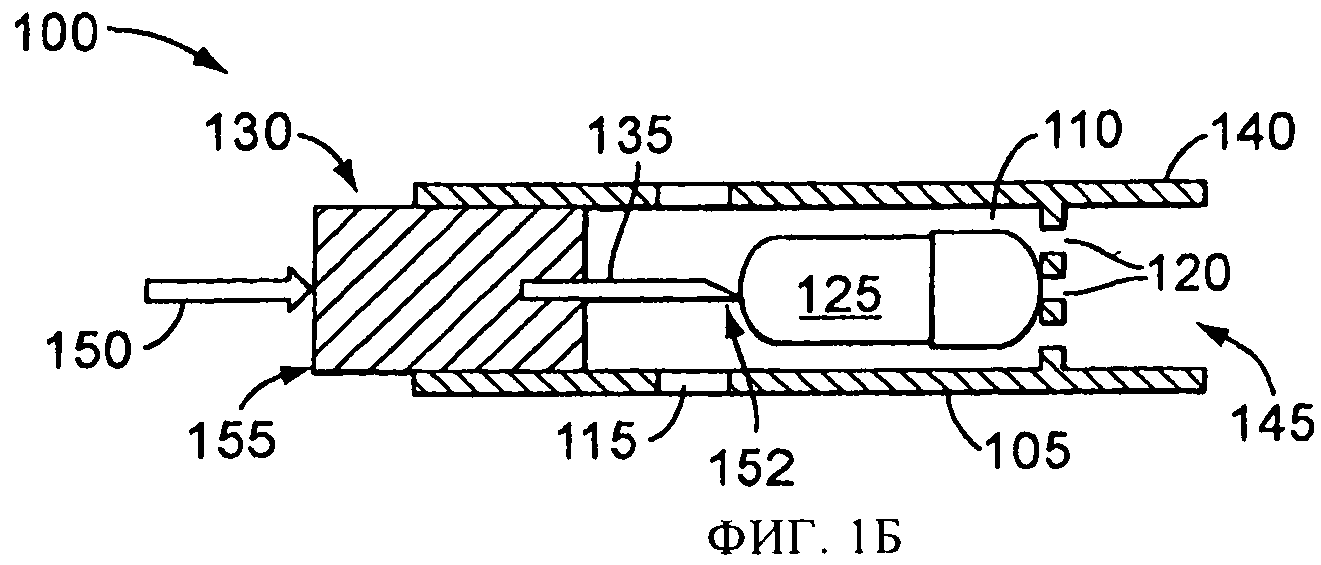
на фиг.1Б схематически представлен в сечении вид сбоку распылительного устройства и емкости, показанных на фиг.1А, в начале процесса вскрытия емкости;
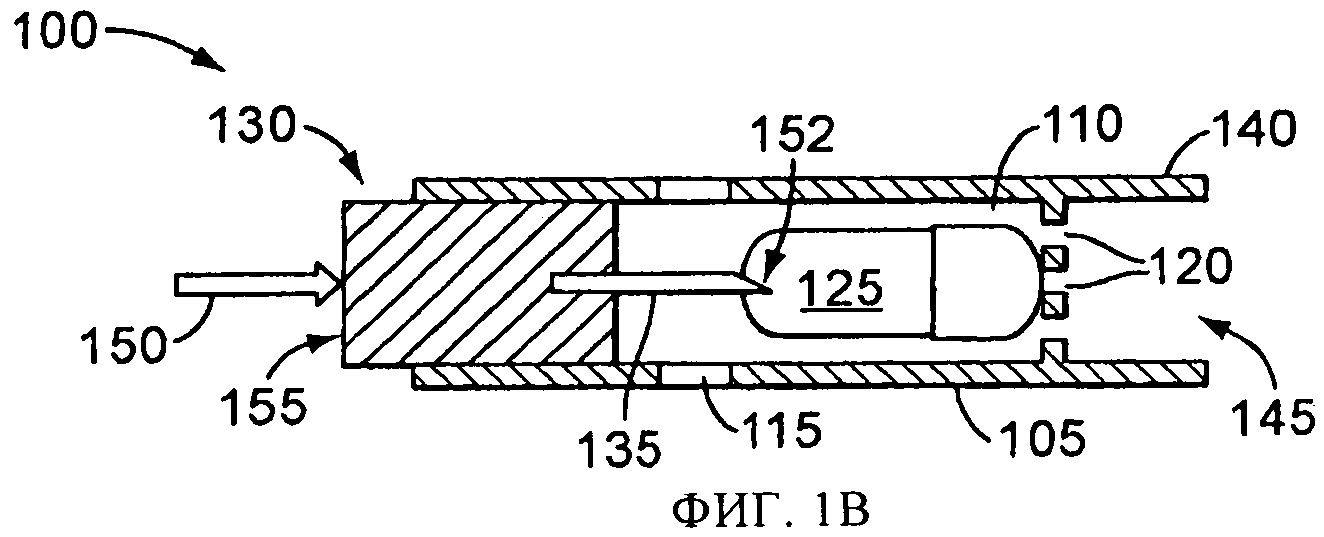
на фиг.1В схематически представлен в сечении вид сбоку распылительного устройства и емкости, показанных на фиг.1А, во время процесса вскрытия емкости;
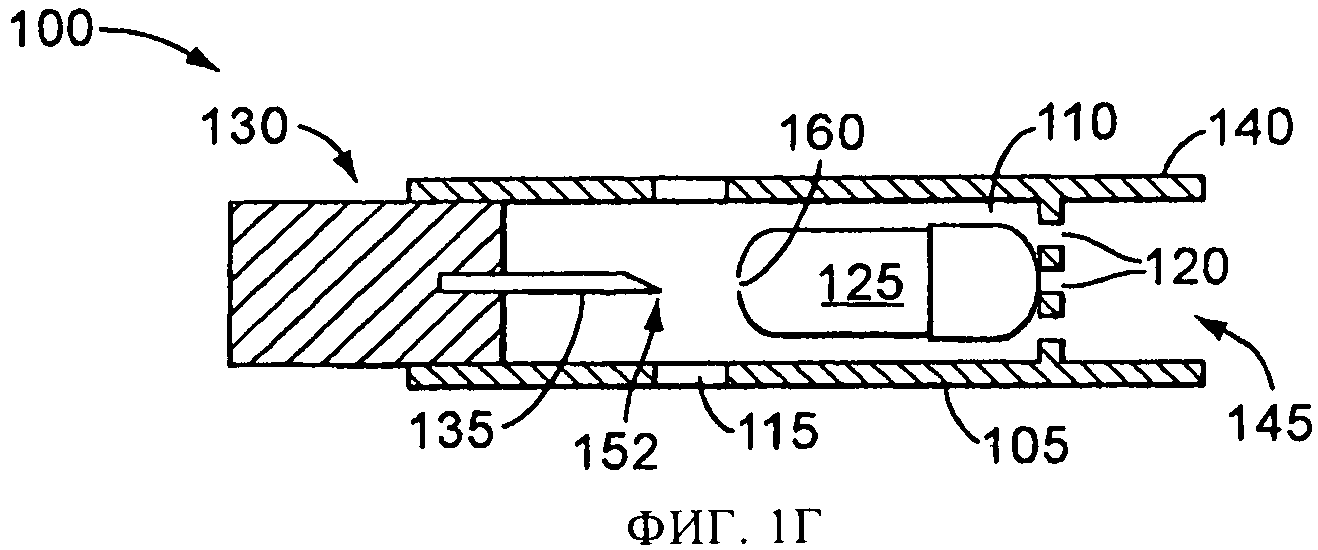
на фиг.1Г схематически представлен в сечении вид сбоку распылительного устройства и емкости, показанных на фиг.1А, в начале процесса распыления;
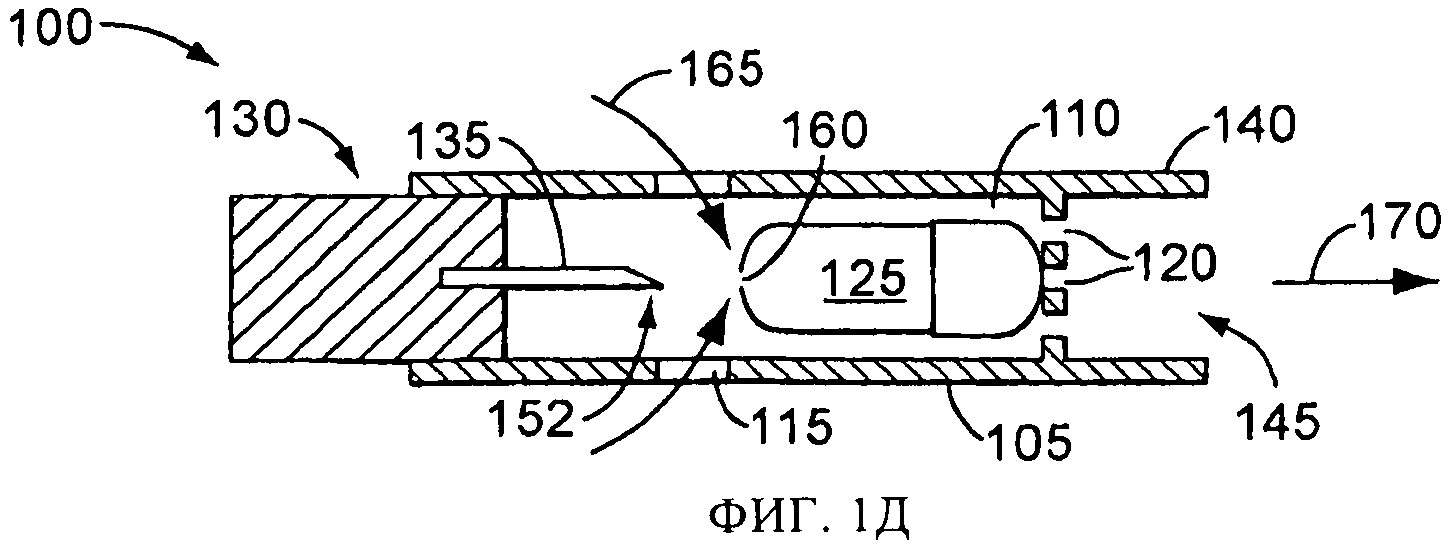
на фиг.1Д схематически представлен в сечении вид сбоку распылительного устройства и емкости, показанных на фиг.1А, во время процесса распыления;
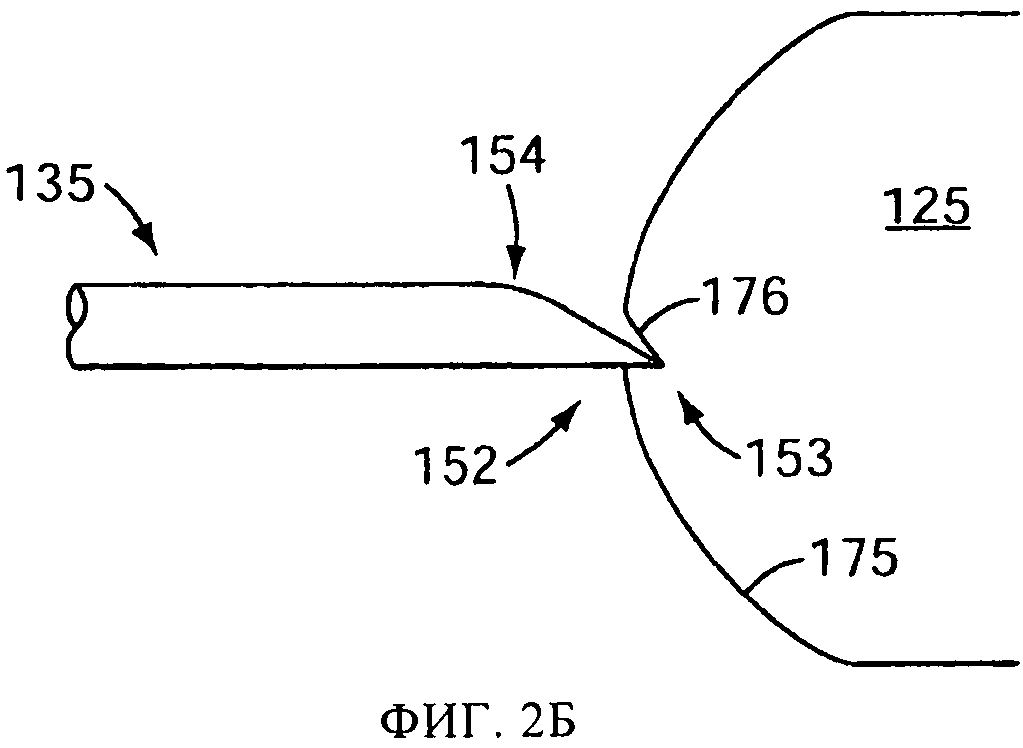
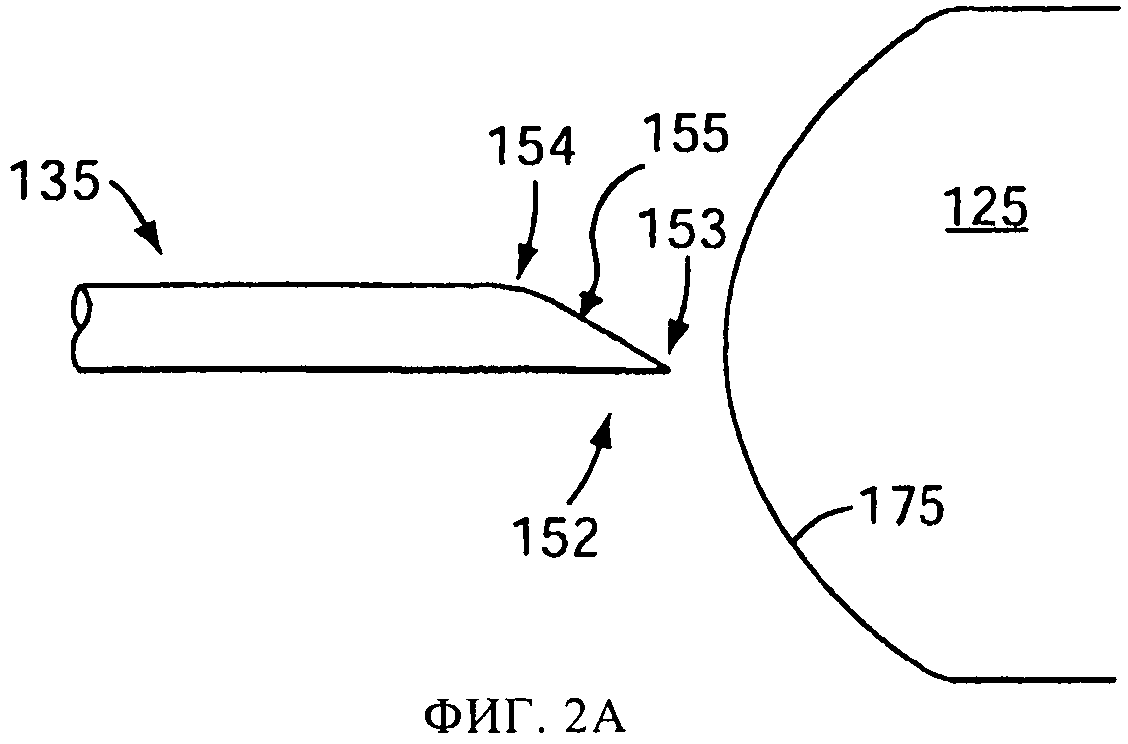
на фиг.2А и 2Б схематически представлены перспективные виды версии емкости, в соответствии с изобретением, в невскрытом и частично вскрытом состоянии, соответственно;
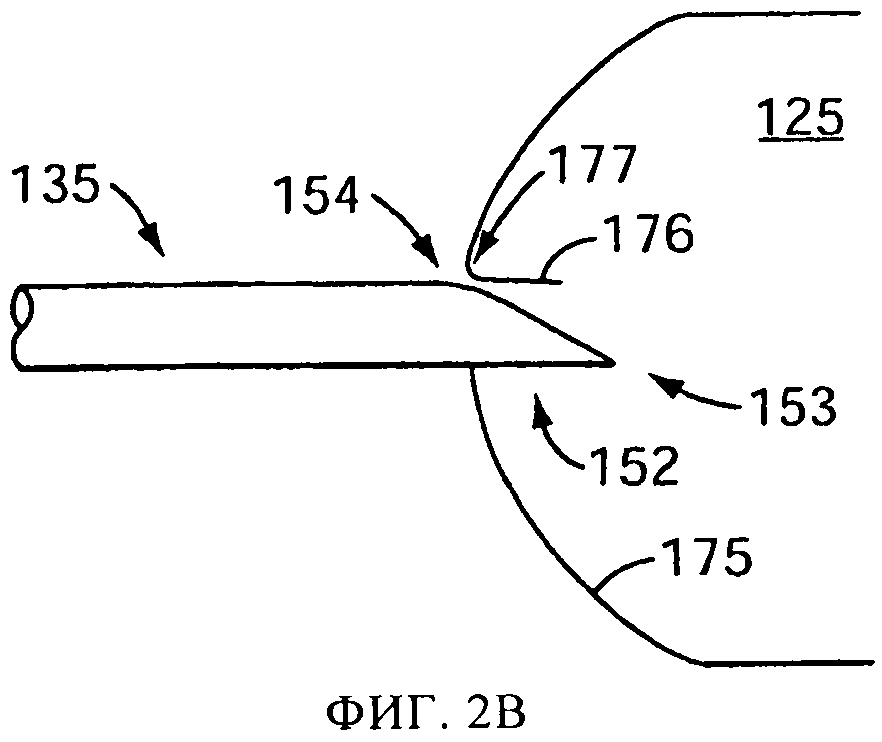
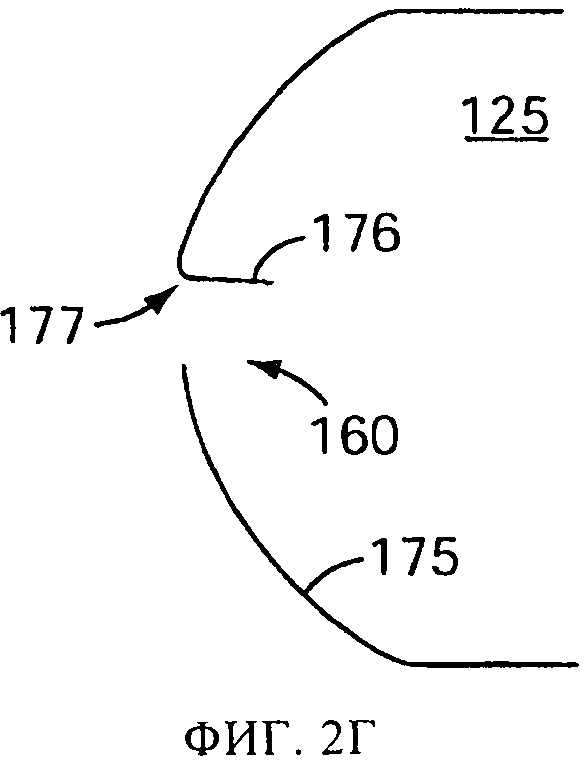
на фиг.2В и 2Г схематически представлены перспективные виды версии емкости, в соответствии с изобретением, в частично вскрытом и вскрытом состоянии, соответственно;
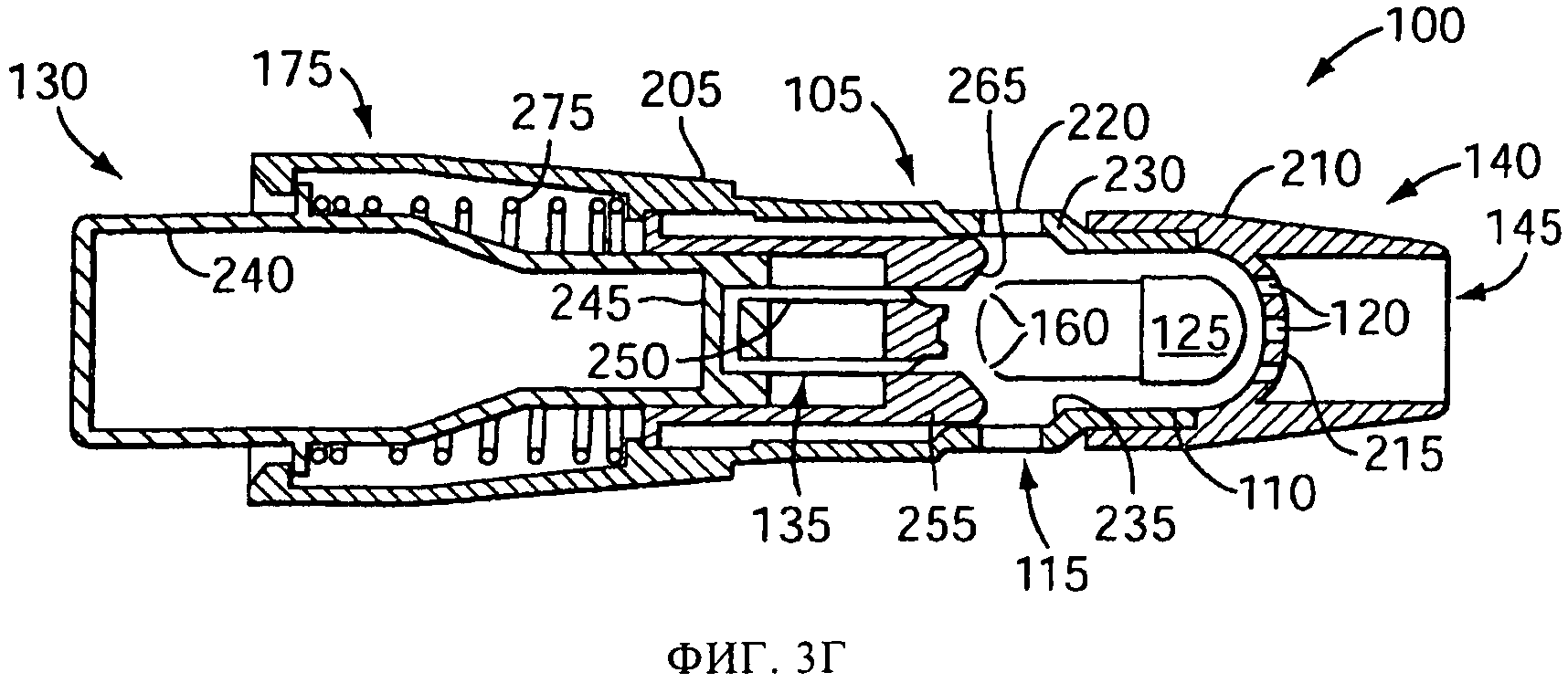
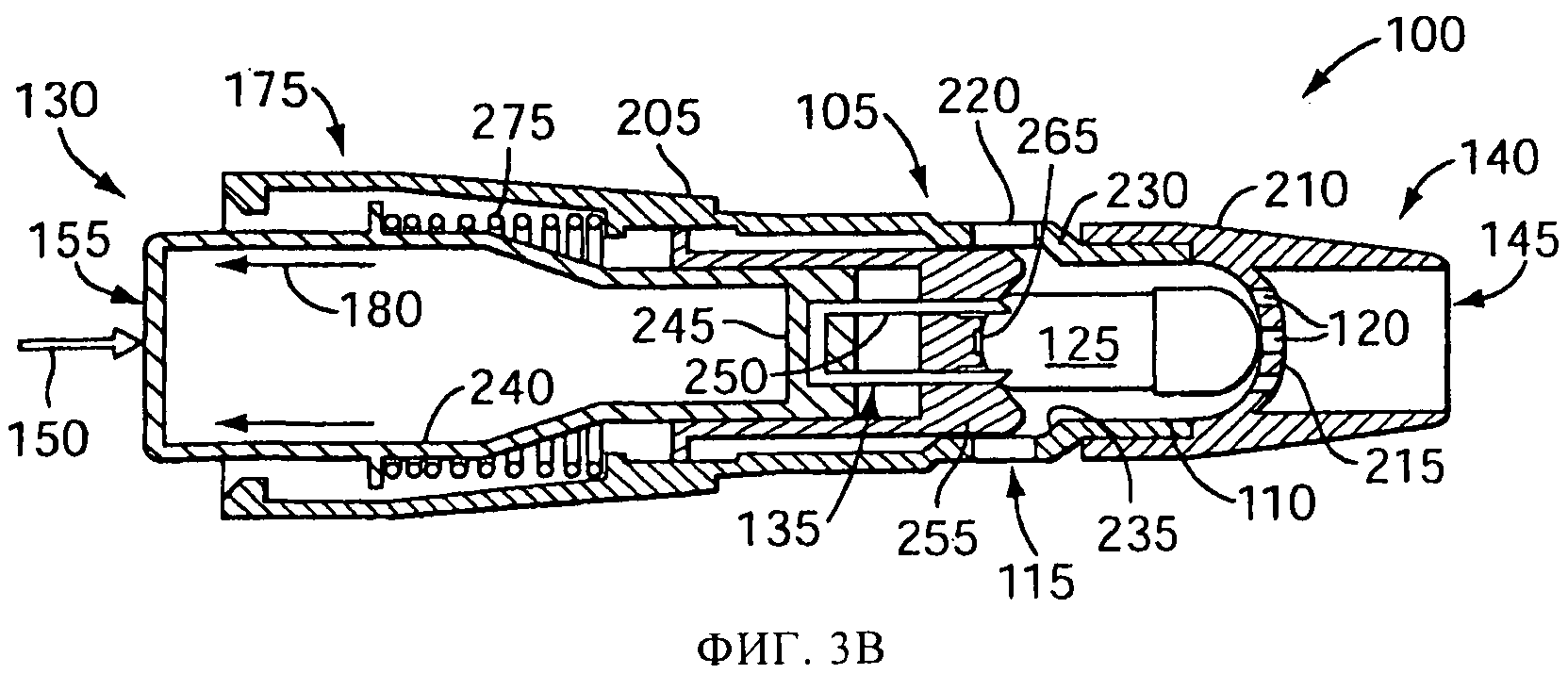
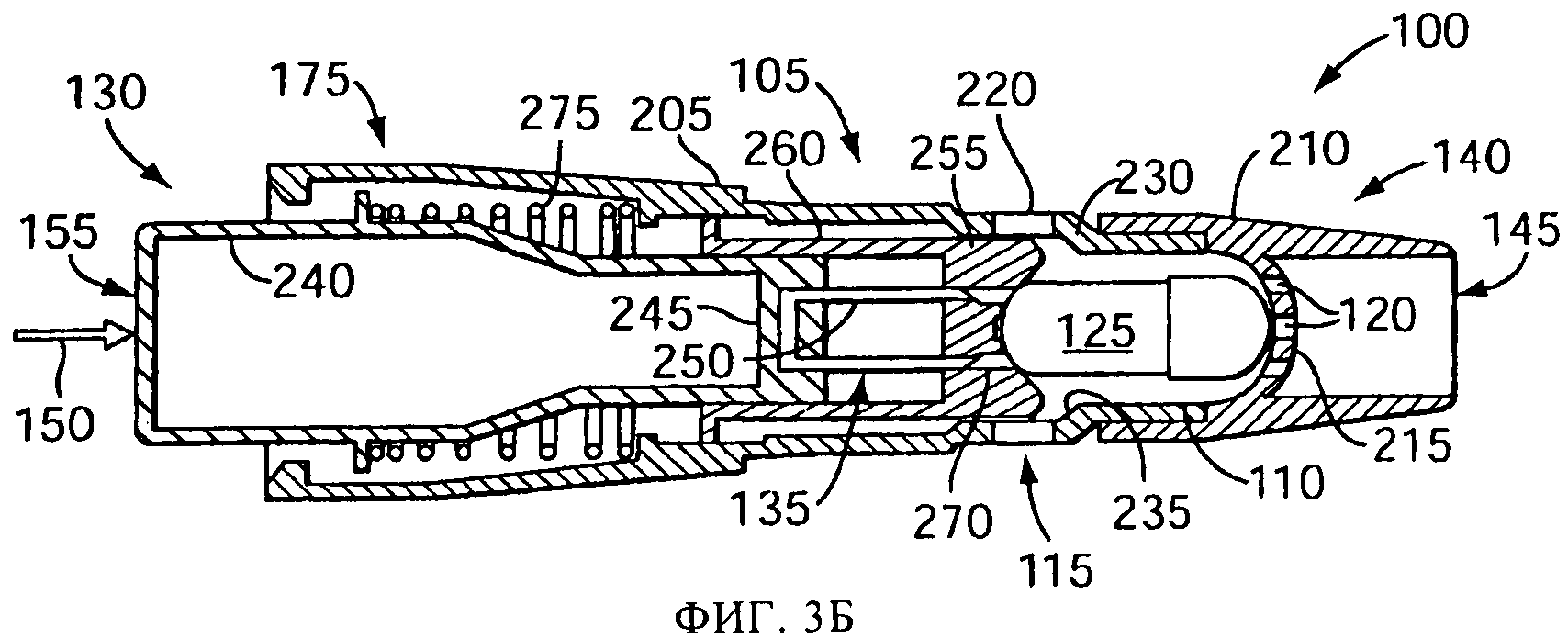
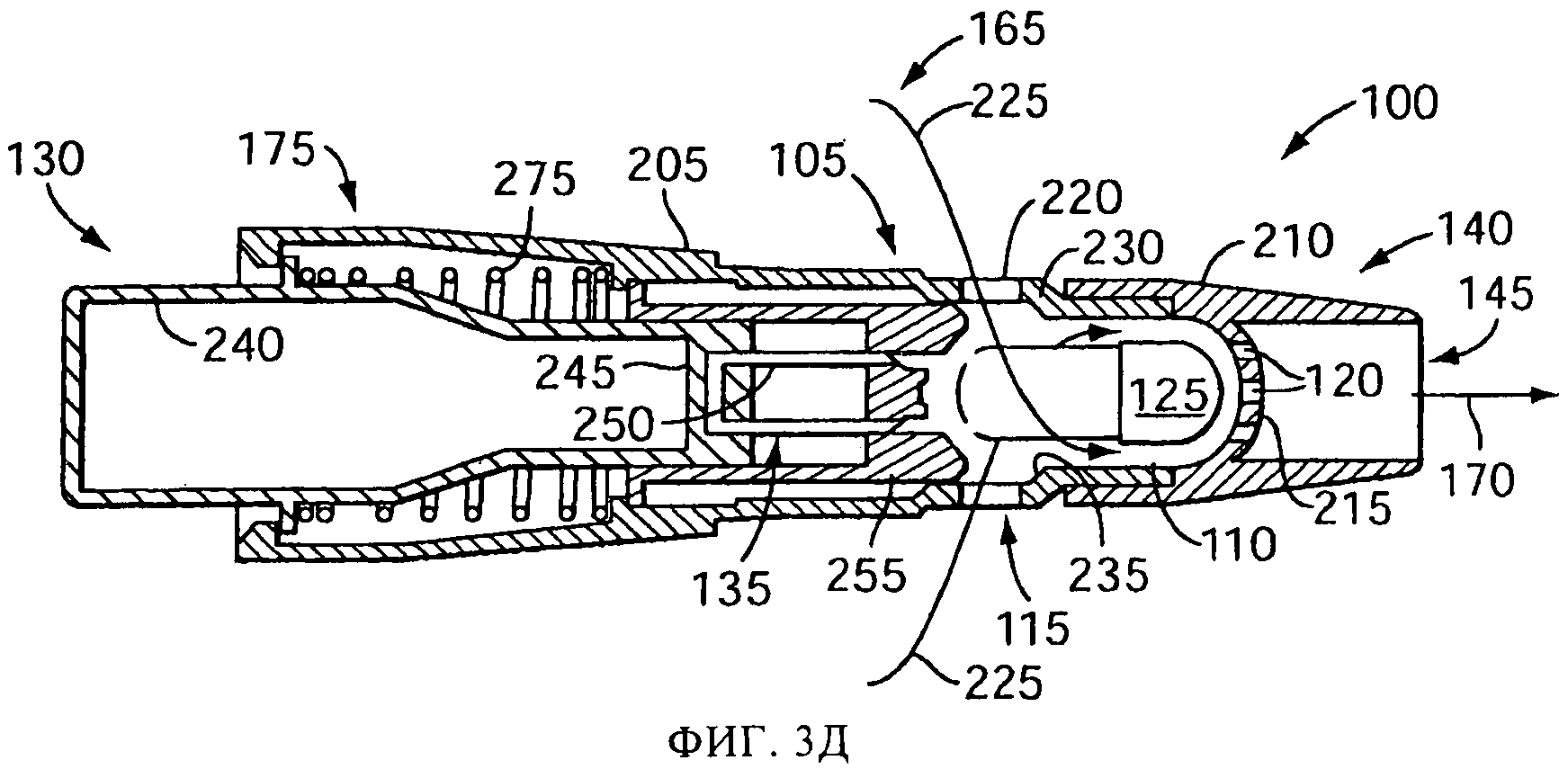
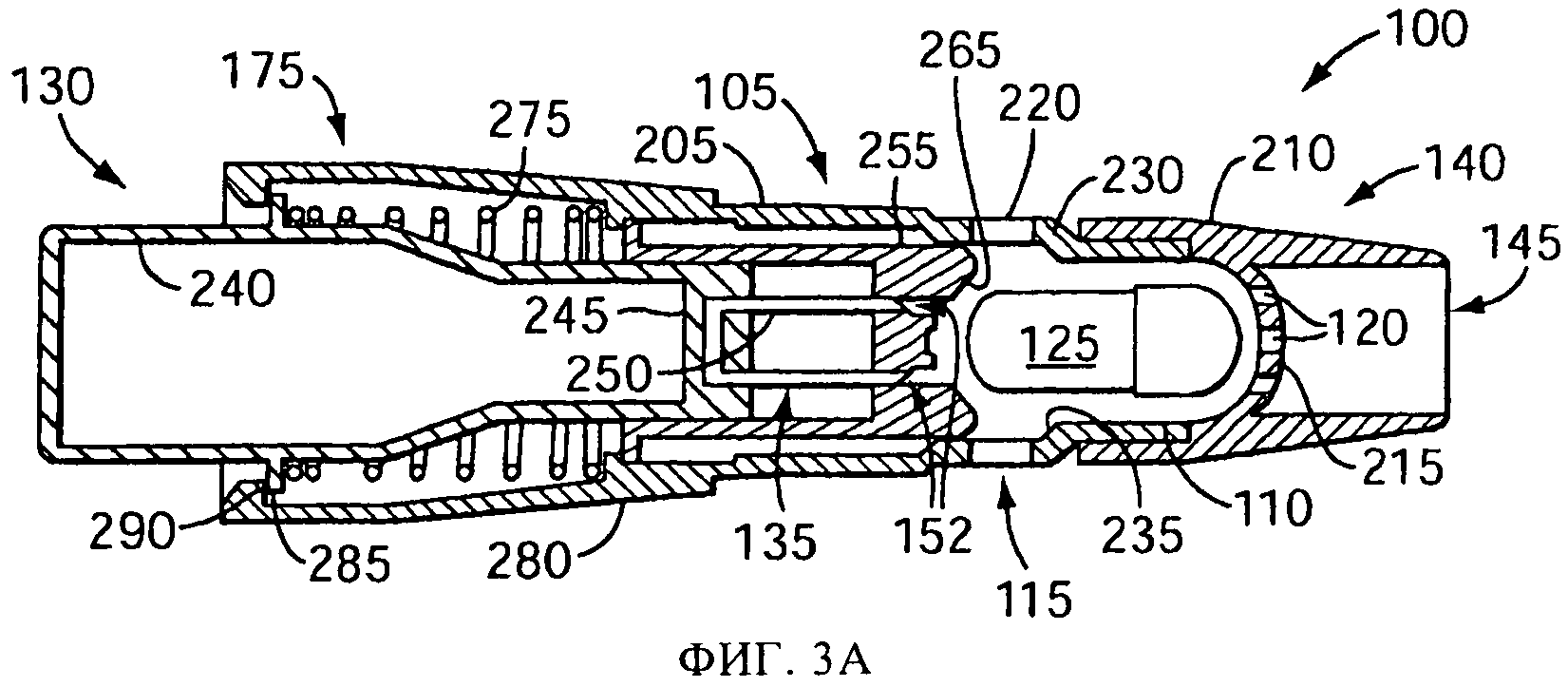
на фиг.3А-3Д схематически представлены в сечении виды сбоку процедуры вскрытия емкости и процесса распыления с использованием емкости, в соответствии с изобретением, для другого варианта распылительного устройства;
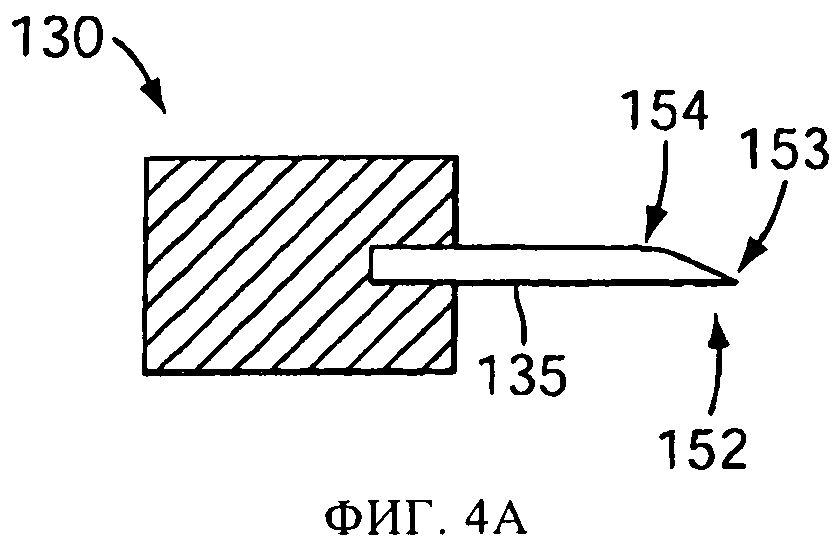
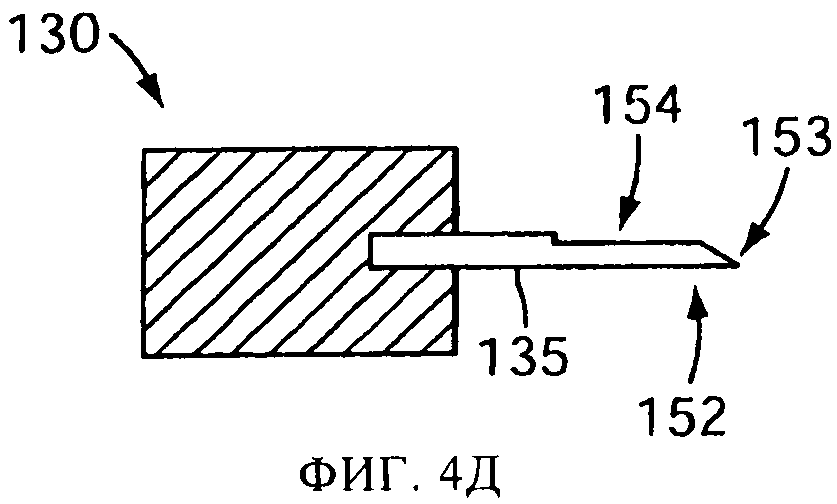
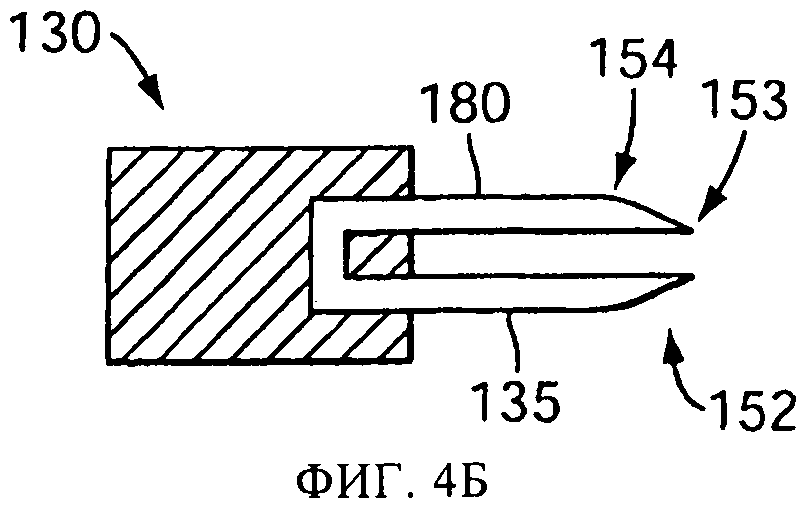
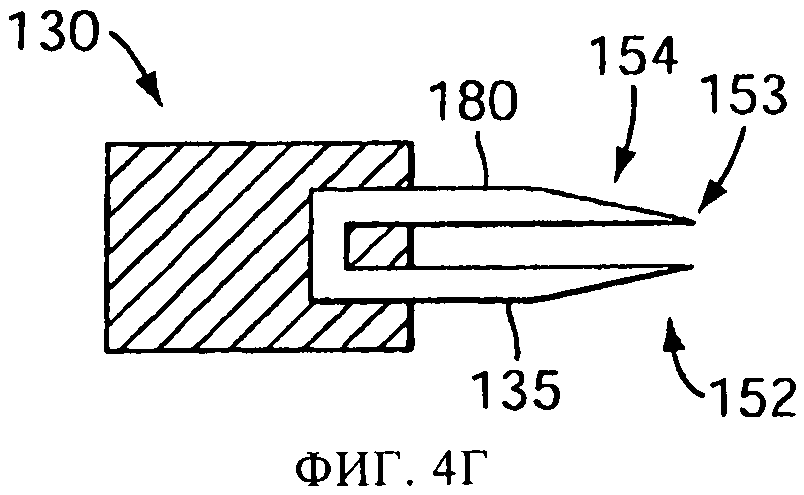
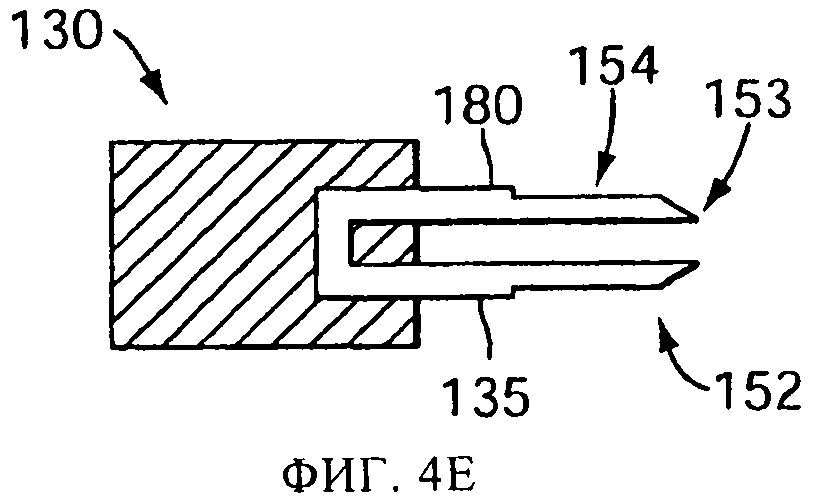
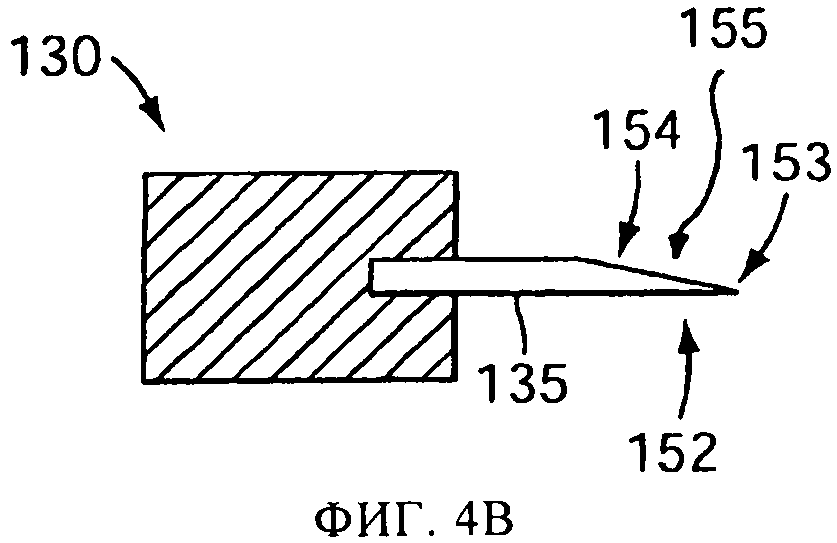
на фиг.4А-4Е схематически представлены в сечении виды сбоку прокалывающих элементов, или наконечников, в соответствии с одним или более вариантов осуществления настоящего изобретения;
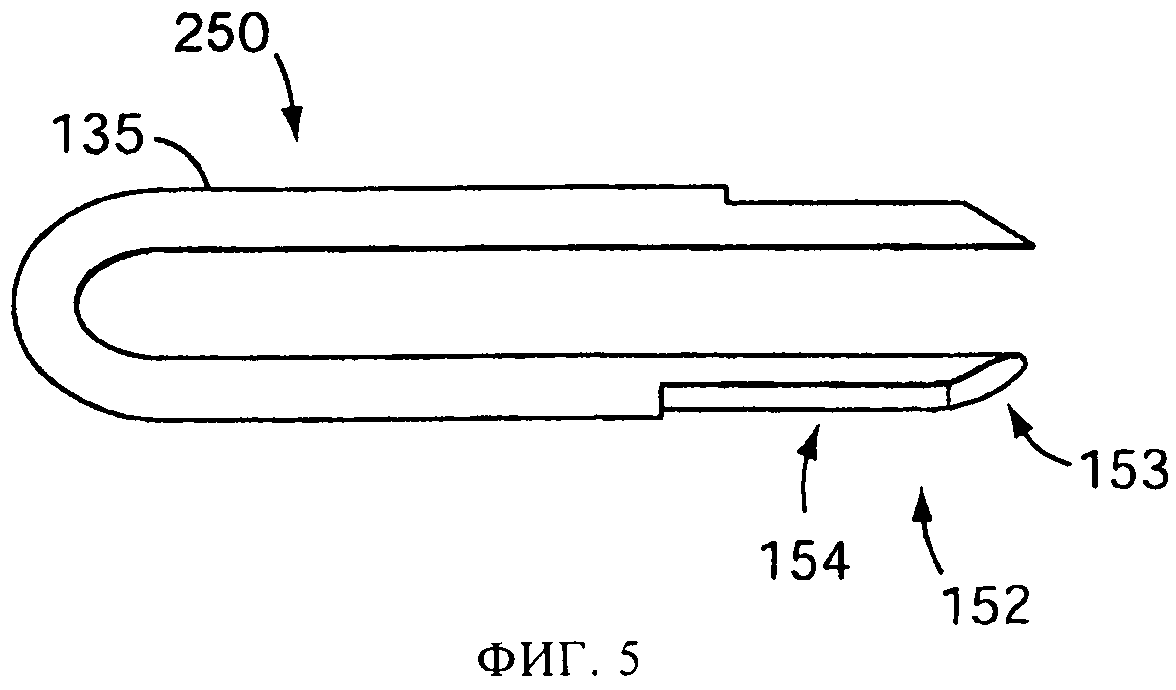
на фиг.5 представлен увеличенный вид сбоку прокалывающего элемента, в соответствии с одним или более вариантами осуществления настоящего изобретения;
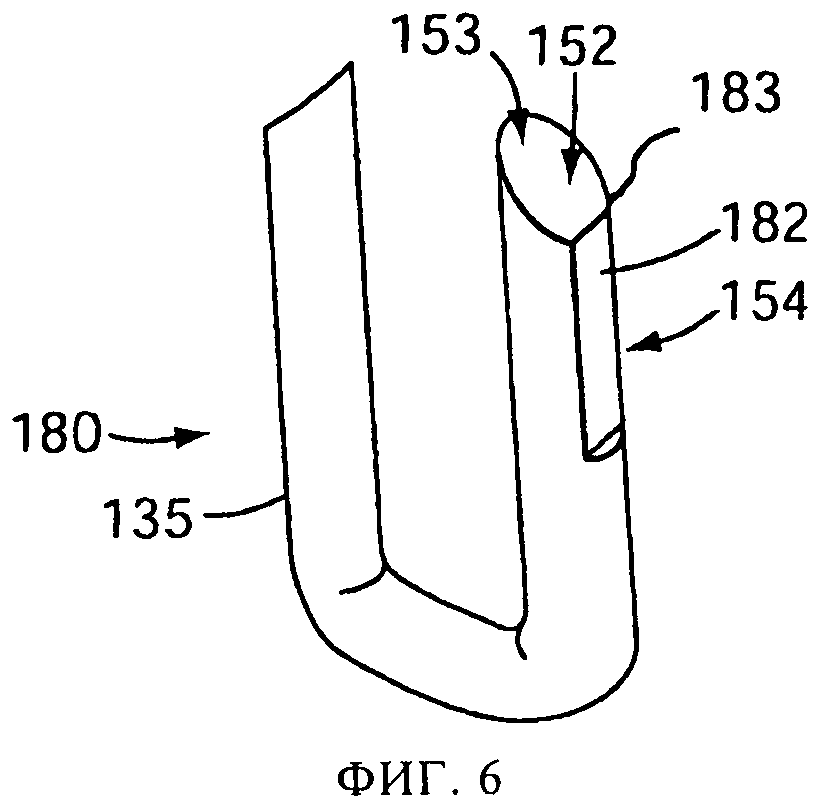
на фиг.6 представлен увеличенный перспективный вид прокалывающего - элемента в соответствии с одним или более вариантами осуществления настоящего изобретения;
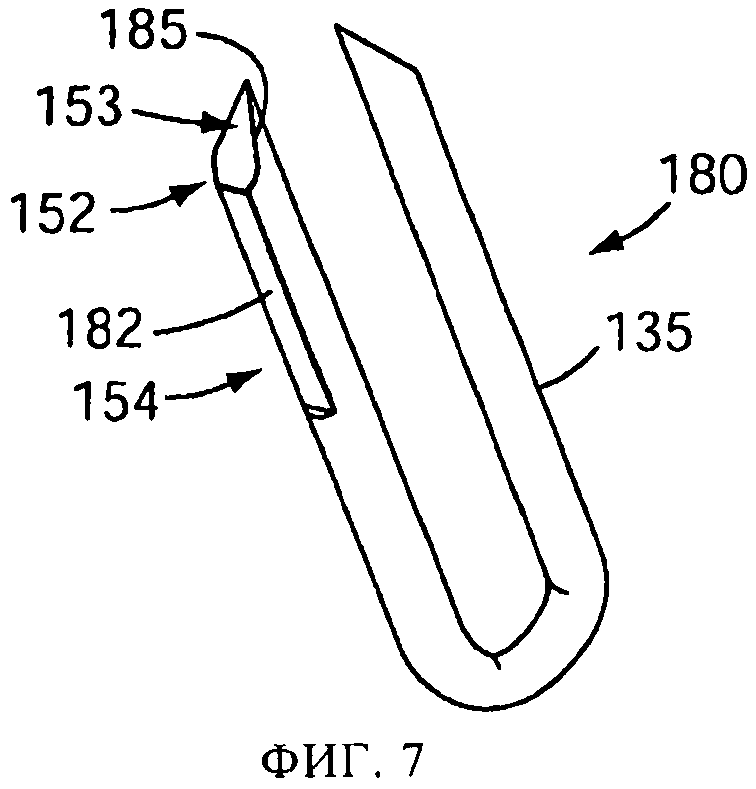
на фиг.7 представлен увеличенный перспективный вид прокалывающего элемента в соответствии с одним или более вариантами осуществления настоящего изобретения;
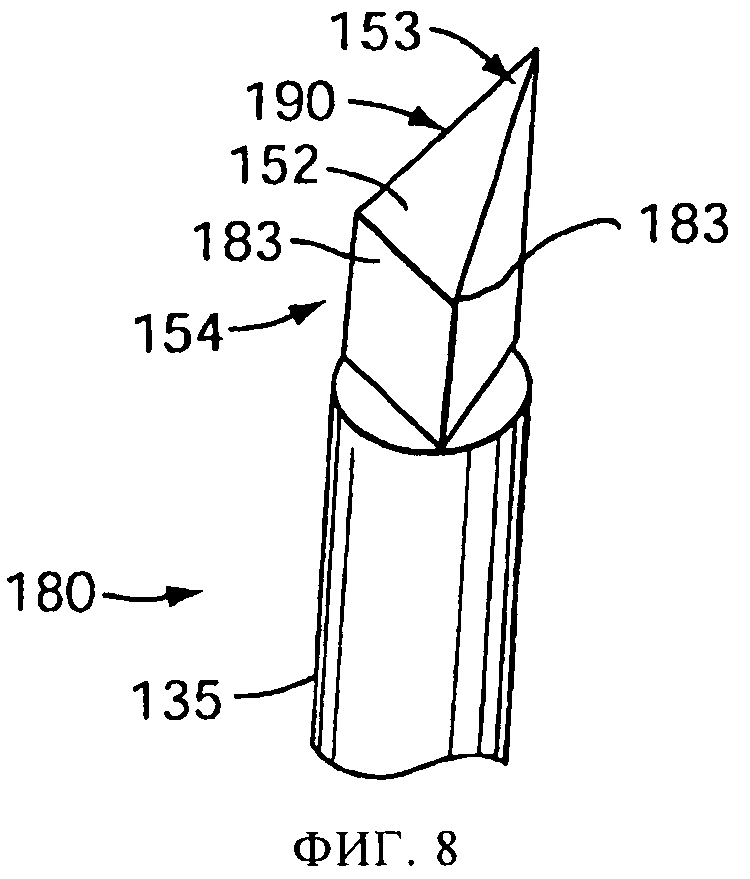
на фиг.8 представлен увеличенный перспективный вид прокалывающего элемента, показывающий один вариант прокалывающего наконечника, в соответствии с одним или более вариантами осуществления настоящего изобретения;
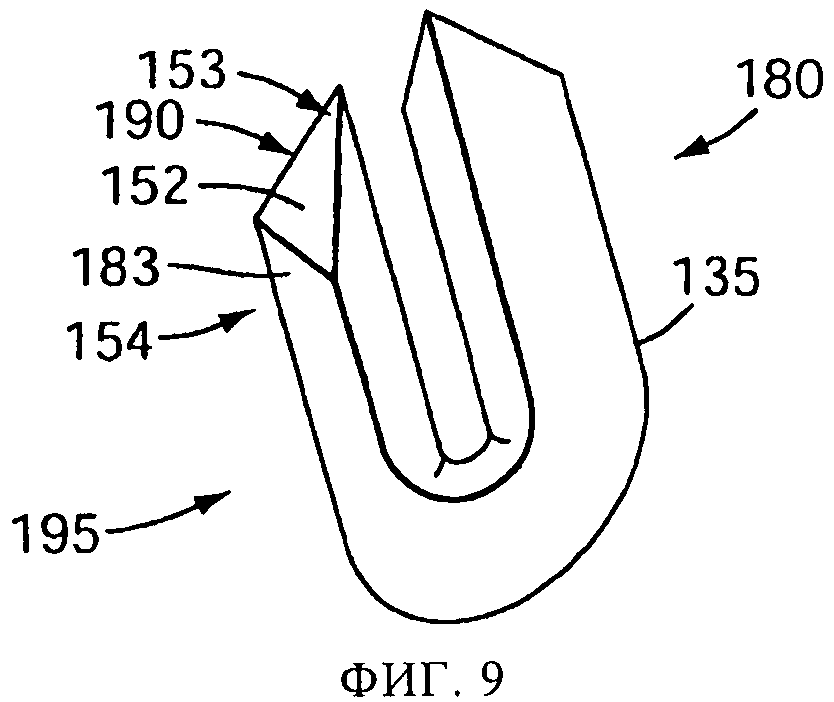
на фиг.9 представлен увеличенный перспективный вид прокалывающих элементов, в соответствии с одним или более вариантами осуществления настоящего изобретения;
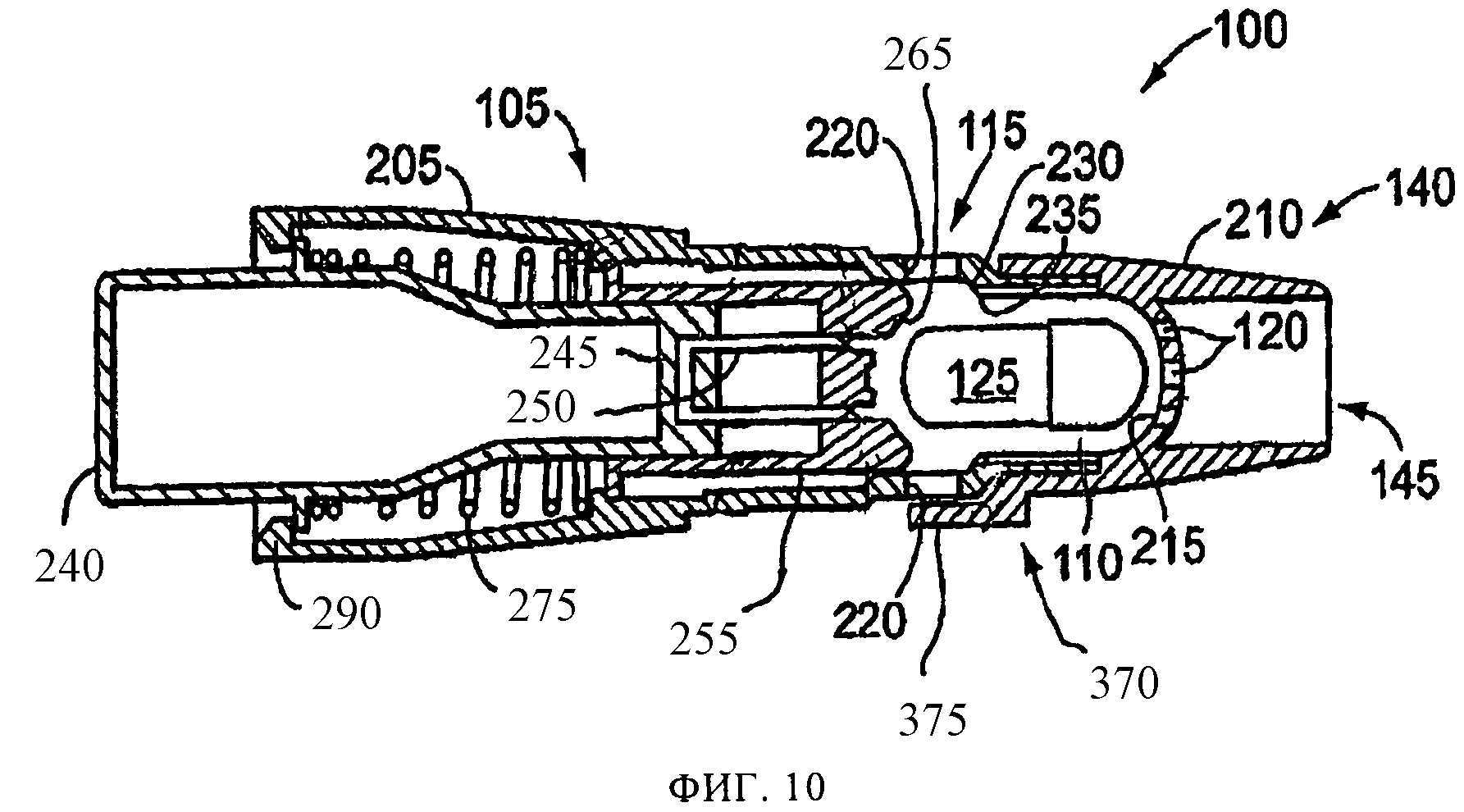
на фиг.10 схематически представлены в сечении виды сбоку варианта осуществления распылительного устройства и емкости, в соответствии с настоящим изобретением; и
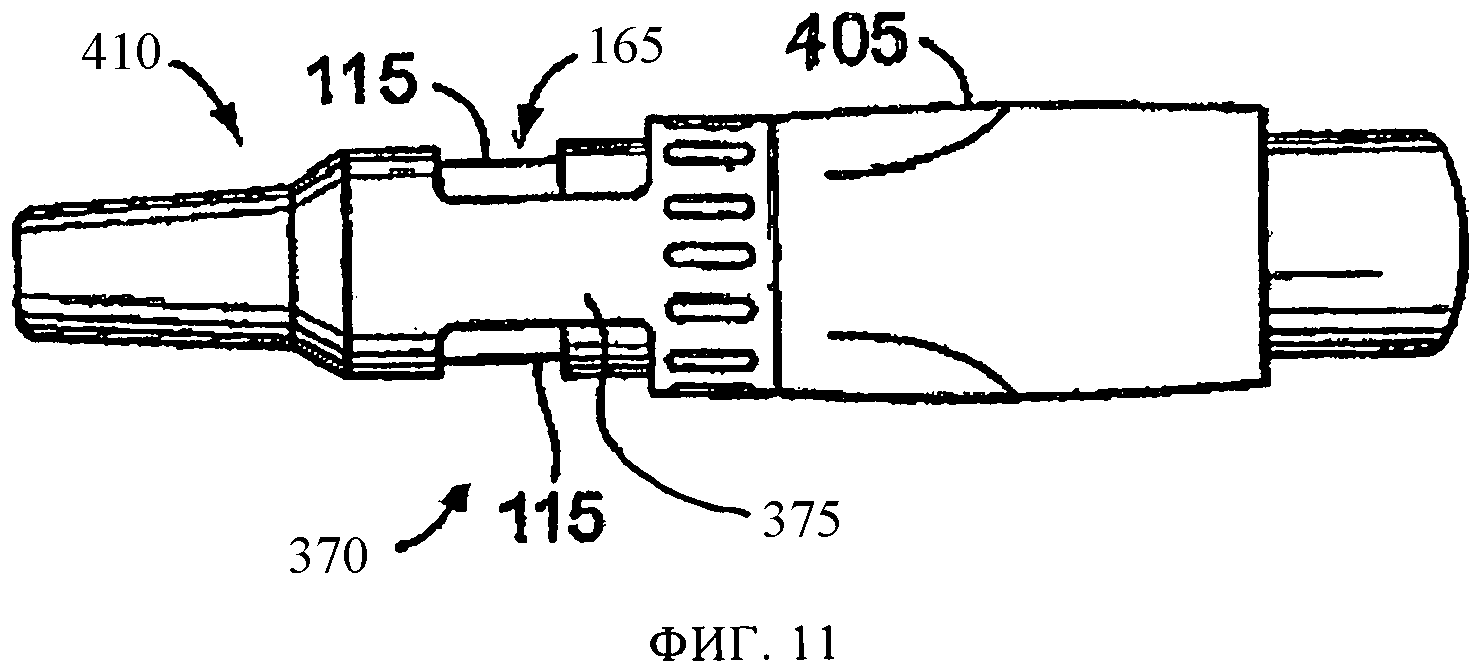
на фиг.11 представлен вид сбоку варианта осуществления распылительного устройства, в соответствии с настоящим изобретением.
Осуществление изобретения
Следует иметь в виду, что если не указано иначе, настоящее изобретение не сводится к конкретному устройству, конструкции, компонентам препарата, системам ввода лекарства, технологиям изготовления, этапам ввода лекарства и т.п., которые могут изменяться. При этом если не указано иначе, ссылка на композицию или компонент включает композицию или компонент сам по себе, так же как и композицию в комбинации с другими композициями или компонентами, например, смеси композиций.
Перед дальнейшим рассмотрением, для облегчения понимания вариантов осуществления настоящего изобретения, приведем определения следующих терминов.
В настоящем описании грамматические обозначения форм единственного числа включают и множественное число, если контекст определенно не указывает иное. Так, например, ссылка на "фосфолипид" включает как одиночный фосфолипид, так и два или более фосфолипида в комбинации или примеси, если в контексте ясно не показано иное.
Ссылки на "один вариант осуществления", "одна версия" или "одна особенность" должны включать один или более таких вариантов осуществления, версий или особенностей, если из контекста не следует иное.
При упоминании действующего вещества, термин охватывает не только конкретную молекулярную сущность, но также и ее фармацевтически приемлемые, фармакологически активные аналоги, включая, без ограничения, соли, эфиры, амиды, гидразиды, N-алкил производные, N-ацил производные, лекарственные формы, конъюгаты, активные метаболиты, и другие подобные производные, аналоги и родственные композиции.
Если не указано иначе, численные толщины стенки представляют собой математически средние значения.
Используемое в описании выражение "активный ингалятор сухого порошка" относится к ингаляционному устройству, в котором для рассеяния и распыления лекарственного препарата, содержащегося в устройстве в резервуаре или в форме единичной дозы, используется не только усилие вдоха пациента. Активные ингаляторы сухого порошка включают ингаляторные устройства, которые содержат средства создания энергии для рассеяния и распыления лекарственного препарата, например, сжатый газ и(или) вибрирующие или вращающиеся элементы.
В настоящем описании, выражение "пассивный ингалятор сухого порошка" относится к ингаляционному устройству, в котором для рассеяния и распыления лекарственного препарата, содержащегося в устройстве в резервуаре или в форме единичной дозы, используется усилие вдоха пациента, и не включает ингаляционные устройства, содержащие средства создания энергии для рассеяния и распыления лекарственного препарата, например, сжатый газ и(или) вибрирующие или вращающиеся элементы. Таким образом, пассивные ингаляторы для получения энергии распыления могут использовать только усилие вдоха пациента.
Настоящая изобретение включает посредством ссылки полные раскрытия публикаций патентных заявок US №№2005-0056280; 2005-0022813; 2003-0106827; и 2005-0150492, и патентной заявки US сер. №10/821,652, которые все вместе с настоящим изобретением принадлежат одному владельцу. Каждая патентная заявка, публикация патентной заявки или патент, упоминаемые здесь, полностью включены в настоящее описание посредством ссылки.
Настоящее изобретение относится к изделию, используемому для хранения лекарственного препарата. Несмотря на то, что изделие и процесс проиллюстрированы в контексте хранения в емкости порошкового лекарственного препарата или препарата с активно действующим компонентом (далее также называемого активным веществом) аэрозольного применения в емкости, настоящее изобретение может быть использовано с другими или в других процессах, системах, изделиях и компонентах, и не должно сводиться только к приведенным здесь примерам.
В вариантах осуществления настоящее изобретение включает емкость для лекарственного препарата аэрозольного применения, в котором препарат извлекается прокалыванием емкости, имеющей по существу однородную толщину стенки, составляющую по меньшей мере примерно 100 мкм, а размер и конфигурация области или областей по существу однородной толщины стенки приспособлены для совмещения с прокалывающими средствами емкости.
В вариантах осуществления настоящее изобретение включает емкость для препарата аэрозольного применения, имеющую стенку толщиной примерно от 100 до 235 мкм, которая может прокалываться для обеспечения выпуска и рассеивания находящегося в нем препарата.
В вариантах осуществления настоящее изобретение включает капсулу для лекарственного препарата или препарата действующего вещества аэрозольного применения, где препарат выпускается путем прокалывания капсулы, толщина стенки которой составляет примерно от 110 до 180 мкм.
В вариантах осуществления настоящее изобретение включает емкость для лекарственного препарата аэрозольного применения, где препарат выпускается прокалыванием емкости, имеющей стенку по существу однородной толщины примерно от 120 до 160 мкм.
В вариантах осуществления настоящее изобретение включает несколько капсул для лекарственного препарата или препарата действующего вещества аэрозольного применения, где препарат выпускается прокалыванием капсулы или капсул, каждая из которых имеет стенку по существу однородной толщины примерно от 120 до 160 мкм.
В вариантах осуществления настоящее изобретение включает емкость для лекарственного препарата аэрозольного применения, где препарат выпускается прокалыванием емкости, имеющей стенку по существу однородной толщины, которая, в месте прокалывания не меняется более чем примерно на 10 мкм.
В вариантах осуществления настоящее изобретение включает капсулу из целлюлозы для лекарственного препарата аэрозольного применения, где препарат выпускается путем прокалывания капсулы, имеющей стенку по существу однородной толщины примерно от 110 до 180 мкм.
В вариантах осуществления настоящее изобретение включает капсулу из алкилметилцеллюлозы для лекарственного препарата аэрозольного применения, где препарат выпускается путем прокалывания капсулы, имеющей стенку толщиной примерно от 110 до 180 мкм, которая, в месте прокалывания, не меняется более чем на примерно 7 мкм.
В вариантах осуществления настоящее изобретение включает емкость для препарата аэрозольного применения, имеющий одну или более областей, включающих стенку с толщиной примерно от 100 до 235 мкм, в котором по меньшей мере одна область стенки может прокалываться для выпуска и рассеяния находящегося там препарата.
В вариантах осуществления настоящее изобретение включает капсулу для лекарственного препарата или препарата действующего вещества аэрозольного применения, где препарат выпускается путем прокалывания одной или более областей стенки капсулы, имеющей одну или более областей с толщиной стенки примерно от 110 до 180 мкм.
В вариантах осуществления настоящее изобретение включает емкость для лекарственного препарата аэрозольного применения, где препарат выпускается прокалыванием емкости, имеющей одну или более областей со стенкой толщиной примерно от 120 до 160 мкм.
В вариантах осуществления настоящее изобретение включает несколько капсул для лекарственного препарата или препарата действующего вещества аэрозольного применения, где препарат выпускается прокалыванием капсулы или капсул, каждая из которых имеет одну или более областей со стенкой толщиной примерно от 120 до 160 мкм.
В вариантах осуществления настоящее изобретение включает емкость для лекарственного препарата аэрозольного применения, где препарат выпускается прокалыванием емкости, имеющей прокалываемую область со стенкой по существу однородной толщины, которая, в месте прокалывания не меняется более чем примерно на 10 мкм.
В вариантах осуществления настоящее изобретение включает капсулу из целлюлозы для лекарственного препарата аэрозольного применения, где препарат выпускается путем прокалывания капсулы, имеющей прокалываемую область со стенкой по существу однородной толщины примерно от 110 до 180 мкм.
В вариантах осуществления настоящее изобретение включает систему для распыления порошковых действующих веществ, например, лекарственных препаратов, включающую корпус, образующий камеру с одним или более отверстием для впуска воздуха, размеры которой обеспечивают помещение в ней капсулы, содержащей лекарственный препарат аэрозольного применения; прокалывающие средства внутри корпуса, включающие прокалывающий элемент, имеющий передний конец, образующий режущую кромку, обеспечивающую эффективное прорезывание стенки капсулы для создания отверстия в капсуле; и концевую секцию, связанную с корпусом, размеры и форма которой приспособлены для помещения ее в рот или нос пользователя с тем, чтобы пользователь мог сделать вдох через концевую секцию для ингаляции распыленного лекарственного препарата, содержавшегося в капсуле, сквозь отверстие, созданное в средствах крепления капсулы, когда препарат выводится посредством прокалывания емкости, имеющей стенку толщиной примерно от 100 до 180 мкм, не изменяющуюся в месте прокалывания более чем на 10 мкм.
В вариантах осуществления настоящее изобретение включает способ распыления лекарственного препарата, включающий заполнение препаратом емкости, например, капсулы, имеющей однородную толщину стенки в месте прокалывания примерно от 100 до 180 мкм, помещение емкости в камеру, продвижение прокалывающих средств в емкость, в результате чего стенка прокалывается и содержимое емкости освобождается для ингаляции.
В вариантах осуществления настоящее изобретение включает емкость для лекарственного препарата аэрозольного применения, где препарат выпускается прокалыванием емкости, имеющей стенку толщиной примерно 100-240 мкм, которая, в месте прокалывания не меняется более чем на 15 мкм.
В вариантах осуществления настоящее изобретение включает несколько капсул из целлюлозы для лекарственного препарата аэрозольного применения, где препарат выпускается путем прокалывания капсул, каждая из которых имеет стенку однородной толщины примерно от 110 до 180 мкм, и где толщина стенки не меняется более чем примерно на 10 мкм от капсулы к капсуле.
В вариантах осуществления настоящее изобретение включает несколько капсул из целлюлозы для лекарственного препарата аэрозольного применения, где препарат выпускается путем прокалывания капсул, каждая из которых имеет стенку однородной толщины примерно от 100 до 240 мкм, и где распределение капсул по толщине стенок таково, что по меньшей мере 99,7% капсул имеют толщину стенок примерно от 100 до 240 мкм.
В вариантах осуществления настоящее изобретение включает несколько капсул из целлюлозы для лекарственного препарата аэрозольного применения, где препарат извлекается путем прокалывания капсул, каждая из которых имеет стенку однородной толщины примерно от 100 до 240 мкм, и где распределение толщины по капсулам таково, что по меньшей мере 95% капсул имеют толщину стенок примерно от 105 до 225 мкм.
В вариантах осуществления настоящее изобретение включает капсулу из целлюлозы для лекарственного препарата аэрозольного применения, где препарат выпускается путем прокалывания капсулы прокалывающими средствами, капсула имеет стенку однородной толщины примерно от 120 до 160 мкм, а прокалывающие средства включают заостренные средства любой формы, например, заостренный элемент, элемент с кромкой или их комбинации.
В вариантах осуществления, материал емкости включает целлюлозный или полимерный материал.
В вариантах осуществления, материал емкости включает алкил целлюлозу или гидроксиалкилцеллюлозу.
В вариантах осуществления, емкость имеет купол или полусферическую часть.
В вариантах осуществления емкость имеет овальную форму. В вариантах осуществления емкость имеет сферическую форму. В вариантах осуществления емкость имеет эллипсоидную форму. В вариантах осуществления место прокалывания емкостей находится в области криволинейной или полусферической части стенки.
В вариантах осуществления место прокалывания емкостей находится в области прямой части стенки.
В вариантах осуществления упомянутая область емкости включает всю емкость.
Другие варианты осуществления настоящего изобретения могут включать два или более из описанных выше признаков, особенностей, версий или вариантов осуществления.
Один вариант осуществления распылительного устройства, в соответствии с настоящим изобретением, показан схематически на фиг.1А-1Д с цифровым обозначением 100, и включает емкость(контейнер) или капсулу 125 для лекарственного препарата. Распылительное устройство 100 имеет корпус 105, образующий камеру 110, имеющую одно или более отверстий 115 для впуска воздуха, и одно или более отверстий 120 для выпуска воздуха. Размеры камеры 110 обеспечивают размещение в ней емкости 125, содержащей лекарственный препарат, аэрозольного применения. Вскрывающий механизм 130 включает вскрывающий или прокалывающий элемент 135, который может перемещаться внутри камеры 110. Вблизи отверстия 120 или прилегая к нему, находится концевая секция 140, размеры и форма которой обеспечивают ее введение в рот или нос пользователя с тем, чтобы пользователь мог сделать вдох через отверстие 145 в концевой секции 140, которое соединено с выпускным отверстием 120. В альтернативном варианте, концевая секция соединена для передачи текучей среды с любым интерфейсом пациента для обеспечения ингаляции и введения лекарственного препарата.
Распылительное устройство 100 использует поток воздуха, проходящий сквозь камеру 110 для распыления лекарственного препарата, находящегося в емкости 125. Например, на фиг.1А-1Д показана работа версии распылительного устройства 100, в котором воздух, протекающий сквозь впускное отверстие 115, используется для распыления лекарственного препарата, а распыленный лекарственный препарат выходит сквозь выпускное отверстие 120 так, что он может быть введен пользователю сквозь отверстие 145 в концевой секции 140. На фиг.1А распылительное устройство 100 показано в исходном состоянии. Емкость 125 помещена внутри камеры 110, а лекарственный препарат содержится внутри емкости 125.
Для использования распылительного устройства 100, лекарственный препарат, находящийся в емкости 125, обнажается для его распыления. В показанных на фиг.1А-1Д версиях, вскрывающий механизм 130 смещается вперед внутри камеры 110 приложением силы 150 к вскрывающему механизму 130. Например, пользователь может надавить на нижнюю поверхность вскрывающего механизма 130, чтобы вскрывающий механизм начал скользить внутри корпуса 105 для приведения вскрывающего или прокалывающего элемента 135 в соприкосновение с емкостью 125 в камере 110, как это показано на фиг.1Б. При дальнейшем приложении силы 150, вскрывающий элемент 135 смещается вперед, упираясь в переднюю стенку 122 емкости 125, как это показано на фиг.1В. Вскрывающий механизм может включать один или более наконечников 152 (которые могут быть заостренными, заточенными, угловыми, гранеными или затупленными), которые входят в соприкосновение с емкостью 125, в результате чего создается отверстие в емкости 125. Затем вскрывающий механизм 130 отводится в положение, показанное на фиг.1Г, оставляя сквозное отверстие 160 в стенке емкости 125, обнажающее лекарственный препарат, находящийся в емкости 125.
Затем сквозь впускное отверстие или впускные отверстия 115 входит воздух или другой газ, как это показано стрелками 165 на фиг.1Д. Поток воздуха вызывает распыление лекарственного препарата. Когда пользователь делает вдох (при этом возникает воздушный поток, показанный стрелкой 170 на фиг.1Д), распыленный лекарственный препарат сквозь концевую секцию 140 вводится в дыхательные пути пользователя. В одной версии, воздушный поток 165 может быть создан вдохом пользователя. В другой версии, во впускное отверстие 115 может впрыскиваться сжатый воздух или другой газ для создания распыляющего воздушного потока 165.
Для повышения результативности и эффективности распылительного устройства 100, прокалывающий элемент 135 может включать заостренный наконечник 152, имеющий передний конец 153, задний край 154 и промежуточную плоскую часть 155 между ними (показана на фиг.2). На переднем конце 153 сформировано острие или режущая кромка, эффективно прорезающие стенку капсулы 125. Такая форма включает, в вариантах осуществления, эллиптическую или частично эллипсоидальную форму, образуемую косым срезом элемента 135 круглого поперечного сечения. В вариантах осуществления на заднем крае 154 режущей поверхности нет. Например, в одной версии, задний край 154 может быть прошлифован с образованием пологого профиля, как показано на фиг.2А. На фиг.2А-2Г представлен процесс прокалывания капсулы с использованием одного варианта осуществления прокалывающего элемента 135, в соответствии с настоящим изобретением. Когда прокалывающий элемент 135 сдвигается вперед из положения, показанного на фиг.2А, в положение, показанное на фиг.2Б, острие на переднем конце 153 прорезает стенку 175 капсулы. При дальнейшем движении вперед прокалывающего элемента 135, как показано на фиг.2В, отгиб 176 материала стенки проталкивается внутрь в капсулу 125. Поскольку задний край 154 не обладает режущим профилем, часть 177 отгиба 176 напротив первоначально прорезанной части изгибается и испытывает скорее пластическую деформацию, чем деформацию среза, оставляя после отведения прокалывающего элемента 135 отверстие 160, показанное на фиг.2Г.
На фиг.3А-3Д представлен пример распылительного устройства с камерой 110, более полно описанного в US 4069819 и US 4995385, которые полностью включены в настоящее описание посредством ссылки. В такой конструкции продольная ось камеры 110 лежит в целом в направлении ингаляции, и емкость 125 вставляется вдоль по длине камеры 110 с тем, чтобы продольная ось емкости могла быть параллельной продольной оси камеры 110. В версии, показанной на фиг.3А-3Д, размер камеры 110 обеспечивает установку в нее емкости 125, содержащей лекарственный препарат, так, чтобы емкость могла двигаться внутри камеры 110. В задней части емкости 125, в версии, показанной на фиг.3А-3Д, посредством прокалывающего механизма 130, который может скользить внутри основной части 205, создается несколько отверстий 160.
Впускные отверстия 115 могут включать несколько расположенных по касательной щелей 220. Когда пользователь делает вдох (стрелки 170 на фиг.1Д) через наконечник 210, наружный воздух втягивается сквозь расположенные по касательной щели 220, как это показано стрелками 225 на фиг.3Д. Воздушный поток 225 создает вихревой воздушный поток внутри камеры 110. Вихревой воздушный поток вводит емкость 125 в соприкосновение с перегородкой 215 (включающей одно или более выпускных отверстий 120) и, затем, так перемещает его внутри камеры 110, что лекарственный препарат покидает емкость 125 и захватывается воздушным вихревым потоком. В одной или более версий перегородка 215 имеет куполообразную или полусферическую форму. В одной или более версий емкость может поворачиваться внутри камеры 110 так, что продольная ось емкости, которая может представлять собой капсулу, составляет угол менее 80 градусов, а в предпочтительном варианте, менее 45 градусов, с продольной осью камеры. Движение емкости 125 в камере 110 может быть вызвано тем, что ширина камеры 110 меньше длины емкости 125. В одной конкретной версии, камера 110 включает суживающуюся секцию 230, которая заканчивается бортиком 25. Во время возникающего на вдохе вихревого потока воздуха в камере 110, передний конец емкости 125 может прийти в соприкосновение с перегородкой 215 и упереться в нее, а боковая стенка емкости 125 может касаться бортика 235 и скользить и(или) поворачиваться вдоль бортика 235. Такое движение емкости 125, которая может представлять собой капсулу, особенно эффективно для выталкивания большого количества лекарственного препарата сквозь несколько отверстий 160 в задней части емкости 125.
Вскрывающий механизм 130, показанный в исходном положении на фиг.3А, включает поршень 240, прикрепленный своим передним концом 245 к вскрывающему элементу 135, который в показанной версии представляет собой U-образную скобку 250, имеющей несколько наконечников 152, например, два наконечника, показанные в данной версии. Вскрывающий механизм 130 также включает посадочный элемент (также иногда называемый направляющей) 255, который соприкасается с поршнем 240 и(или) вскрывающим элементом 135, и может скользить относительно поршня 240 и вскрывающего элемента 135. Для создания отверстий 160 в емкости 125, пользователь прикладывает силу 150 к поршню 240, как это показано на фиг.3Б, например, надавливая пальцем на конец поршня 240. Под действием силы 150, поршень скользит внутри основной части 205. Небольшое фрикционное сцепление между поршнем 240 и задней секцией 260 посадочного элемента 255 заставляет посадочный элемент 255 также скользить внутри основной части 205, пока передняя посадочная поверхность 265 посадочного элемента 255 не войдет в соприкосновение с емкостью 125, как это показано на фиг.3Б. Передняя посадочная поверхность 265, форма которой в целом согласована со стыкуемой поверхностью (например, куполообразной) емкости 125, фиксирует емкость 125 между посадочным элементом 255 и перегородкой 125, которая по форме также может в целом соответствовать емкости 125. Продолжающееся приложение силы 150 заставляет поршень 240 и вскрывающий элемент 135 скользить относительно посадочного элемента 255, как это показано на фиг.3В, продвигая вперед вскрывающий элемент 135 сквозь отверстия 270 в передней опорной поверхности 265 к емкостью 125 для создания отверстий 160, как это было описано выше. При снятии силы 150 пружина 275 или иной элемент создания опорного усилия возвращают вскрывающий механизм 130 обратно в исходное положение. Например, пружина 275 может упираться в уступ 280 в основной части 205, и давить на фланец 285 на поршне 240, толкая его к ободку 290 на основной части 205. Фрикционное сцепление между поршнем 240 и посадочным элементом 255 также способствует возвращению посадочного элемента 255 в его отведенное положение.
В вариантах осуществления системы 100 распыления, в соответствии с настоящим изобретением, лекарственный препарат в капсуле 125 открывается воздействию окружающего воздуха для превращения в аэрозоль. В версии, представленной на фиг.3А-3Д, прокалывающий механизм 130 двигается вперед внутри камеры 110 приложением силы 150 к прокалывающему механизму 130. В исходном положении посадочный элемент 255 и прокалывающий элемент 135 двигаются вперед как единое целое до положения, показанного на фиг.3Б. В этом положении посадочная поверхность 265, размеры и конфигурация которой сделаны в целом согласующимися со стенкой емкости, например, куполообразной стенкой нижнего конца капсулы, соприкасается с капсулой 125, и центрирует капсулу 125 внутри камеры 110, а также устанавливает ее так, что продольная ось капсулы 125 становится параллельной центральной линии устройства. Это позволяет выставить капсулу надлежащим образом для прокалывания, обеспечивая этим оптимальное распыление содержимого. При продолжающемся приложении силы 150, прокалывающий элемент 135 входит в стенку капсулы 125 и проходит сквозь нее. После этого прокалывающий механизм 130 отводится в положение, показанное на фиг.3А, оставляя отверстие или отверстия 160 в стенке капсулы 125, обнажающие лекарственный препарат, находящийся в капсуле 125.
Создание, надлежащим образом, отверстия 160 в капсуле 125 способствует результативному и эффективному введению пользователю лекарственного препарата аэрозольного применения. Напротив, отверстие 160, созданное неправильно, может способствовать неэффективному и менее результативному введению лекарства пользователю. Поэтом правильно сконструированный заостренный конец 152 может способствовать созданию в капсуле отверстий со стабильными параметрами. Кроме того, важно иметь такой наконечник 152, например, заостренный наконечник, при использовании которого часть стенки капсулы 125, которая перемещена для создания отверстия 160, не отделилась бы от капсулы 125, и не могла превратиться в один или более оторванных фрагментов. Эти фрагменты, при их вдохе пользователем, могут вызвать дискомфорт.
Прокалывающий элемент 135, имеющий заостренный наконечник 152 с нережущим задним краем 154 дает много преимуществ. Например, обычный прокалывающий элемент может быть сформирован из круглой проволоки, которая срезана или прошлифована по плоскости на заднем крае, либо может быть сформирована так, чтобы заостренный наконечник включал непрямую кромку на заднем крае, например, скругленную кромку, сформированную с использованием ромбовидной проволоки. При использовании подобных прокалывающих элементов отгиб 176 (фиг.2) может быть в некоторых случаях отрезан на части 177, в результате чего отгиб 176 отделяется от стенки 175 (например, от куполообразной концевой части) емкости 125 и может попасть в аэрозоль. При использовании заднего края 154, не обладающего режущим свойством, число таких оторванных отгибов 176 сокращается существенно, и получаются проколы с более стабильными параметрами.
Не обладающий режущими свойствами задний край 154 заостренного наконечника 152 может быть выполнен путем шлифовки заднего края 154, как это было описано выше, либо приданием формы заостренному наконечнику 152 другим способом. Примеры заостренных наконечников 152 с не обладающими режущими свойствами задними краями показаны на фиг.4А, 4Б, 4В, 4Г, 4Д, 4Е и 5-9. В версии фиг.4Б два наконечника расположены по противоположным концам U-образного прокалывающего элемента 250. В версиях, показанных на фиг.4В и 4Г, заостренный конец получается плоским срезом или шлифовкой прокалывающего элемента 135. В этой версии, срез имеет достаточную длину и(или) угол наклона, чтобы задний край 154 никогда не коснулся капсулы 125. Соответственно, только передний конец 153 и промежуточная плоская часть 155 соприкасаются с капсулой, и капсула не подвержена потенциально повреждающим воздействиям от контакта с задним краем 154. В некоторых версиях распылительного устройства смещение вперед прокалывающего элемента на фиг.4А и 4Б ограничивается, для предотвращения соприкосновения капсулы с задним краем 154.
В одной или более версий, представленных на фиг.5, 6 и 7, показано, как у обычного круглого провода с плоским срезом наконечника дополнительной обработкой срезается задний край 154, с удалением режущей части заднего края, в результате чего получается плоская поверхность 182, заканчивающаяся прямой кромкой 183. При этом, как показано на фиг.5, 6 и 7, образуется заостренный наконечник 152 примерно D-образной формы. Плоская поверхность 182, заканчивающаяся прямой кромкой 183, имеет преимущество перед скругленной или заостренной кромкой обычного прокалывающего элемента в том, что образуется меньше оторванных отгибов 176, снижается вероятность захвата прокалывающего элемента внутри капсулы, и снижается износ распылительного устройства 100 из-за того, что на обычных кромках происходит соскабливание пластически деформируемого материала с соприкасающихся поверхностей устройства. Версия, представленная на фиг.7, аналогична версии фиг.6, но имеет одну или более граней 185 на переднем конце 153 для облегчения прохождения наконечника сквозь стенку 175 капсулы. В версиях на фиг.8 и 9 заостренный наконечник 152 имеет по существу треугольную форму 190. Получающиеся при создании треугольной формы 190 плоская поверхность 182 и прямая кромка 183 обладают по существу тем же преимуществом, что и плоская поверхность 182 и прямая кромка 183, получающиеся у D-образного наконечника.
Как показано на фиг.10 и 11, в вариантах осуществления распылительной системы в соответствии с настоящим изобретением, используется защитный элемент 370 отверстий для впуска воздуха, включающий закрывающую часть 375, которая по меньшей мере частично накрывает одно или более отверстий 115 для впуска воздуха. Защитный элемент 370 предотвращает перекрытие воздушного потока, не допуская закупоривания по меньшей мере одного из впускных отверстий 115 пальцами или рукой пользователя в процессе использования. Соответственно, если пользователь случайно возьмет устройство в области впускных отверстий 115, пользователь захватит защитный элемент 370, а не одно или более впускных отверстий 115, и воздух будет продолжать поступать в камеру 110. Как более подробно описано в WO 2004/091705, размеры и конфигурация защитного элемента 370 и закрывающей части 375 могут быть выбраны так, что воздушный поток 165 может пойти по более извилистому пути в области защитного элемента 370, либо размеры и конфигурация защитного элемента 370 и(или) закрывающей части 375 могут быть выбраны так, что сопротивление потоку через устройство увеличивается и желательно накрыть все или несколько из впускных отверстий. В одной или более версий, защитный элемент 370 накрывает менее половины впускных отверстий 115, обеспечивая прохождение достаточного воздушного потока сквозь устройство, вне зависимости от расположения пальцев пользователя. Термин "накрывать" включает перекрытие в радиальном или наружном направлении, или и то и другое.
Версия распылительного устройства 100, включающего защитный элемент 370, показана на.фиг.11. В этой версии корпус 105 распылительного устройства 100, включает основную часть 405 и съемный колпачок 410. Колпачок 410 может сниматься с основной части 405 для ввода емкости 125 в камеру 110, которая образуется, когда соединяются основная часть 405 и колпачок.
Было установлено, что надежность и(или) повторяемость вскрытия, и(или) постоянство формы может зависеть от одного или более из таких факторов, как толщина стенки, однородность толщины стенки и распределение толщины стенки в емкости 125. В вариантах осуществления настоящего изобретения емкость имеет стенку однородной толщины, составляющей примерно от 100 до 240 мкм. В вариантах осуществления нижний предел толщины стенки составляет 100, или 105, или 110, или 115, или 120, или 125, или 130, или 135, или 140, или 145, или 150, или 155, или 160 микрон. В вариантах осуществления верхний предел толщины стенки составляет 240, или 235, или 230, или 225, или 220, или 215, или 210, или 205, или 200. или 195, или 190, или 185, или 180, или 175, или 170, или 165, или 160, или 155, или 150, или 145, или 135, или 130, или 125, или 120 микрон. В вариантах осуществления используется интервал толщин стенки, в котором любой нижний предел может быть скомбинирован с любым верхним пределом, превышающим нижний предел. В вариантах осуществления используется интервал толщин стенки, в котором любой верхний предел может быть скомбинирован с любым нижним пределом, который ниже верхнего предела.
В вариантах осуществления любое раскрытое здесь цифровое значение может рассматриваться как значение середины интервала размера, где весь интервал составляет 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 25, 30, 35 или 40 микрон. Значения середины интервала, если не указано иное, являются средними значениями.
В вариантах осуществления толщина стенки составляет примерно от 130 до 155 мкм.
В вариантах осуществления используется множество капсул, в которых толщина стенки распределена так, что по меньшей мере примерно 99,7% толщин составляют примерно от 100 до 235 мкм; и(или) по меньшей мере примерно 95% толщин составляют примерно от 105 до 225 мкм; и(или) по меньшей мере примерно 90% толщин составляют примерно от 110 до 200 мкм.
Каждый из рассматриваемых здесь интервалов толщины может относиться ко всей поверхности емкости, либо может относиться только к той поверхности капсулы, которая должна протыкаться или прокалываться прокалывающим устройством, например, к стенке 175 на фиг.2.
В вариантах осуществления емкость включает капсулу, и прокалываемая поверхность может представлять собой криволинейную или куполообразную концевую поверхность, например, как показано на фиг.1-3. В вариантах осуществления, концевая поверхность может быть определена уравнением (1):
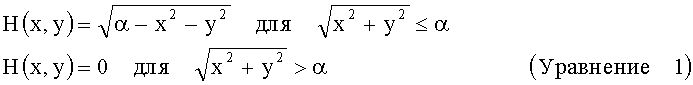
В вариантах осуществления при использовании стенок однородной толщины с указанными интервалами толщин, могут быть получены неожиданные преимущества. Например, сводятся к минимуму или исключаются случаи образования вмятины в капсуле и, соответственно, снижения или отсутствия выхода порошка и(или) рассеивания из капсулы. Прокол капсулы становится более надежным и эффективным, и сводится к минимуму необходимость создания режущей кромки специальной конструкции. При этом емкости, в соответствии с настоящим изобретением, могут надежно использоваться с режущими кромками различных конструкций и форм, например, иглы, конусы, лезвия и их комбинации. В вариантах осуществления, достигается надежное прокалывание емкости, например, капсулы, даже если прокалывающая поверхность не является совершенно гладкой или свободной от дефектов и неоднородностей. В вариантах осуществления, достигается надежное прокалывание емкости, например, капсулы, даже если прокалывающая поверхность не полностью сцентрирована с поверхностью, которая подлежит прокалыванию.
В вариантах осуществления различные варианты интервалов размеров однородных стенок, и распределения снижают повреждающее воздействие влажности на надежность и повторяемость прокалывания капсулы.
В других версиях конфигурация распылительного устройства 100 может отличаться от показанной на фиг.1А-1Д и фиг.3А-3Д. Например, размеры и форма камеры 110 могут быть выбраны так, чтобы емкость 125 устанавливалась в камеру перпендикулярно направлению ингаляции, как это описано в US 3991761. В US 3991761 также показано, что вскрывающий механизм 130 может вступать в контакт с обоими концами емкости 125. В другой версии, емкость 125 может вставляться в камеру так, что воздушные потоки протекают сквозь емкость 125, как это описано, например, в US 4338931 и в US 5619985. В другой версии, распыление лекарственного препарата может выполняться сжатым газом, втекающим сквозь впускные отверстия, как это показано, например, в US 5458135, US 5785049, US 6257233, либо газом-вытеснителем, как описано в публикации РСТ WO 00/72904 и в US 4114615. Все приведенные документы полностью включены в настоящее описание посредством ссылки.
В вариантах настоящего изобретения емкость 125 включает (представляет собой) емкость капсульного типа. Капсула может быть подходящей формы, размера и материала для размещения в ней лекарственного препарата и для обеспечения пригодного для использования состояния лекарственного препарата. Например, капсула может иметь стенку 175 (показана на фиг.2А-2Г), которая включает материал, не вступающий в побочные реакции с лекарственным препаратом. Кроме того, стенка может включать материал, обеспечивающий вскрытие капсулы для распыления лекарственного препарата. В одной версии, стенка состоит из одного или более материалов из группы, включающей желатин, целлюлозный материал, например, алкил- или арилметилцеллюлоза, гидроксиалкилметилцеллюлоза, гидроксипропилметилцеллюлоза, гидроксипропилметилцеллюлоза, смешанная с полиэтиленгликолем, гидроксипропилцеллюлоза, агар, поливиниловый спирт, поливинилацетат, их сополимеры и их комбинации. В качестве альтернативы или дополнительно, стенка капсулы может включать полимерный материал, например, поливинилхлорид (ПВХ). В качестве альтернативы или дополнительно, стенка капсулы может включать металл, например, алюминий.
В вариантах осуществления капсула может включать телескопически соединяемые секции, как описано, например, в US 4247066, полностью включенном в настоящее описание посредством ссылки. Внутри капсула может быть заполнена подходящим количеством лекарственного препарата, а размер капсулы может выбираться так, чтобы она могла помещать требуемое количество лекарственного препарата. Размеры обычно находятся в интервале от размера 5 до размера 000, при этом наружные диаметры находятся в интервале примерно от 4,91 до 9,97 мм, высота - в интервале примерно от 11,10 мм до 26,14 мм, а объем составляет примерно от 0,13 мл до 1,37 мл, соответственно. Примеры размеров капсул и соответствующих им объемов приведены ниже в таблице:
|
Подходящие капсулы производятся, например, компаниями Qualicaps Inc. в Витсетт, Сев. Каролина и Nara, Япония, и Capsugel в Гринвуд, Южн. Каролина. После заполнения верхняя часть может быть помещена на нижнюю часть, образуя капсулу, как это описано в US 4846876, в US 6357490, и в публикации РСТ WO 00/07572 от 17 февраля 2000, полностью включенных в настоящее описание посредством ссылки.
В вариантах осуществления в изобретении предлагаются система и способ распыления лекарственного препарата и введения лекарственного препарата в дыхательные пути пользователя, и, в частности, в легкие пользователя. Лекарственный препарат может включать порошковые лекарственные средства, жидкие растворы и суспензии и т.п. и может включать действующее вещество. В вариантах система и способ распыления лекарственного препарата и введения лекарственного препарата включает один или более вариантов осуществления емкости, например, описанной здесь капсулы.
Активно действующий компонент, описанный в настоящем изобретении, представляет собой агент, лекарственное средство, сочетание лекарственных средств, химическое соединение или смесь химических соединений, которые оказывают фармакологическое, обычно благотворное, влияние. Сюда относятся пищевые продукты, пищевые добавки, питательные вещества, лекарственные средства, вакцины, витамины и другие благотворно влияющие вещества. При использовании в настоящем раскрытии изобретения, эти термины далее включают любой физиологически или фармакологически активно действующий компонент, обеспечивающий локальное воздействие или общее воздействие на организм пациента. Активно действующий компонент для включения в фармацевтический состав по настоящему изобретению, может быть неорганическим или органическим соединением, включая, без ограничений, лекарственные средства, воздействующие на: периферическую нервную систему, адренергические рецепторы, холинергические рецепторы, скелетные мышцы, сердечно-сосудистую систему, гладкие мышцы, систему кровообращения, синоптические локализации, атриовентрикулярные локализации нейроэффектора, эндокринную и гормональную системы, иммунную систему, репродуктивную систему, костную систему, легочный круг кровообращения, системы физиологически активных веществ, пищеварительную и выделительную системы, систему образования гистамина и центральную нервную систему. Приемлемые активно действующие компоненты могут быть выбраны, например, из снотворных средств, успокоительных средств, антидепрессантов, транквилизаторов, лекарственных препаратов, воздействующих на органы дыхания, противосудорожных препаратов, мышечных релаксантов, средств против дрожательного паралича (антагонистов дофаминовых рецепторов), анальгетиков, противовоспалительных средств, успокоительных (анксиолитических) средств, средств, подавляющих аппетит, средств против мигрени, средств для мышечных сокращений, противоинфекционных средств (антибиотиков, антивирусных средств, противогрибковых средств, вакцин), противоартритных препаратов, противомалярийных средств, противорвотных средств, противоэпилептических средств, бронходилататоров, цитокинов, стимуляторов роста, противоопухолевых препаратов, антитромботических препаратов, противогипертонических средств, сердечно-сосудистых средств, антиаритмических препаратов, антиоксидантов, противоастматических средств, гормональных средств, включая противозачаточные средства, симпатомиметических средств, мочегонных средств, липид-регулирующих средств, антиандрогенных веществ, антипаразитарных средств, антикоагулянтов, относящихся к опухолям и противоопухолевых средств, гипогликемических средств, питательных веществ и добавок, добавок, способствующих росту, противоэнтеритных средств, вакцин, антител, диагностических и контрастных веществ. Активно действующий компонент может быть введен ингаляцией, может иметь локальное или общее воздействие на организм пациента.
Активно действующий компонент может относиться к одной из нескольких структурных групп, включая по меньшей мере небольшие молекулы, пептиды, полипептиды, протеины, полисахариды, стероиды, способные к физиологическим воздействиям протеины, нуклеотиды, олигонуклеотиды, полинуклиотиды, жиры, электролиты и т.п.
Примеры активно действующих компонентов, приемлемых для использования в настоящем изобретении, включают, но не ограничиваются одним или несколькими такими активно действующими компонентами, как кальцитонин, амфоторицин В, эритропоэтин (ЕРО), фактор VIII, фактор IX, цередаза, церезим, циклоспорин, гранулоцитарный колониестимулирующий фактор (GCSF), тромбопоэтин (ТРО), ингибитор альфа-1 протеиназы,элькатонин, гранулоцитарный-моноцитарный колониестимулирующий фактор (GMCSF), гормон роста, гормон роста человека (HGH), гормон, высвобождающий гормон роста (GHRH), гепарин, низкомолекулярный гепарин (LMWH), интерферон-альфа, интерферон-бета, интерферон-гамма, рецептор интерлейкина-1, интерлейкин-2, гибридный белок интерлейкина-2, антагонист рецептора интерлейкина-1, интерлейкин-3, интерлейкин-4, интерлейкин-6, интерлейкин-11, рилизинг-фактор лютеинизирующего гормона (LHRH), инсулин, проинсулин, аналоги инсулина (например, моноацильный инсулин, как описано в патенте US 5922675, включенном в настоящую заявку в качестве ссылки в полном объеме), амилин, С-пептид, соматостатин, аналоги соматостатина, включая октреодид, вазопрессин, фолликуло-стимулирующий гормон (FSH), инсулиноподобный фактор роста (IGF), белок, связывающий инсулиноподобный фактор роста (например, IGFBP3), инсулинтропин, колониестимулирующий фактор макрофагов (M-CSF), фактор роста нервной ткани (NGF), факторы роста соединительный ткани, фактор роста кератиноцитов (KGF), фактор роста глии (GGF), фактор некроза опухолей (TNF), фактор роста эндотелия сосудов, паратиреоидный гормон (РТН), глюкагоноподобный пептид-тимозин альфа 1, ингибитор IIb/IIIa, альфа-1 антитрипсин, соединения фосфодиэстеразы (PDE), ингибиторы VLA-4, бифосфонаты, антитело респираторно-синцитиального вируса, фактор трансмембранного регулятора муковисцидоза (CFTR), дезоксирибонуклеаза (DNase), бактерицидный белок, увеличивающий проницаемость клеточной мембраны (BPI), антитело цитомегаловируса (anti-CMV), 13-цис ретиноевая кислота, макролиды, например, эритромицин, олеандомицин, тролеандомицин, рокситромицин, кларитромицин, даверцин, азитромицин, флуритромицин, диритромицин, джозамицин, спиромицин, мидекамицин, лейкомицин, миокамицин, рокитамицин, андацитромицин, и звинолид А; фторохинолоны, например ципрофлоксацин, офлоксацин, левофлоксацин, тровафлоксацин, алатрофлоксацин, моксифлоксицин, норфлоксацин, эноксацин, грепафлоксацин, гатифлоксацин, ломефлоксацин, спарфлоксацин, темафлоксацин, перфлоксацин, амифлоксацин, флероксацин, тозуфлоксацин, прулифлоксацин, ирлоксацин, пазуфлоксацин, клинафлоксацин и ситафлоксацин; аминогликозины, например гентамицин, нетилмицин, парамеции, тобрамицин, амикацин, канамицин, неомицин и стрептомицин, ванкомицин, тейкопланин, рамполанин, мидепланин, колистин, даптомицин, грамицидин, колистиметат, полимиксины, например, полимиксин В, капреомицин, бацитрацин, пенемс; пенициллины, включая пеникллиназ-чувствительные соединения, например пенициллин G, пенициллин V, пеникллиназ-устойчивые соединения, например мецитиллин, оксациллин, клоксациллин, диклоксациллин, флоксациллин, нафциллин; активнодействующие компоненты грамотрицательных микроорганизмов, например, ампициллин, амоксициллин и гетациллин, циллин и галампициллин; антипсевдомонадные пенициллины, например карбенициллин, тикарциллин, азлоциллин, мезлоциллин и пиперациллин; цефалоспорины, например цефподоксим, цефпрозил, цефтбутен, цефтизоксим, цефтриаксон, цефалотин, цефапирин, цефалексин, цефрадрин, цефокситин, цефамандол, цефазолин, цефалоридин, цефаклор, цефадроксил, цефалоглицин, цефуроксим, цефоранид, цефотаксим, цефатризин, цефацетрил, цефепим, цефиксим, цетоницид, цефоперазон, цефотетан, цефьетазол, цефтазидим, лоракарбеф и максалактам; монобактамы, например азтреонам; и карбапенемы, например имипенем, меропенем, пентамидин изеционат, альбутерол сульфат, лидокаин, метапротеренол сульфат, беклометазон дипрепионат, триамцинолон ацетонид, будесонид ацетонид, флутиказон, ипратропий бромид, флунизолид, натрий кромолин, эрготамин, тартрат; и, если приемлемо, аналоги, агонисты, антагонисты, ингибиторы и фармацевтически приемлемые солевые формы вышеуказанных соединений. Что касается пептидов и протеинов, то настоящее изобретение охватывает синтетические, природные, гликозилированные, негликозилированные, пегилированные формы и их биологически активные фрагменты и аналоги.
Активно действующие компоненты, которые могут быть использованы по настоящему изобретению, далее включают кислоты в качестве простых молекул нуклеиновой кислоты, переносчиков, сопутствующие вирусные частицы, плазмидную дизоксирубонуклеиновую кислоту (ДНК) или плазмидную РНК, РНК-интереференцию или другие типы составляющих нуклеиновой кислоты, приемлемые для трансфекции или трансформации клеток, т.е. приемлемые для генной терапии, включая генную терапию с использованием "антисмысловых последовательностей". Далее, активно действующие компоненты могут включать живые ослабленные или уничтоженные вирусы, пригодные для использования в качестве вакцин. К прочим используемым лекарственным средствам можно отнести те, которые перечислены в Настольном Справочнике Врача (Physician's Desk Reference) (самое последние издание).
Количество активно действующего компонента в составе лекарственного препарата будет зависеть от необходимого для доставки терапевтически эффективного количества активно действующего компонента в разовой дозе для достижения желательного результата. На практике это будет значительно различаться в зависимости от конкретного агента, его активности, условий лечения, пациентов, требуемых доз и желаемого терапевтического эффекта. Состав (композиция) в общем может содержать примерно от 1 масс.% до примерно 99 масс.% активно действующего компонента, в частности от 2 масс.% до примерно 95 масс.%, предпочтительно от 5 масс.% до примерно 85 масс.%, и будет также зависеть от относительных количеств добавок, содержащихся в составе. Составы настоящего изобретения, в частности, полезны для активно действующих компонентов, доставляемых в дозах от 0,001 до 100 мг/сутки, предпочтительно от 0,01 до 75 мг/сутки, и более предпочтительно от 0,1 до 50 мг/сутки. Понятно, что более одного активно действующего компонента может быть введено в описанные препараты и, что термин действующий компонент/агент не исключает использование и двух, и более таких компонентов.
Лекарственное средство может содержать фармацевтически приемлемое вспомогательное вещество (эксципиент) или носитель, которые могут доставляться в легкие без существенного неблагоприятного токсического эффекта для пользователя, в частности, для его легких. В дополнение к активно действующим компонентам, лекарственное средство может, при необходимости, включать одну или несколько фармацевтических эксципиентов, пригодных для легочного введения. Эти эксципиенты, если используются, то в количестве от примерно 0,01 до примерно 95 масс.%, предпочтительно от примерно 0,5 до примерно 80 масс.% и более предпочтительно от примерно 1 до примерно 60 масс.%. Предпочтительно, такие эксципиенты, в частности, служат для улучшения характеристик активно действующего компонента, например, для обеспечения более эффективной и воспроизводимой доставки этого компонента, улучшения характеристик порошка в отношении управляемости, таких как сыпучесть и консистенция, и/или облегчения производства и заполнения разовых дозируемых форм. В частности, вспомогательные материалы могут использоваться для улучшения и физической и химической стабильности активно действующего компонента, минимизируя остаточное содержание влаги и препятствующие влагопоглощению, и улучшения гранулометрического состава частиц, степени агрегации, поверхностных свойств частиц, такие как шероховатость, облегчения ингаляции и доставки частиц в легкие. Один или несколько эксципиентов могут также служить в качестве наполнителей при желании уменьшить концентрацию активно действующего компонента в составе препарата.
Фармацевтические вспомогательные вещества или добавки, полезные для используемого в настоящем изобретении лекарственного средства, могут без ограничения включать аминокислоты, пептиды, протеины, небиологические полимеры, биологические полимеры, углеводы, такие как сахара, производные сахаров, такие как альдиты, альдоновые кислоты, этерифицированные сахара и полимеры сахаров, которые могут присутствовать по одному или в комбинации. Подходящие вспомогательные вещества раскрыты в публикации WO 96/32096, содержание которой полностью включено в настоящее описание посредством ссылки. Вспомогательное вещество может иметь температуру стеклования (Tg) выше около 35°С, предпочтительно выше около 40°С, более предпочтительно выше около 45°С, наиболее предпочтительно выше около 55°С.
Примеры протеиновых вспомогательных веществ включают альбумины, такие как серумальбумин, рекомбинантный человеческий альбумин (rHA), желатин, казеин, гемоглобин и подобное. Подходящие аминокислоты, которые могут также функционировать в качестве буферов, включают аланин, глицин, аргинин, бетаин, хистидин, глютаминовую кислоту, аспарагиновую кислоту, цистеин, лизин, лейцин, изолейцин, валин, метионин, фенилаланин, аспартам, тирозин, трифтофан и подобное. Предпочтительны аминокислоты и полипептиды, функционирующие как диспергирующие агенты. Аминокислоты этой категории включают гидрофобные аминоксилоты, такие как лейцин, валин, изолейцин, трифтофан, аланин, метионин, фенилаланин, тирозин, гистидин и пролин. Диспергирующие пептидные вспомогательные вещества включают димеры, тримеры, тетрамеры и пентамеры, содержащие одну или несколько гидрофобных аминоксилотных компонентов, таких как описанные выше.
Углеводные вспомогательные вещества, подходящие для использования в настоящем изобретении, включают, например, моносахариды, такие как фруктоза, малтоза, галактоза, глюкоза, Д-манноза, сорбоза и подобное; дисахариды, такие как лактоза, сукроза, трехалоза, целлобиоза и подобное; полисахариды, такие как раффиноза, мелицитоза, мальтодекстрины, декстрины, крахмалы и подобное; и алдитолы, такие как маннитол, ксилитол, малтитол, лактитол, сорбитол ксилитола (глюцитол), сорбитол пираносила, мионозитол и подобное.
Лекарственное средство может также включать буферы или агенты, регулирующие рН, обычно соли органических кислот или основания. Представители буферов включают соли органических кислот, таких как лимонная кислота, аскорбиновая кислота, глюконовая кислота, карбоновая кислота, винная кислота, янтарная кислота, уксусная кислота или фталевая кислота, трис, гидрохлорид трометамина или фосфатные буферы.
Лекарственное средство может также включать полимерные вспомогательные вещества/добавки, например, поливинилпирролидоны, производные целлюлозы, такие как гидроксиметилцеллюлоза, гидроксиэтилцеллюлоза, гидроксипропилметилцеллюлоза, фиколлы (полимерный сахар), гидроксиэтилкрахмал, декстраты (например, циклодкстрин, такой как 2-гидрокипропил-β-циклодкстрин и 2-сульфобутилэфир-β-циклодкстрин), полиэтилен, гликоли и пектин.
Лекарственное средство может также дополнительно включать ароматизаторы, вещества, исправляющие вкус, неорганическая соли (например, хлорид натрия), антибактериальные агенты (например, бензалконий хлорид), подсластители, антиоксиданты, антистатики, поверхностно-активные вещества (например, полисорбаты, такие как "Tween 20" и "Tween 80"); эфиры сорбитанов, липиды (например, фосфолипиды, такие как лецитин и другие фосфатидилхолины, фосфатидилэтаноламины), жирные кислоты и жирные эфиры, стероиды (например, холестерол), и хелатирующие агенты (например, ЭДТК, цинк и другие подходящие катоны). Другие фармацевтические вспомогательные вещества и/или добавки, составов, используемых в настоящем изобретении, перечислены в публикациях Remington: "The Science & Practice of Pharmacy", 19 th ed., Williams & Williams, (1995), и "Physician's Desk Reference", 52 nd ed., Medical Economics, Montvale, NJ (1998), содержание которыхполностью включено в настоящее описание посредством ссылки.
"Массовый срединный диаметр" или "MMD" (от англ. mass median diameter) представляет собой меру среднего размера частицы, поскольку порошки в изобретении обычно являются полидисперсными системами (т.е., состоят из частиц с размерами, распределенными в интервале значений). Значения MMD, указанные здесь, определены осаждением центрифугированием, хотя для измерения среднего размера частиц могут быть использованы любые из достаточно большого числа распространенных способов. "Срединный массовый аэродинамический диаметр", или "MMAD" (от англ. mass median aerodynamic diameter) представляет собой меру аэродинамического размера дисперсных частиц. Аэродинамический диаметр используется для описания распыленного порошка в терминах процесса осаждения, и представляет собой диаметр сферы единичной плотности, имеющей ту же скорость осаждения, как правило, в воздухе, что и частица. Аэродинамический диаметр учитывает форму частицы, ее плотность и физический размер. В настоящем описании MMAD относится к средней точке или медиане распределения аэродинамического размера частицы распыленного порошка, определенного каскадным импактором.
В одной или более версиях порошковый препарат для использования в настоящем изобретении включает сухой порошок, размер частиц которого обеспечивает их проникновение в альвеолы легких. В одной или более версиях размер порошка соответствует массовому срединному диаметру (MMD) менее примерно 20 мкм (микрон), например, менее примерно 10 мкм, менее примерно 8 мкм, менее примерно 5 мкм, или менее примерно 3 мкм. В одной или более версиях размер порошка соответствует MMD примерно в интервале от 0,1 мкм до 12 мкм, или примерно от 1 мкм до 6 мкм, В одной или более версиях эффективность введения дозы (DDE - от англ. delivered dose efficiency) этих порошков может быть более примерно 30%, или более примерно 40%, или более примерно 50%, или более примерно 60%, или более примерно 70%, или более примерно 80%.
В одной или более версиях аэродинамический размер порошка имеет срединный массовый аэродинамический диаметр (MMAD) менее примерно 8 мкм (микрон), или менее примерно 5 мкм, или менее примерно 3 мкм, или менее примерно 1 мкм. В одной или более версиях распределение размеров аэрозольных частиц имеет срединный массовый аэродинамический диаметр (MMAD), например, примерно от 0,3 до 8 мкм, например, примерно 0,5-5 мкм, или примерно 1-4 мкм, или примерно 1,5-3 мкм. Содержание влаги в этих сухих порошках составляет менее примерно 10 масс.%, обычно менее примерно 5 масс.%, и желательно, менее 3 масс.%. Такие порошки описаны в WO 95/24183, WO 96/32149, WO 99/16419 и WO 99/16422, каждая из которых полностью включена в настоящее описание посредством ссылки.
Хотя настоящее изобретение было описано достаточно подробно в отношении некоторых его предпочтительных версий, возможны и другие версии, и специалисту, ознакомившемуся с описанием и изучившим чертежи, будут очевидны изменения, трансформации и эквиваленты показанной версии. Например, взаимодействующие компоненты могут быть обращены, или использованы в большем или меньшем числе. Кроме того, различные признаки приведенных версий могут быть скомбинированы различными способами для создания дополнительных версий настоящего изобретения. Далее, некоторые термины были использованы для ясности описания и не ограничивают изобретения. Поэтому любой пункт приложенной формулы не должен считаться ограниченным описанными здесь предпочтительными версиями, и должен включать все подобные альтернативы, трансформации и эквиваленты, охватываемые существом и областью притязаний настоящего изобретения.