Результат интеллектуальной деятельности: БЕТУЛИНСОДЕРЖАЩИЕ ЭКСТРАКТЫ ИЗ БЕРЕЗОВОЙ КОРЫ И СОСТАВ НА ИХ ОСНОВЕ
Вид РИД
Изобретение
СCЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[1] Настоящая заявка испрашивает преимущество согласно предварительной заявке США № 62/613646, поданной 4 января 2018 года, полное содержание которой настоящим включено посредством ссылки во всей ее полноте и для любых целей.
Область техники, к которой относится настоящее изобретение
[2] Настоящее изобретение относится к фармацевтическим составам, полученным из экстрактов из березовой коры.
Уровень техники настоящего изобретения
[3] Известно, что тритерпены, содержащиеся в экстрактах из березовой коры, обладают ранозаживляющими свойствами. Способы экстрагирования данных тритерпенов из березовой коры описаны в патенте США № 7482383. Такие способы предусматривают получение твердых экстрактов из березовой коры, которые можно применять в фармацевтических составах. Например, эмульсии, содержащие такие экстракты, описаны в патенте США № 7482383, а олеогели, содержащие такие экстракты, описаны в патентах США №№ 9352041; 8828444 и 8536380.
[4] При клиническом использовании в лечении ран олеогель необходимо наносить путем прикосновения к участку кожи, требующему лечения. Нанесение прикосновением является нежелательным для лечения определенных состояний кожи (например, буллезного эпидермолиза), поскольку простое воздействие при нанесении олеогеля может привести к ухудшению состояния кожи.
[5] Следовательно, существует потребность в составах для заживления ран, содержащих твердые экстракты из березовой коры, которые можно наносить на кожу без ухудшения состояния пациента.
[6] В настоящем изобретении представлены преимущественные с клинической точки зрения составы для заживления ран (в том числе олеогели, эмульсии и пены) с улучшенными реологическими свойствами, которые позволяют преодолеть недостатки известных эмульсий и олеогелей, содержащих твердую березовую кору.
Краткое описание настоящего изобретения
[7] В настоящем изобретении представлен твердый экстракт из березовой коры, который содержит по меньшей мере приблизительно 70% по весу бетулина и один или более тритерпенов, выбранных из группы, состоящей из бетулиновой кислоты, олеаноловой кислоты, эритродиола и лупеола. Описанные в настоящем документе твердые экстракты из березовой коры можно составлять в виде олеогеля, который обладает преимущественными с клинической точки зрения реологическими свойствами.
[8] В настоящем изобретении также представлен способ получения твердого экстракта из березовой коры, который можно диспергировать в неполярном растворителе с получением преимущественного с клинической точки зрения олеогеля, который предусматривает стадии (a) приведения березовой коры в контакт с подходящим растворителем с получением экстрактного раствора, содержащего бетулин и по меньшей мере один тритерпен; (b) отделения березовой коры от экстрактного раствора; (c) охлаждения экстрактного раствора для кристаллизации части бетулина и тритерпена из раствора; (d) отделения кристаллизованного бетулина и тритерпена; (e) высушивания отделенного кристаллизованного бетулина и тритерпена с получением твердого экстракта из березовой коры. В настоящем изобретении также представлены твердые экстракты из березовой коры, полученные в соответствии с такими способами.
[9] В настоящем изобретении представлен преимущественный с клинической точки зрения олеогель, содержащий от приблизительно 1% до приблизительно 20% по весу частиц твердого экстракта из березовой коры, диспергированных в от приблизительно 80% до приблизительно 99% одной или более неполярных жидкостей, при этом при диспергировании твердых экстрактов из березовой коры в подходящей неполярной жидкости образуется олеогель. Также представлена стерильная повязка на рану, содержащая прокладку и терапевтически эффективное количество олеогеля.
[10] В настоящем изобретении представлена эмульсия, содержащая олеогель по настоящему изобретению, и дополнительно представлена пена, содержащая эмульсию по настоящему изобретению.
[11] В настоящим изобретением также представлены способы лечения раны у пациента путем местного нанесения эффективного количества олеогеля, эмульсии или пены по настоящему изобретению на по меньшей мере часть раны.
[12] В настоящем изобретении также представлены способы лечения буллезного эпидермолиза у нуждающегося в этом пациента, предусматривающие местное нанесение эффективного количества олеогеля, эмульсии или пены по настоящему изобретению на участок с буллезным эпидермолизом у пациента.
[13] В настоящем изобретении представлены твердый экстракт из березовой коры, олеогель, стерильная повязка на рану, способ получения, эмульсия, пена, контейнер под давлением, способ лечения раны и способ лечения буллезного эпидермолиза в соответствии со следующими пронумерованными вариантами осуществления:
1. Твердый экстракт из березовой коры, содержащий по меньшей мере приблизительно 70 вес. % бетулина и один или более тритерпенов, выбранных из группы, состоящей из бетулиновой кислоты, олеаноловой кислоты, эритродиола и лупеола.
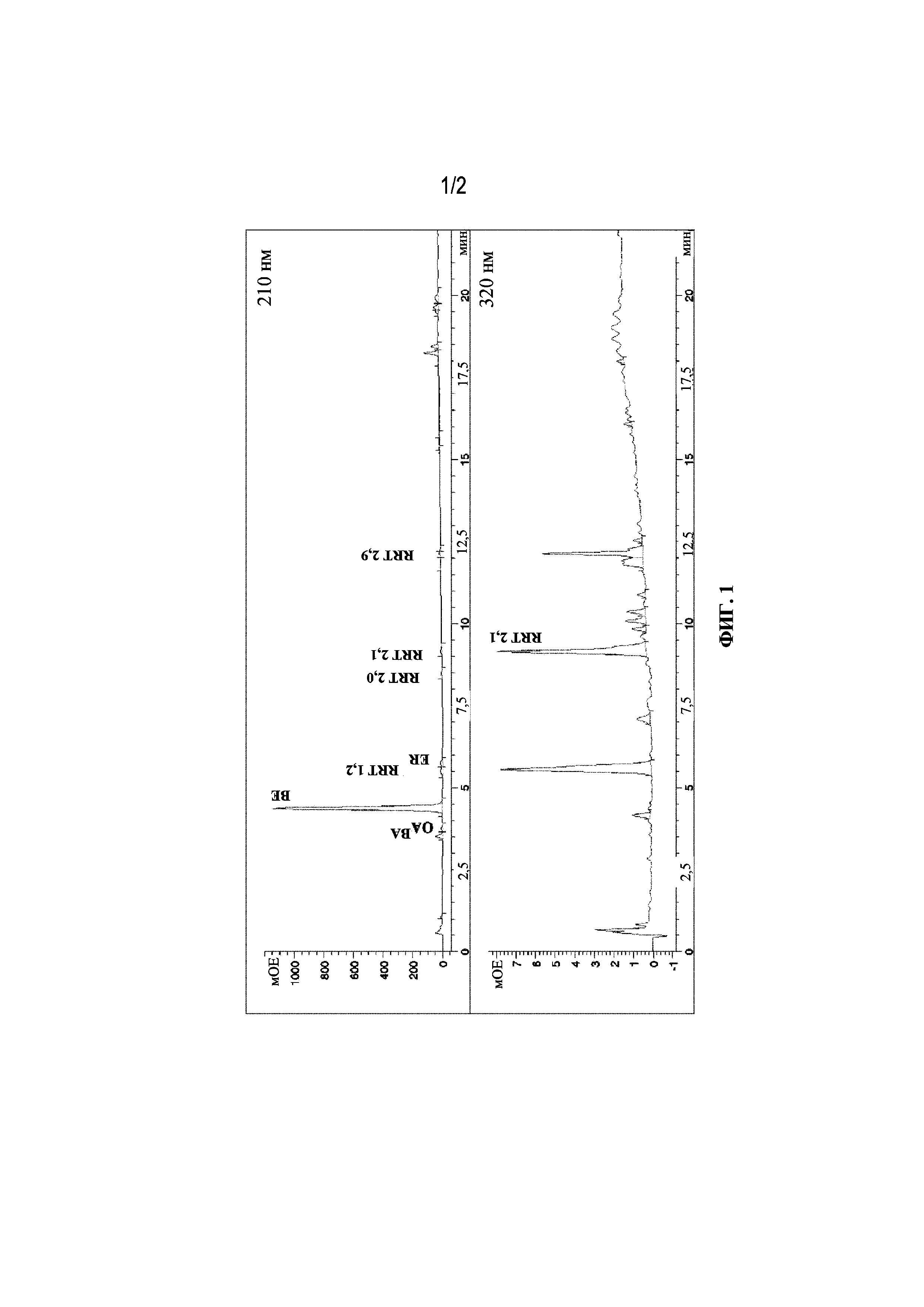
2. Твердый экстракт из березовой коры согласно варианту осуществления 1, где твердый экстракт из березы характеризуется ВЭЖХ-хроматограммой, которая по сути идентична изображенной на фигуре 1, полученной с помощью хроматографии согласно следующему ВЭЖХ-способу:
|
колонка: С18, 2,6 мкм, 150 х 2,1 мм; детектор: 210 и 320 нм;
где бетулиновая кислота характеризуется относительным временем удерживания, составляющим приблизительно 0,75-0,90, олеаноловая кислота характеризуется относительным временем удерживания, составляющим приблизительно 0,84-0,97, бетулин характеризуется относительным временем удерживания, составляющим 1,00, эритродиол характеризуется относительным временем удерживания, составляющим приблизительно 1,25-1,40, и лупеол характеризуется относительным временем удерживания, составляющим приблизительно 3,50-4,15.
3. Твердый экстракт из березовой коры согласно варианту осуществления 1 или 2, полученный с помощью способа, предусматривающего:
(a) приведение березовой коры в контакт с фармацевтически приемлемым растворителем с образованием экстрактного раствора, содержащего бетулин и один или более тритерпенов;
(b) отделение березовой коры от экстрактного раствора;
(c) охлаждение экстрактного раствора, при этом часть бетулина и один или более тритерпенов кристаллизуются из охлажденного экстрактного раствора;
(d) отделение кристаллизованного бетулина и одного или более тритерпенов от охлажденного экстрактного раствора;
(e) высушивание отделенного кристаллизованного бетулина и одного или более тритерпенов с получением твердого экстракта из березовой коры;
где после высушивания диспергирование от приблизительно 1 вес. % до приблизительно 20 вес. % высушенного твердого экстракта из березовой коры, полученного на стадии (е), в очищенном подсолнечном масле образует олеогель.
4. Твердый экстракт из березовой коры согласно варианту осуществления 3, где одна или более из стадий (а), (с) и (е) осуществляются при следующих условиях:
(i) указанное приведение в контакт на стадии (а) осуществляется при температуре от приблизительно 60°С до приблизительно 130°С;
(ii) указанное охлаждение на стадии (c) осуществляется при температуре от приблизительно -20°С до приблизительно 35°С;
(iii) указанное высушивание на стадии (e) осуществляется при температуре от приблизительно 75°С до приблизительно 95°С при давлении, составляющем менее приблизительно 70 мбар.
5. Твердый экстракт из березовой коры согласно варианту осуществления 3, где две или более из стадий (а), (с) и (е) осуществляются при следующих условиях:
(i) указанное приведение в контакт на стадии (а) осуществляется при температуре от приблизительно 60°С до приблизительно 130°С;
(ii) указанное охлаждение на стадии (c) осуществляется при температуре от приблизительно -20°С до приблизительно 35°С;
(iii) указанное высушивание на стадии (e) осуществляется при температуре от приблизительно 75°С до приблизительно 95°С при давлении, составляющем менее приблизительно 70 мбар.
6. Твердый экстракт из березовой коры согласно варианту осуществления 3, где стадии (а), (с) и (е) осуществляются при следующих условиях:
(i) указанное приведение в контакт на стадии (а) осуществляется при температуре от приблизительно 60°С до приблизительно 130°С;
(ii) указанное охлаждение на стадии (c) осуществляется при температуре от приблизительно -20°С до приблизительно 35°С;
(iii) указанное высушивание на стадии (e) осуществляется при температуре от приблизительно 75°С до приблизительно 95°С при давлении, составляющем менее приблизительно 70 мбар.
7. Твердый экстракт из березовой коры согласно любому из вариантов осуществления 3-6, где фармацевтически приемлемый растворитель представляет собой углеводород или спирт или их комбинации.
8. Твердый экстракт из березовой коры согласно любому из вариантов осуществления 3-7, где фармацевтически приемлемый растворитель представляет собой углеводород, выбранный из группы, состоящей из н-пентана, н-гексана или н-гептана.
9. Твердый экстракт из березовой коры согласно варианту осуществления 8, где фармацевтически приемлемый растворитель представляет собой н-гептан, и при этом указанное приведение в контакт осуществляется при температуре от приблизительно 60°C до приблизительно 130°C в течение приблизительно 8-12 минут.
10. Твердый экстракт из березовой коры согласно любому из вариантов осуществления 3-9, где на стадии (c) охлажденный экстракционный раствор перенасыщен в по меньшей мере приблизительно 2 раза.
11. Твердый экстракт из березовой коры согласно варианту осуществления 10, где охлажденный экстрактный раствор перенасыщен в приблизительно 5 раз.
12. Твердый экстракт из березовой коры согласно любому из вариантов осуществления 3-11, где количество остаточного экстрагента составляет не более приблизительно 0,5 вес. %.
13. Олеогель, содержащий от приблизительно 1 вес. % до приблизительно 20 вес. % частиц твердого экстракта из березовой коры согласно любому из вариантов осуществления 1-12, характеризующихся средним размером частиц, составляющим менее приблизительно 50 мкм, диспергированных в от приблизительно 80 вес. % до приблизительно 99 вес. % одной или более неполярных жидкостей.
14. Олеогель согласно варианту осуществления 13, где в олеогеле диспергированные частицы твердого экстракта из березовой коры являются единственным средством, образующим олеогель.
15. Олеогель согласно варианту осуществления 13 или 14, содержащий приблизительно 10 вес. % частиц твердого экстракта из березовой коры.
16. Олеогель согласно любому из вариантов осуществления 13-15, где неполярная жидкость содержит по меньшей мере один триглицерид.
17. Олеогель согласно любому из вариантов осуществления 13-16, где неполярная жидкость содержит по меньшей мере один углеводород с C7 или большим числом атомов углерода.
18. Олеогель согласно варианту осуществления 16, где неполярная жидкость содержит одно или более растительных масел.
19. Олеогель согласно варианту осуществления 18, где неполярная жидкость содержит подсолнечное масло.
20. Олеогель согласно любому из вариантов осуществления 13-19, где неполярная жидкость характеризуется пероксидным числом, составляющим менее приблизительно 10.
21. Олеогель согласно варианту осуществления 20, где пероксидное число составляет не более приблизительно 3.
22. Олеогель согласно любому из вариантов осуществления 13-21, где олеогель по сути не содержит частиц твердого экстракта из березовой коры с размером более приблизительно 50 мкм.
23. Олеогель согласно любому из вариантов осуществления 13-22, где олеогель является стерильным.
24. Олеогель согласно варианту осуществления 23, где олеогель стерилизован с помощью ионизирующего излучения в дозах, составляющих менее приблизительно 20 кГр.
25. Олеогель согласно варианту осуществления 24, где олеогель стерилизован с помощью ионизирующего излучения в дозах, находящихся в диапазоне от приблизительно 11 до приблизительно 20 кГр.
26. Олеогель согласно любому из вариантов осуществления 13-25, где отделение неполярной жидкости от олеогеля составляет менее приблизительно 10% после центрифугирования при 25°C в течение 30 мин при 2750 g.
27. Олеогель согласно любому из вариантов осуществления 13-26, где вязкость при 200/с олеогеля находится в диапазоне от приблизительно 0,5 до приблизительно 4,0 Па с, и показатель тиксотропности олеогеля находится в диапазоне от приблизительно 200 до приблизительно 1200 Па с, что измерено в соответствии с методом ротационной вискозиметрии, описанным в монографии 2.2.10 Европейской фармакопеи, с использованием вискозиметра типа «конус-плита».
28. Олеогель согласно любому из вариантов осуществления 13-27, где плотность олеогеля находится в диапазоне от приблизительно 300 до 3000 мН, что измерено с использованием анализатора текстуры.
29. Олеогель согласно любому из вариантов осуществления 13-28, дополнительно содержащий дезинфицирующее средство.
30. Олеогель согласно варианту осуществления 29, где дезинфицирующее средство выбрано из группы, состоящей из этанола, н-пропанола и изопропанола.
31. Олеогель согласно любому из вариантов осуществления 13-28, дополнительно содержащий липофильный антибиотик.
32. Стерильная повязка на рану, содержащая:
(а) прокладку и
(b) терапевтически эффективный слой, содержащий олеогель согласно любому из вариантов осуществления 13-31, расположенный на по меньшей мере одной поверхности прокладки.
33. Стерильная повязка на рану согласно варианту осуществления 32, где прокладка представляет собой впитывающую прокладку.
34. Способ получения твердого экстракта из березовой коры согласно варианту осуществления 1 или 2, предусматривающий:
(a) приведение березовой коры в контакт с фармацевтически приемлемым растворителем с образованием экстрактного раствора, содержащего бетулин и один или более тритерпенов;
(b) отделение березовой коры от экстрактного раствора;
(c) охлаждение экстрактного раствора, при этом часть бетулина и один или более тритерпенов кристаллизуются из охлажденного экстрактного раствора;
(d) отделение кристаллизованного бетулина и одного или более тритерпенов от охлажденного экстрактного раствора;
(e) высушивание отделенного кристаллизованного бетулина и одного или более тритерпенов с получением твердого экстракта из березовой коры;
где после высушивания диспергирование от приблизительно 1 вес. % до приблизительно 20 вес. % высушенного твердого экстракта из березовой коры, полученного на стадии (е), в очищенном подсолнечном масле образует олеогель.
35. Способ согласно варианту осуществления 34, где одну или более из стадий (а), (с) и (е) осуществляют при следующих условиях:
(i) указанное приведение в контакт на стадии (а) осуществляют при температуре от приблизительно 60°С до приблизительно 130°С;
(ii) указанное охлаждение на стадии (c) осуществляют при температуре от приблизительно -20°С до приблизительно 35°С;
(iii) указанное высушивание на стадии (e) осуществляют при температуре от приблизительно 75°С до приблизительно 95°С при давлении, составляющем менее приблизительно 70 мбар.
36. Способ согласно варианту осуществления 34, где две или более из стадий (а), (с) и (е) осуществляют при следующих условиях:
(i) указанное приведение в контакт на стадии (а) осуществляют при температуре от приблизительно 60°С до приблизительно 130°С;
(ii) указанное охлаждение на стадии (c) осуществляют при температуре от приблизительно -20°С до приблизительно 35°С;
(iii) указанное высушивание на стадии (e) осуществляют при температуре от приблизительно 75°С до приблизительно 95°С при давлении, составляющем менее приблизительно 70 мбар.
37. Способ согласно варианту осуществления 34, где стадии (а), (с) и (е) осуществляют при следующих условиях:
(i) указанное приведение в контакт на стадии (а) осуществляют при температуре от приблизительно 60°С до приблизительно 130°С;
(ii) указанное охлаждение на стадии (c) осуществляют при температуре от приблизительно -20°С до приблизительно 35°С;
(iii) указанное высушивание на стадии (e) осуществляют при температуре от приблизительно 75°С до приблизительно 95°С при давлении, составляющем менее приблизительно 70 мбар.
38. Способ согласно любому из вариантов осуществления 34-37, где фармацевтически приемлемый растворитель представляет собой углеводород, выбранный из группы, состоящей из н-пентана, н-гексана или н-гептана.
39. Способ согласно любому из вариантов осуществления 34-38, где фармацевтически приемлемый растворитель представляет собой н-гептан, и при этом указанное приведение в контакт осуществляют при температуре от приблизительно 115°C до приблизительно 130°C в течение приблизительно 8-12 минут.
40. Способ согласно любому из вариантов осуществления 34-39, где на стадии (c) охлажденный экстрактный раствор перенасыщен в по меньшей мере приблизительно 2 раза.
41. Способ согласно варианту осуществления 40, где охлажденный экстрактный раствор перенасыщен в приблизительно 5 раз.
42. Способ согласно любому из вариантов осуществления 34-41, где количество остаточного экстрагента составляет не более приблизительно 0,5 вес. %.
43. Эмульсия, содержащая твердый экстракт из березовой коры согласно любому из вариантов осуществления 1-12.
44. Эмульсия, содержащая олеогель согласно любому из вариантов осуществления 13-31.
45. Эмульсия согласно варианту осуществления 43 или 44, где указанная эмульсия представляет собой эмульсию типа «вода в масле».
46. Эмульсия согласно варианту осуществления 45, которая по сути не содержит эмульгатор.
47. Эмульсия согласно любому из вариантов осуществления 43-46, состоящая по сути из твердого экстракта из березовой коры или олеогеля, масла и воды.
48. Эмульсия согласно любому из вариантов осуществления 44-46, состоящая из олеогеля, масла и воды.
49. Эмульсия согласно любому из вариантов осуществления 43-46, дополнительно содержащая дезинфицирующее средство.
50. Эмульсия согласно варианту осуществления 49, где дезинфицирующее средство выбрано из группы, состоящей из этанола, н-пропанола и изопропанола.
51. Эмульсия согласно любому из вариантов осуществления 43-46, дополнительно содержащая липофильный антибиотик.
52. Пена, содержащая эмульсию согласно любому из вариантов осуществления 43-51.
53. Пена согласно варианту осуществления 52, дополнительно содержащая дезинфицирующее средство.
54. Пена согласно варианту осуществления 53, где дезинфицирующее средство выбрано из группы, состоящей из этанола, н-пропанола и изопропанола.
55. Пена согласно варианту осуществления 52, дополнительно содержащая липофильный антибиотик.
56. Пена согласно любому из вариантов осуществления 52-55, где межфазное поверхностное натяжение эмульсии составляет более приблизительно 4 мН/м.
57. Пена согласно любому из вариантов осуществления 52-56, где индекс вспенивания составляет более приблизительно 2.
58. Пена согласно варианту осуществления 52, где олеогель состоит из от приблизительно 5 вес. % до приблизительно 10 вес. % твердого экстракта из березовой коры, и при этом эмульсия представляет собой эмульсию типа «вода в масле», состоящую из олеогеля и от приблизительно 20 вес. % до приблизительно 30 вес. % воды.
59. Пена согласно варианту осуществления 58, где олеогель состоит из приблизительно 7 вес. % твердого экстракта из березовой коры, и при этом количество воды в эмульсии составляет приблизительно 25 вес. %.
60. Пена согласно любому из вариантов осуществления 52-56, дополнительно содержащая эмульгатор, выбранный из группы, состоящей из фосфатидилхолина, дистеарата полиглицерил-3-метилглюкозы и их комбинаций.
61. Контейнер под давлением, заполненный смесью, содержащей эмульсию согласно любому из вариантов осуществления 43-51 и фармацевтически приемлемый пропеллент, при этом эмульсия образует пену при выпускании по меньшей мере части смеси из контейнера.
62. Способ лечения раны у пациента, предусматривающий местное нанесение олеогеля согласно любому из вариантов осуществления 13-31 на по меньшей мере часть раны.
63. Олеогель согласно любому из вариантов осуществления 13-31, предназначенный для применения в способе лечения раны.
64. Способ или олеогель для применения согласно варианту осуществления 63, где рана выбрана из группы, состоящей из ожогов, хирургических повреждений кожи, поверхностных повреждений, хронических ран, пролежней, язв, обусловленных синдромом диабетической стопы, хронических трофических венозных язв, язв, обусловленных недостаточностью артериального кровообращения, ран, связанных с видами эстетического лечения кожи, ран, связанных с видами абляционного лазерного лечения кожи, ран, связанных с видами химического пилинга, ран, связанных с дермабразией, ран, вызванных нежелательными реакциями на лекарственное средство, ран, вызванных токсическим эпидермальным некролизом, ран, вызванных синдромом Лайелла, ран, вызванных синдромом Стивенса-Джонсона, и ран, вызванных лучевым дерматитом.
65. Способ лечения раны у пациента, предусматривающий местное нанесение эмульсии согласно любому из вариантов осуществления 43-51 на по меньшей мере часть раны.
66. Эмульсия согласно любому из вариантов осуществления 43-51, предназначенная для применения в способе лечения раны.
67. Способ или эмульсия для применения согласно варианту осуществления 66, где рана выбрана из группы, состоящей из ожогов, хирургических повреждений кожи, поверхностных повреждений, хронических ран, пролежней, язв, обусловленных синдромом диабетической стопы, хронических трофических венозных язв, язв, обусловленных недостаточностью артериального кровообращения, ран, связанных с видами эстетического лечения кожи, ран, связанных с видами абляционного лазерного лечения кожи, ран, связанных с видами химического пилинга, ран, связанных с дермабразией, ран, вызванных нежелательными реакциями на лекарственное средство, ран, вызванных токсическим эпидермальным некролизом, ран, вызванных синдромом Лайелла, ран, вызванных синдромом Стивенса-Джонсона, и ран, вызванных лучевым дерматитом.
68. Способ лечения раны у пациента, предусматривающий местное нанесение пены согласно любому из вариантов осуществления 52-60 на по меньшей мере часть раны.
69. Пена согласно любому из вариантов осуществления 52-60, предназначенная для применения в способе лечения раны.
70. Способ или пена для применения согласно варианту осуществления п. 69, где рана выбрана из группы, состоящей из ожогов, хирургических повреждений кожи, поверхностных повреждений, хронических ран, пролежней, язв, обусловленных синдромом диабетической стопы, хронических трофических венозных язв, язв, обусловленных недостаточностью артериального кровообращения, ран, связанных с видами эстетического лечения кожи, ран, связанных с видами абляционного лазерного лечения кожи, ран, связанных с видами химического пилинга, ран, связанных с дермабразией, ран, вызванных нежелательными реакциями на лекарственное средство, ран, вызванных токсическим эпидермальным некролизом, ран, вызванных синдромом Лайелла, ран, вызванных синдромом Стивенса-Джонсона, и ран, вызванных лучевым дерматитом.
71. Способ лечения буллезного эпидермолиза у нуждающегося в этом пациента, предусматривающий местное нанесение на участок с буллезным эпидермолизом у пациента олеогеля согласно любому из вариантов осуществления 13-31.
72. Олеогель согласно любому из вариантов осуществления 13-31, предназначенный для применения в способе лечения буллезного эпидермолиза.
73. Способ лечения буллезного эпидермолиза у нуждающегося в этом пациента, предусматривающий местное нанесение на участок с буллезным эпидермолизом у пациента эмульсии согласно любому из вариантов осуществления 43-51.
74. Эмульсия согласно любому из вариантов осуществления 43-51, предназначенная для применения в способе лечения буллезного эпидермолиза.
75. Способ лечения буллезного эпидермолиза у нуждающегося в этом пациента, предусматривающий местное нанесение на участок с буллезным эпидермолизом у пациента пены согласно любому из вариантов осуществления 52-60.
76. Пена согласно любому из вариантов осуществления 52-60, предназначенная для применения в способе лечения буллезного эпидермолиза.
Подробное описание графических материалов
[14] На фиг. 1. показана ВЭЖХ-хроматограмма, полученная для твердого экстракта из березовой коры, с регистрацией данных на 210 нм (верхняя фигура) и 320 нм (нижняя фигура). На фиг. 1 на оси х представлено время удерживания (мин), а на оси Y представлен максимум интенсивности (мОЕ - миллиотносительных единиц).
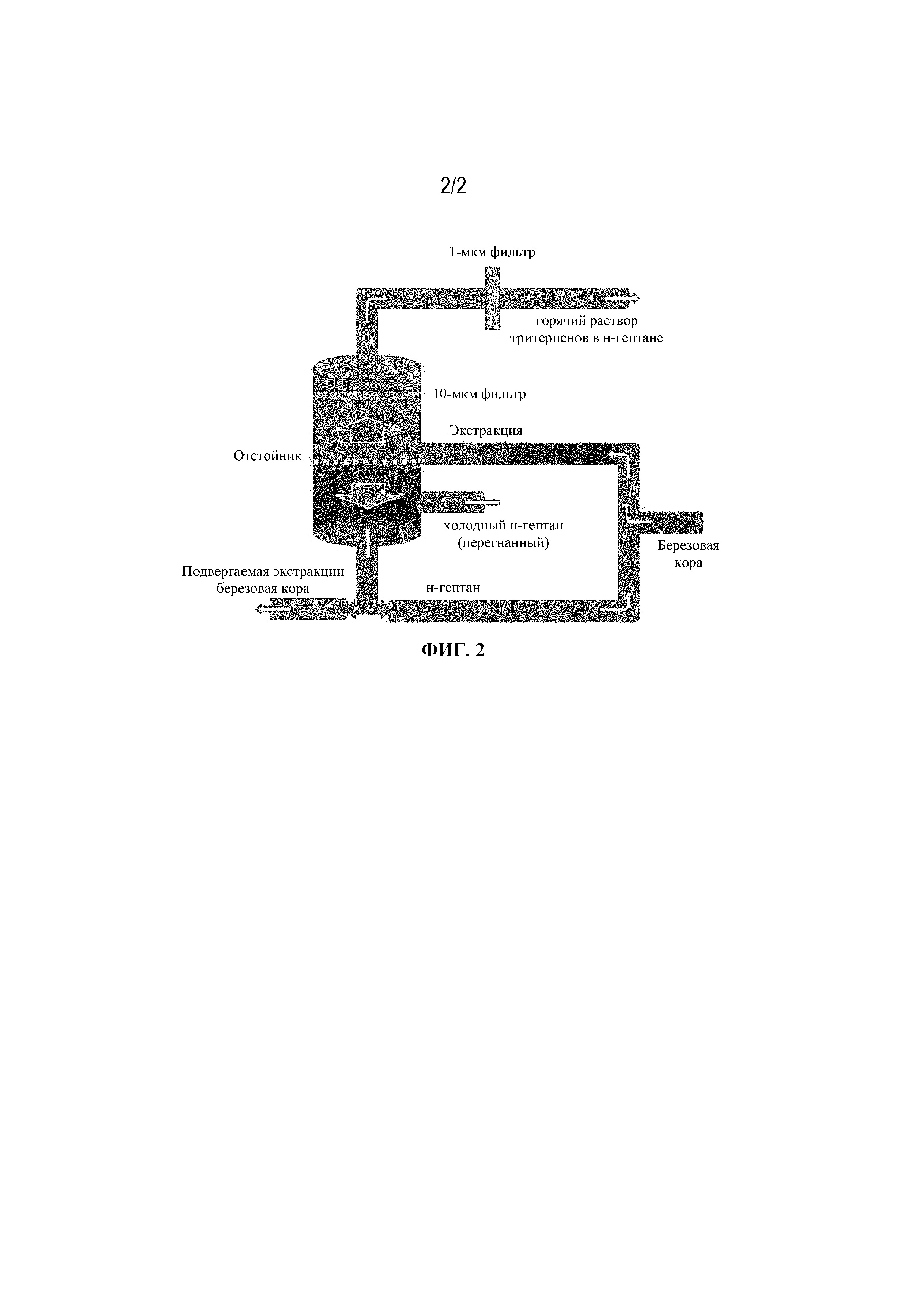
[15] На фиг. 2 проиллюстрирована непрерывная экстракция березовой коры с получением экстрактного раствора, содержащего бетулин и один или более тритерпенов.
Подробное описание настоящего изобретения
Определения
[16] Хотя считается, что последующие термины хорошо известны специалисту в данной области техники, далее приведены определения для облегчения понимания раскрываемого объекта изобретения.
[17] Следует понимать, что используемая в данном документе терминология предназначена только для описания конкретных вариантов осуществления и не предназначена для ограничения.
[18] Если не указано иное, все технические и научные термины, используемые в данном документе, имеют те же значения, которые обычно понимаются специалистом в области техники, к которой относится настоящее изобретение. Описаны предпочтительные способы, устройства и материалы, хотя при реализации на практике или тестировании настоящего изобретения можно использовать любые способы и материалы, подобные или эквивалентные тем, которые описаны в данном документе. Все источники, упомянутые в данном документе (в том числе патенты США №№ 9352041, 8828444, 8536380 и 7482383), включены посредством ссылки во всей их полноте и для любых целей.
[19] В соответствии с исторически сложившейся конвенцией о патентном праве, при использовании в данной заявке, в том числе в формуле изобретения, термины в форме единственного числа и множественного числа обозначают «одно или более». Так, например, ссылка на «носитель» включает смеси одного или более носителей, двух или более носителей и им подобные.
[20] Если не указано иное, все числа, выражающие количества ингредиентов, условий реакции и т. д., используемые в данном описании и формуле изобретения, следует понимать как модифицируемые во всех случаях термином «приблизительно». Соответственно, если не указано иное, числовые параметры, изложенные в данном описании и прилагаемой формуле настоящего изобретения, являются приблизительными значениями, которые могут варьировать в зависимости от требуемых свойств, которые должны быть получены по настоящей заявке. Обычно используемое в данном документе выражение «приблизительно», если оно относится к измеряемому значению, такому как величина веса, времени, дозы и т. д., понимают как охватывающее в одном примере отклонения ±15% или ±10%, в другом примере ±5%, в другом примере ±1% и в еще одном примере ±0,1% от указанного количества, поскольку такие отклонения являются подходящими для реализации раскрываемого способа.
[21] «Применение» предусматривает любой путь введения, такой как пероральный, подкожный, сублингвальный, трансмукозальный, парентеральный, внутривенный, внутриартериальный, трансбуккальный, сублингвальный, местный, вагинальный, ректальный, офтальмический, ушной, назальный, ингаляционный и трансдермальный. «Применение» может также предусматривать предписание или заполнение рецепта лекарственной формы, содержащей конкретное соединение. «Применение» также может предусматривать предоставление инструкций для осуществления способа, предусматривающего применение конкретного соединения или лекарственной формы, содержащей соединение.
[22] В контексте данного документа глагол «содержать», который используют в данном описании и в формуле изобретения, а также его спряжения используют в их неограничивающем смысле для обозначения того, что включены идущие за словом элементы, но не исключаются элементы, которые конкретно не упомянуты.
[23] Термин «березовая кора» означает кору деревьев белой березы. Предпочтительные варианты осуществления включают березовую кору, полученную из Betula pendula Roth и Betula pubescens Ehrh, а также гибридов обоих видов.
[24] Термин «относительное время удерживания» (или «RRT») означает соотношение времени удерживания для пика неизвестного и времени удерживания для пика бетулина, и оно рассчитывается по следующему уравнению:
RRT=RTнеизвестного/RTбетулина,
где RTнеизвестного обозначает время удерживания для пика неизвестного, а RTбетулина обозначает время удерживания для пика бетулина (210 нм), измеренное с помощью следующего ВЭЖХ-способа:
|
колонка: Phenomenex Kinetix C18, 2,6 мкм, 150×2,1 мм.
[25] Термин «по сути идентичный», используемый в данном документе, означает аналитический спектр, такой как HPLC-хроматограмма, ЯМР-спектр и т. д., который в значительной степени является сходным с эталонным спектром как по расположению пиков, так и по их интенсивности. Например, HPLC-хроматограмма «по сути идентична» эталонной хроматограмме, если положения пиков (показатели относительного времени удерживания) в ВЭЖХ-хроматограмме варьируют не более чем на ±5% от положений пиков (показателей относительного времени удерживания) в эталонной хроматограмме. В некоторых вариантах осуществления показатели относительной интенсивности пиков на HPLC-хроматограмме могут варьировать не более чем на ±10% от показателей интенсивности пиков на эталонной хроматограмме.
[26] «Терапевтически эффективное количество» означает количество активного вещества, которое при введении субъекту с целью лечения заболевания, нарушения или другого нежелательного медицинского состояния является достаточным для достижения положительного эффекта в отношении данного заболевания, нарушения или состояния. Терапевтически эффективное количество будет варьироваться в зависимости от химической идентичности и формы состава активного вещества, заболевания или состояния и его тяжести, а также возраста, веса и других соответствующих характеристик пациента, подлежащего лечению. Определение терапевтически эффективного количества данного активного вещества хорошо известно специалисту в данной области техники и обычно требует проведения простейшего эксперимента.
[27] Термин «по сути не содержит» означает, что указанный ингредиент отсутствует или присутствует лишь в незначительных количествах. В одном варианте осуществления «по сути не содержит» означает менее приблизительно 10% (например, менее приблизительно 10 вес. %). В других вариантах осуществления «по сути не содержит» означает менее приблизительно 5% (например, менее приблизительно 5 вес. %), менее приблизительно 2% (например, менее приблизительно 2 вес. %), или менее приблизительно 1% (например, менее приблизительно 1 вес. %), или приблизительно 0% (например, приблизительно 0 вес. %). Например, эмульсия, которая по сути не содержит эмульгатор, действительно не содержит какой-либо эмульгатор в значительном количестве (например, содержит менее приблизительно 10 вес. %, менее приблизительно 5 вес. %, менее приблизительно 2 вес. % или менее приблизительно 1 вес. % эмульгатора или содержит 0 вес. % эмульгатора). Аналогично олеогель, который по сути не содержит частиц твердого экстракта из березовой коры с размером более приблизительно 50 мкм, действительно не содержит в значительном количестве каких-либо частиц твердого экстракта из березовой коры с размером более приблизительно 50 мкм (например, содержит менее приблизительно 10 вес. %, менее приблизительно 5 вес. %, менее приблизительно 2 вес. % или менее приблизительно 1 вес. % частиц твердого экстракта из березовой коры с размером более приблизительно 50 мкм или содержит 0 вес. % частиц твердого экстракта из березовой коры с размером более приблизительно 50 мкм).
Твердые экстракты из березовой коры
[28] В настоящем изобретении представлены твердые экстракты из березовой коры, которые могут быть составлены в преимущественные с клинической точки зрения олеогели. Не ограничиваясь какой-либо теорией, полагают, что данные преимущества обусловлены химическим составом и морфологией частиц твердых экстрактов из березовой коры, полученных в соответствии с способами по настоящему изобретению.
[29] Твердые экстракты из березовой коры по настоящему изобретению можно охарактеризовать на основе их химического состава. В некоторых вариантах осуществления твердые экстракты из березовой коры по настоящему изобретению содержат лупановые и олеанановые тритерпены. В частности, экстракты из березовой коры могут содержать лупановые тритерпены: бетулин, лупеол и бетулиновую кислоту, а олеанановые тритерпены: эритродиол и олеаноловую кислоту.
[30] Присутствие конкретного тритерпена в экстракте из березы можно определить по значениям относительного времени удерживания, полученных с помощью ВЭЖХ-хроматографии. Для определения химического состава твердых экстрактов из березовой коры по настоящему изобретению используют следующий ВЭЖХ-способ:
|
колонка: Phenomenex Kinetix C18, 2,6 мкм, 150×2,1 мм.
[31] Колонка Phenomenex Kinetix C18 является примером колонки для ВЭЖХ, имеющей стационарную фазу из модифицированного диоксида кремния C-18 на твердой подложке из диоксида кремния со структурой ядро/оболочка (2,6 мкм HILIC 100Å), с указанными выше размерами колонки.
[32] При проведении описанного выше способа ВЭЖХ-хроматографии с твердым экстрактом из березовой коры бетулиновая кислота характеризуется относительным временем удерживания, составляющим приблизительно 0,75-0,90, олеаноловая кислота характеризуется относительным временем удерживания, составляющим приблизительно 0,84-0,97, бетулин характеризуется относительным временем удерживания, составляющим 1,00, эритродиол характеризуется относительным временем удерживания, составляющим приблизительно 1,25-1,40, и лупеол характеризуется относительным времен удержания, составляющим приблизительно 3,50-4,15.
[33] В определенных вариантах осуществления твердый экстракт березовой коры имеет ВЭЖХ-хроматограмму, практически идентичную изображенной на фигуре 1.
[34] В некоторых вариантах осуществления твердый экстракт из березовой коры содержит по меньшей мере приблизительно 50 вес. %, по меньшей мере приблизительно 55 вес. %, по меньшей мере приблизительно 60 вес. %, по меньшей мере приблизительно 65 вес. %, по меньшей мере приблизительно 70 вес. %, по меньшей мере приблизительно 75 вес. %, по меньшей мере приблизительно 80 вес. %, по меньшей мере приблизительно 85 вес. % или по меньшей мере приблизительно 90 вес. % бетулина и один или более тритерпенов. В некоторых вариантах осуществления один или более тритерпенов выбраны из группы, состоящей из бетулиновой кислоты, олеаноловой кислоты, эритродиола и лупеола.
[35] В некоторых вариантах осуществления твердый экстракт из березовой коры содержит по меньшей мере одно из следующих веществ: 3-β-каффеоилбетулин, ацетат сложного метилового эфира бетулиновой кислоты, ацетилолеаноловую кислоту, аллобетулин, бетулиновый альдегид, бетулоновую кислоту, бетулоновый альдегид, лупан-3β,20,28-триол, лупан-3β,20-диол (моногинол), олеаноловый альдегид, ситостерол, урсоловую кислоту или β-амирин.
[36] Твердый экстракт из березовой коры по настоящему изобретению можно охарактеризовать на основе размера частиц твердого экстракта из березовой коры. В некоторых вариантах осуществления средний размер частиц твердого экстракта из березовой коры составляет менее приблизительно 100 мкм, менее приблизительно 90 мкм, менее приблизительно 80 мкм, менее приблизительно 70 мкм, менее приблизительно 60 мкм, менее приблизительно 50 мкм, менее приблизительно 40 мкм, менее приблизительно 30 мкм или менее приблизительно 25 мкм.
[37] В других вариантах осуществления твердый экстракт из березовой коры по настоящему изобретению по сути не содержит частиц твердого экстракта из березовой коры с размером частиц, составляющим более приблизительно 30 мкм, более приблизительно 40 мкм, более приблизительно 50 мкм, более приблизительно 60 мкм, более приблизительно 70 мкм, более приблизительно 80 мкм, более приблизительно 90 мкм или более приблизительно 100 мкм.
[38] В предпочтительных вариантах осуществления твердые экстракты из березовой коры получены из Betula pendula Roth и Betula pubescens Ehrh, а также из гибридов обоих видов.
Способы получения твердых экстрактов из березовой коры
[39] В настоящем изобретении представлены способы получения твердых экстрактов из березовой коры, которые могут быть составлены в преимущественные с клинической точки зрения олеогели. Как правило, способы предусматривают стадии получения деревьев березы, снятия коры с указанных берез и ее обработки, приведения обработанной березовой коры в контакт с подходящим растворителем с получением экстрактного раствора, содержащего бетулин и один или более тритерпенов, и выделения и высушивания экстракта из березовой коры, содержащего бетулин и один или более тритерпенов, из экстрактного раствора. В некоторых вариантах осуществления выделенный экстракт из березовой коры имеет форму твердого вещества.
[40] В некоторых вариантах осуществления способ предусматривает: (а) приведение березовой коры в контакт с фармацевтически приемлемым растворителем с получением экстрактного раствора, содержащего бетулин и один или более тритерпенов; (b) отделение березовой коры от экстрактного раствора; (c) охлаждение экстрактного раствора, при этом часть бетулина и один или более тритерпенов кристаллизуются из охлажденного экстрактного раствора; (d) отделение кристаллизованного бетулина и одного или более тритерпенов от охлажденного экстрактного раствора; и (e) высушивание отделенного кристаллизированного бетулина и одного или более тритерпенов с получением твердого экстракта из березовой коры.
[41] В некоторых вариантах осуществления березовую кору, используемую на стадии (a), сначала обрабатывают для улучшения эффективности экстракции бетулина и одного или более тритерпенов из березовой коры. Например, в результате экспериментов было показано, что выход сухого экстракта из березовой коры является максимальным, если экстрагируемые частицы березовой коры имеют малые размеры. В определенных вариантах осуществления размер частиц березовой коры уменьшают перед стадией (а) с использованием мельницы или другого подходящего оборудования до тех пор, пока полученная березовая кора не будет проходить через сито с размером ячейки, составляющим приблизительно 1,25 мм.
[42] В некоторых вариантах осуществления березовую кору приводят в контакт с фармацевтически приемлемым растворителем при температуре, составляющей от приблизительно 50°С до приблизительно 200°С. В других вариантах осуществления температура составляет от приблизительно 60°С до приблизительно 100°С, от приблизительно 60°С до приблизительно 110°С, от приблизительно 60°С до приблизительно 120°С, от приблизительно 60°С до приблизительно 130°С, от приблизительно 70°C до приблизительно 130°С, от приблизительно 80°C до приблизительно 130°С, от приблизительно 90°C до приблизительно 130°С или от приблизительно 100°C до 150°С. В определенных других вариантах осуществления температура составляет от приблизительно 115°C до 130°С.
[43] В некоторых вариантах осуществления березовую кору приводят в контакт с фармацевтически приемлемым растворителем при давлении, составляющим от приблизительно 2 до 10 бар. В одном варианте осуществления давление составляет приблизительно 4,5 бара.
[44] Фармацевтически приемлемые растворители известны специалистам в данной области техники и включают углеводороды, спирты, кетоны, простые эфиры, сложные эфиры, сульфоксиды и т. д. Примеры фармацевтически приемлемых растворителей включают без ограничения 1-бутанол, 1-пентанол, 1-пропанол, 2-бутанол, 2-метил-1-пропанол, 2-пропанол, 3-метил-1-бутанол, уксусную кислоту, ацетон, анизол, бутилацетат, диметилсульфоксид, этанол, этилацетат, этиловый эфир, этилформиат, муравьиную кислоту, гептан, гексан, изобутилацетат, изопропилацетат, метилацетат, метилэтилкетон, метилизобутилкетон, пентан, пропилацетат, простой трет-бутилметиловый эфир, простой диизопропиловый эфир, простой метил-трет-бутиловый эфир, метилизопропилкетон и метилтетрагидрофуран.
[45] В некоторых вариантах осуществления для получения фармацевтически приемлемого растворителя смешивают два или более фармацевтически приемлемых растворителя.
[46] В некоторых вариантах осуществления березовую кору приводят в контакт с н-гептаном при температуре от приблизительно 60°С до приблизительно 130°С в течение 8-12 минут.
[47] В некоторых вариантах осуществления (a) приведение березовой коры в контакт с фармацевтически приемлемым растворителем с получением экстрактного раствора, содержащего бетулин и один или более тритерпенов, и (b) отделение березовой коры от экстрактного раствора проводят с помощью способа непрерывной экстракции (показанного на фигуре 2).
[48] В одном варианте осуществления способа непрерывной экстракции березовую кору смешивают с н-гептаном в пропорции, составляющей от приблизительно 1:14 до 1:16 (вес/объем). Смесь непрерывно экстрагируют с использованием н-гептана в качестве экстрагента при температуре, составляющей приблизительно 115-130°С, и при давлении, составляющем приблизительно 4,5 бара (азот). На нижнем конце отстойника подвергаемый экстракции слой коры промывают холодным н-гептаном, а на верхнем конце отстойника экстракт (горячий раствор тритерпенов в н-гептане) фильтруют (через 10 мкм фильтр) и перемещают через второй фильтр (через 1 мкм фильтр) на стадию кристаллизации.
[49] В некоторых вариантах осуществления охлаждение на стадии (с) проводят при температуре от приблизительно -20°С до приблизительно 35°С, от приблизительно -15°С до приблизительно 35°С, от -10°С до приблизительно 35°С, от приблизительно -5°С до приблизительно 35°С или от приблизительно 0°С до приблизительно 35°С. В других вариантах осуществления на стадии (с) охлажденный экстракционный раствор перенасыщен в по меньшей мере приблизительно 1 раз, в приблизительно 2 раза, в приблизительно 3 раза, в приблизительно 4 раза, в приблизительно 5 раз или в приблизительно 6 раз. В предпочтительных вариантах осуществления на стадии (с) охлажденный экстракционный раствор перенасыщен в приблизительно 2 раза или в приблизительно 5 раз.
[50] В некоторых вариантах осуществления стадию высушивания (е) проводят в вакууме при температуре, составляющей по меньшей мере 50°С, по меньшей мере 60°С, по меньшей мере 70°С, по меньшей мере 80°С или по меньшей мере 85°С. В определенных вариантах осуществления стадию высушивания (е) проводят при температуре, составляющей от приблизительно 65°С до приблизительно 75°С, от приблизительно 70°С до приблизительно 80°С, от приблизительно 75°С до приблизительно 85°С или от приблизительно 85°С до приблизительно 95°С.
[51] В некоторых вариантах осуществления стадию высушивания (е) проводят в вакууме при давлении, составляющем менее приблизительно 90 мбар, менее приблизительно 80 мбар, менее приблизительно 70 мбар, менее приблизительно 60 мбар или менее приблизительно 50 мбар. В определенных вариантах осуществления стадия высушивания (е) уменьшает количество фармацевтически приемлемого растворителя в сухом экстракте из березовой коры до менее приблизительно 0,5% (вес/вес).
[52] В настоящем изобретении также представлены твердые экстракты из березовой коры, полученные в соответствии с описанными выше способами.
Композиции, содержащие твердые экстракты из березовой коры
[53] В настоящем изобретении представлены преимущественные с клинической точки зрения составы для заживления ран, содержащие твердые экстракты из березовой коры. Композиции включают олеогели, эмульсии, пены и пропитанные олеогелем стерильные повязки на раны. Композиции применимы в качестве местных средств для заживления ран.
[54] Гели представляют собой тонкодисперсные системы, содержащие жидкую фазу и твердую фазу. Твердая фаза образует целостный трехмерный каркас, при этом данные две фазы проникают друг в друга. Олеогели представляют собой гидрофобные гели на основе неполярной жидкости (например, масла, воска или парафина), в которую добавляют гелеобразующее средство для достижения требуемых физических свойств.
[55] В настоящем изобретении представлены олеогели, содержащие неполярную жидкость и средство, образующее олеогель. Подходящие неполярные жидкости для применения в олеогелях по настоящему изобретению включают, например, растительные, животные или синтетические масла, воски и парафины. В некоторых вариантах осуществления неполярная жидкость представляет собой растительное масло, выбранное из группы, состоящей из касторового масла, арахисового масла, масла жожоба, подсолнечного масла, оливкового масла, масла авокадо и миндального масла. В предпочтительном варианте осуществления неполярная жидкость представляет собой подсолнечное масло.
[56] В некоторых вариантах осуществления неполярная жидкость содержит по меньшей мере один триглицерид. В определенных вариантах осуществления по меньшей мере один триглицерид представляет собой миглиол. В других вариантах осуществления неполярная жидкость содержит по меньшей мере один углеводород с C7 или большим числом атомов углерода. В определенных вариантах осуществления по меньшей мере один углеводород с С7 или большим числом атомов углерода представляет собой парафин.
[57] В некоторых вариантах осуществления неполярная жидкость, используемая в олеогеле, характеризуется пероксидным числом, составляющим менее приблизительно 15, менее приблизительно 10, менее приблизительно 5, менее приблизительно 4, менее приблизительно 3 или менее приблизительно 2. В определенных вариантах осуществления неполярная жидкость характеризуется пероксидным числом, составляющим не более приблизительно 3. Термин «пероксидное число», используемый в данном документе, означает, что пероксидное число определяют в соответствии с монографией 2.5.5. Европейской фармакопеи.
[58] В настоящем изобретении представлены способы получения олеогелей. В некоторых вариантах осуществления после высушивания твердого экстракта из березовой коры от приблизительно 1 вес. % до приблизительно 20 вес. % сухого твердого экстракта из березовой коры диспергируют в неполярной жидкости с получением олеогеля. В определенных вариантах осуществления неполярная жидкость представляет собой подсолнечное масло.
[59] В определенных вариантах осуществления олеогель является стерильным. Олеогель можно простерилизовать подходящими способами, известными специалистам в данной области техники, например, с помощью ионизирующего излучения, такого как поток электронов (EB), рентгеновское излучение или гамма-излучение. В некоторых вариантах осуществления олеогель стерилизуют с помощью ионизирующего (например, гамма) излучения в дозах, составляющих менее приблизительно 40 кГр, менее приблизительно 35 кГр, менее приблизительно 30 кГр, менее приблизительно 25 кГр, менее приблизительно 20 кГр или менее приблизительно 15 кГр. В определенных вариантах осуществления олеогель стерилизуют с помощью ионизирующего (например, гамма) излучения в дозах, которые варьируются от приблизительно 5 до приблизительно 25 кГр, от приблизительно 9 до приблизительно 25 кГр, от приблизительно 10 до приблизительно 25 кГр, от приблизительно 11 до приблизительно 25 кГр, от приблизительно 12 до приблизительно 25 кГр или от приблизительно 11 до приблизительно 20 кГр.
[60] В некоторых вариантах осуществления олеогель содержит от приблизительно 1 вес. % до приблизительно 30 вес. % твердого экстракта из березовой коры, диспергированного в от приблизительно 70 вес. % до приблизительно 99 вес. % одной или более неполярных жидкостей, при этом олеогель помимо частиц твердого экстракта из березовой коры содержит по меньшей мере одно средство, образующее олеогель. В некоторых вариантах осуществления олеогель содержит от приблизительно 1 вес. % до приблизительно 20 вес. % твердого экстракта из березовой коры, диспергированного в от приблизительно 80 вес. % до приблизительно 99 вес. % одной или более неполярных жидкостей, при этом олеогель помимо частиц твердого экстракта из березовой коры содержит по меньшей мере одно средство, образующее олеогель.
[61] В других вариантах осуществления олеогель содержит от приблизительно 1 вес. % до приблизительно 30 вес. % частиц твердого экстракта из березовой коры, диспергированных в от приблизительно 70 вес. % до приблизительно 99 вес. % одной или более неполярных жидкостей, при этом в олеогеле диспергированные частицы твердого экстракта из березовой коры являются единственным средством, образующим олеогель. В некоторых вариантах осуществления олеогель содержит от приблизительно 1 вес. % до приблизительно 20 вес. % твердого экстракта из березовой коры, диспергированного в от приблизительно 80 вес. % до приблизительно 99 вес. % одной или более неполярных жидкостей, при этом олеогель помимо частиц твердого экстракта из березовой коры содержит по меньшей мере одно средство, образующее олеогель.
[62] В определенных вариантах осуществления олеогель содержит приблизительно 5 вес. % частиц твердого экстракта из березовой коры, диспергированных в приблизительно 95 вес. % одной или более неполярных жидкостей; приблизительно 10 вес. % частиц твердого экстракта из березовой коры, диспергированных в приблизительно 90 вес. % одной или более неполярных жидкостей; приблизительно 15 вес. % частиц твердого экстракта из березовой коры, диспергированных в приблизительно 85 вес. % одной или более неполярных жидкостей; или приблизительно 20 вес. % частиц твердого экстракта из березовой коры, диспергированных в приблизительно 80 вес. % одной или более неполярных жидкостей.
[63] В вышеприведенных вариантах осуществления количество частиц твердого экстракта из березовой коры (например, от приблизительно 1 вес. % до приблизительно 20 вес. %) включает до приблизительно 0,5 вес. % частиц твердого экстракта из березовой коры, которые растворены в неполярной жидкости.
[64] Нагрузка на олеогель, которой его подвергают путем центрифугирования, дает информацию о тенденции олеогеля к отделению (или отслоению) неполярной жидкости. В некоторых вариантах осуществления олеогелей по настоящему изобретению отслоение неполярной жидкости в олеогеле составляет менее приблизительно 10%, приблизительно 9%, приблизительно 8%, приблизительно 7%, приблизительно 6%, приблизительно 5%, приблизительно 4%, приблизительно 3%, приблизительно 2%, приблизительно 1%, приблизительно 0,5% или приблизительно 0,1% после центрифугирования при 25°С в течение приблизительно 30 минут при 2750 g (например, 4400 об./мин).
[65] Олеогели по настоящему изобретению можно охарактеризовать по их вязкости. В определенных вариантах осуществления вязкость при 200/с олеогеля находится в диапазоне от приблизительно 0,5 до приблизительно 4,0 Па·с, и показатель тиксотропности олеогеля находится в диапазоне от приблизительно 200 до приблизительно 1200 Па·с, что измерено в соответствии с методом ротационной вискозиметрии, описанным в монографии 2.2.10 Европейской фармакопеи, с использованием вискозиметра типа «конус-плита».
[66] Олеогели по настоящему изобретению также можно охарактеризовать с помощью значений их плотности, которые определяют с помощью анализатора текстуры. Анализ текстуры преимущественно связан с измерением механических свойств продукта, рассчитанных по результатам теста с анализом профиля текстуры с двумя циклами. Анализаторы текстуры осуществляют данный тест путем приложения контролируемых сил к продукту и регистрации его реакции в виде силы, деформации и времени.
[67] В настоящем изобретении плотность представляет собой силу [мН], необходимую для проникновения на 1 см в образец (например, олеогель), которую измеряют с помощью устройства для тестирования материалов (анализатора текстуры) с цилиндрическим проникающим объектом (0,5 дюйма=1,27 см). Скорость проникновения составляет 0,4 мм/с.
[68] Олеогели по настоящему изобретению можно отличить от простых загущенных смесей твердых экстрактов из березовой коры на основе значений их плотности. В частности, олеогели по настоящему изобретению могут характеризоваться значением плотности, составляющим менее приблизительно 3000 мН и по меньшей мере приблизительно 250 мН, что измерено с помощью анализатора текстуры. В некоторых вариантах осуществления значение плотности олеогелей составляет приблизительно 300-2000 мН, что измерено с помощью анализатора текстуры.
[69] В настоящем изобретении также представлены способы получения олеогелей. В некоторых вариантах осуществления способ предусматривает диспергирование твердого экстракта из березовой коры в подходящей неполярной жидкости.
[70] В некоторых вариантах осуществления представлена стерильная повязка на рану, содержащая прокладку и терапевтически эффективный слой, содержащий олеогель по настоящему изобретению. В определенных вариантах осуществления прокладка представляет собой абсорбирующую прокладку. В других вариантах осуществления прокладка представляет собой любой плотный материал, подходящий для покрытия раны, включая хлопчатобумажную марлю. В некоторых вариантах осуществления терапевтически эффективный слой олеогеля наносят на одну или более поверхностей прокладки (например, на поверхность прокладки, предназначенную для непосредственного контакта с кожей или раной пациента). В других вариантах осуществления прокладка погружена в олеогель с тем, чтобы олеогель располагался на по меньшей мере части наружных поверхностей прокладки и необязательно на по меньшей мере частях внутренней части прокладки.
[71] В некоторых вариантах осуществления прокладка может содержать материал, подходящий для перевязки раны, который растворяется при применении с высвобождением олеогеля. Такие материалы могут включать абсорбируемые материалы, содержащие коллаген, альгинат и т. д.
[72] Термин «эмульсия» относится к гетерогенным системам, состоящим из двух жидкостей, которые не смешиваются друг с другом или смешиваются только в ограниченной степени, которые обычно обозначаются как фазы. В эмульсии одна из двух жидкостей диспергирована в другой жидкости в форме мелких капель.
[73] В некоторых вариантах осуществления представлена эмульсия, содержащая твердый экстракт из березовой коры по настоящему изобретению. В других вариантах осуществления представлены эмульсии, содержащие олеогели по настоящему изобретению.
[74] В некоторых вариантах осуществления эмульсии по настоящему изобретению включают эмульгатор. В определенных вариантах осуществления эмульгатор представляет собой (гидропропил)метилцеллюлозу. В определенных других вариантах осуществления эмульсии по сути не содержат эмульгатор.
[75] В случае лечения ран кожи пены могут превосходить олеогели, поскольку пены можно наносить на раны практически бесконтактным способом, тогда как для нанесения олеогеля требуется контакт. Основой для пен обычно являются эмульсии, в которых пропеллент смешан с диспергированной липидной фазой эмульсии.
[76] В настоящем изобретении представлены пены, содержащие описанную выше эмульсию, содержащую твердый экстракт из березовой коры.
[77] В определенных вариантах осуществления пена содержит олеогель, состоящий из от приблизительно 5 вес. % до приблизительно 10 вес. % твердого экстракта из березовой коры, и при этом эмульсия представляет собой эмульсию типа «вода в масле», состоящую из олеогеля и от приблизительно 20 вес. % до приблизительно 30 вес. % воды.
[78] В определенных других вариантах осуществления пена содержит олеогель, состоящий из приблизительно 7 вес. % твердого экстракта из березовой коры, и при этом эмульсия представляет собой эмульсию типа «вода в масле», состоящую из олеогеля и приблизительно 25 вес. % воды.
[79] В определенных вариантах осуществления пены по настоящему изобретению дополнительно содержат эмульгатор. Эмульгаторы хорошо известны в данной области техники в качестве веществ, которые стабилизируют эмульсии, и к ним относятся поверхностно-активные вещества. Эмульгаторы, применимые в настоящем изобретении, представляют собой эмульгаторы, которые являются приемлемыми для фармацевтического применения, в частности для контакта с кожей или раной. В некоторых вариантах осуществления подходящие эмульгаторы включают эмульгирующие воски, цетеариловый спирт, полисорбат 20, цетеарет 20 и т. д. В определенных дополнительных вариантах осуществления эмульгатор выбран из группы, состоящей из фосфатидилхолина, дистеарата полиглицерил-3-метилглюкозы и их комбинаций.
[80] В определенных вариантах осуществления олеогели, эмульсии и пены по настоящему изобретению дополнительно содержат дезинфицирующее средство. В некоторых дополнительных вариантах осуществления дезинфицирующее средство выбрано из группы, состоящей из этанола, пропан-1-ола (н-пропанола) и пропан-2-ола (изопропанола). В других вариантах осуществления олеогели, эмульсии и пены по настоящему изобретению дополнительно содержат антибиотик, в частности липофильные антибиотики, такие как фторхинолоны, макролиды, тигециклин, линкозамиды, рифампин, линезолид, тетрациклины и хлорамфеникол.
[81] В определенных вариантах пены по настоящему изобретению обладают определенными физическими свойствами. В некоторых вариантах осуществления индекс вспенивания составляет более приблизительно 2. В других вариантах осуществления эмульсия, используемая в пене, характеризуется межфазным поверхностным натяжением, составляющим более приблизительно 4 нМ/м, что измерено с использованием способов, известных в данной области техники. Используемый в данном документе термин «индекс вспенивания» обозначает соотношение плотностей указанного материала во вспененном и в невспененном состояниях. Например, индекс вспенивания для определенной пены представляет собой соотношение плотности вспененного материала и плотности материала до вспенивания.
[82] В настоящем изобретении также представлены контейнеры под давлением, заполненные эмульсией по настоящему изобретению и фармацевтически приемлемым пропеллентом, при этом эмульсия образует пену при выпускании по меньшей мере части смеси из контейнера.
Способы применения твердых экстрактов из березовой коры
[83] В настоящим изобретением также представлены способы лечения раны у пациента путем местного нанесения эффективного количества олеогеля, эмульсии или пены по настоящему изобретению на по меньшей мере часть раны.
[84] В определенных вариантах осуществления подвергаемая лечению рана выбрана из группы, состоящей из ожогов (как, например, ожогов легкой или тяжелой степени), хирургических повреждений кожи, поверхностных повреждений, хронических ран (как, например, пролежней, язв, обусловленных синдромом диабетической стопы, хронических трофических венозных язв, язв, обусловленных недостаточностью артериального кровообращения, и т. д.), ран, связанных с видами эстетического лечения кожи (как, например, связанных с видами абляционного лазерного лечения кожи, видами химического пилинга, дермабразией и т. д.), ран, вызванных нежелательными реакциями на лекарственное средство (как, например, токсический эпидермальный некролиз, синдром Лайелла, синдром Стивенса-Джонсона, лучевой дерматит, дерматит, вызванный химиотерапией, и т. д), редких заболеваний кожи (как, например, буллезный эпидермолиз, обыкновенная пузырчатка, пемфигоид, буллезный пемфигоид, листовидная пузырчатка, гангренозная пиодермия и т. д.) и их комбинаций.
[85] В настоящем изобретении также представлены способы лечения буллезного эпидермолиза у нуждающегося в этом пациента, предусматривающие местное нанесение эффективного количества олеогеля, эмульсии или пены по настоящему изобретению на участок с буллезным эпидермолизом у пациента.
ВКЛЮЧЕНИЕ ПОСРЕДСТВОМ ССЫЛКИ
[86] Все ссылки, статьи, публикации, патенты, патентные публикации и патентные заявки, упоминаемые в данном документе, включены посредством ссылки во всей своей полноте для любых целей. Тем не менее, указание любой ссылки, статьи, публикации, патента, патентной публикации и патентной заявки, упоминаемых в данном документе, не является и не должно восприниматься как подтверждение или какая-либо форма предположения о том, что они представляют собой действующий предшествующий уровень техники или являются частью общедоступных сведений в любой стране мира.