Результат интеллектуальной деятельности: ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ КОНЪЮГАТА АНТИТЕЛА К HER2-ЛЕКАРСТВЕННОГО СРЕДСТВА
Вид РИД
Изобретение
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[0001] Настоящее изобретение относится к фармацевтической композиции конъюгата антитела к Her2-лекарственного средства, который относится к области противоопухолевых лекарственных средств.
[0002]
УРОВЕНЬ ТЕХНИКИ
[0001] Направленная противоопухолевая биотерапия привлекает все больше внимания в исследовании лечения рака. Среди таких средств терапия моноклональными антителами обладает высокой специфичностью в отношении мишени и низким уровнем побочных эффектов, но имеет относительно ограниченную эффективность при использовании в отдельности. В настоящее время наиболее успешно применяемыми противоопухолевыми средствами на основе моноклональных антител являются лекарственные средства, направленно воздействующие на лимфоцитарные опухоли, такие как неходжкинскую лимфому (НХЛ), хронический лимфолейкоз (ХЛЛ) и т.д.
[0002] ErbB2, также известный как Her2/neu, является вторым представителем семейства EGFR, который играет биологическую роль, образуя гетеродимер с другими тремя представителями семейства EGFR. Ген neu, кодирующий ErbB2, был впервые выделен из нейробластомы крысы. Ген, гомологичный гену neu в соматических клетках человека, называемый Her2, расположен на длинном плече хромосомы 17 (17q21.1). ErbB2, продукт, кодируемый Her2, состоит из 1255 аминокислот и имеет молекулярную массу около 185 кДа, в положениях 720-987 которого находится активный тирозинкиназный домен. Помимо действия через сигнальные пути PI3K и MAPK, ErbB2 может снижать экспрессию циклина D и c-myc, снижая, таким образом, экспрессию ингибитора циклин-зависимой киназы (CDK) p27kipl. Активность CDK2 ингибируется, что приводит к пролиферации клеток. В ходе постоянных и глубоких исследований было обнаружено, что HER2 экспрессируется и оверэкспрессируется в различных опухолях. Таким образом, существует острая потребность в лекарственных средствах, направленно воздействующих на HER2, для эффективного лечения злокачественных опухолей. В настоящее время на рынке присутствуют три моноклональных антитела, направленно воздействующих на Her2 (см. Таблицу 1).
[0003] Таблица 1 Одобренные FDA лекарственные средства на основе моноклональных антител, направленно воздействующих на Her2
|
[0004] На основе характеристик направленного воздействия антител появилось новое поколение лекарственных средств биологического направленного действия, конъюгат антитело-лекарственное средство (ADC). ADC состоит из трех частей: антитела, цитотоксина и соединяющего их линкера. После конъюгирования моноклонального антитела с цитотоксином конъюгат антитело-лекарственное средство использует направляющее действие моноклонального антитела для специфического распознавания рецептора на поверхности раковой клетки, связывается с рецептором, после чего проникает в клетку и высвобождает цитотоксическое вещество при посредстве внутриклеточной протеазы, останавливая размножение раковых клеток и вызывая их гибель. В уровне техники для получения антитела обычно используют культуру клеток млекопитающего, и высокоочищенное антитело конъюгируют с цитотоксином, таким как MMAE, через линкер с получением конъюгата антитела-лекарственного средства (ADC). Технология конъюгирования антител с лекарственными средствами объединяет низкомолекулярный лекарственный токсин и биологический белок, при этом он обладает преимуществами их обоих, становясь терапевтическим продуктом нового поколения, который значительно повышает эффективность лекарственного средства при одновременном снижении токсических и побочных эффектов. В настоящее время на рынке присутствуют четыре препарата ADC, одобренные FDA США (см. Таблицу 2).
Таблица 2 Четыре препарата ADC, доступные на рынке
|
[0005] Как и другие лекарственные средства на основе биомакромолекул, ADC склонны к деградации, например, окислению, дезамидированию и фрагментации, или к образованию микрочастиц и агрегатов. Кроме того, сама конъюгация может снижать стабильность и изменять физико-химические свойства антитела. Например, конъюгирование DM1 с антителом к HER2 трастузумабом приводит к потере стабильности CH2 домена антитела (Ссылка 1: Physicochemical Stability of the Antibody-Drug Conjugate Trastuzumab-DM1: Changes due to Modification and Conjugation Processes. Aditya A. Wakankar et al., Bioconjugate Chemistry 2010: 21 (9), 1588-1595). Лекарство ADC обычно является гидрофобно и в целом может быть менее растворимым, чем неконъюгированное антитело, и поэтому становится в большей степени склонным к агрегации, образованию микрочастиц или поверхностной адсорбции. Для получения лекарственных средств ADC, которые являются стабильными при транспортировке и хранении, каждый вспомогательный компонент в фармацевтической композиции требуется тщательно подбирать. Вспомогательные компоненты ADC, представленные в настоящее время на рынке, показаны в Таблице 3. Поскольку типы вспомогательных компонентов, используемых в составе ADC, присутствующих в настоящее время на рынке, очень ограничены, и при этом существует множество вариантов выбора соответствующего компонента в составе, разработка комбинации вспомогательных веществ в составе ADC, которые являются стабильными во время транспортировки и хранения, включает скрининг большого количества вспомогательных компонентов, кроме того, определение подходящей концентрации требует больших усилий и времени.
Таблица 3 Вспомогательные компоненты препаратов ADC, присутствующих на рынке
|
[0006] Также по вспомогательным компонентам представленных выше четырех составов ADC можно заметить, что каждый состав уникален по используемым вспомогательным компонентам. Из-за низкой стабильности и сложной структуры лекарственных средств на основе моноклональных антител такие лекарственные средства чрезвычайно сложно производить и хранить. Из-за гетерогенной структуры антител, в частности, определяющих комплементарность областей (CDR) и Fc гликозилирования, разработку различных композиций моноклональных антител требуется проводить индивидуально в зависимости от конкретного случая (Ссылка 2: Monoclonal antibodies: formulations of marketed products and recent advances in novel delivery system, Yanan Cui et al., Drug Development and Industrial Pharmacy, Том 43, №4, стр. 519-530, 2017). Кроме того, разработка составов ADC более уникальна из-за последующего использования конъюгирования и молекулы токсина.
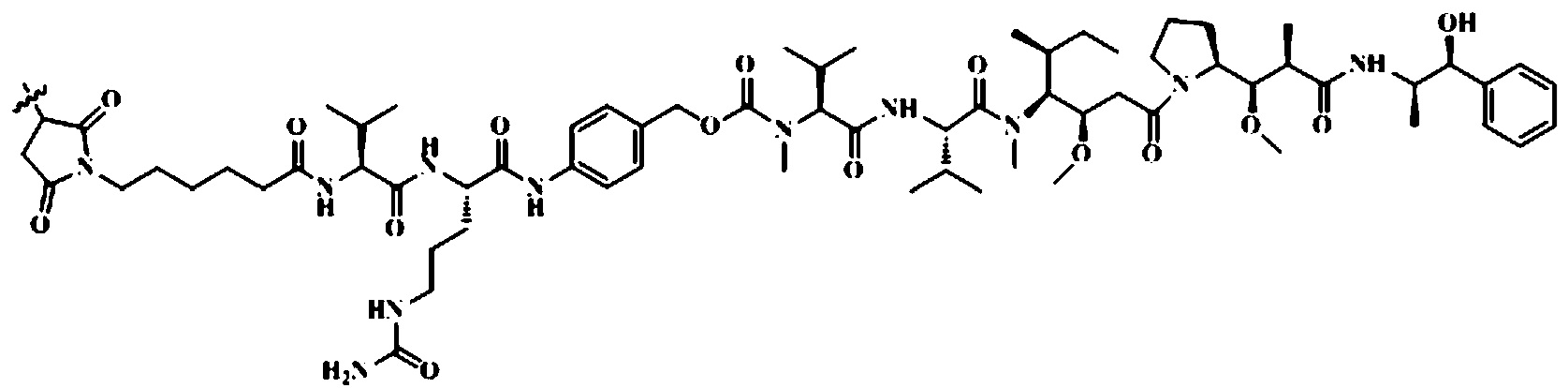
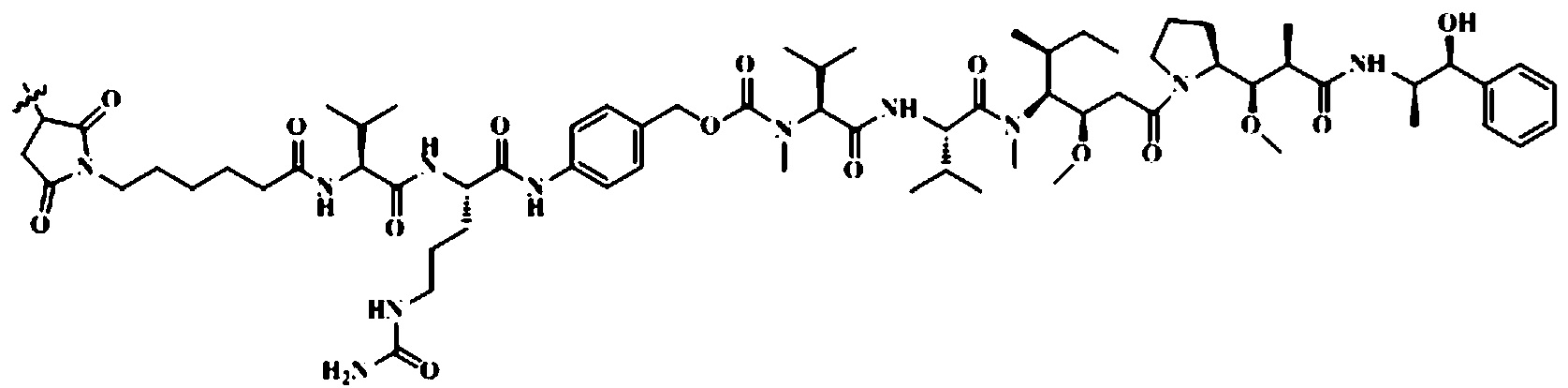
[0007] В заявке на патент (CN105008398A или WO2015074528A1) раскрыт конъюгат гуманизированного антитела RC48 с лекарственным средством, в котором гуманизированное антитело RC48 представляет собой моноклональное антитело, направленно взаимодействующее с Her2 (антитело, секретированное из клеток яичников хомяка (клетки СНО), которые были депонированы в Китайском центре Коллекции типовых культур под депозитарным номером C2013170, или антитело, полученное на его основе), а цитотоксин является монометилуристатином E (MMAE), который представляет собой производное доластатина. Линкером в этом ADC является малеимидо-капроил-валин-цитруллин-п-аминоБензилоксикарбонил (mc-VC-PAB), и конъюгат рекомбинантного гуманизированного моноклонального антитела Her2-MMAE сформирован из моноклонального антитела и MMAE, связанных линкером через цистеин. Данное лекарственное средство показало хорошие терапевтические эффекты при Her2-положительной опухоли.
[0008] Предварительные эксперименты показали, что после очистки конъюгат рекомбинантного гуманизированного моноклонального антитела против Her2 с MMAE имеет плохую растворимость в обычном буфере, при этом начинают появляться видимые нерастворимые микрочастицы, что не соответствует стандартам для инъекции. Однако если необходимо достичь клинически эффективной терапевтической дозы, концентрация белка должна быть выше 5 мг/мл. Следовательно, существует потребность в решении проблемы нерастворимых частиц при обеспечении некоторой эффективной концентрации. Кроме того, когда раствор белка лиофилизируют в вакууме, необходимо добавлять лиопротектор для защиты белка от разрушения в ходе лиофилизации и в то же время для обеспечения хорошего внешнего вида лиофилизированного порошка. Чтобы избежать медленного разложения лиофилизированного порошка белка во время длительного хранения, необходимо добавлять соответствующий стабилизатор белка. Чтобы разработать и определить подходящий стабилизатор белка, необходимо провести множество экспериментов.
[0009] Таким образом, цель настоящего изобретения состоит в разработке комбинации вспомогательных веществ для конъюгата моноклонального антитела против Her2 с MMAE посредством обширного скрининга, а также скрининга диапазона концентраций для достижения следующих технических эффектов: конъюгат моноклонального антитела против Her2 с MMAE может хорошо растворяться до и после лиофилизации, при этом нерастворимые микрочастицы, как и видимый осадок, соответствуют стандартам для введения человеку путем инъекции; кроме того, конъюгат может быть стабильным в течение длительного времени во время лиофилизации и хранения, не поддаваться полимеризации или разложению после восстановления и при этом сохранять хорошую биологическую активность.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0010] В настоящем изобретении предложена водная жидкая фармацевтическая композиция конъюгата антитела-лекарственного средства, где композиция включает конъюгат антитела-лекарственного средства, невосстанавливающий сахар, аминокислоту и солюбилизатор; где невосстанавливающий сахар выбран из маннита, сахарозы, трегалозы и их комбинации; аминокислота выбрана из гистидина, аланина, аргинина, глицина, глутаминовой кислоты и их комбинации; и солюбилизатор выбран из глицерина, Tween 80 и их комбинации.
[0011] В некоторых вариантах осуществления концентрация маннита составляет 100-300 ммоль/л, предпочтительно 190-300 ммоль/л, более предпочтительно 200-260 ммоль/л, наиболее предпочтительно 240-260 ммоль/л. Концентрация сахарозы составляет 0-100 ммоль/л, предпочтительно 40-100 ммоль/л, более предпочтительно 60-100 ммоль/л, наиболее предпочтительно 40-60 ммоль/л.
[0012] В некоторых вариантах осуществления гистидин представляет собой гидрохлорид гистидина в концентрации 0-100 ммоль/л, предпочтительно 5-50 ммоль/л, более предпочтительно 5-20 ммоль/л, наиболее предпочтительно 10 ммоль/л. Аргинин представляет собой гидрохлорид аргинина в концентрации 0-160 ммоль/л, предпочтительно 20-100 ммоль/л, более предпочтительно 30-90 ммоль/л, наиболее предпочтительно приблизительно 35 ммоль/л.
[0013] В некоторых вариантах осуществления содержание глицерина составляет 0-1%, предпочтительно 0,2-0,5% (масс./об.). Процентное содержание Tween 80 по массе составляет 0-0,02% (масс./об.).
[0014] Кроме того, антитело в конъюгате антитела-лекарственного средства представляет собой моноклональное антитело против HER2; и лекарственным средством, с которым конъюгировано антитело, является MMAE, MMAF, DM1, DM4 или их производное.
[0015] Кроме того, конъюгат антитела против HER2 с лекарственным средством представляет собой моноклональное антитело против HER2-vc-MMAE, где моноклональное антитело против HER2 соединено с MMAE через линкер vc, при этом структура, образующаяся при соединении линкера и MMAE, является следующей:
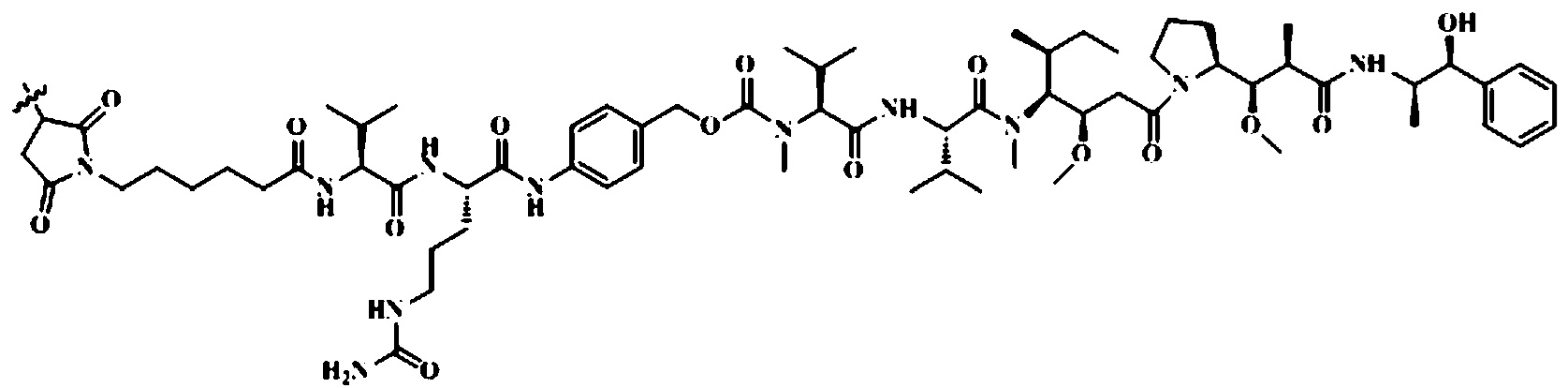
[0016] Кроме того, моноклональное антитело против HER2 включает тяжелую цепь и легкую цепь,
(i) тяжелая цепь включает CDR-области 1-3, имеющие аминокислотные последовательности, показанные в SEQ ID NO: 1, 2 и 3, соответственно; и/или
(ii) легкая цепь включает CDR-области 1-3, имеющие аминокислотные последовательности, показанные в SEQ ID NO: 4, 5 и 6, соответственно.
[0017] Кроме того, моноклональное антитело предпочтительно является химерным антителом или гуманизированным антителом.
[0018] В некоторых вариантах осуществления концентрация моноклонального антитела против HER2-vc-MMAE составляет 5-30 мг/мл.
[0019] В некоторых вариантах осуществления невосстанавливающий сахар представляет собой 240-260 ммоль/л маннита и/или 40 ммоль/л-60 ммоль/л сахарозы, аминокислота представляет собой 8-12 ммоль/л гидрохлорида гистидина, и солюбилизатор представляет собой 0-0,02% (масс./об.) Tween 80.
[0020] В некоторых вариантах осуществления, где невосстанавливающий сахар представляет собой приблизительно 260 ммоль/л маннита и приблизительно 40 ммоль/л сахарозы, аминокислота представляет собой приблизительно 10 ммоль/л гидрохлорида гистидина, концентрация конъюгата антитела-лекарственного средства составляет приблизительно 10 мг/мл, а солюбилизатор представляет собой приблизительно 0,02% (масс./об.) Tween 80.
[0021] В некоторых вариантах осуществления, где невосстанавливающий сахар представляет собой приблизительно 240 ммоль/л маннита и приблизительно 60 ммоль/л сахарозы, аминокислота представляет собой приблизительно 10 ммоль/л гидрохлорида гистидина, концентрация конъюгата антитела-лекарственного средства составляет приблизительно 10 мг/мл, а солюбилизатор представляет собой приблизительно 0,02% (масс./об.) Tween 80.
[0022] Кроме того, композиция имеет pH 4,5-7, предпочтительно 5,6-6,8, более предпочтительно 5,6-6,5, 5,6-6,4, 5,6-6,3, 6,1-6,4 или 6,1-6,3.
[0023] pH композици доводят NaOH или соляной кислотой.
[0024] В некоторых вариантах осуществления лиофилизированную фармацевтическую композицию получают при лиофилизации вышеуказанной водной жидкой фармацевтической композиции.
[0025] Кроме того, перед лиофилизацией водная жидкая фармацевтическая композиция включает приблизительно 260 ммоль/л маннита, приблизительно 40 ммоль/л сахарозы, приблизительно 10 ммоль/л гидрохлорида гистидина, приблизительно 0,02% (масс./об.) Tween 80 и приблизительно 10 мг/мл моноклонального антитела против HER2-vc-MMAE, и имеет pH 5,6-6,8.
[0026] Кроме того, перед лиофилизацией водная жидкая фармацевтическая композиция включает приблизительно 240 ммоль/л маннита, приблизительно 60 ммоль/л сахарозы, приблизительно 10 ммоль/л гидрохлорида гистидина, 0,02% Tween 80 и приблизительно 10 мг/мл моноклонального антитела против HER2-vc-MMAE, и имеет pH 5,6-6,8.
[0027] Кроме того, перед лиофилизацией невосстанавливающие сахара, содержащиеся в водной жидкой фармацевтической композиции, представляют собой маннит и сахарозу в концентрациях приблизительно 47,36 мг/мл и приблизительно 13,69 мг/мл, соответственно, и аминокислота представляет собой гидрохлорид гистидина в концентрации приблизительно 2,10 мг/мл, и солюбилизатор представляет собой Tween 80 в количестве приблизительно 0,02% (масс./об.).
[0028] Кроме того, перед лиофилизацией невосстанавливающие сахара, содержащиеся в водной жидкой фармацевтической композиции, представляют собой маннит и сахарозу в концентрациях приблизительно 43,72 мг/мл и приблизительно 20,54 мг/мл, соответственно, и аминокислота представляет собой гидрохлорид гистидина в концентрации приблизительно 2,10 мг/мл, и солюбилизатор является Tween 80 в количестве приблизительно 0,02% (масс./об.).
[0029] В настоящем изобретении также предложено применение вышеуказанных фармацевтических композиций в производстве лекарственного средства для лечения заболевания, вызванного нарушением экспрессии Her2, предпочтительно рака; более предпочтительно Her2-положительного рака; более предпочтительно рака молочной железы, рака яичника, рака желудка, уротелиального рака, гастроэзофагеального рака, рака пищевода, рака эндометрия, рака легкого или рака мочевого пузыря (Ссылка 3: Human Epidermal Growth Factor Receptor 2 (HER2) in Cancers: Overexpression and Therapeutic Implications, Nida Iqbal and Naveed Iqbal, Molecular Biology International, Том 2014, идентификатор статьи 852748; и Ссылка 4: CN201810998055.4).
[0030] В настоящем изобретении также предложен способ получения фармацевтической композиции конъюгата антитела-лекарственного средства, включающий:
(1) приготовление композиции любого из указанного выше; и
(2) оценку стабильности конъюгата антитела-лекарственного средства в композиции.
[0031] КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
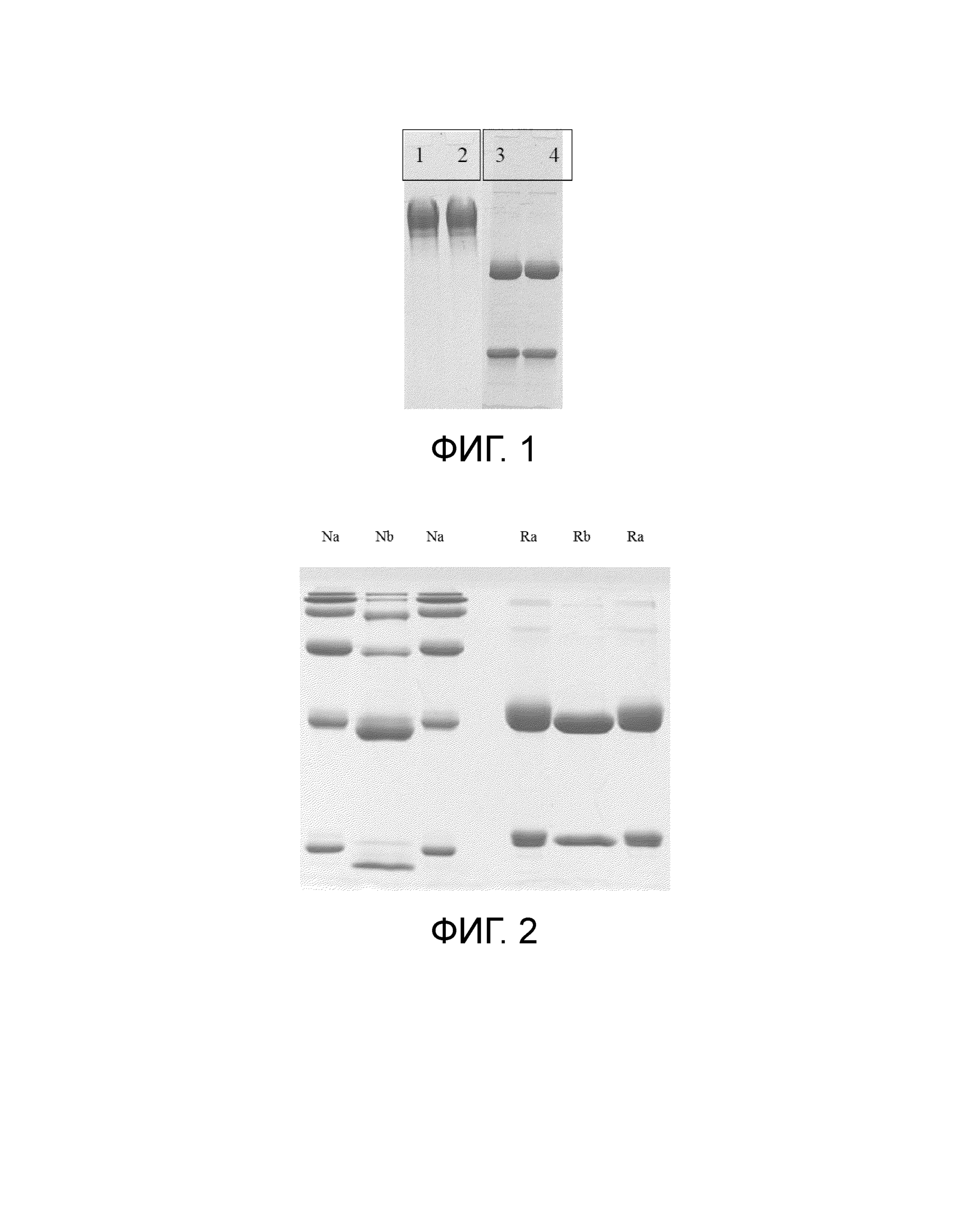
[0032] На Фигуре 1 показан электрофорез в ДСН-ПААГ голого антитела после очистки, где 1-2: невосстанавливающий электрофорез; и 3-4: восстанавливающий электрофорез. Результат на Фигуре 1 показывает, что чистота моноклонального антитела, полученного в эксперименте, удовлетворяет требованиям дальнейших экспериментов.
[0033] На Фигуре 2 показан электрофорез ADC в 10% ДСН-ПААГ после конъюгирования, где, Na: невосстанавливающий электрофорез; Nb: невосстанавливающий электрофорез после восстановления антитела TCEP; Ra: восстанавливающий электрофорез RC48-vc-MMAE; и Rb: восстанавливающий электрофорез после восстановления антитела TCEP. Результат на Фигуре 2 показывает, что чистота полученного ADC после конъюгирования удовлетворяет требованиям дальнейших экспериментов.
ПРИМЕРЫ
Пример 1 Очистка антитела
[0034] Полученное в Мышиных моноклональное антитело mRC48 и родственное гуманизированное антитело RC48 получали на основе способов, описанных в Примере заявки на патент (CN105008398A или WO2015074528A1), где RC48 включает константную область тяжелой цепи IgG1κ человека и вариабельную область тяжелой цепи RC48-VH, и константную область легкой цепи IgG1κ человека и вариабельную область легкой цепи RC48-VL. Каждый из указанных выше фрагментов амплифицировали и затем субклонировали в вектор экспрессии pcDNA3.0, соответственно. Сконструированные плазмиды трансфицировали в суспендированные клетки СНО (Invitrogen). Клетки культивировали в стандартных условиях. После израсходования питательных веществ в среде и прекращения роста клеток, культуральную смесь собирали. Затем клетки разделяли с помощью центрифугирования или фильтрации и супернатант, содержащий белок антитела, собирали и наносили на колонку для аффинной хроматографии с белком A для первой очистки. Элюированный целевой белок наносили на хроматографическую колонку, заполненную катионным наполнителем, для второй очистки. Целевой белок собирали и затем наносили на третью колонку для третьей очистки в режиме проскока целевого белка. Затем очищенный белок, который прошел исследование по различным показателям, концентрировали с помощью ультрафильтрации с получением белка с концентрацией приблизительно 20-30 мг/мл, который представлял собой стоковый раствор белка антитела, и который можно было хранить при -80°C в течение длительного времени.
[0035] Где CDR-последовательность антитела RC48 является следующей.
Таблица 4 CDR-последовательности антитела RC48
|
Пример 2 Конъюгирование антитела с MMAE
[0036] Конъюгирование гуманизированного антитела RC48 с молекулами лекарственного средства
[0037] Сначала стоковые растворы TCEP (трис-2-карбоксиэтилфосфина) и DTPA (диэтилентриаминпентауксусной кислоты) растворяли/разбавляли в буфере для конъюгирования соответственно, а затем смешивали с моноклональным антителом в соотношении 1:1 по объему (об:об=1:1), при котором молярное отношение конечной концентрации TCEP к антителу составляло 1,9:1, конечная концентрация DTPA составляла 1 ммоль/л, и проводили реакцию с перемешиванием при 25°C в течение 2 ч. Восстановительная реакция с ТСЕР имеет хорошую воспроизводимость, при этом количество свободного тиола после восстановления может достигать 3,5-4,5.
[0038] После восстановления с использованием TCEP антитело можно непосредственно подвергать последующему конъюгированию. Лекарственные средства (vc-MMAE, vc-MMAF, mc-MMAF) растворяли в ДМСО (диметилсульфоксиде) в концентрации 10 ммоль/л. Лекарственные средства медленно добавляли в молярном соотношении лекарственного средства и тиола к антителу 1,1:1 и проводили реакцию с перемешиванием при 25°C в течение 2 часов. Концентрацию свободного тиола определяли при 412 нм с помощью метода DTNB (близкая к нулю), остаточные непрореагировавшие лекарственные средства и свободные малые молекулы, такие как ДМСО, удаляли при очистке, и результат конъюгирования определяли с помощью электрофореза в ДСН-ПААГ, методами SEC и ВЭЖХ. Реакция конъюгирования имеет хорошую воспроизводимость, при этом свободный тиол может быть полностью конъюгирован со степенью конъюгирования 3,5-4,5.
Пример 3 Влияние pH на растворение и чистоту конъюгата рекомбинантного гуманизированного антитела к Her-2-MMAE (RC48-vc-MMAE)
[0039] Экспериментальная методика
[0040] 2 г конъюгата рекомбинантного гуманизированного моноклонального антитела против Her2-MMAE для инъекций подвергали ультрафильтрации и диализу в буфере, содержащем 0,1 моль/л лимонной кислоты, 0,02 моль/л тригидроксиметиламинометана, 0,02 моль/л дигидрофосфата натрия и 0,15 моль/л хлорида натрия в диализном отношении не меньше 104 раз. Полученный раствор делили на 13 равных частей и каждую часть концентрировали до концентрации белка 10 мг/мл с помощью центрифужной ультрафильтрационной пробирки с размером пор 30 кДа, а затем доводили pH до 4,2, 4,6, 5,0, 5,4, 5,6, 5,8, 6,0, 6,2, 6,4, 6,6, 6,8, 7,0 или 7,4 соляной кислотой или раствором гидроксида натрия. Наблюдали прозрачный раствор и обнаруживали изменение концентрации (результаты показаны в Таблице 5). Образцы соответственно фильтровали в стерильные флаконы для пенициллина объемом 20 мл с помощью стерильного шприцевого фильтра с размером пор мембраны 0,22 мкм в чистом боксе, используя по 3 флакона для каждого значения pH. Каждый флакон закрывали стерильной резиновой пробкой, фиксировали алюминиевым колпачком и хранили при 25°C. Образцы отбирали стерильным шприцем через 0 час, 1 день, 3 дня и 7 дней для анализа методом SEC ВЭЖХ, результаты представлены в Таблице 6.
[0041] Исследования показали, что pH белка в экспериментальных условиях оказывает огромное влияние на растворение белка. Белок образовывал осадок ниже pH 5,4 и хорошо растворялся выше pH 5,6; при этом белковые агрегаты не были повышены после 3 дней и немного повышены после 7 дней, при хранении ниже pH 6,8, постепенно повышались выше pH 7,0, и чем выше был pH, тем больше агрегатов образовывалось (см. Таблицу 5 и Таблицу 6).
Таблица 5 Прозрачность раствора и концентрация белка
|
Таблица 6 Чистота
|
Пример 4 Скрининг вспомогательных веществ
[0042] С помощью анализа большого объема информации и скрининга в 5 экспериментах на ранней стадии, сахароза, маннит, глицерин, гистидин, аргинин, полисорбат 80 (т.е. Tween 80) и подобные были предварительно идентифицированы в качестве вероятных вспомогательных веществ для дальнейшего скрининга, после чего проводили следующие исследования.
Таблица 7 Скрининг вспомогательных веществ для инъекции RC48-vc-MMAE
|
Таблица 8 Прозрачность RC48-vc-MMAE инъекции
|
[0043] Примечание: "-" означает, что количество белых точек (видимых частиц осадка) меньше 3, "+" означает, что количество белых точек (видимых частиц осадка) в пределах 3-5, и "++" означает, что количество белых точек (видимых частиц осадка) больше 5.
Таблица 9 Чистота инъекции RC48-vc-MMAE
|
[0044] Из приведенных выше результатов можно видеть, что добавление аргинина не оказывало очевидного эффекта на удаление видимого осадка белка. Тогда как добавление сахарозы, глицерина и полисорбата 80 может улучшить состояние белка. Таким образом, было определено, что соответствующее количество сахарозы может быть добавлено к препарату для защиты белка, а глицерин и полисорбат 80 могут быть добавлены для ускорения растворения белка.
Пример 5 Вакуумная лиофилизация
[0045] Стоковый раствор белка извлекали из морозильной камеры на -80°C, размораживали, аккуратно разбавляли "1× буфером для композиции" до концентрации белка 10 мг/мл и фасовали в стерильные, апирогенные стандартные флаконы для лиофилизированного пенициллина на 20 мл, по 6 мл на флакон, и затем подвергали лиофилизации в вакууме.
[0046] Условия лиофилизации
[0047] Предварительное замораживание: -45°C в течение 5 часов;
[0048] Первичная сушка: -26°C в течение 40 часов при уровне вакуума 10-15 Па; и
[0049] Вторичная сушка: 25°C в течение 10 часов, при уровне вакуума 10-15 Па.
[0050] После лиофилизации флакон укупоривали резиновой пробкой в вакууме, извлекали из лиофилизатора и фиксировали алюминиевым колпачком.
Пример 6: Скрининг составов
[0051] На основе составов, разработанных в Таблице 10, исследовали внешний вид и стабильность формирования лиофилизированных порошков композиций. После лиофилизации образцы хранили при 4°C и 37°C. Внешний вид образцов наблюдали в дни 0, 1, 3 и 7, соответственно, и отбирали соответствующие составы с лучшим внешним видом и формой. Результаты показаны в Таблице 11.
Таблица 10 Список составов буферов для инъекции RC48-vc-MMAE
|
Таблица 11 Визуальное исследование внешнего вида лиофилизированных порошков
|
[0052] Примечание: 1) "-" означает, что объем продукта уменьшается меньше чем до половины его объема до лиофилизации; "-" означает, что объем продукта уменьшается больше чем до половины его объема до лиофилизации; "+" означает, что только край немного сжимается, а объем продукта при этом остается по существу таким же, как до лиофилизации; и "++" означает, что объем совершенно не изменяется, и объем продукта совпадает с объемом до лиофилизации. 2) Установленными стандартами внешнего вида лиофилизированных порошков являются: однородный цвет, ровные и плотные поры, а также объем и форма до и после лиофилизации, которые по существу не изменяются, демонстрируя цельную или губчатую структуру. Из Таблицы 11 можно видеть, что композиция, содержащая глицерин в своем составе, показала небольшую усадку после помещения на 37°C на один день и показала очевидную усадку и схлопывание после помещения на 37°C на семь дней. Таким образом, глицерин был исключен в качестве вспомогательного вещества для композиции ADC.
Пример 7 Определение состава и анализ стабильности лиофилизированных порошков
[0053] Формулы B7-B12 исключали после контроля внешнего вида лиофилизированных порошков. Вспомогательные вещества составов B1-B6 также проверяли путем контроля на влагосодержание, видимый осадок, нерастворимые микрочастицы и стабильность.
[0054] Лиофилизированные порошки каждого состава хранили при 37°C, 25°C и 4°C, а отбирали пробы в разное время и подвергали анализам ДСН-ПААГЭ, обращенно-фазовой ВЭЖХ, анализу связывания лиганда, биологической активности, влагосодержания, внешнего вида, значения pH, наличия видимого осадка, нерастворимых микрочастиц и т.п.
Таблицы 12 Визуальное исследование внешнего вида лиофилизированных порошков
|
[0055] Примечание: "-" означает, что объем продукта уменьшается меньше чем до половины его объема до лиофилизации; "-" означает, что объем продукта уменьшается больше чем до половины его объема до лиофилизации; "+" означает, что только край немного сжимается, а объем остается по существу таким же, как до лиофилизации; и "++" означает, что сжатие вообще отсутствует, а объем продукта совпадает с объемом до лиофилизации.
[0056] Из Таблицы 12 можно увидеть, что внешний вид лиофилизированных порошков всех составов B1-B6 удовлетворяет требованиям стандарта.
[0057] Три образца были отобраны из каждого состава и исследованы на влагосодержание согласно установленному методу. Среднее значение влагосодержания было вычислено, результаты показаны в Таблице 12.
Таблица 12 Влагосодержание лиофилизированных порошков
|
[0058] Влагосодержание всех формул B1, B2, B3, B4, B5 и B6 составляло меньше 3%, что соответствовало установленному значению.
[0059] По пять образцов каждого состава выбирали случайным образом и исследовали наличие видимого осадка после повторного растворения образца согласно установленному методу. Затем выбирали три из пяти образцов каждого состава и измеряли содержание нерастворимых микрочастиц согласно установленному методу. Результаты показаны в Таблице 13.
Таблица 13 Видимый осадок и нерастворимые микрочастицы после повторного растворения лиофилизированных порошков
|
[0060] На основе результатов присутствия видимого осадка и нерастворимых микрочастиц можно видеть, что составы B1, B3 и B5 не удовлетворяли требованиям и поэтому были исключены.
Таблица 14 Результаты анализа стабильности после хранения при 37°C в течение 1 месяца
|
Таблица 15 Результаты анализа стабильности после хранения при 25°C в течение 3 месяцев
|
Таблица 16 Результаты анализа стабильности после хранения при 4°C в течение 6 месяцев
|
Примечание: стандарт внешнего вида: "-" означает, что объем продукта уменьшается меньше чем до половины его объема до лиофилизации; "-" означает, что объем продукта уменьшается больше чем до половины его объема до лиофилизации; "+" означает, что только край немного сжимается, а объем продукта остается по существу таким же, как до лиофилизации; и "++" означает, что сжатие вообще отсутствует, а объем продукта совпадает с объемом до лиофилизации.
[0061] Из приведенных выше результатов видно, что продукты составов B2 и B4 имеют лучшую стабильность при различных температурах (4°C, 25°C, 37°C), тогда как продукт состава B6 содержит много нерастворимых частиц, и поэтому был исключен. Из приведенных выше тестов видно, что лиофилизированные порошки формул B2 и B4 обладают превосходными характеристиками с точки зрения внешнего вида, влагосодержания, видимых осадков и нерастворимых микрочастиц после повторного растворения лиофилизированного порошка, и стабильности.
[0062] На основании приведенных выше экспериментальных данных можно увидеть, что выбор конкретных вспомогательных веществ из класса таких соединений, как невосстанавливающие сахара, аминокислоты и солюбилизатор, оказывает непредсказуемое влияние на готовую композицию. В случае конъюгата моноклонального антитела к Her2-лекарственного средства согласно настоящему изобретению необходимо провести большое количество экспериментов для проверки различных свойств, чтобы в итоге получить хорошую комбинацию компонентов. Например, добавление аргинина не оказывает очевидного влияния на устранение видимых осадков белка, а добавление сахарозы, глицерина и полисорбата 80 может снизить агрегацию белка. Однако добавление глицерина сделает лиофилизированный продукт склонным к явной усадке и ухудшению внешнего вида восстановленного водного раствора после восстановления. Кроме того, слишком высокая концентрация сахарозы или слишком низкая концентрация маннозы приведет к увеличению содержания нерастворимого вещества после восстановления. Специалистам в данной области будет сложно спрогнозировать эти результаты до проведения соответствующих исследований. Кроме того, поскольку композиция ADC включает комбинированное применение множества вспомогательных веществ, исследований долговременной стабильности и других факторов, это довольно сильно осложняет разработку композиции ADC. Путем большого количества экспериментов авторы изобретения определили комбинацию композиции Her2 ADC с превосходными характеристиками во всех отношениях. Конъюгат моноклонального антитела против Her2-MMAE может хорошо растворяться до и после лиофилизации, и при этом содержание нерастворимых микрочастиц и видимых осадков соответствует стандартам для инъекции человеку; в то же время конъюгат может оставаться стабильным в течение длительного времени во время лиофилизации и хранения, в особенности, он сохраняет хорошую стабильность после длительного хранения при высокой температуре 25°C или 37°C. Кроме того, композиция ADC не поддается полимеризации или разложению после восстановления и сохраняет хорошую биологическую активность.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Rongchang Biopharmaceutical (Yantai) Co., Ltd.
<120> ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ КОНЪЮГАТА АНТИТЕЛА
К HER2-ЛЕКАРСТВЕННОГО СРЕДСТВА
<130> Unitalen 0413
<150> CN 201910231203.4
<151> 2019-03-26
<160> 6
<170> PatentIn version 3.5
<210> 1
<211> 5
<212> БЕЛОК
<213> Mus musculus
<400> 1
Asp Tyr Tyr Ile His
1 5
<210> 2
<211> 17
<212> БЕЛОК
<213> Mus musculus
<400> 2
Arg Val Asn Pro Asp His Gly Asp Ser Tyr Tyr Asn Gln Lys Phe Lys
1 5 10 15
Asp
<210> 3
<211> 9
<212> БЕЛОК
<213> Mus musculus
<400> 3
Ala Arg Asn Tyr Leu Phe Asp His Trp
1 5
<210> 4
<211> 11
<212> БЕЛОК
<213> Mus musculus
<400> 4
Lys Ala Ser Gln Asp Val Gly Thr Ala Val Ala
1 5 10
<210> 5
<211> 7
<212> БЕЛОК
<213> Mus musculus
<400> 5
Trp Ala Ser Ile Arg His Thr
1 5
<210> 6
<211> 7
<212> БЕЛОК
<213> Mus musculus
<400> 6
His Gln Phe Ala Thr Tyr Thr
1 5
<---