Результат интеллектуальной деятельности: АНТИ-TIGIT АНТИГЕНСВЯЗЫВАЮЩИЕ БЕЛКИ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ
Вид РИД
Изобретение
[0001] Данная заявка заявляет приоритет по предварительной заявке США №62/235990, поданной 1 октября 2015 года, которая тем самым включена в данный документ в полном объеме посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
[0002] Согласно настоящему изобретению предложены антиген-связывающие белки (АВР) со специфичностью связывания с Т-клеточным иммунорецептором с доменами Ig и ITIM (TIGIT), и композиции, содержащие такие АВР, включая фармацевтические композиции, диагностические композиции и наборы. Также предложены способы получения TIGIT АВР, и способы применения TIGIT АВР, например, в терапевтических целях, в диагностических целях и в исследовательских целях.
УРОВЕНЬ ТЕХНИКИ
[0003] TIGIT был идентифицирован как ко-ингибирующий рецептор, который ограничивает реакцию Т-лимфоцитов на рак и хроническую инфекцию. См. Grogan et al., J. Immunol., 2014, 192: (Дополнение 1) 203.15., включен в данный документ посредством ссылки в полном объеме. Показано, что блокировка TIGIT способствует усилению эффекторной функции CD8+ Т-лимфоцитов и улучшению вирусного клиренса и опухолевого отторжения. См. Id.
[0004] Таким образом, существует потребность в терапевтических средствах, которые могут антагонизировать TIGIT. Согласно настоящему изобретению предложены АВР, которые удовлетворяют эту потребность.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0005] Согласно настоящему изобретению предложены АВР, которые специфически связывают TIGIT, и способы применения таких АВР.
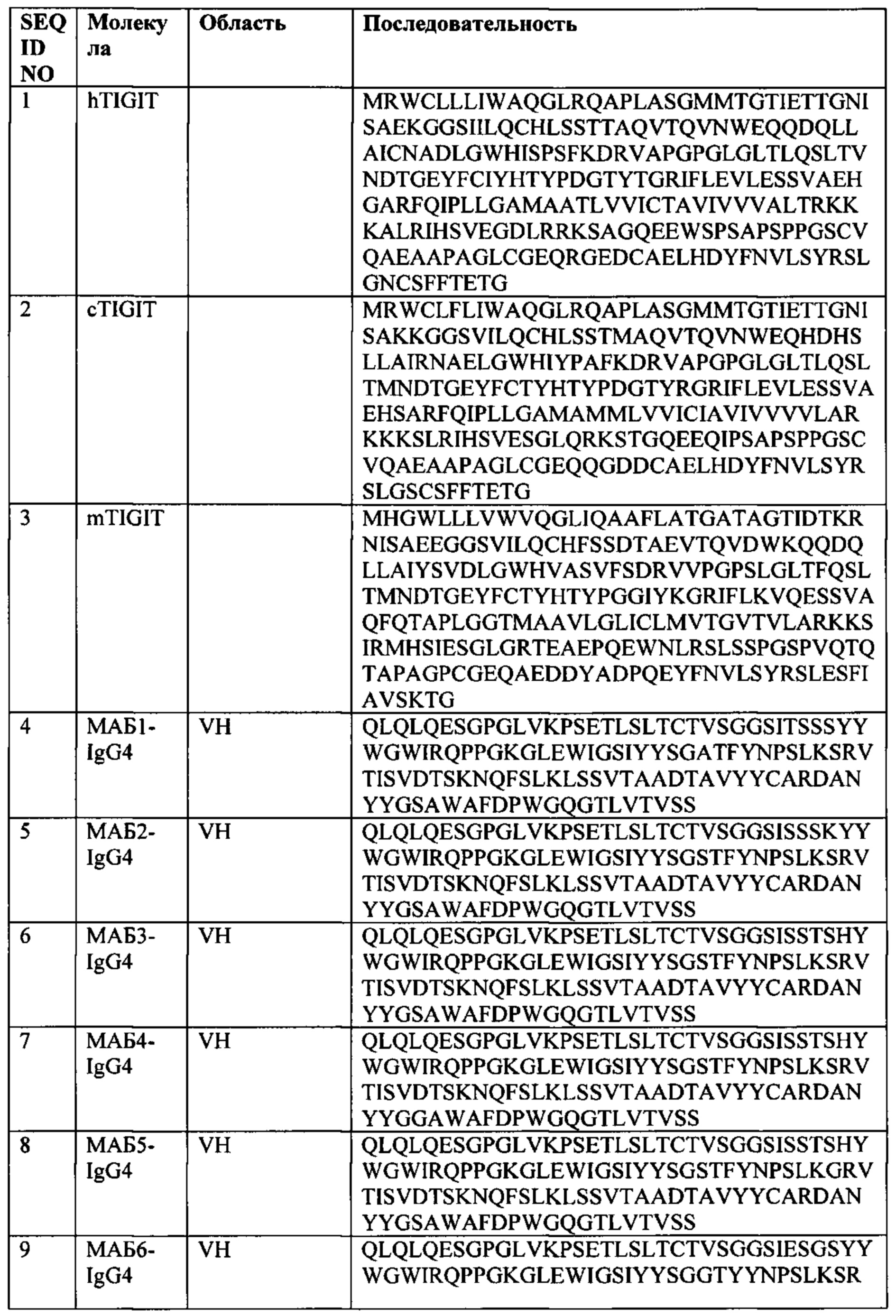
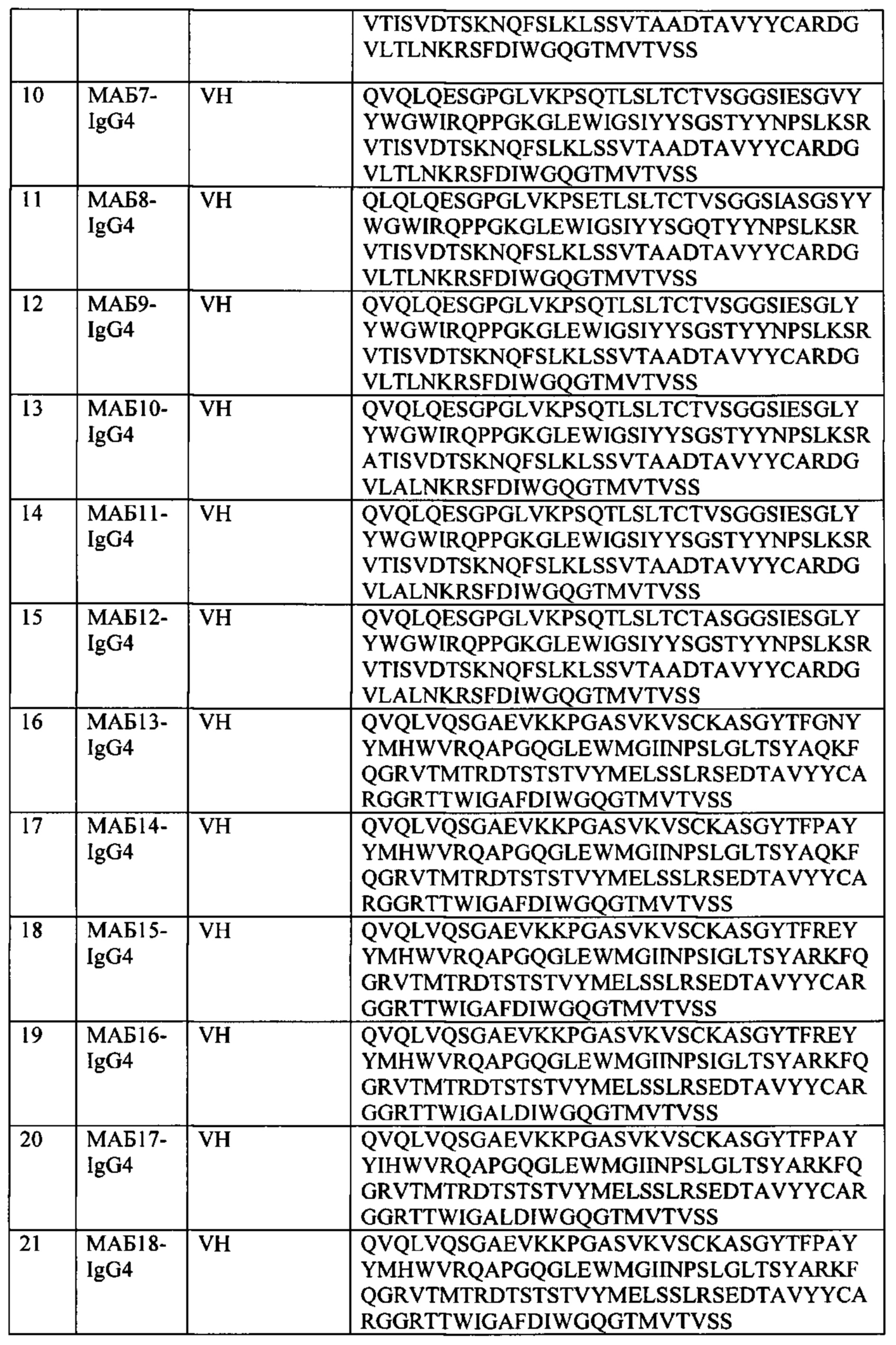
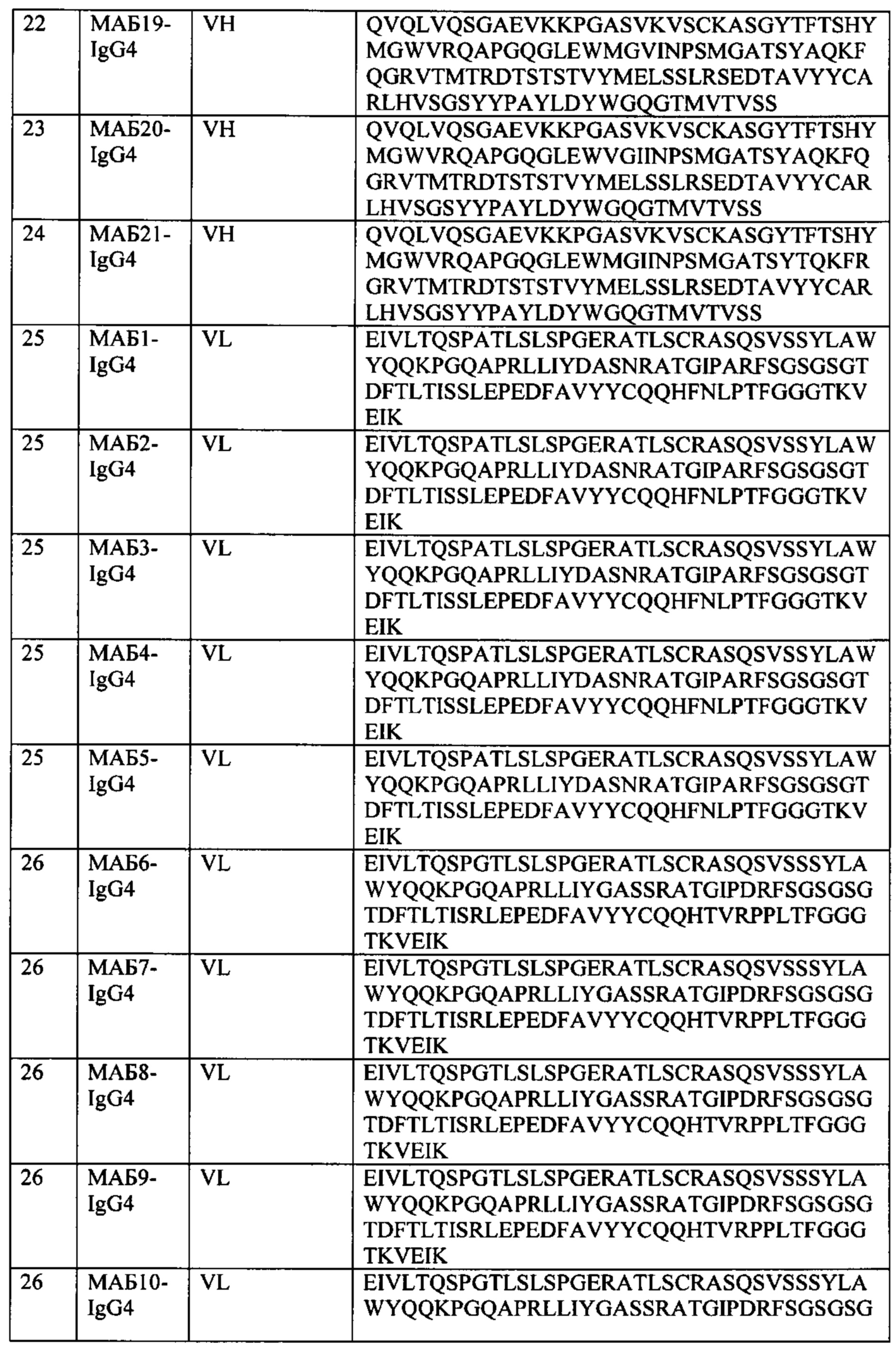
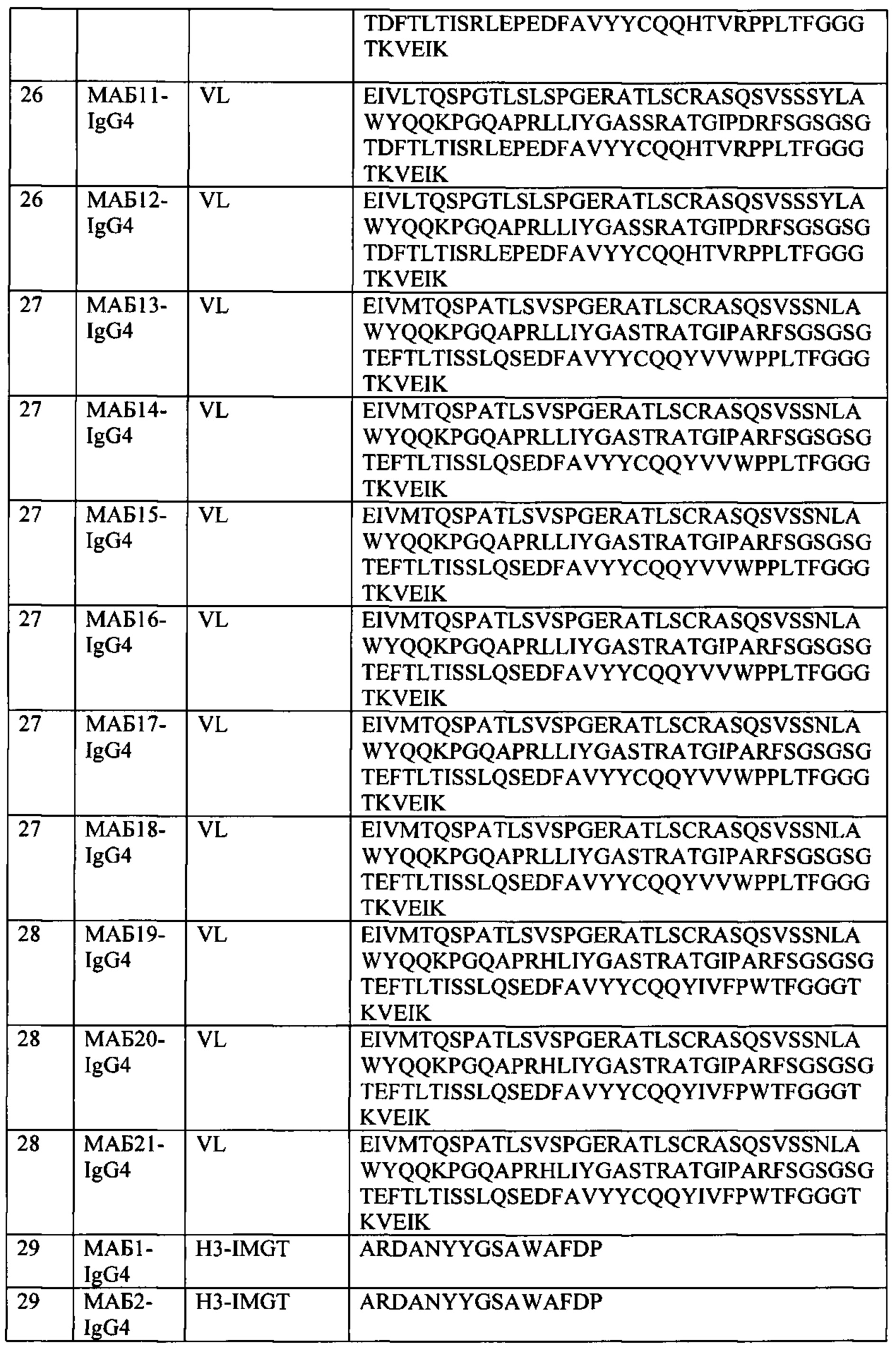
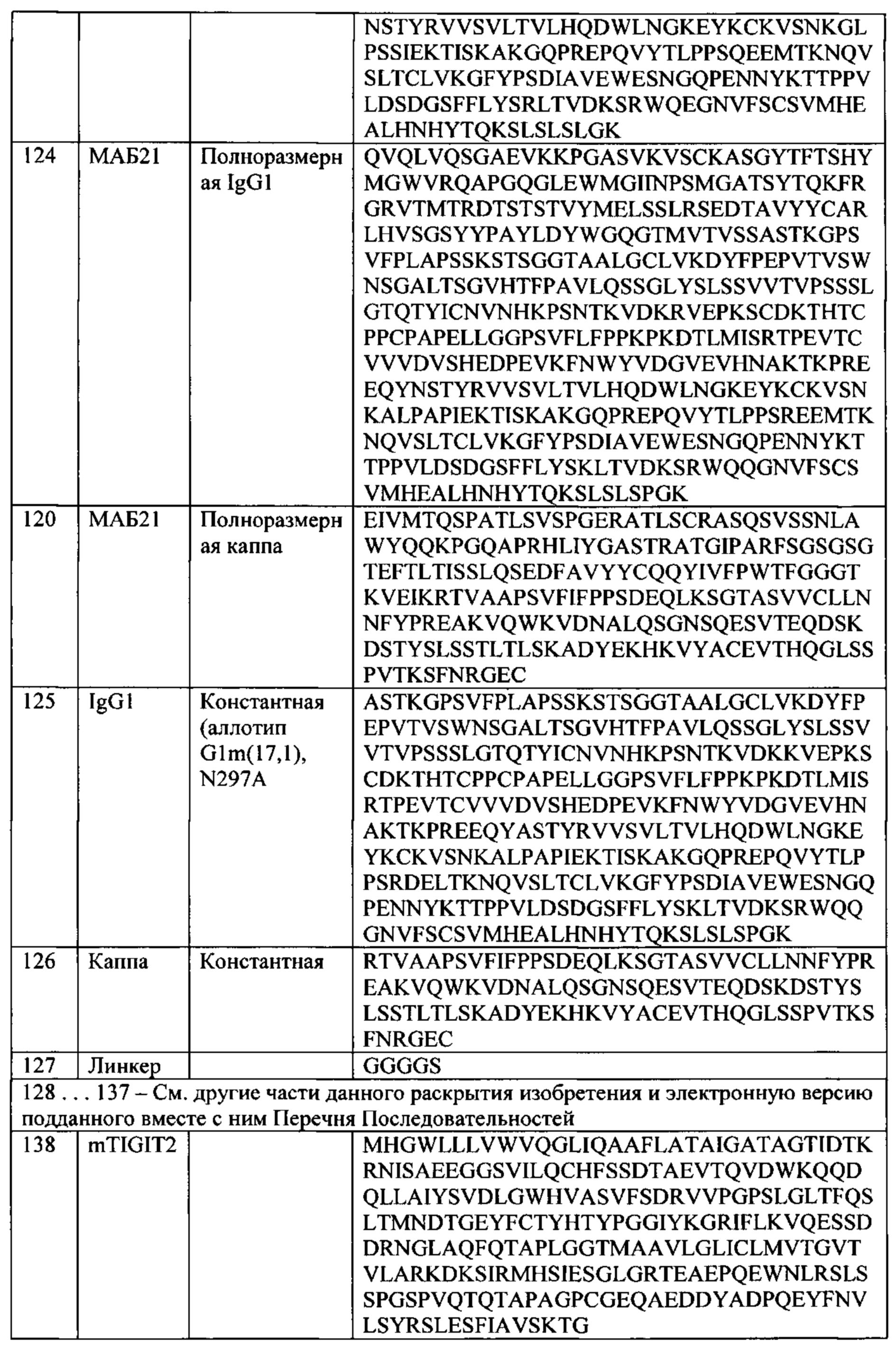
[0006] В некоторых вариантах осуществления, TIGIT выбирают из TIGIT человека («hTIGIT», SEQ ID NO: 1), TIGIT яванского макака («cTIGIT», SEQ ID NO: 2) и TIGIT мыши («mTIGIT», SEQ ID NO: 3 или 138).
[0007] В некоторых вариантах осуществления, АВР содержит антитело. В некоторых аспектах, антитело представляет собой моноклональное антитело. В некоторых аспектах, антитело представляет собой химерное антитело. В некоторых аспектах антитело представляет собой гуманизированное антитело. В некоторых аспектах антитело представляет собой человеческое антитело. В некоторых аспектах, АВР содержит фрагмент антитела. В некоторых вариантах осуществления, АВР содержит альтернативный каркас.
[0008] В некоторых вариантах осуществления, TIGIT экспрессируется на поверхности клетки-мишени. В некоторых аспектах, АВР антагорнизирует TIGIT, экспрессируемый на поверхности клетки-мишени.
[0009] В некоторых вариантах осуществления, клетку-мишень выбирают из эффекторного Т-лимфоцита, регуляторного Т-лимфоцита, клетки естественного киллера (NK) и Т-лимфоцита естественного киллера (NKT). В некоторых аспектах, клетка-мишень представляет собой эффекторный Т-лимфоцит, выбранный из Т-хелпера (CD4-позитивный, «CD4+»), цитотоксического Т-лимфоцита (CD8-позитивный, «CD8+»), и их комбинаций. В некоторых аспектах, клетка-мишень представляет собой регуляторный Т-лимфоцит, выбранный из регуляторного Т-лимфоцита CD4+CD25+Foxp3+, регуляторного Т-лимфоцита CD8+CD25+, и их комбинаций.
[0010] В некоторых вариантах осуществления, АВР предложенные в данном документе индуцируют различные биологические эффекты, связанные с ингибированием TIGIT. В некоторых аспектах, предложенный в данном документе АВР предотвращает ингибирование эффекторного Т-лимфоцита. В некоторых аспектах, АВР ко-стимулирует эффекторный Т-лимфоцит. В некоторых аспектах, АВР ингибирует подавление эффекторного Т-лимфоцита регуляторным Т-лимфоцитом. В некоторых аспектах, АВР увеличивает количество эффекторных Т-лимфоцитов в ткани или в кровеносной системе. В некоторых аспектах, ткань представляет собой опухоль. В некоторых аспектах, ткань представляет собой ткань, которая заражена вирусом.
[0011] Также предложены наборы, содержащие один или большее количество АВР, предложенных в данном документе, и инструкции для применения АВР. Также предложены наборы, содержащие одну или большее количество фармацевтических композиций, предложенных в данном документе, и инструкции для применения фармацевтической композиции.
[0012] Также предложены выделенные полинуклеотиды, кодирующие АВР, предложенные в данном документе, и их части.
[0013] Также предложены векторы, содержащие такие полинуклеотиды.
[0014] Также предложены рекомбинантные клетки-хозяева, содержащие такие полинуклеотиды, и рекомбинантные клетки-хозяева, содержащие такие векторы.
[0015] Также предложены способы получения АВР, предложенного в данном документе, с применением полинуклеотидов, векторов или клеток-хозяев, предложенных в данном документе.
[0016] Также предложены фармацевтические композиции, содержащие АВР, предложенные в данном документе, и фармацевтически приемлемый наполнитель.
[0017] Также предложены способы лечения или профилактики заболевания или патологии у субъекта, нуждающегося в этом, включая введение субъекту эффективного количества АВР, предложенного в данном документе, или фармацевтической композиции, содержащей такой АВР. В некоторых аспектах, заболевание или патология представляет собой рак. В некоторых аспектах, заболевание или патология представляет собой вирусную инфекцию. В некоторых аспектах, способ дополнительно включает введение одного или большего количества дополнительных терапевтических агентов. В некоторых аспектах, дополнительный терапевтический агент представляет собой иммуностимулирующий агент.
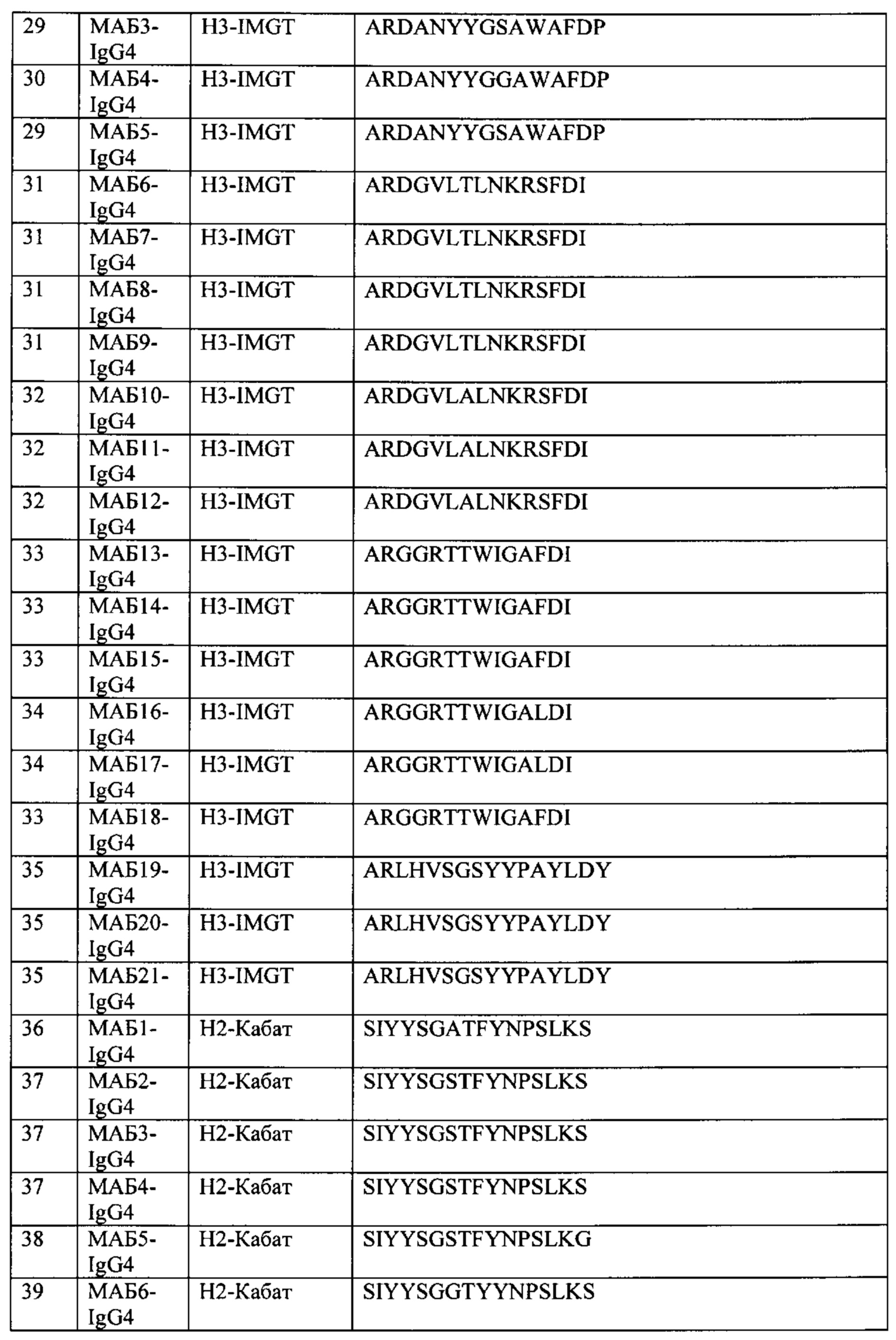
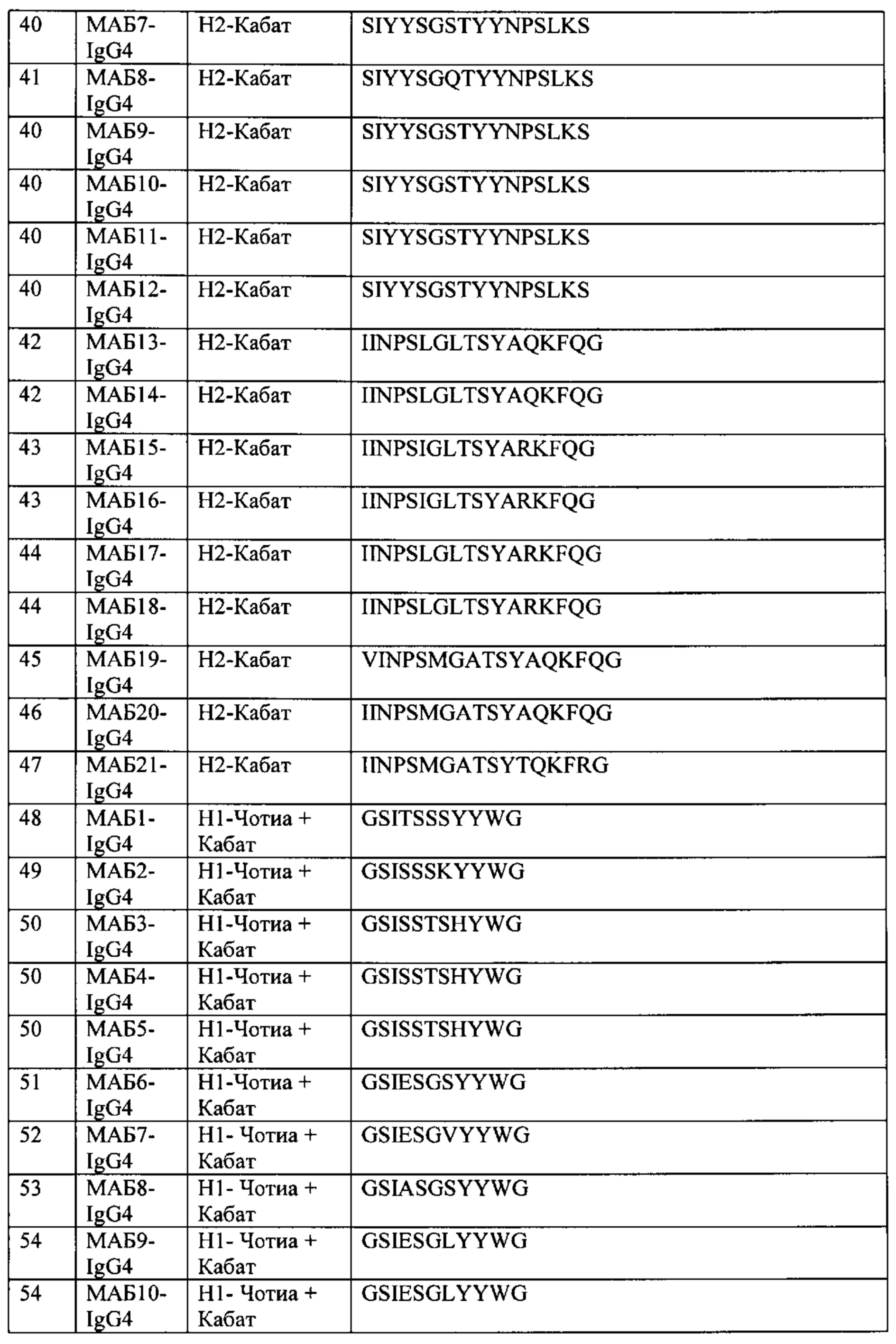
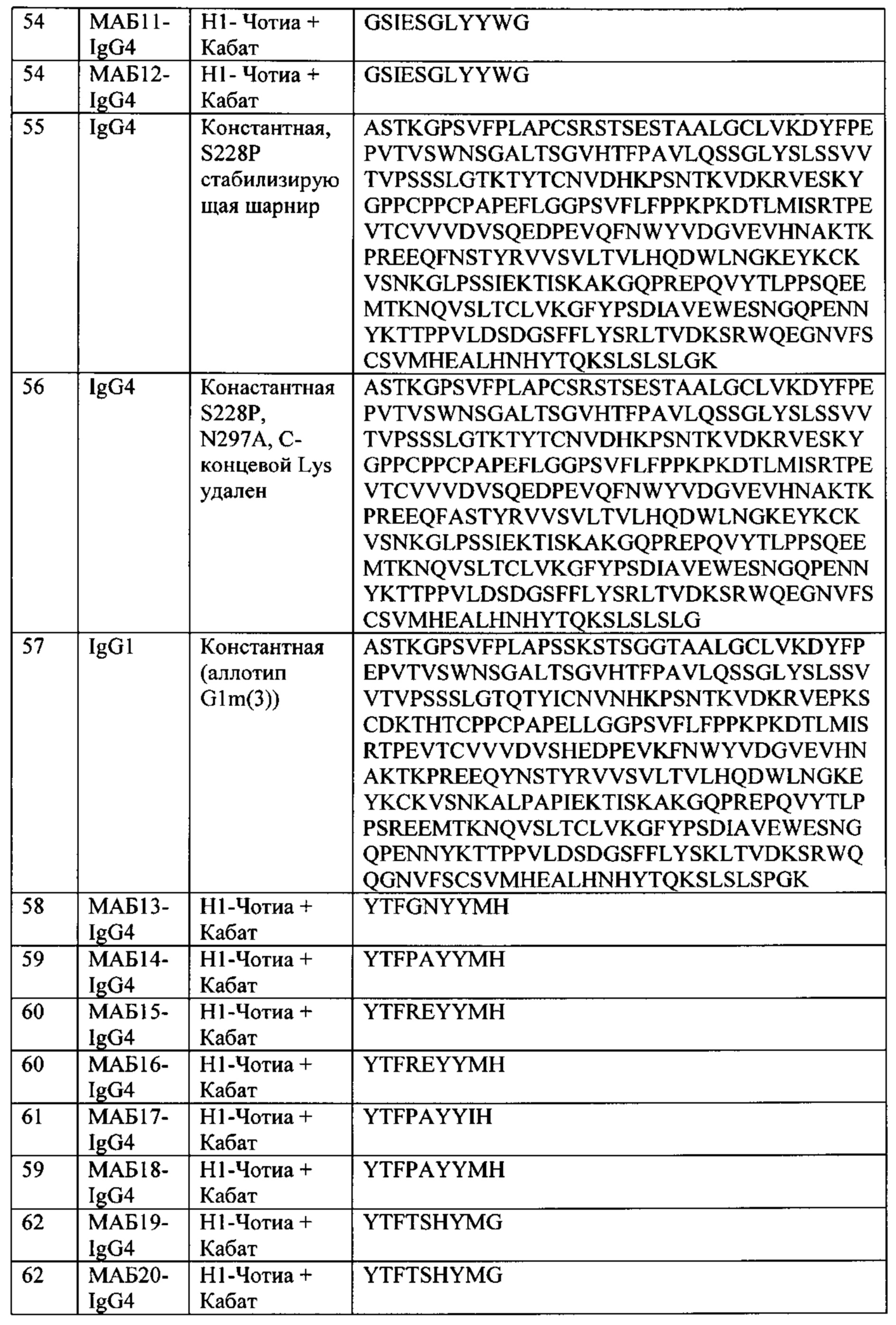
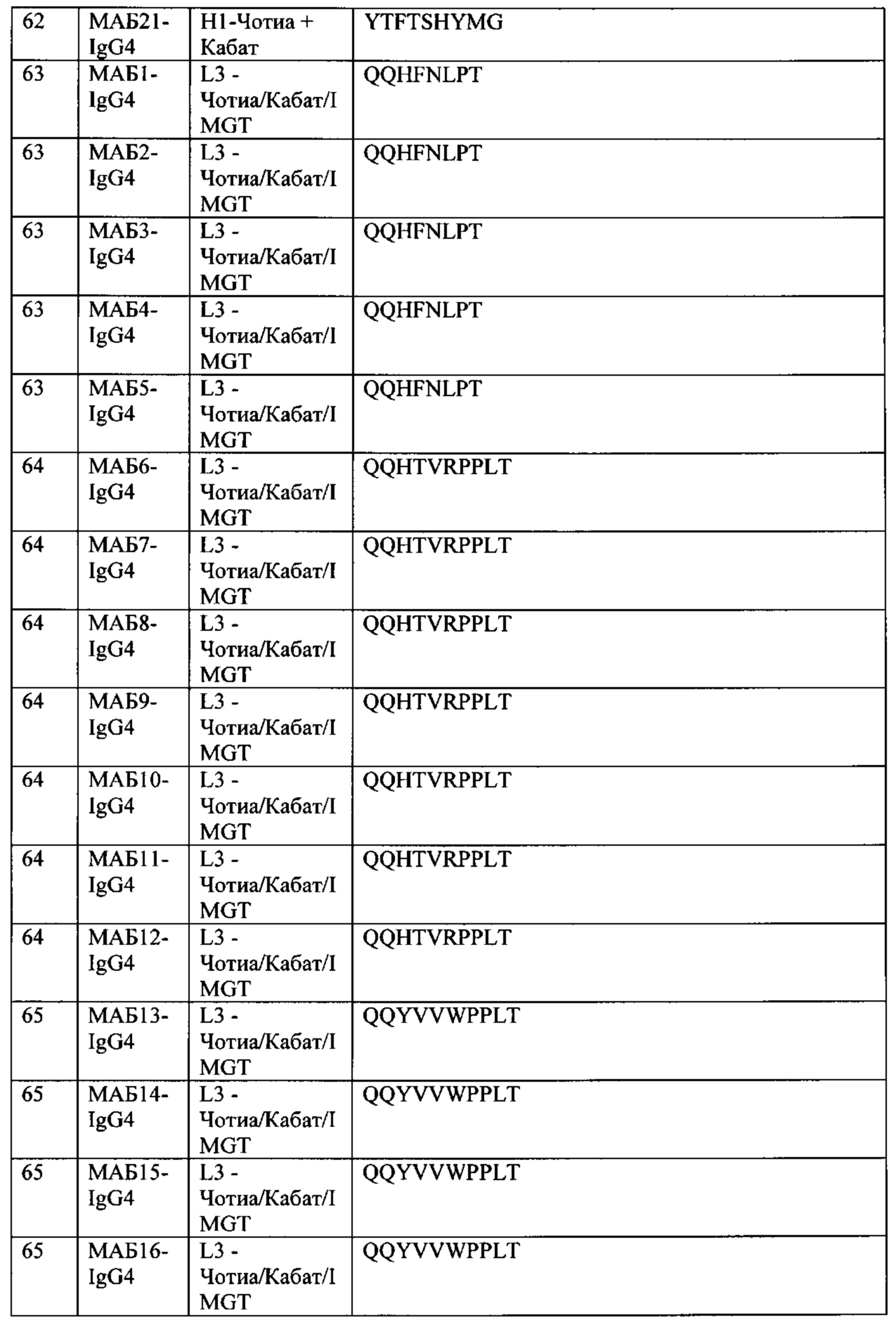
[0018] В некоторых вариантах осуществления, в данном документе предложено первое семейство АВР, причем АВР такого семейства содержит следующие шесть последовательностей CDR: а) CDR-H3, имеющую последовательность A-R-D-G-V-L-X1-L-N-K-R-S-F-D-I, в которой X1 представляет собой А или Т (SEQ ID NO: 128); b) CDR-H2, имеющую последовательность S-I-Y-Y-S-G-X2-T-Y-Y-N-P-S-L-K-S, в которой Х2 представляет собой S, Q или G (SEQ ID NO: 129); с) CDR-H1, имеющую последовательность G-S-I-X3-S-G-X4-Y-Y-W-G, в которой Х3 представляет собой Е или А, и Х4 представляет собой L, V или S (SEQ ID NO: 130); d) CDR-L3, имеющую последовательность QQHTVRPPLT (SEQ ID NO: 64); e) CDR-L2, имеющую последовательность GASSRAT (SEQ ID NO: 68); и f) CDR-L1, имеющую последовательность RASQSVSSSYLA (SEQ ID NO: 71). В некоторых вариантах осуществления, в данном документе предложен АВР такого первого семейства.
[0019] В некоторых вариантах осуществления, АВР такого первого семейства содержит: а) CDR-H3 SEQ ID NO: 32, CDR-H2 SEQ ID NO: 40, CDR-H1 SEQ ID NO: 54, CDR-L3 SEQ ID NO: 64, CDR-L2 SEQ ID NO: 68, и CDR-L1 SEQ ID NO: 71; b) CDR-H3 SEQ ID NO: 31, CDR-H2 SEQ ID NO: 40, CDR-H1 SEQ ID NO: 54, CDR-L3 SEQ ID NO: 64, CDR-L2 SEQ ID NO: 68, и CDR-L1 SEQ ID NO: 71; c) CDR-H3 SEQ ID NO: 31, CDR-H2 SEQ ID NO: 39, CDR-H1 SEQ ID NO: 51, CDR-L3 SEQ ID NO: 64, CDR-L2 SEQ ID NO: 68, и CDR-L1 SEQ ID NO: 71; d) CDR-H3 SEQ ID NO: 31, CDR-H2 SEQ ID NO: 40, CDR-H1 SEQ ID NO: 52, CDR-L3 SEQ ID NO: 64, CDR-L2 SEQ ID NO: 68, и CDR-L1 SEQ ID NO: 71; или e) CDR-H3 SEQ ID NO: 31, CDR-H2 SEQ ID NO: 41, CDR-H1 SEQ ID NO: 53, CDR-L3 SEQ ID NO: 64, CDR-L2 SEQ ID NO: 68, и CDR-L1 SEQ ID NO: 71.
[0020] В некоторых вариантах осуществления, АВР такого первого семейства содержит: а) последовательность VH SEQ ID NO: 13 и последовательность VL SEQ ID NO: 26; b) последовательность VH SEQ ID NO: 12 и последовательность VL SEQ ID NO: 26; c) последовательность VH SEQ ID NO: 14 и последовательность VL SEQ ID NO: 26; d) последовательность VH SEQ ID NO: 15 и последовательность VL SEQ ID NO: 26; e) последовательность VH SEQ ID NO: 9 и последовательность VL SEQ ID NO: 26; f) последовательность VH SEQ ID NO: 10 и последовательность VL SEQ ID NO: 26; или g) последовательность VH SEQ ID NO: 11 и последовательность VL SEQ ID NO: 26.
[0021] В некоторых вариантах осуществления, АВР такого первого семейства содержит: а) (i) тяжелую цепь SEQ ID NO: 99 и легкую цепь SEQ ID NO: 92; или (ii) тяжелую цепь SEQ ID NO: 100 и легкую цепь SEQ ID NO: 92; b) (i) тяжелую цепь SEQ ID NO: 97 и легкую цепь SEQ ID NO: 92; или (ii) тяжелую цепь SEQ ID NO: 98 и легкую цепь SEQ ID NO: 92; c) (i) тяжелую цепь SEQ ID NO: 101 и легкую цепь SEQ ID NO: 92; или (ii) тяжелую цепь SEQ ID NO: 102 и легкую цепь SEQ ID NO: 92; d) (i) тяжелую цепь SEQ ID NO: 103 и легкую цепь SEQ ID NO: 92; или (ii) тяжелую цепь SEQ ID NO: 104 и легкую цепь SEQ ID NO: 92; e) (i) тяжелую цепь SEQ ID NO: 90 и легкую цепь SEQ ID NO: 92; или (ii) тяжелую цепь SEQ ID NO: 91 и легкую цепь SEQ ID NO: 92; f) (i) тяжелую цепь SEQ ID NO: 93 и легкую цепь SEQ ID NO: 92; или (ii) тяжелую цепь SEQ ID NO: 94 и легкую цепь SEQ ID NO: 92; или g) (i) тяжелую цепь SEQ ID NO: 95 и легкую цепь SEQ ID NO: 92; или (ii) тяжелую цепь SEQ ID NO: 96 и легкую цепь SEQ ID NO: 92.
[0022] В некоторых вариантах осуществления, в данном документе предложено второе семейство АВР, причем АВР такого семейства содержит следующие шесть последовательностей CDR: а) CDR-H3, имеющую последовательность A-R-D-A-N-Y-Y-G-X1-A-W-A-F-D-P, в которой X1 представляет собой S или G (SEQ ID NO: 131); b) CDR-H2, имеющую последовательность S-I-Y-Y-S-G-X2-T-F-Y-N-P-S-L-K-X3, в которой Х2 представляет собой S или А, и Х3 представляет собой S или G (SEQ ID NO: 132); с) CDR-Н1, имеющую последовательность G-S-I-X4-S-X5-X6-X7-Y-W-G, в которой Х4 представляет собой S или Т, Х5 представляет собой S или Т, Х6 представляет собой S или K, и Х7 представляет собой Н или Y (SEQ ID NO: 133); d) CDR-L3, имеющую последовательность QQHFNLPT (SEQ ID NO: 63); е) CDR-L2, имеющую последовательность DASNRAT (SEQ ID NO: 67); и f) CDR-L1, имеющую последовательность RASQSVSSYLA (SEQ ID NO: 70). В некоторых вариантах осуществления, в данном документе предложен АВР такого второго семейства.
[0023] В некоторых вариантах осуществления, АВР такого второго семейства содержит: а) CDR-H3 SEQ ID NO: 29, CDR-H2 SEQ ID NO: 37, CDR-H1 SEQ ID NO: 49, CDR-L3 SEQ ID NO: 63, CDR-L2 SEQ ID NO: 67 и CDR-L1 SEQ ID NO: 70; b) CDR-H3 SEQ ID NO: 30, CDR-H2 SEQ ID NO: 37, CDR-H1 SEQ ID NO: 50, CDR-L3 SEQ ID NO: 63, CDR-L2 SEQ ID NO: 67 и CDR-L1 SEQ ID NO: 70; c) CDR-H3 SEQ ID NO: 29, CDR-H2 SEQ ID NO: 38, CDR-H1 SEQ ID NO: 50, CDR-L3 SEQ ID NO: 63, CDR-L2 SEQ ID NO: 67 и CDR-L1 SEQ ID NO: 70; d) CDR-H3 SEQ ID NO: 29, CDR-H2 SEQ ID NO: 36, CDR-H1 SEQ ID NO: 48, CDR-L3 SEQ ID NO: 63, CDR-L2 SEQ ID NO: 67 и CDR-L1 SEQ ID NO: 70; или e) CDR-H3 SEQ ID NO: 29, CDR-H2 SEQ ID NO: 37, CDR-H1 SEQ ID NO: 50, CDR-L3 SEQ ID NO: 63, CDR-L2 SEQ ID NO: 67 и CDR-L1 SEQ ID NO: 70.
[0024] В некоторых вариантах осуществления, АВР такого второго семейства содержит: а) последовательность VH SEQ ID NO: 5 и последовательность VL SEQ ID NO: 25; b) последовательность VH SEQ ID NO: 7 и последовательность VL SEQ ID NO: 25; c) последовательность VH SEQ ID NO: 8 и последовательность VL SEQ ID NO: 25; d) последовательность VH SEQ ID NO: 4 и последовательность VL SEQ ID NO: 25; или e) последовательность VH SEQ ID NO: 6 и последовательность VL SEQ ID NO: 25.
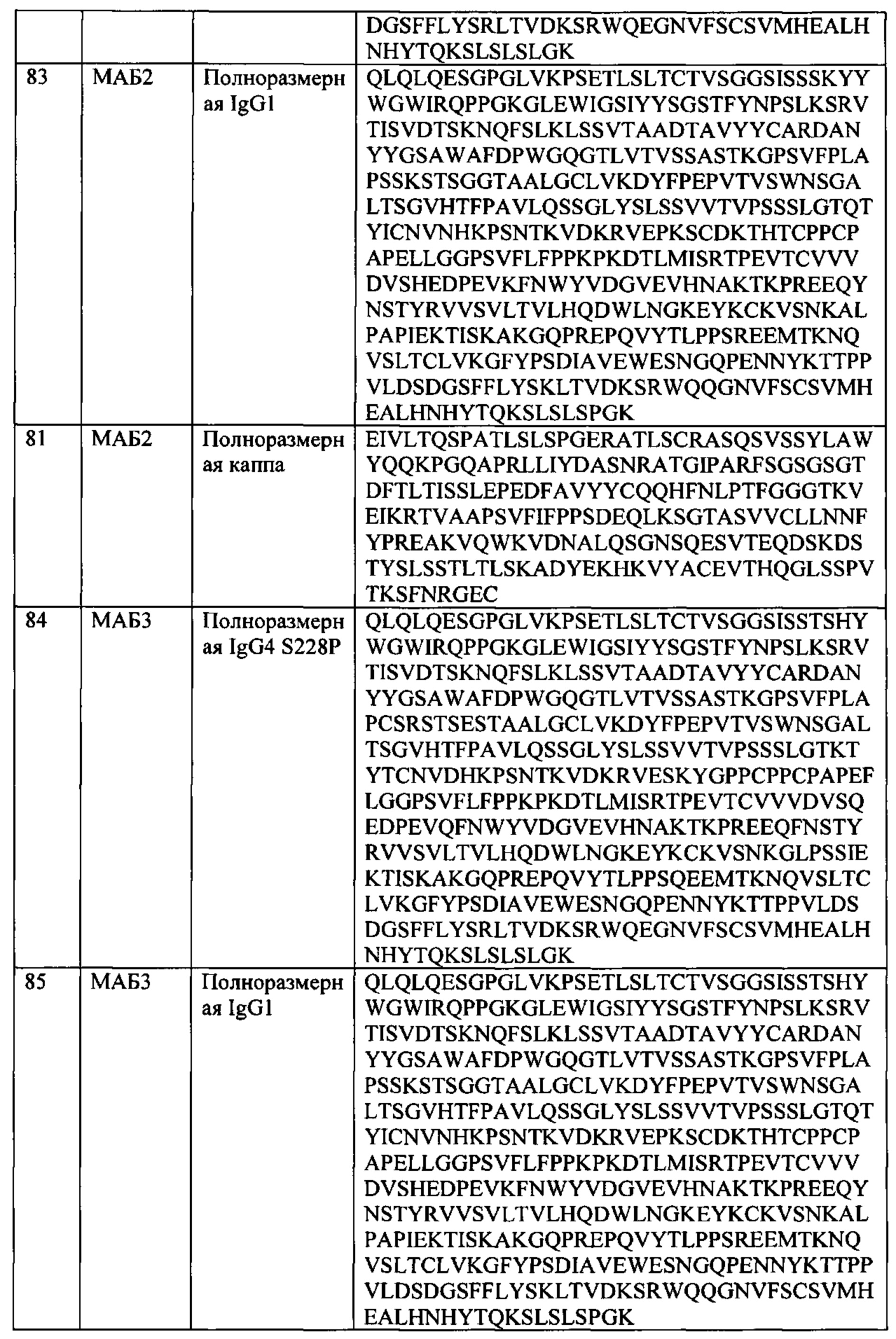
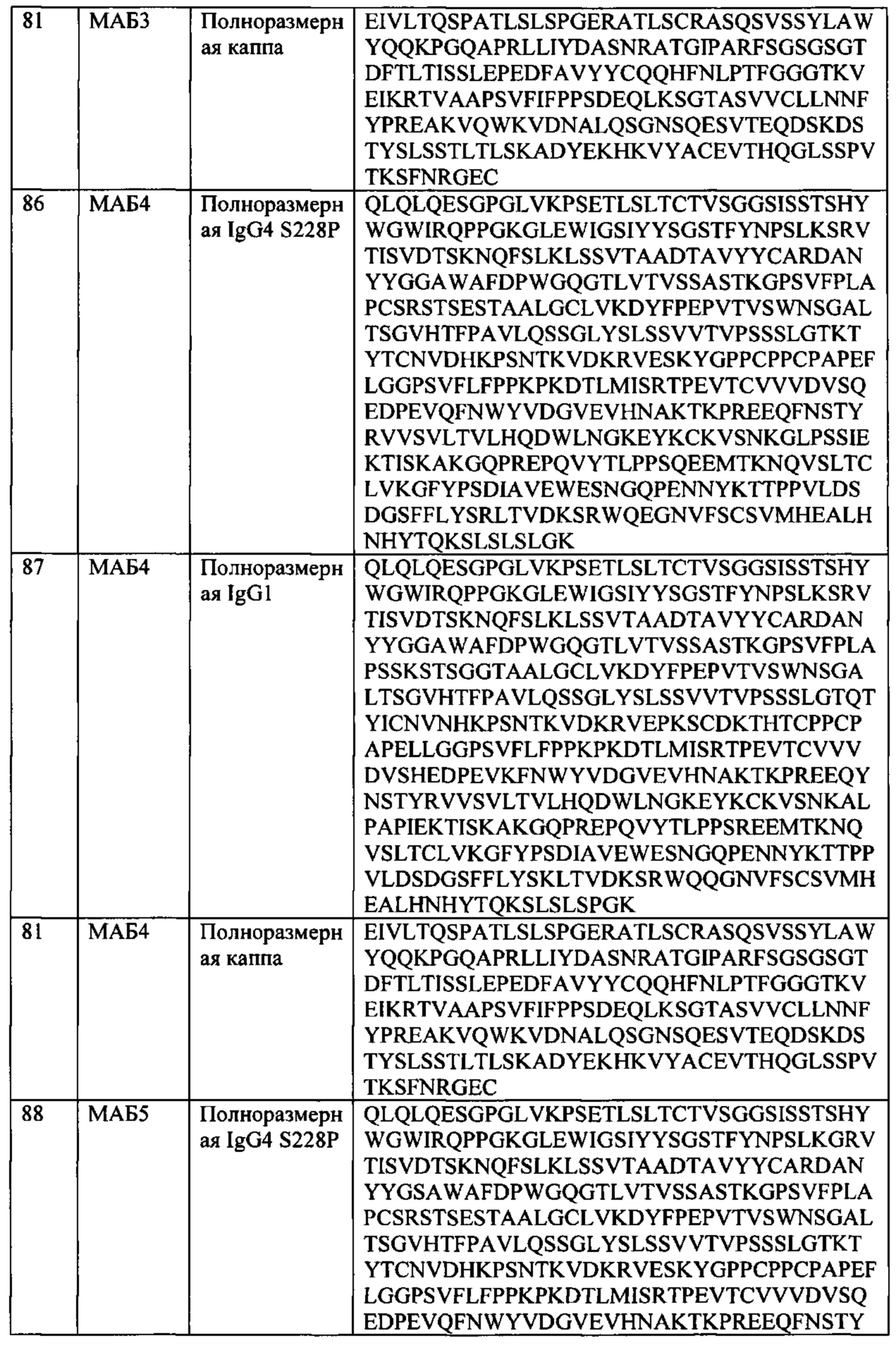
[0025] В некоторых вариантах осуществления, АВР такого второго семейства содержит: а) (i) тяжелую цепь SEQ ID NO: 82 и легкую цепь SEQ ID NO: 81; или (ii) тяжелую цепь SEQ ID NO: 83 и легкую цепь SEQ ID NO: 81; b) (i) тяжелую цепь SEQ ID NO: 86 и легкую цепь SEQ ID NO: 81; или (ii) тяжелую цепь SEQ ID NO: 87 и легкую цепь SEQ ID NO: 81; с) (i) тяжелую цепь SEQ ID NO: 88 и легкую цепь SEQ ID NO: 81; или (ii) тяжелую цепь SEQ ID NO: 89 и легкую цепь SEQ ID NO: 81; d) (i) тяжелую цепь SEQ ID NO: 79 и легкую цепь SEQ ID NO: 81; или (ii) тяжелую цепь SEQ ID NO: 80 и легкую цепь SEQ ID NO: 81; или e) (i) тяжелую цепь SEQ ID NO: 84 и легкую цепь SEQ ID NO: 81; или (ii) тяжелую цепь SEQ ID NO: 85 и легкую цепь SEQ ID NO: 81.
[0026] В некоторых вариантах осуществления, в данном документе предложено третье семейство АВР, причем АВР такого семейства содержит следующие шесть последовательностей CDR: а) CDR-H3, имеющую последовательность A-R-G-G-R-T-T-W-I-G-A-X1-D-I, в которой X1 представляет собой F или L (SEQ ID NO: 134); b) CDR-H2, имеющую последовательность I-I-N-P-S-X2-G-L-T-S-Y-A-X3-K-F-Q-G, в которой Х2 представляет собой L или I, и Х3 представляет собой Q или R (SEQ ID NO: 135); с) CDR-Н1, имеющую последовательность Y-T-F-X4-X5-Y-Y-X6-H, в которой Х4 представляет собой G, Р или R, и Х5 представляет собой N, А или Е, и Х6 представляет собой М или I (SEQ ID NO: 136); d) CDR-L3, имеющую последовательность QQYVVWPPLT (SEQ ID NO: 65); e) CDR-L2, имеющую последовательность GASTRAT (SEQ ID NO: 69); и f) CDR-L1, имеющую последовательность RASQSVSSNLA (SEQ ID NO: 72). В некоторых вариантах осуществления, в данном документе предложен АВР такого третьего семейства.
[0027] В некоторых вариантах осуществления АВР такого третьего семейства содержит: а) CDR-H3 SEQ ID NO: 33, CDR-H2 SEQ ID NO: 43, CDR-H1 SEQ ID NO: 60, CDR-L3 SEQ ID NO: 65, CDR-L2 SEQ ID NO: 69 и CDR-L1 SEQ ID NO: 72; b) CDR-H3 SEQ ID NO: 34, CDR-Н2 SEQ ID NO: 43, CDR-H1 SEQ ID NO: 60, CDR-L3 SEQ ID NO: 65, CDR-L2 SEQ ID NO: 69 и CDR-L1 SEQ ID NO: 72; c) CDR-H3 SEQ ID NO: 33, CDR-H2 SEQ ID NO: 44, CDR-H1 SEQ ID NO: 59, CDR-L3 SEQ ID NO: 65, CDR-L2 SEQ ID NO: 69 и CDR-L1 SEQ ID NO: 72; d) CDR-H3 SEQ ID NO: 33, CDR-H2 SEQ ID NO: 42, CDR-H1 SEQ ID NO: 58, CDR-L3 SEQ ID NO: 65, CDR-L2 SEQ ID NO: 69 и CDR-L1 SEQ ID NO: 72; e) CDR-H3 SEQ ID NO: 33, CDR-H2 SEQ ID NO: 42, CDR-H1 SEQ ID NO: 59, CDR-L3 SEQ ID NO: 65, CDR-L2 SEQ ID NO: 69 и CDR-L1 SEQ ID NO: 72; или f) CDR-H3 SEQ ID NO: 34, CDR-H2 SEQ ID NO: 44, CDR-H1 SEQ ID NO: 61, CDR-L3 SEQ ID NO: 65, CDR-L2 SEQ ID NO: 69 и CDR-L1 SEQ ID NO: 72.
[0028] В некоторых вариантах осуществления, АВР такого третьего семейства содержит: а) последовательность VH SEQ ID NO: 18 и последовательность VL SEQ ID NO: 27; b) последовательность VH SEQ ID NO: 19 и последовательность VL SEQ ID NO: 27; c) последовательность VH SEQ ID NO: 21 и последовательность VL SEQ ID NO: 27; d) последовательность VH SEQ ID NO: 16 и последовательность VL SEQ ID NO: 27; e) последовательность VH SEQ ID NO: 17 и последовательность VL SEQ ID NO: 27; или f) последовательность VH SEQ ID NO: 20 и последовательность VL SEQ ID NO: 27.
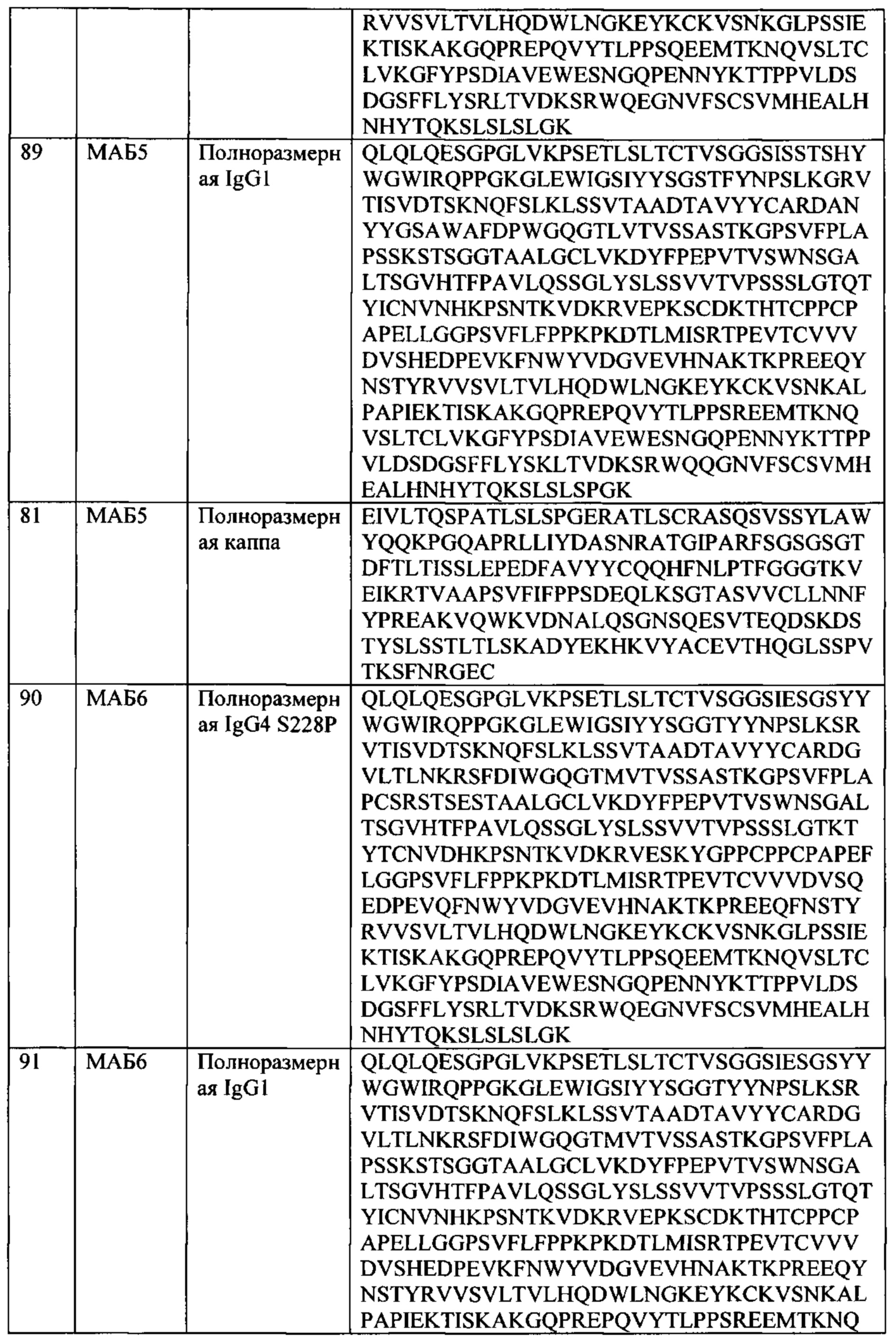
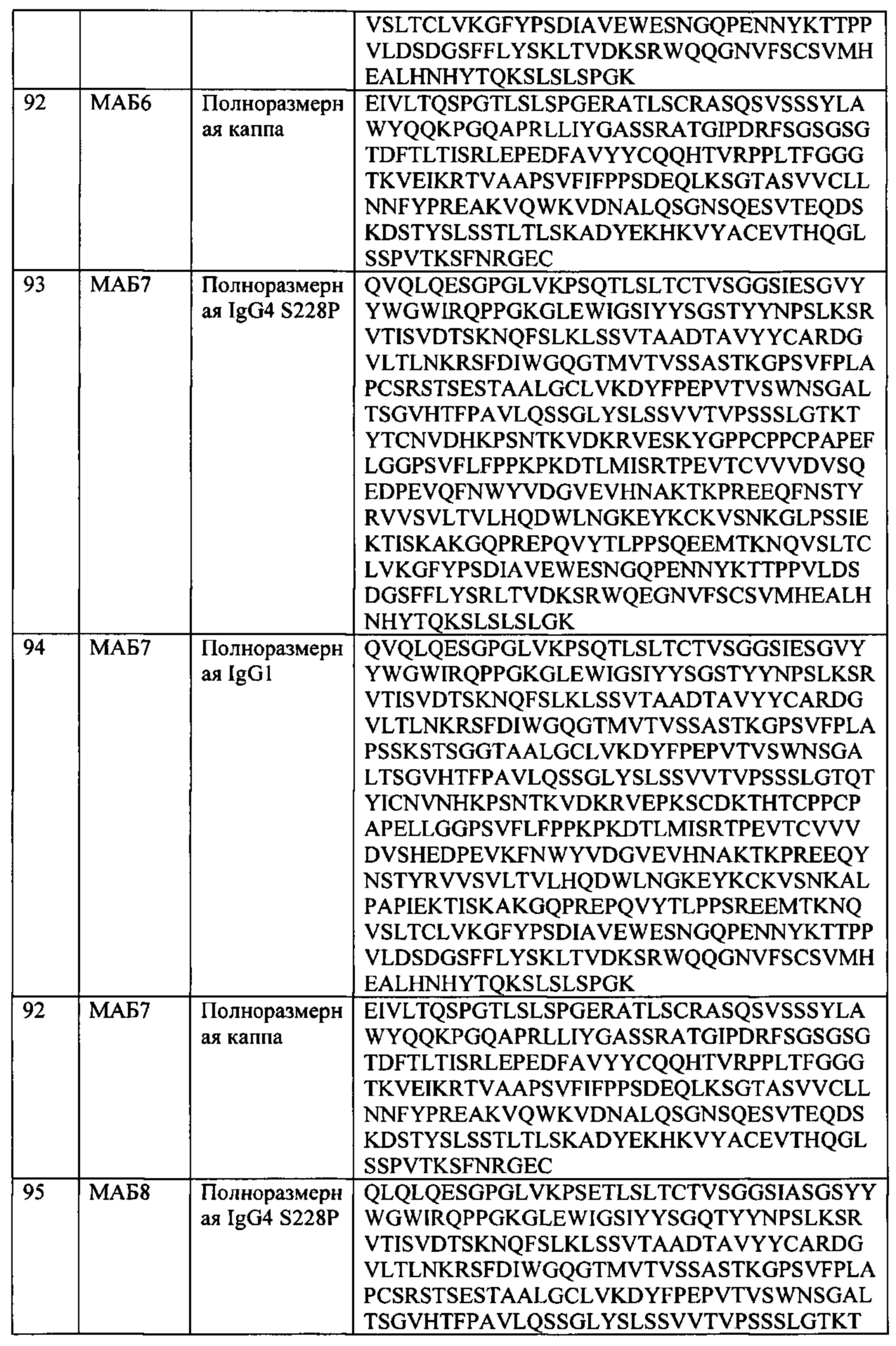
[0029] В некоторых вариантах осуществления, АВР такого третьего семейства содержит: а) (i) тяжелую цепь SEQ ID NO: 110 и легкую цепь SEQ ID NO: 107; или (ii) тяжелую цепь SEQ ID NO: 111 и легкую цепь SEQ ID NO: 107; b) (i) тяжелую цепь SEQ ID NO: 112 и легкую цепь SEQ ID NO: 107; или (ii) тяжелую цепь SEQ ID NO: 113 и легкую цепь SEQ ID NO: 107; с) (i) тяжелую цепь SEQ ID NO: 116 и легкую цепь SEQ ID NO: 107; или (ii) тяжелую цепь SEQ ID NO: 117 и легкую цепь SEQ ID NO: 107; d) (i) тяжелую цепь SEQ ID NO: 105 и легкую цепь SEQ ID NO: 107; или (ii) тяжелую цепь SEQ ID NO: 106 и легкую цепь SEQ ID NO: 107; e) (i) тяжелую цепь SEQ ID NO: 108 и легкую цепь SEQ ID NO: 107; или (ii) тяжелую цепь SEQ ID NO: 109 и легкую цепь SEQ ID NO: 107; или f) (i) тяжелую цепь SEQ ID NO: 114 и легкую цепь SEQ ID NO: 107; или (ii) тяжелую цепь SEQ ID NO: 115 и легкую цепь SEQ ID NO: 107.
[0030] В некоторых вариантах осуществления, в данном документе предложено четвертое семейство АВР, причем АВР такого семейства содержит следующие шесть последовательностей CDR: а) CDR-H3, имеющую последовательность ARLHVSGSYYPAYLDY (SEQ ID NO: 35); b) CDR-H2, имеющую последовательность X1-I-N-P-S-M-G-A-T-S-Y-X2-Q-K-F-X3-G, в которой X1 представляет собой V или I, Х2 представляет собой А или Т, и Х3 представляет собой Q или R (SEQ ID NO: 137); с) CDR-Н1 имеющую последовательность YTFTSHYMG (SEQ ID NO: 62); d) CDR-L3 имеющую последовательность QQYIVFPWT (SEQ ID NO: 66); e) CDR-L2 имеющую последовательность GASTRAT (SEQ ID NO: 69); и f) CDR-L1 имеющую последовательность RASQSVSSNLA, (SEQ ID NO: 72). В некоторых вариантах осуществления, в данном документе предложен АВР такого четвертого семейства.
[0031] В некоторых вариантах осуществления, АВР такого четвертого семейства содержит: a) CDR-H3 SEQ ID NO: 35, CDR-H2 SEQ ID NO: 46, CDR-H1 SEQ ID NO: 62, CDR-L3 SEQ ID NO: 66, CDR-L2 SEQ ID NO: 69 и CDR-L1 SEQ ID NO: 72; b) CDR-H3 SEQ ID NO: 35, CDR-H2 SEQ ID NO: 47, CDR-H1 SEQ ID NO: 62, CDR-L3 SEQ ID NO: 66, CDR-L2 SEQ ID NO: 69 и CDR-L1 SEQ ID NO: 72; или с) CDR-H3 SEQ ID NO: 35, CDR-H2 SEQ ID NO: 45, CDR-H1 SEQ ID NO: 62, CDR-L3 SEQ ID NO: 66, CDR-L2 SEQ ID NO: 69 и CDR-L1 SEQ ID NO: 72.
[0032] В некоторых вариантах осуществления, АВР такого четвертого семейства содержит: а) последовательность VH SEQ ID NO: 23 и последовательность VL SEQ ID NO: 28; b) последовательность VH SEQ ID NO: 24 и последовательность VL SEQ ID NO: 28; или с) последовательность VH SEQ ID NO: 22 и последовательность VL SEQ ID NO: 28.
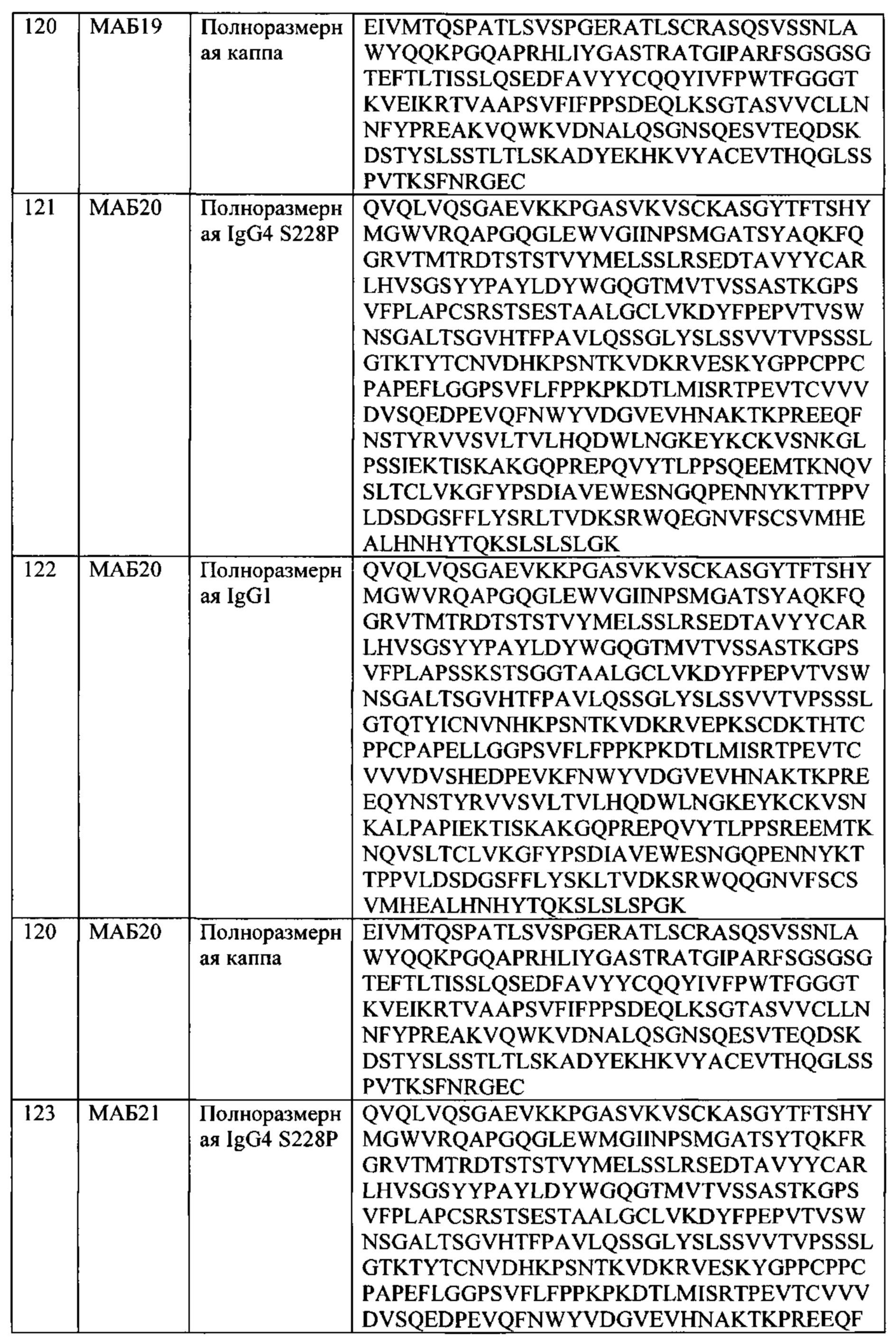
[0033] В некоторых вариантах осуществления, АВР такого четвертого семейства содержит: a) (i) тяжелую цепь SEQ ID NO: 121 и легкую цепь SEQ ID NO: 120; или (ii) тяжелую цепь SEQ ID NO: 122 и легкую цепь SEQ ID NO: 120; b) (i) тяжелую цепь SEQ ID NO: 123 и легкую цепь SEQ ID NO: 120; или (ii) тяжелую цепь SEQ ID NO: 124 и легкую цепь SEQ ID NO: 120; или с) (i) тяжелую цепь SEQ ID NO: 118 и легкую цепь SEQ ID NO: 120; или (ii) тяжелую цепь SEQ ID NO: 119 и легкую цепь SEQ ID NO: 120.
[0034] В некоторых вариантах осуществления, в данном документе предложен выделенный антиген-связывающий белок (АВР), который специфически связывает TIGIT человека (hTIGIT; SEQ ID NO: 1), содержащий: a) CDR-H3, имеющую по меньшей мере примерно 80% идентичности с CDR-H3 области VH, выбранной из SEQ ID NO: 4-24; b) CDR-H2, имеющую по меньшей мере примерно 80% идентичности с CDR-H2 области VH, выбранной из SEQ ID NO: 4-24; с) CDR-H1, имеющую по меньшей мере примерно 80% идентичности с CDR-H1 области VH, выбранной из SEQ ID NO: 4-24; d) CDR-L3, имеющую по меньшей мере примерно 80% идентичности CDR-L3 области VL, выбранной из SEQ ID NO: 25-28; е) CDR-L2, имеющую по меньшей мере примерно 80% идентичности с CDR-L2 области VL, выбранной из SEQ ID NO: 25-28; и f) CDR-L1, имеющую по меньшей мере примерно 80% идентичности с CDR-L1 области VL, выбранной из SEQ ID NO: 25-28. В некоторых вариантах осуществления, CDR-H3, CDR-H2, CDR-H1, CDR-L3, CDR-L2 и CDR-L1 каждую идентифицируют в соответствии со схемой нумерации, выбранной из схемы нумерации по Кабату, схемы нумерации по Чотиа или схема нумерации по IMGT (ImMunoGeneTics). В некоторых вариантах осуществления, CDR-H1 идентифицируют, как определено схемами нумерации по Чотиа и Кабату, включая границы обеих схем нумерации. В некоторых вариантах осуществления: а) CDR-H3 содержит CDR-H3, выбранную из SEQ ID NO: 29-35, или ее вариант, имеющий 1, 2 или 3 аминокислотные замены; b) CDR-H2 содержит CDR-Н3, выбранную из SEQ ID NO: 36-47, или ее вариант, имеющий 1, 2 или 3 аминокислотные замены; с) CDR-H1 содержит CDR-H1, выбранную из SEQ ID NO: 48-54 или 58-62, или ее вариант, имеющий 1 или 2 аминокислотные замены; d) CDR-L3 содержит CDR-L3, выбранную из SEQ ID NO: 63-66, или ее вариант, имеющий 1 или 2 аминокислотные замены; е) CDR-L2 содержит CDR-L2, выбранную из SEQ ID NO: 67-69, или ее вариант, имеющий 1 аминокислотную замену; и f) CDR-L1 содержит CDR-L1, выбранную из SEQ ID NO: 70-72, или ее вариант, имеющий 1 или 2 аминокислотные замены.
[0035] В некоторых вариантах осуществления, в данном документе предложен выделенный антиген-связывающий белок (АВР), который специфически связывает TIGIT человека (hTIGIT; SEQ ID NO: 1) содержащий: а) область VH, имеющую по меньшей мере примерно 90% идентичности с областью VH, выбранной из SEQ ID NO: 4-24; и b) область VL, имеющую по меньшей мере примерно 90% идентичности с областью VL, выбранной из SEQ ID NO: 25-28. В некоторых вариантах осуществления: а) область VH содержит область VH, выбранную из SEQ ID NO: 4-24, или ее вариант, имеющий 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12 аминокислотных замен; и b) область VL содержит область VL, выбранную из SEQ ID NO: 25-28, или ее вариант, имеющий 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 аминокислотных замен. В некоторых вариантах осуществления, аминокислотные замены представляют собой консервативные аминокислотные замены.
[0036] В некоторых вариантах осуществления, любой из вышеуказанных АВР: а) конкурирует за связывание с TIGIT с антителом, выбранным из МАБ1, МАБ2, МАБ3, МАБ4, МАБ5, МАБ6, МАБ7, МАБ8, МАБ9, МАБ10, МАБ11, МАБ12, МАБ13, МАБ14, МАБ15, МАБ16, МАБ17, МАБ18, МАБ19, МАБ20 или МАБ21, каждое из которых представлено в Таблице 5 данного описания; b) ингибирует связывание CD155 с TIGIT; с) ингибирует связывание CD112 с TIGIT; d) ингибирует ассоциацию CD226 с TIGIT; е) активирует эффекторный Т-лимфоцит или естественный киллер (NK); f) уменьшает количество регуляторных Т-лимфоцитов в ткани или в кровеносной системе; g) ингибирует подавление эффекторного Т-лимфоцита регуляторным Т-лимфоцитом; h) не связывается специфически с любыми из PVRL1, PVRL2, PVRL3 или PVRL4; или i) допускает любую комбинацию a)-h).
[0037] В некоторых вариантах осуществления, любой из вышеуказанных АВР: а) специфически связывает TIGIT яванского макака (cTIGIT; SEQ ID NO: 2); b) связывает TIGIT мыши (mTIGIT; SEQ ID NO: 3) с аффинностью ниже (на что указывает более высокая KD), чем аффинность АВР к hTIGIT, или не связывает mTIGIT; или с) допускает любую комбинацию а)-b).
[0038] В некоторых вариантах осуществления, любой из вышеуказанных АВР: а) специфически связывает cTIGIT (SEQ ID NO: 2); b) связывает mTIGIT (SEQ ID NO: 3) с аффинностью ниже (на что указывает более высокая KD), чем аффинность АВР к hTIGIT и cTIGIT; и с) ингибирует связывание CD155 с TIGIT.
[0039] В некоторых вариантах осуществления, в данном документе предложен АВР, который конкурирует за связывание с TIGIT с любым из вышеуказанных АВР, причем АВР: а) специфически связывает cTIGIT (SEQ ID NO: 2); b) связывает mTIGIT (SEQ ID NO: 3) с аффинностью ниже (на что указывает более высокая KD), чем аффинность АВР к hTIGIT и cTIGIT; и с) ингибирует связывание CD155 с TIGIT.
[0040] В некоторых вариантах осуществления, любой из вышеуказанных АВР содержит антитело. В некоторых вариантах осуществления, антитело представляет собой моноклональное антитело. В некоторых вариантах осуществления, антитело выбрано из человеческого антитела, гуманизированного антитела или химерного антитела.
[0041] В некоторых вариантах осуществления, любой из вышеуказанных АВР является мультиспецифичным. В некоторых вариантах осуществления, мультиспецифичный АВР связывает больше чем один антиген (т.е. TIGIT и другой (не-TIGIT) антиген). В некоторых вариантах осуществления, мультиспецифичный АВР связывает больше чем один эпитоп на одном антигене (т.е. два или более эпитопа на TIGIT).
[0042] В некоторых вариантах осуществления, любой из вышеуказанных АВР содержит фрагмент антитела.
[0043] В некоторых вариантах осуществления, любой из вышеуказанных АВР содержит альтернативный каркас.
[0044] В некоторых вариантах осуществления, любой из вышеуказанных АВР содержит константную область иммуноглобулина. В некоторых вариантах осуществления, АВР содержит константную область тяжелой цепи класса, выбранного из IgA, IgD, IgE, IgG или IgM. В некоторых вариантах осуществления, АВР содержит константную область тяжелой цепи класса IgG, и подкласс выбран из IgG4, IgG1, IgG2 или IgG3.
[0045] В некоторых вариантах осуществления, любой из вышеуказанных АВР связывает hTIGIT (SEQ ID NO: 1) с KD меньшей чем около 10 нМ, как измерено интерферометрией биослоя. В некоторых вариантах осуществления, любой из вышеуказанных АВР связывает hTIGIT (SEQ ID NO: 1) с KD меньшей чем около 5 нМ, как измерено интерферометрией биослоя. В некоторых вариантах осуществления, любой из вышеуказанных АВР связывает hTIGIT (SEQ ID NO: 1) с KD меньшей чем около 2 нМ, как измерено интерферометрией биослоя. В некоторых вариантах осуществления, любой из вышеуказанных АВР связывает cTIGIT (SEQ ID NO: 2) с KD меньшей чем около 100 нМ, как измерено интерферометрией биослоя. В некоторых вариантах осуществления, любой из вышеуказанных АВР связывает cTIGIT (SEQ ID NO: 2) с KD меньшей чем около 10 нМ, как измерено интерферометрией биослоя. В некоторых вариантах осуществления, любой из вышеуказанных АВР не показывает значительного связывания с mTIGIT в анализе интерферометрии биослоя. В некоторых вариантах осуществления, любой из вышеуказанных АВР связывается с mTIGIT клеточной поверхности с KD меньшей чем около 50 нМ. В некоторых вариантах осуществления, mTIGIT содержит SEQ ID NO: 3. В некоторых вариантах осуществления, mTIGIT содержит SEQ ID NO: 138.
[0046] В некоторых вариантах осуществления, любой из вышеуказанных АВР содержит полипептидную последовательность, имеющую остаток пироглутамата (рЕ) на своем N-конце. В некоторых вариантах осуществления, любой из вышеуказанных АВР содержит последовательность VH, в которой Q N-конца замещен на рЕ. В некоторых вариантах осуществления, любой из вышеуказанных АВР содержит последовательность VL, в которой Е N-конца замещена на рЕ. В некоторых вариантах осуществления, любой из вышеуказанных АВР содержит последовательность тяжелой цепи, в которой Q N-конца замещен на рЕ. В некоторых вариантах осуществления, любой из вышеуказанных АВР содержит последовательность легкой цепи, в которой Е N-конеца замещена на рЕ.
[0047] В некоторых вариантах осуществления, в данном документе предложены любые из вышеуказанных АВР для применения в качестве терапевтического агента. В некоторых вариантах осуществления, в данном документе предложены любые из вышеуказанных АВР для лечения рака или вирусной инфекции. В некоторых вариантах осуществления, в данном документе предложены любые из вышеуказанных АВР для лечения рака, причем рак выбран из солидной опухоли или гематологической опухоли. В некоторых вариантах осуществления, в данном документе предложены любые из вышеуказанных АВР для применения в качестве терапевтического агента в лечении заболевания или патологии, что не отвечало(а) на предшествующее лечение. В некоторых вариантах осуществления, предшествующее лечение представляло собой лечение, включающее агент, который ингибирует взаимодействие между PD-1 и PD-L1.
[0048] В некоторых вариантах осуществления, в данном документе предложен выделенный полинуклеотид, кодирующий любой из вышеуказанных АВР, его VH, его VL, его легкую цепь, его тяжелую цепь или его антиген-связывающую часть. В некоторых вариантах осуществления, в данном документе предложен вектор, содержащий полинуклеотид. В некоторых вариантах осуществления, в данном документе предложена клетка-хозяин, содержащая полинуклеотид и/или вектор. В некоторых вариантах осуществления, в данном документе предложен способ получения любого из вышеуказанных ABP, включающий экспрессию АВР в клетке-хозяине и выделение экспрессированного АВР.
[0049] В некоторых вариантах осуществления, в данном документе предложена фармацевтическая композиция, содержащая любой из вышеуказанных ABP. В некоторых вариантах осуществления, количество АВР в фармацевтической композиции является достаточным для: а) увеличения активности эффекторных Т-лимфоцитов; b) увеличения активности цитолитических Т-лимфоцитов; c) увеличения активности NK-клеток; d) ингибирования опосредованного TIGIT сигналинга; e) ингибирования или блокирования связывание CD155 и CD112 с TIGIT; или f) любой комбинации a)-e), у субъекта. В некоторых вариантах осуществления, любая из вышеуказанных фармацевтических композиций дополнительно содержит антитело, которое антагонизирует PD-1 или блокирует взаимодействие PD-L1 с PD-1. В некоторых вариантах осуществления, любая из вышеуказанных фармацевтических композиций предназначена для применения в качестве терапевтического агента. В некоторых вариантах осуществления, любая из вышеуказанных фармацевтических композиций предназначена для лечения рака или вирусной инфекции. В некоторых вариантах осуществления, любая из вышеуказанных фармацевтических композиций предназначена для лечения рака, причем рак выбирают из солидной опухоли и гематологической опухоли. В некоторых вариантах осуществления, любая из вышеуказанных фармацевтических композиций предназначена для применения в качестве терапевтического агента при лечении заболевания или патологии, что не реагирует на предшествующее лечение. В некоторых вариантах осуществления, предшествующее лечение представляло собой лечение, включающее агент, который ингибирует взаимодействие между PD-1 и PD-L1.
[0050] В некоторых вариантах осуществления, в данном документе предложен способ лечения или профилактики заболевания или патологии у субъекта, нуждающегося в этом, включая введение субъекту эффективного количества любого из вышеуказанных ABP или любой из вышеуказанных фармацевтических композиций. В некоторых вариантах осуществления, заболевание или патология представляет собой рак или вирусную инфекцию. В некоторых вариантах осуществления, заболевание или патология представляет собой рак, и рак выбирают из солидной опухоли и гематологической опухоли. В некоторых вариантах осуществления, в данном документе предложен способ модулирования иммунного ответа у субъекта, нуждающегося в этом, включая введение субъекту эффективного количества любого из вышеуказанных ABP или любой из вышеуказанных фармацевтических композиций. В некоторых вариантах осуществления, любой из вышеуказанных способов дополнительновключает введение одного или большего количества дополнительных терапевтических агентов субъекту. В некоторых вариантах осуществления, дополнительный терапевтический агент выбирают из агента, который ингибирует взаимодействие между PD-1 и PD-L1, химиотерапиии, иммуностимулирующего агента, излучения и их комбинаций.
[0051] В некоторых вариантах осуществления, дополнительный терапевтический агент для применения в любом из вышеуказанных способов лечения, применяя АВР или применяя фармацевтическую композицию, представляет собой агент, который ингибирует взаимодействие между PD-1 и PD-L1, и причем агент, который ингибирует взаимодействие между PD-1 и PD-L1, выбирают из антитела, пептидомиметика, малой молекулы или нуклеиновой кислоты, кодирующей такой агент. В некоторых вариантах осуществления, агент, который ингибирует взаимодействие между PD-1 и PD-L1, выбирают из пембролизумаба, ниволумаба, атезолизумаба, авелумаба, дурвалаумаба, BMS-936559, сульфамономэтоксина 1 и сульфаметизола 2.
[0052] В некоторых вариантах осуществления, дополнительный терапевтический агент для применения в любом из вышеуказанных способов лечения, применяя АВР или применяя фармацевтическую композицию, представляет собой иммуностимулирующий агент, выбранный из: а) агента, который блокирует сигналинг ингибирующего рецептора иммунной клетки или его лиганд, или нуклеиновой кислоты, кодирующей такой агент; b) агониста стимулирующего рецептора иммунной клетки или нуклеиновой кислоты, кодирующей такой агонист; с) цитокина или нуклеиновой кислоты, кодирующей цитокин; d) онколитического вируса или нуклеиновой кислоты, кодирующей онколитический вирус; e) Т-лимфоцита, экспрессирующего рецептор химерного антигена; f) би- или мультиспецифического антитела, направленного на Т-лимфоцит, или нуклеиновой кислоты, кодирующей такое антитело; g) анти-TGF-β антитела или нуклеиновой кислоты, кодирующей такое антитело; h) ловушки TGF-β или нуклеиновой кислоты, кодирующей такую ловушку; i) вакцины к ассоциированному с раком антигену, включая такой антиген или нуклеиновую кислоту, кодирующую такой антиген, и j) их комбинаций. В некоторых вариантах осуществления, дополнительный терапевтический агент представляет собой агент, который блокирует сигналинг ингибирующего рецептора иммунной клетки или его лиганд, или нуклеиновую кислоту, кодирующую такой агент, и ингибирующий рецептор или его лиганд выбирают из CTLA-4, PD-1, PD-L1, PD-L2, LAG-3, Tim3, нейритина, BTLA, СЕСАМ-1, СЕСАМ-5, VISTA, LAIR1, CD160, 2В4, TGF-R, KIR и их комбинаций. В некоторых вариантах осуществления, дополнительный терапевтический агент является агонистом стимулирующего рецептора иммунной клетки, или нуклеиновой кислотой, кодирующей такой агонист, и стимулирующий рецептор иммунной клетки выбирают из ОХ40, CD2, CD27, CDS, ICAM-1, LFA-1 (CD11a/CD18), ICOS (CD278), 4-1BB (CD137), GITR, CD28, CD30, CD40, BAFFR, HVEM, CD7, LIGHT, NKG2C, SLAMF7, NKp80, CD160, B7-H3, лиганда CD83, и их комбинаций. В некоторых вариантах осуществления, дополнительный терапевтический агент представляет собой цитокин или нуклеиновую кислоту, кодирующую цитокин, выбранный из ИЛ-2, ИЛ-5, ИЛ-7, ИЛ-12, ИЛ-15, ИЛ-21, и их комбинаций. В некоторых вариантах осуществления, дополнительный терапевтический агент представляет собой онколитический вирус или нуклеиновую кислоту, кодирующую онколитический вирус, выбранный из вируса простого герпеса, вируса везикулярного стоматита, аденовируса, вируса болезни Ньюкасла, вируса коровьей оспы, вируса мараба и их комбинаций.
[0053] В некоторых вариантах осуществления, дополнительный терапевтический агент входит в состав той же фармацевтической композиции, что и АВР. В некоторых вариантах осуществления, дополнительный терапевтический агент входит в состав фармацевтической композиции, отличающейся от фармацевтической композиции с АВР. В некоторых вариантах осуществления, дополнительный терапевтический агент применяют до введения АВР. В некоторых вариантах осуществления, дополнительный терапевтический агент применяют после введения АВР. В некоторых вариантах осуществления, дополнительный терапевтический агент применяют одновременно с АВР.
[0054] В некоторых вариантах осуществления, субъект является субъектом, которого лечили с помощью агента, который ингибирует взаимодействие между PD-1 и PD-L1 перед выполнением такого способа.
[0055] В некоторых вариантах осуществления, болезнь или патология, поражающая субъекта, не реагировала на предшествующую терапию. В некоторых вариантах осуществления, предшествующее лечение представляло собой лечение, включающее агент, который ингибирует взаимодействие между PD-1 и PD-L1.
[0056] В некоторых вариантах осуществления, в данном документе предложен набор, содержащий любую из вышеуказанных фармацевтических композиций, и инструкции по применению такой фармацевтической композиции. В некоторых вариантах осуществления, набор дополнительно содержит дополнительную фармацевтическую композицию, содержащую дополнительный терапевтический агент и инструкции для применения такого дополнительного терапевтического агента. В некоторых вариантах осуществления, дополнительный терапевтический агент выбирают из агента, который ингибирует взаимодействие между PD-1 и PD-L1, химиотерапиии, иммуностимулирующего агента, излучения и их комбинаций. В некоторых вариантах осуществления, дополнительный терапевтический агент представляет собой агент, который ингибирует взаимодействие между PD-1 и PD-L1, и при этом агент, ингибирующий взаимодействие между PD-1 и PD-L1, выбирают из антитела, пептидомиметика, малой молекулы или нуклеиновой кислоты, кодирующей такой агент. В некоторых вариантах осуществления, агент, который ингибирует взаимодействие между PD-1 и PD-L1, выбирают из пембролизумаба, ниволумаба, атезолизумаба, авелумаба, дурвалаумаба, BMS-936559, сульфамономэтоксина 1 и сульфаметизола 2. В некоторых вариантах осуществления, дополнительный терапевтический агент представляет собой иммуностимулирующий агент, выбранный из: а) агента, который блокирует сигналинг ингибирующего рецептора иммунной клетки или его лиганд, или нуклеиновой кислоты, кодирующей такой агент; b) агониста стимулирующего рецептора иммунной клетки или нуклеиновой кислоты, кодирующей такой агонист; с) цитокина или нуклеиновой кислоты, кодирующей цитокин; d) онколитического вируса или нуклеиновой кислоты, кодирующей онколитический вирус; е) Т-лимфоцита, экспрессирующего рецептор химерного антигена; f) би- или мультиспецифического антитела, направленного на Т-лимфоцит, или нуклеиновой кислоты, кодирующей такое антитело; g) анти-TGF-β антитела или нуклеиновой кислоты, кодирующей такое антитело; h) ловушки TGF-β или нуклеиновой кислоты, кодирующей такую ловушку; i) вакцины к ассоциированному с раком антигену, включая такой антиген или нуклеиновую кислоту, кодирующую такой антиген, и j) их комбинаций. В некоторых вариантах осуществления, дополнительный терапевтический агент представляет собой агент, который блокирует сигналинг ингибирующего рецептора иммунной клетки или его лиганд, или нуклеиновую кислоту, кодирующую такой агент, и ингибирующий рецептор или его лиганд выбирают из CTLA-4, PD-1, PD-L1, PD-L2, LAG-3, Tim3, нейритина, BTLA, СЕСАМ-1, СЕСАМ-5, VISTA, LAIR1, CD160, 2В4, TGF-R, KIR и их комбинаций. В некоторых вариантах осуществления, дополнительный терапевтический агент является агонистом стимулирующего рецептора иммунной клетки, или нуклеиновой кислотой, кодирующей такой агонист, и стимулирующий рецептор иммунной клетки выбирают из ОХ40, CD2, CD27, CDS, ICAM-1, LFA-1 (CD11a/CD18), ICOS (CD278), 4-1BB (CD137), GITR, CD28, CD30, CD40, BAFFR, HVEM, CD7, LIGHT, NKG2C, SLAMF7, NKp80, CD160, B7-H3, лиганда CD83, и их комбинаций. В некоторых вариантах осуществления, дополнительный терапевтический агент представляет собой цитокин или нуклеиновую кислоту, кодирующую цитокин, выбранный из ИЛ-2, ИЛ-5, ИЛ-7, ИЛ-12, ИЛ-15, ИЛ-21, и их комбинаций. В некоторых вариантах осуществления, дополнительный терапевтический агент представляет собой онколитический вирус или нуклеиновую кислоту, кодирующую онколитический вирус, выбранный из вируса простого герпеса, вируса везикулярного стоматита, аденовируса, вируса болезни Ньюкасла, вируса коровьей оспы, вируса мараба и их комбинаций.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[0057] На Фиг. 1А-1В показаны выравнивания последовательностей различных молекул, описанных дополнительно в Примерах. На Фиг. 1А показаны выравнивания последовательностей внеклеточных доменов TIGIT из человека, яванского макака, мыши (SEQ ID NO: 3) и референсных последовательностей TIGIT крысы. На Фиг. 1В показано выравнивание внеклеточных доменов человеческих TIGIT и PVRL4.
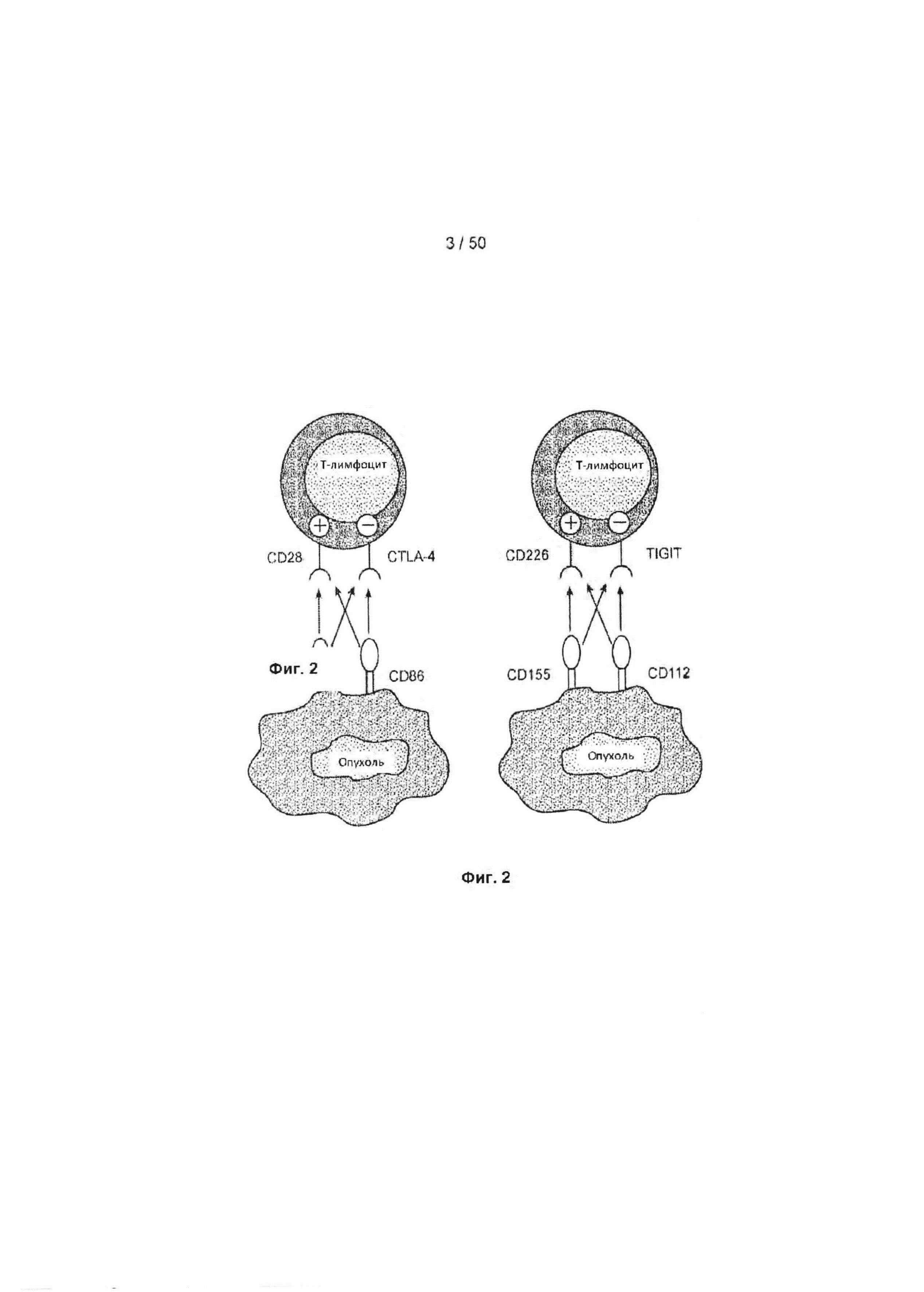
[0058] Фиг. 2 иллюстрирует сходство между путями CD28-CTLA4 и CD226-TIGIT и, следовательно, полезность TIGIT в качестве целевой контрольной точки иммунной системы. Биология костимуляции/коингибирования CD226/TIGIT аналогична таковой CD28/CTLA4; TIGIT обеспечивает подавляющий сигнал для Т-лимфоцитов, в то время как CD226 обеспечивает сигнал костимуляции для Т-лимфоцитов. Лиганды TIGIT CD155 и CD112 широко экспрессируются в опухолях, обеспечивая подавляющую иммунитет среду.
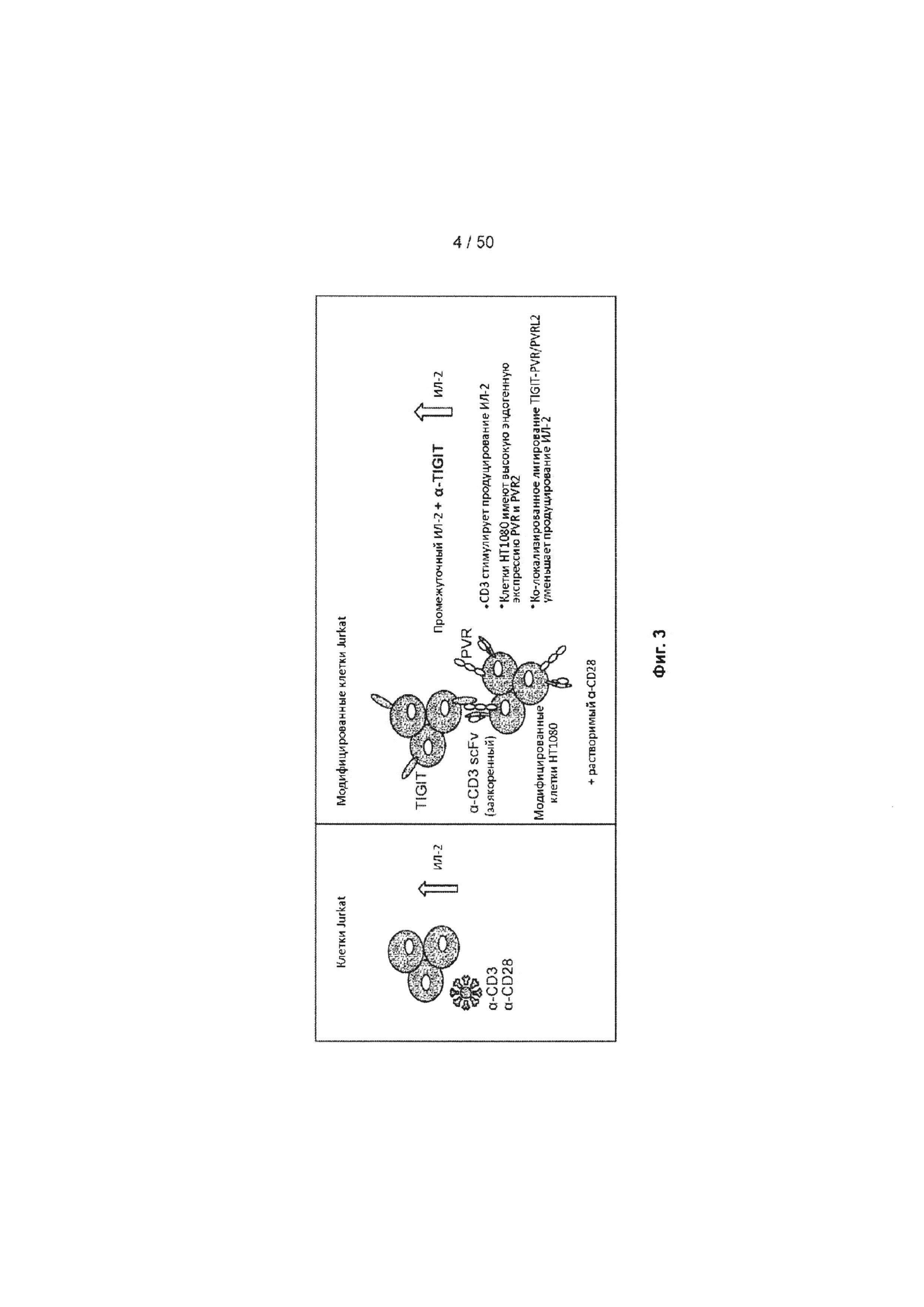
[0059] На Фиг. 3 показана схематическая диаграмма анализа совместного культивирования TIGIT Jurkat/анти-CD3 НТ-1080, описанного в Примере 7.
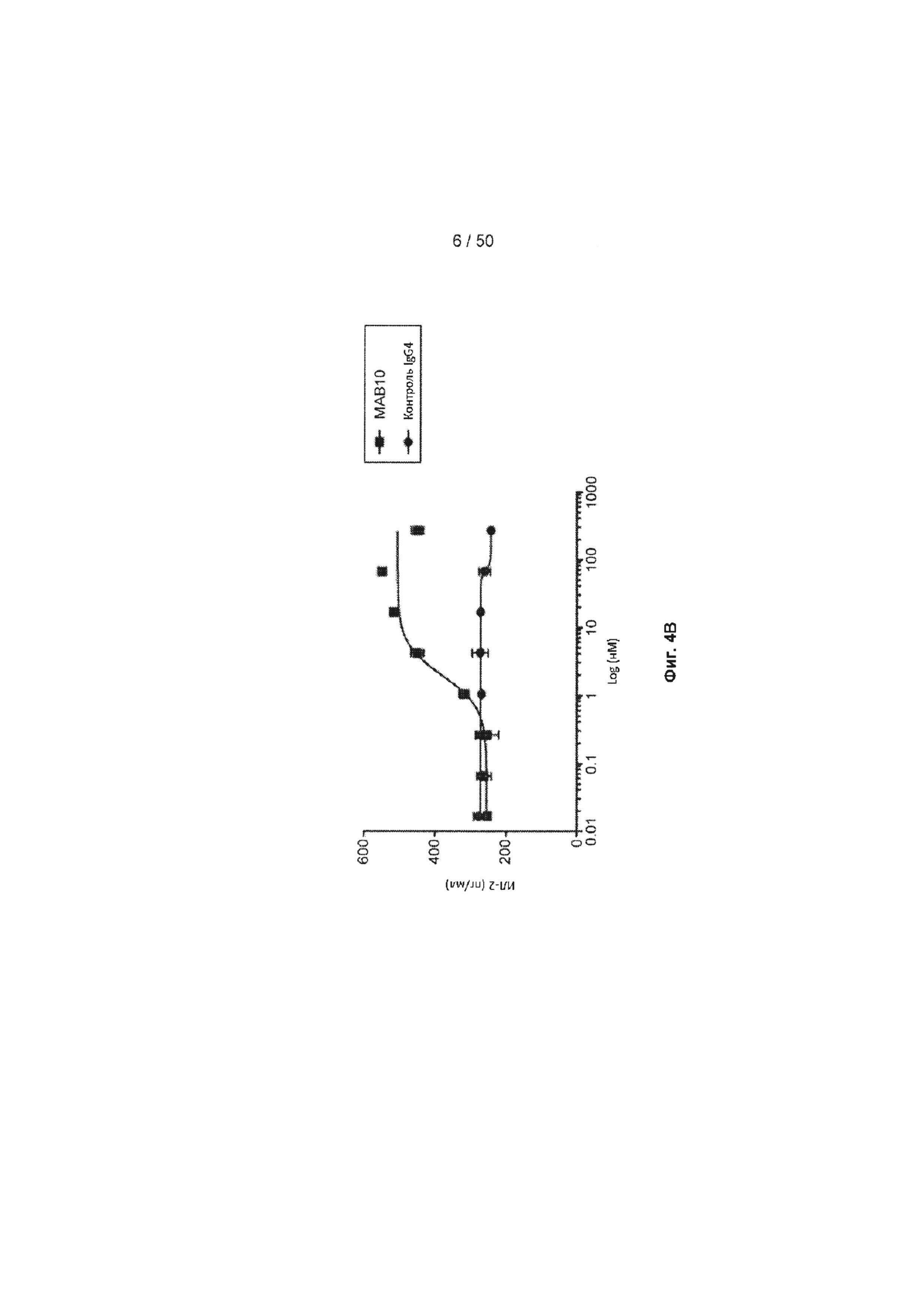
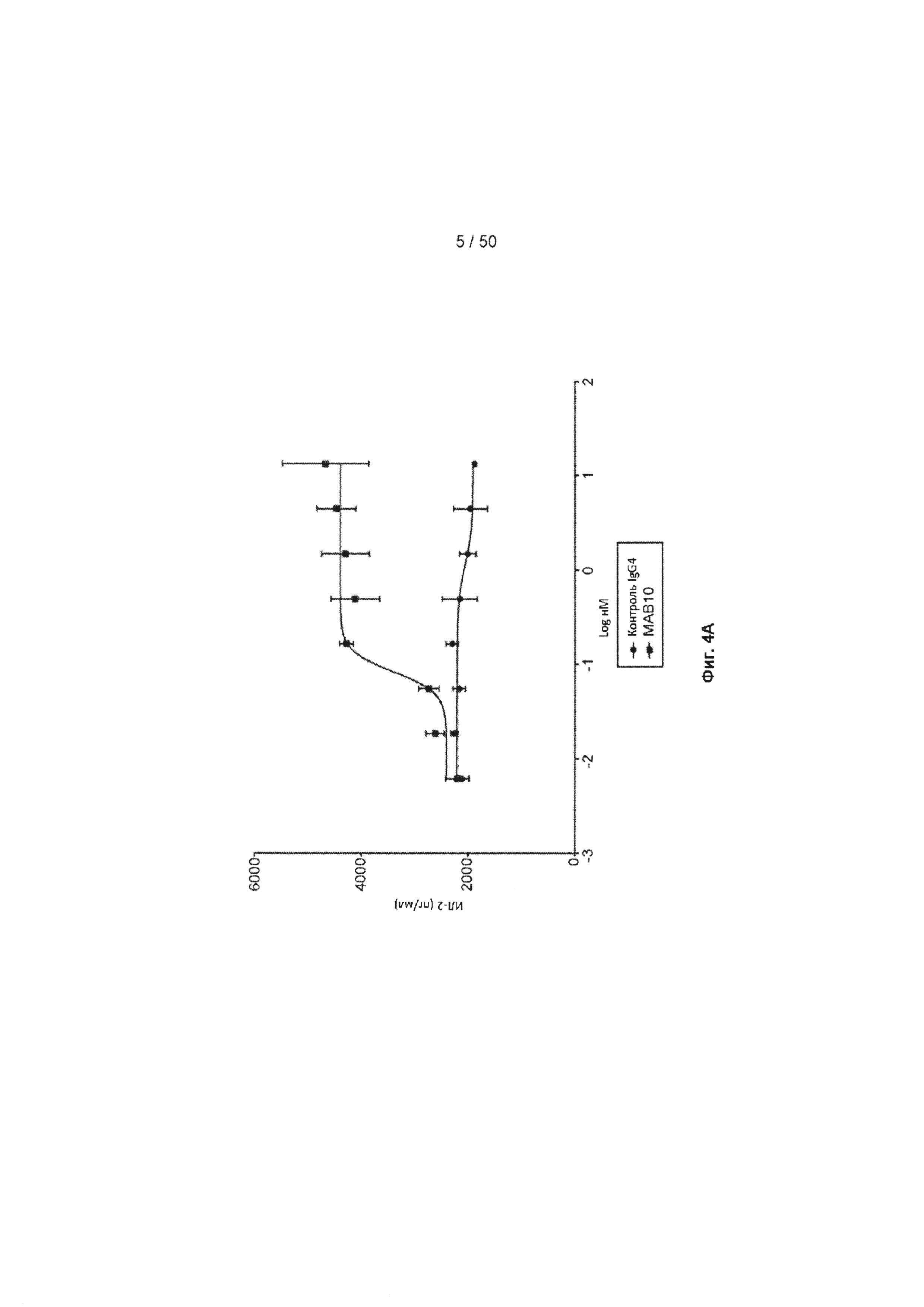
[0060] На Фиг. 4А показаны кривые EC50 из иллюстративных экспериментов, сравнивающих способность МАБ10 и изотипного контрольного IgG4 индуцировать продуцирование ИЛ-2 в модифицированных клетках Jurkat, экспрессирующих TIGIT человека. На Фиг. 4В показаны кривые ЕС50 из иллюстративных экспериментов, сравнивающих способность МАБ10 и изотипного контрольного IgG4 индуцировать продуцирование ИЛ-2 в модифицированных клетках Jurkat, экспрессирующих TIGIT яванского макака.
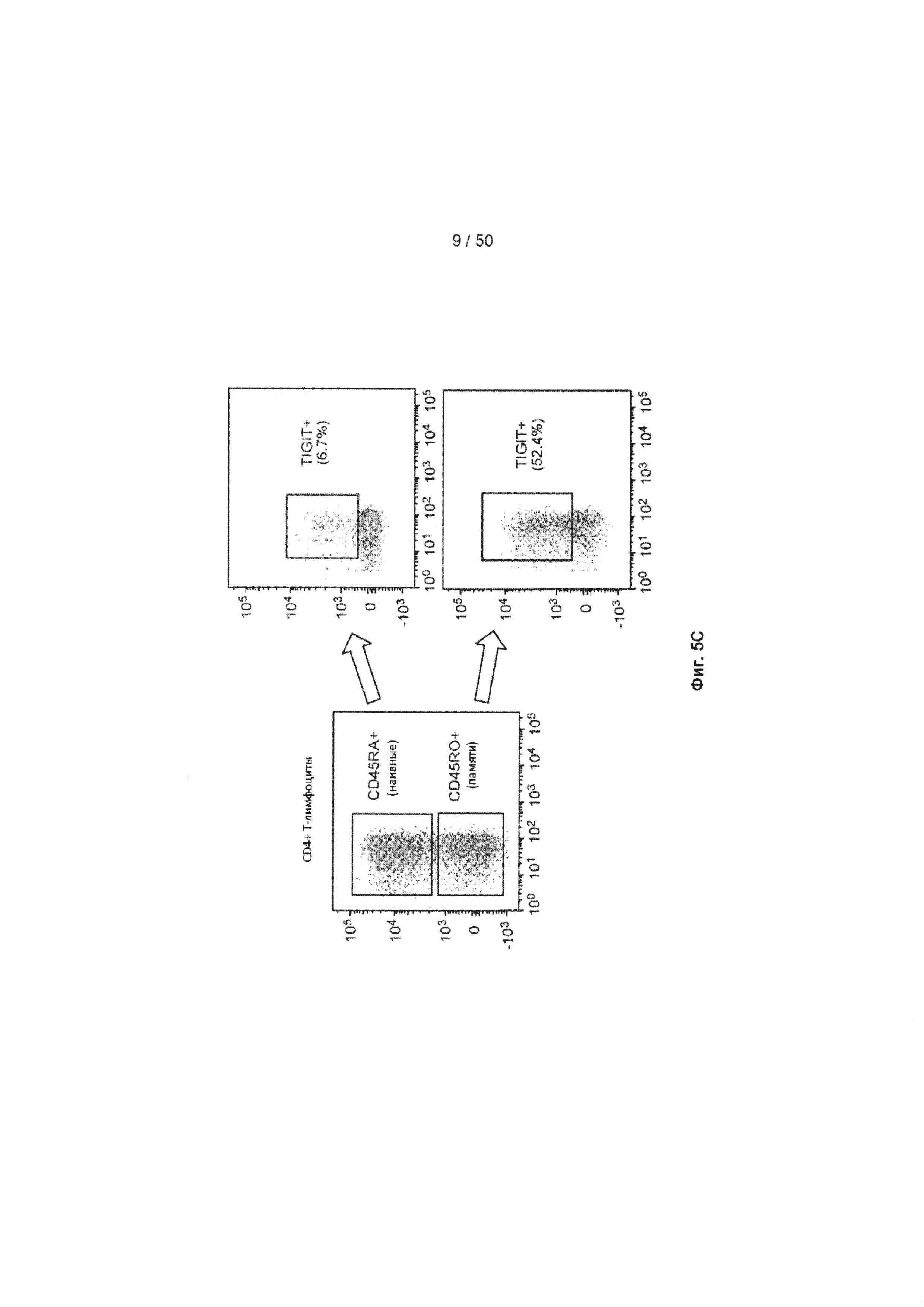
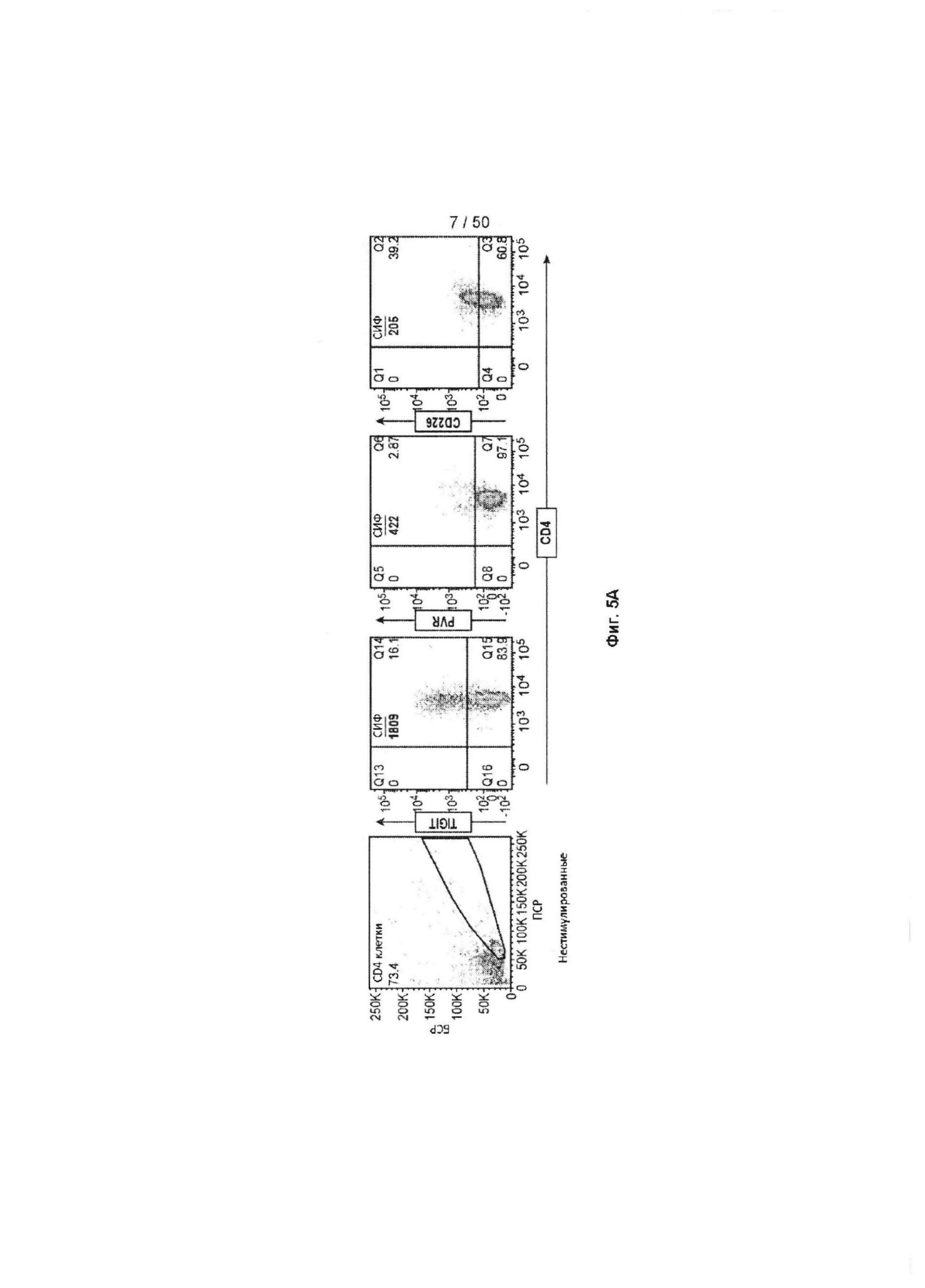
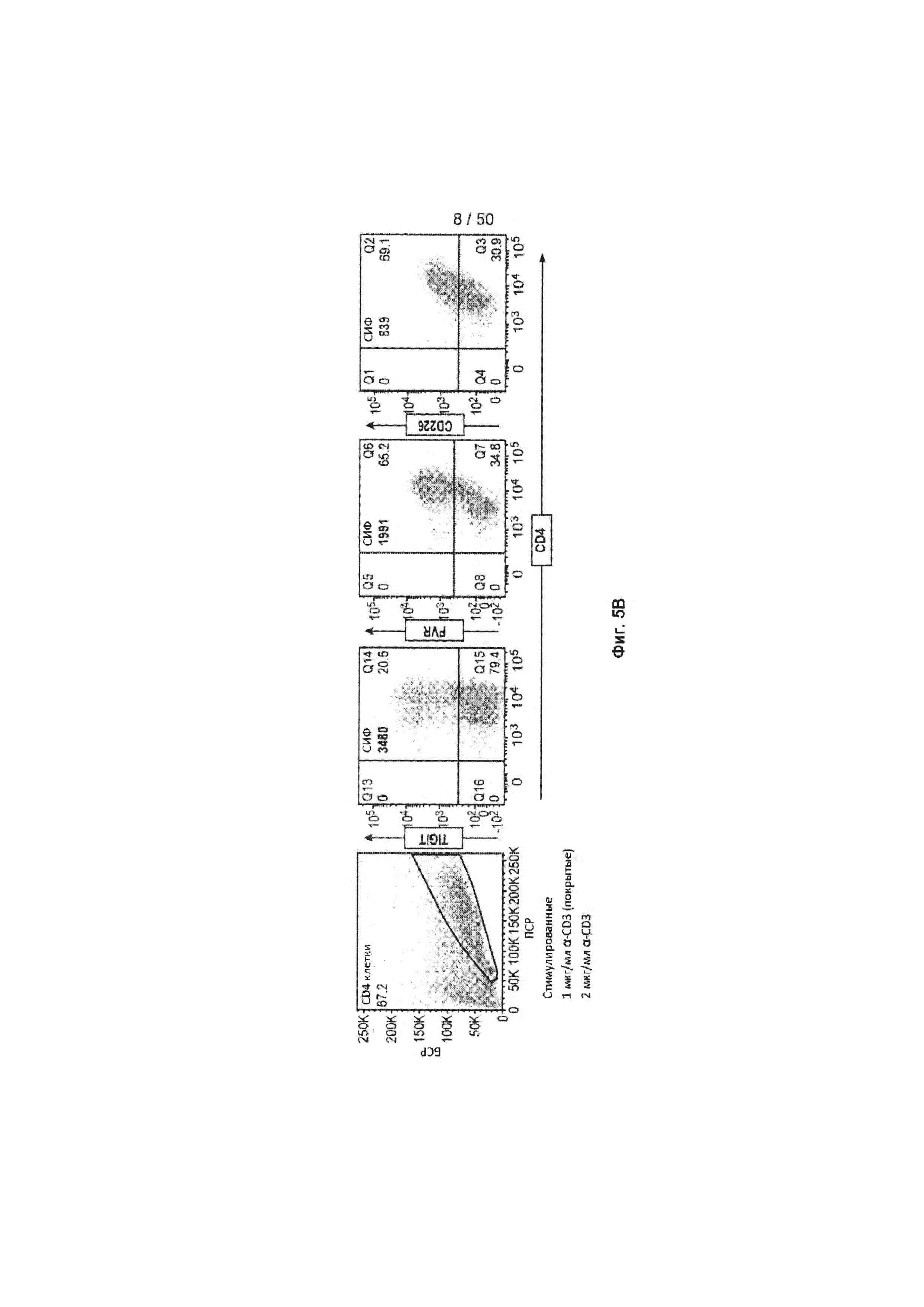
[0061] На Фиг. 5А-5С показан анализ экспрессии TIGIT на CD4+ Т-лимфоцитах человека с помощью FACS. На Фиг. 5А и 5В показан ряд графиков, показывающих анализ экспрессии TIGIT, PVR и CD226 на нестимулированных (Фиг. 5А) и стимулированных (Фиг. 5В) CD4+ Т-лимфоцитах. На Фиг. 5С показан анализ экспрессии TIGIT на наивном CD4+ Т-лимфоците (позитивный по CD45RA, маркере наивных Т-лимфоцитов, верхняя правая панель) и CD4+ Т-лимфоците памяти (позитивный по CD45RO, маркере активированных Т-лимфоцитов, нижняя правая панель).
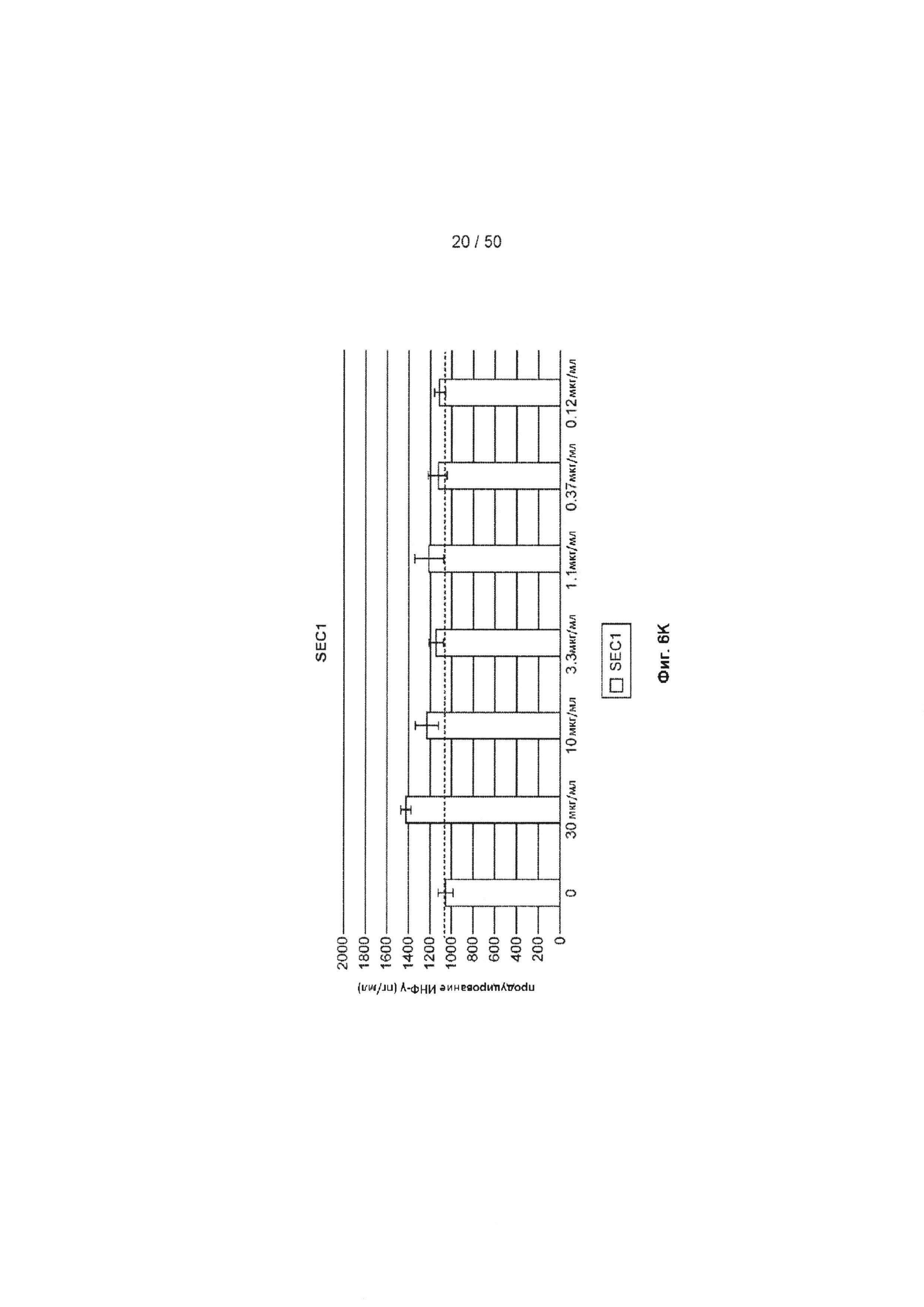
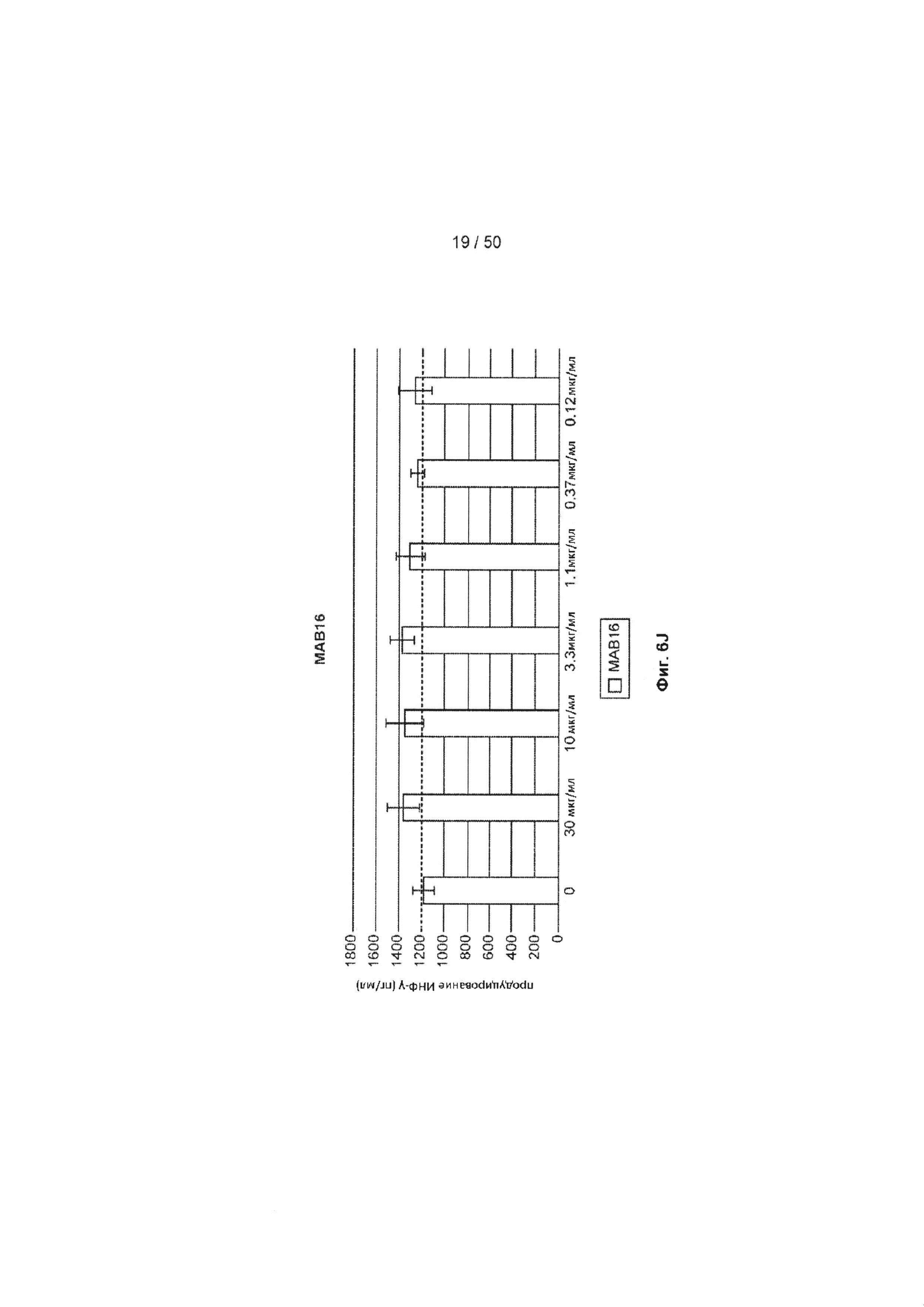
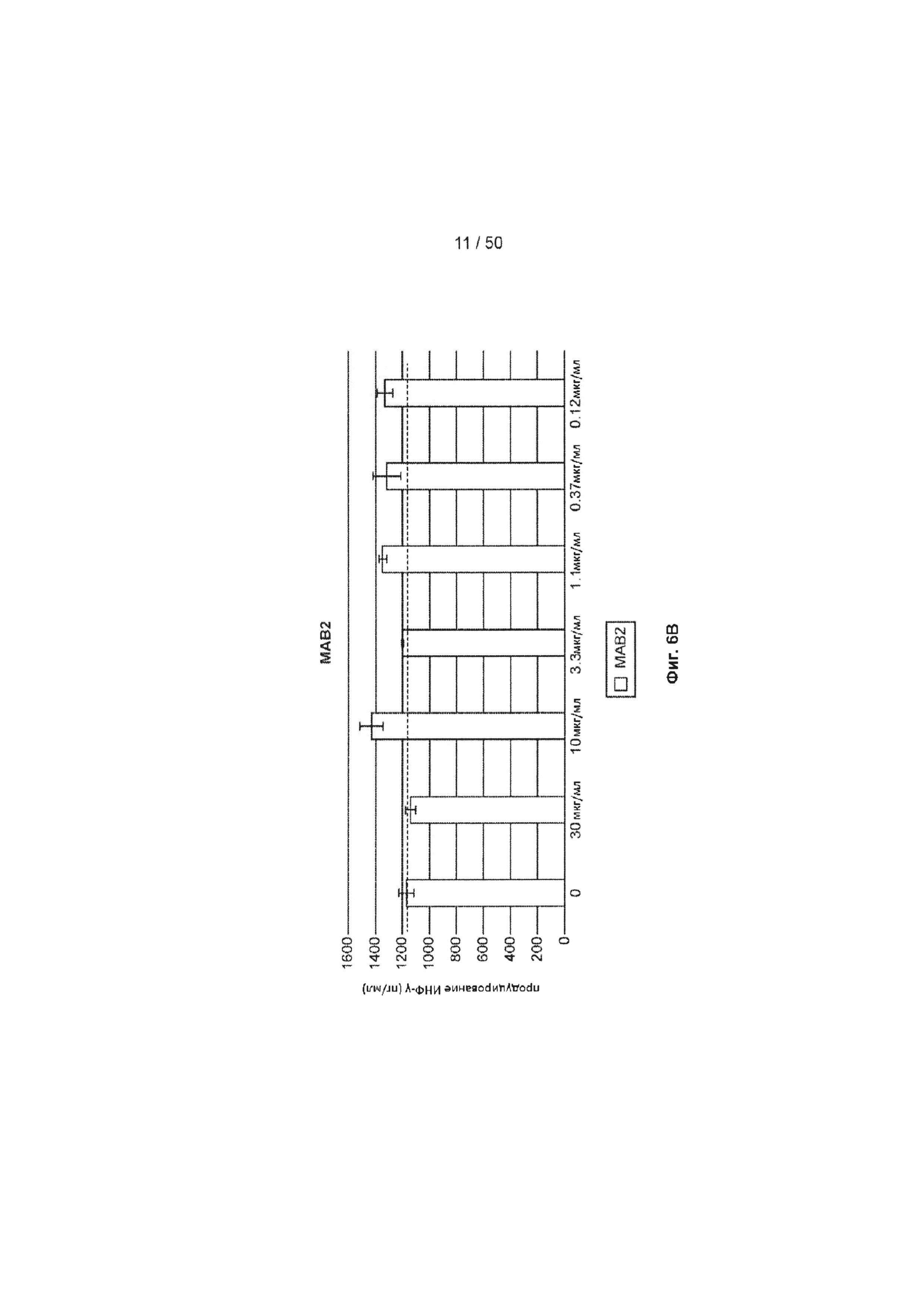
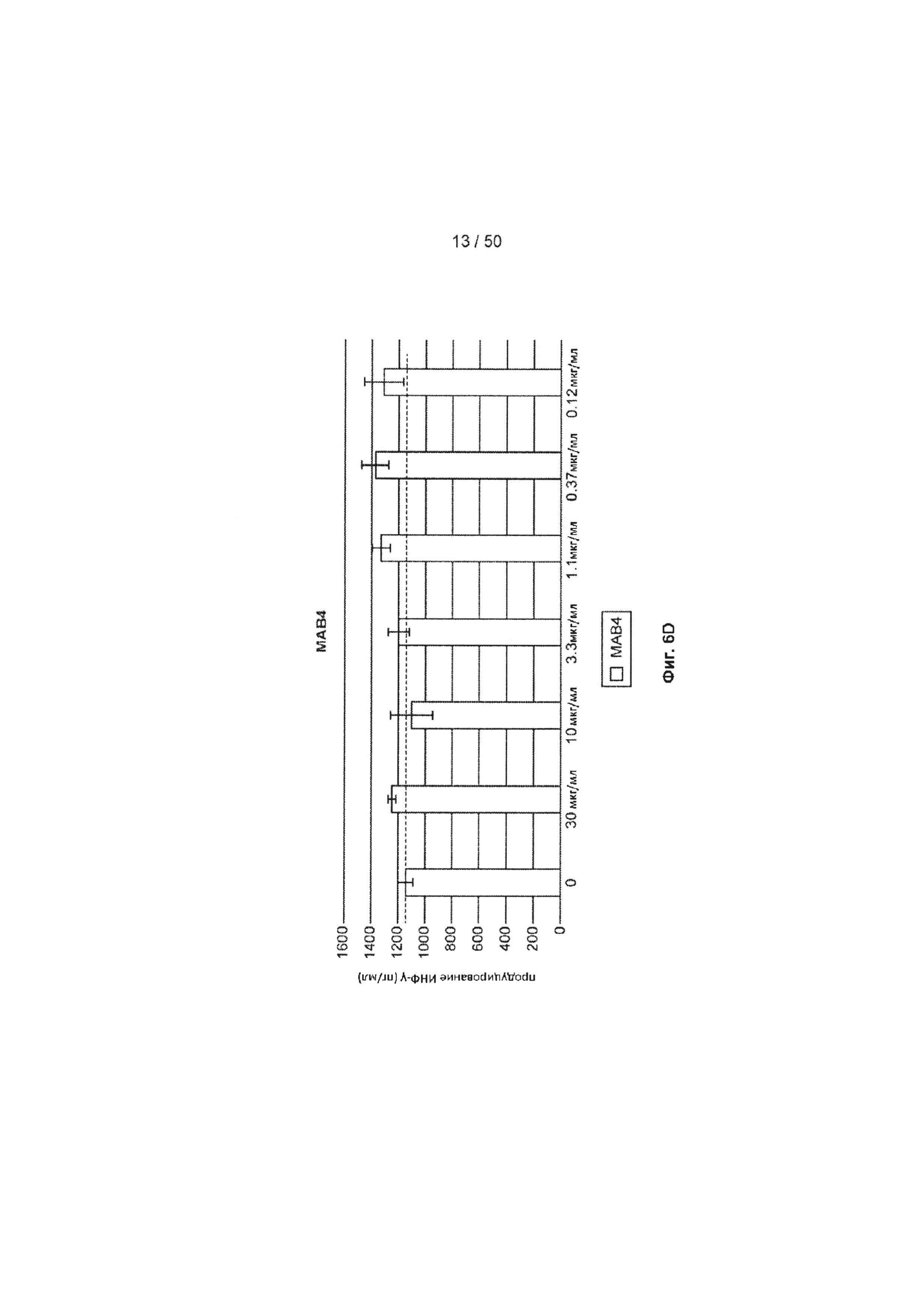
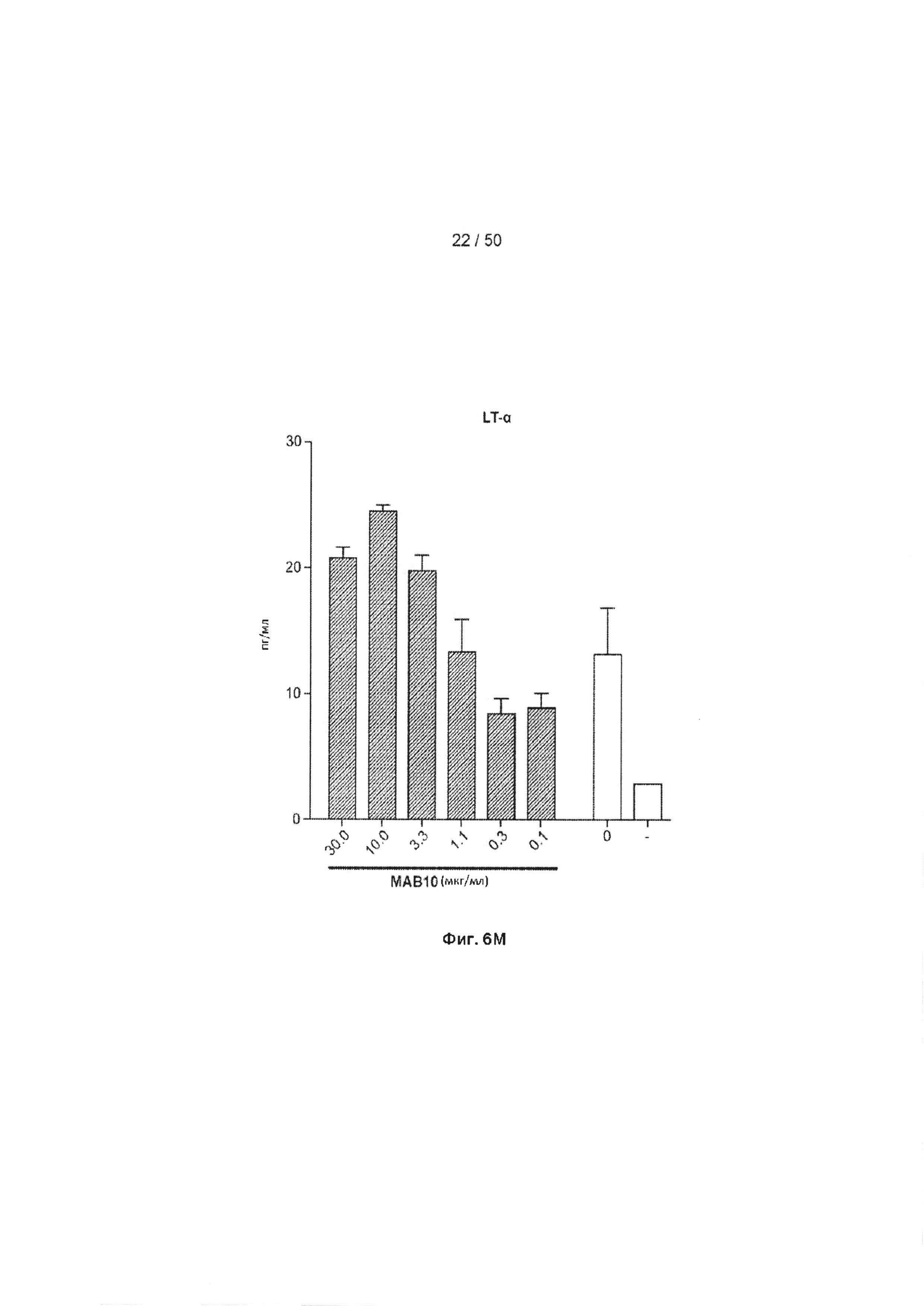
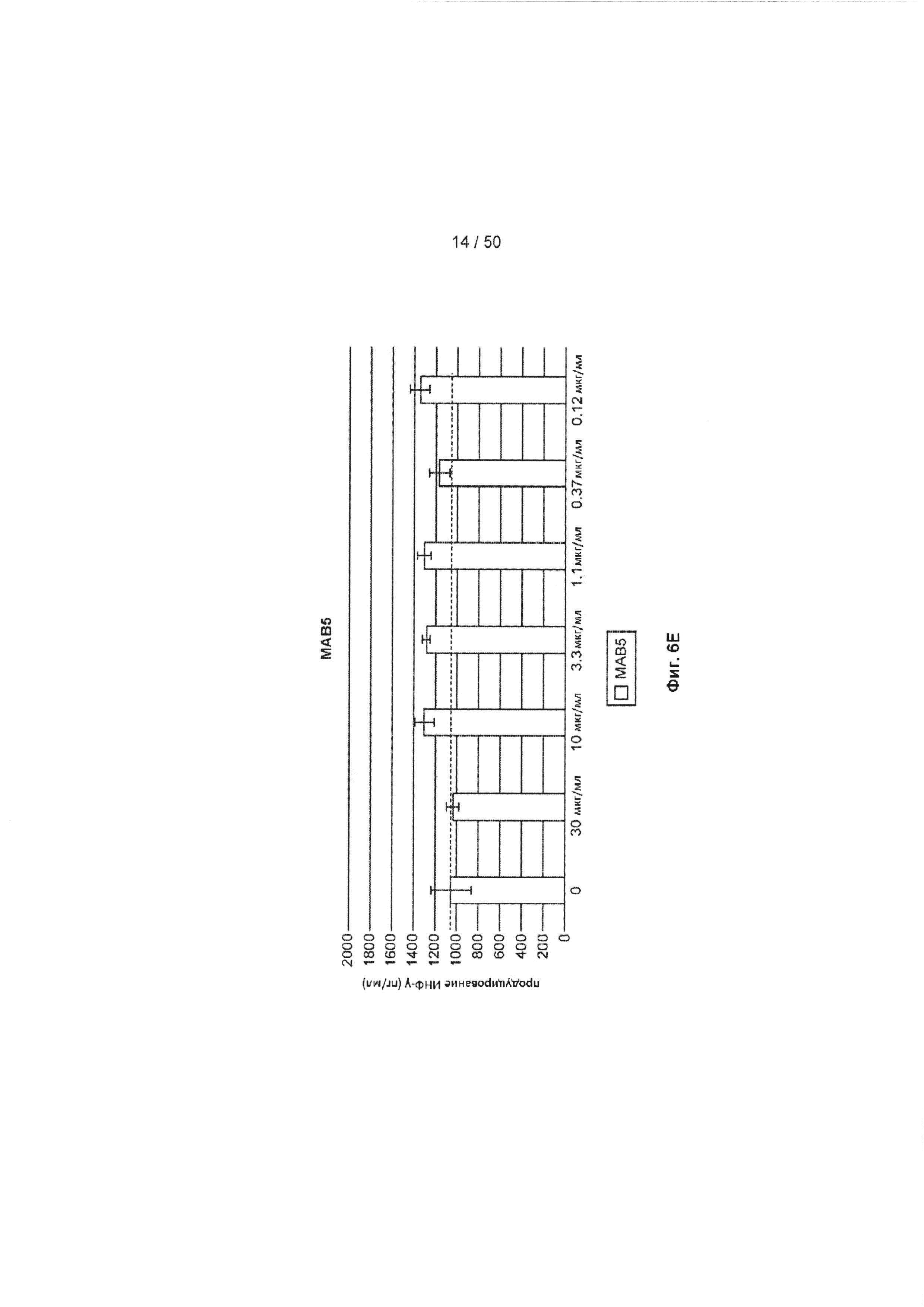
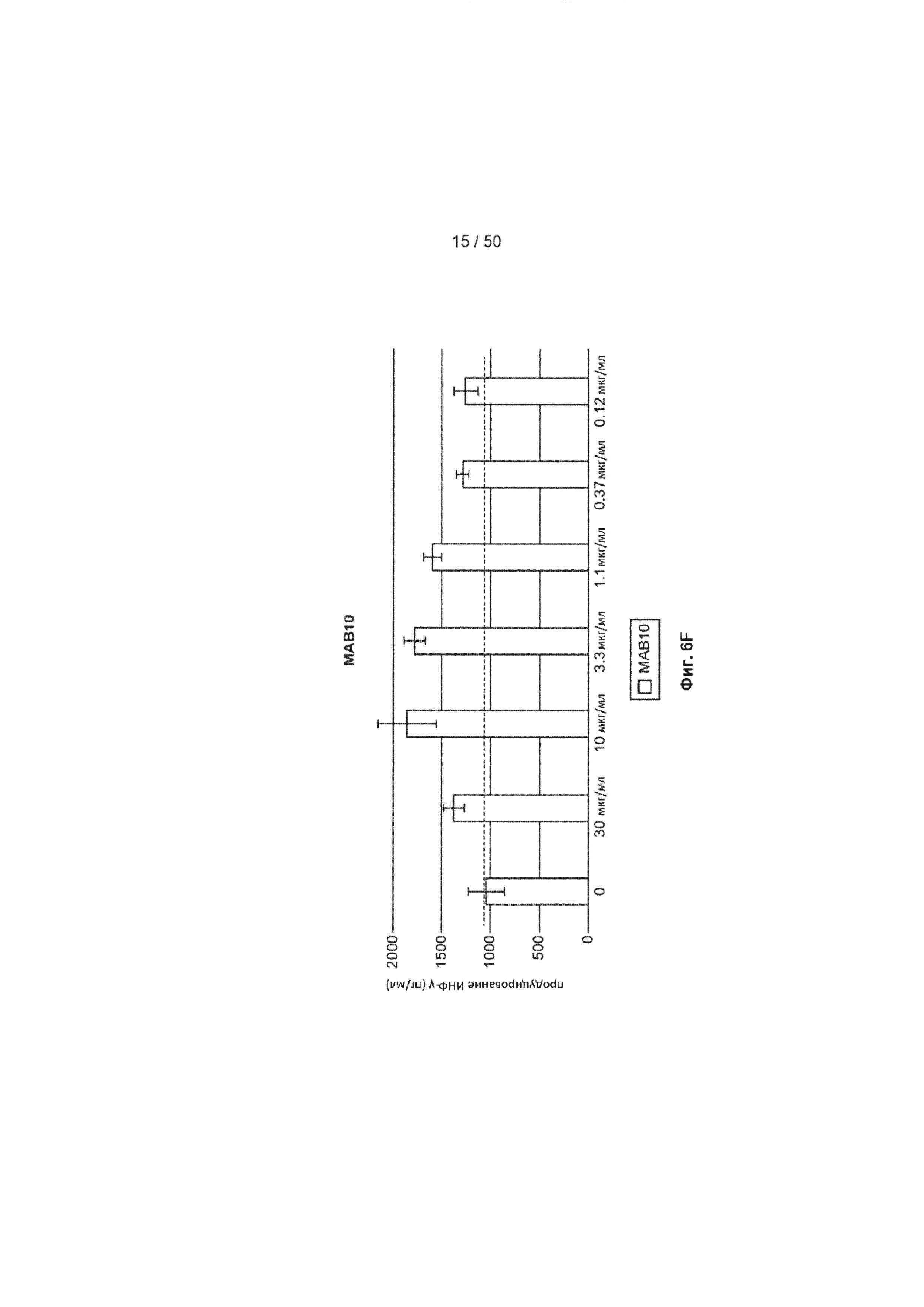
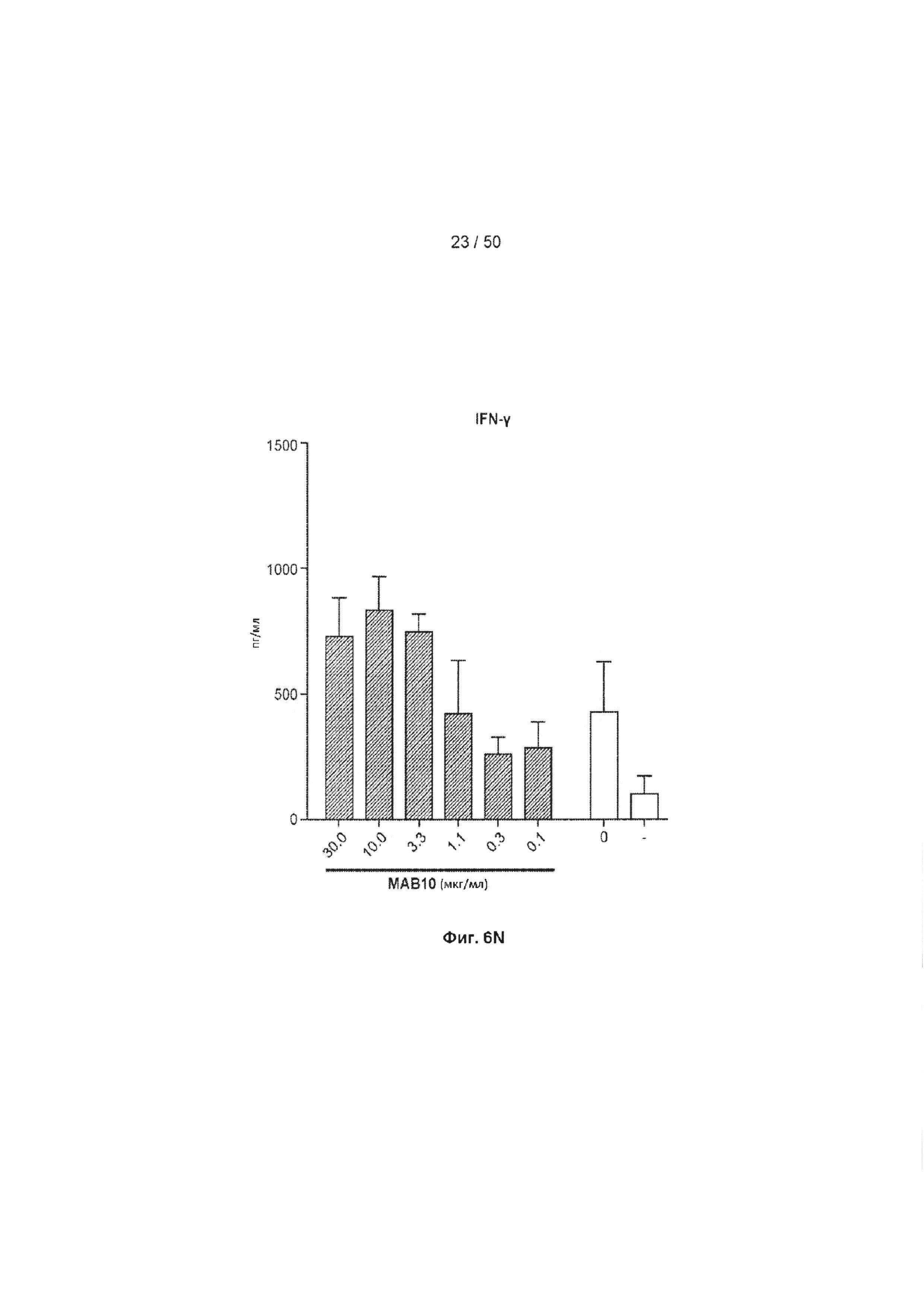
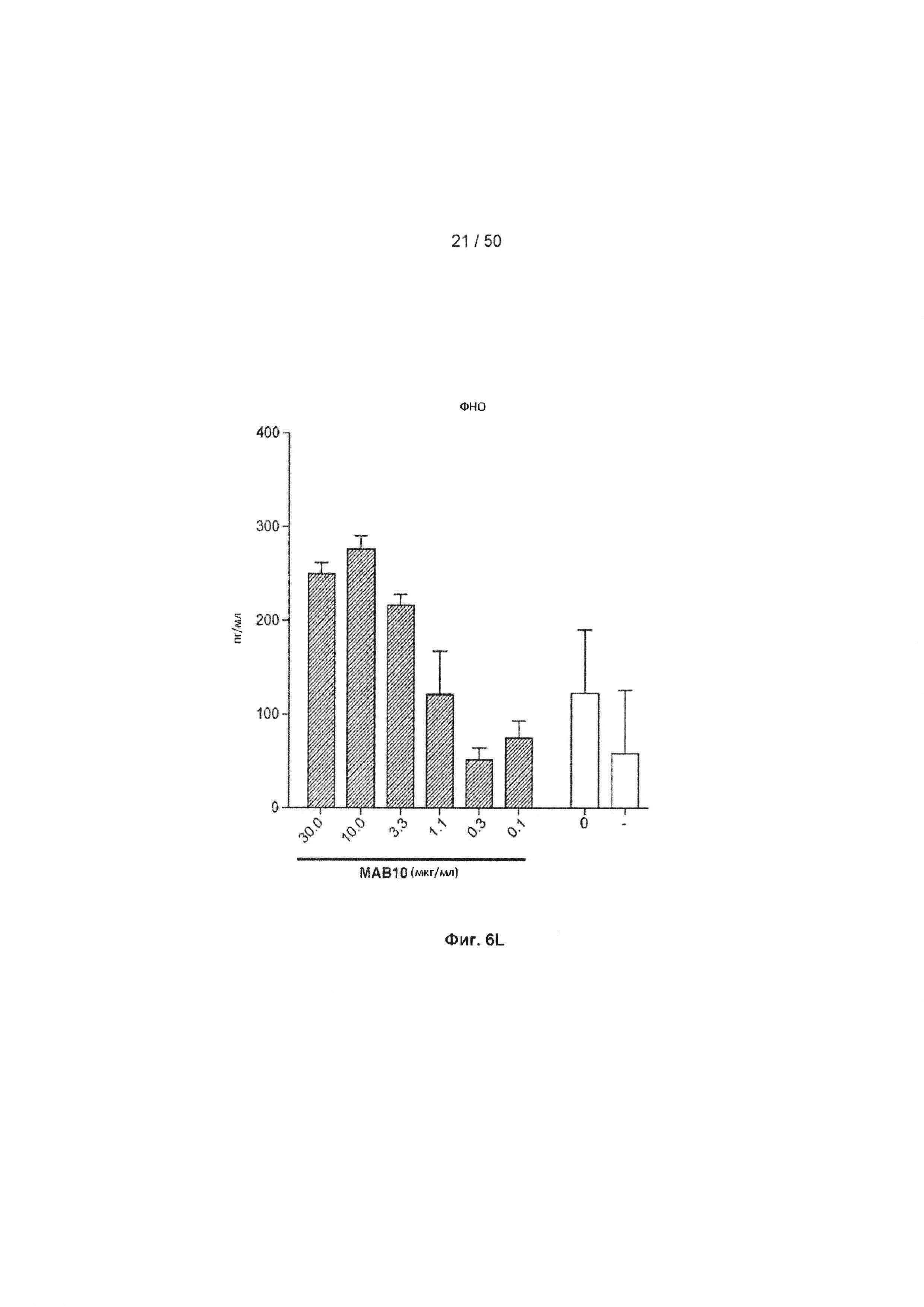
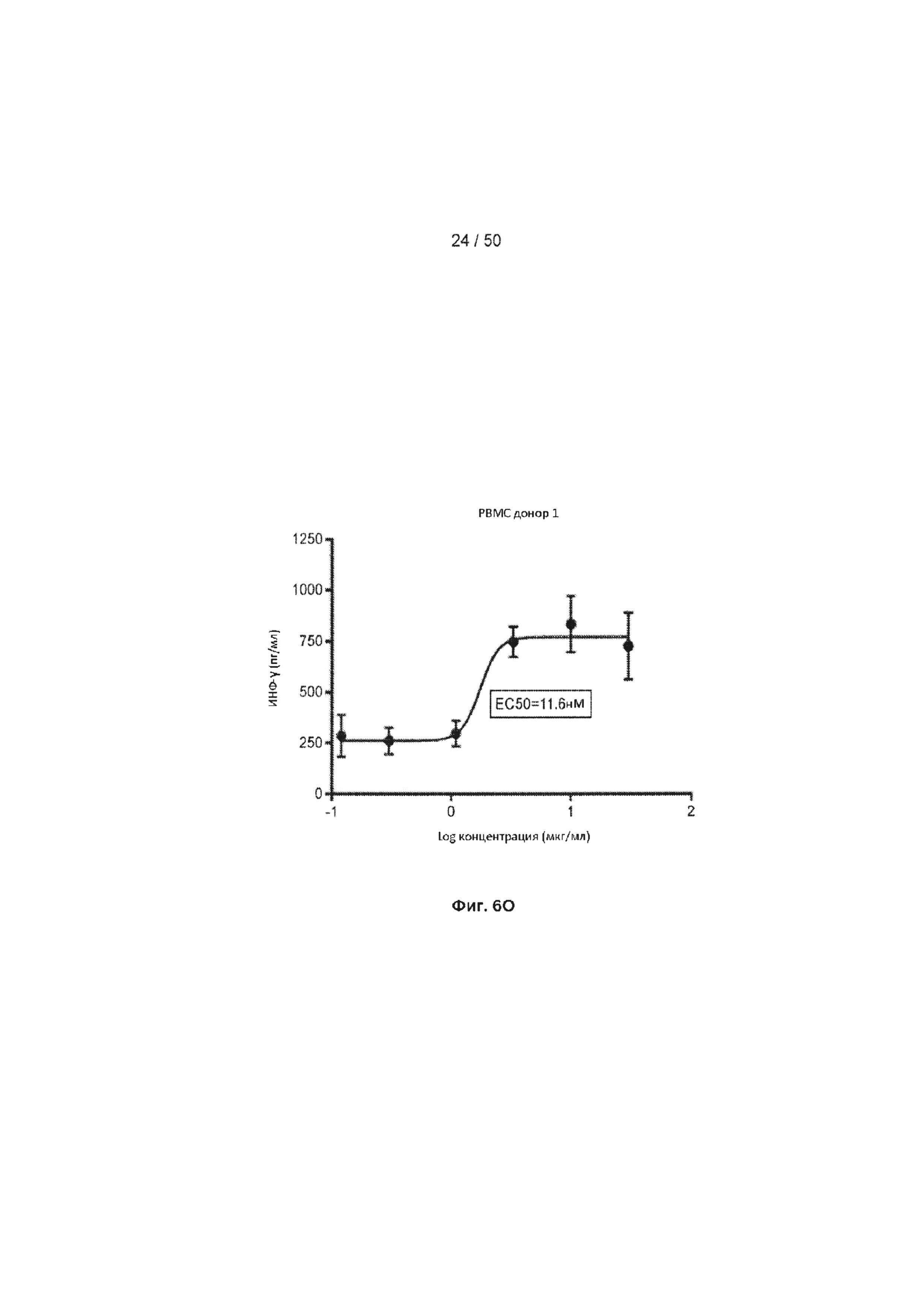
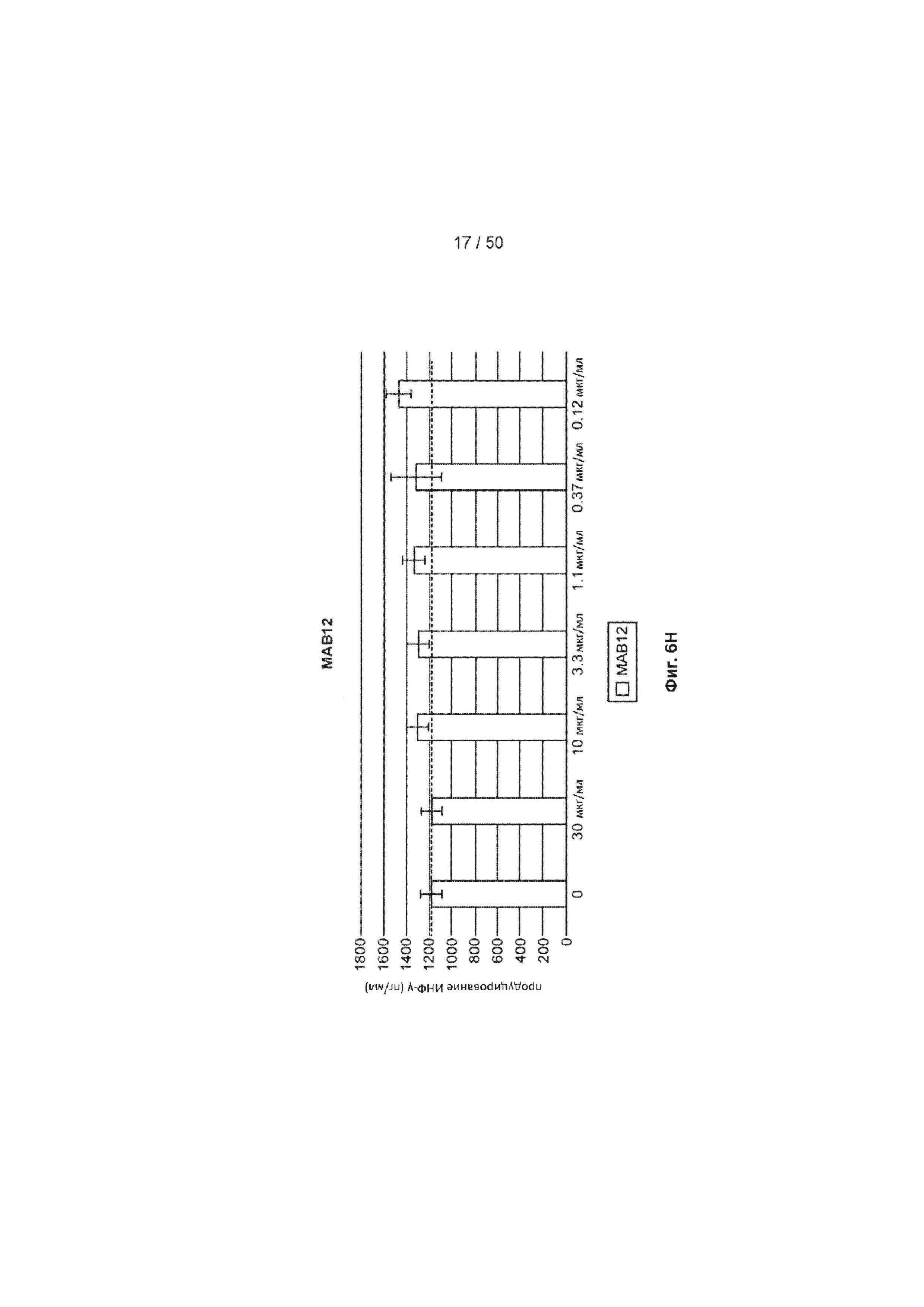
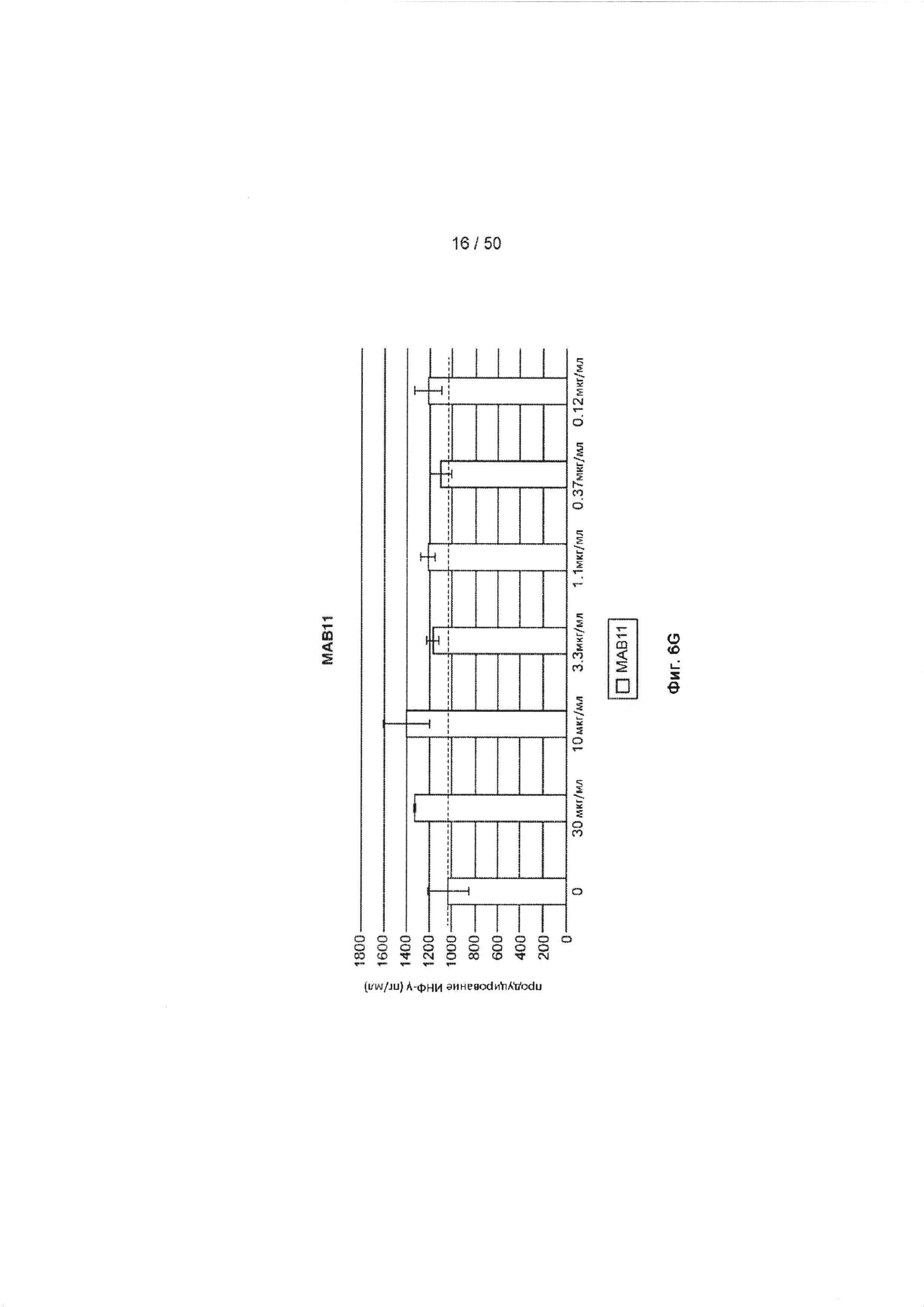
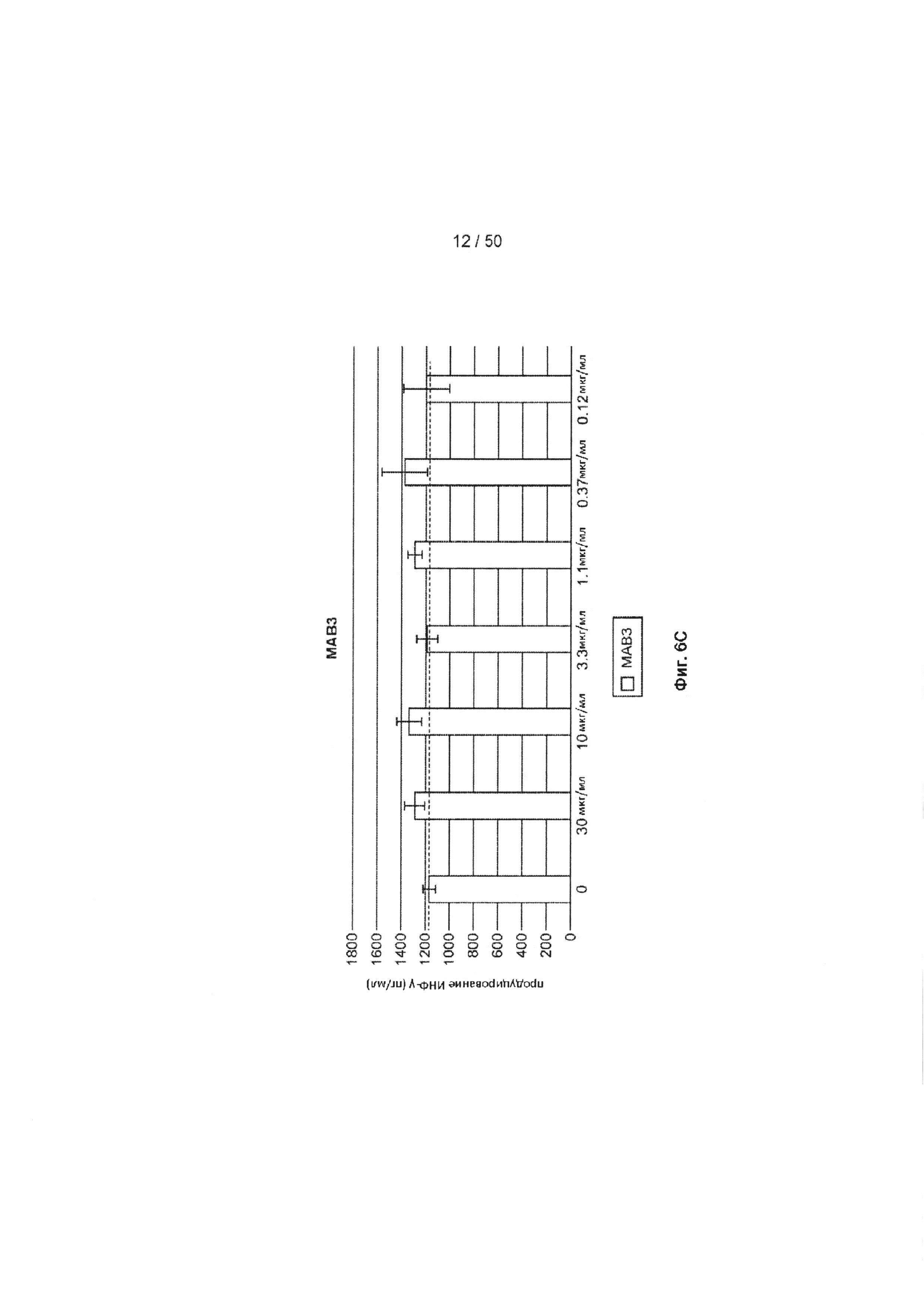
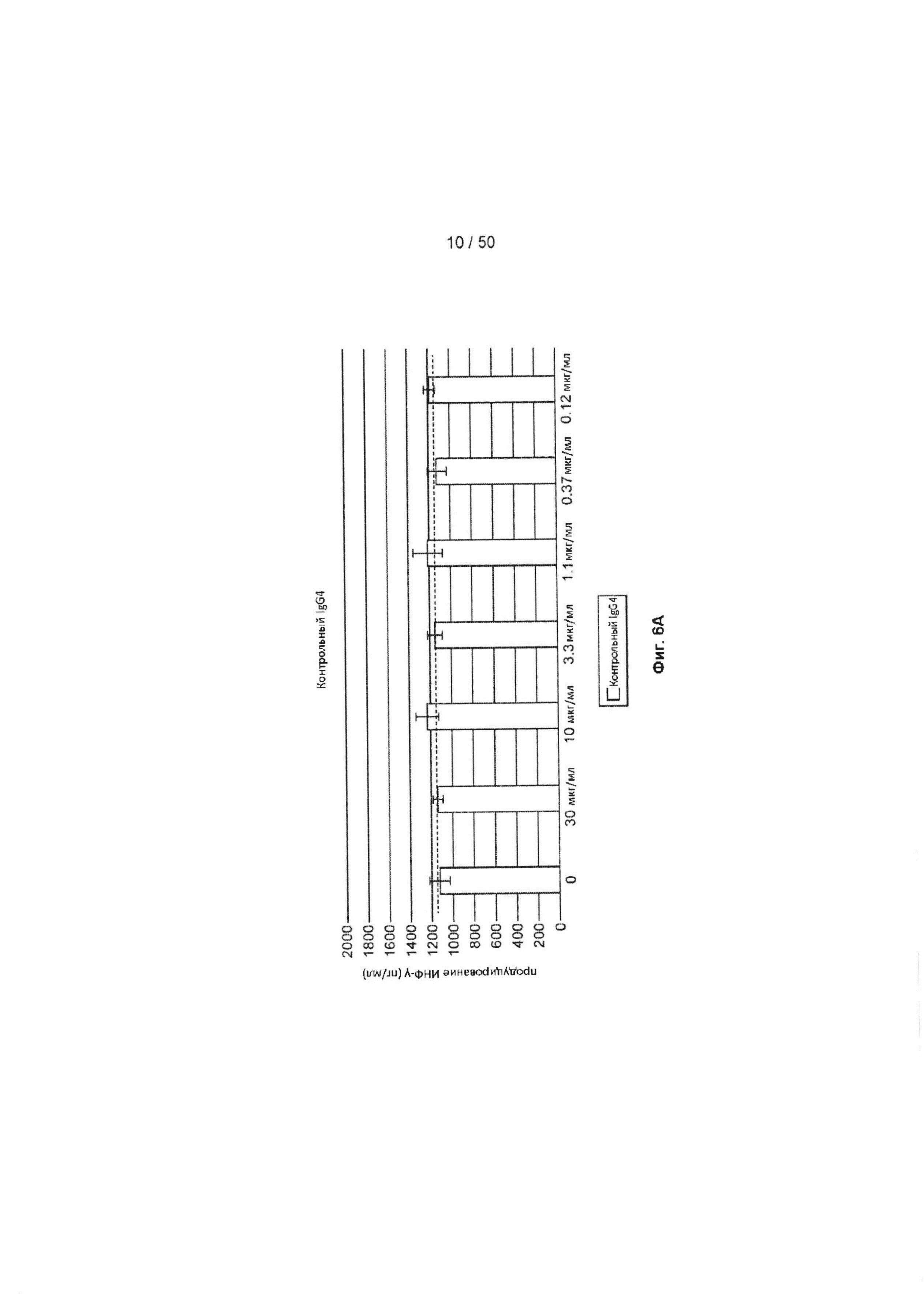
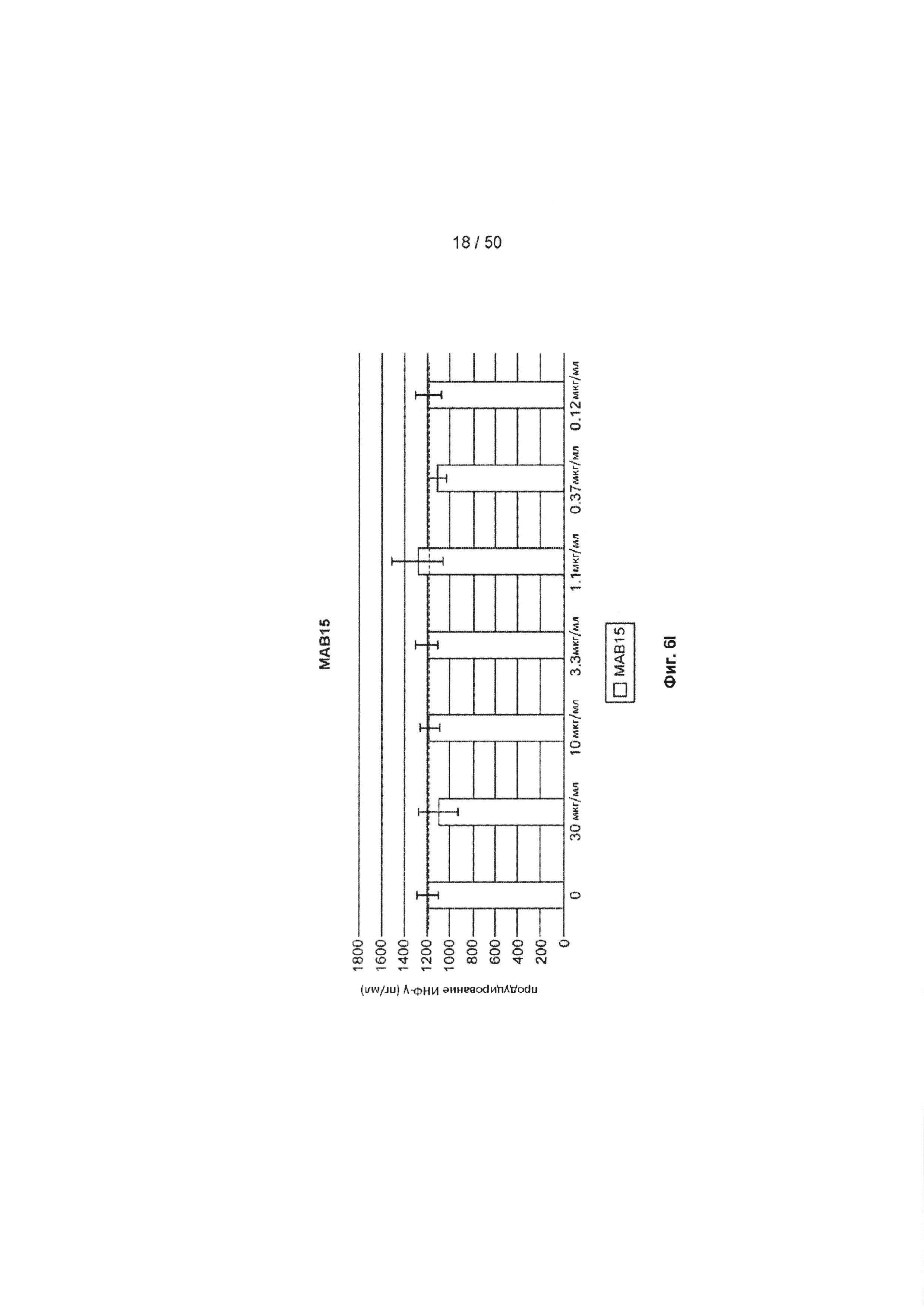
[0062] На Фиг. 6А-6O показан эффект лечения с помощью МАБ на субоптимально стимулированных МКПК из человеческих доноров. МАБ тестировали на их способность индуцировать ИНФ-γ в МКПК из человеческих доноров, включая контрольное антитело IgG4 (Фиг. 6А), МАБ2 (Фиг. 6В), МАБ3 (Фиг. 6С), МАБ4 (Фиг. 6D), МАБ5 (Фиг. 6Е), МАБ10 (Фиг. 6F), МАБ11 (Фиг. 6G), МАБ12 (Фиг. 6Н), МАБ15 (Фиг. 6I), МАБ16 (Фиг. 6J) и SEC1 (антитело хомяка против TIGIT мыши, Фиг. 6K). Обработка МКПК из донора 1 с помощью МАБ10 вызывает повышение экспрессии нескольких провоспалительных цитокинов, включая фактор некроза опухоли альфа (ФНО, Фиг. 6L), лимфотоксин альфа (LT-α, Фиг. 6М) и интерферон-гамма (ИНФ-γ, Фиг. 6N). На Фиг. 6O показан график, иллюстрирующий ЕС50 МАБ10 в МКПК из донора 1, как измерено по продуцированию ИНФ-γ.
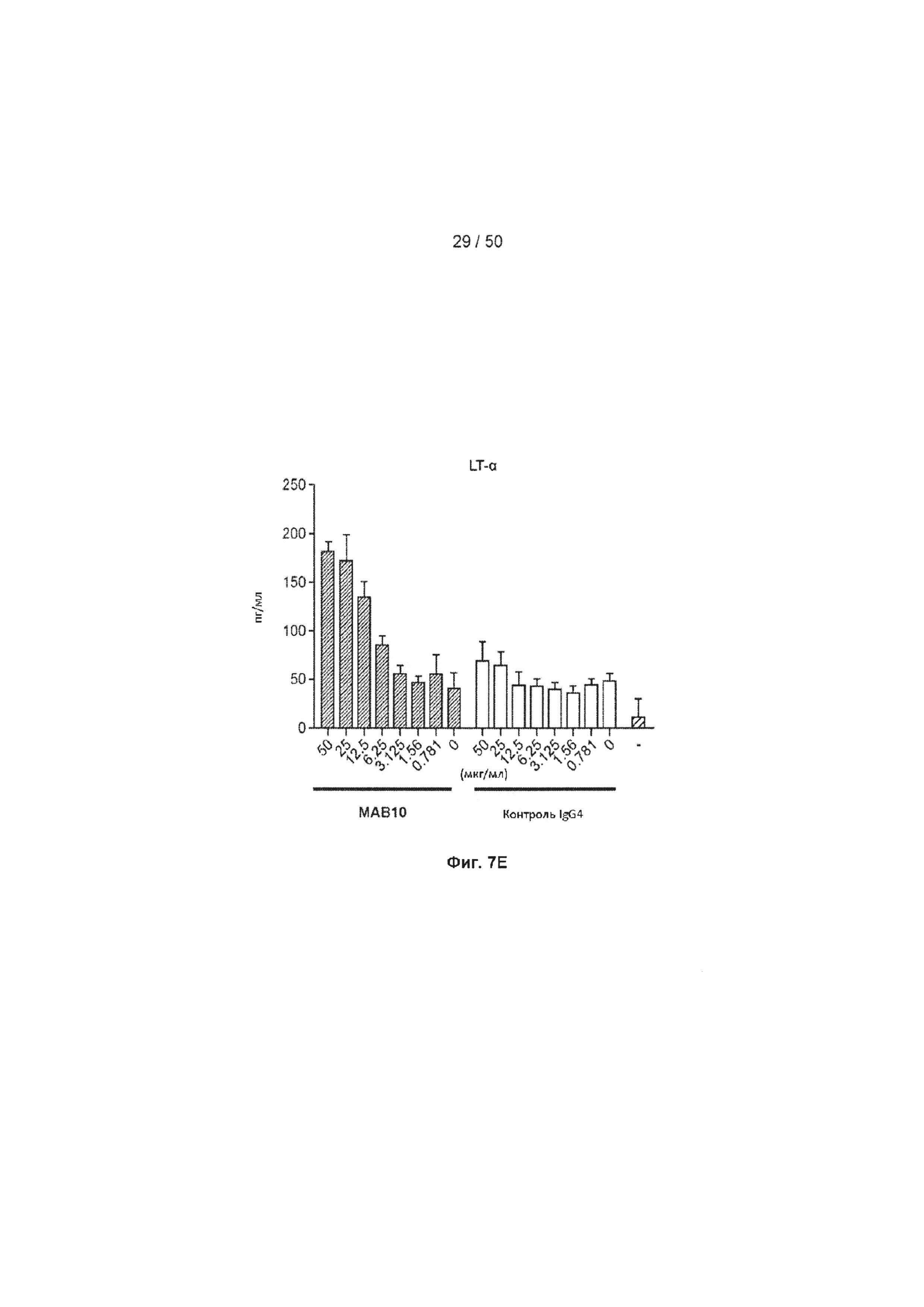
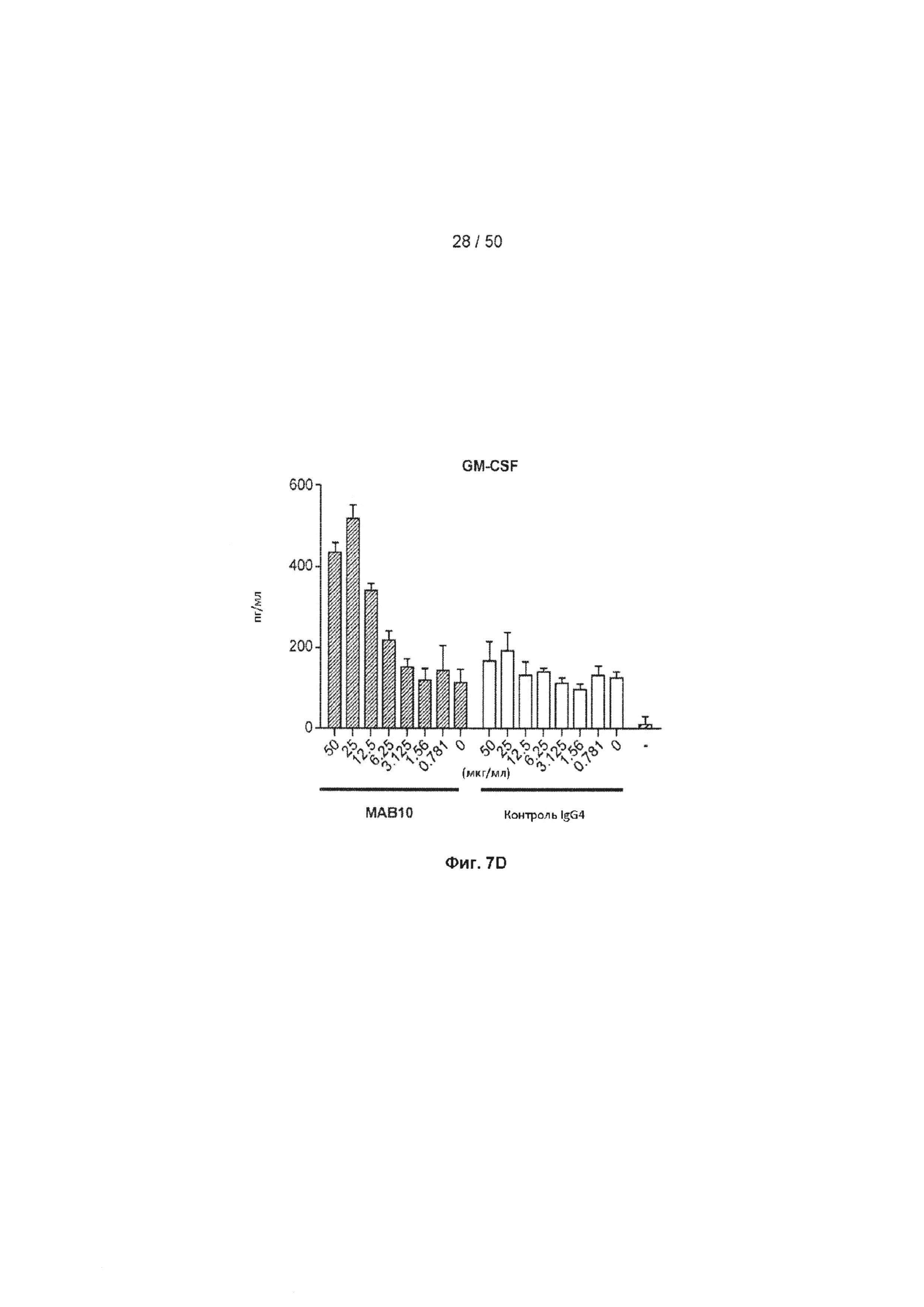
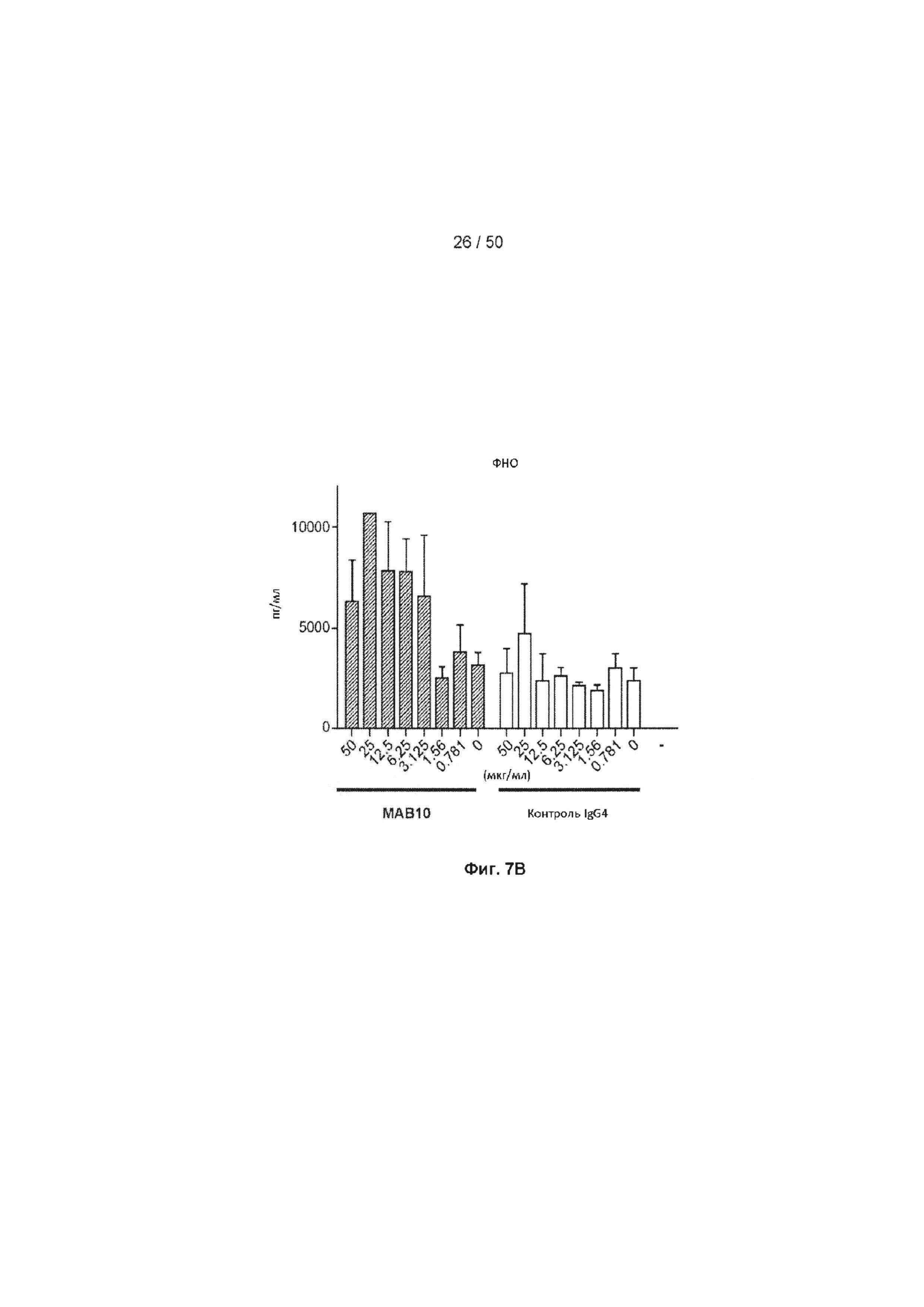
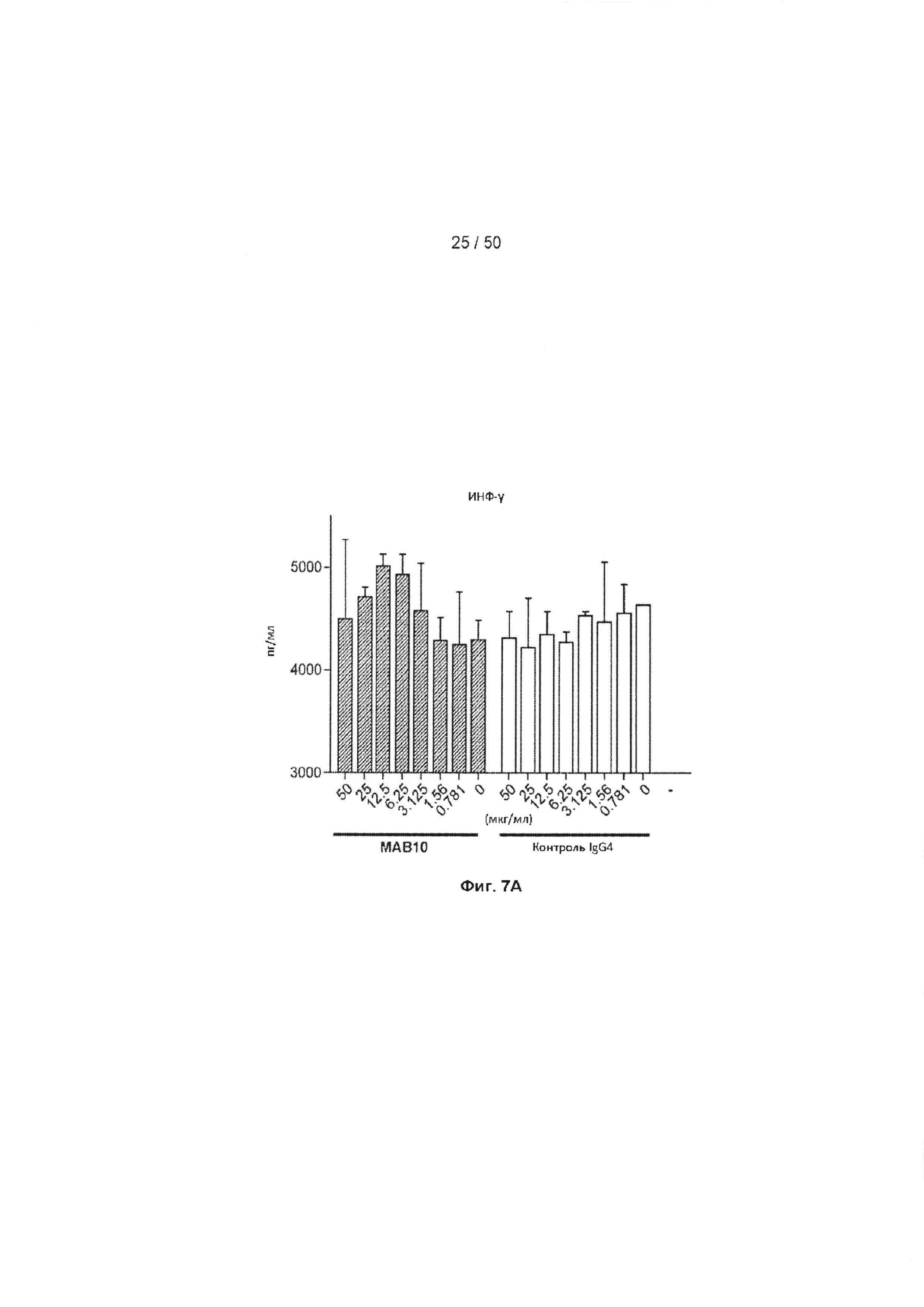
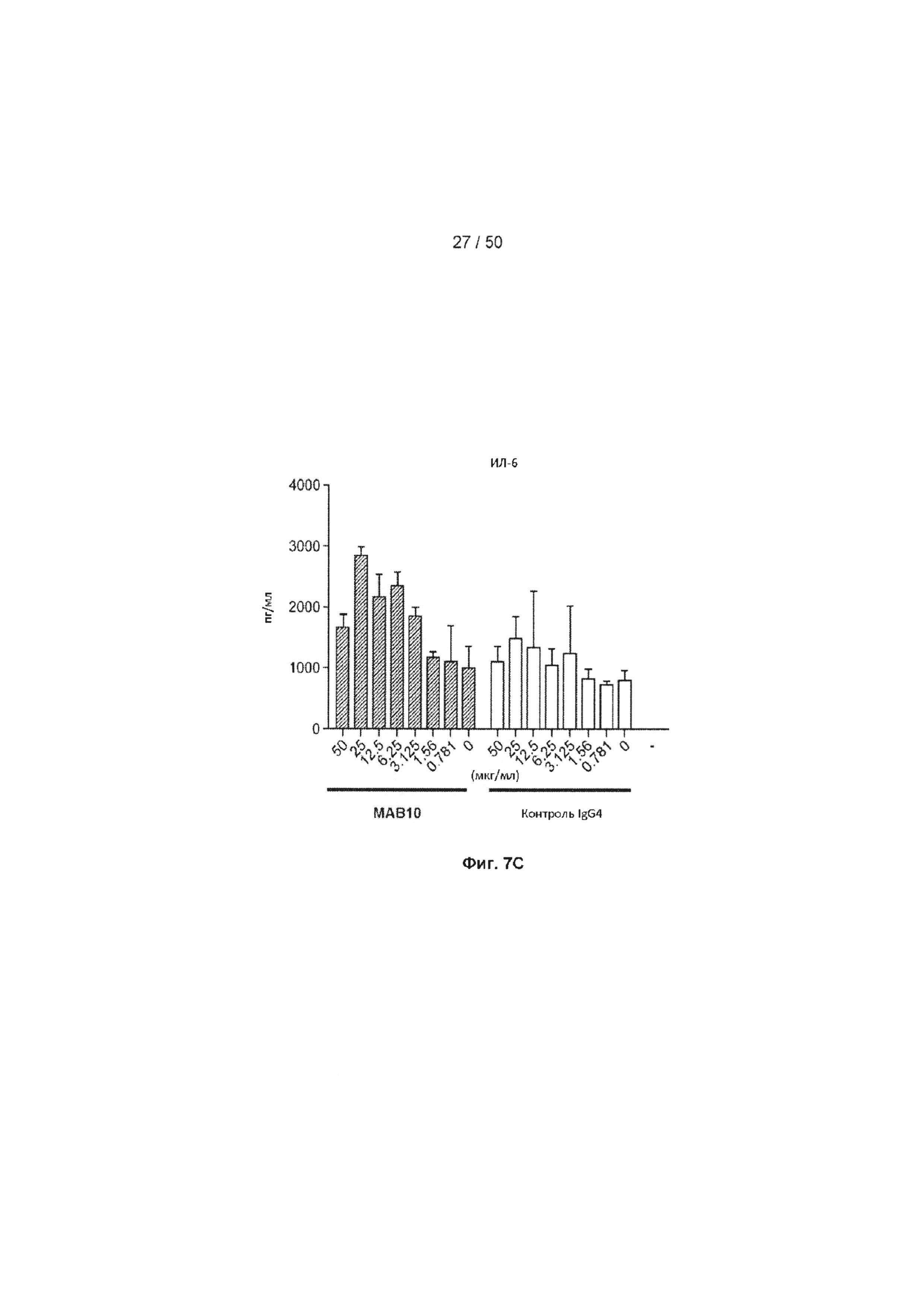
[0063] На Фиг. 7А-7Е представлена серия графиков, показывающих влияние МАБ10 на секрецию цитокинов в субоптимально стимулированных МКПК из донора 2, включая ИНФ-γ (Фиг. 7А), ФНО (Фиг. 7В), интерлейкин 6 (ИЛ-6, Фиг. 7С), гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF, Фиг. 7D) и LT-α (Фиг. 7Е). Данные из клеток, обработанных МАБ10, показаны как черные столбцы, а данные из клеток, обработанных изотипом контрольного IgG4, показаны как светло-серые столбцы. Концентрация антитела для каждого столбца указана в мкг/мл.
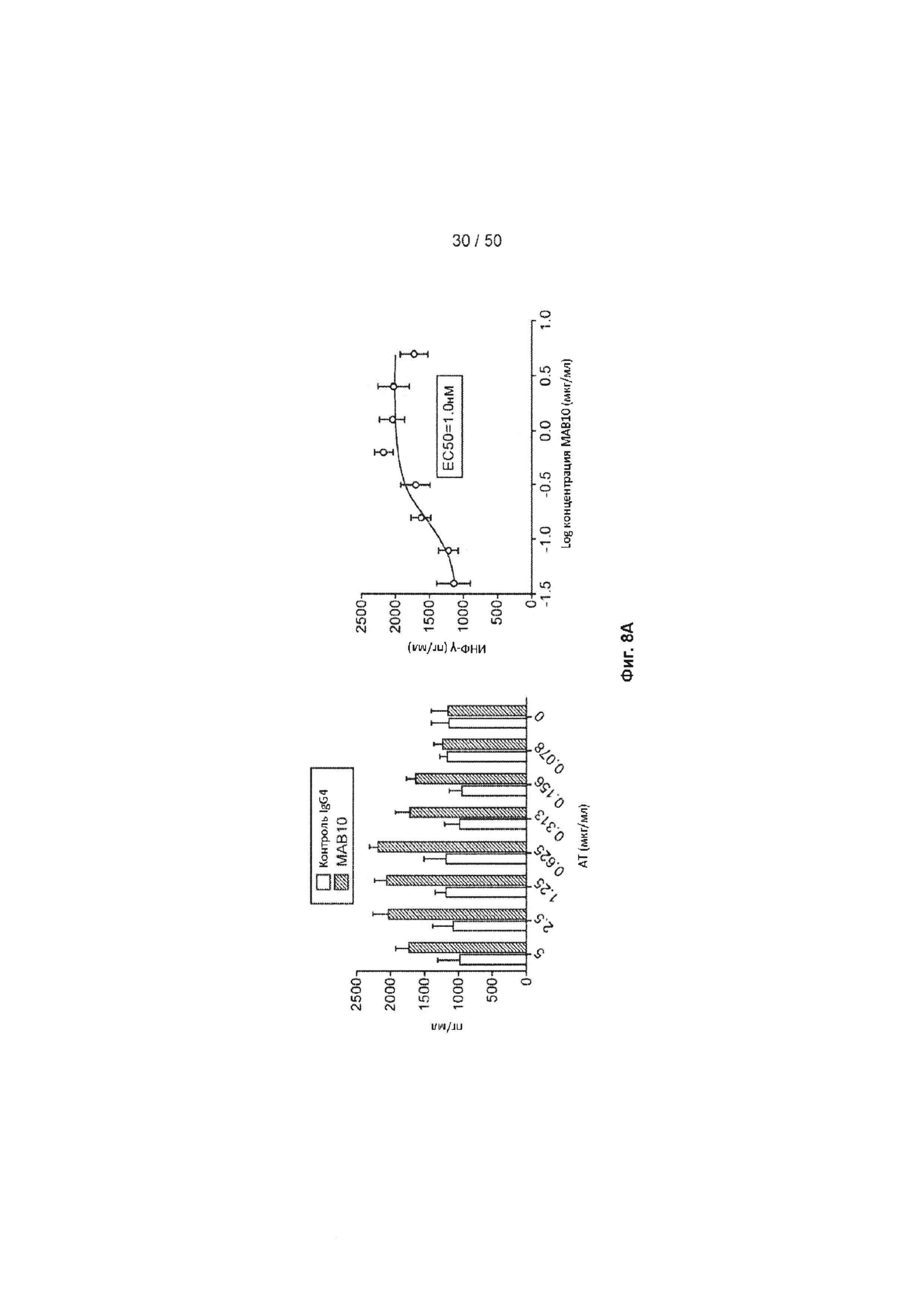
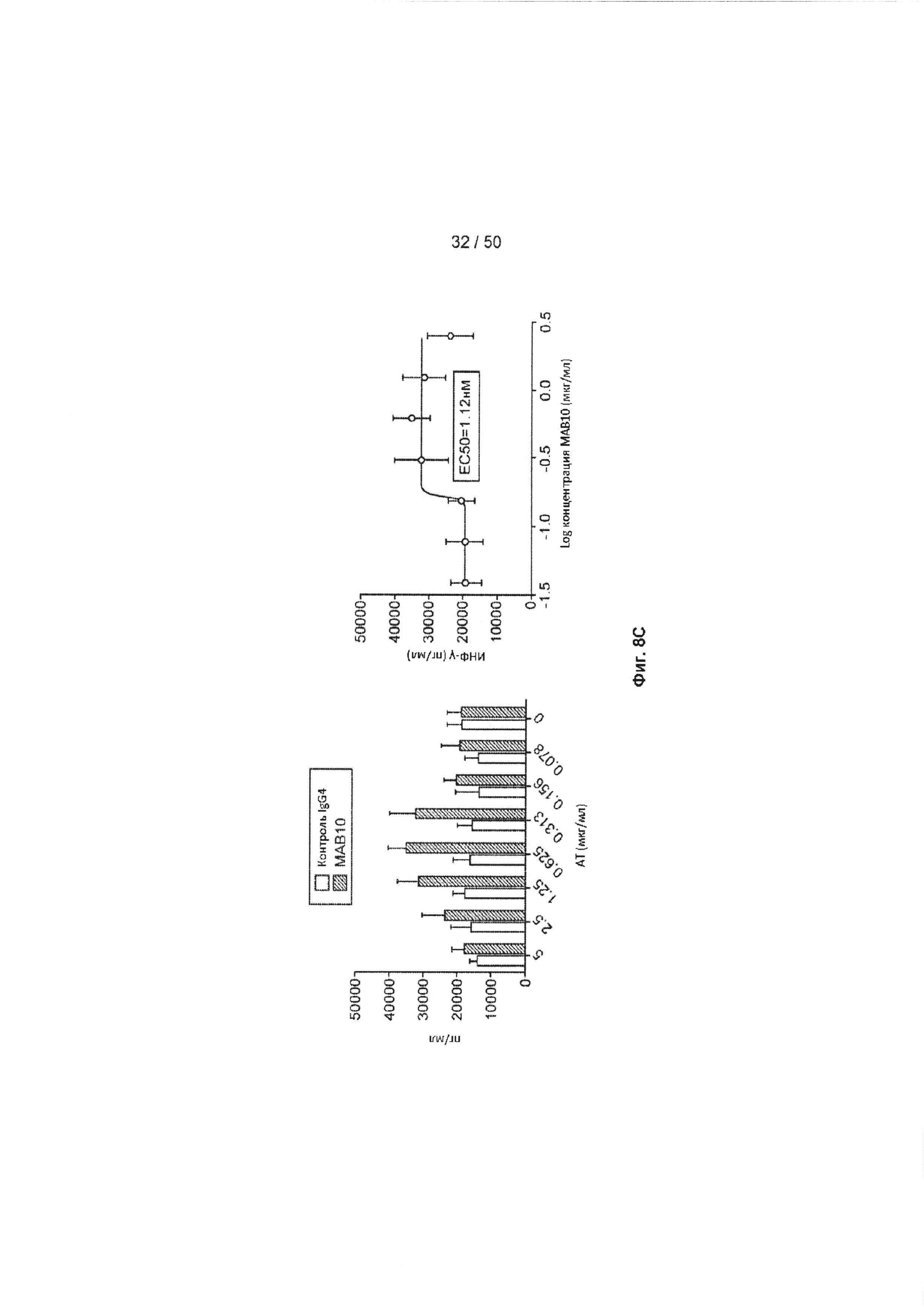
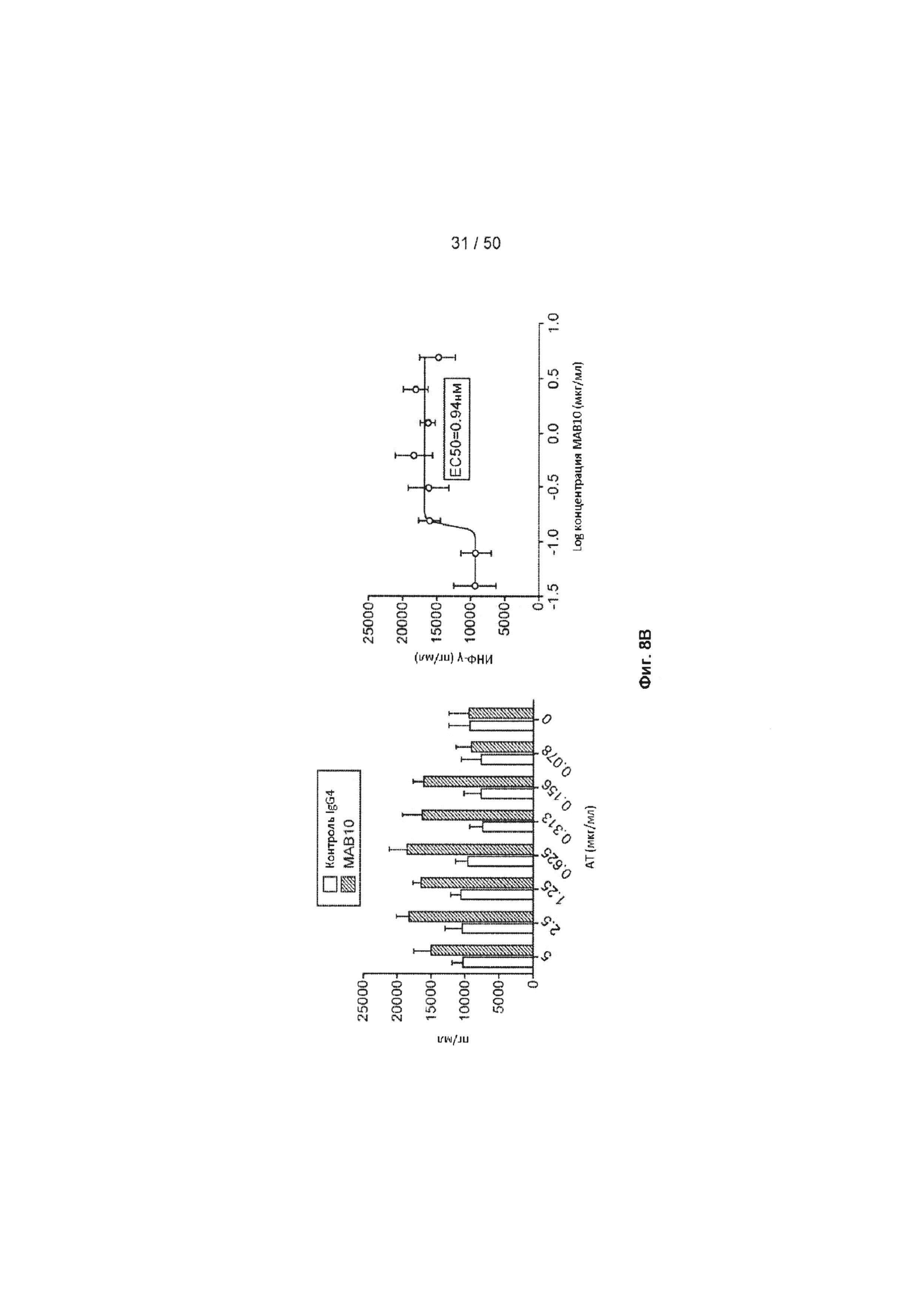
[0064] На Фиг. 8А-8С представлен ряд графиков, показывающих, что антагонистическое анти-TIGIT антитело МАБ10 увеличивает ИФН-γ в анализе CD4+ клеток с применением клеток, полученных от трех разных доноров. На Фиг. 8А показаны результаты, полученные для CD4+ клеток, полученных от донора 1. На Фиг. 8В показаны результаты, полученные для CD4+ клеток, полученных от донора 2. На Фиг. 8С показаны результаты, полученные для CD4+ клеток, полученных от донора 3. Продуцирование ИНФ-γ в клетках, обработанных либо МАБ10 (черные столбцы), либо изотипом контрольного IgG4 (светло-серые столбцы), показано на левой панели каждой Фиг. 8А-8С. Среднее значение ЕС50 для МАБ10 в данном анализе рассчитывали путем определения концентрации МАБ10, необходимой для индукции 50% увеличения сигнала ИНФ-γ (нанесенного на график в правой панели каждой из Фиг. 8А-8С).
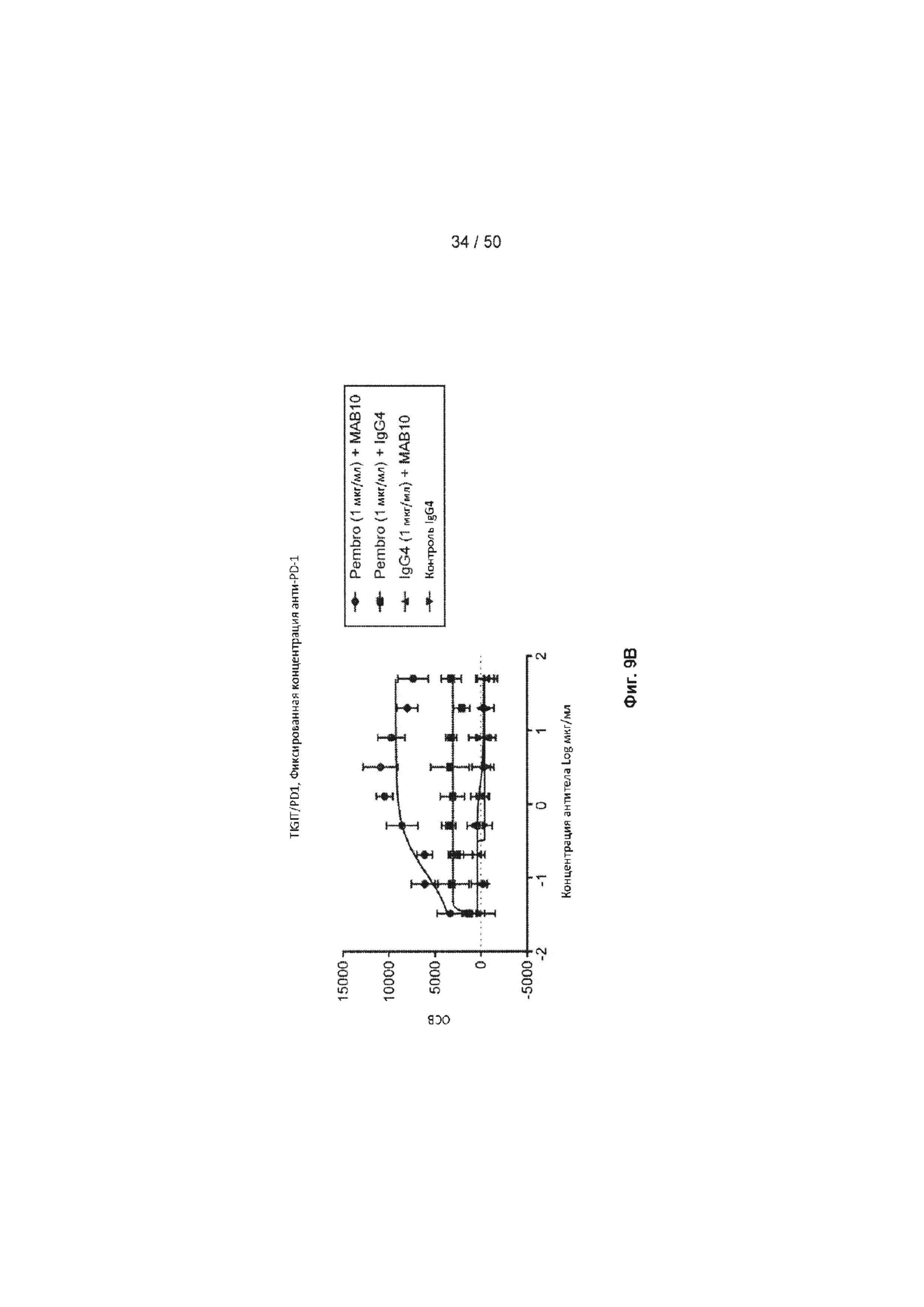
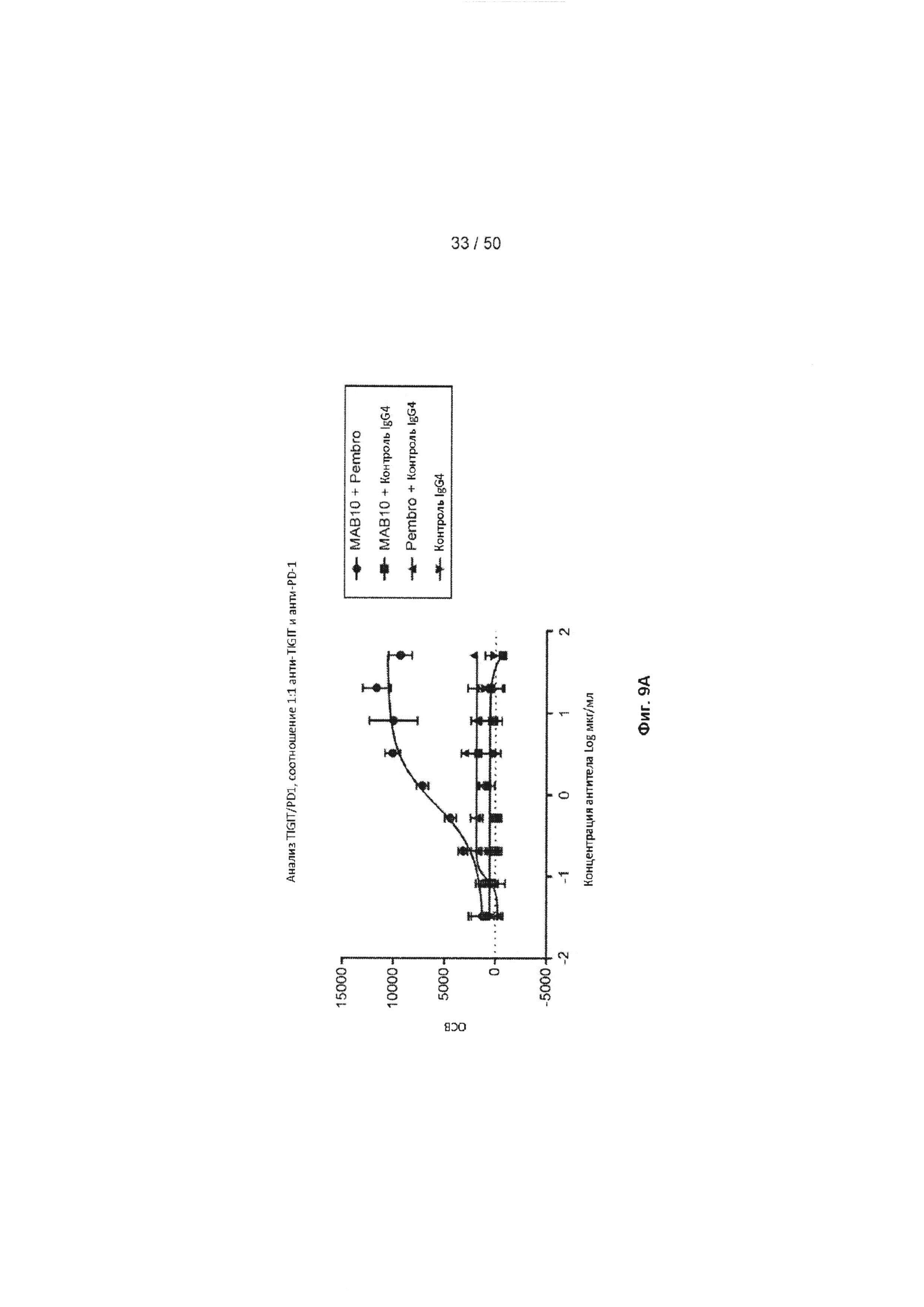
[0065] На Фиг. 9А показаны результаты анализа, в котором использовали соотношение 1:1 МАБ10 и пембролизумаба (анти-PD-1 антитело) в комбинированном биоанализе, основанном на механизме действия PD-1/TIGIT. Концентрации для каждого антитела составляли 25, 10, 4, 1,6, 0,64, 0,256, 0,1024, 0,04096 и 0,016384 мкг/мл. В качестве контроля использовали нецелевой IgG4. Как показано на Фиг. 9А, только комбинация МАБ10 и пембролизумаба (ЕС50 5,06 нМ) блокировала связывание в достаточной степени, чтобы индуцировать активность люциферазы в клетках Jurkat. На Фиг. 9В показаны результаты анализа с фиксированной дозой (1 мкг/мл) пембролизумаба (или контрольного IgG4) и варьирующей дозой МАБ10 (50, 20, 8, 3,2, 1,28, 0,512, 0,2048, 0,08192 и 0,032768 мкг/мл). На Фиг. 9А и 9В показано что, ни контрольный IgG4, ни комбинация IgG4 + МАБ10 не индуцировали активность люциферазы.
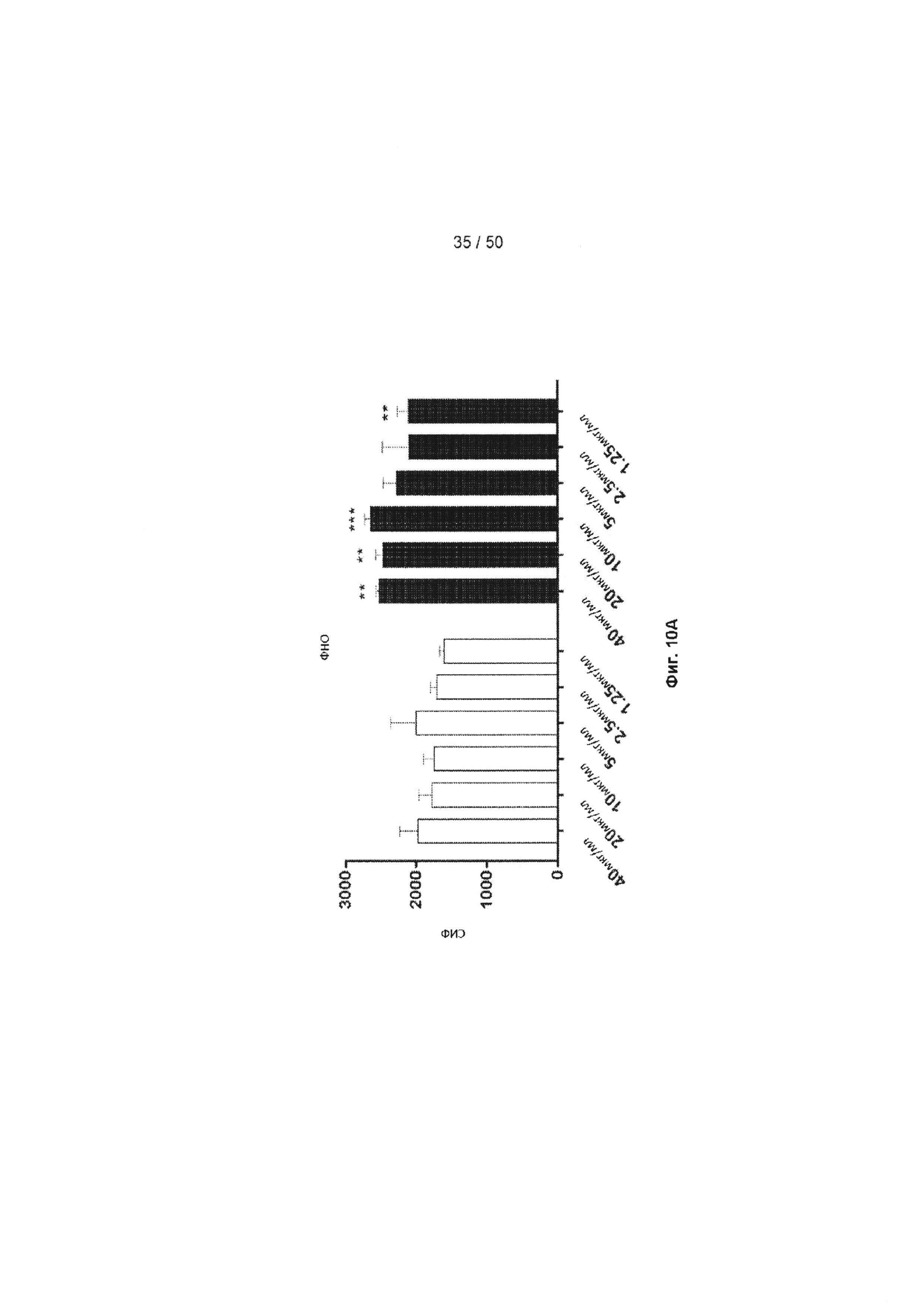
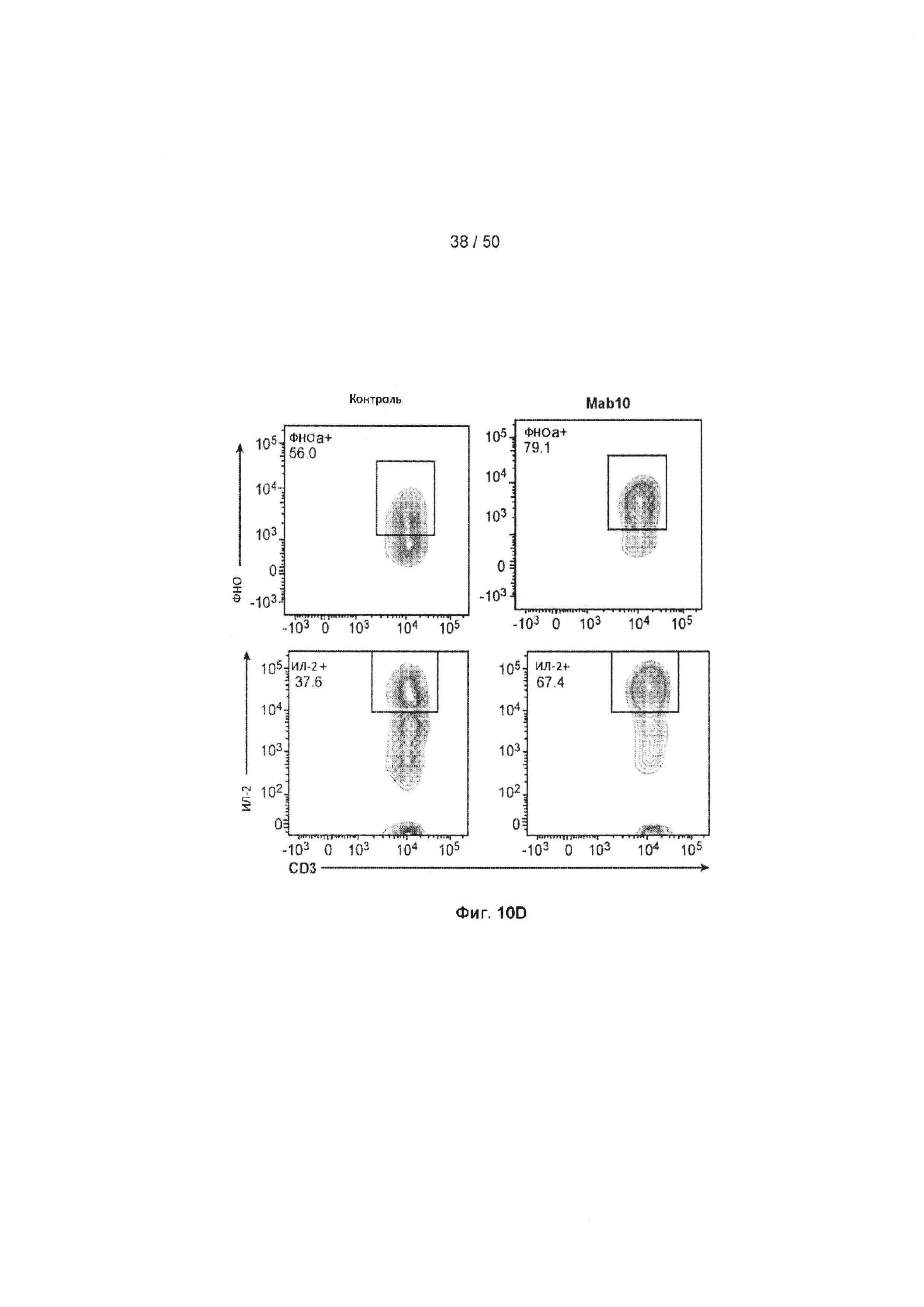
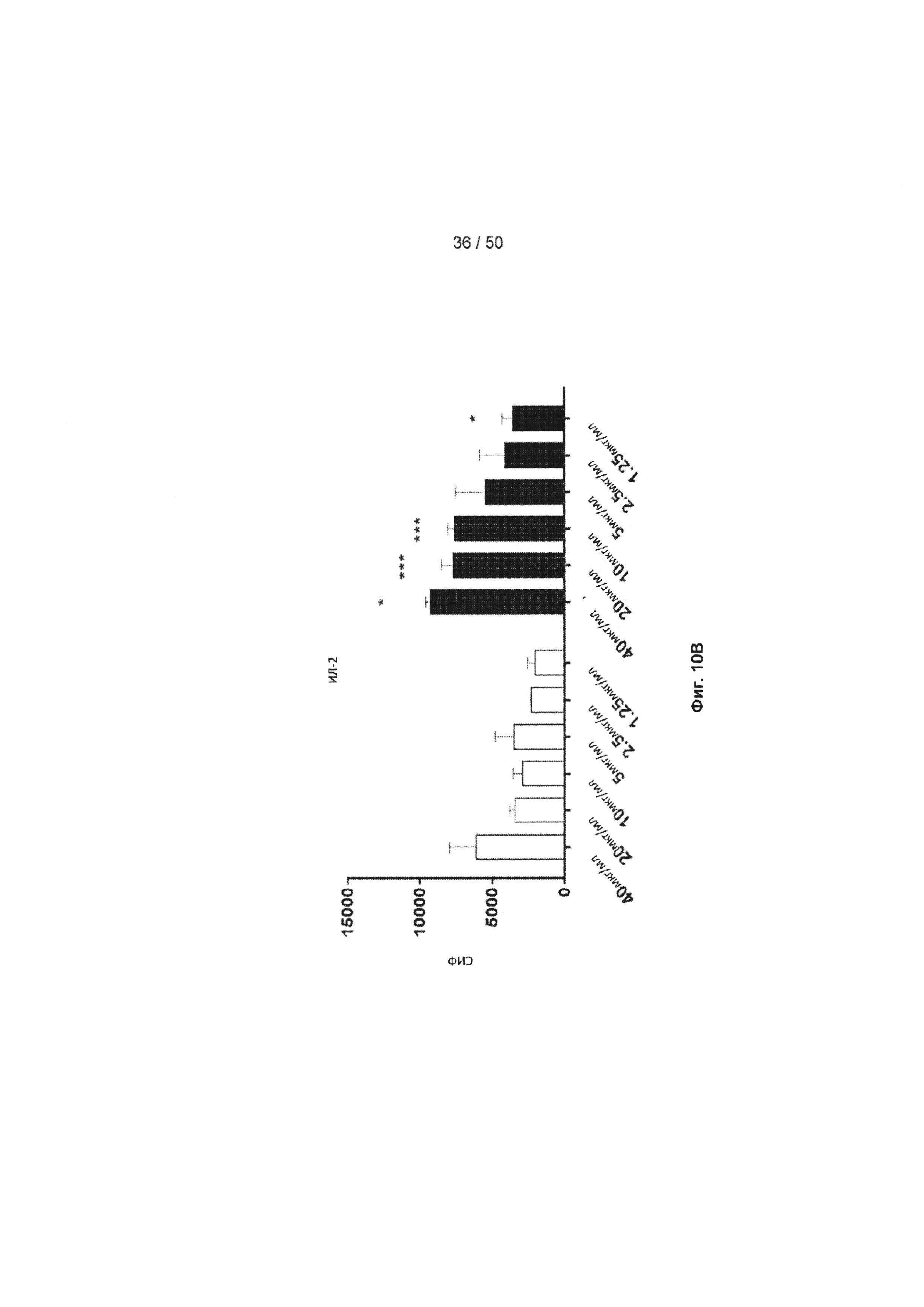
[0066] Фиг. 10A-10D представляют собой ряд графиков, показывающих эффект МАБ10 на ЦМВ-стимулированные CD4+ Т-лимфоциты из человеческого донора с применением окрашивания внутриклеточных цитокинов. Инкубация CD4+ клеток с МАБ10 (черные столбцы) увеличивает продуцирование эффекторных цитокинов дозозависимым образом, включая ФНО (Фиг. 10А), ИЛ-2 (Фиг. 10В) и ИНФ-γ (фиг. 10С) по сравнению с клетками, инкубированными с контрольным IgG4 (белые столбцы). На Фиг. 10D показано, что инкубация с МАБ10 увеличивает долю антигенспецифических активированных CD4+ Т-лимфоцитов. На Фиг. 10D показано что, клетки, которые обрабатывали 20 мкг/мл контрольного IgG4 или МАБ10, анализировали с помощью FACS по экспрессии CD3 (маркер зрелых Т-лимфоцитов) и экспрессии ФНО и ИЛ-2. Статистические различия были рассчитаны между группами МАБ10 и контрольный IgG4 (обработка теми же концентрациями) с применением t-критерия Стьюдента (*=р<0,05, **=р<0,01, ***=р<0,005, ****=р<0,001)
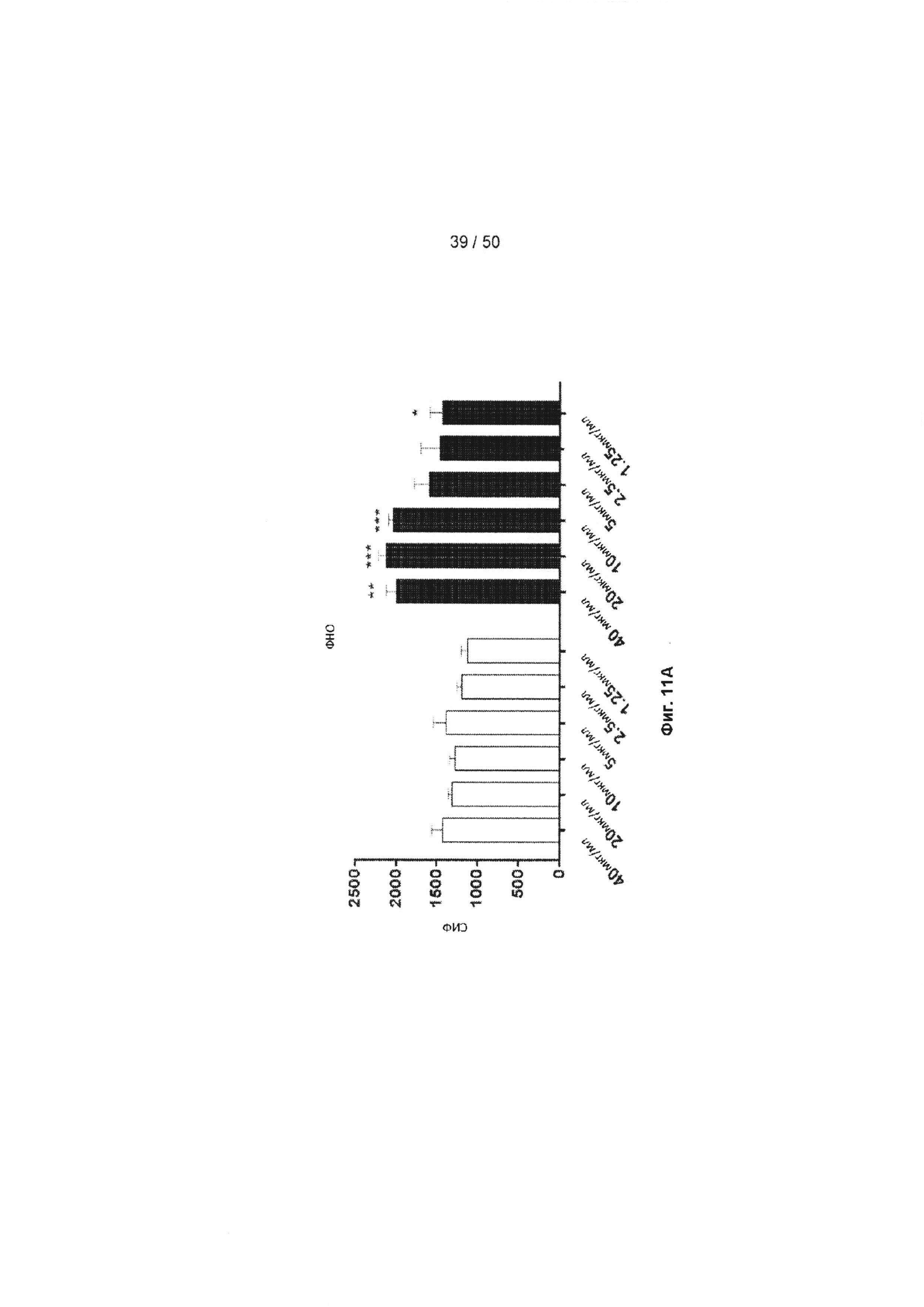
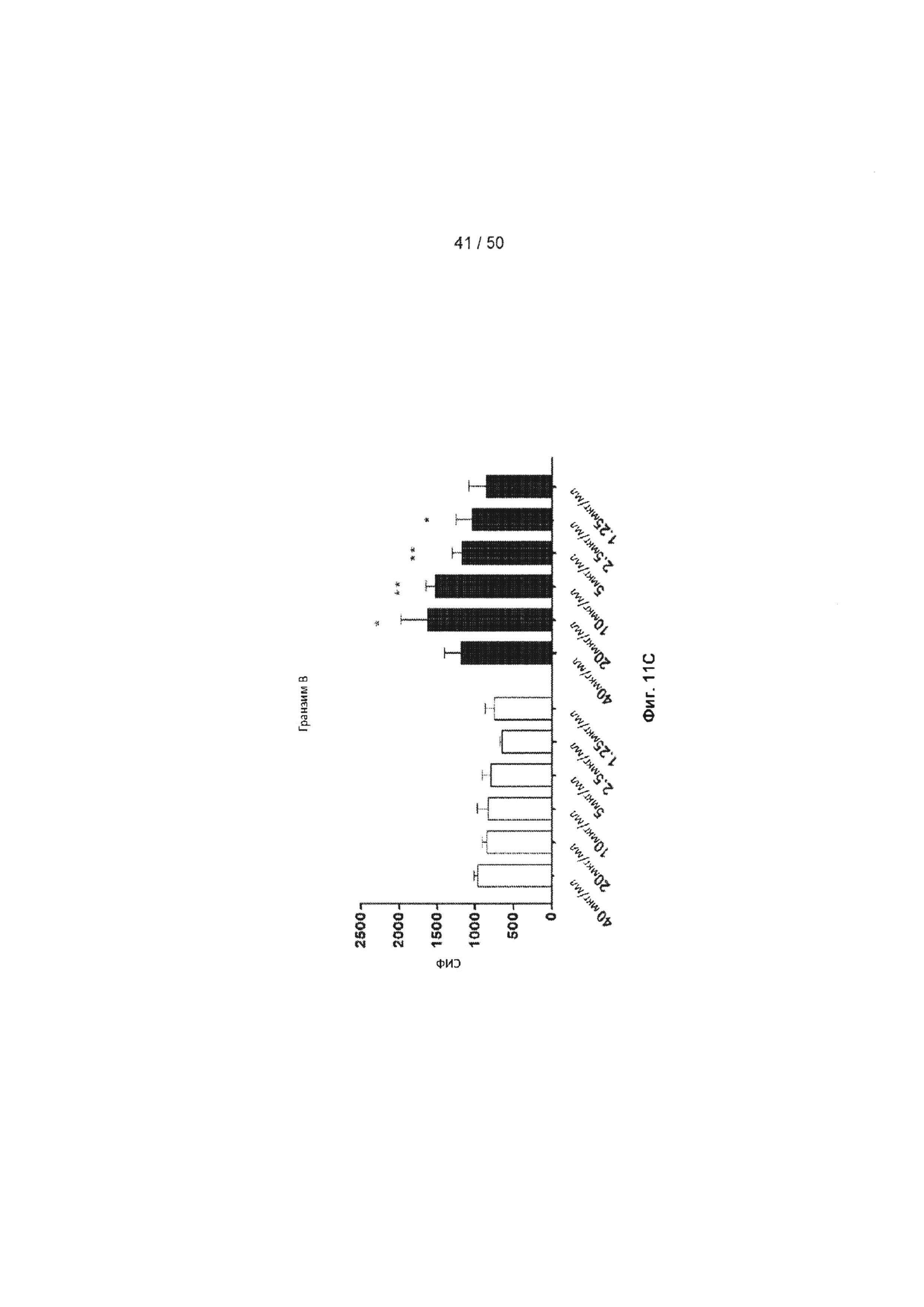
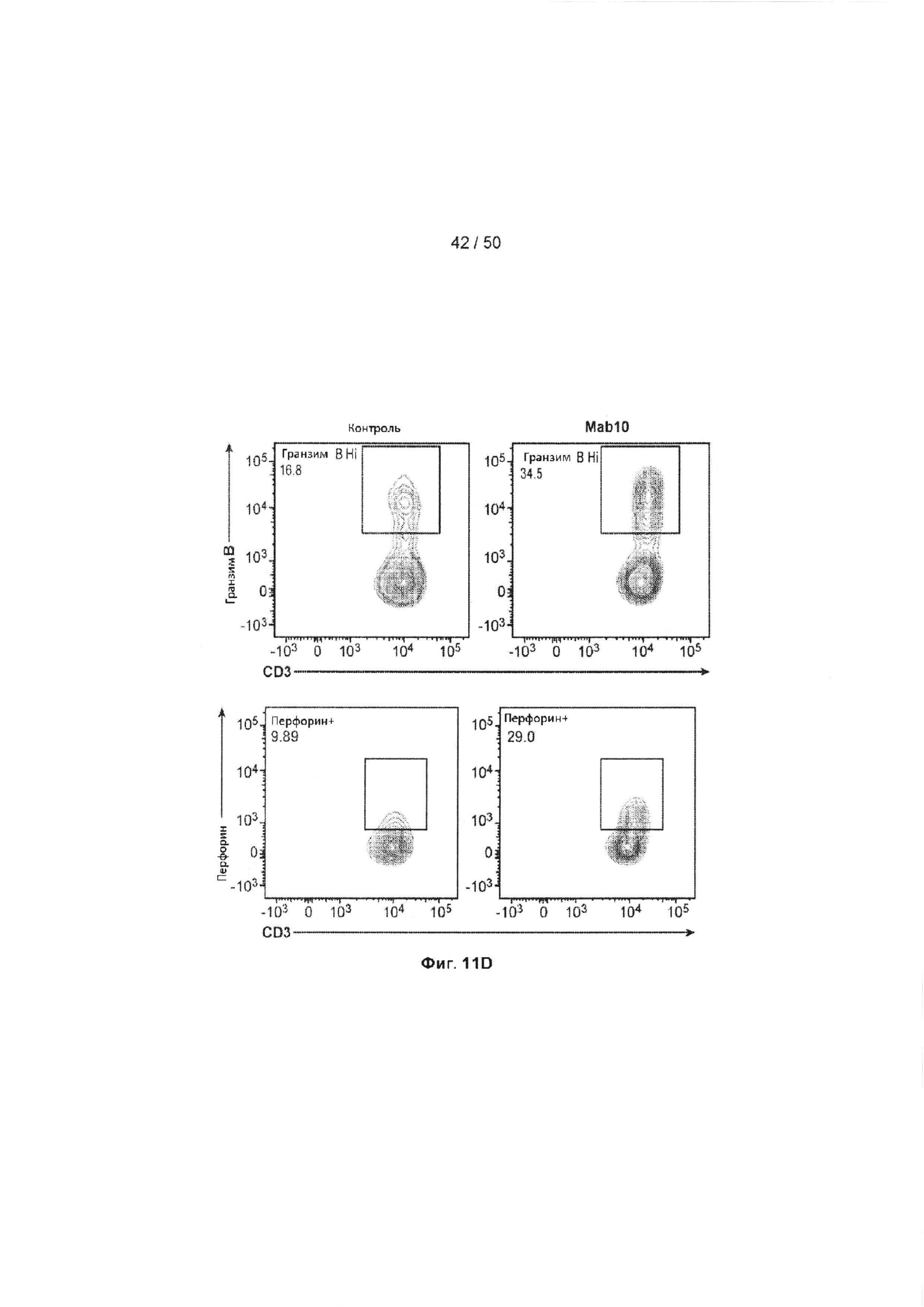
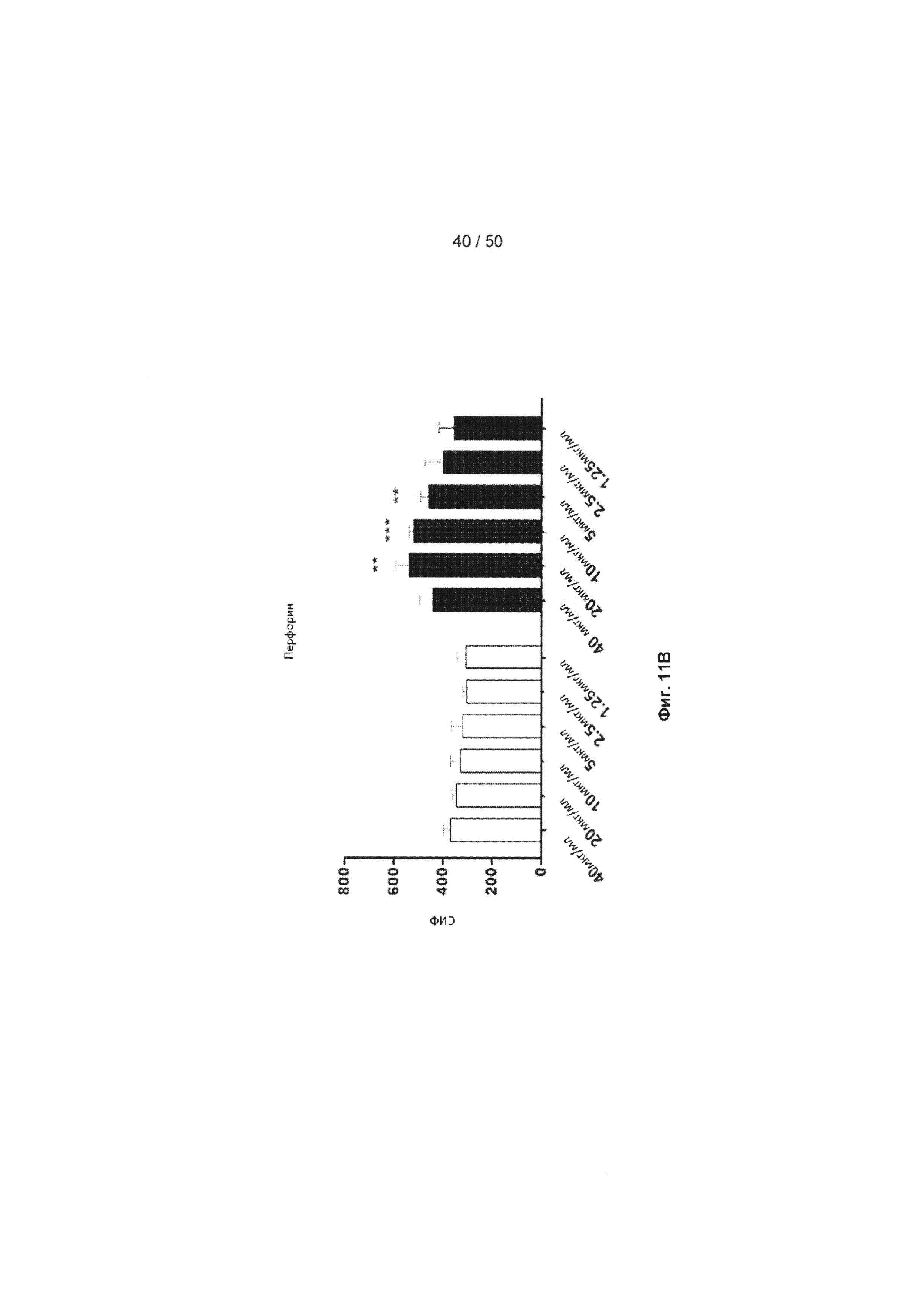
[0067] Фиг. 11A-11D представляют собой ряд графиков, подобных Фиг. 10, но с применением CD8+ клеток, и показывающие продуцирование ФНО (Фиг. 11А), перфорина (Фиг. 11В) и гранзима В (Фиг. 11С) такими клетками, обработанными МАБ10 или контрольным IgG4. На Фиг. 11D показано, что инкубация с МАБ10 увеличивает долю антигенспецифических активированных CD8+ Т-лимфоцитов. Клетки, которые были обработаны 20 мкг/мл контрольного IgG4 или МАБ10, анализировали с помощью FACS по экспрессии CD3, и экспрессии перфорина и гранзима В. Статистические различия были рассчитаны между группами МАБ10 и контрольный IgG4 (обработка теми же концентрациями) с применением t-критерия Стьюдента (*=р<0,05, **=р<0,01, ***=р<0,005, ****=р<0,001)
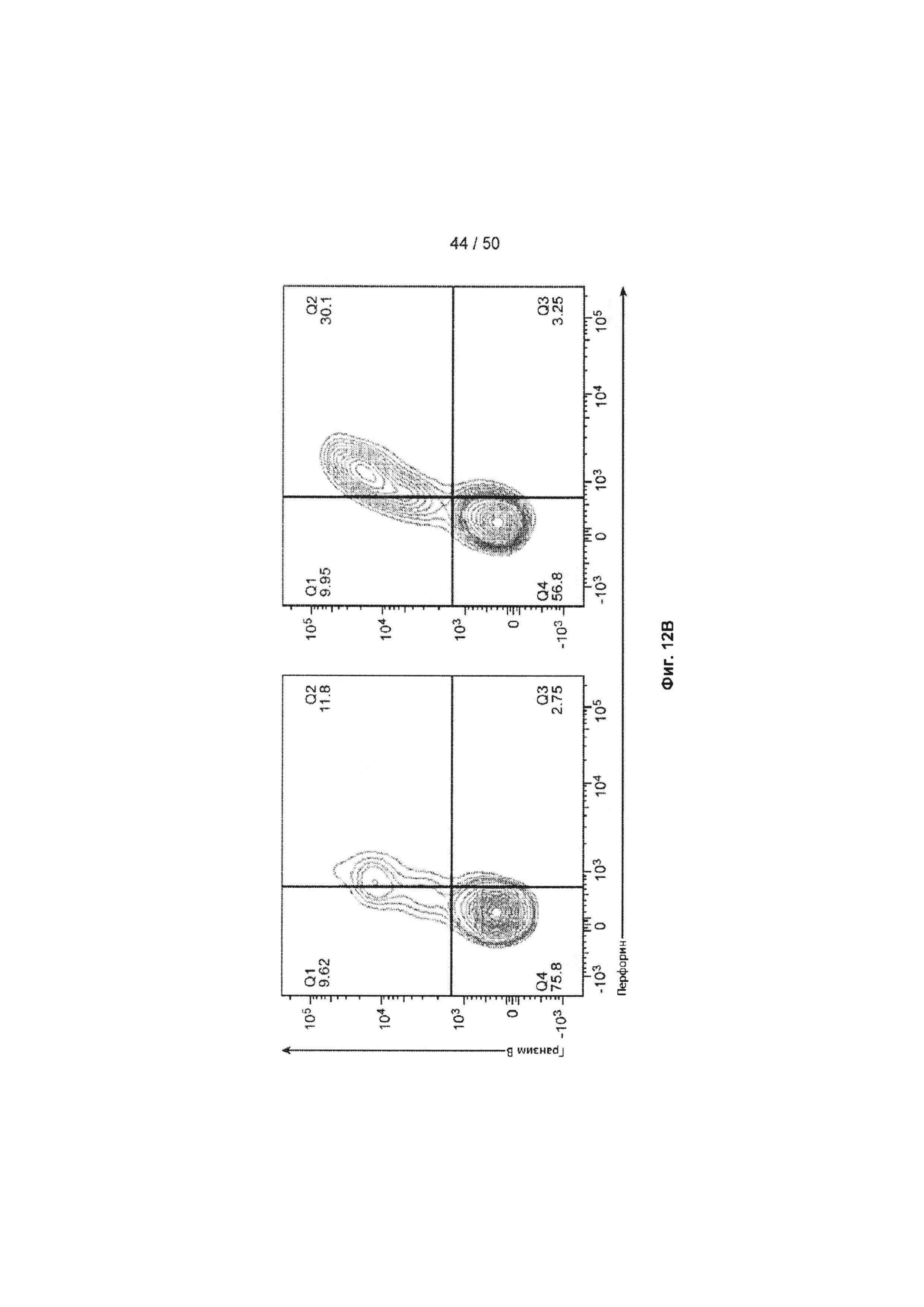
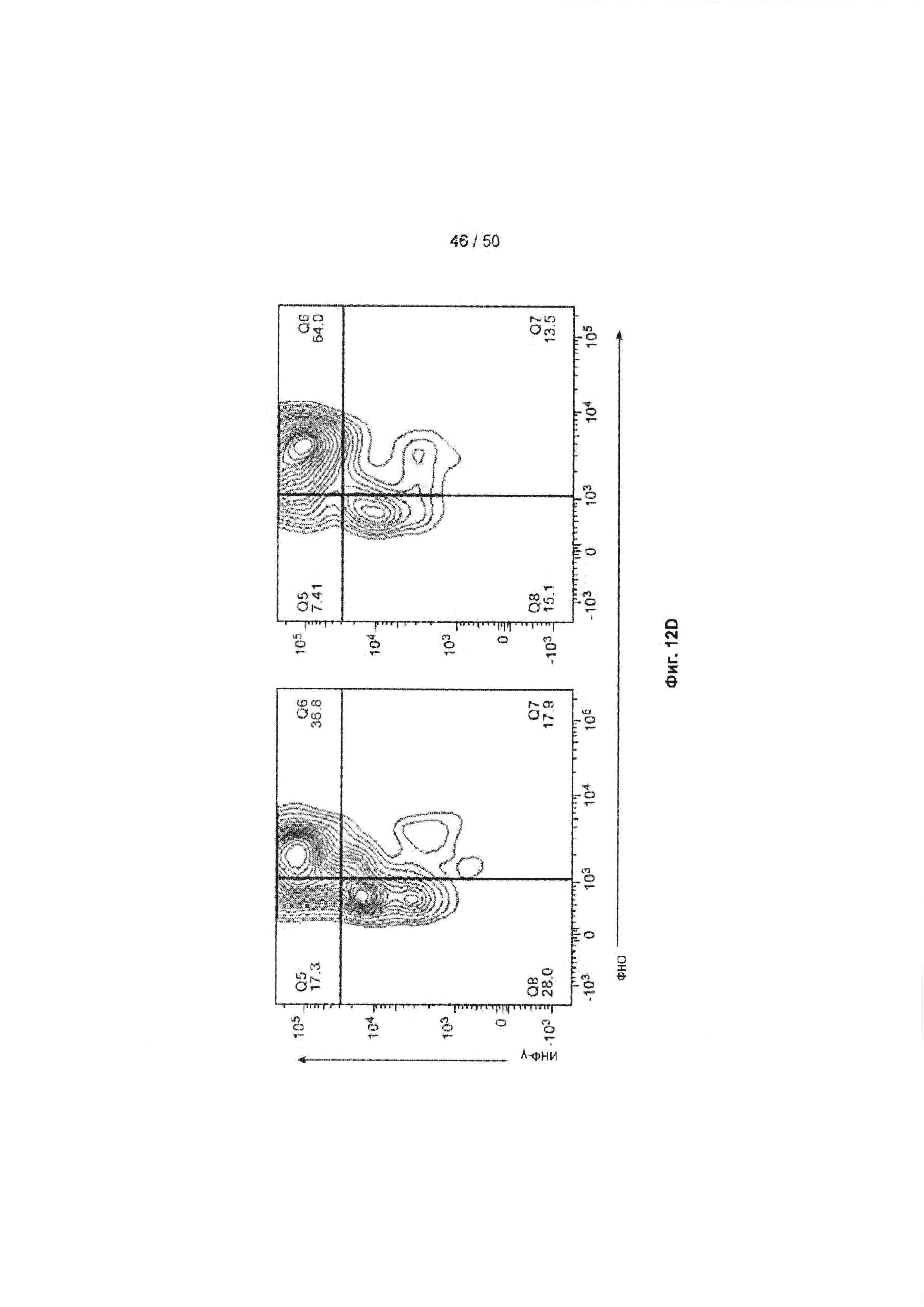
[0068] На Фиг. 12A-12D показано результаты обработки клеток из того же донора, причем блокирование МАБ10 усиливает ЦМВ-специфичные ответы CD8+ Т-лимфоцитов. Клетки инкубировали с рядом концентраций МАБ10 (черные столбцы) или с контрольным IgG4 (белые столбцы), и анализировали процент популяции, дважды позитивной по перфорин + гранзим В + (Фиг. 12А) или ИНФ-γ + ФНО + (Фиг. 12С). Статистические различия были рассчитаны между группами МАБ10 и контрольный IgG4 (обработка теми же концентрациями) с применением t-критерия Стьюдента (*=р<0,05, **=р<0,01, ***=р<0,005, ****=р<0,001) На Фиг. 12В (анализ перфорин + гразим В +) и Фиг. 12D (анализ ИНФ-γ + ФНО +) показана доля дважды позитивных клеток, сравниваемых с клетками, обработанными 20 мкг/мл контрольного антитела (левые панели) или 20 мкг/мл МАБ10 (правые панели).
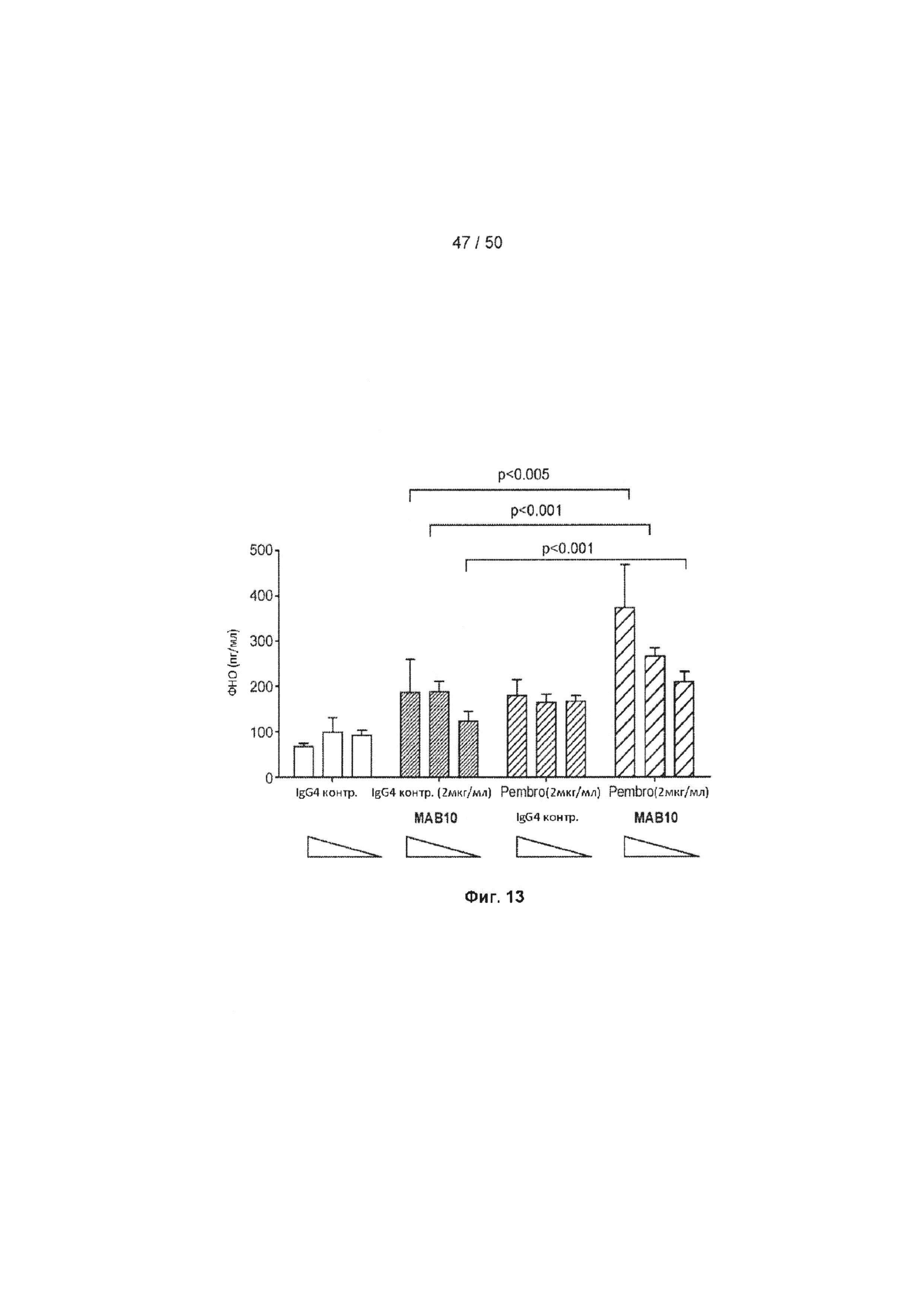
[0069] На Фиг. 13 показан график, демонстрирующий комбинированный эффект МАБ10 и PD-1 антитела пембролизумаба на клетках из того же донора, которого применяли для Фиг. 10-12. Клетки стимулировали лизатами ЦМВ и обрабатывали 2 мкг/мл пембролизумаба или контрольного IgG4, и 10, 20 или 40 мкг/мл контрольного антитела или МАБ10, и измеряли продуцирование ФНО. Тестировали четыре группы клеток, обработанных контрольным IgG4 (белые столбцы, самая левая группа), константным количество контрольного IgG4 и титрами МАБ10 (темно-серые столбцы, вторая группа слева), константным количество пембролизумаба и титрами контрольного IgG4 (светло-серые столбцы, вторая группа справа), или константным количество пембролизумаба и титрами МАБ10 (черные полосы, правая группа).
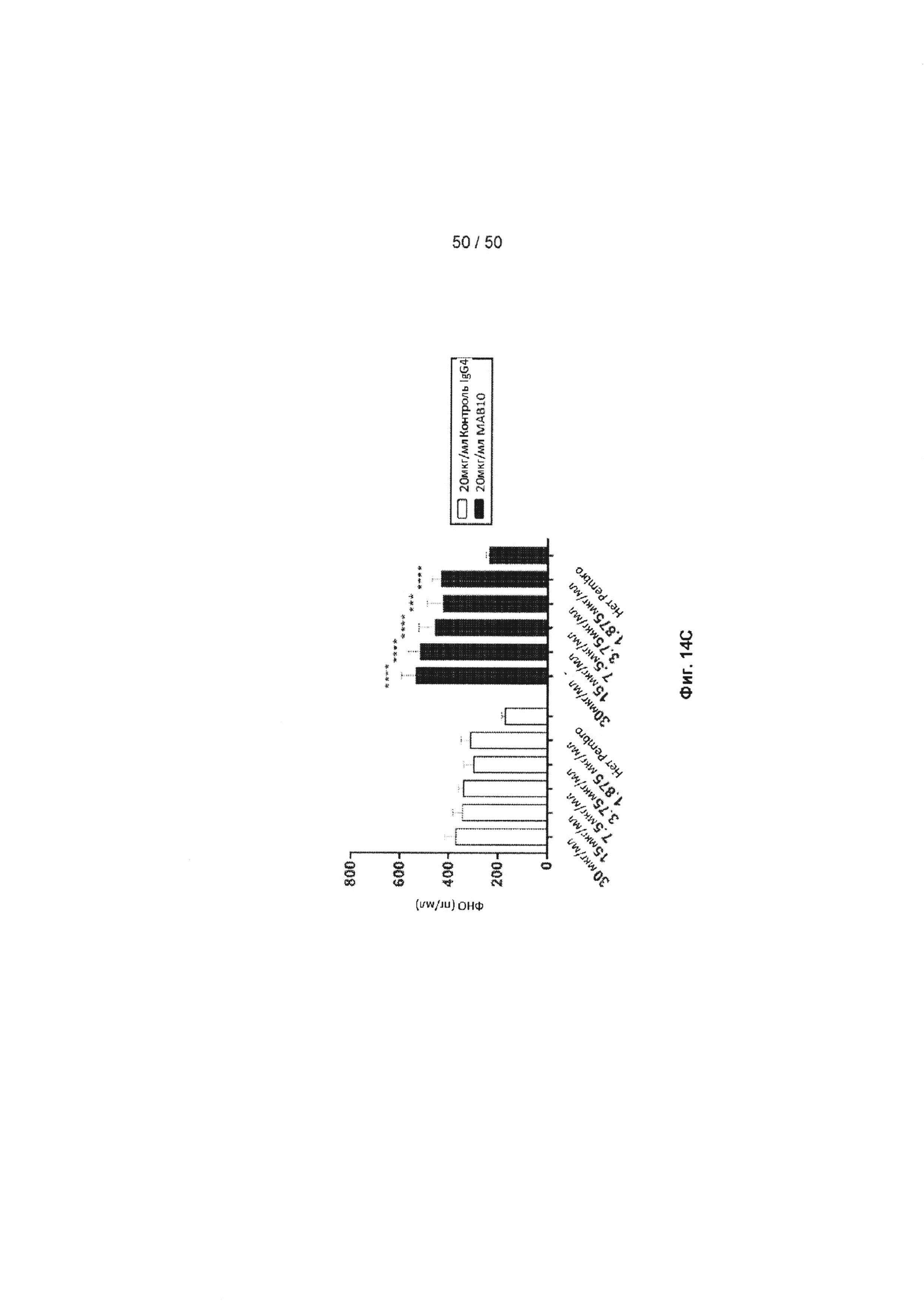
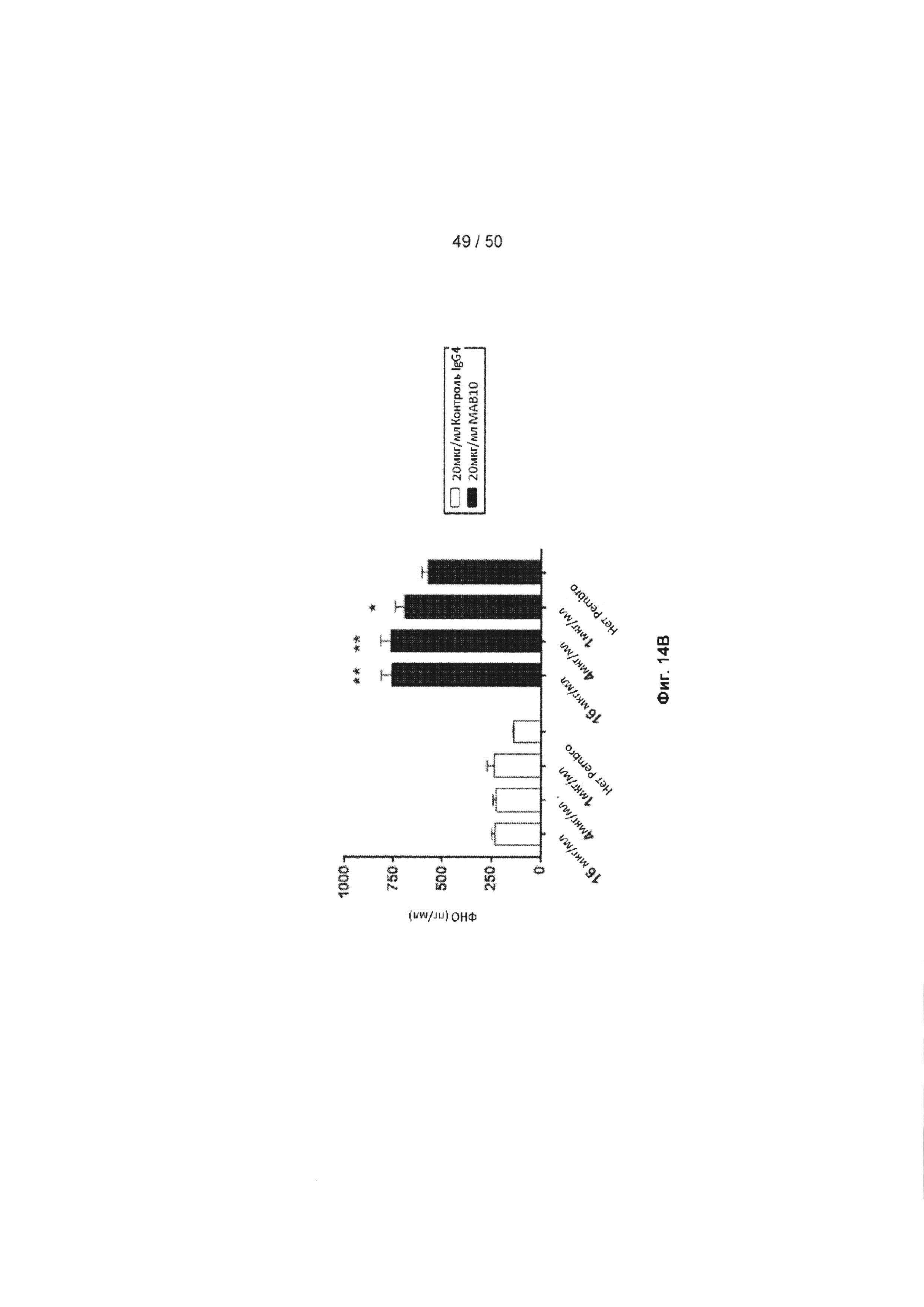
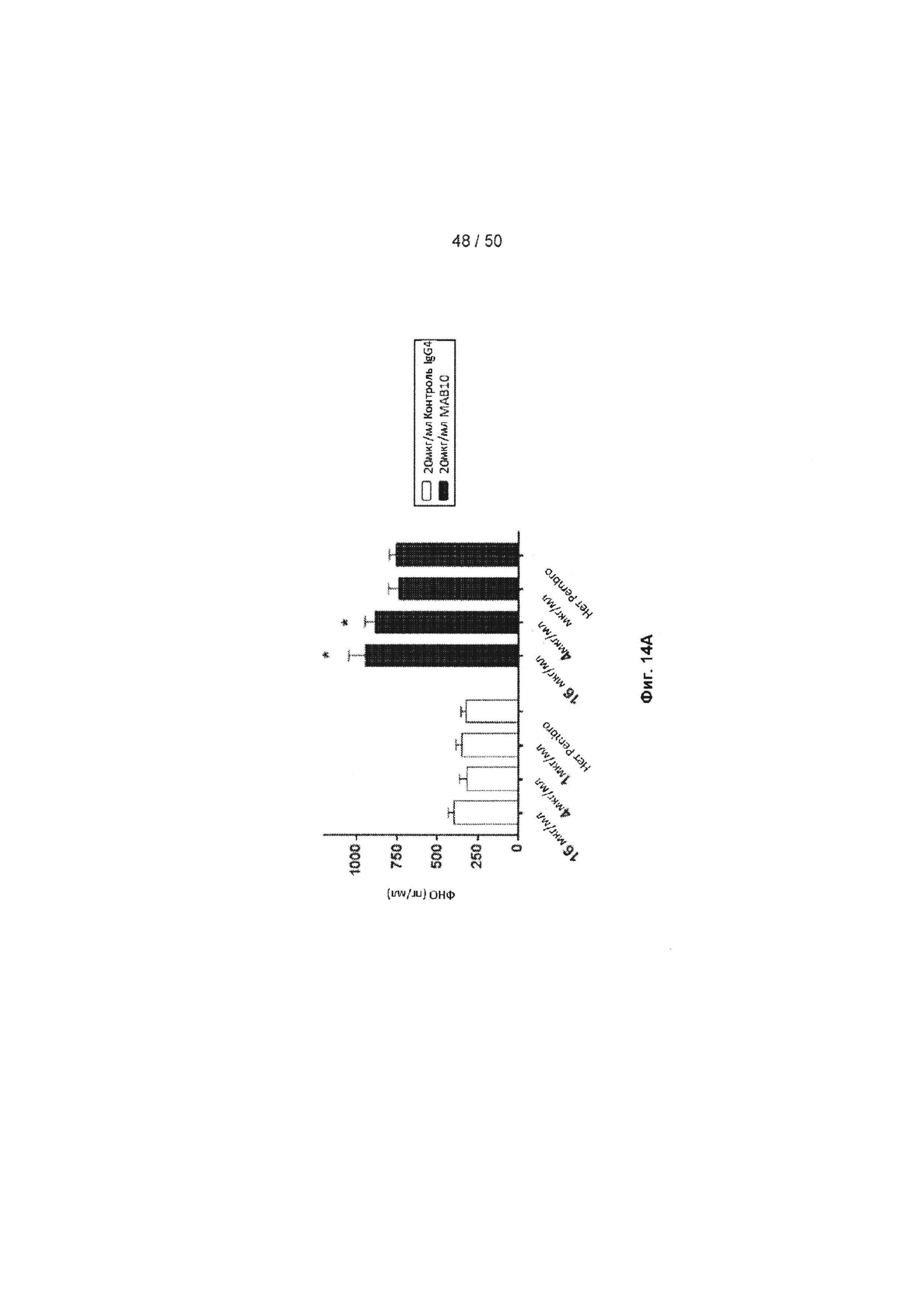
[0070] Фиг. 14А-14С представляют собой ряд графиков, показывающих эффект обработки МАБ10 + пембролизумаб на клетки из трех различных доноров. Клетки стимулировали 0,1 мкг/мл лизата ЦМВ, и обрабатывали 20 мкг/мл МАБ10 или 20 мкг/мл контрольного антитела IgG4, и титрами пембролизумаба, когда измеряли продуцирование ФНО. На Фиг. 14А показаны результаты анализа с применением клеток из донора 1; на Фиг. 14В показаны результаты анализа с применением клеток из донора 2; на Фиг. 14С показаны результаты анализа с применением клеток из донора 3. Добавление МАБ10 (черные столбцы), отдельно или в сочетании с возрастающими концентрациями пембролизумаба, приводит к увеличению продуцирования ФНО по сравнению с группой контрольное антитело + пембролизумаб (белые столбцы). Кроме того, МАБ10 (черные столбцы) в комбинации с пембролизумабом также приводило к увеличению активации по сравнению с только МАБ10. Статистические различия были рассчитаны между только МАБ10 и группами МАБ10 + пембролизумаб с применением t-критерия Стьюдента (*=р<0,05, **=р<0,01, ***=р<0,005, ****=р<0,001)
ПОДРОБНОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
1. Определения
[0071] Если не указано иное, все термины области техники, обозначения и другая научная терминология, используемые в данном документе, предназначены для того, чтобы иметь значения, которые обычно подразумеваются специалистами в данной области техники, к которой относится настоящее изобретение. В некоторых случаях, термины с общепринятыми значениями определены в данном документе для ясности и/или в качестве готовой ссылки, и включение таких определений в данном документе не обязательно должно истолковываться как представляющее разницу в отношении того, что обычно подразумевается в данной области техники. Методы и процедуры, описанные или упомянутые в данном документе, в целом, как правило, понятны и широко используются при применении традиционных методик специалистами в данной области техники, таких как, например, широко используемые методики молекулярного клонирования, описанные в Sambrook et al., Molecular Cloning: A Laboratory Manual 4th ed. (2012) Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY. При необходимости процедуры, связанные с применением коммерчески доступных наборов и реагентов, в целом, как правило, выполняются в соответствии с установленными изготовителем протоколами и условиями, если не указано иное.
[0072] Как применяется в данном документе, единственное число существительного также включает множественное число существительного, если контекст явно не указывает на иное. Термины «включать», «такие как» и т.д. предназначены для передачи включения без ограничения, если специально не указано иное.
[0073] Как применяется в данном документе, термин «содержащий» также специфически включает в себя варианты осуществления «состоящий из» и «состоящий в основном из» указанных элементов, если специально не указано иное. Например, мультиспецифичный АВР «содержащий диатело» включает в себя мультиспецифичный АВР «состоящий из диатела», и мультиспецифичный АВР «состоящий в основном из диатела».
[0074] Термин «около» указывает на значение, и охватывает указанное значение и диапазон выше и ниже этого значения. В некоторых вариантах осуществления, термин «около» указывает на обозначенное значение ±10%, ±5% или ±1%. В некоторых вариантах осуществления, где применимо, термин «около» указывает на обозначенное(нные) значение(ния) ± одно стандартное отклонение этого значения(ний).
[0075] Термины «TIGIT», «белок TIGIT» и «антиген TIGIT» применяются в данном документе взаимозаменяемо для обозначения TIGIT человека или любых вариантов (например, сплайс-вариантов и аллельных вариантов), изоформ и гомологов TIGIT человека, которые естественно экспрессируются клетками, или которые экспрессируются клетками, трансфицированными геном tigit. В некоторых аспектах, белок TIGIT представляет собой белок TIGIT, естественным образом экспрессируемый приматом (например, обезьяной или человеком), грызуном (например, мышью или крысой), собакой, верблюдом, кошкой, коровой, козой, лошадью или овцой. В некоторых аспектах, белок TIGIT представляет собой TIGIT человека (hTIGIT; SEQ ID NO: 1). Не ограничиваясь теорией, считается, что позиции 1-21 SEQ ID NO: 1 кодируют сигнальный пептид; позиции 22-141 SEQ ID NO: 1 кодируют внеклеточный домен зрелого белка TIGIT; позиции 142-162 SEQ ID NO: 1 кодируют трансмембранный домен; и позиции 163-244 SEQ ID NO: 1 кодируют цитоплазматический домен. См. UniProt KB - Q495A1 (TIGIT_HUMAN), на www.uniprot.org/uniprot/Q495A1, доступно с 28 сентября 2015 года. В некоторых аспектах, белок TIGIT представляет собой TIGIT яванского макака (cTIGIT; SEQ ID NO: 2). В некоторых аспектах, белок TIGIT представляет собой TIGIT мыши (mTIGIT), имеющий последовательность, представленную в SEQ ID NO: 3. В некоторых аспектах, белок TIGIT представляет собой TIGIT мыши (mTIGIT), имеющий последовательность, представленную в SEQ ID NO: 138. Как применяется в данном документе, если не указывается SEQ ID NO, то термины «mTIGIT», «мышиный TIGIT» и «TIGIT мыши» обозначают SEQ ID NO: 3 и/или SEQ ID NO: 138. В некоторых аспектах, белок TIGIT представляет собой полноразмерный или непроцесированный белок TIGIT. В некоторых аспектах, белок TIGIT представляет собой укороченный или процессированный белок TIGIT, полученный в результате посттрансляционной модификации. TIGIT также известен по множеству синонимов, включая WUCAM, VSIG9 и Vstm3.
[0076] Термин «иммуноглобулин» относится к классу структурно родственных белков, обычно содержащих две пары полипептидных цепей: одну пару легких (L) цепей и одну пару тяжелых (Н) цепей. В «интактном иммуноглобулине» все четыре из этих цепей связаны между собой дисульфидными связями. Структура иммуноглобулинов хорошо охарактеризована. См., например, Paul, Fundamental Immunology 7th ed., Ch. 5 (2013) Lippincott Williams & Wilkins, Philadelphia, PA. Вкратце, каждая тяжелая цепь обычно содержит вариабельную область тяжелой цепи (VH) и константную область тяжелой цепи (CH). Константная область тяжелой цепи обычно содержит три домена, сокращенно CH1, CH2 и CH3. Каждая легкая цепь обычно содержит вариабельную область легкой цепи (VL) и константную область легкой цепи. Константная область легкой цепи обычно содержит один домен, сокращенно CL.
[0077] Термин «антиген-связывающий белок» (АВР) относится к белку, содержащему один или больше антиген-связывающих доменов, которые специфически связываются с антигеном или эпитопом. В некоторых вариантах осуществления, антиген-связывающий домен связывает антиген или эпитоп со специфичностью и аффинностью, сходными с таковыми встречающихся в природе антител. В некоторых вариантах осуществления, АВР содержит антитело. В некоторых вариантах осуществления, АВР состоит из антитела. В некоторых вариантах осуществления, АВР состоит в основном из антитела. В некоторых вариантах осуществления, АВР содержит альтернативный каркас. В некоторых вариантах осуществления, АВР состоит из альтернативного каркаса. В некоторых вариантах осуществления, АВР состоит в основном из альтернативного каркаса. В некоторых вариантах осуществления, АВР содержит фрагмент антитела. В некоторых вариантах осуществления, АВР состоит из фрагмента антитела. В некоторых вариантах осуществления, АВР состоит в основном из фрагмента антитела. «TIGIT АВР», «анти-TIGIT АВР» или «TIGIT-специфический АВР» представляет собой АВР, как предложено в данном документе, который специфически связывается с антигеном TIGIT. В некоторых вариантах осуществления, АВР связывает внеклеточный домен TIGIT. В некоторых вариантах осуществления, TIGIT АВР, предложенный в данном документе, связывается с эпитопом TIGIT, который является консервативным между белками или среди белков TIGIT из разных видов.
[0078] Термин «антитело» применяется в данном документе в самом широком смысле и включает в себя определенные типы иммуноглобулиновых молекул, содержащих один или больше антиген-связывающих доменов, которые специфически связываются с антигеном или эпитопом. Антитело специфически включает в себя интактные антитела (например, интактные иммуноглобулины), фрагменты антител и мультиспецифические антитела. Антитело представляет собой один тип АВР.
[0079] Термин «альтернативный каркас» относится к молекуле, в которой одна или больше областей могут быть варьированы для получения одного или большего количества антиген-связывающих доменов, которые специфически связываются с антигеном или эпитопом. В некоторых вариантах осуществления, антиген-связывающий домен связывает антиген или эпитоп со специфичностью и аффинностью, аналогичной таковым антитела. Иллюстративные альтернативные каркасы включают в себя те, которые получены из фибронектина (например, Adnectins™), β-слоистой структуры (например, iMab), липокалина (например, Anticalins®), EETI-II/AGRP, BPTI/LACI-D1/ITI-D2 (например, домены Куницца), аптамеров тиоредоксинового пептида, белка А (например, Affibody®), анкириновых повторов (например, DARPin), гамма-В-кристаллина/убиквитина (например, Аффилины), CTLD3 (например, Тетрантектины), Финомеров и (модуля LDLR-A) (например, Авимеры). Дополнительная информация об альтернативных каркасах приведена в Binz et al., Nat. Biotechnol., 2005 23:1257-1268; Skerra, Current Opin. in Biotech., 2007 18:295-304; и Silacci et al., J. Biol. Chem., 2014, 289:14392-14398; каждый источник из которых включен посредством ссылки в полном объеме. Альтернативный каркас - это один из типов АВР.
[0080] Термин «антиген-связывающий домен» обозначает часть АВР, которая способна специфически связываться с антигеном или эпитопом. Одним из примеров антиген-связывающего домена является антиген-связывающий домен, сформированный димером VH-VL антитела. Другим примером антиген-связывающего домена является антиген-связывающий домен, сформированный путем варьирования определенных петель из десятого домена типа III фибронектина Аднектина.
[0081] Термины «полноразмерное антитело», «интактное антитело» и «цельное антитело» применяются в данном документе взаимозаменяемо, обозначая антитело, имеющее структуру, по существу, сходную встречающейся в природе структурой антитела, и имеющее тяжелые цепи, которые содержат Fc-область. Например, когда используется для обозначения молекулы IgG, «полноразмерное антитело» представляет собой антитело, которое содержит две тяжелые цепи и две легкие цепи.
[0082] Термин «область Fc» обозначает С-концевую область тяжелой цепи иммуноглобулина, которая в встречающихся в природе антителах взаимодействует с Fc-рецепторами и некоторыми белками системы комплемента. Структуры областей Fc различных иммуноглобулинов, и сайты гликозилирования, содержащиеся в них, известны в данной области техники. См. Schroeder and Cavacini, J. Allergy Clin. Immunol., 2010, 125:S41-52, включен посредством ссылки в полном объеме. Область Fc может быть встречающейся в природе Fc-областью или областью Fc, модифицированной, как описано в данной области техники или в другом месте в данном раскрытии.
[0083] Области VH и VL могут быть далее подразделены на области гипервариабельности («гипервариабельные области (HVR)», также называемые «областями, определяющими комплементарность» (CDR)), чередующиеся с областями, которые являются более консервативными. Более консервативные области называются каркасными областями (FR). Каждая VH и VL в целом, как правило, содержит три CDR и четыре FR, расположенных в следующем порядке (от N-конца до С-конца): FR1-CDR1-FR2-CDR2-FR3-CDR3-FR4. CDR участвуют в связывании антигена и влияют на антигенную специфичность и аффинность связывания антитела. См. Kabat et al., Sequences of Proteins of Immunological Interest 5th ed. (1991) Public Health Service, National Institutes of Health, Bethesda, MD, включен посредством ссылки в полном объеме.
[0084] Легкая цепь из любых видов позвоночных может быть отнесена к одному из двух типов, называемому каппа (κ) и лямбда (λ), в зависимости от последовательности ее константной области.
[0085] Тяжелая цепь из любых видов позвоночных может быть отнесена к одному из пяти различных классов (или изотипов): IgA, IgD, IgE, IgG и IgM. Эти классы также обозначаются как α, δ, ε, γ и μ соответственно. Классы IgG и IgA далее подразделяются на подклассы на основе различий в последовательности и функции. Люди экспрессируют следующие подклассы: IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2.
[0086] Границы аминокислотной последовательности CDR могут быть определены специалистом в данной области техники с применением любой из ряда известных схем нумерации, включая те, которые описаны в Kabat et al., supra (схема нумерации «Кабат»); Al-Lazikani et al., 1997, J. Mol. Biol., 273:927-948 (схема нумерации «Чотиа»); MacCallum et al., 1996, J. Mol. Biol. 262:732-745 (схема нумерации «Контакт»); Lefranc et al., Dev. Comp. Immunol., 2003, 27:55-77 (схема нумерации «IMGT»); и Honegge and  J. Mol. Biol., 2001, 309:657-70 (схема нумерации «AHo»); каждый из которых включен посредством ссылки в полном объеме.
J. Mol. Biol., 2001, 309:657-70 (схема нумерации «AHo»); каждый из которых включен посредством ссылки в полном объеме.
[0087] В Таблице 1 представлены позиции CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3, как определено схемами по Кабату и Чотиа. Для CDR-H1 нумерация остатков обеспечивается с применением схем нумерации по Кабату и Чотиа.
[0088] CDR могут быть обозначены, например, с применением программного обеспечения нумерации антител, такого как Abnum, доступного по адресу www.bioinf.org.uk/abs/abnum/ и описанного в Abhinandan and Martin, Immunology, 2008, 45:3832-3839, включен посредством ссылки в полном объеме.
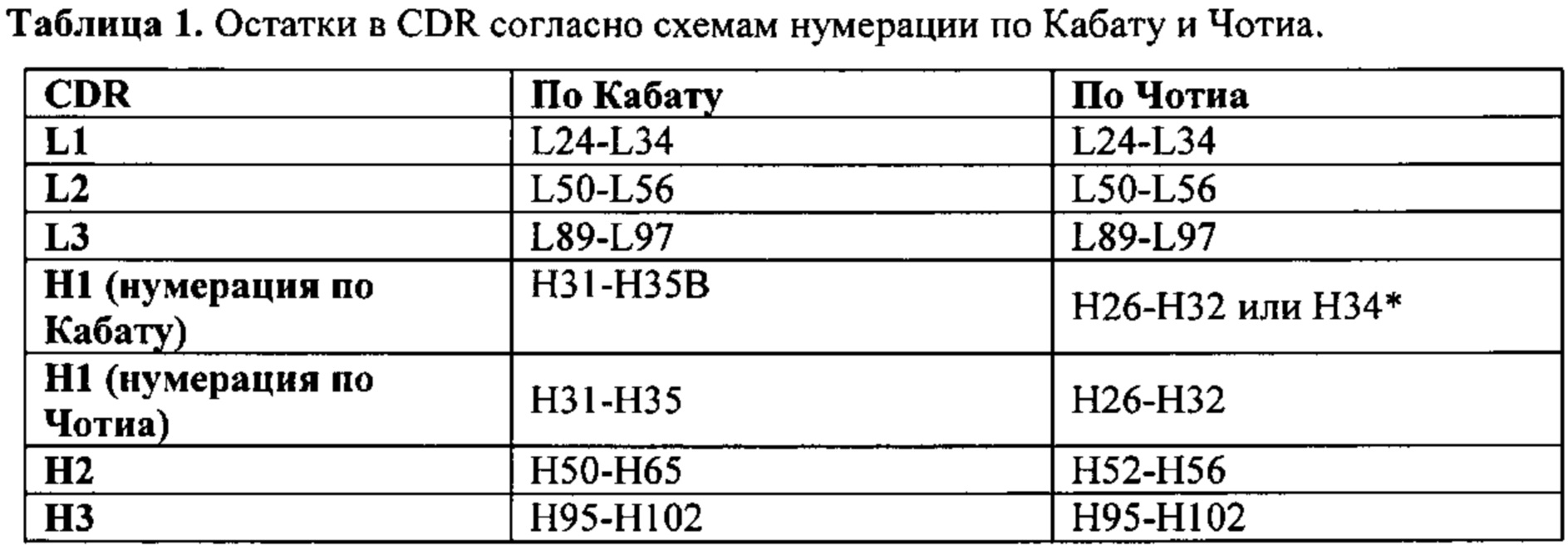
* С-конец CDR-H1 при нумерации с применением соглашения о нумерации по Кабату варьирует между Н32 и Н34, в зависимости от длины CDR.
[0089] «Схема нумерации ЕС» в целом, как правило применяется при отсылке к остатку в константной области тяжелой цепи антитела (например, как описано в Kabat et al., выше). Если не указано иное, схема нумерации ЕС применяется для обозначения остатков в константных областях тяжелой цепи антитела, описанных в данном документе.
[0090] «Фрагмент антитела» содержит часть интактного антитела, такого как антиген-связывающая или вариабельная область интактного антитела. Фрагменты антитела включают в себя, например, Fv-фрагменты, Fab-фрагменты, фрагменты F(ab')2, фрагменты Fab', фрагменты scFv (sFv) и фрагменты scFv-Fc.
[0091] Фрагменты «Fv» содержат нековалентно связанный димер одного вариабельного домена тяжелой цепи и одного вариабельного домена легкой цепи.
[0092] Фрагменты «Fab» содержат, помимо вариабельных доменов тяжелой и легкой цепей, константный домен легкой цепи и первый константный домен (CH1) тяжелой цепи. Fab-фрагменты могут быть получены, например, рекомбинантными способами или путем расщепления папаином полноразмерного антитела.
[0093] Фрагменты «F(ab')2» содержат два фрагмента Fab', соединенных, вблизи области шарнира, дисульфидными связями. Фрагменты F(ab')2 могут быть получены, например, рекомбинантными способами или путем расщепления пепсином интактного антитела. Фрагменты F(ab') могут быть диссоциированы, например, обработкой β-меркаптоэтанолом.
[0094] «Одноцепочечные Fv» или «sFv» или «scFv» фрагменты антитела содержат домен VH и домен VL в одной полипептидной цепи. VH и VL в целом, как правило, связаны пептидным линкером. См.  А. (1994). Может применятся любой подходящий линкер. В некоторых вариантах осуществления, линкер представляет собой (GGGGS)n (SEQ ID NO: 127). В некоторых вариантах осуществления, n=1, 2, 3, 4, 5 или 6. См. Antibodies from Escherichia coli. In Rosenberg M. & Moore G.P. (Eds.), The Pharmacology of Monoclonal Antibodies vol. 113 (pp. 269-315), Springer-Verlag, Нью-Йорк, включен посредством ссылки в полном объеме.
А. (1994). Может применятся любой подходящий линкер. В некоторых вариантах осуществления, линкер представляет собой (GGGGS)n (SEQ ID NO: 127). В некоторых вариантах осуществления, n=1, 2, 3, 4, 5 или 6. См. Antibodies from Escherichia coli. In Rosenberg M. & Moore G.P. (Eds.), The Pharmacology of Monoclonal Antibodies vol. 113 (pp. 269-315), Springer-Verlag, Нью-Йорк, включен посредством ссылки в полном объеме.
[0095] Фрагменты «scFv-Fc» содержат scFv, прикрепленный к домену Fc. Например, домен Fc может быть присоединен к С-концу scFv. Домен Fc может следовать за VH или VL в зависимости от ориентации вариабельных доменов в scFv (то есть VH-VL или VL-VH). Может быть использован любой подходящий домен Fc, известный в данной области техники или описанный в данном документе. В некоторых случаях, домен Fc содержит домен Fc IgG4.
[0096] Термин «однодоменное антитело» относится к молекуле, в которой один вариабельный домен антитела специфически связывается с антигеном без присутствия другого вариабельного домена. Однодоменные антитела и их фрагменты описаны в Arabi Ghahroudi et al., FEBS Letters, 1998, 414:521-526 и Muyldermans et al., Trends in Biochem. Sci., 2001, 26:230-245, каждый из которых включен посредством ссылки в полном объеме. Однодоменные антитела также известны как sdAbs или нанотела.
[0097] « мультиспецифичный АВР» представляет собой АВР, который содержит два или больше разных антиген-связывающих домена, которые в совокупности специфически связывают два или больше разных эпитопа. Два или больше различных эпитопа могут быть эпитопами на одном и том же антигене (например, одной молекуле TIGIT, экспрессированной клеткой) или на разных антигенах (например, разных молекулах TIGIT, экспрессированных одной и той же клеткой, или молекуле TIGIT и не-TIGIT молекуле). В некоторых аспектах, мультиспецифичный АВР связывает два разных эпитопа (т.е. «биспецифический АВР»). В некоторых аспектах, мультиспецифичный АВР связывает три разных эпитопа (т.е. «триспецифический АВР»). В некоторых аспектах, мультиспецифичный АВР связывает четыре разных эпитопа (т.е. «квадроспецифический АВР»). В некоторых аспектах, мультиспецифическый АВР связывает пять различных эпитопов (т.е. «квинтиспецифический АВР»). В некоторых аспектах, мультиспецифичный АВР связывает 6, 7, 8 или больше разных эпитопов. Каждая связывающая специфичность может присутствовать в любой подходящей валентности. Примеры мультиспецифических АВР приведены в других частях данного раскрытия.
[0098] «Моноспецифический АВР» представляет собой АВР, который содержит один или больше сайтов связывания, которые специфически связываются с одним эпитопом. Примером моноспецифического АВР является встречающаяся в природе молекула IgG, которая, будучи двухвалентной (т.е. имеющей два антиген-связывающих домена), распознает один и тот же эпитоп в каждом из двух антиген-связывающих доменов. Специфичность связывания может быть представлена в любой подходящей валентности.
[0099] Термин «моноклональное антитело» относится к антителу из популяции по существу гомогенных антител. Популяция по существу гомогенных антител содержит антитела, которые по существу похожи и которые связывают один и тот же эпитоп(ы), за исключением вариантов, которые обычно могут возникать в процессе получения моноклонального антитела. Такие варианты в целом, как правило, присутствуют только в незначительных количествах. Моноклональное антитело обычно получают способом, который включает в себя выбор одного антитела из множества антител. Например, процесс отбора может быть выбором уникального клона из множества клонов, таких как пул гибридомных клонов, фаговых клонов, дрожжевых клонов, бактериальных клонов или других клонов рекомбинантных ДНК. Выбранное антитело может быть дополнительно изменено, например, для улучшения сродства к мишени («аффиное созревание»), для гуманизации антитела, для улучшения его продуцирования в культуре клеток и/или для снижения его иммуногенности у субъекта.
[0100] Термин «химерное антитело» относится к антителу, в котором часть тяжелой и/или легкой цепи получена из конкретного источника или вида, тогда как остальная часть тяжелой и/или легкой цепи получена из другого источника или вида.
[0101] «Гуманизированные» формы нечеловеческих антител представляют собой химерные антитела, которые содержат минимальную последовательность, полученную из нечеловеческого антитела. Гуманизированное антитело в целом, как правило, представляет собой человеческое антитело (антитело-реципиент), в котором остатки из одного или большего количества CDR заменяются остатками из одного или большего количества CDR нечеловеческого антитела (донорное антитело). Донорным антителом может быть любое подходящее нечеловеческое антитело, такое как мышиное, крысиное, кроличье, куриное или антитело низших приматов, имеющее желаемую специфичность, сродство или биологический эффект. В некоторых случаях, выбранные остатки каркасной области антитела-реципиента заменяются соответствующими остатками каркасной области из донорного антитела. Гуманизированные антитела могут также содержать остатки, которые не обнаружены ни в антителе-реципиенте, ни в донорном антителе. Такие модификации могут быть сделаны для дополнительного улучшения функции антител. Для дополнительных деталей, см. Jones et al., Nature, 1986, 321:522-525; Riechmann et al., Nature, 1988, 332:323-329; и Presta, Curr. Op. Struct. Biol., 1992, 2:593-596, каждый из которых включен посредством ссылки в полном объеме.
[0102] «Человеческое антитело» представляет собой такое антитело, которое обладает аминокислотной последовательностью, соответствующей таковой антитела, продуцируемого человеком или клеткой человека, или полученной из нечеловеческого источника, который использует репертуар человеческих антител или последовательностей, кодирующих человеческие антитела (например, полученные из человеческих источников или разработанные de novo). Человеческие антитела специфически исключают гуманизированные антитела.
[0103] «Выделенный АВР» или «выделенная нуклеиновая кислота» представляет собой АВР или нуклеиновую кислоту, который(рая) был отделен(на) от и/или выделен(на) из компонента его(ее) естественной среды. Компоненты природной среды могут включать ферменты, гормоны и другие белковые или небелковые материалы. В некоторых вариантах осуществления, выделенный АВР очищают до степени, достаточной для получения по меньшей мере 15 остатков N-концевой или внутренней аминокислотной последовательности, например, с помощью секвенатора с вращающимся стаканом. В некоторых вариантах осуществления, выделенный АВР очищают до гомогенности с помощью гель-электрофореза (например, SDS-PAGE) в восстанавливающих или невосстанавливающих условиях с обнаружением окрашиванием синим Кумасси или серебром. В некоторых вариантах осуществления, выделенный АВР может включать в себя АВР in situ в рекомбинантных клетках, поскольку по меньшей мере один компонент природной среды АВР отсутствует. В некоторых аспектах, выделенный АВР или выделенную нуклеиновую кислоту получают, по меньшей мере, на одной стадии очистки. В некоторых вариантах осуществления, выделенный АВР или выделенную нуклеиновую кислоту очищают по меньшей мере до 80%, 85%, 90%, 95% или 99% по массе. В некоторых вариантах осуществления, выделенный АВР или выделенную нуклеиновую кислоту очищают по меньшей мере до 80%, 85%, 90%, 95% или 99% по объему. В некоторых вариантах осуществления, выделенный АВР или выделенную нуклеиновую кислоту предоставляют в виде раствора, содержащего по меньшей мере 85%, 90%, 95%, 98%, от 99% до 100% АВР или нуклеиновой кислоты по массе. В некоторых вариантах осуществления, выделенный АВР или выделенную нуклеиновую кислоту предоставляют в виде раствора, содержащего по меньшей мере 85%, 90%, 95%, 98%, от 99% до 100% АВР или нуклеиновой кислоты по объему.
[0104] «Аффинность» относится к силе суммарного количества нековалентных взаимодействий между одним сайтом связывания молекулы (например, АВР) и ее партнером по связыванию (например, антигеном или эпитопом). Если не указано иное, как используется в данном документе, термин «аффинность» относится к аффинности характерного связывания, которая отражает взаимодействие 1:1 между членами пары связывания (например, АВР и антигеном или эпитопом). Аффинность молекулы X к ее партнеру Y может быть представлена константой равновесия при диссоциации (KD). Кинетические компоненты, которые вносят вклад в константу равновесия при диссоциации, более подробно описаны ниже. Аффинность может быть измерена обычными способами, известными в данной области техники, включая описанные в данном документе, такие как технология поверхностного плазмонного резонанса (SPR) (например, BIACORE®) или интерферометрия биослоя (например, FORTEBIO®).
[0105] Что касается связывания АВР с молекулой-мишенью, термины «связывать», «специфическое связывание», «специально связывается с», «специфически», «избирательно связывается» и «избирательно к» конкретному антигену (например, полипептидная мишень) или эпитопу на определенном антигене обозначают связывание, которое заметно отличается от неспецифического или неселективного взаимодействия (например, с нецелевой молекулой). Специфическое связывание может быть измерено, например, путем измерения связывания с молекулой-мишенью и сравнения его со связыванием с молекулой, не являющейся мишенью. Специфическое связывание может также определяться конкуренцией с контрольной молекулой, которая имитирует эпитоп, распознаваемый на молекуле-мишени. В этом случае, указывается специфическое связывание, если связывание АВР с молекулой-мишенью конкурентно ингибируется контрольной молекулой. В некоторых аспектах, аффинность TIGIT АВР к нецелевой молекуле составляет меньше чем примерно 50% от сродства к TIGIT. В некоторых аспектах, аффинность TIGIT АВР к нецелевой молекуле составляет меньше чем примерно 40% от сродства к TIGIT. В некоторых аспектах, аффинность TIGIT АВР к нецелевой молекуле составляет меньше чем примерно 30% от сродства к TIGIT. В некоторых аспектах, аффинность TIGIT АВР к нецелевой молекуле составляет меньше чем примерно 20% от сродства к TIGIT. В некоторых аспектах, аффинность TIGIT АВР к нецелевой молекуле составляет меньше чем примерно 10% от сродства к TIGIT. В некоторых аспектах, аффинность TIGIT АВР к нецелевой молекуле составляет меньше чем примерно 1% от сродства к TIGIT. В некоторых аспектах, аффинность TIGIT АВР к нецелевой молекуле составляет меньше чем примерно 0,1% от сродства к TIGIT.
[0106] Как применяется в данном документе, термин «kd» (с-1) относится к константе скорости диссоциации конкретного взаимодействия АВР-антиген. Данное значение также упоминается как значение koff.
[0107] Как применяется в данном документе, термин «ka» (М-1×с-1) относится к константе скорости ассоциации конкретного взаимодействия АВР-антиген. Данное значение также упоминается как значение kon.
[0108] Как применяется в данном документе, термин «KD» (М) относится к константе равновесия при диссоциации конкретного взаимодействия АВР-антиген. KD=kd/ka. В некоторых вариантах осуществления, аффинность АВР описывается в терминах KD для взаимодействия между таким АВР и его антигеном. Для ясности, как известно в данной области техники, меньшее значение KD указывает на более высокую аффинность взаимодействие, тогда как большее значение KD указывает на более низкую аффинность взаимодействие.
[0109] Как применяется в данном документе, термин «KA» (М-1) относится к константе равновесия при ассоциации конкретного взаимодействия АВР-антиген. KA=ka/kd.
[0110] АВР с «созревшей аффинностью» представляет собой АВР с одним или больше изменениями (например, в одной или нескольких CDR, или FR) относительно родительского АВР (то есть АВР, из которого получен или сконструирован измененный АВР), что приводит к улучшению в аффинности АВР к его антигену, по сравнению с родительским АВР, который не обладает изменением(ями). В некоторых вариантах осуществления, АВР с созревшей аффинностью имеет наномолярное или пикомолярное сродство к целевому антигену. АВР с созревшей аффинностью могут быть получены с применением различных способов, известных в данной области техники. Например, Marks et al. (Bio/Technology, 1992, 10:779-783, включен посредством ссылки в полном объеме) описывает аффиное созревание путем перестановки доменов VH и VL. Случайный мутагенез CDR и/или каркасных остатков описывается, например, Barbas et al. (Proc. Nat. Acad. Sci. U.S.A., 1994, 91:3809-3813); Schier et al., Gene, 1995, 169:147-155; Yelton et al., J. Immunol., 1995, 155:1994-2004; Jackson et al., J. Immunol., 1995, 154:3310-33199; и Hawkins et al, J. Mol. Biol., 1992, 226:889-896; каждый из которых включен посредством ссылки в полном объеме.
[0111] «Иммуноконъюгат» представляет собой АВР, конъюгированный с одной или большим количеством гетерологичных молекул, например терапевтическим или диагностическим агентом.
[0112] «Эффекторные функции» относятся к той биологической активности, которая опосредуется областью Fc антитела, активность которой может варьировать в зависимости от изотипа антитела. Примеры эффекторных функций антител включают C1q-связывание для активации комплемент-зависимой цитотоксичности (КЗЦ), связывания Fc-рецептора для активации антителозависимой клеточной цитотоксичности (АЗКЦ) и антителозависимого клеточного фагоцитоза (АЗКФ).
[0113] При использовании в данном документе в контексте двух или больше АВР термин «конкурирует с» или «перекрестно конкурирует с» означает, что два или более АВР конкурируют за связывание с антигеном (например, TIGIT). В одном иллюстративном анализе, поверхность покрывают TIGIT и приводят в контакт с первым TIGIT АВР, после чего добавляют второй TIGIT АВР. В другом иллюстративном анализе, поверхность покрывают первым TIGIT АВР и приводят в контакт с TIGIT, после чего добавляют второй TIGIT АВР. Если присутствие первого TIGIT АВР уменьшает связывание второго TIGIT АВР, в любом из анализов, то АВР конкурируют друг с другом. Термин «конкурирует с» также включает комбинации АВР, где один АВР уменьшает связывание другого АВР, но не наблюдается конкуренция, когда АВР добавляют в обратном порядке. Однако в некоторых вариантах осуществления, первый и второй АВР блокируют связывание друг друга, независимо от порядка, в котором они добавлены. В некоторых вариантах осуществления, один АВР уменьшает связывание другого АВР с его антигеном по меньшей мере на 25%, по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90% или по меньшей мере на 95%. Специалист в данной области техники может выбрать концентрации антител, используемых в конкурентных анализах, на основе аффинности АВР к TIGIT и валентности АВР. Анализы, описанные в данном определении, являются иллюстративными, и квалифицированный специалист может использовать любой подходящий анализ для определения того, конкурируют ли антитела друг с другом. Подходящие анализы описаны, например, в Сох et al., «Immunoassay Methods», в Assay Guidance Manual [Internet], обновлено 24 декабря, 2014 года (www.ncbi.nlm.nih.gov/books/NBK92434/; доступно с 29 сентября, 2015 года); Silman et al., Cytometry, 2001, 44:30-37; и Finco et al., J. Pharm. Biomed. Anal., 2011, 54:351-358; каждый из которых включен посредством ссылки в полном объеме.
[0114] Термин «эпитоп» обозначает часть антигена, которая специфически связывается с АВР. Эпитопы часто состоят из доступных на поверхности аминокислотных остатков и/или сахарных боковых цепей, и могут иметь специфические трехмерные структурные характеристики, а также характеристики удельного заряда. Конформационный и неконформационный эпитопы отличаются тем, что связывание с первым, но не последним, может быть утрачено в присутствии денатурирующих растворителей. Эпитоп может содержать аминокислотные остатки, которые непосредственно участвуют в связывании, и другие аминокислотные остатки, которые непосредственно не участвуют в связывании. Эпитоп, с которым связывается АВР, может быть определен с применением известных методов определения эпитопа, таких как, например, тестирование связывания АВР с вариантами TIGIT с различными точечными мутациями или с химерными вариантами TIGIT.
[0115] Процент «идентичности» между полипептидной последовательностью и эталонной последовательностью определяется как процент аминокислотных остатков в полипептидной последовательности, которые идентичны аминокислотным остаткам в эталонной последовательности после выравнивания последовательностей и внесения пробелов, если необходимо, для достижения максимального процента идентичности последовательностей. Выравнивание для целей определения процента идентичности аминокислотной последовательности может быть достигнуто различными способами, которые входят в компетенцию специалиста в данной области техники, например, с применением общедоступного компьютерного программного обеспечения, такого как BLAST, BLAST-2, ALIGN, MEGALIGN (DNASTAR), CLUSTALW, CLUSTAL OMEGA или MUSCLE. Специалисты в данной области техники могут определить соответствующие параметры для выравнивания последовательностей, включая любые алгоритмы, необходимые для достижения максимального выравнивания по всей длине сравниваемых последовательностей.
[0116] «Консервативная замена» или «консервативная замена аминокислоты» относится к замене аминокислоты на химически или функционально подобную аминокислоту. Таблицы консервативных замен, предоставляющие схожие аминокислоты, хорошо известны в данной области техники. В качестве примера, группы аминокислот, предложенные в Таблицах 2-4, в некоторых вариантах осуществления, рассматривают как консервативные замены друг для друга.

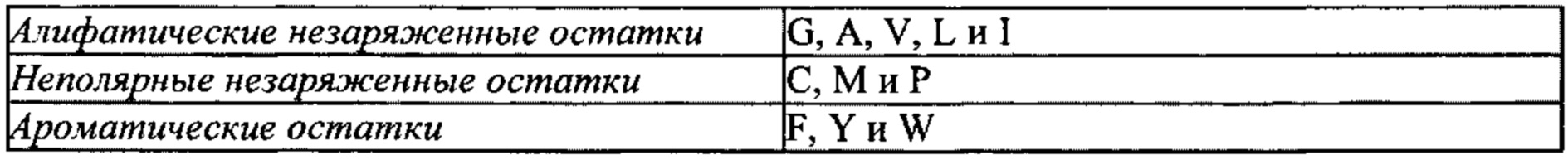


[0117] Дополнительные консервативные замены могут быть найдены, например, в Creighton, Proteins: Structures and Molecular Properties 2nd ed. (1993) W.H. Freeman & Co., New York, NY. АВР, полученный путем внесения одной или нескольких консервативных замен аминокислотных остатков в исходную АВР, называется «консервативно модифицированным вариантом».
[0118] Термин «аминокислота» относится к двадцати общепринятым встречающимся в природе аминокислотам. Естественно встречающиеся аминокислоты включают в себя: аланин (Ala; А), аргинин (Arg; R), аспарагин (Asn; N), аспарагиновую кислоту (Asp; D), цистеин (Cys; С); глутаминовую кислоту (Glu; Е), глутамин (Gln; Q), глицин (Gly; G); гистидин (His, Н), изолейцин (Ile; I), лейцин (Leu; L), лизин (Lys; K), метионин (Met; М), фенилаланин (Phe; F), пролин (Pro; Р), серин (Ser; S), треонин (Thr; Т), триптофан (Trp; W), тирозин (Tyr; Y) и валин (Val; V).
[0119] Как применяется в данном документе, термин «вектор» относится к молекуле нуклеиновой кислоты, способной размножать другую нуклеиновую кислоту, с которой она связана. Термин включает в себя вектор как самовоспроизводящуюся структуру нуклеиновой кислоты, также как и вектор, встроенный в геном клетки-хозяина, в которую он был введен. Некоторые векторы способны направлять экспрессию нуклеиновых кислот, с которыми они функционально связаны. Такие векторы упоминаются в данном документе как «векторы экспрессии».
[0120] Термины «клетка-хозяин», «линия клеток-хозяев» и «культура клеток-хозяев» используются взаимозаменяемо и относятся к клеткам, в которые была введена экзогенная нуклеиновая кислота, и к потомству таких клеток. Клетки-хозяева включают в себя «трансформанты» (или «трансформированные клетки») и «трансфектанты» (или «трансфицированные клетки»), каждая из которых включает в себя первичную трансформированную или трансфицированную клетку и полученное от нее потомство. Такое потомство не может быть полностью идентичным по содержанию нуклеиновой кислоты по отношению к родительской клетке, и может содержать мутации.
[0121] Термин «проводить лечение» (и его вариации, такие как «лечить» или «лечение») относится к клиническому вмешательству в попытке изменить естественный ход заболевания или патологии у субъекта, нуждающегося в этом. Лечение может быть выполнено как для профилактики, так и во время клинической патологии. Желательные эффекты лечения включают в себя предотвращение возникновения или рецидива заболевания, облегчение симптомов, уменьшение любых прямых или косвенных патологических последствий заболевания, предотвращение метастазов, снижение скорости прогрессирования заболевания, улучшение или ослабление состояния болезни, и ремиссию или улучшение прогноза.
[0122] Как применяется в данном документе, термин «терапевтически эффективное количество» или «эффективное количество» относится к количеству АВР или фармацевтической композиции, предложенных в данном документе, которое при введении субъекту эффективно для лечения заболевания или патологии.
[0123] Как применяется в данном документе, термин «субъект» обозначает субъект-млекопитающее. Иллюстративные субъекты включают в себя людей, обезьян, собак, кошек, мышей, крыс, коров, лошадей, верблюдов, коз, кроликов и овец. В некоторых вариантах осуществления, субъектом является человек. В некоторых вариантах осуществления, субъект имеет заболевание или патологию, которое(ую) можно лечить с помощью АВР, предложенного в данном документе. В некоторых аспектах, заболевание или патология представляет собой рак. В некоторых аспектах, заболевание или патология представляет собой вирусную инфекцию.
[0124] Термин «листок-вкладыш в упаковке» используется для обозначения инструкций, обычно включаемых в коммерческие упаковки терапевтических или диагностических продуктов (например, наборы), которые содержат информацию о показаниях, использовании, дозировке, введении, комбинированной терапии, противопоказаниях и/или предупреждениях, касающихся применения таких терапевтических или диагностических продуктов.
[0125] Как применяется в данном документе, термин «цитотоксический агент» относится к веществу, которое ингибирует или блокирует клеточную функцию, и/или вызывает гибель, или разрушение клеток.
[0126] «Химиотерапевтическое средство» относится к химическому соединению, полезному для лечения рака. Химиотерапевтические агенты включают в себя «антигормональные средства» или «эндокринные терапевтические агенты», которые действуют, чтобы регулировать, уменьшать, блокировать или ингибировать эффекты гормонов, которые могут способствовать росту рака.
[0127] Термин «цитостатический агент» относится к соединению или композиции, которая останавливает рост клетки как in vitro, так и in vivo. В некоторых вариантах осуществления, цитостатический агент представляет собой агент, который уменьшает процент клеток в S-фазе. В некоторых вариантах осуществления, цитостатический агент уменьшает процент клеток в S-фазе, по меньшей мере на 20%, по меньшей мере на около 40%, по меньшей мере на около 60% или по меньшей мере на около 80%.
[0128] Термин «опухоль» относится к любому росту и пролиферации опухолевых клеток, будь то злокачественные или доброкачественные, и ко всем предраковым и раковым клеткам и тканям. Термины «рак», «раковый», «клеточная пролиферативная патология», «пролиферативная патология» и «опухоль» не являются взаимоисключающими, как указано в данном. Термины «клеточная пролиферативная патология» и «пролиферативная патология» относятся к нарушениям, которые связаны с некоторой степенью аномальной клеточной пролиферации. В некоторых вариантах осуществления, клеточная пролиферативная патология представляет собой рак. В некоторых аспектах, опухоль представляет собой солидную опухоль. В некоторых аспектах, опухоль представляет собой гематологическое злокачественное новообразование.
[0129] Термин «фармацевтическая композиция» относится к препарату, который находится в такой форме, чтобы биологическая активность активного ингредиента, содержащегося в нем, была эффективной при лечении субъекта и которая не содержит дополнительных компонентов, которые неприемлемо токсичны для субъекта в количествах, указанных в фармацевтической композиции.
[0130] Термины «модулировать» и «модулирование» относятся к уменьшению или ингибированию или, в качестве альтернативы, активации или увеличению, указанной переменной.
[0131] Термины «увеличить» и «активировать» относятся к увеличению на 10%, 20%, 30%, 40%, 50%, 60%, 70%, 75%, 80%, 85%, 90%, 95% 100%, 2-кратно, 3-кратно, 4-кратно, 5-кратно, 10-кратно, 20-кратно, 50-кратно, 100-кратно или больше для указанной переменной.
[0132] Термины «уменьшить» и «ингибировать» относятся к уменьшению на 10%, 20%, 30%, 40%, 50%, 60%, 70%, 75%, 80%, 85%, 90%, 95%, 2-кратно, 3-кратно, 4-кратно, 5-кратно, 10-кратно, 20-кратно, 50-кратно, 100-кратно или больше для указанной переменной.
[0133] Термин «агонизм» относится к активации рецепторного сигналинга для индукции биологического ответа, связанного с активацией рецептора. «Агонист» представляет собой сущность, которая связывает и выступает агонистом для рецептора.
[0134] Термин «антагонизировать» относится к ингибированию рецепторного сигналинга для ингибирования биологического ответа, связанного с активацией рецептора. «Антагонист» представляет собой сущность, которая связывает и выступает антагонистом для рецептора.
[0135] Термин «эффекторный Т-лимфоцит» включает в себя Т-хелперы (т.е. CD4+) и цитотоксические (т.е. CD8+) Т-лимфоциты. CD4+ эффекторные Т-лимфоциты способствуют развитию нескольких иммунологических процессов, включая созревание В-лимфоцитов в плазматические клетки и В-лимфоциты памяти, а также активацию цитотоксических Т-лимфоцитов и макрофагов. CD8+ эффекторные Т-лимфоциты уничтожают инфицированные вирусом клетки и опухолевые клетки. См. Seder and Ahmed, Nature Immunol., 2003, 4:835-842, включен посредством ссылки в полном объеме, для получения дополнительной информации об эффекторных Т-лимфоцитах.
[0136] Термин «регуляторный Т-лимфоцит» включает в себя клетки, которые регулируют иммунологическую толерантность, например, путем подавления эффекторных Т-лимфоцитов. В некоторых аспектах, регуляторный Т-лимфоцит имеет фенотип CD4+CD25+Foxp3+. В некоторых аспектах, регуляторный Т-лимфоцит имеет фенотип CD8+CD25+. См. Nocentini et al., Br. J. Pharmacol., 2012, 165:2089-2099, включен посредством ссылки в полном объеме, для дополнительной информации о регуляторных Т-лимфоцитах, экспрессирующих TIGIT.
[0137] Термин «дендритная клетка» относится к специализированной антигенпредставляющей клетке, способной активировать наивный Т-лимфоцит и стимулировать рост и дифференциацию В-лимфоцита.
2. TIGIT антиген-связывающие белки
2.1. Связывание TIGIT и клетки-мишени
[0138] Согласно настоящему изобретению предложены АВР, которые специфически связываются с TIGIT. В некоторых аспектах, TIGIT представляет собой hTIGIT (SEQ ID NO: 1). В некоторых аспектах, TIGIT представляет собой cTIGIT (SEQ ID NO: 2). В некоторых аспектах, TIGIT представляет собой mTIGIT с последовательностью, представленной в SEQ ID NO: 3. В некоторых аспектах, TIGIT представляет собой mTIGIT с последовательностью, представленной в SEQ ID NO: 138.
[0139] В некоторых вариантах осуществления, АВР, предложенные в данном документе, специфически связываются с hTIGIT (SEQ ID NO: 1), cTIGIT (SEQ ID NO: 2), и mTIGIT SEQ ID NO: 3. В некоторых вариантах осуществления, АВР, предложенные в данном документе, специфически связываются с hTIGIT (SEQ ID NO: 1), cTIGIT (SEQ ID NO: 2), и mTIGIT SEQ ID NO: 138. В некоторых вариантах осуществления, АВР, предложенные в данном документе, специфически связываются с hTIGIT (SEQ ID NO: 1), cTIGIT (SEQ ID NO: 2). В некоторых вариантах осуществления, АВР, предложенные в данном документе, специфически связываются с hTIGIT (SEQ ID NO: 1). В некоторых вариантах осуществления, АВР, предложенные в данном документе, не связываются с mTIGIT SEQ ID NO: 3. В некоторых вариантах осуществления, АВР, предложенные в данном документе, не связываются с mTIGIT SEQ ID NO: 138.
[0140] В некоторых вариантах осуществления, АВР, предложенные в данном документе, специфически связываются с внеклеточным доменом TIGIT.
[0141] В некоторых вариантах осуществления, АВР, предложенный в данном документе, представляет собой антитело. В некоторых вариантах осуществления, АВР, предложенный в данном документе, представляет собой фрагмент антитела. В некоторых вариантах осуществления, АВР, предложенный в данном документе, представляет собой альтернативный каркас.
[0142] TIGIT может быть экспрессирован на поверхности любой подходящей клетки-мишени. В некоторых вариантах осуществления, клетка-мишень представляет собой Т-лимфоцит. В некоторых вариантах осуществления, клетка-мишень представляет собой эффекторный Т-лимфоцит. В некоторых вариантах осуществления, клетка-мишень представляет собой регуляторный Т-лимфоцит. В некоторых вариантах осуществления, клетка-мишень представляет собой естественный киллер (NK). В некоторых вариантах осуществления, клетка-мишень представляет собой естественный киллер (NKT) Т-лимфоцит.
[0143] В некоторых вариантах осуществления, АВР, предложенные в данном документе, содержат иммуноглобулиновую молекулу. В некоторых вариантах осуществления, АВР, предложенные в данном документе, состоят из иммуноглобулиновой молекулы. В некоторых вариантах осуществления, АВР, предложенные в данном документе, состоят в основном из иммуноглобулиновой молекулы. В некоторых аспектах, иммуноглобулиновая молекула содержит антитело. В некоторых аспектах, иммуноглобулиновая молекула состоит из антитела. В некоторых аспектах, иммуноглобулиновая молекула состоит в основном из антитела.
[0144] В некоторых вариантах осуществления, АВР, предложенные в данном документе, содержат легкую цепь. В некоторых аспектах, легкая цепь представляет собой легкую цепь каппа. В некоторых аспектах, легкая цепь представляет собой легкую цепь лямбда.
[0145] В некоторых вариантах осуществления, АВР, предложенные в данном документе, содержат легкую цепь каппа, содержащую SEQ ID NO: 126.
[0146] В некоторых вариантах осуществления, АВР, предложенные в данном документе, содержат тяжелую цепь. В некоторых аспектах, тяжелая цепь представляет собой IgA. В некоторых аспектах, тяжелая цепь представляет собой IgD. В некоторых аспектах, тяжелая цепь представляет собой IgE. В некоторых аспектах, тяжелая цепь представляет собой IgG. В некоторых аспектах, тяжелая цепь представляет собой IgM. В некоторых аспектах, тяжелая цепь представляет собой IgG1. В некоторых аспектах, тяжелая цепь представляет собой IgG2. В некоторых аспектах, тяжелая цепь представляет собой IgG3. В некоторых аспектах, тяжелая цепь представляет собой IgG4. В некоторых аспектах, тяжелая цепь представляет собой IgA1. В некоторых аспектах, тяжелая цепь представляет собой IgA2.
[0147] В некоторых вариантах осуществления, АВР, предложенные данном документе, содержат тяжелую цепь IgG4, содержащую последовательность, выбранную из SEQ ID NO: 55 и SEQ ID NO: 56. В некоторых вариантах осуществления, АВР, предложенные данном документе, содержат тяжелую цепь IgG1, содержащую последовательность, выбранную из SEQ ID NO: 57 и SEQ ID NO: 125.
[0148] В некоторых вариантах осуществления, АВР, предложенные в данном документе, содержат фрагмент антитела. В некоторых вариантах осуществления, АВР, предложенные в данном документе, состоят из фрагмента антитела. В некоторых вариантах осуществления, АВР, предложенные в данном документе, состоят в основном из фрагмента антитела. В некоторых аспектах, фрагмент антитела представляет собой Fv-фрагмент. В некоторых аспектах, фрагмент антитела представляет собой Fab-фрагмент. В некоторых аспектах, фрагмент антитела представляет собой фрагмент F(ab')2. В некоторых аспектах, фрагмент антитела представляет собой фрагмент Fab'. В некоторых аспектах, фрагмент антитела представляет собой фрагмент scFv (sFv). В некоторых аспектах, фрагмент антитела представляет собой фрагмент scFv-Fc. В некоторых аспектах, фрагмент антитела представляет собой фрагмент однодоменного антитела.
[0149] В некоторых вариантах осуществления, фрагмент антитела, предложенный в данном документе, получают из иллюстративного антитела, предложенного в данном документе. В некоторых вариантах осуществления, фрагменты антитела, предложенные в данном документе, не получают из иллюстративного антитела, предложенного в данном документе, и могут, например, быть выделены de novo в соответствии с предложенными в данном документе способами для получения фрагментов антител.
[0150] В некоторых вариантах осуществления, предложенный фрагмент антитела специфически связывает hTIGIT. В некоторых вариантах осуществления, фрагмент антитела, предложенный в данном документе, специфически связывает cTIGIT. В некоторых вариантах осуществления, фрагмент антитела, предложенный в данном документе, специфически связывает mTIGIT. В некоторых вариантах осуществления, фрагмент антитела, предложенный в данном документе, специфически связывает hTIGIT и cTIGIT. В некоторых вариантах осуществления, фрагмент антитела, предложенный в данном документе, специфически связывает hTIGIT и mTIGIT. В некоторых вариантах осуществления, фрагмент антитела, предложенный в данном документе, специфически связывает cTIGIT и mTIGIT. В некоторых вариантах осуществления, фрагмент антитела, предложенный в данном документе, специфически связывает hTIGIT, cTIGIT и mTIGIT.
[0151] В некоторых вариантах осуществления, фрагмент антитела, полученный из антитела, предложенного в данном документе, сохраняет аффинность, как измерено по KD, к hTIGIT, которая находится в пределах примерно 1,5-кратной, примерно 2-кратной, примерно 3-кратной, примерно 4-кратной, примерно 5-кратной, примерно 6-кратной, примерно 7-кратной, примерно 8-кратной, примерно 9-кратной или примерно 10-кратной аффиности такого антитела. В некоторых вариантах осуществления, фрагмент антитела, полученный из антитела, предложенного в данном документе, сохраняет аффинность, как измерено по KD, к cTIGIT, которая находится в пределах примерно 1,5-кратной, примерно 2-кратной, примерно 3-кратной, примерно 4-кратной, примерно 5-кратной, примерно 6-кратной, примерно 7-кратной, примерно 8-кратной, примерно 9-кратной или примерно 10-кратной аффиности такого антитела. В некоторых вариантах осуществления, фрагмент антитела, полученный из антитела, предложенного в данном документе, сохраняет аффинность, как измерено по KD, к mTIGIT, которая находится в пределах примерно 1,5-кратной, примерно 2-кратной, примерно 3-кратной, примерно 4-кратной, примерно 5-кратной, примерно 6-кратной, примерно 7-кратной, примерно 8-кратной, примерно 9-кратной или примерно 10-кратной аффиности такого антитела. В некоторых вариантах осуществления, фрагмент антитела, полученный из антитела, предложенного в данном документе, сохраняет аффинность, как измерено по KD, как к hTIGIT так и к cTIGIT, которая находится в пределах примерно 1,5-кратной, примерно 2-кратной, примерно 3-кратной, примерно 4-кратной, примерно 5-кратной, примерно 6-кратной, примерно 7-кратной, примерно 8-кратной, примерно 9-кратной или примерно 10-кратной аффиности такого антитела. В некоторых вариантах осуществления, фрагмент антитела, полученный из антитела, предложенного в данном документе, сохраняет аффинность, как измерено по KD, как к hTIGIT так и к mTIGIT, которая находится в пределах примерно 1,5-кратной, примерно 2-кратной, примерно 3-кратной, примерно 4-кратной, примерно 5-кратной, примерно 6-кратной, примерно 7-кратной, примерно 8-кратной, примерно 9-кратной или примерно 10-кратной аффиности такого антитела. В некоторых вариантах осуществления, фрагмент антитела, полученный из антитела, предложенного в данном документе, сохраняет аффинность, как измерено по KD, как к cTIGIT так и к mTIGIT, которая находится в пределах примерно 1,5-кратной, примерно 2-кратной, примерно 3-кратной, примерно 4-кратной, примерно 5-кратной, примерно 6-кратной, примерно 7-кратной, примерно 8-кратной, примерно 9-кратной или примерно 10-кратной аффиности такого антитела. В некоторых вариантах осуществления, фрагмент антитела, полученный из антитела, предложенного в данном документе, сохраняет аффинность, как измерено по KD, ко всем трем hTIGIT, cTIGIT и mTIGIT, которая находится в пределах примерно 1,5-кратной, примерно 2-кратной, примерно 3-кратной, примерно 4-кратной, примерно 5-кратной, примерно 6-кратной, примерно 7-кратной, примерно 8-кратной, примерно 9-кратной или примерно 10-кратной аффиности такого антитела.
[0152] В некоторых вариантах осуществления, фрагмент антитела, предложенный в данном документе, сохраняет способность антагонизировать TIGIT, как измерено одним или больше анализами или биологическими эффектами, описанными в данном документе. В некоторых вариантах осуществления, фрагмент антитела, предложенный в данном документе, сохраняет способность предотвращать взаимодействие TIGIT с одним или большим количеством его лигандов, как описано в данном документе.
[0153] В некоторых вариантах осуществления, фрагмент антитела, предложенный в данном документе, конкурирует за связывание с TIGIT с антителом, выбранным из МАБ1, МАБ2, МАБ3, МАБ4, МАБ5, МАБ6, МАБ7, МАБ8, МАБ9, МАБ10, МАБ11, МАБ12, МАБ13, МАБ14, МАБ15, МАБ16, МАБ17, МАБ18, МАБ19, МАБ20 или МАБ21, каждое из которых представлено в Таблице 5 данного раскрытия изобретения.
[0154] В некоторых вариантах осуществления, фрагмент антитела, предложенный в данном документе, ингибирует связывание CD155 с TIGIT. В некоторых вариантах осуществления, фрагмент антитела, предложенный в данном документе, ингибирует связывание CD112 с TIGIT. В некоторых вариантах осуществления, фрагмент антитела, предложенный в данном документе, ингибирует связывание CD226 с TIGIT.
[0155] В некоторых вариантах осуществления, фрагмент антитела, предложенный в данном документе, активирует эффекторный Т-лимфоцит или клетку естественный киллер (NK). В некоторых вариантах осуществления, фрагмент антитела, предложенный в данном документе, уменьшает количество регуляторных Т-лимфоцитов в ткани или в кровеносной системе. В некоторых вариантах осуществления, фрагмент антитела, предложенный в данном документе, ингибирует подавление эффекторного Т-лимфоцита регуляторным Т-лимфоцитом.
[0156] В некоторых вариантах осуществления, фрагмент антитела, предложенный в данном документе, не связывается специфически с любыми из PVRL1, PVRL2, PVRL3 или PVRL4.
[0157] В некоторых вариантах осуществления, фрагмент антитела, предложенный в данном документе, связывает TIGIT мыши (mTIGIT; SEQ ID NO: 3) с аффинностью ниже (как указано более высоким KD), чем аффинность фрагмента антитела к hTIGIT, или не связывает mTIGIT.
[0158] В некоторых вариантах осуществления, фрагмент антитела, предложенный в данном документе, связывает один и тот же эпитоп TIGIT в качестве такого антитела.
[0159] В некоторых вариантах осуществления, АВР, предложенные в данном документе, являются моноклинальными антителами. В некоторых вариантах осуществления, АВР, предложенные в данном документе, являются поликлональными антителами.
[0160] В некоторых вариантах осуществления, АВР, предложенные в данном документе, содержат химерное антитело. В некоторых вариантах осуществления, АВР, предложенные в данном документе, состоят из химерного антитела. В некоторых вариантах осуществления, АВР, предложенные в данном документе, состоят в основном из химерного антитела. В некоторых вариантах осуществления, АВР, предложенные в данном документе, содержат гуманизированное антитело. В некоторых вариантах осуществления, АВР, предложенные в данном документе, состоят из гуманизированного антитела. В некоторых вариантах осуществления, АВР, предложенные в данном документе, состоят в основном из гуманизированного антитела. В некоторых вариантах осуществления, АВР, предложенные в данном документе, содержат человеческое антитело. В некоторых вариантах осуществления, АВР, предложенные в данном документе, состоят из человеческого антитела. В некоторых вариантах осуществления, АВР, предложенные в данном документе, состоят в основном из человеческого антитела.
[0161] В некоторых вариантах осуществления, АВР, предложенные в данном документе, являются с созревшей аффинностью. В некоторых аспектах, АВР с созревшей аффинностью являются АВР с созревшей аффинностью, полученными из иллюстративного АВР, предложенного в данном документе.
[0162] В некоторых вариантах осуществления, АВР, предложенные в данном документе, содержат альтернативный каркас. В некоторых вариантах осуществления, АВР, предложенные в данном документе, состоят из альтернативного каркаса. В некоторых вариантах осуществления, АВР, предложенные в данном документе, состоят в основном из альтернативного каркаса. Может применятся любой подходящий альтернативный каркас. В некоторых аспектах, альтернативный каркас выбирают из Adnectin™, iMab, Anticalin®, EETI-II/AGRP, домена Kunitz, аптамера тиоредоксинового пептида, Affibody®, DARPin, Аффилина, Тетранектина, Финомера и Авимера.
[0163] В некоторых вариантах осуществления, АВР, предложенный в данном документе, ингибирует связывание TIGIT с одним или большим количеством лигандов TIGIT. В некоторых аспектах, лиганд TIGIT выбирают из одного или большего количества рецепторов полиовируса (PVR, CD155) и нектина-2 (CD112, PVRL2). В некоторых аспектах, АВР ингибирует связывание TIGIT с одним или большим количеством лигандов TIGIT по меньшей мере на 50%. В некоторых аспектах, АВР ингибирует связывание TIGIT с одним или большим количеством лигандов TIGIT по меньшей мере на 75%. В некоторых аспектах, АВР ингибирует связывание TIGIT с одним или большим количеством лигандов TIGIT по меньшей мере на 90%. В некоторых аспектах, АВР ингибирует связывание TIGIT с одним или большим количеством лигандов TIGIT по меньшей мере на 95%.
[0164] В некоторых вариантах осуществления, АВР по изобретению представляет собой АВР, который конкурирует с иллюстративным АВР, предложенным в данном документе. В некоторых аспектах, АВР, который конкурирует с иллюстративным АВР, предложенным в данном документе, связывает тот же эпитоп, что и иллюстративный АВР, предложенный в данном документе.
[0165] В некоторых вариантах осуществления, АВР, предложенный в данном документе, не связывает PVRL4.
[0166] Известно, что когда антитело экспрессируется в клетках, антитело модифицируется после трансляции. Примеры посттрансляционной модификации включают: отщепление лизина на С-конце тяжелой цепи карбоксипептидазой; модификацию глутамина или глутаминовой кислоты на N-конце тяжелой цепи и легкой цепи до пироглутаминовой кислоты путем пироглутамилирования; гликозилирование; окисление; деамидирование; и гликирование, и известно, что такие посттрансляционные модификации происходят в различных антителах (см. Journal of Pharmaceutical Sciences, 2008, Vol. 97, p. 2426-2447, включен посредством ссылки в полном объеме). В некоторых вариантах осуществления, АВР по изобретению представляет собой антитело или его антиген-связывающий фрагмент, которое(ый) подверглось(гся) посттрансляционному модифицированию. Примеры антитела или его антиген-связывающего фрагмента, которые подверглись посттрансляционному модифицированию, включают антитело или его антиген-связывающие фрагменты, которые подверглись пироглутамилированию на N-конце вариабельной области тяжелой цепи и/или удалению лизина на С-конце тяжелой цепи. В данной области техники известно, что такое посттрансляционное модифицирование, вызванное пироглутамилированием на N-конце и удалением лизина на С-конце, не оказывает никакого влияния на активность антитела или его фрагмента (Analytical Biochemistry, 2006, Vol. 348, p. 24-39, включен посредством ссылки в полном объеме).
2.2. Последовательности TIGIT антиген-связывающих белков
2.2.1. Домены VH
[0167] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH, выбранную из SEQ ID NO: 4-24. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 4. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 5. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 6. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 7. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 8. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 9. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 10. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 11. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 12. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 13. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 14. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 15. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 16. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 17. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 18. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 19. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 20. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 21. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 22. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 23. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 24.
[0168] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH, имеющую по меньшей мере 50%, 60%, 70%, 80%, 90%, 95% или 99% идентичности с иллюстративной последовательностью VH, предложенной в SEQ ID NO: 4-24. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH, предложенную в SEQ ID NO: 4-24, с вплоть до 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25 аминокислотными заменами. В некоторых аспектах, аминокислотные замены представляют собой консервативные аминокислотные замены. В некоторых вариантах осуществления, АВР, описанные в этом параграфе, упоминаются в данном документе как «варианты». В некоторых вариантах осуществления, такие варианты получают из последовательности, предложенной в данном документе, например, аффиным созреванием, сайт-направленным мутагенезом, случайным мутагенезом или любым другим способом, известным в данной области техники или описанным в данном документе. В некоторых вариантах осуществления, такие варианты не получены из последовательности, предложенной в данном документе, и могут, например, быть выделены de novo в соответствии с предложенными в данном документе способами для получения АВР.
2.2.2. Домены VL
[0169] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VL, выбранную из SEQ ID NO: 25-28. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VL SEQ ID NO: 25. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VL SEQ ID NO: 26. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VL SEQ ID NO: 27. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VL SEQ ID NO: 28.
[0170] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VL, имеющую по меньшей мере 50%, 60%, 70%, 80%, 90%, 95% или 99% идентичности с иллюстративной последовательностью VL, предложенной в SEQ ID NO: 25-28. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VL, предложенную в SEQ ID NO: 25-28, с вплоть до 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25 аминокислотными заменами. В некоторых аспектах, аминокислотные замены представляют собой консервативные аминокислотные замены. В некоторых вариантах осуществления, АВР, описанные в этом параграфе, упоминаются в данном документе как «варианты». В некоторых вариантах осуществления, такие варианты получают из последовательности, предложенной в данном документе, например, аффиным созреванием, сайт-направленным мутагенезом, случайным мутагенезом или любым другим способом, известным в данной области техники или описанным в данном документе. В некоторых вариантах осуществления, такие варианты не получены из последовательности, предложенной в данном документе, и могут, например, быть выделены de novo в соответствии с предложенными в данном документе способами для получения АВР.
2.2.3. Комбинации VH-VL
[0171] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH, выбранную из SEQ ID NO: 4-24, и последовательность VL, выбранную из SEQ ID NO: 25-28.
[0172] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 4, и последовательность VL SEQ ID NO: 25. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 5, и последовательность VL SEQ ID NO: 25. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 6, и последовательность VL SEQ ID NO: 25. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 7, и последовательность VL SEQ ID NO: 25. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 8, и последовательность VL SEQ ID NO: 25. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 9, и последовательность VL SEQ ID NO: 26. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 10, и последовательность VL SEQ ID NO: 26. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 11, и последовательность VL SEQ ID NO: 26. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 12, и последовательность VL SEQ ID NO: 26. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 13, и последовательность VL SEQ ID NO: 26. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 14, и последовательность VL SEQ ID NO: 26. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 15, и последовательность VL SEQ ID NO: 26. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 16, и последовательность VL SEQ ID NO: 27. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 17, и последовательность VL SEQ ID NO: 27. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 18, и последовательность VL SEQ ID NO: 27. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 19, и последовательность VL SEQ ID NO: 27. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 20, и последовательность VL SEQ ID NO: 27. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 21, и последовательность VL SEQ ID NO: 27. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 22, и последовательность VL SEQ ID NO: 28. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 23, и последовательность VL SEQ ID NO: 28. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 24, и последовательность VL SEQ ID NO: 28.
[0173] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 4, и последовательность VL SEQ ID NO: 26. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 4, и последовательность VL SEQ ID NO: 27. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 4, и последовательность VL SEQ ID NO: 28.
[0174] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 5, и последовательность VL SEQ ID NO: 26. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 5, и последовательность VL SEQ ID NO: 27. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 5, и последовательность VL SEQ ID NO: 28.
[0175] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 6, и последовательность VL SEQ ID NO: 26. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 6, и последовательность VL SEQ ID NO: 27. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 6, и последовательность VL SEQ ID NO: 28.
[0176] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 7, и последовательность VL SEQ ID NO: 26. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 7, и последовательность VL SEQ ID NO: 27. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 7, и последовательность VL SEQ ID NO: 28.
[0177] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 8, и последовательность VL SEQ ID NO: 26. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 8, и последовательность VL SEQ ID NO: 27. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 8, и последовательность VL SEQ ID NO: 28.
[0178] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 9, и последовательность VL SEQ ID NO: 25. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 9, и последовательность VL SEQ ID NO: 27. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 9, и последовательность VL SEQ ID NO: 28.
[0179] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 10, и последовательность VL SEQ ID NO: 25. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 10, и последовательность VL SEQ ID NO: 27. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 10, и последовательность VL SEQ ID NO: 28.
[0180] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 11, и последовательность VL SEQ ID NO: 25. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 11, и последовательность VL SEQ ID NO: 27. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 11, и последовательность VL SEQ ID NO: 28.
[0181] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 12, и последовательность VL SEQ ID NO: 25. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 12, и последовательность VL SEQ ID NO: 27. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 12, и последовательность VL SEQ ID NO: 28.
[0182] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 13, и последовательность VL SEQ ID NO: 25. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 13, и последовательность VL SEQ ID NO: 27. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 13, и последовательность VL SEQ ID NO: 28.
[0183] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 14, и последовательность VL SEQ ID NO: 25. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 14, и последовательность VL SEQ ID NO: 27. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 14, и последовательность VL SEQ ID NO: 28.
[0184] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 15, и последовательность VL SEQ ID NO: 25. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 15, и последовательность VL SEQ ID NO: 27. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 15, и последовательность VL SEQ ID NO: 28.
[0185] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 16, и последовательность VL SEQ ID NO: 25. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 16, и последовательность VL SEQ ID NO: 26. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 16, и последовательность VL SEQ ID NO: 28.
[0186] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 17, и последовательность VL SEQ ID NO: 25. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 17, и последовательность VL SEQ ID NO: 26. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 17, и последовательность VL SEQ ID NO: 28.
[0187] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 18, и последовательность VL SEQ ID NO: 25. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 18, и последовательность VL SEQ ID NO: 26. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 18, и последовательность VL SEQ ID NO: 28.
[0188] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 19, и последовательность VL SEQ ID NO: 25. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 19, и последовательность VL SEQ ID NO: 26. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 19, и последовательность VL SEQ ID NO: 28.
[0189] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 20, и последовательность VL SEQ ID NO: 25. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 20, и последовательность VL SEQ ID NO: 26. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 20, и последовательность VL SEQ ID NO: 28.
[0190] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 21, и последовательность VL SEQ ID NO: 25. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 21, и последовательность VL SEQ ID NO: 26. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 21, и последовательность VL SEQ ID NO: 28.
[0191] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 22, и последовательность VL SEQ ID NO: 25. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 22, и последовательность VL SEQ ID NO: 26.
В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO:22, и последовательность VL SEQ ID NO: 27.
[0192] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 23, и последовательность VL SEQ ID NO: 25. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 23, и последовательность VL SEQ ID NO: 26. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 23, и последовательность VL SEQ ID NO: 27.
[0193] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 24, и последовательность VL SEQ ID NO: 25. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 24, и последовательность VL SEQ ID NO: 26. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH SEQ ID NO: 24, и последовательность VL SEQ ID NO: 27.
[0194] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH, имеющую по меньшей мере 50%, 60%, 70%, 80%, 90%, 95% или 99% идентичности с иллюстративной последовательностью VH, предложенной в SEQ ID NO: 4-24, и последовательность VL, имеющую по меньшей мере 50%, 60%, 70%, 80%, 90%, 95% или 99% идентичности с иллюстративной последовательностью VL, предложенной в SEQ ID NO: 25-28. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит последовательность VH, предложенную в SEQ ID NO: 4-24, с вплоть до 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25 аминокислотными заменами, и последовательность VL, предложенную в SEQ ID NO: 25-28, с вплоть до 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25 аминокислотными заменами. В некоторых аспектах, аминокислотные замены представляют собой консервативные аминокислотные замены. В некоторых вариантах осуществления, АВР, описанные в этом параграфе, упоминаются в данном документе как «варианты». В некоторых вариантах осуществления, такие варианты получают из последовательности, предложенной в данном документе, например, аффинным созреванием, сайт-направленным мутагенезом, случайным мутагенезом или любым другим способом, известным в данной области техники или описанным в данном документе. В некоторых вариантах осуществления, такие варианты не получены из последовательности, предложенной в данном документе, и могут, например, быть выделены de novo в соответствии с предложенными в данном документе способами для получения АВР.
2.2.4. CDR
[0195] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит от одного до трех CDR домена VH, выбранного из SEQ ID NO: 4-24. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит от двух до трех CDR домена VH, выбранного из SEQ ID NO: 4-24. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит три CDR домена VH, выбранного из SEQ ID NO: 4-24. В некоторых аспектах, CDR представляют собой CDR по Кабату. В некоторых аспектах, CDR представляют собой CDR по Чотиа. В некоторых аспектах, CDR представляют собой CDR по IMGT.
[0196] В некоторых вариантах осуществления, CDR представляют собой CDR, имеющие по меньшей мере около 50%, 75%, 80%, 85%, 90% или 95% идентичности с CDR-H1, CDR-Н2 или CDR-H3 SEQ ID NO: 4-24. В некоторых вариантах осуществления, CDR-H1 представляет собой CDR-H1 домена VH, выбранного из SEQ ID NO: 4-24, с вплоть до 1, 2, 3, 4 или 5 аминокислотными заменами. В некоторых вариантах осуществления, CDR-H2 представляет собой CDR-H2 домена VH, выбранного из SEQ ID NO: 4-24, с вплоть до 1, 2, 3, 4, 5, 6, 7 или 8 аминокислотными заменами. В некоторых вариантах осуществления, CDR-Н3 представляет собой CDR-H3 домена VH, выбранного из SEQ ID NO: 4-24, с вплоть до 1, 2, 3, 4, 5, 6, 7 или 8 аминокислотными заменами. В некоторых аспектах, аминокислотные замены представляют собой консервативные аминокислотные замены. В некоторых вариантах осуществления, АВР, описанные в этом параграфе, упоминаются в данном документе как «варианты». В некоторых вариантах осуществления, такие варианты получают из последовательности, предложенной в данном документе, например, аффинным созреванием, сайт-направленным мутагенезом, случайным мутагенезом или любым другим способом, известным в данной области техники или описанным в данном документе. В некоторых вариантах осуществления, такие варианты не получены из последовательности, предложенной в данном документе, и могут, например, быть выделены de novo в соответствии с предложенными в данном документе способами для получения АВР.
[0197] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит от одного до трех CDR домена VL, выбранного из SEQ ID NO: 25-28. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит от двух до трех CDR домена VL, выбранного из SEQ ID NO: 25-28. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит три CDR домена VL, выбранного из SEQ ID NO: 25-28. В некоторых аспектах, CDR представляют собой CDR по Кабату. В некоторых аспектах, CDR представляют собой CDR по Чотиа. В некоторых аспектах, CDR представляют собой CDR по IMGT.
[0198] В некоторых вариантах осуществления, CDR представляют собой CDR, имеющие по меньшей мере около 50%, 75%, 80%, 85%, 90% или 95% идентичности с CDR-L1, CDR-L2 или CDR-L3 SEQ ID NO: 25-28. В некоторых вариантах осуществления, CDR-L1 представляет собой CDR-L1 домена VL, выбранного из SEQ ID NO: 25-28, с вплоть до 1, 2, 3, 4, 5 или 6 аминокислотными заменами. В некоторых вариантах осуществления, CDR-L2 представляет собой CDR-L2 домена VL, выбранного из SEQ ID NO: 25-28, с вплоть до 1, 2, 3 или 4 аминокислотными заменами. В некоторых вариантах осуществления, CDR-L3 представляет собой CDR-L3 домена VL, выбранного из SEQ ID NO: 25-28, с вплоть до 1, 2, 3, 4 или 5 аминокислотными заменами. В некоторых аспектах, аминокислотные замены представляют собой консервативные аминокислотные замены. В некоторых вариантах осуществления, АВР, описанные в этом параграфе, упоминаются в данном документе как «варианты». В некоторых вариантах осуществления, такие варианты получают из последовательности, предложенной в данном документе, например, аффинным созреванием, сайт-направленным мутагенезом, случайным мутагенезом или любым другим способом, известным в данной области техники или описанным в данном документе. В некоторых вариантах осуществления, такие варианты не получены из последовательности, предложенной в данном документе, и могут, например, быть выделены de novo в соответствии с предложенными в данном документе способами для получения АВР.
[0199] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит от одного до трех CDR домена VH, выбранного из SEQ ID NO: 4-24, и от одного до трех CDR домена VL, выбранного из SEQ ID NO: 25-28. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит от двух до трех CDR домена VH, выбранного из SEQ ID NO: 4-24, и от одного до трех CDR домена VL, выбранного из SEQ ID NO: 25-28. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит три CDR домена VH, выбранного из SEQ ID NO: 4-24, и три CDR домена VL, выбранного из SEQ ID NO: 25-28. В некоторых аспектах, CDR представляют собой CDR по Кабату. В некоторых аспектах, CDR представляют собой CDR по Чотиа. В некоторых аспектах, CDR представляют собой CDR по IMGT.
[0200] В некоторых вариантах осуществления, CDR представляют собой CDR, имеющие по меньшей мере около 50%, 75%, 80%, 85%, 90% или 95% идентичности с CDR-H1, CDR-Н2 или CDR-H3 SEQ ID NO: 4-24, и по меньшей мере около 50%, 75%, 80%, 85%, 90% или 95% идентичности с CDR-L1, CDR-L2 или CDR-L3 SEQ ID NO: 25-28. В некоторых вариантах осуществления, CDR-H1 представляет собой CDR-H1 домена VH, выбранного из SEQ ID NO: 4-24, с вплоть до 1, 2, 3, 4 или 5 аминокислотными заменами; CDR-H2 представляет собой CDR-H2 домена VH, выбранного из SEQ ID NO: 4-24, с вплоть до 1, 2, 3, 4, 5, 6, 7 или 8 аминокислотными заменами; CDR-H3 представляет собой CDR-H3 домена VH, выбранного из SEQ ID NO: 4-24, с вплоть до 1, 2, 3, 4, 5, 6, 7 или 8 аминокислотными заменами; CDR-L1 представляет собой CDR-L1 домена VL, выбранного из SEQ ID NO: 25-28, с вплоть до 1, 2, 3, 4, 5 или 6 аминокислотными заменами; CDR-L2 представляет собой CDR-L2 домена VL, выбранного из SEQ ID NO: 25-28, с вплоть до 1, 2, 3 или 4 аминокислотными заменами; CDR-L3 представляет собой CDR-L3 домена VL, выбранного из SEQ ID NO: 25-28, с вплоть до 1, 2, 3, 4 или 5 аминокислотными заменами. В некоторых аспектах, аминокислотные замены представляют собой консервативные аминокислотные замены. В некоторых вариантах осуществления, АВР, описанные в этом параграфе, упоминаются в данном документе как «варианты». В некоторых вариантах осуществления, такие варианты получают из последовательности, предложенной в данном документе, например, аффинным созреванием, сайт-направленным мутагенезом, случайным мутагенезом или любым другим способом, известным в данной области техники или описанным в данном документе. В некоторых вариантах осуществления, такие варианты не получены из последовательности, предложенной в данном документе, и могут, например, быть выделены de novo в соответствии с предложенными в данном документе способами для получения АВР.
[0201] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-H3, выбранную из SEQ ID NO: 29-35. В некоторых аспектах, CDR-H3 имеет по меньшей мере около 50%, 75%, 80%, 85%, 90% или 95% идентичности с CDR-H3 SEQ ID NO: 29-35. В некоторых аспектах, CDR-H3 представляет собой CDR-H3 в соответствии с системой нумерации IMGT. В некоторых вариантах осуществления, CDR-H3 представляет собой CDR-H3, выбранную из SEQ ID NO: 29-35, с вплоть до 1, 2, 3, 4, 5, 6, 7 или 8 аминокислотными заменами. В некоторых аспектах, аминокислотные замены представляют собой консервативные аминокислотные замены. В некоторых вариантах осуществления, АВР, описанные в этом параграфе, упоминаются в данном документе как «варианты». В некоторых вариантах осуществления, такие варианты получают из последовательности, предложенной в данном документе, например, аффинным созреванием, сайт-направленным мутагенезом, случайным мутагенезом или любым другим способом, известным в данной области техники или описанным в данном документе. В некоторых вариантах осуществления, такие варианты не получены из последовательности, предложенной в данном документе, и могут, например, быть выделены de novo в соответствии с предложенными в данном документе способами для получения АВР.
[0202] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-H2, выбранную из SEQ ID NO: 36-47. В некоторых аспектах, CDR-H2 имеет по меньшей мере около 50%, 75%, 80%, 85%, 90% или 95% идентичности с CDR-H2 SEQ ID NO: 36-47. В некоторых аспектах, CDR-H2 представляет собой CDR-H2 в соответствии с системой нумерации по Кабату. В некоторых вариантах осуществления, CDR-H2 представляет собой CDR-H2, выбранную из SEQ ID NO: 36-47, с вплоть до 1, 2, 3, 4, 5, 6, 7 или 8 аминокислотными заменами. В некоторых аспектах, аминокислотные замены представляют собой консервативные аминокислотные замены. В некоторых вариантах осуществления, АВР, описанные в этом параграфе, упоминаются в данном документе как «варианты». В некоторых вариантах осуществления, такие варианты получают из последовательности, предложенной в данном документе, например, аффинным созреванием, сайт-направленным мутагенезом, случайным мутагенезом или любым другим способом, известным в данной области техники или описанным в данном документе. В некоторых вариантах осуществления, такие варианты не получены из последовательности, предложенной в данном документе, и могут, например, быть выделены de novo в соответствии с предложенными в данном документе способами для получения АВР.
[0203] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-H1, выбранную из SEQ ID NO: 48-54 или 58-62. В некоторых аспектах, CDR-Н1 имеет по меньшей мере около 50%, 75%, 80%, 85%, 90% или 95% идентичности с CDR-H1 SEQ ID NO: 48-54 или 58-62. В некоторых аспектах, CDR-H1 представляет собой CDR-Н1, которая охватывает CDR-H1, как определено системами нумерации по Чотиа и Кабату. В некоторых вариантах осуществления, CDR-H1 представляет собой CDR-H1, выбранную из SEQ ID NO: 48-54 или 58-62, с вплоть до 1, 2, 3, 4 или 5 аминокислотными заменами. В некоторых аспектах, аминокислотные замены представляют собой консервативные аминокислотные замены. В некоторых вариантах осуществления, АВР, описанные в этом параграфе, упоминаются в данном документе как «варианты». В некоторых вариантах осуществления, такие варианты получают из последовательности, предложенной в данном документе, например, аффинным созреванием, сайт-направленным мутагенезом, случайным мутагенезом или любым другим способом, известным в данной области техники или описанным в данном документе. В некоторых вариантах осуществления, такие варианты не получены из последовательности, предложенной в данном документе, и могут, например, быть выделены de novo в соответствии с предложенными в данном документе способами для получения АВР.
[0204] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-H3, выбранную из SEQ ID NO: 29-35, и CDR-H2, выбранную из SEQ ID NO: 36-47. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-H3, выбранную из SEQ ID NO: 29-35, CDR-H2, выбранную из SEQ ID NO: 36-47, и CDR-H1, выбранную из SEQ ID NO: 48-54 или 58-62. В некоторых вариантах осуществления, CDR-H3 имеет по меньшей мере около 50%, 75%, 80%, 85%, 90% или 95% идентичности с CDR-H3 SEQ ID NO: 29-35, CDR-H2 имеет по меньшей мере около 50%, 75%, 80%, 85%, 90% или 95% идентичности с CDR-H2 SEQ ID NO: 36-47, CDR-H1 имеет по меньшей мере около 50%, 75%, 80%, 85%, 90% или 95% идентичности с CDR-H1 SEQ ID NO: 48-54 или 58-62. В некоторых вариантах осуществления, CDR-H3 представляет собой CDR-H3, выбранную из SEQ ID NO: 29-35, с вплоть до 1, 2, 3, 4, 5, 6, 7 или 8 аминокислотными заменами; CDR-H2 представляет собой CDR-H2, выбранную из SEQ ID NO: 36-47, с вплоть до 1, 2, 3, 4, 5, 6, 7 или 8 аминокислотными заменами; и CDR-H1 представляет собой CDR-H1, выбранную из SEQ ID NO: 48-54 или 58-62, с вплоть до 1, 2, 3, 4 или 5 аминокислотными заменами. В некоторых аспектах, аминокислотные замены представляют собой консервативные аминокислотные замены. В некоторых вариантах осуществления, АВР, описанные в этом параграфе, упоминаются в данном документе как «варианты». В некоторых вариантах осуществления, такие варианты получают из последовательности, предложенной в данном документе, например, аффинным созреванием, сайт-направленным мутагенезом, случайным мутагенезом или любым другим способом, известным в данной области техники или описанным в данном документе. В некоторых вариантах осуществления, такие варианты не получены из последовательности, предложенной в данном документе, и могут, например, быть выделены de novo в соответствии с предложенными в данном документе способами для получения АВР.
[0205] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-L3, выбранную из SEQ ID NO: 63-66. В некоторых аспектах, CDR-L3 имеет по меньшей мере около 50%, 75%, 80%, 85%, 90% или 95% идентичности с CDR-L3 SEQ ID NO: 63-66. В некоторых аспектах, CDR-L3 представляет собой CDR-L3 в соответствии с системами нумерации по Кабату, Чотиа и IMGT. В некоторых вариантах осуществления, CDR-L3 представляет собой CDR-L3, выбранную из SEQ ID NO: 63-66, с вплоть до 1, 2, 3, 4 или 5 аминокислотными заменами. В некоторых аспектах, аминокислотные замены представляют собой консервативные аминокислотные замены. В некоторых вариантах осуществления, АВР, описанные в этом параграфе, упоминаются в данном документе как «варианты». В некоторых вариантах осуществления, такие варианты получают из последовательности, предложенной в данном документе, например, аффинным созреванием, сайт-направленным мутагенезом, случайным мутагенезом или любым другим способом, известным в данной области техники или описанным в данном документе. В некоторых вариантах осуществления, такие варианты не получены из последовательности, предложенной в данном документе, и могут, например, быть выделены de novo в соответствии с предложенными в данном документе способами для получения АВР.
[0206] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-L2, выбранную из SEQ ID NO: 67-69. В некоторых аспектах, CDR-L2 имеет по меньшей мере около 50%, 75%, 80%, 85%, 90% или 95% идентичности с CDR-L2 SEQ ID NO: 67-69. В некоторых аспектах, CDR-L2 представляет собой CDR-L2 в соответствии с системами нумерации по Кабату и Чотиа. В некоторых вариантах осуществления, CDR-L2 представляет собой CDR-L2, выбранную из SEQ ID NO: 67-69, с вплоть до 1, 2, 3 или 4 аминокислотными заменами. В некоторых аспектах, аминокислотные замены представляют собой консервативные аминокислотные замены. В некоторых вариантах осуществления, АВР, описанные в этом параграфе, упоминаются в данном документе как «варианты». В некоторых вариантах осуществления, такие варианты получают из последовательности, предложенной в данном документе, например, аффинным созреванием, сайт-направленным мутагенезом, случайным мутагенезом или любым другим способом, известным в данной области техники или описанным в данном документе. В некоторых вариантах осуществления, такие варианты не получены из последовательности, предложенной в данном документе, и могут, например, быть выделены de novo в соответствии с предложенными в данном документе способами для получения АВР.
[0207] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-L1, выбранную из SEQ ID NO: 70-72. В некоторых аспектах, CDR-L1 имеет по меньшей мере около 50%, 75%, 80%, 85%, 90% или 95% идентичности с CDR-L1 SEQ ID NO: 70-72. В некоторых аспектах, CDR-L1 представляет собой CDR-L1 в соответствии с системами нумерации по Кабату и Чотиа. В некоторых вариантах осуществления, CDR-L1 представляет собой CDR-L1, выбранную из SEQ ID NO: 70-72, с вплоть до 1, 2, 3, 4, 5 или 6 аминокислотными заменами. В некоторых аспектах, аминокислотные замены представляют собой консервативные аминокислотные замены. В некоторых вариантах осуществления, АВР, описанные в этом параграфе, упоминаются в данном документе как «варианты». В некоторых вариантах осуществления, такие варианты получают из последовательности, предложенной в данном документе, например, аффинным созреванием, сайт-направленным мутагенезом, случайным мутагенезом или любым другим способом, известным в данной области техники или описанным в данном документе. В некоторых вариантах осуществления, такие варианты не получены из последовательности, предложенной в данном документе, и могут, например, быть выделены de novo в соответствии с предложенными в данном документе способами для получения АВР.
[0208] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-L3, выбранную из SEQ ID NO: 63-66, и CDR-L2, выбранную из SEQ ID NO: 67-69. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-L3, выбранную из SEQ ID NO: 63-66, CDR-L2, выбранную из SEQ ID NO: 67-69, и CDR-L1, выбранную из SEQ ID NO: 70-72. В некоторых вариантах осуществления, CDR-L3 имеет по меньшей мере около 50%, 75%, 80%, 85%, 90% или 95% идентичности с CDR-L3 SEQ ID NO: 63-66, CDR-L2 имеет по меньшей мере около 50%, 75%, 80%, 85%, 90% или 95% идентичности с CDR-L2 SEQ ID NO: 67-69, и CDR-L1 имеет по меньшей мере около 50%, 75%, 80%, 85%, 90% или 95% идентичности с CDR-L1 SEQ ID NO: 70-72. В некоторых вариантах осуществления, CDR-L3 представляет собой CDR-L3, выбранную из SEQ ID NO: 63-66, с вплоть до 1, 2, 3, 4 или 5 аминокислотными заменами; CDR-L2 представляет собой CDR-L2, выбранную из SEQ ID NO: 67-69, с вплоть до 1, 2, 3 или 4 аминокислотными заменами; и CDR-L1 представляет собой CDR-L1, выбранную из SEQ ID NO: 70-72, с вплоть до 1, 2, 3, 4, 5 или 6 аминокислотными заменами. В некоторых аспектах, аминокислотные замены представляют собой консервативные аминокислотные замены. В некоторых вариантах осуществления, АВР, описанные в этом параграфе, упоминаются в данном документе как «варианты». В некоторых вариантах осуществления, такие варианты получают из последовательности, предложенной в данном документе, например, аффинным созреванием, сайт-направленным мутагенезом, случайным мутагенезом или любым другим способом, известным в данной области техники или описанным в данном документе. В некоторых вариантах осуществления, такие варианты не получены из последовательности, предложенной в данном документе, и могут, например, быть выделены de novo в соответствии с предложенными в данном документе способами для получения АВР.
[0209] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-H3, выбранную из SEQ ID NO: 29-35, CDR-H2, выбранную из SEQ ID NO: 36-47, CDR-H1, выбранную из SEQ ID NO: 48-54 или 58-62, CDR-L3, выбранную из SEQ ID NO: 63-66, CDR-L2, выбранную из SEQ ID NO: 67-69, и CDR-L1, выбранную из SEQ ID NO: 70-72. В некоторых вариантах осуществления, CDR-H3 имеет по меньшей мере около 50%, 75%, 80%, 85%, 90% или 95% идентичности с CDR-H3 SEQ ID NO: 29-35, CDR-H2 имеет по меньшей мере около 50%, 75%, 80%, 85%, 90% или 95% идентичности с CDR-H2 SEQ ID NO: 36-47, CDR-H1 имеет по меньшей мере около 50%, 75%, 80%, 85%, 90% или 95% идентичности с CDR-H1 SEQ ID NO: 48-54 или 58-62, CDR-L3 имеет по меньшей мере около 50%, 75%, 80%, 85%, 90% или 95% идентичности с CDR-L3 SEQ ID NO: 63-66, CDR-L2 имеет по меньшей мере около 50%, 75%, 80%, 85%, 90% или 95% идентичности с CDR-L2 SEQ ID NO: 67-69, CDR-L1 имеет по меньшей мере около 50%, 75%, 80%, 85%, 90% или 95% идентичности с CDR-L1 SEQ ID NO: 70-72. В некоторых вариантах осуществления, CDR-H3 представляет собой CDR-H3, выбранную из SEQ ID NO: 29-35, с вплоть до 1, 2, 3, 4, 5, 6, 7 или 8 аминокислотными заменами; CDR-H2 представляет собой CDR-H2, выбранную из SEQ ID NO: 36-47, с вплоть до 1, 2, 3, 4, 5, 6, 7 или 8 аминокислотными заменами; CDR-H1 представляет собой CDR-H1, выбранную из SEQ ID NO: 48-54 или 58-62, с вплоть до 1, 2, 3, 4 или 5 аминокислотными заменами; CDR-L3 представляет собой CDR-L3, выбранную из SEQ ID NO: 63-66, с вплоть до 1, 2, 3, 4 или 5 аминокислотными заменами; CDR-L2 представляет собой CDR-L2, выбранную из SEQ ID NO: 67-69, с вплоть до 1, 2, 3 или 4 аминокислотными заменами; CDR-L1 представляет собой CDR-L1, выбранную из SEQ ID NO: 70-72, с вплоть до 1, 2, 3, 4, 5 или 6 аминокислотными заменами. В некоторых аспектах, аминокислотные замены представляют собой консервативные аминокислотные замены. В некоторых вариантах осуществления, АВР, описанные в этом параграфе, упоминаются в данном документе как «варианты». В некоторых вариантах осуществления, такие варианты получают из последовательности, предложенной в данном документе, например, аффинным созреванием, сайт-направленным мутагенезом, случайным мутагенезом или любым другим способом, известным в данной области техники или описанным в данном документе. В некоторых вариантах осуществления, такие варианты не получены из последовательности, предложенной в данном документе, и могут, например, быть выделены de novo в соответствии с предложенными в данном документе способами для получения АВР.
[0210] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-H3 SEQ ID NO: 29, CDR-H2 SEQ ID NO: 36, CDR-H1 SEQ ID NO: 48, CDR-L3 SEQ ID NO: 63, CDR-L2 SEQ ID NO: 67 и CDR-L1 SEQ ID NO: 70.
[0211] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-H3 SEQ ID NO: 29, CDR-H2 SEQ ID NO: 37, CDR-H1 SEQ ID NO: 49, CDR-L3 SEQ ID NO: 63, CDR-L2 SEQ ID NO: 67 и CDR-L1 SEQ ID NO: 70.
[0212] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-H3 SEQ ID NO: 29, CDR-H2 SEQ ID NO: 37, CDR-H1 SEQ ID NO: 50, CDR-L3 SEQ ID NO: 63, CDR-L2 SEQ ID NO: 67 и CDR-L1 SEQ ID NO: 70.
[0213] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-H3 SEQ ID NO: 30, CDR-H2 SEQ ID NO: 37, CDR-H1 SEQ ID NO: 50, CDR-L3 SEQ ID NO: 63, CDR-L2 SEQ ID NO: 67 и CDR-L1 SEQ ID NO: 70.
[0214] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-H3 SEQ ID NO: 29, CDR-H2 SEQ ID NO: 38, CDR-H1 SEQ ID NO: 50, CDR-L3 SEQ ID NO: 63, CDR-L2 SEQ ID NO: 67 и CDR-L1 SEQ ID NO: 70.
[0215] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-H3 SEQ ID NO: 31, CDR-H2 SEQ ID NO: 39, CDR-H1 SEQ ID NO: 51, CDR-L3 SEQ ID NO: 64, CDR-L2 SEQ ID NO: 68 и CDR-L1 SEQ ID NO: 71.
[0216] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-H3 SEQ ID NO: 31, CDR-H2 SEQ ID NO: 40, CDR-H1 SEQ ID NO: 52, CDR-L3 SEQ ID NO: 64, CDR-L2 SEQ ID NO: 68 и CDR-L1 SEQ ID NO: 71.
[0217] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-H3 SEQ ID NO: 31, CDR-H2 SEQ ID NO: 41, CDR-H1 SEQ ID NO: 53, CDR-L3 SEQ ID NO: 64, CDR-L2 SEQ ID NO: 68 и CDR-L1 SEQ ID NO: 71.
[0218] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-H3 SEQ ID NO: 31, CDR-H2 SEQ ID NO: 40, CDR-H1 SEQ ID NO: 54, CDR-L3 SEQ ID NO: 64, CDR-L2 SEQ ID NO: 68 и CDR-L1 SEQ ID NO: 71.
[0219] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-H3 SEQ ID NO: 32, CDR-H2 SEQ ID NO: 40, CDR-H1 SEQ ID NO: 54, CDR-L3 SEQ ID NO: 64, CDR-L2 SEQ ID NO: 68 и CDR-L1 SEQ ID NO: 71.
[0220] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-H3 SEQ ID NO: 32, CDR-H2 SEQ ID NO: 40, CDR-H1 SEQ ID NO: 54, CDR-L3 SEQ ID NO: 64, CDR-L2 SEQ ID NO: 68 и CDR-L1 SEQ ID NO: 71.
[0221] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-H3 SEQ ID NO: 32, CDR-H2 SEQ ID NO: 40, CDR-H1 SEQ ID NO: 54, CDR-L3 SEQ ID NO: 64, CDR-L2 SEQ ID NO: 68 и CDR-L1 SEQ ID NO: 71.
[0222] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-H3 SEQ ID NO: 33, CDR-H2 SEQ ID NO: 42, CDR-H1 SEQ ID NO: 58, CDR-L3 SEQ ID NO: 65, CDR-L2 SEQ ID NO: 69 и CDR-L1 SEQ ID NO: 72.
[0223] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-H3 SEQ ID NO: 33, CDR-H2 SEQ ID NO: 42, CDR-H1 SEQ ID NO: 59, CDR-L3 SEQ ID NO: 65, CDR-L2 SEQ ID NO: 69 и CDR-L1 SEQ ID NO:72.
[0224] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-H3 SEQ ID NO: 33, CDR-H2 SEQ ID NO:43, CDR-H1 SEQ ID NO: 60, CDR-L3 SEQ ID NO: 65, CDR-L2 SEQ ID NO: 69 и CDR-L1 SEQ ID NO: 72.
[0225] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-H3 SEQ ID NO: 34, CDR-H2 SEQ ID NO: 43, CDR-H1 SEQ ID NO: 60, CDR-L3 SEQ ID NO: 65, CDR-L2 SEQ ID NO: 69 и CDR-L1 SEQ ID NO: 72.
[0226] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-H3 SEQ ID NO: 34, CDR-H2 SEQ ID NO: 44, CDR-H1 SEQ ID NO: 61, CDR-L3 SEQ ID NO: 65, CDR-L2 SEQ ID NO: 69 и CDR-L1 SEQ ID NO: 72.
[0227] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-H3 SEQ ID NO: 33, CDR-H2 SEQ ID NO: 44, CDR-H1 SEQ ID NO: 59, CDR-L3 SEQ ID NO: 65, CDR-L2 SEQ ID NO: 69 и CDR-L1 SEQ ID NO: 72.
[0228] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-H3 SEQ ID NO: 35, CDR-H2 SEQ ID NO: 45, CDR-H1 SEQ ID NO: 62, CDR-L3 SEQ ID NO: 66, CDR-L2 SEQ ID NO: 69 и CDR-L1 SEQ ID NO: 72.
[0229] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-H3 SEQ ID NO: 35, CDR-H2 SEQ ID NO: 46, CDR-H1 SEQ ID NO: 62, CDR-L3 SEQ ID NO: 66, CDR-L2 SEQ ID NO: 69 и CDR-L1 SEQ ID NO: 72.
[0230] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит CDR-H3 SEQ ID NO: 35, CDR-H2 SEQ ID NO: 47, CDR-H1 SEQ ID NO: 62, CDR-L3 SEQ ID NO: 66, CDR-L2 SEQ ID NO: 69 и CDR-L1 SEQ ID NO: 72.
2.2.5. Тяжелые цепи и легкие цепи
[0231] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит VH, выбранную из VH SEQ ID NO: 4-24 (или варианта, описанного в данном документе), и константную область, выбранную из SEQ ID NO: 55-57 или 125. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит VL, выбранную из VL SEQ ID NO: 25-28 (или варианта, описанного в данном документе), и константную область SEQ ID NO: 126.
[0232] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 79. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 80. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит легкую цепь SEQ ID NO: 81. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 79 и легкую цепь SEQ ID NO: 81. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 80 и легкую цепь SEQ ID NO: 81.
[0233] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 82. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 83. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 82 и легкую цепь SEQ ID NO: 81. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 83 и легкую цепь SEQ ID NO: 81.
[0234] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 84. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 85. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 84 и легкую цепь SEQ ID NO: 81. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 85 и легкую цепь SEQ ID NO: 81.
[0235] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 86. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 87. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 86 и легкую цепь SEQ ID NO: 81. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 87 и легкую цепь SEQ ID NO: 81.
[0236] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 88. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 89. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 88 и легкую цепь SEQ ID NO: 81. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 89 и легкую цепь SEQ ID NO: 81.
[0237] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 90. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 91. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит легкую цепь SEQ ID NO: 92. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 90 и легкую цепь SEQ ID NO: 92. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 91 и легкую цепь SEQ ID NO: 92.
[0238] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 93. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 94. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 93 и легкую цепь SEQ ID NO: 92. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 94 и легкую цепь SEQ ID NO: 92.
[0239] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 95. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 96. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 95 и легкую цепь SEQ ID NO: 92. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 96 и легкую цепь SEQ ID NO: 92.
[0240] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 97. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 98. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 97 и легкую цепь SEQ ID NO: 92. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 98 и легкую цепь SEQ ID NO: 92.
[0241] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 99. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 100. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 99 и легкую цепь SEQ ID NO: 92. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 100 и легкую цепь SEQ ID NO: 92.
[0242] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 101. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 102. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 101 и легкую цепь SEQ ID NO: 92. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 102 и легкую цепь SEQ ID NO: 92.
[0243] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 103. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 104. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 103 и легкую цепь SEQ ID NO: 92. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 104 и легкую цепь SEQ ID NO: 92.
[0244] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 105. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 106. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит легкую цепь SEQ ID NO: 107. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 105 и легкую цепь SEQ ID NO: 107. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 106 и легкую цепь SEQ ID NO: 107.
[0245] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 108. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 109. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 108 и легкую цепь SEQ ID NO:107. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 109 и легкую цепь SEQ ID NO: 107.
[0246] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 110. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 111. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 110 и легкую цепь SEQ ID NO: 107. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 111 и легкую цепь SEQ ID NO: 107.
[0247] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 112. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 113. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 112 и легкую цепь SEQ ID NO: 107. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 113 и легкую цепь SEQ ID NO: 107.
[0248] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 114. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 115. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 114 и легкую цепь SEQ ID NO: 107. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 115 и легкую цепь SEQ ID NO: 107.
[0249] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 116. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 117. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 116 и легкую цепь SEQ ID NO: 107. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 117 и легкую цепь SEQ ID NO: 107.
[0250] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 118. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 119. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит легкую цепь SEQ ID NO: 120. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 118 и легкую цепь SEQ ID NO: 120. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 119 и легкую цепь SEQ ID NO: 120.
[0251] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 121. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 122. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 121 и легкую цепь SEQ ID NO: 120. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 122 и легкую цепь SEQ ID NO: 120.
[0252] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 123. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 124. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 123 и легкую цепь SEQ ID NO: 120. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит тяжелую цепь SEQ ID NO: 124 и легкую цепь SEQ ID NO: 120.
2.2.6. Консенсусные последовательности
[0253] В некоторых вариантах осуществления, в данном документе предложено первое семейство АВР, причем АВР такого семейства содержит следующие шесть последовательностей CDR: а) CDR-H3, имеющую последовательность A-R-D-G-V-L-X1-L-N-K-R-S-F-D-I, в которой X1 представляет собой А или Т (SEQ ID NO: 128); b) CDR-H2, имеющую последовательность S-I-Y-Y-S-G-X2-T-Y-Y-N-P-S-L-K-S, в которой Х2 представляет собой S, Q или G (SEQ ID NO: 129); с) CDR-H1, имеющую последовательность G-S-I-X3-S-G-X4-Y-Y-W-G, в которой Х3 представляет собой Е или А, и Х4 представляет собой L, V или S (SEQ ID NO: 130); d) CDR-L3, имеющую последовательность QQHTVRPPLT (SEQ ID NO: 64); e) CDR-L2, имеющую последовательность GASSRAT (SEQ ID NO: 68); и f) CDR-L1, имеющую последовательность RASQSVSSSYLA (SEQ ID NO: 71). В некоторых вариантах осуществления, в данном документе предложен АВР такого первого семейства.
[0254] В некоторых вариантах осуществления, в данном документе предложено второе семейство АВР, причем АВР такого семейства содержит следующие шесть последовательностей CDR: а) CDR-H3, имеющую последовательность A-R-D-A-N-Y-Y-G-X1-A-W-A-F-D-P, в которой X1 представляет собой S или G (SEQ ID NO: 131); b) CDR-H2, имеющую последовательность S-I-Y-Y-S-G-X2-T-F-Y-N-P-S-L-K-X3, в которой Х2 представляет собой S или А, и Х3 представляет собой S или G (SEQ ID NO: 132); с) CDR-Н1, имеющую последовательность G-S-I-X4-S-X5-X6-X7-Y-W-G, в которой Х4 представляет собой S или Т, Х5 представляет собой S или Т, Х6 представляет собой S или K, и X7 представляет собой Н или Y (SEQ ID NO: 133); d) CDR-L3, имеющую последовательность QQHFNLPT (SEQ ID NO: 63); е) CDR-L2, имеющую последовательность DASNRAT (SEQ ID NO: 67); и f) CDR-L1, имеющую последовательность RASQSVSSYLA (SEQ ID NO: 70). В некоторых вариантах осуществления, в данном документе предложен АВР такого второго семейства.
[0255] В некоторых вариантах осуществления, в данном документе предложено третье семейство АВР, причем АВР такого семейства содержит следующие шесть последовательностей CDR: а) CDR-H3, имеющую последовательность A-R-G-G-R-T-T-W-I-G-A-X1-D-I, в которой X1 представляет собой F или L (SEQ ID NO: 134); b) CDR-H2, имеющую последовательность I-I-N-P-S-X2-G-L-T-S-Y-A-X3-K-F-Q-G, в которой Х2 представляет собой L или I, и Х3 представляет собой Q или R (SEQ ID NO: 135); с) CDR-Н1, имеющую последовательность Y-T-F-X4-X5-Y-Y-X6-H, в которой X4 представляет собой G, Р или R, и X5 представляет собой N, А или Е, и Х6 представляет собой М или I (SEQ ID NO: 136); d) CDR-L3, имеющую последовательность QQYVVWPPLT (SEQ ID NO: 65); e) CDR-L2, имеющую последовательность GASTRAT (SEQ ID NO: 69); и f) CDR-L1, имеющую последовательность RASQSVSSNLA (SEQ ID NO: 72). В некоторых вариантах осуществления, в данном документе предложен АВР такого третьего семейства.
[0256] В некоторых вариантах осуществления, в данном документе предложено четвертое семейство АВР, причем АВР такого семейства содержит следующие шесть последовательностей CDR: а) CDR-H3, имеющую последовательность ARLHVSGSYYPAYLDY (SEQ ID NO: 35); b) CDR-H2, имеющую последовательность X1-I-N-P-S-M-G-A-T-S-Y-X2-Q-K-F-X3-G, в которой X1 представляет собой V или I, X2 представляет собой А или Т, и Х3 представляет собой Q или R (SEQ ID NO: 137); с) CDR-Н1 имеющую последовательность YTFTSHYMG (SEQ ID NO: 62); d) CDR-L3 имеющую последовательность QQYIVFPWT (SEQ ID NO: 66); e) CDR-L2 имеющую последовательность GASTRAT (SEQ ID NO: 69); и f) CDR-L1 имеющую последовательность RASQSVSSNLA, (SEQ ID NO: 72). В некоторых вариантах осуществления, в данном документе предложен АВР такого четвертого семейства.
2.2.7. Функциональные свойства вариантов АВР
[0257] Как описано выше, и в других местах данного раскрытия изобретения, варианты АВР, предложенные в данном документе, определенны на основе процента идентичности с иллюстративной последовательностью АВР, предложенной в данном документе, или замены аминокислотных остатков по сравнению с иллюстративной последовательностью АВР, предложенной в данном документе.
[0258] В некоторых вариантах осуществления, вариант АВР, предложенный в данном документе, имеет специфичность к hTIGIT. В некоторых вариантах осуществления, вариант АВР, предложенный в данном документе, имеет специфичность к cTIGIT. В некоторых вариантах осуществления, вариант АВР, предложенный в данном документе, имеет специфичность к mTIGIT. В некоторых вариантах осуществления, вариант АВР, предложенный в данном документе, имеет специфичность к hTIGIT и cTIGIT. В некоторых вариантах осуществления, вариант АВР, предложенный в данном документе, имеет специфичность к hTIGIT и mTIGIT. В некоторых вариантах осуществления, вариант АВР, предложенный в данном документе, имеет специфичность к cTIGIT и mTIGIT. В некоторых вариантах осуществления, вариант АВР, предложенный в данном документе, имеет специфичность к hTIGIT, cTIGIT и mTIGIT.
[0259] В некоторых вариантах осуществления, вариант АВР, который получен из иллюстративной последовательности АВР, предложенной в данном документе, сохраняет аффинность, как измерено по KD, к hTIGIT, которая находится в пределах примерно 1,5-кратной, примерно 2-кратной, примерно 3-кратной, примерно 4-кратной, примерно 5 кратной, примерно 6-кратной, примерно 7-кратной, примерно 8-кратной, примерно 9-кратной или примерно 10-кратной аффиности такого иллюстративного АВР. В некоторых вариантах осуществления, вариант АВР, который получен из иллюстративной последовательности АВР, предложенной в данном документе, сохраняет аффинность, как измерено по KD, к cTIGIT, которая находится в пределах примерно 1,5-кратной, примерно 2-кратной, примерно 3-кратной, примерно 4-кратной, примерно 5-кратной, примерно 6-кратной, примерно 7-кратной, примерно 8-кратной, примерно 9-кратной или примерно 10-кратной аффиности такого иллюстративного АВР. В некоторых вариантах осуществления, вариант АВР, который получен из иллюстративной последовательности АВР, предложенной в данном документе, сохраняет аффинность, как измерено по KD, к mTIGIT, которая находится в пределах примерно 1,5-кратной, примерно 2-кратной, примерно 3-кратной, примерно 4-кратной, примерно 5-кратной, примерно 6-кратной, примерно 7-кратной, примерно 8-кратной, примерно 9-кратной или примерно 10-кратной аффиности такого иллюстративного АВР. В некоторых вариантах осуществления, вариант АВР, который получен из иллюстративной последовательности АВР, предложенной в данном документе, сохраняет аффинность, как измерено по KD, как к hTIGIT так и к cTIGIT, которая находится в пределах примерно 1,5-кратной, примерно 2-кратной, примерно 3-кратной, примерно 4-кратной, примерно 5-кратной, примерно 6-кратной, примерно 7-кратной, примерно 8-кратной, примерно 9-кратной или примерно 10-кратной аффиности такого иллюстративного АВР. В некоторых вариантах осуществления, вариант АВР, который получен из иллюстративной последовательности АВР, предложенной в данном документе, сохраняет аффинность, как измерено по KD, как к hTIGIT так и к mTIGIT, которая находится в пределах примерно 1,5-кратной, примерно 2-кратной, примерно 3-кратной, примерно 4-кратной, примерно 5-кратной, примерно 6-кратной, примерно 7-кратной, примерно 8-кратной, примерно 9-кратной или примерно 10-кратной аффиности такого иллюстративного АВР. В некоторых вариантах осуществления, вариант АВР, который получен из иллюстративной последовательности АВР, предложенной в данном документе, сохраняет аффинность, как измерено по KD, как к cTIGIT так и к mTIGIT, которая находится в пределах примерно 1,5-кратной, примерно 2-кратной, примерно 3-кратной, примерно 4-кратной, примерно 5-кратной, примерно 6-кратной, примерно 7-кратной, примерно 8-кратной, примерно 9-кратной или примерно 10-кратной аффиности такого иллюстративного АВР. В некоторых вариантах осуществления, вариант АВР, который получен из иллюстративной последовательности АВР, предложенной в данном документе, сохраняет аффинность, как измерено по KD, к всем трем hTIGIT, cTIGIT и mTIGIT, которая находится в пределах примерно 1,5-кратной, примерно 2-кратной, примерно 3-кратной, примерно 4-кратной, примерно 5-кратной, примерно 6-кратной, примерно 7-кратной, примерно 8-кратной, примерно 9-кратной или примерно 10-кратной аффиности такого иллюстративного АВР.
[0260] В некоторых вариантах осуществления, вариант АВР, предложенный в данном документе, сохраняет способность антагонизировать TIGIT, как измерено одним или больше анализами или биологическими эффектами, описанными в данном документе. В некоторых вариантах осуществления, вариант АВР, предложенный в данном документе, сохраняет способность предотвращать взаимодействие TIGIT с одним или большим количеством его лигандов, как описано в данном документе.
[0261] В некоторых вариантах осуществления, вариант АВР, предложенный в данном документе, конкурирует за связывание с TIGIT с антителом, выбранным из МАБ1, МАБ2, МАБ3, МАБ4, МАБ5, МАБ6, МАБ7, МАБ8, МАБ9, МАБ10, МАБ11, МАБ12, МАБ13, МАБ14, МАБ15, МАБ16, МАБ17, МАБ18, МАБ19, МАБ20 или МАБ21, каждое из которых представлено в Таблице 5 данного раскрытия изобретения.
[0262] В некоторых вариантах осуществления, вариант АВР, предложенный в данном документе, ингибирует связывание CD155 с TIGIT. В некоторых вариантах осуществления, вариант АВР, предложенный в данном документе, ингибирует связывание CD112 с TIGIT. В некоторых вариантах осуществления, вариант АВР, предложенный в данном документе, ингибирует связывание CD226 с TIGIT.
[0263] В некоторых вариантах осуществления, вариант АВР, предложенный в данном документе, активирует эффекторный Т-лимфоцит или клетку естественный киллер (NK). В некоторых вариантах осуществления, вариант АВР, предложенный в данном документе, уменьшает количество регуляторных Т-лимфоцитов в ткани или в кровеносной системе. В некоторых вариантах осуществления, вариант АВР, предложенный в данном документе, ингибирует подавление эффекторного Т-лимфоцита регуляторным Т-лимфоцитом.
[0264] В некоторых вариантах осуществления, вариант АВР, предложенный в данном документе, не связывается специфически с любыми из PVRL1, PVRL2, PVRL3 или PVRL4.
[0265] В некоторых вариантах осуществления, вариант АВР, предложенный в данном документе, связывает TIGIT мыши (SEQ ID NO: 3) с аффинностью ниже (как указано более высоким KD), чем аффинность варианта АВР к hTIGIT, или не связывает mTIGIT. В некоторых вариантах осуществления, вариант АВР, предложенный в данном документе, связывает TIGIT мыши (SEQ ID NO: 138) с аффинностью ниже (как указано более высоким KD), чем аффинность варианта АВР к hTIGIT, или не связывает mTIGIT.
[0266] В некоторых вариантах осуществления, вариант АВР, предложенный в данном документе, связывает один и тот же эпитоп TIGIT в качестве такого АВР.
2.2.8. Другие функциональные свойства АВР
[0267] В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет одно или большее количество свойств, перечисленных в следующих a)-j): а) конкурирует за связывание с TIGIT с антителом, выбранным из МАБ1, МАБ2, МАБ3, МАБ4, МАБ5, МАБ6, МАБ7, МАБ8, МАБ9, МАБ10, МАБ11, МАБ12, МАБ13, МАБ14, МАБ15, МАБ16, МАБ17, МАБ18, МАБ19, МАБ20 или МАБ21, каждое из которых представлено в Таблице 5 данного раскрытия изобретения; b) ингибирует связывание CD 155 с TIGIT; с) ингибирует связывание CD112 с TIGIT; d) ингибирует ассоциацию CD226 с TIGIT; е) активирует эффекторный Т-лимфоцит или естественный киллер (NK); f) уменьшает количество регуляторных Т-лимфоцитов в ткани или в кровеносной системе; g) ингибирует подавление эффекторного Т-лимфоцита регуляторным Т-лимфоцитом; h) не связывается специфически с любыми из PVRL1, PVRL2, PVRL3 или PVRL4; i) специфически связывает TIGIT яванского макака (cTIGIT; SEQ ID NO: 2); или j) связывает TIGIT мыши (mTIGIT; SEQ ID NO: 3) с аффинностью ниже (как указано более высоким KD), чем аффинность АВР к hTIGIT, или не связывает mTIGIT. В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет два или больше свойств, перечисленных в вышеуказанных a)-j). В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет три или больше свойств, перечисленных в вышеуказанных a)-j). В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет четыре или больше свойств, перечисленных в вышеуказанных а)-j). В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет пять или больше свойств, перечисленных в вышеуказанных a)-j). В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет шесть или больше свойств, перечисленных в вышеуказанных a)-j). В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет семь или больше свойств, перечисленных в вышеуказанных a)-j). В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет восемь или больше свойств, перечисленных в вышеуказанных а)-j). В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет девять или больше свойств, перечисленных в вышеуказанных a)-j). В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет десять или больше свойств, перечисленных в вышеуказанных a)-j).
[0268] В некоторых вариантах осуществления, АВР, предложенный в данном документе, проявляет комбинацию свойств, перечисленных в следующих a)-j): а) конкурирует за связывание с TIGIT с антителом, выбранным из МАБ1, МАБ2, МАБ3, МАБ4, МАБ5, МАБ6, МАБ7, МАБ8, МАБ9, МАБ10, МАБ11, МАБ12, МАБ13, МАБ14, МАБ15, МАБ16, МАБ17, МАБ18, МАБ19, МАБ20 или МАБ21, каждое из которых представлено в Таблице 5 данного раскрытия изобретения; b) ингибирует связывание CD155 с TIGIT; с) ингибирует связывание CD112 с TIGIT; d) ингибирует ассоциацию CD226 с TIGIT; е) активирует эффекторный Т-лимфоцит или естественный киллер (NK); f) уменьшает количество регуляторных Т-лимфоцитов в ткани или в кровеносной системе; g) ингибирует подавление эффекторного Т-лимфоцита регуляторным Т-лимфоцитом; h) не связывается специфически с любыми из PVRL1, PVRL2, PVRL3 или PVRL4; i) специфически связывает TIGIT яванского макака (cTIGIT; SEQ ID NO: 2); или j) связывает TIGIT мыши (mTIGIT; SEQ ID NO: 3) с аффинностью ниже (как указано более высоким KD), чем аффинность АВР к hTIGIT, или не связывает mTIGIT. В некоторых вариантах осуществления, такой АВР проявляет комбинацию свойств, выбранных из (а и b), (а и с), (а и d), (а и е), (а и f), (а и g), (а и h), (а и i), (а и j), (b и а), (b и с), (b и d), (b и е), (b и f), (b и g), (b и h), (b и i), (b и j), (с и а), (с и b), (с и d), (с и е), (с и f), (с и g), (с и h), (с и i), (с и j), (d и a), (d и b), (d и с), (d и е), (d и f), (d и g), (d и h), (d и i), (d и j), (e и a), (e и b), (e и с), (e и d), (e и f), (e и g), (e и h), (e и i), (e и j), (f и a), (f и b), (f и с), (f и d), (f и e), (f и g), (f и h), (f и i), (f и j), (g и a), (g и b), (g и с), (g и d), (g и e), (g и f), (g и h), (g и i), (g и j), (h и a), (h и b), (h и с), (h и d), (h и e), (h и f), (h и g), (h и i), (h и j), (i и a), (i и b), (i и с), (i и d), (i и e), (i и f), (i и g), (i и h), (i и j), (j и a), (j и b), (j и с), (j и d), (j и e), (j и f), (j и g), (j и h) и (j и i). В некоторых вариантах осуществления, такой АВР проявляет комбинацию свойств, выбранных из (а и b и с), (а и b и d), (а и b и е), (а и b и f), (а и b и g), (a, b и h), (а и b и i), (а и b и j), (а, с и b), (а и с и d), (а и с и е), (а и с и f), (а и с и g), (а, с и h), (а и с и i), (а и с и j), (a, d и b), (а и d и с), (а и d и е), (a, d и f), (а и d и g), (a, d и h), (а и d и i), (а и d и j), (а и е и b), (а и е и с), (а и е и d), (а и е и f), (а и е и g), (а и е и h), (а и е и i), (а и е и j), (а и f и b), (а и f и с), (а и f и d), (а и f и е), (а и f и g), (а и f и h), (а и f и i), (а и f и j), (а и g и b), (а и g и с), (а и g и d), (а и g и е), (а и g и f), (а и g и h), (а и g и i), (а и g и j), (а и h и b), (а и h и с), (а и h и d), (а и h и е), (а и h и f), (а и h и g), (а и h и i), (а и h и j), (а и i и b), (а и i и с), (а и i и d), (а и i и е), (а и i и f), (а и i и g), (а и i и h), (а и i и j), (а и j и b), (а и j и с), (а и j и d), (а и j и е), (а и j и f), (а и j и g), (а и j и h), (а и j и i), (b и а и j), (b и а и с), (b и а и d), (b и а и е), (b и а и f), (b, а и g), (b и а и h), (b и а и i), (b и с и j), (b и с и а), (b и с и d), (b и с и е), (b и с и f), (b и с и g), (b и с и h), (b и с и i), (b и d и j), (b и d и а), (b и d и с), (b и d и е), (b и d и f), (b и d и g), (b и d и h), (b и d и i), (b и е и j), (b и е и а), (b и е и с), (b, е и d), (b и е и f), (b и е и g), (b и е и h), (b и е и i), (b и f и j), (b и f и a), (b и f и с), (b и f и d), (b и f и е), (b и f и g), (b и f и h), (b и f и i), (b и g и j), (b и g и a), (b и g и с), (b и g и d), (b и g и e), (b и g и f), (b и g и h), (b и g и i), (b и h и j), (b и h и a), (b и h и с), (b и h и d), (b и h и e), (b и h и f), (b и h и g), (b и h и i), (b и i и j), (b и i и a), (b и i и с), (b и i и d), (b и i и e), (b и i и f), (b и i и g), (b и i и h), (b и j и i), (b и j и a), (b и j и с), (b и j и d), (b и j и e), (b и j и f), (b и j и g), (b и j и h), (с и а и i), (с и а и j), (с и а и b), (с и а и d), (с и а и е), (с и а и f), (с и а и g), (с и а и h), (с и b и i), (с и b и j), (с и b и а), (с и b и d), (с и b и е), (с и b и f), (с и b и g), (с и b и h), (с и d и i), (с и d и j), (с и d и а), (с и d и b), (с и d и е), (с и d и f), (с и d и g), (с и d и h), (с и е и i), (с и е и j), (с и е и а), (с и е и b), (с и е и d), (с и е и f), (с и е и g), (с и е и h), (с и f и i), (с и f и j), (с и f и а), (с и f и b), (с и f и d), (с и f и е), (с и f и g), (с и f и h), (с и g и i), (с и g и j), (с и g и а), (с и g и b), (с и g и d), (с и g и е), (с и g и f), (с и g и h), (с и h и i), (с и h и j), (с и h и а), (с и h и b), (с и h и d), (с и h и е), (с и h и f), (с и h и g), (с и i и h), (с и i и j), (с и i и а), (с и i и b), (с и i и d), (с и i и е), (с и i и f), (с и i и g), (с и j и h), (с и j и i), (с и j и а), (с и j и b), (с и j и d), (с и j и е), (с и j и f), (с и j и g), (d и а и h), (d и а и i), (d и а и j), (d и а и b), (d и а и с), (d и а и е), (d и а и f), (d и а и g), (d и b и h), (d и b и i), (d и b и j), (d и b и a), (d и b и с), (d и b и e), (d и b и f), (d и b и g), (d и с и h), (d и с и i), (d и с и j), (d и с и a), (d и с и b), (d и с и е), (d и с и f), (d и с и g), (d и е и h), (d и е и i), (d и е и j), (d и е и a), (d и е и b), (d и е и с), (d и е и f), (d и е и g), (d и f и h), (d и f и i), (d и f и j), (d и f и a), (d и f и b), (d и f и с), (d и f и e), (d и g и g), (d и g и h), (d и g и i), (d и g и j), (d и g и a), (d и g и b), (d и g и с), (d и g и e), (d и g и f), (d и h и g), (d и h и i), (d и h и j), (d и h и a), (d и h и b), (d и h и с), (d и h и e), (d и h и f), (d и i и g), (d и i и h), (d и i и j), (d и i и a), (d и i и b), (d и i и с), (d и i и e), (d и i и f), (d и j и g), (d и j и h), (d и j и i), (d и j и a), (d и j и b), (d и j и с), (d и j и e), (d и j и f), (e и а и g), (e и а и h), (e и а и i), (e и а и j), (e и а и b), (e и а и с), (e и а и d), (e и а и f), (e и b и g), (e и b и h), (e и b и i), (e и b и j), (e и b и a), (e и b и с), (e и b и d), (e и b и f), (e и с и g), (e и с и h), (е и с и i), (е и с и j), (е и с и а), (е и с и b), (е и с и d), (е и с и f), (е и d и g), (е и d и h), (е и d и i), (е и d и j), (е и d и а), (е и d и b), (е и d и с), (е и d и f) (е и f и g), (е и f и h), (е и f и i), (е и f и j), (е и f и а), (е и f и b), (е и f и с), (е и f и d), (е и g и f), (е и g и h), (е и g и i), (е и g и j), (е и g и а), (е и g и b), (е и g и с), (е, g и d), (е и h и f), (е и h и g), (е и h и i), (е и h и j), (е и h и а), (е и h и b), (е и h и с), (е и h и d), (е и i и f), (е и i и g), (е и i и h), (е и i и j), (е и i и а), (е и i и b), (е и i и с), (е и i и d), (е и j и f), (е и j и g), (е и j и h), (е и j и i), (е и j и а), (е и j и b), (е и j и с), (е и j и d), (f и а и е), (f и а и g), (f и а и h), (f и а и i), (f и а и j), (f и а и b), (f и а и с), (f и а и d), (f и b и е), (f и b и g), (f и b и h), (f и b и i), (f и b и j), (f и b и a), (f и b и с), (f и b и d), (f и с и e), (f и с и g), (f и с и h), (f и с и i), (f и с и j), (f и с и a), (f и с и b), (f и с и d), (f и d и е), (f и d и g), (f и d и h), (f и d и i), (f и d и j), (f и d и a), (f и d и b), (f и d и с), (f и e и d), (f и e и g), (f и e и h), (f и e и i), (f и e и j), (f и e и a), (f и e и b), (f и e и с), (f и g и d), (f и g и e), (f и g и h), (f и g и i), (f и g и j), (f и g и a), (f и g и b), (f и g и с), (f и h и d), (f и h и e), (f и h и g), (f и h и i), (f и h и j), (f и h и a), (f и h и b), (f и h и с), (f и i и d), (f и i и e), (f и i и g), (f и i и h), (f и i и j), (f и i и a), (f и i и b), (f и i и с), (f и j и d), (f и j и e), (f и j и g), (f и j и h), (f и j и i), (f и j и a), (f и j и b), (f и j (g и а и d), (g и а и e), (g и а и f), (g и а и h), (g и а и i), (g и а и j), (g и а и b), (g и а и с), (g и b и d), (g и b и е), (g и b и f), (g и b и h), (g и b и i), (g и b и j), (g и b и a), (g и b и с), (g и с и d), (g и с и е), (g и с и f), (g и с и h), (g и с и i), (g и с и j), (g и с и a), (g и с и b), (g и d и с), (g и d и е), (g и d и f), (g и d и h), (g и d и i), (g и d и j), (g и d и a), (g и d и b), (g и e и с), (g и e и d), (g и e и f), (g и e и h), (g и e и i), (g и e и j), (g и e и a), (g и e и b), (g и f и с), (g и f и d), (g и f и e), (g и f и h), (g и f и i), (g и f и j), (g и f и a), (g и f и b), (g и h и с), (g и h и d), (g и h и e), (g и h и f), (g и h и i), (g и h и j), (g и h и a), (g и h и b), (g и i и с), (g и i и d), (g и i и e), (g и i и f), (g и i и h), (g и i и j), (g и i и a), (g и j и b), (g и j и с), (g и j и d), (g и j и e), (g и j и f), (g и j и h), (g и j и i), (g и j и a), (g и j и b), (h и а и с), (h и а и d), (h и а и e), (h и а и f), (h и а и g), (h и а и i), (h и а и j), (h, а и b), (h и b и с), (h и b и d), (h и b и e), (h и b и f), (h и b и g), (h и b и i), (h и b и j), (h и b и a), (h и с и b), (h и с и d), (h и с и е), (h и с и f), (h и с и g), (h и с и i), (h и с и j), (h и с и a), (h и d и b), (h и d и с), (h и d и е), (h и d и f), (h и d и g), (h и d и i), (h и d и j), (h и d и a), (h и e и b), (h и e и с), (h и e и d), (h и e и f), (h и e и g), (h и e и i), (h и e и j), (h и e и a), (h и f и b), (h и f и с), (h и f и d), (h и f и e), (h и f и g), (h и f и i), (h и f и j), (h и f и a), (h и g и b), (h и g и с), (h и g и d), (h и g и e), (h и g и f), (h и g и i), (h и g и j), (h и g и a), (h и i и b), (h и i и с), (h, i и d), (h и i и e), (h и i и f), (h и i и g), (h и i и j), (h и i и a), (h и j и b), (h и j и с), (h и j и d), (h и j и e), (h и j и f), (h и j и g), (h и j и i), (h и j и a), (i и а и b), (i и а и с), (i и а и d), (i и а и e), (i и а и f), (i и а и g), (i и а и h), (i и а и j), (i и b и a), (i и b и с), (i и b и d), (i и b и e), (i и b и f), (i и b и g), (i и b и h), (i и b и j), (i и с и a), (i и с и b), (i и с и d), (i и с и е), (i и с и f), (i и с и g), (i и с и h), (i и с и j), (i и d и a), (i и d и b), (i и d и с), (i и d и е), (i и d и f), (i и d и g), (i и d и h), (i и d и j), (i и е и a), (i и е и b), (i и е и с), (i и е и d), (i и е и f), (i и е и g), (i и е и h), (i и е и j), (i и f и a), (i и f и b), (i и f и с), (i и f и d), (i и f и е), (i и f и g), (i и f и h), (i и f и j), (i и g и a), (i и g и b), (i и g и с), (i и g и d), (i и g и e), (i и g и f), (i и g и h), (i и g и j), (i и h и a), (i и h и b), (i и h и с), (i и h и d), (i и h и e), (i и h и f), (i и h и g), (i и h и j), (i и j и a), (i и j и b), (i и j и с), (i и j и d), (i и j и e), (i и j и f), (i иj и g), (i и j и h), (j и а и i), (j, а и b), (j и а и с), (j и а и d), (j и а и e), (j и a и f), (j и а и g), (j и а и h), (j и b и i), (j и b и a), (j и b и с), (j и b и d), (j и b и e), (j и b и f), (j и b и g), (j и b и h), (j и с и i), (j и с и а), и (j и с и b), (j и с и d), (j и с и е), (j и с и f), (j и с и g), (j и с и h), (j и d и i), (j и d и a), (j и d и b), (j и d и с), (j и d и е), (j и d и f), (j и d и g), (j и d и h), (j и е и i), (j и е и a), (j и е и b), (j и е и с), (j и е и d), (j и е и f), (j и е и g), (j и е и h), (j и f и i), (j и f и a), (j и f и b), (j и f и с), (j и f и d), (j и f и е), (j и f и g), (j и f и h), (j и g и i), (j и g и а), (j и g и b), (j и g и с), (j и g и d), (j и g и е), (j и g и f), (j и g и h), (j и h и i), (j и h и a), (j и h и b), (j и h и с), (j и h и d), (j и h и е), (j и h и f), (j и h и g), (j и i и h), (j и i и a), (j и i и b), (j и i и с), (j и i и d), (j и i и е), (j и i и f) и (j и i и g).
2.3. Зародышевая линия
[0269] Предложенные в данном документе АВР могут содержать любые подходящие последовательности VH и VL зародышевой линии.
[0270] В некоторых вариантах осуществления, область VH АВР, предложенного в данном документе, представляет собой область из зародышевой линии VH4. В некоторых вариантах осуществления, область VH АВР, предложенного в данном документе, представляет собой область из зародышевой линии VH1.
[0271] В некоторых вариантах осуществления, область VH АВР, предложенного в данном документе, представляет собой область из зародышевой линии VH4-39. В некоторых вариантах осуществления, область VH АВР, предложенного в данном документе, представляет собой область из зародышевой линии VH4-31. В некоторых вариантах осуществления, область VH АВР, предложенного в данном документе, представляет собой область из зародышевой линии VH1-46.
[0272] В некоторых вариантах осуществления, область VL АВР, предложенного в данном документе, представляет собой область из зародышевой линии VK3.
[0273] В некоторых вариантах осуществления, область VL АВР, предложенного в данном документе, представляет собой область из зародышевой линии VK3-11. В некоторых вариантах осуществления, область VL АВР, предложенного в данном документе, представляет собой область из зародышевой линии VK3-20. В некоторых вариантах осуществления, область VL АВР, предложенного в данном документе, представляет собой область из зародышевой линии VK3-15.
2.4. Моноспецифические и мультиспецифические белки, связывающие антиген TIGIT
[0274] В некоторых вариантах осуществления, АВР, предложенные в данном документе, представляют собой моноспецифические АВР.
[0275] В некоторых вариантах осуществления, АВР, предложенные в данном документе, представляют собой мультиспецифические АВР.
[0276] В некоторых вариантах осуществления, мультиспецифичный АВР, предложенный в данном документе, связывает больше одного антигена. В некоторых вариантах осуществления, мультиспецифическое антитело связывает 2 антигена. В некоторых вариантах осуществления, мультиспецифическое антитело связывает 3 антигена. В некоторых вариантах осуществления, мультиспецифическое антитело связывает 4 антигена. В некоторых вариантах осуществления, мультиспецифическое антитело связывает 5 антигенов.
[0277] В некоторых вариантах осуществления, мультиспецифическое антитело, предложенное в данном документе, связывает больше одного эпитопа на антигене TIGIT. В некоторых вариантах осуществления, мультиспецифическое антитело связывает 2 эпитопа на антигене TIGIT. В некоторых вариантах осуществления, мультиспецифическое антитело связывает 3 эпитопа на антигене TIGIT.
[0278] Многие мультиспецифические конструкции АВР являются известными в данной области техники, и АВР, предложенные в данном документе, могут быть предоставлены в виде любой подходящей мультиспецифической конструкции.
[0279] В некоторых вариантах осуществления, мультиспецифичный АВР содержит иммуноглобулин, содержащий по меньшей мере две различные вариабельные области тяжелой цепи, каждая в паре с общей вариабельной областью легкой цепи (то есть «общим антителом легкой цепи»). Общая вариабельная область легкой цепи формирует отдельный антиген-связывающий домен с каждой из двух различных вариабельных областей тяжелой цепи. См. Merchant et al., Nature Biotechnol., 1998, 16:677-681, включен посредством ссылки в полном объеме.
[0280] В некоторых вариантах осуществления, мультиспецифичный АВР содержит иммуноглобулин, содержащий антитело или его фрагмент, присоединенный к одному или большему количеству N- или С-концов тяжелых или легких цепей такого иммуноглобулина. См. Coloma и Morrison, Nature Biotechnol., 1997, 15:159-163, включен посредством ссылки в полном объеме. В некоторых аспектах, такой АВР содержит четырехвалентное биспецифическое антитело.
[0281] В некоторых вариантах осуществления, мультиспецифичный АВР содержит гибридный иммуноглобулин, содержащий по меньшей мере две различные вариабельные области тяжелой цепи, и по меньшей мере две различные вариабельные области легкой цепи. См. Milstein and Cuello, Nature, 1983, 305:537-540; и Staerz and Bevan, Proc. Natl. Acad. Sci. USA, 1986, 83:1453-1457; каждый из которых включен посредством ссылки в полном объеме.
[0282] В некоторых вариантах осуществления, мультиспецифичный АВР содержит иммуноглобулиновые цепи с изменениями для уменьшения формирования побочных продуктов, которые не обладают мультиспецифичностью. В некоторых аспектах, АВР содержат одну или больше модификаций «выступы-во-впадину», как описано в патенте США №5731168, включен посредством ссылки в полном объеме.
[0283] В некоторых вариантах осуществления, мультиспецифичный АВР содержит иммуноглобулиновые цепи с одной или больше электростатическими модификациями для содействия сборке гетеро-мультимеров Fc. См. WO 2009/089004, включен посредством ссылки в полном объеме.
[0284] В некоторых вариантах осуществления, мультиспецифичный АВР содержит биспецифическую одноцепочечную молекулу. См. Traunecker et al., EMBOJ., 1991, 10:3655-3659; и Gruber et al., J. Immunol., 1994, 152:5368-5374; каждый из которых включен посредством ссылки в полном объеме.
[0285] В некоторых вариантах осуществления, мультиспецифичный АВР содержит вариабельный домен тяжелой цепи и вариабельный домен легкой цепи, соединенные полипептидным линкером, где длина линкера выбрана так, что способствует сборке мультиспецифических АВР с желаемой мультиспецифичностью. Например, моноспецифические scFvs в целом, как правило, формируются, когда вариабельный домен тяжелой цепи и вариабельный домен легкой цепи соединяют полипептидным линкером из более чем 12 аминокислотных остатков. См. патент США №4946778 и 5132405, каждый из которых включен посредством ссылки в полном объеме. В некоторых вариантах осуществления, уменьшение длины полипептидного линкера до менее чем 12 аминокислотных остатков предотвращает формирование пар вариабельных доменов тяжелой и легкой цепей на одной и той же полипептидной цепи, тем самым делая возможным формирование пар вариабельных доменов тяжелой и легкой цепей из одной цепи с комплементарными доменами на другой цепи. Таким образом, полученные АВР имеют мультиспецифичность, причем специфичность каждого сайта связывания создается более чем одной полипептидной цепью. Полипептидные цепи, содержащие вариабельные домены тяжелой и легкой цепей, которые соединены линкерами с длинной между 3 и 12 аминокислотными остатками, формируют преимущественно димеры (называемые диателами). В случае линкеров с длинной между 0 и 2 аминокислотными остатками, преимущественно будут тримеры (называемые триателами) и тетрамеры (называемые тетрателами). Однако точный тип олигомеризации, по-видимому, зависит от аминокислотного состава и порядка вариабельного домена в каждой полипептидной цепи (например, VH-линкер-VL против VL-линкер-VH), в дополнение к длине линкера. Специалист в данной области техники может выбрать подходящую длину линкера исходя из желаемой мультиспецифичности.
[0286] В некоторых вариантах осуществления, мультиспецифичный АВР содержит диатело. См. Hollinger et al., Proc. Natl. Acad. Sci. USA, 1993, 90:6444-6448, включен посредством ссылки в полном объеме. В некоторых вариантах осуществления, мультиспецифичный АВР содержит триатело. См. Todorovska et al., J. Immunol. Methods, 2001, 248:47-66, включен посредством ссылки в полном объеме. В некоторых вариантах осуществления, мультиспецифичный АВР содержит тетратело. См. id., включен посредством ссылки в полном объеме.
[0287] В некоторых вариантах осуществления, мультиспецифичный АВР содержит триспецифическое производное F(ab')3. См. Tutt et al. J. Immunol., 1991, 147:60-69, включен посредством ссылки в полном объеме.
[0288] В некоторых вариантах осуществления, мультиспецифичный АВР содержит перекрестно-сшитое антитело. См. патент США №4676980; Brennan et al., Science, 1985, 229:81-83; Staerz, et al. Nature, 1985, 314:628-631; и ЕР 0453082; каждый из которых включен посредством ссылки в полном объеме.
[0289] В некоторых вариантах осуществления, мультиспецифичный АВР содержит антиген-связывающие домены, собранные лейциновыми зиперами. См. Kostelny et al., J. Immunol, 1992, 148:1547-1553, включен посредством ссылки в полном объеме.
[0290] В некоторых вариантах осуществления, мультиспецифичный АВР содержит комплементарные белковые домены. В некоторых аспектах, комплементарные белковые домены содержат якорный домен (AD), и домен димеризации и докинга (DDD). В некоторых вариантах осуществления, AD и DDD связываются друг с другом и тем самым обеспечивают сборку мультиспецифических структур АВР посредством подхода «докинг и захват» (DNL). Могут быть собраны АВР с многими специфичностями, включая биспецифические АВР, триспецифические АВР, тетраспецифические АВР, квинтспецифические АВР и гексаспецифические АВР. Мультиспецифические АВР, содержащие комплементарные белковые домены, описаны, например, в патентах США №7521056; 7550143; 7534866; и 7527787; каждый из которых включен посредством ссылки в полном объеме.
[0291] В некоторых вариантах осуществления, мультиспецифичный АВР содержит антитело Fab двойного действия (DAF), как описано в публикации патентна США №2008/0069820, включенной посредством ссылки в полном объеме.
[0292] В некоторых вариантах осуществления, мультиспецифичный АВР содержит антитело, сформированное путем восстановления двух родительских молекул с последующим смешиванием двух родительских молекул и повторным окислением с целью сборки гибридной структуры. См. Carlring et al., PLoS One, 2011, 6:e22533, включен посредством ссылки в полном объеме.
[0293] В некоторых вариантах осуществления, мультиспецифичный АВР содержит DVD-Ig™. DVD-Ig™ представляет собой иммуноглобулин с двойным вариабельным доменом, который может связываться с двумя или больше антигенами. DVD-Igs™ описаны в патенте США №7612181, который включен посредством ссылки в полном объеме.
[0294] В некоторых вариантах осуществления, мультиспецифичный АВР содержит DART™. DART™ описаны в Moore et al., Blood, 2011, 117:454-451, включен посредством ссылки в полном объеме.
[0295] В некоторых вариантах осуществления, мультиспецифичный АВР содержит DuoBody®. DuoBodies® описаны в Labrijn et al., Proc. Natl. Acad. Sci. USA, 2013, 110:5145-5150; Gramer et al., mAbs, 2013, 5:962-972; и Labrijn et al., Nature Protocols, 2014, 9:2450-2463; каждый из которых включен посредством ссылки в полном объеме.
[0296] В некоторых вариантах осуществления, мультиспецифичный АВР содержит фрагмент антитела, присоединенный к другому антителу или фрагменту. Присоединение может быть ковалентным или нековалентным. Когда присоединение является ковалентным, оно может быть в форме гибридного белка или через химический линкер. Иллюстративные примеры мультиспецифических АВР, содержащих фрагменты антител, присоединенные к другим антителам, включают четырехвалентные биспецифические антитела, где scFv слит с С-концом СH3 из IgG. См. Coloma and Morrison, Nature Biotechnol., 1997, 15:159-163. Другие примеры включают антитела, в которых молекула Fab присоединена к константной области иммуноглобулина. См. Miler et al., J. Immunol., 2003, 170:4854-4861, включен посредством ссылки в полном объеме. Можно использовать любой подходящий фрагмент, включая любой из фрагментов, описанных в данном документе или известных в данной области техники.
[0297] В некоторых вариантах осуществления, мультиспецифичный АВР содержит CovX-Body. CovX-Bodies описаны, например, в Doppalapudi et al., Proc. Natl. Acad. Sci. USA, 2010, 107:22611-22616, включен посредством ссылки в полном объеме.
[0298] В некоторых вариантах осуществления, мультиспецифичный АВР содержит антитело Fcab, где один или больше антиген-связывающих доменов вносят в область Fc. Антитела Fcab описаны в Wozniak-Knopp et al., Protein Eng. Des. Sel., 2010, 23:289-297, включен посредством ссылки в полном объеме.
[0299] В некоторых вариантах осуществления, мультиспецифичный АВР содержит антитело TandAb®. Антитела TandAb® описаны в Kipriyanov et al., J. Mol. Biol., 1999, 293:41-56 и Zhukovsky et al., Blood, 2013, 122:5116, каждый из которых включен посредством ссылки в полном объеме.
[0300] В некоторых вариантах осуществления, мультиспецифичный АВР содержит тандем Fab. Тандемные Fab описаны в WO 2015/103072, включен посредством ссылки в полном объеме.
[0301] В некоторых вариантах осуществления, мультиспецифичный АВР содержит Zybody™. Zybodies™ описаны в LaFleur et al., mAbs, 2013, 5:208-218, включен посредством ссылки в полном объеме.
2.5. Антагонизм TIGIT
[0302] В некоторых вариантах осуществления, АВР, предложенные в данном документе, антагонизируют TIGIT при связывании.
[0303] В некоторых вариантах осуществления, антагонизирование TIGIT с помощью АВР, предложенного в данном документе, приводит к димеризации и/или активации CD226 (также известного как DNAM-1), ко-стимулирующего рецептора, димеризация и функционирование которого нарушается путем прямого взаимодействия с TIGIT. См. Grogan et al., J. Immunol., 2014, 192 (1 приложение) 2013.15., включен в данный документ посредством ссылки в полном объеме. На Фиг. 2 показана иллюстрация пути CD226-TIGIT по сравнению с путем CD28/CTLA4, который имеет аналогичную биохимию костимуляции/коингибирования.
[0304] В некоторых вариантах осуществления, антагонизирование TIGIT с помощью АВР, предложенного в данном документе, увеличивает количество CD226 и CD155, которое взаимодействует, по сравнению с количеством, которое взаимодействует в отсутствие АВР.
[0305] В некоторых вариантах осуществления, антагонизирование TIGIT с помощью АВР, предложенного в данном документе, приводит к активации эффекторного Т-лимфоцита. В некоторых аспектах, эффекторный Т-лимфоцит представляет собой CD8+Т-лимфоцит. В некоторых аспектах, эффекторный Т-лимфоцит представляет собой CD4+Т-лимфоцит.
[0306] В некоторых вариантах осуществления, антагонизирование TIGIT с помощью АВР, предложенного в данном документе, приводит к активации клетки NK. В некоторых вариантах осуществления, антагонизирование TIGIT с помощью АВР, предложенного в данном документе, приводит к активации клетки NKT.
[0307] В некоторых вариантах осуществления, антагонизирование TIGIT с помощью АВР, предложенного в данном документе, приводит к уменьшению ингибирующей активности регуляторного Т-лимфоцита в отношении эффекторного Т-лимфоцита.
[0308] В некоторых вариантах осуществления, антагонизирование TIGIT с помощью АВР, предложенного в данном документе, приводит к усиленной секреции ИЛ-2, ИЛ-6, GM-CSF, ФНО, LT-α и/или ИНФ-γ клеткой-мишенью.
[0309] В некоторых вариантах осуществления, антагонизирование TIGIT с помощью АВР, предложенного в данном документе, увеличивает пролиферацию, выживание и/или функцию эффекторного Т-лимфоцита. В некоторых аспектах, эффекторный Т-лимфоцит представляет собой эффекторный CD4+Т-лимфоцит.В некоторых аспектах, эффекторный Т-лимфоцит представляет собой эффекторный CD8+Т-лимфоцит.
[0310] В некоторых вариантах осуществления, антагонизирование TIGIT с помощью АВР, предложенного в данном документе, отменяет подавление эффекторного Т-лимфоцита регуляторным Т-лимфоцитом. В некоторых аспектах, регуляторный Т-лимфоцит представляет собой CD4+CD25+Foxp3+регуляторный Т-лимфоцит. В некоторых аспектах, регуляторный Т-лимфоцит представляет собой CD8+CD25+регуляторный Т-лимфоцит.
[0311] В некоторых вариантах осуществления, антагонизирование TIGIT с помощью АВР, предложенного в данном документе, приводит к усилению иммунного ответа.
[0312] В некоторых вариантах осуществления, антагонизирование TIGIT с помощью АВР, предложенного в данном документе, приводит к предотвращению образования опухоли. В некоторых вариантах осуществления, антагонизм TIGIT с помощью АВР, предложенного в данном документе, приводит к задержке начала образования опухоли. В некоторых вариантах осуществления, антагонизирование TIGIT с помощью АВР, предложенного в данном документе, приводит к уменьшению размера опухоли. В некоторых вариантах осуществления, антагонизирование TIGIT с помощью АВР, предложенного в данном документе, приводит к устранению опухоли. В некоторых вариантах осуществления, антагонизивание TIGIT с помощью АВР, предложенного в данном документе, приводит к уменьшению количества метастаз.
[0313] В некоторых вариантах осуществления, антагонизирование TIGIT с помощью АВР, предложенного в данном документе, приводит к предотвращению вирусной болезни. В некоторых вариантах осуществления, антагонизирование TIGIT с помощью АВР, предложенного в данном документе, приводит к задержке начала вирусного заболевания. В некоторых вариантах осуществления, антагонизирование TIGIT с помощью АВР, предложенного в данном документе, приводит к уменьшению вирусной нагрузки у субъекта. В некоторых вариантах осуществления, антагонизирование TIGIT с помощью АВР, предложенного в данном документе, приводит к устранению вирусной инфекции.
2.6. Аффинность и кинетика антиген-связывающих белков к TIGIT;
Эффективность
[0314] В некоторых вариантах осуществления, аффинность АВР, предложенного в данном документе, к TIGIT, как определенно по KD, составляет меньше чем около 10-5 М, меньше чем около 10-6 М, меньше чем около 10-7 М, меньше чем около 10-8 М, меньше чем около 10-9 М, меньше чем около 10-10 М, меньше чем около 10-11 М или меньше чем около 10-12 М. В некоторых вариантах осуществления, аффинность АВР находится в интервале между около 10-7М и 10-12 М. В некоторых вариантах осуществления, аффинность АВР находится в интервале между около 10-7 М и 10-11 М. В некоторых вариантах осуществления, аффинность АВР находится в интервале между около 10-7 М и 10-10 М. В некоторых вариантах осуществления, аффинность АВР находится в интервале между около 10-7 М и 10-9 М. В некоторых вариантах осуществления, аффинность АВР находится в интервале между около 10-7 М и 10-8 М. В некоторых вариантах осуществления, аффинность АВР находится в интервале между около 10-8 М и 10-12 М. В некоторых вариантах осуществления, аффинность АВР находится в интервале между около 10-8 М и 10-11 М. В некоторых вариантах осуществления, аффинность АВР находится в интервале между около 10-9 М и 10-11 М. В некоторых вариантах осуществления, аффинность АВР находится в интервале между около 10-10 М и 10-11 М.
[0315] В некоторых вариантах осуществления, аффинность АВР, предложенного в данном документе, к hTIGIT, как определенно по KD, измеренной с помощью ForteBio, как указано в Примере 4, выбирают из около 5,24×10-10 М, около 4,57×10-10 М, около 3,32×10-10 М, около 2,46×10-10 М, около 1,96×10-10 М, около 3,11×10-9 М, около 2,54×10-9 М, около 3,13×10-9 М, около 2,83×10-9 М, около 1,71×10-9 М, около 2,47×10-9 М, около 2,35×10-9 М, около 1,44×10-9 М, около 1,23×10-9 М, около 5,26×10-10 М, около 3,78×10-10 М, около 4,29×10-10 М, или около 4,48×10-10 М. В некоторых вариантах осуществления, такая аффинность составляет от около 3,13×10-9 М до около 1,96×10-10 М. В некоторых вариантах осуществления, такая КD составляет около 3,13×10-9 М или меньше.
[0316] В некоторых вариантах осуществления, аффинность АВР, предложенного в данном документе, к cTIGIT, как определенно по KD, измеренной с помощью ForteBio, как указано в Примере 4, выбирают из около 2,64×10-9 М, около 6,55×10-9 М, около 8,14×10-9 М, около 6,57×10-9 М, около 7,94×10-8 М, около 7,04×10-8 М, около 1,10×10-7 М, около 7,20×10-8 М, около 1,57×10-9 М, около 8,02×10-10 М, около 3,67×10-10 М, около 8,98×10-10 М, около 1,75×10-8 М, около 2,58×10-8 М, около 9,35×10-9 М. В некоторых вариантах осуществления, такая аффинность составляет от около 1,10×10-7 М до около 3,69×10-10 М. В некоторых вариантах осуществления, такая КD составляет около 1,10×10-7 М или меньше.
[0317] В некоторых вариантах осуществления, аффинность АВР, предложенного в данном документе, к hTIGIT, как определенно по KD, измеренной с помощью способов произведения растворимости (MSD-SET), как указано в Примере 4, выбирают из около 5,40×10-11 М, около 1,10×10-10 М, около 1,50×10-10 М, около 5,60×10-11 М, около 4,00×10-10 М, около 3,80×10-10 М, около 2,10×10-10 М, около 7,00×10-11 М, около 4,10×10-11 М, около 2,50×10-11 М, около 3,00×10-11 М, около 8,00×10-11 М, около 8,10×10-12 М, около 5,00×10-12 М, или около 4,90×10-12 М. В некоторых вариантах осуществления, такая аффинность составляет от около 4,00×10-10 М до около 4,90×10-12 М. В некоторых вариантах осуществления, такая КD составляет около 4,00×10-10 М или меньше.
[0318] В некоторых вариантах осуществления, аффинность АВР, предложенного в данном документе, к cTIGIT, как определенно по KD, измеренной с помощью MSD-SET, как указано в Примере 4, выбирают из около 3,20×10-10 М, около 2,30×10-10 М, около 3,50×10-11 М, около 1,50×10-11 М, или около 4,60×10-11 М. В некоторых вариантах осуществления, такая аффинность составляет от около 3,20×10-10 М до около 1,50×10-11 М. В некоторых вариантах осуществления, такая КD составляет около 3,20×10-10 М или меньше.
[0319] В некоторых вариантах осуществления, аффинность АВР, предложенного в данном документе, к hTIGIT, как определенно по KD, измеренной с помощью ForteBio, как указано в Примере 6, выбирают из около 7,1×10-10 М, около 8,1×10-11 М, около 1,9×10-10 М, около 5,6×10-10 М, около 2,4×10-10 М, около 2,8×10-10 М, около 1,6×10-10 М, около 5,8×10-10 М, около 1,1×10-9 М, около 8,1×10-10 М, около 4,6×10-10 М, около 3,6×10-10 М. В некоторых вариантах осуществления, такая аффинность составляет от около 1,1×10-9 М до около 8,1×10-11 М. В некоторых вариантах осуществления, такая КD составляет около 1,1×10-9 М или меньше.
[0320] В некоторых вариантах осуществления, аффинность АВР, предложенного в данном документе, к hTIGIT, как определенно по KD, измеренной с помощью ForteBio, как указано в Примере 6, составляет около 2,4×10-10 М. В некоторых вариантах осуществления, аффинность АВР, предложенного в данном документе, к cTIGIT, как определенно по KD, измеренной с помощью ForteBio, как указано в Примере 6, составляет около 6,2×10-9 М. В некоторых вариантах осуществления, такая КD составляет около 6,2×10-9 М или меньше.
[0321] В некоторых вариантах осуществления, аффинность АВР, предложенного в данном документе, к hTIGIT, экспрессированом на поверхности клетки Jurkat, как определено по KD, описанной в Примере 6, составляет около 5,1×10-10 М. В некоторых вариантах осуществления, такая КD составляет около 5,1×10-10 М или меньше.
[0322] В некоторых вариантах осуществления, аффинность АВР, предложенного в данном документе, к cTIGIT, экспрессированом на поверхности клетки Jurkat, как определено по KD, описанной в Примере 6, составляет около 4,0×10-10 М. В некоторых вариантах осуществления, такая КD составляет около 4,0×10-10 М или меньше.
[0323] В некоторых вариантах осуществления, аффинность АВР, предложенного в данном документе, к mTIGIT (SEQ ID NO: 3), экспрессированом на поверхности клетки Jurkat, как определено по KD, описанной в Примере 6, составляет около 9,8×10-9 М. В некоторых вариантах осуществления, такая КD составляет около 9,8×10-9 М или меньше. В некоторых вариантах осуществления, такая КD составляет около 9,8×10-9 М или больше.
[0324] В некоторых вариантах осуществления, аффинность АВР, предложенного в данном документе, к hTIGIT, экспрессированом на поверхности человеческого CD8+Т-лимфоцита, как определено по KD, описанной в Примере 6, составляет около 1,3×10-9 М. В некоторых вариантах осуществления, такая КD составляет около 1,3×10-9 М или меньше.
[0325] В некоторых вариантах осуществления, аффинность АВР, предложенного в данном документе, к cTIGIT, экспрессированом на поверхности CD8+Т-лимфоцита яванского макака, как определено по KD, описанной в Примере 6, составляет около 2,8×10-9 М. В некоторых вариантах осуществления, такая КD составляет около 2,8×10-9 М или меньше.
[0326] В некоторых вариантах осуществления, аффинность АВР, предложенного в данном документе, к mTIGIT, экспрессированом на поверхности регуляторного Т-лимфоцита мыши (например, mTIGIT как он естественно встречается на таких клетках, в независимости от того принадлежит ли такой mTIGIT к SEQ ID NO: 3 или 138, но включая такие SEQ ID NO), как определено по KD, описанной в Примере 6, составляет около 2,5×10-8 М. В некоторых вариантах осуществления, такая КD составляет около 2,5×10-8 М или меньше.
[0327] В некоторых вариантах осуществления, АВР, предложенные в данном документе, специфически связываются с hTIGIT (SEQ ID NO: 1) c KD X и cTIGIT (SEQ ID NO: 2) или mTIGIT (SEQ ID NO: 3 или 138) с Kd≤10X. В некоторых вариантах осуществления, АВР, предложенные в данном документе, специфически связываются с hTIGIT (SEQ ID NO: 1) с KD Х и с cTIGIT (SEQ ID NO: 2) или mTIGIT (SEQ ID NO: 3 или 138) с KD<=5X. В некоторых вариантах осуществления, АВР, предложенные в данном документе, специфически связываются с hTIGIT (SEQ ID NO: 1) сKD X и с cTIGIT (SEQ ID NO: 2) или mTIGIT (SEQ ID NO: 3 или 138) с KD≤2X. В некоторых аспектах, X представляет собой любую KD, описанную в данном раскрытии изобретения. В некоторых аспектах, X составляет 0,01 нМ, 0,1 нМ, 1 нМ, 10 нМ, 20 нМ, 50 нМ или 100 нМ.
[0328] В некоторых вариантах осуществления, соотношение KD(hTIGIT) : KD(cTIGIT) для АВР, предложенного в данном документе, как измерено с помощью ForteBio, как указано в Примере 4, выбирают из около 1,98×10-1, около 2,61×10-1, около 3,03×10-1, около 3,58×10-1, около 6,62×10-3, около 1,98×10-1, около 5,37×10-3, около 3,90×10-3, около 6,22×10-3, около 2,91×10-1, около 4,14×10-1, около 6,67×10-1, около 2,18×10-1, около 1,78×10-1, около 1,21×10-1, или около 3,03×10-1. В некоторых вариантах осуществления, такое соотношение составляет от около 3,90×10-3 до около 6,67×10-1.
[0329] В некоторых вариантах осуществления, соотношение KD(hTIGIT) : KD(cTIGIT) для АВР, предложенного в данном документе, как измерено с помощью ForteBio, как указано в Примере, составляет около 3,87×10-2.
[0330] В некоторых вариантах осуществления, соотношение KD(hTIGIT) : KD(cTIGIT) для АВР, предложенного в данном документе, как измерено с помощью MSD-SET, как указано в Примере 4, выбирают из около 3,33×10-1, около 2,31×10-1, около 1,09×10-1, около 1,07×10-1, или около 1,69×10-1. В некоторых вариантах осуществления, такое соотношение находится в пределах от около 1,07×10-1 М до около 3,33×10-1 М.
[0331] В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет kа по меньшей мере около 104 М-1×с-1 В некоторых вариантах осуществления, АВР имеет kа по меньшей мере около 105 М-1×с-1 В некоторых вариантах осуществления, АВР имеет kа по меньшей мере около 106 М-1×с-1 В некоторых вариантах осуществления, АВР имеет kа между около 104 М-1×с-1 и около 105 М-1×с-1. В некоторых вариантах осуществления, АВР имеет kа между около 105 М-1×с-1 и около 106 М-1×с-1. В некоторых вариантах осуществления, такая kа составляет по меньшей мере около 105 М-1×с-1.
[0332] В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет kа для hTIGIT, как измерено с помощью ForteBio, как указано в Примере 6, выбранную из около 3,2×105 М-1×с-1, около 7,0×105 М-1×с-1, около 7,7×105 М-1×с-1, около 1,6×106 М-1×с-1, около 2,0×106 М-1×с-1, около 1,3×106 М-1×c-1, около 1,5×106 М-1×с-1, около 1,1×106 М-1×с-1, около 4,5×105 M-1×c-1, около 7,5×105 М-1×с-1, около 8,9×105 М-1×с-1, или около 1,4×106 М-1×с-1. В некоторых вариантах осуществления, такая kа находится в пределах от около 3,2×105 М-1×с-1 до около 2,0×106 М-1×с-1. В некоторых вариантах осуществления, такая kd составляет около 2,0×106 М или меньше.
[0333] В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет kа для hTIGIT, как измерено с помощью ForteBio, как указано в Примере 6, около 2,0×106 М-1×с-1. В некоторых вариантах осуществления, такая kа составляет по меньшей мере около 2,0×106 М-1×c-1.
[0334] В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет kа для cTIGIT, как измерено с помощью ForteBio, как указано в Примере 6, около 7,9×105 М-1×с-1. В некоторых вариантах осуществления, такая kа составляет по меньшей мере около 7,9×105М-1×с-1.
[0335] В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет kd около 10-5 с-1 или меньше. В некоторых вариантах осуществления, АВР имеет kd около 10-4 с-1 или меньше. В некоторых вариантах осуществления, АВР имеет kd около 10-3 с-1 или меньше. В некоторых вариантах осуществления, АВР имеет kd между около 10-2 с-1 и около 10-5 с-1. В некоторых вариантах осуществления, АВР имеет kd между около 10-2 с-1 и около 10-4 с-1. В некоторых вариантах осуществления, АВР имеет kd между около 10-3 с-1 и около 10-5 с-1.
[0336] В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет kd для hTIGIT, как измерено с помощью ForteBio, как указано в Примере 6, выбранную из около 2,3×10-4 с-1, около 6,3×10-5 с-1, около 1,4×10-4 с-1, около 8,5×10-4 с1, около 3,8×10-4 с-1, около 3,5×10-4 с-1, около 2,4×10-4 с-1, около 6,6×10-4 с-1, около 5,9×10-4 с-1, или около 5,0×10-4 с-1. В некоторых вариантах осуществления, такая kd находится в пределах от около 6,3×10-5 с-1 до около 8,5×10-4 с-1. В некоторых вариантах осуществления, такая kd составляет меньше чем около 8,5×10-4 с-1.
[0337] В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет kd для hTIGIT, как измерено с помощью ForteBio, как указано в Примере 6, около 3,8×10-4 с-1. В некоторых вариантах осуществления, такая kd составляет меньше чем около 3,8×10-4 с-1.
[0338] В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет kd для cTIGIT, как измерено с помощью ForteBio, как указано в Примере 6, около 4,6×10-3 с-1. В некоторых вариантах осуществления, такая kd составляет меньше чем около 4,6×10-3 с-1.
[0339] В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет kа для hTIGIT около 3,2×105 М-1×с-1, kd для hTIGIT около 2,3×10-4 с-1, и KD для hTIGIT около 7,1×10-10 М. В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет kа для hTIGIT около 7,0×105 М-1×с-1, kd для hTIGIT около 6,3×10-5 с-1, и KD для hTIGIT около 8,1×10-11 М. В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет kа для hTIGIT около 7,7×105 М-1 с-1, kd для hTIGIT около 1,4×10-4 с-1, и KD для hTIGIT около 1,9×10-10 М. В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет kа для hTIGIT около 1,6×106 M-1 × c-1, kd для hTIGIT около 8,5×10-4 с-1, и KD для hTIGIT около 5,6×10-10 М. В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет kа для hTIGIT около 2,0×106 M-1 × c-1, kd для hTIGIT около 3,8×10-4 с-1, и KD для hTIGIT около 2,4×10-10 М. В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет kа для hTIGIT около 1,3×106 M-1 × c-1, kd для hTIGIT около 3,5×10-4 с-1, и KD для hTIGIT около 2,8×10-10 М. В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет ka для hTIGIT около 1,5×106 М-1 с-1, kd для hTIGIT около 2,4×10-4 с-1, и KD для hTIGIT около 1,6×10-10 М. В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет ka для hTIGIT около 1,1×106 М-1×с-1, kd для hTIGIT около 6,6×10-4 с-1, и KD для hTIGIT около 5,8×10-10 М. В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет ka для hTIGIT около 4,5×105 M-1 × c-1, kd для hTIGIT около 3,5×10-4 с-1, и KD для hTIGIT около 1,1×10-9 М. В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет kа для hTIGIT около 7,5×105 М-1×с-1, kd для hTIGIT около 5,9×10-4 с-1, и KD для hTIGIT около 8,1×10-10 М. В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет kа для hTIGIT около 8,9×105 М-1 × с-1, kd для hTIGIT около 3,8×10-4 с-1, и KD для hTIGIT около 4,6×10-10 М. В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет ka для hTIGIT около 1,4×106 M-1 × c-1, kd для hTIGIT около 5,0×10-4 с-1, и KD для hTIGIT около 3,6×10-10 М. В некоторых вариантах осуществления, такие ka, kd и KD определяют в соответствии со способами, представленными в Примере 6.
[0340] В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет ka для hTIGIT около 2,0×106 М-1 × c-1, kd для hTIGIT около 3,8×10-4 с-1, и KD для hTIGIT около 2,4×10-10 М, ka для cTIGIT около 7,9×105 М-1 × с-1, kd для cTIGIT около 4,6×10-3 с-1, и KD для cTIGIT около 6,2×10-9 М и KD для mTIGIT (SEQ ID NO: 3) больше чем 7,0 10-7 М. В некоторых вариантах осуществления, такие ka, kd и KD определяют в соответствии со способами, представленными в Примере 6.
[0341] В некоторых вариантах осуществления, KD, ka и kd определяют с применением поверхностного плазмонного резонанса (SPR). В некоторых аспектах, в анализе SPR использует инструмент BIACORE®. В некоторых аспектах, антиген иммобилизуют на карбоксиметилированном декстрановом биосенсорном чипе (СМ4 или СМ5) и приводят в контакт с АВР, предложенным в данном документе. Константы скорости ассоциации и диссоциации могут быть рассчитаны с применением программного обеспечения BIAevaluation® и один-к-одному модели связывания Ленгмюра. В некоторых аспектах, анализ проводят при 25°С. В некоторых аспектах анализ проводят при 37°С.
[0342] В некоторых вариантах осуществления, KD, ka и kd определяют с применением интерферометрии биослоя (BLI). Может быть использован любой подходящий способ BLI. В некоторых аспектах, в анализе BLI применяется инструмент FORTEBIO® В некоторых аспектах, биосенсор захвата анти-IgG Fc человека (АНС) применяется для захвата АВР на поверхность сенсора. В дальнейшем, связывание АВР и антигена наблюдают путем приведения в контакт иммобилизованного АВР с различными концентрациями TIGIT. Диссоциацию антигена и АВР затем измеряют в буфере без TIGIT. Константы скорости ассоциации и диссоциации рассчитывают с применением кинетических модулей программного обеспечения FORTEBIO®. В некоторых аспектах, анализ проводят при 30°С.
[0343] В других вариантах осуществления, KD может быть определено с помощью антиген-связывающего анализа с радиоактивным мечением, как описано в Chen et al. J. Mol. Biol., 1999, 293:865-881, включен посредством ссылки в полном объеме.
[0344] В других вариантах осуществления, KD может быть определено применяя MSD-SET, как описано в Примере 4.
[0345] В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет ЕС50, как измерено по продуцированию ИЛ-2 в анализе совместного культивирования человеческого TIGIT Jurkat, как описано в Примере 7, около 0,22 нМ, около 0,31 нМ, около 0,33 нМ, около 0,34 нМ, около 0,25 нМ, около 0,24 нМ, около 0,11 нМ, около 0,06 нМ, около 0,14 нМ, около 0,16 нМ, около 1,40 нМ, около 0,71 нМ, около 0,21 нМ, около 1,11 нМ, около 0,13 нМ, около 0,20 нМ, около 0,68 нМ или около 0,61 нМ. В некоторых вариантах осуществления, такая ЕС50 находится в пределах от около 0,06 нМ до около 1,40 нМ. В некоторых вариантах осуществления, такая ЕС50 составляет около 1,40 нМ или меньше.
[0346] В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет ЕС50, как измерено по продуцированию ИЛ-2 в анализе совместного культивирования TIGIT яванского макака Jurkat, как описано в Примере 7, около 2,87 нМ. В некоторых вариантах осуществления, такая ЕС50 составляет около 2,87 нМ или меньше. В некоторых вариантах осуществления, соотношение ЕС50(cTIGIT) : ЕС50(hTIGIT) в таком анализе находится в пределах от около 2,05 до около 47,8.
[0347] В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет ЕС10, как измерено по продуцированию ФНО в МКПК, выделенных из человеческого донора и обработанных, как описано в Примере 9, в диапазоне от около 5,02 нМ до около 18,86 нМ. В некоторых вариантах осуществления, такая ЕС10 составляет около 18,86 нМ или меньше.
[0348] В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет ЕС50, как измерено по продуцированию ФНО в МКПК, выделенных из человеческого донора и обработанных, как описано в Примере 9, в диапазоне от около 12,60 нМ до около 20,60 нМ. В некоторых вариантах осуществления, такая EC50 составляет около 20,60 нМ или меньше.
[0349] В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет ЕС90, как измерено по продуцированию ФНО в МКПК, выделенных из человеческого донора и обработанных, как описано в Примере 9, в диапазоне от около 22,49 нМ до около 31,59 нМ. В некоторых вариантах осуществления, такая ЕС90 составляет около 31,59 нМ или меньше.
[0350] В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет ЕС10 в диапазоне от около 5,02 нМ до около 18,86 нМ, ЕС50 в диапазоне от около 12,60 нМ до около 20,60 нМ, и ЕС90 в диапазоне от около 22,49 нМ до около 31,59 нМ, в каждом случае как измерено по продуцированию ФНО в МКПК, выделенных из человеческого донора и обработанных, как описано в Примере 9.
[0351] В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет ЕС10 около 11,94 нМ или меньше, ЕС50 около 16,60 нМ или меньше, и ЕС90 около 27,04 нМ или меньше, в каждом случае как измерено по продуцированию ФНО в МКПК, выделенных из человеческого донора и обработанных, как описано в Примере 9.
[0352] В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет ЕС10 около 18,86 нМ или меньше, ЕС50 около 20,06 нМ или меньше, и ЕС90 около 31,59 нМ или меньше, в каждом случае как измерено по продуцированию ФНО в МКПК, выделенных из человеческого донора и обработанных, как описано в Примере 9.
[0353] В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет ЕС10 около 5,02 нМ или меньше, ЕС50 около 12,60 нМ или меньше, и ЕС90 около 22,49 нМ или меньше, в каждом случае как измерено по продуцированию ФНО в МКПК, выделенных из человеческого донора и обработанных, как описано в Примере 9.
[0354] В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет ЕС10, как измерено по продуцированию ИНФ-γ в CD4+Т-лимфоцитах, выделенных из человеческого донора и обработанных, как описано в Примере 9, в диапазоне от около 0,37 нМ до около 1,05 нМ. В некоторых вариантах осуществления, такая ЕС10 составляет около 1,05 нМ или меньше.
[0355] В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет ЕС50, как измерено по продуцированию ИНФ-γ в CD4+Т-лимфоцитах, выделенных из человеческого донора и обработанных, как описано в Примере 9, в диапазоне от около 0,94 нМ до около 1,12 нМ. В некоторых вариантах осуществления, такая ЕС50 составляет около 1,12 нМ или меньше.
[0356] В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет ЕС90, как измерено по продуцированию ИНФ-γ в CD4+Т-лимфоцитах, выделенных из человеческого донора и обработанных, как описано в Примере 9, в диапазоне от около 1,04 нМ до около 2,72 нМ. В некоторых вариантах осуществления, такая ЕС90 составляет около 2,72 нМ или меньше.
[0357] В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет ЕС10 в диапазоне от около 0,37 нМ до около 1,05 нМ, ЕС50 в диапазоне от около 0,94 нМ до около 1,12 нМ, и ЕС90 в диапазоне от около 1,04 нМ до около 2,72 нМ, в каждом случае как измерено по продуцированию ИНФ-γ в МКПК, выделенных из человеческого донора и обработанных, как описано в Примере 9.
[0358] В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет ЕС10 около 0,37 нМ или меньше, ЕС50 около 1,00 нМ или меньше, и ЕС90 около 2,72 нМ или меньше, в каждом случае как измерено по продуцированию ИНФ-γ в МКПК, выделенных из человеческого донора и обработанных, как описано в Примере 9.
[0359] В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет ЕС10 около 0,85 нМ или меньше, ЕС50 около 0,94 нМ или меньше, и ЕС90 около 1,04 нМ или меньше, в каждом случае как измерено по продуцированию ИНФ-γ в МКПК, выделенных из человеческого донора и обработанных, как описано в Примере 9.
[0360] В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет ЕС10 около 1,05 нМ или меньше, ЕС50 около 1,12 нМ или меньше, и ЕС90 около 1,19 нМ или меньше, в каждом случае как измерено по продуцированию ИНФ-γ в МКПК, выделенных из человеческого донора и обработанных, как описано в Примере 9.
[0361] В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет ЕС10 около 0,75 нМ или меньше, ЕС50 около 1,02 нМ или меньше, и ЕС90 около 1,65 нМ или меньше, в каждом случае как измерено по продуцированию ИНФ-γ в МКПК, выделенных из человеческого донора и обработанных, как описано в Примере 9.
[0362] В некоторых вариантах осуществления, АВР, предложенный в данном документе, связывает hTIGIT с KD около 5,24×10-10 М (как определено ForteBio), cTIGIT с KD около 2,64×10-9 М (как определено ForteBio), hTIGIT с KD около 5,40×10-11 М (как определено MSD-SET), и cTIGIT с KD около 3,20×10-10 М (как определено MSD-SET), в каждом случае определяли в соответствии с способами, представленными в Примере 4.
[0363] В некоторых вариантах осуществления, АВР, предложенный в данном документе, связывает hTIGIT с KD около 4,57×10-10 М (как определено ForteBio), cTIGIT с KD около 1,57×10-9 М (как определено ForteBio), hTIGIT с KD около 2,50×10-11 М (как определено MSD-SET), и cTIGIT с KD около 2,30×10-10 М (как определено MSD-SET), в каждом случае определяли в соответствии с способами, представленными в Примере 4.
[0364] В некоторых вариантах осуществления, АВР, предложенный в данном документе, связывает hTIGIT с KD около 3,32×10-10 М (как определено ForteBio), cTIGIT с KD около 8,02×10-10 M (как определено ForteBio), hTIGIT с KD около 8,10×10-12 М (как определено MSD-SET), и cTIGIT с KD около 3,50×10-1 М (как определено MSD-SET), в каждом случае определяли в соответствии с способами, представленными в Примере 4.
[0365] В некоторых вариантах осуществления, АВР, предложенный в данном документе, связывает hTIGIT с KD около 2,46×10-10 М (как определено ForteBio), cTIGIT с KD около 3,69×10-10 М (как определено ForteBio), hTIGIT с KD около 5,00×10-12 М (как определено MSD-SET), и cTIGIT с KD около 1,50×10-11 М (как определено MSD-SET), в каждом случае определяли в соответствии с способами, представленными в Примере 4.
[0366] В некоторых вариантах осуществления, АВР, предложенный в данном документе, связывает hTIGIT с KD около 1,96×10-10 М (как определено ForteBio), cTIGIT с KD около 8,98×10-10 М (как определено ForteBio), hTIGIT с KD около 4,90×10-12 М (как определено MSD-SET), и cTIGIT с KD около 4,60×10-11 М (как определено MSD-SET), в каждом случае определяли в соответствии с способами, представленными в Примере 4.
[0367] В некоторых вариантах осуществления, АВР, предложенный в данном документе, связывает hTIGIT с KD около 3,11×10-9 М (как определено ForteBio) и cTIGIT с KD около 1,75×10-8 М (как определено ForteBio), в каждом случае определяли в соответствии с способами, представленными в Примере 4.
[0368] В некоторых вариантах осуществления, АВР, предложенный в данном документе, связывает hTIGIT с KD около 2,54×10-9 М, как определено ForteBio в соответствии с способами, представленными в Примере 4.
[0369] В некоторых вариантах осуществления, АВР, предложенный в данном документе, связывает hTIGIT с KD около 3,13×10-9 М (как определено ForteBio) и cTIGIT с KD около 2,58×10-8 М (как определено ForteBio), в каждом случае определяли в соответствии с способами, представленными в Примере 4.
[0370] В некоторых вариантах осуществления, АВР, предложенный в данном документе, связывает hTIGIT с KD около 2,83×10-9 М (как определено ForteBio) и cTIGIT с KD около 9,35×10-9 М (как определено ForteBio), в каждом случае определяли в соответствии с способами, представленными в Примере 4.
[0371] В некоторых вариантах осуществления, АВР, предложенный в данном документе, связывает hTIGIT с KD около 1,71×10-9 М (как определено ForteBio), cTIGIT с KD около 6,55×10-9 М (как определено ForteBio) и hTIGIT с KD около 1,10×10-10 М (как определено MSD-SET), в каждом случае определяли в соответствии с способами, представленными в Примере 4.
[0372] В некоторых вариантах осуществления, АВР, предложенный в данном документе, связывает hTIGIT с KD около 2,47×10-9 М (как определено ForteBio), cTIGIT с KD около 8,14×10-9 М (как определено ForteBio) и hTIGIT с KD около 1,50×10-10 М (как определено MSD-SET), в каждом случае определяли в соответствии с способами, представленными в Примере 4.
[0373] В некоторых вариантах осуществления, АВР, предложенный в данном документе, связывает hTIGIT с KD около 2,35×10-9 М (как определено ForteBio), cTIGIT с KD около 6,57×10-9 М (как определено ForteBio) и hTIGIT с KD около 5,60×10-11 М (как определено MSD-SET), в каждом случае определяли в соответствии с способами, представленными в Примере 4.
[0374] В некоторых вариантах осуществления, АВР, предложенный в данном документе, связывает hTIGIT с KD около 1,44×10-9 М (как определено ForteBio) и hTIGIT с KD около 4,00×10-10 М (как определено MSD-SET), в каждом случае определяли в соответствии с способами, представленными в Примере 4.
[0375] В некоторых вариантах осуществления, АВР, предложенный в данном документе, связывает hTIGIT с KD около 1,23×10-9 М (как определено ForteBio) и hTIGIT с KD около 3,80×10-10 М (как определено MSD-SET), в каждом случае определяли в соответствии с способами, представленными в Примере 4.
[0376] В некоторых вариантах осуществления, АВР, предложенный в данном документе, связывает hTIGIT с KD около 5,26×10-10 М (как определено ForteBio), cTIGIT с KD около 7,94×10-8 М (как определено ForteBio) и hTIGIT с KD около 2,10×10-10 М (как определено MSD-SET), в каждом случае определяли в соответствии с способами, представленными в Примере 4.
[0377] В некоторых вариантах осуществления, АВР, предложенный в данном документе, связывает hTIGIT с KD около 3,78×10-10 М (как определено ForteBio), cTIGIT с KD около 7,04×10-8 М (как определено ForteBio) и hTIGIT с KD около 7,00×10-11 М (как определено MSD-SET), в каждом случае определяли в соответствии с способами, представленными в Примере 4.
[0378] В некоторых вариантах осуществления, АВР, предложенный в данном документе, связывает hTIGIT с KD около 4,29×10-10 М (как определено ForteBio), cTIGIT с KD около 1,10×10-7 М (как определено ForteBio) и hTIGIT с KD около 4,10×10-11 М (как определено MSD-SET), в каждом случае определяли в соответствии с способами, представленными в Примере 4.
[0379] В некоторых вариантах осуществления, АВР, предложенный в данном документе, связывает hTIGIT с KD около 4,48×10-10 М (как определено ForteBio) и cTIGIT с KD около 7,20×10-8 М (как определено ForteBio), в каждом случае определяли в соответствии с способами, представленными в Примере 4.
[0380] В некоторых вариантах осуществления, АВР, предложенный в данном документе, связывает hTIGIT с KD около 3,00×10-11 М, как определено MSD-SET в соответствии с способами, представленными в Примере 4.
[0381] В некоторых вариантах осуществления, АВР, предложенный в данном документе, связывает hTIGIT с KD около 8,00×10-11 М, как определено MSD-SET в соответствии с способами, представленными в Примере 4.
[0382] В некоторых вариантах осуществления, АВР, предложенный в данном документе, ингибирует связывание PVR с TIGIT с IC50 около 2,2 нМ, около 2,3 нМ, около 1,6 нМ, около 1,9 нМ, около 1,7 нМ, около 3,2 нМ, около 2,6 нМ, около 2,9 нМ, около 3,3 нМ, около 2 нМ, около 2,2 нМ, около 2,1 нМ, около 1,8 нМ, около 6,4 нМ или около 1 нМ. В некоторых вариантах осуществления, такая IC50 находится в пределах от около 1 нМ до около 6,4 нМ. В некоторых вариантах осуществления, такая IC50 составляет около 6,4 нМ или меньше. В некоторых вариантах осуществления, такую IC50 определяют как описано в Примере 5.
[0383] В некоторых вариантах осуществления, АВР, предложенный в данном документе, ингибирует связывание PVRL2 с TIGIT с IC50 около 1,4 нМ, около 1,3 нМ, около 1,2 нМ, около 1,6 нМ, около 2 нМ, около 1,2 нМ, около 1,1 нМ, около 1 нМ, около 1,8 нМ, около 1,9 нМ, около 2 нМ или около 0,8 нМ. В некоторых вариантах осуществления, такая IC50 находится в пределах от около 0,8 нМ до около 2 нМ. В некоторых вариантах осуществления, такая IC50 составляет около 2 нМ или меньше. В некоторых вариантах осуществления, такую IC50 определяют как описано в Примере 5.
[0384] В некоторых вариантах осуществления, АВР, предложенный в данном документе, ингибирует связывание PVR с TIGIT с IC50 около 2,2 нМ и ингибирует связывание PVRL2 с TIGIT с IC50 около 1,4 нМ. В некоторых вариантах осуществления, АВР, предложенный в данном документе, ингибирует связывание PVR с TIGIT с IC50 около 2,3 нМ и ингибирует связывание PVRL2 с TIGIT с IC50 около 1,3 нМ. В некоторых вариантах осуществления, АВР, предложенный в данном документе, ингибирует связывание PVR с TIGIT с IC50 около 1,6 нМ и ингибирует связывание PVRL2 с TIGIT с IC50 около 1,2 нМ. В некоторых вариантах осуществления, АВР, предложенный в данном документе, ингибирует связывание PVR с TIGIT с IC50 около 1,9 нМ и ингибирует связывание PVRL2 с TIGIT с IC50 около 1,6 нМ. В некоторых вариантах осуществления, АВР, предложенный в данном документе, ингибирует связывание PVR с TIGIT с IC50 около 1,7 нМ и ингибирует связывание PVRL2 с TIGIT с IC50 около 1,4 нМ. В некоторых вариантах осуществления, АВР, предложенный в данном документе, ингибирует связывание PVR с TIGIT с IC50 около 3,2 нМ и ингибирует связывание PVRL2 с TIGIT с IC50 около 1,4 нМ. В некоторых вариантах осуществления, АВР, предложенный в данном документе, ингибирует связывание PVR с TIGIT с IC50 около 2,6 нМ и ингибирует связывание PVRL2 с TIGIT с IC50 около 2 нМ. В некоторых вариантах осуществления, АВР, предложенный в данном документе, ингибирует связывание PVR с TIGIT с IC50 около 2,9 нМ и ингибирует связывание PVRL2 с TIGIT с IC50 около 1,2 нМ. В некоторых вариантах осуществления, АВР, предложенный в данном документе, ингибирует связывание PVR с TIGIT с IC50 около 1,9 нМ и ингибирует связывание PVRL2 с TIGIT с IC50 около 1,1 нМ. В некоторых вариантах осуществления, АВР, предложенный в данном документе, ингибирует связывание PVR с TIGIT с IC50 около 3,3 нМ и ингибирует связывание PVRL2 с TIGIT с IC50 около 1 нМ. В некоторых вариантах осуществления, АВР, предложенный в данном документе, ингибирует связывание PVR с TIGIT с IC50 около 2 нМ и ингибирует связывание PVRL2 с TIGIT с IC50 около 1,2 нМ. В некоторых вариантах осуществления, АВР, предложенный в данном документе, ингибирует связывание PVR с TIGIT с IC50 около 1,7 нМ и ингибирует связывание PVRL2 с TIGIT с IC50 около 1,2 нМ. В некоторых вариантах осуществления, АВР, предложенный в данном документе, ингибирует связывание PVR с TIGIT с IC50 около 2,1 нМ и ингибирует связывание PVRL2 с TIGIT с IC50 около 1,8 нМ. В некоторых вариантах осуществления, АВР, предложенный в данном документе, ингибирует связывание PVR с TIGIT с IC50 около 2,6 нМ и ингибирует связывание PVRL2 с TIGIT с IC50 около 1,6 нМ. В некоторых вариантах осуществления, АВР, предложенный в данном документе, ингибирует связывание PVR с TIGIT с IC50 около 2,2 нМ и ингибирует связывание PVRL2 с TIGIT с IC50 около 1,1 нМ. В некоторых вариантах осуществления, АВР, предложенный в данном документе, ингибирует связывание PVR с TIGIT с IC50 около 2,1 нМ и ингибирует связывание PVRL2 с TIGIT с IC50 около 1,3 нМ. В некоторых вариантах осуществления, АВР, предложенный в данном документе, ингибирует связывание PVR с TIGIT с IC50 около 2,6 нМ и ингибирует связывание PVRL2 с TIGIT с IC50 около 1,9 нМ. В некоторых вариантах осуществления, АВР, предложенный в данном документе, ингибирует связывание PVR с TIGIT с IC50 около 1,8 нМ и ингибирует связывание PVRL2 с TIGIT с IC50 около 1,9 нМ. В некоторых вариантах осуществления, АВР, предложенный в данном документе, ингибирует связывание PVR с TIGIT с IC50 около 6,4 нМ и ингибирует связывание PVRL2 с TIGIT с IC50 около 2 нМ. В некоторых вариантах осуществления, АВР, предложенный в данном документе, ингибирует связывание PVR с TIGIT с IC50 около 2,3 нМ и ингибирует связывание PVRL2 с TIGIT с IC50 около 1,9 нМ. В некоторых вариантах осуществления, АВР, предложенный в данном документе, ингибирует связывание PVR с TIGIT с IC50 около 1 нМ и ингибирует связывание PVRL2 с TIGIT с IC50 около 0,8 нМ. В некоторых вариантах осуществления, такая IC50 составляет около 2 нМ или меньше. В некоторых вариантах осуществления, такую IC50 определяют как описано в Примере 5.
2.6.1. Варианты гликозилирования
[0385] В некоторых вариантах осуществления, АВР, предложенный в данном документе, может быть изменен для увеличения, уменьшения или устранения степени до которой он гликозилирован. Гликозилирование полипептидов обычно представляет собой либо «N-связаное», либо «О-связаное».
[0386] «N-связаное» гликозилирование относится к присоединению углеводного фрагмента к боковой цепи аспарагинового остатка. Трипептидные последовательности аспарагин-Х-серин и аспарагин-Х-треонин, где X представляет собой любую аминокислоту кроме пролина, являются последовательностями распознавания для ферментативного присоединения углеводного фрагмента к боковой цепи аспарагина. Таким образом, присутствие любой из этих трипептидных последовательностей в полипептиде создает потенциальный сайт гликозилирования.
[0387] «О-связаное» гликозилирование относится к присоединению одного из сахаров N-ацетилгалактозамина, галактозы или ксилозы к гидроксиаминокислоте, чаще всего к серину или треонину, хотя также может быть использован 5-гидроксипролин или 5-гидроксилизин.
[0388] Добавление или удаление N-связаных сайтов гликозилирования к или из АВР, предложенного в данном документе, может быть осуществлено путем изменения аминокислотной последовательности таким образом, чтобы одна или большее количество из описанных выше трипептидных последовательностей были созданы или удалены. Добавление или удаление О-связанных сайтов гликозилирования может быть выполнено путем добавления, удаления или замены одного или большего количества остатков серина или треонина в или к (если это возможно) последовательности АВР.
[0389] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит мотив гликозилирования, который отличается от встречающегося в природе АВР. Любой подходящий встречающийся в природе мотив гликозилирования может быть модифицирован в АВР, предложенных в данном документе. Структурные свойства и свойства гликозилирования иммуноглобулинов, например, являются известными в данной области техники и обобщены, например, в Schroeder and Cavacini, J. Allergy Clin. Immunol, 2010, 125:S41-52, включен посредством ссылки в полном объеме.
[0390] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит область Fc IgG1 с модификацией в виде олигосахарида, присоединенного к аспарагину 297 (Asn 297). Антитела IgG1 естественного происхождения, продуцируемые клетками млекопитающих, обычно содержат разветвленный двухветочный олигосахарид, который обычно присоединен через N-связывание к Asn 297 домена CH2 области Fc. См. Wright et al., TIBTECH, 1997, 15:26-32, включен посредством ссылки в полном объеме. Олигосахарид, присоединенный к Asn 297, может включать в себя различные углеводы, такие как манноза, N-ацетилглюкозамин (GlcNAc), галактоза и сиаловая кислота, а также фукоза, присоединенные к GlcNAc в «стебель» двухветочной олигосахаридной структуры.
[0391] В некоторых вариантах осуществления, олигосахарид, присоединенный к Asn 297, является модифицированным с целью создания АВР с измененным АЗКЦ. В некоторых вариантах осуществления, олигосахарид изменяют для улучшения АЗКЦ. В некоторых вариантах осуществления, олигосахарид изменяют для снижения АЗКЦ.
[0392] В некоторых аспектах, АВР, предложенный в данном документе, содержит домен IgG1 с сниженным содержанием фукозы в позиции Asn 297 по сравнению с встречающимся в природе доменом IgG1. Известно, что такие домены Fc имеют улучшенную АЗКЦ. См. Shields et al., J. Biol. Chem., 2002, 277:26733-26740, включен посредством ссылки в полном объеме. В некоторых аспектах, такие АВР не содержат никакой фукозы в позиции Asn 297. Количество фукозы может быть определено с применением любого подходящего способа, например, как описано в WO 2008/077546, включенном посредством ссылки в полном объеме.
[0393] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит разделенный на две части олигосахарид, такой как двухветочный олигосахарид, присоединенный к области Fc АВР, который разделен на две части GlcNAc. Такие варианты АВР могут иметь сниженное фукозилирование и/или улучшенную функцию АЗКЦ. Примеры таких вариантов АВР описаны, например, в WO 2003/011878; патенте США №6602684; и публикации патента США №2005/0123546; каждый из которых включен посредством ссылки в полном объеме.
[0394] Другие иллюстративные варианты гликозилирования, которые могут быть включены в АВР, предложенные в данном документе, описаны, например, в публикациях патентов США №2003/0157108, 2004/0093621, 2003/0157108, 2003/0115614, 2002/0164328, 2004/0093621, 2004/0132140, 2004/0110704, 2004/0110282, 2004/0109865; международных публикациях патентов №2000/61739, 2001/29246, 2003/085119, 2003/084570, 2005/035586, 2005/035778; 2005/053742, 2002/031140; Okazaki et al., J. Mol. Biol, 2004, 336:1239-1249; и Yamane-Ohnuki et al., Biotech. Bioeng., 2004, 87: 614-622; каждый из которых включен посредством ссылки в полном объеме.
[0395] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит область Fc с по меньшей мере одним галактозным остатком в олигосахариде, присоединенном к области Fc. Такие варианты АВР могут иметь улучшенную функцию CDC. Примеры таких вариантов АВР описаны, например, в WO 1997/30087; WO 1998/58964; и WO 1999/22764; каждый из которых включен посредством ссылки в полном объеме.
[0396] Примеры клеточных линий, способных продуцировать дефукозилированные АВР, включают клетки Lec13 СНО, которые неполноценны по белковому фукозилированию (см. Ripka et al., Arch. Biochem. Biophys., 1986, 249:533-545; публикацию патента США №2003/0157108; WO 2004/056312; каждый из которых включен посредством ссылки в полном объеме), и нокаутные клеточные линии, такие как клетки СНО нокаутные по гену альфа-1,6-фукозилтрансферазы или FUT8 (см. Yamane-Ohnuki et al., Biotech. Bioeng., 2004, 87:614-622; Kanda et al., Biotechnol. Bioeng., 2006, 94:680-688; и WO 2003/085107; каждый из которых включен посредством ссылки в полном объеме).
[0397] В некоторых вариантах осуществления, АВР, предложенный в данном документе, представляет собой агликозилированный АВР. Агликозилированный АВР может быть получен любым способом, известным в данной области техники или описанным в данном документе. В некоторых аспектах, агликозилированный АВР получают путем модифицирования АВР для удаления всех сайтов гликозилирования. В некоторых аспектах, сайты гликозилирования удаляют только из области Fc АВР. В некоторых аспектах, агликозилированный АВР получают путем экспрессии АВР в организме, который не способен к гликозилированию, такому как Е. coli, или путем экспрессии АВР в бесклеточной реакционной смеси.
[0398] В некоторых вариантах осуществления, АВР, предложенный в данном документе, имеет константную область с уменьшенной эффекторной функцией по сравнению с нативным антителом IgG1. В некоторых вариантах осуществления, аффинность константной области Fc-области АВР, представленного в данном документе, к рецептору Fc, меньше, чем аффинность нативной константной области IgG1 к такому рецептору Fc.
2.7. Варианты аминокислотной последовательности области Fc
[0399] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит область Fc с одной или больше аминокислотными заменами, вставками или делециями по сравнению с встречающейся в природе областью Fc. В некоторых аспектах, такие замены, вставки или делеции дают АВР с измененной стабильностью, гликозилированием или другими характеристиками. В некоторых аспектах, такие замены, вставки или делеции дают агликозилированные АВР.
[0400] В некоторых аспектах, область Fc АВР, предложенного в данном документе, модифицирована для получения АВР с измененной аффинностью к рецептору Fc, или АВР, который является более иммунологически нейтральным. В некоторых вариантах осуществления, варианты АВР, предложенного в данном документе, обладают некоторыми, но не всеми, эффекторными функциями. Такие АВР могут быть полезны, например, когда время полувыведения АВР являться важным in vivo, за исключением когда некоторые эффекторные функции (например, активация комплемента и АЗКЦ) являются ненужными или вредными.
[0401] В некоторых вариантах осуществления, область Fc АВР, представленного в данном документе, представляет собой область Fc IgG4 человека, содержащую одну или больше стабилизирующих шарнирную область мутаций S228P и L235E. См. Aalberse et al., Immunology, 2002, 105:9-19, включен посредством ссылки в полном объеме. В некоторых вариантах осуществления, область Fc IgG4 содержит одну или больше следующих мутаций: Е233Р, F234V и L235A. См. Armour et al., Mol. Immunol., 2003, 40:585-593, включен посредством ссылки в полном объеме В некоторых вариантах осуществления, область Fc IgG4 содержит делецию в позиции G236.
[0402] В некоторых вариантах осуществления, область Fc АВР, предложенного в данном документе, представляет собой область Fc IgG1 человека, содержащую одну или больше мутаций для снижения связывания рецептора Fc. В некоторых аспектах, одна или больше мутаций находятся в остатках, выбранных из S228 (например, S228A), L234 (например, L234A), L235 (например, L235A), D265 (например, D265A) и N297 (например, N297A). В некоторых аспектах, АВР содержит мутацию PVA236. PVA236 означает, что аминокислотная последовательность ELLG, от аминокислотной позиции 233 к 236 IgG1 или EFLG IgG4, замещена PVA. См. патент США №9150641, включен посредством ссылки в полном объеме.
[0403] В некоторых вариантах осуществления, область Fc АВР, предложенная в данном документе, является модифицированной, как описано в Armour et al., Eur. J. Immunol., 1999, 29:2613-2624; WO 1999/058572; и/или заявке на патент Великобритании №98099518; каждый из которых включен посредством ссылки в полном объеме.
[0404] В некоторых вариантах осуществления, область Fc АВР, предложенного в данном документе, представляет собой область Fc IgG2 человека, содержащую одну или больше мутаций A330S и P331S.
[0405] В некоторых вариантах осуществления, область Fc АВР, предложенного в данном документе, имеет аминокислотную замену в одной или больше позициях, выбранных из 238, 265, 269, 270, 297, 327 и 329. См. патент США №6737056, включен посредством ссылки в полном объеме. Такие Fc-мутанты включают в себя Fc-мутанты с заменами в двух или больше аминокислотных позициях 265, 269, 270, 297 и 327, включая так называемый «DANA» Fc-мутант с заменой остатков 265 и 297 на аланин. См. патент США №7332581, включен посредством ссылки в полном объеме. В некоторых вариантах осуществления, АВР содержит аланин в аминокислотной позиции 265. В некоторых вариантах осуществления, АВР содержит аланин в аминокислотной позиции 297.
[0406] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит область Fc с одной или больше аминокислотными заменами, которые улучшают АЗКЦ, например замену в одной или больше позициях 298, 333 и 334 области Fc. В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит область Fc с одной или больше аминокислотными заменами, в позициях 239, 332 и 330, как описано в Lazar et al., Proc. Natl. Acad. Sci. USA, 2006, 103:4005-4010, включен посредством ссылки в полном объеме.
[0407] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит одно или больше изменений, которые улучшают или уменьшают связывание C1q и/или CDC. См. патент США №6194551; WO 99/51642; и Idusogie et al., J. Immunol., 2000, 164:4178-4184; каждый из которых включен посредством ссылки в полном объеме.
[0408] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит одно или больше изменений для увеличения периода полувыведения. АВР с увеличенным периодом полувыведения и улучшенным связыванием с неонатальным рецептором Fc (FcRn) описаны, например, в Hinton et al., J. Immunol., 2006, 176:346-356; и публикации патента США №2005/0014934; каждый из которых включен посредством ссылки в полном объеме. Такие варианты Fc включают те, у которых замены по одному или больше остатках области Fc: 238, 250, 256, 265, 272, 286, 303, 305, 307, 311, 312, 314, 317, 340, 356, 360, 362, 376, 378, 380, 382, 413, 424, 428 и 434 IgG.
[0409] В некоторых вариантах осуществления, АВР, предложенный в данном документе, содержит один или больше вариантов области Fc, как описано в патентах США №7371826, 5648260 и 5624821; Duncan and Winter, Nature, 1988, 322:738-740; и WO 94/29351; каждый из которых включен посредством ссылки в полном объеме.
2.8. Пироглутамат
[0410] Как известно в данной области техники, как глутамат (Е), так и глутамин (Q) на N-концах рекомбинантных белков могут спонтанно циклизоваться с образованием пироглутамата (рЕ) in vitro и in vivo. См. Liu et al., J. Biol. Chem., 2011, 286:11211-11217, включен посредством ссылки в полном объеме.
[0411] В некоторых вариантах осуществления, в данном документе предложены АВР, содержащие полипептидную последовательность, имеющую остаток рЕ в N-концевой позиции. В некоторых вариантах осуществления, в данном документе предложены АВР, содержащие полипептидную последовательность, в которой N-концевой остаток был преобразован из Q в рЕ. В некоторых вариантах осуществления, в данном документе предложены АВР, содержащие полипептидную последовательность, в которой N-концевой остаток был преобразован из Е в рЕ.
[0412] В некоторых вариантах осуществления, в данном документе предложены АВР, содержащие последовательность VH, имеющую остаток рЕ в N-концевой позиции. В некоторых вариантах осуществления, в данном документе предложены АВР, содержащие последовательность VH, в которой N-концевой остаток был преобразован из Q в рЕ. В некоторых вариантах осуществления, в данном документе предложен АВР, содержащий последовательность VH, выбранную из SEQ ID NO: 4-24, причем N-концевой остаток Q был преобразован в рЕ. В некоторых вариантах осуществления, в данном документе предложенахкомпозиция, содержащая АВР, причем АВР содержит VH, выбранную из SEQ ID NO: 4-24, в которой по меньшей мере около 20%, по меньшей мере около 40%, по меньшей мере около 60%, при по меньшей мере, около 80%, по меньшей мере около 90%, по меньшей мере около 95% или по меньшей мере около 99% N-концевых остатков такой VH в такой композиции были преобразованы из Q в рЕ.
[0413] В некоторых вариантах осуществления, в данном документе предложены АВР, содержащие последовательность VL, имеющую остаток рЕ в N-концевой позиции. В некоторых вариантах осуществления, в данном документе предложены АВР, содержащие последовательность VL, в которой N-концевой остаток был преобразован из Е в рЕ. В некоторых вариантах осуществления, в данном документе предложен АВР, содержащий последовательность VL, выбранную из SEQ ID NO: 25-28, причем N-концевой остаток Е был преобразован в рЕ. В некоторых вариантах осуществления, в данном документе предложена композиция, содержащая АВР, причем АВР содержит VL, выбранную из SEQ ID NO: 25-28, в которой по меньшей мере около 20%, по меньшей мере около 40%, по меньшей мере около 60%, при по меньшей мере, около 80%, по меньшей мере около 90%, по меньшей мере около 95% или по меньшей мере около 99% N-концевых остатков такой VL в такой композиции были преобразованы из Е в рЕ.
[0414] В некоторых вариантах осуществления, в данном документе предложены АВР, содержащие последовательности тяжелой цепи, имеющие остаток рЕ в N-концевой позиции. В некоторых вариантах осуществления, в данном документе предложены АВР, содержащие последовательность тяжелой цепи, в которой N-концевой остаток был преобразован из Q в рЕ. В некоторых вариантах осуществления, в данном документе предложен АВР, содержащий последовательность тяжелой цепи, выбранную из SEQ ID NO: 79, 80, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 121, 122, 123 или 124, причем N-концевой остаток Q был преобразован в рЕ. В некоторых вариантах осуществления, в данном документе предложена композиция, содержащая АВР, причем АВР содержит тяжелую цепь, выбранную из SEQ ID NO: 79, 80, 82, 83, 84, 85, 86, 87, 88, 89, 90,91,93,94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 121, 122, 123 или 124, в которой по меньшей мере около 20%, по меньшей мере около 40%, по меньшей мере около 60%, по меньшей мере около 80%, по меньшей мере около 90%, по меньшей мере около 95% или по меньшей мере около 99% N-концевых остатков такой тяжелой цепи в такой композиции были преобразованы из Q в рЕ.
[0415] В некоторых вариантах осуществления, в данном документе предложены АВР, содержащие последовательности легкой цепи, имеющие остаток рЕ в N-концевой позиции. В некоторых вариантах осуществления, в данном документе предложены АВР, содержащие последовательность легкой цепи, в которой N-концевой остаток был преобразован из Е в рЕ. В некоторых вариантах осуществления, в данном документе предложен АВР, содержащий последовательность легкой цепи, выбранную из SEQ ID NO: 81, 92, 107 или 120, причем N-концевой остаток Е был преобразован в рЕ. В некоторых вариантах осуществления, в данном документе предложена композиция, содержащая АВР, причем АВР содержит легкую цепь, выбранную из SEQ ID NO: 81, 92, 107 или 120, в которой по меньшей мере около 20%, по меньшей мере около 40%, по меньшей мере около 60%, при по меньшей мере, около 80%, по меньшей мере около 90%, по меньшей мере около 95% или по меньшей мере около 99% N-концевых остатков такой легкой цепи в такой композиции были преобразованы из Е в рЕ.
2.9. Варианты антиген-связывающего белка с внесенным цистеином
[0416] В некоторых вариантах осуществления, в данном документе предложены АВР с внесенным цистеином, также известные как «thioMAb», в которых один или больше остатков АВР замещены остатками цистеина. В конкретных вариантах осуществления, замещенные остатки встречаются в доступных для растворителях сайтах АВР. Путем замещения таких остатков цистеином вводят реакционноспособные тиольные группы в доступные для растворителя сайты АВР, и они могут быть использованы для конъюгирования АВР с другими фрагментами, такими как лекарственные фрагменты или линкер-лекарственные фрагменты, например, для создания иммуноконъюгата.
[0417] В некоторых вариантах осуществления, любой один или большее количество из следующих остатков могут быть замещены цистеином: V205 легкой цепи; А118 области Fc тяжелой цепи; и S400 области Fc тяжелой цепи. АВР с внесенным цистеином могут быть получены, как описано, например, в патенте США №7521541, который включен посредством ссылки в полном объеме.
2.9.1. Иммуноконъюгаты
2.9.1.1. Конъюгаты антиген-связывающего белка-полимера
[0418] В некоторых вариантах осуществления, АВР, предложенный в данном документе, получают путем конъюгации с полимером. Любой подходящий полимер может быть конъюгирован с АВР.
[0419] В некоторых вариантах осуществления, полимер представляет собой водорастворимый полимер. Иллюстративные примеры водорастворимых полимеров включают в себя: полиэтиленгликоль (ПЭГ), сополимеры этиленгликоля/пропиленгликоля, карбоксиметилцеллюлозу, декстран, поливиниловый спирт, поливинилпирролидон, поли-1,3-диоксолан, поли-1,3,6-триоксан, этилен/сополимер малеинового ангидрида, полиаминокислоты (либо гомополимеры, либо случайные сополимеры), поли(н-винилпирролидон)-со-полиэтиленгликоль, гомополимеры пропиленгликоля, сополимеры полипропиленоксида/этиленоксида, полиоксиэтилированные полиолы (например, глицерин), поливиниловый спирт, и их смеси. В некоторых аспектах, пропиональдегид полиэтиленгликоля может быть полезен для производственных целей из-за его стабильности в воде.
[0420] Полимер может иметь любую молекулярную массу и может быть разветвленным или неразветвленным. Количество полимеров, прикрепленных к каждому АВР может варьировать, и если присоединено больше одного полимера, они могут быть одинаковыми полимерами или разными полимерами. В целом, как правило, количество и/или тип полимеров, используемых для дериватизации, могут быть определены на основе соображений, включающих конкретные свойства или функции АВР, которые необходимо улучшить, и предполагаемое применение АВР.
2.9.1.2. Конъюгаты антиген-связывающий белок-лекарство
[0421] В некоторых вариантах осуществления, АВР, предложенные в данном документе, конъюгируют с одним или больше терапевтическим агентом. Любой подходящий терапевтический агент может быть конъюгирован с АВР. Иллюстративные терапевтические агенты включают в себя цитокины, хемокины и другие агенты, которые индуцируют желаемую активность Т-лимфоцитов, такие как OX40L, 4-1BBL, ФНО-альфа (как используется в данном документе, «ФНО»), ИЛ-2, ИЛ-15, CXCL9, CXCL10, ловушка ИЛ-10, ловушка ИЛ-27 и ловушка ИЛ-35. Цитокиновые ловушки и их применение известны в данной области техники и описаны, например, в Economides et al., Nature Medicine, 2003, 9:47-52, включен посредством ссылки в полном объеме.
3. Способы получения белков, связывающих антиген TIGIT
3.1. Подготовка антигена TIGIT
[0422] Антиген TIGIT, используемый для выделения АВР, предложенных в данном документе, может быть интактным TIGIT или фрагментом TIGIT. Антиген TIGIT может быть, например, в виде выделенного белка или белка, экспрессируемого на поверхности клетки.
[0423] В некоторых вариантах осуществления, антиген TIGIT представляет собой не встречающийся в природе вариант TIGIT, такой как белок TIGIT, имеющий аминокислотную последовательность или посттрансляционную модификацию, которая не встречается в природе.
[0424] В некоторых вариантах осуществления, антиген TIGIT усекают путем удаления, например, внутриклеточных или трансмембранных последовательностей, или сигнальных последовательностей. В некоторых вариантах осуществления, антиген TIGIT слит на своем С-конце с доменом Fc IgGl человека или полигистидиновой меткой.
3.2. Способы получения моноклональных антител
[0425] Моноклональные антитела могут быть получены, например, с применением гибридомного способа, впервые описанного Kohler et al., Nature, 1975, 256:495-497 (включен посредством ссылки в полном объеме) и/или способами рекомбинантной ДНК (см., например, патент США №4816567, включен посредством ссылки в полном объеме). Моноклональные антитела также могут быть получены, например, с применением фаговых или дрожжевых библиотек. См., например, патенты США №8258082 и 8691730, каждый из которых включен посредством ссылки в полном объеме.
[0426] В гибридомном способе мышь или другое подходящее животное-хозяин иммунизируют для выработки лимфоцитов, которые продуцируют или способны продуцировать антитела, которые будут специфически связываться с белком, применяемым для иммунизации. В альтернативном варианте, лимфоциты могут быть иммунизированы in vitro. Затем лимфоциты гибридизируют с клетками миеломы с применением подходящего агента для гибридизации, такого как полиэтиленгликоль, с образованием гибридомной клетки. См. Goding J.W., Monoclonal Antibodies: Principles and Practice 3rd ed. (1986) Academic Press, San Diego, CA, включен посредством ссылки в полном объеме.
[0427] Гибридомные клетки высевают и выращивают в подходящей культуральной среде, которая содержит одно или больше веществ, которые ингибируют рост или выживание негибридизированных исходных миеломных клеток. Например, если в исходных миеломных клетках отсутствует фермент гипоксантин гуанинфосфорибозилтрансфераза (HGPRT или HPRT), культуральная среда для гибридом обычно будет включать в себя гипоксантин, аминоптерин и тимидин (среда HAT), которые предотвращают рост HGPRT-неполноценных клеток.
[0428] Полезными миеломными клетками являются те, которые эффективно гибридизируются, поддерживают стабильное высокоэффективное продуцирование антител выбранными продуцирующими антитела клетками, и являются чувствительными к условиям среды, таким как наличие или отсутствие среды HAT. Среди них предпочтительными линиями миеломных клеток являются мышиные миеломные линии, такие как линии, полученные из опухолей мышей МОР-21 и МС-11 (доступны в Центре распространения клеток институт Салка, Сан-Диего, Калифорния), и SP-2 или X63-Ag8-653 (доступны в Американской коллекции типовых культур, Роквилл, Мэриленд). Для производства человеческих моноклональных антител также описаны клеточные линии миеломы человека и мышино-человеческой гетеромиеломы. См., например, Kozbor, J. Immunol., 1984, 133:3001, включен посредством ссылки в полном объеме.
[0429] После идентификации гибридомных клеток, которые продуцируют антитела с желаемой специфичностью, аффинностью и/или биологической активностью, выбранные клоны могут быть субклонированы путем процедур предельного разбавления, и выращены с помощью стандартных способов. См. Goding, выше. Подходящие культуральные среды для данной цели включают в себя, например, среду D-MEM или RPMI-1640. Кроме того, гибридомные клетки можно выращивать in vivo в виде асцитных опухолей у животного.
[0430] ДНК, кодирующая моноклональные антитела, может быть легко выделена и секвенирована с применением обычных процедур (например, с применением олигонуклеотидных зондов, которые способны специфически связываться с генами, кодирующими тяжелые и легкие цепи моноклональных антител). Таким образом, гибридомные клетки могут служить полезным источником ДНК-кодирующих антител с желаемыми свойствами. ДНК после выделения может быть помещена в экспрессирующие векторы, которые затем трансфицируют в клетки-хозяева, такие как бактерии (например, Е. coli), дрожжи (например, Saccharomyces или Pichia sp.), клетки COS, клетки яичника китайского хомяка (СНО) или клетки миеломы, которые в других случаях не продуцируют антитело, для получения моноклональных антител.
3.3. Способы получения химерных антител
[0431] Иллюстративные способы получения химерных антител описаны, например, в патенте США №4816567; и Morrison et al., Proc. Natl. Acad. Sci. USA, 1984, 81:6851-6855; каждый из которых включен посредством ссылки в полном объеме. В некоторых вариантах осуществления, химерное антитело получают с применением рекомбинантных методов для комбинирования нечеловеческой вариабельной области (например, вариабельной области, полученной из мыши, крысы, хомяка, кролика или низшего примата, такого как обезьяна) с константной областью человека.
3.4. Способы получения гуманизированных антител
[0432] Гуманизированные антитела могут быть получены путем замены большинства или всех структурных частей нечеловеческого моноклонального антитела, на соответствующие последовательности антитела человека. Следовательно, получают гибридную молекулу, в которой только антигенспецифическая вариабельная область, или CDR, состоит из нечеловеческой последовательности. Способы получения гуманизированных антител включают те, которые описаны, например, в Winter and Milstein, Nature, 1991, 349:293-299; Rader et al., Proc. Nat. Acad. Sci. U.S.A., 1998, 95:8910-8915; Steinberger et al., J. Biol. Chem., 2000, 275:36073-36078; Queen et al., Proc. Natl. Acad. Sci. U.S.A., 1989, 86:10029-10033; и патентах США №5585089, 5693761, 5693762, и 6180370; каждый из которых включен посредством ссылки в полном объеме.
3.5. Способы создания человеческих антител
[0433] Человеческие антитела могут быть получены с помощью различных методов, известных в данной области техники, например, с применением трансгенных животных (например, гуманизированных мышей). См., например, Jakobovits et al., Proc. Natl. Acad. Sci. U.S.A., 1993, 90:2551; Jakobovits et al., Nature, 1993, 362:255-258; Bruggermann et al., Year in Immuno., 1993, 7:33; и патенты США №5591669, 5589369 и 5545807; каждый из которых включен посредством ссылки в полном объеме. Человеческие антитела также могут быть получены из библиотек фагового дисплея (см., например, Hoogenboom et al., J. Mol. Biol., 1991, 227:381-388; Marks et al., J. Mol. Biol., 1991, 222: 581-597; и патенты США №5565332 и 5573905; каждый из которых включен посредством ссылки в полном объеме). Человеческие антитела также могут быть продуцированы активированными in vitro В-лимфоцитами (см., например, патенты США №5567610 и 5229275, каждый из которых включен посредством ссылки в полном объеме). Человеческие антитела могут также быть получены из дрожжевых библиотек (см., например, патент США №8691730, включен посредством ссылки в полном объеме).
3.6. Способы получения фрагментов антитела
[0434] Описанные в данном документе фрагменты антител могут быть получены любым подходящим способом, включая описанные в данном документе иллюстративные способы или те, которые известны в данной области техники. Подходящие способы включают в себя рекомбинантные методы и протеолитическое расщепление целых антител. Иллюстративные способы получения фрагментов антител описаны, например, в Hudson et al., Nat. Med., 2003, 9:129-134, включен посредством ссылки в полном объеме. Способы получения антител scFv описаны, например, в  , The Pharmacology of Monoclonal Antibodies, vol. 113, Rosenburg и Moore eds., Springer-Verlag, New York, pp. 269-315 (1994); WO 93/16185; и патентах США №5571894 и 5587458; каждый из которых включен посредством ссылки в полном объеме.
, The Pharmacology of Monoclonal Antibodies, vol. 113, Rosenburg и Moore eds., Springer-Verlag, New York, pp. 269-315 (1994); WO 93/16185; и патентах США №5571894 и 5587458; каждый из которых включен посредством ссылки в полном объеме.
3.7. Способы получения альтернативных каркасов
[0435] Альтернативные каркасы, предложенные в данном документе, могут быть получены любым подходящим способом, включая описанные в данном документе иллюстративные способы или те, которые известны в данной области техники. Например, способы приготовления Adnectins™ описаны в Emanuel et al., mAbs, 2011, 3:38-48, включен посредством ссылки в полном объеме. Способы получения iMab описаны в публикации патента США №2003/0215914, включен посредством ссылки в полном объеме. Способы приготовления Anticalins® описаны в Vogt и Skerra, Chem. Biochem., 2004, 5:191-199, включен посредством ссылки в полном объеме. Способы получения доменов Куницца описаны в Wagner et al., Biochem. & Biophys. Res. Comm., 1992, 186:118-1145, включен посредством ссылки в полном объеме. Способы получения аптамеров тиоредоксинового пептида приведены в Geyer и Brent, Meth. Enzymol., 2000, 328:171-208, включен посредством ссылки в полном объеме. Способы получения аффител представлены в Fernandez, Curr. Opinion in Biotech., 2004, 15:364-373, включен посредством ссылки в полном объеме. Способы получения DARPin приведены в Zahnd et al., J. Mol. Biol., 2007, 369:1015-1028, включен посредством ссылки в полном объеме. Способы получения аффилинов приведены в работе Ebersbach et al., J. Mol. Biol., 2007, 372:172-185, включен посредством ссылки в полном объеме. Способы получения тетраэктинов приведены в Graversen et al., J. Biol. Chem., 2000, 275:37390-37396, включен посредством ссылки в полном объеме. Способы получения авимеров приведены в Silverman et al., Nature Biotech., 2005, 23:1556-1561, включен посредством ссылки в полном объеме. Способы получения финомеров приведены в Silacci et al., J. Biol. Chem., 2014, 289:14392-14398, включен посредством ссылки в полном объеме.
[0436] Дополнительная информация об альтернативных каркасах представлена в Binz et al., Nat. Biotechnol, 2005 23:1257-1268; и Skerra, Current Opin. in Biotech., 2007 18:295-304, каждый из которых включен посредством ссылки в полном объеме.
3.8. Способы получения мультиспецифических АВР
[0437] Мультиспецифические АВР, предложенные в данном документе, могут быть получены любым подходящим способом, включая описанные в данном документе иллюстративные способы или те, которые известны в данной области техники. Способы получения антител с общей легкой цепью описаны в Merchant et al., Nature Biotechnol., 1998, 16:677-681, включен посредством ссылки в полном объеме. Способы получения четырехвалентных биспецифических антител описаны в Coloma and Morrison, Nature Biotechnol., 1997, 15:159-163, включен посредством ссылки в полном объеме. Способы получения гибридных иммуноглобулинов описаны в Milstein and Cuello, Nature, 1983, 305:537-540; и Staerz and Bevan, Proc. Natl Acad. Sci. USA, 1986, 83:1453-1457; каждый из которых включен посредством ссылки в полном объеме. Способы получения иммуноглобулинов с модификацией «выступ-во-впадину» описаны в патенте США №№5731168, включен посредством ссылки в полном объеме. Способы получения иммуноглобулинов с электростатическими модификациями приведены в WO 2009/089004, включен посредством ссылки в полном объеме. Способы получения биспецифических одноцепочечных антител описаны в Traunecker et al., EMBO J., 1991, 10:3655-3659; и Gruber et al., J. Immunol., 1994, 152:5368-5374; каждый из которых включен посредством ссылки в полном объеме. Способы получения одноцепочечных антител, длина линкер которых может разнится, описаны в патентах США №4946778 и 5132405, каждый из которых включен посредством ссылки в полном объеме. Способы получения диател описаны в Hollinger et al., Proc. Natl. Acad. Sci. USA, 1993, 90:6444-6448, включен посредством ссылки в полном объеме. Способы получения триател и тетрател описаны в Todorovska et al., J. Immunol. Methods, 2001, 248:47-66, включен посредством ссылки в полном объеме. Способы получения триспецифических производных F(ab')3 описаны в Tutt et al. J. Immunol., 1991, 147:60-69, включен посредством ссылки в полном объеме. Способы получения перекрестно-сшитых антител описаны в патенте США №4676980; Brennan et al., Science, 1985, 229:81-83; Staerz, et al. Nature, 1985, 314:628-631; и ЕР 0453082; каждый из которых включен посредством ссылки в полном объеме. Способы получения антиген-связывающих доменов, собранных с помощью лейциновых зиперов, описаны в Kostelny et al., J. Immunol., 1992, 148:1547-1553, включен посредством ссылки в полном объеме. Способы получения АВР через подход DNL описаны в патентах США №7521056; 7550143; 7534866; и 7527787; каждый из которых включен посредством ссылки в полном объеме. Способы получения гибридов антител и молекул не-антител описаны в WO 93/08829, включен посредством ссылки в полном объеме, для примеров таких АВР. Способы получения антител DAF описаны в публикации патента США №2008/0069820, включен посредством ссылки в полном объеме. Способы получения АВР путем восстановления и окисления описаны в Carlring et al., PLoS One, 2011, 6:e22533, включен посредством ссылки в полном объеме. Способы получения DVD-Ig™ описаны в патенте США №7612181, включен посредством ссылки в полном объеме. Способы получения DART™ описаны в Moore et al., Blood, 2011, 117:454-451, включен посредством ссылки в полном объеме. Способы получения DuoBodies® описаны в Labrijn et al., Proc. Natl Acad. Sci. USA, 2013, 110:5145-5150; Gramer et al., mAbs, 2013, 5:962-972; и Labrijn et al., Nature Protocols, 2014, 9:2450-2463; каждый из которых включен посредством ссылки в полном объеме. Способы получения антител, содержащих scFvs, слитые с С-концом СH3 из IgG, описаны в Coloma и Morrison, Nature Biotechnol., 1997, 15:159-163, включен посредством ссылки в полном объеме. Способы получения антител, в которых молекула Fab присоединена к константной области иммуноглобулина, описаны в Miler et al., J. Immunol., 2003, 170:4854-4861, включен посредством ссылки в полном объеме. Способы получения CovX-Bodies описаны, например, в Doppalapudi et al., Proc. Natl. Acad. Sci. USA, 2010, 107:22611-22616, включен посредством ссылки в полном объеме. Способы получения антител антител Fcab описаны в Wozniak-Knopp et al., Protein Eng. Des. Sel, 2010, 23:289-297, включен посредством ссылки в полном объеме. Способы получения антител TandAb® описаны в Kipriyanov et al., J. Mol Biol., 1999, 293:41-56 и Zhukovsky et al., Blood, 2013, 122:5116, каждый из которых включен посредством ссылки в полном объеме. Способы получения тандемных Fabs описаны в WO 2015/103072, включен посредством ссылки в полном объеме. Способы получения Zybodies™ описаны в LaFleur et al., mAbs, 2013, 5:208-218, включен посредством ссылки в полном объеме.
3.9. Способы получения вариантов
[0438] В некоторых вариантах осуществления, АВР, предложенный в данном документе, представляет собой вариант исходного АВР с с созревшей аффинностью, который может быть получен, например, с применением методов аффинного созревания на основе фагового дисплея. Вкратце, один или больше остатков CDR могут быть мутированы, а варианты АВР, или их части, представлены на фаге и скринированы на аффинность. Такие изменения могут быть сделаны в «горячих точках» CDR или остатках, кодируемых кодонами, которые подвергаются мутации с высокой частотой во время процесса соматического созревания (см. Chowdhury, Methods Mol. Biol., 2008, 207:179-196, включен посредством ссылки в полном объеме) и/или остатках, которые контактируют с антигеном.
[0439] Может быть использован любой подходящий способ для внесения вариабельности в полинуклеотидную последовательность(ти), кодирующую АВР, включая вносящую ошибки ПЦР, перетасовку цепей, и олигонуклеотид-направленный мутагенез, такой как тринуклеотид-направленный мутагенез (TRIM). В некоторых аспектах, рандомизируют несколько остатков CDR (например, 4-6 остатков за раз). Остатки CDR, участвующие в связывании антигена, могут быть специфически идентифицированы, например, с применением аланинового сканирующего мутагенеза или моделирования. CDR-H3 и CDR-L3, в частности, часто являются мишенями для мутирования.
[0440] Внесения разнообразия в вариабельные области и/или CDR можно использовать для создания вторичной библиотеки. Затем вторичную библиотеку проверяют, чтобы идентифицировать варианты АВР с улучшенной аффинностью. Созревание аффинности путем конструирования и повторного отбора из вторичных библиотек было описано, например, в Hoogenboom et al., Methods in Molecular Biology, 2001, 178:1-37, включен посредством ссылки в полном объеме.
3.10. Векторы, клетки-хозяева и рекомбинантные способы
[0441] Также предложены выделенные нуклеиновые кислоты, кодирующие TIGIT АВР, векторы, содержащие нуклеиновые кислоты, и клетки-хозяева, содержащие векторы и нуклеиновые кислоты, а также рекомбинантные методы для получения АВР.
[0442] Для рекомбинантного продуцирования АВР нуклеиновая(вые) кислота(ты), кодирующая ее, может быть выделена и вставлена в реплицируемый вектор для дальнейшего клонирования (т.е. амплификации ДНК) или экспрессии. В некоторых аспектах, нуклеиновая кислота может быть получена путем гомологичной рекомбинации, например, как описано в патенте США №5204244, включен посредством ссылки в полном объеме.
[0443] В данной области техники известно много разных векторов. Компоненты вектора в целом, как правило, включают в себя одно или большее количество из следующего: сигнальную последовательность, сайт начала репликации, один или больше маркерных генов, энхансер, промотор и последовательность терминации транскрипции, например, как описано в патенте США №5534615, включен посредством ссылки в полном объеме.
[0444] Иллюстративные примеры подходящих клеток-хозяев приведены ниже. Данные клетки-хозяева не предназначены для ограничения, и любая подходящая клетка-хозяин может быть использована для получения предложенных в данном документе АВР.
[0445] Подходящие клетки-хозяева включают в себя любые прокариотические клетки (например, бактериальные), клетки низших эукариот (например, дрожжей) или клетки высших эукариот (например, млекопитающих). Подходящие прокариоты включают в себя эубактерии, такие как Грамм-негативные или Грамм-позитивные организмы, например, Enterobacteriaceae такие как Escherichia (Е. coli), Enterobacter, Erwinia, Klebsiella, Proteus, Salmonella (S. typhimurium), Serratia (S. marcescans), Shigella, Bacilli (B. subtilis и В. licheniformis), Pseudomonas (P. aeruginosa), и Streptomyces. Одним полезным клонирующим хозяином в виде Е. coli является Е. coli 294, хотя также подходят другие штаммы, такие как Е. coli В, Е. coli X1776 и Е. coli W3110.
[0446] В дополнение к прокариотам, эукариотические микробы, такие как нитчатые грибы или дрожжи, также являются подходящими клонирующими или экспрессирующими хозяевами для векторов, кодирующих TIGIT АВР. Saccharomyces cerevisiae, или обычные пекарские дрожжи, является обычно используемым микроорганизмом хозяином из низших эукариот. Однако доступны и полезны многие другие роды, виды и штаммы, такие как Schizosaccharomyces pombe, Kluyveromyces (K. lactis, K. fragilis, K. bulgaricus K. wickeramii, K. waltii, K. drosophilarum, K. thermotolerans и K. marxianus), Yarrowia, Pichia pastoris, Candida (С.albicans), Trichoderma reesia, Neurospora crassa, Schwanniomyces (S. occidentalis), и нитчатые грибы, такие как, например, Penicillium, Tolypocladium и Aspergillus (A. nidulans и A. niger).
[0447] Полезные клетки-хозяева млекопитающих включают в себя: клетки COS-7, клетки HEK293; клетки почки детеныша хомяка (ВНК); клетки яичника китайского хомячка (СНО); клетки Сертоли мыши; клетки почки африканской зеленой мартышки (VERO-76) и тому подобные.
[0448] Клетки-хозяева, используемые для получения TIGIT АВР согласно данному изобретению, могут быть культивированы в различных средах. Коммерчески доступные среды, такие как, например, F10 Хама, минимальная питательная среда (MEM), RPMI-1640 и среда Игла в модификации Дульбекко (DMEM), являются пригодными для культивирования клеток-хозяев. Кроме того, может быть использована любая среда, описанная в Ham et al., Meth. Enz., 1979, 58:44; Barnes et al., Anal. Biochem., 1980, 102:255; и патентах США №4767704, 4657866, 4927762, 4560655 и 5122469; или WO 90/03430 и WO 87/00195. Каждый из вышеуказанных источников включен в данный документ посредством ссылки в полном объеме.
[0449] Любая из этих сред может быть дополнена, по мере необходимости, гормонами и/или другими фактороми роста (такими как инсулин, трансферрин или эпидермальный фактор роста), солями (такими как хлорид натрия, кальций, магний и фосфат), буферами (такими как HEPES), нуклеотидами (такими как аденозин и тимидин), антибиотиками, микроэлементами (определяемыми как неорганические соединения, обычно присутствующими в конечных концентрациях в микромолярном диапазоне), и глюкозой или эквивалентным источником энергии. Любые другие необходимые добавки также могут быть включены в соответствующих концентрациях, которые будут известны специалистам в данной области техники.
[0450] Условия культивирования, такие как температура, рН и тому подобное, являются такими, которые ранее использовались клеткой-хозяином, отобранной для экспрессии, и будут очевидны для обычного квалифицированного специалиста.
[0451] АВР, при применении рекомбинантных методов, может быть продуцирован внутриклеточно, в периплазматическое пространство, или непосредственно секретирован в среду. Если АВР продуцируют внутриклеточно, в качестве первой стадии, нерастворимые частицы, либо клетки-хозява, либо лизированные фрагменты удаляют, например, путем центрифугирования или ультрафильтрации. Например, Carter et al. (Bio/Technology, 1992, 10:163-167, включен посредством ссылки в полном объеме) описывает процедуру выделения АВР, которые секретируются в периплазматическое пространство Е. coli. Вкратце, клеточный экстракт оттаивают в присутствии ацетата натрия (рН 3,5), ЭДТА и фенилметилсульфонилфторида (ФМСФ) в течение примерно 30 мин. Клеточный дебрис может быть удален центрифугированием.
[0452] В некоторых вариантах осуществления, АВР получают в бесклеточной системе. В некоторых аспектах, бесклеточная система представляет собой транскрипционную и трансляционную систему in vitro, как описано в Yin et al., MAbs, 2012, 4:217-225, включен посредством ссылки в полном объеме. В некоторых аспектах, бесклеточная система использует бесклеточный экстракт из эукариотической клетки или из прокариотической клетки. В некоторых аспектах, прокариотическая клетка представляет собой Е. coli. Бесклеточная экспрессия АВР может быть полезна, например, когда АВР накапливается в клетке в виде нерастворимого агрегата или когда выход продукта при периплазматической экспрессии является низким.
[0453] Когда АВР секретируется в среду, супернатанты из таких экспрессионных систем в целом, как правило, сначала концентрируют, используя коммерчески доступный фильтр для концентрации белка, например, ультрафильтрационную установку Amicon® или Millipore® Pellcon®. Ингибитор протеазы, такой как PMSF, может быть включен в любую из вышеуказанных стадий для ингибирования протеолиза, и антибиотики могут быть включены для предотвращения роста непредусмотренных загрязнителей.
[0454] Композицию АВР, полученную из клеток, можно очистить, используя, например, гидроксилапатитную хроматографию, гель-электрофорез, диализ и аффинную хроматографию, причем аффинная хроматография является особенно полезным методом очистки. Пригодность белка А в качестве аффинного лиганда зависит от вида и изотипа любого домена Fc иммуноглобулина, который присутствует в АВР. Белок А может быть использован для очистки АВР, которые содержат тяжелые цепи γ1, γ2 или γ4 человека (Lindmark et al., J. Immunol. Meth., 1983, 62:1-13, включен посредством ссылки в полном объеме). Белок G полезен для всех изотипов мыши и для γ3 человека (Guss et al., EMBO J., 1986, 5:1567-1575, включен посредством ссылки в полном объеме).
[0455] Матрица, к которой присоединен аффинный лиганд, чаще всего является агарозной, но доступны другие матрицы. Механически стабильные матрицы, такие как стекло с заданным размером пор или поли(стиролдивинил)бензол, обеспечивают более высокие скорости потока и более короткое временя обработки, чем может быть достигнуто с помощью агарозы. Если АВР содержит домен СH3, смола BakerBond АВХ® является полезной для очистки.
[0456] Также доступны другие способы очистки белка, такие как фракционирование на ионообменной колонке, осаждение этанолом, ВЭЖХ с обращенной фазой, хроматография на двуокиси кремния, хроматография на гепарине Sepharose®, хроматофокусировка, ДСН-ПААГ и осаждение сульфатом аммония, которые могут применяться специалистом в данной области техники.
[0457] После любой предварительной стадии(ий) очистки, смесь, содержащая АВР интереса и загрязняющие вещества, может быть подвергнута хроматографии с низким рН гидрофобного взаимодействия с применением буфера для элюирования при рН от около 2,5 до около 4,5, обычно при низких концентрациях соли (например, от около 0 до около 0,25 М соли).
4. Анализы
[0458] Для определения и характеристики описанных в данном документе TIGIT АВР могут быть применены различные анализы, известные в данной области техники.
4.1. Анализ связывания, конкуренции и картирования эпитопа
[0459] Специфическая антиген-связывающая активность АВР, предложенного в данном документе, может быть оценена любым подходящим способом, включая применение SPR, BLI, RIA и MSD-SET, как описано в другом месте данного раскрытия изобретения. Кроме того, антиген-связывающую активность можно оценить с помощью анализов ELISA и Вестерн-блоттинга.
[0460] Анализы для измерения конкуренции между двумя АВР, или АВР и другой молекулой (например, одним или больше лигандами TIGIT) описаны в другом месте данного раскрытия изобретения и, например, в Harlow and Lane, Antibodies: A Laboratory Manual ch.14, 1988, Cold Spring Harbor Laboratory, Cold Spring Harbor, N.Y, включен посредством ссылки в полном объеме.
[0461] Анализы для картирования эпитопов, с которыми связываются предложенные в данном документе АВР, описаны, например, в Morris "Epitope Mapping Protocols," in Methods in Molecular Biology vol. 66, 1996, Humana Press, Totowa, N.J., включен посредством ссылки в полном объеме. В некоторых вариантах осуществления, эпитоп определяют конкуренцией пептидов. В некоторых вариантах осуществления, эпитоп определяют масс-спектрометрией. В некоторых вариантах осуществления, эпитоп определяют кристаллографией.
4.2. Анализ антагонизирования TIGIT
[0462] В некоторых вариантах осуществления, проводят скрининг АВР, предложенных в данном документе, для идентификации и характеристики АВР с антагонистической активностью по отношению к TIGIT. Может применятся любой подходящий анализ для идентификации или характеристики таких АВР. В некоторых аспектах, анализ измеряет количество цитокина, секретируемого эффекторным Т-лимфоцитом, после приведения в контакт эффекторного Т-лимфоцита с АВР, предложенным в данном документе. В некоторых аспектах, цитокин выбирают из ИЛ-2, ИЛ-6, LT-α, ФНО, GM-CSF, ИНФγ и их комбинаций. В некоторых аспектах цитокин выбирают из sCD40L, VEGF, TGF-α, RANTES, PDGF-AB/BB, PDGF-AA, MIP-1β, MIP-1α, MDC (CCL22), MCP-3, MCP-1, IP-10, ИЛ-17А, ИЛ-2Rα, ИЛ-15, ИЛ-13, ИЛ-12 (p70), ИЛ-12 (p40), ИЛ-10, ИЛ-9, ИЛ-8, ИЛ-7, ИЛ-5, ИЛ-4, ИЛ-3, ИЛ-2, ИЛ-2Rα, ИЛ-1RA, ИЛ-1β, ИЛ-1α, ИНФγ, ИНФα2, GRO, GM-CSF, G-CSF, фракталкина, лиганда Flt-3, FGF-2, эотаксина, EGF и их комбинаций.
[0463] В некоторых вариантах осуществления, эффекторные клетки совместно стимулируют агонистом CD3, чтобы способствовать секреции цитокинов эффекторной клеткой. В некоторых аспектах, агонист CD3 предоставляется на субмаксимальном уровне.
[0464] В некоторых аспектах, такие анализы могут измерять пролиферацию эффекторного Т-лимфоцита после приведения в контакт эффекторного Т-лимфоцита с АВР, предложенным в данном документе. В некоторых аспектах, пролиферацию эффекторного Т-лимфоцита измеряют путем разбавления красителя (например, карбоксифлуоресцеинового диацетата сукцинимидилового эфира, CFSE), путем поглощения меченого тритием тимидина, с помощью анализов жизнеспособности люминесцентных клеток или других анализов, известных в данной области техники.
[0465] В некоторых аспектах, такие анализы могут измерять дифференциацию, производство цитокинов, жизнеспособность (например, выживание), пролиферацию или супрессивную активность регуляторного Т-лимфоцита после приведения в контакт регуляторного Т-лимфоцита с АВР, предложенным в данном документе.
[0466] В некоторых аспектах, такие анализы могут измерять цитотоксическую активность NK-клетки после приведения в контакт NK-клетки с АВР, предложенным в данном документе. В некоторых аспектах, цитотоксическую активность NK-клетки измеряют с применением анализа цитотоксичности, который количественно оценивает NK-опосредованное уничтожение клеток-мишеней (например, клеточной линии K562). См. Ann. Clin. Lab. Sci., 2012, 42:42-49, включен посредством ссылки в полном объеме.
[0467] В некоторых аспектах, такие анализы могут измерять количество гранзима В. В некоторых аспектах такие анализы могут измерять количество перфорина.
4.3. Анализы на эффекторные функции
[0468] Эффекторную функцию после обработки с помощью АВР, предложенных в данном документе, можно оценить с применением различных анализов in vitro и in vivo, известных в данной области техники, в том числе описанных в Ravetch and Kinet, Annu. Rev. Immunol., 1991, 9:457-492; патентах США №5500362, 5821337; Hellstrom et al., Proc. Nat'l Acad. Sci. USA, 1986, 83:7059-7063; Hellstrom et al., Proc. Nat'l Acad. Sci. USA, 1985, 82:1499-1502; Bruggemann et al., J. Exp. Med., 1987, 166:1351-1361; Clynes et al., Proc. Nat'l Acad. Sci. USA, 1998, 95:652-656; WO 2006/029879; WO 2005/100402; Gazzano-Santoro et al., J. Immunol. Methods, 1996, 202:163-171; Cragg et al., Blood, 2003, 101:1045-1052; Cragg et al. Blood, 2004, 103:2738-2743; и Petkova et al., Int'l. Immunol., 2006, 18:1759-1769; каждый из которых включен посредством ссылки в полном объеме.
5. Фармацевтические композиции
[0469] Предложенные в данном документе АВР могут быть приготовлены в виде любой подходящей фармацевтической композиции и введены любым подходящим способом введения. Подходящие пути введения включают, но не ограничиваются лишь этими: внутриартериальный, внутрикожный, внутримышечный, внутрибрюшинный, внутривенный, назальный, парентеральный, легочный и подкожный пути.
[0470] Фармацевтическая композиция может содержать один или больше фармацевтических наполнителей. Может быть использован любой подходящий фармацевтический наполнитель, и специалист в данной области техники может выбирать подходящие фармацевтические наполнители. Соответственно, фармацевтические наполнители, представленные ниже, предназначены для иллюстрации, а не для ограничения. Дополнительные фармацевтические наполнители включают в себя, например, те, которые описаны в Handbook of Pharmaceutical Excipients, Rowe et al. (Eds.) 6th Ed. (2009), включен посредством ссылки в полном объеме.
[0471] В некоторых вариантах осуществления, фармацевтическая композиция содержит агент антивспенивания. Может использоваться любой подходящий агент антивспенивания. В некоторых аспектах, агент антивспенивания выбирают из спирта, эфира, масла, воска, силикона, поверхностно-активного вещества и их комбинаций. В некоторых аспектах, агент антивспенивания выбирают из: минерального масла, растительного масла, этилен-бисстеарамида, парафинового воска, эфирного воска, спирта жирного ряда, длинноцепочечного жирного спирта, жирно-кислотного мыла, сложного эфира жирной кислоты, кремниевого гликоля, фторсиликона, сополимера полиэтиленгликоля и полипропиленгликоля, полидиметилсилоксанового диоксида кремния, простого эфира, октилового спирт, каприлового спирта, триолеата сорбитана, этилового спирт, 2-этилгексанола, диметикона, олеилового спирта, симетикона, и их комбинаций.
[0472] В некоторых вариантах осуществления, фармацевтическая композиция содержит сорастворитель. Иллюстративные примеры сорастворителей включают этанол, поли(этилен)гликоль, бутиленгликоль, диметилацетамид, глицерин, пропиленгликоль и их комбинации.
[0473] В некоторых вариантах осуществления, фармацевтическая композиция содержит буфер. Иллюстративные примеры буферов включают ацетат, борат, карбонат, лактат, малат, фосфат, цитрат, гидроксид, диэтаноламин, моноэтаноламин, глицин, метионин, гуаровую камедь, глутамат натрия и их комбинации.
[0474] В некоторых вариантах осуществления, фармацевтическая композиция содержит переносчик или наполнитель. Иллюстративные примеры переносчиков или наполнителей включают лактозу, мальтодекстрин, маннит, сорбит, хитозан, стеариновую кислоту, ксантановую камедь, гуаровую камедь и их комбинации.
[0475] В некоторых вариантах осуществления, фармацевтическая композиция содержит поверхностно-активное вещество. Иллюстративные примеры поверхностно-активных веществ включают в себя: d-альфа-токоферол, бензалконийхлорид, бензетонийхлорид, цетримид, цетилпиридинийхлорид, докузат натрия, глицерилбегенат, глицерилмоноолеат, лауриновую кислоту, макрогол 15 гидроксистеарат, миристиловый спирт, фосфолипиды, полиоксиэтиленалкиловые эфиры, сложные эфиры полиоксиэтиленсорбитан-жирной кислоты, полиоксиэтиленстеараты, полиоксиглицериды, лаурилсульфат натрия, сложные эфиры сорбита, полиэтилен(гликоль) витамина Е и их комбинации.
[0476] В некоторых вариантах осуществления, фармацевтическая композиция содержит агент, предотвращающий слеживание. Иллюстративные примеры агентов антислеживания включают фосфат кальция (трехосновный), гидроксиметилцеллюлозу, гидроксипропилцеллюлозу, оксид магния и их комбинации.
[0477] Другие наполнители, которые могут быть использованы с фармацевтическими композициями, включают, например, альбумин, антиоксиданты, антибактериальные агенты, противогрибковые агенты, биологически абсорбируемые полимеры, хелатирующие агенты, вещества с контролируемым высвобождением, разбавители, диспергирующие агенты, усилители растворения, эмульгаторы, гелеобразователи, мазевые основы, усилители проникновения, консерванты, солюбилизирующие агенты, растворители, стабилизирующие агенты, сахара и их комбинаций. Конкретные примеры каждого из этих агентов описаны, например, в Handbook of Pharmaceutical Excipients, Rowe et al. (Eds.) 6th Ed. (2009), The Pharmaceutical Press, включен посредством ссылки в полном объеме.
[0478] В некоторых вариантах осуществления, фармацевтическая композиция содержит растворитель. В некоторых аспектах, растворитель представляет собой солевой раствор, такой как стерильный изотонический солевой раствор или раствор декстрозы. В некоторых аспектах, растворителем является вода для инъекций.
[0479] В некоторых вариантах осуществления, фармацевтические композиции находятся в форме частиц, таких как микрочастица или наночастица. Микрочастицы и наночастицы могут быть сформированы из любого подходящего материала, такого как полимер или липид. В некоторых аспектах, микрочастицы или наночастицы представляют собой мицеллы, липосомы или полимеры.
[0480] Дополнительно в данном документе предложены безводные фармацевтические композиции и лекарственные формы, содержащие АВР, поскольку вода может способствовать деградации некоторых АВР.
[0481] Безводные фармацевтические композиции и лекарственные формы, предложенные в данном документе, могут быть получены с применением безводных или низкомолекулярных ингредиентов и условий низкой влажности или низкой влажности воздуха. Фармацевтические композиции и лекарственные формы, которые содержат лактозу и по меньшей мере один активный ингредиент, который содержит первичный или вторичный амин, могут быть безводными, если ожидается значительный контакт с влагой и/или влагой воздуха во время изготовления, упаковки и/или хранения.
[0482] Безводную фармацевтическую композицию следует готовить и хранить таким образом, чтобы поддерживался ее безводный характер. Соответственно, безводные композиции могут быть упакованы с применением материалов, известных как предотвращающие воздействие воды, так что они могут быть включены в подходящие наборы составов. Примеры подходящей упаковки включают, но не ограничиваются лишь этими: герметически закрытые пленки, пластмассы, контейнеры с единичной дозой (например, флаконы), блистерные упаковки и контурные упаковки ленточного типа.
5.1. Парентеральные лекарственные формы
[0483] В некоторых вариантах осуществления, АВР, предложенные в данном документе, приготовлены в виде парентеральных лекарственных форм. Парентеральные лекарственные формы могут вводиться субъектам различными путями, включая, но не ограничиваясь лишь этими: подкожно, внутривенно (включая Инфузии и болюсные инъекции), внутримышечно и внутриартериально. Поскольку их введение обычно обходит естественную защиту субъектов от загрязняющих веществ, парентеральные лекарственные формы обычно являются стерильными или пригодными для стерилизации перед введением субъекту. Примеры парентеральных лекарственных форм включают, но не ограничиваются лишь этими: растворы, готовые для инъекций, сухие (например, лиофилизированные) продукты, готовые к растворению или суспендированию в фармацевтически приемлемом носителе для инъекций, суспензии, готовые для инъекций, и эмульсии.
[0484] Подходящие наполнители, которые могут использоваться для получения парентеральных лекарственных форм, хорошо известны специалистам в данной области техники. Примеры включают, но не ограничиваются лишь этими: вода для инъекций USP; водные наполнители, такие как, но не ограничены этими, физиологический раствор для инъекций, раствор Рингера для инъекций, раствор декстрозы для инъекций, раствор декстрозы и физиологический раствор для инъекций, раствор Рингера с лактатом для инъекций; смешивающиеся с водой наполнители, такие как, но не ограничены этими, этиловый спирт, полиэтиленгликоль и полипропиленгликоль; и неводные наполнители, такие как, но не ограничены этими, кукурузное масло, хлопковое масло, арахисовое масло, кунжутное масло, этилолеат, изопропилмиристат и бензилбензоат.
[0485] Наполнители, которые увеличивают растворимость одного или большего количества из АВР, описанных в данном документе, также могут быть включены в парентеральные лекарственные формы.
[0486] В некоторых вариантах осуществления, парентеральную лекарственную форму лиофилизируют. Типичные лиофилизированные составы описаны, например, в патентах США №6267958 и 6171586; и WO 2006/044908; каждый из которых включен посредством ссылки в полном объеме.
6. Дозировка и единичные лекарственные формы
[0487] В терапии человека врач определит, какое дозирование он считает наиболее подходящим в соответствии с профилактическим лечением или лечением до полного излечения, и в соответствии с возрастом, весом, состоянием и другими факторами, характерными для подлежащего лечению субъекта.
[0488] В некоторых вариантах осуществления, композиция, предложенная в данном документе, представляет собой фармацевтическую композицию или однократную единичную лекарственную форму. Фармацевтические композиции и однократные единичные лекарственные формы, предложенные в данном документе, содержат профилактически или терапевтически эффективное количество одного или большего количества профилактических или терапевтических АВР.
[0489] Количество АВР или композиции, которое будет эффективным при профилактике или лечении патологии, или одного или большего количества симптомов, будет изменятся в зависимости от характера и тяжести заболевания или патологии, и от способа, которым вводится АВР. Частота и дозировка также будут изменятся в зависимости от факторов, специфичных для каждого субъекта, в зависимости от конкретной терапии (например, лекарственных или профилактических средств), тяжести заболевания, заболевания или патологии, пути введения, а также возраста, тела, веса, реакции на лечение и прошлой истории болезни субъекта. Эффективные дозы могут быть экстраполированы из кривых доза-ответ, полученных из тест-систем in vitro или животных.
[0490] В некоторых вариантах осуществления, иллюстративные дозы композиции включают количество АВР в миллиграммах или микрограммах на килограмм массы субъекта или взвешенного образца (например, от около 10 микрограммов на килограмм до около 50 миллиграммов на килограмм, от около 100 микрограммов на килограмм до около 25 миллиграммов на килограмм, или около 100 мкг/кг до около 10 миллиграммов на килограмм). В определенном варианте осуществления, дозировка АВР, предложенного в данном документе, исходя из массы АВР, вводимого для предотвращения, лечения, контроля или облегчения патологии, или одного или большего количества ее симптомов у субъекта составляет 0,1 мг/кг, 1 мг/кг, 2 мг/кг, 3 мг/кг, 4 мг/кг, 5 мг/кг, 6 мг/кг, 10 мг/кг или 15 мг/кг или больше для массы тела пациента. В некоторых случаях может потребоваться применение доз АВР вне диапазонов, описанных в данном документе, как это будет очевидно специалистам в данной области техники. Кроме того, отмечается, что врач-клиницист или лечащий врач будет знать, как и когда прерывать, корректировать или прекращать лечение в сочетании с реакцией субъекта на лечение.
[0491] Различные терапевтически эффективные количества могут быть применимы к различным заболеваниям и патологиям, как это явно будет известно специалистам в данной области техники. Аналогичным образом, количества, достаточные для предотвращения, контроля, лечения или облегчения таких нарушений, но недостаточные для того, чтобы вызвать неблагоприятные эффекты, или достаточные для снижения неблагоприятных эффектов, связанных с АВР, предложенными в данном документе, также охватываются дозированными количествами и расписаниями частоты введения доз, предложенными в данном документе. Кроме того, когда субъекту вводят множество доз композиции, предложенной в данном документе, не все дозы должны быть одинаковыми. Например, дозировка, вводимая субъекту, может быть увеличена для улучшения профилактического или лечебного эффекта композиции, или может быть уменьшена для уменьшения одного или нескольких побочных эффектов, которые испытывает конкретный субъект.
[0492] В некоторых вариантах осуществления, лечение или профилактику можно инициировать с помощью одной или большего количества нагрузочных доз АВР или композиции, представленного(ной) в данном документе, за которой(ыми) следует одна или больше поддерживающих доз.
[0493] В некоторых вариантах осуществления, доза АВР или композиции, предложенного(ной) в данном документе, может быть введена для достижения стационарной концентрации АВР в крови или сыворотке субъекта. Стационарная концентрация может быть определена путем измерения в соответствии с методами, доступными специалистам, или может быть основана на физических характеристиках субъекта, таких как рост, вес и возраст.
[0494] В некоторых вариантах осуществления, введение одной и той же композиции может повторяться, и введения могут быть разделены по меньшей мере 1 днем, 2 днями, 3 днями, 5 днями, 10 днями, 15 днями, 30 днями, 45 днями, 2 месяцами, 75 днями, 3 месяцами или 6 месяцами.
[0495] Как обсуждалось более подробно в другом месте данного раскрытия изобретения, АВР, предложенный в данном документе, необязательно может быть введен с одним или большим дополнительными агентами, полезными для предотвращения или лечения заболевания или патологии. Эффективное количество таких дополнительных агентов может зависеть от количества АВР, присутствующего в препарате, типа нарушения, или лечения, и других факторов, известных в данной области техники или описанных в данном документе.
7. Терапевтические применения
[0496] Для терапевтических применений АВР по изобретению вводят млекопитающему, в целом, как правило, человеку, в фармацевтически приемлемой лекарственной форме, такой как известные в данной области техники и таких, которые обсуждались выше. Например, АВР по изобретению может быть введено человеку внутривенно в виде болюса или путем непрерывной инфузии в течение определенного периода времени, внутримышечным, внутрибрюшинным, внутриспинномозговым, подкожным, внутрисуставным, внутрисиновиальным, интратекальным или внутриматочным путями. АВР также пригодны для введения околоопухолевым, внутриочаговым или околоочаговым путями, чтобы оказывать местный, а также системный лечебные эффекты. Внутрибрюшинный путь может быть особенно полезен, например, при лечении опухолей яичников.
[0497] АВР, предложенные в данном документе, могут быть полезны для лечения любого заболевания или патологии с участием TIGIT. В некоторых вариантах осуществления, заболевание или патология представляет собой заболевание или патологию, которые могут быть полезны при лечении анти-TIGIT АВР. В некоторых вариантах осуществления, заболевание или патология представляет собой опухоль. В некоторых вариантах осуществления, заболевание или патология является клеточным пролиферативным нарушением. В некоторых вариантах осуществления, заболевание или патология представляет собой рак. В некоторых вариантах осуществления, заболевание или патология представляет собой вирусную инфекцию.
[0498] В некоторых вариантах осуществления, АВР, предложенные в данном документе, предназначены для применения в качестве терапевтического агента. В некоторых вариантах осуществления, АВР, предложенные в данном документе, предложены для применения при изготовлении или приготовлении терапевтического агента. В некоторых вариантах осуществления, терапевтический агент предназначен для лечения заболевания или патологии, которое может получить благоприятный эффект от анти-TIGIT АВР. В некоторых вариантах осуществления, заболевание или патология представляет собой опухоль. В некоторых вариантах осуществления, заболевание или патология является клеточным пролиферативным нарушением. В некоторых вариантах осуществления, заболевание или патология представляет собой рак. В некоторых вариантах осуществления, заболевание или патология представляет собой вирусную инфекцию.
[0499] В некоторых вариантах осуществления, в данном документе предложен способ лечения заболевания или патологии у субъекта, нуждающегося в этом, путем введения субъекту эффективного количества АВР, предложенного в данном документе. В некоторых аспектах, заболевание или патология представляет собой рак. В некоторых аспектах, заболевание или патология представляет собой вирусную инфекцию.
[0500] Любой подходящий рак можно лечить с помощью АВР, предложенных в данном документе. Иллюстративные подходящие для лечения виды рака включают в себя, например: острый лимфобластный лейкоз (ALL), острый миелоидный лейкоз (AML), адренокортикальный рак, анальный рак, рак аппендикса, астроцитому, базально-клеточный рак, опухоль головного мозга, рак желчных протоков, рак мочевого пузыря, рак молочной железы, бронхиальную опухоль, карцинома с неизвестным первичным происхождением, опухоль сердца, рак шейки матки, хордому, рак толстой кишки, колоректальный рак, краниофарингиому, протоковую карциному, эмбриональную опухоль, рак эндометрия, эпендимому, рак пищевода, эстезионейробластому, фиброзную гистиоцитому, саркому Юинга, рак толстой кишки, рак голени, рак желчного пузыря, рак желудка, рак желудочно-кишечного тракта, желудочно-кишечную стромальную опухоль, гестационный трофобластный рак, глиому, рак головы и шеи, гепатоцеллюлярный рак, гистиоцитоз, лимфому Ходжкина, рак гипофарингеальной системы, внутриглазную меланому, опухоль островковых клеток, саркому Капоши, рак почки, гистиоцитоз клеток Лангерганса, рак гортани, рак губ и ротовой полости, рак печени, рак легкого, макроглобулинемию, злокачественную фиброзную гистиоцитому, меланому, карциному клеток Меркель, мезотелиому, метастатический плоскоклеточный рак шеи с скрытым первичным происхождением, карциному срединной линии с участием гена NUT, рак полости рта, синдром множественной эндокринной неоплазии, множественную миелому, грибовидный микоз, миелодиспластический синдром, миелодиспластическое/миелопролиферативное новообразование, рак полости носа и носовой пазухи, рак носоглотки, нейробластому, немелкоклеточный рак легких, ротоглоточный рак, остеосаркому, рак яичников, рак поджелудочной железы, папилломатоз, параганглиому, рак паращитовидной железы, рак полового члена, фарингеальный рак, феохромоцитому, опухоль гипофиза, плевролегочную бластому, первичную лимфому центральной нервной системы, рак простаты, ректальный рак, рак почечной лоханки и мочеточника, ретинобластому, рабдоидную опухоль, рак слюнной железы, синдром Сезари, рак кожи, мелкоклеточный рак легкого, рак тонкой кишки, саркому мягких тканей, опухоль спинного мозга, рак желудка, Т-лимфоцитарную лимфому, тератоидную опухоль, рак яичек, рак горла, тимому и рак щитовидной железы, рак щитовидной железы, рак уретры, рак матки, рак влагалища, рак вульвы и опухоль Вильмса.
[0501] Любой подходящий вирус можно лечить с помощью АВР, предложенных в данном документе. Иллюстративные, подходящие для лечения вирусы включают в себя, например: адено-ассоциированный вирус, вирус Айчи, лизавирус австралийских летучих мышей, полиомавирус ВК, вирус Банна, вирус леса Барма, вирус Баньямвера, Bunyavirus La Crosse, Bunyavirus малого зайца-беляка, герпес вируса Cercopithecine, вирус Чандипура, вирус Чикунгунья, Косавирус А, вирус коровьей оспы, вирус Коксаки, вирус конго-крымской геморрагической лихорадки, вирус Денге, вирус Дори, вирус Дагбе, вирус Дювенхаге, вирус восточного энцефалита лошадей, эболавирус, эховирус, вирус энцефаломиокардита, вирус Эпштейна-Барра, лизавирус эвропейских литучих мышей, GB вирус С/вирус гепатита G, вирус Хантана, вирус Гендра, вирус гепатита А, вирус гепатита В, вирус гепатита С, вирус гепатита Е, вирус гепатита дельта, оспа лошадей, аденовирус человека, астровирус человека, коронавирус человека, цитомегаловирус человека, энтеровирус человека, вирус герпеса 1 человека, вирус герпеса 2 человека, вирус герпеса 6 человека, вирус герпеса 7 человека, вирус герпеса 8 человека, вирус иммунодефицита человека, папилломавирус 1 человека, папилломавирус 2 человека, папилломавирус человека, парагрипп человека, парвовирус В19 человека, респираторно-синцитиальный вирус человека, риновирус человека, вируса SARS человека, спумаретровирус человека, Т-лимфотропный вирус человека, торовирус человека, вирус гриппа А, вирус гриппа В, вирус гриппа С, вирус Исфхана, вирус полиомиелита JC, вирус японского энцефалита, аренавирус Джунина, вируса полиомиелита KI, вирус Куниджин, вирус лагской летучей мыши, марбургвирус озера Виктория, Langat virus, вируса Ласса, вируса Лордсдейл, вирусный энцефаломиелит овец, вирус лимфоцитарного хориоменингита, вируса Мачупо, вируса Майаро, коронавирус MERS, вирус кори, вируса энцефаломиокардита Мендо, вирус энцефаломиокардита Меркеля, вируса Мокола, вирус контагиозного моллюска, вирус оспы обезьян, вирус эпидемического паротита, вирус энцефалита долины Мерри, вирус Нью-Йорка, вирус Нипа, вируса Норуолк, вирус 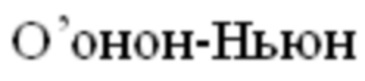 , вирус Орфа, вирус Оропуша, вирус Пичинде, полиовирус, фребовирус Пунта торо, вирус Пуумала, вирус бешенства, вирус лихорадки Рифт-Валли, розавирус А, вирус Росса-ривер, ротавирус А, ротавирус В, ротавирус С, вирус краснухи, вирус Сагиама, саливирус А, Сицилийский вирус москитной лихорадки, вирус Саппоро, вирус леса Семлики, вирус Сеула, вирус пенистости обезьян, вирус 5 обезьян, вирус Синдбис, вирус Саутгемптона, вирус энцефалита Сент-Луиса, переносимый клещами вирус повассан, вирус гепатита TTV, вирус Тосканы, вирус Укунимими, вирус коровьей оспы, вирус ветряной оспы, вирус натуральной оспы, вирус венесуэльского энцефалита лошадей, вирус везикулярного стоматита, вирус западного энцефалита лошадей, полиомавирус WU, вирус западного Нила, вирус опухоли обезьяны Яба, вирус, подобный болезни Яба, вирус желтой лихорадки и вирус Зики.
, вирус Орфа, вирус Оропуша, вирус Пичинде, полиовирус, фребовирус Пунта торо, вирус Пуумала, вирус бешенства, вирус лихорадки Рифт-Валли, розавирус А, вирус Росса-ривер, ротавирус А, ротавирус В, ротавирус С, вирус краснухи, вирус Сагиама, саливирус А, Сицилийский вирус москитной лихорадки, вирус Саппоро, вирус леса Семлики, вирус Сеула, вирус пенистости обезьян, вирус 5 обезьян, вирус Синдбис, вирус Саутгемптона, вирус энцефалита Сент-Луиса, переносимый клещами вирус повассан, вирус гепатита TTV, вирус Тосканы, вирус Укунимими, вирус коровьей оспы, вирус ветряной оспы, вирус натуральной оспы, вирус венесуэльского энцефалита лошадей, вирус везикулярного стоматита, вирус западного энцефалита лошадей, полиомавирус WU, вирус западного Нила, вирус опухоли обезьяны Яба, вирус, подобный болезни Яба, вирус желтой лихорадки и вирус Зики.
[0502] В некоторых вариантах осуществления, в данном документе предложен способ антагонизирования TIGIT в клетке-мишени субъекта, нуждающегося в этом, путем введения субъекту эффективного количества АВР, предложенного в данном документе. В некоторых аспектах, антагонизирование TIGIT с помощью АВР, предложенного в данном документе, приводит к увеличению секреции клеткой-мишенью ИЛ-2, LT-α, ИЛ-6, ФНО, GM-CSF, ИНФγ или их комбинаций.
[0503] В некоторых вариантах осуществления, в данном документе предложен способ увеличения пролиферации, выживания, и/или функции эффекторного Т-лимфоцита у субъекта, нуждающегося в этом, путем введения субъекту эффективного количества АВР, предложенного в данном документе. В некоторых аспектах, эффекторный Т-лимфоцит представляет собой эффекторный CD4+ Т-лимфоцит. В некоторых аспектах, эффекторный Т-лимфоцит представляет собой эффекторный CD8+ Т-лимфоцит.
[0504] В некоторых вариантах осуществления, в данном документе предложен способ подавления супрессии эффекторного Т-лимфоцита регуляторным Т-лимфоцитом у субъекта, нуждающегося в этом, путем введения субъекту эффективного количества АВР, предложенного в данном документе. В некоторых аспектах, регуляторный Т-лимфоцит представляет собой CD4+CD25+Foxp3+ регуляторный Т-лимфоцит. В некоторых аспектах, регуляторный Т-лимфоцит представляет собой CD8+CD25+ регуляторный Т-лимфоцит.
[0505] В некоторых вариантах осуществления, в данном документе предложен способ увеличения активности клетки естественного киллера (NK) или Т-лимфоцита натурального киллера (NKT) у субъекта, нуждающегося в этом, путем введения субъекту эффективного количества АВР, предложенного в данном документе.
[0506] В некоторых вариантах осуществления, в данном документе предложен способ стимуляции иммунного ответа у субъекта, нуждающегося в этом, путем введения субъекту эффективного количества АВР, предложенного в данном документе.
[0507] В некоторых вариантах осуществления, в данном документе предложен способ задержки начала возникновения опухоли у субъекта, нуждающегося в этом, путем введения субъекту эффективного количества АВР, предложенного в данном документе.
[0508] В некоторых вариантах осуществления, в данном документе предложен способ предотвращения начала возникновения опухоли у субъекта, нуждающегося в этом, путем введения субъекту эффективного количества АВР, предложенного в данном документе.
[0509] В некоторых вариантах осуществления, в данном документе предложен способ задержки начала возникновения рака у субъекта, нуждающегося в этом, путем введения субъекту эффективного количества АВР, предложенного в данном документе.
[0510] В некоторых вариантах осуществления, в данном документе предложен способ предотвращения начала возникновения рака у субъекта, нуждающегося в этом, путем введения субъекту эффективного количества АВР, предложенного в данном документе.
[0511] В некоторых вариантах осуществления, в данном документе предложен способ уменьшения размера опухоли у субъекта, нуждающегося в этом, путем введения субъекту эффективного количества АВР, предложенного в данном документе.
[0512] В некоторых вариантах осуществления, в данном документе предложен способ уменьшения числа метастаз у субъекта, нуждающегося в этом, путем введения субъекту эффективного количества АВР, предложенного в данном документе.
[0513] В некоторых вариантах осуществления, в данном документе предложен способ задержки начала проявления вирусной инфекции у субъекта, нуждающегося в этом, путем введения субъекту эффективного количества АВР, предложенного в данном документе.
[0514] В некоторых вариантах осуществления, в данном документе предложен способ предотвращения начала проявления вирусной инфекции у субъекта, нуждающегося в этом, путем введения субъекту эффективного количества АВР, предложенного в данном документе.
[0515] В некоторых вариантах осуществления, в данном документе предложен способ уменьшения вирусного титра у субъекта, нуждающегося в этом, путем введения субъекту эффективного количества АВР, предложенного в данном документе.
[0516] В некоторых вариантах осуществления, в данном документе предложен способ удаления вируса из субъекта, нуждающегося в этом, путем введения субъекту эффективного количества АВР, предложенного в данном документе.
[0517] В некоторых вариантах осуществления, в данном документе предложен способ для продления периода общего выживания, среднего времени выживания, или выживания без прогрессирования у субъекта, нуждающегося в этом, путем введения субъекту эффективного количества АВР, предложенного в данном документе.
[0518] В некоторых вариантах осуществления, в данном документе предложен способ лечения субъекта, у которого возникла стойкость к лекарственному препарату стандартного лечения, путем введения субъекту эффективного количества АВР, предложенного в данном документе. В некоторых вариантах осуществления, лекарственный препарат стандартного лечения, к которому субъект стал устойчивым, является ингибитором PD-1. В некоторых вариантах осуществления, лекарственный препарат стандартного лечения, к которому субъект стал устойчивым, является ингибитором PD-L1. В некоторых вариантах осуществления, лекарственный препарат стандартного лечения, к которому субъект стал устойчивым, является ингибитором CTLA-4.
8. Комплексное лечение
[0519] В некоторых вариантах осуществления АВР, предложенный в данном документе, вводят, по меньшей мере, с одним дополнительным терапевтическим агентом. Любой подходящий дополнительный терапевтический агент можно вводить с АВР, предложенным в данном документе. В некоторых аспектах, дополнительный терапевтический агент выбирают из: излучения, цитотоксического агента, химиотерапевтического агента, цитостатического агента, антигормонального агента, ингибитора EGFR, иммуностимулирующего агента, антиангиогенного агента и их комбинаций.
[0520] В некоторых вариантах осуществления, дополнительный терапевтический агент содержит иммуностимулирующий агент.
[0521] В некоторых вариантах осуществления, иммуностимулирующим агентом является агент, который блокирует сигналинг ингибирующего рецептора иммунной клетки или его лиганд. В некоторых аспектах, ингибирующий рецептор или лиганд выбирают из CTLA-4, PD-1, PD-L1, LAG-3, Tim3, TIGIT, нейритина, BTLA, KIR и их комбинаций. В некоторых аспектах, агент выбирают из анти-PD-1 анитела (например, пембролизумаба или ниволумаба) и анти-PD-L1 антитела (например, атезолизумаба), анти-СТLA-4 антитела (например, ипилимумаба), и их комбинаций. В некоторых аспектах, агент представляет собой пембролизумаб. В некоторых аспектах, агент представляет собой ниволумаб. В некоторых аспектах, агент представляет собой атезолизумаб.
[0522] В некоторых вариантах осуществления, дополнительный терапевтический агент является агентом, который ингибирует взаимодействие между PD-1 и PD-L1. В некоторых аспектах, дополнительный терапевтический агент, который ингибирует взаимодействие между PD-1 и PD-L1, выбирают из антитела, пептидомиметика и малой молекулы. В некоторых вариантах осуществления, дополнительный терапевтический агент, который ингибирует взаимодействие между PD-1 и PD-L1, выбирают из пембролизумаба, ниволумаба, атезолизумаба, авелумаба, дурвалаумаба, BMS-936559, сульфамономэтоксина 1 и сульфаметизола 2. В некоторых вариантах осуществления, дополнительный терапевтический агент, который ингибирует взаимодействие между PD-1 и PD-L1, представляет собой любой лекарственный препарат, известный в данной области техники, имеющий такую активность, например, как описано в Weinmann et al., Chem Med Chem, 2016, 14:1576 (DOI: 10.1002/cmdc.201500566), включен посредством ссылки в полном объеме. В некоторых вариантах осуществления, агент, который ингибирует взаимодействие между PD-1 и PD-L1, входит в состав той же фармацевтической композиции, что и АВР. В некоторых вариантах осуществления, агент, который ингибирует взаимодействие между PD-1 и PD-L1, входит в состав другой фармацевтической композиции, отличающейся от композиции с АВР, предложенным в данном документе. В некоторых вариантах осуществления, агент, который ингибирует взаимодействие между PD-1 и PD-L1, вводят перед введением АВР, предложенного в данном документе. В некоторых вариантах осуществления, агент, который ингибирует взаимодействие между PD-1 и PD-L1, вводят после введения АВР, предложенного в данном документе. В некоторых вариантах осуществления, агент, который ингибирует взаимодействие между PD-1 и PD-L1, вводят одновременно с АВР, предложенным в данном документе, но агент и АВР вводят в раздельных фармацевтических композициях.
[0523] В некоторых вариантах осуществления, иммуностимулирующий агент является агонистом ко-стимулирующего рецептора иммунной клетки. В некоторых аспектах, ко-стимулирующий рецептор выбирают из ОХ40, ICOS, CD27, CD28, 4-1 ВВ или CD40. В некоторых вариантах осуществления, агонист представляет собой антитело.
[0524] В некоторых вариантах осуществления, иммуностимулирующим агентом является цитокин. В некоторых аспектах, цитокин выбран из ИЛ-2, ИЛ-5, ИЛ-7, ИЛ-12, ИЛ-15, ИЛ-21 и их комбинаций.
[0525] В некоторых вариантах осуществления, иммуностимулирующим агентом является онколитический вирус. В некоторых аспектах, онколитический вирус выбирают из вируса простого герпеса, вируса везикулярного стоматита, аденовируса, вируса болезни Ньюкасла, вируса коровьей оспы и вируса марабы.
[0526] В некоторых вариантах осуществления, иммуностимулирующим агентом является Т-лимфоцит с химерным антигенным рецептором (CAR-T-лимфоцит). В некоторых вариантах осуществления, иммуностимулирующим агентом является би- или мультиспецифическое антитело, направленное на Т-лимфоцит. В некоторых вариантах осуществления, иммуностимулирующим агентом является анти-TGF-β антитело. В некоторых вариантах осуществления, иммуностимулирующим агентом является ловушка TGF-β.
[0527] В некоторых вариантах осуществления, дополнительный терапевтический агент представляет собой вакцину к опухолевому антигену. Любой подходящий антиген может быть мишенью вакцины при условии, что он присутствует в опухоли, обработанной способами, предложенными в данном документе. В некоторых аспектах, опухолевой антиген представляет собой опухолевый антиген, который сверхэкспрессируется в сравнении с его уровнями экспрессии в нормальной ткани. В некоторых аспектах, опухолевой антиген выбирают из антигена рака яичка, антигена дифференциации, NY-ESO-1, MAGE-A1, MART и их комбинаций.
[0528] Другие примеры дополнительных терапевтических агентов включают в себя: таксан (например, паклитаксел или доцетаксел); платиновый агент (например, карбоплатин, оксалиплатин и/или цисплатин); ингибитор топоизомеразы (например, иринотекан, топотекан, этопозид и/или митоксантрон); фолиновую кислоту (например, лейковорин); или нуклеозидный метаболический ингибитор (например, фторурацил, капецитабин и/или гемцитабин). В некоторых вариантах осуществления, дополнительным терапевтическим агентом является фолиновая кислота, 5-фторурацил и/или оксалиплатин. В некоторых вариантах осуществления, дополнительный терапевтический агент представляет собой 5-фторурацил и иринотекан. В некоторых вариантах осуществления, дополнительный терапевтический агент представляет собой таксан и платиновый агент. В некоторых вариантах осуществления, дополнительным терапевтическим средством является паклитаксел и карбоплатин. В некоторых вариантах осуществления, дополнительным терапевтическим агентом является пеметрексат. В некоторых вариантах осуществления, дополнительный терапевтический агент представляет собой целевой терапевтический агент, такой как EGFR, RAF или MEK-целевой агент.
[0529] Дополнительный терапевтический агент может быть введен любым подходящим способом. В некоторых вариантах осуществления, АВР, предложенный в данном документе, и дополнительный терапевтический агент включены в одну и ту же фармацевтическую композицию. В некоторых вариантах осуществления, АВР, предложенный в данном документе, и дополнительный терапевтический агент включены в различные фармацевтические композиции.
[0530] В вариантах осуществления, где АВР, предложенный в данном документе, и дополнительный терапевтический агент включены в различные фармацевтические композиции, введение АВР может происходить до, одновременно и/или после введения дополнительного терапевтического агента. В некоторых аспектах, введение АВР, предложенного в данном документе, и дополнительного терапевтического агента происходит в течение примерно около одного месяца друг от друга. В некоторых аспектах, введение АВР, предложенного в данном документе, и дополнительного терапевтического агента происходит в течение примерно около одной недели друг от друга. В некоторых аспектах, введение АВР, предложенного в данном документе, и дополнительного терапевтического агента происходит в течение примерно около одного дня друг от друга. В некоторых аспектах, введение АВР, предложенного в данном документе, и дополнительного терапевтического агента происходит в течение примерно около двенадцати часов друг от друга. В некоторых аспектах, введение АВР, предложенного в данном документе, и дополнительного терапевтического агента происходит в течение примерно около одного часа друг от друга.
9. Способы диагностики
[0531] Также предложены способы обнаружения присутствия TIGIT на клетках из субъекта. Такие способы могут быть использованы, например, для прогнозирования и оценки реакции на лечение с помощью АВР, предложенного в данном документе.
[0532] В некоторых вариантах осуществления, образец крови получают из субъекта и определяют фракцию клеток, экспрессирующих TIGIT. В некоторых аспектах, определяют относительное количество TIGIT, экспрессирванного такими клетками. Фракция клеток, экспрессирующих TIGIT, и относительное количество TIGIT, экспрессированное такими клетками, могут быть определены любым подходящим способом. В некоторых вариантах осуществления, применяют проточную цитометрию для проведения таких измерений. В некоторых вариантах осуществления, для проведения такого измерения применяют сортировку клеток с помощью флуоресценции (FACS). См. Li et al., J. Autimmunity, 2003, 21:83-92 для способов оценки экспрессии TIGIT в периферической крови.
10. Наборы
[0533] Также предложены наборы, содержащие АВР, предложенные в данном документе Наборы могут использоваться для лечения, профилактики и/или диагностики заболевания или патологии, как описано в данном документе.
[0534] В некоторых вариантах осуществления, набор содержит контейнер и этикетку, или листок-вкладыш, на контейнере или вместе с ним. Подходящие контейнеры включают, например, бутылки, флаконы, шприцы и пакеты для ВВ (внутривенный, IV) раствора. Контейнеры могут быть изготовлены из различных материалов, таких как стекло или пластик. Контейнер содержит композицию, которая сама по себе или в сочетании с другой композицией, является эффективной для лечения, профилактики и/или диагностики заболевания или патологии. Контейнер может иметь стерильный порт доступа. Например, если контейнер представляет собой внутривенный пакет для раствора, или флакон, он может иметь порт, который может быть проколот иглой. По меньшей мере один активный агент в композиции представляет собой АВР, предложенный в данном документе. Этикетка или листок-вкладыш указывает на то, что композицию применяют для лечения выбранного состояния.
[0535] В некоторых вариантах осуществления, набор содержит (а) первый контейнер с первой композицией, содержащейся в нем, причем первая композиция содержит АВР, предложенный в данном документе; и b) второй контейнер с второй композицией, содержащейся в нем, при этом вторая композиция содержит дополнительный терапевтический агент. Набор, в данном варианте осуществления изобретения, может дополнительно содержать листок-вкладыш, указывающий на то, что композиции могут применятся для лечения конкретного состояния.
[0536] В альтернативном варианте, или дополнительно, набор может дополнительно содержать второй (или третий) контейнер, содержащий фармацевтически приемлемый наполнитель. В некоторых аспектах, наполнитель представляет собой буфер. Набор может дополнительно включать в себя другие материалы, желательные с коммерческой и пользовательской точек зрения, включая фильтры, иглы и шприцы.
11. Другие иллюстративные варианты осуществления
[0537] Представленные ниже варианты осуществления являются неограничивающими и предложены в качестве иллюстрации некоторых вариантов осуществления и аспектов изобретения в дополнение к тем, которые описаны в данном раскрытии изобретения.
[0538] Вариант осуществления 1: Антиген-связывающий белок, который специфически связывается с человеческим TIGIT (hTIGIT) и который способен по меньшей мере на одно из следующего: а) ингибирует связывание hTIGIT с CD155 и CD112; b) усиливает функцию эффекторного Т-лимфоцита; с) усиливает функцию клетки естественного киллера (NK); d) уменьшает количество регуляторных Т-лимфоцитов в тканях или в кровеносной системе; е) подавляет регуляторный Т-лимфоцит или активность регуляторного Т-лимфоцита; f) ингибирует ассоциацию TIGIT и CD226; и не связывается специфически с Nectin-4 (также известный как полиовирус-рецептор-подобный 4, PVRL4).
[0539] Вариант осуществления 2: Антиген-связывающий белок по варианту осуществления 1, причем антиген-связывающий белок имеет одно или больше из следующих свойств: а) представляет собой моноклональное антитело; b) представляет собой человеческое антитело, гуманизированное антитело или химерное антитело; с) представляет собой биспецифическое антитело, мультиспецифическое антитело, диатело или мультивалентное антитело; d) относится к типу IgG1, IgG2, IgG3, IgG4 или изотипу IgG4 с заменой S228P; е) представляет собой антиген-связывающий фрагмент антитела; f) представляет собой фрагмент Fab, фрагмент Fab', фрагмент F(ab')2 или фрагмент Fv; g) представляет собой одноцепочечное антитело, однодоменное антитело или нанотело.
[0540] Вариант осуществления 3: Фармацевтическая композиция, содержащая эффективное количество антитела, которое связывается с hTIGIT и: а) усиливает клеточно-опосредованный иммунитет; b) увеличивает активность Т-лимфоцитов; с) увеличивает активность цитолитического Т-лимфоцита (CTL); d) увеличивает активность клетки естественного киллера (NK); е) является антагонистом опосредуемого TIGIT сигналинга; f) подавляет сигналинг TIGIT; g) ингибирует или блокирует взаимодействие между PVR и TIGIT; (h) ингибирует или блокирует взаимодействие TIGIT и лиганда CD155 и/или CD112; но не ингибирует взаимодействие между PVR и CD226.
[0541] Вариант осуществления 4: Фармацевтическая композиция, содержащая антиген-связывающий белок по варианту осуществления 1 или варианту осуществления 2.
[0542] Вариант осуществления 5: Фармацевтическая композиция по варианту осуществления 4, дополнительно содержащая эффективное количество анти-PD-1 антитела.
[0543] Вариант осуществления 6: Антиген-связывающий белок по варианту осуществления 1, причем антиген-связывающий белок имеет одно или большее количество из следующих свойств: а) связывается с полипептидом TIGIT человека или его вариантом, или как в другом случае предложено в данном документе с KD меньшей, чем около 20 нМ; или b) связывается с полипептидом TIGIT яванского макака (также «яванский» или «ява») или его вариантом, или как в другом случае предложено в данном документе с KD меньшей, чем около 200 нМ; с) связывается с полипептидом TIGIT мыши или его вариантом, или как в другом случае предложено в данном документе с KD меньшей, чем около 200 нМ; или d) комбинацию по меньшей мере двух из а), b) и с).
[0544] Вариант осуществления 7: Антиген-связывающий белок, который конкурирует или способен конкурировать за связывание с TIGIT человека с эталонным антиген-связывающим белком, причем эталонный антиген-связывающий белок является антиген-связывающим белком по варианту осуществления 1.
[0545] Вариант осуществления 8: Антиген-связывающий белок по варианту осуществления 7, причем антиген-связывающий белок и эталонное антитело перекрестно конкурируют или способны перекрестно конкурировать за связывание с TIGIT человека.
[0546] Вариант осуществления 9: Антиген-связывающий белок по варианту осуществления 1, содержащий константную область тяжелой цепи, содержащую константную область тяжелой цепи человека или ее фрагмент или ее вариант, причем вариант константной области содержит до 20 консервативно модифицированных аминокислотных замен.
[0547] Вариант осуществления 10: Антиген-связывающий белок по варианту осуществления 1, который конкурирует или способен конкурировать за связывание с TIGIT человека с белком CD155 и/или белком CD112.
[0548] Вариант осуществления 11: Антиген-связывающий белок по варианту осуществления 1, который способен антагонизировать сигналинг TIGIT специфичным для Т-лимфоцитов способом.
[0549] Вариант осуществления 12: Выделенная молекула антитела, способная связываться с TIGIT человека (hTIGIT), содержащая вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность VHCDR1 SEQ ID NO: 48-62, аминокислотную последовательность VHCDR2 SEQ ID NO: 36-47 и аминокислотную последовательность VHCDR3 SEQ ID NO: 29-35; и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность VLCDR1 SEQ ID NO: 70-72, аминокислотную последовательность VLCDR2 SEQ ID NO: 67-69 и аминокислотную последовательность VLCDR3 SEQ ID NO: 63-66.
[0550] Вариант осуществления 13: Выделенная нуклеиновая кислота, кодирующая антиген-связывающий белок в соответствии с вариантом осуществления 1.
[0551] Вариант осуществления 14: Вектор экспрессии, содержащий нуклеиновую кислоту согласно варианту осуществления 13.
[0552] Вариант осуществления 15: Прокариотическая или эукариотическая клетка-хозяин, содержащая вектор варианта осуществления 14.
[0553] Вариант осуществления 16: Способ получения рекомбинантного белка, включающий стадии экспрессии нуклеиновой кислоты согласно варианту осуществления 13 в прокариотической или эукариотической клетке-хозяине и выделение указанного белка из указанной клетки или супернатанта клеточной культуры.
[0554] Вариант осуществления 17: Способ лечения субъекта, страдающего от рака или воспалительного заболевания, включающий стадию введения субъекту фармацевтической композиции, содержащей эффективное количество антиген-связывающего белка по варианту осуществления 1.
[0555] Вариант осуществления 18: Способ по варианту осуществления 17, причем рак представляет собой солидный рак.
[0556] Вариант осуществления 19: Способ по варианту осуществления 17, причем рак является гематологическим раком.
[0557] Вариант осуществления 20: Способ модуляции функции иммунной системы у нуждающегося в этом человеческого субъекта, включающий стадию контактирования популяции Т-лимфоцитов человеческого субъекта с фармацевтической композицией, содержащей эффективное количество антиген-связывающего белка по варианту осуществления 1, в условиях, при которых иммунная система модулируется.
[0558] Вариант осуществления 21: Способ индуцирования или усиления иммунного ответа у субъекта, включающий стадию введения субъекту фармацевтической композиции, содержащей антиген-связывающий белок, или биспецифическое антитело, или комплексообразующий антиген-связывающий белок по любому из предыдущих вариантов осуществления, причем иммунный ответ вызывается против опухолевого антигена.
[0559] Вариант осуществления 22: Способ по варианту осуществления 21, причем антиген-связывающий белок, биспецифическое антитело или комплексообразующий антиген-связывающий белок вводят в количестве, достаточном для достижения одного или больше из следующего у субъекта: а) снижения супрессии регуляторными Т-лимфоцитами активности эффекторных Т-лимфоцитов; b) снижения уровней регуляторных Т-лимфоцитов; с) активации эффекторных Т-лимфоцитов; d) индуцирования или усиления пролиферации эффекторных Т-лимфоцитов; е) ингибирования роста опухоли; и f) индуцирования регрессии опухоли.
[0560] Вариант осуществления 23: Способ по варианту осуществления 22, причем способ дополнительно включает одно или больше из следующих а) применение химиотерапии; b) применение лучевой терапии; или с) введение одного или большего количества дополнительных терапевтических агентов.
[0561] Вариант осуществления 24: Способ по варианту осуществления 23, причем дополнительный терапевтический агент содержит иммуностимулирующий агент.
[0562] Вариант осуществления 25: Способ по варианту осуществления 24, причем иммуностимулирующий агент содержит антагонист ингибирующего рецептора иммунной клетки.
[0563] Вариант осуществления 26: Способ по варианту осуществления 25, причем ингибирующим рецептором является CTLA-4, PD-1, PD-L1, PD-L2, LAG-3, Tim3, нейритин, BTLA, СЕСАМ-1, СЕСАМ-5, VISTA, LAIR1, CD160, 2В4, TGF-R или KIR.
[0564] Вариант осуществления 27: Способ по варианту осуществления 24, причем иммуностимулирующий агент содержит агонист ко-стимулирующего рецептора иммунной клетки.
[0565] Вариант осуществления 28: Способ по варианту осуществления 27, причем ко-стимулирующий рецептор представляет собой ОХ40, CD2, CD27, CDS, ICAM-1, LFA-1 (CD11a/CD18), ICOS (CD278), 4-1ВВ (CD137), GITR, CD28, CD30, CD40, BAFFR, HVEM, CD7, LIGHT, NKG2C, SLAMF7, NKp80, CD160, B7-H3 или CD83.
[0566] Вариант осуществления 29: Способ по варианту осуществления 24, причем иммуностимулирующий агент содержит цитокин.
[0567] Вариант осуществления 30: Способ по варианту осуществления 29, причем цитокин представляет собой ИЛ-2, ИЛ-5, ИЛ-7, ИЛ-12, ИЛ-15 или ИЛ-21.
[0568] Вариант осуществления 31: Способ по варианту осуществления 24, причем иммуностимулирующий агент содержит онколитический вирус.
[0569] Вариант осуществления 32: Способ по варианту осуществления 31, причем онколитический вирус представляет собой вирус простого герпеса, вирус везикулярного стоматита, аденовирус, вирус болезни Ньюкасла, вирус коровьей оспы или вирус мараби.
[0570] Вариант осуществления 33: Способ по варианту осуществления 24, в котором иммуностимулирующий агент содержит химерный антигенный Т-лимфоцит.
[0571] Вариант осуществления 34: Способ по варианту осуществления 24, причем иммуностимулирующий агент содержит би- или мультиспецифическое антитело, направленное на Т-лимфоцит.
[0572] Вариант осуществления 35: Способ по варианту осуществления 23, в котором дополнительный терапевтический агент содержит aнти-TGF-бета антитело или ловушку рецептора TGFβ.
[0573] Вариант осуществления 36: Способ по любому из вариантов осуществления 20-35, причем введение фармацевтической композиции приводит к индукции или усилению пролиферации эффекторного Т-лимфоцита, или модуляции I-κВ и/или NF-κВ в Т-лимфоците, или модуляции активности TIGIT в Т-лимфоците, или индуцированному Т-клеточным рецептором сигналингу в эффекторном Т-лимфоците или их комбинации.
[0574] Вариант осуществления 37: Способ скрининга тестируемых соединений, содержащих антиген-связывающий белок по варианту осуществления 1, который способен ингибировать взаимодействие лиганда TIGIT с TIGIT, включающий следующие этапы: приведение в контакт образца, содержащего лиганд TIGIT и TIGIT с соединением; и определение того, уменьшается ли взаимодействие лиганда TIGIT с TIGIT в образце относительно взаимодействия лиганда TIGIT с TIGIT в образце, не приведенного в контакт с соединением, в результате чего уменьшение взаимодействие лиганда TIGIT с TIGIT в образце, приведенном в контакте с соединением, идентифицирует соединение как соединение, которое ингибирует взаимодействие лиганда TIGIT с TIGIT.
[0575] Вариант осуществления 38: Антиген-связывающий белок по варианту осуществления 1, который способен ингибировать фосфорилирование домена ITIM полипептида TIGIT.
[0576] Вариант осуществления 1А: Выделенный антиген-связывающий белок (АВР), который специфически связывается с TIGIT, при этом антитело: а) конкурирует за связывание с TIGIT с антителом, выбранным из МАБ1, МАБ2, МАБ3, МАБ4, МАБ5, МАБ6, МАБ7, МАБ8, МАБ9, МАБ10, МАБ11, МАБ12, МАБ13, МАБ14, МАБ15, МАБ16, МАБ17, МАБ18, МАБ19, МАБ20 или МАБ21, каждое из которых представлено в Таблице 5 данного раскрытия изобретения; b) ингибирует связывание CD155 с TIGIT; с) ингибирует связывание CD112 с TIGIT; d) ингибирует ассоциацию CD226 с TIGIT; е) активирует эффекторный Т-лимфоцит или естественный киллер (NK); f) уменьшает количество регуляторных Т-лимфоцитов в ткани или в кровеносной системе; g) ингибирует подавление эффекторного Т-лимфоцита регуляторным Т-лимфоцитом; h) не связывается специфически с любыми из PVRL1, PVRL2, PVRL3 или PVRL4; или i) допускает любую комбинацию а)-h).
[0577] Вариант осуществления 2А: АВР по варианту осуществления 1А, причем АВР содержит CDR-H3 области VH, выбранной из SEQ ID NO: 4-24, или CDR-H3, имеющую по меньшей мере около 80% идентичности с CDR-H3 области VH, выбранной из SEQ ID NO: 4-24.
[0578] Вариант осуществления 3А: АВР по варианту осуществления 2А, причем CDR-H3 идентифицирован в соответствии с схемами нумерации по Кабату, Чотиа или IMGT.
[0579] Вариант осуществления 4А: АВР по любому из вариантов осуществления 2А-3А, причем CDR-H3 выбран из SEQ ID NO: 29-35.
[0580] Вариант осуществления 5А: АВР по любому из вариантов осуществления 1А-4А, причем АВР содержит CDR-H2 области VH, выбранной из SEQ ID NO: 4-24, или CDR-H2, имеющую по меньшей мере около 80% идентичности с CDR-H2 области VH, выбранной из SEQ ID NO: 4-24
[0581] Вариант осуществления 6А: АВР по варианту осуществления 5А, причем CDR-H2 идентифицирован в соответствии с схемами нумерации по Кабату, Чотиа или IMGT.
[0582] Вариант осуществления 7А: АВР по любому из вариантов осуществления 5А-6А, причем CDR-H2 выбран из SEQ ID NO: 36-47.
[0583] Вариант осуществления 8А: АВР по любому из вариантов осуществления 1А-7А, причем АВР содержит CDR-H1 области VH, выбранной из SEQ ID NO: 4-24, или CDR-H1, имеющую по меньшей мере около 80% идентичности с CDR-H1 области VH, выбранной из SEQ ID NO: 4-24
[0584] Вариант осуществления 9А: АВР по варианту осуществления 8А, причем CDR-H1 идентифицирован в соответствии с схемами нумерации по Кабату, Чотиа, по Кабату плюс Чотиа, или по IMGT.
[0585] Вариант осуществления 10А: АВР по любому из вариантов осуществления 8А-9А, причем CDR-H1 выбран из SEQ ID NO: 48-54 и 58-62.
[0586] Вариант осуществления 11А: АВР по любому из вариантов осуществления 1А-10А, причем АВР содержит CDR-L3 области VL, выбранной из SEQ ID NO: 25-28, или CDR-L3, имеющую по меньшей мере около 80% идентичности с CDR-L3 области VL, выбранной из SEQ ID NO: 25-28.
[0587] Вариант осуществления 12А: АВР по варианту осуществления 11А, причем CDR-L3 идентифицирован в соответствии с схемами нумерации по Кабату, Чотиа или IMGT.
[0588] Вариант осуществления 13А: АВР по любому из вариантов осуществления 11А-12А, причем CDR-L3 выбран из SEQ ID NO: 63-66.
[0589] Вариант осуществления 14А: АВР по любому из вариантов осуществления 1А-13А, причем АВР содержит CDR-L2 области VL, выбранной из SEQ ID NO: 25-28, или CDR-L2, имеющую по меньшей мере около 80% идентичности с CDR-L2 области VL, выбранной из SEQ ID NO: 25-28.
[0590] Вариант осуществления 15А: АВР по варианту осуществления 14А, причем CDR-L2 идентифицирован в соответствии с схемами нумерации по Кабату, Чотиа или IMGT.
[0591] Вариант осуществления 16А: АВР по любому из вариантов осуществления 14А-15А, причем CDR-L2 выбран из SEQ ID NO: 67-69.
[0592] Вариант осуществления 17А: АВР по любому из вариантов осуществления 1А-16А, причем АВР содержит CDR-L1 области VL, выбранной из SEQ ID NO: 25-28, или CDR-L1, имеющую по меньшей мере около 80% идентичности с CDR-L1 области VL, выбранной из SEQ ID NO: 25-28.
[0593] Вариант осуществления 18А: АВР по варианту осуществления 17А, причем CDR-L1 идентифицирован в соответствии с схемами нумерации по Кабату, Чотиа или IMGT.
[0594] Вариант осуществления 19А: АВР по любому из вариантов осуществления 17А-18А, причем CDR-L1 выбран из SEQ ID NO: 70-72.
[0595] Вариант осуществления 20А: АВР по любому из вариантов осуществления 1А-19А, причем АВР содержит область VH выбранную из SEQ ID NO: 4-24.
[0596] Вариант осуществления 21А: АВР по любому из вариантов осуществления 1А-20А, причем АВР содержит область VL выбранную из SEQ ID NO: 25-28.
[0597] Вариант осуществления 22А: АВР по любому из вариантов осуществления 1А-21 А, причем TIGIT выбран из hTIGIT (SEQ ID NO: 1), cTIGIT (SEQ ID NO: 2) и mTIGIT (SEQ ID NO: 3 или 138).
[0598] Вариант осуществления 23А: АВР по любому из вариантов осуществления 1А-22А, причем АВР содержит антитело.
[0599] Вариант осуществления 24А: АВР по варианту осуществления 23А, причем антитело содержит VH и VL, совмещенные в пару, как предложено для антитела, выбранного из МАБ1, МАБ2, МАБ3, МАБ4, МАБ5, МАБ6, МАБ7, МАБ8, МАБ9, МАБ10, МАБ11, МАБ12, МАБ13, МАБ14, МАБ15, МАБ16, МАБ17, МАБ18, МАБ19, МАБ20 или МАБ21, каждое из которых представлено в Таблице 5 данного раскрытия изобретения.
[0600] Вариант осуществления 25А: АВР по варианту осуществления 24А, причем АВР представляет собой антитело, выбранное из МАБ1, МАБ2, МАБ3, МАБ4, МАБ5, МАБ6, МАБ7, МАБ8, МАБ9, МАБ10, МАБ11, МАБ12, МАБ13, МАБ14, МАБ15, МАБ16, МАБ17, МАБ18, МАБ19, МАБ20 или МАБ21, каждое из которых представлено в Таблице 5 данного раскрытия изобретения.
[0601] Вариант осуществления 26А: АВР по любому из вариантов осуществления 23А-25А, причем антитело представляет собой моноклональное антитело.
[0602] Вариант осуществления 27А: АВР по любому из вариантов осуществления 23А-26А, причем антитело представляет собой химерное, гуманизированное или человеческое антитело.
[0603] Вариант осуществления 28А: АВР по любому из вариантов осуществления 1А-27А, причем АВР является мультиспецифичным.
[0604] Вариант осуществления 29А: АВР по любому из вариантов осуществления 1А-28А, причем АВР содержит фрагмент антитела.
[0605] Вариант осуществления 30А: АВР по любому из вариантов осуществления 1А-29А, причем АВР содержит альтернативный каркас.
[0606] Вариант осуществления 31А: АВР по любому из вариантов осуществления 1А-30А, причем АВР содержит константную область иммуноглобулина.
[0607] Вариант осуществления 32А: АВР по любому из вариантов осуществления 1А-31А, причем АВР содержит антитело, выбранное из IgA, IgD, IgE, IgG или IgM.
[0608] Вариант осуществления 33А: АВР по варианту осуществления 32А, причем АВР содержит IgG, выбранный из IgG4, IgG1, IgG2 или IgG3.
[0609] Вариант осуществления 34А: АВР по любому из вариантов осуществления 1А-33А, причем АВР связывает hTIGIT (SEQ ID NO: 1) с аффинностью меньше чем около 20 нМ.
[0610] Вариант осуществления 35А: АВР по любому из вариантов осуществления 1А-34А, причем АВР связывает cTIGIT (SEQ ID NO: 2) с аффинностью меньше чем около 200 нМ.
[0611] Вариант осуществления 36А: АВР по любому из вариантов осуществления 1А-35А, причем АВР связывает mTIGIT (SEQ ID NO: 3 или 138) с аффинностью меньше чем около 200 нМ.
[0612] Вариант осуществления 37А: Выделенный полинуклеотид, кодирующий АВР по любому из вариантов осуществления 1А-36А, его VH или VL, или его антиген-связывающую часть.
[0613] Вариант осуществления 38А: Вектор, содержащий полинуклеотид по варианту осуществления 37А.
[0614] Вариант осуществления 39А: Клетка-хозяин, содержащая вектор по варианту осуществления 38А.
[0615] Вариант осуществления 40А: Способ получения АВР по любому из вариантов осуществления 1А-36А, включающий экспрессию АВР в клетке-хозяине по варианту осуществления 39А и выделение экспрессированного АВР.
[0616] Вариант осуществления 41А: Фармацевтическая композиция, содержащая АВР по любому из вариантов осуществления 1А-36А.
[0617] Вариант осуществления 42А: Фармацевтическая композиция по варианту осуществления 41А, причем количество АВР в фармацевтической композиции является достаточным для: а) увеличения активности эффекторного Т-лимфоцита; b) увеличения активности цитолитического Т-лимфоцита; с) увеличения активности клетки NK; d) ингибирования опосредованного TIGIT сигналинга; е) ингибирования или блокирования связывание CD155 и или CD112 с TIGIT; или f) любой комбинации а)-е), у субъекта.
[0618] Вариант осуществления 43А: Фармацевтическая композиция по любому из вариантов осуществления 41А-42А, дополнительно содержащая антитело, которое антагонизирует PD-1.
[0619] Вариант осуществления 44А: способ лечения или профилактики заболевания или состояния у субъекта, нуждающегося в этом, включающий введение субъекту эффективного количества АВР по любому из вариантов осуществления 1А-36А, или фармацевтической композиции по любому из вариантов осуществления 41А-43А.
[0620] Вариант осуществления 45А: Способ по варианту осуществления 44А, причем заболевание или патология представляет собой рак или вирусную инфекцию.
[0621] Вариант осуществления 46А: способ модуляции иммунного ответа у субъекта, нуждающегося в этом, включающий введение субъекту эффективного количества АВР по любому из вариантов осуществления 1А-36А, или фармацевтической композиции по любому из вариантов осуществления 41А-43А.
[0622] Вариант осуществления 47А: Способ по любому из вариантов осуществления 44А-46А, дополнительно включающий введение одного или большего количества дополнительных терапевтических агентов субъекту.
[0623] Вариант осуществления 48А: Способ по варианту осуществления 47А, причем дополнительный терапевтический агент выбран из антитела антагониста PD-1, химиотерапии, иммуностимулирующего агента и излучения.
[0624] Вариант осуществления 49А: Способ по варианту осуществления 47А, причем дополнительный терапевтический агент представляет собой иммуностимулирующий агент, который блокирует сигналинг ингибирующего рецептора иммунной клетки, или его лиганд.
[0625] Вариант осуществления 50А: Способ по варианту осуществления 49А, причем ингибирующий рецептор или его лиганд выбирают из CTLA-4, PD-1, PD-L1, PD-L2, LAG-3, Tim3, нейритина, BTLA, СЕСАМ-1, СЕСАМ-5, VISTA, LAIR1, CD160, 2В4, TGF-R, KIR и их комбинаций.
[0626] Вариант осуществления 51А: Способ по варианту осуществления 48А, причем дополнительный терапевтический агент представляет собой иммуностимулирующий агент, который является агонистом для стимулирующего рецептора иммунной клетки.
[0627] Вариант осуществления 52А: Способ по варианту осуществления 51А, причем стимулирующий рецептор иммунной клетки выбирают из ОХ40, CD2, CD27, CDS, ICAM-1, LFA-1 (CD11a/CD18), ICOS (CD278), 4-1BB (CD137), GITR, CD28, CD30, CD40, BAFFR, HVEM, CD7, LIGHT, NKG2C, SLAMF7, NKp80, CD160, B7-H3, лиганда CD83 и их комбинаций.
[0628] Вариант осуществления 53А: Способ по варианту осуществления 48А, причем дополнительный терапевтический агент представляет собой иммуностимулирующий агент, который представляет собой цитокин.
[0629] Вариант осуществления 54А: Способ по варианту осуществления 53А, причем цитокин выбран из ИЛ-2, ИЛ-5, ИЛ-7, ИЛ-12, ИЛ-15, ИЛ-21 и их комбинаций.
[0630] Вариант осуществления 55А: Способ по варианту осуществления 48А, причем дополнительный терапевтический агент представляет собой иммуностимулирующий агент, который является онколитическим вирусом.
[0631] Вариант осуществления 56А: Способ по варианту осуществления 55А, причем онколитический вирус выбран из вируса простого герпеса, вируса везикулярного стоматита, аденовируса, вируса болезни Ньюкасла, вируса коровьей оспы, вируса мараби и их комбинаций.
[0632] Вариант осуществления 57А: Способ по варианту осуществления 48А, причем иммуностимулирующий агент содержит Т-лимфоцит, экспрессирующий рецептор химерного антигена.
[0633] Вариант осуществления 58А: Способ по варианту осуществления 48А, причем иммуностимулирующий агент содержит би- или мультиспецифическое антитело, направленное на Т-лимфоцит.
[0634] Вариант осуществления 59А: Способ по варианту осуществления 48А, причем иммуностимулирующий агент содержит анти-TGF-β антитело, ловушку TGF-β или их комбинацию.
[0635] Вариант осуществления 60А: Способ по варианту осуществления 48А, причем иммуностимулирующий агент содержит вакцину к антигену, ассоциированному с раком.
[0636] Вариант осуществления 61А: способ скрининга АВР, способных ингибировать взаимодействие лиганда TIGIT с TIGIT, включающий: а) приведение в контакт образца, содержащего лиганд TIGIT и TIGIT, с АВР по любому из вариантов осуществления 1А-36А; и b) определение того, уменьшается ли связывание лиганда TIGIT с TIGIT в присутствии АВР, по сравнению с связыванием лиганда TIGIT с TIGIT при отсутствии АВР.
ПРИМЕРЫ
[0637] Ниже приведены примеры способов и композиций изобретения. Понятно, что различные другие варианты осуществления могут быть реализованы на практике с учетом общего раскрытия изобретения, предложенного в данном документе.
Пример 1: Отбор белков, связывающих антиген TIGIT
[0638] TIGIT АВР были отобраны из синтетической библиотеки человеческих антител, экспрессированных и представленных на поверхности дрожжевых клеток в форме IgG, как описано, например, в WO 2009036379; WO 2010105256; WO 2012009568; и Xu et al., Protein Eng. Des. Sel., 2013, 26:663-670 (включен посредством ссылки в полном объеме) и, более конкретно, как показано ниже. Последовательности и свойства АВР, выделенных из рекомбинантной библиотеки, приведены в Таблице 5.
[0639] Восемь наивных человеческих синтетических дрожжевых библиотек, каждая с разнообразием 109, размножали, как описано в WO 2009036379; WO 2010105256; WO 2012009568; и Xu et al., Protein Eng. Des. Sel., 2013, 26:663-670; каждый включен посредством ссылки в полном объеме. В течение первых двух раундов отбора была проведена методика сортировки магнитными гранулами, использующая систему Miltenyi MACS®, как описано в Siegel et al., J. Immunol. Meth, 2004, 286:141-153. Вкратце, дрожжевые клетки (~1010 клеток/библиотека) инкубировали с биотинилированным антигеном TIGIT-Fc в промывочном буфере FACS (фосфатно-солевой буферный раствор (PBS)/0,1% бычий сывороточный альбумин (BSA)). После однократного промывания 50 мл ледяного промывочного буфера осадок клеток ресуспендировали в 40 мл промывочного буфера и 500 мкл стрептавидина MicroBeads™ (Miltenyi Biotec) добавляли к дрожжам и инкубировали в течение 15 мин при 4°С. Затем дрожжи гранулировали, ресуспендировали в 5 мл промывочного буфера и загружали в колонку Miltenyi LS. После загрузки 5 мл, колонку промывали 3 раза 3 мл промывочного буфера FACS. Затем колонку убирали из магнитного поля и дрожжи элюировали 5 мл среды для роста и затем выращивали в течение ночи. Следующие раунды сортировки выполняли с применением проточной цитометрии. Примерно 1×108 дрожжей гранулировали, три раза промывали промывочным буфером и инкубировали с уменьшающимися концентрациями биотинилированного гибридного антигена TIGIT-Fc (100-1 нМ) в равновесных условиях при комнатной температуре. Дрожжи затем дважды промывали и окрашивали LC-FITC (разбавленный 1:100), и либо SA-633 (разбавленный 1:500), либо ЕА-РЕ (разбавленный 1:50) вторичными реагентами в течение 15 минут при 4°С. После двухкратного промывания ледяным промывочным буфером клеточные осадки ресуспендировали в 0,4 мл промывочного буфера и переносили в пробирки с фильтрами для сортировки. Сортировку выполняли с применением сортировщика FACS ARIA (BD Biosciences), и сортировочные ворота были назначены для отбора конкретных связующих веществ относительно контроля. Последующие раунды отбора были использованы для уменьшения количества неспецифических связующих веществ, используя растворимые мембранные белки из клеток СНО (см. WO 2014179363 и Xu et al., Protein Eng. Des. Sel, 2013, 26:663-670, каждый включен посредством ссылки в полном объеме) и идентификации связующих вещества с улучшенной аффиностью к TIGIT с применением антигена TIGIT-Fc. После последнего раунда сортировки дрожжи высевали и отдельные колонии были выбраны для определения свойств и для отбора в кандидаты клонов по аффинному созреванию.
Пример 2. Созревание аффинности
[0640] Оптимизацию наивных клонов проводили с применением трех стратегий созревания: варьирование легкой цепи; варьирование CDR-H1 и CDR-H2; и осуществления мутагенеза VH.
[0641] Варьирование легкой цепи: плазмиды с тяжелой цепью были извлечены из наивных полученных клонов (описанных выше) и преобразованы в библиотеку легкой цепи с разнообразием 1×106. Отборы выполняли как описано выше, с одним раундом сортировки MACS (активируемая магнитным полем сортировка клеток) и двумя раундами сортировки FACS (сортировка клеток с возбуждением флуоресценции) с применением 10 нМ или 1 нМ биотинилированного антигена TIGIT-Fc для соответствующих раундов.
[0642] Отбор CDR-H1 и CDR-H2: CDR-H3 из клонов, отобранных при процедуре варьирования легкой цепи, были рекомбинированы в полуготовую библиотеку с вариантами CDR-H1 и CDR-H2 с разнообразием 1×108, а отборы проводили с применением мономерного антигена HIS-TIGIT. Применяли давления аффинности используя уменьшающие концентрации биотинилированного антигена HIS-TIGIT (100-1 нМ) в равновесных условиях при комнатной температуре.
[0643] Отбор VHmut: Клоны, полученные с помощью процедуры отбора CDR-H1 и CDR-Н2, были подвергнуты дополнительным раундам аффинного созревания с помощью мутагенеза тяжелой цепи на основе вносящей ошибки ПЦР. Отборы проводили с применением HIS-TIGIT в качестве антигена, в целом как описано выше, но с добавлением применения сортировки FACS для всех отборочных раундов.
Пример 3: Получение и очистка антител
[0644] Чтобы получить достаточное количество отобранных антител для дополнительной характеристики свойств, клоны дрожжей выращивали до насыщения, а затем встряхивали в течение 48 ч при 30°С. После индукции дрожжевые клетки осаждали и супернатанты собирали для очистки. IgG очищали с применением колонки с белком А и элюировали уксусной кислотой, рН 2,0. Фрагменты Fab были получены путем расщепления папаином и очищены через KappaSelect® (GE Healthcare LifeSciences).
[0645] Антитела также получали путем временной трансфекции клеток Expi293 в соответствии с протоколом изготовителя (Thermo Fisher), временной трансфекции клеток СНО, или стабильной экспрессией клетками СНО. Антитела очищали хроматографией с белком А.
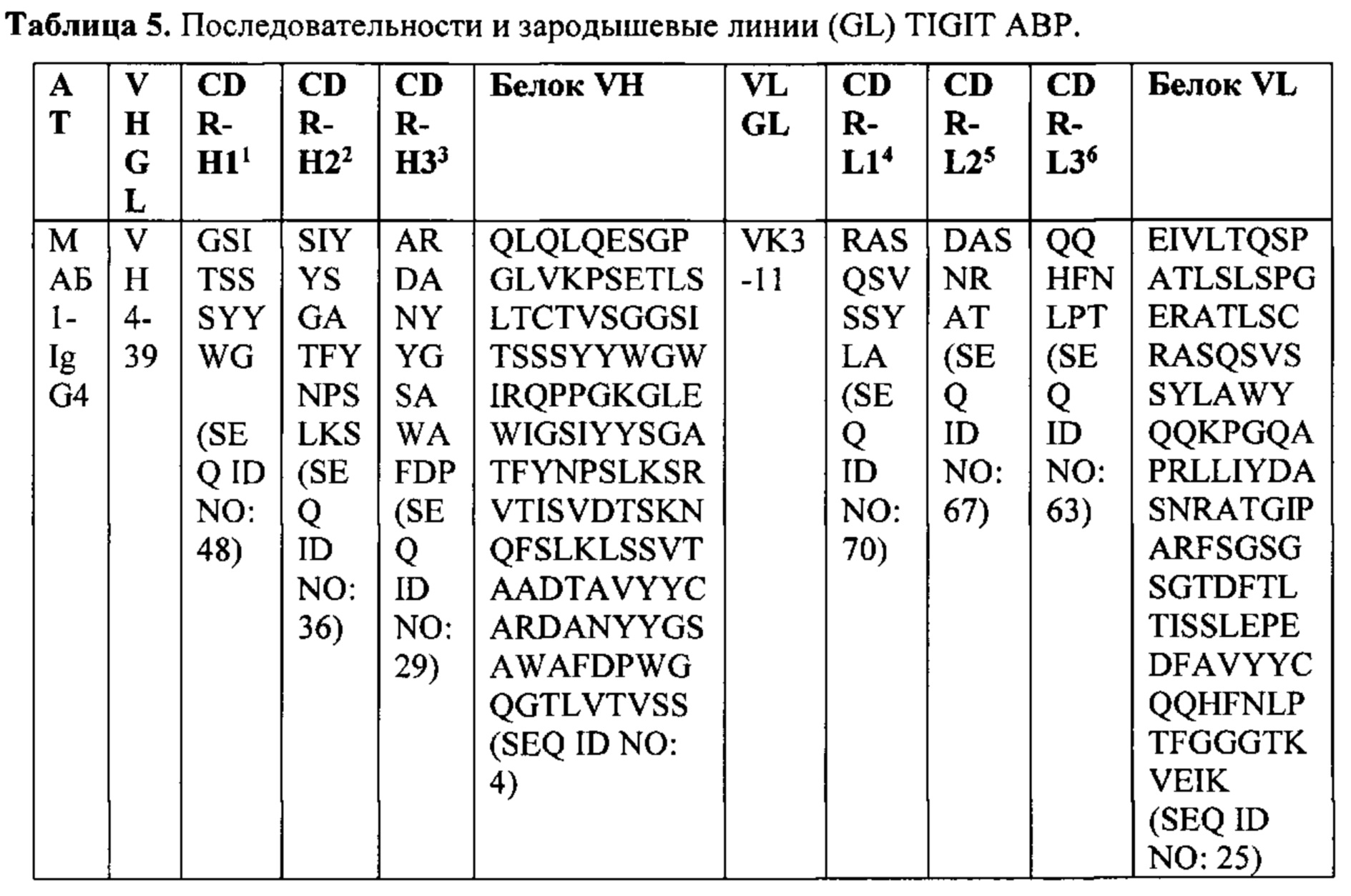
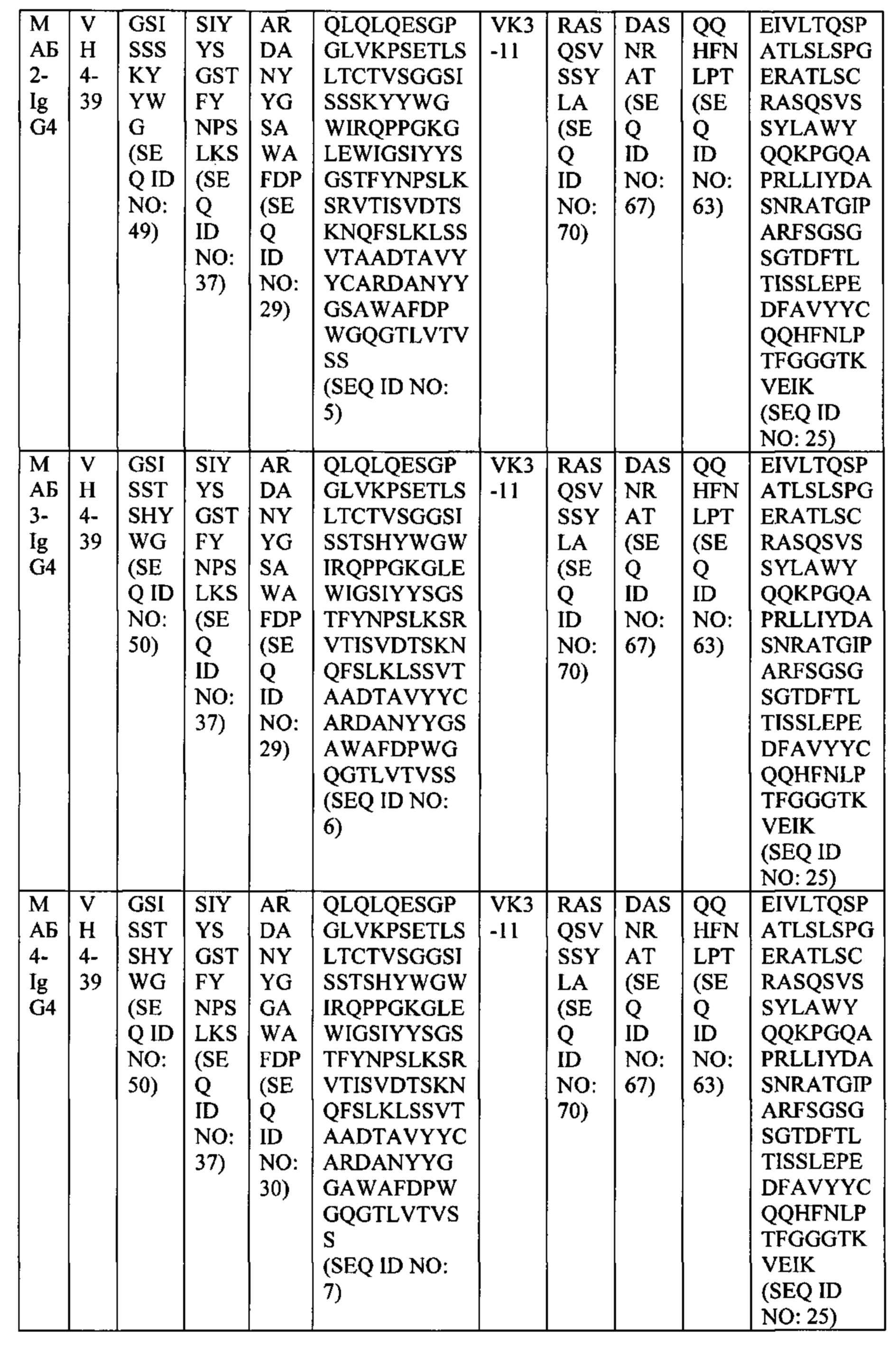
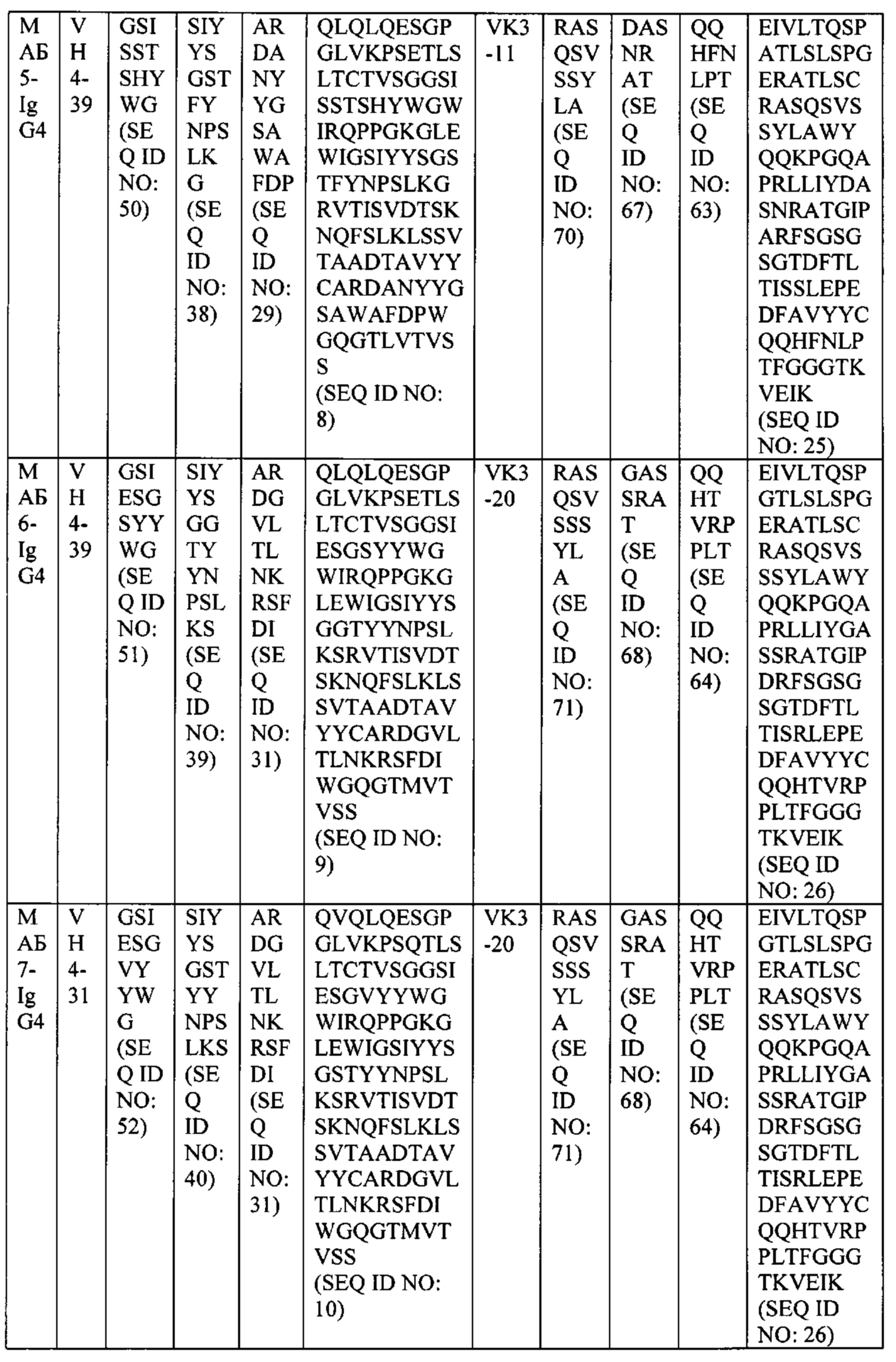
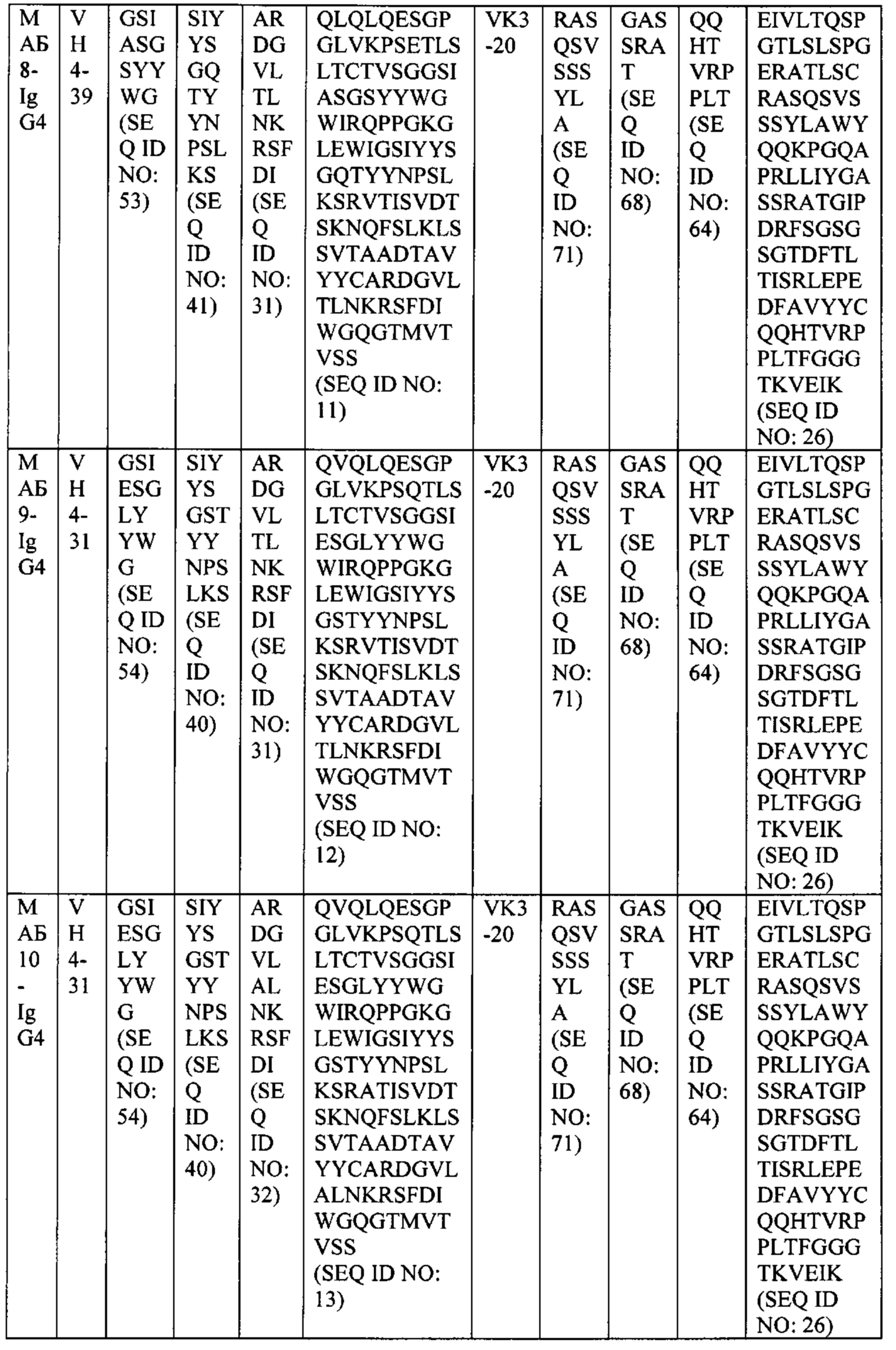
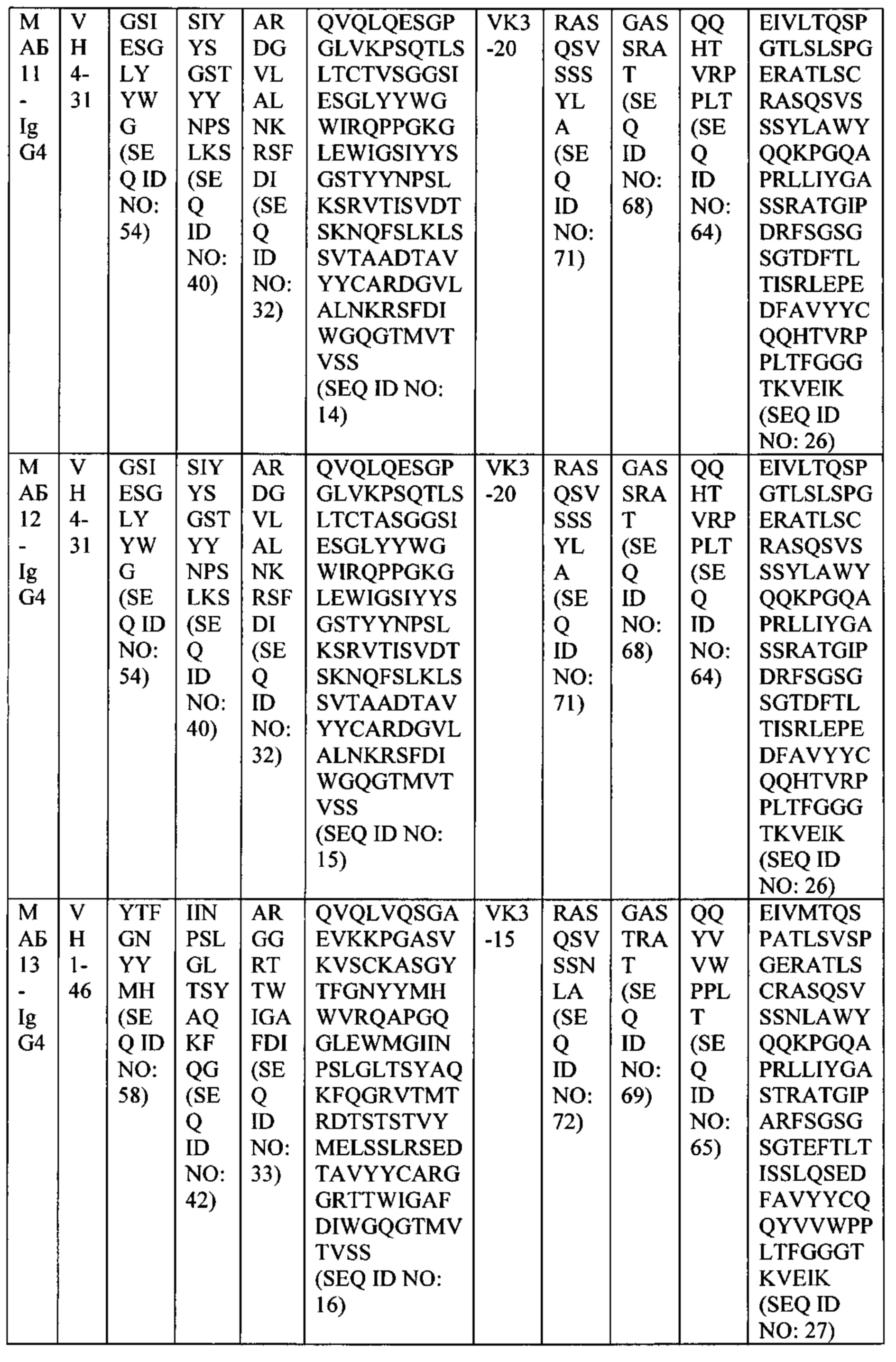
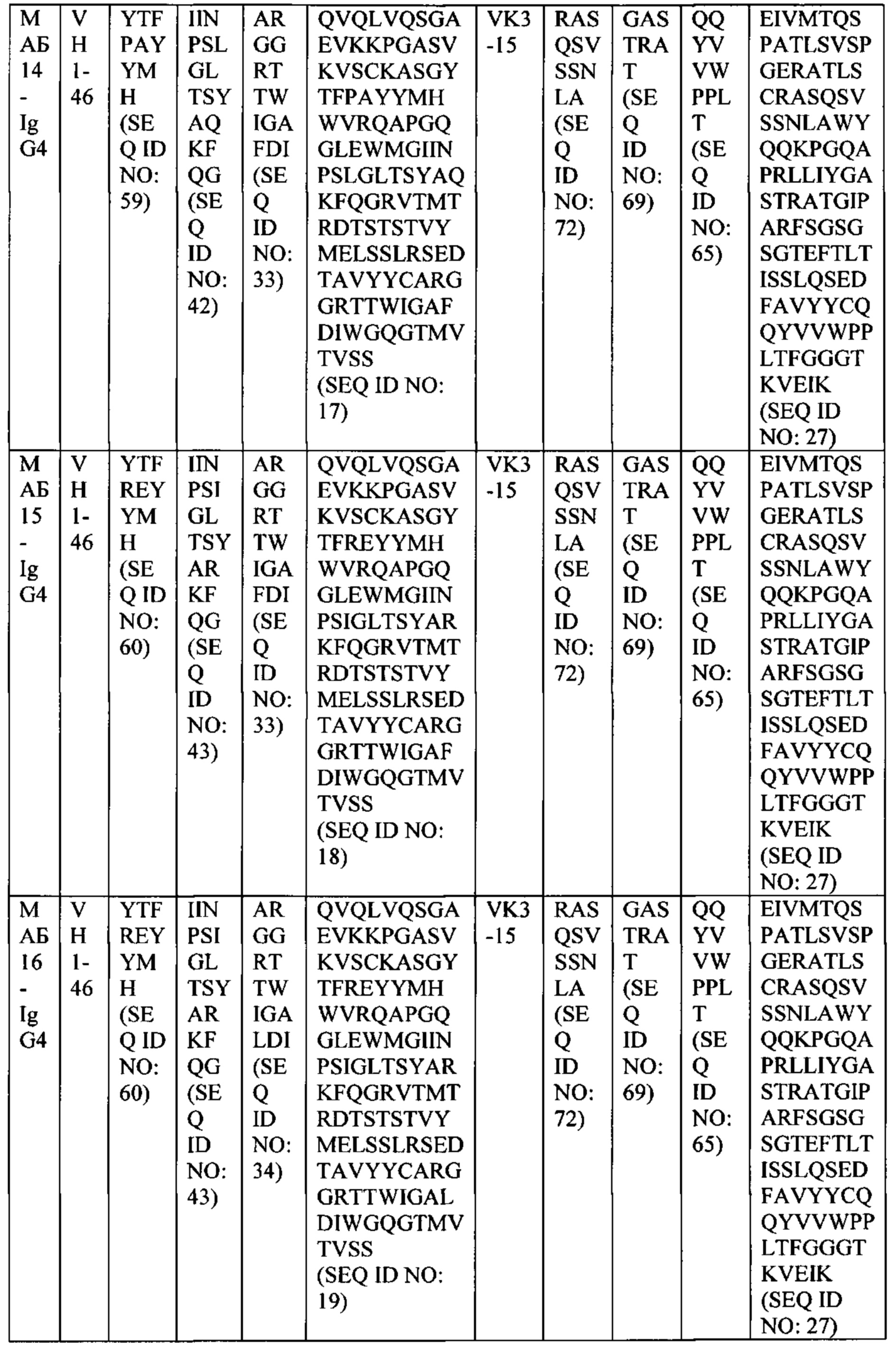
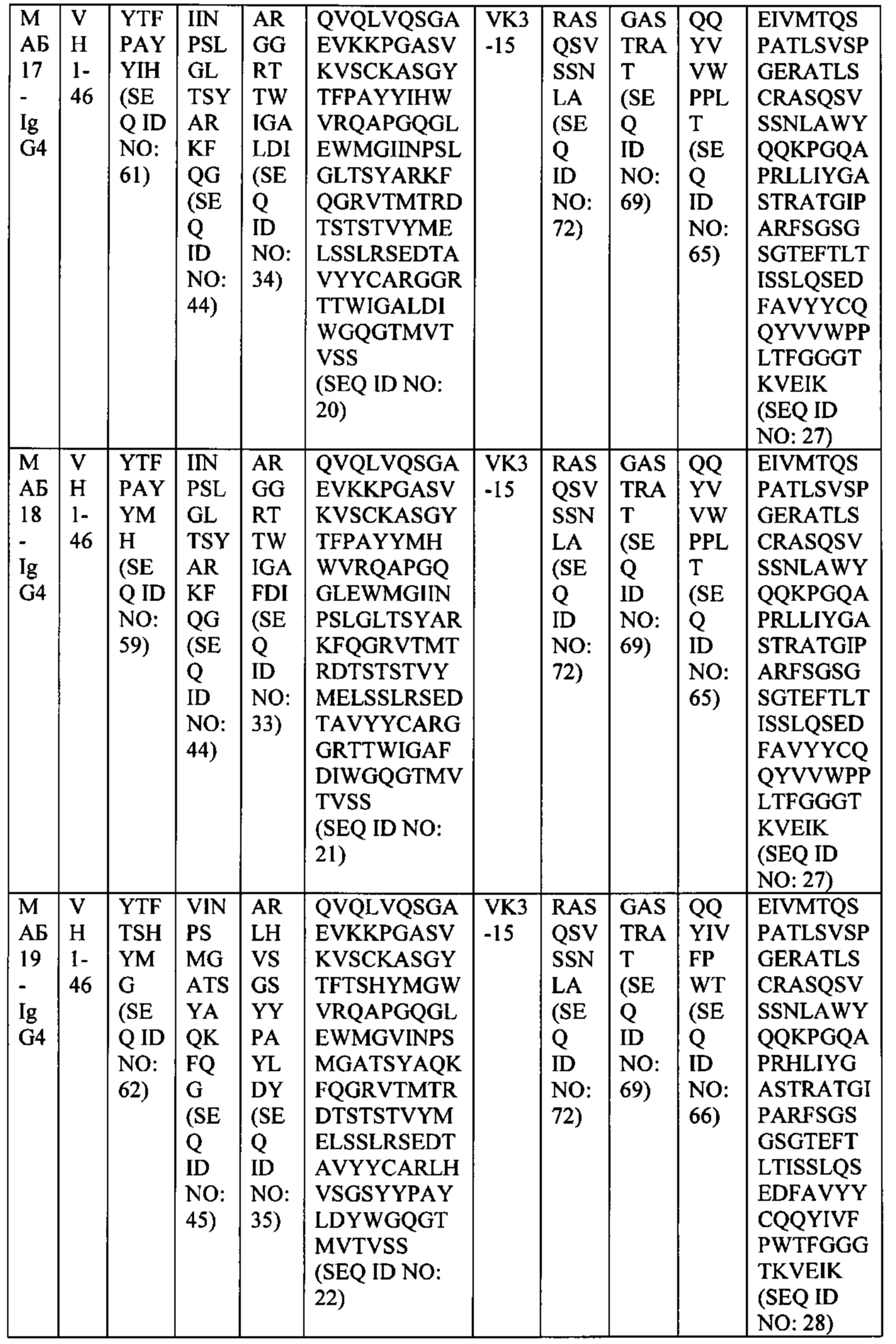
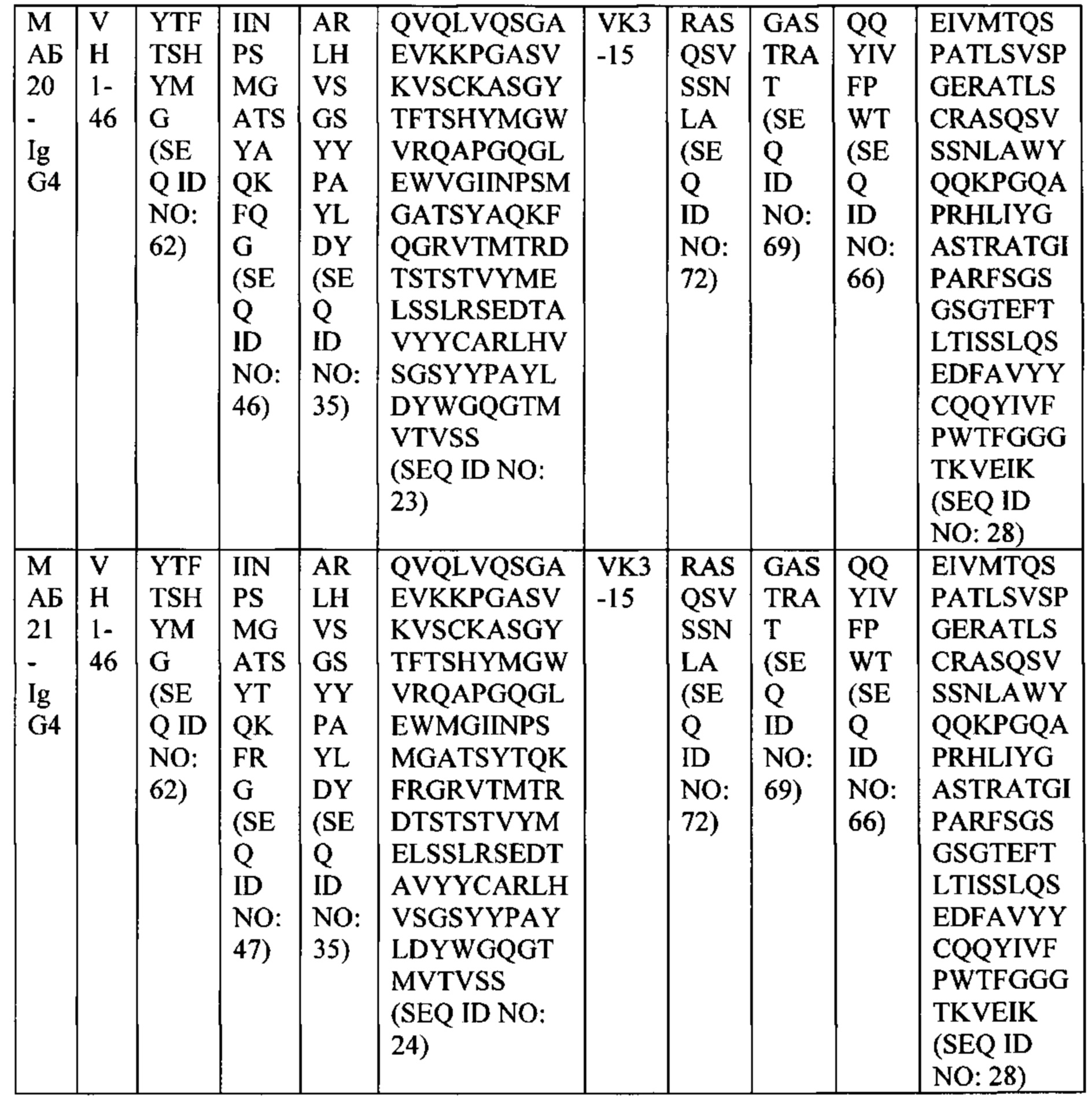
1 Включает CDR-H1, как определено системами нумерации по Чотиа и Кабату, включая границы обеих систем нумерации.
2 Согласно системе нумерации по Кабату.
3 Согласно системе нумерации IMGT.
4 Согласно системам нумерации по Кабату и Чотиа.
5 Согласно системам нумерации по Кабату и Чотиа.
6 Согласно системам нумерации по Кабату, Чотиа и IMGT.
Пример 4. Характеристика свойств антитела
[0646] Измерения KD ForteBio: количественное связывание антител с рекомбинантным мономерным TIGIT человека, мыши (SEQ ID NO: 3), яванского макака измеряли с применением интерферометрии биослоя (BLI) с помощью FORTEBIO®. Измерения аффинности выбранных антител проводили в целом, как описано в Estep et al., Mabs, 2013, 5:270-278, включен посредством ссылки в полном объеме. Измерения аффинности FORTEBIO проводили путем загрузки IgG в интерактивном режиме на датчики AHQ. Датчики уравновешивали в автономном режиме в буфере для анализа в течение 30 мин, а затем контролировали в интерактивном режиме в течение 60 секунд для установления базовой линии. Датчики с загруженными IgG подвергали воздействию одной концентрации антигена (100 нМ) в течение 3 минут. Затем их переносили в буфер для анализа на 3 минуты для измерения скорости диссоциации. Кинетику анализировали с применением модели связывания 1:1. Краткое изложение измерений KD для антител, связывающих одну концентрацию TIGIT человека, яванского макака и мыши (SEQ ID NO: 3), приведено в Таблице 6 ниже.
[0647] Измерения KD MSD-SET: Измерения аффинности при равновесии в растворе для выбранных антител, связывающихся с мономерным рекомбинантным TIGIT человека и яванского макака, проводили в целом, как правило, как описано ранее. См. Estep et al., выше, включен посредством ссылки в полном объеме. Вкратце, титрования равновесного раствора (SET) проводили в PBS+0,1% IgG-Free BSA (PBSF) с антигеном (мономер TIGIT), который поддерживали константным на 10-100 пМ и инкубировали с 3-5-кратными серийными разведениями Fab или мАТ (антитело мыши) начиная с 10 пМ-10 нМ. Антитела (20 нМ в PBS) наносили на стандартные связующие MSD-ECL-плашки в течение ночи при 4°С или при комнатной температуре в течение 30 мин. Затем плашки блокировали с помощью BSA в течение 30 мин при встряхивании 700 об/мин, с последующими тремя промывками промывочным буфером (PBSF+0,05% Tween 20). Образцы SET применяли и инкубировали в плашках в течение 150 с при встряхивании 700 об/мин с последующей одной промывкой. Антиген, захваченный на плашке, обнаруживали с помощью 250 нм/мл меченого сульфометкой стрептавидина в PBSF путем инкубации в плашке в течение 3 мин. Плашки трижды промывали промывочным буфером, а затем считывали на приборе MSD Sector Imager 2400 с применением 1х буфера Т чтения с поверхностно-активным веществом. Процент свободного антигена был нанесен на график как функция титрованного антитела в Prism и соответствовал квадратичному уравнению для извлечения KD. Чтобы повысить пропускную способность, во всех экспериментах MSD-SET использовались роботы для работы с жидкостями, включая подготовку образцов SET.

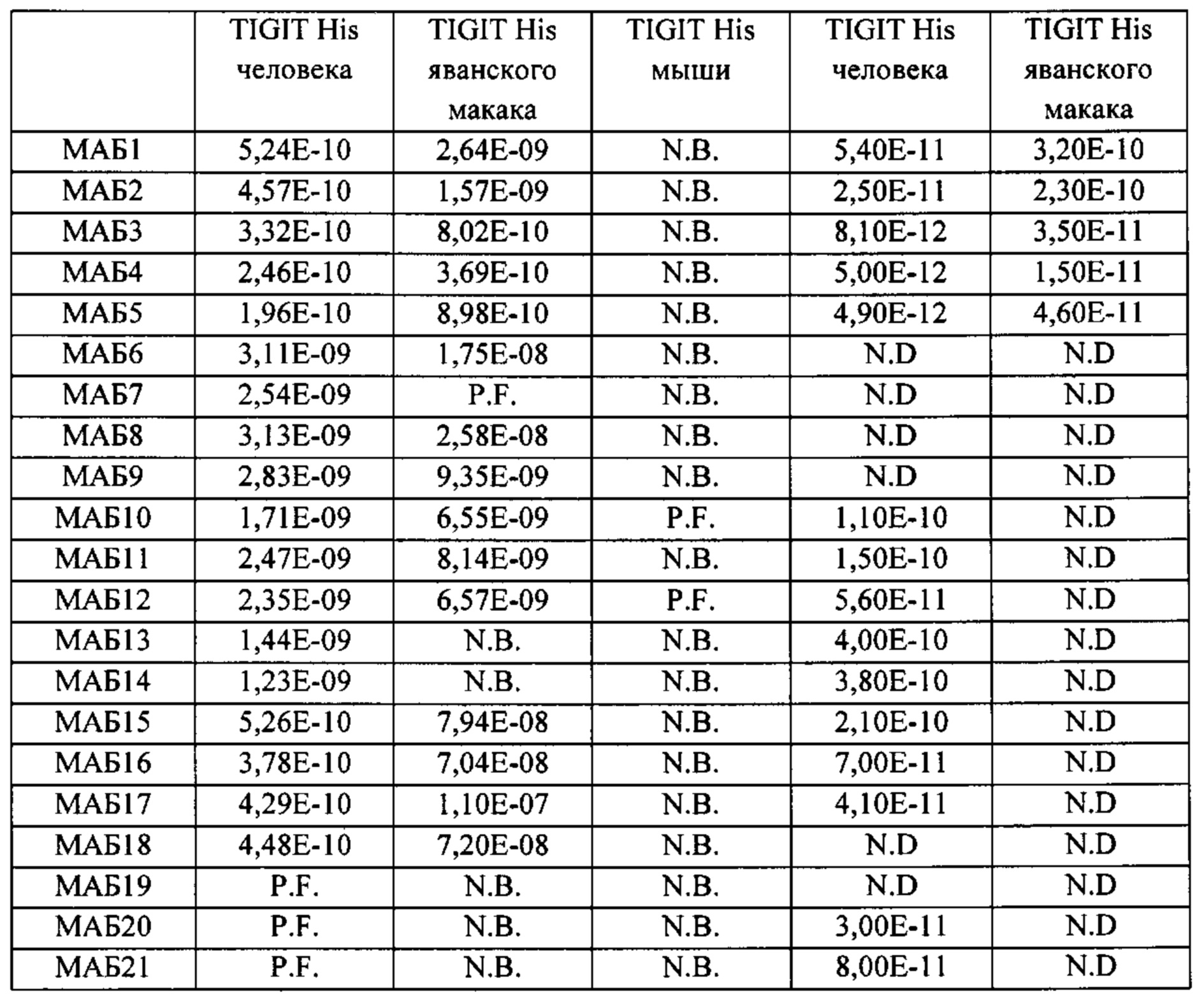
N.B.: не связующее или слабо связывающее
P.F.: плохой подбор (хорошая реакция связывания с неудовлетворительным KD на основе модели 1:1)
N.D.: измерение аффинности MSD не выполнялось
Пример 5: Оценка блокирования лигандов TIGIT
[0648] Количественные исследования блокирования лигандов проводили с применением анализа связывания TIGIT на клеточной поверхности. Связывание флуоресцентно меченого PVR-Fc или PVRL2-Fc с экспрессирующими человеческий TIGIT клетками Jurkat измеряли с помощью проточной цитометрии. Ряд разведений каждого тестируемого антитела инкубировали с клетками TIGIT Jurkat, чтобы измерить способность каждого антитела блокировать связывание PVR-Fc или PVRL2-Fc и определить значения IC50, указанные в Таблице 7.
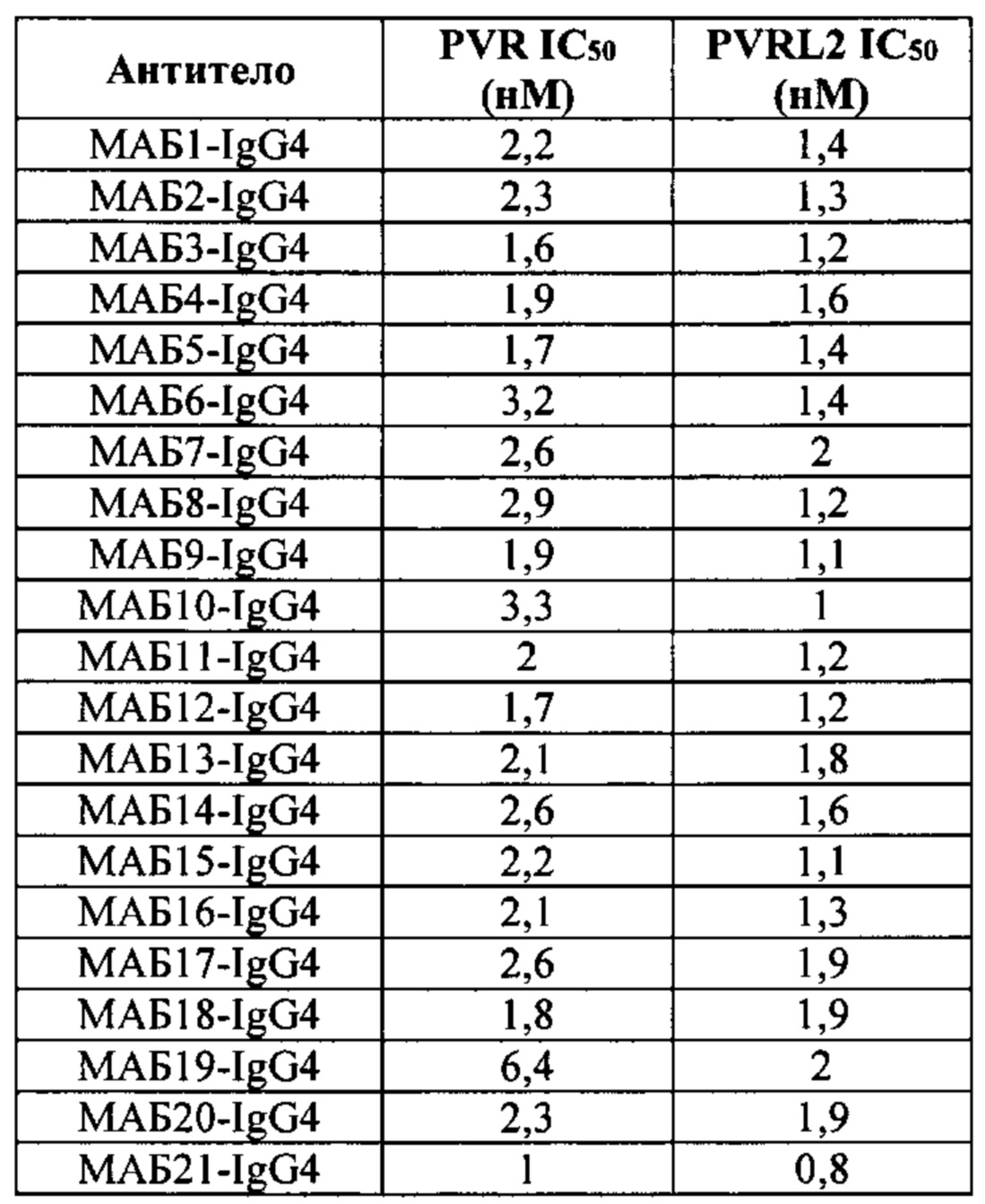
Пример 6: Дополнительные анализы связывания TIGIT для измерения аффинности и перекрестной реактивности антител к TIGIT
[0649] Аффиность антител, связывающихся с TIGIT человека, измеряли с помощью нескольких концентраций антигена для того, чтобы более точно измерить кинетику связывания. Кроме того, количественное связывание МАБ10 с TIGIT человека, мыши (SEQ ID NO: 3), яванского макака измеряли с применением интерферометрии биослоя (BLI) и проточной цитометрии. На Фиг. 1А показано выравнивание TIGIT разных видов. Проценты идентичности по всему белку TIGIT приведены в Таблице 8 ниже.
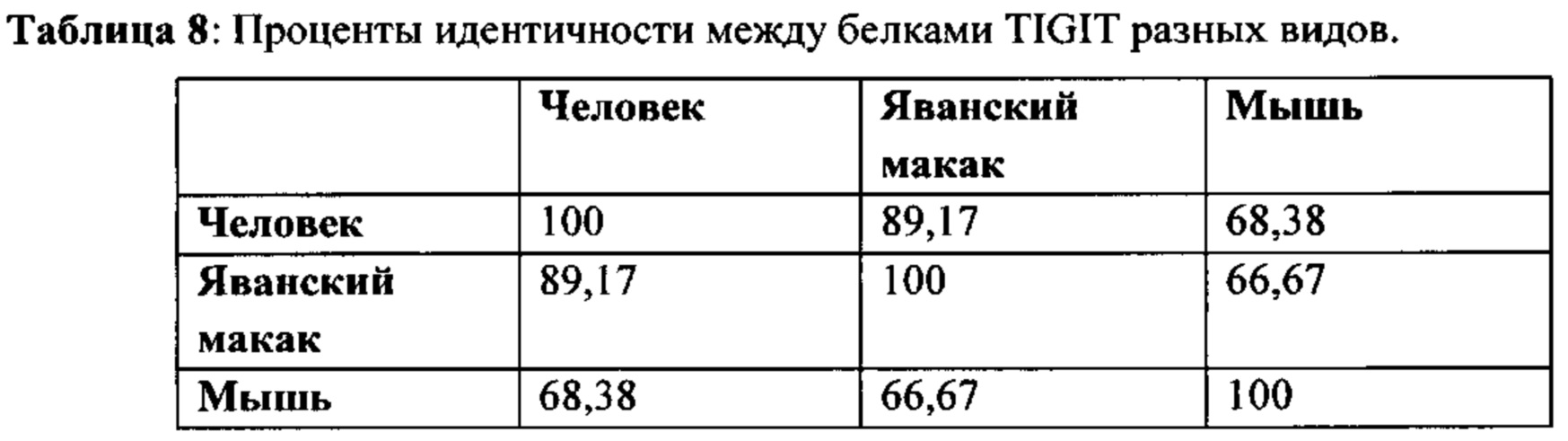
Кинетические измерения для антител, связывающих TIGIT человека, яванского макака и мыши
[0650] Аффинности и кинетику связывания для антител, связывающихся с TIGIT-His человека измеряли с применением инструмента Octet® QKe (ForteBio) способом, аналогичным описанному выше в Примере 4, но с множественными концентрациями используемого антигена. Кроме того, измеряли связывание МАБ10 с TIGIT-His яванского макака и мыши (SEQ ID NO: 3). Стратегия захвата анти-TIGIT антител на датчиках после ассоциации/диссоциации мономерных белков TIGIT использовалась для того, чтобы избежать эффекта авидности в анализе. Анализ BLI проводили при 29°С с применением 1х кинетического буфера (ForteBio) в качестве буфера для анализа. Биосенсоры захвата анти-IgG Fc человека (АНС) сначала были предварительно замочены в буфере для анализа в течение более пяти минут. Анти-TIGIT антитело (5 мкг/мл) захватывали на датчике в течение 300 секунд. Затем датчики погружали в буфер для анализа в течение 120 секунд, чтобы определить базовую линию перед измерением связывания с каждым белком TIGIT. Затем датчики погружали в различные концентрации TIGIT-His человека (от 12,4 до 0,8 нМ или от 6,2 до 0,8 нМ, 2-кратные разведения в буфере для анализа), TIGIT-His яванского макака (от 24,6 до 1,5 нМ или от 12,3 до 1,5 нМ, 2-кратные разведения в буфере для анализа, только для МАБ10) или TIGIT-His мыши (от 303 до 4,7 нМ, 2-кратные разведения в буфере для анализа, только для МАБ10) в течение 300 секунд или 600 секунд, в зависимости от эксперимента, для измерения ассоциации. Диссоциацию TIGIT измеряли путем погружения датчиков в буфер для анализа на 600, 1200 или 1800 секунд, в зависимости от эксперимента (600 секунд использовались только для TIGIT-His мыши). Перемешивание на всех стадиях составляло 1000 об/мин.
[0651] Кинетические параметры были сгенерированы с помощью программного обеспечения Octet® Data Analysis Software 8.2.0.7 с применением вычитания контроля, межшаговой коррекции на основе диссоциации, модели связывания 1 к 1 и глобальной подгонки (Rmax не связано с датчиком). Константа скорости ассоциации (ka), константа скорости диссоциации (kd) и константа равновесия (KD) были отдельно усреднены по всем экспериментам, а краткое изложение данных для антител, связывающихся с TIGIT человека, показано в Таблице 9. Краткое описание связывания МАБ10 с мономерным TIGIT человека, яванской макаки и мыши (SEQ ID NO: 3) показано в Таблице 10.
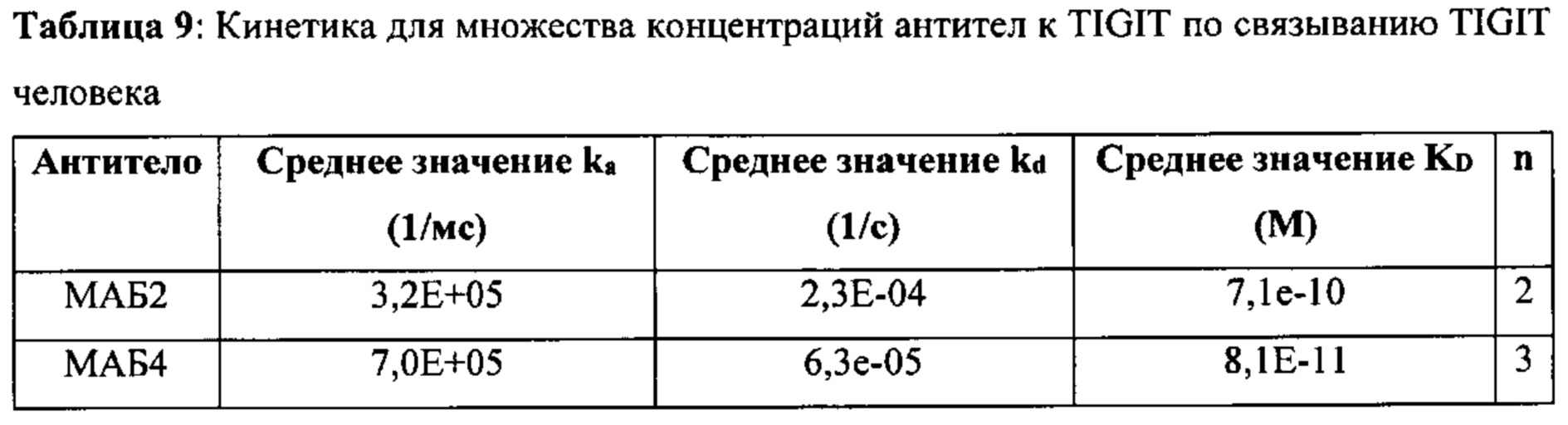
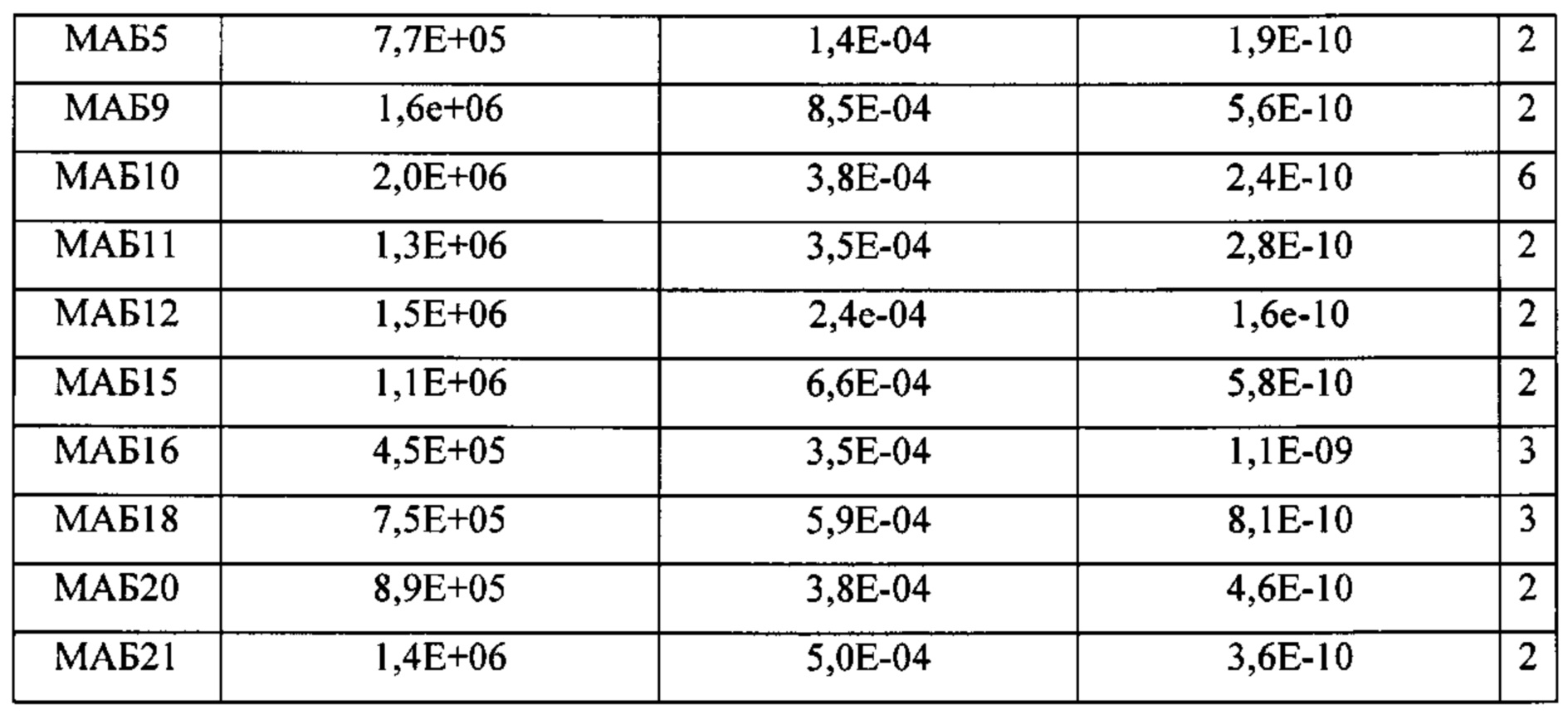

*KD не может быть определено из-за минимального связывания (очень низкий ответ связывания), что указывает на то, что любое связывание хуже, чем предел чувствительности инструмента.
Измерения KD для связывания с клетками, модифицированными для экспрессирования TIGIT
[0652] KD для связывания МАБ10 с TIGIT клеточной поверхности в модифицированных клеточных линиях измеряли с применением проточной цитометрии. Клетки Jurkat (Т-лимфоциты острого лейкоза, АТСС® TIB-152™) были модифицированы так, чтобы стабильно экспрессировать TIGIT человека или яванского макака, а клетки СНО-K1 были модифицированные так, чтобы стабильно экспрессировать TIGIT мыши (SEQ ID NO: 3). Значения KD показаны в Таблице 11. Значения KD для связывания МАБ10 с TIGIT человека и яванского макака на клеточной поверхности очень похожи.


Измерения KD для связывания с первичными клетками
[0653] KD для связывания МАБ10 с TIGIT клеточной поверхности на первичных клетках измеряли с применением проточной цитометрии. Для МКПК человека и яванского макака, CD8+ Т-лимфоциты имели наибольшую обнаруживаемую экспрессию TIGIT, и поэтому были использованы для расчета связывания МАБ10 с первичными клетками у данных видов. Для целей анализа CD8+ Т-лимфоциты определяли как клетки с размером и зернистостью лимфоцитов, которые экспрессировали следующую комбинацию молекулярных маркеров: CD3+CD4-CD8+. Точно так же Tregs мыши продемонстрировали наивысшее связывание МАБ10 и поэтому использовались для данных расчетов. Tregs мыши были определены как CD4+CD8-CD25+FoxP3+ клетки с размером и зернистостью лимфоцитов. Значения KD показаны в Таблице 12. Значения KD для связывания МАБ10 с TIGIT человека и яванского макака на клеточной поверхности первичных клеток очень похожи.
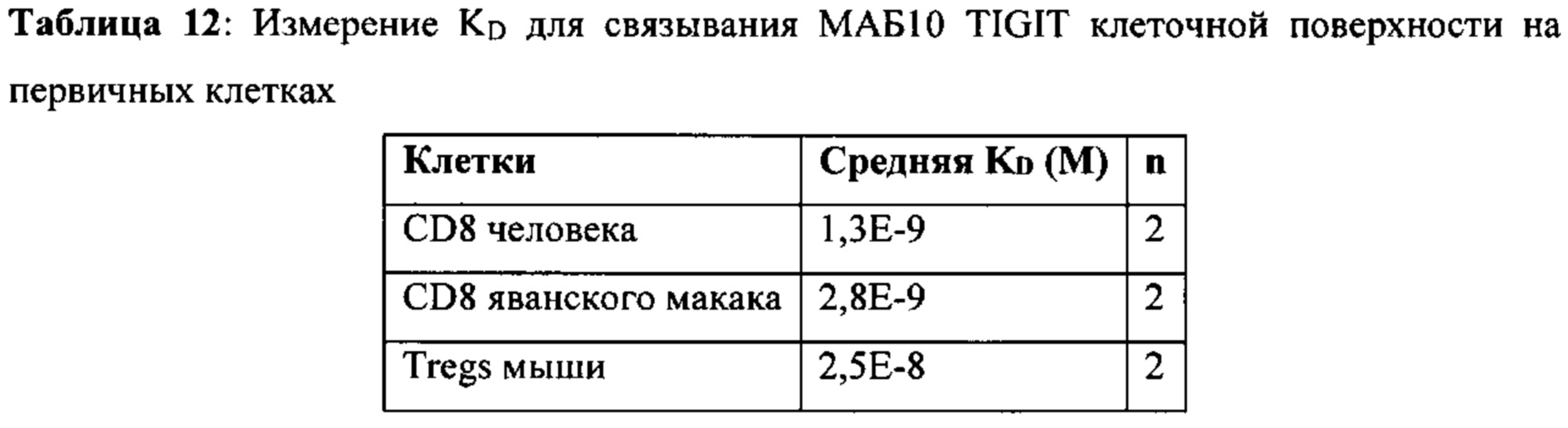
Связывание антитела с PVRL4 человека
[0654] Чтобы подтвердить специфичность анти-TIGIT антитела, с помощью BLI было измерено связывание с PVRL4 человека, членом семейства Ig, наиболее близким к TIGIT (29% идентичности в внеклеточной области гомолога). На Фиг. 1В показано выравнивание внеклеточных доменов человеческих TIGIT и PVRL4. Анализ BLI проводили при 30°С с применением 1X кинетического буфера в качестве буфера для анализа. Датчики АНС сначала предварительно промывали в буфере для анализа больше чем 5 минут. Антитело (5 мкг/мл) фиксировали на датчике в течение 300 секунд. Затем датчики погружали в буфер для анализа в течение 120 секунд, чтобы определить базовую линию перед измерением связывания с белком PVRL4-His человека. Затем датчики погружали в PVRL4-His человека (200 нМ в буфере для анализа) в течение 200 секунд для измерения ассоциации. Диссоциацию PVRL4 затем измеряли путем погружения датчиков в буфер для анализа в течение 200 секунд. Результаты были проанализированы с применением программного обеспечения Octet® Data Analysis версии 8.2.0.7. МАБ1-МАБ21 не связывали PVRL4, демонстрируя тем самым, что МАБ, раскрытые в данном документе, являются высокоспецифичными к TIGIT.
Пример 7: Продуцирование ИЛ-2 в клетках Jurkat, модифицированных для ответа на сигналинг TIGIT человека после обработки анти-TIGIT антителами
[0655] Анализ для тестирования способности антител ингибировать функцию TIGIT был разработан с применением двух модифицированных клеточных линий. Данный анализ совместного культивирования был разработан для имитации взаимодействия экспрессирующего TIGIT Т-лимфоцита с второй клеткой, экспрессирующей лиганд TIGIT (PVR и PVRL2), таким образом имитируя способность TIGIT подавлять активацию Т-лимфоцита. Данное взаимодействие вызывает ингибирование функции Т-лимфоцита (например, выделение цитокинов) в экспрессирующей TIGIT клетке. Клетки Jurkat (Т-лимфоциты острого лейкоза) обычно экспрессируют ИЛ-2 при стимуляции Т-клеточного рецептора (с применением анти-CD33 и анти-CD28-агонистических антител). Экспрессия TIGIT в клетках Jurkat должна была б уменьшать экспрессию ИЛ-2, индуцированную анти-CD3/CD28-агонистами, если бы PVR и/или PVRL2 присутствовали и связывались с TIGIT, тем самым обуславливая сигнал подавления для клетки Jurkat. Таким образом, линия клеток Jurkat была разработана для экспрессии TIGIT человека.
[0656] Вторая клеточная линия, НТ-1080 (линия клеток фибросаркомы человека, АТСС® CCL121™), была сконструирована для экспрессии мембран-сцепленного анти-CD3 антитела с одной цепью Fv (scFv), которое может обеспечить активирующий сигнал для клеток TIGIT Jurkat. Активирующий сигнал также усиливали добавлением растворимого анти-CD28 антитела агониста. Клетки НТ-1080 естественным образом экспрессируют высокие уровни PVR и PVRL2, предоставляя таким образом лиганд для TIGIT в анализе совместного культивирования TIGIT Jurkat/анти-CD3 НТ-1080. В данном совместном анализе антитела к антагонистам TIGIT увеличивают продукцию ИЛ-2 по сравнению с антителами отрицательного контроля. Обзор данной системы анализа показан на Фиг. 3.
[0657] Анализ совместного культивирования использовали для определения EC50 анти-TIGIT антитела путем обработки рядом доз антитела. ECso измеряли для анти-TIGIT антител МАБ1-МАБ21, а также анти-мышиного антитела хомяка SEC1 (см. Пример 8) и коммерческого анти-человеческого анти-TIGIT антитела MBSA43 (доступного, например, из eBioscience, каталожный номер 16-9500). Супернатанты собирали, как описано выше, через 24 часа после обработки и анализировали с помощью ИЛ-2 ELISA. Краткое изложение экспериментально определенных значений ЕС50 в клетках TIGIT человека Jurkat приведено в Таблице 13. Как видно из Таблицы 13, все МАБ, за исключением МАБ13, МАБ 14, МАБ 16 и SEC1, показали себя лучше в данном анализе, чем коммерческое антитело MBSA43.
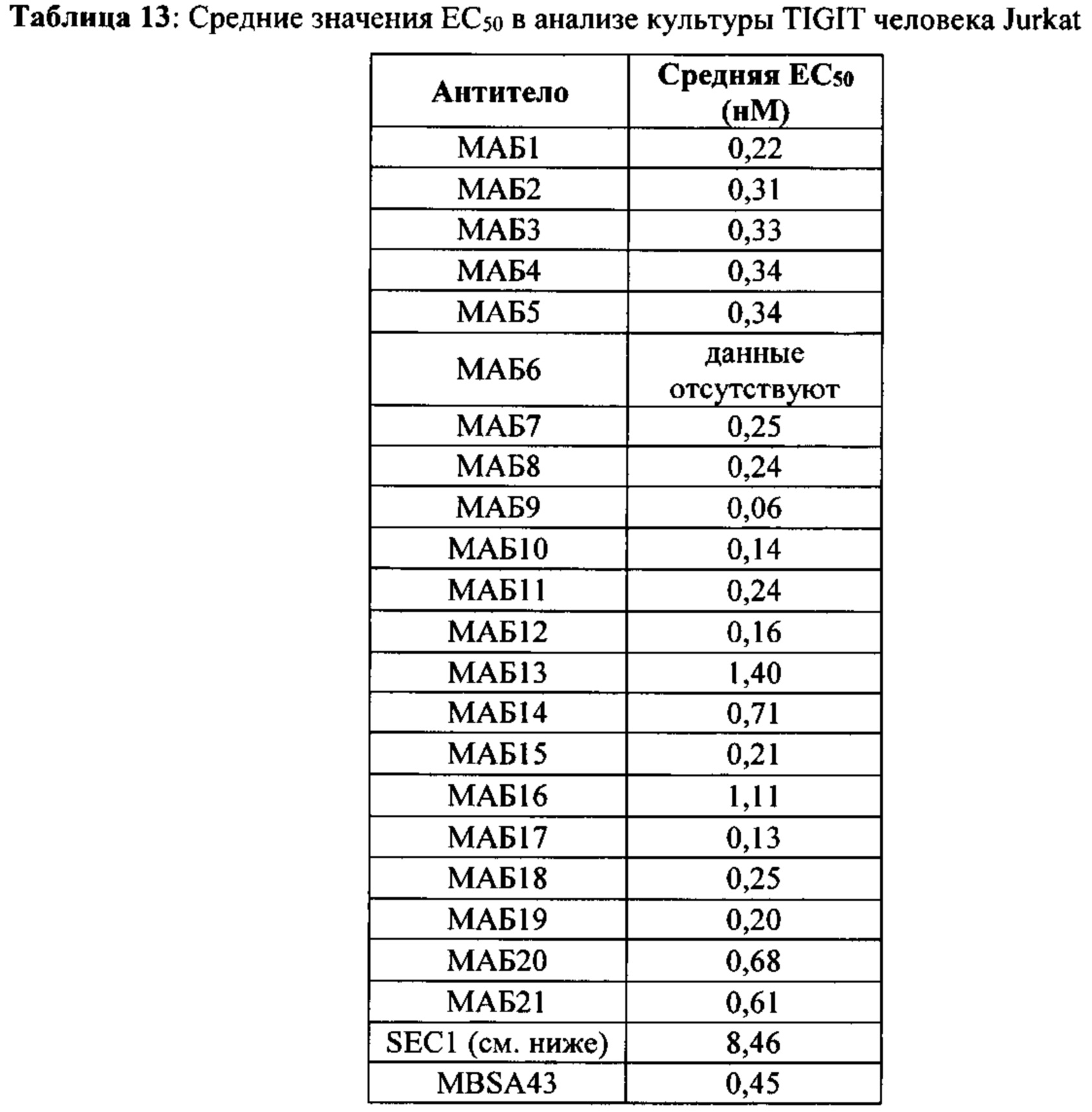
[0658] Кроме того, анализ совместного культивирования Jurkat повторяли с МАБ10 с применением субклонированного изолята клеток анти-CD3 scFv НТ1080. На Фиг. 4А показаны кривые ЕС50 из иллюстративного эксперимента, сравнивающего МАБ10 и контрольным IgG4. Данный эксперимент проводили 3 раза, а средняя ЕС50 составлял 0,11 нМ.
[0659] Как описано выше для экспрессирующих TIGIT человека клеток Jurkat, анализ стимуляции при совместном культивировании был подготовлен с клетками анти-CD3 scFv НТ-1080 в присутствии экспрессирующих TIGIT яванского макака клеток Jurkat и растворимого анти-человеческого CD28. На Фиг. 4В показаны кривые ЕС50 из иллюстративного эксперимента, сравнивающего МАБ10 и контрольный IgG4. Как показано на Фиг. 4В, МАБ10 индуцирует продуцирование ИЛ-2 в клетках Jurkat, экспрессирующих TIGIT яванского макака, тогда как контроль в виде изотипа IgG4 не индуцирует. Среднее значение ЕС50 для МАБ10 в анализе совместного культивирования TIGIT яванского макака Jurkat/анти-CD3 НТ-1080 было определено как равное 2,87 нМ.
Пример 8: Характеристика анти-TIGIT антитела «SEC1»
[0660] Были проведены дополнительные исследования, чтобы охарактеризовать анти-TIGIT антитело 10А7 хомяка (раскрытое, например, в публикации патента США №20090258013). Антитело 10А7 было изменено двумя различными способами для применения в данном исследовании. Первым было получение химерного антитела с вариабельными областями хомяка и IgG4 S228P человека (тяжелая цепь S228P человека, SEQ ID NO:73) и константными областями каппа (константные области, используемые для МАБ10, SEQ ID NO:75). Во-вторых, было получено химерное антитело с вариабельными областями хомяка и IgG2a N297A мыши, и константными областями каппа (тяжелая цепь: SEQ ID NO:77, легкая цепь: SEQ ID NO:79). Вариабельные области антител представлены в SEQ ID NO:74, 76, 78 и 80. Измененные антитела 10А7 упоминаются в данном документе как «SEC1».
Кинетические измерения для связывания SEC1 с рекомбинантным TIGIT человека, яванского макака и мыши
[0661] Аффинности связывания и кинетику связывания SEC1 IgG2a мыши N297A с TIGIT-His человека, TIGIT-His яванского макака и TIGIT-His мыши (SEQ ID NO: 3) измеряли с применением BLI с помощью инструмента Octet QKe. Применяли стратегию захвата SEC1 на датчиках, с последующей ассоциацией/диссоциацией мономерных белков TIGIT для предотвращения авидных эффектов в анализе. Анализ BLI проводили при 29°С с применением 1X кинетического буфера (ForteBio) в качестве буфера для анализа. Биосенсоры захвата анти-IgG Fc мыши (АМС) (ForteBio) сначала были предварительно замочены в буфере для анализа более 5 минут. SEC1 IgG2a N297A мыши (5 мкг/мл) фиксировали на датчике в течение 300 секунд. Затем датчики погружали в буфер для анализа в течение 120 секунд, чтобы определить базовую линию перед измерением связывания с каждым белком TIGIT. Затем датчики погружали в различные концентрации TIGIT-His человека (от 33,8 до 1,25 нМ, 3-кратные разведения в буфере для анализа), TIGIT-His яванского макака (от 302,8 до 0,42 нМ, 3-кратные разведения в буфере для анализа) или TIGIT-His мыши (от 33 до 1,22 нМ, 3-кратные разведения в буфере для анализа) в течение 300 секунд для измерения ассоциации.
Диссоциацию TIGIT затем измеряли, погружая датчики в буфер анализа в течение 600 секунд. Перемешивание на всех стадиях составляло 1000 об/мин. Кинетические параметры и сенсограммы были получены с помощью программного обеспечения Octet® Data Analysis Software, с применением вычитания контроля, межшаговой коррекции на основе диссоциации, модели связывания 1 к 1 и глобальной подгонки (Rmax не связано с датчиком). Значения KD показаны в Таблице 14.

Измерения KD для связывания с первичными клетками
[0662] KD для связывания SEC1 (IgG4 S228P) с TIGIT клеточной поверхности на первичных клетках измеряли с применением проточной цитометрии, как описано в Примере 6. Для МКПК как человека так и яванского макака, CD8+ Т-лимфоциты имели наибольшую обнаруживаемую экспрессию TIGIT, и поэтому они были использованы для расчета связывания SEC1 с первичными клетками у данных видов. Для целей анализа CD8+ Т-лимфоциты определяли как клетки с размером и зернистостью лимфоцитов, которые экспрессировали следующую комбинацию молекулярных маркеров: CD3+CD4-CD8+. Точно так же, Tregs мыши продемонстрировали наибольшую экспрессию TIGIT и поэтому они использовались для данных расчетов. Tregs мыши были определены как CD4+CD8-CD25+FoxP3+ клетки с размером и зернистостью лимфоцитов. Значения KD показаны в Таблице 15.

Анализ модифицированных TIGIT Jurkat/анти-CD3 HT-1080
[0664] SEC1 антагонизирует функцию TIGIT в анализе совместного культивирования модифицированных TIGIT человека Jurkat/aHTH-CD3 НТ-1080, описанном в Примере 7. Эксперимент проводили 3 раза, а средняя ЕС50 составляла 8,5 нМ. Для сравнения, среднее значение ЕС50 для МАБ10 в этом анализе составляет 0,14 нм.
[0665] Как и МАБ10, SEC1 было описан как антитело, блокирующее лиганд, и оба антитела ингибируют функцию TIGIT в анализе совместного культивирования модифицированных TIGIT человека Jurkat/aHTH-CD3 НТ-1080.
Пример 9: Увеличение продуцирования цитокинов в субоптимально стимулированных Т-лимфоцитах человека после обработки МАБ10
[0666] Было составлено исследование, чтобы определить, является ли МАБ10 эффективным в клеточной in vitro системе с применением первичных Т-лимфоцитов человека, полученных от здоровых доноров. Применяли две различные формы анализа: стимуляцию Т-лимфоцитов в смеси МКПК и стимуляцию CD4+ Т-лимфоцитов после выделения из МКПК. TIGIT экспрессируется в истощенных внутриопухолевых CD8+ Т-лимфоцитах, клетках NK и регуляторных Т-лимфоцитах. Данное исследование было составлено для идентификации и получения более доступного TIGIT, экспрессирующегося первичными Т-лимфоцитами человека, для применения в качестве суррогатной системы для внутриопухолевых клеток-мишеней.
[0667] В CD4+ Т-лимфоцитах экспрессия TIGIT в основном ограничена клетками памяти (CD45RO+). Субоптимальная стимуляция CD4+ Т-лимфоцитов позволяет анализировать эффективность МАБ10 путем измерения увеличения продуцирования ИНФ-γ после ингибирования взаимодействий TIGIT-лиганд.
[0668] Первичные Т-лимфоциты человека были получены от здоровых доноров. Совокупность мононуклеарных клеток периферической крови (МКПК) была выделена из препаратов лейкафереза, a CD4+ Т-лимфоциты в свою очередь были выделены из МКПК.
[0669] МКПК очищали с применением градиентов плотности Ficoll®. Затем МКПК использовали для очистки CD4+ клеток с применением отрицательного отбора (набор выделения CD4 Т-лимфоцитов, Miltenyi) по протоколу производителя.
Анализ FACS ключевых маркеров на человеческих CD4+ Т-лимфоцитах.
[0670] CD4+ Т-лимфоциты субоптимально стимулировали связанным с плашкой анти-CD3 антителом (1 мкг/мл) и растворимым анти-CD28 антителом (2 мкг/мл) в течение 60 часов. Для окрашивания и анализа FACS применяли клетки из нестимулированных и стимулированных образцов. Для окрашивания применяли следующие антитела: анти-TIGIT-PE-Cy7, анти-PVR-PE, анти-CD4-APC-eFluor780 и анти-CD45RA-APC, анти-CD45RO PerCP-eFluor710 и CD226-FITC. Клетки анализировали с помощью проточной цитометрии с применением прибора BD LSRFortessa™.
[0671] Субоптимальной стимуляции МКПК достигали путем добавления низких концентраций анти-CD3 антитела (0,2 мкг/мл). Субоптимальная стимуляция CD4+ Т-лимфоцитов была достигнута путем культивирования клеток в 96-луночных плашках с плоским дном, которые ранее были покрыты 1 мкг/мл анти-CD3 антитела и 2 мкг/мл растворимого анти-CD28 антитела. После 60 часов культивирования супернатанты собирали и замораживали для количественного определения цитокинов с применением ELISA, AlphaLISA® или технологии мультиплекс/Luminex®. Эффект добавления МАБ10 сравнивали с добавлением неспецифического контрольного антитела IgG4.
[0672] Очищенные CD4+ Т-лимфоциты оставляли нестимулированными или их стимулировали в течение 60 часов с применением связанного с плашкой анти-CD3 антитела (1 мкг/мл) и растворимого анти-CD28 антитела (2 мкг/мл). Анализ FACS проводили как с нестимулированными (Фиг. 5А), так и с стимулированными клетками (Фиг. 5В). Были рассчитаны процентное содержание популяции и средняя интенсивность флуоресценции (СИФ). Анализ экспрессии клеточных маркеров TIGIT, PVR и CD226 до и после активации показал, что процентное соотношение как для PVR, так и для CD226-позитивных клеток увеличивается после активации. Для TIGIT процент положительных по TIGIT клеток только умеренно увеличивался при данных условиях активации, но значения СИФ указывали на явное усиление экспрессии TIGIT в популяции позитивных клеток. Анализ FACS также подтвердил, что экспрессия TIGIT ограничивалась в основном клетками памяти (CD45RO+). CD4+ Т-лимфоциты из типичного донора окрашивали по CD45RA (маркер наивных Т-лимфоцитов) и маркеру CD45RO (маркер активированного Т-лимфоцита или Т-лимфоцита памяти), чтобы дифференцировать наивные Т-лимфоциты и Т-лимфоциты памяти. Уровни экспрессии TIGIT были проанализированы в каждой из данных популяций (см. Фиг. 5С).
[0673] Очищенные МКПК, полученные от здоровых доноров, стимулировали в течение 60 часов с применением растворимого анти-CD3 антитела (0,2 мкг/мл) в присутствии различных концентраций МАБ или контрольного антитела IgG4. Супернатанты клеточной культуры собирали и использовали для измерения продуцирования провоспалительных цитокинов. Анализ образцов двух человеческих доноров, показанные на Фиг. 6А-6К, показал, что лечение с помощью каждого МАБ индуцирует повышенную экспрессию ИНФ-γ. Затем МАБ10 применяли для индукции продуцирования нескольких провоспалительных цитокинов в МКПК из донора 1, включая фактор некроза опухоли альфа (ФНО, Фиг. 6L), лимфотоксин альфа (LT-α, Фиг. 6М) и интерферон-гамма (ИНФ-γ, Фиг. 6N). Графический анализ ЕС50 для ИНФ-γ показан на Фиг. 6O. МКПК из донора 2 были одинаково обработаны с помощью МАБ10, и цитокины были индуцированы как показано на Фиг. 7А (ИНФ-γ), Фиг. 7В (ФНО), Фиг. 7С (ИЛ-6), Фиг. 7D (GM-CSF) и Фиг. 7Е (LT-α)). Значение EC50 для МАБ10 в данном анализе по двух тестируемых донорах усреднялось как ~16 нМ, путем определения концентрации МАБ10, необходимой для индукции 50% увеличения сигнала ИНФ-γ, ФНО и LT-α. Краткое изложение данных по ФНО для двух доноров (Фиг. 6) показано в Таблице 16.
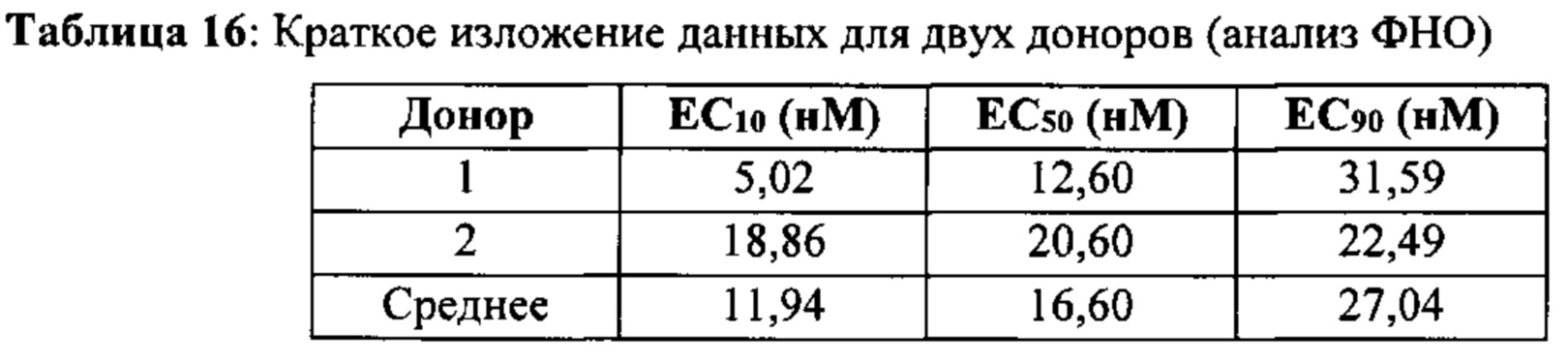
[0674] Очищенные CD4+ Т-лимфоциты, полученные от 3-х здоровых доноров, стимулировали в течение 60 часов с применением связанного с плашками анти-CD3 антитела (1 мкг/мл) и растворимого анти-CD28 антитела (2 мкг/мл) в присутствии различных концентраций контрольного антитела IgG4 или МАБ10. Супернатанты клеточной культуры собирали и использовали для измерения уровней продуцирования ИНФ-γ.
[0675] В данных субоптимально стимулированных CD4+ Т-лимфоцитах добавление МАБ10 приводит к увеличению экспресси ИНФ-γ дозозависимым образом у всех трех доноров, демонстрируя анти-TIGIT антагонистическую функцию МАБ10 (см. Фиг. 8А (донор 1), Фиг. 8В (донор 2) и Фиг. 8С (донор 3)). Продуцирование ИНФ-γ в клетках, обработанных либо МАБ10 (черные столбцы), либо контрольным изотипом IgG4 (светлосерые столбцы), показано на левой панели каждой фигуры. Среднее значение EC50 для МАБ10 в данном анализе рассчитывали как 1,02 нМ путем определения концентрации МАБ10, необходимой для индукции 50% увеличения сигнала ИНФ-γ (нанесенного на график в правой панели каждой из Фиг. 8А-8С). Данные приведены в Таблице 17.
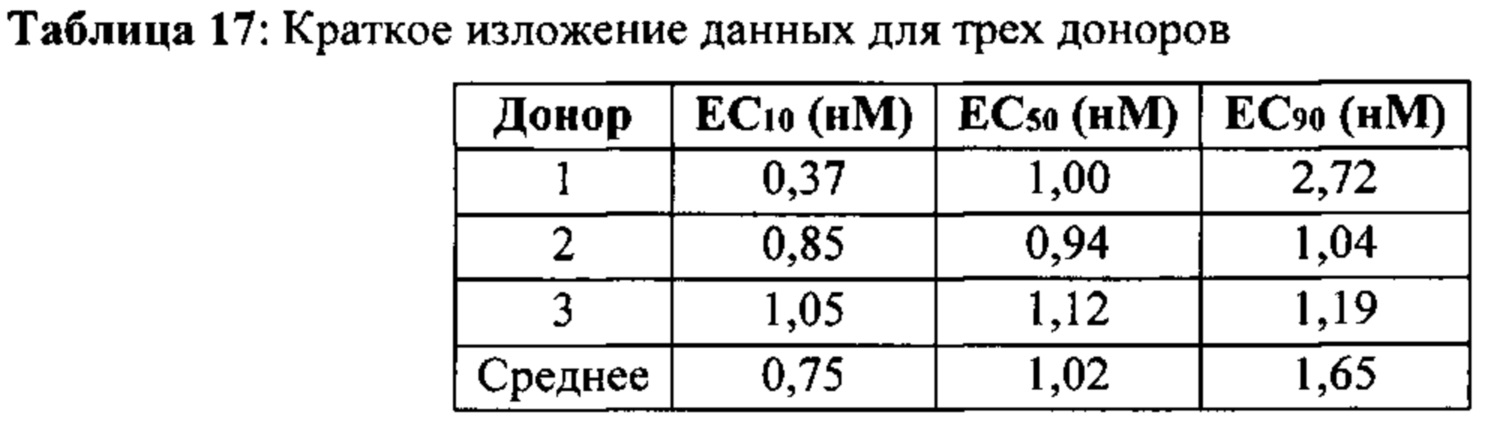
[0676] Как описано выше, добавление МАБ10 к субоптимально стимулированным Т-лимфоцитам человека антагонизирует функцию TIGIT и индуцирует повышение экспрессии провоспалительных цитокинов (например, ИНФ-γ и ФНО) по сравнению с неспецифическим контрольным антителом IgG4. Данный эффект зависит от дозы с оценкой ЕС50 1 нМ для анализа выделенных CD4+ Т-лимфоцитов. Эти данные демонстрируют in vitro эффективность МАБ10 в нормальных первичных Т-лимфоцитах человека.
Пример 10: Характеристика МАБ10 в комбинированном биоанализе PD-1/TIGIT
[0677] PD-1 представляет собой иммунный ингибирующий рецептор, экспрессируемый на активированных Т-лимфоцитах и В-лимфоцитах, и он играет критическую роль в регуляции иммунных реакций на опухолевые антигены и аутоантигены. Активация PD-1 одним из его лигандов PD-L1 или PD-L2 на соседней клетке ингибирует сигналинг Т-клеточного рецептора (TCR) и опосредованные TCR пролиферацию, активацию транскрипции и продуцирование цитокинов. Терапевтические антитела и гибридные белки Fc, спроектированы для блокирования взаимодействия PD-1/PD-L1, показывают многообещающие результаты в клинических испытаниях для лечения различных видов рака.
[0678] Комбинированный биоанализ PD-1/TIGIT (Promega) является биологически релевантным механизмом основанного на действии анализа, который может быть использован для измерения эффективности и стабильности антител и других биологических препаратов, предназначенных для блокирования PD-1/PD-L1 и TIGIT/CD155 в комбинации. Анализ состоит из двух генетически модифицированных клеточных линий: эффекторных клеток PD-1/TIGIT, которые являются Jurkat Т-лимфоцитами, стабильно экспрессирующими PD-1 человека, TIGIT и репортер люциферазы, и клеток PD-L1/CD155 АРС/СНО-K1, которые представляют собой клетки СНО-K1, стабильно экспрессирующие PD-L1 человека, CD155 человека и белок клеточной поверхности (в данном случае TIGIT), предназначенный для активации родственных TCRs антиген-независимым образом.
[0679] Когда совместно культивируются два типа клеток, взаимодействия PD-1/PD-L1 и TIGIT/CD155 ингибируют сигналинг TCR и активность люциферазы. Добавление антитела, например АВР, раскрытого в данном документе или известного в данной области техники, которое связывает TIGIT и блокирует связывание с лигандом (например, CD 155) в комбинации с вторым антителом, которое блокирует взаимодействие PD-1 с его лигандом (например, PD-L1), высвобождает ингибирующий сигнал и вызывает сигналинг TCR и активность люциферазы, опосредованную NFAT.
[0680] На Фиг. 9А показаны результаты анализа, в котором использовалось соотношение 1:1 МАБ10 и пембролизумаба (анти-PD-1 антитело). Концентрации для каждого антитела составляли 25, 10, 4, 1,6, 0,64, 0,256, 0,1024, 0,04096 и 0,016384 мкг/мл. В качестве контроля использовали нецелевой IgG4. Как показано на Фигуре, только комбинация МАБ10 и пембролизумаба (ЕС50 5,06 нМ) блокировала связывание в достаточной степени, чтобы индуцировать активность люциферазы в клетках Jurkat. Ни контрольное IgG4, ни комбинация IgG4+МАБ10 не индуцировали люциферазу.
[0681] Затем анализ повторяли с фиксированной дозой пембролизумаба 1 мкг/мл (и фиксированной дозой IgG4 1 мкг/мл) и варьирующей дозой МАБ10 (50, 20, 8, 3,2, 1,28, 0,512, 0,2048, 0,08192 и 0,032768 мкг/мл). Как показано на Фиг. 9В, в то время как фиксированная доза пембролизумаба приводила к низкому уровню активации индукции люциферазы, комбинация пембролизумаба и МАБ10 была намного более эффективной при индукции люциферазы с EC50 0,78 нМ. Как и на Фиг. 9А, ни только контрольный IgG4, ни комбинация IgG4+МАБ10 не индуцировали активность люциферазы.
Пример 11: Комбинированная терапия ЦМВ+ Т-лимфоцитов с помощью МАБ10 и пембролизумаба
[0682] Анализ лимфопролиферации применяли для тестирования Т-клеточных ответов в положительных на цитомегаловирус (ЦМВ+) Т-лимфоцитах. МКПК от разных доноров, которые были скринированы на реактивность к антигену ЦМВ, были приобретены у Astarte Biologics (Бовелл, Вашингтон). Клеточные лизаты из клеток, инфицированных ЦМВ, также были приобретены у Astarte Biologics. МКПК высевали и проводили антигенспецифическую стимуляцию путем добавления клеточного лизата, который стимулирует ЦМВ+ Т-лимфоциты в образце. Добавляли МАБ10, контрольный IgG4 и/или анти-PD-1 антитело пембролизумаб. Клетки культивировали в течение пяти дней, и супернатанты собирали и анализировали для получения эффекторного цитокина ФНО. Дополнительные данные были собраны, проводя окрашивание внутриклеточных цитокинов для других эффекторных молекул, включая ИЛ-2, ИНФ-γ, перфорин и гранзим-В.
[0683] Клетки из одного донора (донор 1) стимулировали и культивировали, как описано выше. Как показано на Фиг. 10, путем пропускания CD4+ клеток, инкубация с МАБ10 (черные столбцы) увеличивает продуцирование эффекторных цитокинов дозозависимым способом, как измерено с помощью внутриклеточного окрашивания, включая ФНО (Фиг. 10А), ИЛ-2 (Фиг. 10В) и ФНО-γ (Фиг. 10С) в большей степени, чем клетки, инкубированные с контрольным IgG4 (белые столбцы). Инкубация с МАБ10 также увеличивает долю антигенспецифических активированных CD4+ Т-лимфоцитов, как показано на Фиг. 10D, в которой клетки, которые обрабатывались 20 мкг/мл контрольного IgG4 или МАБ10, анализировали с помощью FACS по экспрессии CD3 (маркер зрелых Т-лимфоцитов) и экспрессии ФНО и ИЛ-2.
[0684] Аналогичные результаты были получены путем пропускания CD8+ клеток. Как показано на Фиг. 11, на пропущенных CD8+ клетках, инкубация с МАБ10 (черные столбцы) увеличивает продуцирование эффекторных цитокинов дозозависимым способом, включая ФНО (Фиг. 11А), перфорин (Фиг. 11В) и гранзим В (Фиг. 11С) по сравнению с клетками, инкубированными с контрольным IgG4 (белые столбцы). Перфорин и гранзим В являются маркерами активированных цитотоксических Т-лимфоцитов. Инкубация с МАБ10 также увеличивает долю антигенспецифических активированных CD8+ Т-лимфоцитов, как показано на Фиг. 11D. Клетки, которые были обработаны 20 мкг/мл контрольного IgG4 или МАБ10, анализировали с помощью FACS по экспрессии CD3, и экспрессии перфорина и гранзима В.
[0685] Клетки из того же донора использовали в аналогичном наборе экспериментов, чтобы показать, что блокирование МАБ10 усиливает ЦМВ-специфичные ответы CD8+ Т-лимфоцитов. Клетки инкубировали с рядом концентраций МАБ10 (черные столбцы) или с контрольным IgG4 (белые столбцы), и анализировали процент популяции, дважды позитивной по перфорин + гранзим В + (Фиг. 12А) или ИНФ-γ+ФНО+ (Фиг. 12С). На Фиг. 12В (анализ перфорин + гразим В +) и 12D (анализ ИНФ-γ+ФНО+) показана доля дважды позитивных клеток, сравниваемых с клетками, обработанными 20 мкг/мл контрольного антитела (левые панели) или 20 мкг/мл МАБ10 (правые панели). Клетки, обработанные МАБ10, показали гораздо большее продуцирование эффекторных цитокинов по сравнению с клетками, обработанным контролем.
[0686] Комбинированный эффект МАБ10 и PD-1 антитела пембролизумаба тестировали с применением того же донора, который описан выше. Клетки стимулировали лизатами ЦМВ, как описано выше, и обрабатывали 2 мкг/мл пембролизумаба или контрольного IgG4, и 10, 20 или 40 мкг/мл контрольного антитела или МАБ10, и измеряли продуцирование ФНО в супернатанте. Как показано на Фиг. 13, тестировали четыре группы клеток, обработанные контрольным IgG4 (белые столбцы, самая левая группа), константным количество контрольного IgG4 и титрами МАБ10 (темно-серые столбцы, вторая группа слева), константным количество пембролизумаба и титрами IgG4 (светло-серые столбцы, вторая группа справа), или константным количество пембролизумаба и титрами МАБ10 (черные полосы, правая группа). Комбинация пембролизумаб и МАБ10 увеличивала продукцию ФНО выше эффекта, наблюдаемого с помощью отдельных агентов.
[0687] Комбинацию снова тестировали на трех разных донорах, применяя описанный выше анализ. Клетки стимулировали лизатом ЦМВ, и обрабатывали 20 мкг/мл МАБ10 или 20 мкг/мл контрольного IgG4-антитела, и титрами пембролизумаба, и измеряли продуцирование ФНО. Как показано на Фиг. 14А (донор 1), Фиг. 14В (донор 2) и Фиг. 14С (донор 3), добавление МАБ10 (черные столбцы), отдельно или в сочетании с возрастающими концентрациями пембролизумаба, приводит к увеличению продуцирования ФНО по сравнению с контрольной группой антитело + пембролизумаб (белые столбцы). Кроме того, МАБ10 (черные столбцы) в комбинации с пембролизумабом также приводило к увеличению активации по сравнению с только МАБ10. Статистические различия были рассчитаны только между МАБ10 и группами МАБ10+пембролизумаб с применением t-критерия Стьюдента (*=р<0,05, **=р<0,01, ***=р<0,005, ****=р<0,001)
[0688] В совокупности данные, представленные в примере, демонстрируют явный дозозависимый эффект МАБ10 как единственного агента в антигенспецифических анализах ответа. Кроме того, данные показывают повышенную эффективность при комбинировании МАБ10 и пембролизумаба для нескольких доноров, что указывает на ценность АВР, раскрытых в данном документе, и ингибиторов PD-1 или ингибиторов PD-L1 в качестве комбинированной терапии.
ВКЛЮЧЕНИЕ ПОСРЕДСТВОМ ССЫЛКИ
[0689] Все раскрытия всех патентных и непатентных публикаций, цитируемых в настоящем документе включены посредством ссылки в полном объеме для всех целей.
ДРУГИЕ ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ
[0690] Раскрытие изобретения, изложенное выше, может охватывать множество различных изобретений с независимой полезностью. Хотя каждое из данных изобретений раскрыто в его предпочтительной форме(-ах), его конкретные варианты осуществления, как раскрыто и проиллюстрировано в данном документе, не должны рассматриваться в ограничивающем смысле, поскольку возможны многочисленные вариации. Объект изобретений включает все новые и неочевидные комбинации и подкомбинации различных элементов, признаков, функций и/или свойств, раскрытых в данном документе. Нижеследующие пункты формулы особым образом указывают на некоторые комбинации и подкомбинации, которые считаются новыми и неочевидными. Изобретения, воплощенные в других комбинациях и подкомбинациях признаков, функций, элементов и/или свойств, могут быть заявлены в данной заявке, в заявках, претендующих на приоритет по данной заявке, или в связанных заявках. Такие пункты формулы, независимо от того, направлены ли они на другое изобретение или на одно и то же изобретение, и более широкие, более узкие, равные или разные по объему по сравнению с первоначальными пунктами формулы изобретения, также считаются включенными в объект изобретений настоящего раскрытия изобретения.
ПРИЛОЖЕНИЕ А: ТАБЛИЦА ССЫЛОК НА ПОСЛЕДОВАТЕЛЬНОСТИ