Результат интеллектуальной деятельности: ПРЕПАРАТ АКТИВАТОРА ГЛЮКОКИНАЗЫ ДЛЯ ПЕРОРАЛЬНОГО ВВЕДЕНИЯ И СПОСОБ ЕГО ПОЛУЧЕНИЯ
Вид РИД
Изобретение
[0001] Настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, точнее, настоящее изобретение относится к препарату для перорального введения активатора глюкокиназы с модифицированным высвобождением действующего вещества, способу его получения и его применению для лечения конкретных заболеваний.
[0002] В дополнительном варианте осуществления настоящее изобретение относится к регулированию высвобождения действующего вещества препарата активатора глюкокиназы для перорального введения в организме человека для достижения повышения эффективности и снижения побочных эффектов. В организме человека модифицированное высвобождение действующего вещества препарата активатора глюкокиназы для перорального введения, раскрытого в настоящем изобретении, соответствует фармакокинетике (ФК) с фармакодинамикой (ФД) (корреляция ФК/ФД) во время лечения заболевания. Модифицированное высвобождение действующего вещества включает медленное высвобождение действующего вещества препарата активатора глюкокиназы для перорального введения в желудочно-кишечном тракте организма человека и быстрое высвобождение действующего вещества препарата активатора глюкокиназы для перорального высвобождения в тонком кишечнике в организме человека. Настоящее изобретение относится к твердой дисперсии активатора глюкокиназы, используемой в препарате активатора глюкокиназы для перорального введения, композиции твердой дисперсии активатора глюкокиназы и способу их получения, а также к типам полимерных носителей. Настоящее изобретение также относится к способу получения препарата активатора глюкокиназы для перорального введения.
[0003] Настоящее изобретение относится к применению препарата активатора глюкокиназы для перорального введения, твердой дисперсии и композиции твердой дисперсии для лечения и/или предотвращения выбранных заболеваний и медицинских расстройств, в частности одного или нескольких заболеваний, выбранных из группы, состоящей из диабета I типа, диабета II типа, нарушения толерантности к глюкозе, нарушения гликемии натощак и гипергликемии. Кроме того, настоящее изобретение относится к способу лечения и/или предотвращения указанных заболеваний и медицинских расстройств, включающему введение терапевтически эффективного количества препаратов для перорального введения, раскрытых в настоящем изобретении, в том числе препарата для перорального введения с модифицированным высвобождением действующего вещества, пациенту, нуждающемуся в этом.
Уровень техники изобретения
Диабет II типа и активаторы глюкокиназы
[0004] Сахарный диабет стал широко распространенным по всему миру заболеванием: в мире им страдают 415 миллионов пациентов, в Китае - 110 миллионов пациентов (International Diabetes Federation, Diabetes Atlas, 2015). Пациенты с сахарным диабетом II типа, т.е. инсулинорезистентным сахарным диабетом (non-insulin dependent diabetes mellitus - NIDDM), составляют более 90% пациентов, страдающих диабетом. Это хроническое гипергликемическое нарушение обмена веществ, возникающее в результате дисбаланса в крови гомеостаза глюкозы в организме человека, вызванного нарушением секреции инсулина и инсулинорезистентностью. Баланс содержания глюкозы в крови в организме человека регулируется, в основном, двумя гормонами, которые контролируют уровень глюкозы в крови, включая инсулин и глюкагон. GLP-1 (глюкагоноподобный пептид-1) участвует в регуляции секреции инсулина, а также является молекулярным фактором и терапевтическим лекарственным средством при диабете, играющим важную роль в поддержании баланса глюкозы в крови в организме человека. Аналоги инсулина и GLP-1 стали высокоэффективными лекарственными средствами для лечения сахарного диабета.
[0005] Глюкокиназа (GK) представляет собой IV изотип фермента гексокиназы (Colowick, S.P., The hexokinase, in The Enzymes, 3rd ed., Boyer, P.D., Ed., Vol. 9, Academic Press, New York, 1973, chap. 1), а изменение ее активности регулируется концентрацией глюкозы. Она может реагировать на изменение концентрации глюкозы в организме, регулировать секрецию гормонов метаболизма глюкозы, включая инсулин, глюкагон и GLP-1, и при этом быстро превращать поглощенную после принятия пищи глюкозу в печеночный гликоген в печени для поддержания баланса сахара в крови. Таким образом, глюкокиназа играет центральную роль в стабилизации баланса содержания глюкозы в крови в организме человека. Юношеский инсулинорезистентный диабет взрослого типа (MODY-2) - это функциональное нарушение, вызванное функциональной мутацией гена глюкокиназы, в результате чего мутированная глюкокиназа активируется при более высоких концентрациях глюкозы. Это ухудшает глюкозо-стимулированную функцию секреции инсулина в островках пациентов, снижает способность синтеза гликогена в печени и в конечном итоге приводит к гипергликемии. Исследования показали, что экспрессия и функция глюкокиназы в печени и островках пациентов с диабетом II типа значительно ниже, чем у здоровых пациентов. Поэтому повышение активности глюкокиназы у пациентов с диабетом может применяться для лечения гипергликемии и диабета II типа, вызванного нарушением толерантности к глюкозе.
[0006] Глюкокиназа распределяется, главным образом, в печени, которая в ответ на повышенное содержание глюкозы в крови быстро превращает глюкозу в печеночный гликоген для «хранения», снижая такие образом ее содержание в крови. Глюкокиназа экспрессируется в эндокринных клетках и в альфа- и бета-клетках островков, а также в L-клетках в кишечнике и является основным функциональным белком, который регулирует секрецию глюкагона, инсулина и GLP-1, стимулированную глюкозой. Активаторы глюкокиназы разрабатываются в соответствии с характеристиками этих мишеней и способны систематически стабилизировать уровень глюкозы в крови в организме повышением чувствительности альфа-, бета- и L-клеток к изменениям концентрации глюкозы; улучшением функциональной секреции инсулина, глюкагона и GLP-1, регулируемой глюкозой; регулированием экспорта глюкозы в печень для стимулирования синтеза гликогена в печени и других синергических механизмов. Поэтому активаторы глюкокиназы стали одним из самых популярных предметов разработки для получения новых лекарственных средств для лчения диабета II типа (диабет 2 типа) (Matschinsky FM, Nat. Rev. Drug Discov. 2009, 8(5): 399-416).
[0007] Снижение экспрессии и функции глюкокиназы вызывает нарушение секреции инсулина на ранней стадии и нарушение выработки гликогена в печени. Лекарственные средства для лечения диабета в современном клиническом применении, включая инсулин, не могут решить эту проблему. Существует клиническая потребность в области лечения диабета. [1-((R)-2,3-дигидроксипропил)-1H-пиразол-3-ил]амид (S)-2-[4-(2-хлорфенокси)-2-оксо-2,5-дигидропиррол-1-ил]-4-метилпентановой кислоты (называемый далее в описании «соединение HMS5552») в настоящее время является наиболее перспективным лекарственным средством для лечения диабета, которое может удовлетворить вышеупомянутые клинические потребности. Гипогликемические лекарственные средства для перорального введения представляют собой препараты первого выбора для клинического применения ввиду легкости их введения, хорошей переносимости и безопасности. Новые лекарственные активаторы глюкокиназы также подходят для получения препаратов для перорального введения, особенно для получения твердых препаратов для перорального введения. Препараты для перорального введения могут подразделяться на твердые препараты для перорального введения и жидкие препараты для перорального введения. Твердые препараты для перорального введения включают таблетки, капсулы, гранулы, порошки, пастилки, пилюли и т.п.
Сущность изобретения
[0008] В сочетании характеристик изменения содержания глюкозы в крови у пациентов с сахарным диабетом в течение дня, включая регуляцию содежания глюкозы натощак и в постпрандиальном периоде, мишени и механизма глюкокиназы, ее распределения в организме человека, а также функции рецептора регулирования уровня глюкозы в крови и др., авторы настоящего изобретения разрабатывают и предоставляют препарат для перорального введения, подходящий для активаторов глюкокиназы, у которого фармакокинетика (ФК) и фармакодинамика (ФД) являются согласованными (корреляция ФК/ФД).
[0009] Поскольку основные органы-мишени глюкокиназы распределяются в печени, поджелудочной железе и кишечнике, настоящее изобретение предусматривает достижение своевременной или одновременной активации каждого органа-мишени активатором глюкокиназы, тем самым обеспечивая эффективность и безопасность лекарственного средства.
[0010] Препарат активатора глюкокиназы для перорального введения по настоящему изобретению разработан для 1) достижения подходящего снижения высвобождения действующего вещества в желудке и быстрого высвобождения в тонком кишечнике; 2) использования рН кишечной среды для регулирования высвобождения и абсорбции активатора глюкокиназы. Быстрое высвобождение активатора глюкокиназы в тонком кишечнике человека способствует своевременному или одновременному поступлению лекарственных средств в кишечник, островки и органы-мишени печени, достижению мишеней на множестве сайтов, синергическому гипогликемическому, клинически полезному действию и проявлению лучшего терапевтического эффекта при снижени токсических или побочных эффектов.
[0011] Соответственно, предметом настоящего изобретения является препарат активатора глюкокиназы для перорального введения, в частности препарат для перорального введения с модифицированным высвобождением действующего вещества, и способ его получения, где препарат содержит твердую дисперсию активатора глюкокиназы и эксципиенты.
[0012] Другим предметом настоящего изобретения является твердая дисперсия, содержащая активатор глюкокиназы, включая композицию твердой дисперсии, способ ее получения и типы полимерных носителей.
[0013] Еще одним предметом настоящего изобретения является композиция твердой дисперсии, содержащая активатор глюкокиназы, включая твердую дисперсию по изобретению, и эксципиенты.
[0014] Еще одним предметом настоящего изобретения является способ и применение для лечения и/или предотвращения одного или нескольких заболеваний, выбранных из группы, состоящей из диабета I типа, диабета II типа, нарушения толерантности к глюкозе, нарушения гликемии натощак и гипергликемии, препарата активатора глюкокиназы для перорального введения, включая препарат для перорального введения с модифицированным высвобождением действующего вещества, твердую дисперсию или композицию твердой дисперсии.
[0015] Другие предметы настоящего изобретения станут понятными специалистам в данной области техники из описания и примеров.
Определения
[0016] Термин «примерно», когда используется в настоящем изобретении, означает указанное значение ±5% указанного значения.
[0017] Термин «% по массе» (% масс.) означает процент из расчета на общую массу твердой дисперсии.
[0018] Термин «твердая дисперсия» (solid dispersion - SD) означает твердую дисперсионную систему, полученную диспергированием одного или нескольких фармацевтических активных ингредиентов в неактивных адъювантах или носителях. В твердой дисперсии лекарственные средства в носителях находятся в виде молекулы, коллоида, микрокристаллической формы, аморфной формы или их смеси и т.п. (Naveen Dutt Dixit, Suneel Kumar Niranjan. A REVIEW: SOLID DISPERSION. WORLD JOURNAL OF PHARMACY AND PHARMACEUTICAL SCIENCES, 2014, Vol. 3, Issue 9: 238-257). Твердые дисперсии в зависимости от распределения молекул лекарственного средства в твердых носителях включают следующие типы: смесь, полученная при совместном плавлении; твердый раствор, в том числе сплошной твердый раствор и несплошной твердый раствор; раствор заместительной кристаллизации; раствор кристаллизации внедрения; аморфный твердый раствор; стекловидный раствор, стекловидная суспензия и т.д. (Shrawan Baghel, Helen Cathcart, Niall J. O'Reilly. Polymeric Amorphous Solid Dispersions: A Review of Amorphization, Crystallization, Stabilization, Solid-State Characterization, and Aqueous Solubilization of Biopharmaceutical Classification System Class II Drugs. Journal of Pharmaceutical Sciences 105 (2016) 2527-2544). Твердые дисперсии могут быть получены методами экструзии горячего расплава твердой смеси, распылительной сушки жидкой смеси, «расплав-растворитель» и т.п. (T. Vasconcelos, B. Sarmento, P. Costa, Solid dispersions as strategy to improve oral bioavailability of poor water soluble drugs, Drug Disc.Today 12 (2007) 1068-1075).
[0019] EUDRAGIT - это торговое название синтетических фармацевтических адъювантов, которые включают сополимер метакриловой кислоты и сополимер метакрилата и широко известны как полиакрилатные смолы. Полиакрилатные смолы подразделяют на различные типы в зависимости от их композиции, соотношения компонентов и степени полимеризации. Среди них Eudragit E представляет собой полимер диметиламиноэтилметакрилата и метакрилата; Eudragit L - полимер метакриловой кислоты и метилметакрилата, где соотношение свободный карбоксил:эфир составляет 1:1, Eudragit S - полимер метакриловой кислоты и метилметакрилата, где соотношение свободный карбоксил:эфир составляет 1:2.
[0020] Термины «эффективное количество» или «терапевтически эффективное количество» относятся к количеству лекарственного средства, достаточному для обеспечения желаемого биологического результата. Биологическим результатом может быть уменьшение и/или облегчение признаков, симптомов или причин заболевания или любое другое желаемое изменение биологической системы. Например, «эффективное количество» для терапевтического применения представлят собой количество композиции, содержащей соединение по настоящему изобретению, необходимое для обеспечения клинически значимого уменьшения тяжести заболевания. Подходящее «эффективное» количество в любом отдельном варианте осуществления может быть определено специалистом в данной области техники с использованием стандартных экспериментов. Таким образом, выражение «эффективное количество» обычно относится к количеству, в котором действующее вещество оказывает терапевтическое действие.
[0021] Термины «лечить» или «лечение», когда используются в настоящем изобретении, являются синонимами термина «предотвращать» и предназначены для обозначения задержки развития заболеваний, предотвращения развития заболеваний и/или снижения тяжести таких симптомов, которые будут развиваться или ожидается, что будут развиваться. Таким образом, эти термины включают уменьшение интенсивности существующих симптомов заболевания, предотвращение появления дополнительных симптомов, уменьшение интенсивности или предотвращение появления основных метаболических причин симптомов, ингибирование расстройства или заболевания, например предотвращение развития расстройства или заболевания, облегчение расстройства или заболевания, вызывающее регрессию расстройства или заболевания, облегчение состояния, вызванного заболеванием или расстройством, или купирование симптомов заболевания или расстройства.
[0022] Термин «фармацевтически приемлемый» или «фармакологически приемлемый» означает материал, который не является биологически или иным образом нежелательным, т.е. материал может вводиться индивидууму без причинения минимального нежелательного биологического эффекта или без вредного взаимодействия с любым из компонентов композиции, в которой он содержится.
[0023] Термин «пациент» или «субъект», когда используется в настоящем описании, включает млекопитающих и не млекопитающих. Примеры млекопитающих включают, но без ограничения, любого представителя класса млекопитающих: людей, приматов кроме человека, таких как шимпанзе и другие виды приматов и обезьян; сельскохозяйственных животных, таких как крупный рогатый скот, лошади, овцы, козы, свиньи; домашних животных, таких как кролики, собаки и кошки; лабораторных животных, включая грызунов, таких как крысы, мыши и морские свинки, и т.п. Примерами не млекопитающих являются, но без ограничения, птицы, рыбы и т.п. В одном варианте настоящего изобретения млекопитающим является человеком.
[0024] Соединения, которые могут использоваться в качестве активного ингредиента твердой дисперсии активатора глюкокиназы по настоящему изобретению, могут образовывать соли, которые также включены в область настоящего изобретеия. Подразумевается, что ссылка на соединение, раскрытое в настоящем документе, включает ссылку на его соли, если не указано иное. Термин «соль(и)», когда используется в настоящем изобретении, означает соли, образованные с неорганическими и/или органическими кислотами, а также соли, образованные с неорганическими и/или органическими основаниями. Кроме того, когда соединение содержит основной фрагмент, такой как, но без ограничения, пиридин или имидазол, и кислотный фрагмент, такой как, но без ограничения, карбоновую кислоту, могут образовываться цвиттерионы («внутренние соли»), которые включены в термин «соль(и)», используемый в настоящем описании. Фармацевтически приемлемые (т.е. нетоксичные, физиологически приемлемые) соли являются предпочтительными, хотя также применимы и другие соли. Соли соединений могут быть получены, например, взаимодействием соединения, описанного в настоящем изобретении, с количеством кислоты или основания, таким как эквивалентное количество, в среде, такой как среда, из которой осаждается соль, или в водной среде (с использованием лиофилизации после взаимодействия).
[0025] Подразумевается, что различные соединения и их соли, сольваты, сложные эфиры и пролекарства и их полиморфы включены в настоящее изобретение.
[0026] Следует иметь ввиду, что используемая в описании терминология предназначена для описания конкретных вариантов осуществления, но не предназначена для ограничения. Кроме того, хотя любые способы, устройства и материалы, аналогичные или эквивалентные описанным в настоящем изобретении, могут использоваться при практическом применении или испытании настоящего изобретения, описанные в изобретении способы, устройства и материалы являются предпочтительными.
[0027] Термин «алкил», когда используется в настоящем изобретении сам по себе или в сочетании с другими группами, относится к разветвленному или прямому одновалентному насыщенному алифатическому углеводородному радикалу, содержащему от одного до двадцати атомов углерода, предпочтительно от одного до шестнадцати атомов углерода, более предпочтительно от одного до десяти атомов углерода.
[0028] Термин «низший алкил» сам по себе или в сочетании с другими группами относится к разветвленному или прямому алкильному радикалу, содержащему от одного до девяти атомов углерода, предпочтительно от одного до шести атомов углерода. Этот термин иллюстрируется такими радикалами, как метил, этил, н-пропил, изопропил, н-бутил, сим-бутил, изобутил, трет-бутил, н-пентил, 1-этилпропил, 3-метилбутил, н-гексил, 2-этилбутил и т.п. Особенно предпочтительными являются метил и этил.
[0029] Термин «низший алкенил», когда используется в настоящем изобретении сам по себе или в комбинации с другими группами, относится к прямой или разветвленной углеводородной группе, содержащей от одного до девяти атомов углерода, предпочтительно от одного до шести атомов углерода, и олефиновые связи. Предпочтительным низшим алкенилом является 2-пропенил.
[0030] Термин «циклоалкил» относится к моновалентному моно- или поликарбоциклическому радикалу, содержащему от трех до десяти атомов углерода, предпочтительно от трех до семи атомов углерода, более предпочтительно от четырех до шести атомов углерода. Этот термин иллюстрируется такими радикалами, как циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, бомил, адамантил, бицикло[2.2.1]гептил, инденил и т.п. В предпочтительном варианте термин «циклоалкил» означает циклобутил, циклопентил или циклогексил.
[0031] Термин «гетероциклил» означает моно- или полициклическое насыщенное кольцо, в котором один, два или три атома углеродного кольца заменены гетероатомами, такими как атомы N, O или S. Примеры гетероциклильных групп включают, но без ограничения, морфолинил, тиоморфолинил, пиперазинил, пиперидинил, пирролидинил, тетрагидропиранил, тетрагидрофуранил, 1,3-диоксанил и т.п. Предпочтительными гетероциклильными группами являются пирролидинил, пиперидинил, морфолинил или тетрагидропиранил. Гетероциклильные группы могут быть незамещенными или замещенными, и присоединение может осуществляться по углеродной структуре или через гетероатом(ы), когда это приемлемо, с учетом того, что указанные заместители, в свою очередь, не замещаются далее, если в приведенных ниже примерах или формуле изобретения не указано иное.
[0032] Термин «арил» относится к ароматическому моно- или поликарбоциклическому радикалу, содержащему от 6 до 12 атомов углерода и включающему по меньшей мере одно ароматическое кольцо. Примеры таких групп включают, но без ограничения, фенил, нафтил, 1,2,3,4-тетрагидронафталин, 1,2-дигидронафталин, инданил, 1H-инденил и т.п. Предпочтительными арильными группами являются фенил или нафтил, причем фенил является особенно предпочтительным.
[0033] Термин «гетероарил» относится к ароматическому моно- или полициклическому радикалу, содержащему от 5 до 12 атомов и включающему по меньшей мере одно ароматическое кольцо с одним, двумя или тремя гетероатомами в кольце, выбранными из атомов N, O и S, при этом остальными атомами кольца являются атомы C. Один или два атома углерода в кольце гетероарильной группы могут быть замещены на карбонильную группу. Предпочтительные гетероарильные кольца выбраны из группы, состоящей из пирролила, пиразолила, имидазолила, триазолила, тетразолила, оксазолила, оксадиазолила, изоксазолила, тиадиазолила, тиазолила, фуранила, тиенила, пиранила, пиридила, пиразинила, пиримидинила, пиридазинила, индолила, изоиндолила, индазолила, 7-азаиндолила, хинолинила, изохинолинила, изохинолинила, цинолинила, пиразоло[1,5-а]пиридила, имидазо[1,2-а]пиридила, хиноксалинила, бензофуранила, бензоксазинила, бензотиазолила, бензотриазолила, хроменила, хроманила, изохроманила, кумаринила, изокумаринила и бензопиранила. Предпочтительные гетероарильные группы выбраны из группы, состоящей из 1Н-пиразол-3-ила, тиазол-2-ила, [1,2,4]тиадиазол-5-ила, [1,3,4]тиадиазол-2-ила, пиридила, пиразинила и пиримидинила.
[0034] Термин «гетероарил» относится к ароматическому моно- или полициклическому радикалу, содержащему от 5 до 12 атомов и включающему по меньшей мере одно ароматическое кольцо с одним, двумя или тремя гетероатомами в кольце, выбранными из атомов N, O и S, при этом остальными атомами кольца являются атомы C. Один или атома углерода в кольце гетероарильной группы могут быть замещены на карбонильную группу.
[0035] Термин «низший алкокси», когда используется в настоящем изобретении, означает группу R'-O-, где R' представляет собой низший алкил, а значение термина «низший алкил» определено ранее. Примерами низших алкоксигрупп являются метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, втор-бутокси и трет-бутокси, предпочтительно метокси и этокси.
[0036] Термин «низший алкоксиалкил» относится к группе -Rʺ-O-R', где R' означает низшую алкильную группу, определенную в настоящем описании, и Rʺ представляет собой низшую алкиленовую группу, такую как метилен, этилен или пропилен. Примерами низших алкоксиалкильных групп являются метоксиметил или 2-метоксиэтил.
[0037] Термин «галоген», когда используется в настоящем изобретении, означает радикал фтора, хлора, брома или йода, предпочтительно радикал фтора, хлора или брома, более предпочтительно радикал фтора или хлора.
[0038] Термин «низший галогеналкил» относится к низшим алкильным группам, определенным выше, в которых по меньшей мере один из атомов водорода замещен атомом галогена, предпочтительно фтора или хлора, наиболее предпочтительно атомом фтора. К предпочтительным галогенированным низшим алкильным группам относятся трифторметил, дифторметил, трифторэтил, 2,2-дифторэтил, фторметил и хлорметил, причем трифторметил является особенно предпочтительным.
[0039] Термин «карбоксил» означает группу -СООН, тогда как термин «аминокарбонил» относится к группе -СО-NH2.
[0040] Термин «низший алкоксикарбонил» относится к группе -СО-OR', где R' представляет собой низший алкил, который определен ранее. Предпочтительными низшими алкоксикарбонильными группами являются метоксикарбонил или этоксикарбонил.
[0041] Термин «низший алкилтиоалкил» относится к группе -Rʺ-S-R', где R' представляет собой низший алкил, который определен выше, и Rʺ представляет собой низший алкилен, такой как метилен, этилен и пропилен. Примерами низшей алкилтиоалкильной группы являются метилтиометил или 2-метилтиоэтил.
[0042] Термин «низший алкоксикарбониламино» относится к группе -NH-CO-OR', где R' представляет собй низший алкил.
[0043] Термин «низший алкенилоксикарбонил» относится к группе -СО-OR*, где R* представляет собой низшую алкенильную группу. Предпочтительной низшей алкенилоксикарбонильной группой является 2-пропен-1-илоксикарбонил или аллилоксикарбонил.
[0044] Термин «низший алканоил», когда используется в настоящем изобретении, означает группу -CO-R', где R' представляет собой низший алкил, который определен ранее. Предпочтительной низшей алканоильной группой является ацетил.
[0045] Соединения, используемые в качестве активных ингредиентов, содержат один или несколько асимметричных атомов углерода и могут существовать в виде оптически чистых энантиомеров, смесей энантиомеров, таких как, например, рацематы, оптически чистых диастереоизомеров, смесей диастереоизомеров, диастереоизомерных рацематов или смесей диастереоизомерных рацематов. Оптически активные формы могут быть получены, например, разделением рацематов, асимметричным синтезом или асимметричной хроматографией (хроматография с хиральными адсорбентами или элюентом). Настоящее изобретение охватывает все эти формы.
[0046] Доза соединения по настоящему изобретению зависит от ряда факторов, таких как, например, способ введения, возраст и масса тела пациента, а также состояние больного, который будет проходить лечение, и, в конечном счете, будет определяться лечащим врачом или ветеринаром. Такое количество активного соединения, которое определено лечащим врачом или ветеринаром, упоминается в настоящем документе и в формуле изобретения как «терапевтически эффективное количество». Например, доза соединения по настоящему изобретению обычно находится в интервале от примерно 1 до примерно 1000 мг в день. Предпочтительно, терапевтически эффективное количество представляет собой количество от примерно 1 мг до примерно 500 мг в день.
[0047] Способы получения твердой дисперсии включают способ плавки, способ растворителя, способ плавки-растворителя, способ распылительной сушки, способ лиофильной сушки, способ измельчения и т.п. Способ плавки включает смешивание и плавление лекарственного средства с материалом-носителем, быстрое охлаждение расплава до твердого состояния, а затем выдерживание твердого вещества при определенной температуре для достижения хрупкого состояния, такого как пилюля (dropping pill). Способ подходит для термически стабильных лекарственных средств и для материалов-носителей с низкой температурой плавления и плохой растворимостью в органическом растворителе, таких как PEG, лимонная кислота, сахар и т.п. Способ растворителя также называют способ совместного осаждения, т.е. лекарственное средство и носитель совместно растворяют в органическом растворителе и затем растворитель выпаривают, так что лекарственное средство и материал носителя осаждаются одновременно. Таким образом, после сушки получают твердую дисперсию лекарственного средства и материала носителя. Способ подходит для материалов носителей, которые являются летучими, термически нестабильными и расворимы в органических растворителях.
[0048] Распылительная сушка представляет собой способ, в котором для сушки жидких материалов применяется технология псевдоожиженного слоя. Основной принцип заключается в том, что система жидких материалов (раствор, суспензия, эмульсия и т.д.) распыляется газом в сушильной башне (камере). При контакте с горячим воздухом влага (растворитель) быстро испаряется, и в результате получают высушенный порошкообразный продукт. Способ может использоваться непосредственно для сушки раствора, суспензии, эмульсии и т.п. с получением порошкообразного или гранулированного продукта, минуя процедуры испарения и измельчения.
[0049] Способ распылительной сушки включает распылительную сушку под давлением, центробежную распылительную сушку и воздушную распылительную сушку.
[0050] (1) Распылительная сушка под давлением:
[0051] ① Принцип: С помощью насоса высокого давления материал пропускают через атомизатор (пушку) с давлением от 70 до 200 атмосфер (6865-19610 кПА), и полученные таким образом частицы тумана от 10 до 200 непосредственно контактируют с горячим воздухом для теплообмена, и сушка завершается в короткий срок.
[0052] (2) Центробежная распылительная сушка:
[0053] ① Принцип: Диск, который вращается с высокой скоростью в горизонтальном направлении, обеспечивает центробежную силу для раствора, поэтому он должен распределяться с высокой скоростью с образованием пленки, нити или капли. Вследствие трения, задержке и отрыву от воздуха в сочетании с тангенциальным ускорением, создаваемым вращением диска, и радиальным ускорением, создаваемым центробежной силой, пленка, нить или капля движутся на диске с комбинированной скоростью со следом спиральной формы. Жидкость диспергируется на крошечные капли после ее выброса диска по спирали, затем капли движутся в направлении диаметрального разреза со средней скоростью. При этом капли падают под действием силы тяжести. Вследствие разницы размеров распыляемых частиц, расстояния, которые они пролетают в воздухе, различаются. Частицы, падающие на разных расстояниях, образуют цилиндр, симметричный относительно центра вала.
[0054] (3) Воздушная распылительная сушка:
[0055] ① Принцип: Влажные материалы подаются в сушилку по транспортеру с нагретым воздухом окружающей среды и после этого интенсивно перемешиваются. Благодаря большой площади тепло- и массообмена, испарительная сушка достигается в короткий срок.
[0056] Методы распылительной сушки широко используются в пищевой промышленности (например, в производстве сухого молока), фармацевтической промышленности (сушка продуктов традиционной китайской медицины, получение твердых дисперсий, уменьшение размера частиц и т.д.), химической промышленности, производстве пластмасс и производстве керамики.
Краткое описание чертежей
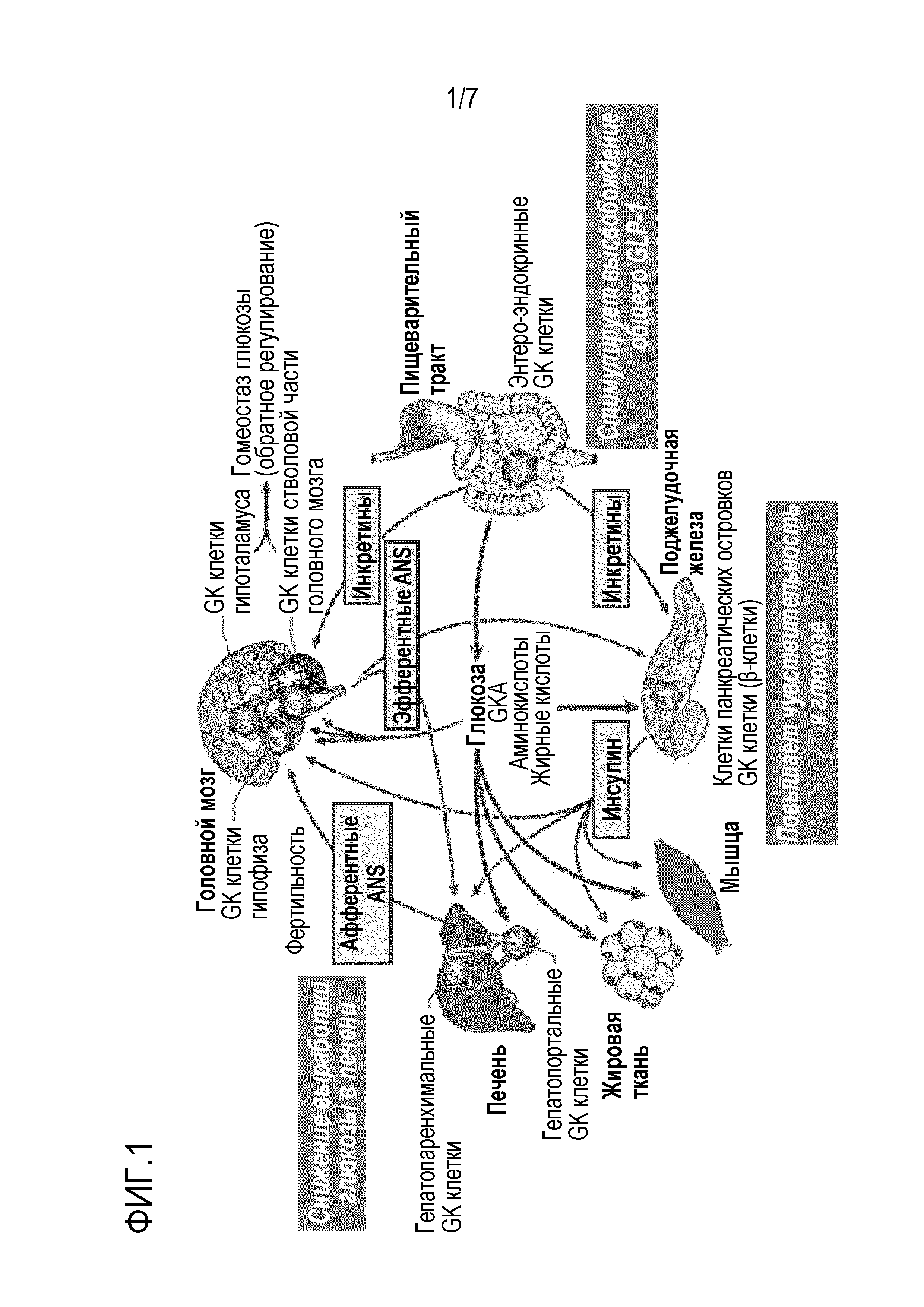
[0057] На фигуре 1 представлено графическое изображение распределения глюкокиназы in vivo.
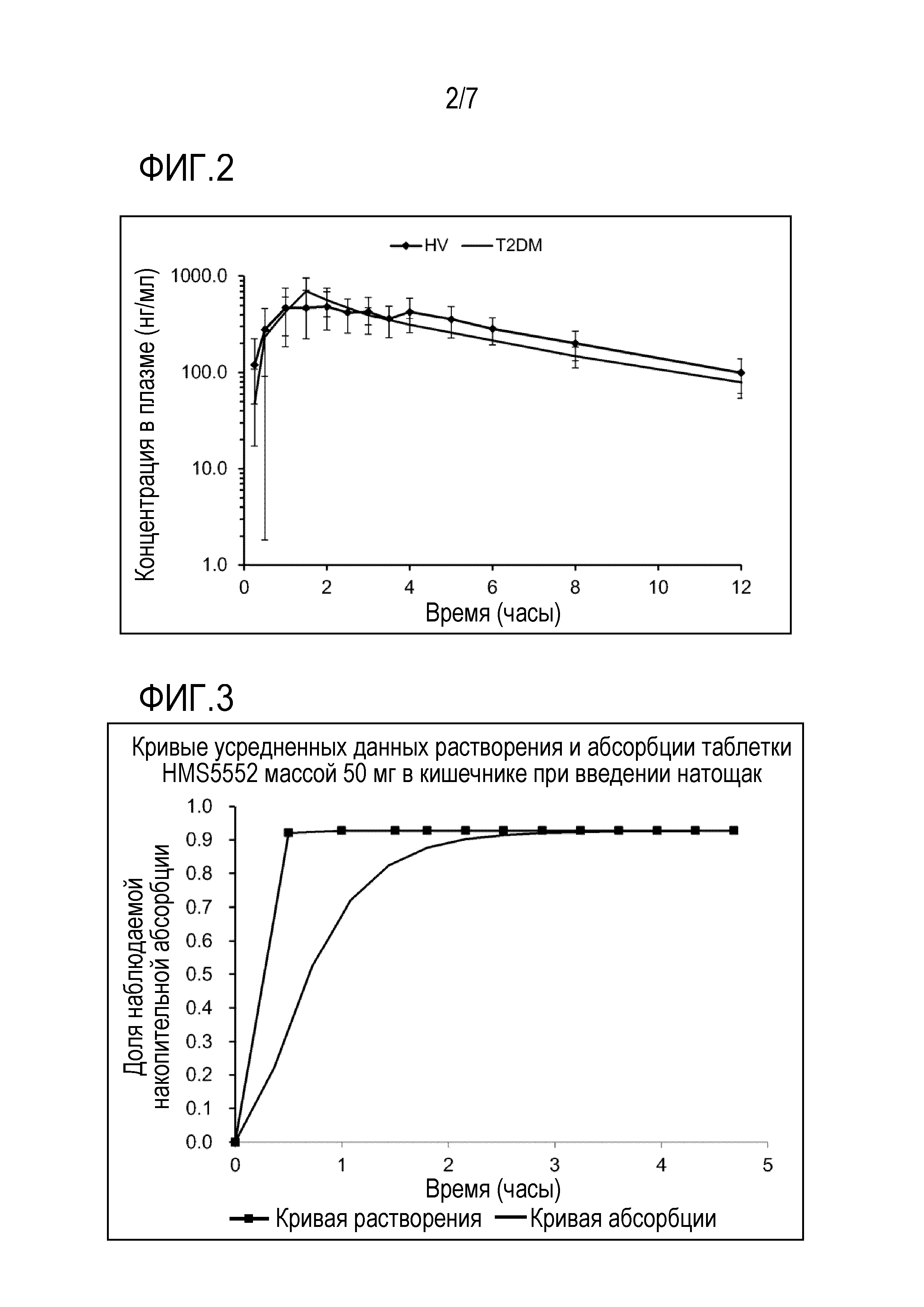
[0058] На фигуре 2 представлена (полулогарифмическая) кривая, которая показывает концентрацию лекарственного средства в плазме по времени таблетки HMS5552 в организмах здоровых пациентов (HV) и пациентов с диабетом 2 типа (T2DM) после введения разовой дозы 50 мг.
[0059] На фигуре 3 представлены моделируемые профили усредненного растворения и усредненной абсорбции таблетки НMSС5552 массой 50 мг в кишечном тракте человека при введении натощак.
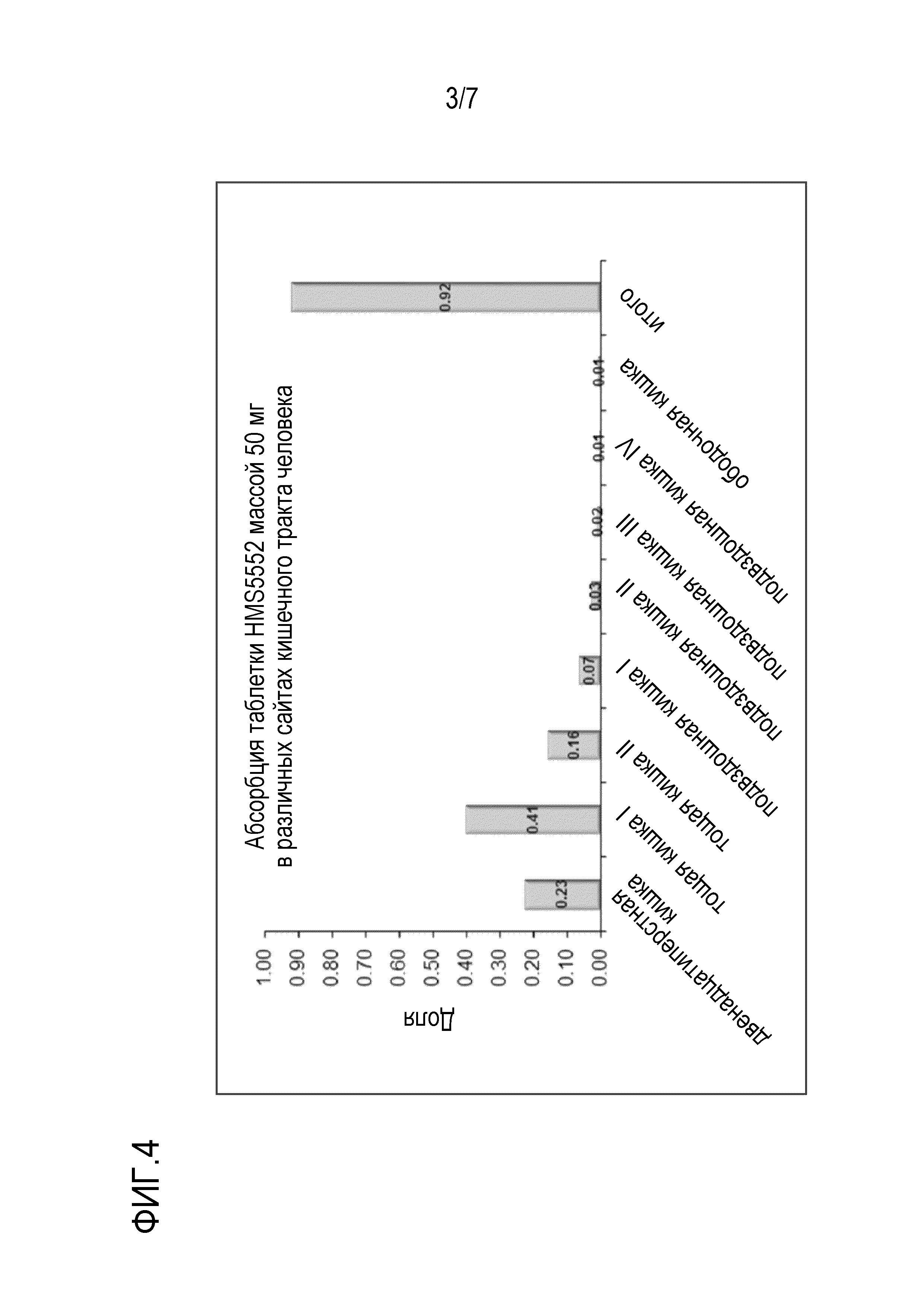
[0060] На фигуре 4 представлен график, показывающий смоделированное распределение абсорбции таблетки HMS5552 массой 50 мг в различных участках желудочно-кишечного тракта человека при введении натощак.
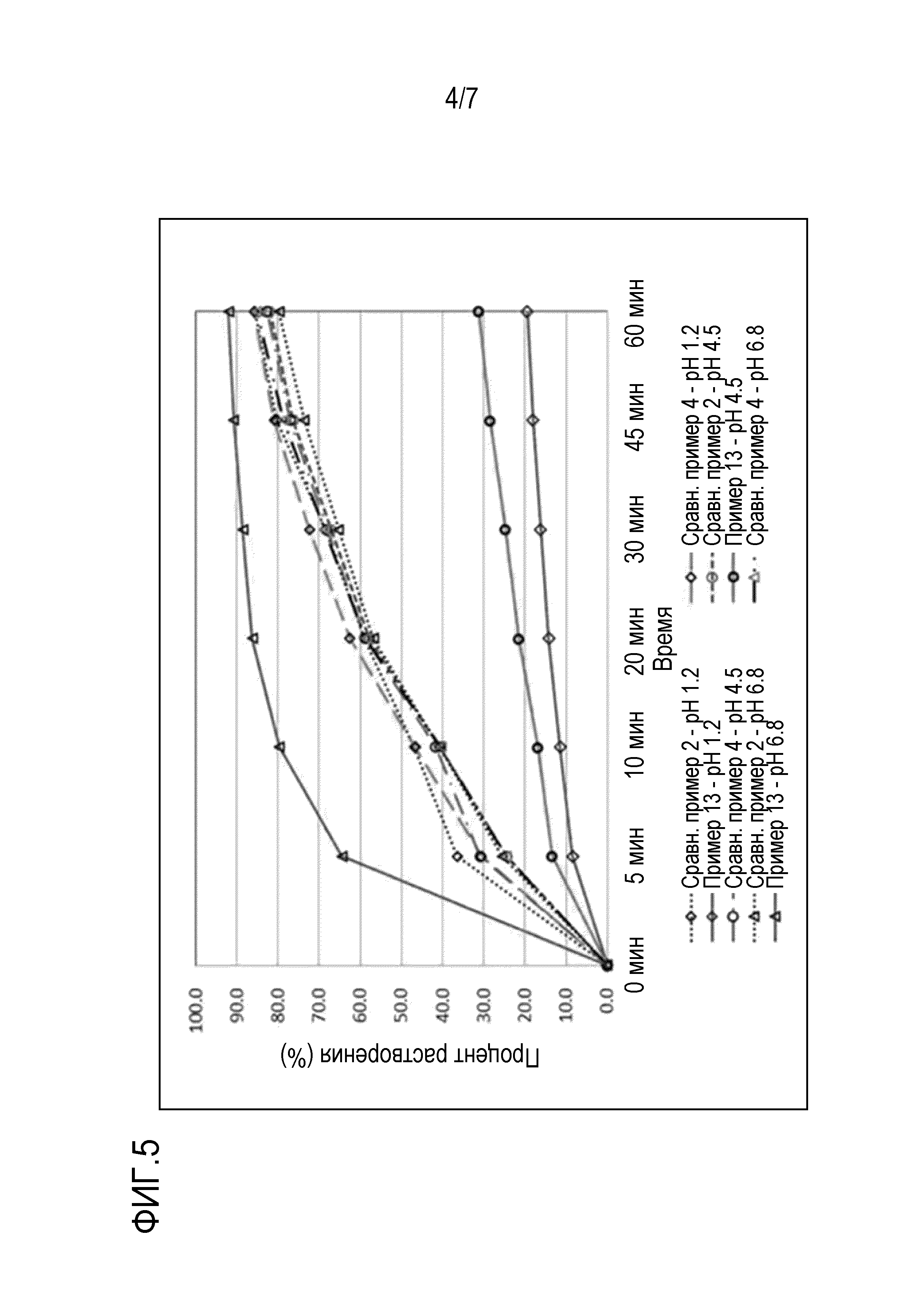
[0061] На фигуре 5 представлен график, показывающий кривые растворения таблеток массой 75 мг, полученных в примере 13, сравнительном примере 2 и сравнительном примере 4, при рН 1,2, рН 4,5 и рН 6,8, соответственно.
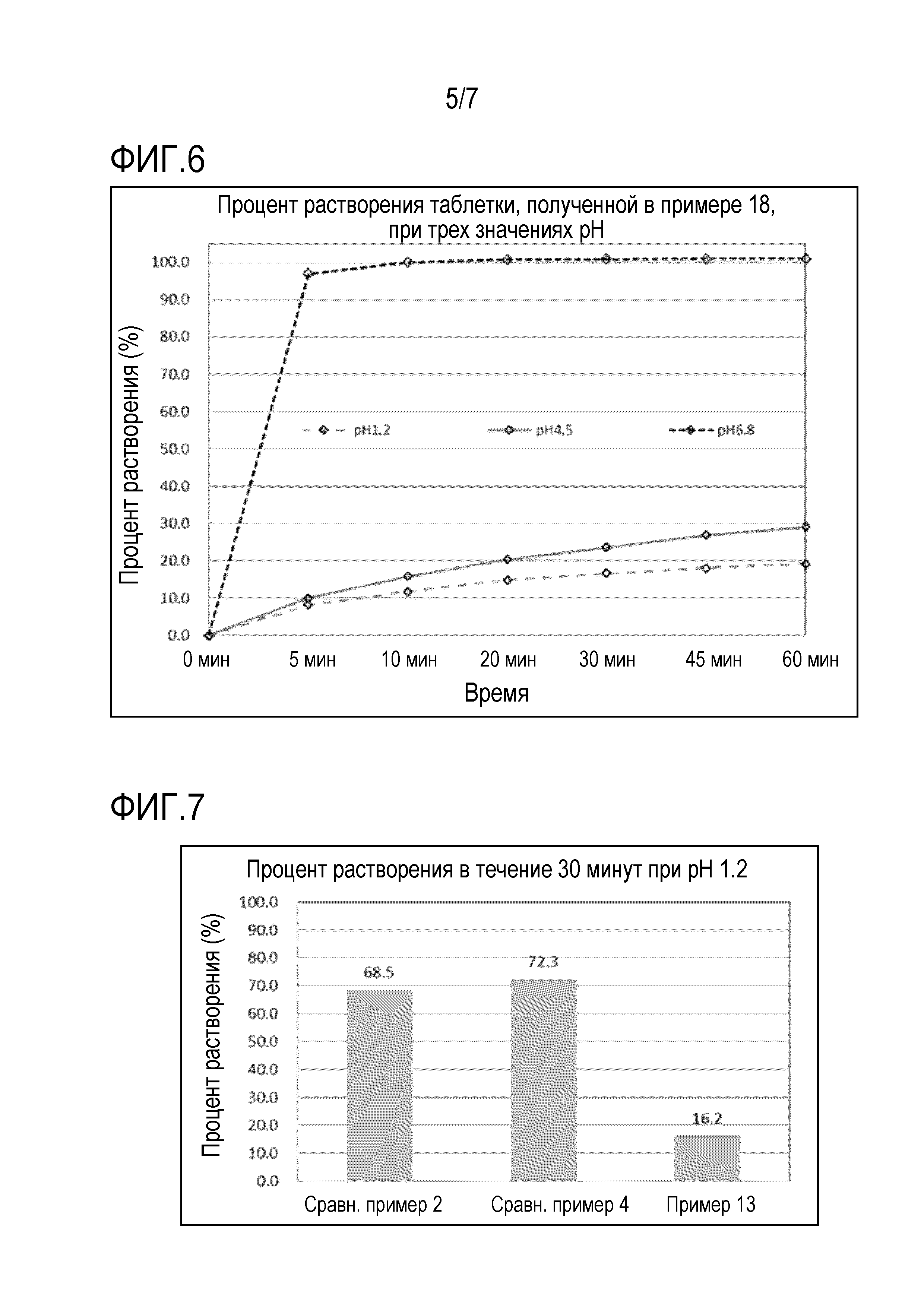
[0062] На фигуре 6 представлен график, показывающий кривую растворения таблетки массой 75 мг с покрытием, полученной в примере 18, при рН 1,2, рH 4,5 и рH 6,8.
[0063] На фигуре 7 представлена гистограмма, показывающая результаты растворения в течение 30 мин. таблеток массой 75 мг, полученных в примере 13, сравнительном примере 2 и сравнительном примере 4, при рН 1,2.
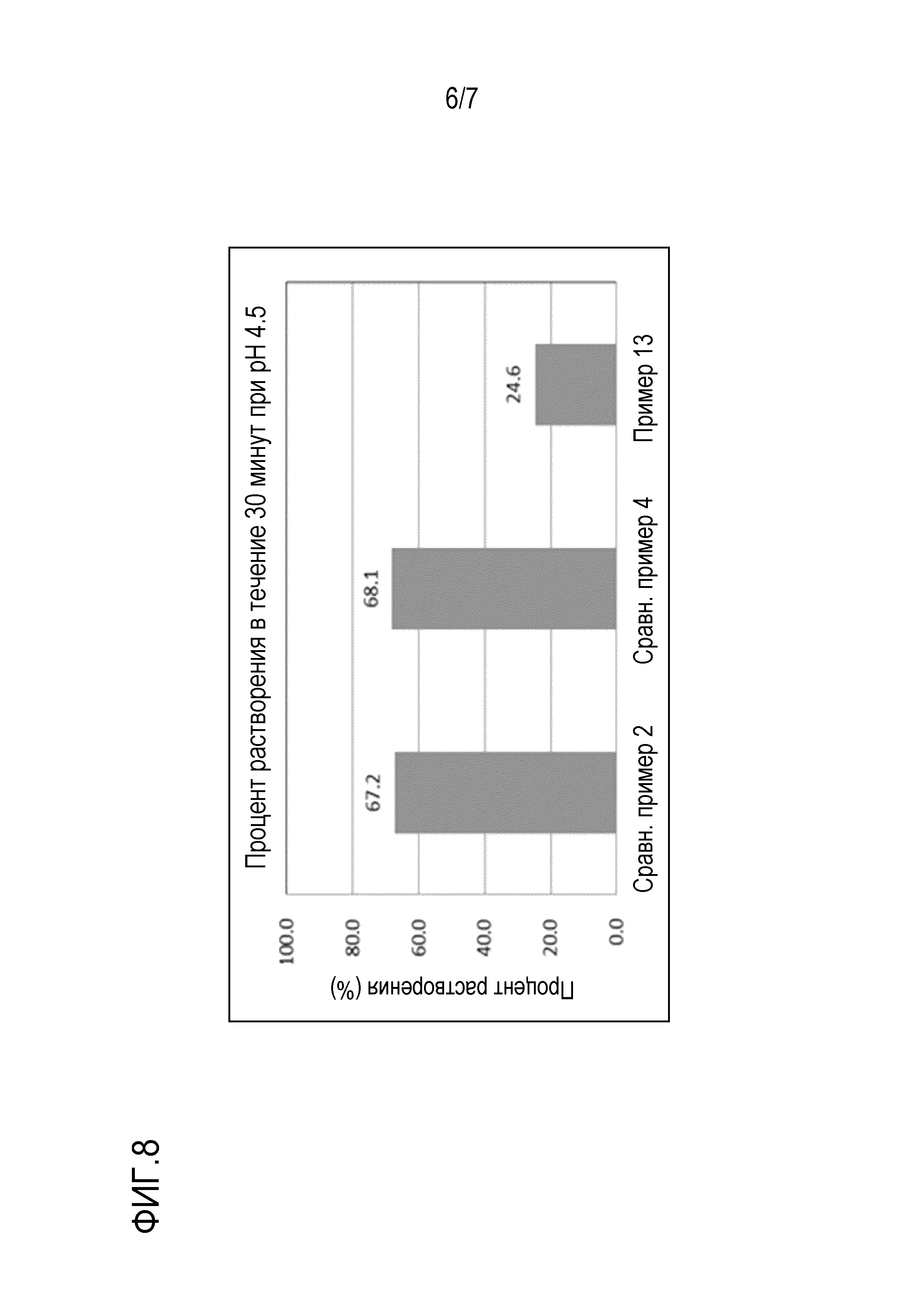
[0064] На фигуре 8 представлена гистограмма, показывающая результаты растворения в течение 30 мин. таблеток массой 75 мг, полученных в примере 13, сравнительном примере 2 и сравнительном примере 4, при рН 4,5.
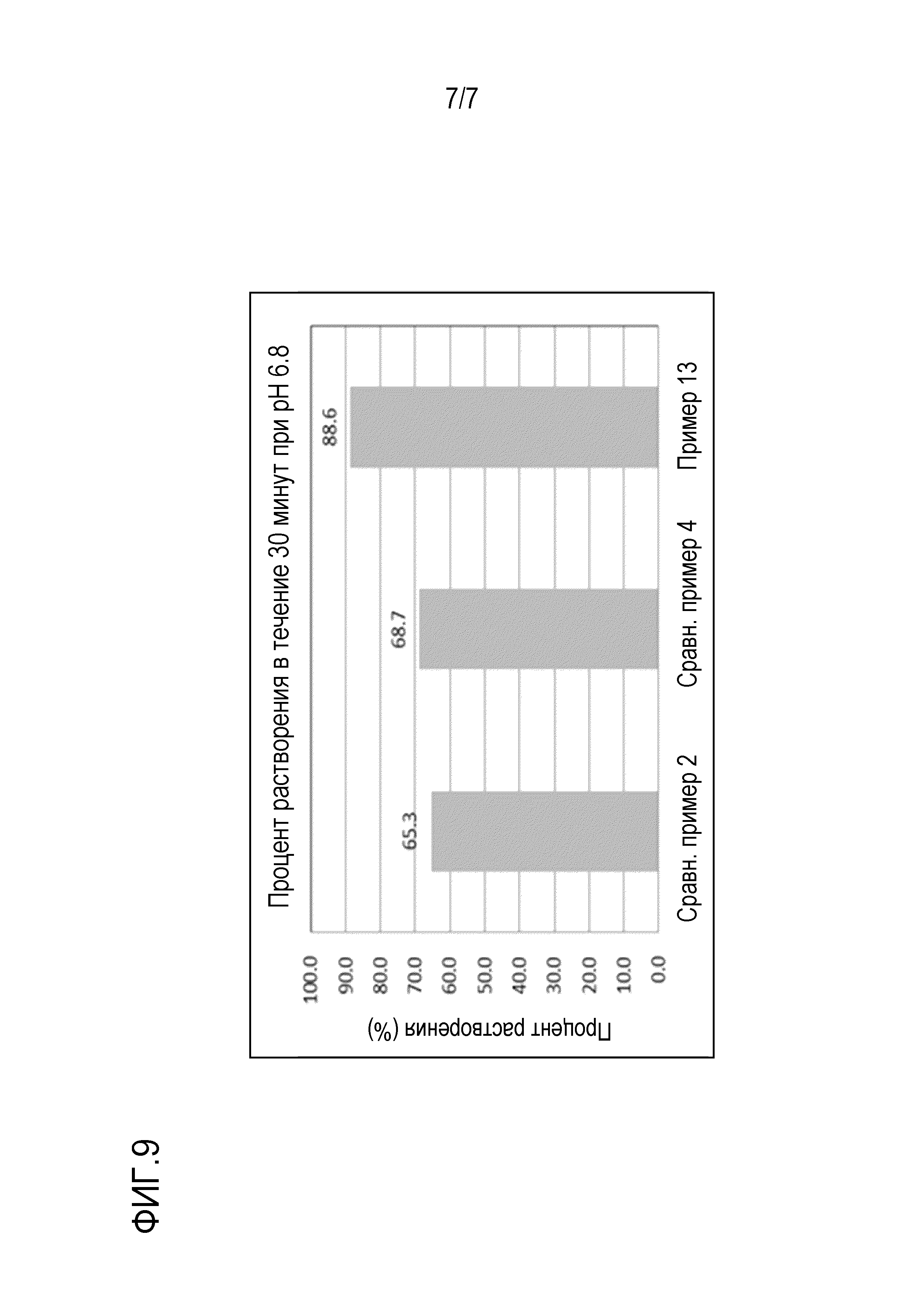
[0065] На фигуре 9 представлена гистограмма, показывающая результаты растворения в течение 30 мин. таблеток массой 75 мг, полученных в примере 13, сравнительном примере 2 и сравнительном примере 4, при рН 6,8.
Варианты осуществления изобретения
[0066] Настоящее изобретение относится к модифицированному высвобождению активатора глюкокиназы. В частности, настоящее изобретение относится к разработке и получению препарата активатора глюкокиназы для перорального введения. Препарат для перорального введения, препочтительно препарат для перорального введения с модифицированным высвобождением действующего вещества, более предпочтительно твердый препарат для перорально введения, в желудочном соке высвобождает небольшое количество действующего вещества, но в кишечнике быстро высвобождает действующее вещество и постепенно абсорбируется, так что в организме человека фармакокинетика (ФК) будет сочетаться с фармакодинамикой (ФД) (корреляция ФК/ФД). Кривая концентрации в плазме в зависимости от времени (кривая С~t) в организме человека имеет форму перевернутой буквы U.
[0067] В одном варианте осуществления настоящее изобретение относится к твердой дисперсии, которая содержит активатор глюкокиназы, его изотопно-меченые аналоги или его фармацевтически приемлемые соли и полимерные носители.
[0068] В одном варианте осуществления настоящее изобретение относится к твердой дисперсии, где активатор глюкокиназы представляет собой соединение формулы (Ia)
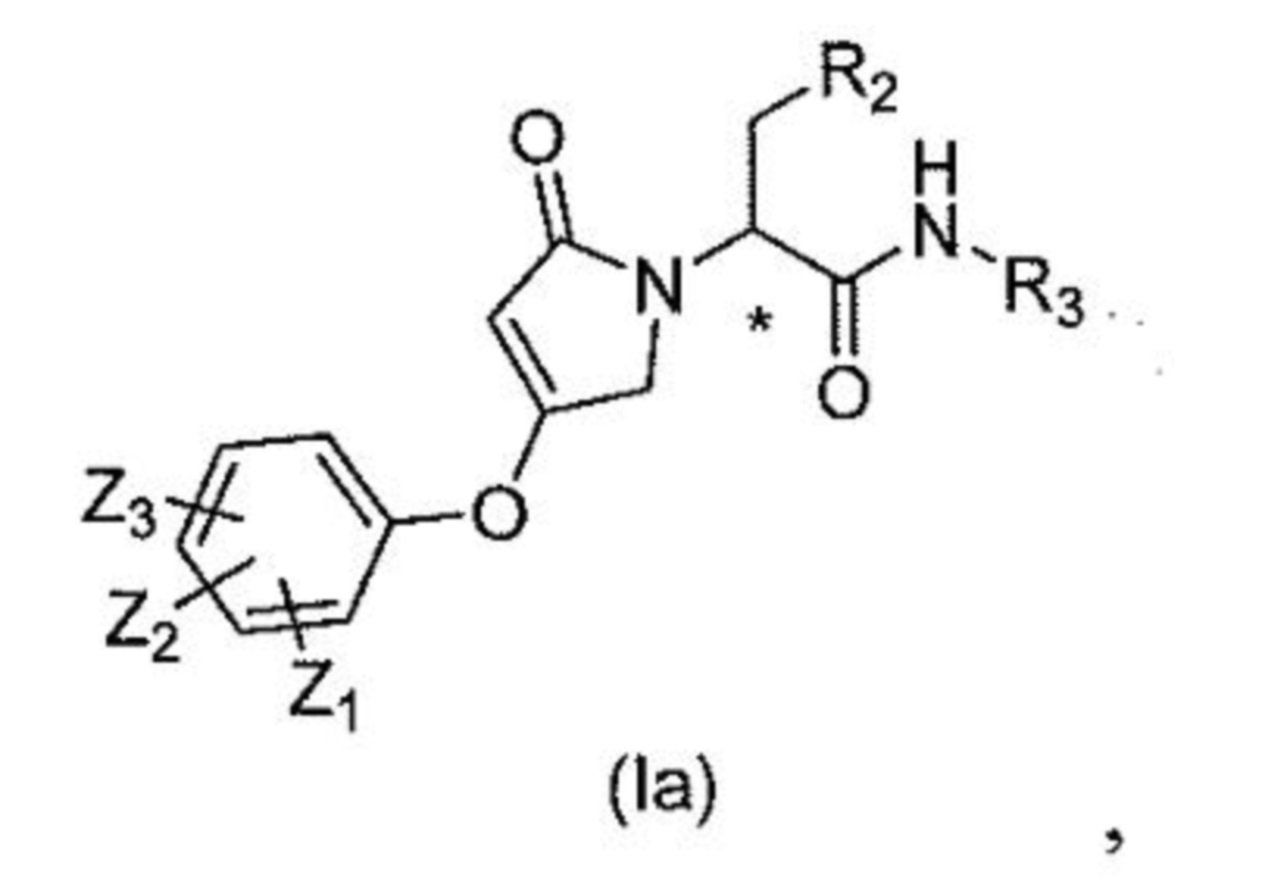
[0069] где
[0070] Z1, Z2, Z3 независимо друг от друга представляют собой водород, низший алкил, низший алкенил, гидроксильную группу, -NH2, галоген, низший алкокси, -CF3, -OCF3, -S(CH3), -S(O2)CH3, -CH2-арил, гетероарил, циано, низший алканоил, -О-арил, -О-СН2-арил, --N(CH3)2, циклоалкил, гетероциклил, -С(О)-гетероциклил или низший алкил, моно- или дизамещенный гидроксильной группой;
[0071] R2 выбран из группы, состоящей из низшего алкила, низшего алкила, моно- или дизамещенного гидроксильной группой, низшего галоалкила, низшего алкоксиалкила, низшего алкилтиоалкила, низшего алкокси, циклоалкила, где указанный циклоалкил является незамещенным или независимо моно- или дизамещенным галогеном или низшим алкилом, гетероциклилом и арилом, где указанный арил является незамещенным или независимо моно- или дизамещенным галогеном; и
[0072] R3 представляет собой низший алкилкарбамоил или
[0073] незамещенный или замещенный гетероарил, соединенный с аминной группой, как показано на рисунке, через атом углерода в кольце, где один из гетероатомов представляет собой атом азота и является соседним по отношению к соединяющему атому углерода кольца, причем указанный замещенный гетероарил является независимо замещенным в положении, которое не является соседним по отношению к соединяющему атому углерода кольца, группой, выбранной из группы, состоящей из
[0074] низшего алкила, галогена, низшего алкоксикарбонила, циано, карбоксильной группы, циклоалкила, арила, 2-оксоoксазолидин-5-илметила, -N(низший алкил)2, 2,2-диметил-[1,3]диоксолан-4-ила, -СН2-диметил-[1,3]диоксолана, трет-бутил-диметилсиланилоксиэтила, незамещенного -СН2-арила, -СН2-арила, замещеного циано или алкоксигруппой, гетероциклила, -СН2-гетероциклила, трет-бутилового эфира -6-(СН2)-2,2-диметил-[1,3]диоксан-4-ил-уксусной кислоты, и низшего алкила, независимо моно-, ди- или тризамещенного гидроксильной группой, галогеном, алкокси, -N(низший алкил)2, -NH2, низшим алканоилом, низшим алкоксикарбонилом, низшим алкенилоксикарбонилом, карбоксильной группой, аминокарбонилом или низший алкоксикарбониламиногруппой,
[0075] его изотопно-меченые аналоги или фармацевтически приемлемые соли.
[0076] В одном варианте осуществления настоящее изобретение относится к твердой дисперсии, где активатор глюкокиназы выбран из следующих соединений, их изотопно-меченых аналогов или фармацевтически приемлемых солей:
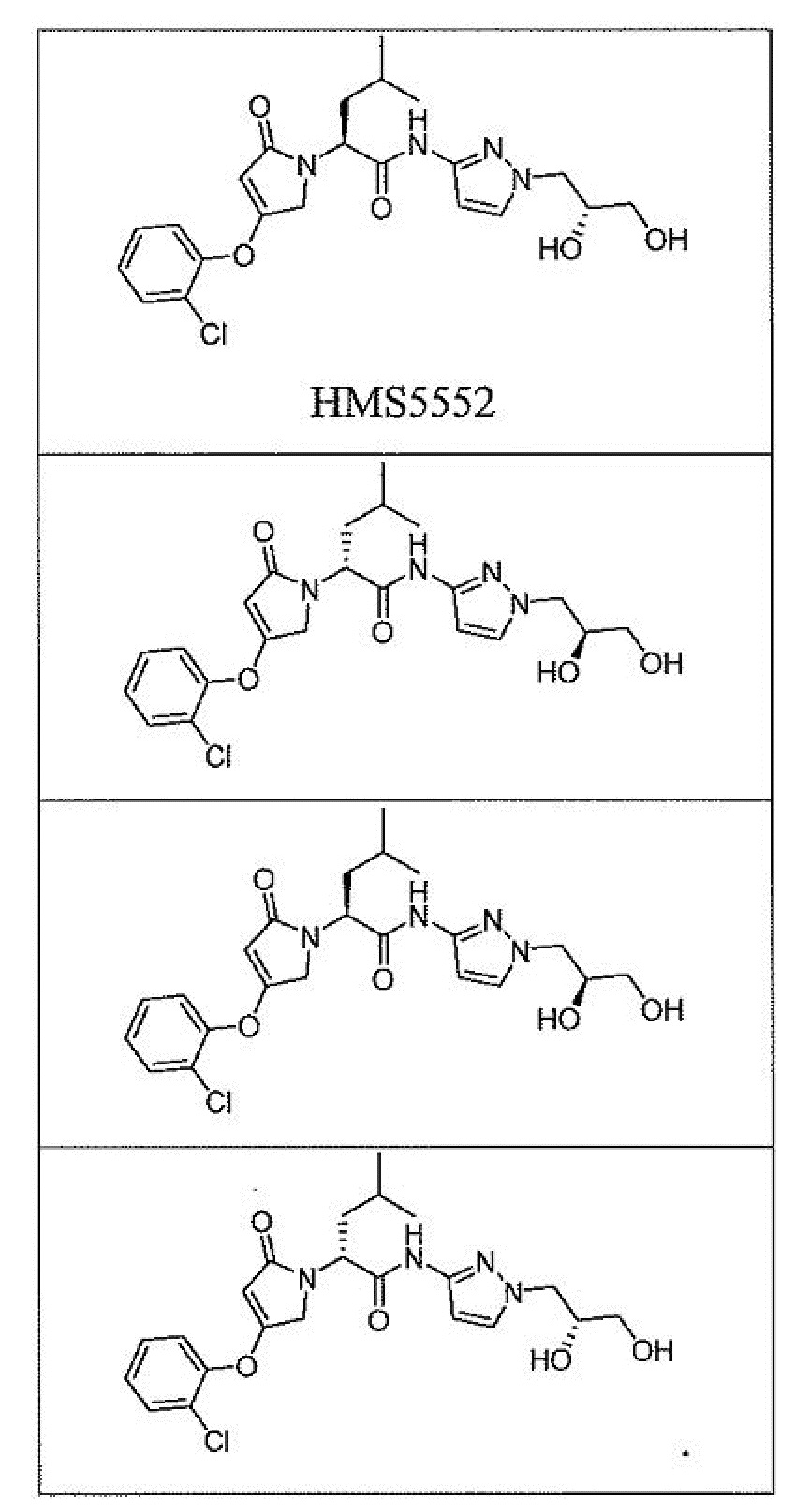
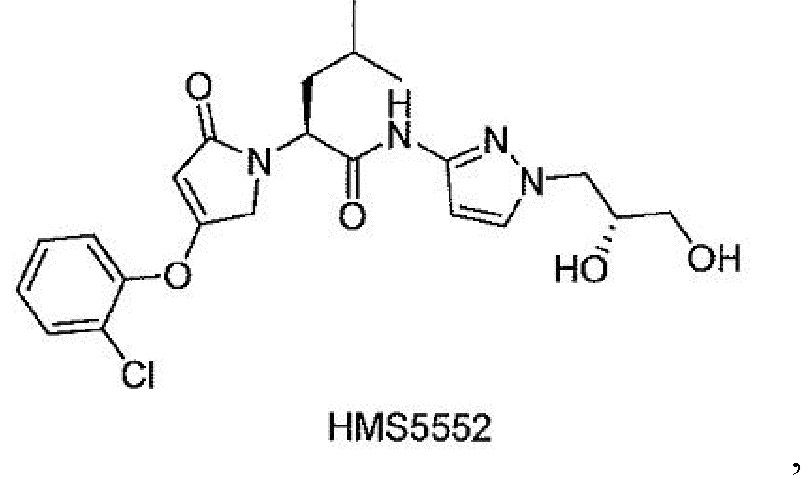
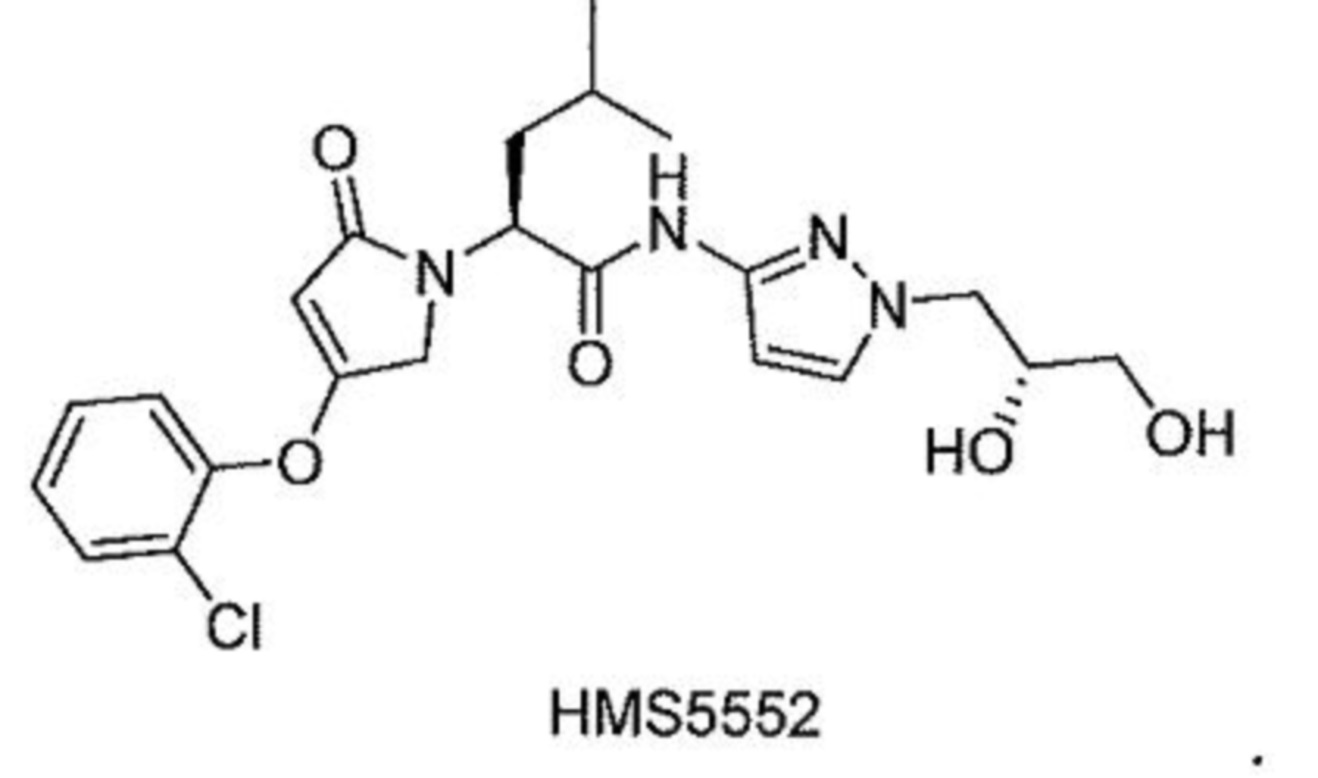
[0077] В одном варианте осуществления настоящее изобретение относится к твердой дисперсии, где активатор глюкокиназы представляет собой соединение HMS5552, его изотопно-меченые аналоги или фармацевтически приемлемые соли:
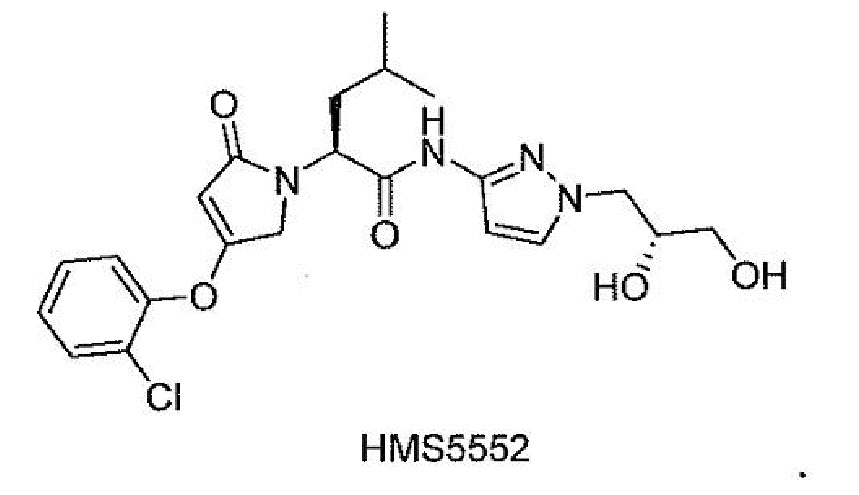
[0078] В одном варианте осуществления настоящее изобретение относится к твердой дисперсии, где активатор глюкокиназы выбран из группы, состоящей из следующих соединений:
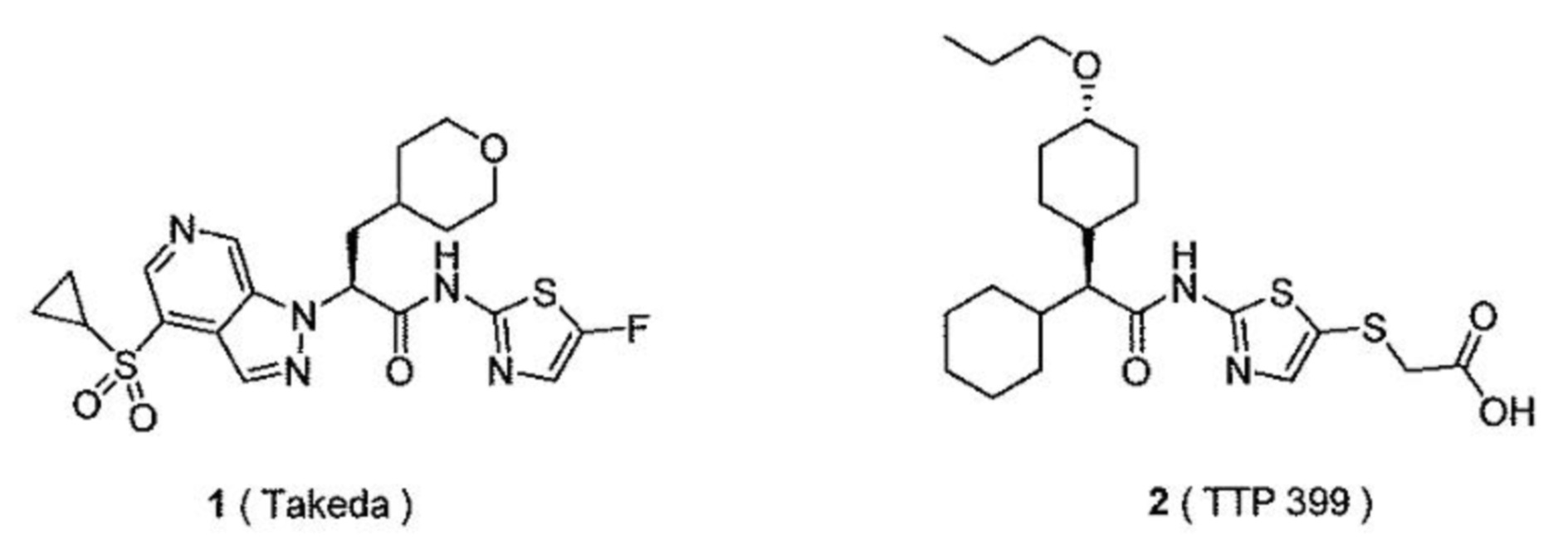
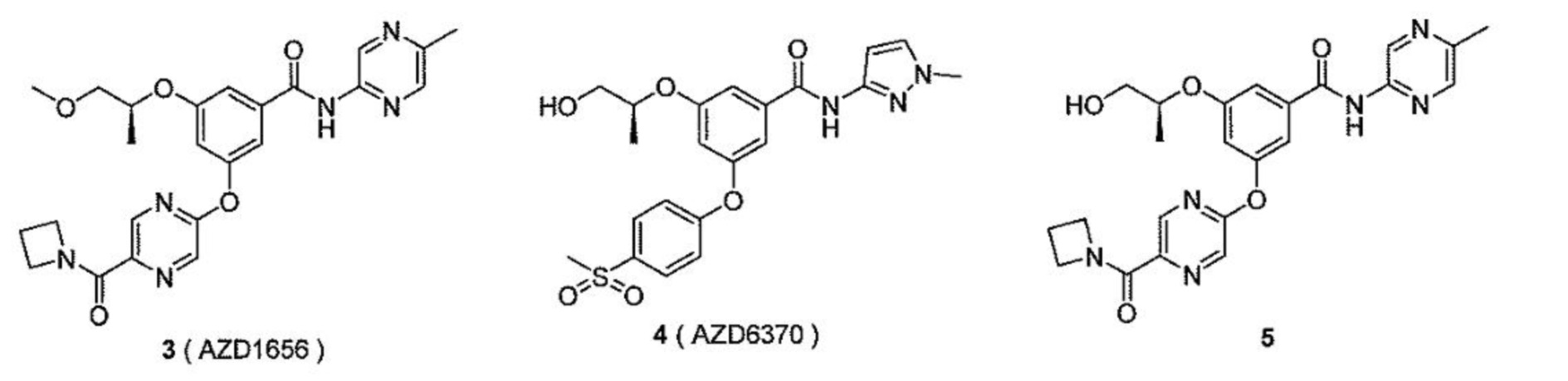
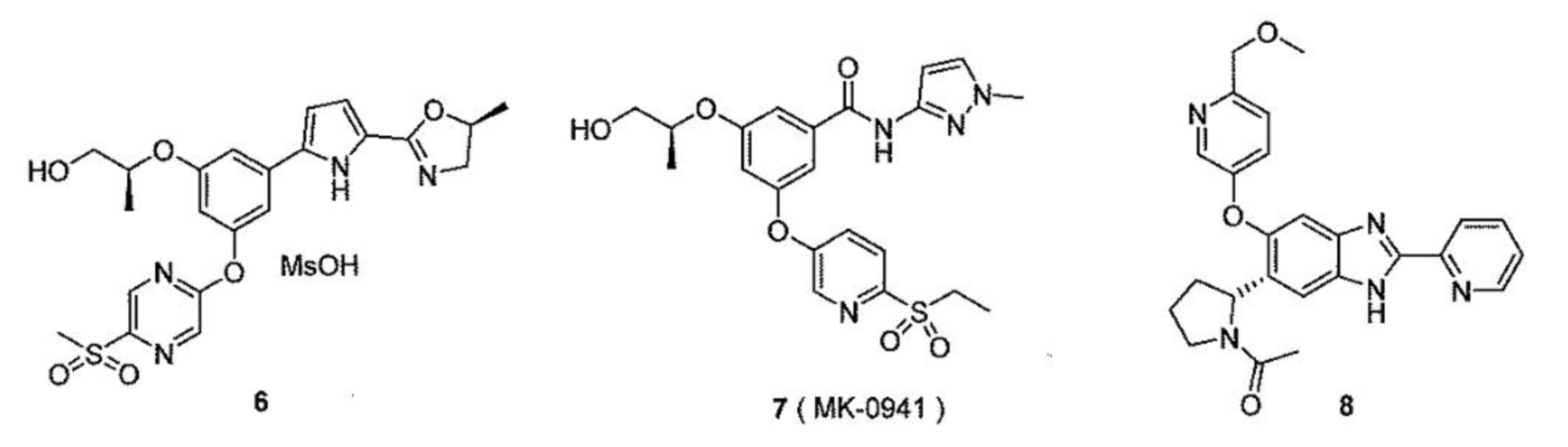
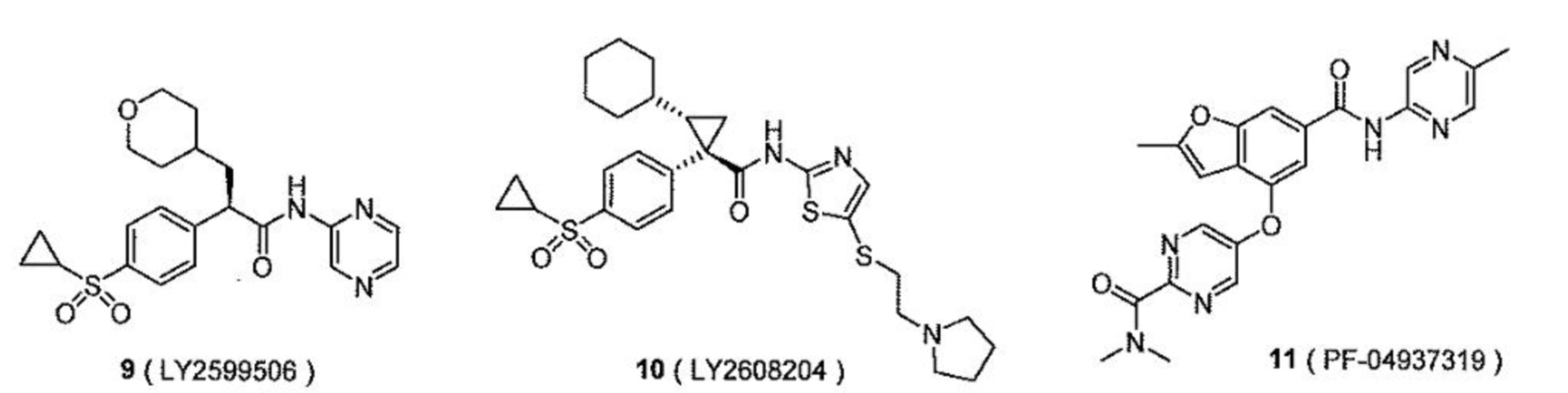
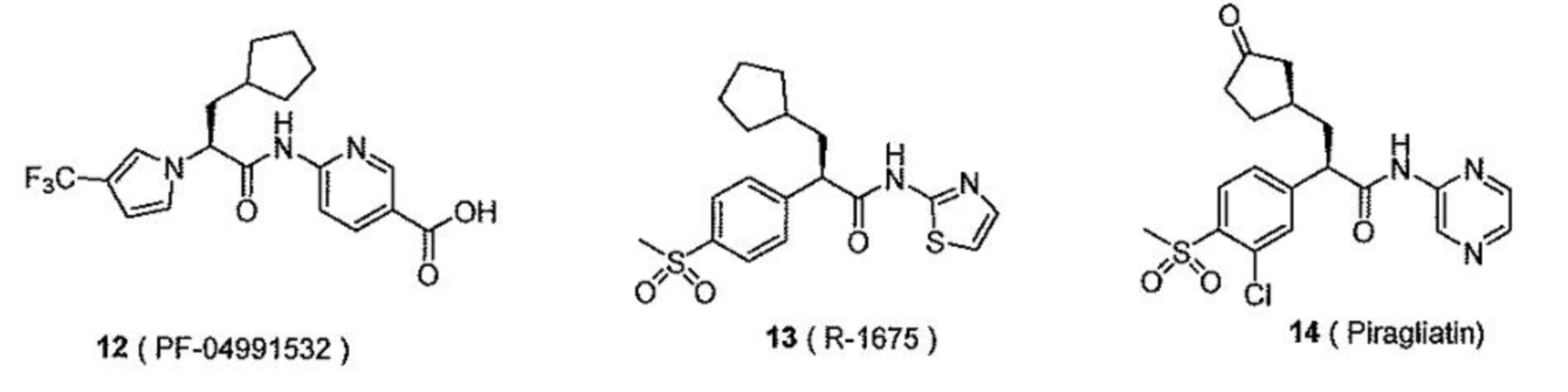
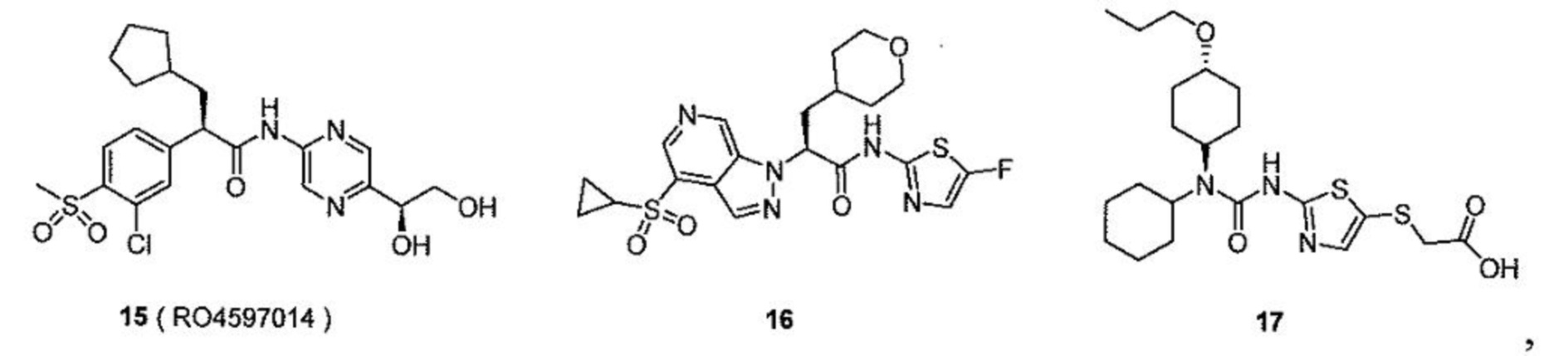
[0079] их изотопно-меченых аналогов или фармацевтически приемлемых солей.
[0080] В одном варианте осуществления настоящее изобретение относится к твердой дисперсии, где активатор глюкокиназы выбран из группы, состоящей из TTP399, PF-04937319, RO4597014 и LY2608204, их изотопно-меченых аналогов или фармацевтически приемлемых солей.
[0081] В одном варианте осуществления настоящее изобретение относится к твердой дисперсии, где полимерные носители являются носителями контролируемого высвобождения действующего вещества.
[0082] В одном варианте осуществления настоящее изобретение относится к твердой дисперсии, где полимерными носителями являются полимеры полиакрилатных смол.
[0083] В одном варианте осуществления настоящее изобретение относится к твердой дисперсии, где полимерные носители выбраны из группы, состоящей из сополимера метакриловой кислоты и сополимера метакрилата.
[0084] В одном варианте осуществления настоящее изобретение относится к твердой дисперсии, где полимерные носители выбраны из группы, состоящей из сополимера бутилметакрилата, диметиламиноэтилметакрилата и метилметакрилата; сополимера метакриловой кислоты и этилакрилата; сополимера метакриловой кислоты и метилметакрилата; сополимера этилакрилата, метилметакрилата и хлортриметиламиноэтилметакрилата; сополимера этилакрилата и метилметакрилата; сополимера метакриловой кислоты, метилакрилата и метилметакрилата; сополимера метакриловой кислоты и бутилакрилата.
[0085] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где полимерные носители выбраны из группы, состоящей из бутилметакрилата, сополимера диметиламиноэтилметакрилата и метилметакрилата (1:2:1), сополимера метакриловой кислоты и этилакрилата (1:1), сополимера метакриловой кислоты и метилметакрилата (1:2), сополимера этилакрилата, метилметакрилата и хлортриметиламиноэтилметакрилата (1:2:0,2), сополимера этилакрилата, метилметакрилата и хлортриметиламиноэтилметакрилата (1:2:0,1), сополимера этилакрилата и метилметакрилата (2:1), сополимера метакриловой кислоты и бутилакрилата (35:65), сополимера метакриловой кислоты и метилметакрилата (1:1), сополимера метакриловой кислоты и метилметакрилата (1:1), сополимера метакриловой кислоты и метилметакрилата (35:65).
[0086] В одном варианте осуществления настоящее изобретение относится к твердой дисперсии, где полимерный носитель выбран из Eudragit.
[0087] В одном варианте осуществления настоящее изобретение относится к твердой дисперсии, где полимерные носители выбраны из группы, состоящей из Eudragit E, Eudragit L и Eudragit S.
[0088] В одном варианте осуществления настоящее изобретение относится к твердой дисперсии, где полимерные носители выбраны из группы, состоящей из Eudragit L100, Eudragit S 100, Eudragit E PO, Eudragit E 100 и Eudragit L 100-55.
[0089] В одном варианте осуществления настоящее изобретение относится к твердой дисперсии, где полимерным носителем является Eudragit L100, т.е. сополимер метакриловой кислоты типа А, который является анионным сополимером метакриловой кислоты и метилметакрилата (1:1).
[0090] В одном варианте осуществления настоящее изобретение относится к твердой дисперсии, где массовое соотношение активатора глюкокиназы и полимерного носителя составляет от 1:10 до 10:1.
[0091] В одном варианте осуществления настоящее изобретение относится к твердой дисперсии, где массовое соотношение активатора глюкокиназы и полимерных носителей составляет от 1:9 до 9:1, от 1:4 до 4:1, от 3:7 до 7:3, от 2:3 до 3:2, от 3:4 до 4:3, от 4:5 до 5:4 или от 5:6 до 6:5.
[0092] В одном варианте осуществления настоящее изобретение относится к твердой дисперсии, где массовое соотношение активатора глюкокиназы и полимерных носителей составляет 1:1.
[0093] В одном варианте осуществления настоящее изобретение относится к твердой дисперсии, где количество активатора глюкокиназы составляет от 10% мас. до 90% мас. твердой дисперсии.
[0094] В одном варианте осуществления настоящее изобретение относится к твердой дисперсии, где количество активатора глюкокиназы составляет от 30% мас. до 80% мас. твердой дисперсии.
[0095] В одном варианте осуществления настоящее изобретение относится к твердой дисперсии, где количество активатора глюкокиназы составляет от 40% мас. до 80% мас. твердой дисперсии.
[0096] В одном варианте осуществления настоящее изобретение относится к твердой дисперсии, где количество активатора глюкокиназы составляет от 50% мас. до 80% мас. твердой дисперсии.
[0097] В одном варианте осуществления настоящее изобретение относится к твердой дисперсии, где количество активатора глюкокиназы составляет 50% мас. твердой дисперсии.
[0098] В одном варианте осуществления настоящее изобретение относится к твердой дисперсии, где количество полимерных носителей составляет от 10% мас. до 90% мас. твердой дисперсии.
[0099] В одном варианте осуществления настоящее изобретение относится к твердой дисперсии, где твердая дисперсия получена распылительной сушкой.
[00100] В одном варианте осуществления настоящее изобретение относится к композиции твердой дисперсии, которая включает твердую дисперсию по настоящему изобретению и эксципиенты.
[00101] В одном варианте осуществления настоящее изобретение относится к композиции твердой дисперсии, где наполнители выбраны из одного или нескольких эксципиентов из группы, состоящей из разбавителя, подсластителей или вкусовых веществ, поверхностно-активных веществ, наполнителей, связующих веществ, дезинтеграторов (разрыхлителей), смазывающих веществ, веществ для предотвращения слипания/антиадгезивов, модификаторов высвобождения действующего вещества, стабилизаторов, агентов покрытий, эмульгаторов и/или солюбилизаторов и отдушек.
[00102] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, который содержит твердую дисперсию или композицию твердой дисперсии.
[00103] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, который представляет собой препарат активатора глюкокиназы для перорального введения с модифицированным высвобождением действующего вещества.
[00104] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, который представляет собой твердый препарат активатора глюкокиназы для перорального введения с модифицированным высвобождением действующего вещества.
[00105] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где твердый препарат для перорального введения с модифицированным высвобождением действующего вещества активатора глюкокиназы выбран из группы, состоящей из таблетки, капсулы, гранулы, порошка, пастилки и пилюли.
[00106] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где твердый препарат для перорального введения с модифицированным высвобождением действующего вещества активатора глюкокиназы представляет собой таблетку.
[00107] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где таблетка содержит твердую дисперсию по изобретению, наполнители, связующие вещества, дезинтеграторы (разрыхлители) и смазывающие вещества.
[00108] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где в таблетке содержание твердой дисперсии активатора глюкокиназы составляет от 1% мас. до 90% мас., содержание наполнителей составляет от 1% мас. до 95% мас., содержание связующих веществ составляет от 0,5% мас. до 10% мас., содержание дезинтеграторов (разрыхлителей0 составляет от 0,5% мас. до 7,5% мас., содержание смазывающих веществ составляет от 0,25% мас. до 5% мас.
[00109] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где в таблетке наполнитель представляет собой силицированную микрокристаллическую целлюлозу, микрокристаллическую целлюлозу или лактозу, связующие вещества представляют собой гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу и поливинилпирролидон, дезинтеграторы (разрыхлители) представляют собой кроскармеллозу натрия или карбоксиметилкрахмал натрия, и смазывающие вещества представляют собой стеарат магния или стеарилфумарат натрия.
[00110] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где в таблетке наполнители представляют собой силицированную микрокристаллическую целлюлозу, связующие вещества представляют собой гидроксипропилцеллюлозу, дезинтеграторы (разрыхлители) представляют собой кроскармеллозу натрия, смазывающие вещества представляют собой стеарат магния.
[00111] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где таблетка представляет собой таблетку с покрытием.
[00112] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где таблетка с покрытием содержит агенты покрытия, выбранные из группы, состоящей из натриевой соли карбоксиметилцеллюлозы, ацетата целлюлозы, ацетатфталата целлюлозы, этилцеллюлозы, желатина, фармацевтической глазури, гидроксипропилцеллюлозы, гидроксипропилметилцеллюлозы, фталата гидроксипропилметилцеллюлозы, сополимера метакриловой кислоты, метилцеллюлозы, полиэтиленгликоля, фталата поливинилацетата, шеллака, сахарозы, диоксида титана, карнаубского воска, микрокристаллического воска, зеина и Opadry.
[00113] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где агент покрытия в таблетке с покрытием представляет собой Opadry.
[00114] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где в таблетке с покрытиемй содержание твердой дисперсии активатора глюкокиназы составляет от 1% мас. до 90% мас., содержание наполнителей составляет от 1% мас. до 95% мас., содержание связующих веществ составляет от 0,5% мас. до 10% мас., содержание дезинтеграторов (разлыхлителей) составляет от 0,5% мас. до 7,5% мас., содержание смазывающих веществ составляет от 0,25% мас. до 5% мас., и содержание агентов покрытия составляет от 1% мас. до 10% мас.
[00115] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где капсула представляет собой желатиновую капсулу, HPMC капсулу растительного происхождения, кишечнорастворимую капсулу или мягкую капсулу.
[00116] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где капсула содержит твердую дисперсию по настоящему изобретению, наполнитель и/или связующее вещество и/или дезинтегратор (разрыхлитель) и/или смазывающее вещество.
[00117] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где в препарате в форме капсулы содержание твердой дисперсии составляет от 1% мас. до 90% мас., содержание наполнителей составляет от 5% мас. до 95% мас., содержание связующих веществ составляет от 0% мас. до 10% мас., содержание дезинтеграторов (разрыхлителей) составляет от 0,5% мас. до 7,5% мас., и содержание смазывающих веществ составляет от 0% мас. до 5% мас.
[00118] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где в препарате в форме капсулы содержание твердой дисперсии составляет от 1% мас. до 90% мас., содержание наполнителей составляе от 5% мас. до 95% мас., содержание связующих веществ составляет от 0,5% мас. до 10% мас.
[00119] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где в препарате в форме капсулы содержание твердой дисперсии составляет от 1% мас. до 90% мас., содержание наполнителей составляет от 5% мас. до 95% мас., содержание дезинтеграторов (разрыхлителей) составляет от 0,5% мас. до 7,5% мас.
[00120] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где в препарате в форме капсулы наполнитель представляет собой силицированную микрокристаллическую целлюлозу, связующее вещество представляет собой гидроксипропилцеллюлозу, дезинтегратор (разрыхлитель) представляет собой кроскармеллозу натрия, смазывающее вещество представляет собой стеарат магния.
[00121] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, у которого скорость растворения составляет <45% при рН 1,2~4,5 в течение 30 мин. и скорость растворения составляет >85% при рН 6,0~7,0 в течение 30 мин.
[00122] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где скорость растворения препарата в форме таблетки составляет <40% при рН 1,2~4,5 в течение 30 мин., и скорость растворения препарата в форме таблетки составляет >85% при рН 6,0~7,0 в течение 30 мин.
[00123] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, который представляет собой таблетку, у которой скорость растворения составляет <30% при рН 1,2 в течение 30 мин., скорость растворения составляет <40% при рН 4,5 в течение 30 мин., скорость растворения составляет >85% при рН 6,8 в течение 30 мин.
[00124] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где таблетка представляет собой таблетку с покрытием, у которой скорость растворения составляет <30% при рН 1,2 в течение 30 мин., скорость растворения составляет <40% при рН 4,5 в течение 30 мин., скорость растворения составляет >85% при рH 6,8 в течение 30 мин.
[00125] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, который представляет собой капсулу, у которой скорость растворения составляет <45% при рН 1,2 в течение 30 мин., скорость растворения составляет <45% при рН 4,5 в течение 30 мин., скорость растворения составляет >85% при рН 6,8 в течение 30 мин.
[00126] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где в препарате стандартной дозы количество активатора глюкокиназы составляет от примерно 1 мг до примерно 200 мг, в дополительном варианте составляет от примерно 2 мг до примерно 150 мг, в дополнительном варианте составляет от примерно 2,5 мг до примерно 150 мг, в дополнительном варианте составляет от примерно 5 мг до примерно 150 мг, и в дополнительном варианте, составляет от примерно 5 мг до примерно 100 мг.
[00127] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где в таблетке стандартной дозы количество активатора глюкокиназы составляет от примерно 1 мг до примерно 200 мг, от примерно 2 мг до примерно 150 мг, от примерно 2,5 мг до примерно 150 мг, от примерно 5 мг до примерно 150 мг или от примерно 5 мг до примерно 100 мг.
[00128] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где в таблетке стандартной дозы с покрытием количество активатора глюкокиназы составляет от примерно 1 мг до примерно 200 мг, от примерно 2 мг до примерно 150 мг, от примерно 2,5 мг до примерно 150 мг, от примерно 5 мг до примерно 150 мг или от примерно 5 мг до примерно 100 мг.
[00129] В одном варианте осуществления настоящее изобретение относится к применению твердой дисперсии, композиции твердой дисперсии или препарата активатора глюкокиназы для перорального введения в получении лекарственного средства для лечения и/или предотвращения выбранных заболеваний и расстройств, в частности одного или нескольких заболеваний и расстройств, выбранных из группы, состоящей из диабета I типа, диабета II типа, нарушения толерантности к глюкозе, нарушения гликемии натощак и гипергликемии.
[00130] В одном варианте осуществления настоящее изобретение относится к способу лечения и/или предотвращения выбранных заболеваний и расстройств, в частности одного или нескольких заболеваний или расстройств, выбранных из группы, состоящей из диабета I типа, диабета II типа, нарушения толерантности к глюкозе, нарушения гликемии натощак и гипергликемии, твердой дисперсией, композицией твердой дисперсии или препаратом для перорального введения активатора глюкокиназы, включающему введение пациенту терапевтически эффективного количества твердой дисперсии, композиции твердой дисперсии или препарата активатора глюкокиназы для перорального введения по настоящему изобретению.
[00131] В одном варианте осуществления настоящее изобретение относится к способу получения твердой дисперсии по настоящему изобретению, включая способ расплава, способ растворителя, способ расплава-растворителя, способ распылительной сушки, способ лиофильной сушки испособ измельчения.
[00132] В одном варианте осуществления настоящее изобретение относится к способу получения твердой дисперсии по настоящему изобретению, который включает следующие стадии:
[00133] (1) получение раствора для распылительной сушки, включающее растворение полимерного(ых) носителя(ов) и активатора(ов) глюкокиназы в растворителе;
[00134] (2) распылительная сушка;
[00135] где растворителем является безводный этанол, метанол, изопропанол, этилацетат, ацетон, ацетонитрил, изобутанол, н-гексан, бензол и толуол, их смесь или смесь указанного растворителя с водой.
[00136] В частности, в одном варианте осуществления настоящего изобретения в способе получения твердой дисперсии на стадии распылительной сушки температура входящего воздуха составляет 90-150°С, расход входящего воздуха находится в интервале 0,3-0,5 м3/мин., расход распыляющего газа составляет 10-30 л/мин., и скорость распыления раствора составляет 5-200 мл/мин.
[00137] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, который содержит твердую дисперсию активатора глюкокиназы или композицию твердой дисперсии и эксципиенты.
[00138] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где твердая дисперсия активатора глюкокиназы содержит активатор глюкокиназы или его изотопно-меченые аналоги или фармацевтически приемлемые соли и полимерные носители.
[00139] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где активатор глюкокиназы представляет собой соединение формулы (Ia)

[00140] где
[00141] Z1, Z2, Z3 независимо друг от друга представляют собой водород, низший алкил, низший алкенил, гидроксильную группу, -NH2, галоген, низший алкокси, -CF3, -OCF3, -S(CH3), -S(O2)CH3, -CH2-арил, гетероарил, циано, низший алканоил, -О-арил, -О-СН2-арил, --N(CH3)2, циклоалкил, гетероциклил, -С(О)-гетероциклил или низший алкил, моно- или дизамещенный гидроксильной группой;
[00142] R2 выбран из группы, состоящей из низшего алкила, низшего алкила, моно- или дизамещенного гидроксильной группой, низшего галоалкила, низшего алкоксиалкила, низшего алкилтиоалкила, низшего алкокси, циклоалкила, где указанный циклоалкил является незамещенным или независимо моно- или дизамещенным галогеном или низшим алкилом, гетероциклилом и арилом, где указанный арил является незамещенным или независимо моно- или дизамещенным галогеном; и
[00143] R3 представляет собой низший алкилкарбамоил или
[00144] незамещенный или замещенный гетероарил, соединенный с аминной группой, как показано на рисунке, через атом углерода в кольце, где один из гетероатомов является атомом азота и является соседним по отношению к соединяющему атому углерода кольца, причем указанный замещенный гетероарил является независимо замещенным в положении, которое не является соседним по отношению к соединяющему атому углерода кольца, группой, выбранной из группы, состоящей из
[00145] низшего алкила, галогена, низшего алкоксикарбонила, циано, карбоксильной группы, циклоалкила, арила, 2-оксоoксазолидин-5-илметила, -N(низший алкил)2, 2,2-диметил-[1,3]диоксолан-4-ила, -СН2-диметил-[1,3]диоксолана, трет-бутил-диметилсиланилоксиэтила, незамещенного -СН2-арила, -СН2-арила, замещеного циано или алкоксигруппой, гетероциклила, -СН2-гетероциклила, трет-бутилового эфира -6-(СН2)-2,2-диметил-[1,3]диоксан-4-ил-уксусной кислоты, и низшего алкила, независимо моно-, ди- или тризамещенного гидроксильной группой, галогеном, алкокси, -N(низший алкил)2, -NH2, низшим алканоилом, низшим алкоксикарбонилом, низшим алкенилоксикарбонилом, карбоксильной группой, аминокарбонилом или низший алкоксикарбониламиногруппой,
[00146] его изотопно-меченые аналоги или фармацевтически приемлемые соли.
[00147] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где активатор глюкокиназы выбран из группы, состоящей из следующих соединений или изотопно-меченых аналогов или их фармацевтически приемлемых солей:
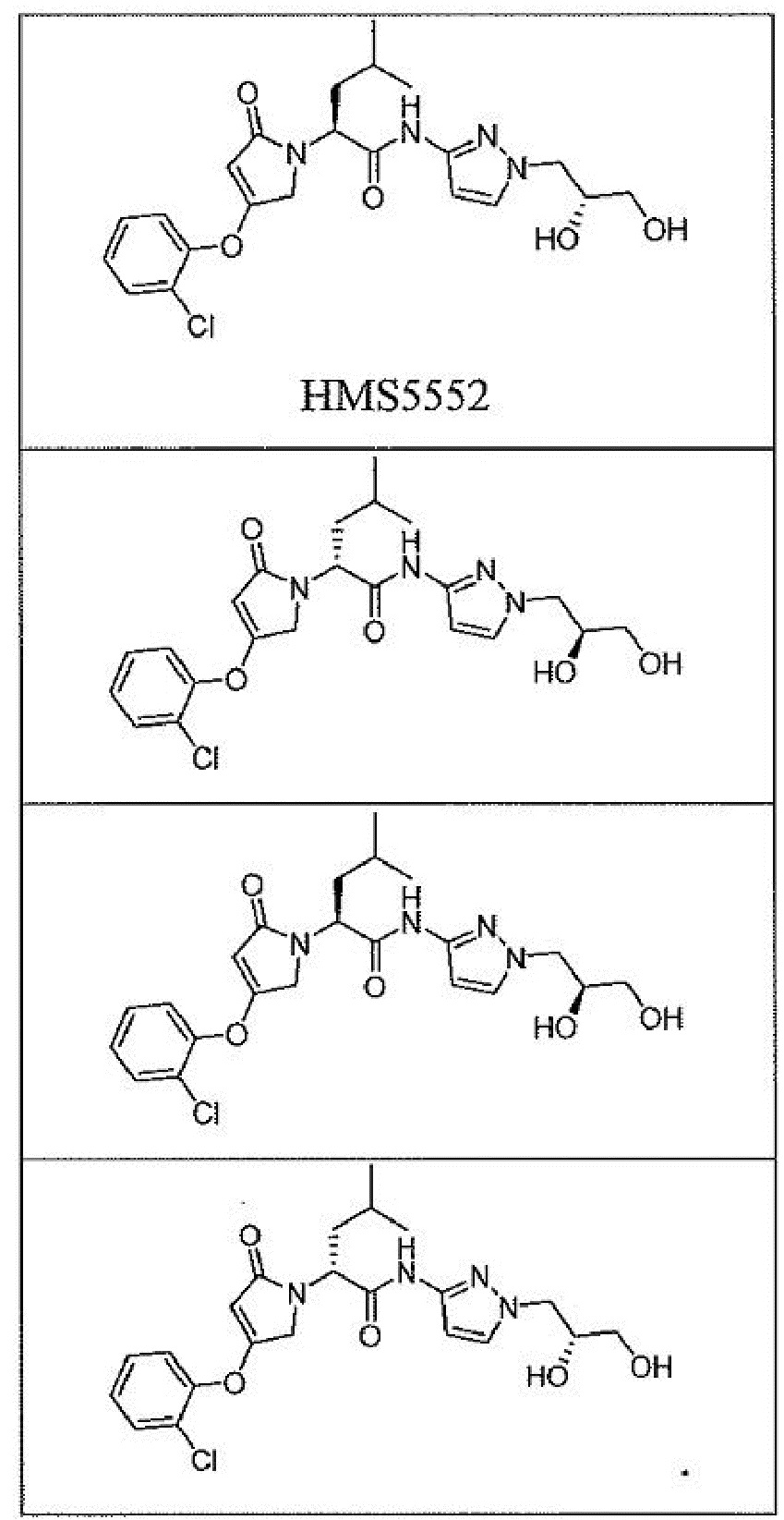
[00148] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где активатор глюкокиназы представляет собой соединение HMS5552 или его изотопно-меченые аналоги или их фармацевтически приемлемые соли.
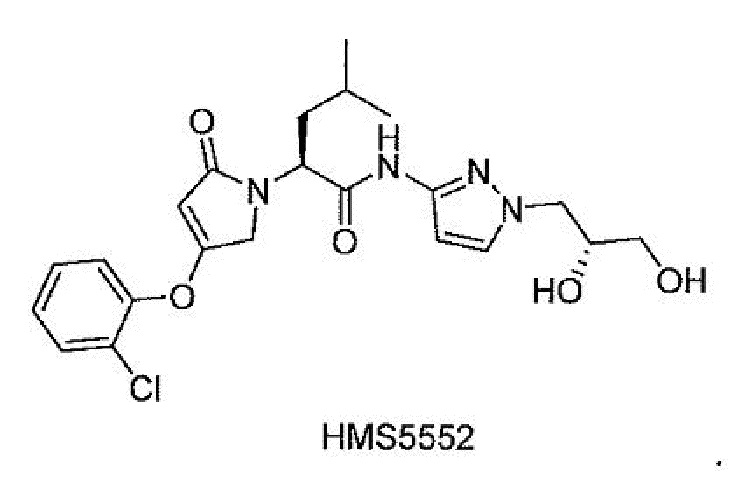
[00149] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где активатор глюкокиназы выбран из группы, состоящей из следующих соединений:

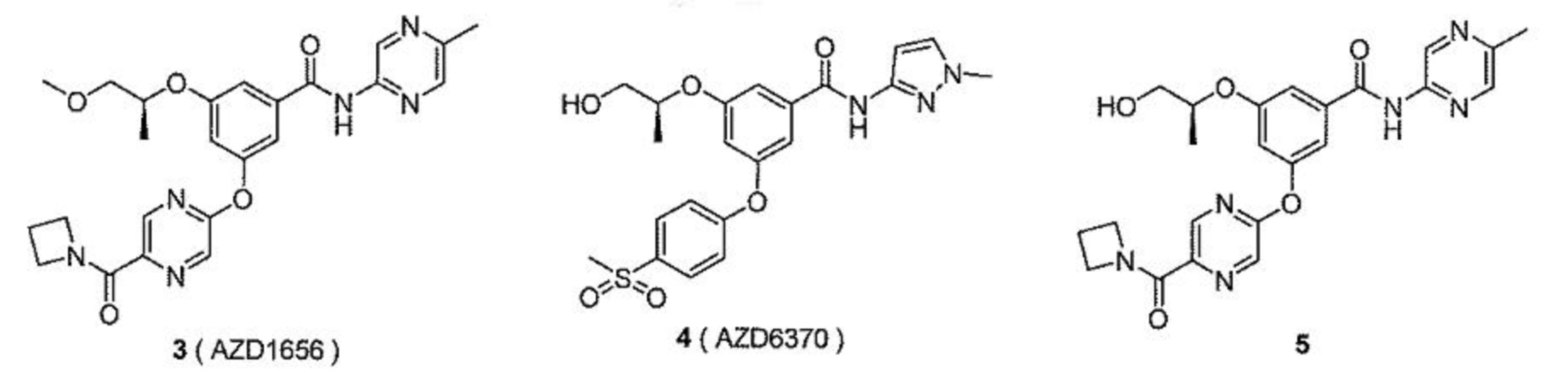
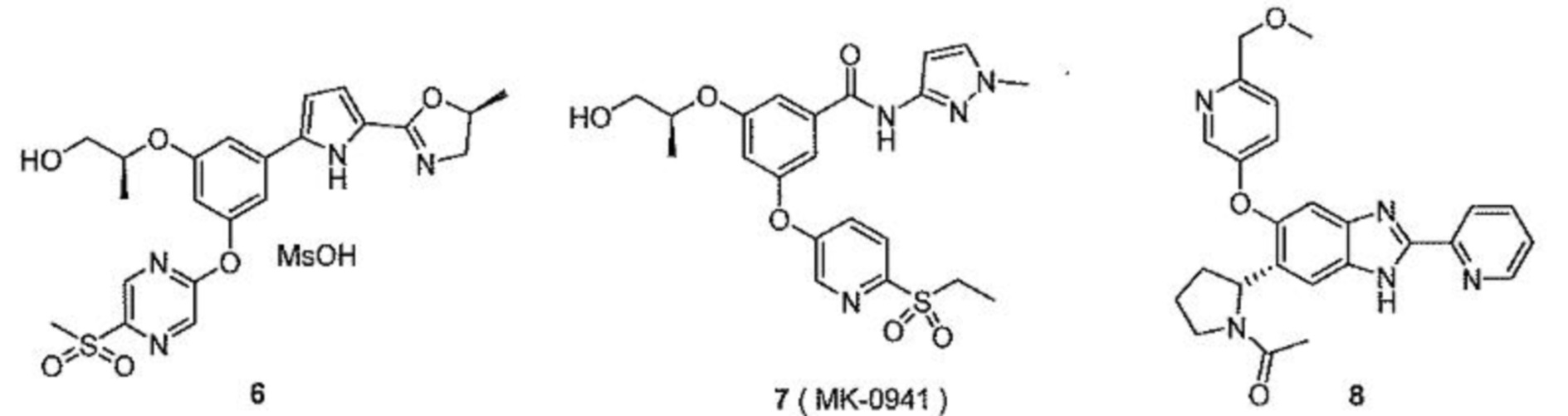
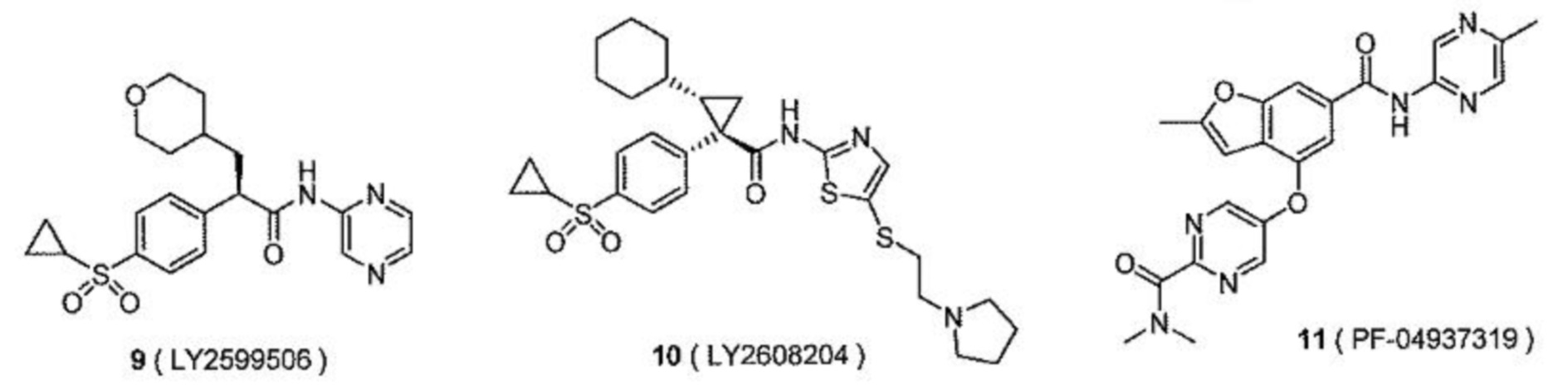
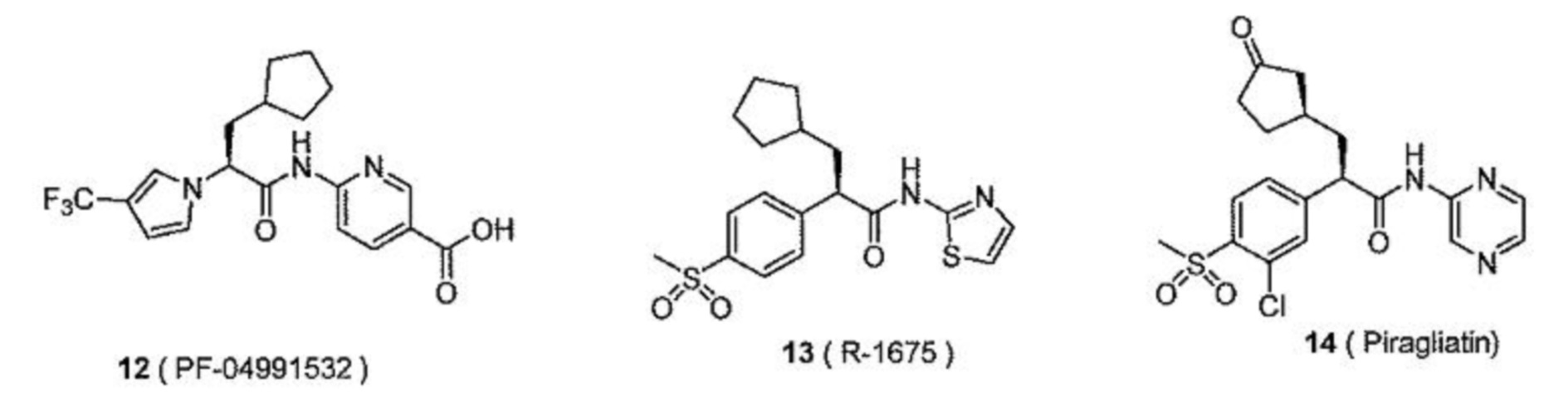
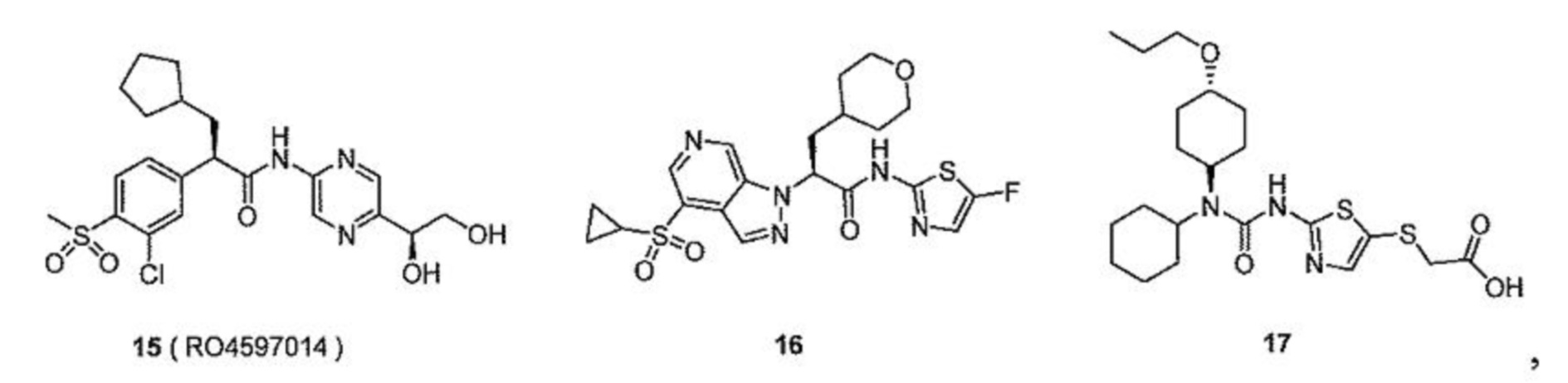
[00150] или их изотопно-меченые аналогов или фармацевтически приемлемых солей.
[00151] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где активатор глюкокиназы выбран из группы, состоящей из TTP399, PF-04937319, RO4597014 и LY2608204, их изотопно-меченых аналогов или фармацевтически приемлемых солей.
[00152] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где полимерные носители представляют собой носители контролируемого высвобождения действующего вещества.
[00153] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где полимерные носители представляют собой полимеры полиакрилатной смолы.
[00154] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где полимерные носители выбраны из группы, состоящей из сополимера метакриловой кислоты и сополимера метакрилата.
[00155] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где полимерные носители выбраны из группы, состоящей из сополимера бутилметакрилата, диметиламиноэтилметакрилата и метилметакрилата; сополимера метакриловой кислоты и этилакрилата; сополимера метакриловой кислоты и метилметакрилата; сополимера этилакрилата, метилметакрилата и хлортриметиламиноэтилметакрилата; сополимера этилакрилата и метилметакрилата; сополимера метакриловой кислоты, метилакрилата и метилметакрилата; сополимера метакриловой кислоты и бутилакрилата.
[00156] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где полимерные носители выбраны из группы, состоящей из бутилметакрилата, сополимера диметиламиноэтилметакрилата и метилметакрилата (1:2:1), сополимера метакриловой кислоты и этилакрилата (1:1), сополимера метакриловой кислоты и метилметакрилата (1:2), сополимера этилакрилата, метилметакрилата и хлортриметиламиноэтилметакрилата (1:2:0,2), сополимера этилакрилата, метилметакрилата и хлортриметиламиноэтилметакрилата (1:2:0,1), сополимера этилакрилата и метилметакрилата (2:1), сополимера метакриловой кислоты и бутилакрилата (35:65), сополимера метакриловой кислоты и метилметакрилата (1:1), сополимера метакриловой кислоты и метилметакрилата (1:1), сополимера метакриловой кислоты и метилметакрилата (35:65).
[00157] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где полимерный носитель выбран из Eudragit.
[00158] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где полимерные носители выбраны из группы, состоящей из Eudragit Е, Eudragit L, Eudragit S.
[00159] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где полимерные носители выбраны из группы, состоящей из Eudragit L100, Eudragit S100, Eudragit Е РО, Eudragit Е 100 или Eudragit L100-55.
[00160] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где полимерные носители представляют собой Eudragit L100, который является сополимером метакриловой кислоты А типа, и анионный сополимер метакриловой кислоты и метилметакрилата (1:1). В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где количество активатора глюкокиназы составляет от 10% мас. до 90% мас. твердой дисперсии.
[00161] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где количество активатора глюкокиназы составляет от 30% мас. до 80% мас. твердой дисперсии.
[00162] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где количество активатора глюкокиназы составляет от 40 до 80% мас. твердой дисперсии.
[00163] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где количество активатора глюкокиназы составляет от 50% мас. до 80% мас. твердой дисперсии.
[00164] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где количество активатора глюкокиназы составляет 50% мас. твердой дисперсии.
[00165] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где количество полимерных носителей составляет от 10% мас. до 90% мас. твердой дисперсии.
[00166] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где твердая дисперсия получена распылительной сушкой.
[00167] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где эксципиенты выбраны из одного или нескольких эксципиентов из группы, состоящей из разбавителя, подсластителя или вкусового вещества, поверхностно-активного вещества, наполнителя, связующего вещества, дезинтегратора (разрыхлителя), смазывающего вещества, вещества для предотвращения слипания/антиадгезивов, модификатора высвобождения действующего вещества, стабилизатора, агента покрытия, эмульгатора и/или солюбилизатора и отдушек.
[00168] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, который представляет собой препарат активатора глюкокиназы для перорального введения с модифицированным высвобождением действующего вещества.
[00169] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, который представляет собой твердый препарат активатора глюкокиназы для перорального введения с модифицированным высвобождением действующего вещества.
[00170] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где твердый препарат активатора глюкокиназы для перорального введения с модифицированным высвобождением действующего вещества выбран из группы, состоящей из таблетки, капсулы, гранулы, порошка, пастилки и пилюли.
[00171] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, который содержит твердую дисперсию по настоящему изобретению и/или наполнители и/или связующие вещества и/или дезинтеграторы (разрыхлители) и/или смазывающие вещества.
[00172] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где твердый препарат активатора глюкокиназы для перорального введения с модифицированным высвобождением действующего вещества представляет собой таблетку.
[00173] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где таблетка содержит твердую дисперсию по настоящему изобретению, наполнители, связующие вещества, дезинтеграторы (разрычлители) и смазывающие вещества.
[00174] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где в таблетке содержание твердой дисперсии активатора глюкокиназы составляет от 1% мас. до 90% мас., содержание наполнителей составляет от 1% мас. до 95% мас., содержание связующих веществ составляет от 0,5% мас. до 10% мас., содержание дезинтеграторов (разрыхлителей) составляет от 0,5% мас. до 7,5% мас., содержание смазывающих веществ составляет от 0,25% мас. до 5% мас.
[00175] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где в таблетке наполнитель представляет собой силицированную микрокристаллическую целлюлозу, микрокристаллическую целлюлозу или лактозу, связующее вещество представляет собой гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу или поливинилпирролидон, дезинтегратор (разрыхлитель) представляет собой кроскармеллозу натрия или карбоксиметилкрахмал натрия, смазывающее вещество представляет собой стеарат магния или натрий стеарилфумарат.
[00176] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где в таблетке наполнитель представляет собой силицированную микрокристаллическую целлюлозу, связующее вещество представляет собой гидроксипропилцеллюлозу, дезинтегратор (разрыхлитель) представляет собой кроскармеллозу натрия, смазывающее вещество представляет собой стеарат магния.
[00177] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где таблетка представляет собой таблетку с покрытием.
[00178] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где таблетка с покрытием содержит агенты покрытия, выбранные из группы, состоящей из натриевой соли карбоксиметилцеллюлозы, ацетата целлюлозы, ацетатфталата целлюлозы, этилцеллюлозы, желатина, фармацевтической глазури, гидроксипропилцеллюлозы, гидроксипропилметилцеллюлозы, фталата гидроксипропилметилцеллюлозы, сополимера метакриловой кислоты, метилцеллюлозы, полиэтиленгликоля, фталата поливинилацетата, шеллака, сахарозы, диоксида титана, карнаубского воска, микрокристаллического воска, зеина и Opadry.
[00179] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где агент покрытия в таблетке с покрытием представляет собой Opadry.
[00180] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где в таблетке с покрытием содержание твердой дисперсии активатора глюкокиназы составляет от 1% мас. до 90% мас., содержание наполнителя составляет от 1% мас. до 95% мас., содержание связующего вещества составляет от 0,5% мас. до 10% мас., содержание дезинтегратора (разрыхлителя) составляет от 0,5% мас. до 7,5% мас., содержание смазывающих веществ составляет от 0,25% мас. до 5% мас., содержание агентов покрытия составляет от 1% мас. до 10% мас.
[00181] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где капсула представляет собой желатиновую капсулу, капсулу HPMC растительного происхождения, кишечнорастворимую капсулу или мягкую капсулу.
[00182] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где капсула содержит твердую дисперсию по настоящему изобретению, наполнители и/или связующие вещества и/или дезинтеграторы (разрыхлители) и/или смазывающие вещества.
[00183] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где в капсуле содержание твердой дисперсии составляет от 1% мас. до 90% мас., содержание наполнителей составляет от 5% мас. до 95% мас., и/или содержание связующих веществ составляет от 0% мас. до 10% мас., и/или содержание дезинтеграторов (разрыхлителей) составляет от 0,5% мас. до 7,5% мас., и/или содержание смазывающих веществ составляет от 0% мас. до 5% мас.
[00184] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где в капсуле наполнитель представляет собой силицированную микрокристаллическую целлюлозу, связующее вещество представляет собой гидроксипропилцеллюлозу, дезинтегратор (разрыхлитель) представляет собой кроскармеллозу натрия, смазывающее вещество представляет собой стеарат магния.
[00185] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, у которого скорость растворения составляет <45% при рН 1,2~4,5 в течение 30 мин., скорость растворения составляет >85% при рН 6,0~7,0 в течение 30 мин.
[00186] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, который представляет собой таблетку, у которой скорость растворения составляет <40% при рН 1,2~4,5 в течение 30 мин., и скорость растворения составляет >85% при рН 6,0~7,0 в течение 30 мин.
[00187] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, который представляет собой таблетку, у которой скорость растворения составляет <30% при рН 1,2 в течение 30 мин., скорость растворения составляет <40% при рН 4,5 в течение 30 мин., и скорость растворения составляет >85% при рН 6,8 в течение 30 мин.
[00188] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где таблетка представляет собой таблетку с покрытием, у которой скорость растворения составляет <30% при рН 1,2 в течение 30 мин., скорость растворения составляет <40% при рН 4,5 в течение 30 мин., и скорость растворения составляет >85% на при рН 6,8 в течение 30 мин.
[00189] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, который представляет собой капсулу, у которой скорость растворения составляет <45% при рН 1,2 в течение 30 мин., скорость растворения составляет <45% при рН 4,5 в течение 30 мин., скорость растворения составляет >85% при рН 6,8 в течение 30 мин.
[00190] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где в препарате стандартной дозы количество активатора глюкокиназы составляет от примерно 1 мг до примерно 200 мг, в одном варианте - от примерно 2 мг до примерно 150 мг, в другом варианте - от примерно 2,5 мг до примерно 150 мг, в еще одном варианте - от примерно 5 мг до примерно 150 мг, в еще одном варианте - от примерно 5 мг до примерно 100 мг.
[00191] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где в таблетке стандартной дозы количество активатора глюкокиназы составляет от примерно 1 мг до примерно 200 мг, от примерно 2 мг до примерно 150 мг, от примерно 2,5 мг до примерно 150 мг, от примерно 5 мг до примерно 150 мг или от примерно 5 мг до примерно 100 мг.
[00192] В одном варианте осуществления настоящее изобретение относится к препарату активатора глюкокиназы для перорального введения, где в таблетке стандартной дозы с покрытием количество активатора глюкокиназы составляет от примерно 1 мг до примерно 200 мг, от примерно 2 мг до примерно 150 мг, от примерно 2,5 мг до примерно 150 мг, от примерно 5 мг до примерно 150 мг или от примерно 5 мг до примерно 100 мг.
[00193] В одном варианте осуществления настоящее изобретение относится к применению препарата активатора глюкокиназы для перорального введения в получении лекарственного средства для лечения и/или предотвращения выбранных заболеваний и расстройств, в частности одного или нескольких заболеваний и расстройств, выбранных из группы, состоящей из диабета I типа, диабета II типа, нарушения толерантности к глюкозе, нарушения гликемии натощак и гипергликемии.
[00194] В одном варианте осуществления настоящее изобретение относится к способу лечения и/или предотвращения выбранных заболеваний и расстройств, в частности одного или нескольких заболеваний и расстройств, выбранных из группы, состоящей из диабета I типа, диабета II типа, нарушения толерантности к глюкозе, нарушения гликемии натощак и гипергликемии, с помощью препарата активатора глюкокиназы для перорального введения, включающему введение пациенту терапевтически эффективного количества препарата активатора глюкокиназы для перорального введения по настоящему изобретению.
[00195] В одном варианте осуществления настоящее изобретение относится к способу получения твердой дисперсии, который включает следующии стадии:
[00196] (1) получение раствора для распылительной сушки, включающее растворение полимерных носителей и активатора глюкокиназы в растворителе;
[00197] (2) распылительная сушка;
[00198] где растворителем является безводный этанол, метанол, изопропанол, этилацетат, ацетон, ацетонитрил, изобутанол, н-гексан, бензол и толуол, их смесь или смесь указанного растворителя с водой.
[00199] В частности, в стадии распылительной сушки температура входящего воздуха составляет 90-150°С, расход входящего воздуха находится в интервале 0,3-0,5 м3/мин., расход распыляющего газа составляет 10-30 л/мин., и скорость распыления раствора составляет 5-200 мл/мин.
[00200] В одном варианте осуществления настоящее изобретение относится к способу получения таблетки активатора глюкокиназы для перорального введения, который включает следующие стадии:
[00201] (1) взвешивание и просеивание: взвешивание предопределенного количества каждого компонента, где смазывающее вещество просивается перед использованием;
[00202] (2) гранулирование: a. добавление внутригранулярных наполнителей, твердой дисперсии и связующих веществ во влажный гранулятор, предварительное смешивание в соответствии с заданными параметрами и добавление взвешенной чистой воды для влажного гранулирования, а затем после выгрузки - влажное гранулирование гранул в мельнице и сушка (сушка в аппарате коробчатого типа или сушка в псевдоожиженном слое), а затем сухое гранулирование гранул в мельнице; или b. добавление внутригранулярных наполнителей и твердой дисперсии во влажный гранулятор, предварительное смешивание в соответствии с заданными параметрами, добавление полученного раствора связующего вещества для влажного гранулирования, затем после выгрузки - мокрое гранулирование гранул в мельнице и сушка (сушка в аппарате коробчатого типа или сушка в псевдоожиженном слое) и затем сухое гранулирование гранул в мельнице;
[00203] (3) смешивание: взвешивание фактически полученных гранул, добавление экстрагранулярных наполнителей, дезинтеграторов (разрыхлителей) и смазывающих веществ в заданном соотношении и смешивание;
[00204] (4) прессование: загрузка смешанных гранул в роторный таблеточный пресс и прессование.
[00205] В одном варианте осуществления настоящее изобретение относится к способу получения таблетки активатора глюкокиназы с покрытием, который включает следующие стадии:
[00206] (1) получение таблеток активатора глюкокиназы;
[00207] (2) получение раствора покрытия: получение суспензии покрытия при перемешивании до получения однородной смеси;
[00208] (3) покрытие: взвешивание таблеток активатора глюкокиназы, выгружка на поддон для получения покрытия, распыление раствора покрытия на таблетки для получения таблеток с покрытием, затем выгрузка таблеток с нанесенных на них покрытием.
[00209] Настоящее изобретение также относится к изотопно-меченым активаторам глюкокиназы, которые идентичны описанным в изобретении за исключением того, что один или несколько их атомов замещены атомом с атомной массой или массовым числом, которые отличаются от атомной массы и массового числа, обычно встречающихся в природе. Примеры изотопов, которые могут быть включены в соединения по настоящему изобретению, включают изотопы водорода, углерода, азота, кислорода, фосфора, фтора и хлора, такие как 2H, 3H, 13C, 14C, 15N, 18O, 17O, 31P, 32P, 35S, 18F и 36Cl, соответственно.
[00210] Некоторые изотопно-меченые соединения (например, соединения, меченые 3H и 14C) могут применяться в исследовании распределения соединений и/или субстрата в тканях. Изотопы, меченные тритием (например, 3Н) и углеродом-14 (т.е. 14С), особенно предпочтительны вследствие простоты получения и легкой распознаваемости. Кроме того, замещение более тяжелыми изотопами, такими как дейтерий (т.е. H), может привести к терапевтическим преимуществам, которые являются результатом большей метаболической стабильности (например, увеличенного периода полувыведения in vivo или снижению необходимой дозы), и, следовательно, в некоторых случаях может быть предпочтительным. Изотопно-меченые соединения обычно могут быть получены в соответствии с методиками, аналогичными описанным в схемах и/или в приведенных ниже примерах, заменой изотопно-немеченого реагента соответствующим изотопно-меченым реагентом.
[00211] В одном варианте осуществления настоящего изобретения препарат для перорального введения с модифицированным высвобождением действующего вещества представляет собой твердый препарат для перорального введения и жидкий препарат для перорального введения.
[00212] В одном варианте осуществления настоящего изобретения твердый препарат для перорального ввещения выбран из группы, состоящей из таблетки, капсулы, гранулы, порошка, пастилки или пилюли.
[00213] В дополнительном варианте осуществления таблетка представляет собой таблетку с покрытием.
[00214] В другом аспекте настоящее изобретение относится к композиции твердой дисперсии активатора глюкокиназы, котоая содержит твердую дисперсию активаторы глюкокиназы и эксципиенты, и эксципиенты выбраны из группы, состоящей из растворителя, например растворителя для таблетки и/или капсулы; подсластителя или вкусового вещества; антиоксиданата; поверхностно-активного вещества; наполнителя; связующего вещества; дезинтегратора (разрыхлителя), например дезинтегратора (разрыхлителя) для таблетки; смазывающего вещества, например смазывающего вещества для таблетки и/или капсулы; вещества для предотвращения слипания/антиадгезива; модификатора высвобождения действующего вещества; стабилизатора; агентов покрытий; красителя; хелатообразующего агента; эмульгатора и/или солюбилизатора; вкусовой добавки и отдушки; полимерные носители.
[00215] В настоящем изобретении описанная композиция твердой дисперсии активатора глюкокиназы может использоваться непосредственно, или она может быть представлена в различных лекарственных формах в соответствии с необходимостью лечения или предотвращения.
[00216] Композиция твердой дисперсии активатора глюкокиназы по настоящему изобретению может быть получена в различных лекарственных формах, таких как таблетки, капсулы, гранулы, порошки, пастилки и пилюли, и может быть получена известным способом. Например, препарат может быть получен посредством таких стадий, как смешивание, грануляция, наполнение капсулы или прессование и нанесние покрытия.
[00217] Однин вариант осуществления настоящего изобретения представляет собой способ получения твердой дисперсии активатора глюкокиназы по настоящему изобретению, и способ выбран из группы, состоящей из распылительной сушки, сушки в псевдоожиженном слое, способа растворителя, экструзии расплава и т.п.
[00218] Один вариант настоящего изобретения представляет собой твердую дисперсию активатора глюкокиназы, полученную способом распылительной сушки, и указанный способ включает следующие стадии:
[00219] (1) получение раствора для распылительной сушки, включающее растворение полимерных носителей и активатора глюкокиназы в растворителе;
[00220] (2) распылительная сушка с контролем температуры и количества входящего воздуха, расхода и давления распыляющего газового потока, а также скорости распыления раствора и т.д.
[00221] В вариантах осуществления настоящего изобретения растворители для препарата твердой дисперсии активатора глюкокиназы включают, но без ограничения, алканолы, эфиры, нитрилы, циклоалканы, ароматические углеводороды, кетоны и т.п. В частности, растворители выбираны из группы, состоящей из безводного этанола, метанола, изопропанола, этилацетата, ацетона, ацетонитрила, изобутанола, н-гексана, бензола и толуола. Это может быть единственный растворитель, смесь растворителей или смесь органического(их) растворителя(ей) с водой.
[00222] В дополнительном варианте осуществления настоящее изобретение относится к способу лечения и/или предотвращения выбранных заболеваний и расстройств, в частности одного или нескольких заболеваний и расстройств, выбранных из группы, состоящей из диабета I типа, диабета II типа, нарушения толерантности к глюкозе, нарушения гликемии натощак и гипергликемии, твердой дисперсией или препаратом активатора глюкокиназы по настоящему изобретению, включающему введение пациенту терапевтически эффективного количества препарата активатора глюкокиназы для перорального введения по настоящему изобретению.
[00223] В дополнительном варианте осуществления настоящее изобретение относится к применению твердой дисперсии активатора глюкокиназы или препарата, содержащего композицию, в получении лекарственного средства для лечения и/или предотвращения выбранных заболеваний и расстройств, в частности одного или нескольких заболеваний и расстройств, выбранных из группы, состоящей из диабета I типа, диабета II типа, нарушения толерантности к глюкозе, нарушения гликемии натощак и гипергликемии.
[00224] Количество активатора глюкокиназы, используемое в твердой дисперсии активатора глюкокиназы по настоящему изобретению, может изменяться в интервале от примерно 1% мас. до примерно 99% мас. из расчета на общую массу твердой дисперсии. В одном варианте осуществления настоящего изобретения диапазон содержания активатора глюкокиназы составляет примерно 1% мас., примерно 2% мас., примерно 3% мас., примерно 4% мас., примерно 5% мас., примерно 6% мас., примерно 7% мас., примерно 8% мас., примерно 9% мас., примерно 10% мас., примерно 11% мас., примерно 12% мас., примерно 13% мас., примерно 14% мас., примерно 15% мас., примерно 16% мас., примерно 17% мас., примерно 18% мас., примерно 19% мас., примерно 20% мас., примерно 21% мас., примерно 22% мас., примерно 23% мас., примерно 24% мас., примерно 25% мас., примерно 26% мас., примерно 27% мас., примерно 28% мас., примерно 29% мас., примерно 30% мас., примерно 31% мас., примерно 32% мас., примерно 33% мас., примерно 34% мас., примерно 35% мас., примерно 36% мас., примерно 37% мас., примерно 38% мас., примерно 39% мас., примерно 40% мас., примерно 41% мас., примерно 42% мас., примерно 43% мас., примерно 44% мас., примерно 45% мас., примерно 46% мас., примерно 47% мас., примерно 48% мас., примерно 49% мас., примерно 50% мас., примерно 51% мас., примерно 52% мас., примерно 53% мас., примерно 54% мас., примерно 55% мас., примерно 56% мас., примерно 57% мас., примерно 58% мас., примерно 59% мас., примерно 60% мас., примерно 61% мас., примерно 62% мас., примерно 63% мас., вес примерно 64%, примерно 65% мас., примерно 66% мас., примерно 67% мас., приблизительно 68% мас., примерно 69% мас., примерно 70% мас., вес примерно 71%, примерно 72% мас., примерно 73% мас., примерно 74% мас., примерно 75% мас., примерно 76% мас., примерно 77% мас., примерно 78% мас., примерно 79% мас., примерно 80% мас., примерно 81%, примерно 82% мас., примерно 83%, примерно 84% мас., примерно 85% мас., примерно 86% мас., примерно 87% мас., примерно 88% мас., примерно 89% мас., примерно 90% мас., примерно 91% мас., примерно 92% мас., примерно 93% мас., примерно 94% мас., примерно 95% мас., примерно 96% мас., примерно 97% мас., примерно 98% мас. или примерно 99% мас., или любой поддиапазон между ними. В одном варианте осуществления интервал количества активатора глюкокиназы составляет от примерно 1% мас. до примерно 20% мас. В дополнительном варианте осуществления интервал количества активатора глюкокиназы составляе от примерно 2% мас. до примерно 40% мас. В еще одном дополнительном варианте осуществления интервал количества активатора глюкокиназы составляет от примерно 30% мас. до примерно 60% мас. В еще одном дополнительном варианте осуществления интервал количества активатора глюкокиназы составляет от примерно 60% мас. до примерно 80% мас. В еще одном пополнительном варианте осуществления интервал количества активатора глюкокиназы составляет от примерно 70% мас. до примерно 90% мас. В еще одном дополнительном варианте осуществления интервал количества активатора глюкокиназы составляет от примерно 80% мас. до примерно 100% мас.
[00225] Количество полимерных носителей, используемое в твердой дисперсии активатора глюкокиназы, может изменяться в интервале от примерно 1% мас. до примерно 99% мас. из расчета на общую массу твердой дисперсии. В одном варианте осуществления настоящего изобретения интервал содержания полимерных носителей составляет примерно 1% мас., примерно 2% мас., примерно 3% мас., примерно 4% мас., примерно 5% мас., примерно 6% мас., примерно 7% мас., примерно 8% мас., примерно 9% мас., примерно 10% мас., примерно 11% мас., примерно 12% мас., примерно 13% мас., примерно 14% мас., примерно 15% мас., примерно 16% мас., примерно 17% мас., примерно 18% мас., примерно 19% мас., примерно 20% мас., примерно 21% мас., примерно 22% мас., примерно 23% мас., примерно 24% мас., примерно 25% мас., примерно 26% мас., примерно 27% мас., примерно 28% мас., примерно 29% мас., примерно 30% мас., вес примерно 31%, примерно 32% мас., примерно 33% мас., примерно 34% мас., примерно 35% мас., примерно 36% мас., примерно 37% мас., примерно 38% мас., примерно 39% мас., примерно 40% мас., примерно 41% мас., примерно 42% мас., примерно 43% мас., вес примерно 44%, примерно 45% мас., примерно 46% мас., примерно 47% мас., примерно 48% мас., примерно 49% мас., примерно 50% мас., примерно весе 51%, примерно 52%, примерно 53%, примерно 54% мас., примерно 55% мас., примерно 56% мас., примерно 57% мас., примерно 58%, примерно 59%, примерно 60% мас., примерно 61%, примерно 62% мас., примерно 63% мас., примерно 64% мас., примерно 65% мас., примерно 66% мас., примерно 67% мас., примерно 68% мас., примерно 69% мас., примерно 70% мас., примерно 71% мас., примерно 72% мас., примерно 73% мас., примерно 74% мас., примерно 75% мас., примерно 76% мас., примерно 77% мас., примерно 78% мас., примерно 79% мас., примерно 80% мас., примерно 81% мас., примерно 82% мас., примерно 83% мас., примерно 84% мас., примерно 85% мас., примерно 86% мас., примерно 87% мас., примерно 88% мас., примерно 89% мас., примерно 90% мас., примерно 91% мас., примерно 92% мас., примерно 93% мас., примерно 94% мас., примерно 95% мас., примерно 96% мас., вес примерно 97%, примерно 98% мас. или примерно 99% мас. или любой поддиапазон между ними. В одном варанте осуществления настоящего изобретения интервал содержания полимерных носителей составляет от 1% мас. до 20% мас. В дополнительном варианте осуществления настоящего изобретения интервал содержания может составлять от 2% масс. до примерно 40% масс. В дополнительном варианте осуществления настоящего изобретения интервал содержания составляет от 30% мас. до 60% мас. В дополнительном варианте осуществления настоящего изобретения интервал содержания составляет от 60% мас. до 80% мас. В дополнительном варианте осуществления настоящего изобретения интервал содержания составляет от 70% мас. до 90% мас. В дополнительном варианте осуществления настоящего изобретения интервал содержания составляет от 80% мас. до примерно 100% мас.
[00226] Предпочтительно, в твердой дисперсии активатора глюкокиназы по настоящему изобретению интервал содержания активатора глюкокиназы составляет 30-60% мас., а интервал содержания полимерных носителей составляет 40-70% мас. из расчета на общую массу твердой дисперсии.
[00227] Более предпочтительно, в твердой дисперсии активатора глюкокиназы по настоящему изобретению интервал содержания активатора глюкокиназы составляет 40-60% мас., а интервал содержания полимерных носителей составляет 40-60% мас. из расчета на общую массу твердой дисперсии.
[00228] В одном варанте осуществления настоящего изобретения полимерные носители в твердой дисперсии выбраны из группы, состоящей из полимера на основе полипропиленовой смолы, который представляет собой полимерное соединение, полученное полимеризацией акриловой кислоты (или метакриловой кислоты и ее сложных эфиров, таких как метиловый эфир, этиловые эфиры и т.п.) (мономер) или полученное полимеризацией двух мономеров (бинарная полимеризация) или трех мономеров (тройная полимеризация) в определенном соотношении, используя акриловую кислоту и метакриловую кислоту (или ее сложный эфир, такой как метиловый эфир, этиловый эфир, диметиламиноэтиловый эфир и т.д.).
[00229] Полимерные носители, используемые в твердой дисперсии по настоящему изобретению, выбраны из группы, состоящей из сополимера бутилметакрилата, диметиламиноэтилметакрилата и метилметакрилата; сополимера метакриловой кислоты и этилакрилата; сополимера метакриловой кислоты и метилметакрилата; сополимера этилакрилата, метилметакрилата и хлортриметиламиноэтилметакрилата; сополимера этилакрилата и метилметакрилата; сополимера метакриловой кислоты, метилакрилата и метилметакрилата и сополимера метакриловой кислоты и бутилакрилата.
[00230] Кроме того, полимерные носители выбраны из группы, состоящей из сополимера бутилметакрилата, диметиламиноэтилметакрилата и метилметакрилата (1:2:1), сополимера метакриловой кислоты и этилакрилата (1:1), сополимера метакриловой кислоты и метилметакрилата (1:2), сополимера этилакрилата, метилметакрилата и хлортриметиламиноэтилметакрилата (1:2:0,2), сополимера этилакрилата, метилметакрилата и хлортриметиламиноэтилметакрилата (1:2:0,1), сополимера этилакрилата и метилметакрилата (2:1), сополимера метакриловой кислоты и бутилакрилата (35:65), сополимера метакриловой кислоты и метилметакрилата (1:1), сополимера метакриловой кислоты и метилметакрилата (35:65).
[00231] Кроме того, полимерный носитель представляет собой Eudragit, в том числе Eudragit Е, Eudragit L и Eudragit S, Eudragit RL и Eudragit RS, где Eudragit E получают полимеризацией диметиламинометакрилата и других нейтральных метакрилатов, включая сополимеры метакрилата и метилметакрилата; Eudragit L и Eudragit S получают полимеризацией метакриловой кислоты и метакрилатов в различных соотношениях, включая метакриловую кислоту и метилметакрилат в соотношении свободный карбоксил:эфир=1:1 или метакриловую кислоту и метилметакрилат в соотношении свободный карбоксил:эфир=1:2; Eudragit RL и Eudragit RS представляют собой сополимеры акриловой кислоты, содержащей некоторые четвертичные аминные группы, и метакрилата, включая сополимер акриловой кислоты, содержащей 10% четвертичной аминной группы, и метакрилата, и сополимер акриловой кислоты, содержащей 5% четвертичной аминной группы, и метакрилата.
[00232] Кроме того, полимерные носители выбраны из группы, состоящей из
[00233] Eudragit E100, который представляет собой сополимер бутилметакрилата, диметиламиноэтилметакрилата и метилметакрилата (1:2:1), включая Eudragit E PO;
[00234] Eudragit L100, который представляет собой сополимер метакриловой кислоты А типа, который представляет собой анионогенный сополимер метакриловой кислоты и метилметакрилата (1:1);
[00235] Eudragit S100, который представляет собой сополимер метакриловой кислоты и метилметакрилата (1:2);
[00236] а также может быть понятно, что примеры дополнительных эксципиентов, используемых в композиции твердой дисперсии и препарате активатора глюкокиназы по настоящему изобретению, включают, но без ограничения, разбавитель, такой как разбавитель для таблетки и/или капсулы; подсластитель или вкусовую добавку; антиоксидант; поверхностно-активное вещество; наполнитель; связующее вещество; дезинтегратор (разрыхлитель0, такой как дезинтегратор (разрыхлитель) для таблетки; смазывающее вещество, такое как смазывающее вещество для таблетки и/или капсулы; вещество для предотвращения слипания/антиадгезив; модификатор высвобождения действующего вещества; стабилизатор; вещества покрытия; краситель; хелатообразующий агент; эмульгатор и/или солюбилизатор; вкусовое вещество и отдушку.
[00237] Примеры разбавителей, которые подходят для использования в настоящем изобретении, включают, но без ограничения, омега-3 жирные кислоты или их производные, лактозу, декстрозу, сахарозу, маннит, сорбит, целлюлозу, включая силицированную микрокристаллическую целлюлозу, сахарин натрия, глюкозу и/или глицин. Кроме того, в дополнение к перечисленным выше разбавители для таблеток и/или капсул, которые подходят для настоящего изобретения, включают, но без ограничения, карбонат кальция, фосфат кальция, фосфат кальция, сульфат кальция, целлюлозный порошок, глюкановое связующее вещество, фруктозу, каолин, крахмал, прежелатинированный крахмал, прессованный сахар, кондитерский сахар и их комбинации.
[00238] Примеры подсластителей или вкусовых веществ, которые подходят для настоящего изобретения, включают, но без ограничения, эфирные масла, водорастворимые экстракты, сахар, моносахариды, олигосахариды, альдозу, кетозу, декстрозу, мальтозу, лактозу, глюкозу, фруктозу, сахарозу, маннит, ксилит, D-сорбит, эритрит, пентит, гексит, мальтит, ацесульфам калия, талин, глицирризин, сукралозу, аспартам, сахарин, сахарин натрия, цикламат натрия, ароматизаторы альдегида евгенилформиата и их комбинации.
[00239] Примеры антиоксидантов, которые подходят для настоящего изобретения, включают, но без ограничения, α-токоферол, аскорбиновую кислоту, аскорбилпальмитат, бутилированный гидроксианизол, бутилированный гидрокситолуол, тиоглицерин, метабисульфит калия, пропионовую кислоту, пропилгаллат, аскорбат натрия, бисульфит натрия, метабисульфит натрия и сульфит натрия и их комбинации.
[00240] Примеры поверхностно-активных веществ, которые подходят для настоящего изобретения, включают, но без ограничения соль алкилсульфата, такую как диэтаноламмониевая соль лаурилсульфата; алкиларилсульфонат, такой как додецилбензолсульфонат кальция; продукт присоединения алкилфенола и оксиалкилена, такой как этоксилат нонилфенола-С18; продукт соединения спирта и алкиленоксида, такой как тридециловый спирт-этоксилат С16; мыло, такое как стеарат натрия; алкилнафталинсульфонат, такой как дибутилнафталин натрия; диалкиловый эфир сульфосукцината, такой как бис(2-этилгексил)сульфосукцинат натрия; сложный эфир сорбита, такой как сорбитолеат; четвертичные аммониевые соли, такие как хлорид лаурилметиламмония; сложные полиэтиленгликолевые эфиры жирных кислот, такие как стеарат полиэтиленгликоля; блок-сополимер оксида этилена и окисида пропилена; соль моноалкилфосфата и соль диалкилфосфата; растительное масло, такое как соевое масло, рапсовое масло, оливковое масло, касторовое масло, подсолнечное масло, кокосовое масло, кукурузное масло, хлопковое масло, льняное масло, пальмовое масло, арахисовое масло, сафлоровое масло, кунжутное масло, тунговое масло и т.д.; сложные эфиры вышеуказанных растительных масел и их сочетание.
[00241] Примеры наполнителей, которые подходят для настоящего изобретения, включают, но без ограничения, производные целлюлозы, такие как микрокристаллическая целлюлоза или лигноцеллюлоза (в том числе микрокристаллическая целлюлоза и силицированная микрокристаллическая целлюлоза), лактозу, безводную лактозу или моногидрат лактозы, сахарозу, крахмал, желатинированный крахмал, декстрозу, маннит (включая маннит Pearlitol SD и 200), фруктозу, ксилит, сорбит, кукурузный крахмал, модифицированный кукурузный крахмал, неорганические соли, такие как карбонат кальция, фосфат кальция, дикальций фосфат, сульфат кальция, декстриновое/глюкозное связующее вещество, мальтодекстрин, прессованный сахар и другие известные компатибилизаторы или наполнители/или смеси двух или нескольких из них.
[00242] Примеры связующих веществ, которые подходят для настоящего изобретения, включают, но без ограничения, карбоксиметилцеллюлозу (в том числе и карбоксиметилцеллюлозу натрия), гидроксипропилцеллюлозу (в том числе гидроксипропилцеллюлозу EXF), кукурузный крахмал, желатинированный крахмал, модифицированный кукурузный крахмал, поливинилпирролидон (ПВП), гидроксипропилметилцеллюлозу (ГПМЦ) (в том числе гидроксипропилметилцеллюлозу 2208), лактозу, гуммиарабик, этилцеллозолу, ацетат целлюлозы и восковые связующие вещества, такие как карнаубский воск, парафин, цетиловый воск, полиэтиленовый или микрокристаллический воск и другое обычно применяемое связующее вещество и/или смеси двух или нескольких из них. Кроме того, в дополнение к вышеуказанным связующим веществам связующие вещества для таблеток, подходящие для использования в настоящем изобретении, включают, но без ограничения, альгиновую кислоту, микрокристаллическую целлюлозу, декстрин, желатин, жидкую глюкозу, гуаровую камедь, метилцеллюлозу, полиэтиленоксид, повидон, сироп и их комбинацию.
[00243] Примеры дезинтеграторов (разрыхлителей), которые подходят для настоящего изобретения, включают, но без ограничения, кроскармеллозу натрия, кросповидон, крахмал, картофельный крахмал, прежелатинированный крахмал, кукурузный крахмал, карбоксиметилкрахмал натрия, крахмалгликолят натрия, микрокристаллическую целлюлозу, низкозамещенную гидроксипропилцеллюлозу и другие известные дезинтеграторы. Некоторые специфические типов дезинтеграторов подходят для использования в препаратах, описанных в настоящем документе. Например, может использоваться кросповидон любого сорта, включая, например, кросповидон XL-10 и кросповидон, выбранный из Kollidon CL®, Polyplasdone XL®, Kollidon CL-M®, Polyplasdone XL-10® и Polyplasdone INF-10®. Кроме того, в дополнение к вышеуказанным дезинтеграторам подходящий для использования в таблетке по настоящему изобретению дезинтегратор, включает, но без ограничения, альгиновую кислоту, polakolin калий, крахмалгликолят натрия, прежелатинированный крахмал и их комбинации.
[00244] Примеры смазывающих веществ, которые подходят для настоящего изобретения, включают, но без ограничения, стеарат магния, стеарат цинка, стеарат кальция, тальк, карнаубский воск, стеариновую кислоту, пальмитиновую кислоту, стеарилфумарат натрия, лаурилсульфат натрия, глицерилпальмитостеарат, пальмитиновую кислоту, миристиновую кислоту, гидрированное растительное масло и гидрированный жир и другие известные смазывающие вещества и/или смеси двух или более из них. Кроме того, в дополнение к вышеупомянутым смазывающим веществам смазывающие вещества, подходящие для использования в таблетках и/или капсулах по настоящему изобретению, включают, но без ограничения, бегенат глицерина, легкое минеральное масло, полиэтиленгликоль, высокоочищенную стеариновую кислоту и их комбинациями.
[00245] Примеры веществ для предотвращения слипания и/или антиадгезивов, которые подходят для настоящего изобретения, включают, но без ограничения, диоксид кремния, коллоидный диоксид кремния, силикат магния, трисиликат магния, тальк и другие формы диоксида кремния, такие как агрегированный силикат и гидратированный диоксид кремния.
[00246] Примеры модификаторов высвобождения действующего вещества, которые подходят для настоящего изобретения, включают, но без ограничения, гидроксипропилметилцеллюлозу, поливиниловый спирт (ПВС), этилцеллюлозу, полимер метакриловой кислоты (сложный эфир), гидроксипропилцеллюлозу, крахмал, камедь, простой эфир целлюлозы, производное белка, нейлон, акриловую смолу, полимолочную кислоту, поливинилхлорид, поливинилпирролидон, ацетатфталат целлюлозы и их комбинации.
[00247] Стабилизаторы, которые подходят для настоящего изобретения, включают, но без ограничения ими, жирные кислоты, такие как олеиновая кислота и ее натриевая соль, холевая кислота и дезоксихолевая кислота, катионные липиды, такие как стеарамид, и анионные стабилизаторы, такие как фосфатидилэтаноламин, фосфатидилсерин, фосфолипиды, фосфатидилглицерины и их комбинации. В одном варианте осуществления настоящего изобретения стабилизатор представляет собой олеиновую кислоту.
[00248] Вещества покрытия, которые подходят для настоящего изобретения, включают, но без ограничения, карбоксиметилцеллюлозу натрия, ацетат целлюлозы, ацетатфталат целлюлозы, этилцеллюлозу, желатин, фармацевтическую глазурь, гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу, фталат гидроксипропилметилцеллюлозы, сополимер метакриловой кислоты, метилцеллюлозу, полиэтиленгликоль, поливинилацетат фталат, шеллак, сахарозу, диоксид титана, карнаубский воск, микрокристаллический воск, зеин, Opadry, такой как Opadry 03k12429, и их комбинации.
[00249] Красители, которые подходят для настоящего изобретения, включают, но без ограничения, карамель, красный краситель, желтый краситель, черный краситель или их смеси, оксид железа и их комбинации.
[00250] Хелатообразующие агенты, которые подходят для настоящего изобретения, включают, но без ограничения, этилендиаминтетрауксусную кислоту и ее соли (ЭДТУК), эдетовую кислоту, этанолмаид гентизиновой кислоты, оксихинолинсульфат и их комбинации.
[00251] Эмульгаторы и/или солюбилизаторы, которые подходят для настоящего изобретения, включают, но без ограничения, гуммиарабик, холестерин, диэтаноламин, глицерилмоностеарат, ланолиновые спирты, лецитин, моно- и диглицериды, моноэтаноламин, олеиновую кислоту, олеиловый спирт, полоксамер, полиоксиэтилен 50 стеарат, полиоксиэтилен 35 касторовое масло, полиоксиэтилен 40 гидрогенизированное касторовое масло, полиоксиэтилен 10 олеиловый эфир, полиоксиэтилен 20 цетостеариловый эфир, полиоксиэтилен 40 стеарат, полисорбат 20, полисорбат 40, полисорбат 60, полисорбат 80, пропиленгликольдиацетат, пропиленгликольмоностеарат, лаурилсульфат натрия, стеарат натрия, сорбитанмонолаурат, сорбитанмоноолеат, сорбитанмонопальмитат, сорбитанмоностеарат, стеариновую кислоту, триэтаноламин, эмульгирующий воск и их комбинации.
[00252] Вкусовые добавки и отдушки, которые подходят для настоящего изобретения, включают, но без ограничения, анетол, бензальдегид, этилванилин, ментол, метилсалицилат, глутамат натрия, масло цветов апельсина, мяту перечную, масло мяты, мятный спиртовой раствор, розовое масло, розовую воду с более сильным запахом, тимол, настойку толуанского бальзама, ваниль, ванильную настойку, ванилин и их комбинацию.
[00253] Растворители, подходящие для использования в настоящем изобретении, включают, но без ограничения, ацетон, спирт, безводный этанол, разбавленный спирт, пентенгидрат, бензилбензоат, бутанол, четыреххлористый углерод, хлороформ, кукурузное масло, хлопковое масло, этилацетат, глицерин, гександиол, изопропанол, метанол, дихлорметан, метилизобутилкетон, минеральное масло, арахисовое масло, полиэтиленгликоль, пропиленкарбонат, пропиленгликоль, кунжутное масло, воду для инъекций, стерильную воду для инъекций, стерильную промывную воду, чистую воду и ее сочетание.
[00254] Количество активного ингредиента в препарате стандартной дозы может изменяться от примерно 1 мг до примерно 200 мг, предпочтительно от примерно 2 мг до примерно 150 мг, более предпочтительно от примерно 2,5 мг до примерно 150 мг, еще более предпочтительно от примерно 5 мг до примерно 150 мг, в зависимости от конкретного применения.
[00255] В частности, содержание активатора глюкокиназы в таблетке стандартной дозы по настоящему изобретению составляет от примерно 1 мг до примерно 200 мг, предпочтительно от примерно 2 мг до примерно 150 мг, более предпочтительно от примерно 5 мг до примерно 100 мг.
[00256] Далее изобретение будет описано со ссылкой на прилагаемые чертежи и конкретные варианты осуществления, но изобретение не ограничивается представленными вариантами осуществления, а различные модификации и замены, сделанные на основе технологии изобретения, входят в сферу применения изобретения.
Примеры
Получение твердой дисперсии активатора глюкокиназы
[00257] Химические соединения, используемые в настоящем изобретении, являются коммерчески доступными от компаний, включая Shin-Etsu Japan, Evonik Germany, J.T.Baker US, SCR China, Ashland US, FMC US, JRS Germany, Colorcon US, Capsugel, BASF, Zhenxing China и т.п. Производстводственное оборудование и стенды аналитических испытаний и т.п. коммерчески доступны от таких компаний, как Sartorius, Nikon, Sympatec, Bruker, Gea Niro, Korsch, Erweka, Agilent, Quadro Engineering, Canada; Warters, US; TA, US; SOTAX, Switzerland; Mettler Toledo Instrument Newark, DE.
I. Получение твердой дисперсии активатора глюкокиназы
1.1 Получение раствора твердой дисперсии, используемого для распылительной сушки
Пример 1 (массовое соотношение активных ингредиентов и полимерных носителей составляет 1:9)
[00258] 6,75 г Eudragit L100 (Evonik Germany) взвешивают и добавляют к безводному этанолу (J.T. Baker) при перемешивании. После его полного растворения к раствору добавляют 0,75 г соединения HMS5552. Перемешивание продолжают после добавления достаточного количества безводного этанола для получения 50 мл раствора от желтого до оранжевого цвета.
Пример 2 (массовое соотношение активных ингредиентов и полимерных носителей составляет 3:7)
[00259] 5,25 г Eudragit L100 (Evonik Germany) взвешивают и добавляют к безводному этанолу (J.T. Baker) при перемешивании. После его полного растворения добавляют 2,25 г соединения HMS5552. Перемешивание продолжают после добавления достаточного количества безводного этанола для получения 50 мл раствора от желтого до оранжевого цвета.
Пример 3 (массовое соотношение активных ингредиентов и полимерных носителей составляет 5:5)
[00260] 3,75 г Eudragit L100 (Evonik Germany) взвешивают и добавляют к безводному этанолу (J.T. Baker) при перемешивании. После его полного растворения добавляют 3,75 г соединения HMS5552. Перемешивание продолжают после добавления достаточного количества безводного этанола для получения 50 мл раствора от желтого до оранжевого цвета.
Пример 4 (массовое соотношение активных ингредиентов и полимерных носителей составляет 7:3)
[00261] 2,25 г Eudragit L100 (Evonik Germany) взвешивают и добавляют к безводному этанолу (J.T. Baker) при перемешивании. После его полного растворения к раствору добавляют 5,25 г соединения HMS5552. Перемешивание продолжают после добавления достаточного количества безводного этанола для получения 50 мл раствора от желтого до оранжевого цвета.
Пример 5 (массовое соотношение активных ингредиентов и полимерных носителей составляет 8:2)
[00262] 1,5 г Eudragit L100 (Evonik Germany) взвешивают и добавляют к безводному этанолу (J.T. Baker) при перемешивании. После его полного растворения к раствору добавляют 6 г соединения HMS5552. Перемешивание продолжают после добавления достаточного количества безводного этанола для получения 50 мл от раствора желтого до оранжевого цвета.
Пример 6 (массовое соотношение активных ингредиентов и полимерных носителей составляет 9:1)
[00263] 0,75 г Eudragit L100 (Evonik Germany) взвешивают и добавляют к безводному этанолу (J.T. Baker) при перемешивании. После его полного растворения к раствору добавляют 6,75 г соединения HMS5552. Перемешивание продолжают после добавления достаточного количества безводного этанола для получения 50 мл раствора от желтого до оранжевого цвета.
Пример 7 (массовое соотношение активных ингредиентов и полимерных носителей составляет 6:4)
[00264] 3,0 г Eudragit L100 (Evonik Germany) взвешивают и добавляют к безводному этанолу (J.T. Baker) при перемешивании. После его полного растворения добавляют 4,5 г соединения HMS5552. Перемешивание продолжают после добавления достаточного количества безводного этанола для получения 50 мл раствора от желтого до оранжевого цвета.
Пример 8 (массовое соотношение активных ингредиентов и полимерных носителей составляет 4:6)
[00265] 4,5 г Eudragit L100 (Evonik Germany) взвешивают и добавляют к безводному этанолу (J.T. Baker) при перемешивании. После его полного растворения к раствору добавляют 3,0 г соединения HMS5552. Перемешивание продолжают после добавления достаточного количества безводного этанола для получения 50 мл раствора от желтого до оранжевого цвета.
Пример 9 (массовое соотношение активных ингредиентов и полимерных носителей составляет 5:5)
[00266] 187,5 г Eudragit L100 (Evonik Germany) взвешивают и добавляют к безводному этанолу (Zhenxing China). После его полного растворения к раствору добавляют 187,5 г соединения HMS5552. Перемешивание продолжают после добавления достаточного количества безводного этанола для получения 2500 мл раствора от желтого до оранжевого цвета.
1.2 Получение твердой дисперсии активатора глюкокиназы
[00267] Твердую дисперсию активатора глюкокиназы получают распылительной сушкой полученного выше раствора. Нумерация полученных образов твердой дисперсии соответствует нумерации приведенных выше примеров. Устройства распылительной сушки, которые могут быть использованы для настоящего изобретения, включают, но без ограничения ими, устройства распылительной сушки производства компаний Niro GEA Process Engineering Inc., Buchi Labortechnik AG, ProCept и SPX ANHYDROUS. Распылительная сушка может проводиться подбором соотвествующей температуры входящего сухого газа, количества входящего газа, скорости подачи и давления распыляюшего потока так, чтобы капли при достижении стенки устройства были достаточно сухими. Это может гарантировать, что высушенные капли являются по существу твердыми и представлены в виде мелкого порошка, который не будет прилипать к стенке и который можно легко собрать в циклоне. Полученный порошок подвергают вторичной сушке, чтобы убедиться, что продукт соответствует требованиям качества.
Описание способа получения для производства твердой дисперсии активатора глюкокиназы распылительной сушкой
[00268] Твердые дисперсии получают распылительной сушкой раствора, полученного в приведенных выше примерах 1-8, при этом температура входного воздуха распылительной сушилки составляет 90-150°С, расход входного воздуха 0,3-0,5 м3/мин., расход воздушного потока 15-30 л/мин., а скорость распыления указанных растворов составляет 5-7 мл/мин. Твердые дисперсии 1-8 получают распылительной сушкой.
[00269] Твердую дисперсию получают распылительной сушкой раствора, полученного в приведенном выше примере 9, при этом температура входного воздуха распылительной сушилки составляет 90-150°С, расход входного воздуха составляет 20-30 кг/час., расход воздушного потока составляет 3-30 кг/час., скорость распыления указанных растворов составляет 5-200 мл/мин. Твердую дисперсию 9 получают распылительной сушкой.
[00270] Твердые дисперсии 1-9 получают в соответствии со способом, описанным выше, где
[00271] процент по массе соединения HMS5552 в твердой дисперсии 1 составляет 10%; процент по массе соединения HMS5552 в твердой дисперсии 2 составляет 30%; процент по массе соединения HMS5552 в твердой дисперсии 3 составляет 50%; процент по массе соединения HMS5552 в твердой дисперсии 4 составляет 70%; процент по массе соединения HMS5552 в твердой дисперсии 5 составляет 80%; процент по массе соединения HMS5552 в твердой дисперсии 6 составляет 90%; процент по массе соединения HMS5552 в твердой дисперсии 7 составляет 60%; процент по массе соединения HMS5552 в твердой дисперсии 8 составляет 40%; процент по массе соединения HMS5552 в твердой дисперсии 9 составляет 50%.
II. Получение таблеток активатора глюкокиназы
[00272] Таблетки с покрытием могут быть получены с использованием препарата, описанного под заголовком «Получение таблеток активатора глюкокиназы», или отдельного препарата. Пленочное покрытие способствует, главным образом, увеличению твердости, повышению стойкости к влаге, улучшению эстетичного внешнего вида, облегчению проглатывания и т.п. Способ получения таблетки активатора глюкокиназы с покрытием включает следующие стадии.
[00273] (1) Получение таблеток активатора глюкокиназы, в которых препарат и способ его получения описаны выше.
[00274] (2) Получение раствора покрытия: суспензию покрытия с содержанием твердых веществ 15% мас. готовят при перемешивании до получения однородной смеси.
[00275] (3) Покрытие: ядро таблетки взвешивают в поддоне для покрытия. После достижения температуры слоя покрытия 30-60°С, начинают покрытие. Увеличение массы таблетки при нанечении покрытия составляет от 2% мас. до 4% мас., и распыление раствора покрытия прекращают после достижения желаемой массы. После охлаждения слоя покрытия до 25-30°С таблетки высвобождают.
[00276] В соответствии с этим способом получают представленные ниже таблетки с покрытием указанных доз активатора глюкокиназы.
Пример 10 Препарат в форме таблетки массой 5 мг (из расчета на 1000 таблеток), т.е. количество активного ингредиента составляет 5 мг
|
Пример 11 Препарат в форме таблетки массой 100 мг (из расчета на 1000 таблеток), т.е. количество активного ингредиента составляет 100 мг
|
Пример 12 Препарат в форме таблетки массой 25 мг (из расчета на 1000 таблеток), т.е. количество активного ингредиента составляет 25 мг
|
Пример 13 Препарат в форме таблетки массой 75 мг (из расчета на 1000 таблеток), т.е. количество активного ингредиента составляет 75 мг
|
Пример 14 Препарат в форме таблетки массой 25 мг (из расчета на 1000 таблеток), т.е. количество активного ингредиента составляет 25 мг
|
Пример 15 Препарат в форме таблетки массой 50 мг (из расчета на 1000 таблеток), т.е. количество активного ингредиента составляет 50 мг
|
Пример 16 Препарат таблетки массой 100 мг (из расчета на 1000 таблеток), т.е. количество активного ингредиента составляет 100 мг
|
III. Получение таблеток активатора глюкокиназы c покрытием
[00277] Таблетки с покрытием могут быть получены с использованием препарата, описанного под заголовком «Получение таблеток активатора глюкокиназы», или отдельного препарата. Пленочное покрытие способствует, главным образом, повышению твердости, облегчению стойкости к влаге, улучшению эстетичного внешнего вида, облегчению проглатывания и т.п. Способ получения таблетки активатора глюкокиназы с покрытием включает следующие стадии.
[00278] (1) Получение таблеток активатора глюкокиназы, где препарат и способ его получения описаны выше.
[00279] (2) Получение раствора покрытия: суспензию покрытия с содержанием твердых веществ 15% мас. готовят при перемешивании до получения однородной смеси.
[00280] (3) Покрытие: ядро таблетки взвешивают в поддоне для получения покрытия. После достижения температуры слоя покрытия 30-60°С начинают нанесение покрытия. Увеличение массы таблетки после нанесения покрытия составляет от 2% мас. до 4% мас., и распыление раствора покрытия прекращают после достижения желаемой массы. После охлаждения слоя покрытия до 25-30°С таблетки высвобождают.
[00281] В соответствии с этим способом получают представленные ниже таблетки указанных доз активатора глюкокиназы с покрытием. Препараты с форме таблеток с покрытием представлены ниже.
Пример 17 Препарат в форме таблеток массой 50 мг (из расчета на 1000 таблеток), т.е. количество активного ингредиента составляет 50 мг
|
Пример 18 Препарат в форме таблетки массой 75 мг с покрытием (из расчета на 1000 таблеток), т.е. количество активного ингредиента составляет 75 мг
|
V. Получение капсул активатора глюкокиназы
Способ получения капсул 1:
[00282] (1) Взвешивание и просеивание: компоненты препарата взвешивают и просеивают перед использованием.
[00283] (2) Гранулирование: внутригранулярную микрокристаллическую целлюлозу, твердую дисперсию (твердая дисперсия 9, полученная выше) и гидроксипропилцеллюлозу помещают во влажный гранулятор, предварительно смешивая в соответствии с заданными параметрами, и для влажного гранулирования добавляют взвешенную чистую воду. После загрузки гранулы влажно гранулируют в мельнице, сушат до LOD 2-3% мас., а затем подвергают сухому гранулированию в мельнице.
[00284] (3) Заполнение капсул: капсулы заполняют гранулами. Для использования в настоящем изобретении подходящими являются следующие типы оболочек капсул: желатиновые капсулы животного происхождения, капсулы HPMC растительного происхождения, кишечнорастворимые капсулы, мягкие капсулы и т.п.
Пример 19 Препарат в форме капсулы массой 50 мг (из расчета на 1000 капсул), т.е. количество активного ингредиента составляет 50 мг
|
Способ получения капсул 2:
[00285] (1) Взвешивание и просеивание: компоненты препарата взвешивают и просеивают перед использованием.
[00286] (2) Заполнение капсулы: капсулы заполняют порошковой смесью. Для использования в настоящем изобретении подходящими являются следующие типы оболочек капсул: желатиновые капсулы животного происхождения, капсулы HPMC растительного происхождения, кишечнорастворимые капсулы и т.п.
Пример 20 Препарат в форме капсулы массой 50 мг (из расчета на 1000 капсул), т.е. количество активного ингредиента составляет 50 мг
|
Пример 21 Препарат в форме капсулы массой 25 мг (из расчета на 1000 капсул), т.е. количество активного ингредиента составляет 25 мг
|
V. Cравнительные примеры
[00287] Препараты сравнительного примера 1 и сравнительного примера 2 получают заменой твердой дисперсии 9 в препаратах примера 12 и примера 13 соединением HMS5552 в качестве фармацевтически активного ингредиента, корректировкой количества микрокристаллической целлюлозы в рецептуре при сохранении других компонентов и их соотношения неизменными, а также с использованием описанного выше способа получения таблеток активатора глюкокиназы.
Сравнительный пример 1 Препарат в форме таблетки массой 25 мг (из расчета на 1000 таблеток), т.е. количество активного ингредиента составляет 25 мг
|
Сравнительный пример 2 Препарат в форме таблетки массой 75 мг (из расчета на 1000 таблеток), т.е. количество активного ингредиента составляет 75 мг
|
[00288] Препараты сравнительного примера 3 и сравнительного примера 4 получают заменой твердой дисперсии 9 в препаратах примера 12 и примера 13 соединением HMS5552 в качестве фармацевтически активного ингредиента соединением HMS5552 и Eudragit L100, сохраняя другие компоненты и их соотношение неизменными и используя описанный выше способ получения таблеток активатора глюкокиназы.
Сравнительный пример 3 Препарат в форме таблетки массой 25 мг (из расчета на 1000 таблеток), т.е. количество активного ингредиента составляет 25 мг
|
Сравнительный пример 4 Препарат в форме таблетки массой 75 мг (из расчета на 1000 таблеток), т.е. количество активного ингредиента составляет 75 мг
|
[00289] Таблетки активатора глюкокиназы других доз или концентраций могут быть получены аналогичным образом.
VI. Тест
1. Фармакокинетика препарата активатора глюкокиназы для перорального введения в организме человека
[00290] Используют таблетки, полученные в приведенных выше примерах или аналогичным образом. В тесте исследования действия однократных нарастающих доз (Single Ascending Dose - SAD) концентрация активного ингредиента в плазме быстро возрастает после однократного перорального введения дозы 5 мг, 10 мг, 15 мг, 25 мг, 35 мг и 50 мг активного ингредиента здоровым пациентам со средним временем достижения максимального значения 1,25-2,5 часов, после чего стабильно снижается, и конечный элиминационный период полувыведения составляет примерно 4,5-7,5 часов.
[00291] Используют таблетки, полученные в приведенных выше примерах или способами, аналогичными описанным выше в примерах. В тесте исследования действия многократных нарастающих доз (Multiple Ascending Dose - MAD) концентрации активного ингредиента в плазме быстро возрастают после перорального введения разовой дозы 25 мг, 50 мг, 100 мг, 150 мг и 200 мг активного ингредиента пациентам с сахарным диабетом 2 типа (type 2 diabetes T2DM) со средним временем достижения максимального значения 1,5-2 часа, после чего стабильно снижается, и конечный элиминационный период полувыведения составляет примерно 6,8-8,6 часов, что существенно не отличается от показателей у здоровых субъектов; при пероральном введении 25 мг, 50 мг, 100 мг, 150 мг, 200 мг два раза в день в течение 5,5 дней подряд для достижения устойчивого состояния среднее время достижения максимальной концентрации в плазме составляет 1,5-3 часа, и конечный элиминационный период полувыведения составляет примерно 7,7-10,3 часов. Воздействие на плазму в основном не было накоплением по сравнению с однократным введением пациентам с T2DM (диапазон коэффициента накопления 1-1,8).
[00292] На фигуре 2 представлена концентрация лекарственного средства в плазме в зависимости от времени после однократного перорального введения здоровым субъектам (HV) и пациентам с T2DM (T2DM) таблеток соединения HMS5552, полученных как описано в примере 12, с содержанием активного ингредиента 50 мг, т.е. двух таблеток с содержанием активного ингредиента 25 мг.
2. Абсорбция препарата активатора глюкокиназы для перорального ввещения в кишечном тракте человека, моделируемая в модели PBPK
[00293] Физиологически обоснованную ФК модель (PBPK модель) получают с использование програмного обеспечения Simcyp для имитации степени абсорбции и основного сайта абсорбции соединения HMS5552 в кишечном тракте человека после перорального введения натощак однократной дозы таблетки 50 мг HMS5552 здоровым субъекта.
[00294] На фигуре 3 представлен график, показывающий среднюю скорость растворения и профиль абсорбции препарата активатора глюкокиназы для перорального введения в кишечнике после однократного введения натощак препарата для перорального введения в дозе 50 мг здоровым людям, смоделированную в модели PBPK. Как видно из фигуры 3, препарат активатора глюкокиназы для перорального введения быстро растворяется в кишечнике со скоростью растворения 90% или выше в течение 30 минут; в сравнении с растворением активатор глюкокиназы полностью абсорбируется, но несколько медленнее, достигая плато поглощения примерно через 2-3 часа после введения. Результат согласуется с клинически наблюдаемым временем достижения максимальной концентрации в плазме для активатора глюкокиназы в организме человека, что позволяет предположить, что модель может дать хороший прогноз скорости растворения и абсорбции активатора глюкокиназы в организме человека.
[00295] На фигуре 4 представлено распределение абсорбции активатора глюкокиназы в различных отделах кишечника человека при однократном введении натощак 50 мг здоровым людям, моделируемое в модели PBPK. Из фигуры видно, что после однократного введения таблетки HMS5552 в организм человека основной сайт абсорбции находится в двенадцатиперстной кишке переднего конца кишечника, сегменте I тощей кишки и сегменте II тощей кишки. Общая доля абсорбции в этих трех сайтах равна 0,8, что составляет 87% от общей доли поглощения (0,92).
3. Тест растворения in vitro
[00296] Cкорость растворения таблеток и капсул тестируют соответствии со способом с использованием лопастной мешалки Китайской Фармакопеи (издание 2010 года), который используют в трех различных средах растворения при рН 1,2 и/или pH 4,5 и/или pH 6,8, соответственно, через 5 минут, 10 минут, 20 минут, 30 минут, 45 минут и 60 минут. Каждый раз образец объемом 5 мл отбирают для анализа ВЭЖХ.
[00297] Вышеуказанные таблетки и капсулы 5 доз испытывают на их растворение согласно описанному выше тесту, полученные результаты представлены ниже.
Таблица 1: Скорость растворения таблетки массой 25 мг, полученной в примере 12
|
Таблица 2: Скорость растворения таблетки массой 5 мг, полученной в примере 10
|
Таблица 3: Скорость растворения таблетки массой 50 мг с покрытием, полученной в примере 17
|
Таблица 4: Скорость растворения таблетки массой 75 мг с покрытием, полученной в примере 18
|
Таблица 5: Скорость растворения таблетки массой 100 мг, полученной в примере 11
|
Таблица 6: Скорость растворения капсулы массой 25 мг, полученной в примере 21
|
Таблица 7: Скорость растворения таблетки массой 75 мг, полученной в примере 13
|
Таблица 8: Скорость растворения таблетки массой 25 мг, полученной в примере 14
|
Таблица 9: Скорость растворения таблетки массой 50 мг, полученной в примере 15
|
Таблица 10: Скорость растворения таблетки массой 100 мг, полученной в примере 16
|
Таблица 11: Скорость растворения таблетки массой 25 мг, полученной в сравнительном примере 1
|
Таблица 12: Скорость растворения таблетки массой 75 мг, полученной в сравнительном примере 2
|
Таблица 13: Скорость растворения таблетки массой 25 мг, полученной в сравнительном примере 3
|
Таблица 14: Скорость растворения таблетки массой 75 мг, полученной в сравнительном примере 4
|
Выводы:
[00298] Скорость растворения препаратов для перорального введения, полученных способом получения твердой дисперсии по настоящему изобретению, значительно различается при различных рН; в таблетках, полученных обычными способами, эта характеристика не проявляется. Как показано на фигуре 5, хотя способ получения и композиция таблеток являются одинаковыми или схожими, различные формы соединения HMS5552 приводят к различной скорости растворения активного ингредиента HMS5552 в препарате для перорального введенияе, т.е. чистого порошка HMS5552 (сравнительный пример 2), простой смеси HMS5552+Eudragit L100 (сравнительный пример 4) или формы твердой дисперсии (пример 13).
[00299] Описанное выше различие указывает на то, что растворение таблетки, полученной способом получения твердой дисперсии по настоящему изобретению, является рН-зависмым. То есть скорость растворения в течение 30 мин. не превышает 45% при pH 1,2~4,5, скорость растворения в течение 30 мин. составляет не менее 85% при pH 6,0~7,0 (таблицы 1-10).
[00300] Кроме того, как показано на фигурах 7-9, таблетки, полученные в сравнительном примере 2 и сравнительном примере 4, имеют одинаковую скорость растворения в течение 30 мин. при рН 1,2, рН 4,5 и рН 6,8. В то же время, у таблетки примера 13, полученной в соответствии со способом получения твердой дисперсии по настоящему изобретению, скорость растворения в течение 30 мин. составляет 16,2%, 24,6% и 88,6% при рН 1,2, рН 4,5 и рН 6,8 соответственно.