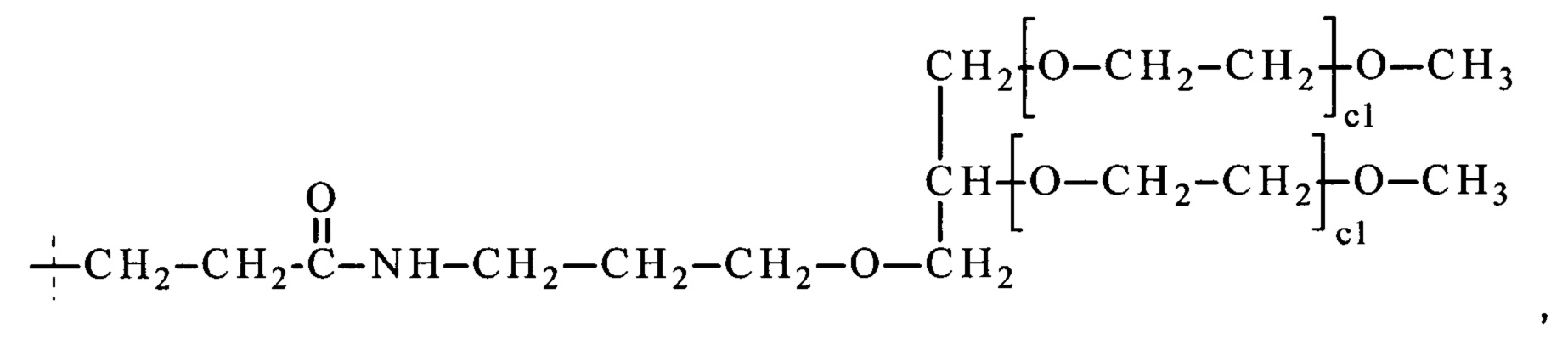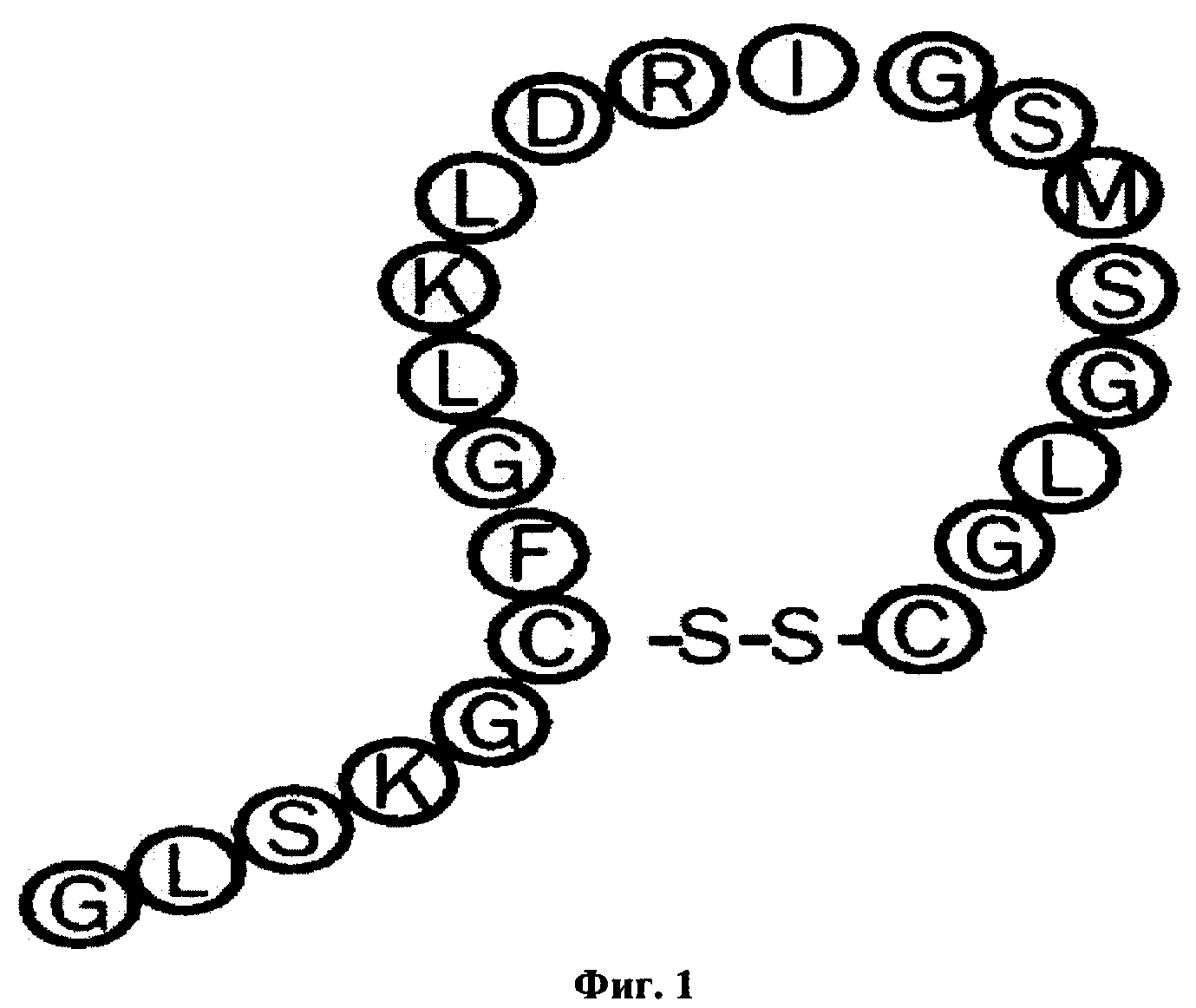Результат интеллектуальной деятельности: CNP ПРОЛЕКАРСТВА
Вид РИД
Изобретение
Настоящее изобретение относится к CNP пролекарствам, их фармацевтически приемлемой соли, фармацевтическим композициям, содержащим такие CNP пролекарства или их фармацевтически приемлемую соль, и их применениям.
Мутации приобретения функций в FGFR3 приводят к ахондроплазии (АСН), гипохондроплазии (ГХГ) и танатофорической дисплазии (TD). Эти состояния все обусловлены повышенной сигнализацией рецептора фактора роста фибробластов 3 (FGFR3), характеризуются непропорциональной ризомелической карликовостью и различаются по степени тяжести, которая варьируется от легкой (НСН) до тяжелой (АСН) и летальной (TD). FGFR3 является ключевым регулятором роста хрящевой кости и передает сигнал через некоторые внутриклеточные пути, включая внутриклеточные пути переносчика сигнала и активатора транскрипции (STAT) и митоген-активированной протеинкиназы (MAPK). Конститутивная активация FGFR3 нарушает пролиферацию и конечную дифференциацию хондроцитов пластин роста и синтез внеклеточного матрикса. Активация FGFR3 связана с увеличением фосфорилирования путей STAT и MAPK. MAPK сигнальный путь регулируется натрийуретическим пептидом С-типа (CNP). Связывание CNP с его рецептором, рецептором натрийуретического пептида В (NPR-B), ингибирует FGFR3 нисходящими сигналами и, таким образом, запускает хрящевой рост и чрезмерный рост скелета, как наблюдается как у мышей, так и у людей, у которых происходит чрезмерная экспрессия CNP. Чрезмерное продуцирование CNP в хряще или непрерывная доставка CNP посредством внутривенного (iv) введения нормализует карликовость ахондроплазической мыши, предполагая, что введение CNP при сверхфизиологических дозах является стратегией для лечения АСН.
Однако, учитывая его короткий период полувысвобождения (через 2 мин после внутривенного (iv) введения), CNP в качестве терапевтического средства является сомнительным в отношении педиатрической популяции, потому что он потребует непрерывного введения. Кроме того, поскольку CNP сильно инактивируется в подкожной основе, требуется внутривенное введение.
Potter (FEBS Journal 278 (2011) 1808-1817) описывает клиренс CNP двумя путями деградации: опосредованной рецептором деградацией и деградацией внеклеточными протеазами. CNP разрушается под действием нейтральной эндопептидазы 24.11 (NEP) и удаляется большим кругом кровообращения посредством очищающего рецептора натрийуретического пептида NPR-C, который связывается с и откладывает CNP в лизосомы, где CNP разрушается.
Способность отдельных органов удалять молекулы из круга кровообращения описывается коэффициентом экстракции, который рассчитывается путем вычитания венозной концентрации из артериальной концентрации и деления этого значения на концентрацию молекулы в артериальной крови. Эта так называемая разница A/V количественно показывает, насколько эффективно орган удаляет или расщепляет рассматриваемую молекулу. У людей градиенты A/V для CNP являются отрицательными для почечной, печеночной и легочной ткани, что соответствует разрушению CNP, происходящему в этих тканях.
Снижение деградации одним или обоими из этих путей клиренса могло бы продлить период полувысвобождения CNP.
Из-за ограниченного размера полости его активного сайта NEP предпочтительно распознает субстраты, меньшие, чем около 3 кДа. В US 8,377,884 В2 описываются варианты CNP, которые необязательно перманентно конъюгированы с ПЭГ полимером с увеличением резистентности к NEP расщеплению. Однако было установлено, что добавление ПЭГ, даже настолько небольшое как 0,6 кДа, к CNP дикого типа снижает активность CNP, и добавление более чем около 2 или 3 кДа ПЭГ к CNP или его вариантам уменьшают функциональную активность CNP зависимым от размера образом. Поэтому присоединение молекул ПЭГ более 2-3 кДа для снижения NEP расщепления сопровождается потерей активности, что может уменьшить терапевтический потенциал таких молекул.
В дополнение к отрицательному влиянию на активность пептида, конъюгирование ПЭГ или другой макромолекулы с CNP также может помешать эффективному распределению на пластинку роста. Farnum et al. (Anat Rec A Discov Mol Cell Evol Biol. 2006 January; 288(1): 91-103) показали, что распределение молекул от системной сосудистой сети до пластины роста зависит от размера и что маленькие молекулы (до 10 кДа) могут распространяться на пластину роста, тогда как молекулярный размер 40 кДа и больше мешает доступу к пластинке роста.
Международная заявка WO 2009/156481 А1 относится к обратимым ПЭГ-конъюгатам BNP, причем указанный термин был определен как включающий всех членов семейства натрийуретических пептидов. Эта заявка сфокусирована только на сердечнососудистых эффектах этого класса пептидов, которые опосредованы натрийуретическим пептидным рецептором A (NPR-A). В WO 2009/156481 А1 не раскрываются специфические свойства CNP в отношении регуляции роста, пролиферации и дифференциации хондроцитов пластины роста хряща, опосредованных активацией рецептора натрийуретического пептида В (NPR-B).
Другой подход к созданию NEP-резистентной молекулы CNP и возможное подкожное введение были описана в The American Journal of Человеческий Genetics 91, 1108-1114. BMN-111 представляет собой модифицированный рекомбинантный натрийуретический пептид С-типа человека (CNP), в котором 17 аминокислот были добавлены с образованием фармакологического аналога CNP из 39 аминокислот.BMN-111 имитирует фармакологическую активность CNP на пластине роста и имеет увеличенный период полувысвобождения в результате резистентности к нейтральной эндопептидазе (NEP), что обеспечивает подкожное (SC) введение один раз в день. Поскольку BMN-111 не является природным пептидом, риск индицирования иммунного ответа увеличивается по сравнению с природным пептидом, и, как описано Martz в "sFGFR for achondroplasia" (SciBx, Biocentury October 2013), иммунный ответ на BMN-111 наблюдался в исследованиях на животных, причем присутствие антител не влияло на фармакологическую активность лекарственного средства. Тем не менее, BMN-111 имеет период полувысвобождения, равный 20 минут, что при ежедневном дозировании связано с кратковременным действием эффективных уровней лекарственного средства.
Для увеличения воздействия эффективных уровней лекарственного средства, доза лекарственного средства, обладающего активностью CNP, может быть увеличена. Поскольку натрийуретические пептиды представляют собой семейство гормонов, которые могут влиять на объем крови и кровяное давление, увеличение дозы может быть связано с сердечнососудистыми побочными эффектами. Исследования BMN-111 на животных и людях показали, что по мере увеличения дозы артериальное кровяное давление падает, и частота сердечных сокращений возрастает. Дозы BMN-111 до 15 мкг/кг были связаны с легкой гипотензией у здоровых добровольцев. Поэтому увеличение дозы лекарственного средства, имеющего активность CNP, для увеличения эффективности лекарственного средства, может быть связано с неприемлемыми сердечнососудистыми побочными эффектами.
Таким образом, существует потребность в более удобном и/или эффективном CNP лечении.
Поэтому задача настоящего изобретения состоит в по меньшей мере частичном преодолении недостатков, описанных выше.
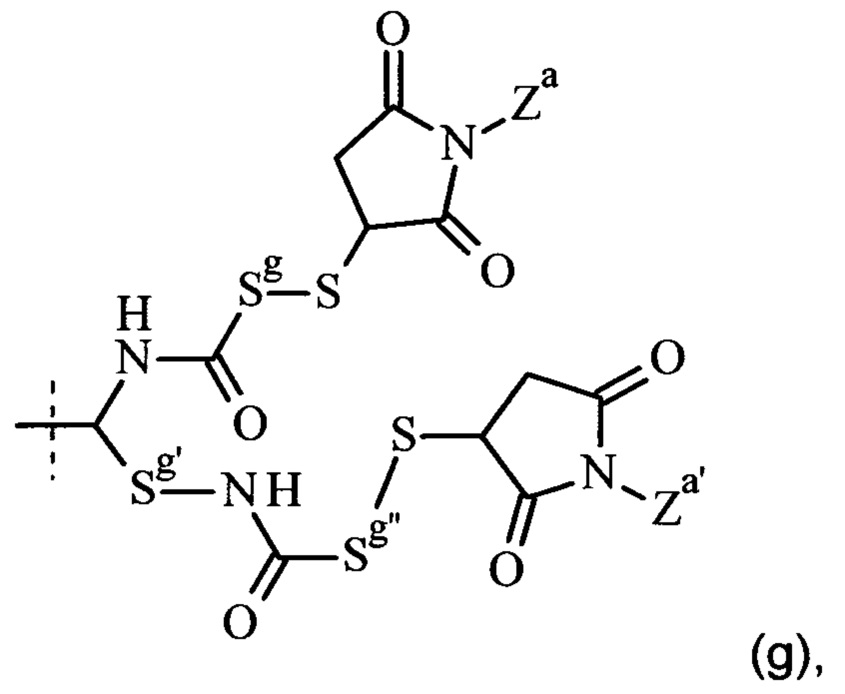
Эта задача решается посредством CNP пролекарства или его фармацевтически приемлемые соли, где пролекарство имеет формулу (Ia) или (Ib)
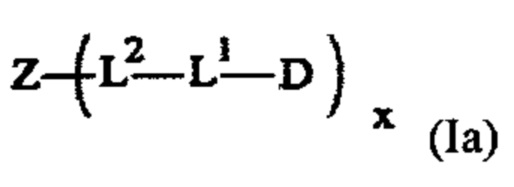
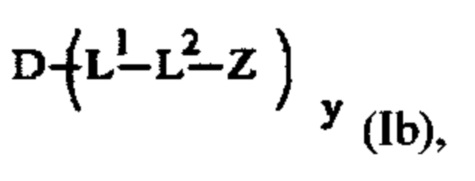
где
-D представляет собой CNP составляющую;
-L1 - представляет собой обратимую линкерную составляющую пролекарства;
-L2- представляет собой одинарную химическую связь или спейсерную составляющую;
-Z представляет собой растворимую в воде составляющую-носитель;
х представляет собой целое число, выбранное из группы, состоящей из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 и 16; и
у представляет собой целое число, выбранное из группы, состоящей из 1,2, 3, 4 и 5.
В другом варианте настоящее изобретение относится к CNP пролекарству или его фармацевтически приемлемые соли, содержащим конъюгат D-L, где
-D представляет собой CNP составляющую; и
-L содержит обратимую линкерную составляющую -L1-;
где -L1 - имеет в качестве заместителя -L2-Z’ и необязательно дополнительно замещена; где
-L2- представляет собой одинарную химическую связь или спейсерную составляющую; и
-Z’ представляет собой нерастворимую в воде составляющую-носитель.
Понятно, что множество составляющих -L2-L1-D соединены с нерастворимым в воде носителем -Z’.
Неожиданно было обнаружено, что CNP пролекарства согласно настоящему и их фармацевтически приемлемые соли обеспечивают увеличенное время циркуляции CNP в кровотоке, что приводит к более удобному и приятному для пациента способу введения, такому как подкожная инъекция один раз в неделю или вплоть до одного раза в месяц. В то же время высвобождается немодифицированный CNP, что обеспечивает эффективное распределение активного агента на пластине роста. Поскольку CNP пролекарства согласно настоящему изобретению имеют низкую остаточную активность, т.е. связывание с NPR-B, риск сердечнососудистых побочных эффектов, таких как, гипотензия, значительно снижается.
Кроме того, неожиданно было обнаружено, что соединения согласно настоящему изобретению достигают более стабильных уровней в крови, чем те, которые наблюдаются после ежедневных болюсных инъекций, что более точно имитирует физиологическое воздействие эндогенным CNP. Эти более стабильные уровни в крови сохраняются для различных режимов дозирования, таких как, например, ежедневное введение; введение каждые два дня, каждые три дня, каждые четыре дня, каждые пять дней, каждые шесть дней; еженедельное введение; введение каждые две недели и введение один раз в месяц.
Кроме того, неожиданно было обнаружено, что непрерывное высвобождение CNP, как например, из системы с контролируемым высвобождением, как например, из пролекарств согласно настоящему изобретению, является более эффективным, чем болюсная инъекция один раз в день.
В контексте настоящего изобретения применяемые термины имеют следующие значения.
Как применяется в настоящей заявке термин "CNP" относится ко всем полипептидам CNP, предпочтительно видов млекопитающих, более предпочтительно человека и видов млекопитающих, более предпочтительно человека и видов мышиные, а также их вариантам, аналогам, ортологам, гомологам и производным и фрагментам, которые характеризуются регуляцией роста, пролиферации и дифференциации хондроцитов пластины роста хряща. Предпочтительно, термин "CNP" относится к CNP полипептидной последовательности SEQ ID NO: 1, а также к ее вариантам, гомологам и производным, проявляющим по существу такую же биологическую активность, т.е. регулирующим рост, пролиферацию и дифференциацию хондроцитов пластины роста хряща. Более предпочтительно, термин "CNP" относится к полипептидной последовательности SEQ ID NO: 1. В равно степени предпочтительно, что термин "CNP" относится к SEQ ID NO: 24, т.е. к CNP составляющей, состоящей из 38 аминокислот, а также к ее вариантам, гомологам и производным, проявляющим по существу такую же биологическую активность, т.е. регулирующим рост, пролиферацию и дифференциацию хондроцитов пластины роста хряща.
SEQ ID NO: 1 имеет следующую последовательность:
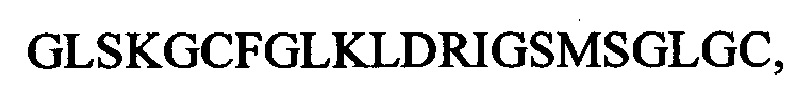
где цистеины в положении 6 и 22 соединены через дисульфидный мостик, как проиллюстрировано на Фиг. 1.
SEQ ID NO: 24 имеет следующую последовательность:
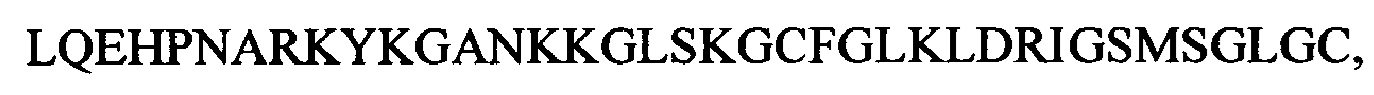
где цистеины в положении 22 и 38 соединены через дисульфидный мостик.
Термин "CNP" также включает все варианты, аналоги, ортологи, гомологи и производные CNP и их фрагменты, как описано в WO 2009/067639 А2 и WO 2010/135541 А2, которые включены в настоящую заявку посредством ссылки.
Соответственно, термин "CNP" также относится предпочтительно к следующим пептидным последовательностям:
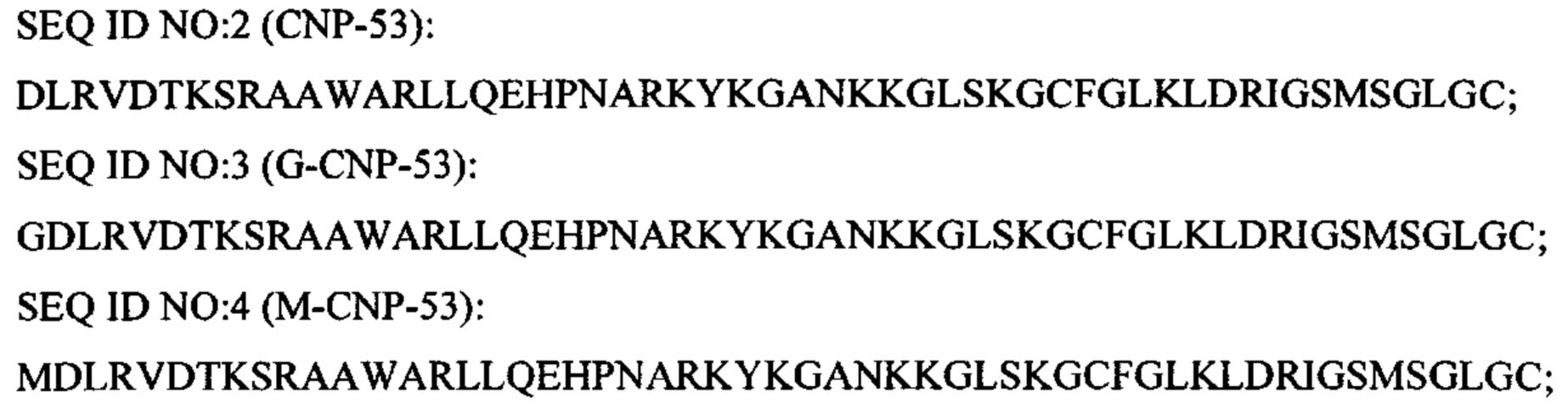






Понятно, что эквиваленты цистеинов в положениях 6 и 22 последовательности SEQ ID NO: 1 также соединены через дисульфидный мостик в SEQ ID NO: 2-92.
Более предпочтительно, термин "CNP" относится к последовательностям SEQ ID:NO 2, 19, 20, 21, 22, 23, 24, 25, 26, 30, 32, 38, 39, 40, 41, 42, 43, 91, 92. Даже более предпочтительно, термин "CNP" относится к последовательностям SEQ ID:NO 23, 24, 25, 26, 38, 39, 91 и 92. В особенно предпочтительном варианте выполнения настоящего изобретения термин "CNP" относится к последовательностям SEQ ID NO: 24.
В особенно предпочтительном варианте выполнения настоящего изобретения термин "CNP" относится к последовательностям SEQ ID NO: 23, 24, 25 и 38, даже более предпочтительно к последовательностям SEQ ID NO: 24 и 25 и наиболее предпочтительно к последовательностям SEQ ID NO: 25. В равно предпочтительном варианте выполнения настоящего изобретения термин "CNP" относится к последовательности SEQ ID NO: 24.
В другом предпочтительном варианте выполнения настоящего изобретения термин "CNP" относится к последовательности SEQ ID NO: 93
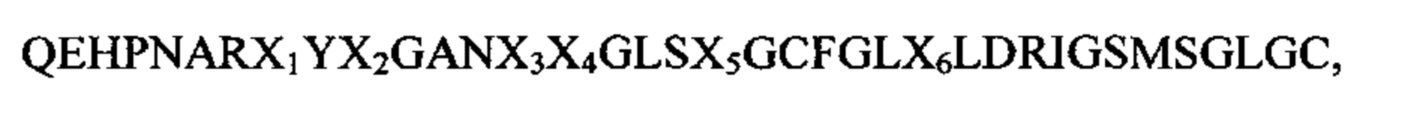
где X1, Х2, Х3, Х4, Х5 и Х6 независимо друг от друга выбирают из группы, состоящей из K, R, Р, S и Q, при условии, что по меньшей мере один из X1, Х2, Х3, Х4, Х5 и Х6 выбирают из группы, состоящей из R, Р, S и Q; предпочтительно X1, Х2, Х3, Х4, Х5 и Х6 выбирают из группы, состоящей из K и R, при условии, что по меньшей мере один из X1, Х2, Х3, Х4, Х5 и Х6 представляет собой R;
даже более предпочтительно к последовательности SEQ ID NO: 94
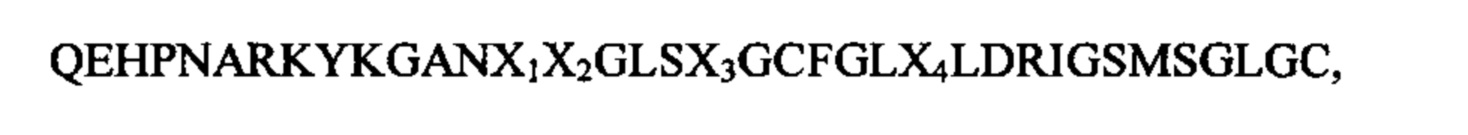
где X1, Х2, Х3 и Х4 независимо друг от друга выбирают из группы, состоящей из K, R, Р, S и Q, при условии, что по меньшей мере один из X1, Х2, Х3 и Х4 выбирают из группы, состоящей из R, Р, S и Q; предпочтительно X1, Х2, Х3 и Х4 выбирают из K и R, при условии, что по меньшей мере один из X1, Х2, Х3 и Х4 представляет собой R;
и наиболее предпочтительно к последовательности SEQ ID NO: 95
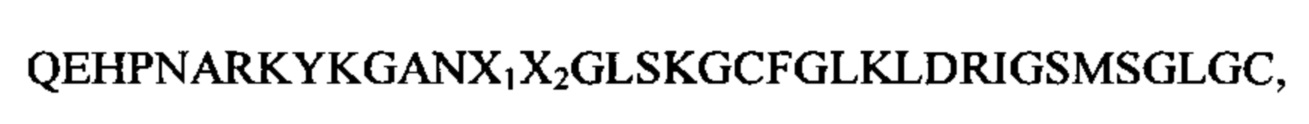
где Х1Х2 выбирают из группы, состоящей из KR, RK, KP, PK, SS, RS, SR, QK, QR, KQ, RQ, RR и QQ.
Понятно, что во всех последовательностях CNP, приведенных в настоящей заявке, эквиваленты цистеинов в положениях 6 и 22 последовательности SEQ ID NO: 1 также соединены через дисульфидный мостик в SEQ ID NO: 93-95.
Понятно, что настоящее изобретение также охватывает варианты CNP, в которых любой один или более, вплоть до всех, остатков, чувствительных к деамидированию или реакции, подобной деамидированию (например, изомеризации), могут быть превращены в другой остаток (остатки) посредством деамидирования или реакции, подобной деамидированию, в любой степени, до 100% превращения на превращенный остаток. В некоторых вариантах выполнения настоящего изобретения изобретение охватывает варианты CNP, в которых:
(1) любой один или более, вплоть до всех, остатков аспарагина (Asn/N) могут быть превращены в аспарагиновую кислоту или аспартат и/или в изоаспарагиновую кислоту или изоаспартат, посредством деамидирования вплоть до около 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или 100% превращения на превращенный остаток; или
(2) любой один или более, вплоть до всех, остатков глютамина (Gln/Q) могут быть превращены в глутаминовую кислоту или глутамат и/или в изоглутаминовую кислоту или изоглутамат, посредством деамидирования вплоть до около 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или 100% превращения на превращенный остаток; или
(3) любой один или более, вплоть до всех, остатков аспарагиновой кислоты или аспартата (Asp/D) могут быть превращены в изоаспарагиновую кислоту или изоаспартат посредством реакции, подобной деамидированию (также называется изомеризацией) вплоть до около 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или 100% превращения на превращенный остаток; или
(4) любой один или более, вплоть до всех, остатков глутаминовой кислоты или глутамата (Glu/E) могут быть превращены в изоглутаминовую кислоту или изоглутамат посредством реакции, подобной деамидированию (также называется изомеризацией) вплоть до около 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или 100% превращения на превращенный остаток;
(5) N-терминальный глютамин (если присутствует) может быть превращен в пироглутамат вплоть до около 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или 100% превращения; или
(5) комбинация вышеуказанных.
Как применяется в настоящей заявке, термин "вариант полипептида CNP " относится к полипептиду из того же самого вида, который отличается от ссылочного полипептида CNP. Предпочтительно, такая ссылочная CNP полипептидная последовательность представляет собой последовательность SEQ ID NO: 1. В равно предпочтительном варианте выполнения настоящего изобретения ссылочная CNP полипептидная последовательность представляет собой последовательность SEQ ID NO: 24. В общем, различия ограничены таким образом, что аминокислотные последовательности ссылочного полипептида и варианта в общем очень подобны и, во многих областях, идентичны. Предпочтительно, варианты полипептида CNP на по меньшей мере 70%, 80%, 90%, или 95% идентичны ссылочному полипептиду CNP, предпочтительно CNP полипептидной последовательности SEQ ID NO: 1. B равно предпочтительном варианте выполнения настоящего изобретения варианты полипептида CNP на по меньшей мере 70%, 80%, 90%, или 95% идентичны ссылочному полипептиду CNP, предпочтительно CNP полипептидной последовательности SEQ ID NO: 24. Под полипептидном, имеющим аминокислотную последовательность на по меньшей мере, например, 95% "идентичную" рассматриваемой аминокислотной последовательности понимается, что аминокислотная последовательность данного полипептида идентична рассматриваемой последовательности, за исключением того, что данная полипептидная последовательность может включать вплоть до пяти аминокислотных изменений на каждые 100 аминокислот рассматриваемой аминокислотной последовательности. Эти замены в ссылочной последовательности могут происходить при амино (N-терминальное) или карбокси концевых (С-терминальное) положениях ссылочной аминокислотной последовательности или в любом мести между этими концевыми положениями, распределяясь либо по отдельности среди остатков в ссылочной последовательности, либо в виде одной или более соприкасающихся групп в ссылочной последовательности. Рассматриваемая последовательность может быть либо полностью аминокислотной последовательностью ссылочной последовательности, либо любым фрагментом, уточненным как описано в настоящей заявке. Предпочтительно, рассматриваемой последовательностью является последовательность SEQ ID NO: 1. В равно предпочтительном варианте выполнения настоящего изобретения рассматриваемой последовательностью является последовательность SEQ ID NO: 24.
Такие варианты полипептида CNP могут быть вариантами, встречающимися в природе, как например встречающиеся в природе аллельные варианты, кодируемые одной из нескольких альтернативных форм CNP, занимающих данный локус на хромосоме или организме, или изоформы, кодируемые встречающимися в природе вариантами сплайсинга, происходящими из одного первичного транскрипта. Альтернативно вариант полипептида CNP может быть вариантом, который, как известно, не встречается в природе, и который может быть получен методиками мутагенеза, известными в данной области техники.
В данной области известно, что одна или более аминокислот могут быть удалены с N-конца или С-конца биоактивного пептида или белка без существенной потери биологической функции. Такие N- и/или С-концевые делеции также охватываются термином вариант полипептида CNP.
Специалистам в данной области техники также известно, что некоторые аминокислотные последовательности полипептидов CNP могут быть изменены без значительного влияния структуры или функции пептида. Такие мутанты включают делеции, вставки, инверсии, повторы и замены, выбранные в соответствии с общими правилами, известными в данной области техники, чтобы иметь небольшой эффект на активность. Например, указания относительно того, как сделать фенотипически молчащие аминокислота замены, приведены в Bowie et al. (1990), Science 247:1306-1310, который полностью включен в настоящее описание посредством ссылки, где авторы указывают, что существуют два основных подхода к изучению толерантности аминокислотной последовательности к изменению.
Термин полипептид CNP также охватывает все полипептиды CNP, кодируемые аналогами, ортологами и/или видовыми гомологами CNP. Как применяется в настоящей заявке, термин "аналог CNP" относится к CNP различных и не связанных между собой организмов, которые выполняют одни и те же функции в каждом организме, но которые не происходят из родовой структуры, которую имели предки организмов. Вместо этого аналогичные CNP возникали отдельно, а затем эволюционировали для выполнения одних и тех же или подобных функций. Другими словами, аналогичные полипептиды CNP представляют собой полипептиды с совершенно различными аминокислотными последовательностями, но которые имеют одну и ту же биологическую активность, а именно регулируют рост, пролиферацию и дифференциацию хондроцитов пластины роста хряща.
Как применяется в настоящей заявке термин "отртолог CNP" относится к CNP двух различных видов, последовательности которых связаны друг с другом через общий гомологичный CNP в родоначальном виде, но которые в ходе эволюции стали отличными друг от друга.
Как применяется в настоящей заявке, термин "гомолог CNP" относится к CNP различных организмов, которые осуществляют одну и ту же функцию в каждом организме и которые происходят из родоначальной структуры, которую в общем имели предки организмов. Другими словами, гомологичные CNP полипептиды представляют собой полипептиды с совершенно подобными аминокислотными последовательностями, которые имеют одну и ту же биологическую активность, а именно регулируют рост, пролиферацию и дифференциацию хондроцитов пластины роста хряща. Предпочтительно, гомологи полипептида CNP могут определяться как полипептиды, имеющие идентичность по меньшей мере 40%, 50%, 60%, 70%, 80%, 90% или 95% со ссылочным полипептидом CNP, предпочтительно полипептидом CNP последовательности SEQ ID NO: 1. В равно предпочтительном варианте выполнения настоящего изобретения ссылочным полипептидом CNP является полипептид CNP последовательности SEQ ID NO: 24.
Таким образом, полипептидом CNP в соответствии с настоящим изобретением может быть, например: (i) полипептид, в котором по меньшей мере один из аминокислотных остатков имеет в качестве заместителя консервативный или неконсервированный аминокислотный остаток, предпочтительно консервативный аминокислотный остаток, и такой замещенный аминокислотный остаток может или не может быть кодирован генетическим кодом; и/или (ii) полипептид, в котором по меньшей мере один из аминокислотных остатков включает группу заместителя; и/или (iii) полипептид, где полипептид CNP слит с другим соединением, как например соединение для увеличения периода полувысвобождения полипептида (например, полиэтилэтенгликоль); и/или (iv) полипептид, в котором дополнительные аминокислоты слиты с полипептидом CNP, как например, пептидная или лидерная или секреторная последовательность области слияния IgG Fc или последовательность, которая используется для очистки вышеуказанной формы полипептида, или последовательность белка-предшественника.
Как применяется в настоящей заявке, термин "фрагмент полипептида CNP" относится к любому пептиду, содержащему последовательный промежуток части аминокислотной последовательности CNP полипептида, предпочтительно полипептида последовательности SEQ ID NO: 1. В равно предпочтительном варианте выполнения настоящего изобретения термин "фрагмент полипептида CNP" относится к любому пептиду, содержащему последовательный промежуток части аминокислотной последовательности полипептида последовательности SEQ ID NO: 24.
Более конкретно, фрагмент полипептида CNP содержит по меньшей мере 6, как например по меньшей мере 8, по меньшей мере 10 или по меньшей мере 17 последовательных аминокислот CNP полипептида, более предпочтительно полипептида последовательности SEQ ID NO: 1. В равной степени предпочтительно, что фрагмент полипептида CNP содержит по меньшей мере 6, как например по меньшей мере 8, по меньшей мере 10 или по меньшей мере 17 последовательных аминокислот CNP полипептида последовательности SEQ ID NO: 24. Фрагмент полипептида CNP может быть дополнительно описан как подвид CNP полипептидов, содержащих по меньшей мере 6 аминокислот, где "по меньшей мере 6" определяется как целое число между 6 и целым числом, обозначающим С-концевую аминокислоту CNP полипептида, предпочтительно полипептида последовательности SEQ ID NO: 1 или - в равной степени предпочтительно - последовательности SEQ ID NO: 24. Также включены виды фрагментов полипептида CNP из по меньшей мере 6 аминокислот в длину, как описано выше, которые дополнительно уточнены с точки зрения их N-концевых и С- концевых положений. Также термином "фрагмент полипептида CNP" охватываются в качестве отдельных видов все фрагменты полипептида CNP из по меньшей мере 6 аминокислот в длину, как описано выше, которые могут быть в частности уточнены их N-концевым и С-концевым положением. То есть, каждая комбинация N-концевого и С-концевого положения, которые составляющая из по меньшей мере 6 последовательных аминокислотных остатков в длину может занимать, на любой данной аминокислотной последовательности CNP полипептида, предпочтительно CNP полипептида последовательности SEQ ID:NO1 или - в равной степени предпочтительно - последовательности SEQ ID NO: 24, включена в настоящее изобретение.
Термин "CNP" также включает поли(аминокислотные) конъюгаты, которые имеют последовательность, как описано выше, но имеющие основную цепь, содержит как амидные, так и неамидные связи, как например сложноэфирные связи, как например депсипептиды. Депсипептиды представляют собой цепи аминокислотных остатков, в которых основная цепь содержит как амидные (пептидные), так и сложноэфирные связи. Соответственно, термин "боковая цепь", как применяется в настоящей заявке, относится либо к составляющей, присоединенной к альфа-атому углерода аминокислотной составляющей, если аминокислотная составляющая соединена через аминные связи, как например в полипептидах, либо к любой составляющей, содержащей атом углерода, присоединенной к основной цепи поли(аминокислотного) конъюгата, как например в случае депсипептидов. Предпочтительно, термин "CNP" относится к полипептидам, имеющим основную цепь, образованную через амидные (пептидные) связи.
Поскольку термин CNP включает вышеописанные варианты, аналоги, ортологи, гомологи, производные и фрагменты CNP, все ссылки на конкретные положения в ссылочной последовательности также включают эквивалентные положения в вариантах, аналогах, ортологах, гомологах, производных и фрагментах CNP составляющей, даже если специально не указано.
Как применяется в настоящей заявке, термин «кольцевой фрагмент» относится к участку последовательных аминокислотных остатков CNP лекарственного средства или составляющей, который расположен между двумя остатками цистеина, которые образуют внутримолекулярный дисульфидный мостик, или между гомологичными аминокислотными остатками, которые связаны через химический линкер. Предпочтительно, кольцевой фрагмент расположен между двумя остатками цистеина, которые образуют внутримолекулярный дисульфидный мостик. Эти два цистеины соответствуют цистеинам в положении 22 и положению 38 в последовательности CNP-38 (SEQ ID NO: 24). Соответственно, аминокислоты от 23 до 37 находятся в указанном кольцевом фрагменте, если CNP лекарственное средство или составляющая имеет последовательность CNP-38.
Независимо от длины CNP составляющей, последовательностью кольцевого фрагмента CNP дикого типа является
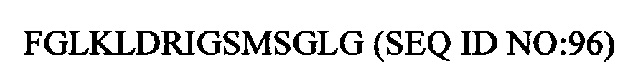 .
.
Как описано выше, термин "CNP" относится к CNP лекарственным средствам или составляющим, имеющим различные количества аминокислот. Специалист в данной области понимает, что в CNP лекарственных средствах или составляющих различной длины меняются положения эквивалентных аминокислот, и квалифицированный специалист не будет испытывать трудности с идентификацией двух цистеинов, образующих дисульфидный мостик, или их двух гомологичных аминокислотных остатков, связанных друг с другом через химический линкер, в более длинных, более коротких и/или модифицированных вариантах CNP.
Так как термин CNP включает вышеописанные варианты, аналоги, ортологи, гомологи, производные и фрагменты CNP, термин "кольцевой фрагмент" также включает соответствующие варианты, аналоги, ортологи, гомологи, производные и фрагменты последовательности SEQ ID NO: 96. Соответственно, все ссылки на конкретное положение в ссылочной последовательности также включают эквивалентные положения в вариантах, аналогах, ортологах, гомолагах, производных и фрагментах CNP составляющей, даже если специально не указано.
Как применяется в настоящей заявке термин "фармацевтическая композиция" относится к композиции, содержащей один или более активных ингредиентов, например лекарственное средство или пролекарство, в настоящей заявке в частности CNP пролекарства согласно настоящему изобретению и необязательно один или более эксципиентов, а также любой продукт, который, прямо или косвенно, является результатом комбинации, комплексообразования или агрегация любых двух или более ингредиентов композиции, или диссоциации одного или более ингредиентов, или других типов реакций или взаимодействий одного или более ингредиентов. Соответственно, фармацевтическая композиция согласно настоящему изобретению охватывает любую композицию, полученную путем смешивания одного или более CNP пролекарств согласно настоящему изобретению и необязательно фармацевтически приемлемого эксципиента.
Как применяется в настоящей заявке термин "жидкая композиция" относится к смеси, содержащей растворимое в воде CNP пролекарство и один или более растворителей, как например вода.
Термин "композиция в виде суспензии" относится к смеси, содержащей нерастворимое в воде CNP пролекарство, где например носитель Z’ представляет собой гидрогель, и один или более растворителей, как например вода. Из-за нерастворимого в воде полимера, полимерное пролекарство не может быть растворено, и пролекарство находится в форме частиц.
Как применяется в настоящей заявке, термин "сухая композиция" означает, что фармацевтическая композиция обеспечивается в сухой форме. Подходящими способами сушки является распылительная сушка и лиофилизация, т.е. сушка замораживанием. Такая сухая композиция пролекарства имеет остаточное содержание воды, равное максимум 10%, предпочтительно менее 5% и более предпочтительно менее 2%, как определено по методу Карла Фишера. Предпочтительно, фармацевтическая композиция согласно настоящему изобретению высушивается посредством лиофилизации.
Термин "лекарственное средство", как применяется в настоящей заявке, относится к веществу, применяемому для лечения, облегчения, профилактики или диагностике заболевания или, в противном случае, для улучшения физического или умственного здоровья. Если лекарственное средство конъюгировано с другой составляющей, составляющая полученного продукта, которая происходит из лекарственного средства, обозначается как "биологически активная составляющая".
Как применяется в настоящей заявке термин "пролекарство" относится к биологически активной составляющей, обратимо и ковалентно соединенной со специализированной защитной группой через обратимую линкерную составляющую пролекарства, которая представляет собой линкерную составляющую, содержащую обратимую связь с биологически активной составляющей, и где специализированная защитная группа изменяет или уменьшает нежелательные свойства в родоначальной молекуле. Это также включает усиления желательных свойств лекарственного средства и подавление нежелательных свойств. Специализированная нетоксичная защитная группа обозначается как "носитель". Пролекарство высвобождает обратимо и ковалентно связанную биологически активную составляющую в форме соответствующего ей лекарственного средства. Другими словами, пролекарство представляет собой конъюгат, содержащий биологически активную составляющую, которая обратимо и ковалентно конъюгирована с составляющей-носителем через обратимую линкерную составляющую пролекарства, где ковалентное или обратимое конъюгирование носителя с обратимой линкерной составляющей пролекарства является либо непосредственным, либо через спейсер. Такой конъюгат высвобождает прежде конъюгированную биологически активную составляющую в форме свободного лекарственного средства.
Термины "биодеградируемая связь" или "обратимая связь" означает связь, которая является гидролитически разрушаемой, т.е. расщепляемой, в отсутствии ферментов при физиологических условиях (водный буфер при рН 7.4, 37°С) с периодом полувысвобождения в интервале от одного часа до шести месяцев, предпочтительно от одного часа до четырех месяцев, даже более предпочтительно от одного часа до трех месяцев, даже более предпочтительно от одного часа до двух месяцев, даже более предпочтительно от одного часа до одного месяца. Соответственно, стабильная связь представляет собой связь, имеющую период полувысвобождения при физиологических условиях (водный буфер при рН 7.4, 37°С), равный более чем шести месяцам.
Соответственно, "обратимая линкерная составляющая пролекарства" представляет собой составляющую, которая ковалентно конъюгирована с биологически активной составляющей, как например CNP, через обратимую связь и также ковалентно конъюгирована с составляющей-носителем, как например -Z или Z', где ковалентное конъюгирование с указанной составляющей-носителем является либо непосредственным, либо через спейсерную составляющую, как например -L2-. Предпочтительно связью между -Z или Z' и L2- является стабильная связь.
Как применяется в настоящей заявке, термин "бесследный линкер пролекарства" означает обратимый линкер пролекарства, который при расщеплении высвобождает лекарственное средство в его свободной форме. Как применяется в настоящей заявке, термин "свободная форма" лекарственного средства означает лекарственное средство в его немодифицированной, фармакологически активной форме.
Как применяется в настоящей заявке, термин "эксципиент" относится к разбавителю, вспомогательному средству или носителю, совместно с которым вводится терапевтическое средство, как например лекарственное средство или пролекарство. Такой фармацевтический эксципиент может представлять собой стерильную жидкость, такую как вода и масла, включая жидкости нефтяного, животного, растительного или синтетического происхождения, включая, но без ограничения к этому, арахисовое масло, соевое масло, минеральное масло, сезамовое масло и тому подобное. Вода является предпочтительным эксципиентом, когда фармацевтическая композиция вводится перорально. Соляной раствор и водный раствор декстрозы являются предпочтительными наполнителями, когда фармацевтическая композиция вводится внутривенно. Соляные растворы и водные растворы декстрозы и глицерина предпочтительно применяются в качестве жидких эксципиентов для инъецируемых растворов. Подходящие фармацевтические эксципиенты включают крахмал, глюкозу, лактозу, сахарозу, маннит, трегалозу, желатин, солод, рис, муку, мел, силикагель, стеарат натрия, глицерин моностеарат, тальк, хлорид натрия, сухое молоко, глицерин, пропиленгликоль, воду, этанол и тому подобное. Композиция при желании может содержать также небольшие количества увлажняющих или эмульгирующих средств, рН-буферных средств, таких как, например, ацетат, сукцинат, трис, карбонат, фосфат, HEPES (4-(2-гидроксиэтил)-1-пиперазинэтансульфокислота, MES (2-(N-морфолин)этансульфокислота) или может содержать детергенты, такие как Tween, полоксамеры, полоксамины, CHAPS, Igepal, или аминокислоты, такие как, например, глицин, лизин или гистидин. Такие фармацевтические композиции могут иметь форму растворов, суспензий, эмульсий, таблеток, пилюль, капсул, порошков, препаратов с замедленным высвобождением и тому подобное. Фармацевтическая композиция может иметь вид суппозитория, с традиционными связующими средствами и эксципиентами, такими как триглицериды. Препарат для перорального введения может содержать стандартные эксципиенты, такие как фармацевтические марки маннита, лактозы, крахмала, стеарата магния, сахарина натрия, целлюлозы, карбоната магния и т.д. Такие композиции содержат терапевтически эффективное количество лекарственного средства или биологически активной составляющей, вместе с подходящим количеством эксципиента, так чтобы получилась форма, подходящая для введения пациенту. Композиция должна соответствовать способу введения.
Как применяется в настоящей заявке, термин "реагент" означает химическое соединение, которое содержит по меньшей мере одну функциональную группу для реакции с функциональной группой другого химического соединения или лекарственного средства. Понятно, что лекарственное средство, содержащее функциональную группу (как например первичный или вторичный амин или гидроксильная функциональная группа) также представляет собой реагент.
Как применяется в настоящей заявке, термин "составляющая" означает часть молекулы, в которой отсутствует один или более атомов по сравнению с соответствующим реагентов. Если, например, реагент формулы "Н-Х-Н" реагирует с другим реагентом и становится частью продукта реакции, соответствующая составляющая продукта реакции имеет структуру "Н-X-" или "-Х-", где каждый "-" обозначает присоединение к другой составляющей. Соответственно, биологически активная составляющая высвобождается из пролекарства в качестве лекарственного средства.
Понятно, что если обеспечивается последовательность или химическая структура группы атомов, где группа атомов присоединяется к двум составляющим или прерывает составляющую, указанная последовательность или структура может быть присоединена к двум составляющим в любой ориентации, если иного не указано. Например, составляющая "-C(O)N(R12)-" может быть присоединена к двум составляющим или прерывать составляющую либо как "-C(O)N(R12)-", либо как "-N(R12)C(O)-". Подобным образом, составляющая
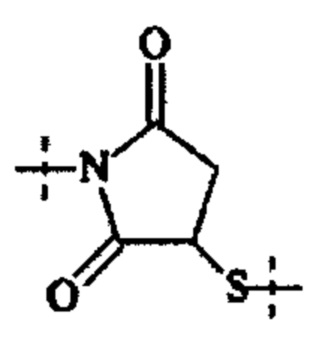
может быть присоединена к двум составляющим или может прерывать составляющую либо как 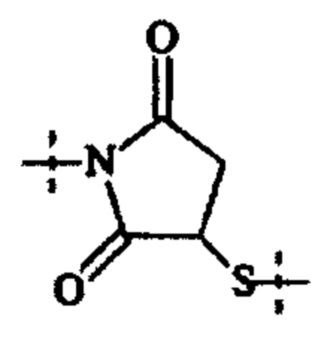 , либо как
, либо как 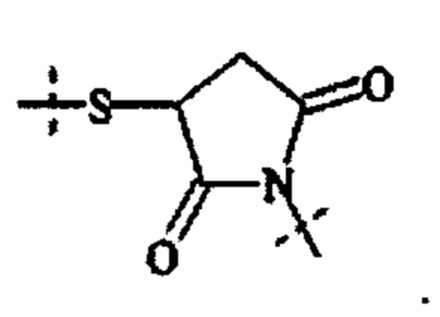
Как применяется в настоящей заявке, термин "функциональная группа" означает группу атомов, которая может реагировать с другими группами атомов. Функциональные группы включают, но без ограничения к этому, следующие группы: карбоновая кислота (-(С=O)ОН), первичный и вторичный амин (-NH2, -NH-), малеимид, тиол (-SH), сульфоновая кислота (-(O=S=O)OH), карбонат, карбамат (-O(C=O)N<), гидроксил (-ОН), альдегид (-(С=O)Н), кетон (-(С=О)-), гидразин (>N-N<), изоцианат, изотиоцианат, фосфорная кислота (-O(Р=O)ОНОН), фосфоновая кислота (-O(Р=O)ОНН), галоацетил, алкилгалогенид, акрилоил, арилфторид, гидроксиламин, дисульфид, сульфонамиды, серная кислота, винилсульфон, винилкетон, диазоалкан, оксиран и азиридин.
В случае, если пролекарства согласно настоящему изобретению содержат одну или более кислотных или основных групп, настоящее изобретение включает также их соответствующие фармацевтически или токсикологически приемлемые соли, в частности их фармацевтически применимые соли. Таким образом, пролекарства согласно настоящему изобретению, содержащие кислотные группы, могут применяться по настоящему изобретению, например, в виде солей щелочных металлов, солей щелочноземельных металлов или аммониевых солей. Более конкретные примеры таких солей включают соли натрия, соли калия, соли кальция, соли магния или соли аммония или с органическими аминами, такими как, например, этиламин, этаноламин, триэтаноламин или аминокислоты. Пролекарства согласно настоящему изобретению, содержащие одну или более основных групп, т.е. групп, которые могут быть протонированы, могут присутствовать и использоваться согласно настоящему изобретению в форме их аддитивных солей с неорганическими или органическими кислотами. Примеры подходящих кислот включают хлорид водорода, бромид водорода, фосфорную кислоту, серную кислоту, азотную кислоту, метансульфокислоту, п-толуолсульфокислоту, нафталинсульфокислоту, щавелевую кислоту, уксусную кислоту, винную кислоту, молочную кислоту, салициловую кислоту, бензойную кислоту, муравьиную кислоту, пропионовую кислоту, пивалоиловую кислоту, диэтилуксусную кислоту, малоновую кислоту, янтарную кислоту, пимелиновую кислоту, фумаровую кислоту, малеиновую кислоту, яблочную кислоту, сульфаминовую кислоту, фенилпропионовую кислоту, глюконовую кислоту, аскорбиновую кислоту, изоникотиновую кислоту, лимонную кислоту, адипиновую кислоту и другие кислоты, известные квалифицированным специалистам в данной области. Специалистам в данной области техники известно превращение основной группы в катион, такие как алкилирование аминной группы с получением положительно заряженной аммониевой группы и соответствующего противоиона соли. Если пролекарства согласно настоящему изобретению одновременно содержат кислотные и основные группы, настоящее изобретение также включает, в дополнение к упомянутым солевым формам, внутренние соли или бетаины (цвиттерионы). Соответствующие соли могут быть получены обычными методами, известными квалифицированным специалистам в данной области, например путем контакта этих пролекарств с органической или неорганической кислотой или основанием в растворителе или диспергирующем средстве, или путем анионного обмена или катионного обмена с другими солями. Настоящее изобретение также включает все соли пролекарств согласно настоящему изобретению, которые, вследствие низкой физиологической совместимости не пригодны непосредственно для применения в фармацевтических продуктах, но которые могут использоваться, например, как промежуточные соединения для химических реакций или для получения фармацевтически приемлемых солей.
Термин "фармацевтически приемлемый" означает вещество, которое не наносит вред при введении пациенту и предпочтительно одобрено надзорным органом, таким как ЕМЕА (Европа) и/или FDA (США) и/или любым другим национальным надзорным органом для применения в отношении животных, предпочтительно человека.
Как применяется в настоящей заявке термин "около" в комбинации с числовым значением применяется для указания на диапазон в интервале и включая числовое значение плюс и минус не более 10% от указанного числового значения, более предпочтительно не более 8% от указанного значения, даже более предпочтительно не более 5% от указанного значения и наиболее предпочтительно не более 2% от указанного значения. Например, фраза "около 200" применяется для обозначения диапазона в интервале и включая 200 +/- 10%, т.е. в интервале и включая 180-220; предпочтительно 200 +/- 8%, т.е. в интервале и включая 184-216; даже более предпочтительно в интервале и включая 200 +/-5%, т.е. в интервале и включая 190-210; и наиболее предпочтительно 200 +/- 2%, т.е. в интервале и включая 196-204. Понятно, что процент, приведенный как "около 20%" не означает "20% +/- 10%", т.е. в интервале и включая 10-30%, но "около 20%" означает в интервале и включая 18-22%, т.е. плюс и минус 10% от числового значения, которое равно 20.
Как применяется в настоящей заявке, термин «полимер» означает молекулу, содержащую повторяющиеся структурные единицы, т.е. мономеры, связанные химическими связями линейным, кольцевым, разветвленным, сшитым или дендримерным образом или их комбинацией, которая может быть синтетического или биологического происхождения или комбинацией обоих. Понятно, что полимер может также содержать одну или более других химических групп и/или составляющей/ составляющих, таких как, например, одна или более функциональные группы. Предпочтительно, растворимый полимер имеет молекулярную массу, равную по меньшей мере 0.5 кДа, например, молекулярную массу, равную по меньшей мере 1 кДа, молекулярную массу, равную по меньшей мере 2 кДа, молекулярную массу, равную по меньшей мере 3 кДа, или молекулярную массу, равную по меньшей мере 5 кДа. Если полимер является растворимым, он предпочтительно имеет молекулярную массу, равную самое большее 1000 кДа, как например самое большее 750 кДа, как например самое большее 500 кДа, как например самое большее 300 кДа, как например самое большее 200 кДа, как например самое большее 100 кДа. Понятно, что для нерастворимых полимеров, как например гидрогели, нет значимых диапазонов молекулярной массы.
Как применяется в настоящей заявке, термин "полимерный" означает реагент или составляющую, содержащую один или более полимеров или полимерную составляющую/составляющие. Полимерный реагент или составляющая может необязательно также содержать одну или более других составляющих, которые предпочтительно выбирают из группы, состоящей из:
• C1-50 алкила, C2-50 алкенила, С2-50 алкинила, С3-10 циклоалкила, 3-10-членного гетероциклила, 8-11-членного гетеробициклила, фенила, нафтила, инденила, инданила и тетралинила; и
• связей, выбранных из группы, содержащей
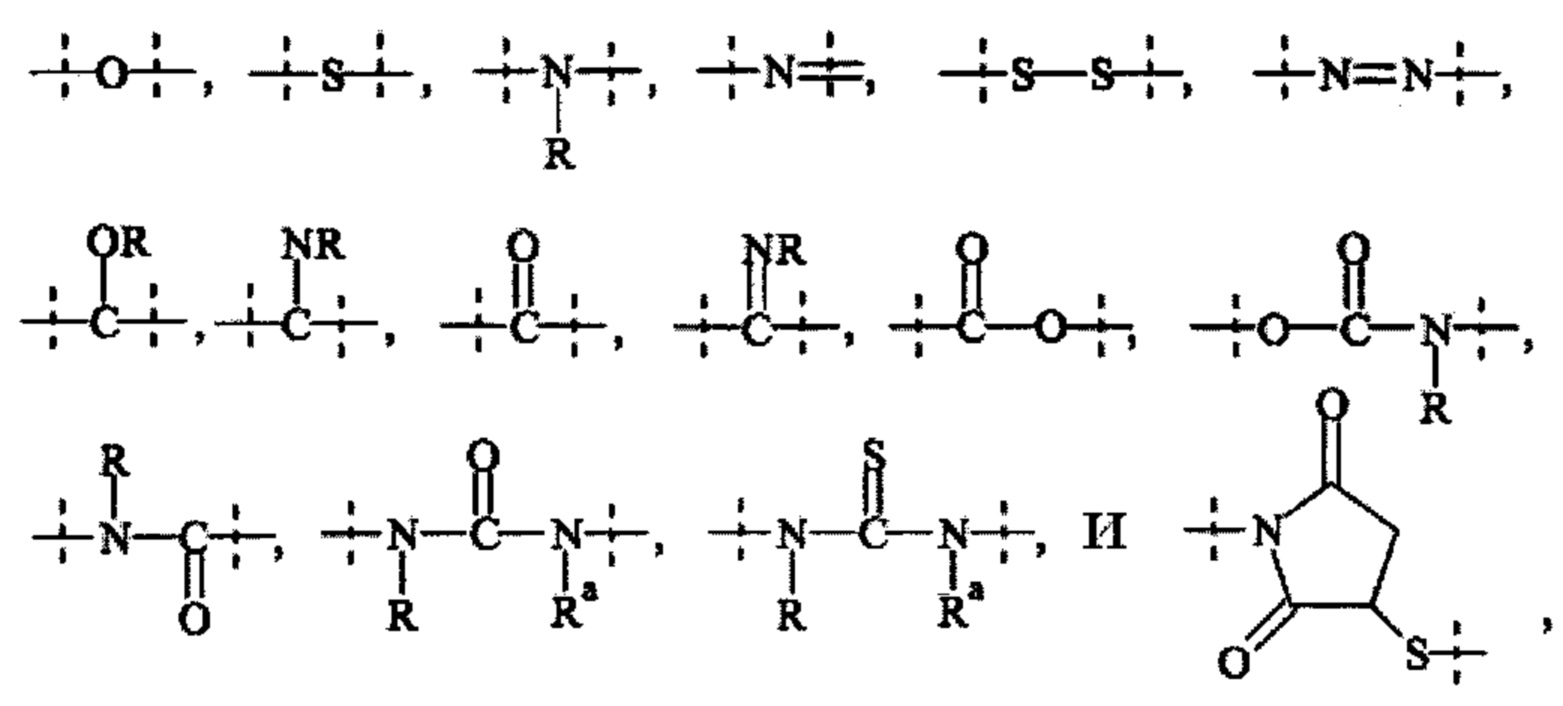
где
пунктирные линии обозначают присоединение к оставшейся части составляющей или реагента, и
-R и Ra независимо друг от друга выбирают из группы, состоящей из -Н, метила, этила, пропила, бутила, пентила и гексила.
Специалист в данной области понимает, что продукты полимеризации, полученные из реакции полимеризации, не все имеют одинаковую молекулярную массу, а скорее имеют молекулярно-массовое распределение. Следовательно, диапазоны молекулярных масс, молекулярные массы, диапазоны количества мономеров в полимере и количества мономеров в полимере, как применяется в настоящей заявке, относятся к среднечисловой молекулярной массе и среднему числу мономеров, т.е. к среднему арифметическому молекулярной массы полимера или полимерного фрагмента и среднему арифметическому числа мономеров полимера или полимерного фрагмента.
Соответственно, в полимерной составляющей, содержащей "х" мономерных единиц, любое целое число, приведенное для "х", поэтому соответствует арифметическому среднему числу мономеров. Любой диапазон целых чисел, приведенный для "х", обеспечивает диапазон целых чисел, в котором лежит арифметическое среднее число мономеров. Целое число для "х", приведенное как "около х", означает, что арифметические средние числа мономеров лежат в диапазоне целых чисел х +/- 10%, предпочтительно х +/- 8%, более предпочтительно х +/- 5% и наиболее предпочтительно х +/- 2%.
Как применяется в настоящей заявке, термин "среднечисловая молекулярная масса" означает обычное среднее арифметическое молекулярных масс отдельных полимеров.
Как применяется в настоящей заявке термин "растворимый в воде" со ссылкой на носитель означает, что когда такой носитель является частью CNP пролекарства согласно настоящему изобретению по меньшей мере 1 г CNP пролекарства, содержащего такой растворимый в воде носитель, может быть растворено в одном литре воды при 20°С с образованием гомогенного раствора. Соответственно, термин "не растворимый в воде" со ссылкой на носитель означает, что когда такой носитель является частью CNP пролекарства согласно настоящему изобретению менее 1 г CNP пролекарства, содержащего такой растворимый в воде носитель, может быть растворено в одном литре воды при 20°С с образованием гомогенного раствора.
Как применяется в настоящей заявке, термин "гидрогель" означает гидрофильную или амфифильную полимерную сеть, состоящую из гомополимеров или сополимеров, которая является не растворимой из-за присутствия ковалентных химических поперечных связей.
Как применяется в настоящей заявке термин «термогелевое» означает соединение, которое представляет собой жидкость или раствор с низкой вязкостью, имеющий вязкость менее 500 сПз при 25°С при скорости сдвига около 0,1/с при низкой температуре, причем низкая температура находится в интервале от около 0°С до около 10°С, но которое представляет собой соединение с более высокой вязкостью менее 10000 сПз при 25°С со скоростью сдвига около 0,1/с при более высокой температуре, причем более высокая температура находится в интервале от около 30°С до около 40°С, например, при температуре около 37°С.
Как применяется в настоящей заявке, термин "на основе ПЭГ" в отношении составляющей или реагента означает, что указанная составляющая или реагент содержит ПЭГ. Предпочтительно, составляющая или реагент на основе ПЭГ содержит по меньшей мере 10% (мас./мас.) ПЭГ, как например по меньшей мере 20% (мас./мас.) ПЭГ, как например по меньшей мере 30% (мас./мас.) ПЭГ, как например по меньшей мере 40% (мас./мас.) ПЭГ, как например по меньшей мере 50% (мас./мас.), как например по меньшей мере 60 (мас./мас.) ПЭГ, как например по меньшей мере 70% (мас./мас.) ПЭГ, как например по меньшей мере 80% (мас./мас.) ПЭГ, как например по меньшей мере 90% (мас./мас.) ПЭГ, как например по меньшей мере 95%. Оставшиеся массовые проценты составляющей или реагента на основе ПЭГ составляют другие составляющие, предпочтительно выбранные из следующих составляющих и связей:
• C1-50 алкил, С2-50 алкенил, С2-50 алкинил, С3-10 циклоалкил, 3-10-членный гетероциклил, 8-11-членный гетеробициклил, фенил, нафтил, инденил, инданил и тетралинил; и
• связей, выбранных из группы, содержащей
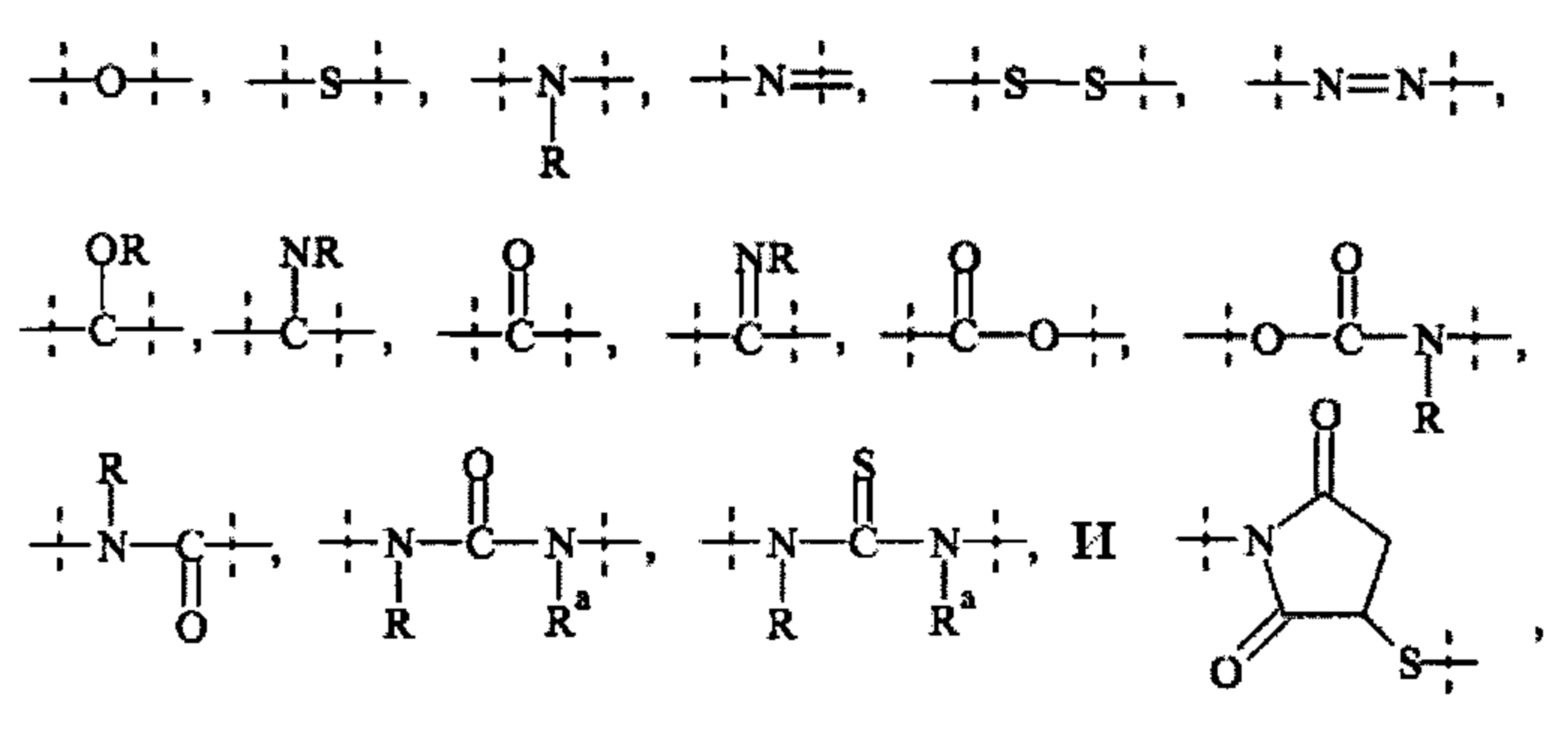
где
пунктирные линии обозначают присоединение к оставшейся части составляющей или реагента, и
-R и Ra независимо друг от друга выбирают из группы, состоящей из -Н, метила, этила, пропила, бутила, пентила и гексила.
Как применяется в настоящей заявке, термин "на основе ПЭГ, содержащий по меньшей мере Х% ПЭГ" в отношении составляющей или реагента означает, что указанная составляющая или реагент содержит по меньшей мере Х% (мас./мас.) единиц этиленгликоля (-СН2СН2О-), где единицы этиленгликоля могут быть расположены блочным, чередующимся образом или могут быть расположены случайным образом в составляющей или реагента, и предпочтительно все единицы этиленгликоля указанной составляющей или реагента присутствуют в одном блоке; оставшиеся массовые проценты составляющей или реагента на основе ПЭГ составляют другие составляющие, предпочтительно выбранные из следующих составляющих и связей:
• С1-50 алкил, С2-50 алкенил, С2-50 алкинил, С3-10 циклоалкил, 3-10-членный гетероциклил, 8-11-членный гетеробициклил, фенил, нафтил, инденил, инданил и тетралинил; и
• связей, выбранных из группы, содержащей
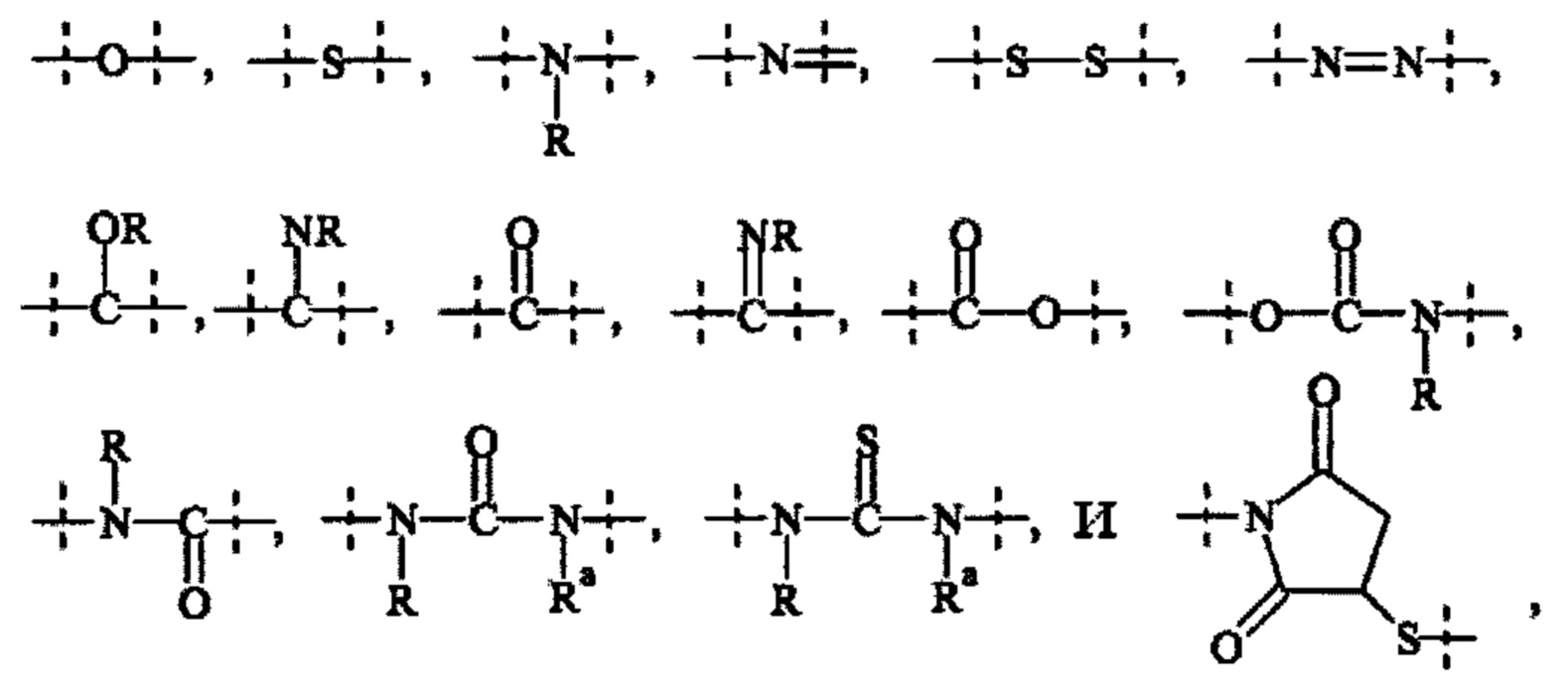
где
пунктирные линии обозначают присоединение к оставшейся части составляющей или реагента, и
-R и Ra независимо друг от друга выбирают из группы, состоящей из -Н, метила, этила, пропила, бутила, пентила и гексила.
Термин "на основе гиалуроновой кислоты, содержащая по меньшей мере Х% гиалуроновая кислота" применяется соответствующим образом.
Термин "замещенный", как применяется в настоящей заявке, означает, что один или более атомов водорода молекулы или составляющей замещены другим атомом или группой атомов, которые обозначаются как "заместитель".
Предпочтительно, одни или более дополнительные необязательные заместители независимо друг от друга выбирают из группы, состоящей из галогена, -CN, -COORx1, -ORx1, -C(O)Rx1, -C(O)N(Rx1Rx1a), -S(O)2N(Rx1Rx1a), -S(O)N(Rx1Rx1a), -S(O)2Rx1, -S(O)Rx1, -N(Rx1)S(O)2N(Rx1aRx1b), -SRx1, -N(Rx1Rx1a), -NO2, -OC(O)Rx1, -N(Rx1)C(O)Rx1a, -N(Rx1)S(O)2Rx1a, -N(Rx1)S(O)Rx1a, -N(Rx1)C(O)ORx1a, -N(Rx1)C(O)N(Rx1aRx1b), -OC(O)N(Rx1Rx1a), -T0, C1-50 алкила, C2-50 алкенила и C2-50 алкинила; где -T0, С1-50 алкил, C2-50 алкенил, и C2-50 алкинил необязательно замещены одним или более заместителями -Rx2, которые являются одинаковыми или различными, и где C1-50 алкил, С2-50 алкенил и С2-50 алкинил необязательно прерваны одной или более группами, выбранными из группы, состоящей из -Т0-, -С(O)O-, -О-, -С(О)-, -C(O)NCRx3)-, -S(O)2N(Rx3)-, -S(O)N(Rx3)-, -S(O)2-, -S(O)-, -N(Rx3)S(O)2N(Rx3a)-, -S-, -N(Rx3)-, -OC(ORx3)(Rx3a)-, -N(Rx3)C(O)N(Rx3a)- и -OC(O)N(Rx3)-;
-Rx1, -Rx1a, -Rx1b независимо друг от друга выбирают из группы, состоящей из -Н, -Т0, С1-50 алкила, С2-50 алкенила и С2-50 алкинила; где -Т0, С1-50 алкил, С2-50 алкенил, и С2-50 алкинил необязательно замещены одним или более заместителями -Rx2, которые являются одинаковыми или различными, и где С1-50 алкил, С2-50 алкенил и С2-50 алкинил необязательно прерваны одной или более группами, выбранными из группы, состоящей из -Т0-, -С(O)O-, -О-, -С(О)-, -C(O)N(Rx3)-, -S(O)2N(Rx3)-, -S(O)N(Rx3)-; -S(O)2-, -S(O)-, -N(Rx3)S(O)2N(Rx3a)-, -S-, -N(Rx3)-, -OC(ORx3)(Rx3a)-, -N(Rx3)C(O)N(Rx3a)- и -OC(O)N(Rx3)-;
каждый T0 независимо выбирают из группы, состоящей из фенила, нафтила, инденила, инданила, тетралинила, С3-10 циклоалкила, 3-10-членного гетероциклила и 8-11-членного гетеробициклила; где каждый Т0 независимо необязательно замещен одним или более заместителями -Rx2, которые являются одинаковыми или различными;
каждый -Rx2 независимо выбирают из группы, состоящей из галогена, -CN, оксо (=O), -COORx4, -ORx4, -C(O)Rx4, -C(O)N(Rx4Rx4a), -S(O)2N(Rx4Rx4a), -S(O)N(Rx4Rx4a), -S(O)2Rx4, -S(O)Rx4, -N(Rx4)S(O)2N(Rx4aRx4b), -SRx4, -N(Rx4Rx4a), -NO2, -OC(O)Rx4, -N(Rx4)C(O)Rx4a, -N(Rx4)S(O)2Rx4a, -N(Rx4)S(O)Rx4a, -N(Rx4)C(O)ORx4a, -N(Rx4)C(O)N(Rx4aRx4b), -OC(O)N(Rx4Rx4a) и C1-6 алкила; где С1-6 алкил необязательно замещен одним или более заместителями галоген, которые являются одинаковыми или различными;
каждый -Rx3, -Rx3a, -Rx4, -Rx4a, -Rx4b независимо выбирают из группы, состоящей из -Н и C1-6 алкила; где C1-6 алкил необязательно замещен одним или более заместителями галоген, которые являются одинаковыми или различными.
Более предпочтительно, одни или более дополнительные необязательные заместители независимо друг от друга выбирают из группы, состоящей из галогена, -CN, -COORx1, -ORx1, -C(O)Rx1, -C(O)N(Rx1Rx1a), -S(O)2N(Rx1Rx1a), -S(O)N(Rx1Rx1a), -S(O)2Rx1, -S(O)Rx1, -N(Rx1)S(O)2N(Rx1aRx1b), -SRx1, -N(Rx1Rx1a), -NO2, -OC(O)Rx1, -N(Rx1)C(O)Rx1a, -N(Rx1)S(O)2Rx1a, -N(Rx1)S(O)Rx1a, -N(Rx1)C(O)ORx1a, -N(Rx1)C(O)N(Rx1aRx1b), -OC(O)N(Rx1Rx1a), -T0, С1-10 алкила, С2-10 алкенила и С2-10 алкинила; где -Т0, С1-10 алкил, С2-10 алкенил и С2-10 алкинил необязательно замещены одним или более заместителями -Rx2, которые являются одинаковыми или различными, и где С1-10 алкил, С2-10 алкенил и С2-10 алкинил необязательно прерваны одной или более группами, выбранными из группы, состоящей из -Т0-, -С(O)O-, -О-, -С(О)-, -C(O)N(Rx3)-, -S(O)2N(Rx3)-, -S(O)N(Rx3)-, -S(O)2-, -S(O)-, -N(Rx3)S(O)2N(Rx3a)-, -S-, -N(Rx3)-, -OC(ORx3)(Rx3a)-, -N(Rx3)C(O)N(Rx3a)- и -OC(O)N(Rx3)-;
каждый -Rx1, -Rx1a, -Rx1b, -Rx3, -Rx3a независимо выбирают из группы, состоящей из -Н, галогена, C1-6 алкила, С2-6 алкенила и С2-6 алкинила;
каждый Т0 независимо выбирают из группы, состоящей из фенила, нафтила, инденила, инданила, тетралинила, С3-10 циклоалкила, 3-10-членного гетероциклила и 8-11-членного гетеробициклила; где каждый Т0 независимо необязательно замещен одним или более заместителями -Rx2, которые являются одинаковыми или различными;
каждый -Rx2 независимо выбирают из группы, состоящей из галогена, -CN, оксо (=O), -COORx4, -ORx4, -C(O)Rx4, -C(O)N(Rx4Rx4a), -S(O)2N(Rx4Rx4a), -S(O)N(Rx4Rx4a), -S(O)2Rx4, -S(O)Rx4, -N(Rx4)S(O)2N(Rx4aRx4b), -SRx4, -N(Rx4Rx4a), -NO2, -OC(O)Rx4, -N(Rx4)C(O)Rx4a, -N(Rx4)S(O)2Rx4a, -N(Rx4)S(O)Rx4a, -N(Rx4)C(O)ORx4a, -N(Rx4)C(O)N(Rx4aRx4b), -OC(O)N(Rx4Rx4a) и C1-6 алкила; где C1-6 алкил необязательно замещен одним или более заместителями галоген, которые являются одинаковыми или различными;
каждый -Rx4, -Rx4a, -Rx4b независимо выбирают из группы, состоящей из -Н, галогена, C1-6 алкила, С2-6 алкенила и С2-6 алкинила;
Даже более предпочтительно, одни или более дополнительные необязательные заместители независимо друг от друга выбирают из группы, состоящей из галогена, -CN, -COORx1, -ORx1, -C(O)Rx1, -C(O)N(Rx1Rx1a), -S(O)2N(Rx1Rx1a), -S(O)N(Rx1Rx1a), -S(O)2Rx1, -S(O)Rx1, -N(Rx1)S(O)2N(Rx1aRx1b), -SRx1, -N(Rx1Rx1a), -NO2, -OC(O)Rx1, -N(Rx1)C(O)Rx1a, -N(Rx1)S(O)2Rx1a, -N(Rx1)S(O)Rx1a, -N(Rx1)C(O)ORx1a, -N(Rx1)C(O)N(Rx1aRx1b), -OC(O)N(Rx1Rx1a), -T0, С1-6 алкила, C2-6 алкенила и С2-6 алкинила; где -Т0, C1-6 алкил, С2-6 алкенил и С2-6 алкинил необязательно замещены одним или более заместителями -Rx2, которые являются одинаковыми или различными, и где C1-6 алкил, С2-6 алкенил и С2-6 алкинил необязательно прерваны одной или более группами, выбранными из группы, состоящей из -Т0-, -С(O)O-, -О-, -С(О)-, -C(O)N(Rx3)-, -S(O)2N(Rx3)-, -S(O)N(Rx3)-, -S(O)2-, -S(O)-, -N(Rx3)S(O)2N(Rx3a)-, -S-, -N(Rx3)-, -OC(ORx3)(Rx3a)-, -N(Rx3)C(O)N(Rx3a)- и -OC(O)N(Rx3)-;
каждый -Rx1, -Rx1a, -Rx1b, -Rx2, -Rx3, -Rx3a независимо выбирают из группы, состоящей из -Н, галогена, C1-6 алкила, С2-6 алкенила и С2-6 алкинила;
каждый Т0 независимо выбирают из группы, состоящей из фенила, нафтила, инденила, инданила, тетралинила, С3-10 циклоалкила, 3-10-членного гетероциклила и 8-11-членного гетеробициклила; где каждый Т0 независимо необязательно замещен одним или более заместителями -Rx2, которые являются одинаковыми или различными.
Предпочтительно, максимум 6 -Н атомов необязательно замещенной молекулы независимо замещены заместителем, например, 5 -Н атомов независимо замещены заместителем, 4 -Н атома независимо замещены заместителем, 3 -Н атома независимо замещены заместителем, 2 -Н атома независимо замещены заместителем, или 1 -Н атом замещен заместителем.
Термин "прерванный" означает, что фрагмент вставлен между двумя атомами углерода или - если вставка находится на одном из концов составляющей - между атомом углерода или гетероатомом и атомом водорода, предпочтительно между атомом углерода и атомом водорода.
Как применяется в настоящей заявке, термин "C1-4 алкил" сам по себе или в комбинации означает неразветвленную или разветвленную алкильную составляющую, имеющую от 1 до 4 атомов углерода. Если присутствует на конце молекулы, примерами неразветвленного или разветвленного C1-4 алкила являются метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор.-бутил и трет.-бутил. Когда две составляющие молекулы связаны C1-4 алкилом, примерами таких C1-4 алкильных групп являются -СН2-, -СН2-СН2-, -СН(СН3)-, -СН2-СН2-СН2-, -СН(С2Н5)-, -С(СН3)2-. Каждый водород C1-4 алкильного углерода может необязательно быть замещен заместителем, как определено выше. Необязательно, C1-4 алкил может быть прерван одной или более составляющими, как определено далее.
Как применяется в настоящей заявке, термин "C1-6 алкил" сам по себе или в комбинации означает неразветвленную или разветвленную алкильную составляющую, имеющую от 1 до 6 атомов углерода. Если присутствует на конце молекулы, примерами неразветвленных или разветвленных C1-6 алкильных групп являются метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор.-бутил, трет-бутил, н-пентил, 2-метилбутил, 2,2-диметилпропил, н-гексил, 2-метилпентил, 3-метилпентил, 2,2-диметилбутил, 2,3-диметилбутил и 3,3-диметилпропил. Когда две составляющие молекулы связаны C1-6 алкильной группой, примерами таких C1-6 алкильных групп являются -СН2-, -СН2-СН2-, -СН(СН3)-, -СН2-СН2-СН2-, -СН(С2Н5)- и С(СН3)2-. Каждый атом водорода при C1-6 атоме углерода может необязательно быть замещен заместителем, как определено выше. Необязательно, C1-6 алкил может быть прерван одной или более составляющими, как определено далее.
Соответственно, "C1-10 алкил", "C1-20 алкил" или "С1-50 алкил" означает алкильную цепь, имеющую от 1 до 10, от 1 до 20 или от 1 до 50 атомов углерода, соответственно, где каждый атом водорода при C1-10, C1-20 или С1-50 атоме углерода может необязательно быть замещен заместителем, как определено выше. Необязательно, С1-10 или С1-50 алкил может быть прерван одной или более составляющими, как определено далее.
Как применяется в настоящей заявке, термин "С2-6 алкенил" сам по себе или в комбинации означает неразветвленную или разветвленную углеводородную составляющую, содержащую по меньшей мере одну двойную связь углерод-углерод, имеющую от 2 до 6 атомов углерода. Если присутствует на конце молекулы, примерами являются СН=СН2, -СН=СН-СН3, -СН2-СН=СН2, -СН=СНСН2-СН3 и -СН=СН-СН=СН2. Когда две составляющие молекулы связаны С2-6 алкенильной группой, тогда примером такого С2-6 алкенила является -СН=СН-. Каждый атом водорода С2-6 алкенильной составляющей может необязательно быть замещен заместителем, как определено выше. Необязательно, С2-6 алкенил может быть прерван одной или более составляющими, как определено далее.
Соответственно, термин "C2-10 алкенил", "С2-20 алкенил" или "С2-50 алкенил" сам по себе или в комбинации означает неразветвленную или разветвленную углеводородную составляющую, содержащую по меньшей мере одну двойную связь углерод-углерод, имеющую от 2 до 10, от 2 до 20 или от 2 до 50 атомов углерода. Каждый атом водорода C2-10 алкенильной, С2-20 алкенильной или C2-50 алкенильной группы может необязательно быть замещен заместителем, как определено выше. Необязательно, C2-10 алкенил, С2-20 алкенил или C2-50 алкенил может быть прерван одной или более составляющими, как определено далее.
Как применяется в настоящей заявке, термин "С2-6 алкинил" сам по себе или в комбинации означает неразветвленную или разветвленную углеводородную составляющую, содержащую по меньшей мере одну тройную связь углерод-углерод, имеющую от 2 до 6 атомов углерода. Если присутствует на конце молекулы, примерами являются -C≡СН, -СН2-ОСН, СН2-СН2-ОСН и СН2-С≡C-СН3. Когда две составляющие молекулы связаны алкинильной группой, тогда примером является -С≡С-. Каждый атом водорода С2-6 алкинильной группы может необязательно быть замещен заместителем, как определено выше. Необязательно, могут присутствовать одна или более двойных связей. Необязательно, С2-6 алкинил может быть прерван одной или более составляющими, как определено далее.
Соответственно, как применяется в настоящей заявке, термин "C2-10 алкинил", "С2-20 алкинил" и "С2-50 алкинил" сам по себе или в комбинации означает неразветвленную или разветвленную углеводородную составляющую, содержащую по меньшей мере одну тройную связь углерод-углерод, имеющую от 2 до 10, от 2 до 20 или от 2 до 50 атомов углерода, соответственно. Каждый атом водорода C2-10 алкинильной, С2-20 алкинильной или С2-50 алкинильной группы может необязательно быть замещен заместителем, как определено выше. Необязательно, могут присутствовать одна или более двойных связей. Необязательно, С2-10 алкинил, С2-20 алкинил или С2-50 алкинил может быть прерван одной или более составляющими, как определено далее.
Как упомянуто выше, C1-4 алкил, C1-6 алкил, C1-10 алкил, С1-20 алкил, С1-50 алкил, С2-6 алкенил, C2-10 алкенил, С2-20 алкенил, С2-50 алкенил, С2-6 алкинил, C2-10 алкинил, С2-20 алкенил или С2-50 алкинил может необязательно быть прерван одной или более составляющими, которые предпочтительно выбирают из группы, состоящей из
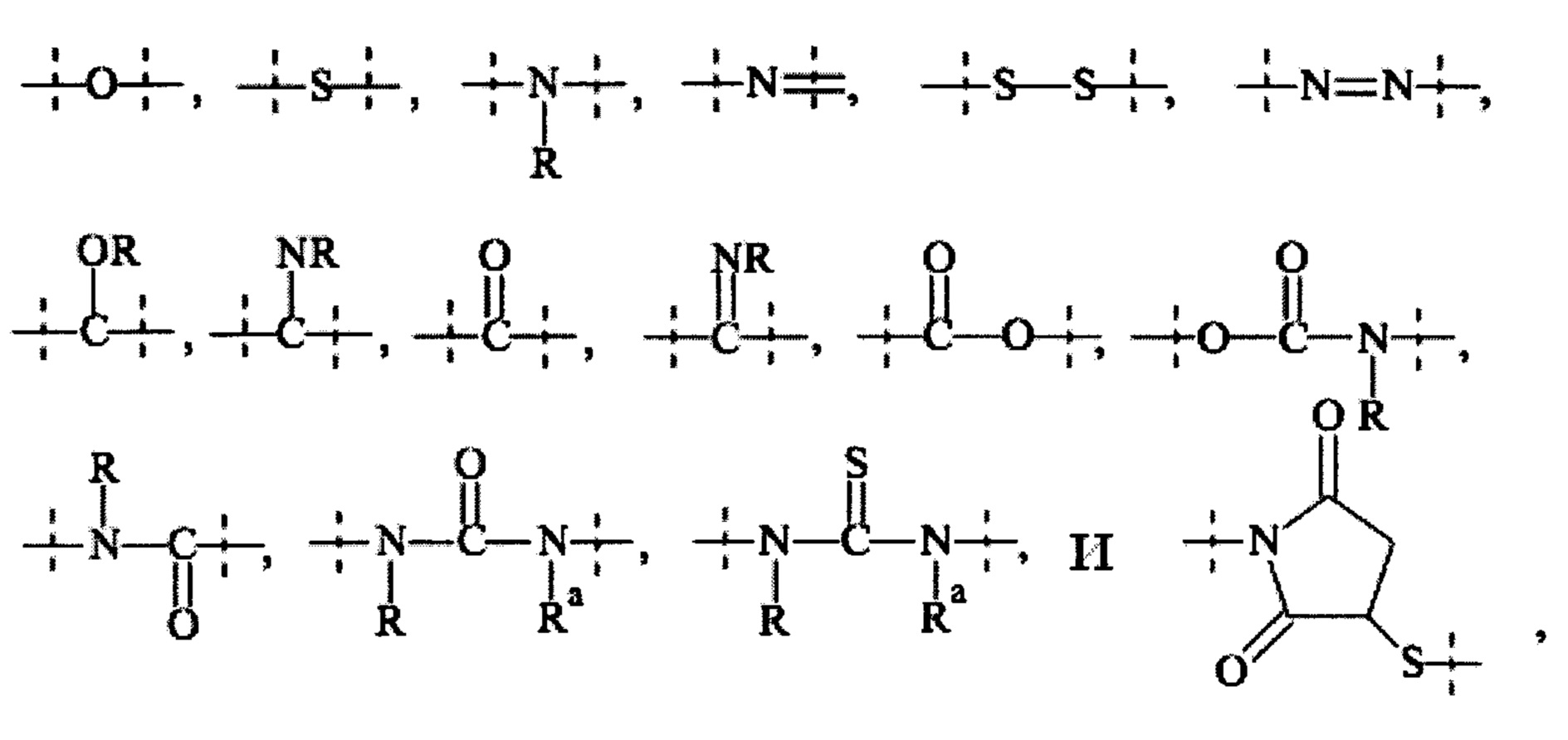
где
пунктирные линии обозначают присоединение к оставшейся части составляющей или реагента,; и
-R и Ra независимо друг от друга выбирают из группы, состоящей из -Н, метила, этила, пропила, бутила, пентила и гексила.
Как применяется в настоящей заявке, термин "C3-10 циклоалкил" означает циклическую алкильную цепь, имеющую от 3 до 10 атомов углерода, которая может быть насыщенной или ненасыщенной, например, циклопропил, циклобутил, циклопентил, циклогексил, циклогексенил, циклогептил, циклооктил, циклононил или циклодецил. Каждый атом водорода C3-10 циклоалкильного углерода может быть замещен заместителем, как определено выше. Термин "C3-10 циклоалкил" также включает мостиковые бициклы, такие как норборнан или норборнен.
Термин "8-30-членный карбополициклил" или "8-30-членный карбополицикл" означает циклическую составляющую из двух или более колец с 8-30 кольцевыми атомами, где два соседних кольца разделяют по мере один кольцевой атом, и которая может содержать до максимального числа двойных связей (ароматическое или неароматическое кольцо, которое является полностью насыщенным, частично ненасыщенным или ненасыщенным). Предпочтительно 8-30-членный карбополициклил означает циклическую составляющую из двух, трех, четырех или пяти колец, более предпочтительно двух, трех или четырех колец.
Как применяется в настоящей заявке, термин "3-10-членный гетероциклил" или "3-10-членный гетероцикл" означает кольцо с 3, 4, 5, 6, 7, 8, 9 или 10 кольцевыми атомами, которое может содержать до максимального числа двойных связей (ароматическое или неароматическое кольцо, которое является полностью насыщенным, частично ненасыщенным или ненасыщенным), где по меньшей мере от одного кольцевого атома до четырех кольцевых атомов замещены гетероатомом, выбранным из группы, состоящей из серы (включая -S(O)-, -S(O)2-), кислорода и азота (включая =N(O)-), и где кольцо связано с остатком молекулы через атом углерода или азота. Примеры 3-10-членных гетероциклов включают, но без ограничения к этому, азиридин, оксиран, тиран, азирин, оксирен, тиирен, азетидин, оксетан, тиетан, фуран, тиофен, пиррол, пирролин, имидазол, имидазолин, пиразол, пиразолин, оксазол, оксазолин, изоксазол, изоксазолин, тиазол, тиазолин, изотиазол, изотиазолин, тиадиазол, тиадиазолин, тетрагидрофуран, тетрагидротиофен, пирролидин, имидазолидин, пиразолидин, оксазолидин, изоксазолидин, тиазолидин, изотиазолидин, тиадиазолидин, сульфолан, пиран, дигидропиран, тетрагидропиран, имидазолидин, пиридин, пиридазин, пиразин, пиримидин, пиперазин, пиперидин, морфолин, тетразол, триазол, триазолидин, тетразолидин, диазепан, азепин или гомопиперазин. Каждый атом водорода 3-10-членного гетеро циклила или 3-10-членной гетероциклической группы может быть замещен заместителем, как определено далее.
Как применяется в настоящей заявке, термин "8-11-членный гетеробициклил" или "8-11-членный гетеробицикл" означает гетероциклическую составляющую из двух колец с 8-11 кольцевыми атомами, где по меньшей мере один кольцевой атом разделен между двумя кольцами, и которая содержит до максимального числа двойных связей (ароматическое или неароматическое кольцо, которое является полностью насыщенным, частично ненасыщенным или ненасыщенным), где по меньшей мере от одного кольцевого атома до шести кольцевых атомов замещены гетероатомом, выбранным из группы, состоящей из серы (включая -S(O)-, -S(O)2-), кислорода и азота (включая =N(O)-), и где кольцо связано с остатком молекулы через атом углерода или азота. Примерами 8-11-членного гетеробицикла являются индол, индолин, бензофуран, бензотиофен, бензоксазол, бензизоксазол, бензотиазол, бензизотиазол, бензимидазол, бензимидазолин, хинолин, хиназолин, дигидрохиназолин, хинолин, дигидрохинолин, тетрагидрохинолин, декагидрохинолин, изохинолин, декагидроизохинолин, тетрагидроизохинолин, дигидроизохинолин, бензазепин, пурин или птеридин. Термин 8-11-членный гетеробицикл также включает спиро-структуры из двух циклов, такие как 1,4-диокса-8-азаспиро[4.5]декан или мостиковые гетероциклы, такие как 8-аза-бицикло[3.2.1]октан. Каждый атом водорода 8-11-членного гетеробициклила или 8-11-членного гетеробицикла может быть замещен заместителем, как определено далее.
Подобным образом, термин "8-30-членный гетерополициклил" или "8-30-членный гетерополицикл" означает гетероциклическую составляющую из более чем двух колец с 8-30 кольцевыми атомами, предпочтительно тремя, четырьмя или пятью кольцами, где два соседних кольца разделяют по мере один кольцевой атом, и которая может содержать до максимального числа двойных связей (ароматическое или неароматическое кольцо, которое является полностью насыщенным, частично ненасыщенным или ненасыщенным), где по меньшей мере от одного кольцевого атома до 10 кольцевых атомов замещены гетероатомом, выбранным из группы, состоящей из серы (включая -S(O)-, -S(O)2-), кислорода и азота (включая =N(O)-), и где кольцо связано с остатком молекулы через атом углерода или азота.
Понятно, что фраза "пара Rx/Ry, соединяется вместе с атомом, к которому они присоединены, с образованием C3-10 циклоалкила или 3-10-членного гетероциклила" в отношении составляющей структуры
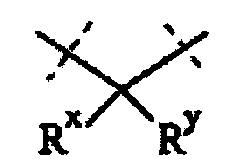
означает, что Rx и Ry образуют следующую структуру:
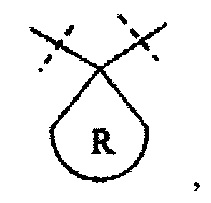
где R представляет собой C3-10 циклоалкил или 3-10-членный гетероциклил.
Также понятно, что фраза "пара Rx/Ry, соединяется вместе с атомом, к которому они присоединены, с образованием кольца А" в отношении составляющей структуры
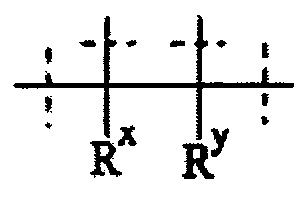
означает, что Rx и Ry образуют следующую структуру:
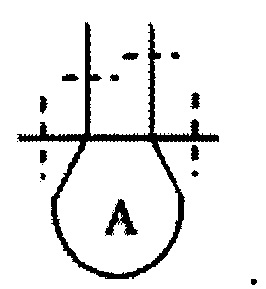
Как применяется в настоящей заявке, термин "терминальный алкин" означает составляющую
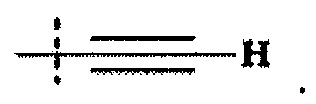
Как применяется в настоящей заявке, "галоген" означает фтор, хлор, бром или иод. В общем предпочтительно, что галогеном является фтор или хлор.
В общем, термин "содержит" или "содержащий" также охватывает "состоит из" или "состоящий из".
Предпочтительно -D имеет последовательность SEQ ID NO:24, SEQ ID NO:25 или SEQ ID NO:30, даже более предпочтительно последовательности SEQ ID NO:24 и SEQ ID NO:25.
В одном варианте выполнения настоящего изобретения -D имеет последовательность SEQ ID NO:25.
В другом варианте выполнения настоящего изобретения -D имеет последовательность SEQ ID NO:30.
В предпочтительном варианте выполнения настоящего изобретения -D имеет последовательность SEQ ID NO:24.
Составляющая -L1- представляет собой обратимый линкер пролекарства, из которого лекарственное средство, т.е. CNP, высвобождается в его свободной форме, т.е. представляет собой бесследный линкер пролекарства. Подходящие пролекарственные линкеры известны в данной области техники, как например обратимые линкерные составляющие пролекарства, раскрываются в WO 2005/099768 А2, WO 2006/136586 А2, WO 2011/089216 А1 и WO 2013/024053 А1, которые включены в настоящую заявку посредством ссылки.
В другом варианте выполнения настоящего изобретения -L1- представляет собой обратимый пролекарственный линкер, как описано в WO 2011/012722 A1, WO 2011/089214 A1, WO 2011/089215 A1, WO 2013/024052 A1 и WO 2013/160340 A1, которые включены в настоящую заявку посредством ссылки.
Составляющая -L1- может быть соединена с -D через любой тип связи, при условии, что она является обратимой. Предпочтительно, -L1- соединена с -D через связь, выбранную из группы, состоящей из амида, сложного эфира, карбамата, ацеталя, аминаля, имина, оксима, гидразона, дисульфида и ацилгуанидина. Даже более предпочтительно -L1- соединена с -D через связь, выбранную из группы, состоящей из амида, сложного эфира, карбамата и ацилгуанидина.
В предпочтительном варианте выполнения настоящего изобретения, составляющая -L1- соединена с -D через амидную связь. Понятно, что амидные связи в общем не являются обратимыми, но что согласно настоящему изобретению соседние группы, содержащиеся в L1, делают амидную связь обратимой.
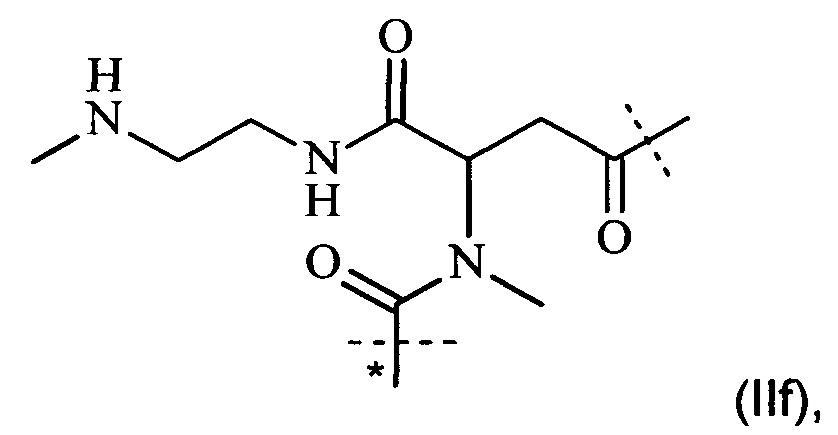
Особенно предпочтительная составляющая -L1- раскрывается в WO 2009/095479 А2. Соответственно, в одном предпочтительном варианте выполнения настоящего изобретения составляющая -L1- имеет формулу (II):
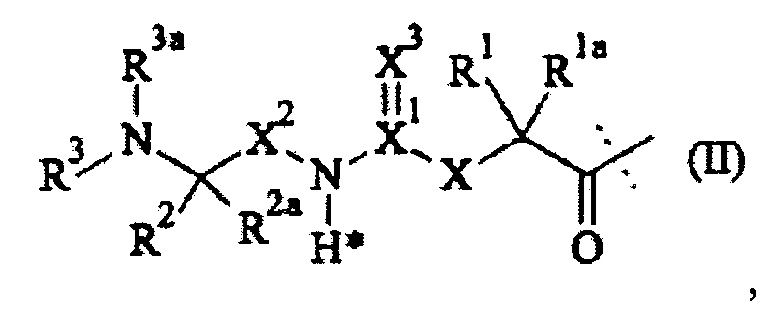
где пунктирная линия обозначает присоединение к атому азота составляющей -D, которая представляет собой CNP составляющую, путем образования амидной связи;
-Х- представляет собой -C(R4R4a)-; -N(R4)-; -О-; -C(R4R4a)-C(R5R5a)-; -C(R5R5a)-C(R4R4a)-; -C(R4R4a)-N(R6)-; -N(R6)-C(R4R4a)-; -C(R4R4a)-O-; -O-C(R4R4a)-; или -C(R7R7a);
X1 представляет собой С; или S(O);
-X2- представляет собой -C(R8R8a)-; или -C(R8R8a)-C(R9R9a)-;
=Х3 представляет собой =O; =S; или =N-CN;
-R1, -R1a, -R2, -R2a, -R4, -R4a, -R5, -R5a, -R6, -R8, -R8a, -R9, -R9a независимо выбирают из группы, состоящей из -Н; и C1-6 алкила;
-R3, -R3a независимо выбирают из группы, состоящей из -Н; и C1-6 алкила, при условии, что в случае, если один из -R3, -R3a или оба отличны от водорода, они соединены с N, к которому они присоединены через SP3-гибридизованный атом углерода;
-R7 представляет собой -N(R10R10a); или -NR10-(C=O)R11;
-R7a, -R10, -R10a, -R11 независимо друг от друга представляют собой -Н; или C1-6 алкил;
необязательно, одна или более из пар -R1a/-R4a, -R1a/-R5a, -R1a/-R7a, -R4a/-R5a, -R8a/-R9a образуют химическую связь;
необязательно, одна или более из пар -R1/-R1a, -R2/-R2a, -R4/-R4a, -R5/-R5a, -R8/-R8a,
-R9/-R9a соединяются вместе с атомом, к которому они присоединены, с образованием C3-10 циклоалкила; или 3-10-членного гетероциклила;
необязательно, одна или более из пар -R1/-R4, -R1/-R5, -R1/-R6, -R1/-R7a, -R4/-R5, -R4/-R6, -R8/-R9, -R2/-R3 соединяются вместе с атомами, к которым они присоединены, с образованием кольца А;
необязательно, R3/R3a соединяются вместе с атомом азота, к которому они присоединены, с образованием 3-10-членного гетероцикла;
А выбирают из группы, состоящей из фенила; нафтила; инденила; инданила; тетралинила; C3-10 циклоалкила; 3-10-членного гетероциклила; и 8-11-членного гетеробициклила; и
где -L1- имеет в качестве заместителя -L2-Z или -L2-Z’, и где -L1- необязательно дополнительно замещена, при условии, что водород, отмеченный звездочкой в формуле (II), не замещен -L2-Z или -L2-Z’ или заместителем;
где
-L2- представляет собой одинарную химическую связь или спейсер;
-Z представляет собой растворимый в воде носитель; и
-Z’ представляет собой нерастворимый в воде носитель.
Предпочтительно -L1- формулы (II) имеет в качестве заместителя одну составляющую -L2-Z или -L2-Z’.
В одном варианте выполнения настоящего изобретения -L1- формулы (II) дополнительно не замещена.
Понятно, что если -R3/-R3a формулы (II) соединяются вместе с атомом азота, к которому они присоединены, с образованием 3-10-членного гетероцикла, только такие 3-10-членные гетероциклы могут быть образованы, в которых атомы, непосредственно соединенные с атомом азота, представляют собой SP3-гибридизованные атомы углерода. Другими словами, такой 3-10-членный гетероцикл, образованный -R3/-R3a вместе с атомом азота, с которыми они соединены, имеет следующую структуру:
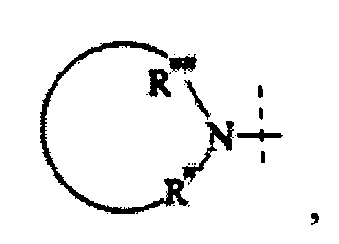
где
пунктирная линия обозначает присоединение к остатку -L1-;
кольцо содержит от 3 до 10 атомов, включая по меньшей мере один атом азота; и
R# и R## представляют собой SP3-гибридизованный атом углерода.
Также понятно, что 3-10-членный гетероцикл может быть дополнительно замещен.
Примерными вариантами выполнения подходящих 3-10-членных гетероциклов, образованных -R3/-R3a формулы (II) вместе с атомом азота, к которому они присоединены, являются следующие:
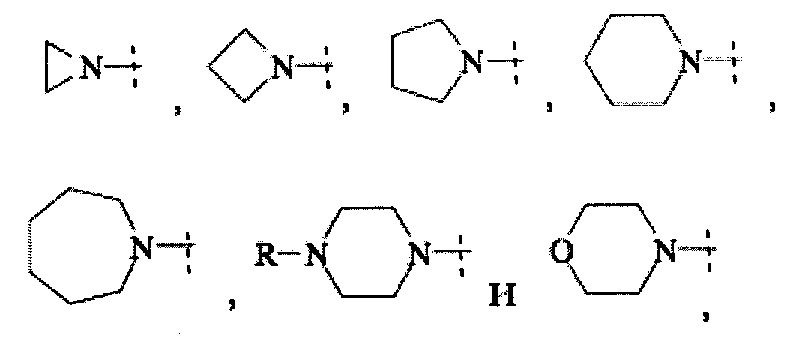
где
пунктирная линия обозначает присоединение к остатку молекулы; и
-R выбирают из группы, состоящей из -Н и C1-6 алкила.
-L1- формулы (II) может необязательно быть дополнительно замещенной. В общем, любой заместитель может применяться, до тех пор, пока принцип расщепления не затронут, т.е. водород, помеченный звездочкой в формуле (II), не заменен, а азот составляющей
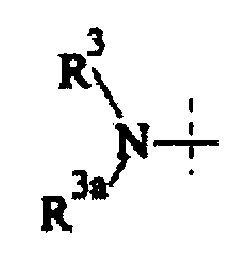
формулы (II) остается частью первичного, вторичного или третичного амина, т.е. -R3 и R3a независимо друг от друга представляют собой -Н или соединены с -N< через SP3-гибридизованный атом углерода.
В одном варианте выполнения настоящего изобретения -R1 или R1a формулы (II) имеет в качестве заместителя -L2-Z или L2-Z’. В другом варианте выполнения настоящего изобретения -R2 или R2a формулы (II) имеет в качестве заместителя -L2-Z или L2-Z’. В другом варианте выполнения настоящего изобретения -R3 или R3a формулы (II) имеет в качестве заместителя -L2-Z или L2-Z’. В другом варианте выполнения настоящего изобретения -R4 формулы (II) имеет в качестве заместителя -L2-Z или L2-Z’. В другом варианте выполнения настоящего изобретения -R5 или R5a формулы (II) имеет в качестве заместителя -L2-Z или L2-Z’. В другом варианте выполнения настоящего изобретения -R6 формулы (II) имеет в качестве заместителя -L2-Z или L2-Z’. В другом варианте выполнения настоящего изобретения -R7 или R7a формулы (II) имеет в качестве заместителя -L2-Z или L2-Z’. В другом варианте выполнения настоящего изобретения -R8 или R8a формулы (II) имеет в качестве заместителя -L2-Z или L2-Z’. В другом варианте выполнения настоящего изобретения -R9 или R9a формулы (II) имеет в качестве заместителя -L2-Z или L2-Z’.
Наиболее предпочтительно -R4 формулы (II) имеет в качестве заместителя -L2-Z или L2-Z’.
Предпочтительно, -Х- формулы (II) представляет собой -C(R4R4a)- или N(R4)-. Наиболее предпочтительно, -Х- формулы (II) представляет собой -C(R4R4a)-.
Предпочтительно, X1 формулы (II) представляет собой С.
Предпочтительно, =Х3 формулы (II) представляет собой =O.
Предпочтительно, -X2- формулы (II) представляет собой -C(R8R8a)-.
Предпочтительно -R8 и -R8a формулы (II) независимо выбирают из группы, состоящей из -Н, метила и этила. Более предпочтительно по меньшей мере один из -R8 и R8a формулы (II) представляет собой -Н. Даже более предпочтительно оба -R8 и R8a формулы (II) представляют собой -Н.
Предпочтительно, -R1 и R1a формулы (II) независимо выбирают из группы, состоящей из -Н, метила и этила. Более предпочтительно, по меньшей мере один из -R1 и R1a формулы (II) представляет собой -Н. Даже более предпочтительно оба -R1 и R1a формулы (II) представляют собой -Н.
Предпочтительно, -R2 и R2a формулы (II) независимо выбирают из группы, состоящей из -Н, метила и этила. Более предпочтительно, по меньшей мере один из -R2 и R2a формулы (II) представляет собой -Н. Даже более предпочтительно оба -R2 и R2a формулы (II) представляют собой Н.
Предпочтительно, -R3 и R3a формулы (II) независимо выбирают из группы, состоящей из -Н, метила, этила, пропила и бутила. Даже более предпочтительно по меньшей мере один из -R3 и R3a формулы (II) представляет собой метил. В равно предпочтительном варианте выполнения настоящего изобретения -R3 и R3a формулы (II) оба представляют собой -Н. В другом равно предпочтительном варианте выполнения настоящего изобретения -R3 и R3a формулы (II) оба представляют собой метил.
Предпочтительно, -R3 формулы (II) представляет собой -Н, и R3a формулы (II) представляет собой метил.
Предпочтительно, -R4 и R4a формулы (II) независимо выбирают из группы, состоящей из -Н, метила и этила. Более предпочтительно, по меньшей мере один из -R4 и R4a формулы (II) представляет собой -Н. Даже более предпочтительно оба -R4 и R4a формулы (II) представляют собой -Н.
Предпочтительно составляющая -L1- имеет формулу (IIa):
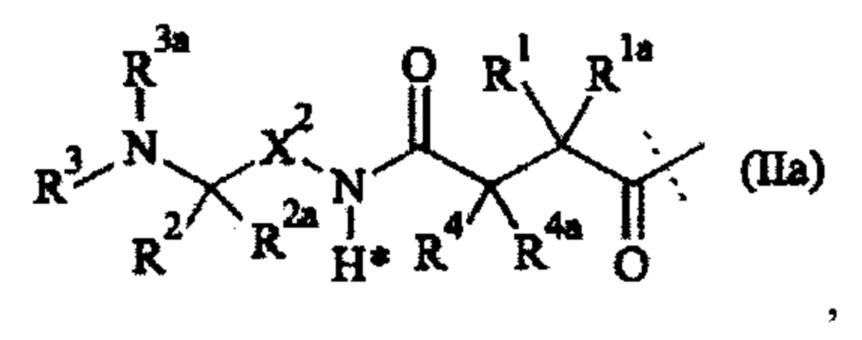
где пунктирная линия обозначает присоединение к атому азота составляющей -D, которая представляет собой CNP составляющую, путем образования амидной связи;
-R1, -R1a, -R2, -R2a, -R3, -R3a, -R4, -R4a и X2 - применяются, как определено в формуле (II); и
где -L1- имеет в качестве заместителя -L2-Z или L2-Z’, и где -L1- необязательно дополнительно замещена, при условии, что водород, отмеченный звездочкой в формуле (IIa), не замещен -L2-Z или L2-Z’ или заместителем.
Предпочтительно -L1- формулы (IIa) имеет в качестве заместителя одну составляющую -L2-Z или L2-Z’.
Предпочтительно составляющая -L1- формулы (IIa) дополнительно не замещена.
Предпочтительно, -R1 и R1a формулы (IIa) независимо выбирают из группы, состоящей из -Н, метила и этила. Более предпочтительно, по меньшей мере один из -R1 и R1a формулы (IIa) представляет собой -Н. Даже более предпочтительно оба -R1 и R1a формулы (IIa) представляют собой -Н.
Предпочтительно, -R4 и R4a формулы (IIa) независимо выбирают из группы, состоящей из -Н, метила и этила. Более предпочтительно, по меньшей мере один из -R4 и R4a формулы (IIa) представляет собой -Н. Даже более предпочтительно оба -R4 и R4a формулы (IIa) представляют собой -Н.
Предпочтительно, -X2- формулы (IIa) представляет собой -C(R8R8a)-.
Предпочтительно -R8 и R8a формулы (IIa) независимо выбирают из группы, состоящей из -Н, метила и этила. Более предпочтительно по меньшей мере один из -R8 и R8a формулы (IIa) представляет собой -Н. Даже более предпочтительно оба -R8 и R8a формулы (IIa) представляют собой -Н.
Предпочтительно, -R2 и R2a формулы (IIa) независимо выбирают из группы, состоящей из -Н, метила и этила. Более предпочтительно, по меньшей мере один из -R2 и R2a формулы (IIa) представляет собой -Н. Даже более предпочтительно оба -R2 и R2a формулы (IIa) представляют собой Н.
Предпочтительно, -R3 и R3a формулы (IIa) независимо выбирают из группы, состоящей из -Н, метила, этила, пропила и бутила. Даже более предпочтительно по меньшей мере один из -R3 и R3a формулы (IIa) представляет собой метил. В равно предпочтительном варианте выполнения настоящего изобретения -R3 и R3a формулы (IIa) оба представляют собой -Н. В другом равно предпочтительном варианте выполнения настоящего изобретения -R3 и R3a формулы (IIa) оба представляют собой метил.
Предпочтительно, -R3 формулы (IIa) представляет собой -Н и R3a формулы (IIa) представляет собой метил.
Предпочтительно составляющая -L1- имеет формулу (IIb):
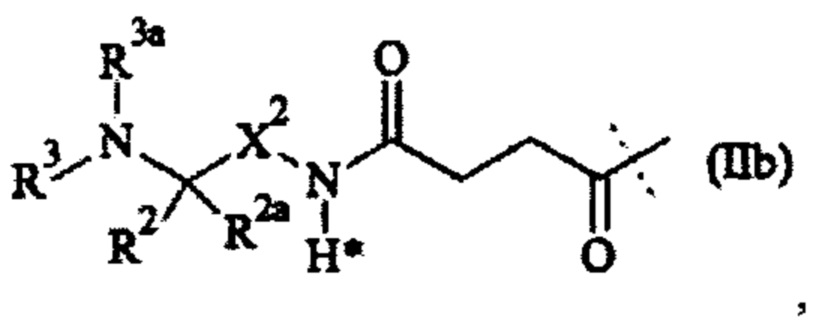
где пунктирная линия обозначает присоединение к атому азота составляющей -D, которая представляет собой CNP составляющую, путем образования амидной связи;
-R2, -R2a, -R3, -R3a и X2 - применяются, как определено в формуле (II); и
где -L1- имеет в качестве заместителя -L2-Z или L2-Z’, и где -L1- необязательно дополнительно замещена, при условии, что водород, отмеченный звездочкой в формуле (IIb), не замещен -L2-Z или L2-Z’ или заместителем.
Предпочтительно -L1- формулы (IIb) имеет в качестве заместителя одну составляющую -L2-Z или L2-Z’.
Предпочтительно составляющая -L1- формулы (IIb) дополнительно не замещена.
Предпочтительно, -X2- формулы (IIb) представляет собой -C(R8R8a)-.
Предпочтительно -R8 и R8a формулы (IIb) независимо выбирают из группы, состоящей из -Н, метила и этила. Более предпочтительно по меньшей мере один из -R8 и R8a формулы (IIb) представляет собой -Н. Даже более предпочтительно оба -R8 и R8a формулы (IIb) представляют собой -Н.
Предпочтительно, -R2 и R2a формулы (IIb) независимо выбирают из группы, состоящей из -Н, метила и этила. Более предпочтительно, по меньшей мере один из -R2 и R2a формулы (IIb) представляет собой -Н. Даже более предпочтительно оба -R2 и R2a формулы (IIb) представляет собой Н.
Предпочтительно, -R3 и R3a формулы (IIb) независимо выбирают из группы, состоящей из -Н, метила, этила, пропила и бутила. Даже более предпочтительно по меньшей мере один из -R3 и R3a формулы (IIb) представляет собой метил. В равно предпочтительном варианте выполнения настоящего изобретения -R3 и R3a формулы (IIb) оба представляют собой -Н. В другом равно предпочтительном варианте выполнения настоящего изобретения -R3 и R3a формулы (IIb) оба представляют собой метил.
Наиболее предпочтительно, -R3 формулы (IIb) представляет собой -Н и R3a формулы (IIb) представляет собой метил.
Даже более предпочтительно составляющая -L1- имеет формулу (IIb’):
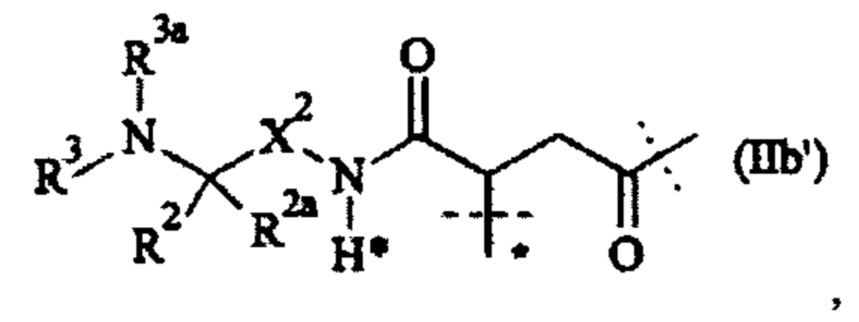
где
где пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой CNP составляющую, путем образования амидной связи;
пунктирная линия, отмеченная звездочкой, обозначает присоединение к -L2-;
-R2, -R2a, -R3, -R3a и X2 - применяются, как определено в формуле (II); и
где -L1- необязательно дополнительно замещена, при условии, что водород, отмеченный звездочкой в формуле (IIb’), не замещена заместителем.
Предпочтительно составляющая -L1- формулы (IIb’) дополнительно не замещена.
Предпочтительно, -X2- формулы (IIb’) представляет собой -C(R8R8a)-.
Предпочтительно -R8 и R8a формулы (IIb’) независимо выбирают из группы, состоящей из -Н, метила и этила. Более предпочтительно по меньшей мере один из -R8 и R8a формулы (IIb’) представляет собой -Н. Даже более предпочтительно оба -R8 и R8a формулы (IIb’) представляют собой -Н.
Предпочтительно, -R2 и R2a формулы (IIb’) независимо выбирают из группы, состоящей из -Н, метила и этила. Более предпочтительно, по меньшей мере один из -R2 и R2a формулы (IIb’) представляет собой -Н. Даже более предпочтительно оба -R2 и R2a формулы (IIb’) представляет собой Н.
Предпочтительно, -R3 и R3a формулы (IIb’) независимо выбирают из группы, состоящей из -Н, метила, этила, пропила и бутила. Даже более предпочтительно по меньшей мере один из -R3 и R3a формулы (IIb’) представляет собой метил. В равно предпочтительном варианте выполнения настоящего изобретения -R3 и R3a формулы (IIb’) оба представляют собой -Н. В другом равно предпочтительном варианте выполнения настоящего изобретения -R3 и R3a формулы (IIb’) оба представляют собой метил.
Наиболее предпочтительно, -R3 формулы (IIb’) представляет собой -Н, и R3a формулы (IIb’) представляет собой метил.
Предпочтительно составляющая -L1- имеет формулу (IIc):
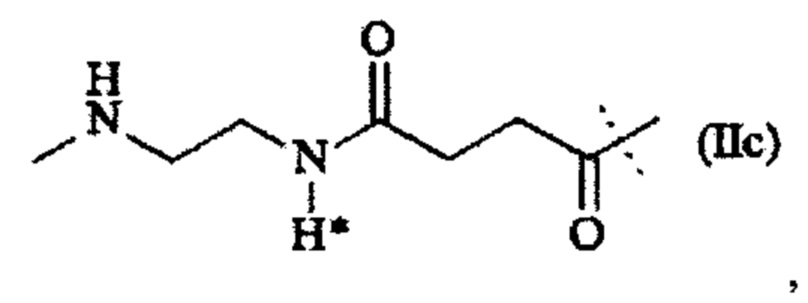
где пунктирная линия обозначает присоединение к атому азота составляющей -D, которая представляет собой CNP составляющую, путем образования амидной связи; и
где -L1- имеет в качестве заместителя -L2-Z или L2-Z’, и где -L1- необязательно дополнительно замещена, при условии, что водород, отмеченный звездочкой в формуле (IIc), не замещен -L2-Z или L2-Z’ или заместителем.
Предпочтительно -L1- формулы (IIc) имеет в качестве заместителя одну составляющую -L2-Z или L2-Z’.
Предпочтительно составляющая -L1- формулы (IIc) дополнительно не замещена.
В другом предпочтительном варианте выполнения настоящего изобретения составляющая -L1- имеет формулу (IIc-а):
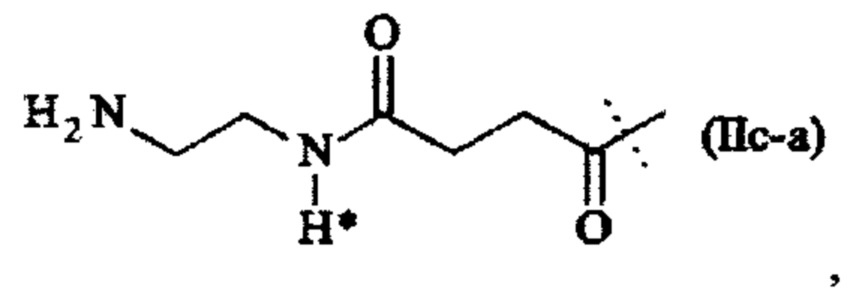
где пунктирная линия обозначает присоединение к атому азота составляющей -D, которая представляет собой CNP составляющую, путем образования амидной связи; и
где -L1- имеет в качестве заместителя -L2-Z или L2-Z’, и где -L1- необязательно дополнительно замещена, при условии, что водород, отмеченный звездочкой в формуле (IIc), не замещен -L2-Z или L2-Z’ или заместителем.
Предпочтительно -L1- формулы (IIc-а) имеет в качестве заместителя одну составляющую -L2-Z или L2-Z’.
Предпочтительно составляющая -L1- формулы (IIc-а) дополнительно не замещена.
В другом предпочтительном варианте выполнения настоящего изобретения составляющая -L1- имеет формулу (IIc-b):
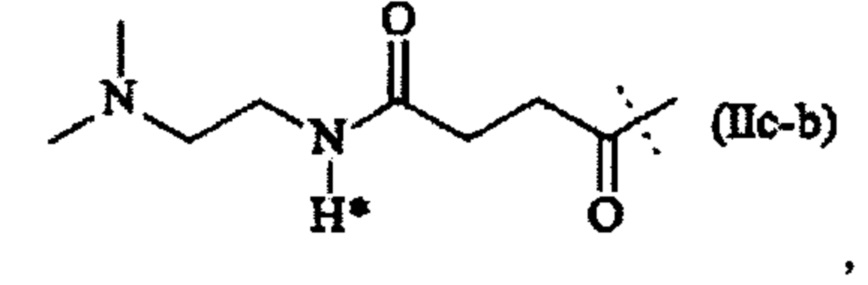
где пунктирная линия обозначает присоединение к атому азота составляющей -D, которая представляет собой CNP составляющую, путем образования амидной связи; и
где -L1- имеет в качестве заместителя -L2-Z или L2-Z’, и где -L1- необязательно дополнительно замещена, при условии, что водород, отмеченный звездочкой в формуле (IIc), не замещен -L2-Z или L2-Z’ или заместителем.
Предпочтительно -L1- формулы (IIc-b) имеет в качестве заместителя одну составляющую -L2-Z или L2-Z’.
Предпочтительно составляющая -L1- формулы (IIc-b) дополнительно не замещена.
Даже более предпочтительно составляющая -L1- выбирают из группы, состоящей из формул (IIc-i), (IIc-ii), (IIc-iii), (IIc-iv) и (IIc-v):
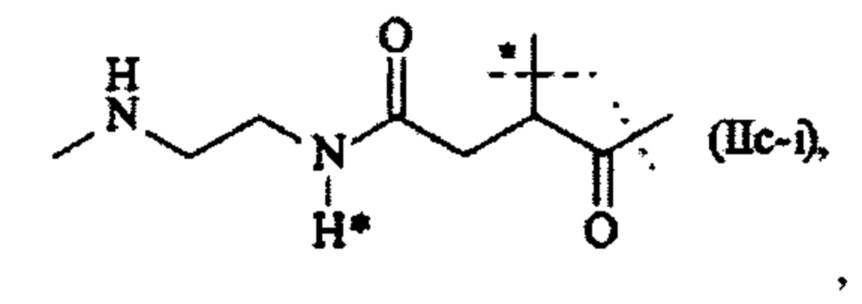
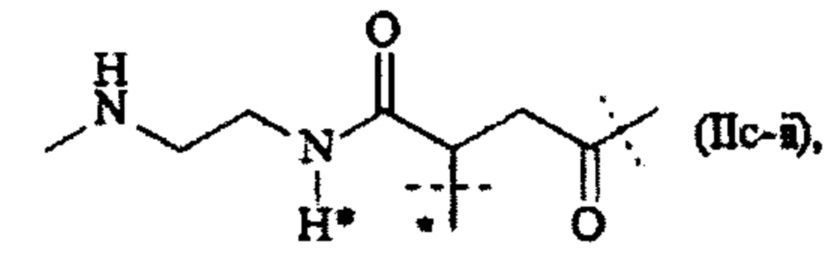
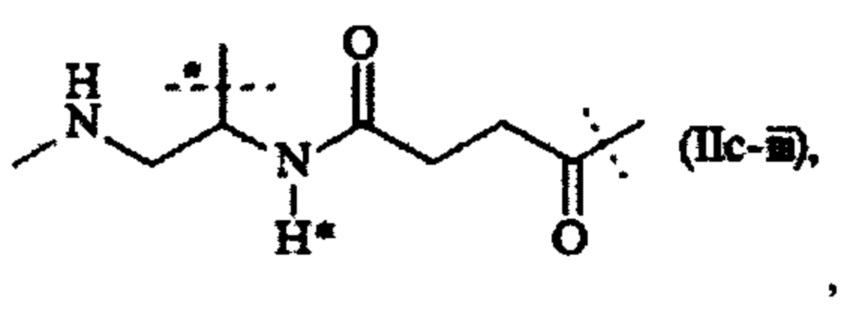
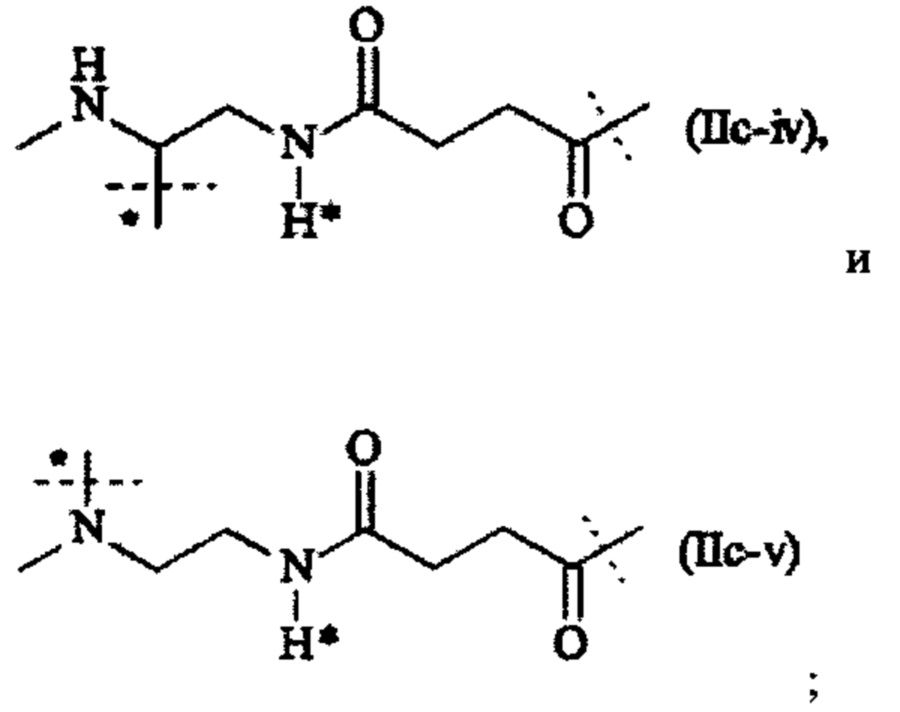
где
неотмеченная пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой CNP составляющую, путем образования амидной связи; и
пунктирная линия, отмеченная звездочкой, обозначает присоединение к L2-Z или L2-Z’; и
-L1- необязательно дополнительно замещена, при условии, что водород, отмеченный звездочкой в формуле (IIc-i), (IIc-ii), (IIc-iii), (IIc-iv) и (IIc-v), не замещена заместителем.
Предпочтительно, составляющая -L1- формулы (IIc-i), (IIc-ii), (IIc-iii), (IIc-iv) и (IIc-v) дополнительно не замещена.
В особенно предпочтительном варианте выполнения настоящего изобретения составляющая -L1- представляет собой
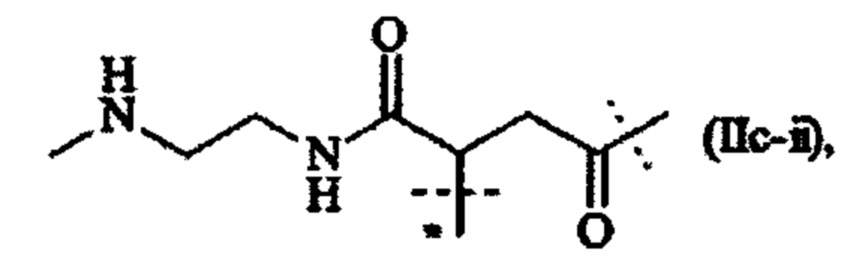
где
неотмеченная пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой CNP составляющую, путем образования амидной связи; и
пунктирная линия, отмеченная звездочкой, обозначает присоединение к -L2-Z или L2-Z’.
Предпочтительно -L1- формулы (IIc-ii) имеет в качестве заместителя одну составляющую -L2-Z или L2-Z’.
В равно предпочтительном варианте выполнения настоящего изобретения составляющая -L1- выбирают из группы, состоящей из формул (IIc-i’), (IIc-ii’), (IIc-iii’), (IIc-iv’) и (IIc-v’):
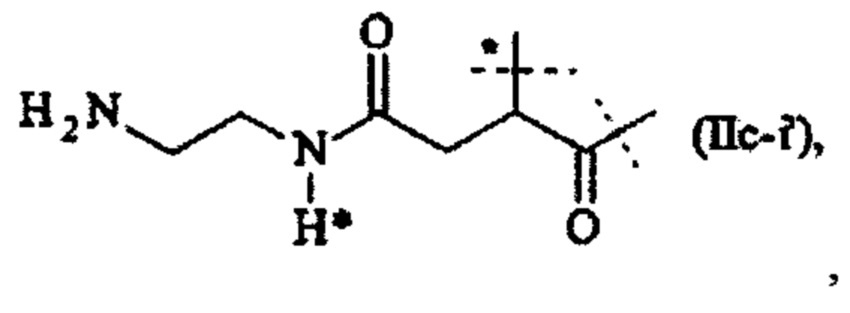
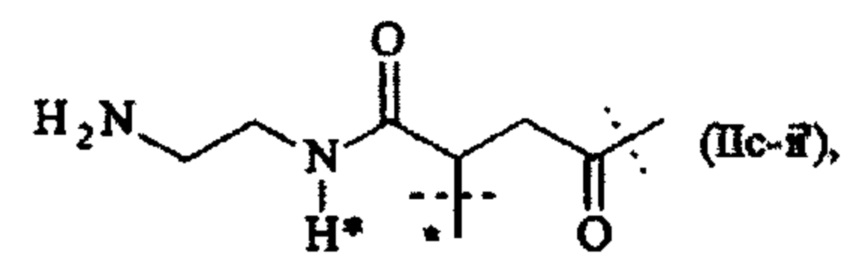
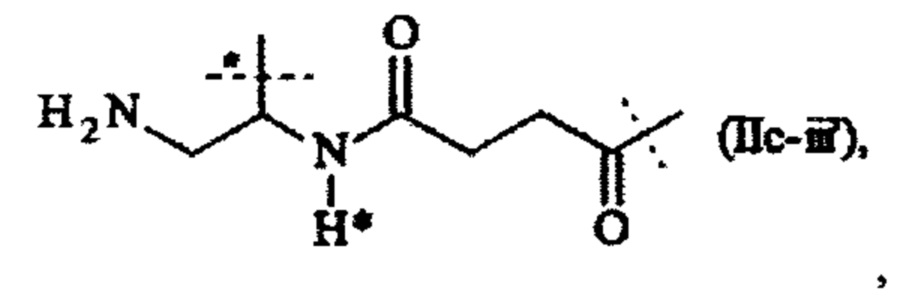
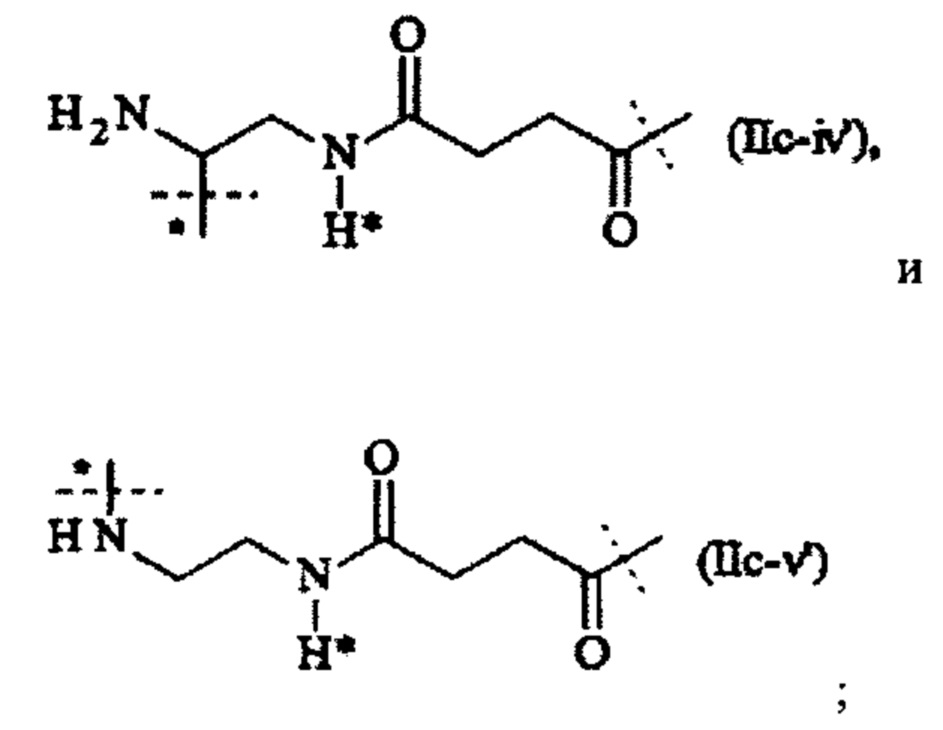
где
неотмеченная пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой CNP составляющую, путем образования амидной связи; и
пунктирная линия, отмеченная звездочкой, обозначает присоединение к -L2-Z или L2-Z’; и
-L1- необязательно дополнительно замещена, при условии, что водород, отмеченный звездочкой в формуле (IIc-i’), (IIc-ii’), (IIc-iii’), (IIc-iv’) и (IIc-v’), не замещена заместителем.
Предпочтительно, составляющая -L1- формулы (IIc-i’), (IIc-ii’), (IIc-iii’), (IIc-iv’) и (IIc-v’) дополнительно не замещена.
В другом особенно предпочтительном варианте выполнения настоящего изобретения составляющая -L1- представляет собой
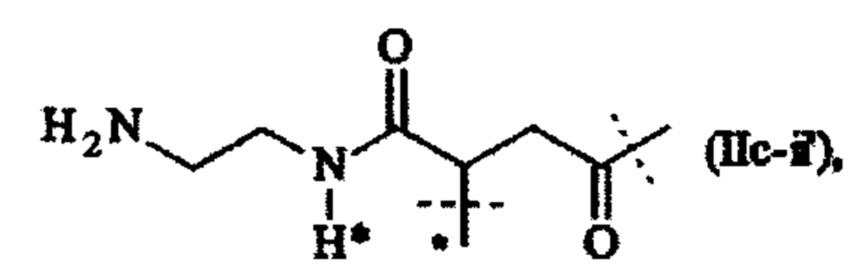
где
неотмеченная пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой CNP составляющую, путем образования амидной связи; и
пунктирная линия, отмеченная звездочкой, обозначает присоединение к -L2-Z или L2-Z’.
Предпочтительно -L1- формулы (IIc-ii’) имеет в качестве заместителя одну составляющую -L2-Z или L2-Z’.
В равно предпочтительном варианте выполнения настоящего изобретения составляющая -L1- выбирают из группы, состоящей из формул (IIc-i’’), (IIc-ii’’), (IIc-iii’’) и (IIc-iv’’):
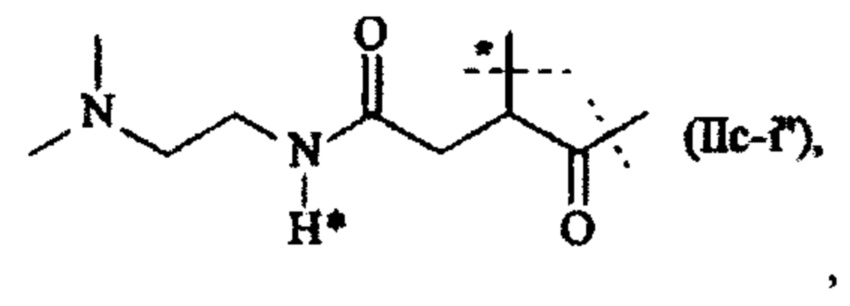
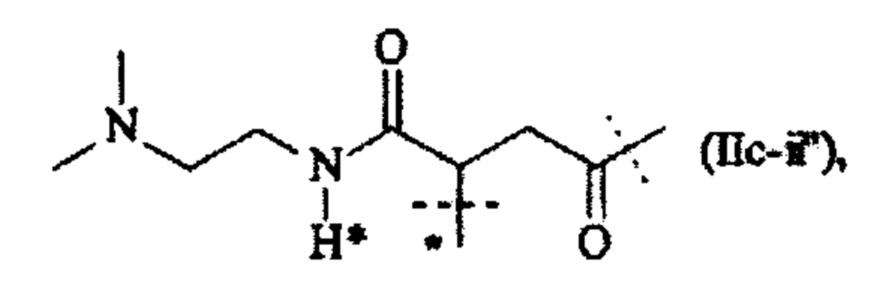
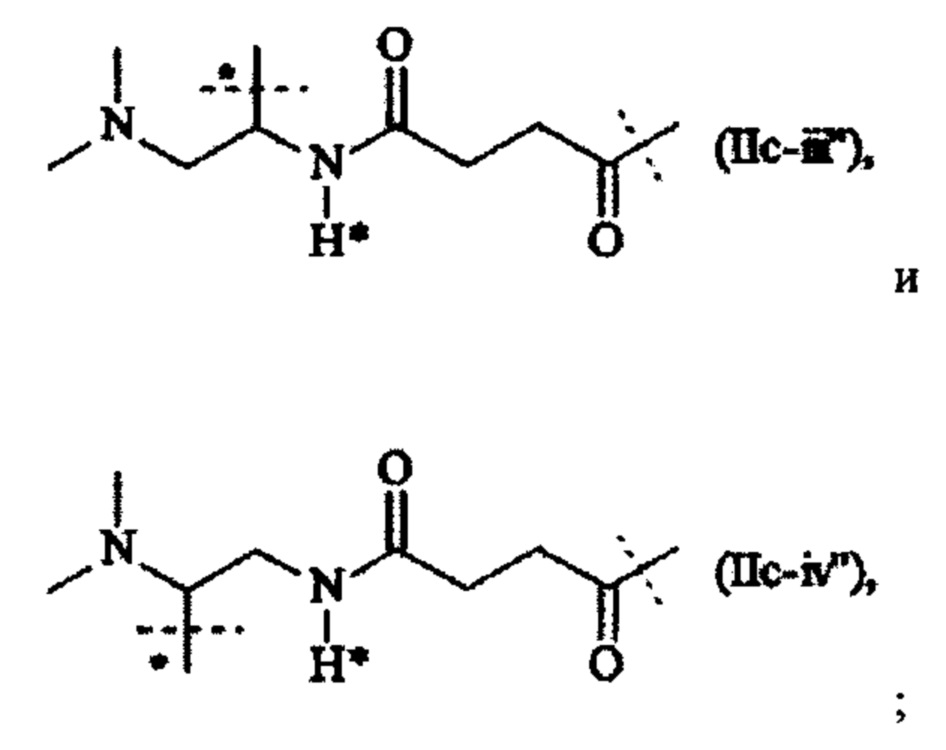
где
неотмеченная пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой CNP составляющую, путем образования амидной связи; и
пунктирная линия, отмеченная звездочкой, обозначает присоединение к -L2-Z или L2-Z’; и
-L1- необязательно дополнительно замещена, при условии, что водород, отмеченный звездочкой в формуле (IIc-i’’), (IIc-ii’’), (IIc-III’’’) и (IIc-iv’’), не замещена заместителем.
Предпочтительно, составляющая -L1- формулы (IIc-i’’), (IIc-ii’’), (IIc-iii’’) и (IIc-iv’’) дополнительно не замещена.
В другом особенно предпочтительном варианте выполнения настоящего изобретения составляющая -L1- представляет собой
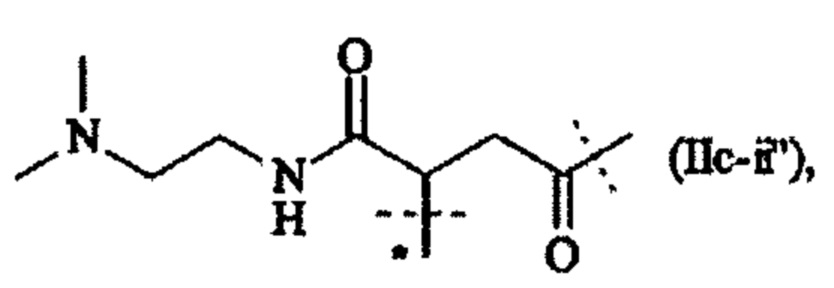
где
неотмеченная пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой CNP составляющую, путем образования амидной связи; и
пунктирная линия, отмеченная звездочкой, обозначает присоединение к -L2-Z или L2-Z’.
Предпочтительно -L1- формулы (IIc-ii’’) имеет в качестве заместителя одну составляющую -L2-Z или L2-Z’.
Необязательные другие заместители составляющей -L1- формулы (II), (IIa), (IIb), (IIb’), (IIc), (IIc-i), (IIc-ii), (IIc-iii), (IIc-iv), (IIc-v), (IIc-i’), (IIc-ii’), (IIc-iii’), (IIc-iv’), (IIc-v’), (IIc-i’’), (IIc-ii’’), (IIc-iii) и (IIc-iv’’) предпочтительно являются такими, как раскрывается выше.
Ругая особенно предпочтительная составляющая-L1- раскрывается в неопубликованной европейской заявке на патент 14180004, которой соответствует международная заявка с номером заявки РСТ/ЕР 2015/067929. Соответственно, в другом предпочтительном варианте выполнения настоящего изобретения составляющая -L1- имеет формулу (III):
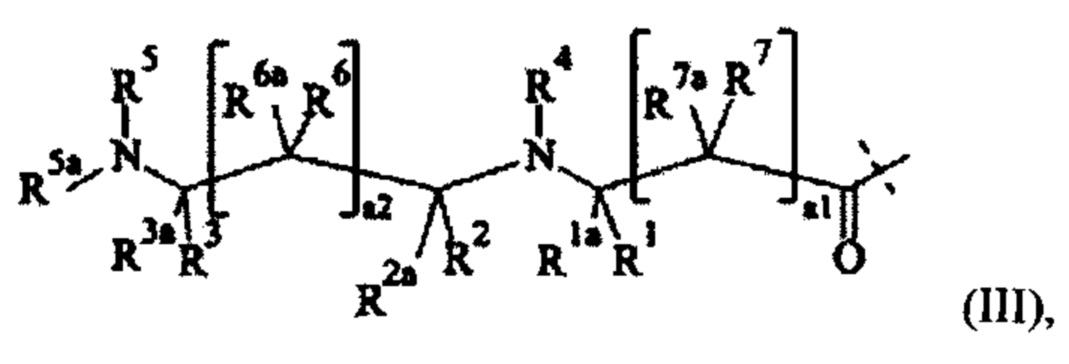
где
пунктирная линия показывает присоединение к первичному или вторичному амину или гидроксилу составляющей D путем образования амидной или сложноэфирной связи, соответственно;
-R1, -R1a, -R2, -R2a, -R3 и R3a независимо друг от друга выбирают из группы, состоящей из -Н, -C(R8R8aR8b), -C(=O)R8, -C≡N, -C(=NR8)R8a, -CR8(=CR8aR8b), -C=CR8 и T;
-R4, -R5 и R5a независимо друг от друга выбирают из группы, состоящей из -Н, -C(R9R9aR9b) и Т;
a1 и а2 независимо друг от друга представляют собой 0 или 1;
каждый -R6, -R6a, -R7, -R7a, -R8, -R8a, -R8b, -R9, -R9a, -R9b независимо друг от друга выбирают из группы, состоящей из -Н, галогена, -CN, -COOR10, -OR10, -C(O)R10, -C(O)N(R10R10a), -S(O)2N(R10R10a), -S(O)N(R10R10a), -S(O)2R10, -S(O)R10, -N(R10)S(O)2N(R10aR10b), -SR10, -N(R10R10a), -NO2, -OC(O)R10, -N(R10)C(O)R10a, -N(R10)S(O)2R10a, -N(R10)S(O)R10a, -N(R10)C(O)OR10a, -N(R10)C(O)N(R10aR10b), -OC(O)N(R10R10a), -T, C1-20 алкила, C2-20 алкенила и C2-20 алкинила; где -T, C1-20 алкил, С2-20 алкенил и С2-20 алкинил необязательно замещены одним или более заместителями -R11, которые являются одинаковыми или различными, и где C1-20 алкил, С2-20 алкенил и С2-20 алкинил необязательно прерваны одной или более группами, выбранными из группы, состоящей из -Т-, -C(O)O-, -О-, -С(О)-, -C(O)N(R12)-, -S(O)2N(R12)-, -S(O)N(R12)-, -S(O)2-, -S(O)-, -N(R12)S(O)2N(R12a)-, -S-, -N(R12)-, -OC(OR12)(R12a)-, -N(R12)C(O)N(R12a)- и -OC(O)N(R12)-;
каждый -R10, -R10a, -R10b независимо выбирают из группы, состоящей из -Н, -Т, C1-20 алкила, С2-20 алкенила и С2-20 алкинила; где -Т, С1-20 алкил, С2-20 алкенил и С2-20 алкинил необязательно замещены одним или более заместителями -R11, которые являются одинаковыми или различными, и где C1-20 алкил, С2-20 алкенил и С2-20 алкинил необязательно прерваны одной или более группами, выбранными из группы, состоящей из -Т-, -C(O)O-, -О-, -С(О)-, -C(O)N(R12)-, -S(O)2N(R12)-, -S(O)N(R12)-, -S(O)2-, -S(O)-, -N(R12)S(O)2N(R12a)-, -S-, -N(R12)-, -OC(OR12)(R12a)-, -N(R12)C(O)N(R12a)- и -OC(O)N(R12)-;
каждый T независимо друг от друга выбирают из группы, состоящей из фенила, нафтила, инденила, инданила, тетралинила, С3-10 циклоалкила, 3-10-членного гетероциклила и 8-11-членного гетеробициклила; где каждый Т независимо необязательно замещен одним или более заместителями -R11, которые являются одинаковыми или различными;
каждый -R11 независимо друг от друга выбирают из галогена, -CN, оксо (=O), -COOR13, -OR13, -C(O)R13, -C(O)N(R13R13a), -S(O)2N(R13R13a), -S(O)N(R13R13a), -S(O)2R13, -S(O)R13, -N(R13)S(O)2N(R13aR13b), -SR13, -N(R13R13a), -NO2, -OC(O)R13, -N(R13)C(O)R13a, -N(R13)S(O)2R13a, -N(R13)S(O)R13a, -N(R13)C(O)OR13a, -N(R13)C(O)N(R13aR13b), -OC(O)N(R13R13a) и C1-6 алкила; где C1-6 алкил необязательно замещен одним или более заместителями галоген, которые являются одинаковыми или различными;
каждый -R12, -R12a, -R13, -R13a, -R13b независимо выбирают из группы, состоящей из -Н и C1-6 алкила; где C1-6 алкил необязательно замещен одним или более заместителями галоген, которые являются одинаковыми или различными;
необязательно, одна или более из пар -R1/-R1a, -R2/-R2a, -R3/-R3a, -R6/-R6a, -R7/-R7a соединяются вместе с атомом, к которому они присоединены, с образованием С3-10 циклоалкила или 3-10-членного гетеро циклила;
необязательно, одна или более из пар -R1/-R2, -R1/-R3, -R1/-R4, -R1/-R5, -R1/-R6, -R1/-R7, -R2/-R3, -R2/-R4, -R2/-R5, -R2/-R6, -R2/-R7, -R3/-R4, -R3/-R5, -R3/-R6, -R3/-R7, -R4/-R5, -R4/-R6, -R4/-R7, -R5/-R6, -R5/-R7, -R6/-R7 соединяются вместе с атомами, к которым они присоединены, с образованием кольца А;
А выбирают из группы, состоящей из фенила; нафтила; инденила; инданила; тетралинила; С3-10 циклоалкила; 3-10-членного гетероциклила; и 8-11-членного гетеробициклила;
где -L1- имеет в качестве заместителя -L2-Z или L2-Z’, и где -L1- необязательно дополнительно замещена;
где
-L2- представляет собой одинарную химическую связь или спейсер;
-Z представляет собой растворимый в воде носитель; и
-Z’ представляет собой нерастворимый в воде носитель.
Необязательные другие заместители составляющей -L1- формулы (III) предпочтительно являются такими, как описано выше.
Предпочтительно -L1- формулы (III) имеет в качестве заместителя одну составляющую -L2-Z или L2-Z’.
В одном варианте выполнения настоящего изобретения -L1- формулы (III) дополнительно не замещена.
Дополнительные предпочтительные варианты выполнения для -L1- раскрываются в ЕР 1536334 В1, WO 2009/009712 A1, WO 2008/034122 A1, WO 2009/143412 A2, WO 2011/082368 A2 и US 8618124 B2, которые включены в настоящую заявку посредством ссылки в полном объеме.
Дополнительные предпочтительные варианты выполнения для -L1- раскрываются в US 8946405 B2 и US 8754190 B2, которые включены в настоящую заявку посредством ссылки в полном объеме. Соответственно, предпочтительная составляющая -L1- имеет формулу (IV):
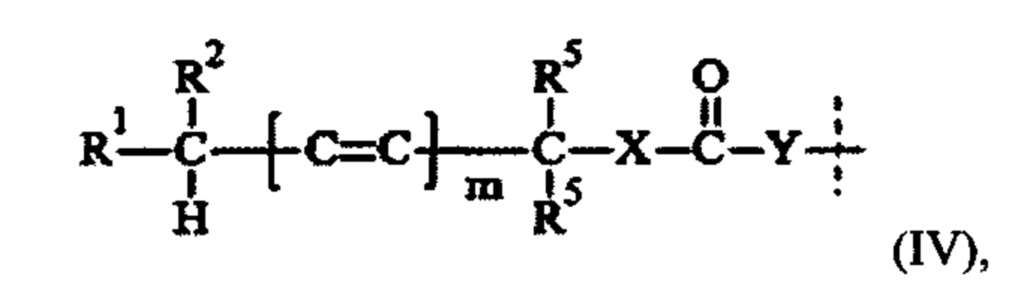
где
пунктирная линия показывает присоединение к -D, которая представляет собой CNP составляющую, и где присоединение осуществляется через функциональную группу составляющей -D, выбранную из группы, состоящей из -ОН, -SH и NH2;
m равно 0 или 1;
по меньшей мере один или оба из -R1 и R2 выбирается/независимо друг от друга выбирают из группы, состоящей из -CN, -NO2, необязательно замещенного арила, необязательно замещенного гетероарила, необязательно замещенного алкенила, необязательно замещенного алкинила, -C(O)R3, -S(O)R3, -S(O)2R3 и -SR4,
один и только один из -R1 и R2 выбирают из группы, состоящей из -Н, необязательно замещенного алкила, необязательно замещенного арилалкила и необязательно замещенного гетероарилалкила;
-R3 выбирают из группы, состоящей из -Н, необязательно замещенного алкила, необязательно замещенного арила, необязательно замещенного арилалкила, необязательно замещенного гетероарила, необязательно замещенного гетероарилалкила, -OR9 и N(R9)2;
-R4 выбирают из группы, состоящей из необязательно замещенного алкила, необязательно замещенного арила, необязательно замещенного арилалкила, необязательно замещенного гетероарила и необязательно замещенного гетероарилалкила;
каждый -R5 независимо выбирают из группы, состоящей из -Н, необязательно замещенного алкила, необязательно замещенного алкенилалкила, необязательно замещенного алкинилалкила, необязательно замещенного арила, необязательно замещенного арилалкила, необязательно замещенного гетероарила и необязательно замещенного гетероарилалкила;
-R9 выбирают из группы, состоящей из -Н и необязательно замещенного алкила;
-Y- отсутствует, и -Х- представляет собой -О- или S-; или
-Y- представляет собой -N(Q)CH2-, и Х- представляет собой -О-;
Q выбирают из группы, состоящей из необязательно замещенного алкила, необязательно замещенного арила, необязательно замещенного арилалкила, необязательно замещенного гетероарила и необязательно замещенного гетероарилалкила;
необязательно, -R1 и R2 могут соединяться с образованием 3-8-членного кольца; и
необязательно, оба -R9 вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо;
где -L1- имеет в качестве заместителя -L2-Z или L2-Z’, и где -L1- необязательно дополнительно замещена;
где
-L2- представляет собой одинарную химическую связь или спейсер;
-Z представляет собой растворимый в воде носитель; и
-Z’ представляет собой нерастворимый в воде носитель.
Только в контексте формулы (IV) применяемые термины имеют следующие значения:
Термин "алкил", как применяется в настоящей заявке, включает линейные, разветвленные или циклические насыщенные углеводородные группы, имеющие от 1 до 8 атомов углерода, или в некоторых вариантах выполнения настоящего изобретения от 1 до 6 или от 1 до 4 атомов углерода.
Термин "алкокси" включает алкильные группы, связанные с кислородом, включая метокси, этокси, изопропокси, циклопропокси, циклобутокси и подобное.
Термин "алкенил" включает неароматические ненасыщенные углеводороды с двойными связями углерод-углерод.
Термин "алкинил" включает неароматические ненасыщенные углеводороды с тройными связями углерод-углерод.
Термин "арил" включает ароматические углеводородные группы, имеющие от 6 до 18 атомов углерода, предпочтительно от 6 до 10 атомов углерода, включая группы, такие как фенил, нафтил и антраценил. Термин "гетероарил" включает ароматические кольца, содержащие от 3 до 15 атомов углерода, содержащие по меньшей мере один N, О или S атом, предпочтительно от 3 до 7 атомов углерода, содержащие по меньшей мере один N, О или S атом, включая группы, такие как пирролил, пиридил, пиримидинил, имидазолил, оксазолил, изооксазолил, тиазолил, изотиазолил, хинолил, индолил, инденил и подобное.
В некоторых случаях, алкенильные, алкинильные, арильные или гетероарильные составляющие могут быть соединены с оставшейся частью молекулы через алкиленовую связь. При этих обстоятельствах заместитель будет называться алкенилалкил, алкинилалкил, арилалкил или гетероарилалкил, что указывает на то, что алкиленовая составляющая находится между алкенилом, алкинилом, арилом или гетероарилом и молекулой, с которой связан алкенил, алкинил, арил или гетероарил.
Термин "галоген" включает бром, фтор, хлор и иод.
Термин "гетероциклическое кольцо" относится к 4-8-членному ароматическому или неароматическому кольцу, содержащему от 3 до 7 атомов углерода и по меньшей мере один N, О, или S атом. Примерами являются пиперидинил, пиперазинил, тетрагидропиранил, пирролидин и тетрагидрофуранил, а также примерные группы, приведенные вые для термина "гетероарил".
Когда кольцевая система необязательно замещена, подходящие заместители выбирают из группы, состоящей из алкила, алкенила, алкинила или дополнительного кольца, где каждый необязательно дополнительно замещен. Необязательные заместители в любой группе, включая вышеуказанные, включают гало, нитро, циано, OR, -SR, -NR2, -OCOR, -NRCOR, -COOR, -CONR2, -SOR, -SO2R, -SONR2, -SO2NR2, где каждый R независимо представляет собой алкил, алкенил, алкинил, арил или гетероарил, или две R группы, взятые вместе с атомами, к которым они присоединены, образуют кольцо.
Предпочтительно -L1- формулы (IV) имеет в качестве заместителя одну составляющую -L2-Z или L2-Z’.
Дополнительный предпочтительный вариант -L1- раскрывается в WO 2013/036857 A1, который включен в настоящую заявку в полном объеме посредством ссылки. Соответственно, предпочтительная составляющая -L1- имеет формулу (V):
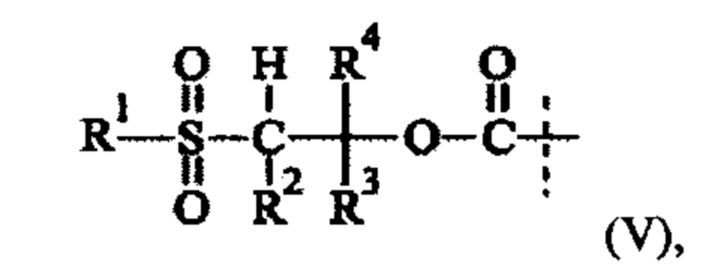
где
пунктирная линия показывает присоединение к -D, которая представляет собой
CNP составляющую, и где присоединение осуществляется через аминную функциональную группу составляющей -D;
-R1 выбирают из группы, состоящей из необязательно замещенного C1-С6 линейного, разветвленного, или циклического алкила; необязательно замещенного арила; необязательно замещенного гетероарила; алкокси; и NR52;
-R2 выбирают из группы, состоящей из -Н; необязательно замещенного C1-С6 алкила; необязательно замещенного арила; и необязательно замещенного гетероарила;
-R3 выбирают из группы, состоящей из -Н; необязательно замещенного C1-С6 алкила; необязательно замещенного арила; и необязательно замещенного гетероарила;
-R4 выбирают из группы, состоящей из -Н; необязательно замещенного C1-C6 алкила; необязательно замещенного арила; и необязательно замещенного гетероарила;
каждый -R5 независимо друг от друга выбирают из группы, состоящей из -Н; необязательно замещенного C1-С6 алкила; необязательно замещенного арила; и необязательно замещенного гетероарила; или взятые вместе два -R5 могут представлять собой циклоалкил или циклогетероалкил;
где -L1- имеет в качестве заместителя -L2-Z или L2-Z’, и где -L1- необязательно дополнительно замещена;
где
-L2- представляет собой одинарную химическую связь или спейсер;
-Z представляет собой растворимый в воде носитель; и
-Z’ представляет собой нерастворимый в воде носитель.
Только в контексте формулы (V) применяемые термины имеют следующие значения:
"Алкил", "алкенил" и "алкинил" включают линейные, разветвленные или циклические углеводородные группы, имеющие от 1 до 8 атомов углерода или 1-6 атомов углерода или 1-4 атомов углерода, где алкилом является насыщенный углеводород, алкенил включает одну или более двойных связей углерод-углерод, и алкинил включает одну или более тройных связей углерод-углерод. Если иного не указано, они содержат 1-6 атомов углерода.
"Арил" включает ароматические углеводородные группы, имеющие от 6 до 18 атомов углерода, предпочтительно 6-10 атомов углерода, включая группы, такие как фенил, нафтил и антрацен. "Гетероарил" включает ароматические кольца, содержащие 3-15 атомов углерода, содержащие по меньшей мере один N, О или S атом, предпочтительно 3-7 атомов углерода, содержащие по меньшей мере один N, О или S атом, включая группы, такие как пирролил, пиридил, пиримидинил, имидазолил, оксазолил, изооксазолил, тиазолил, изотиазолил, хинолил, индолил, инденил и подобное.
Термин "замещенный" означает алкильную, алкенильную, алкинильную, арильную или гетероарильную группу, включающую одну или более групп заместителей вместо одного или более атомов водорода. Заместители могут в общем быть выбраны из галогена, включая F, Cl, Br и I; низшего алкила, включая линейный, разветвленный и циклический; низшего галоалкила, включая фторалкил, хлоралкил, бромалкилииодалкил; ОН; низшего алкокси, включая линейные, разветвленные и циклические; SH; низшего алкилтио, включая линейный, разветвленный и циклический; амино, алкиламино, диалкиламино, силила, включая алкилсилил, алкоксисилил и арилсилил; нитро; циано; карбонила; карбоновой кислоты, сложного эфира карбоновой кислоты, карбоксильного амида, аминокарбонила; аминоацила; карбамата; мочевины; тиокарбамата; тиомочевины; кетона; сульфона; сульфонамида; арила, включая фенил, нафтил и антраценил; гетероарила, включая 5-ти членные гетероарилы, включая пиррол, имидазол, фуран, тиофен, оксазол, тиазол, изоксазол, изотиазол, тиадиазол, триазол, оксадиазол и тетразол, 6-ти членные гетероарилы, включая пиридин, пиримидин, пиразин, и конденсированные гетероарилы, включая бензофуран, бензотиофен, бензоксазол, бензимидазол, индол, бензотиазол, бензизоксазол и бензизотиазол.
Предпочтительно -L1- формулы (V) имеет в качестве заместителя одну составляющую -L2-Z или L2-Z’.
Другой предпочтительный вариант -L1- раскрывается в US 7585837 B2, который включен в настоящую заявку в полном объеме посредством ссылки. Соответственно, предпочтительная составляющая -L1- имеет формулу (VI):
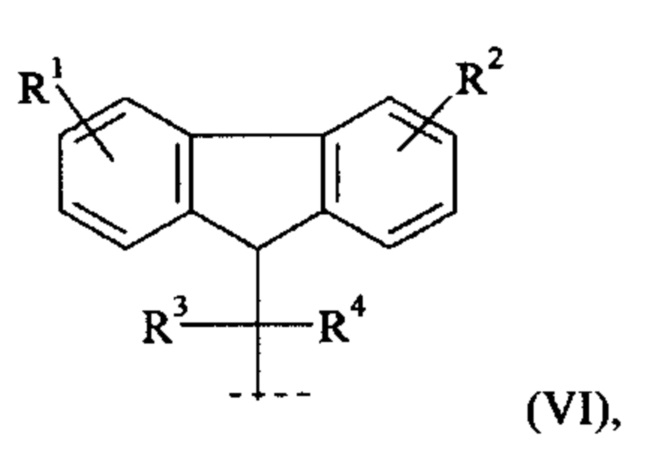
где
пунктирная линия показывает присоединение к -D, которая представляет собой CNP составляющую, и где присоединение осуществляется через аминную функциональную группу составляющей -D;
R1 и R2 независимо выбирают из группы, состоящей из водорода, алкила, алкокси, алкоксиалкила, арила, алкарила, аралкила, галогена, нитро, -SO3H, -SO2NHR5, амино, аммония, карбоксила, РО3Н2 и ОРО3Н2;
R3, R4 и R5 независимо выбирают из группы, состоящей из водорода, алкила и арила;
где -L1- имеет в качестве заместителя -L2-Z или L2-Z’, и где -L1- необязательно дополнительно замещена;
где
-L2- представляет собой одинарную химическую связь или спейсер;
-Z представляет собой растворимый в воде носитель; и
-Z’ представляет собой нерастворимый в воде носитель.
Подходящими заместителями для формулы (VI) являются составляющие алкил (как например C1-6 алкил), алкенил (как например С2-6 алкенил), алкинил (как например С2-6 алкинил), арил (как например фенил), гетероалкил, гетероалкенил, гетероалкинил, гетероарил (как например ароматический 4-7 членный гетероцикл) или галоген.
Только в контексте формулы (VI) применяемые термины имеют следующие значения:
Термины "алкил", "алкокси", "алкоксиалкил", "арил", "алкарил" и "аралкил" означают алкильные радикалы, содержащие 1-8, предпочтительно 1-4 атомов углерода, например, метил, этил, пропил, изопропил и бутил, и арильные радикалы, содержащие 6-10 атомов углерода, например, фенил и нафтил. Термин "галоген" включает бром, фтор, хлор и иод.
Предпочтительно -L1- формулы (VI) имеет в качестве заместителя одну составляющую -L2-Z или L2-Z’.
Другой предпочтительный вариант -L1- раскрывается в WO2002/089789 A1, который включен в настоящую заявку в полном объеме посредством ссылки. Соответственно, предпочтительная составляющая -L1- имеет формулу (VII):
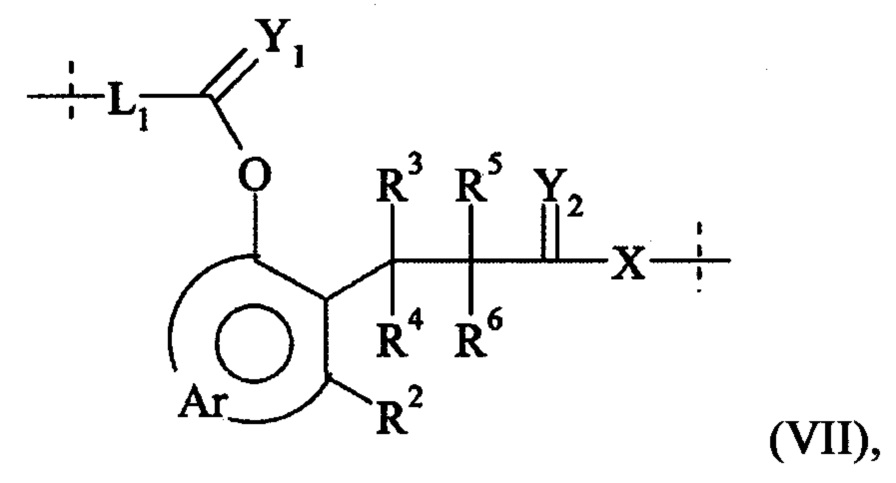
где
пунктирная линия показывает присоединение к -D, которая представляет собой CNP составляющую, и где присоединение осуществляется через аминную функциональную группу составляющей -D;
L1 представляет собой бифункциональную связывающую группу,
Y1 и Y2 независимо представляют собой О, S или NR7;
R2, R3, R4, R5, R6 и R7 независимо выбирают из группы, состоящей из водорода, C1-6 алкилов, С3-12 разветвленных алкилов, С3-8 циклоалкилов, C1-6 замещенных алкилов, С3-8 замещенных циклоалкилов, арилов, замещенных арилов, аралкилов, C1-6 гетероалкилов, замещенных гетероалкилов, C1-6 алкокси, фенокси и C1-6 гетероалкокси;
Ar представляет собой составляющую, которая при включении в формулу (VII), образует мультизамещенный ароматический углеводород или мульти-замещенную гетероциклическую группу;
X представляет собой химическую связь или составляющую, которая активно переносится в клетку-мишень, гидрофобную составляющую или их комбинацию,
у равно 0 или 1;
где -L1- имеет в качестве заместителя -L2-Z или L2-Z’, и где -L1- необязательно дополнительно замещена;
где
-L2- представляет собой одинарную химическую связь или спейсер;
-Z представляет собой растворимый в воде носитель; и
-Z’ представляет собой нерастворимый в воде носитель.
Только в контексте формулы (VII) применяемые термины имеют следующие значения:
Термин "алкил", как следует понимать, включает, например, неразветвленные, разветвленные, замещенные С1-12 алкилы, включая алкокси, С3-8 циклоалкилы или замещенные циклоалкилы, и т.д.
Термин "замещение", как следует понимать, включает добавление или замещение одного или более атомов, содержащихся в функциональной группе, или соединения с одним или более отличными атомами.
Замещенные алкилы включают карбоксиалкилы, аминоалкилы, диалкиламины, гидроксиалкилы и меркаптоалкилы; замещенные циклоалкилы включают составляющие, как например 4-хлорциклогексил; арилы включают составляющие, как например нафтил; замещенные арилы включают составляющие, как например 3-бром-фенил; аралкилы включают составляющие, как например толуил; гетероалкилы включают составляющие, как например этилтиофен; замещенный гетероалкилы включают составляющие, как например 3-метокситиофен; алкокси включает составляющие, как например метокси; и фенокси включает составляющие, как например 3-нитрофенокси. Гало-, как необходимо понимать, включает фтор, хлор, иод и бром.
Предпочтительно -L1- формулы (VII) имеет в качестве заместителя одну составляющую -L2-Z или L2-Z’.
В другом предпочтительном варианте выполнения настоящего изобретения -L1 -содержит подструктуру формулы (VIII)
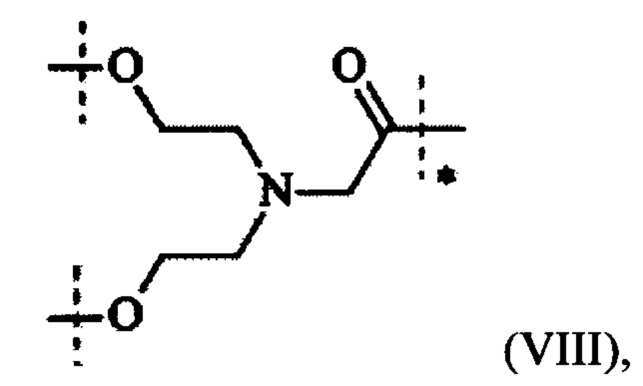
где
пунктирная линия, отмеченная звездочкой, обозначает присоединение к атому азота составляющей- D, которая представляет собой CNP составляющую, путем образования амидной связи;
непомеченные пунктирные линии показывают присоединение к оставшейся части -L1-; и
где -L1- имеет в качестве заместителя -L2-Z или L2-Z’, и где -L1- необязательно дополнительно замещена;
где
-L2- представляет собой одинарную химическую связь или спейсер;
-Z представляет собой растворимый в воде носитель; и
-Z’ представляет собой нерастворимый в воде носитель.
Предпочтительно -L1- формулы (VIII) имеет в качестве заместителя одну составляющую -L2-Z или L2-Z’.
В одном варианте выполнения настоящего изобретения -L1- формулы (VIII) дополнительно не замещена.
В другом предпочтительном варианте выполнения настоящего изобретения -L1- содержит подструктуру формулы (IX)
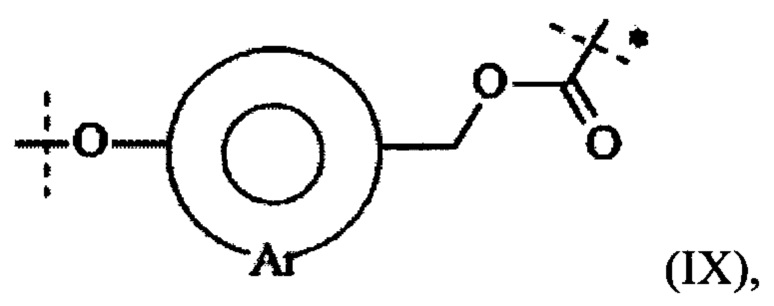
где
пунктирная линия, отмеченная звездочкой, обозначает присоединение к атому азота составляющей- D, которая представляет собой CNP составляющую, путем образования карбаматной связи;
непомеченные пунктирные линии показывают присоединение к оставшейся части -L1-; и
где -L1- имеет в качестве заместителя -L2-Z или L2-Z’, и где -L1- необязательно дополнительно замещена;
где
-L2- представляет собой одинарную химическую связь или спейсер;
-Z представляет собой растворимый в воде носитель; и
-Z’ представляет собой нерастворимый в воде носитель.
Предпочтительно -L1- формулы (IX) имеет в качестве заместителя одну составляющую -L2-Z или L2-Z’.
В одном варианте выполнения настоящего изобретения -L1- формулы (IX) дополнительно не замещена.
Составляющая -L1- может быть соединена с -D через любую функциональную группу составляющей -D и предпочтительно соединена с -D через аминную функциональную группу -D. Это может быть N-терминальная аминная функциональная группа или аминная функциональная группа, обеспеченная боковой цепью лизина, т.е. лизином в положении 4 или 10, если CNP имеет последовательность SEQ ID NO: 1; лизинами в положении 7, 9, 13, 14, 18 и 24, если CNP имеет последовательность SEQ ID NO: 38; лизинами в положении 8, 10, 14, 15, 19 или 25, если CNP имеет последовательность SEQ ID NO: 25; лизинами в положении 9, 11, 15, 16, 20 и 26, если CNP имеет последовательность SEQ ID NO: 24; и лизинами в положении 10, 12, 16, 17, 21 и 27, если CNP составляющая имеет последовательность SEQ ID NO: 23.
В одном варианте выполнения настоящего изобретения CNP составляющая соединена с -L1- через N-терминальную аминную функциональную группу CNP составляющей.
В другом варианте выполнения настоящего изобретения CNP составляющая соединена с -L1- через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 4, если CNP составляющая имеет последовательность SEQ ID NO: 1.
В другом варианте выполнения настоящего изобретения CNP составляющая соединена с -L1- через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 10, если CNP составляющая имеет последовательность SEQ ID NO: 1.
В другом варианте выполнения настоящего изобретения CNP составляющая соединена с -L1- через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 8, если CNP составляющая имеет последовательность SEQ ID NO: 25.
В другом варианте выполнения настоящего изобретения CNP составляющая соединена с -L1- через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 10, если CNP составляющая имеет последовательность SEQ ID NO: 25.
В другом варианте выполнения настоящего изобретения CNP составляющая соединена с -L1- через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 14, если CNP составляющая имеет последовательность SEQ ID NO: 25.
В другом варианте выполнения настоящего изобретения CNP составляющая соединена с -L1- через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 15, если CNP составляющая имеет последовательность SEQ ID NO: 25.
В другом варианте выполнения настоящего изобретения CNP составляющая соединена с -L1- через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 19, если CNP составляющая имеет последовательность SEQ ID NO: 25.
В другом варианте выполнения настоящего изобретения CNP составляющая соединена с -L1- через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 25, если CNP составляющая имеет последовательность SEQ ID NO: 25.
В другом варианте выполнения настоящего изобретения CNP составляющая соединена с -L1- через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 9, если CNP составляющая имеет последовательность SEQ ID NO: 24.
В другом варианте выполнения настоящего изобретения CNP составляющая соединена с -L1- через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 11, если CNP составляющая имеет последовательность SEQ ID NO: 24.
В другом варианте выполнения настоящего изобретения CNP составляющая соединена с -L1- через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 15, если CNP составляющая имеет последовательность SEQ ID NO: 24.
В другом варианте выполнения настоящего изобретения CNP составляющая соединена с -L1- через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 16, если CNP составляющая имеет последовательность SEQ ID NO: 24.
В другом варианте выполнения настоящего изобретения CNP составляющая соединена с -L1- через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 20, если CNP составляющая имеет последовательность SEQ ID NO: 24.
В другом варианте выполнения настоящего изобретения CNP составляющая соединена с -L1- через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 26, если CNP составляющая имеет последовательность SEQ ID NO: 24.
Наиболее предпочтительно CNP составляющая имеет последовательность SEQ ID NO: 24 и соединена с -L1- через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 26.
Неожиданно было обнаружено, что присоединение -L1- к кольцу CNP значительно уменьшает аффинность пролекарства CNP к NPR-B по сравнению с присоединением при N-конце или к некольцевой части CNP, где уменьшенная аффинность к NPR-B в свою очередь снижает риск сердечнососудистых побочных эффектов, таких как гипотония.
Соответственно, -L1- предпочтительно конъюгирована с боковой цепью аминокислотного остатка указанной кольцевого фрагмента составляющей -D или с основной цепью указанной кольцевого фрагмента составляющей -D. Даже более предпочтительно, -L1- ковалентно и обратимо конъюгирована с боковой цепью аминокислотного остатка указанной кольцевого фрагмента составляющей -D.
Указанный аминокислотный остаток, локализованный в кольцевой составляющей -D, предпочтительно представляет собой любую аминокислоту, имеющую функциональную группу.
Предпочтительно, остаток аминокислоты -D, с которой -L1- конъюгирован, содержит функциональную группу, выбранную из группы, состоящей из карбоновой кислоты, первичного и вторичного амина, малеимида, тиола, сульфоновой кислоты, карбоната, карбамата, гидроксила, альдегида, кетона, гидразина, изоцианата, изотиоцианата, фосфорной кислоты, фосфоновой кислоты, галоацетила, алкилгалогенида, акрилоила, арилфторида, гидроксиламина, сульфата, дисульфида, винилсульфона, винилкетона, диазоалкана, оксирана, гуанидина и азиридина. Наиболее предпочтительно остаток аминокислоты -D, с которой -L1- конъюгирован, содержит функциональную группу, выбранную из группы, состоящей из гидроксила, первичного и вторичного амина и гуанидина.
Составляющая -L1- может быть соединена с -D через любой тип связи, при условии, что она является обратимой. Предпочтительно, -L1- соединена с -D через связь, выбранную из группы, состоящей из амида, сложного эфира, карбамата, ацеталя, аминаля, имина, оксима, гидразона, дисульфида и ацилгуанидина. Даже более предпочтительно -L1- соединена с -D через связь, выбранную из группы, состоящей из амида, сложного эфира, карбамата и ацилгуанидина.
В одном варианте выполнения настоящего изобретения -L1- соединена с -D через простоэфирную связь.
В другом варианте выполнения настоящего изобретения -L1- соединена с -D через карбаматную связь.
В другом варианте выполнения настоящего изобретения -L1- соединена с -D через ацилгуанидиновую связь.
В предпочтительном варианте выполнения настоящего изобретения -L1- соединена с -D через амидную связь.
Остаток аминокислоты -D, с которой -L1- конъюгирована, выбирают из группы, состоящей из протеогенных аминокислотных остатков и непротеогенных аминокислотных остатков.
В одном варианте выполнения настоящего изобретения остаток аминокислоты -D, с которой -L1- конъюгирована, представляет собой непротеогенную аминокислоту.
В предпочтительном варианте выполнения настоящего изобретения остаток аминокислоты -D, с которой -L1- конъюгирована, представляет собой протеогенную аминокислоту. Даже более предпочтительно указанная аминокислота выбирают из группы, состоящей из гистидина, лизина, триптофана, серина, треонина, тирозина, аспарагиновой кислоты, глутаминовой кислоты и аргинина. Даже более предпочтительно указанная аминокислота выбирают из группы, состоящей из лизина, аспарагиновой кислоты, аргинина и серина. Даже более предпочтительно указанная аминокислота выбирают из группы, состоящей из лизина, аргинина и серина.
В одном варианте выполнения настоящего изобретения остаток аминокислоты -D, с которой -L1- конъюгирована, представляет собой гистидин. Понятно, что такой гистидин не встречается в последовательности SEQ ID NO: 96 и что он может присутствовать только в ее вариантах, аналогах, ортологах, гомологах и производных.
В одном варианте выполнения настоящего изобретения остаток аминокислоты -D, с которой -L1- конъюгирована, представляет собой триптофан. Понятно, что такой триптофан не встречается в последовательности SEQ ID NO: 96 и что он может присутствовать только в ее вариантах, аналогах, ортологах, гомологах и производных.
В одном варианте выполнения настоящего изобретения остаток аминокислоты -D, с которой -L1- конъюгирована, представляет собой треонин. Понятно, что такой треонин не встречается в последовательности SEQ ID NO: 96 и что он может присутствовать только в ее вариантах, аналогах, ортологах, гомологах и производных.
В одном варианте выполнения настоящего изобретения остаток аминокислоты -D, с которой -L1- конъюгирована, представляет собой тирозин. Понятно, что такой тирозин не встречается в последовательности SEQ ID NO: 96 и что он может присутствовать только в ее вариантах, аналогах, ортологах, гомологах и производных.
В одном варианте выполнения настоящего изобретения остаток аминокислоты -D, с которой -L1- конъюгирована, представляет собой глутаминовую кислоту. Понятно, что такая глутаминовая кислота не встречается в последовательности SEQ ID NO: 96 и что он может присутствовать только в ее вариантах, аналогах, ортологах, гомологах и производных.
В одном варианте выполнения настоящего изобретения остаток аминокислоты -D, с которой -L1- конъюгирована, представляет собой лизин. Предпочтительно, указанной аминокислотой является лизин в положении 4 последовательности SEQ ID NO: 96, который соответствует лизину в положении 26 последовательности SEQ ID NO: 24.
В другом варианте выполнения настоящего изобретения остаток аминокислоты -D, с которой -L1- конъюгирована, представляет собой аспарагиновую кислоту.
Предпочтительно, указанной аминокислотой является аспарагиновая кислота в положении 6 последовательности SEQ ID NO: 96, которая соответствует аспарагиновой кислоте в положении 28 последовательности SEQ ID NO: 24.
В другом варианте выполнения настоящего изобретения остаток аминокислоты -D, с которой -L1- конъюгирована, представляет собой аргинин. Предпочтительно, указанной аминокислотой является аргинин в положении 7 последовательности SEQ ID NO: 96, который соответствует аргинину в положении 29 последовательности SEQ ID NO: 24.
В другом варианте выполнения настоящего изобретения остаток аминокислоты -D, с которой -L1- конъюгирован, является серии. Предпочтительно, указанной аминокислотой является серии в положении 10 или 12 последовательности SEQ ID NO: 96. В одном варианте выполнения настоящего изобретения указанной аминокислотой является серии в положении 10 последовательности SEQ ID NO: 96, который соответствует серину в положении 32 последовательности SEQ ID NO: 24. В другом варианте выполнения настоящего изобретения указанной аминокислотой является серии в положении 12 последовательности SEQ ID NO: 96, который соответствует серину в положении 34 последовательности SEQ ID NO: 24.
В предпочтительном варианте выполнения настоящего изобретения остаток аминокислоты -D, с которой -L1- конъюгирована, представляет собой лизин. Наиболее предпочтительно, -D имеет последовательность SEQ ID NO: 24, и L1- конъюгирован с лизином в положении 26.
Также неожиданно было обнаружено, что увеличение длины CNP последовательности является предпочтительным с точки зрения NEP-стабильности: CNP-22 был более восприимчивым в отношении NEP-разложения, чем CNP-34, который в свою очередь был восприимчивым, чем CNP-38.
В пролекарствах согласно настоящему изобретению -L2- представляет собой химическую связь или спейсерную составляющую.
В одном варианте выполнения настоящего изобретения -L2- представляет собой химическую связь.
В другом варианте выполнения настоящего изобретения -L2- представляет собой спейсерную составляющую.
Когда -L2- отлична от одинарной химической связи, -L2- предпочтительно выбирают из группы, состоящей из -Т-, -С(O)O-, -О-, -С(О)-, -C(O)N(Ry1)-, -S(O)2N(Ry1)-, -S(O)N(Ry1)-, -S(O)2-, -S(O)-, -N(Ry1)S(O)2N(Ry1a)-, -S-, -N(Ry1)-, -OC(ORy1)(Ry1a)-, -N(Ry1)C(O)N(Ry1a)-, -OC(O)N(Ry1)-, С1-50 алкила, C2-50 алкенила и C2-50 алкинила; где -T-, С1-50 алкил, C2-50 алкенил и C2-50 алкинил необязательно замещены одним или более заместителями -Ry2, которые являются одинаковыми или различными, и где C1-50 алкил, C2-50 алкенил и C2-50 алкинил необязательно прерваны одной или более группами, выбранными из группы, состоящей из -Т-, -С(O)O-, -О-, -С(О)-, -C(O)N(Ry3)-, -S(O)2N(Ry3)-, -S(O)N(Ry3)-, -S(O)2-, -S(O)-, -N(Ry3)S(O)2N(Ry3a)-, -S-, -N(Ry3)-, -OC(ORy3)(Ry3a)-, -N(Ry3)C(O)N(Ry3a)- и -OC(O)N(Ry3)-;
-Ry1 и Ry1a независимо друг от друга выбирают из группы, состоящей из -Н, -Т, С1-50 алкила, С2-50 алкенила и С2-50 алкинила; где -Т, С1-50 алкил, C2-50 алкенил и С2-50 алкинил необязательно замещены одним или более заместителями -Ry2, которые являются одинаковыми или различными, и где С1-50 алкил, C2-50 алкенил и С2-50 алкинил необязательно прерваны одной или более группами, выбранными из группы, состоящей из -Т-, -С(O)O-, -О-, -С(О)-, -C(O)N(Ry4)-, -S(O)2N(Ry4)-, -S(O)N(Ry4)-, -S(O)2-, -S(O)-, -N(Ry4)S(O)2N(Ry4a)-, -S-, -N(Ry4)-, -OC(ORy4)(Ry4a)-, -N(Ry4)C(O)N(Ry4a)- и -OC(O)N(Ry4)-;
каждый T независимо выбирают из группы, состоящей из фенила, нафтила, инденила, инданила, тетралинила, С3-10 циклоалкила, 3-10-членного гетероциклила, 8-11-членного гетеробициклила, 8-30-членного карбополициклила и 8-30-членный гетерополициклила; где каждый Т независимо необязательно замещен одним или более заместителями -Ry2, которые являются одинаковыми или различными;
каждый -Ry2 независимо выбирают из группы, состоящей из галогена, -CN, оксо (=O), -COORy5, -ORy5, -C(O)Ry5, -C(O)N(Ry5Ry5a), -S(O)2N(Ry5Ry5a), -S(O)N(Ry5Ry5a), -S(O)2Ry5, -S(O)Ry5, -N(Ry5)S(O)2N(Ry5aRy5b), -SRy5, -N(Ry5Ry5a), -NO2, -OC(O)Ry5, -N(Ry5)C(O)Ry5a, -N(Ry5)S(O)2Ry5a, -N(Ry5)S(O)Ry5a, -N(Ry5)C(O)ORy5a, -N(Ry5)C(O)N(Ry5aRy5b), -OC(O)N(Ry5Ry5a) и C1-6 алкила; где C1-6 алкил необязательно замещен одним или более заместителями галоген, которые являются одинаковыми или различными; и
каждый -Ry3, -Ry3a, -Ry4, -Ry4a, -Ry5, -Ry5a и Ry5b независимо выбирают из группы, состоящей из -Н и C1-6 алкила, где C1-6 алкил необязательно замещен одним или более заместителями галоген, которые являются одинаковыми или различными.
Когда -L2- отлична от одинарной химической связи, -L2- даже более предпочтительно выбирают из -Т-, -С(O)O-, -О-, -С(О)-, -C(O)N(Ry1)-, -S(O)2N(Ry1)-, -S(O)N(Ry1)-, -S(O)2-, -S(O)-, -N(Ry1)S(O)2N(Ry1a)-, -S-, -N(Ry1)-, -OC(ORy1)(Ry1a)-, -N(Ry1)C(O)N(Ry1a)-, -OC(O)N(Ry1)-, C1-50 алкила, C2-50 алкенила и C2-50 алкинила; где -T-, C1-20 алкил, C2-20 алкенил и C2-20 алкинил необязательно замещены одним или более заместителями -Ry2, которые являются одинаковыми или различными, и где С1-20 алкил, C2-20 алкенил и C2-20 алкинил необязательно прерваны одной или более группами, выбранными из группы, состоящей из -Т-, -С(O)O-, -О-, -С(О)-, -C(O)N(Ry3)-, -S(O)2N(Ry3)-, -S(O)N(Ry3)-, -S(O)2-, -S(O)-, -N(Ry3)S(O)2N(Ry3a)-, -S-, -N(Ry3)-, -OC(ORy3)(Ry3a)-, -N(Ry3)C(O)N(Ry3a)- и -OC(O)N(Ry3)-;
-Ry1 и Ry1a независимо друг от друга выбирают из группы, состоящей из -Н, -Т, С1-10 алкила, С2-10 алкенила и С2-10 алкинила; где -Т, С1-10 алкил, С2-10 алкенил и С2-10 алкинил необязательно замещены одним или более заместителями -Ry2, которые являются одинаковыми или различными, и где С1-10 алкил, С2-10 алкенил и С2-10 алкинил необязательно прерваны одной или более группами, выбранными из группы, состоящей из -Т-, -С(O)O-, -О-, -С(О)-, -C(O)N(Ry4)-, -S(O)2N(Ry4)-, -S(O)N(Ry4)-, -S(O)2-, -S(O)-, -N(Ry4)S(O)2N(Ry4a)-, -S-, -N(Ry4)-, -OC(ORy4)(Ry4a)-, -N(Ry4)C(O)N(Ry4a)- и -OC(O)N(Ry4)-;
каждый Т независимо выбирают из группы, состоящей из фенила, нафтила, инденила, инданила, тетралинила, С3-10 циклоалкила, 3-10-членного гетероциклила, 8-11-членного гетеробициклила, 8-30-членного карбополициклила и 8-30-членного гетерополициклила; где каждый Т независимо необязательно замещен одним или более заместителями -Ry2, которые являются одинаковыми или различными;
-Ry2 выбирают из группы, состоящей из галогена, -CN, оксо (=O), -COORy5, -ORy5, -C(O)Ry5, -C(O)N(Ry5Ry5a), -S(O)2N(Ry5Ry5a), -S(O)N(Ry5Ry5a), -S(O)2Ry5, -S(O)Ry5, -N(Ry5)S(O)2N(Ry5aRy5b), -SRy5, -N(Ry5Ry5a), -NO2, -OC(O)Ry5, -N(Ry5)C(O)Ry5a, -N(Ry5)S(O)2Ry5a, -N(Ry5)S(O)Ry5a, -N(Ry5)C(O)ORy5a, -N(Ry5)C(O)N(Ry5aRy5b), -OC(O)N(Ry5Ry5a) и C1-6 алкила; где C1-6 алкил необязательно замещен одним или более заместителями галоген, которые являются одинаковыми или различными; и
каждый -Ry3, -Ry3a, -Ry4, -Ry4a, -Ry5, -Ry5a и Ry5b независимо друг от друга выбирают из группы, состоящей из -Н и C1-6 алкила; где C1-6 алкил необязательно замещен одним или более заместителями галоген, которые являются одинаковыми или различными.
Когда -L2- отлична от одинарной химической связи, -L2- даже более предпочтительно выбирают из группы, состоящей из -Т-, -С(O)O-, -О-, -С(О)-, -C(O)N(Ry1)-, -S(O)2N(Ry1)-, -S(O)N(Ry1)-, -S(O)2-, -S(O)-, -N(Ry1)S(O)2N(Ry1a)-, -S-, -N(Ry1)-, -OC(ORy1)(Ry1a)-, -N(Ry1)C(O)N(Ry1a)-, -OC(O)N(Ry1)-, C1-50 алкила, C2-50 алкенила и C2-50 алкинила; где -T-, C1-50 алкил, C2-50 алкенил и C2-50 алкинил необязательно замещены одним или более заместителями -Ry2, которые являются одинаковыми или различными, и где С1-50 алкил, C2-50 алкенил и C2-50 алкинил необязательно прерваны одной или более группами, выбранными из группы, состоящей из -Т-, -С(O)O-, -О-, -С(О)-, -C(O)N(Ry3)-, -S(O)2N(Ry3)-, -S(O)N(Ry3)-, -S(O)2-, -S(O)-, -N(Ry3)S(O)2N(Ry3a)-, -S-, -N(Ry3)-, -OC(ORy3)(Ry3a)-, -N(Ry3)C(O)N(Ry3a)- и -OC(O)N(Ry3)-;
-Ry1 и Ry1a независимо выбирают из группы, состоящей из -Н, -Т, С1-10 алкила, С2-10 алкенила и С2-10 алкинила;
каждый Т независимо выбирают из группы, состоящей из фенила, нафтила, инденила, инданила, тетралинила, С3-10 циклоалкила, 3-10-членного гетероциклила, 8-11-членного гетеробициклила, 8-30-членного карбополициклила и 8-30-членного гетерополициклила;
каждый -Ry2 независимо выбирают из группы, состоящей из галогена и C1-6 алкила; и
каждый -Ry3, -Ry3a, -Ry4, -Ry4a, -Ry5, -Ry5a и Ry5b независимо друг от друга выбирают из группы, состоящей из -Н и C1-6 алкила; где C1-6 алкил необязательно замещен одним или более заместителями галоген, которые являются одинаковыми или различными.
Даже более предпочтительно, -L2- представляет собой С1-20 алкильную цепь, которая необязательно прервана одной или более группами, независимо выбранными из -О-, -Т- и -C(O)N(Ry1)-; и где С1-20 алкильная цепь необязательно замещена одной или более группами, независимо выбранными из -ОН, -Т и C(O)N(Ry6Ry6a); где -Ry1, -Ry6, -Ry6a независимо выбирают из группы, состоящей из Н и См алкила, и где Т выбирают из группы, состоящей из фенила, нафтила, инденила, инданила, тетралинила, С3-10 циклоалкила, 3-10-членного гетероциклила, 8-11-членного гетеробициклила, 8-30-членного карбополициклила и 8-30-членного гетерополициклила.
Предпочтительно, -L2- имеет молекулярную массу в интервале от 14 г/моль до 750 г/моль.
Предпочтительно, -L2- содержит составляющую, выбранную из
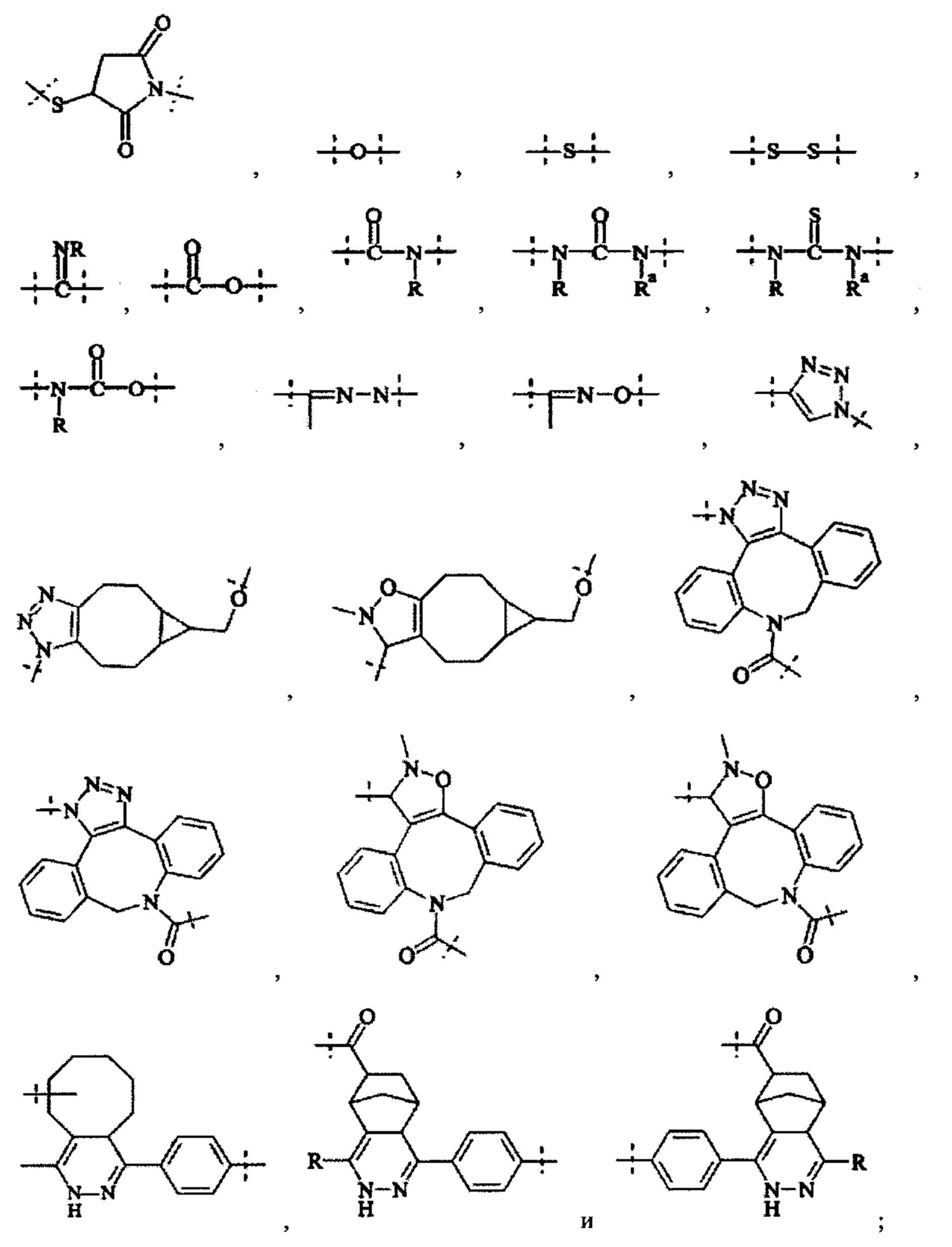
где
пунктирные линии обозначают присоединение к остальной части -L2-, -L1-, -Z и/или -Z', соответственно; и
-R и Ra независимо друг от друга выбирают из группы, состоящей из -Н, метила, этила, пропила, бутила, пентила и гексила.
В одном предпочтительном варианте выполнения настоящего изобретения -L2- имеет длину цепи от 1 до 20 атомов.
Как применяется в настоящей заявке термин "длина цепи" в отношении составляющей -L2- относится к числу атомов -L2-, присутствующих в самом коротком соединении между -L1- и Z.
Предпочтительно, -L2- имеет формулу (i)
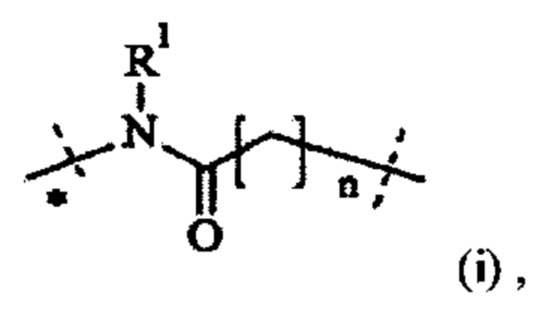
где
пунктирная линия, отмеченная звездочкой, обозначает присоединение к -L1-;
непомеченная пунктирная линия обозначает присоединение к -Z или Z';
-R1 выбирают из группы, состоящей из -Н, C1-6 алкила, С2-6 алкенила и С2-6 алкинила;
n выбирают из группы, состоящей из 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17 и 18; и
где составляющая формулы (i) необязательно дополнительно замещена.
Предпочтительно -R1 формулы (i) выбирают из группы, состоящей из -Н, метила, этила, пропила и бутила. Даже более предпочтительно -R1 формулы (i) выбирают из группы, состоящей из -Н, метила, этила и пропила. Даже более предпочтительно -R1 формулы (i) выбирают из группы, состоящей из -Н и метила. Наиболее предпочтительно -R1 формулы (i) представляет собой метил.
Предпочтительно n формулы (i) выбирают из группы, состоящей из 0, 1, 2, 3, 4, 5, 6, 7, 8, 9 и 10. Даже более предпочтительно n формулы (i) выбирают из группы, состоящей из 0, 1, 2, 3, 4 и 5. Даже более предпочтительно n формулы (i) выбирают из группы, состоящей из 0, 1, 2 и 3. Даже более предпочтительно n формулы (i) выбирают из группы, состоящей из 0 и 1. Наиболее предпочтительно n формулы (i) равно 0.
В одном предпочтительном варианте выполнения настоящего изобретения -L2-представляет собой составляющую, выбранную из группы, состоящей из
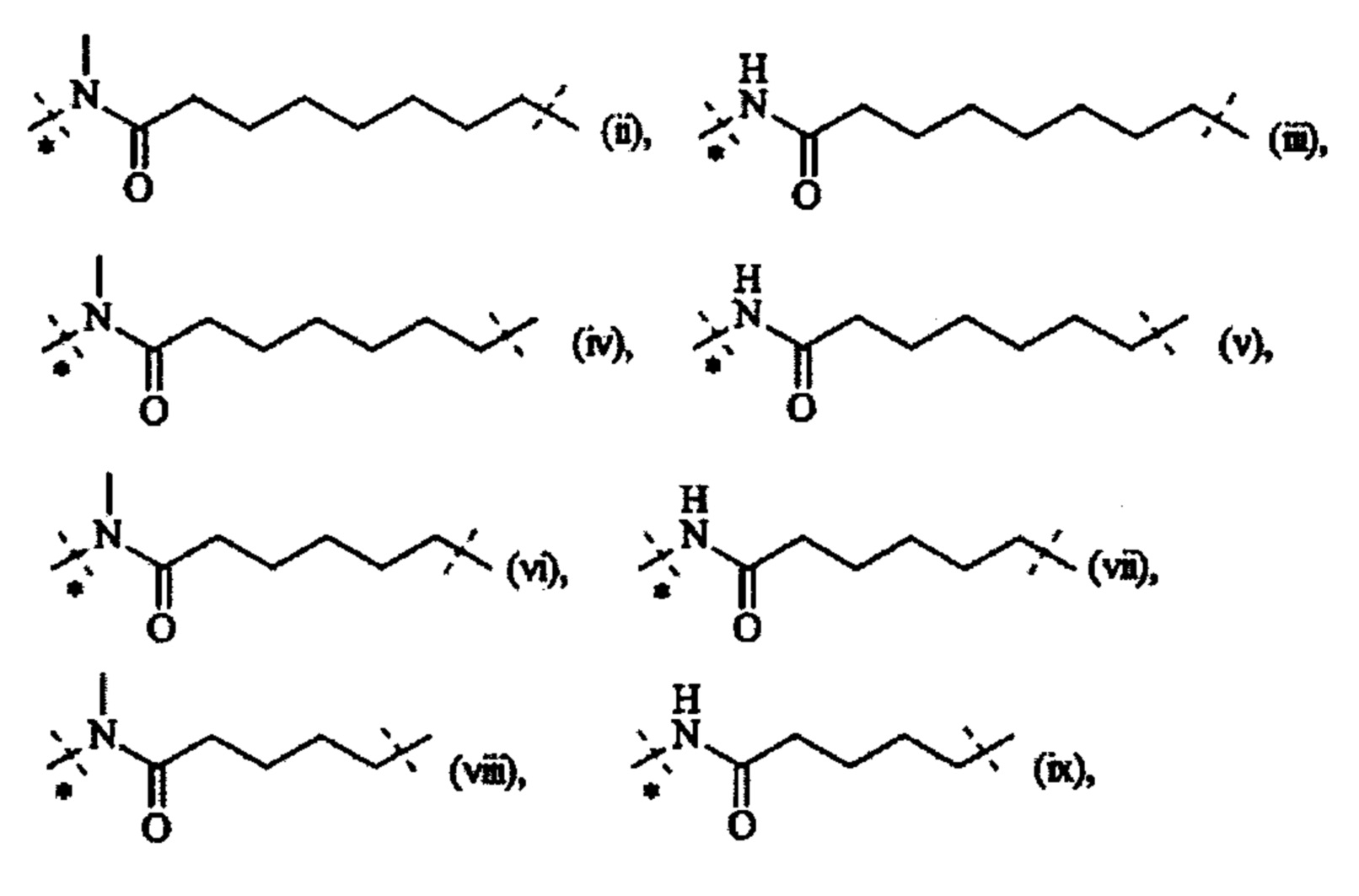
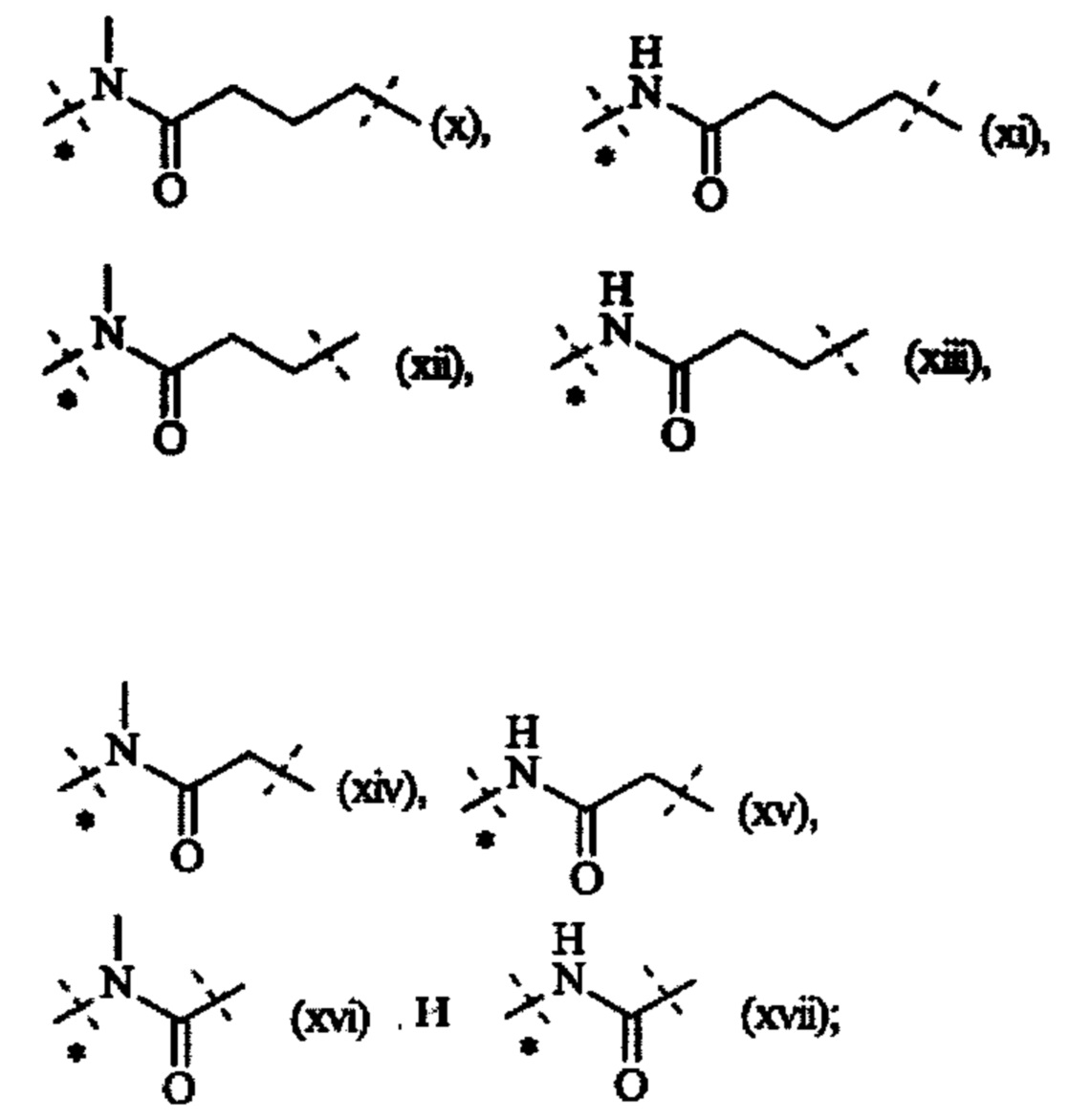
где
пунктирная линия, отмеченная звездочкой, обозначает присоединение к -L1-;
непомеченная пунктирная линия обозначает присоединение к -Z или Z'; и
где составляющие (ii), (iii), (iv), (v), (vi), (vii), (viii), (ix), (x), (xi), (xii), (xiii), (xiv), (xv), (xvi) и (xvii) необязательно дополнительно замещены.
В предпочтительном варианте выполнения настоящего изобретения -L2- выбирают из группы, состоящей из
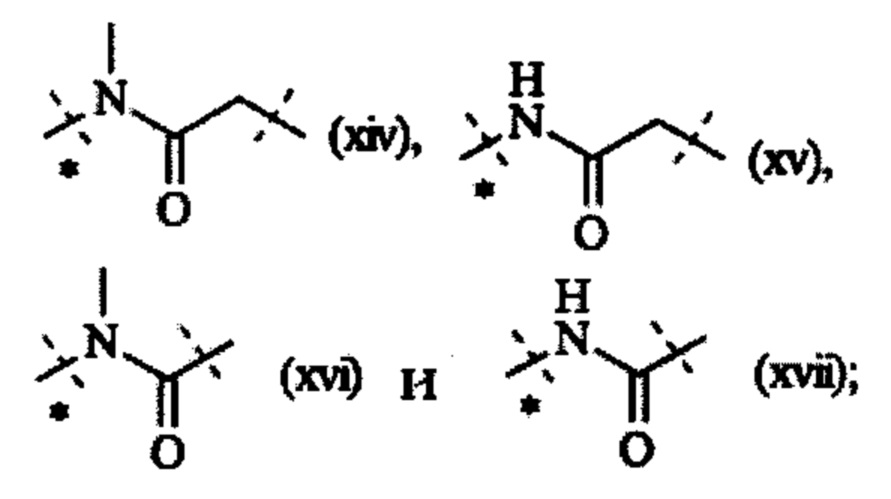
где
пунктирная линия, отмеченная звездочкой, обозначает присоединение к -L1-; и непомеченная пунктирная линия обозначает присоединение к -Z или Z'.
Даже более предпочтительно -L2- выбирают из группы, состоящей из
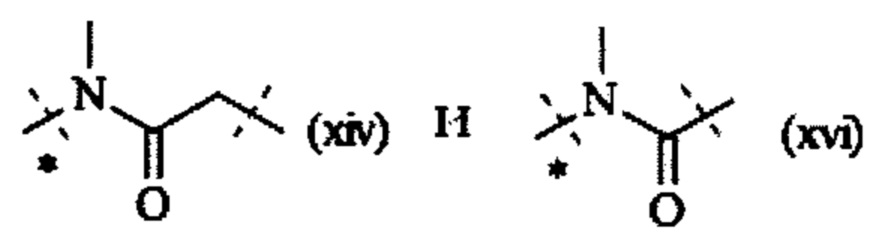
где
пунктирная линия, отмеченная звездочкой, обозначает присоединение к -L1-; и
непомеченная пунктирная линия обозначает присоединение к -Z или Z'.
Даже более предпочтительно -L2- представляет собой

где
пунктирная линия, отмеченная звездочкой, обозначает присоединение к -L1-; и
непомеченная пунктирная линия обозначает присоединение к -Z или Z'.
В одном предпочтительном варианте выполнения настоящего изобретения составляющая -L1-L2- выбирают из группы, состоящей из
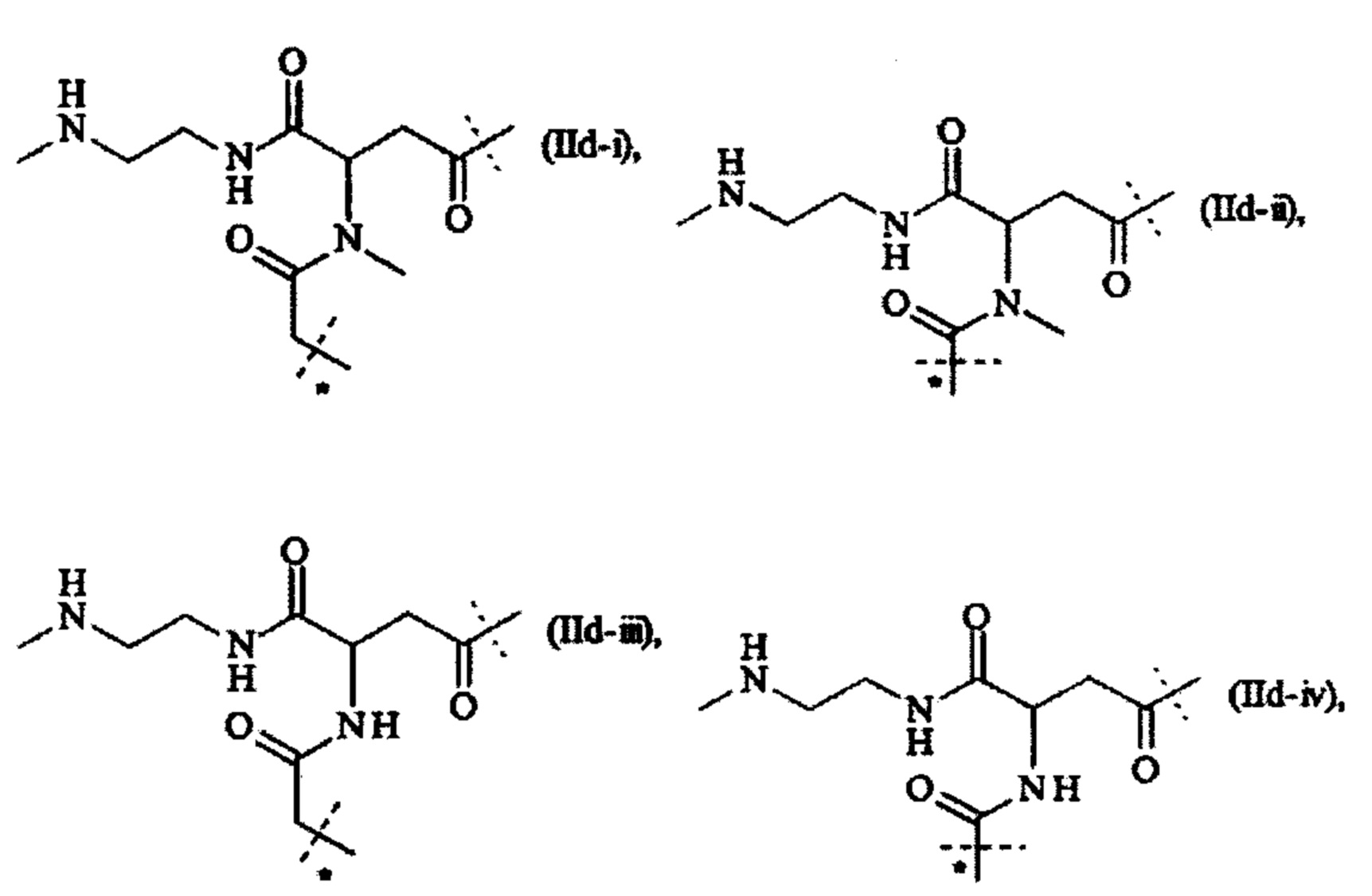
где
неотмеченная пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой CNP составляющую, путем образования амидной связи; и
пунктирная линия, отмеченная звездочкой, обозначает присоединение к -Z или -Z’.
В даже более предпочтительном варианте выполнения настоящего изобретения составляющая -L1-L2- представляет собой
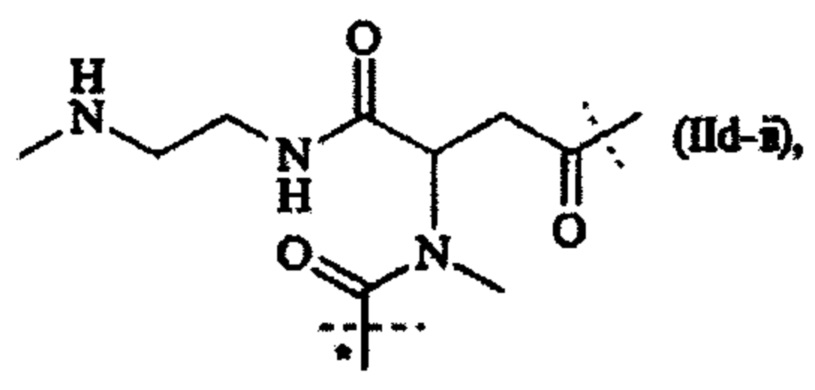
где
неотмеченная пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой CNP составляющую, путем образования амидной связи; и
пунктирная линия, отмеченная звездочкой, обозначает присоединение к -Z или -Z’.
В наиболее предпочтительном варианте выполнения настоящего изобретения составляющая -L1-L2- имеет формулу (IId-ii’)
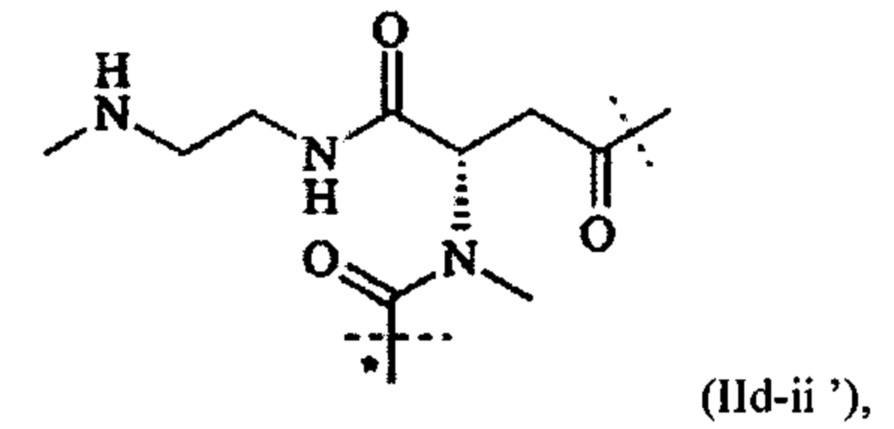
где
неотмеченная пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой CNP составляющую, путем образования амидной связи; и
пунктирная линия, отмеченная звездочкой, обозначает присоединение к -Z или -Z’.
В другом предпочтительном варианте выполнения настоящего изобретения составляющая -L1-L2- выбирают из группы, состоящей из
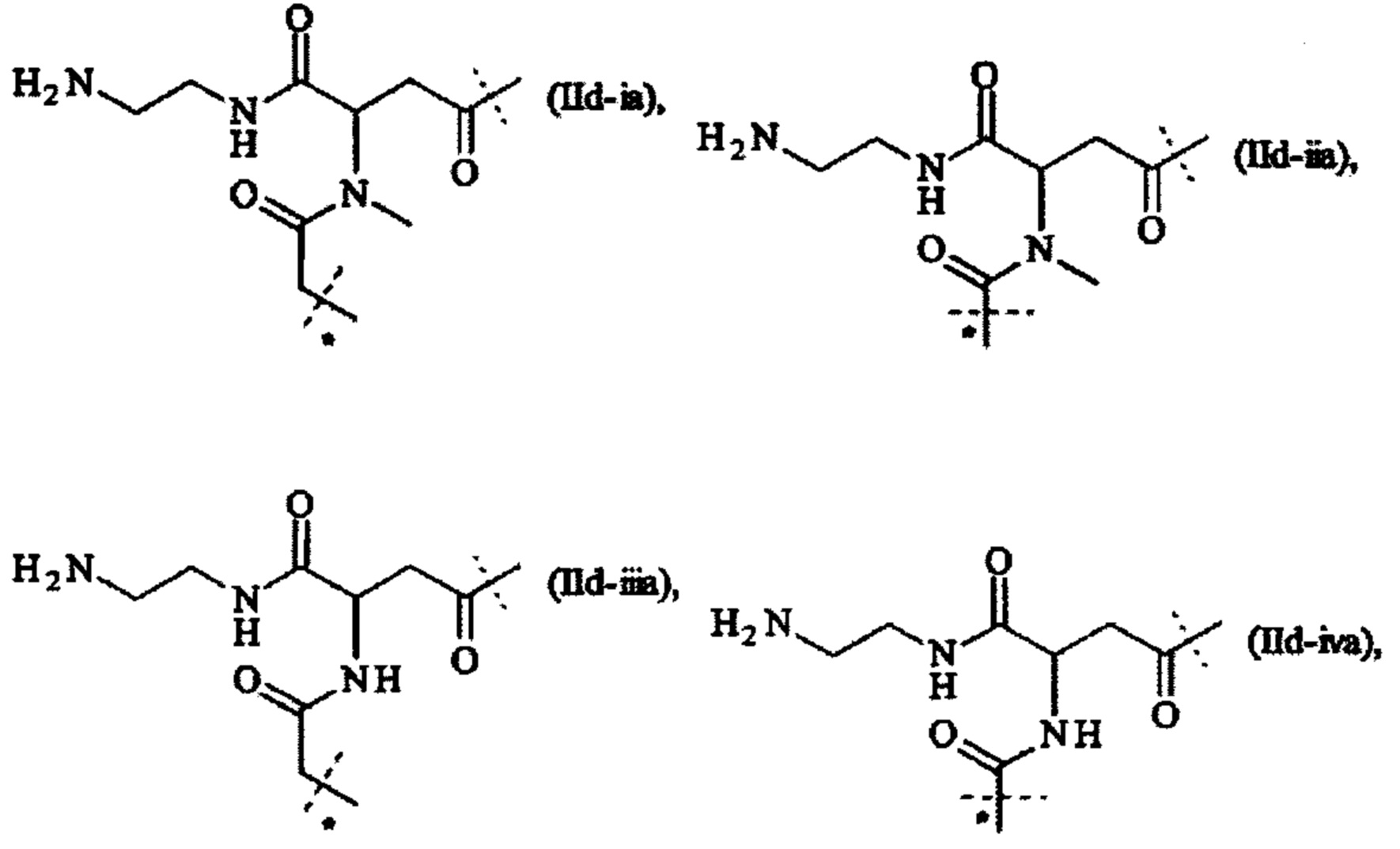
где
неотмеченная пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой CNP составляющую, путем образования амидной связи; и
пунктирная линия, отмеченная звездочкой, обозначает присоединение к -Z или -Z’.
В даже более предпочтительном варианте выполнения настоящего изобретения составляющая -L1-L2- представляет собой
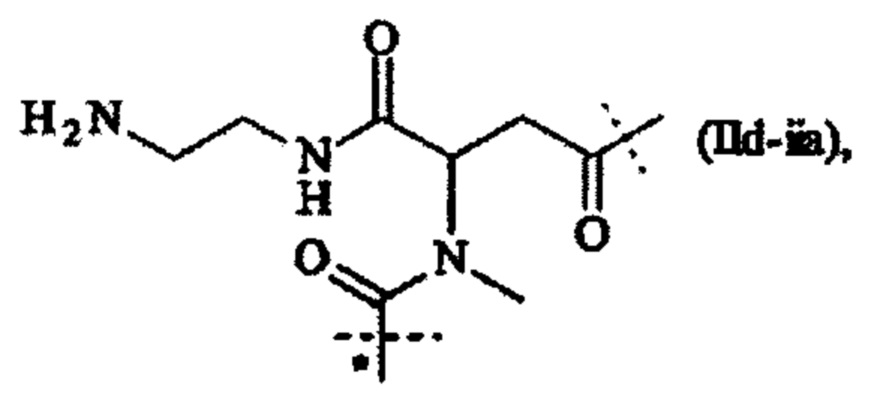
где
неотмеченная пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой CNP составляющую, путем образования амидной связи; и
пунктирная линия, отмеченная звездочкой, обозначает присоединение к -Z или -Z’.
В наиболее предпочтительном варианте выполнения настоящего изобретения составляющая -L1-L2- имеет формулу (IId-iia’)
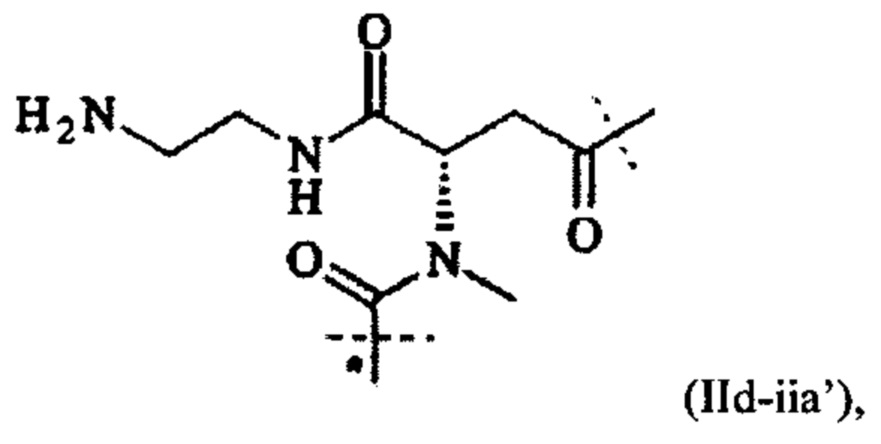
где
неотмеченная пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой CNP составляющую, путем образования амидной связи; и
пунктирная линия, отмеченная звездочкой, обозначает присоединение к -Z или -Z’.
В другом предпочтительном варианте выполнения настоящего изобретения составляющая -L1-L2- выбирают из группы, состоящей из
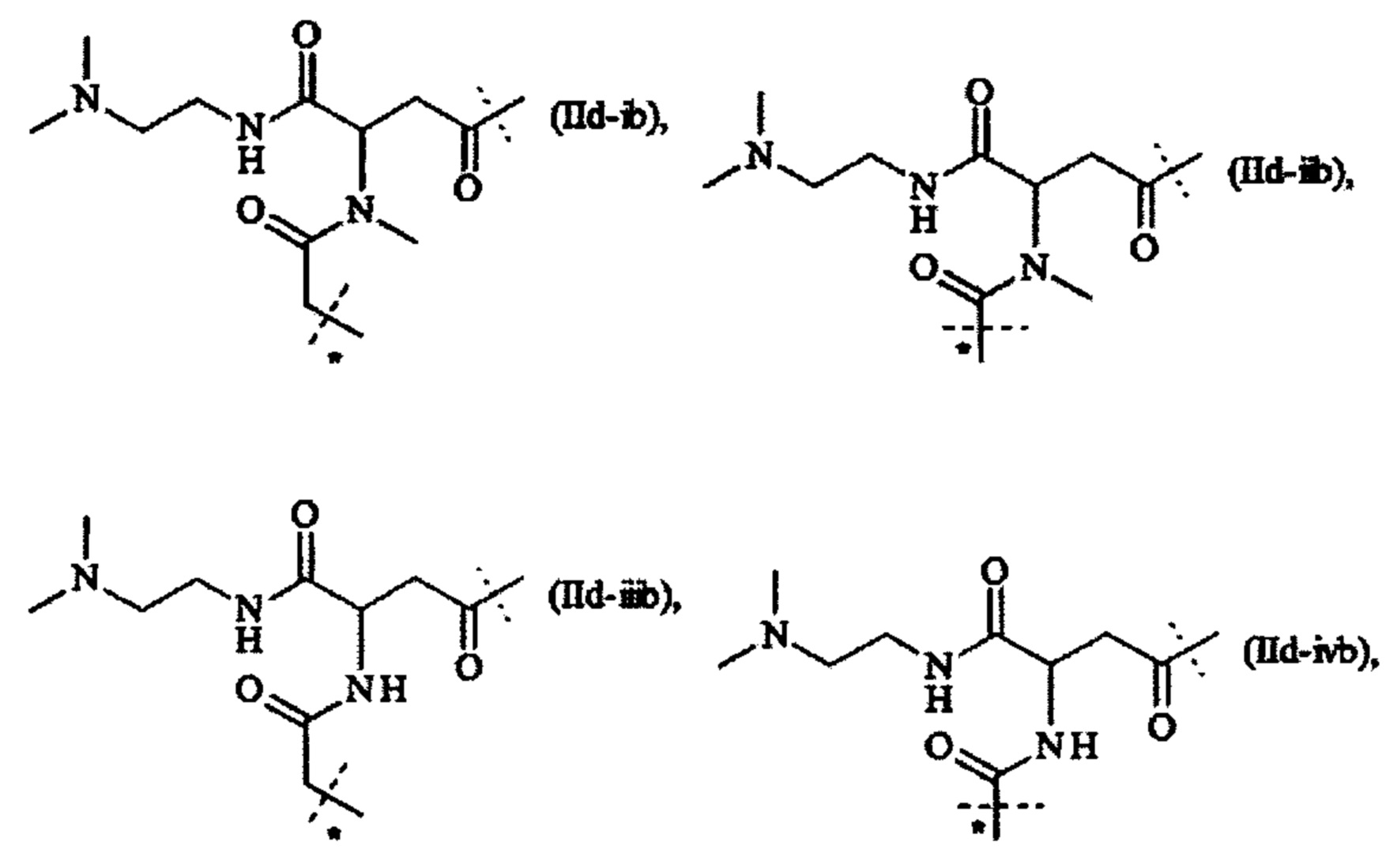
где
неотмеченная пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой CNP составляющую, путем образования амидной связи; и
пунктирная линия, отмеченная звездочкой, обозначает присоединение к -Z или -Z’.
В даже более предпочтительном варианте выполнения настоящего изобретения составляющая -L1-L2- представляет собой
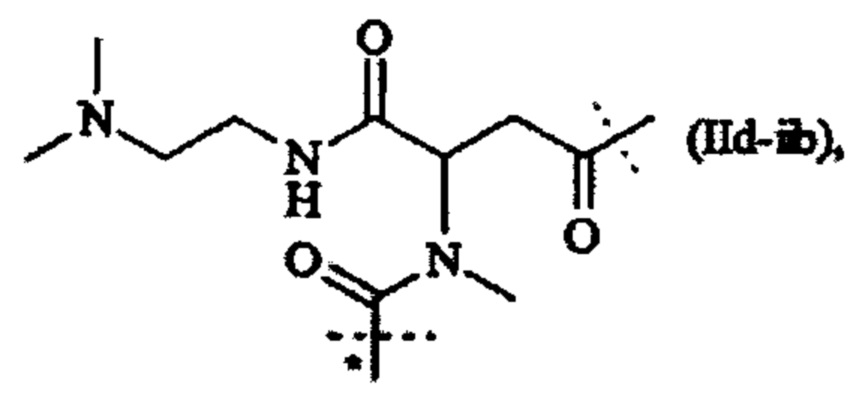
где
неотмеченная пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой CNP составляющую, путем образования амидной связи; и
пунктирная линия, отмеченная звездочкой, обозначает присоединение к -Z или -Z’.
В наиболее предпочтительном варианте выполнения настоящего изобретения составляющая -L1-L2- имеет формулу (IId-iib’)
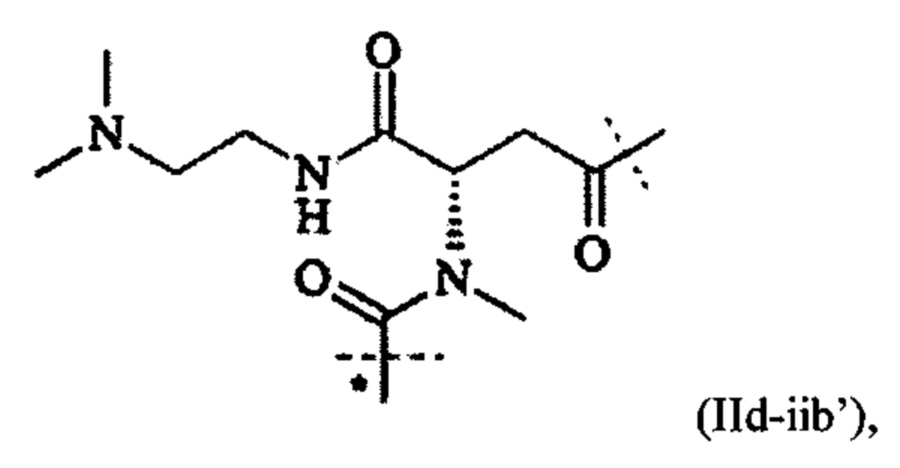
где
неотмеченная пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой CNP составляющую, путем образования амидной связи; и
пунктирная линия, отмеченная звездочкой, обозначает присоединение к -Z или -Z’.
Составляющая -L2- может быть присоединена к -L1- путем замещения любого присутствующего -Н.
Предпочтительно, от одного до пяти, предпочтительно один, из атомов водорода, обеспеченных -R1, -R1a, -R2, -R2a, -R3, -R3a, -R4, -R4a, -R5, -R5a, -R6, -R7, -R7a, -R8, -R8a, -R9, -R9a, -R10, -R10a и/или -R11 формулы (II), замещены на -L2-. Предпочтительно, от одного до пяти, предпочтительно один, из атомов водорода, обеспеченных -R1, -R1a, -R2, -R2a, -R3, -R3a, -R4, -R5, -R5a, -R6, -R6a, -R7, -R7a, -R8, -R8a, -R8b, -R9, -R9a, -R9b, -R10, -R10a, -R10b, -R11, -R12, -R12a, -R13, -R13a и/или -R13b формулы (III) замещены на -L2-.
Предпочтительно, -Z имеет молекулярную массу в интервале от 5 до 200 кДа. Даже более предпочтительно, -Z имеет молекулярную массу в интервале от 8 до 100 кДа, даже более предпочтительно в интервале от 10 до 80 кДа, даже более предпочтительно от 12 до 60, даже более предпочтительно от 15 до 40 и наиболее предпочтительно -Z имеет молекулярную массу, равную около 20 кДа. В другом равно предпочтительном варианте выполнения настоящего изобретения -Z имеет молекулярную массу, равную около 40 кДа.
Носитель -Z содержит С8-24 алкил или полимер. Предпочтительно, -Z содержит полимер, предпочтительно полимер, выбранный из группы, состоящей из 2-метакрилоил-оксиэтила фосфоилхолинов, поли(акриловых кислот), поли(акрилатов), поли(акриламидов), поли(алкилокси) полимеров, поли(амидов), поли(амидоаминов), поли(аминокислот), поли(ангидридов), поли(аспартамидов), поли(масляных кислот), поли(гликолевых кислот), полибутилентерефталатов, поли(капролактонов), поли(карбонатов), поли(цианоакрилатов), поли(диметилакриламидов), поли(сложных эфиров), поли(этиленов), поли(этиленгликолей), поли(этиленоксидов), поли(этилфосфатов), поли(этилоксазолинов), поли(гликолевых кислот), поли(гидроксиэтилакрилатов), поли(гидроксиэтил-оксазолинов), поли(гидроксиметакрилатов), поли(гидроксипропилметакриламидов), поли(гидроксипропил метакрилатов), поли(гидроксипропилоксазолинов), поли(иминокарбонатов), поли(молочных кислот), поли(сополимеров молочных и гликолевых кислот), поли(метакриламидов), поли(метакрилатов), поли(метилоксазолинов), поли(органофосфазенов), поли(ортосложных эфиров), поли(оксазолинов), поли(пропиленгликолей), поли(силоксанов), поли(уретанов), поли(виниловых спиртов), поли(виниламинов), поли(винилметиловых простых эфиров), поли(винилпирролидонов), силиконов, целлюлоз, карбометилцеллюлоз, гидроксипропил метилцеллюлоз, хитинов, хитозанов, декстранов, декстринов, желатинов, гиалуроновых кислот и производных, функционализированных гиалуроновых кислот, маннанов, пектинов, рамногалактуронанов, крахмалов, гидроксиалкил крахмалов, гидроксиэтил крахмалов и других полимеров на основе углеводов, ксиланов и их сополимеров.
В одном варианте выполнения настоящего изобретения такой растворимый в воде носитель -Z содержит белок. Предпочтительные белки выбирают из группы, состоящей из карбоксил-терминального пептида хорионического гонадотропина, как описано в US 2012/0035101 А1, которые включены в настоящую заявку посредством ссылки; альбумина; XTEN, как описано в WO 2011123813 А2, которая включена в настоящую заявку посредством ссылки; последовательностей пролиновых/аланиновых случайных спиралей, как описано в WO 2011/144756 А1, который включен в настоящую заявку посредством ссылки; последовательностей пролина/аланина/серина, как описано в WO 2008/155134 А1 и WO 2013/024049 А1, которые включены в настоящую заявку посредством ссылками; с Fc слитых белков.
В другом предпочтительном варианте выполнения настоящего изобретения, -Z содержит производное жирной кислоты. Предпочтительными производными жирной кислоты являются описанные в WO 2005/027978 А2 и WO 2014/060512 А1, которые включены в настоящую заявку посредством ссылки.
В другом предпочтительном варианте выполнения настоящего изобретения -Z представляет собой полимер на основе гиалуроновой кислоты.
В одном варианте выполнения настоящего изобретения -Z представляет собой носитель, как раскрывается в WO 2012/02047 А1, который включен в настоящую заявку посредством ссылки.
В другом варианте выполнения настоящего изобретения -Z представляет собой носитель, как раскрывается в WO 2013/024048 А1, который включен в настоящую заявку посредством ссылки.
В другом предпочтительном варианте выполнения настоящего изобретения -Z представляет собой полимер на основе ПЭГ. Даже более предпочтительно -Z представляет собой разветвленный полимер или полимер с множеством ветвей на основе ПЭГ. Наиболее предпочтительно, -Z представляет собой полимер с множеством ветвей на основе ПЭГ. Даже более предпочтительно, -Z представляет собой полимер с множеством ветвей на основе ПЭГ, имеющий по меньшей мере 4 ветви на основе ПЭГ.
Предпочтительно, такой -Z разветвленный полимер или полимер с множеством ветвей на основе ПЭГ, предпочтительно -Z полимер с множеством ветвей на основе ПЭГ, соединен с множеством составляющих -L2-L1-D, где каждая составляющая -L2-L1-D предпочтительно соединена с концом разветвления или ветви, предпочтительно с концом ветви. Предпочтительно такой -Z разветвленный полимер или полимер с множеством ветвей на основе ПЭГ, предпочтительно -Z полимер с множеством ветвей на основе ПЭГ соединен с 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 или 16 составляющими -L2-L1-D. Даже более предпочтительно, такой -Z разветвленный полимер или полимер с множеством ветвей на основе ПЭГ, предпочтительно полимер с множеством ветвей на основе ПЭГ, соединен с 2, 3, 4, 6 или 8 составляющими -L2-L1-D. Даже более предпочтительно такой -Z разветвленный полимер или полимер с множеством ветвей на основе ПЭГ, предпочтительно -Z полимер с множеством ветвей на основе ПЭГ соединен с 2, 4 или 6 составляющими -L2-L1-D, даже более предпочтительно такой -Z разветвленный полимер или полимер с множеством ветвей на основе ПЭГ, предпочтительно -Z полимер с множеством ветвей на основе ПЭГ соединен с 4 или 6 составляющими -L2-L1-D, и наиболее предпочтительно такой -Z разветвленный полимер или полимер с множеством ветвей на основе ПЭГ, предпочтительно -Z полимер с множеством ветвей на основе ПЭГ соединен с 4 составляющими -L2-L1-D.
Предпочтительно, если более чем одна составляющая -L2-L1-D соединена с одной составляющей -Z, потому что это обеспечивает достаточно высокую загрузку лекарственного средства, что позволяет получить фармацевтически эффективную дозу CNP в небольшом объеме, что в свою очередь повышает удобство для пациентов.
Предпочтительным растворимым в воде носителем -Z на основе ПЭГ является ПЭГ производное с множеством ветвей, как например подробно описано для продуктов, перечисленных в JenKem Technology, USA (доступно по ссылке http:jenkemusa.com/Pages/ПЭГПродуктs.aspx на 18 декабря 2014), как например ПЭГ производная с 4-мя ветвями, в частности ПЭГ производная с 4-мя ветвями, содержащая ядро из пентаэритрита, ПЭГ производная с восемью ветвями, содержащая ядро из гексаглицерина, и ПЭГ производная с восемью ветвями, содержащая ядро из трипентаэритрита. Более предпочтительно, растворимый в воде носителем -Z на основе ПЭГ содержит составляющую, выбранную из:
ПЭГ-амин с 4-мя ветвями, содержащий ядро из пентаэритрита:
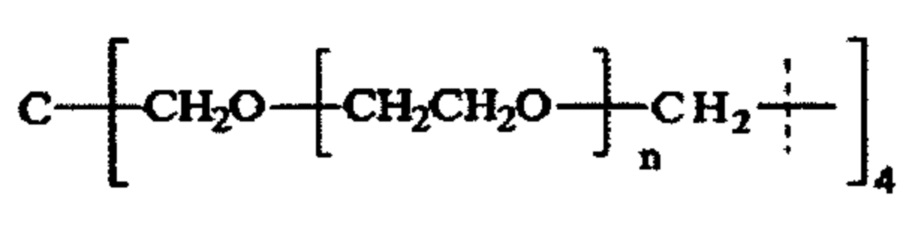
с n в интервале от 20 до 500;
ПЭГ-амин с восемью ветвями, содержащий ядро из гексаглицерина:
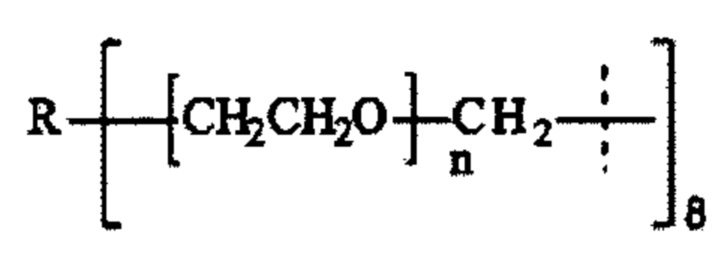
с n в интервале от 20 до 500; и
R = структура ядра из гексаглицерина или трипентаэритрита; и
ПЭГ-амин с шестью ветвями, содержащий ядро из сорбита или дипентаэритрита:
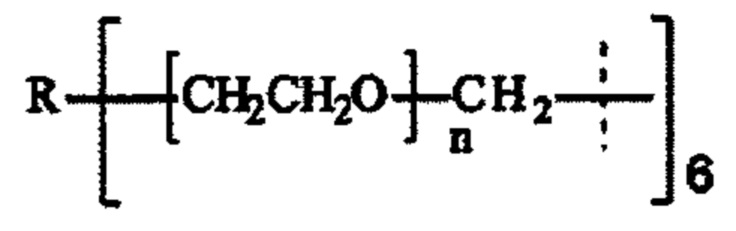
с n в интервале от 20 до 500; и
R = содержащий ядро из сорбита или дипентаэритрита;
и где пунктирные линии обозначают присоединение к остальной части CNP пролекарства.
х формулы (Ia) представляет собой целое число, выбранное из группы, состоящей из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 и 16. Предпочтительно, х представляет собой целое число, выбранное из группы, состоящей из 2, 3, 4, 6 и 8. Более предпочтительно х представляет собой целое число, выбранное из группы, состоящей из 2, 4 и 6. Даже более предпочтительно х представляет собой целое число, выбранное из группы, состоящей из 4 и 6 и наиболее предпочтительно х равно 4.
у формулы (Ib) представляет собой целое число, выбранное из группы, состоящей из 1, 2, 3, 4 или 5. Предпочтительно, у представляет собой целое число, выбранное из группы, состоящей из 1, 2 или 3. В одном предпочтительном варианте выполнения настоящего изобретения у равно 1. В равно предпочтительном варианте выполнения настоящего изобретения у равно 2.
В другом предпочтительном варианте выполнения настоящего изобретения одна составляющая -L2-L1-D соединена с одной составляющей -Z.
В особенно предпочтительном варианте выполнения настоящего изобретения -Z представляет собой разветвленный полимер. В одном варианте выполнения настоящего изобретения -Z представляет собой разветвленный полимер, имеющий одну, две, три, четыре, пять или шесть точек разветвления. Предпочтительно, -Z представляет собой разветвленный полимер, имеющий одну, две или три точки разветвления. В одном варианте выполнения настоящего изобретения -Z представляет собой разветвленный полимер, имеющий одну точку разветвления. В другом варианте выполнения настоящего изобретения -Z представляет собой разветвленный полимер, имеющий две точки разветвления. В другом варианте выполнения настоящего изобретения -Z представляет собой разветвленный полимер, имеющий три точки разветвления.
А точка разветвления предпочтительно выбирают из группы, состоящей из -N<, -СН< и >С<.
Предпочтительно такая разветвленная составляющая -Z основана на ПЭГ.
Предпочтительно, такая разветвленная составляющая -Z имеет молекулярную массу, равную по меньшей мере 10 кДа.
В одном варианте выполнения настоящего изобретения такая разветвленная составляющая -Z имеет молекулярную массу в интервале и включая 10 кДа-500 кДа, более предпочтительно в интервале и включая 10 кДа-250 кДа, даже более предпочтительно в интервале и включая 10 кДа-150 кДа, даже более предпочтительно в интервале и включая 12 кДа-100 кДа и наиболее предпочтительно в интервале и включая 15 кДа-80 кДа.
Предпочтительно, такая разветвленная составляющая -Z имеет молекулярную массу в интервале и включая 10 кДа-80 кДа. В одном варианте выполнения настоящего изобретения молекулярная масса равна около 10 кДа. В другом варианте выполнения настоящего изобретения молекулярная масса такой разветвленной составляющей -Z равна около 20 кДа. В другом варианте выполнения настоящего изобретения молекулярная масса такой разветвленной составляющей -Z равна около 30 кДа. В другом варианте выполнения настоящего изобретения молекулярная масса такой разветвленной составляющей -Z равна около 40 кДа. В другом варианте выполнения настоящего изобретения молекулярная масса такой разветвленной составляющей -Z равна около 50 кДа. В другом варианте выполнения настоящего изобретения молекулярная масса такой разветвленной составляющей -Z равна около 60 кДа. В другом варианте выполнения настоящего изобретения молекулярная масса такой разветвленной составляющей -Z равна около 70 кДа. В другом варианте выполнения настоящего изобретения молекулярная масса такой разветвленной составляющей -Z равна около 80 кДа. Наиболее предпочтительно, такая разветвленная составляющая -Z имеет молекулярную массу, равную около 40 кДа.
Заявитель неожиданно обнаружил, что N-терминальное присоединение составляющей -L1-L2-Z является значительно более эффективным в отношении увеличения NEP-стабильности, чем присоединение при внутреннем сайте, и что наименее эффективный сайт присоединения в отношении повышения стабильности NEP находится при кольцевой части CNP составляющей. Однако заявитель неожиданно обнаружил, что этот недостаток присоединения к кольцу в отношении увеличения NEP-стабильности может быть компенсирован посредством использования разветвленной составляющей -Z, имеющей молекулярную массу, равную по меньшей мере 10 кДа, как например по меньшей мере 12 кДа, как например по меньшей мере 15 кДа, как например по меньшей мере 18 кДа, как например по меньшей мере 20 кДа, как например по меньшей мере 24 кДа, как например по меньшей мере 25 кДа, как например по меньшей мере 27 кДа, как например по меньшей мере 30 кДа. Предпочтительно, такая разветвленная составляющая -Z имеет молекулярную массу, равную не более 500 кДа, предпочтительно не более 250 кДа, предпочтительно не более 200 кДа, предпочтительно не более 150 кДа и наиболее предпочтительно не более 100 кДа. Наиболее предпочтительно такая разветвленная составляющая -Z имеет молекулярную массу, равную около 40 кДа. Следовательно, применение такой разветвленной составляющей -Z при кольцевой части CNP составляющей не только приводит к увеличению NEP-стабильности, но объединяет увеличенную NEP-стабильность с уменьшенным NPR-B связыванием, сопутствующим присоединению к кольцу.
Предпочтительно, -Z или Z' содержит составляющую
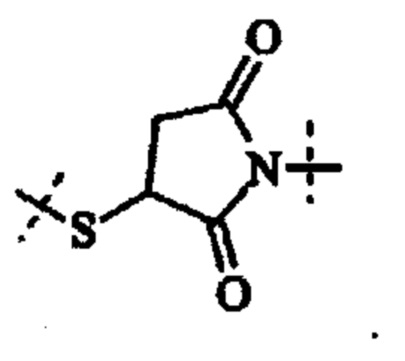
В одном варианте выполнения настоящего изобретения -Z содержит составляющую формулы (а)
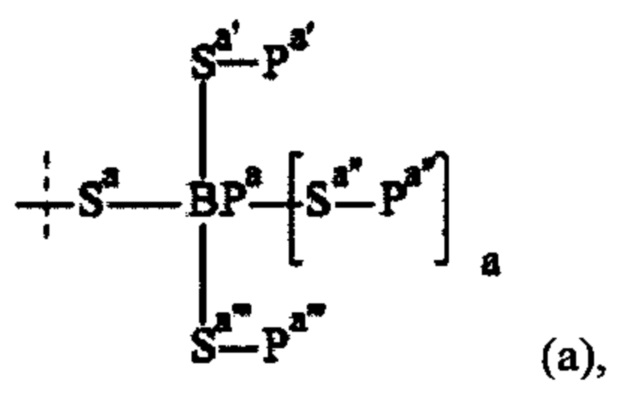
где
пунктирная линия показывает присоединение к -L2- или к оставшейся части -Z;
ВРа представляет собой точку разветвления, выбранную из группы, состоящей из -N<, -CR< и >С<;
-R выбирают из группы, состоящей из -Н и C1-6 алкила;
а равно 0, если ВРа представляет собой -N< или CR<, и n равно 1, если ВРа представляет собой >С<;
-Sa-, -Sa’-, -Sa’’- и Sa’’’- независимо друг от друга представляют собой химическую связь или выбирают из группы, состоящей из С1-50 алкила, С2-50 алкенила и С2-50 алкинила; где С1-50 алкил, С2-50 алкенил и С2-50 алкинил необязательно замещены одним или более заместителями -R1, которые являются одинаковыми или различными, и где С1-50 алкил, С2-50 алкенил и С2-50 алкинил необязательно прерваны одной или более группами, выбранными из группы, состоящей из -Т-, -С(O)O-, -О-, -С(О)-, -C(O)N(R2)-, -S(O)2N(R2)-, -S(O)N(R2)-, -S(O)2-, -S(O)-, -N(R2)S(O)2N(R2a)-, -S-, -N(R2)-, -OC(OR2)(R2a)-, -N(R2)C(O)N(R2a)- и -OC(O)N(R2)-;
каждый -T- независимо выбирают из группы, состоящей из фенила, нафтила, инденила, инданила, тетралинила, С3-10 циклоалкила, 3-10-членного гетероциклила, 8-11-членного гетеробициклила, 8-30-членного карбополициклила и 8-30-членного гетерополициклила; где каждый -Т- независимо необязательно замещен одним или более заместителями -R1, которые являются одинаковыми или различными;
каждый -R1 независимо выбирают из группы, состоящей из галогена, -CN, оксо (=O), -COOR3, -OR3, -C(O)R3, -C(O)N(R3R3a), -S(O)2N(R3R3a), -S(O)N(R3R3a), -S(O)2R3, -S(O)R3, -N(R3)S(O)2N(R3aR3b), -SR3, -N(R3R3a), -NO2, -OC(O)R3, -N(R3)C(O)R3a, -N(R3)S(O)2R3a, -N(R3)S(O)R3a, -N(R3)C(O)OR3a, -N(R3)C(O)N(R3aR3b), -OC(O)N(R3R3a) и C1-6 алкила; где C1-6 алкил необязательно замещен одним или более заместителями галоген, которые являются одинаковыми или различными;
каждый -R2, -R2a, -R3, -R3a и R3b независимо выбирают из группы, состоящей из -Н и C1-6 алкила, где C1-6 алкил необязательно замещен одним или более заместителями галоген, которые являются одинаковыми или различными; и
-Pa’, -Pa’’ и Pa’’’ независимо представляют собой полимерную составляющую.
В одном варианте выполнения настоящего изобретения BPa формулы (а) представляет собой -N<
В другом варианте выполнения настоящего изобретения BPa формулы (а) представляет собой -CR<. Предпочтительно, -R представляет собой -Н. Соответственно, а формулы (а) предпочтительно равно 0.
В другом варианте выполнения настоящего изобретения BPa формулы (а) представляет собой >С<.
В одном варианте выполнения настоящего изобретения -Sa- формулы (а) представляет собой химическую связь.
В другом варианте выполнения настоящего изобретения -Sa- формулы (а) выбирают из группы, состоящей из С1-10 алкила, С2-10 алкенила и С2-10 алкинила, где C1-10 алкил, С2-10 алкенил и С2-10 алкинил необязательно прерваны одной или более химическими группами, независимо выбранными из группы, состоящей из -С(O)O-, -O-, -С(O)-, -C(O)N(R4)-, -S(O)2N(R4)-, -S(O)N(R4)-, -S(O)2-, -S(O)-, -N(R4)S(O)2N(R4a)-, -S-, -N(R4)-, -OC(OR4)(R4a)-, -N(R4)C(O)N(R4a)- и -OC(O)N(R4)-; где -R4 и R4a независимо выбирают из группы, состоящей из -Н, метила, этила, пропила и бутила. Предпочтительно -Sa- формулы (а) выбирают из группы, состоящей из метила, этила, пропила, бутила, которые необязательно прерваны одной или более химическими группами, независимо выбранными из группы, состоящей из -O-, -С(O)- и C(O)N(R4)-.
В одном варианте выполнения настоящего изобретения -Sa’- формулы (а) представляет собой химическую связь.
В другом варианте выполнения настоящего изобретения -Sa’- формулы (а) выбирают из группы, состоящей из C1-10 алкила, С2-10 алкенила и С2-10 алкинила, где C1-10 алкил, С2-10 алкенил и С2-10 алкинил необязательно прерваны одной или более химическими группами, независимо выбранными из группы, состоящей из -С(O)O-, -O-, -С(O)-, -C(O)N(R4)-, -S(O)2N(R4)-, -S(O)N(R4)-, -S(O)2-, -S(O)-, -N(R4)S(O)2N(R4a)-, -S-, -N(R4)-, -OC(OR4)(R4a)-, -N(R4)C(O)N(R4a)- и -OC(O)N(R4)-; где -R4 и R4a независимо выбирают из группы, состоящей из -Н, метила, этила, пропила и бутила. Предпочтительно -Sa’- формулы (а) выбирают из группы, состоящей из метила, этила, пропила, бутила, которые необязательно прерваны одной или более химическими группами, независимо выбранными из группы, состоящей из -O-, -С(O)- и C(O)N(R4)-.
В одном варианте выполнения настоящего изобретения -Sa’’- формулы (а) представляет собой химическую связь.
В другом варианте выполнения настоящего изобретения -Sa’’- формулы (а) выбирают из группы, состоящей из C1-10 алкила, С2-10 алкенила и С2-10 алкинила, где C1-10 алкил, С2-10 алкенил и С2-10 алкинил необязательно прерваны одной или более химическими группами, независимо выбранными из группы, состоящей из -С(O)O-, -O-, -С(O)-, -C(O)N(R4)-, -S(O)2N(R4)-, -S(O)N(R4)-, -S(O)2-, -S(O)-, -N(R4)S(O)2N(R4a)-, -S-, -N(R4)-, -OC(OR4)R4a)-, -N(R4)C(O)N(R4a)- и -OC(O)N(R4)-; где -R4 и R4a независимо выбирают из группы, состоящей из -Н, метила, этила, пропила и бутила. Предпочтительно -Sa’’- формулы (а) выбирают из группы, состоящей из метила, этила, пропила, бутила, которые необязательно прерваны одной или более химическими группами, независимо выбранными из группы, состоящей из -O-, -С(O)- и C(O)N(R4)-.
В одном варианте выполнения настоящего изобретения -Sa’’’- формулы (а) представляет собой химическую связь.
В другом варианте выполнения настоящего изобретения -Sa’’’- формулы (а) выбирают из группы, состоящей из C1-10 алкила, С2-10 алкенила и С2-10 алкинила, где C1-10 алкил, С2-10 алкенил и С2-10 алкинил необязательно прерваны одной или более химическими группами, независимо выбранными из группы, состоящей из -С(O)O-, -O-, -С(O)-, -C(O)N(R4)-, -S(O)2N(R4)-, -S(O)N(R4)-, -S(O)2-, -S(O)-, -N(R4)S(O)2N(R4a)-, -S-, -N(R4)-, -OC(OR4)R4a)-, -N(R4)C(O)N(R4a)- и -OC(O)N(R4)-; где -R4 и R4a независимо выбирают из группы, состоящей из -Н, метила, этила, пропила и бутила. Предпочтительно -Sa’’’- формулы (а) выбирают из группы, состоящей из метила, этила, пропила, бутила, которые необязательно прерваны одной или более химическими группами, независимо выбранными из группы, состоящей из -O-, -С(O)- и C(O)N(R4)-.
Предпочтительно, -Pa’, -Pa’’ и Pa’’’ формулы (а) независимо содержат полимер, выбранный из группы, состоящей из 2-метакрилоил-оксиэтилфосфоилхолинов, поли(акриловых кислот), поли(акрилатов), поли(акриламидов), поли(алкилокси) полимеров, поли(амидов), поли(амидоаминов), поли(аминокислот), поли(ангидридов), поли(аспартамидов), поли(масляных кислот), поли(гликолевых кислот), полибутилентерефталатов, поли(капролактонов), поли(карбонатов), поли(цианоакрилатов), поли(диметилакриламидов), поли(сложных эфиров), поли(этиленов), поли(этиленгликолей), поли(этиленоксидов), поли(этилфосфатов), поли(этилоксазолинов), поли(гликолевых кислот), поли(гидроксиэтилакрилатов), поли(гидроксиэтил-оксазолинов), поли(гидроксиметакрилатов), поли(гидроксипропилметакриламидов), поли(гидроксипропил метакрилатов), поли(гидроксипропилоксазолинов), поли(иминокарбонатов), поли(молочных кислот), поли(сополимеров молочных и гликолевых кислот), поли(метакриламидов), поли(метакрилатов), поли(метилоксазолинов), поли(органофосфазенов), поли(ортосложных эфиров), поли(оксазолинов), поли(пропиленгликолей), поли(силоксанов), поли(уретанов), поли(виниловых спиртов), поли(виниламинов), поли(винилметиловых простых эфиров), поли(винилпирролидонов), силиконов, целлюлоз, карбометил целлюлоз, гидроксипропил метилцеллюлоз, хитинов, хитозанов, декстранов, декстринов, желатинов, гиалуроновых кислот и производных, функционализированных гиалуроновых кислот, маннанов, пектинов, рамногалактуронанов, крахмалов, гидроксиалкил крахмалов, гидроксиэтил крахмалов и других полимеров на основе углеводов, ксиланов и их сополимеров.
Более предпочтительно, -Pa’, -Pa’’ и Pa’’’ формулы (а) независимо содержат составляющую на основе ПЭГ. Даже более предпочтительно, -Pa’, -Pa’’ и Pa’’’ формулы (а) независимо содержат составляющую на основе ПЭГ, содержащую по меньшей мере 20% ПЭГ, даже более предпочтительно по меньшей мере 30%, даже более предпочтительно по меньшей мере 40% ПЭГ, даже более предпочтительно по меньшей мере 50% ПЭГ, даже более предпочтительно по меньшей мере 60% ПЭГ, даже более предпочтительно по меньшей мере 70% ПЭГ, даже более предпочтительно по меньшей мере 80% ПЭГ и наиболее предпочтительно по меньшей мере 90% ПЭГ.
Предпочтительно, -Pa’, -Pa’’ и Pa’’’ формулы (а) независимо имеют молекулярную массу в интервале и включая 5 кДа - 50 кДа, более предпочтительно имеют молекулярную массу в интервале и включая 5 кДа - 40 кДа, даже более предпочтительно в интервале и включая 7.5 кДа - 35 кДа, даже более предпочтительно в интервале от и 7.5-30 кДа, даже более предпочтительно в интервале и включая 10-30 кДа.
В одном варианте выполнения настоящего изобретения -Pa’, -Pa’’ и Pa’’’ формулы (а) имеют молекулярную массу, равную около 5 кДа.
В другом варианте выполнения настоящего изобретения -Pa’, -Pa’’ и Pa’’’ формулы (а) имеют молекулярную массу, равную около 7.5 кДа.
В другом варианте выполнения настоящего изобретения -Pa’, -Pa’’ и Pa’’’ формулы (а) имеют молекулярную массу, равную около 10 кДа.
В другом варианте выполнения настоящего изобретения -Pa’, -Pa’’ и Pa’’’ формулы (а) имеют молекулярную массу, равную около 12.5 кДа.
В другом варианте выполнения настоящего изобретения -Pa’, -Pa’’ и Pa’’’ формулы (а) имеют молекулярную массу, равную около 15 кДа.
В другом варианте выполнения настоящего изобретения -Pa’, -Pa’’ и Pa’’’ формулы (а) имеют молекулярную массу, равную около 20 кДа.
В одном варианте выполнения настоящего изобретения -Z содержит одну составляющую формулы (а).
В другом варианте выполнения настоящего изобретения -Z содержит две составляющие формулы (а).
В другом варианте выполнения настоящего изобретения -Z содержит три составляющие формулы (а).
В другом варианте выполнения настоящего изобретения -Z содержит четыре составляющие формулы (а).
В другом варианте выполнения настоящего изобретения -Z содержит пять составляющих формулы (а).
В другом варианте выполнения настоящего изобретения -Z содержит шесть составляющих формулы (а).
В предпочтительном варианте выполнения настоящего изобретения -Z содержит две составляющие формулы (а).
В предпочтительном варианте выполнения настоящего изобретения -Z содержит составляющую формулы (b)
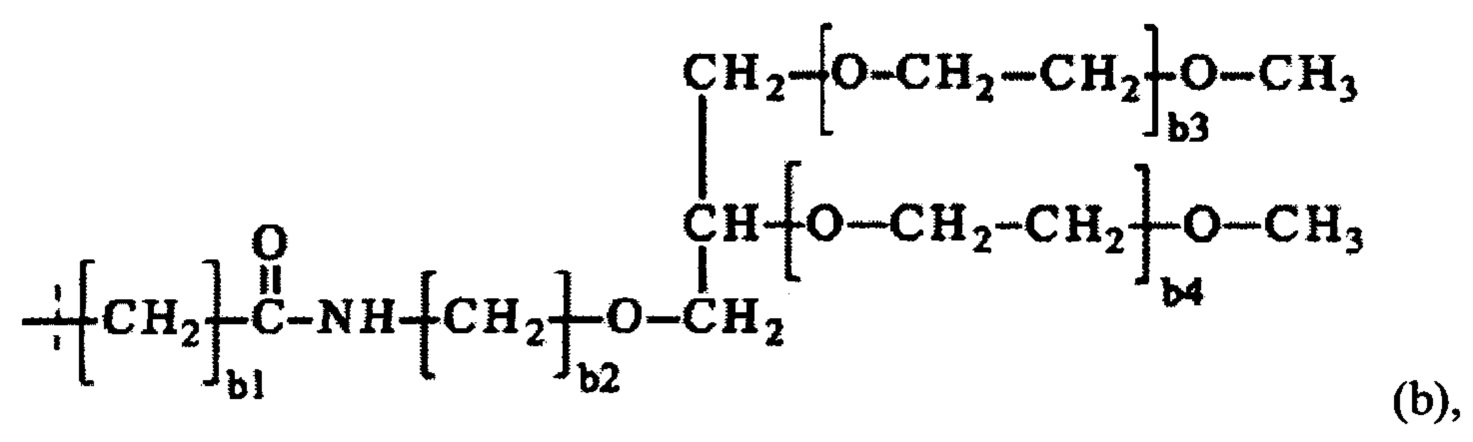
где
пунктирная линия показывает присоединение к -L2- или к оставшейся части -Z;
b1 выбирают из группы, состоящей из 0, 1, 2, 3, 4, 5, 6,7 и 8;
b2 выбирают из группы, состоящей из 1, 2, 3, 4, 5, 6, 7 и 8;
b3 представляет собой целое число в интервале и включая 150-1000; предпочтительно в интервале и включая 150-500; и наиболее предпочтительно в интервале и включая 200-460; и
b4 представляет собой целое число в интервале и включая 150-1000; предпочтительно в интервале и включая 150-500; - наиболее предпочтительно в интервале и включая 200-460.
Предпочтительно, b3 и b4 формулы (b) представляют собой такое же целое число.
В одном предпочтительном варианте выполнения настоящего изобретения b3 и b4 оба целое число в интервале 200-250, и наиболее предпочтительно b3 и b4 формулы (b) равны около 225.
В другом предпочтительном варианте выполнения настоящего изобретения b3 и b4 оба представляют собой целое число в интервале 400-500, и наиболее предпочтительно b3 и b4 формулы (b) равны около 450.
Предпочтительно, b1 формулы (b) выбирают из группы, состоящей из 0, 1, 2, 3 и 4. Более предпочтительно b1 формулы (b) выбирают из группы, состоящей из 1, 2 и 3. Наиболее предпочтительно b1 формулы (b) равно 2.
Предпочтительно, b2 формулы (b) выбирают из группы, состоящей из 1, 2, 3, 4 и 5. Более предпочтительно b2 формулы (b) выбирают из группы, состоящей из 2, 3 и 4. Наиболее предпочтительно b2 формулы (b) равно 3.
В одном особенно предпочтительном варианте выполнения настоящего b1 формулы (b) равно 2, b2 формулы (b) равно 3, и b3 и b4 оба представляют собой около 450.
В другом особенно предпочтительном варианте выполнения настоящего изобретения b1 формулы (b) равно 2, b2 формулы (b) равно 3, и b3 и b4 оба представляют собой около 225.
В одном варианте выполнения настоящего изобретения -Z содержит одну составляющую формулы (b).
В другом варианте выполнения настоящего изобретения -Z содержит две составляющие формулы (b).
В другом варианте выполнения настоящего изобретения -Z содержит три составляющие формулы (b).
В другом варианте выполнения настоящего изобретения -Z содержит четыре составляющие формулы (b).
В другом варианте выполнения настоящего изобретения -Z содержит пять составляющих формулы (b).
В другом варианте выполнения настоящего изобретения -Z содержит шесть составляющих формулы (b).
В предпочтительном варианте выполнения настоящего изобретения -Z содержит две составляющие формулы (b).
В даже более предпочтительном варианте выполнения настоящего изобретения -Z содержит составляющую формулы (с)
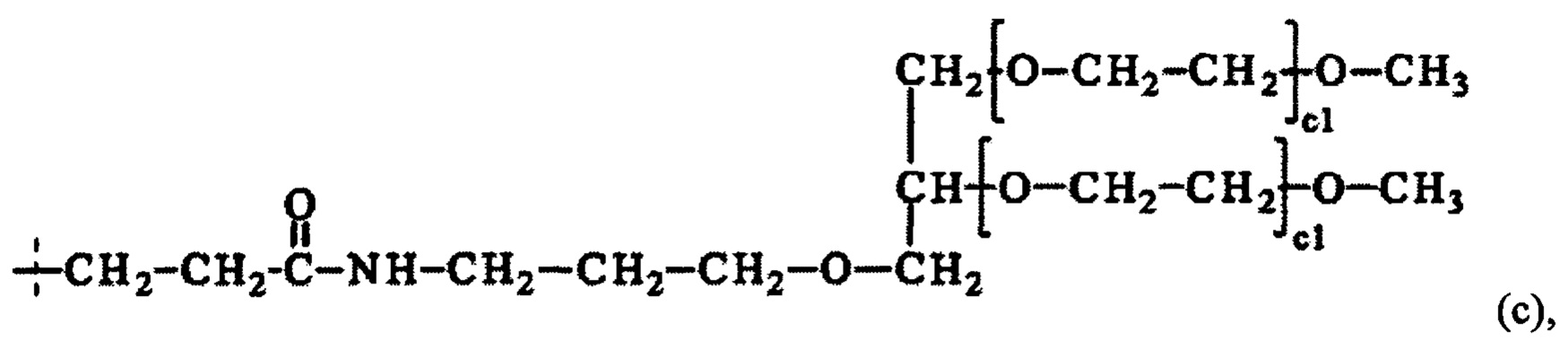
где
пунктирная линия показывает присоединение к -L2- или к оставшейся части -Z;
с1 и с2 независимо представляют собой целое число в интервале и включая 150-500; предпочтительно в интервале и включая 200-460.
Предпочтительно оба с1 и с2 формулы (с) представляют собой такое же целое число.
В одном предпочтительном варианте выполнения настоящего изобретения с1 и с2 формулы (с) находятся в интервале и включают 200-250, и наиболее предпочтительно равны около 225. В другом предпочтительном варианте выполнения настоящего изобретения с1 и с2 формулы (с) находятся в интервале и включают 400-500, и наиболее предпочтительно равны около 450.
В предпочтительном варианте выполнения настоящего изобретения составляющая -Z представляет собой разветвленный полимер на основе ПЭГ, содержащий по меньшей мере 10% ПЭГ, имеет одну точку разветвления и две полимерные ветви на основе ПЭГ и имеет молекулярную массу, равную около 40 кДа. Соответственно, каждая из двух полимерных ветвей на основе ПЭГ имеет молекулярную массу, равную около 20 кДа. Предпочтительно точкой разветвления является -СН<.
В одном варианте выполнения настоящего изобретения -Z содержит одну составляющую формулы (с).
В другом варианте выполнения настоящего изобретения -Z содержит две составляющие формулы (с).
В другом варианте выполнения настоящего изобретения -Z содержит три составляющие формулы (с).
В другом варианте выполнения настоящего изобретения -Z содержит четыре составляющие формулы (с).
В другом варианте выполнения настоящего изобретения -Z содержит пять составляющих формулы (с).
В другом варианте выполнения настоящего изобретения -Z содержит шесть составляющих формулы (с).
В предпочтительном варианте выполнения настоящего изобретения- Z содержит две составляющие формулы (с).
В одном предпочтительном варианте выполнения настоящего изобретения составляющая -Z имеет формулу (d)
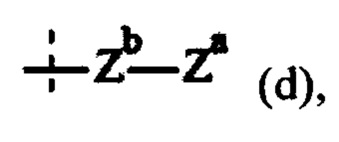
где
пунктирная линия показывает присоединение к -L2-;
-Zb- выбирают из группы, состоящей из С1-50 алкила, C2-50 алкенила и C2-50 алкинила; где C1-50 алкил, C2-50 алкенил и C2-50 алкинил необязательно замещены одним или более заместителями -R1, которые являются одинаковыми или различными, и где C1-50 алкил, C2-50 алкенил и C2-50 алкинил необязательно прерваны одной или более группами, выбранными из группы, состоящей из -Т-, -С(O)O-, -O-, -С(O)-, -C(O)N(R2)-, -S(O)2N(R2)-, -S(O)N(R2)-, -S(O)2-, -S(O)-, -N(R2)S(O)2N(R2a)-, -S-, -N(R2)-, -ОС(OR)2(R2a)-, -N(R2)C(O)N(R2a)- и -OC(O)N(R2)-;
каждый -Т- независимо выбирают из группы, состоящей из фенила, нафтила, инденила, инданила, тетралинила, С3-10 циклоалкила, 3-10-членного гетероциклила, 8-11-членного гетеробициклила, 8-30-членный карбополициклила и 8-30-членного гетерополициклила; где каждый -Т-независимо необязательно замещен одним или более заместителями -R1, которые являются одинаковыми или различными;
каждый -R1 независимо выбирают из группы, состоящей из галогена, -CN, оксо (=O), -COOR3, -OR3, -C(O)R3, -С(O)N(R3R3a), -S(O)2N(R3R3a), -S(O)N(R3R3a), -S(O)2R3, -S(O)R3, -N(R3)S(O)2N(R3aR3b), -SR3, -N(R3R3a), -NO2, -OC(O)R3, -N(R3)C(O)R3a, -N(R3)S(O)2R3a, -N(R3)S(O)R3a, -N(R3)C(O)OR3a, -N(R3)C(O)N(R3aR3b), -OC(O)N(R3R3a) и C1-6 алкила; где C1-6 алкил необязательно замещен одним или более заместителями галоген, которые являются одинаковыми или различными;
каждый -R2, -R2a, -R3, -R3a и R3b независимо выбирают из группы, состоящей из -Н и C1-6 алкила, где C1-6 алкил необязательно замещен одним или более заместителями галоген, которые являются одинаковыми или различными;
и
-Za представляет собой
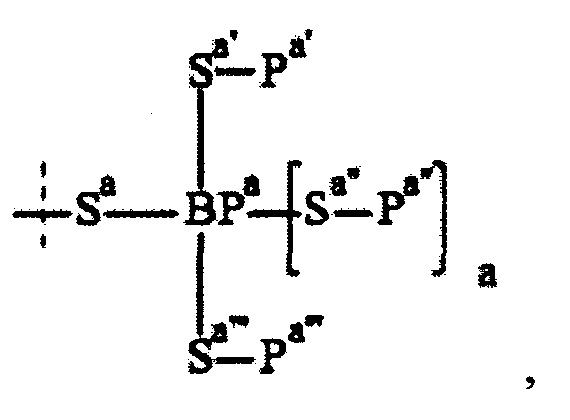
где
BPa, -Sa-, -Sa’-, -Sa’’-, -Sa’’’-, -Pa’, -Pa’’, -Pa’’’ и а являются такими, как определено для формулы (а).
Предпочтительные варианты BPa, -Sa-, -Sa’-, -Sa’’-, -Sa’’’-, -Pa’, -Pa’’, -Pa’’’ формулы (d) являются такими, как определено выше для формулы (а).
В даже более предпочтительном варианте выполнения настоящего изобретения составляющая -Z имеет формулу (е)
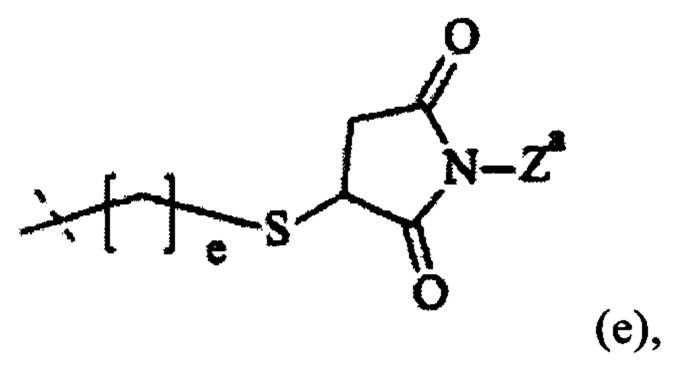
где
пунктирная линия показывает присоединение к -L2-;
е выбирают из группы, состоящей из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 и 15; и
-Za представляет собой
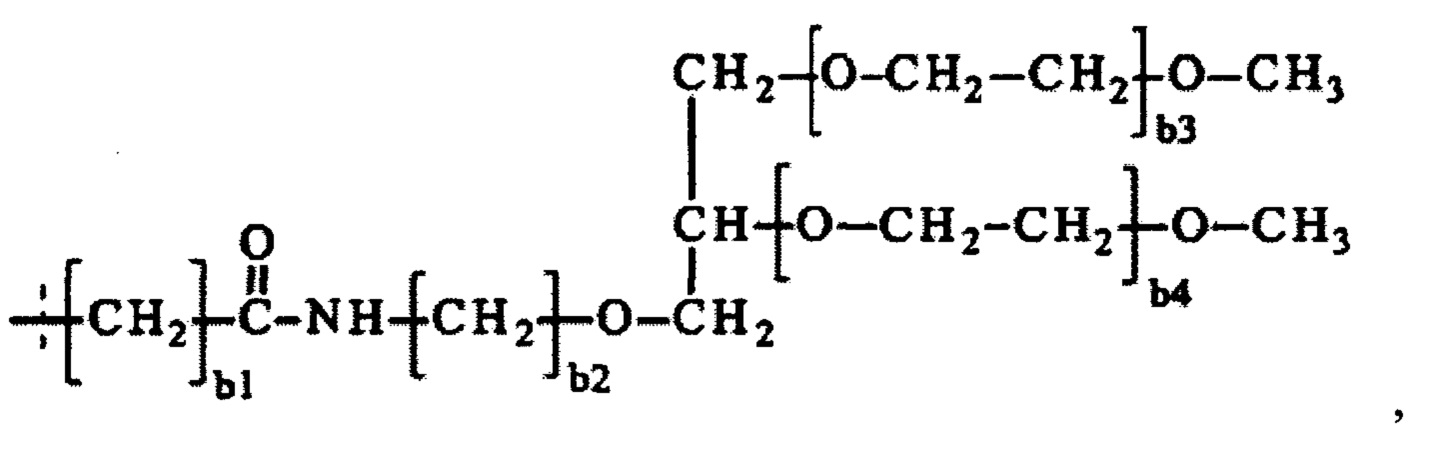
где
b1 выбирают из группы, состоящей из 0, 1, 2, 3, 4, 5, 6, 7 и 8;
b2 выбирают из группы, состоящей из 1,2, 3, 4, 5, 6, 7 и 8;
b3 представляет собой целое число в интервале и включая 150-1000; предпочтительно в интервале и включая 150-500; и наиболее предпочтительно в интервале и включая 200-460; и
b4 представляет собой целое число в интервале и включая 150-1000; предпочтительно в интервале и включая 150-500; и наиболее предпочтительно в интервале и включая 200-460.
Предпочтительные варианты b1, b2, b3 и b4 формулы (е) являются такими, как определено выше для формулы (b).
В одном варианте выполнения настоящего изобретения е формулы (е) равно 1. В другом варианте выполнения настоящего изобретения е формулы (е) равно 2. В другом варианте выполнения настоящего изобретения е формулы (е) равно 3. В другом варианте выполнения настоящего изобретения е формулы (е) равно 4. В другом варианте выполнения настоящего изобретения е формулы (е) равно 5. В другом варианте выполнения настоящего изобретения е формулы (е) равно 6. В другом варианте выполнения настоящего изобретения е формулы (е) равно 7. В другом варианте выполнения настоящего изобретения е формулы (е) равно 8. В другом варианте выполнения настоящего изобретения е формулы (е) равно 9. В другом варианте выполнения настоящего изобретения е формулы (е) равно 10. В другом варианте выполнения настоящего изобретения е формулы (е) равно 11. В другом варианте выполнения настоящего изобретения е формулы (е) равно 12. В другом варианте выполнения настоящего изобретения е формулы (е) равно 13. В другом варианте выполнения настоящего изобретения е формулы (е) равно 14. В другом варианте выполнения настоящего изобретения е формулы (е) равно 15.
Предпочтительно е формулы (е) выбирают из группы, состоящей из 2, 3, 4, 5, 6, 7, 8 и 9. Даже более предпочтительно, е формулы (е) выбирают из 3, 4, 5 и 6. Наиболее предпочтительно е формулы (е) равно 5.
Предпочтительно е формулы (е) равно 5, b1 формулы (е) равно 2, b2 формулы (е) равно 3, и b3 и b4 формулы (е) оба представляют собой около 450.
В другом предпочтительном варианте выполнения настоящего изобретения составляющая -Z представляет собой разветвленный полимер на основе ПЭГ, содержащий по меньшей мере 10% ПЭГ, имеет три точки разветвления и четыре полимерные ветви на основе ПЭГ, и имеет молекулярную массу, равную около 40 кДа. Соответственно, каждая из четырех полимерных ветвей на основе ПЭГ имеет молекулярную массу, равную около 10 кДа. Предпочтительно каждая из трех точек разветвления представляет собой -СН<.
В предпочтительном варианте выполнения настоящего изобретения составляющая -Z имеет формулу (f)
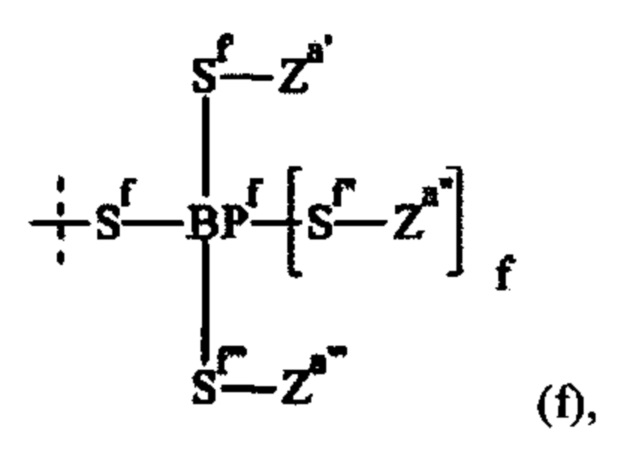
где
пунктирная линия показывает присоединение к -L2-;
BPf представляет собой точку разветвления, выбранную из группы, состоящей из -N<, -CR< и >С<;
-R выбирают из группы, состоящей из -Н и C1-6 алкила;
f равно 0, если BPf представляет собой -N< или CR<, и f равно 1, если BPf представляет собой >С<;’
-Sf-, -Sf’-, -Sf’’- и Sf’’’ - либо независимо представляют собой химическую связь, либо независимо выбирают из группы, состоящей из С1-50 алкила, С2-50 алкенила и С2-50 алкинила; где С1-50 алкил, С2-50 алкенил и С2-50 алкинил необязательно замещены одним или более заместителями -R1, которые являются одинаковыми или различными, и где С1-50 алкил, С2-50 алкенил и С2-50 алкинил необязательно прерваны одной или более группами, выбранными из группы, состоящей из -Т-, -С(O)O-, -О-, -С(О)-, -C(O)N(R2)-, -S(O)2N(R2)-, -S(O)N(R2)-, -S(O)2-, -S(O)-, -N(R2)S(O)2N(R2a)-, -S-, -N(R2)-, -OC(OR2)(R2a)-, -N(R2)C(O)N(R2a)- и -OC(O)N(R2)-;
каждый -T- независимо выбирают из группы, состоящей из фенила, нафтила, инденила, инданила, тетралинила, С3-10 циклоалкила, 3-10-членного гетероциклила, 8-11- членного гетеробициклила, 8- 30- членного карбополициклила и 8-30- членного гетерополициклила; где каждый -Т- независимо необязательно замещен одним или более заместителями -R1, которые являются одинаковыми или различными;
каждый R1 независимо выбирают из группы, состоящей из галогена, -CN, оксо (=O), -COOR3, -OR3, -C(O)R3, -C(O)N(R3R3a), -S(O)2N(R3R3a), -S(O)N(R3R3a), -S(O)2R3, -S(O)R3, -N(R3)S(O)2N(R3aR3b), -SR3, -N(R3R3a), -NO2, -OC(O)R3, -N(R3)C(O)R3a, -N(R3)S(O)2R3a, -N(R3)S(O)R3a, -N(R3)C(O)OR3a, -N(R3)C(O)N(R3aR3b), -OC(O)N(R3R3a) и С1-6 алкила; где C1-6 алкил необязательно замещен одним или более заместителями галоген, которые являются одинаковыми или различными;
каждый -R2, -R2a, -R3, -R3a и R3b независимо выбирают из группы, состоящей из -Н и C1-6 алкила, где C1-6 алкил необязательно замещен одним или более заместителями галоген, которые являются одинаковыми или различными;
и
-Za’, -Za’’ и Za’’’ независимо представляют собой
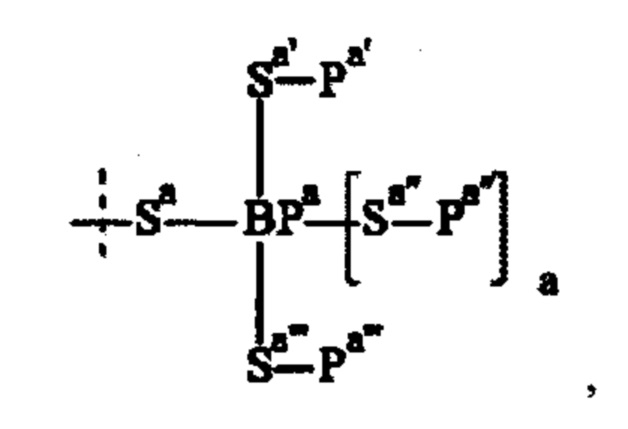
где
BPa, -Sa-, -Sa’-, -Sa’’-, -Sa’’’-, -Ра’, -Ра’’, -Ра’’’ и а являются такими, как определено для формулы (а).
Предпочтительные варианты ВРа, -Sa-, -Sa’-, -Sa’’-, -Sa’’’-, -Ра’, -Ра’’ и Ра’’’ формулы (f) являются такими, как определено выше для формулы (а).
Предпочтительно BP2 формулы (f) представляет собой -CR<, и r равно 0.
Предпочтительно -R представляет собой -Н.
Предпочтительно -Sf- формулы (f) представляет собой химическую связь.
Предпочтительно, -Za’, -Za‘’ и Za’’’ формулы (f) имеют одинаковую структуру.
Предпочтительно, -Za’, -Za‘’ и Za’’’ формулы (f) являются такими же как для формулы (b).
Предпочтительно -Sf- формулы (f) представляет собой химическую связь, ВРа формулы (f) представляет собой -CR<, где -R представляет собой -Н. Даже более предпочтительно -Sf- формулы (f) представляет собой химическую связь, BPa формулы (f) представляет собой -CR<, где -R представляет собой -Н, и Za’, -Za’’ и Za’’’ формулы (f) являются такими же как для формулы (b).
Даже более предпочтительно -Z имеет формулу (g)
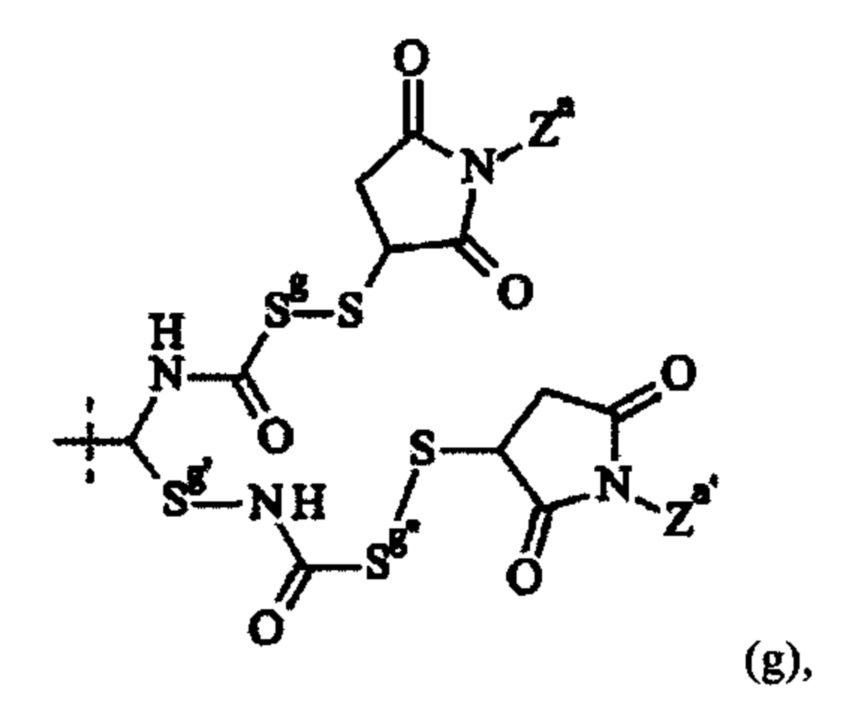
где
пунктирная линия показывает присоединение к -L2-;
-Sg-, -Sg’- и -Sg’’- независимо выбирают из группы, состоящей из С1-50 алкила, С2-50 алкенила и С2-50 алкинила; где С1-50 алкил, С2-50 алкенил и С2-50 алкинил необязательно замещены одним или более заместителями -R1, которые являются одинаковыми или различными, и где С1-50 алкил, С2-50 алкенил и С2-50 алкинил необязательно прерваны одной или более группами, выбранными из группы, состоящей из -Т-, -С(O)O-, -О-, -С(О)-, -C(O)N(R2)-, -S(O)2N(R2)-, -S(O)N(R2)-, -S(O)2- -S(O)-, -N(R2)S(O)2N(R2a)-, -S-, -N(R2)-, -OC(OR2)(R2a)-, -N(R2)C(O)N(R2a)- и -OC(O)N(R2)-;
каждый -T- независимо выбирают из группы, состоящей из фенила, нафтила, инденила, инданила, тетралинила, С3-10 циклоалкила, 3-10-членного гетероциклила, 8-11-членного гетеробициклила, 8-30-членного карбополициклила и 8-30-членного гетерополициклила; где каждый -Т-независимо необязательно замещен одним или более заместителями -R1, которые являются одинаковыми или различными;
каждый R1 независимо выбирают из группы, состоящей из галогена, -CN, оксо (=O), -COOR3, -OR3, -C(O)R3, -C(O)N(R3R3a), -S(O)2N(R3R3a), -S(O)N(R3R3a), -S(O)2R3, -S(O)R3, -N(R3)S(O)2N(R3aR3b), -SR3, -N(R3R3a), -NO2, -OC(O)R3, -N(R3)C(O)R3a, -N(R3)S(O)2R3a, -N(R3)S(O)R3a, -N(R3)C(O)OR3a, -N(R3)C(O)N(R3aR3b), -OC(O)N(R3R3a) и C1-6 алкила; где C1-6 алкил необязательно замещен одним или более заместителями галоген, которые являются одинаковыми или различными;
каждый -R2, -R2a, -R3, -R3a и R3b независимо выбирают из группы, состоящей из -Н и C1-6 алкила, где C1-6 алкил необязательно замещен одним или более заместителями галоген, которые являются одинаковыми или различными;
и
-Za и -Za’ независимо представляют собой
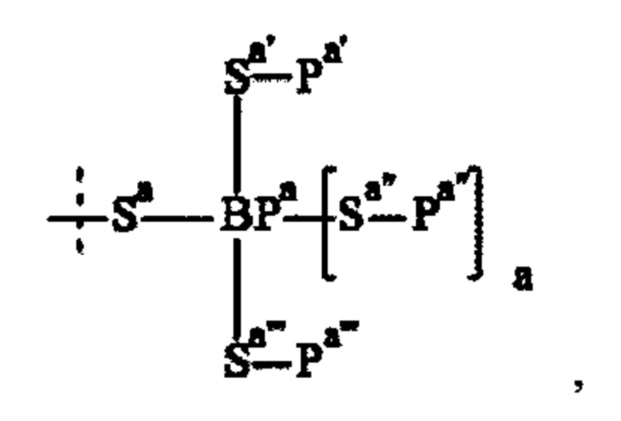
где
BPa, -Sa-, -Sa’-, -Sa’’-, -Sa’’’-, -Ра’, -Ра’’, -Ра’’’ и а являются такими, как определено для формулы (а).
Предпочтительные варианты ВРа, -Sa-, -Sa’-, -Sa’’-, -Sa’’’-, -Pa’, -Pa’’ и Pa’’’ формулы (g) являются такими, как определено выше для формулы (а).
Предпочтительно, -Sg- формулы (g) выбирают из группы, состоящей из C1-6 алкила, С2-6 алкенила и С2-6 алкинила, которые необязательно замещены одним или более заместителями -R1, которые являются одинаковыми или различными,
где
-R1 выбирают из группы, состоящей из галогена, оксо (=O), -COOR3, -OR3, -C(O)R3, -C(O)N(R3R3a), -S(O)2N(R3R3a), -S(O)N(R3R3a), -S(O)2R3, -S(O)R3, -N(R3)S(O)2N(R3aR3b), -SR3, -N(R3R3a), -NO2, -OC(O)R3, -N(R3)C(O)R3a, -N(R3)S(O)2R3a, -N(R3)S(O)R3a, -N(R3)C(O)OR3a, -N(R3)C(O)N(R3aR3b), -OC(O)N(R3R3a) и C1-6 алкила; где C1-6 алкил необязательно замещен одним или более заместителями галоген, которые являются одинаковыми или различными; и
-R3, -R3a и R3b независимо выбирают из -Н, метила, этила, пропила и бутила.
Даже более предпочтительно -Sg- формулы (g) выбирают из C1-6 алкила.
Предпочтительно, -Sg’- формулы (g) выбирают из группы, состоящей из C1-6 алкила, С2-6 алкенила и С2-6 алкинила, которые необязательно замещены одним или более заместителями -R1, которые являются одинаковыми или различными,
где
-R1 выбирают из группы, состоящей из галогена, оксо (=O), -COOR3, -OR3, -C(O)R3, -C(O)N(R3R3a), -S(O)2N(R3R3a), -S(O)N(R3R3a), -S(O)2R3, -S(O)R3, -N(R3)S(O)2N(R3aR3b), -SR3, -N(R3R3a), -NO2, -OC(O)R3, -N(R3)C(O)R3a, -N(R3)S(O)2R3a, -N(R3)S(O)R3a, -N(R3)C(O)OR3a, -N(R3)C(O)N(R3aR3b), -OC(O)N(R3R3a) и С1-6 алкила; где С1-6 алкил необязательно замещен одним или более заместителями галоген, которые являются одинаковыми или различными; и
-R3, -R3a и R3b независимо выбирают из -Н, метила, этила, пропила и бутила.
Даже более предпочтительно -Sg’- формулы (g) выбирают из C1-6 алкила.
Предпочтительно, -Sg’’- формулы (g) выбирают из группы, состоящей из C1-6 алкила, С2-6 алкенила и С2-6 алкинила, которые необязательно замещены одним или более заместителями -R1, которые являются одинаковыми или различными,
где
-R1 выбирают из группы, состоящей из галогена, оксо (=O), -COOR3, -OR3, -C(O)R3, -C(O)N(R3R3a), -S(O)2N(R3R3a), -S(O)N(R3R3a), -S(O)2R3, -S(O)R3, -N(R3)S(O)2N(R3aR3b), -SR3, -N(R3R3a), -NO2, -OC(O)R3, -N(R3)C(O)R3a, -N(R3)S(O)2R3a, -N(R3)S(O)R3a, -N(R3)C(O)OR3a, -N(R3)C(O)N(R3aR3b), -OC(O)N(R3R3a) и C1-6 алкила; где C1-6 алкил необязательно замещен одним или более заместителями галоген, которые являются одинаковыми или различными; и
-R3, -R3a и R3b независимо выбирают из -Н, метила, этила, пропила и бутила.
Даже более предпочтительно -Sg’’- формулы (g) выбирают из C1-6 алкила.
Предпочтительно, -Za и -Za‘ формулы (g) имеют одну и ту же структуру.
Предпочтительно, -Za и -Za‘ формулы (g) являются такими же как для формулы (b).
Даже более предпочтительно -Z имеет формулу (h)
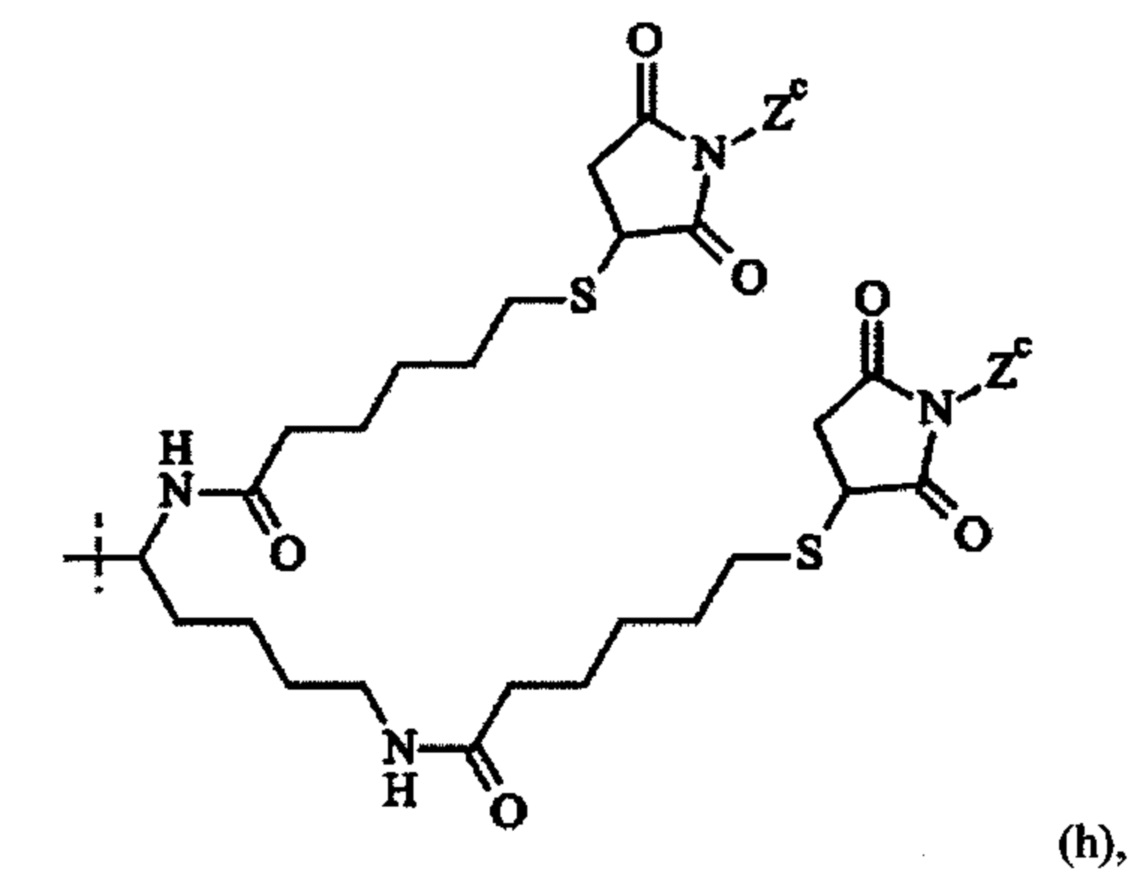
где
пунктирная линия показывает присоединение к -L2-; и
каждый -Zc представляет собой составляющую
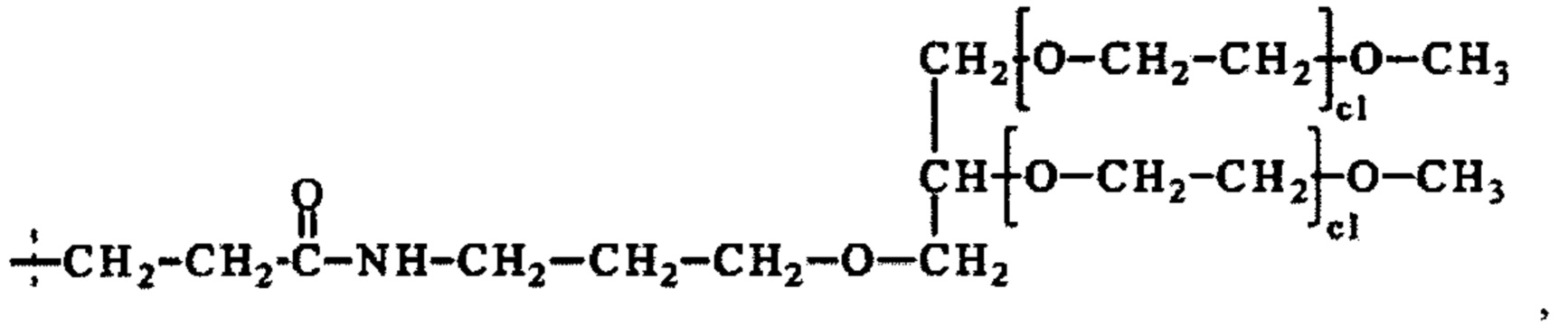
где
каждый c1 независимо представляет собой целое число в интервале от около 200 до 250.
Предпочтительно оба c1 формулы (h) являются одинаковыми.
Предпочтительно оба c1 формулы (h) равны около 225.
В даже более предпочтительном варианте выполнения настоящего изобретения составляющая -Z имеет формулу (h-i)
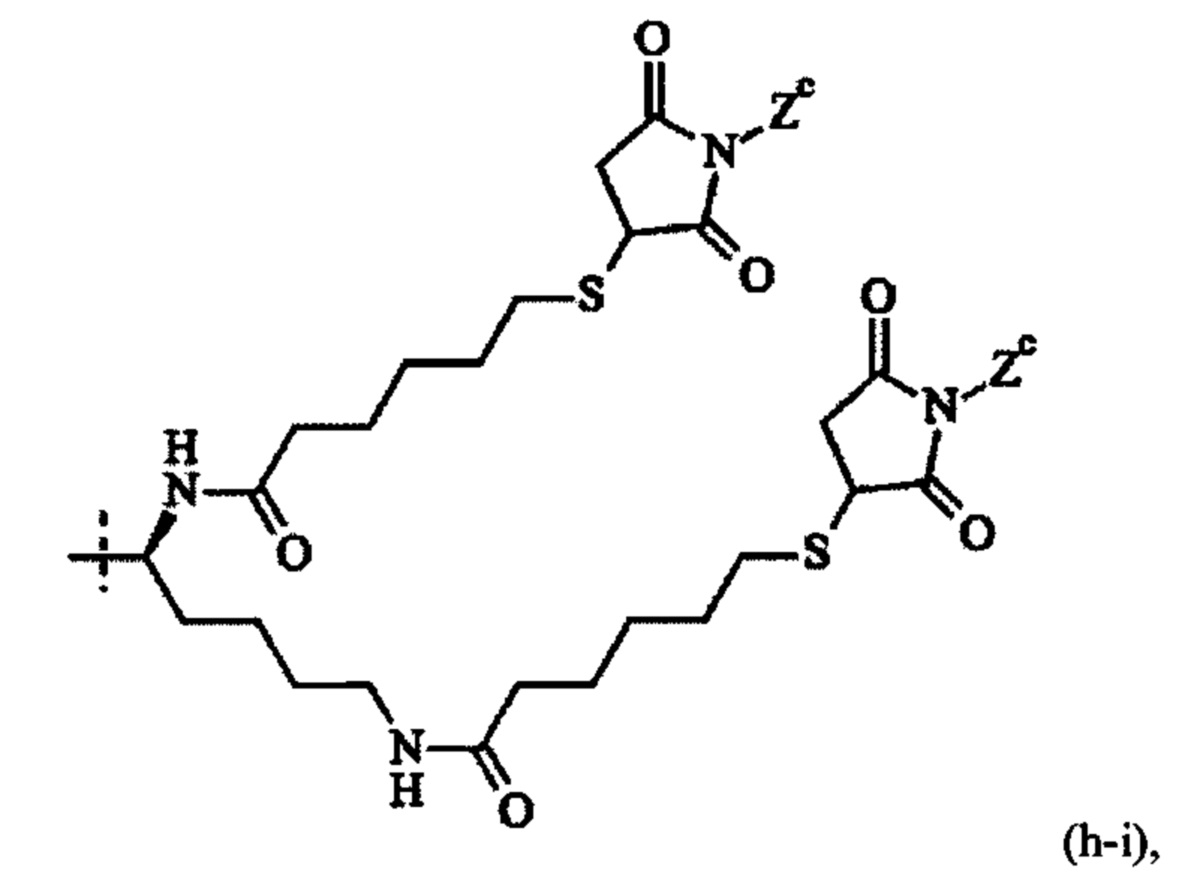
где
пунктирная линия показывает присоединение к -L2-; и
каждый -Zc представляет собой составляющую
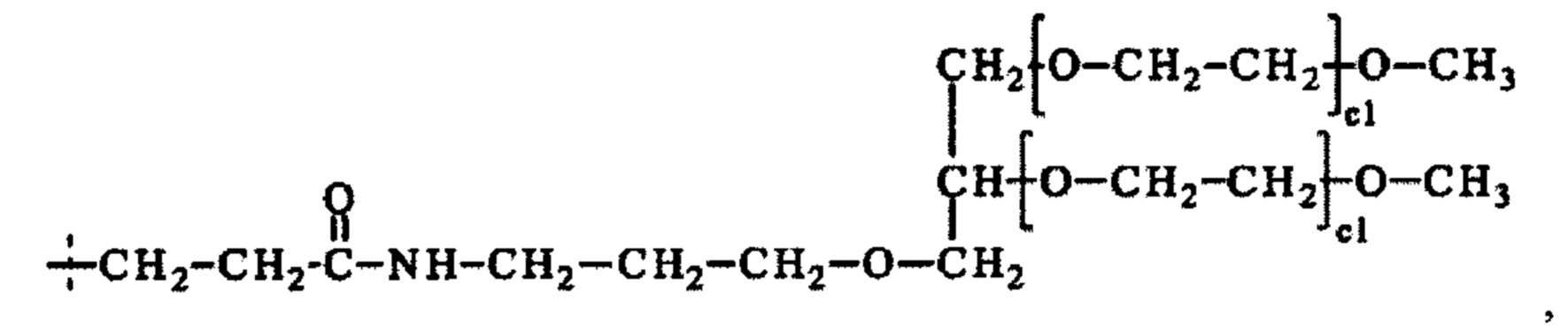
каждый c1 независимо представляет собой целое число в интервале от 200 до 250.
Предпочтительно оба c1 формулы (h-i) являются одинаковыми.
Предпочтительно оба c1 формулы (h-i) равны около 225.
Предпочтительно, CNP пролекарство согласно настоящему изобретению имеет формулу (Ia).
Предпочтительно CNP пролекарство согласно настоящему изобретению имеет формулу (Ia) с х=1.
В предпочтительном варианте выполнения настоящего изобретения CNP пролекарство согласно настоящему изобретению имеет формулу (IIe)
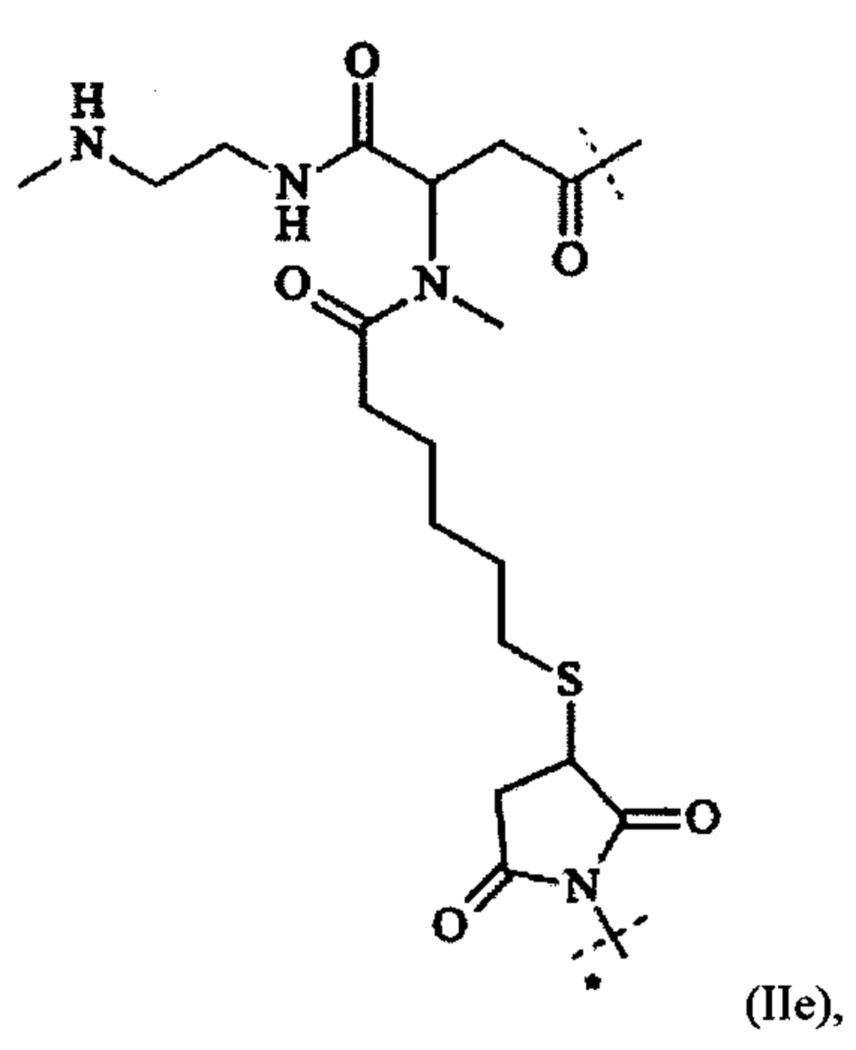
где
неотмеченная пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой CNP составляющую, путем образования амидной связи; и
пунктирная линия, отмеченная звездочкой, обозначает присоединение к составляющей
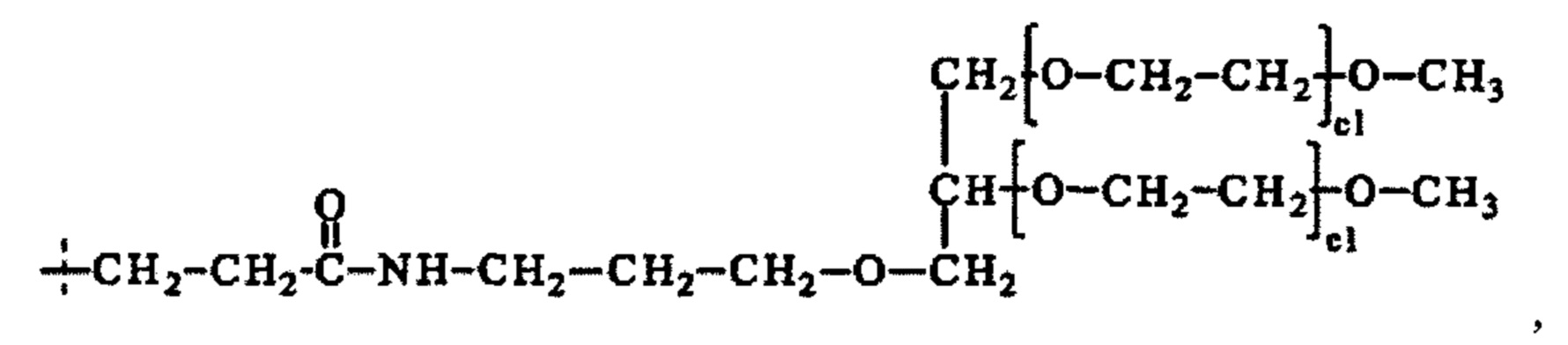
где
каждый c1 независимо представляет собой целое число в интервале от 400 до 500.
Предпочтительно, c1 формулы (IIе) равно около 450.
В равно предпочтительном варианте выполнения настоящего изобретения CNP пролекарство согласно настоящему изобретению имеет формулу (IIe-i)
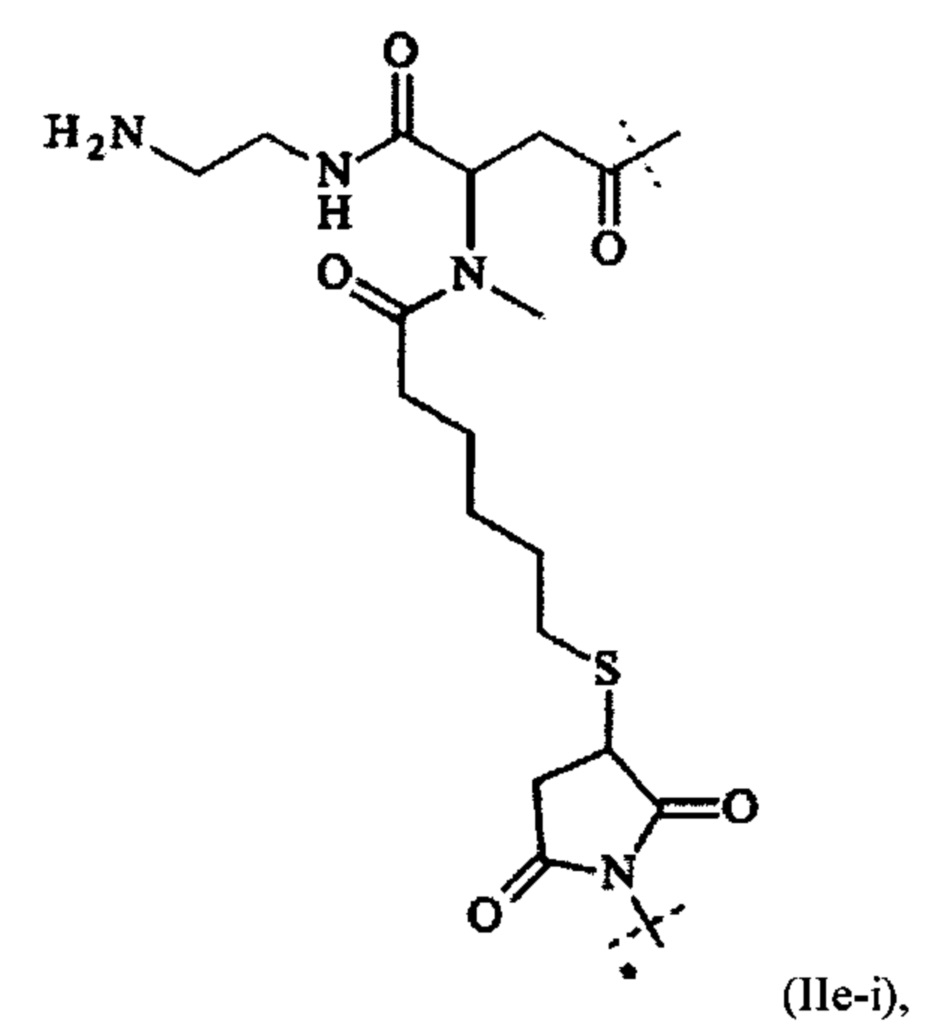
где
неотмеченная пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой CNP составляющую, путем образования амидной связи; и
пунктирная линия, отмеченная звездочкой, обозначает присоединение к составляющей
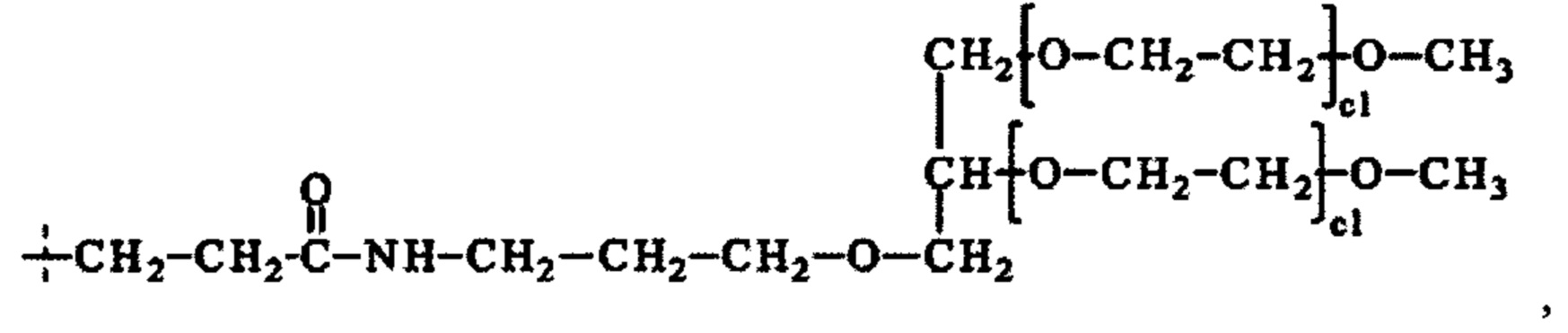
где
каждый c1 независимо представляет собой целое число в интервале от 400 до 500.
Предпочтительно, c1 формулы (IIe-i) равно около 450.
В другом равно предпочтительном варианте выполнения настоящего изобретения CNP пролекарство согласно настоящему изобретению имеет формулу (IIe-ii)
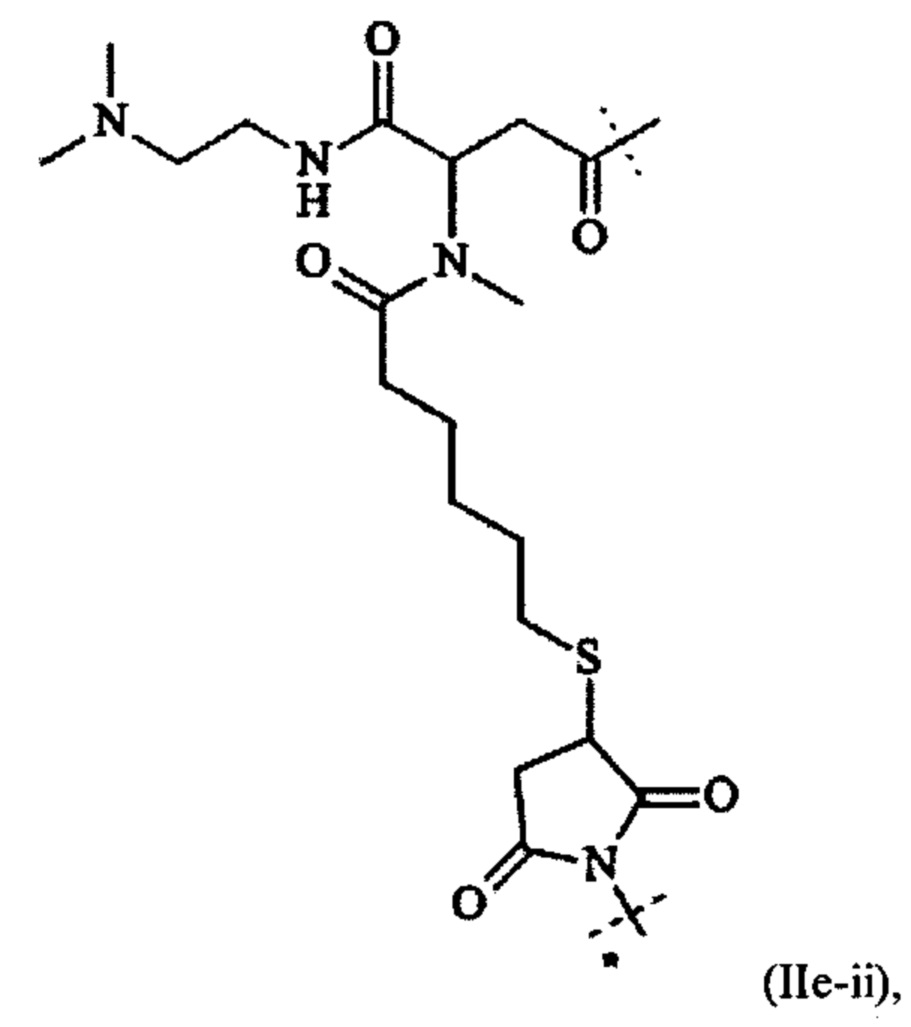
где
неотмеченная пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой CNP составляющую, путем образования амидной связи; и
пунктирная линия, отмеченная звездочкой, обозначает присоединение к составляющей
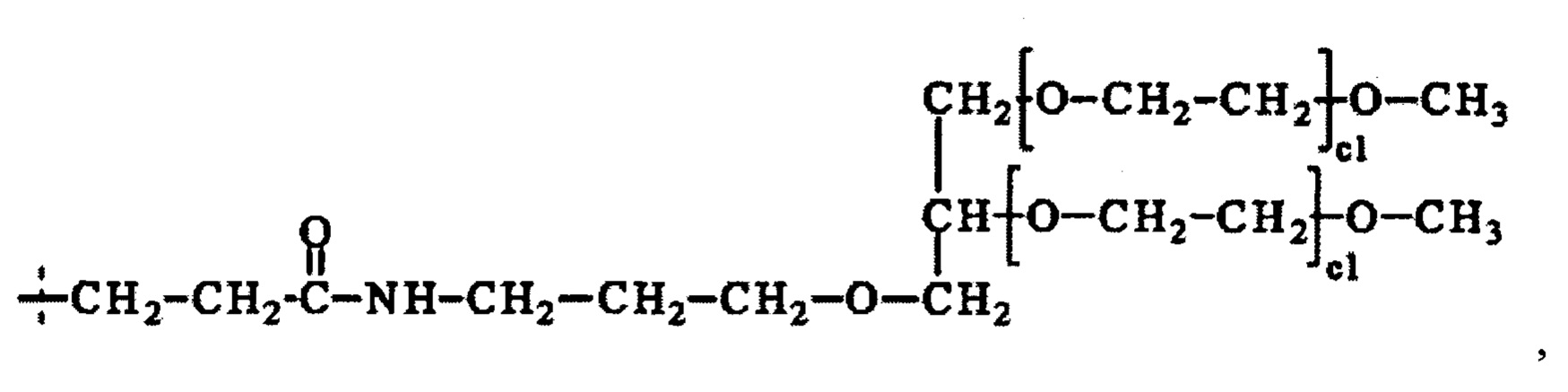
где
каждый c1 независимо представляет собой целое число в интервале от 400 до 500.
Предпочтительно, c1 формулы (IIe-ii) равно около 450.
В одном варианте выполнения настоящего изобретения CNP составляющая CNP пролекарства формулы (IIe), (IIe-i) и (IIe-ii) имеет последовательность SEQ ID NO:25.
В другом варианте выполнения настоящего изобретения CNP составляющая CNP пролекарства формулы (IIe), (IIe-i) и (IIe-ii) имеет последовательность SEQ ID NO:30.
В предпочтительном варианте выполнения настоящего изобретения CNP составляющая CNP пролекарства формулы (IIe), (IIe-i) и (IIe-ii) имеет последовательность SEQ ID NO:24.
В одном варианте выполнения настоящего изобретения CNP составляющая присоединяется к -L1- в CNP про лекарстве формулы (IIe), (IIe-i) и (IIe-ii) через атом азота N-терминальной аминной функциональной группы CNP.
В предпочтительном варианте выполнения настоящего изобретения CNP составляющая присоединяется к -L1- в CNP пролекарстве формулы (IIe), (IIe-i) и (IIe-ii) через атом азота, обеспеченный аминной функциональной группой боковой цепи лизина CNP.
В одном варианте выполнения настоящего изобретения эта боковая цепь лизина не является частью кольца, образованного дисульфидным мостиком между цистеиновыми остатками в положениях 22 и 38, если CNP составляющая имеет последовательность SEQ ID NO:24.
Соответственно, в одном варианте выполнения настоящего изобретения CNP составляющая соединена с -L1- в CNP пролекарстве формулы (IIe), (IIe-i) и (IIe-ii) через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 9, если CNP имеет последовательность SEQ ID NO:24.
В другом варианте выполнения настоящего изобретения CNP составляющая соединена с -L1- в CNP пролекарстве формулы (IIe), (IIe-i) и (IIe-ii) через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 11, если CNP имеет последовательность SEQ ID NO:24.
В другом варианте выполнения настоящего изобретения CNP составляющая соединена с -L1- в CNP пролекарстве формулы (IIe), (IIe-i) и (IIe-ii) через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 15, если CNP имеет последовательность SEQ ID NO:24.
В другом варианте выполнения настоящего изобретения CNP составляющая соединена с -L1- в CNP пролекарстве формулы (IIe), (IIe-i) и (IIe-ii) через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 16, если CNP имеет последовательность SEQ ID NO:24.
В другом варианте выполнения настоящего изобретения CNP составляющая соединена с -L1- в CNP пролекарстве формулы (IIe), (IIe-i) и (IIe-ii) через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 20, если CNP имеет последовательность SEQ ID NO:24.
В предпочтительном варианте выполнения настоящего изобретения боковая цепь лизина для присоединения к остатку CNP пролекарства формулы (IIe), (IIe-i) и (IIe-ii) является частью кольца, образованного дисульфидным мостиком между цистеиновыми остатками в положениях 22 и 38, если CNP составляющая имеет последовательность SEQ ID NO:24.
Соответственно, в предпочтительном варианте выполнения настоящего изобретения CNP составляющая соединена с -L1- в CNP пролекарстве формулы (IIe), (IIe-i) и (IIe- ii) через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 26, если CNP имеет последовательность SEQ ID NO:24.
Понятно, что упомянутые выше положения цистеинов и лизинов меняются в зависимости от длины CNP составляющей, и что специалисту в данной области не составит труда идентифицировать соответствующие цистеины и лизин в более длинных или более коротких вариантах CNP составляющей, и также понятно, что, например некоторые лизины могут отсутствовать в более коротких CNP составляющих. Кроме того, понятно, что в результате, например, сайт-направленного мутагенеза может быть больше остатков лизина в необразующей кольцо части и/или образующей кольцо части CNP составляющей.
В предпочтительном варианте выполнения настоящего изобретения CNP пролекарство согласно настоящему изобретению имеет формулу (IIe), где c1 равно около 450, CNP составляющая имеет последовательность SEQ ID NO:24 и присоединяется к -L1- через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 26.
В другом предпочтительном варианте выполнения настоящего изобретения CNP пролекарство согласно настоящему изобретению имеет формулу (IIe-i), где c1 равно около 450, CNP составляющая имеет последовательность SEQ ID NO:24 и присоединяется к -L1- через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 26.
В другом предпочтительном варианте выполнения настоящего изобретения CNP пролекарство согласно настоящему изобретению имеет формулу (IIe-ii), где c1 равно около 450, CNP составляющая имеет последовательность SEQ ID NO:24 и присоединяется к -L1- через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 26.
Соответственно, в предпочтительном варианте выполнения настоящего изобретения CNP пролекарство согласно настоящему изобретению имеет формулу (IIe’)
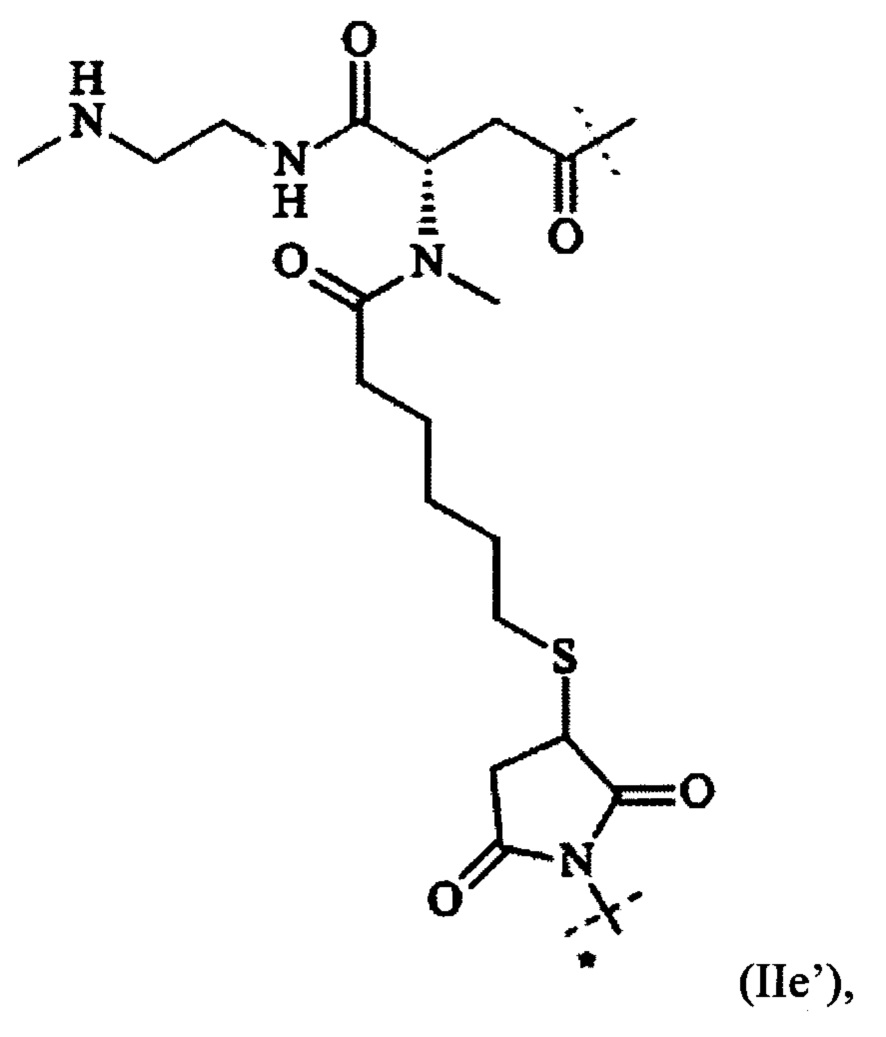
где
непомеченная пунктирная линия показывает присоединение к атому азота, обеспеченному боковой цепью лизина в положении 26 составляющей CNP последовательности SEQ ID NO:24 путем образования амидной связи; и
пунктирная линия, отмеченная звездочкой, обозначает присоединение к составляющей
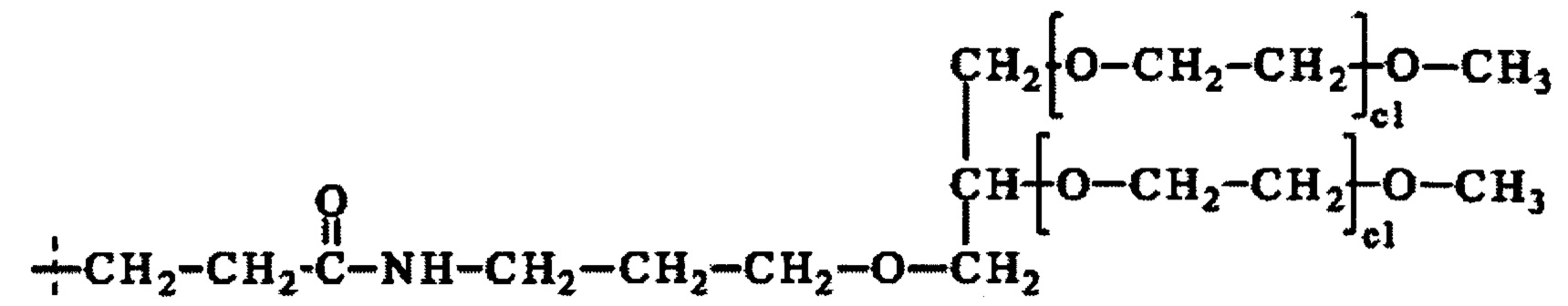
где
каждый c1 независимо представляет собой целое число в интервале от 400 до 500.
Предпочтительно, каждый c1 формулы (IIe') равно около 450.
В другом предпочтительном варианте выполнения настоящего изобретения CNP пролекарство согласно настоящему изобретению имеет формулу (IIe-i’)
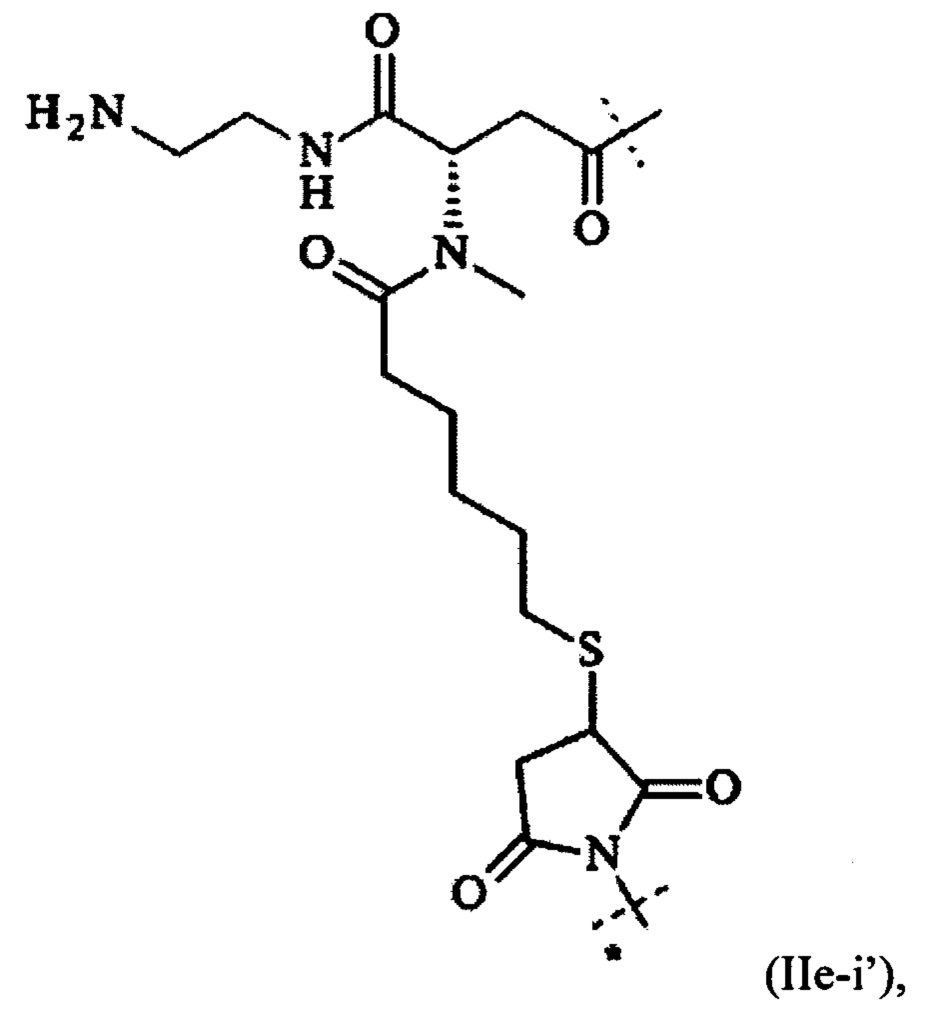
где
непомеченная пунктирная линия показывает присоединение к атому азота, обеспеченному боковой цепью лизина в положении 26 составляющей CNP последовательности SEQ ID NO:24 путем образования амидной связи; и
пунктирная линия, отмеченная звездочкой, обозначает присоединение к составляющей
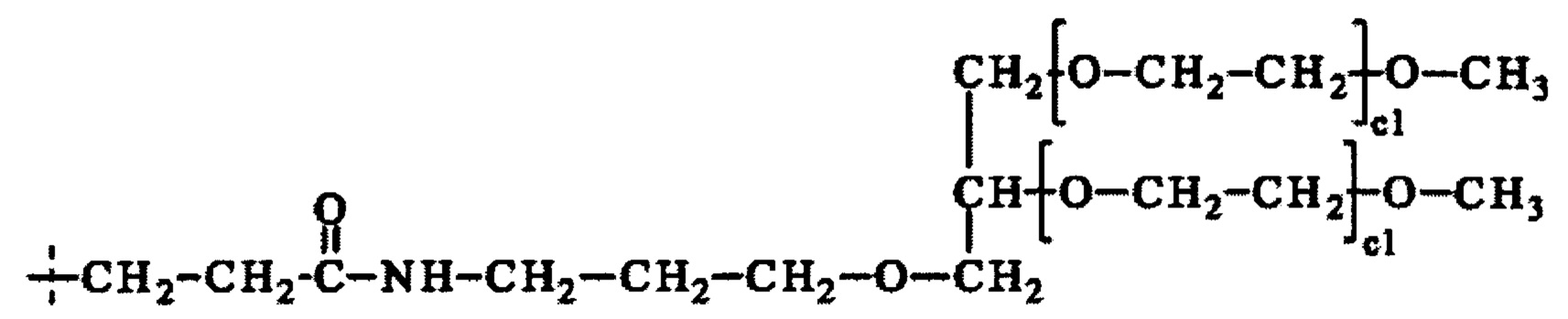
где
каждый c1 независимо представляет собой целое число в интервале от 400 до 500.
Предпочтительно, каждый c1 формулы (IIe-i') равно около 450.
В другом предпочтительном варианте выполнения настоящего изобретения CNP пролекарство согласно настоящему изобретению имеет формулу (IIe-ii’)
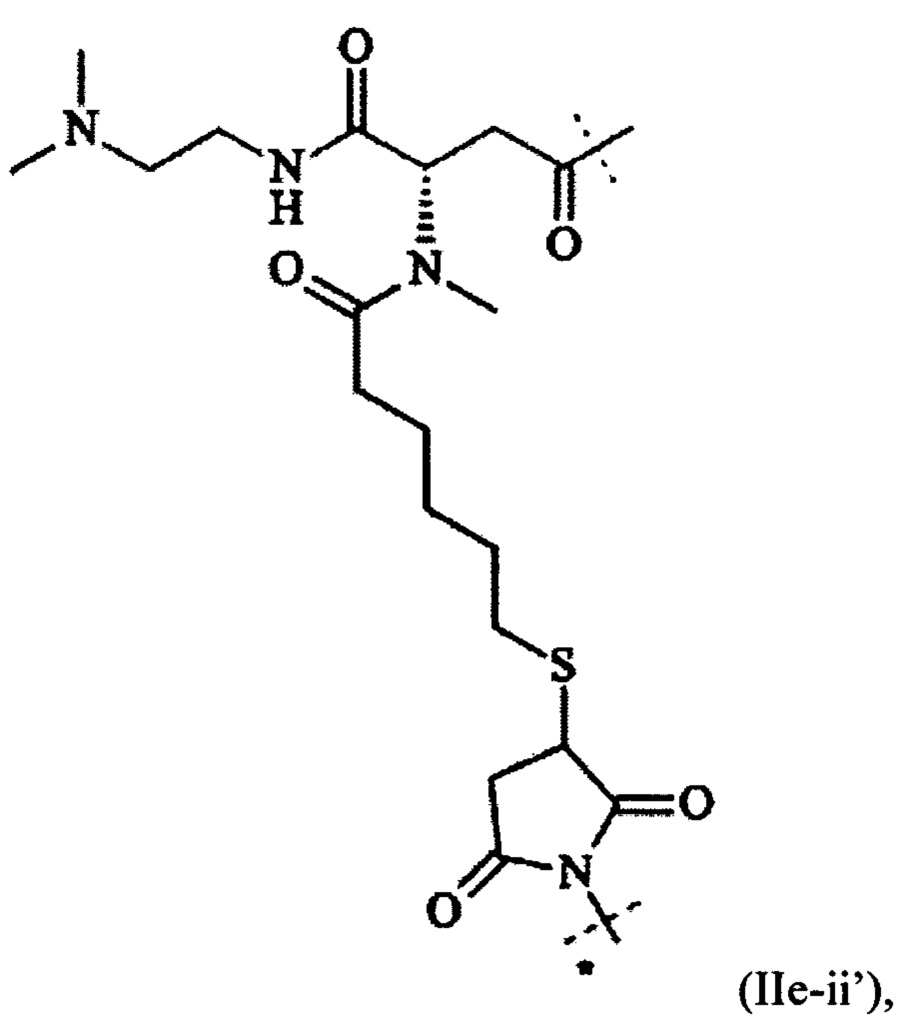
где
непомеченная пунктирная линия показывает присоединение к атому азота, обеспеченному боковой цепью лизина в положении 26 составляющей CNP последовательности SEQ ID NO:24 путем образования амидной связи; и
пунктирная линия, отмеченная звездочкой, обозначает присоединение к составляющей
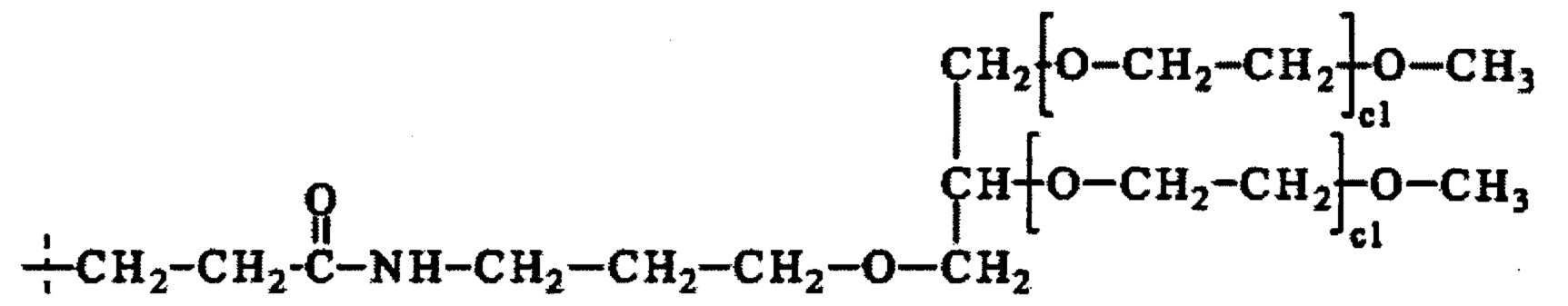
где
каждый c1 независимо представляет собой целое число в интервале от 400 до 500.
Предпочтительно, каждый c1 формулы (IIe-i') равно около 450.
В другом предпочтительном варианте выполнения настоящего изобретения CNP пролекарство согласно настоящему изобретению имеет формулу (IIf)
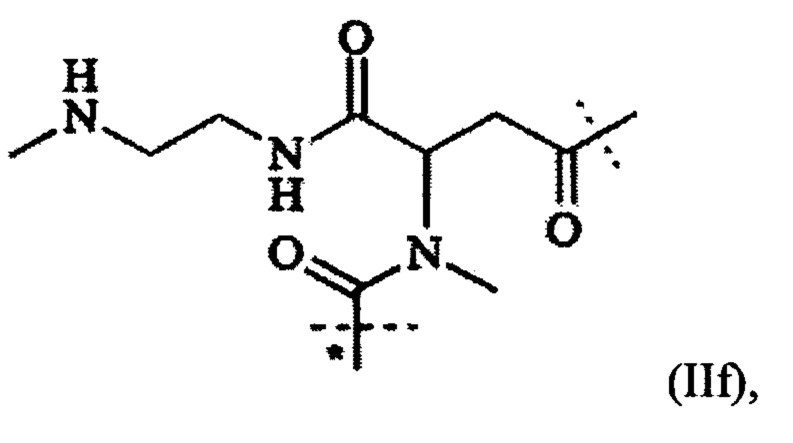
где
неотмеченная пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой CNP составляющую, путем образования амидной связи; и
пунктирная линия, отмеченная звездочкой, обозначает присоединение к -Z, имеющей структуру
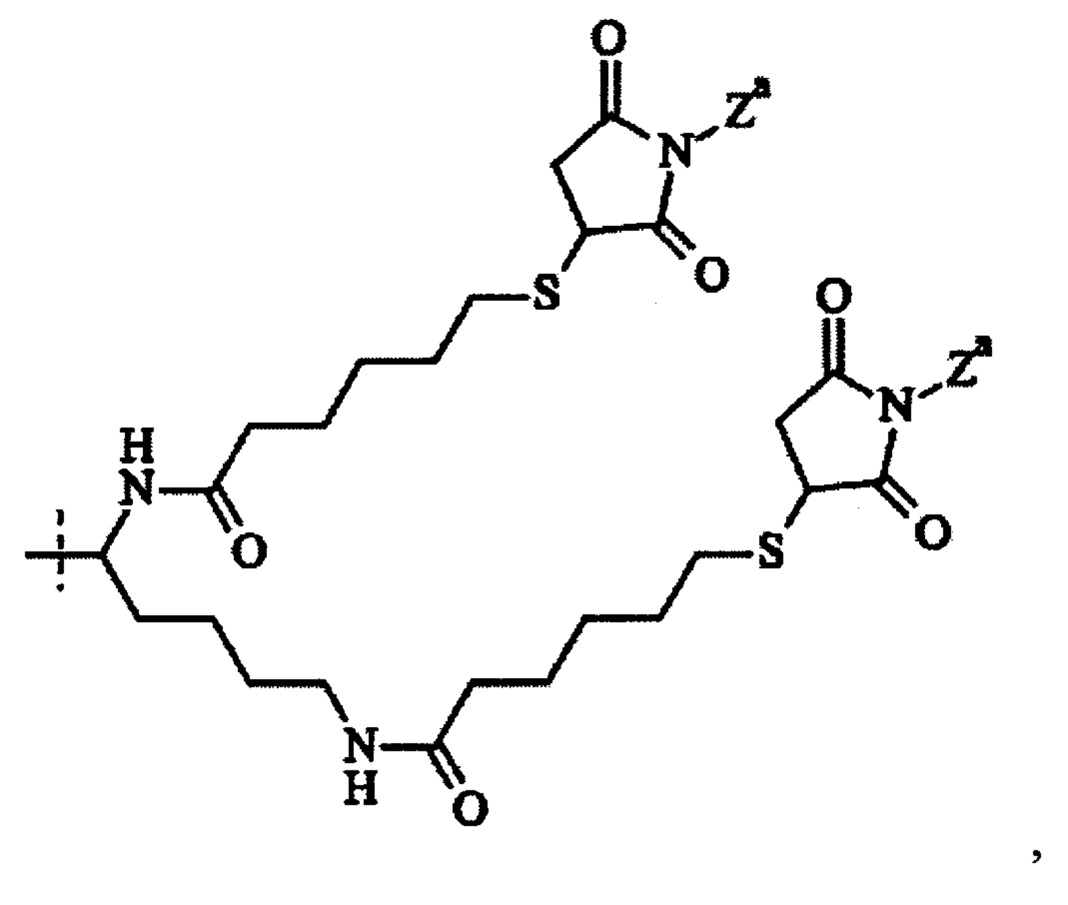
где
каждый -Za представляет собой
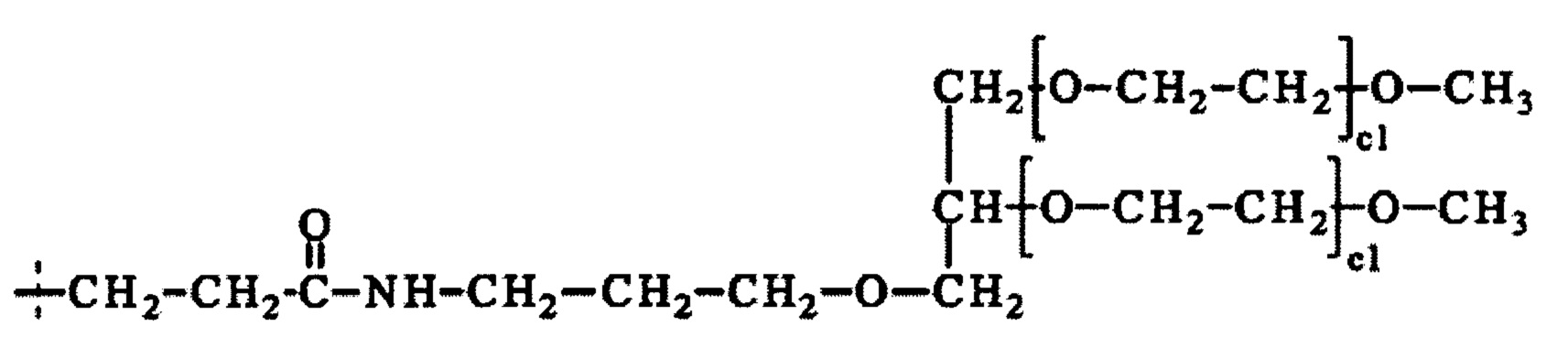
где
каждый c1 независимо представляет собой целое число в интервале от 200 до 250; предпочтительно каждый n равно около 225.
Предпочтительно, каждый c1 формулы (IIf) равно около 225.
В другом предпочтительном варианте выполнения настоящего изобретения CNP пролекарство согласно настоящему изобретению имеет формулу (IIf-i)
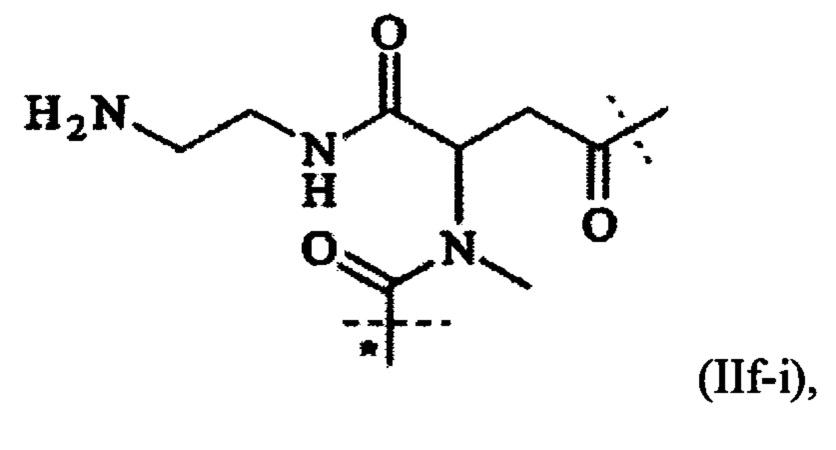
где
неотмеченная пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой CNP составляющую, путем образования амидной связи; и
пунктирная линия, отмеченная звездочкой, обозначает присоединение к -Z, имеющей структуру
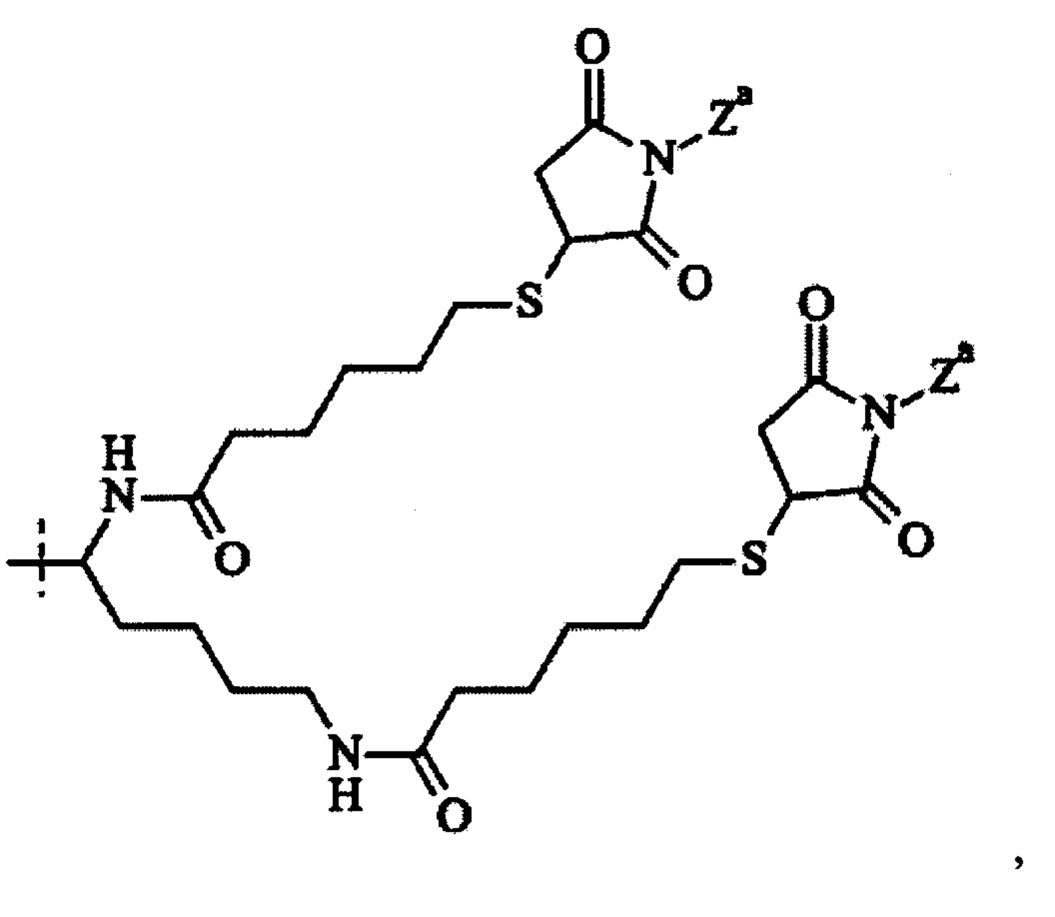
где
каждый -Za представляет собой
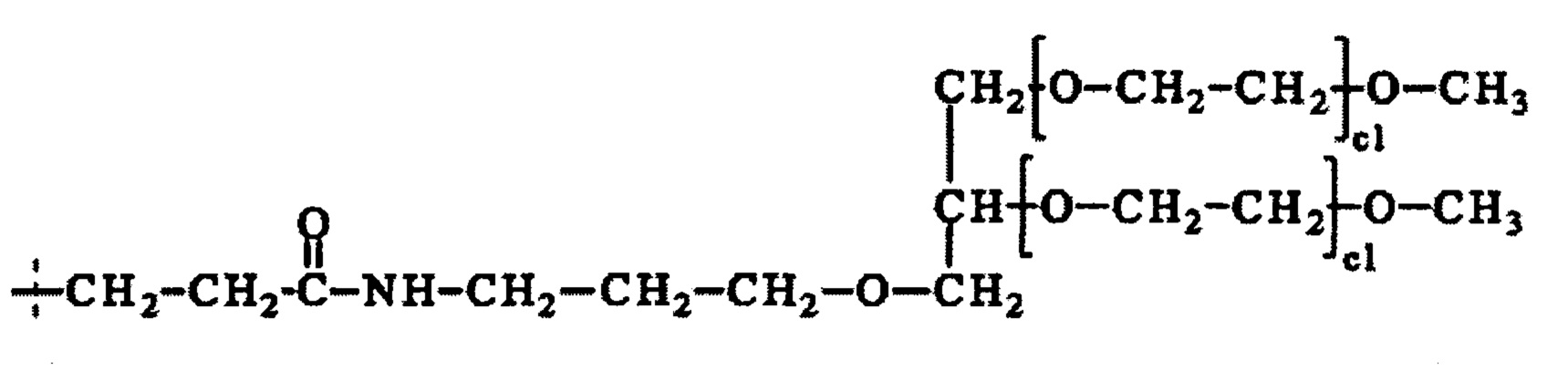
где
каждый c1 независимо представляет собой целое число в интервале от 200 до 250; предпочтительно каждый n равно около 225.
Предпочтительно, каждый c1 формулы (IIf-i) равно около 225.
В другом предпочтительном варианте выполнения настоящего изобретения CNP пролекарство согласно настоящему изобретению имеет формулу (IIf-ii)
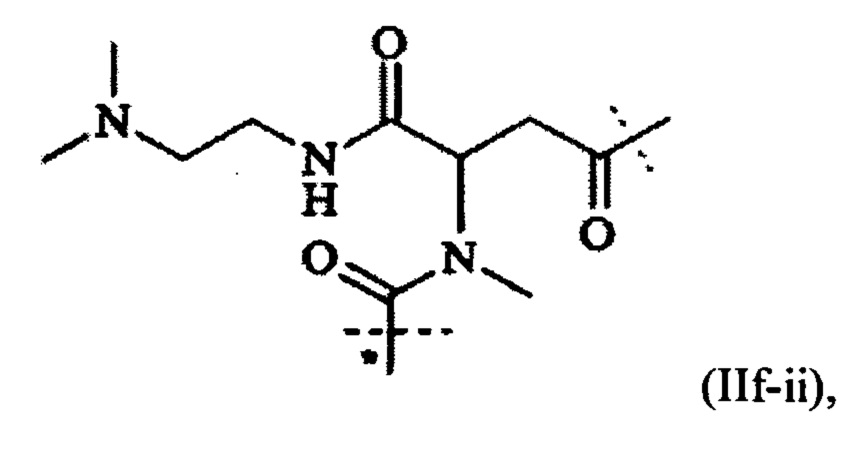
где
неотмеченная пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой CNP составляющую, путем образования амидной связи; и
пунктирная линия, отмеченная звездочкой, обозначает присоединение к -Z, имеющей структуру
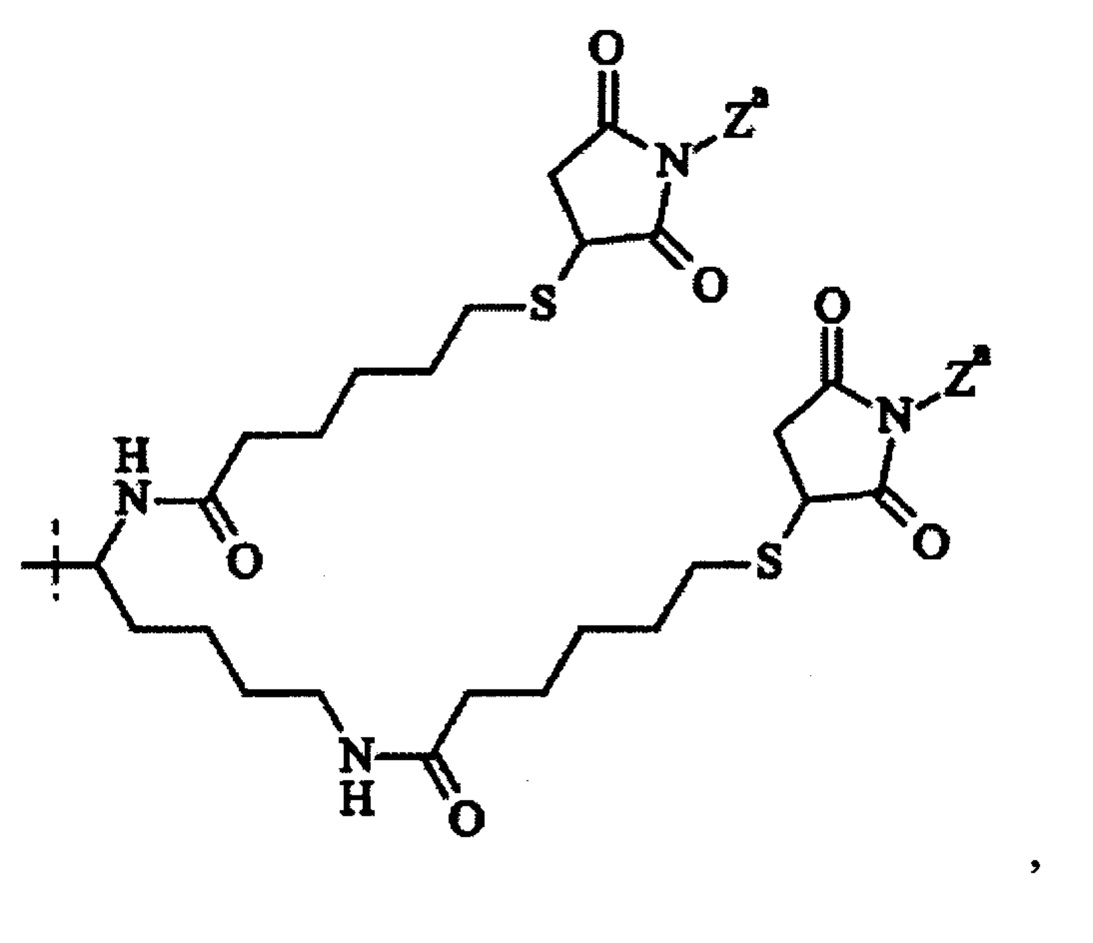
где
каждый -Za представляет собой
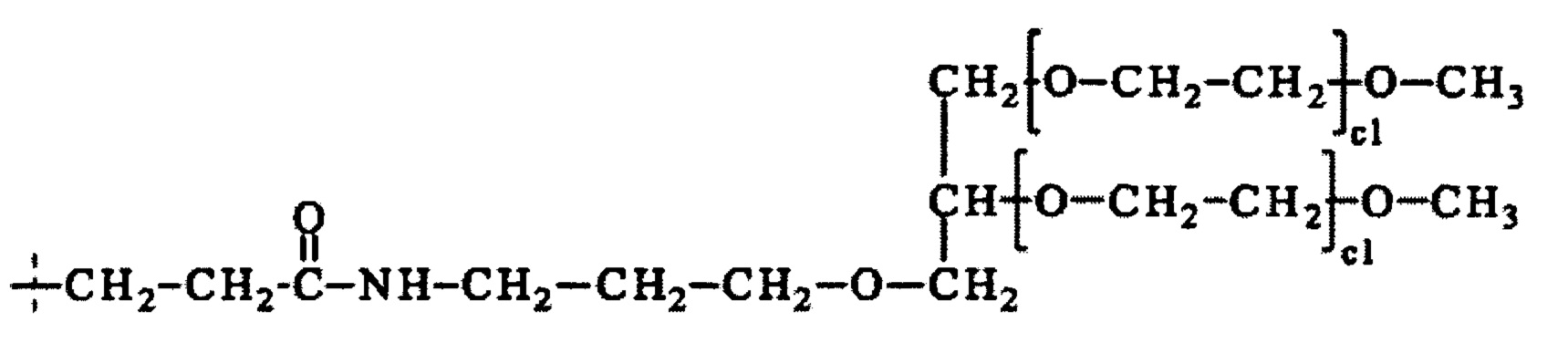
где
каждый c1 независимо представляет собой целое число в интервале от 200 до 250; предпочтительно каждый n равно около 225.
Предпочтительно, каждый c1 формулы (IIf-ii) равно около 225.
В одном варианте выполнения настоящего изобретения CNP составляющая CNP пролекарства формулы (IIf), (IIf-i) и (IIf-ii) имеет последовательность SEQ ID NO:25.
В предпочтительном варианте выполнения настоящего изобретения CNP составляющая CNP пролекарства формулы (IIf), (IIf-i) и (IIf-ii) имеет последовательность SEQ ID NO:24.
В одном варианте выполнения настоящего изобретения CNP составляющая присоединяется к -L1- в CNP пролекарстве формулы (IIf), (IIf-i) и (IIf-ii) через атом азота N-терминальной аминной функциональной группы CNP.
В предпочтительном варианте выполнения настоящего изобретения CNP составляющая присоединяется к -L1- в CNP пролекарстве формулы (IIf), (IIf-i) и (IIf-ii) через атом азота, обеспеченный аминной функциональной группой боковой цепи лизина CNP.
В одном варианте выполнения настоящего изобретения эта боковая цепь лизина не является частью кольца, образованного дисульфидным мостиком между цистеиновыми остатками в положениях 22 и 38, если CNP составляющая имеет последовательность SEQ ID NO:24.
Соответственно, в одном варианте выполнения настоящего изобретения CNP составляющая соединена с -L1- в CNP пролекарстве формулы (IIf), (IIf-i) и (IIf-ii) через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 9, если CNP имеет последовательность SEQ ID NO:24.
В другом варианте выполнения настоящего изобретения CNP составляющая соединена с -L1- в CNP пролекарстве формулы (IIf), (IIf-i) и (IIf-ii) через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 11, если CNP имеет последовательность SEQ ID NO:24.
В другом варианте выполнения настоящего изобретения CNP составляющая соединена с -L1- в CNP пролекарстве формулы (IIf), (IIf-i) и (IIf-ii) через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 15, если CNP имеет последовательность SEQ ID NO:24.
В другом варианте выполнения настоящего изобретения CNP составляющая соединена с -L1- в CNP пролекарстве формулы (IIf), (IIf-i) и (IIf-ii) через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 16, если CNP имеет последовательность SEQ ID NO: 24.
В другом варианте выполнения настоящего изобретения CNP составляющая соединена с -L1- в CNP пролекарстве формулы (IIf), (IIf-i) и (IIf-ii) через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 20, если CNP имеет последовательность SEQ ID NO: 24.
В предпочтительном варианте выполнения настоящего изобретения боковая цепь лизина для присоединения к остатку CNP пролекарства формулы (IIf), (IIf-i) и (IIf-ii) является частью кольца, образованного дисульфидным мостиком между цистеиновыми остатками в положениях 22 и 38, если CNP составляющая имеет последовательность SEQ ID NO: 24.
Соответственно, в предпочтительном варианте выполнения настоящего изобретения CNP составляющая соединена с -L1- в CNP пролекарстве формулы (IIf), (IIf-i) и (IIf-ii) через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 26, если CNP имеет последовательность SEQ ID NO: 24.
Понятно, что упомянутые выше положения цистеинов и лизинов меняются в зависимости от длины CNP составляющей, и что специалисту в данной области не составит труда идентифицировать соответствующие цистеины и лизин в более длинных или более коротких вариантах CNP составляющей, и также понятно, что, например, некоторые лизины могут отсутствовать в более коротких CNP составляющих. Кроме того, понятно, что в результате, например, сайт-направленного мутагенеза может быть больше остатков лизина в необразующей кольцо части и/или образующей кольцо части CNP составляющей.
В предпочтительном варианте выполнения настоящего изобретения CNP про лекарство согласно настоящему изобретению имеет формулу (IIf), где c1 равно около 225, CNP составляющая имеет последовательность SEQ ID NO: 24 и присоединяется к -L1- через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 26.
В другом предпочтительном варианте выполнения настоящего изобретения CNP пролекарство согласно настоящему изобретению имеет формулу (IIf-i), где c1 равно около 225, CNP составляющая имеет последовательность SEQ ID NO: 24 и присоединяется к -L1- через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 26.
В другом предпочтительном варианте выполнения настоящего изобретения CNP пролекарство согласно настоящему изобретению имеет формулу (IIf-ii), где c1 равно около 225, CNP составляющая имеет последовательность SEQ ID NO: 24 и присоединяется к -L1- через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 26.
В другом предпочтительном варианте выполнения настоящего изобретения CNP пролекарство согласно настоящему изобретению имеет формулу (IIf')
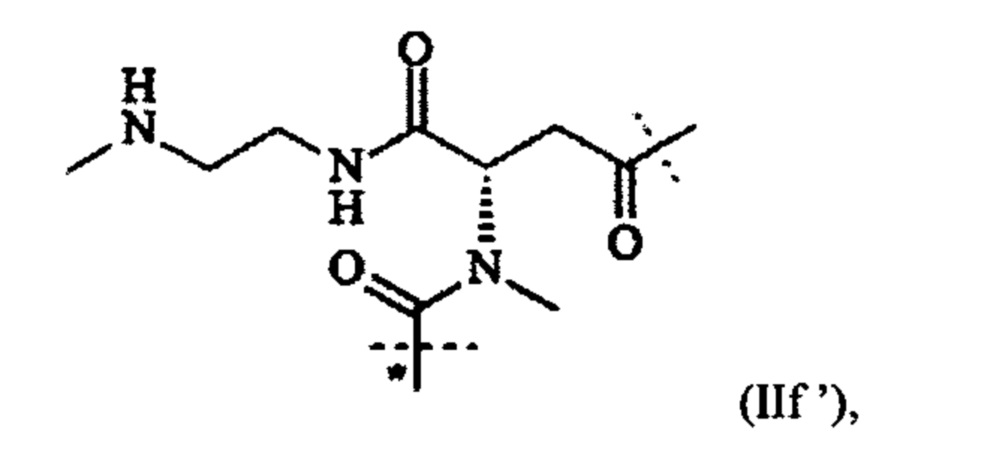
где
непомеченная пунктирная линия показывает присоединение к атому азота, обеспеченному боковой цепью лизина в положении 26 составляющей CNP последовательности SEQ ID NO: 24 путем образования амидной связи; и
пунктирная линия, отмеченная звездочкой, обозначает присоединение к -Z, имеющей структуру
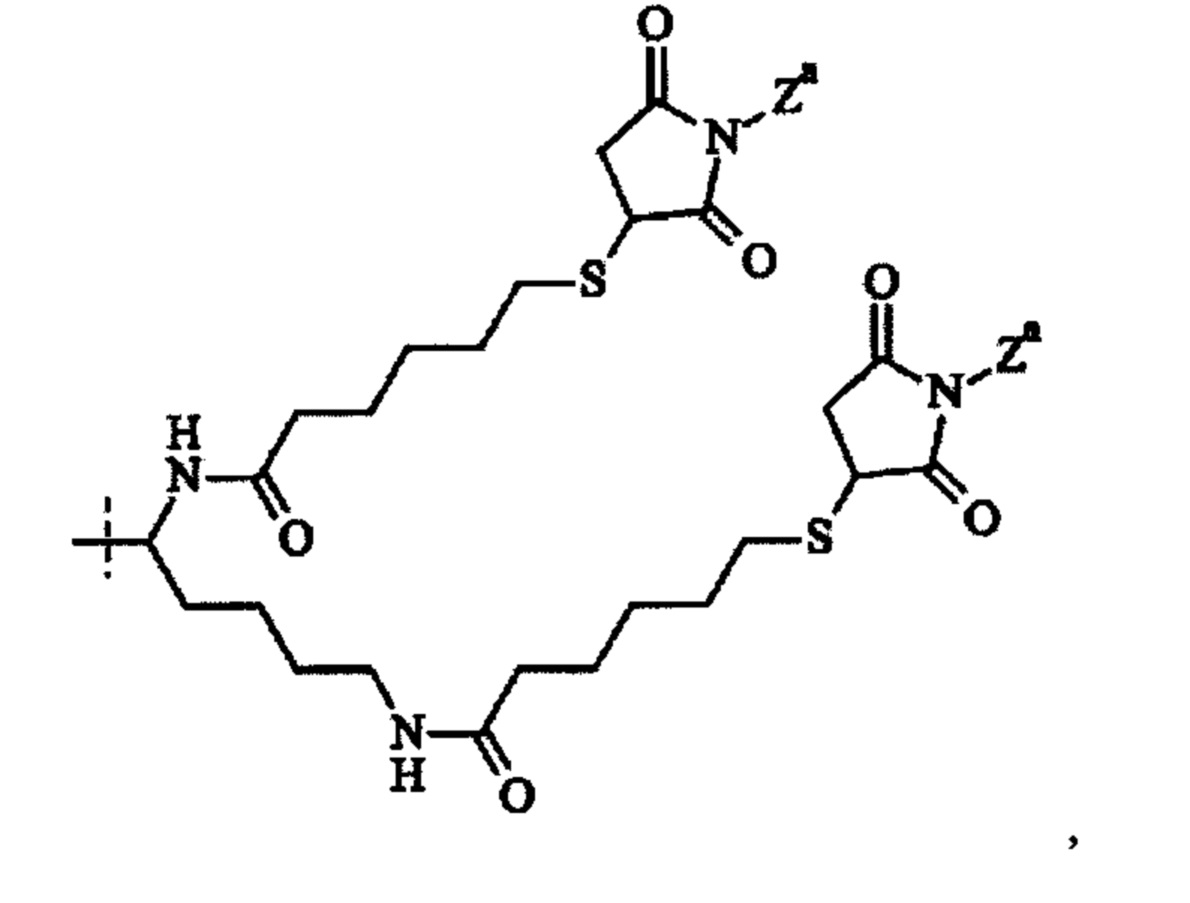
где
каждый Za представляет собой
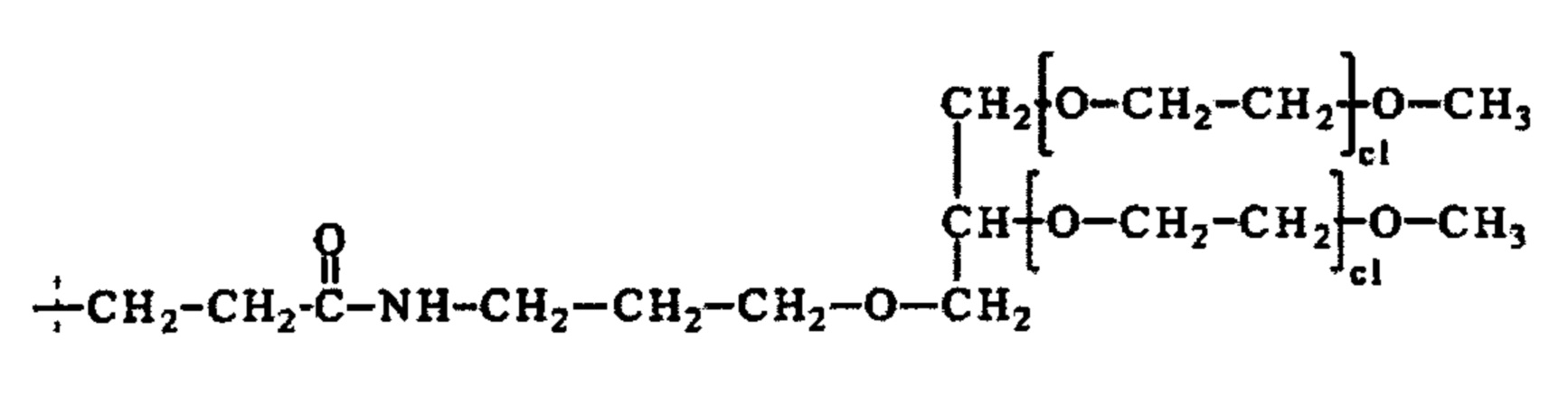
где
каждый c1 независимо представляет собой целое число в интервале от 200 до 250.
Предпочтительно, каждый c1 формулы (IIf') равно около 225.
В другом предпочтительном варианте выполнения настоящего изобретения CNP пролекарство согласно настоящему изобретению имеет формулу (IIf-i')
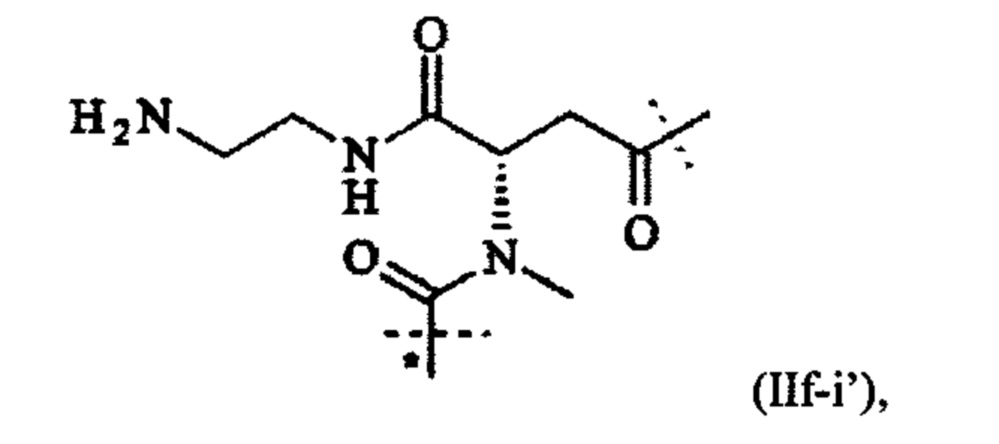
где
непомеченная пунктирная линия показывает присоединение к атому азота, обеспеченному боковой цепью лизина в положении 26 составляющей CNP последовательности SEQ ID NO: 24 путем образования амидной связи; и
пунктирная линия, отмеченная звездочкой, обозначает присоединение к -Z, имеющей структуру
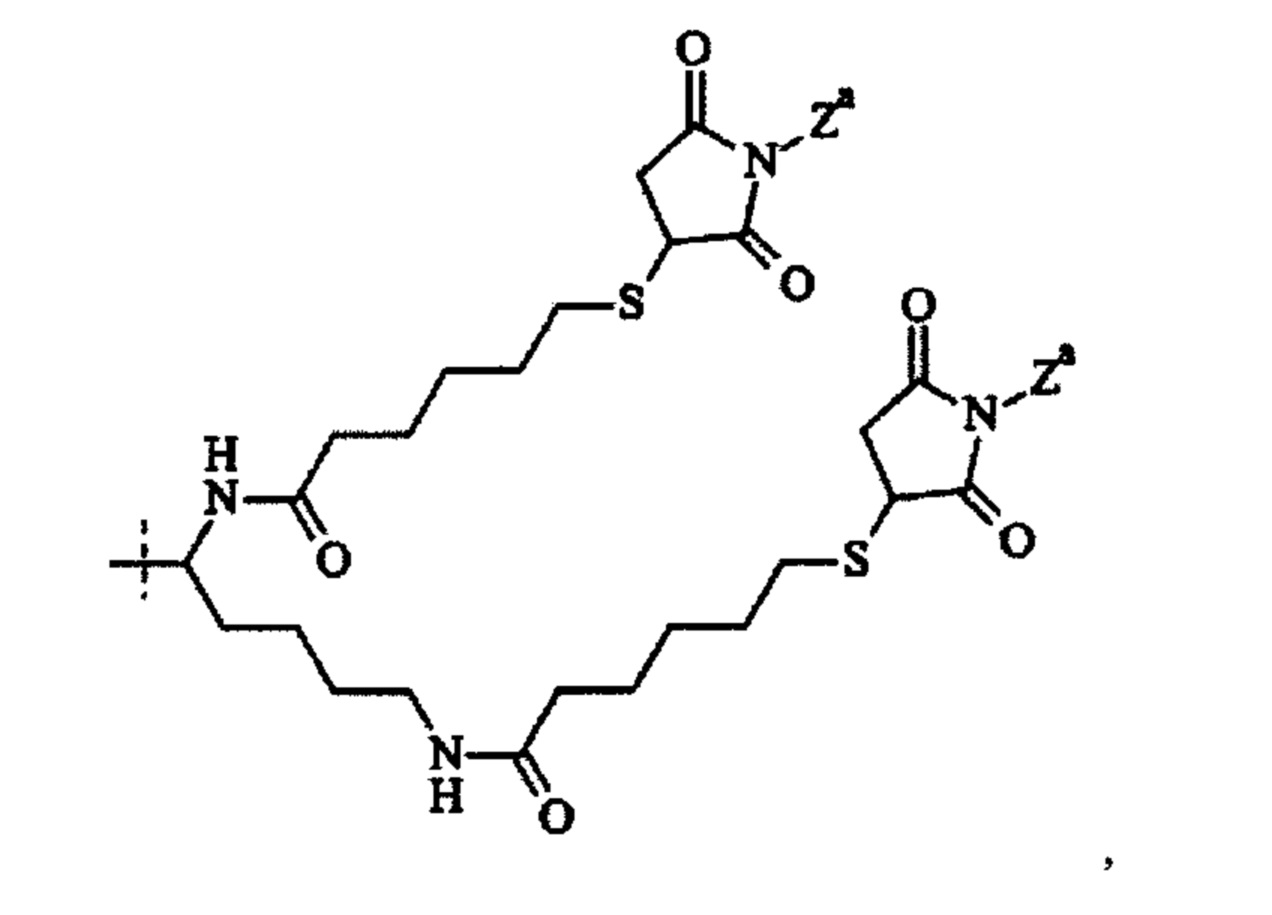
где
каждый Za представляет собой
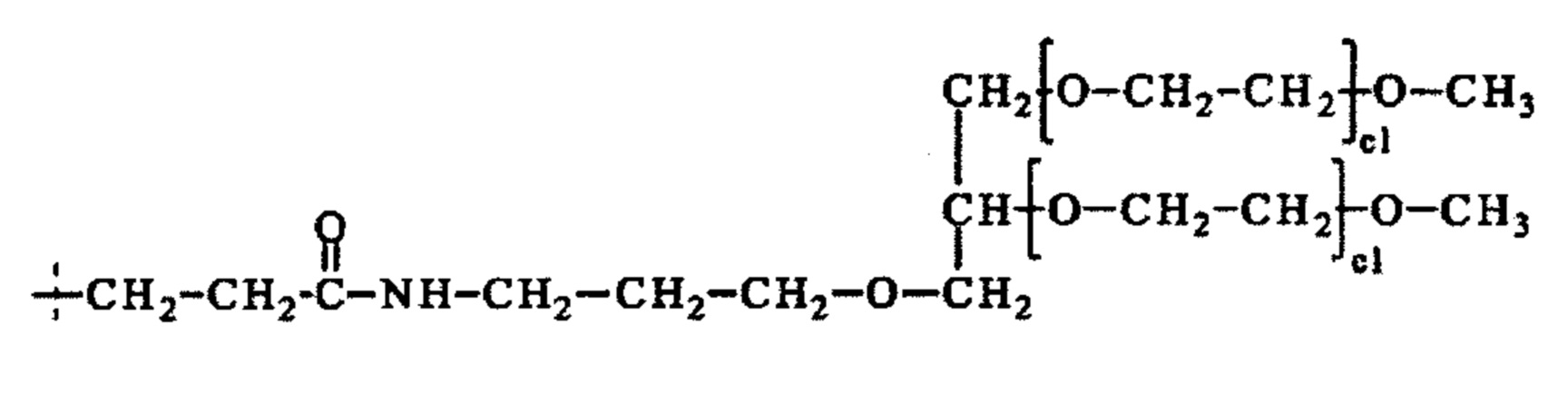
где
каждый c1 независимо представляет собой целое число в интервале от 200 до 250.
Предпочтительно, каждый c1 формулы (IIf-i') равно около 225.
В другом предпочтительном варианте выполнения настоящего изобретения CNP пролекарство согласно настоящему изобретению имеет формулу (IIf-ii')
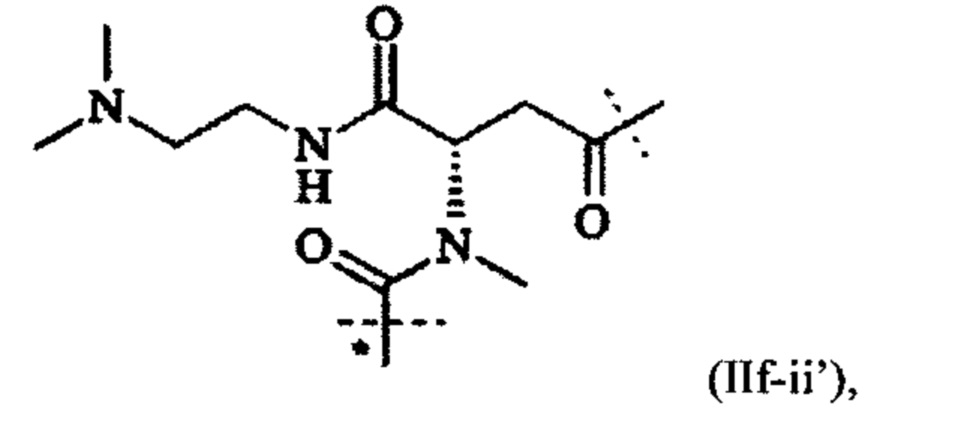
где
непомеченная пунктирная линия показывает присоединение к атому азота, обеспеченному боковой цепью лизина в положении 26 составляющей CNP последовательности SEQ ID NO: 24 путем образования амидной связи; и
пунктирная линия, отмеченная звездочкой, обозначает присоединение к -Z, имеющей структуру
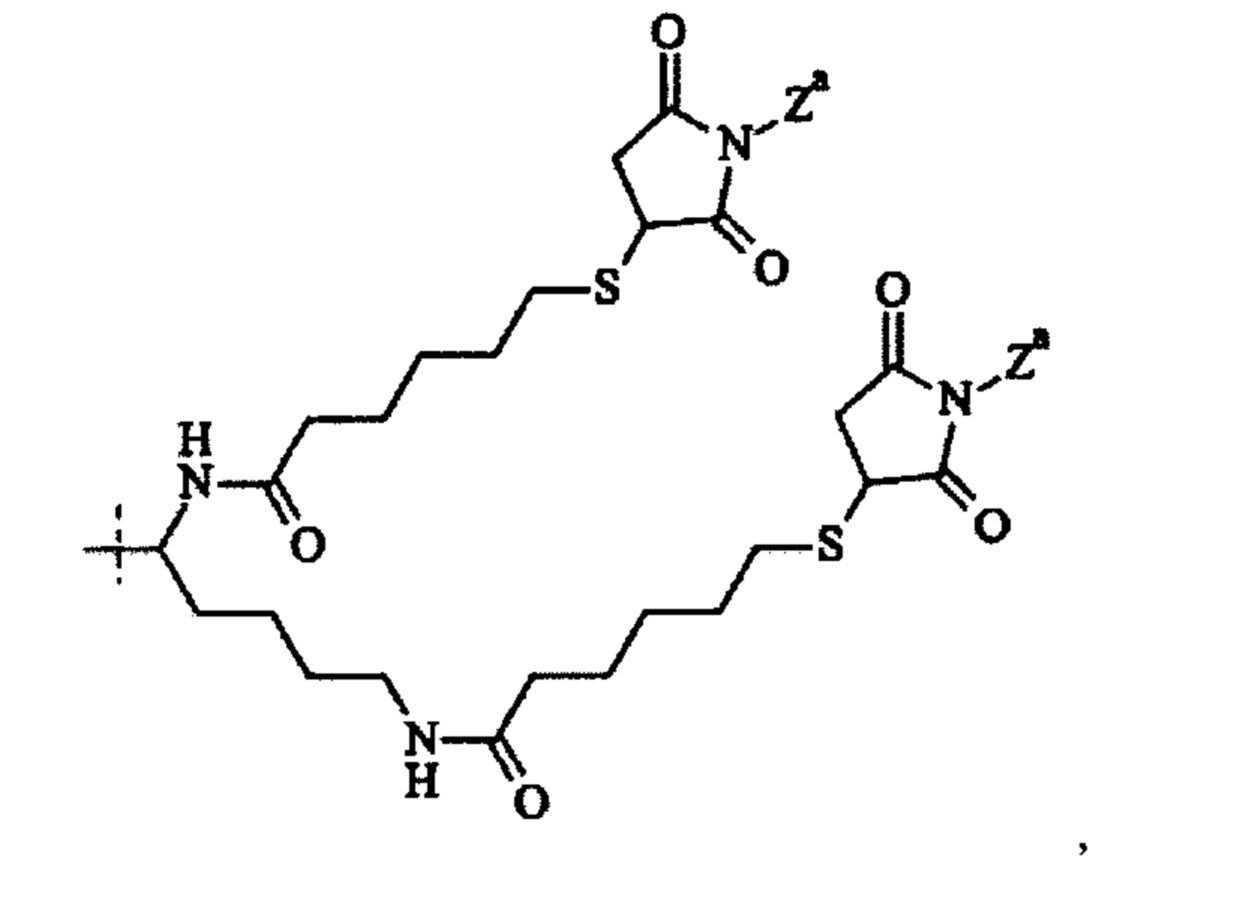
где
каждый Za представляет собой
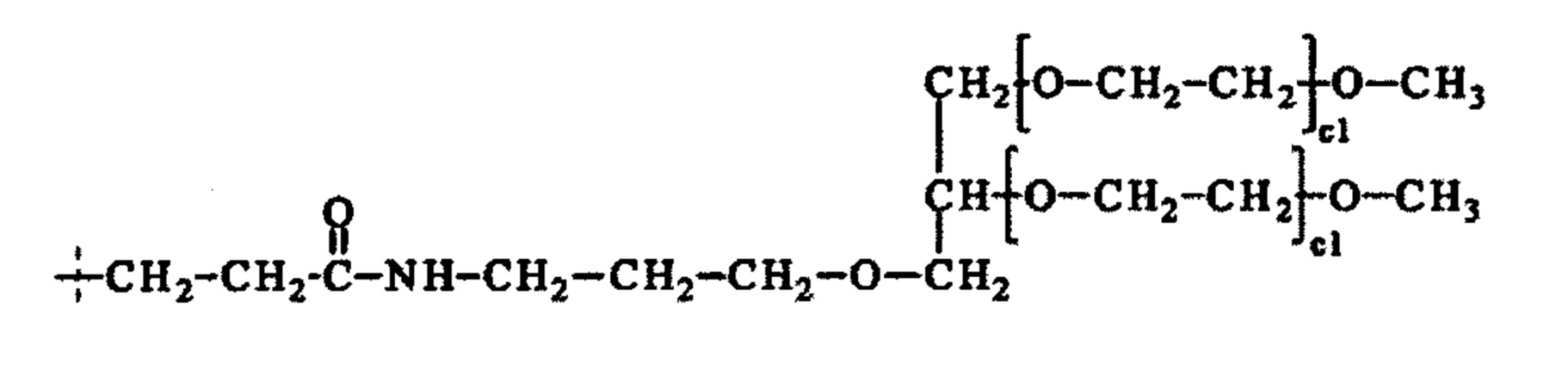
где
каждый c1 независимо представляет собой целое число в интервале от 200 до 250.
Предпочтительно, каждый c1 формулы (IIf-ii') равно около 225.
Таким образом было обнаружено, что комбинация обратимого присоединения -L1- к CNP составляющей через боковую цепь аминокислоты, локализованной в кольцевом фрагменте CNP, применения разветвленной составляющей -Z, имеющей молекулярную массу, равную по меньшей мере 10 кДа, и применения CNP составляющей больше чем CNP-22 приводит к CNP пролекарству с неожиданно длительным периодом полувысвобождения in vivo.
Носитель -Z' представляет собой не растворимый в воде полимер, даже более предпочтительно гидрогель. Предпочтительно, такой гидрогель содержит полимер, выбранный из группы, состоящей из 2-метакрилоил-оксиэтил фосфоилхолинов, поли(акриловых кислот), поли(акрилатов), поли(акриламидов), поли(алкилокси) полимеров, поли(амидов), поли(амидоаминов), поли(аминокислот), поли(ангидридов), поли(аспартамидов), поли(масляных кислот), поли(гликолевых кислот), полибутилентерефталатов, поли(капролактонов), поли(карбонатов), поли(цианоакрилатов), поли(диметилакриламидов), поли(сложных эфиров), поли(этиленов), поли(этиленгликолей), поли(этиленоксидов), поли(этилфосфатов), поли(этилоксазолинов), поли(гликолевых кислот), поли(гидроксиэтилакрилатов), поли(гидроксиэтил-оксазолинов), поли(гидроксиметакрилатов), поли(гидроксипропилметакриламидов), поли(гидроксипропил метакрилатов), поли(гидроксипропилоксазолинов), поли(иминокарбонатов), поли(молочных кислот), поли(сополимеров молочных и гликолевых кислот), поли(метакриламидов), поли(метакрилатов), поли(метилоксазолинов), поли(органофосфазенов), поли(ортосложных эфиров), поли(оксазолинов), поли(пропиленгликолей), поли(силоксанов), поли(уретанов), поли(виниловых спиртов), поли(виниламинов), поли(винилметиловых простых эфиров), поли(винилпирролидонов), силиконов, целлюлоз, карбометил целлюлоз, гидроксипропил метилцеллюлоз, хитинов, хитозанов, декстранов, декстринов, желатинов, гиалуроновых кислот и производных, функционализированных гиалуроновых кислот, маннанов, пектинов, рамногалактуронанов, крахмалов, гидроксиалкил крахмалов, гидроксиэтил крахмалов и других полимеров на основе углеводов, ксиланов и их сополимеров.
Если носитель -Z' представляет собой гидрогель, это предпочтительно гидрогель, содержащий ПЭГ или гиалуроновую кислоту. Наиболее предпочтительно такой гидрогель содержит ПЭГ.
Даже более предпочтительно, носитель -Z' представляет собой гидрогель, как раскрывается в WO 2006/003014 А2, WO 2011/012715 А1 или WO 2014/056926 А1, которые включены в настоящую заявку посредством ссылки в полном объеме.
В другом варианте выполнения настоящего изобретения -Z' представляет собой полимерную сеть, образованную посредством физической агрегации полимерных цепей, причем физическая агрегация предпочтительно вызвана водородными связями, кристаллизацией, спирализацией или комплексообразованием. В одном варианте выполнения настоящего изобретения такая полимерная сеть представляет собой термогелевый полимер.
Предпочтительно, общая масса CNP пролекарства согласно настоящему изобретению составляет по меньшей мере 10 кДа, как например по меньшей мере 12 кДа, как например по меньшей мере 15 кДа, как например по меньшей мере 20 кДа или как например по меньшей мере 30 кДа. Предпочтительно общая масса CNP про лекарства согласно настоящему изобретению составляет самое большее 250 кДа, как например самое большее 200 кДа, 180 кДа, 150 кДа или 100 кДа.
В предпочтительном варианте выполнения настоящего изобретения остаточная активность CNP пролекарства согласно настоящему изобретению составляет менее 10%, более предпочтительно менее 1%, даже более предпочтительно менее 0.1%, даже более предпочтительно менее 0.01%, даже более предпочтительно менее 0.001% и наиболее предпочтительно менее 0.0001%.
Как применяется в настоящей заявке термин "остаточная активность" относится к активности, проявляемой CNP пролекарством согласно настоящему изобретению, где CNP составляющая связана с носителем, относительно активности, проявляемой соответствующим свободным CNP. В этом контексте термин "активность" относится к NPR-B связыванию. Понятно, что измерение остаточной активности CNP пролекарства согласно настоящему изобретению занимает время, входе которого определенное количество CNP будет высвобождено CNP пролекарством согласно настоящему изобретению, и что такой высвобожденный CNP будет портить результаты, измеренные для CNP пролекарства. Таким образом, принято осуществлять испытание остаточной активности пролекарства с конъюгатом, в котором лекарственная составляющая, в данном случае CNP, необратимо, т.е. стабильно, связана с носителем, который насколько возможно близко напоминает структуру CNP пролекарства, для которого должна быть измерена остаточная активность.
Подходящий анализ для измерения CNP активности и остаточной активности CNP пролекарства согласно настоящему изобретению, предпочтительно в форме стабильного аналога, описан в WO 2010/135541 А1, пример 4, стр. 143/144.
Другим объектом настоящего изобретения является фармацевтическая композиция, содержащая по меньшей мере одно CNP пролекарство согласно настоящему изобретению и по меньшей мере один эксципиент.
В одном варианте выполнения настоящего изобретения фармацевтическая композиция, содержащая молекулы CNP пролекарства согласно настоящему изобретению содержит смесь CNP пролекарств, в которых CNP составляющие присоединены к -L1- через различные функциональные группы, предпочтительно через аминные функциональные группы, обеспеченные CNP, т.е. через N-терминальную аминную функциональную группу, через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 4 и/или боковой цепью лизина в положении в положении 10, если CNP имеет последовательность SEQ ID NO: 1; через N-терминальную аминную функциональную группу, через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 8, 10, 14, 15, 19 и/или 25, если CNP имеет последовательность SEQ ID NO: 25; или через N-терминальную аминную функциональную группу, через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 9, 11, 15, 16, 20 и/или 26, если CNP имеет последовательность SEQ ID NO: 24.
В предпочтительном варианте выполнения настоящего изобретения CNP составляющие всех молекул CNP пролекарства, содержащихся в фармацевтической композиции, присоединены к -L1- через одну и ту же аминную функциональную группу, обеспеченную CNP, т.е. либо через N-терминальную аминную функциональную группу или через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 4 или боковой цепью лизина в положении 10, если CNP имеет последовательность SEQ ID NO: 1; через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 8, 10, 14, 15, 19 или 25, если CNP имеет последовательность SEQ ID NO: 25; или через аминную функциональную группу, обеспеченную боковой цепью лизина в положении 9, 11, 15, 16, 20 или 26, если CNP имеет последовательность SEQ ID NO: 24. Наиболее предпочтительно CNP составляющие всех молекул CNP пролекарства, содержащихся в фармацевтической композиции, присоединены к -L1- через одну и ту же аминную функциональную группу, которая представляет собой аминную функциональную группу, обеспеченную боковой цепью лизина в положении 26, если CNP составляющая имеет последовательность SEQ ID:NO 24.
Предпочтительно, фармацевтическая композиция, содержащая по меньшей мере одно CNP пролекарство согласно настоящему изобретению, имеет значение рН в интервале и включая рН 3 - рН 8. Более предпочтительно, фармацевтическая композиция имеет значение рН в интервале и включая рН 4 - рН 6. Наиболее предпочтительно, фармацевтическая композиция имеет значение рН в интервале и включая рН 4 - рН 5.
В одном варианте выполнения настоящего изобретения фармацевтическая композиция, содержащая по меньшей мере одно CNP пролекарство согласно настоящему изобретению и по меньшей мере один эксципиент, представляет собой жидкую композицию или композицию в виде суспензии. Понятно, что фармацевтическая композиция представляет собой композицию в виде суспензии, если CNP пролекарство согласно настоящему изобретению содержит нерастворимый в воде носитель -Z'.
В другом варианте выполнения настоящего изобретения фармацевтическая композиция, содержащая по меньшей мере одно CNP пролекарство согласно настоящему изобретению и по меньшей мере один эксципиент, представляет собой сухую композицию.
Такая жидкая фармацевтическая композиция, фармацевтическая композиция в виде суспензии или сухая фармацевтическая композиция содержит по меньшей мере один эксципиент. Эксципиенты, применяемые в парентеральных композициях, могут быть разделены на категории следующим образом, например, буферные средства, модификаторы изотоничности, консерванты, стабилизаторы, антиадсорбционные средства, средства защиты от окисления, загустители/вещества, увеличивающие вязкость, или другие вспомогательные средства. Однако, в некоторых случаях, один эксципиент может иметь двойные или тройные функции. Предпочтительно, по меньшей мере один эксципиент, содержащийся в фармацевтической композиции согласно настоящему изобретению выбирают из группы, состоящей из следующего:
(i) Буферные средства: физиологически допустимые буферы для поддержания значения рН в желаемом диапазоне, такие как фосфат натрия, бикарбонат, сукцинат, гистидин, цитрат и ацетат, сульфат, нитрат, хлорид, пируват;
нейтролизаторы кислот, такие как Mg(OH)2 или ZnCO3 также могут применяться;
(ii) Модификаторы изотоничности: чтобы минимизировать боль, которая может стать результатом повреждения клеток в ходе разности осмотического давления при инъекции веществ замедленного всасывания; глицерин и хлорид натрия являются примерами; эффективные концентрации могут быть определены осмометрией, применяя допускаемую осмотическую концентрацию раствора, равную 285-315 мОсмоль/кг для сыворотки;
(iii) Консерванты и/или противомикробные средства: мультидозные парентеральные композиции требуют добавления консервантов при достаточной концентрации, чтобы минимизировать риск заражения пациента при инъекции, и соответствующие регулирующие требования должны быть установлены; типичные консерванты включают м-крезол, фенол, метилпарабен, этилпарабен, пропилпарабен, бутилпарабен, хлорбутанол, бензиловый спирт, фенилртути нитрат, тимерозол, сорбиновую кислоту, сорбат калия, бензойную кислоту, хлоркрезол, и бензалкония хлорид;
(iv) Стабилизаторы: Стабилизация достигается за счет усиления стабилизирующих белок сил, дестабилизации денатурированного состояния или прямого связывания эксципиентов с белком; стабилизаторами могут быть аминокислоты, такие как аланин, аргинин, аспарагиновая кислота, глицин, гистидин, лизин, пролин, сахара, такие как глюкоза, сахароза, трегалоза, полиолы, такие как глицерин, маннит, сорбит, соли, такие как фосфат калия, сульфат натрия, хелатирующие средства, такие как EDTA, гексафосфат, лиганды, такие как ионы двухвалентного металла (цинк, кальций и т.д.), другие соли или органические молекулы, такие как фенольные производные; кроме того, могут быть использованы олигомеры или полимеры, такие как циклодекстрины, декстран, дендримеры, ПЭГ или ПВП или протамин или HSA;
(v) Антиадсорбционные средства: В основном ионные или неионные поверхностно-активные вещества или другие белки или растворимые полимеры применяются для покрытия или конкурентным образом адсорбируются на внутренней поверхности контейнера композиции. Например, полоксамер (Pluronic F-68), ПЭГ додециловый простой эфир (Brij 35), полисорбат 20 и 80, декстран, полиэтиленгликоль, ПЭГ-полигистидин, BSA и HSA и желатины; выбранная концентрация и тип эксципиента зависит от эффекта, которого следует избегать, но обычно монослой поверхностно-активного вещества образуется на границе раздела фаз чуть выше значения CMC;
(vi) Средства защиты от окисления: антиоксиданты, такие как аскорбиновая кислота, эктоин, метионин, глутатион, монотиоглицерин, морин, полиэтиленимин (PEI), пропилгаллат и витамин Е; хелатирующие агенты, такие как лимонная кислота, EDTA, гексафосфат и тиогликолевая кислота, также могут применяться;
(vii) Загустители или вещества, увеличивающие вязкость: замедляют осаждение частиц во флаконе и шприце и используются для облегчения смешивания и ресуспендирования частиц и для облегчения введения суспензии (т.е. с малой силой на шприцевом поршне); подходящими загустителями или усилителями вязкости являются, например, карбомерные загустители, такие как Carbopol 940, Carbopol Ultrez 10, производные целлюлозы, такие как гидроксипропилметилцеллюлоза (гипромеллоза, НРМС) или диэтиламиноэтилцеллюлоза (DEAE или DEAE-C), коллоидный силикат магния (Veegum) или силикат натрия, гидроксиапатитный гель, трикальцийфосфатный гель, ксантаны, каррагинаны, такие как камедь Satia UTC 30, алифатические поли(гидроксикислоты), как например поли(Е), L- или L-молочная кислота) (PLA) и поли(гликолевая кислота) (PGA) и их сополимеры (PLGA), терполимеры D, L-лактида, гликолида и капролактона, полоксамеры, гидрофильные поли(оксиэтиленовые) блоки и гидрофобные поли(оксипропиленовые) блоки для создания триблока поли(оксиэтилен)-поли(оксипропилен)-поли(оксиэтилен) (например, Pluronic®), сополимер простого полиэфира и сложного полиэфира, как например сополимер терефталат полиэтиленгликоля/терефталат полибутилена, сахарозы ацетат изобутират (SAJB), декстран или его производные, комбинации декстранов и ПЭГ, полидиметилсилоксан, коллаген, хитозан, поливиниловый спирт (PVA) и производные, полиалкилимиды, поли(акриламид-со-диаллилдиметиламмоний (DADMA)), поливинилпирролидон (ПВП), глюкозаминогликаны (GAG), такие как дерматан сульфат, хондроитин сульфат, кератан сульфат, гепарин, гепаран сульфат, гиалуронан, ABA триблок- или АВ блок-сополимеры, состоящие из гидрофобных А-блоков, как например, полилактид (PLA) или поли(лактид-со-гликолид) (PLGA) и гидрофильные В-блоки, как например полиэтилтенгликоль (ПЭГ) или поливинилпирролидон; такие блок-сополимеры, как и вышеупомянутые полоксамеры, могут проявлять обратимое термическое гелеобразование (состояние жидкости при комнатной температуре для облегчения введения и состояние геля выше температуры перехода золь-гель при температуре тела после инъекции);
(viii) Лиофилизирующий или диффундирующий агент: модифицирует проницаемость соединительной ткани посредством гидролиза компонентов внеклеточного матрикса во интерстициальном пространстве, таких как, но без ограничения к этому, гиалуроновая кислота, полисахарид, обнаруженные в межклеточном пространстве соединительной ткани; лиофилизирующий агент, такой как, но без ограничения к этому, гиалуронидаза, временно снижает вязкость внеклеточной матрицы и способствует диффузии инъецированных лекарственных средств; и
(ix) Другие вспомогательные средства: такие как смачивающие средства, модификаторы вязкости, антибиотики, гиалуронидаза; кислоты и основания, такие как соляная кислота и гидроксид натрия являются вспомогательными средствами, необходимыми для установления значения рН в ходе получения.
Другим объектом настоящего изобретения является применение CNP пролекарства или его фармацевтически приемлемой соли или фармацевтической композиции, содержащей по меньшей мере одно CNP пролекарство согласно настоящему изобретению в качестве лекарственного средства.
Другим объектом настоящего изобретения является CNP пролекарство или его фармацевтически приемлемая соль или фармацевтическая композиция, содержащая по меньшей мере одно CNP пролекарство согласно настоящему изобретению для применения в способе лечения заболевания, которое можно лечить с помощью CNP.
Предпочтительно, указанное заболевание выбирают из группы, состоящей из ахондроплазии, гипохондроплазии, короткого роста, карликовости, остеохондродисплазии, танатофорической дисплазии, несовершенного костеобразования, ахондрогенеза, точечной эпифизарной дисплазии, гомозиготной ахондроплазии, кампомелической дисплазии, врожденной летальной гипофосфатазии, перинатального летального типа несовершенного костеобразования, синдрома коротких ребер-полидактилии, точечной эпифизарной дисплазии ризомелического типа, метафизарной дисплазии типа Янсена, врожденной спондилоэпифизарной дисплазии, ателостеогенеза, диастрофической дисплазии, врожденной короткой бедренной кости, мезомелической дисплазии Лангера, мезомелической дисплазии Нивергельта, синдрома Робинова, синдрома Рейнхардта, акродизостоза, периферического дизостоза, дисплазии Книста, фиброхондрогенеза, синдрома Робертса, акромезомелической дисплазии, микромелии, синдрома Моркио, синдрома Книста, метатрофной дисплазии, спондилоэпифизарной дисплазии, нейрофиброматоза, синдрома Легиуса, синдрома LEOPARD, синдрома Нунан, врожденного фиброматоза десны, нейрофиброматоза типа 1, синдрома Легиуса, кардио-фацио-кожного синдрома, синдрома Костелло, дефицита SHOX, идиопатического короткого роста, дефицита гормона роста, остеоартрита, клейдокраниального дизостоза, краниосиностоза (например, синдрома Мюнке, синдрома Крузона, синдрома Аперта, синдрома Джексона-Вейсса, синдрома Пфайффера, или синдрома Крузона с черным акантозом), дактилии, брахидактилии, камптодактилии, полидактилии, синдактилии, диссегментальной дисплазии, хондроматоза костей, фиброзной дисплазии, множественных костнохрящевых экзостозов, гипофосфатемического рахита, синдрома Джеффи-Лихтенстайна, синдрома Марфана, синдрома Олбрайта-Мак-Кьюна, остеопетроза и врожденной пятнистой множественной остеопатии.
Предпочтительно указанное заболевание выбирают из группы, состоящей из ахондроплазии, гипохондроплазии, короткого роста, карликовости, остеохондродисплазии, танатофорической дисплазии, несовершенного костеобразования, ахондрогенеза, точечной эпифизарной дисплазии, гомозиготной ахондроплазии, кампомелической дисплазии, врожденной летальной гипофосфатазии, перинатального летального типа несовершенного костеобразования, синдрома коротких ребер-полидактилии, точечной эпифизарной дисплазии ризомелического типа, метафизарной дисплазии типа Янсена, врожденной спондилоэпифизарной дисплазии, ателостеогенеза, диастрофической дисплазии, врожденной короткой бедренной кости, мезомелической дисплазии Лангера, мезомелической дисплазии Нивергельта, Синдрома Робинова, синдрома Рейнхардта, акродизостоза, периферического дизостоза, дисплазии Книста, фиброхондрогенеза, синдрома Робертса, акромезомелической дисплазии, микромелии, синдрома Моркио, синдрома Книста, метатрофной дисплазии, спондилоэпифизарной дисплазии, нейрофиброматоза, синдрома Легиуса, синдрома LEOPARD, синдрома Нунан, врожденного фиброматоза десны, нейрофиброматоза типа 1, синдрома Легиуса, кардио-фацио-кожного синдрома, синдрома Костелло, дефицита SHOX, идиопатического короткого роста, дефицита гормона роста и остеоартрита.
В другом варианте выполнения настоящего изобретения заболеванием является офтальмологическое нарушение, как например глаукома и/или повышенное внутриглазное давление.
В другом варианте выполнения настоящего изобретения указанное заболевание связано со сверхактивацией FGFR3 при раке, например, множественная миелома, миелопролиферативный синдром, лейкемия, плазмоклеточный лейкоз, лимфома, глиобластома, рак предстательной железы, рак мочевого пузыря, или рак молочной железы.
В другом варианте выполнения настоящего изобретения указанным заболеванием является нарушение гладкой мускулатуры сосудистых стенок, предпочтительно выбранное из группы, состоящей из гипертонии, рестеноза, артериосклероза, острой декомпенсированной сердечной недостаточности, сердечной недостаточности с застойными явлениями, сердечного отека, почечного отека, печеночного отека, острой почечной недостаточности и хронической почечной недостаточности.
Предпочтительно указанным заболеванием является фенотип ахондроплазии, выбранный из группы, состоящей из замедления роста, деформации черепа, ортодонтических дефектов, сжатия шейного отдела спинного мозга, стеноза спинномозгового канала, гидроцефалии, потери слуха в результате хронического отита, сердечно-сосудистого заболевания, неврологического заболевания и ожирения.
Наиболее предпочтительно указанным заболеванием является ахондроплазия.
В одном варианте выполнения настоящего изобретения пациентом, подвергающимся способу лечения согласно настоящему изобретению, является млекопитающий пациент, предпочтительно человек. В одном варианте выполнения настоящего изобретения этим человеком является взрослый пациент. В предпочтительном варианте выполнения настоящего изобретения человеком является педиатрический пациент.
Другим объектом настоящего изобретения является применение CNP пролекарства или его фармацевтически приемлемой соли или фармацевтической композиции, содержащей по меньшей мере одно CNP пролекарство согласно настоящему изобретению для получения лекарственного средства для лечения заболевания, которое можно лечить с помощью CNP.
Предпочтительно, указанное заболевание выбирают из группы, состоящей из ахондроплазии, гипохондроплазии, короткого роста, карликовости, остеохондродисплазии, танатофорической дисплазии, несовершенного костеобразования, ахондрогенеза, точечной эпифизарной дисплазии, гомозиготной ахондроплазии, кампомелической дисплазии, врожденной летальной гипофосфатазии, перинатального летального типа несовершенного костеобразования, синдрома коротких ребер-полидактилии, точечной эпифизарной дисплазии ризомелического типа, метафизарной дисплазии типа Янсена, врожденной спондилоэпифизарной дисплазии, ателостеогенеза, диастрофической дисплазии, врожденной короткой бедренной кости, мезомелической дисплазии Лангера, мезомелической дисплазии Нивергельта, Синдрома Робинова, синдрома Рейнхардта, акродизостоза, периферического дизостоза, дисплазии Книста, фиброхондрогенеза, синдрома Робертса, акромезомелической дисплазии, микромелии, синдрома Моркио, синдрома Книста, метатрофной дисплазии, спондилоэпифизарной дисплазии, нейрофиброматоза, синдрома Легиуса, синдрома LEOPARD, синдрома Нунан, врожденного фиброматоза десны, нейрофиброматоза типа 1, синдрома Легиуса, кардио-фацио-кожного синдрома, синдрома Костелло, дефицита SHOX, идиопатического короткого роста, дефицита гормона роста, остеоартрита, клейдокраниального дизостоза, краниосиностоза (например, синдрома Мюнке, синдрома Крузона, синдрома Аперта, синдрома Джексона-Вейсса, синдрома Пфайффера, или синдрома Крузона с черным акантозом), дактилии, брахидактилии, камптодактилии, полидактилии, синдактилии, диссегментальной дисплазии, хондроматоза костей, фиброзной дисплазии, множественных костнохрящевых экзостозов, гипофосфатемического рахита, синдрома Джеффи-Лихтенстайна, синдрома Марфана, синдрома Олбрайта-Мак-Кьюна, остеопетроза и врожденной пятнистой множественной остеопатии.
Предпочтительно указанное заболевание выбирают из группы, состоящей из ахондроплазии, гипохондроплазии, короткого роста, карликовости, остеохондродисплазии, танатофорической дисплазии, несовершенного костеобразования, ахондрогенеза, точечной эпифизарной дисплазии, гомозиготной ахондроплазии, кампомелической дисплазии, врожденной летальной гипофосфатазии, перинатального летального типа несовершенного костеобразования, синдрома коротких ребер-полидактилии, точечной эпифизарной дисплазии ризомелического типа, метафизарной дисплазии типа Янсена, врожденной спондилоэпифизарной дисплазии, ателостеогенеза, диастрофической дисплазии, врожденной короткой бедренной кости, мезомелической дисплазии Лангера, мезомелической дисплазии Нивергельта, Синдрома Робинова, синдрома Рейнхардта, акродизостоза, периферического дизостоза, дисплазии Книста, фиброхондрогенеза, синдрома Робертса, акромезомелической дисплазии, микромелии, синдрома Моркио, синдрома Книста, метатрофной дисплазии, спондилоэпифизарной дисплазии, нейрофиброматоза, синдрома Легиуса, синдрома LEOPARD, синдрома Нунан, врожденного фиброматоза десны, нейрофиброматоза типа 1, синдрома Легиуса, кардио-фацио-кожного синдрома, синдрома Костелло, дефицита SHOX, идиопатического короткого роста, дефицита гормона роста и остеоартрита.
В другом варианте выполнения настоящего изобретения заболеванием является офтальмологическое нарушение, как например глаукома и/или повышенное внутриглазное давление.
В другом варианте выполнения настоящего изобретения указанное заболевание связано со сверхактивацией FGFR3 при раке, например, множественная миелома, миелопролиферативный синдром, лейкемия, плазмоклеточный лейкоз, лимфома, глиобластома, рак предстательной железы, рак мочевого пузыря, или рак молочной железы.
В другом варианте выполнения настоящего изобретения указанным заболеванием является нарушение гладкой мускулатуры сосудистых стенок, предпочтительно выбранное из группы, состоящей из гипертонии, рестеноза, артериосклероза, острой декомпенсированной сердечной недостаточности, сердечной недостаточности с застойными явлениями, сердечного отека, почечного отека, печеночного отека, острой почечной недостаточности и хронической почечной недостаточности.
Предпочтительно указанным заболеванием является фенотип ахондроплазии, выбранный из группы, состоящей из замедления роста, деформации черепа, ортодонтических дефектов, сжатия шейного отдела спинного мозга, стеноза спинномозгового канала, гидроцефалии, потери слуха в результате хронического отита, сердечно-сосудистого заболевания, неврологического заболевания и ожирения.
Наиболее предпочтительно указанным заболеванием является ахондроплазия.
В одном варианте выполнения настоящего изобретения заболевание, подлежащее лечению с помощью CNP пролекарства или его фармацевтически приемлемой соли или фармацевтической композиции, содержащей по меньшей мере одно CNP пролекарство согласно настоящему изобретению, возникает у млекопитающего пациента, предпочтительно у пациента человека. В одном варианте выполнения настоящего изобретения этим пациентом является взрослый пациент. В предпочтительном варианте выполнения настоящего изобретения пациентом человеком является педиатрический пациент.
Другим объектом настоящего изобретения является способ лечения, контроля, замедления или профилактики у пациента млекопитающего, предпочтительно человека, нуждающегося в лечении одного или более заболеваний, которые можно лечить с помощью CNP, включающий стадию введения указанному пациенту, нуждающемуся в этом, терапевтически эффективного количества CNP пролекарства или его фармацевтически приемлемой соли или фармацевтической композиции, содержащей CNP пролекарство согласно настоящему изобретению. В одном варианте выполнения настоящего изобретения пациентом является взрослый человек. В предпочтительном варианте выполнения настоящего изобретения пациентом человеком является педиатрический пациент.
Предпочтительно, одно или более заболевания, которые можно лечить с помощью CNP, выбирают из группы, состоящей из ахондроплазии, гипохондроплазии, короткого роста, карликовости, остеохондродисплазии, танатофорической дисплазии, несовершенного костеобразования, ахондрогенеза, точечной эпифизарной дисплазии, гомозиготной ахондроплазии, кампомелической дисплазии, врожденной летальной гипофосфатазии, перинатального летального типа несовершенного костеобразования, синдрома коротких ребер-полидактилии, точечной эпифизарной дисплазии ризомелического типа, метафизарной дисплазии типа Янсена, врожденной спондилоэпифизарной дисплазии, ателостеогенеза, диастрофической дисплазии, врожденной короткой бедренной кости, мезомелической дисплазии Лангера, мезомелической дисплазии Нивергельта, Синдрома Робинова, синдрома Рейнхардта, акродизостоза, периферического дизостоза, дисплазии Книста, фиброхондрогенеза, синдрома Робертса, акромезомелической дисплазии, микромелии, синдрома Моркио, синдрома Книста, метатрофной дисплазии, спондилоэпифизарной дисплазии, нейрофиброматоза, синдрома Легиуса, синдрома LEOPARD, синдрома Нунан, врожденного фиброматоза десны, нейрофиброматоза типа 1, синдрома Легиуса, кардио-фацио-кожного синдрома, синдрома Костелло, дефицита SHOX, идиопатического короткого роста, дефицита гормона роста, остеоартрита, клейдокраниального дизостоза, краниосиностоза (например, синдрома Мюнке, синдрома Крузона, синдрома Аперта, синдрома Джексона-Вейсса, синдрома Пфайффера, или синдрома Крузона с черным акантозом), дактилии, брахидактилии, камптодактилии, полидактилии, синдактилии, диссегментальной дисплазии, хондроматоза костей, фиброзной дисплазии, множественных костнохрящевых экзостозов, гипофосфатемического рахита, синдрома Джеффи-Лихтенстайна, синдрома Марфана, синдрома Олбрайта-Мак-Кьюна, остеопетроза и врожденной пятнистой множественной остеопатии.
В другом варианте выполнения настоящего изобретения одним или более заболеваниями, которые можно лечить с помощью CNP, является офтальмологическое нарушение, как например глаукома и/или повышенное внутриглазное давление.
В другом варианте выполнения настоящего изобретения одно или более заболеваний, которые можно лечить с помощью CNP, связаны со сверхактивацией FGFR3 при раке, например, множественная миелома, миелопролиферативный синдром, лейкемия, плазмоклеточный лейкоз, лимфома, глиобластома, рак предстательной железы, рак мочевого пузыря, или рак молочной железы.
В другом варианте выполнения настоящего изобретения одним или более заболеваниями, которые можно лечить с помощью CNP, является нарушение гладкой мускулатуры сосудистых стенок, предпочтительно выбранное из группы, состоящей из гипертонии, рестеноза, артериосклероза, острой декомпенсированной сердечной недостаточности, сердечной недостаточности с застойными явлениями, сердечного отека, почечного отека, печеночного отека, острой почечной недостаточности и хронической почечной недостаточности.
Предпочтительно одним или более заболеваниями, которые можно лечить с помощью CNP, является фенотип ахондроплазии, выбранный из группы, состоящей из замедления роста, деформации черепа, ортодонтических дефектов, сжатия шейного отдела спинного мозга, стеноза спинномозгового канала, гидроцефалии, потери слуха в результате хронического отита, сердечно-сосудистого заболевания, неврологического заболевания и ожирения.
Наиболее предпочтительно одним или более заболеваниями, которые можно лечить с помощью CNP, является ахондроплазия.
Другим объектом настоящего изобретения является способ введения CNP пролекарства, его фармацевтически приемлемой соли или фармацевтической композиции согласно настоящему изобретению, где способ включает стадию введения CNP пролекарства, его фармацевтически приемлемой соли или фармацевтической композиции согласно настоящему изобретению посредством местного, энтерального или парентерального введения и посредством местного, энтерального или парентерального введения или способами внешнего применения, инъекции или инфузии, включая внутрисуставные, периартикулярные, внутрикожные, подкожные, внутримышечные, внутривенные, внутрикостные, внутрибрюшинные, интратекальные, внутрикапсульные, внутриглазничные, интравитреальные, интратимпанальные, внутрипузырные, внутрисердечные, транстрахеальные, субкутикулярные, подкапсулярные, субарахноидальные, интраспинальные, внутрижелудочковые, интрастернальные инъекции или инфузии, непосредственной доставки в мозг через имплантированное устройство, позволяющее доставку изобретения или тому подобного в ткань головного мозга или мозговые жидкости (например, резервуар Оммайя), прямой интрацеребровентрикулярной инъекции или инфузии, инъекции или инфузии в мозг или области, связанные с мозгом, инъекции в супрахориоидальное пространство, ретро-орбитальной инъекции или глазной инсталляции, предпочтительно посредством подкожной инъекции.
В предпочтительном варианте выполнения настоящего изобретения, настоящее изобретение относится к CNP пролекарству или его фармацевтически приемлемой соли или фармацевтической композиции согласно настоящему изобретению, для применения в лечении ахондроплазии посредством подкожной инъекции.
Другим объектом настоящего изобретения являются необратимые конъюгаты формулы (IVa) и (IVb):
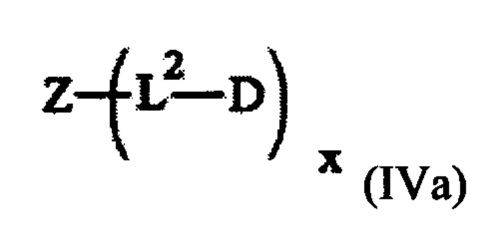
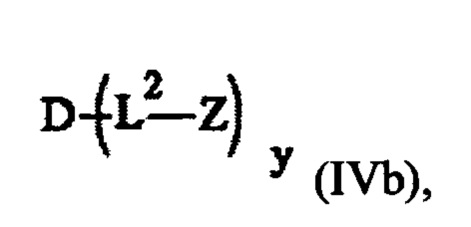
где
-D представляет собой CNP составляющую;
-L2- представляет собой одинарную химическую связь или спейсерную составляющую;
-Z представляет собой растворимую в воде составляющую-носитель;
x представляет собой целое число, выбранное из группы, состоящей из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 и 16; и
y представляет собой целое число, выбранное из группы, состоящей из 1, 2, 3, 4 и 5.
Предпочтительные варианты выполнения для -D, -L -, -Z, x и у являются такими, как описано выше.
Фиг. 1: Структура CNP согласно SEQ ID NO: 1.
Примеры
Вещества и Способы
CNP SEQ ID No: 1 получили у Bachem AG, Bubendorf, Switzerland (CNP-22, человеческий, номер по каталогу Н-1296). CNP-34 SEQ ID No: 40 и CNP-38 SEQ ID No: 24 получили у CASLO ApS, Kongens Lyngby, Denmark.
CNP-38 с защищенной боковой цепью на TCP, имеющий Вос-защищенный N-конец и ivDde-защищенную боковую цепь Lys26 (синтезированный по Fmoc-стратегии) получили у CASLO ApS, Kongens Lyngby, Denmark.
CNP-34 с защищенной боковой цепью на TCP смоле Tentagel, имеющий Вос-защищенный N-конец и ivDde-защищенную боковую цепь либо Lysl2, Lysl6, либо Lys22 (синтезированный по Fmoc-стратегии) получили у Peptide Specialty Laboratories GmbH, Heidelberg, Germany. CNP-38 с защищенной боковой цепью на TCP смоле Tentagel, имеющий свободный N-конец (синтезированный по Fmoc-стратегии) получили у Peptide Specialty Laboratories GmbH, Heidelberg, Germany.
Метокси-ПЭГ-амин 5 кДа получили у Rapp Rapp Polymere GmbH, Tuebingen, Germany. Все другие применяемые в данной работе ПЭГ были предоставлены компанией NOF Europe N.V., Grobbendonk, Belgium.
FmocN-Me-Asp(OtBu)-OH получили у Bachem AG, Bubendorf, Switzerland. S-тритил-6-меркаптокапроновую кислоту приобрели у Polypeptide, Strasbourg, France. HATU получили у Merck Biosciences GmbH, Schwalbach/Ts, Germany.
2,4-Диметилбензиловый спирт получили у abcr GmbH, Karlsruhe, Germany.
Fmoc-N-Me-Asp(OBn)-OH получили у Peptide International Inc., Louisville, KY, USA.
Нейтральную эндопептидазу (NEP) получили у Enzo Life Sciences GmbH, Lorrach, Germany.
Все другие химические соединения и реагенты приобрели у Sigma Aldrich GmbH, Taufkirchen, Germany.
Шприцы, оборудованные полиэтиленовой фриттой (MukiSynTech GmbH, Witten, Germany) применяли в качестве реакционных сосудов или на стадии промывки пептидных смол.
Общая методика удаления ivDde защитной группы у CNP с защищенной боковой цепью на смоле
Смола предварительно разбухла в DMF в течение 30 мин, и растворитель удалили. Группу ivDde удаляли путем инкубации смолы с DMF/гидразин гидратом 4/1 (об./об., 2,5 мл/г смолы) в течение 8×15 мин. Для каждого этапа использовали свежий раствор DMF/гидразин гидрата. Наконец, смолу промыли DMF (10 х), DCM (10 х) и высушили в вакууме.
Очистка посредством ОФ-ВЭЖХ:
Для препаративной ОФ-ВЭЖХ применяли управляющее устройство Waters 600 и детектор 2487 Dual Absorbance, оборудованные следующими колонками: Waters XBridge™ ВЕН300 Prep C18 5 мкм, 150 × 10 мм, скорость потока 6 мл/мин, или Waters XBridge™ ВЕН300 Prep C18 10 мкм, 150 × 30 мм, скорость потока 40 мл/мин. Применяли линейные градиенты системы растворителей А (вода, содержащая 0.1% TFA об./об. или 0.01% конц. НС1 об./об.) и системы растворителей В (ацетонитрил, содержащий 0.1% TFA об./об. или 0.01% конц. HCl об./об.).
ВЭЖХ-фракции, содержащие продукт, объединяли и лиофилизировали, если иного не указано.
Флэш-хроматография
Очистки посредством флэш-хроматографии осуществляли на системе Isolera One от Biotage АВ, Sweden, применяя картриджи с силикагелем Biotage KP-Sil и н-гептан и этилацетат в качестве элюентов. Продукты обнаруживали при 254 нм.
Аналитические методы
Аналитическую сверхвысокоэффективную LC (UPLC) -MS проводили на системе Waters Acquity, оборудованной колонкой Waters ВЕН300 С18 (размер частиц 2,1×50 мм, размер частиц 1,7 мкм, поток: 0,25 мл/мин, растворитель А: вода, содержащая 0,04% TFA (об. /об.), Растворитель В: ацетонитрил, содержащий 0,05% TFA (об./об.)), соединенной с масс-спектрометром LTQ Orbitrap Discovery от Thermo Scientific или соединенной с Waters Microsass ZQ.
Эксклюзионную хроматографию размеров (SEC) проводили с использованием системы Amersham Bioscience AEKTAbasic, оснащенной колонкой Superdex 200 5/150 GL (Amersham Bioscience/GE Healthcare), оснащенной входным фильтром 0,45 мкм, если не указано иное. В качестве подвижной фазы использовали 20 мМ фосфат натрия, 140 мМ NaCl, рН 7,4.
Из-за обратимой природы присоединения -L1-к-D, измерения для NEP-стабильности и аффинности рецепторов были получены с использованием стабильных аналогов CNP пролекарств согласно настоящему изобретению, т.е. они были получены с использованием структур, подобных CNP пролекарствам согласно настоящему изобретению, которые вместо обратимого присоединения -L1-к-D имеют стабильное присоединение.
Это было необходимо, потому что CNP пролекарства согласно настоящему изобретению высвобождали бы CNP в ходе эксперимента, и указанный высвобожденный CNP повлиял бы на результат.
Количественная оценка концентраций общего CNP-38 в плазме
Концентрации общего CNP-38 в плазме определили путем количественного измерения N-терминального сигнатурного пептида (последовательность: LQEHPNAR) и С-терминального сигнатурного пептида (последовательность: IGSMSGLGC) после трипсинового расщепления.
Анализ LC-MS проводили с использованием Agilent 1290 UPLC, соединенной с масс-спектрометром Agilent 6550 iFunnel Q-TOF с помощью зонда ESI. Хроматографию проводили на аналитической колонке Waters XBridge™ ВЕН300 Prep C18 (50×2.1 мм I.D., размер частиц 1.7 мкм) с предварительным фильтром при скорости потока 0,25 мл/мин (Т=25°С). Воду (класс UPLC), содержащую 0,2% муравьиной кислоты (об./об.), применяли в качестве подвижной фазы А, и ацетонитрил (класс UPLC) с 0,2% муравьиной кислотой применяли в качестве подвижной фазы В. Система градиента составляла короткую изократическую стадию при начальных параметрах 0,1% В в течение 3,0 мин и затем линейное увеличение от 0,1% В до 16% В в течение 17 мин. Масс-анализ проводили в режиме мониторинга избранных ионов (SIM), контролируя ионы m/z 482.75 [М+2Н]2+ (N-терминальный) и m/z 824.36 [М+Н]1+ (С-терминальный). В качестве внутреннего стандартного использовали дейтерированный пептид CNP-38.
Калибровочные стандарты CNP-38 конъюгата в пустой плазме готовили следующим образом: Растаявшую Li-гепариновую плазму яванских макак сначала гомогенизировали, затем центрифугировали в течение 5 минут. Композицию CNP-38 конъюгата разбавили до рабочего раствора 10 мкг/мл (конъюгат CNP-38 экв.) в DMSO и добавили в пустую плазму при концентрациях от 9.3 нг/100 мкл (конъюгат CNP-38 экв.) и 139.5 нг/100 мкл (конъюгат CNP-38 экв.). Эти растворы применяли для получения калибровочной кривой. Калибровочные кривые получили 1/х2 для обоих сигнатурных пептидов (N- и С-терминальный). Для контроля качества, получили три образца для контроля качества соответственно с содержаниями 116.2 нг/100 мкл (высокое качество, конъюгат CNP-38 экв.), 69.75 нг /100 мкл (среднее качество, конъюгат CNP-38 экв.) и 23.25 нг /100 мкл (низкое качество, конъюгат CNP-38 экв.).
Для получения образца, осаждение белка осуществляли путем добавления 300 мкл предварительно охлажденного (0°С) метанола к 100 мкл образца плазмы. 200 мкл супернатанта перенесли в новый луночный планшет и выпарили до сухости (при мягком потоке азота при 35°С). 100 мкл восстановленного раствора (Thermo digestion buffer, порядковый номер 60109-101, Thermo Fisher Scientific GmbH, Dreieich, Germany) применяли для растворения остатка. 20 мкг трипсина (порядковый номер V5111, Promega GmbH, Mannheim, Germany) растворили в 20 мкл 10 мМ уксусной кислоты. 2 мкл раствора трипсина добавили в каждую полость.
Через 4 часа инкубации при 37°С (водяная баня), 5 мкл раствора 0.5 М ТСЕР добавили в каждую полость и инкубировали снова в течение 5 мин при 96°С. После того, как образцы охладили до комнатной температуры, 3 мкл ацетонитрила добавили. Элюаты перенесли в ампулы. 10 мкл впрыснули в UPLC-MS систему.
Пример 1
Синтез линкерного реагента 1f
Линкерный реагент 1f синтезировали согласно следующей схеме:
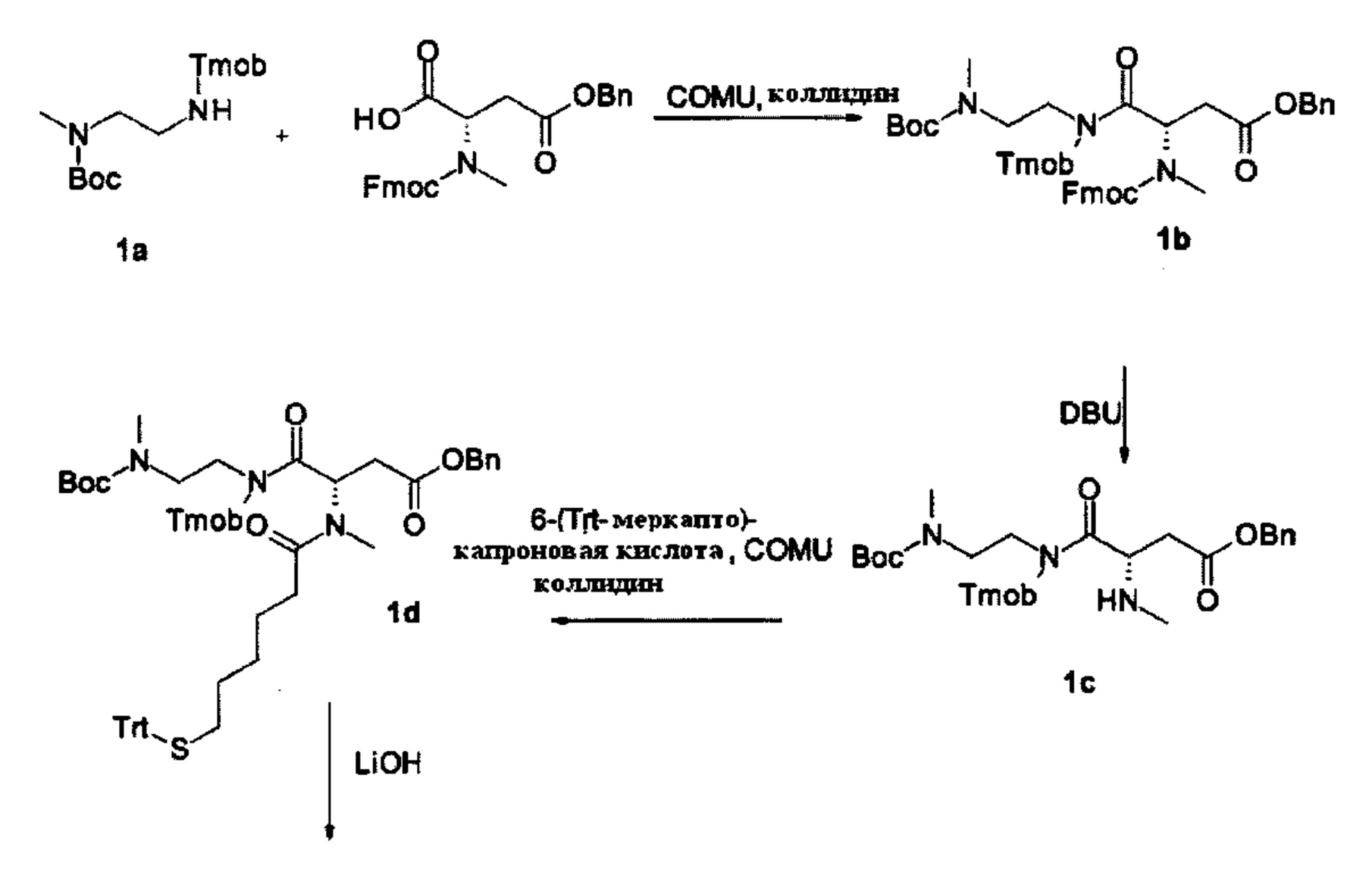
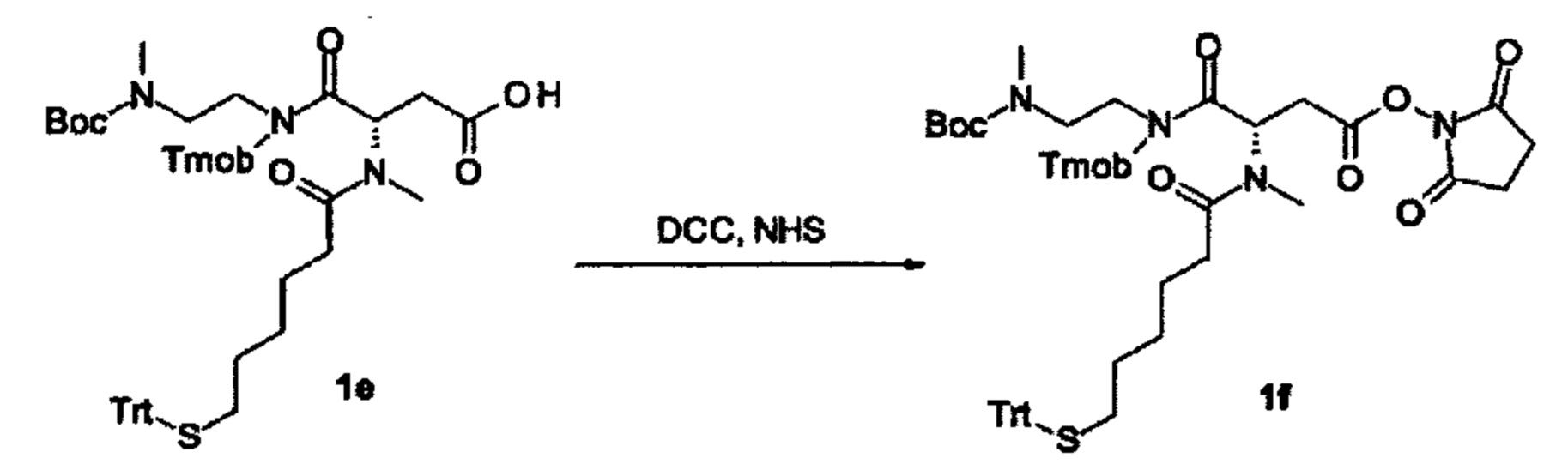
К раствору N-метил-N-Вос-этилендиамина (2 г, 11.48 ммоль) и NaCNBH3 (819 мг, 12.63 ммоль) в МеОН (20 мл) добавили 2,4,6-триметоксибензальдегид (2.08 г, 10.61 ммоль) порционно. Смесь перемешивали при комнатной температуре в течение 90 мин, подкислили с помощью 3 М HCl (4 мл) и перемешивали еще 15 мин. Реакционную смесь добавили к насыщенному раствору NaHCO3 (200 мл) и экстрагировали 5 х с помощью CH2Cl2. Объединенные органические фазы высушили над Na2SO4, и растворители выпарили в вакууме. Полученный N-метил-N-Boc-N'-Tmob-этилендиамин 1a высушили в вакууме и применяли на следующей стадии без дальнейшей очистки.
Выход: 3.76 г (11.48 ммоль, 89% чистота, 1а : дважды Tmob защищенный продукт = 8:1)
MS: m/z 355.22=[М+Н]+, (вычисленная моноизотопическая масса = 354.21.
К раствору 1а (2 г, 5.65 ммоль) в CH2Cl2 (24 мл) COMU (4.84 г, 11.3 ммоль), N-Fmoc-N-Me-Asp(OBn)-OH (2.08 г, 4.52 ммоль) и 2,4,6-коллидин (2.65 мл, 20.34 ммоль) добавили. Реакционную смесь перемешивали в течение 3 ч при комнатной температуре, разбавили с помощью CH2Cl2 (250 мл) и промыли 3 х с помощью 0.1 М H2SO4 (100 мл) и 3 х с помощью соляного раствора (100 мл). Водные фазы повторно экстрагировали с помощью CH2Cl2 (100 мл). Объединенные органические фазы высушили над Na2SO4, отфильтровали, и остаток концентрировали до объема 24 мл. Соединение 1b очистили, применяя флэш-хроматографию.
Выход: 5.31 г (148%, 6.66 ммоль)
MS: m/z 796.38=[M+H]+, (вычисленная моноизотопическая масса = 795.37).
К раствору 1b (5.31 г, макс.4.52 ммоль, обозначается как N-Fmoc-N-Me-Asp(OBn)-ОН) в THF (60 мл) DBU (1.8 мл, 3% об./об.) добавили. Раствор перемешивали в течение 12 мин при комнатной температуре, разбавили с помощью CH2Cl2 (400 мл) и промыли 3 х с помощью 0.1 М H2SO4 (150 мл) и 3 х с помощью соляного раствора (150 мл). Водные фазы повторно экстрагировали с помощью CH2Cl2 (100 мл). Объединенные органические фазы высушили над Na2SO4 и отфильтровали. Соединение 1с выделили при выпаривании растворителя и применяли на следующей стадии без дальнейшей очистки.
MS: m/z 574.31=[М+Н]+, (вычисленная моноизотопическая масса = 573.30).
Соединение 1с (5.31 г, 4.52 ммоль, неочищенное) растворили в ацетонитриле (26 мл) и COMU (3.87 г, 9.04 ммоль), 6-тритилмеркаптокапроновую кислоту (2.12 г, 5.42 ммоль) и 2,4,6-коллидин (2.35 мл, 18.08 ммоль) добавили. Реакционную смесь перемешивали в течение 4 ч при комнатной температуре, разбавили с помощью CH2Cl2 (400 мл) и промыли 3 х с помощью 0.1 М H2SO4 (100 мл) и 3 х с помощью соляного раствора (100 мл). Водные фазы повторно экстрагировали с помощью CH2Cl2 (100 мл). Объединенные органические фазы высушили над Na2SO4, отфильтровали и 1d выделили при выпаривании растворителя. Продукт 1d очистили, применяя флэш-хроматографию.
Выход: 2.63 г (62%, 94% чистота)
MS: m/z 856.41=[М+Н]+, (вычисленная моноизотопическая масса = 855.41).
К раствору 1d (2.63 г, 2.78 ммоль) в i-PrOH (33 мл) и H2O (11 мл) добавили LiOH (267 мг, 11.12 ммоль), и реакционную смесь перемешивали в течение 70 мин при комнатной температуре. Смесь разбавили с помощью CH2Cl2 (200 мл) и промыли 3 х с помощью 0.1 М H2SO4 (50 мл) и 3 х с помощью соляного раствора (50 мл). Водные фазы повторно экстрагировали с помощью CH2Cl2 (100 мл). Объединенные органические фазы высушили над Na2SO4, отфильтровали, и соединение 1е выделили при выпаривании растворителя. Соединение 1е очистили, применяя флэш-хроматографию.
Выход: 2.1 г (88%)
MS: m/z 878.4=[M+Na]+, (вычисленная моноизотопическая масса = 837.40).
К раствору 1е (170 мг, 0.198 ммоль) в безводном DCM (4 мл) добавили DCC (123 мг, 0.59 ммоль) и каталитическое количество DMAP. Через 5 мин N-гидрокси-сукцинимид (114 мг, 0.99 ммоль) добавили, и реакционную смесь перемешивали при комнатной температуре в течение 1 ч. Реакционную смесь отфильтровали, растворитель удалили в вакууме, и остаток растворили в 90% ацетонитриле плюс 0.1% TFA (3.4 мл). Неочищенную смесь очистили посредством ОФ-ВЭЖХ. Фракции продукта нейтрализовали с помощью 0.5 М рН 7.4 фосфатного буфера и концентрировали. Оставшуюся водную фазу экстрагировали с помощью DCM, и 1f выделили при выпаривании растворителя.
Выход: 154 мг (81%)
MS: m/z 953.4=[М+Н]+, (вычисленная моноизотопическая масса = 952.43).
Пример 2
Синтез NεK4/εK10-CNP моно-линкер тиола 2, NεK4-CNP моно-линкер тиола 2с и NεK10-CNP моно -линкер тиола 2d
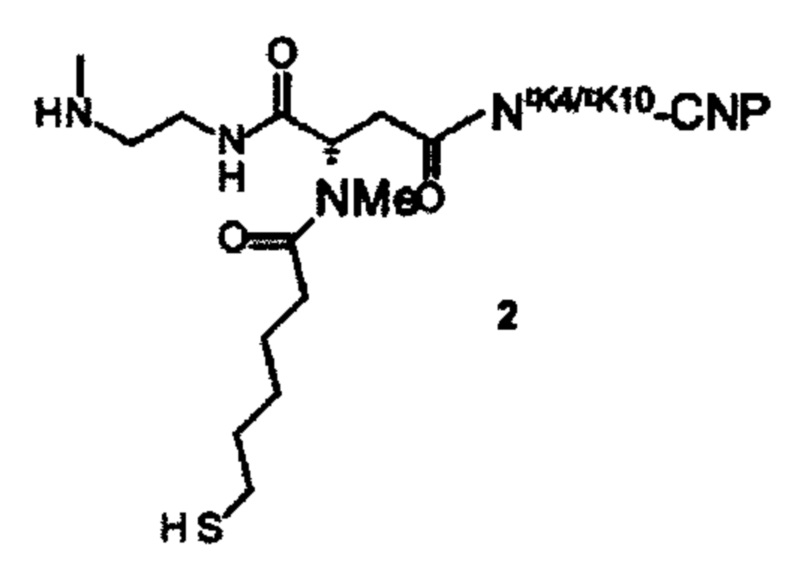
NεK4/εK10-CNP моно-линкер тиол (смесь региоизомеров с линкером, конъюгированным при аминогруппе боковой цепи Lys4 или Lys10) 2 получили путем растворения CNP-22 (5.2 мкмоль) в 0.6 мл DMSO. 0.15 мл 0.375 М боратного буфера, доведенного до рН 8.5 с помощью тетрабутил-аммония гидроксид гидрата, 60 мкл DIPEA и 1f (6.1 мг, 7.1 мкмоль) в 0.34 мл DMSO добавили, и смесь перемешивали в течение 30 мин при комнатной температуре. Реакционную смесь разбавили с помощью 2 мл ацетонитрила/воды 1/1 (об./об.) и 200 мкл АсОН, и защищенный NεK4/εK10-CNP монолинкер конъюгат выделили из реакционной смеси посредством ОФ-ВЭЖХ.
Оптимизированные градиенты ОФ-ВЭЖХ могут применяться для выделения NεK4-CNP моно-линкер тиола 2а и NεK10-CNP моно -линкер тиола 2b.
Удаление защитных групп осуществляется посредством обработки лиофилизированных фракций продукта с помощью 0.6 мл 90/10/2/2 (об./об./об./об.) HFIP/TFA/TES/вода в течение 1 ч при комнатной температуре. NεK4/εK10-CNP монолинкер тиол 2 с удаленными защитными группами очистили посредством ОФ-ВЭЖХ. Идентичность и чистоту продукта определили с помощью ESI-LCMS.
NεK4-CNP моно-линкер тиол 2с и NεK10-CNP моно-линкер тиол 2d с удаленными защитными группами могут быть получены подобным образом из 2а и 2b, соответственно.
Пример 3
Синтез NαG1-CNP моно-линкер тиола 3
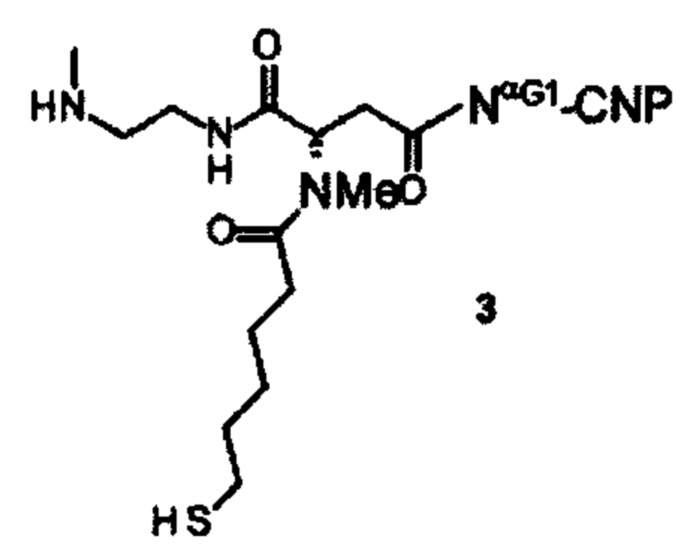
NαG1-CNP моно-линкер тиол 3 получили путем растворения CNP-22 (5.2 мкмоль) в 0.6 мл DMSO. 0.25 мл 0.5 М фосфатного буфера рН 7.4, и 1f (6.1 мг, 7.1 мкмоль) в 0.34 мл DMSO добавили, и смесь перемешивали в течение нескольких часов при комнатной температуре. Реакционную смесь разбавили с помощью 2 мл ацетонитрила/воды 1/1 (об./об.) и 200 мкл АсОН, и NαG1-CNP моно-линкер тиол с защитными группами выделили из реакционной смеси посредством ОФ-ВЭЖХ.
Удаление защитных групп осуществляется посредством обработки лиофилизированных фракций продукта с помощью 0.6 мл 90/10/2/2 (об./об./об./об.) HFIP/TFA/TES/вода в течение 1 ч при комнатной температуре. NαG1-CNP моно-линкер тиол 3 с удаленными защитными группами очистили посредством ОФ-ВЭЖХ. Идентичность и чистоту продукта определили с помощью ESI-LCMS.
Пример 4
ПЭГилирование CNP моно-линкер тиолов 2с, 2d и 3
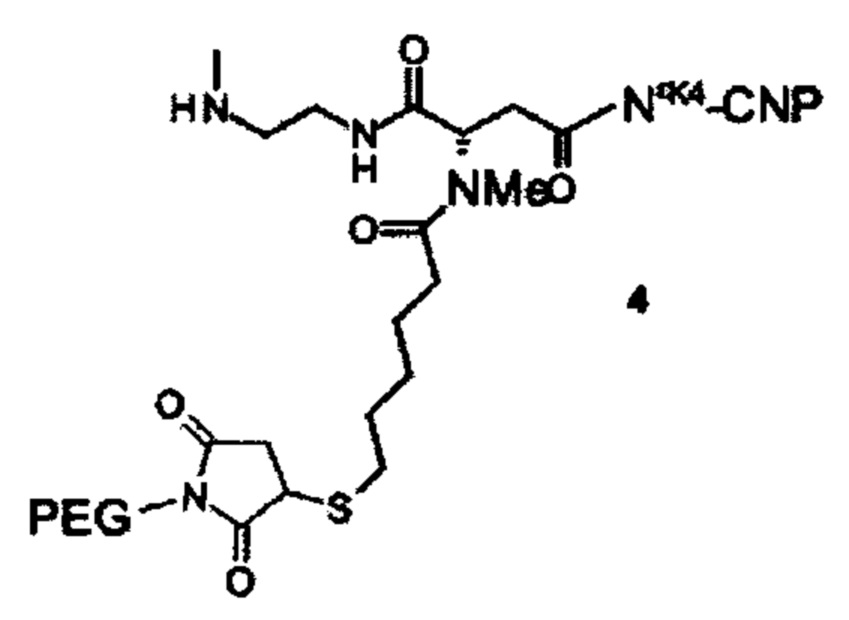
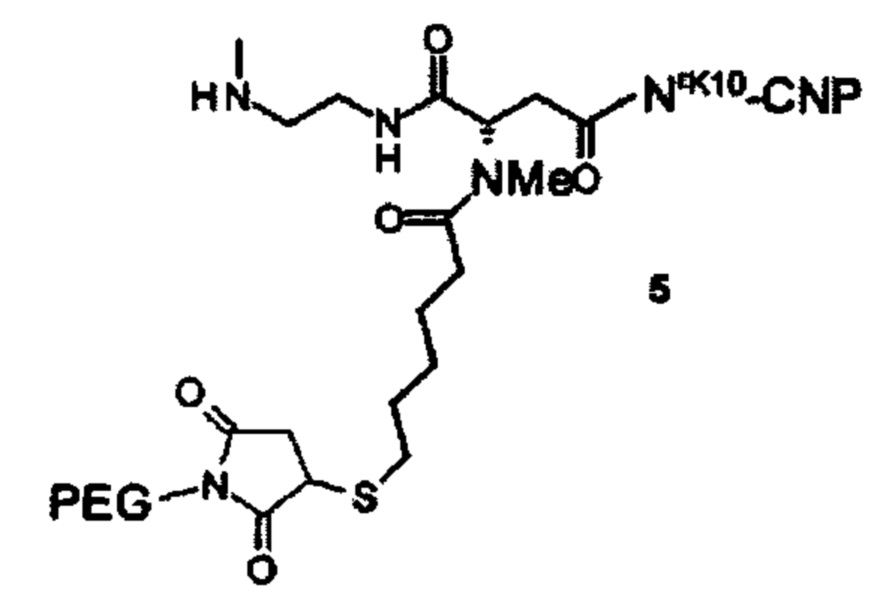
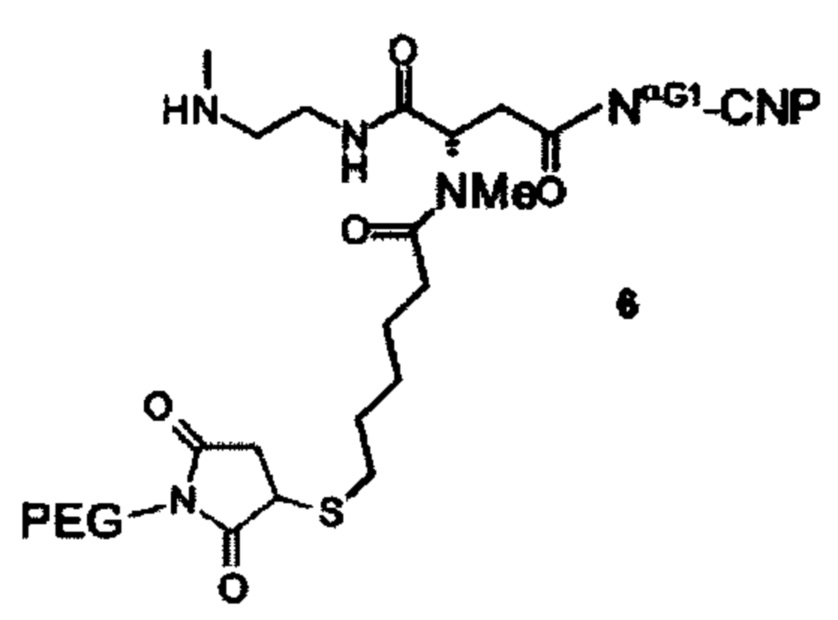
1 мкмоль CNP моно-линкер тиол 2 с растворили в 0.5 мл ацетонитрила/0.2 М сукцинатного буфера рН 3.8 1/1 (об./об.). 1.2 мкмоль линейного 40 кДа ПЭГ-малеимида добавили, и смесь перемешивали при комнатной температуре. Реакцию погасили путем добавления 20 мкл АсОН, и CNP конъюгат 4 очистили посредством препаративной ОФ-ВЭЖХ.
CNP конъюгаты 5 и 6 получили подобным образом из 1 мкмоль CNP моно-линкер тиолов 2d и 3.
Содержание CNP определили путем количественного анализа аминокислоты после общего гидрола при кислотных условиях.
Пример 5
Кинетика высвобождения in vitro
CNP конъюгаты 4, 5 и 6 растворили в 60 мМ фосфате натрия, 3 мМ EDTA, 0.01% Tween-20, рН 7.4 при концентрации около 2 мг/мл и стерильно отфильтровали. Смеси инкубировали при 37°С. Взяли аликвоты во временных точках и проанализировали посредством ОФ-ВЭЖХ и ESI-MS. УФ-сигналы, соответствующие высвобожденному CNP, интегрировали и нанесли на график относительно времени инкубации.
Программное обеспечение для коррекции обрабатываемых кривых применяли для оценки соответствующего периода полувысвобождения.
Пример 6
Фармакокинетика и cGMP продукция в крысах
Эквимолярные дозы CNP-22, CNP конъюгатов 4, 5 или 6 инъецировали внутривенно и подкожно обыкновенным крысам. Уровни CNP и cGMP в плазме с течением времени определяли, как описано в ссылочных источниках (патент США 8,377,884 В2).
Пример 7
Синтез Dmb защищенной 6-меркаптокапроновая кислота 7
Соединение 7 синтезировали согласно следующей схеме:
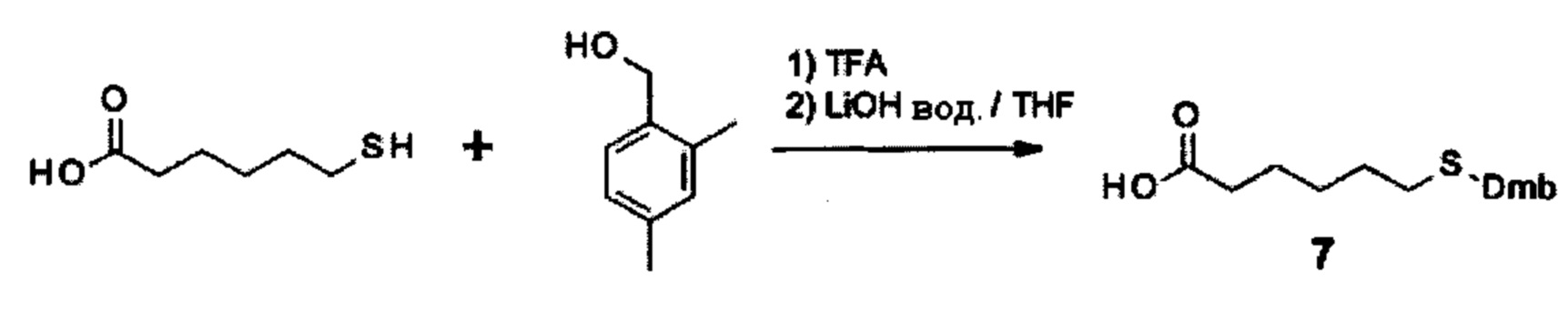
К раствору 6-меркаптокапроновой кислоты (7.10 г, 47.90 ммоль) в трифторуксусной кислоте (20 мл) добавили 2,4-диметилбензиловый спирт (13.5 г, 95.80 ммоль). Смесь перемешивали при комнатной температуре в течение 60 мин и затем трифторуксусную кислоту удалили в вакууме. Остаток растворили в смеси 95.8 мл LiOH (3 М) и THF (81 мл) и перемешивали при комнатной температуре в течение 60 мин. Растворитель удалили в вакууме, и водный остаток экстрагировали 3х с помощью EtOAc (200 мл). Объединенные органические фазы высушили над MgSO4, и растворитель удалили в вакууме. Соединение 7 очистили посредством ОФ-ВЭЖХ.
Выход: 2.27 г (8.52 ммоль, 18%)
MS: m/z 267.01=[М+Н]+, (вычисленная моноизотопическая масса = 266.13).
Пример 8
Синтез линкерного реагент 8с
Линкерный реагент 8с синтезировали согласно следующей схеме:
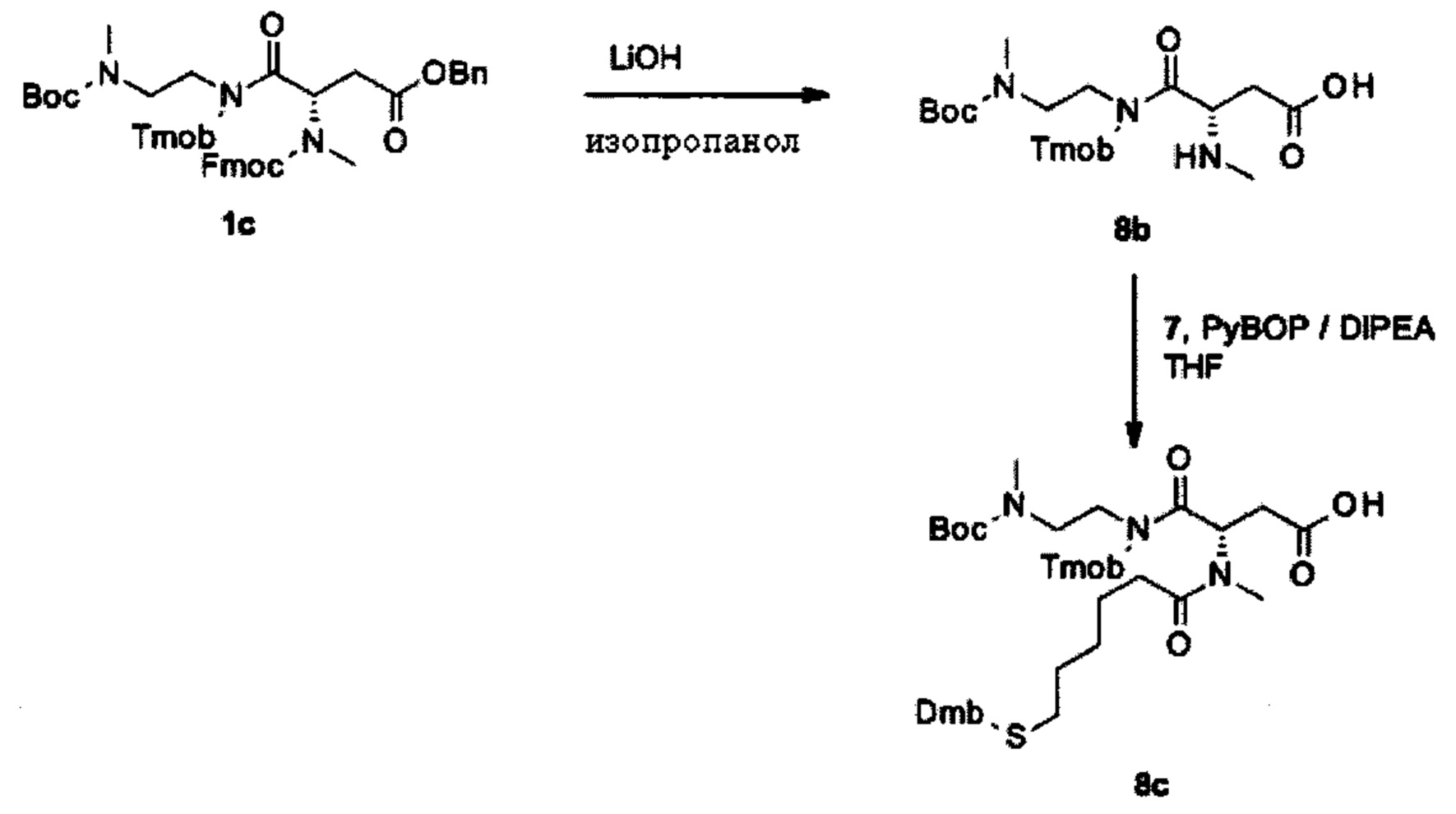
К раствору 1 с (21.6 г, 27.18 ммоль) в изопропаноле (401 мл) добавили воду (130 мл) и LiOH (3.90 г, 163.06 ммоль). Реакционную смесь перемешивали в течение 3 ч при комнатной температуре, затем разбавили с помощью толуола (300 мл) и промыли 3 х с помощью 0.1 М HCl (200 мл). Объединенные водные фазы промыли 3 х с помощью толуола (100 мл). Водную фазу подщелочили с помощью 4 М NaOH (4 мл) до рН 8.5 и экстрагировали 8 х с помощью CH2Cl2 (200 мл). Объединенные CH2Cl2 фазы промыли с помощью соляного раствора (50 мл), высушили над Na2SO4. Соединение 8b выделили при выпаривании растворителя и применяли на следующей стадии без дальнейшей очистки.
Выход: 11.89 г (24.59 ммоль, 90%)
MS: m/z 484.16=[М+Н]+, (вычисленная моноизотопическая масса = 483.26).
К раствору 7 (293 мг, 1.10 ммоль) и РуВОР (572 мг, 1.10 ммоль) в THF (10 мл) добавили DIEA (0.52 мл, 3.00 ммоль) в атмосфере N2. Реакционную смесь перемешивали в течение 60 мин при комнатной температуре. Раствор 8b (484 мг, 1.00 ммоль) в THF (2 мл) добавили, и реакционную смесь перемешивали в течение еще 60 мин. Реакцию погасили с помощью 2 М раствора лимонной кислоты (10 мл), и THF удалили в вакууме. Полученную водную фазу затем экстрагировали 2 х с помощью EtOAc (15 мл), и объединенные органические слои промыли водой (10 мл) и соляным раствором (10 мл) и высушили над MgSO4. Растворитель удалили в вакууме, и 8 с очистили посредством ОФ-ВЭЖХ.
Выход: 330 мг (0.451 ммоль, 45%)
MS: m/z 732.34=[М+Н]+, (вычисленная моноизотопическая масса = 731.38).
Пример 9
Синтез линкерного реагент 9
Линкерный реагент 9 синтезировали согласно следующей схеме:
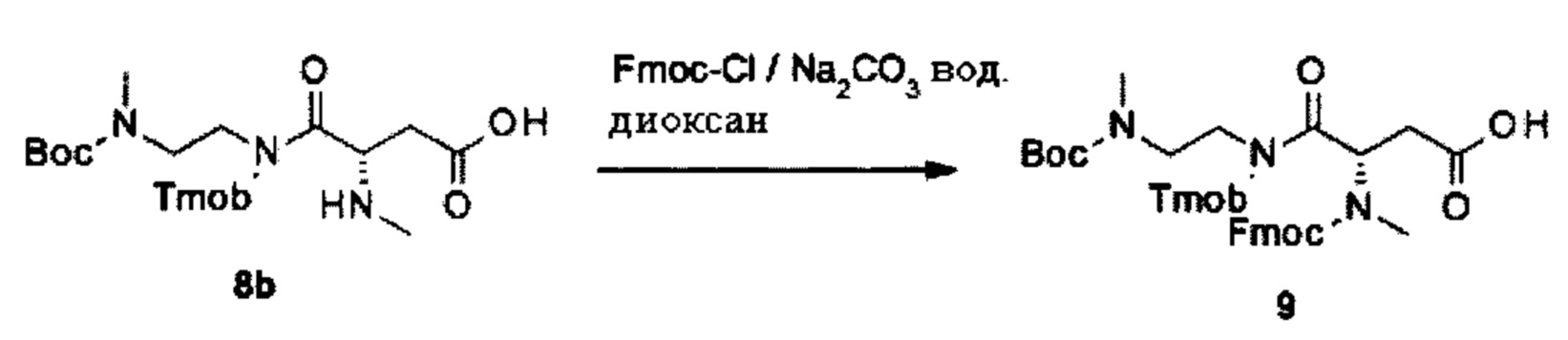
К раствору 8b (2.00 г, 4.14 ммоль) и Fmoc-Cl (1.07 г, 4.14 ммоль) в диоксане (20 мл) добавили 1 М раствор Na2CO3 (20 мл). Реакционную смесь перемешивали в течение 40 мин при комнатной температуре. Воду (100 мл) и простой диэтиловый эфир (100 мл) добавили, и водную фазу экстрагировали 2 х с помощью простого диэтилового эфира (100 мл). Водную фазу подкислили с помощью конц. HCl до рН 1 и снова экстрагировали 3 х с помощью простого диэтилового эфира. Объединенные органические фазы высушили над Na2SO4, и растворитель удалили в вакууме. Соединение 9 применяли на следующей стадии без дальнейшей очистки.
Выход: 2.63 г (3.73 ммоль, 90%)
MS: m/z 728.32=[M+Na]+, (вычисленная моноизотопическая масса = 705.33).
Пример 10
Синтез обратимого Lys26-CNP-3-ПЭГ2×20 кДа конъюгата 10f
Конъюгат 10f синтезировали согласно следующей схеме:
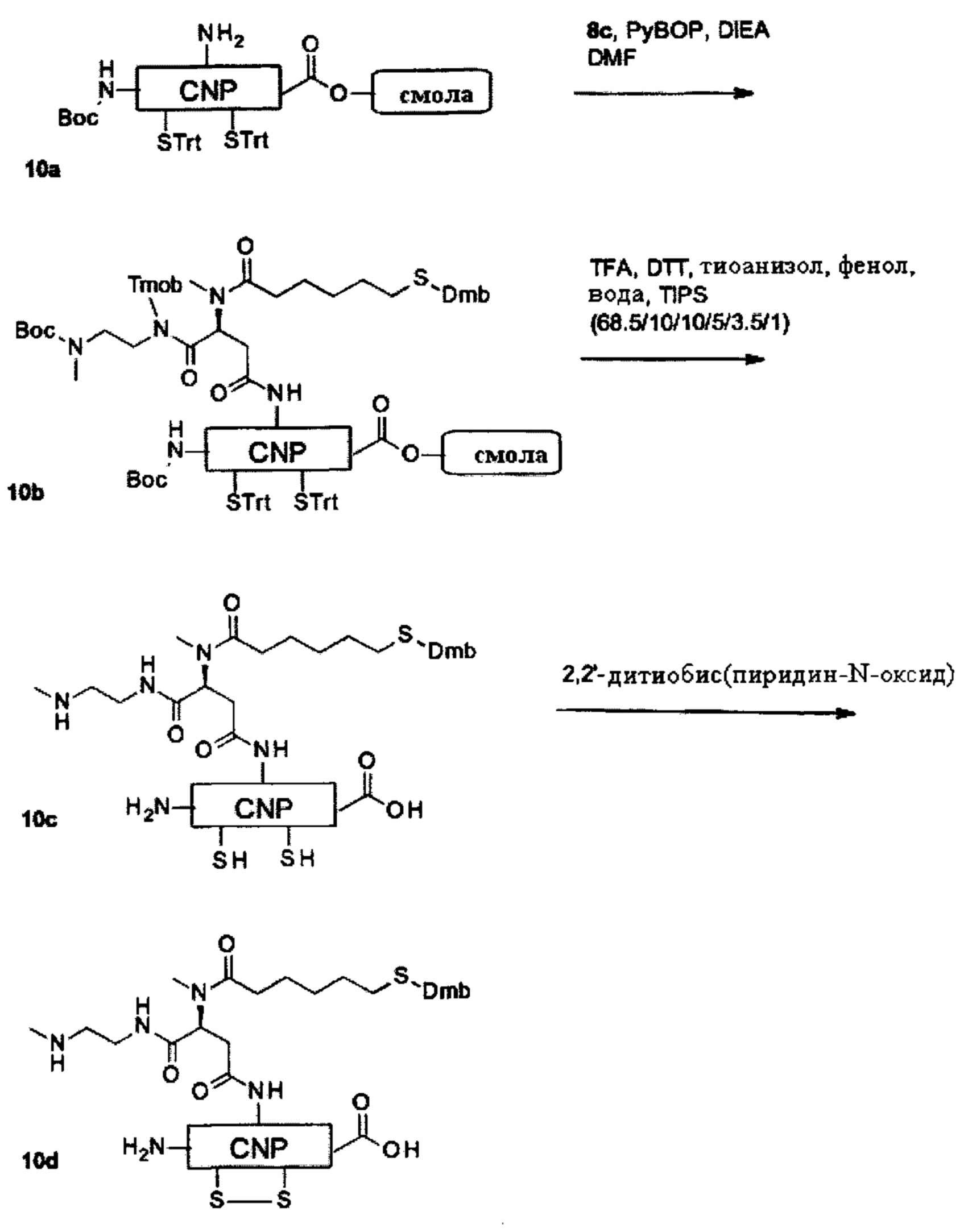
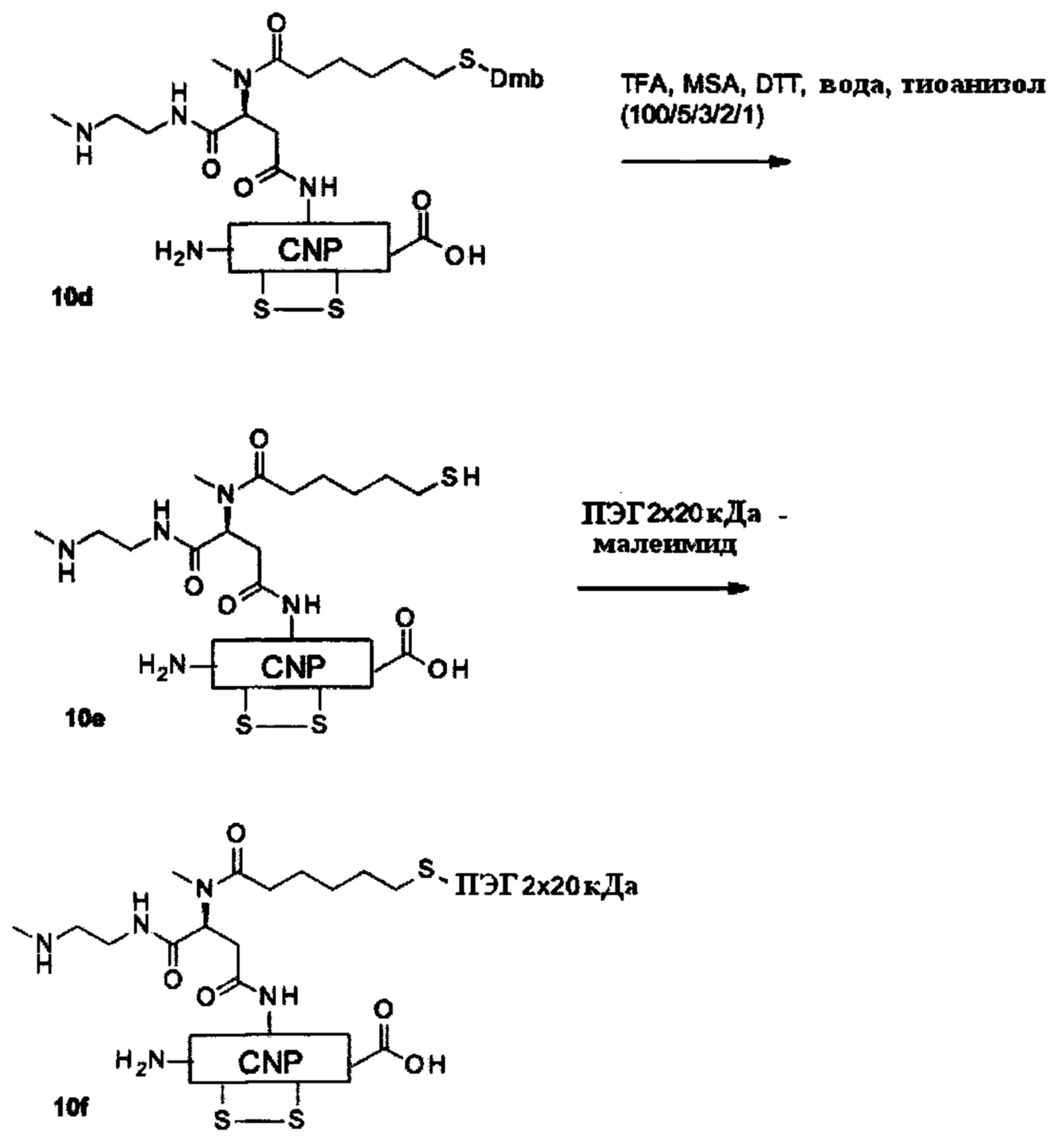
2.00 г (0.21 ммоль) CNP-38 с защищенной боковой цепью на TCP смоле, имеющего Вос-защищенный N-конец и ivDde-защищенную боковую цепь Lys26 подвергли удалению защитной группы ivDde согласно методике, описанной в части Вещества и Способы с получением 10а. Раствор линкерного реагента 8с (336 мг, 0.46 ммоль), РуВОР (239 мг, 0.46 ммоль) и DIEA (182 μL, 1.04 ммоль) в DMF (5 мл) инкубировали в течение 10 мин при комнатной температуре, затем добавили к смоле 10а. Суспензию встряхивали в течение 2 ч при комнатной температуре. Смолу промыли 10 х с помощью DMF (10 мл) и 10 х с помощью DCM (10 мл) и высушили в вакууме в течение 15 мин. Отщепление пептида от смолы и удаление защитных групп достигалось посредством обработки смолы с помощью 15 мл предварительно охлажденного (-18°С) расщепляющего коктейля 68.5/10/10/5/3.5/1 (об./мас./об./об./об./об.) TFA/DTT/тиоанизол/фенол/вода/TIPS. Смеси позволили нагреться до комнатной температуры и взбалтывали в течение 60 мин. Неочищенное 10с осадили в предварительно охлажденном простом диэтиловом эфире (-18°С). Осадок растворили в ACN/вода и очистили посредством ОФ-ВЭЖХ. Объединенные ВЭЖХ-фракции непосредственно применяли на следующей стадии.
MS: m/z 1124.60=[М+4Н]4+, (вычисленная моноизотопическая масса для [М+4Н]4+=1124.59).
К объединенным ВЭЖХ-фракциям 10с (250 мл) добавили 40 мл 0.5 М буфера на основе лимонной кислоты (рН=5.00) и 7 мл 0.01 М раствора 2,2’-дитиобис(пиридин-N-оксида), раствор в 1/1 (об./об.) ацетонитрил/вода. После инкубации в течение 5 мин при комнатной температуре реакцию завершили. Смесь разбавили с помощью 500 мл воды, содержащей 0.1% TFA (об./об.) и подкислили с помощью АсОН (20 мл) до pH около 2. Соединение 10d очистили посредством ОФ-ВЭЖХ.
Выход: 101 мг (17.3 мкмоль, 9%) CNP-38-линкер-Dmb * 10 TFA
MS: m/z 1124.10=[М+4Н]4+, (вычисленная моноизотопическая масса для [М+4Н]4+=1124.09).
Отщепление защитной группы Dmb достигли путем добавления 30 мл предварительно охлажденного (-18°С) расщепляющего коктейля 100/5/3/2/1 (об./об./масс./об./об.) TFA/MSA/DTT/вода/тиоанизол к 10d (101 мг, 17.3 мкмоль) и перемешивания в течение 3 ч при 0°С. Неочищенное 10е осадили в предварительно охлажденном (-18°С) простом диэтиловом эфире. Осадок растворили в воде, содержащей 0.1% TFA (об./об.), и инкубировали в течение 10 мин, чтобы гидролизовать любые сложные эфиры TFA. Соединение 10е очистили посредством ОФ-ВЭЖХ.
Выход: 46 мг (8.34 мкмоль, 48%) CNP-38-линкер-тиол * 10 TFA
MS: m/z 1094.58=[М+4Н]4+, (вычисленная моноизотопическая масса для [М+4Н]4+=1094.57).
К раствору 10е (46 мг, 8.43 мкмоль) в 1.15 мл воды, содержащей 0.1% TFA (об./об.), добавили раствор ПЭГ 2×20 кДа малеимида (Sunbright GL2-400MA, 870 мг, 21.75 мкмоль) и 4.35 мл воды, содержащей 0.1% TFA (об./об.), а затем 0.5 М буфер на основе молочной кислоты (1.07 мл, рН=4.20). Смесь перемешивали при комнатной температуре в течение 4 ч. Конъюгат 10f очистили посредством ОФ-ВЭЖХ.
Выход: 233 мг (5.21 мкмоль, 62%) конъюгат 10f * 10 HCl
Пример 11
Синтез обратимого Lys26-CNP-38-ПЭГ4×10 кДа коньюгата 11i
Конъюгат 11i синтезировали согласно следующей схеме:
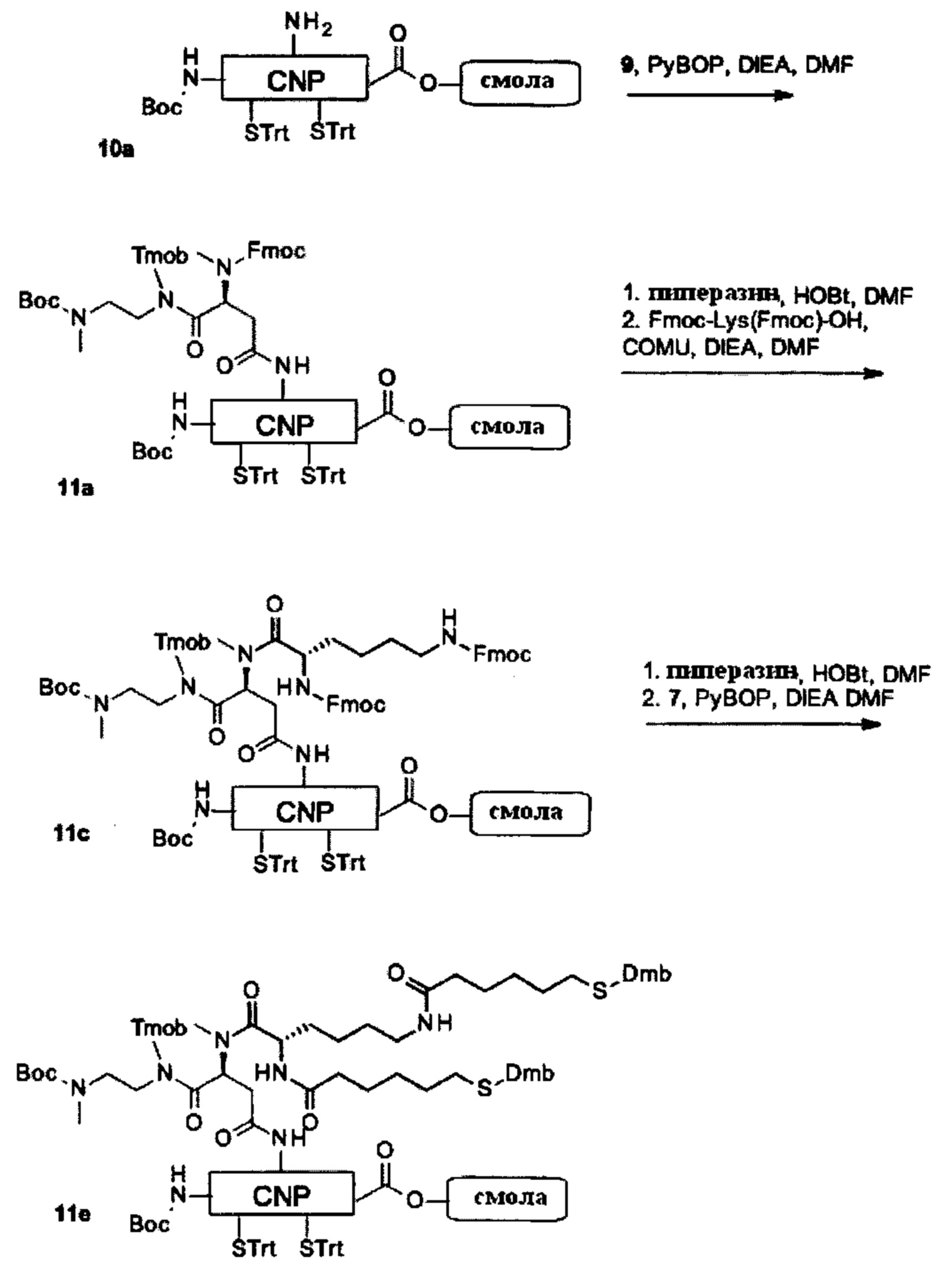
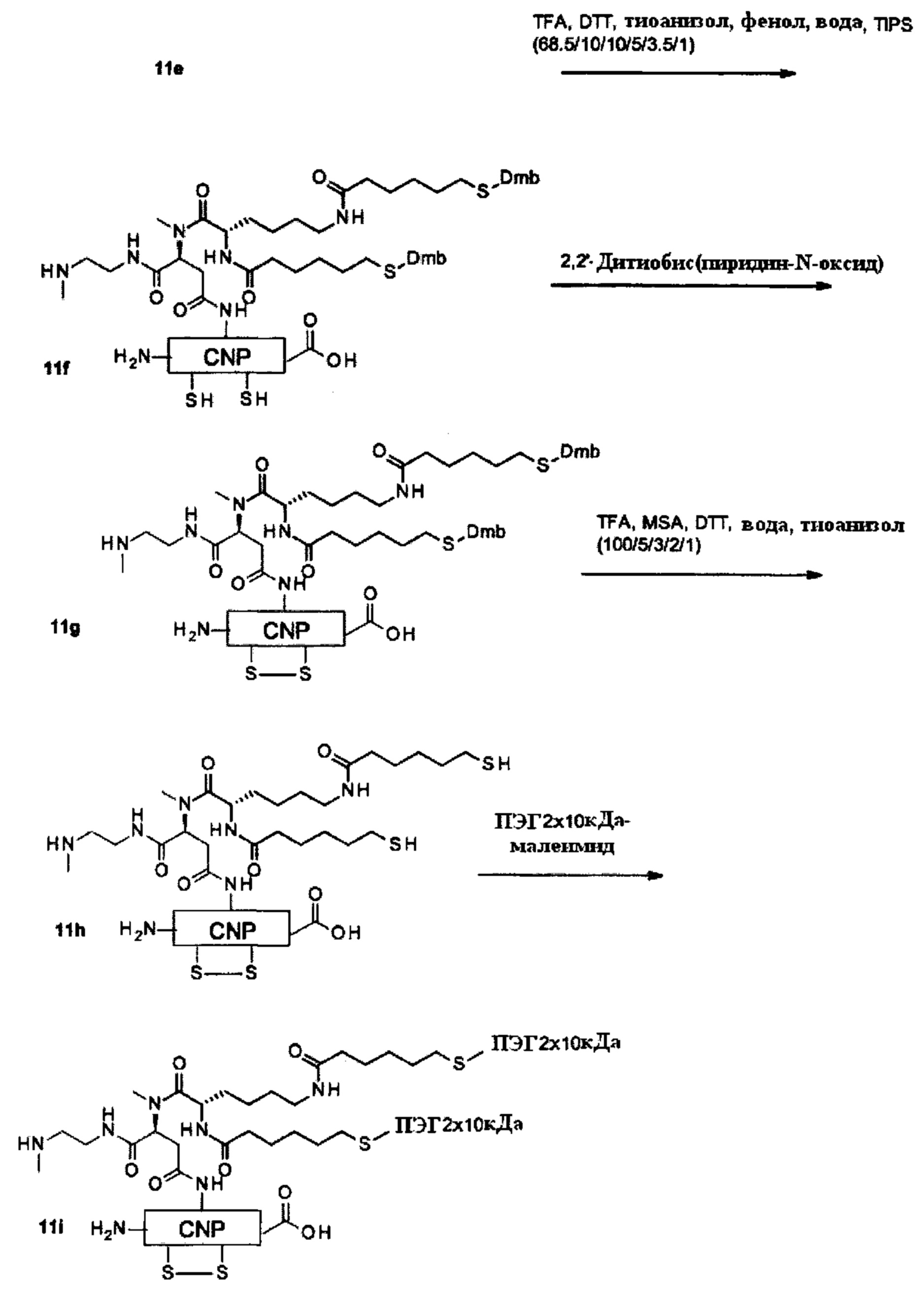
К раствору 9 (353 мг, 0.50 ммоль) и РуВОР (260 мг, 0.50 ммоль) в DMF (9 мл) добавили DIEA (105 мкл, 0.60 ммоль). Эту смесь нанесли на смолу CNP-38 с боковой цепью Lys26 с удаленной защитной группой 10а (2.00 г, 0.21 ммоль), и суспензию встряхивали в течение 2 ч при комнатной температуре, чтобы получить смолу 11а. Смолу промыли 10 х с помощью DMF (7 мл). Отщепление защитной группы Fmoc в 11а осуществили с помощью раствора HOBt (0.68 г, 5.03 ммоль) и пиперазина (3.00 г, 34.83 ммоль) в DMF (47 мл). Для этого смолу инкубировали 5 х с помощью 10 мл расщепляющей смеси в течение 15 мин при комнатной температуре каждый раз. Затем смолу промыли 7 х с помощью DMF (7 мл).
Раствор Fmoc-Lys(Fmoc)-OH (449 мг, 0.76 ммоль), COMU (325 мг, 0.76 ммоль) и DIEA (165 μL, 0.95 ммоль) в DMF (9 мл) получили и нанесли на смолу. Смесь встряхивали в течение 2 ч при комнатной температуре. Процедуру повторили дважды, каждый раз в течение 1 ч со свежеполученной связывающей смесью. Смолу промыли 10 х с помощью DMF (7 мл), и оставшиеся свободные аминогруппы закрыли с помощью 8 мл 1/1/2 (об./об./об.) Ас2О/пиридин/DMF.
Отщепление защитной группы Fmoc в 11с осуществили с помощью раствора HOBt (0.68 г, 5.03 ммоль), пиперазина (3.00 г, 34.83 ммоль) в DMF (47 мл). Для этого смолу инкубировали 5 х с помощью 10 мл расщепляющей смеси в течение 15 мин при комнатной температуре каждый раз. Смолу промыли 7 х с помощью DMF (7 мл)
К раствору 7 (266 мг, 1.00 ммоль) и РуВОР (520 мг, 1.00 ммоль) в DMF (9 мл) добавили DIEA (209 μL, 1.20 ммоль). Эту смесь нанесли на смолу и встряхивали в течение 2 ч при комнатной температуре. Смолу промыли 7 х с помощью DMF (7 мл) с получением смолы 11е. Отщепление пептида от смолы и удаление защитных групп достигалось посредством обработки смолы с помощью 15 мл предварительно охлажденного (-18°С) расщепляющего коктейля 68.5/10/10/5/3.5/1 (об./мас./об./об./об./об.) TFA/DTT/тиоанизол/фенол/вода/TIPS. Смеси позволили нагреться до комнатной температуры и взбалтывали в течение 3 ч. Неочищенное соединение 11f осадили в предварительно охлажденном (-18°С) простом диэтиловом эфире и очистили посредством ОФ-ВЭЖХ. Объединенные ВЭЖХ-фракции непосредственно применяли на следующей стадии.
MS: m/z 1218.66=[M+4H]4+, (вычисленная моноизотопическая масса для [М+4Н]4+=1218.65).
К объединенным D”:{-фракциям продукта 11f (1 L) 160 мл 0.5 М буфера на основе лимонной кислоты (рН=5.00) и добавили 100 мл 50 мМ 2,2’-дитиобис(пиридин-N-оксид) раствора в 9/1 (об./об.) ацетонитрил/вода. Смесь перемешивали в течение 4 ч при комнатной температуре и затем разбавили с помощью 1 Л воды, содержащей 0.1% TFA (об./об.). Соединение 11g очистили посредством ОФ-ВЭЖХ.
Выход: 64.3 мг (10.7 мкмоль, 6%) CNP-38-линкер-DMB * 10 TFA
MS: m/z 1218.15=[М+4Н]4+, (вычисленная моноизотопическая масса для [М+4Н]4+=1218.14).
Отщепление защитной группы Dmb достигли путем добавления 45 мл предварительно охлажденного (-18°С) расщепляющего коктейля 100/5/3/2/1 (об./об./w/об./об.) TFA/MSA/DTT/вода/тиоанизол к 11g (61.8 мг, 10.3 мкмоль) и затем перемешивания в течение 4 ч при 0°С. Неочищенное соединение 11h осадили в предварительно охлажденном (-18°С) простом эфире. Осадок растворили в растворе 1/1 (об./об.) ацетонитрил/вода, содержащая 0.1% TFA (об./об.), и инкубировали в течение 4 ч при комнатной температуре, чтобы гидролизовать любые сложные эфиры TFA. Соединение 11h очистили посредством ОФ-ВЭЖХ.
Выход: 38.4 мг (6.65 мкмоль, 65%) CNP-38-линкер-тиол * 10 TFA
MS: m/z 1159.11=[М+4Н]4+, (вычисленная моноизотопическая масса для [М+4Н]4+=1159.10).
К раствору 11h (34.6 мг, 5.99 мкмоль) в 1 мл воды, содержащей 0.1% TFA (об./об.), добавили раствор ПЭГ 2×10 кДа малеимида (Sunbright GL2-200MA, 1.12 г, 56.03 мкмоль) в 6.1 мл воды, содержащей 0.1% TFA (об./об.), а затем 0.5 М буфер на основе молочной кислоты (1.46 мл, рН=4.00). Смесь перемешивали при комнатной температуре в течение 4 ч. Конъюгат 11i очистили посредством ОФ-ВЭЖХ.
Выход: 227 мг (4.96 мкмоль, 83%) конъюгата 11i * 10 HCl
Пример 12
Синтез перманентного Lys26 CNP-38 ПЭГ4×10 кДа конъюгата 12g
Конъюгат 12g синтезировали согласно следующей схеме:
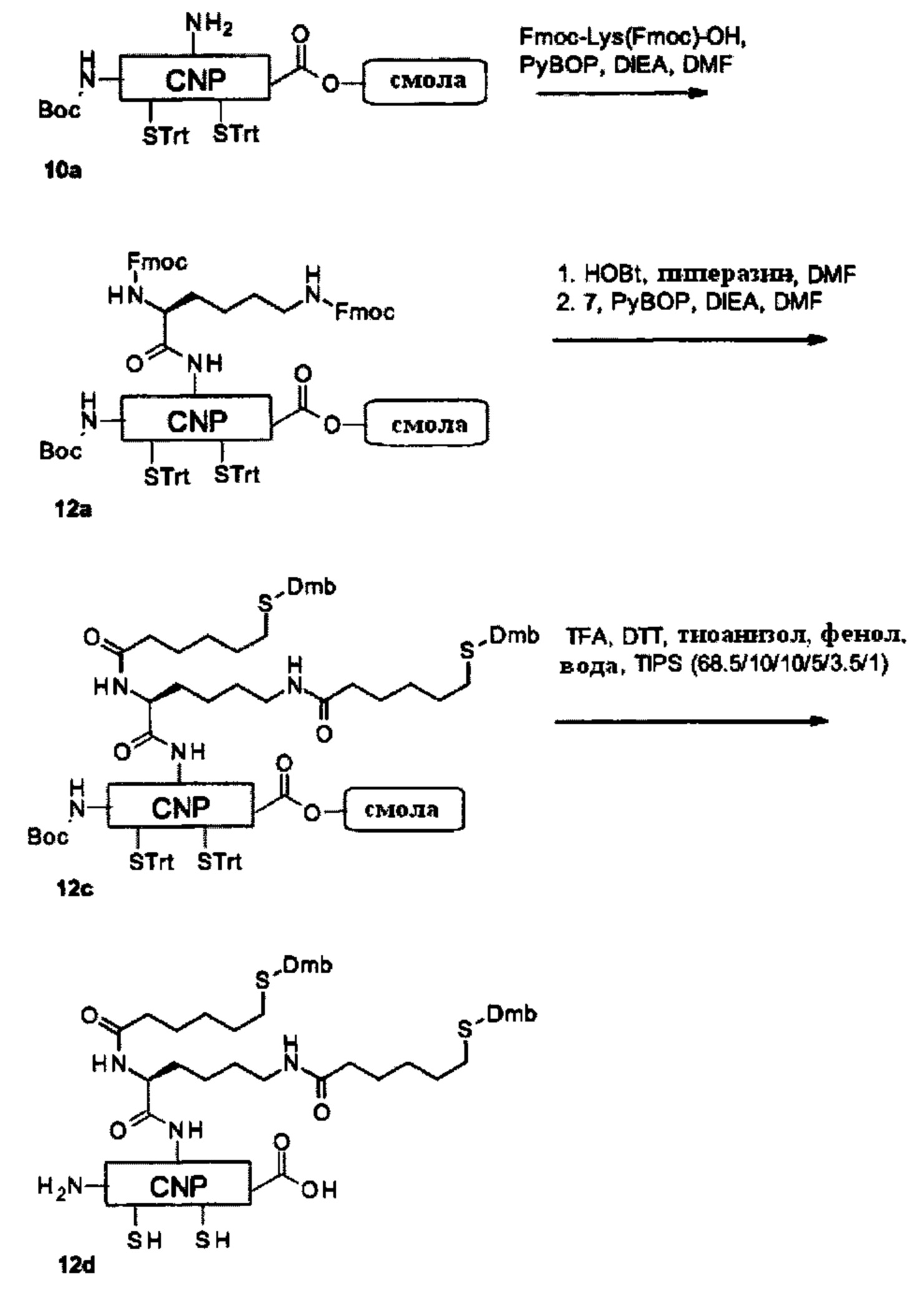
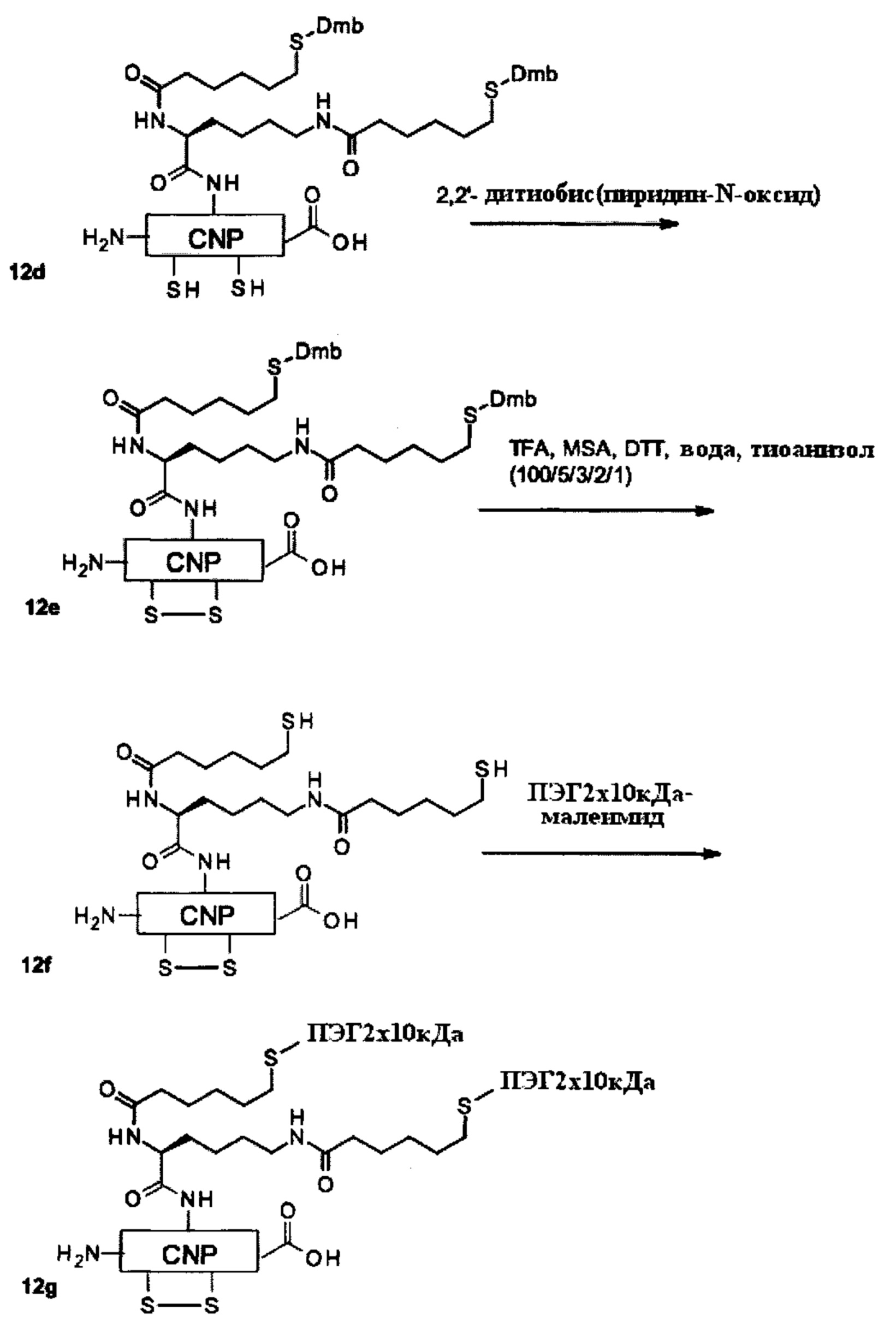
К раствору Fmoc-Lys(Fmoc)-OH (365 мг, 0.62 ммоль) и РуВОР (322 мг, 0.62 ммоль) в DMF (4.6 мл) добавили DIEA (0.11 мл, 0.62 ммоль). Смесь нанесли на смолу 10а (2.0 г, 0.21 ммоль). Суспензию встряхивали в течение 2 ч при комнатной температуре.
Смолу промыли 10 х с помощью DMF (7 мл). Отщепление защитной группы Fmoc в 12а осуществили с помощью раствора HOBt (1.35 г, 9.99 ммоль), пиперазина (6.00 г, 69.66 ммоль) в DMF (94 мл). Для этого смолу инкубировали 5 х с помощью расщепляющей смеси в течение 15 мин при комнатной температуре каждый раз, с получением смолы 12b. Затем смолу промыли 7 х с помощью DMF (7 мл)
К раствору 7 (283 мг, 1.06 ммоль) и РуВОР (552 мг, 1.06 ммоль) в DMF (6.5 мл) добавили DIEA (185 мкл, 1.06 ммоль) и нанесли на смолу 12b (2.07 г, 0.10 ммоль/г, 0.21 ммоль). Смесь встряхивали в течение 2 ч при комнатной температуре. Затем смолу промыли 10 х каждый раз с помощью DMF (7 мл) и CH2Cl2 (7 мл) и высушили в вакууме.
Отщепление пептида от смолы и удаление защитных групп достигалось посредством обработки смолы с помощью 15 мл предварительно охлажденного (-18°С) расщепляющего коктейля 68.5/10/10/5/3.5/1 (об./мас./об./об./об./об.) TFA/DTT/тиоанизол/фенол/вода/TIPS. Смеси позволили нагреться до комнатной температуры и взбалтывали в течение 2.5 ч. Неочищенное соединение 12d осадили в предварительно охлажденном простом диэтиловом эфире (-18°С) и очистили посредством ОФ-ВЭЖХ. Объединенные ВЭЖХ-фракции непосредственно применяли на следующей стадии.
MS: m/z 1172.37=[М+4Н]4+, (вычисленная моноизотопическая масса для [М+4Н]4+=1172.37).
К объединенным ВЭЖХ-фракциям продукта 12d (390 мл) добавили 58.5 мл 0.5 М буфера на основе лимонной кислоты (рН=5.00) и 8.9 мл 10 мМ 2,2’-дитиобис(пиридин-N-оксид) раствора в 1/1 (об./об.) ацетонитрил/вода. Смесь перемешивали в течение 10 мин при комнатной температуре, затем разбавили с помощью 400 мл воды, содержащей 0.1% TFA (об./об.). Соединение 12е очистили посредством ОФ-ВЭЖХ.
Выход: 100 мг (17.5 мкмоль, 8% за 6 стадий) CNP-38-линкер-Dmb * 9 TFA
MS: m/z 1171.87=[M+4H]4+, (вычисленная моноизотопическая масса для [М+4Н]4+=1171.86).
Отщепление защитной группы Dmb достигли путем добавления 65 мл предварительно охлажденного (-18°С) расщепляющего коктейля 100/5/3/2/1 (об./об./мас./об./об.) TFA/MSA/DTT/вода/тиоанизол к соединению 12е (100 мг, 17.5 мкмоль) и перемешивания в течение 3.5 ч при 0°С. Неочищенное соединение 12f осадили в предварительно охлажденном (-18°С) простом диэтиловом эфире. Осадок растворили в воде, содержащей 0.1% TFA (об./об.), и инкубировали в течение 2 ч при комнатной температуре, чтобы гидролизовать любые сложные эфиры TFA. Соединение 12f очистили посредством ОФ-ВЭЖХ.
Выход: 43.4 мг (7.92 мкмоль, 45%) CNP-38-линкер-тиол * 9 TFA
MS: m/z 1112.83=[М+4Н]4+, (вычисленная моноизотопическая масса для [М+4Н]4+=1112.82).
К раствору 12f (39.6 мг, 7.22 мкмоль) в 1 мл воды, содержащей 0.1% TFA (об./об.), добавили раствор ПЭГ 2×10 кДа малеимида (Sunbright GL2-200MA, 1.22 г, 59.94 мкмоль) в 6.16 мл воды, содержащей 0.1% TFA (об./об.), а затем 0.5 М буфер на основе молочной кислоты (1.41 мл, рН=4.20). Смесь перемешивали при комнатной температуре в течение 4 ч. Конъюгат 12g очистили посредством ОФ-ВЭЖХ.
Выход: 204 мг (4.48 мкмоль, 57%) конъюгата 12g * 9 HCl
Пример 13
Синтез ПЭГ5кДа тиола 13с
ПЭГ 5кДа тиол 13с синтезировали согласно следующей схеме:
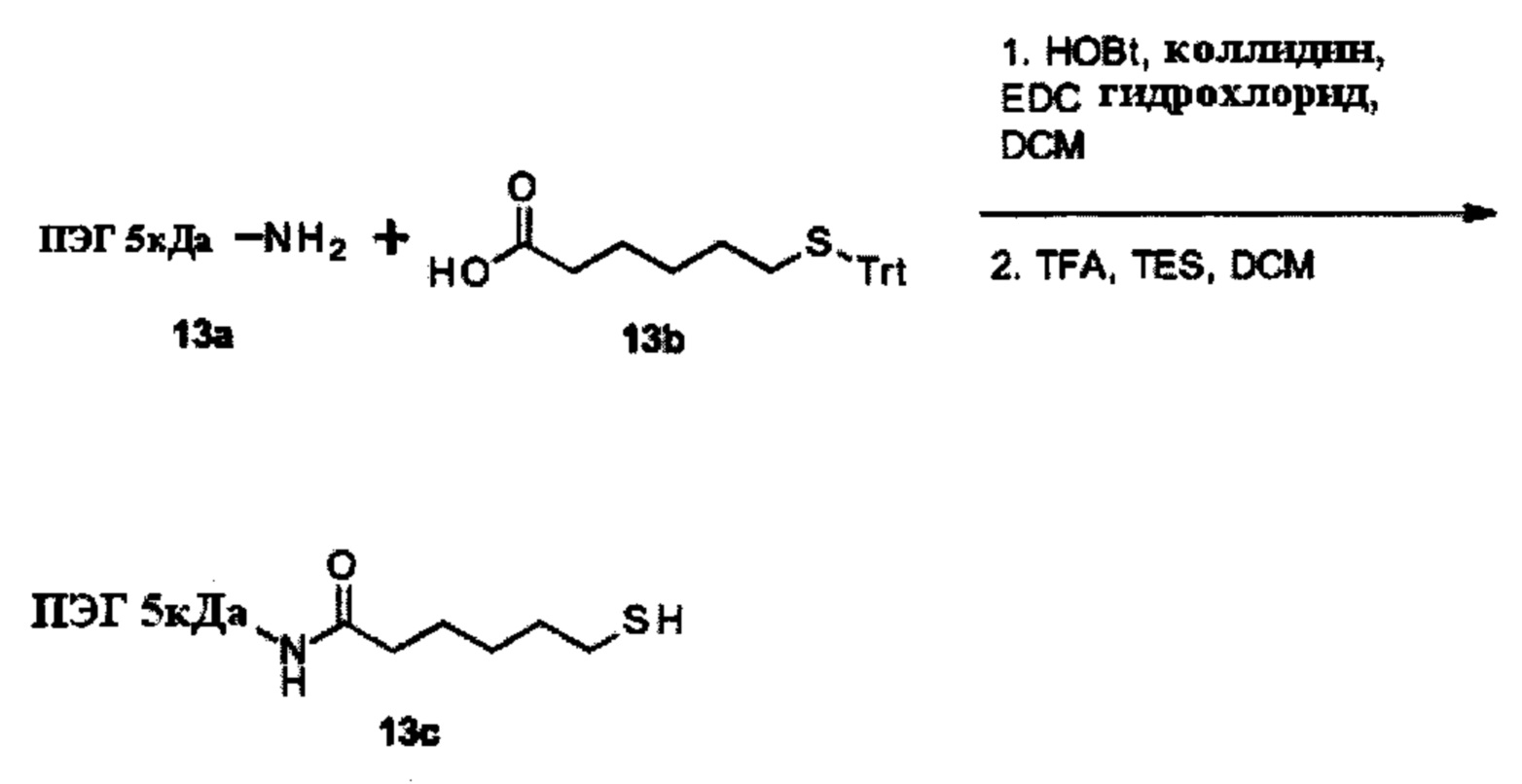
К раствору 13b (58.6 мг, 0.15 ммоль), HOBt (22.9 мг, 0.15 ммоль) и EDC гидрохлорида (28.8 мг, 0.15 ммоль) в DCM (1.00 мл) добавили 2,4,6-коллидин (121 мг, 1.00 ммоль). Затем добавили раствор метокси-ПЭГ-амина 5 кДа 13а (500 мг, 0.10 ммоль) в DCM (4.00 мл), и смесь перемешивали в течение 16 ч при комнатной температуре. Растворитель выпарили, и смесь растворили в ACN/воде и очистили посредством ОФ-ВЭЖХ. Количество растворителя уменьшили в вакууме, и водный остаток экстрагировали с помощью DCM (1×100 мл, 2×50 мл). Объединенные органические слои уменьшили в вакууме до 20 мл. TFA (1.6 мл) и TES (3.5 мл) добавили, и смесь перемешивали при комнатной температуре в течение 4.5 ч. Соединение 13с осадили в простом диэтиловом эфире, хранили всю ночь при - 20°С, отфильтровали и высушили в вакууме.
Выход: 372 мг (72 мкмоль, 72%)
Пример 14
Синтез перманентного N-терминального CNP-34 ПЭГ 5 кДа конъюгата 14е
Конъюгат 14е синтезировали согласно следующей схеме:
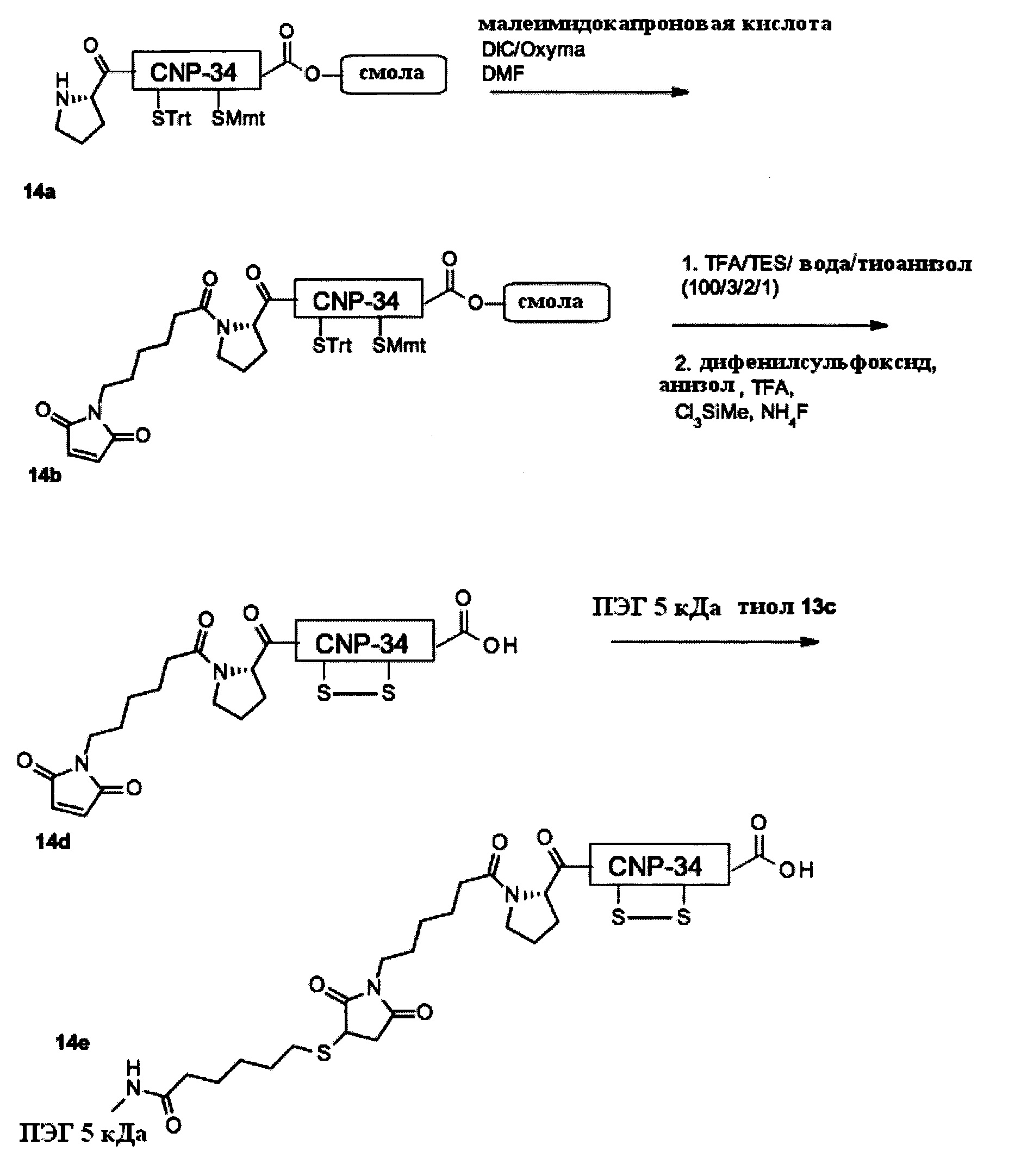
CNP-34 с защищенной боковой цепью на TCP смоле tentagel, имеющий свободный N-конец, 14а (0.78 г, 70 мкмоль) предварительно разбух в DMF в течение 30 мин. Раствор малеимидокапроновой кислоты (85.3 мг, 0.40 ммоль), DIC (50.9 мг, 0.40 ммоль) и оксима (57.4 мл, 0.40 ммоль) в DMF (6 мл) нанесли на смолу, и смесь встряхивали в течение 30 мин при комнатной температуре. Связывание затем повторили один раз со свежеполученным связывающим раствором. Смолу промыли 10 х каждый раз с помощью DMF и CH2Cl2 и высушили в вакууме с получением 14b.
Отщепление пептида от смолы и удаление защитных групп достигалось посредством обработки смолы с помощью 6 мл расщепляющего коктейля 100/3/2/1 (об./об./об./об.) TFA/TES/вода/тиоанизол в течение 1.5 ч при комнатной температуре. Неочищенный пептид осадили в предварительно охлажденном (-18°С) простом диэтиловом эфире.
MS: m/z 937.77 = [М+4Н]4+, (вычисленная моноизотопическая масса для [М+4Н]4+ = 937.74).
Осадок растворили в 15 мл TFA. Раствор дифенилсульфоксида (68.06 мг, 0.34 ммоль) и анизола (0.18 мл, 1.68 ммоль) в 5 мл TFA добавили. Трихлорметилсилан (0.47 мл, 4.17 ммоль) добавили, и смесь перемешивали в течение 15 мин при комнатной температуре. Аммония фторид (0.38 г, 10.3 ммоль) добавили, и раствор встряхивали в течение еще 2 мин. Неочищенное вещество осадили в предварительно охлажденном (-18°С) простом диэтиловом эфире и очистили посредством ОФ-ВЭЖХ, с получением 14d.
Выход: 8.30 мг (1.78 мкмоль, 82% чистота, 1.4% за 3 стадии) CNP-34-Malhx * 8 TFA
MS: m/z 937.26 = [M+4H]4+, (вычисленная моноизотопическая масса для [М+4H]4+ = 937.23).
К раствору 14d (7.34 мг, 1.57 мкмоль) в 200 мкл 1/1 (об./об.) ацетонитрил/вода, содержащая 0.1% TFA (об./об.), добавили раствор 13 с (20 мг, 3.90 мкмоль) в 200 мкл воды, содержащей 0.1% TFA (об./об.), а затем 200 мкл 0.5 М ацетатного буфера (рН=5.00). Смесь инкубировали при комнатной температуре в течение 30 мин. Конъюгат 14е очистили посредством ОФ-ВЭЖХ.
Выход: 9.92 мг (1.01 мкмоль, 57%) конъюгата 14е * 8 TFA
Пример 15
Синтез перманентного N-терминального CNP-38 ПЭГ 5 кДа конъюгата 15е
Конъюгат 15е синтезировали согласно следующей схеме:
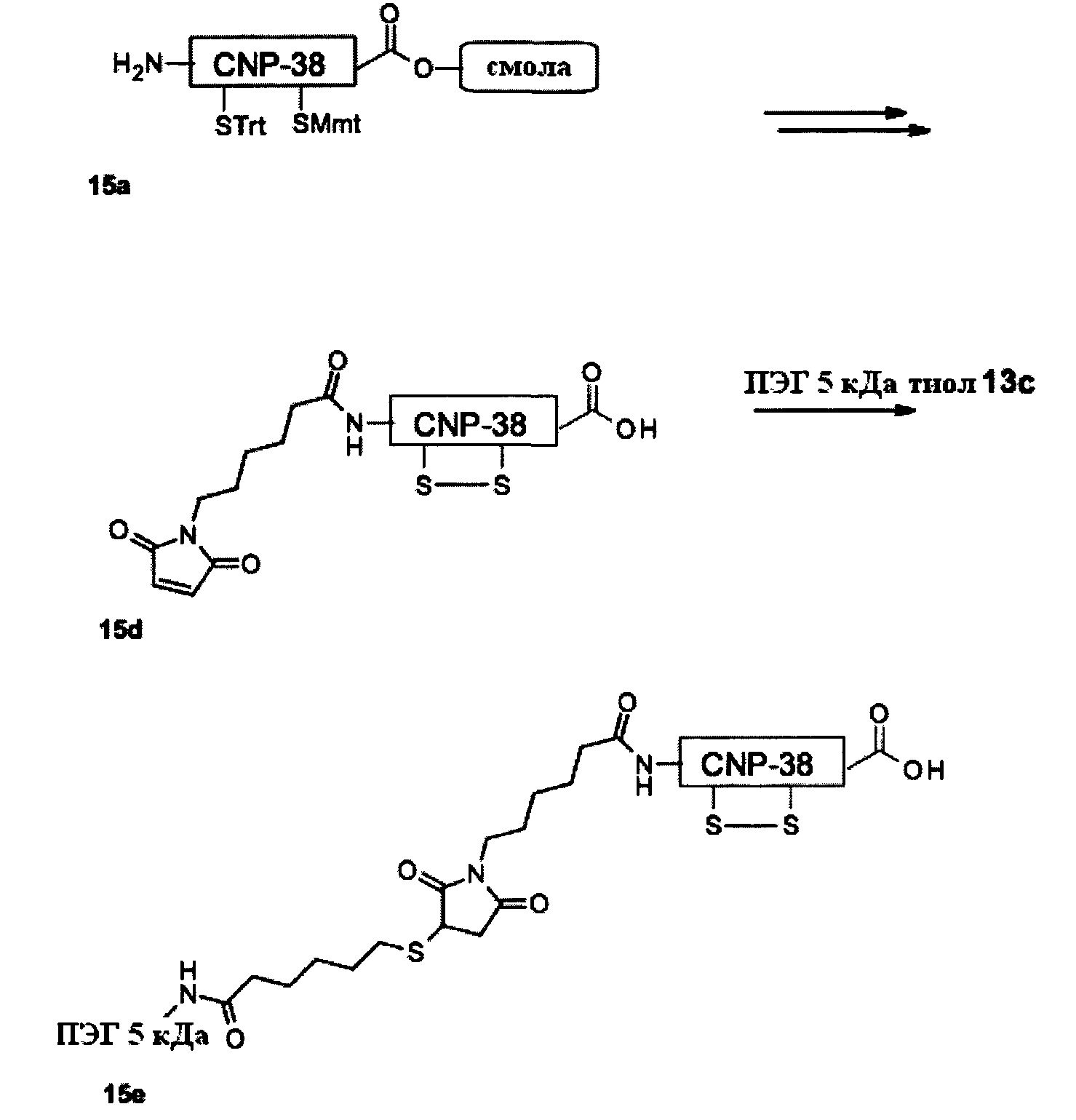
Соединение 15d синтезировали, как описано для 14d, за исключением того, что CNP-38 с защищенной боковой цепью на TCP смоле tentagel, имеющий свободный N-конец, 15а (1.34 г, 0.12 ммоль) применяли в качестве исходного вещества.
Выход: 15.6 мг (2.94 мкмоль, 6.6%) CNP-38-Malhx * 9 TFA
MS: m/z 1064.05 = [M+4H]4+, (вычисленная моноизотопическая масса для [M+4H]4+ = 1064.04).
Конъюгат 15е синтезировали, как описано для 14е, за исключением того, что 15d (8.34 г, 1.58 ммоль) применяли в качестве исходного вещества.
Выход: 9.47 мг (0.91 мкмоль, 31%) конъюгата 15е * 9 TFA
Пример 16
Синтез перманентного Lys12-CNP-34-ПЭГ 5 кДа конъюгата 16е
Конъюгат 16е синтезировали согласно следующей схеме:
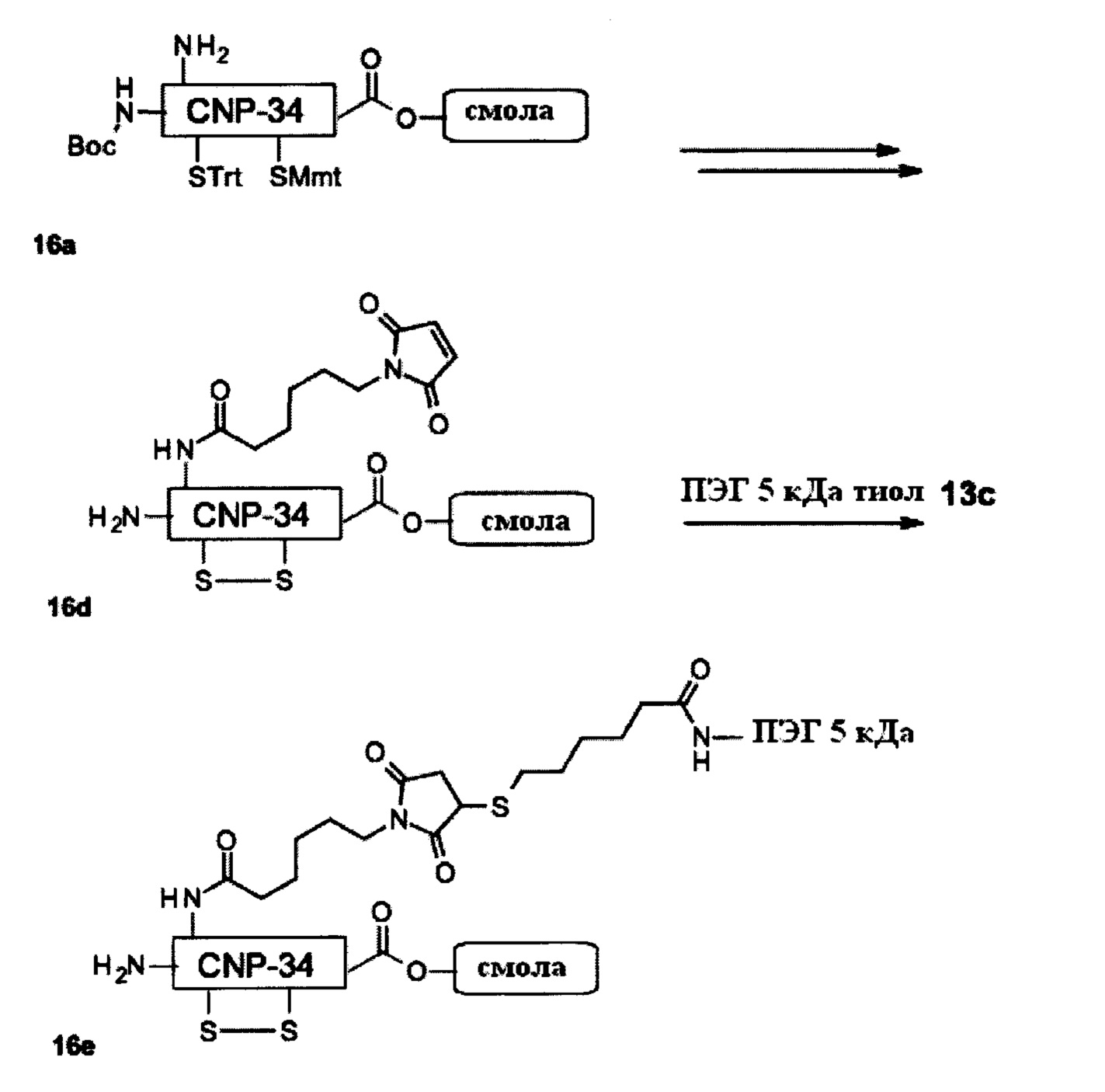
1.00 г (0.10 ммоль) CNP-34 с защищенной боковой цепью на TCP смоле tentagel, имеющего Вос-защищенный N-конец и ivDde-защищенную боковую цепь Lys12, подвергли удалению защитной группы ivDde согласно методике, описанной в части Вещества и Способы, с получением 16а.
Соединение 16d синтезировали, как описано для 14d, за исключением того, что смола 16а (1.00 г, 0.10 ммоль) применялась в качестве исходного вещества.
Выход: 17.0 мг (3.65 мкмоль, 3.7%) CNP-34-Lys12-Malhx * 8 TFA
MS: m/z 937.25 = [М+4Н]4+, (вычисленная моноизотопическая масса для [N+4H]4+ = 937.23).
Конъюгат 16е синтезировали, как описано для 14е, за исключением того, что 16d (17 мг, 3.65 мкмоль) применяли в качестве исходного вещества.
Выход: 12.2 мг (1.25 мкмоль, 34%) конъюгат 16е * 8 TFA
Пример 17
Синтез перманентного Lys16 CNP-34 ПЭГ 5 кДа конъюгата 17е
Конъюгат 17е синтезировали согласно следующей схеме:
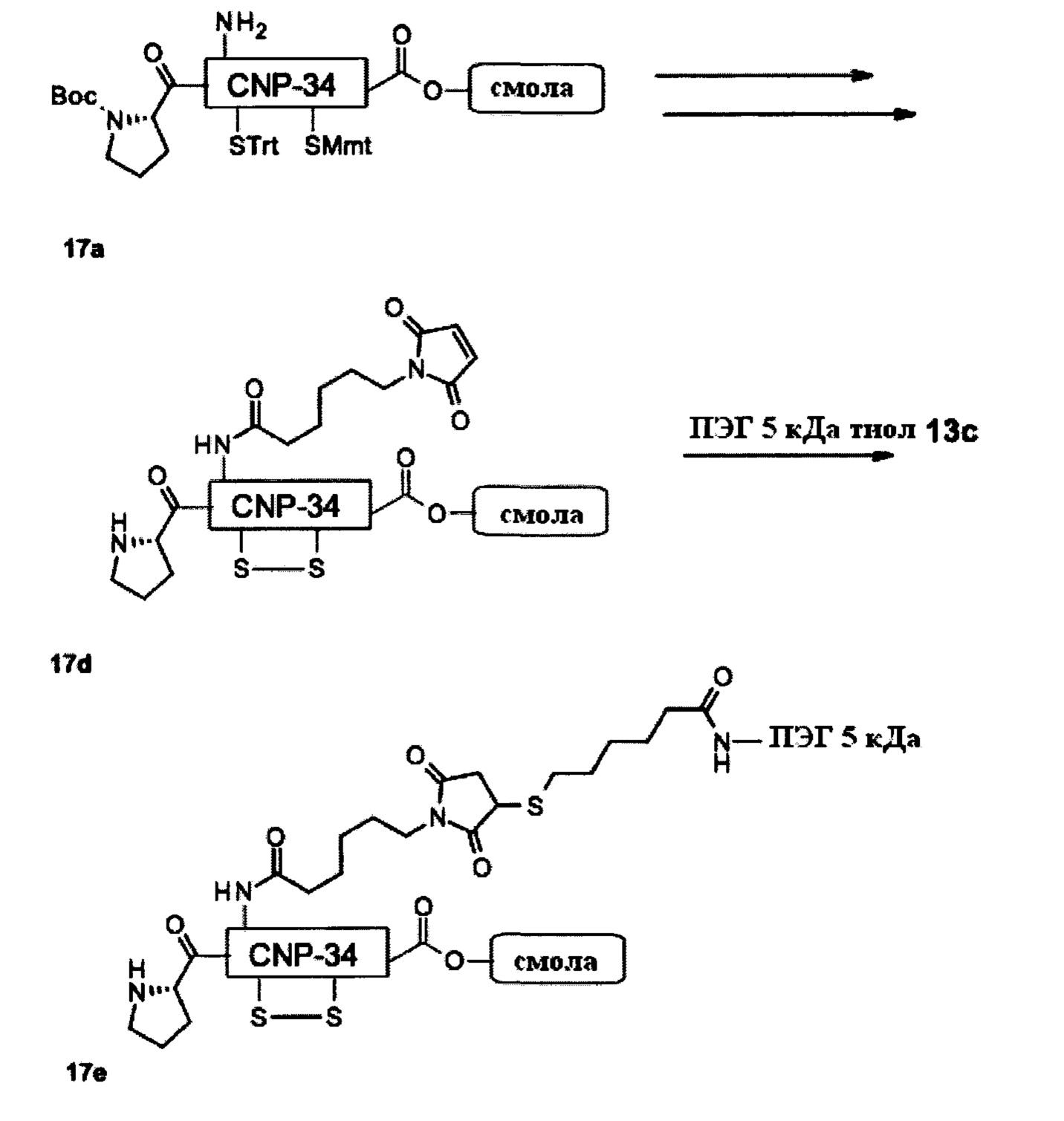
0.78 г (0.07 ммоль) CNP- 34 с защищенной боковой цепью на TCP смоле tentagel, имеющего Вос-защищенный N-конец и ivDde-защищенную боковую цепь Lys16, подвергли удалению защитной группы ivDde согласно методике, описанной в части Вещества и Способы, с получением 17а.
Соединение 17d синтезировали, как описано для 14d, за исключением того, что смола 17а (0.78 г, 0.13 ммоль) применялась в качестве исходного вещества.
Выход: 5.39 мг (1.16 мкмоль, 1.7%) CNP-34-Lys16-Malhx * 8 TFA
MS: m/z 937.26 = [M+4H]4+, (вычисленная моноизотопическая масса для [M+4H]4+ = 937.23).
Конъюгат 17е синтезировали, как описано для 14е, за исключением того, что 17d (5.39 мг, 1.16 мкмоль) применяли в качестве исходного вещества.
Выход: 10.7 мг (1.09 мкмоль, 94%) конъюгат 17е * 8 TFA
Пример 18
Синтез перманентного Lys22 CNP-34 ПЭГ 5 кДа конъюгата 18е
Конъюгат 18е синтезировали согласно следующей схеме:
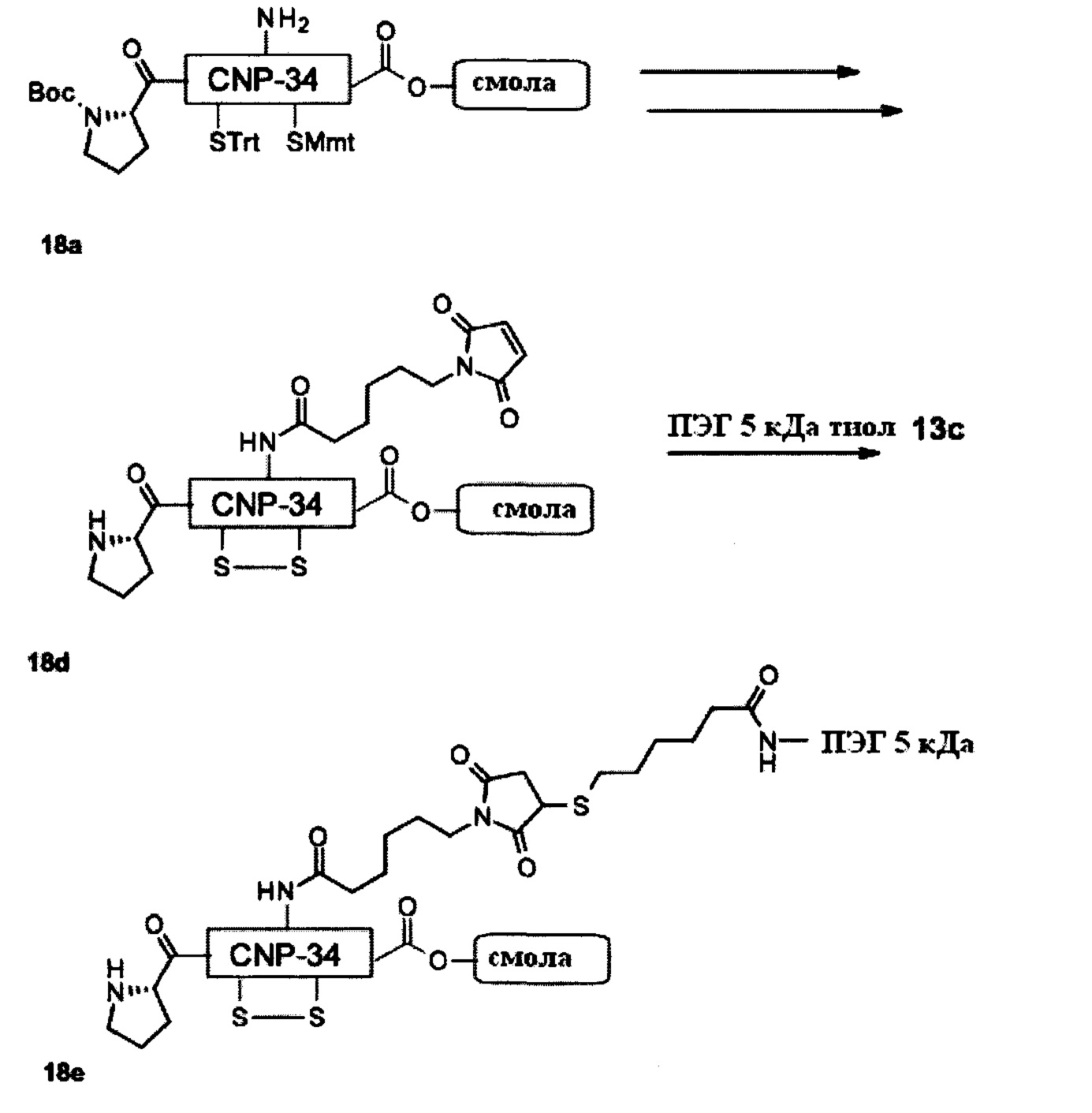
1.07 г (0.11 ммоль) CNP- 34 с защищенной боковой цепью на TCP смоле tentagel, имеющего Вос-защищенный N-конец и ivDde-защищенную боковую цепь Lys12, подвергли удалению защитной группы ivDde согласно методике, описанной в части Вещества и Способы, с получением 18а.
Соединение 18d синтезировали, как описано для 14d, за исключением того, что смола 18а (1.07 г, 0.11 ммоль) применялась в качестве исходного вещества.
Выход: 5.20 мг (1.12 мкмоль, 1.0%) CNP-34-Lys22-Malhx * 8 TFA
MS: m/z 937.26 = [M+4H]4+, (вычисленная моноизотопическая масса для [M+4H]4+ = 937.23).
Конъюгат 18е синтезировали, как описано для 14е, за исключением того, что 18d (5.2 мг, 1.12 мкмоль) применяли в качестве исходного вещества.
Выход: 4.20 мг (0.43 мкмоль, 38%) конъюгата 18е * 8 TFA
Пример 19
Синтез перманентного Lys26 CNP-38 ПЭГ 5 кДа конъюгата 19е
Конъюгат 19е синтезировали согласно следующей схеме:
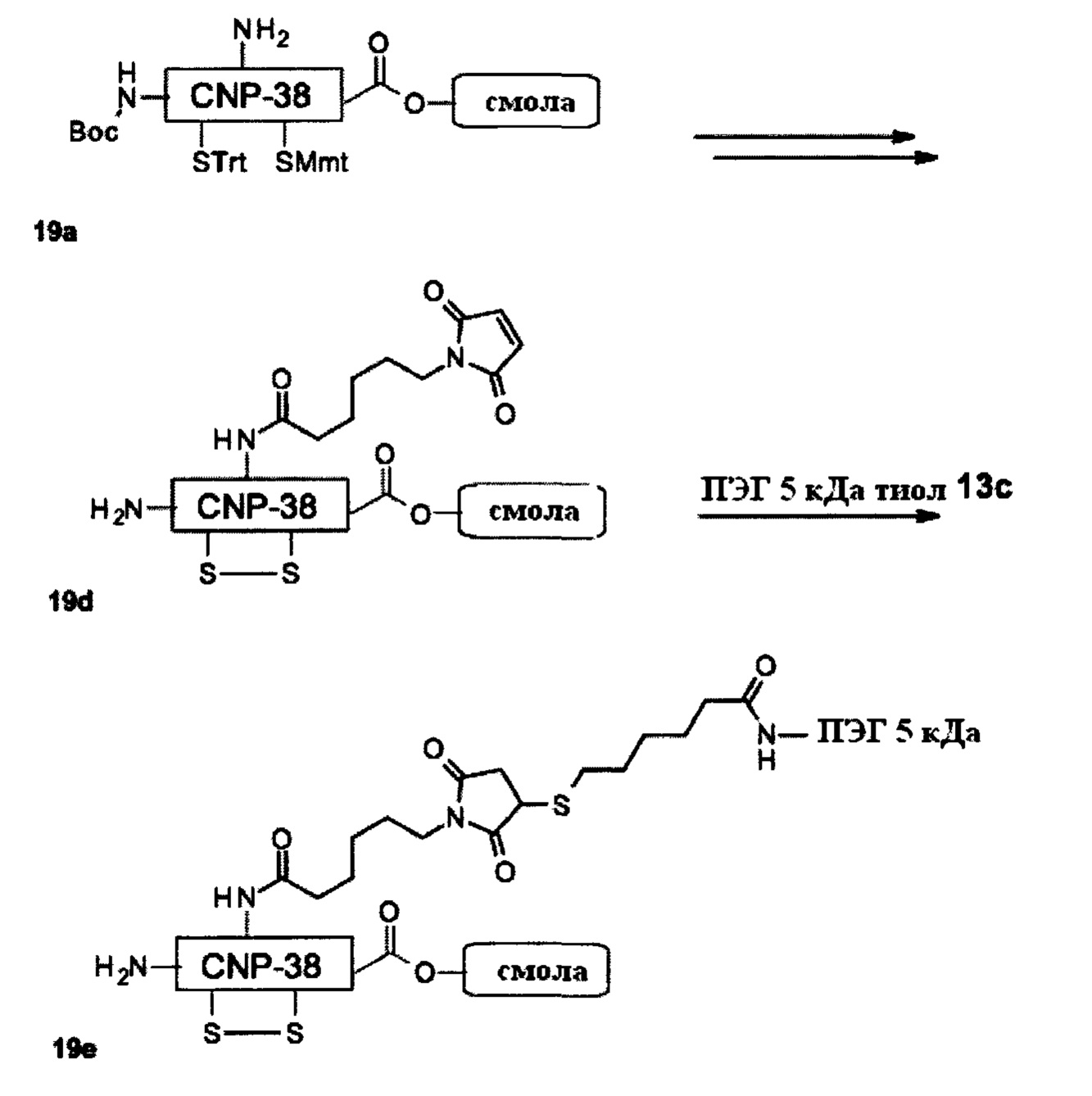
(0.865 г, 0.10 ммоль) CNP-38 с защищенной боковой цепью на TCP смоле tentagel, имеющего Вос-защищенный N-конец и ivDde-защищенную боковую цепь Lys26, подвергли удалению защитной группы ivDde согласно методике, описанной в части Вещества и Способы, с получением 19а.
Соединение 19d синтезировали, как описано для 14d, за исключением того, что смола 19а (0.865 г, 0.10 ммоль) применялась в качестве исходного вещества.
Выход: 10.3 мг (1.95 мкмоль, 2.0%) CNP-38-Lys26-Malhx * 9 TFA
MS: m/z 1064.05 = [M+4H]4+, (вычисленная моноизотопическая масса для [M+4H]4+ = 1064.04).
Конъюгат 19е синтезировали, как описано для 14е, за исключением того, что соединение 19d (4.70 мг, 1.10 мкмоль) применялась в качестве исходного вещества.
Выход: 3.20 мг (0.31 мкмоль, 28%) конъюгата 19е * 9 TFA
Пример 20
Кинетика высвобождения in vitro
CNP конъюгаты 10f и 11i растворили в PBS буфере, содержащем 3 мМ EDTA и 10 мМ метионин, рН 7.4 при концентрации около 1 мг конъюгата/мл. Растворы стерильно отфильтровали и инкубировали при 37°С. Взяли аликвоты во временных точках и проанализировали посредством ОФ-ВЭЖХ и ESI-MS. УФ-сигналы, соответствующие высвобожденному CNP, интегрировали и нанесли на график относительно времени инкубации.
Программное обеспечение для коррекции обрабатываемых кривых применяли для оценки соответствующего периода полувысвобождения.
201
Результаты:
Для конъюгата 10f период полувысвобождения, равный 8.5 д (± 1 д), был получен.
Для конъюгата 11i период полувысвобождения, равный 9.5 д (± 1.5 д), был получен.
Пример 21
Расщепление CNP вариантов нейтральной эндопептидазой In Vitro
Для определения устойчивости in vitro различных вариантов CNP, включая различные длины пептидных цепей и ПЭГилирования с использованием разных сайтов ПЭГирования и молекул ПЭГ, в присутствии нейтральной эндопептидазы (NEP), был проведен анализ NEP расщепления. Этот анализ контролировал расщепление нерасщепленного варианта CNP (нормализованного с помощью внутреннего стандартного PFP) со временем по отношению к to-временной точке.
Более подробно, рекомбинантная человеческая NEP (конечная концентрация 2,5 мкг/мл) и стандартный пентафторфенол (PFP, 40 мкг/мл конечная концентрация) добавили к варианту CNP (100 мкг CNP эквивалентов/мл) в расщепляющем буфере (50 мМ Tris-HCl, РН 7,4, 10 мМ NaCl). Раствор инкубировали при 37°С и 500 оборотах в минуту в течение 4 дней. Образцы брали с разными интервалами времени. Реакцию останавливали комбинированным восстановлением и термической денатурацией, добавляя ТСЕР (трис (2-карбоксиэтил)фосфин; 25 мМ конечная концентрация), и инкубирования смеси при 95°С, 500 оборотах в минуту в течение 5 минут. Полученные продукты реакции определяли с использованием ВЭЖХ-MS. Период полувысвобождения каждого варианта CNP рассчитывался с помощью изменения отношения площадей пиков ВЫЖЭ-UV для CNP и PFP с течением времени. Чтобы компенсировать вариации протеазной активности, в каждом измерении в качестве контроля проводили расщепление CNP-38 или CNP-34.
202
В Таблице 1 перечислены периоды полувысвобождения, на основе in vitro анализа NEP анализа различных вариантов CNP с различной длиной и различными молекулами ПЭГ, присоединенными к различным боковым цепям.
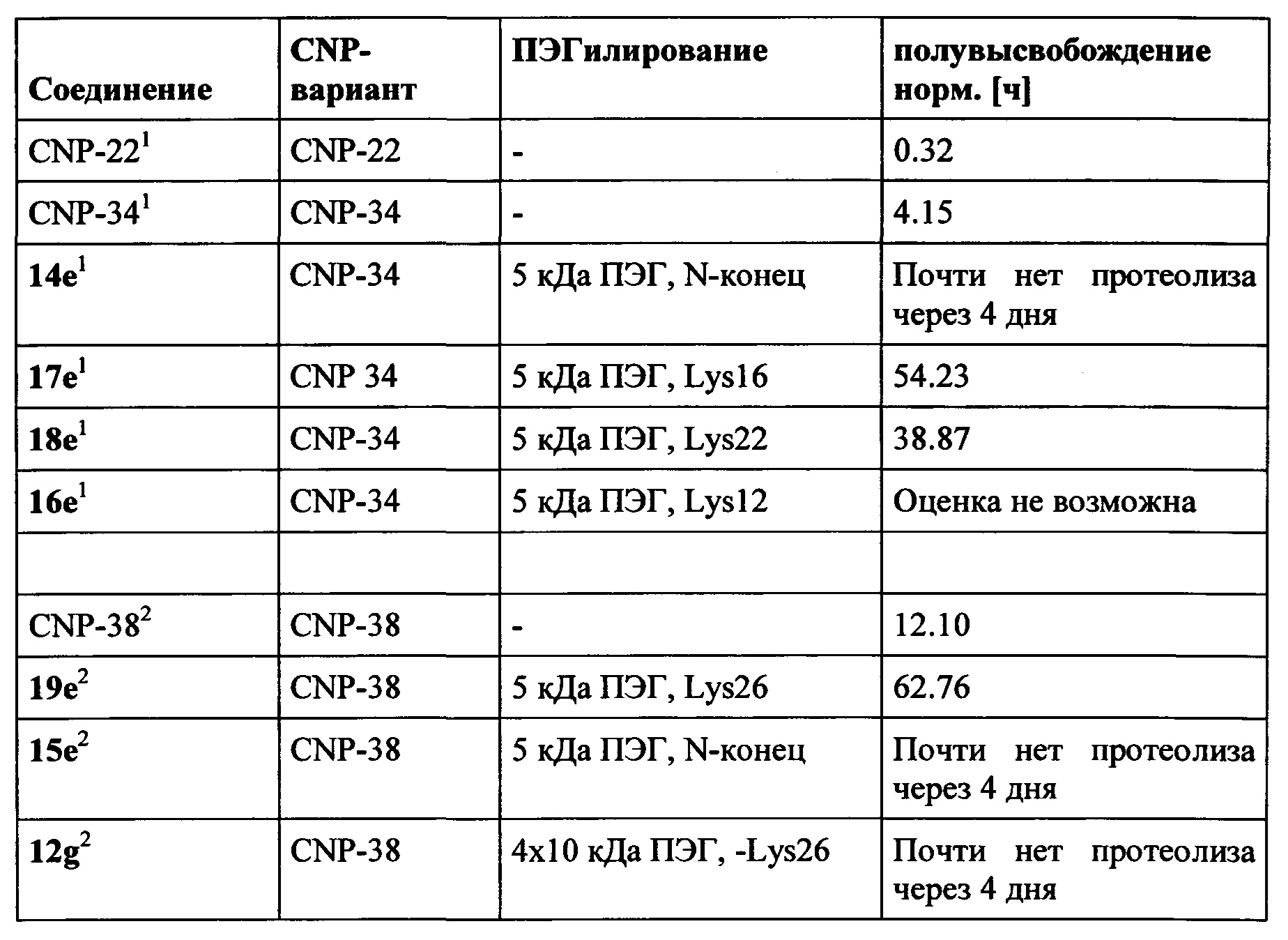
1) Из-за различий в каталитической активности NEP между экспериментами было сформировано среднее значение для всех измерений времени полувысвобождения CNP-34 (4.15 ч), и измерения времени полувысвобождения конъюгатов CNP-34 нормализовали к этому среднему значению с использованием коэффициента для вычисления скорректированного t1/2.
2) Из-за различий в каталитической активности NEP между экспериментами было сформировано среднее значение для всех измерений времени полувысвобождения CNP-38 (12.10h ч), и измерения времени полувысвобождения конъюгатов CNP-38 нормализовали к этому среднему значению с использованием коэффициента для вычисления скорректированного t1/2.
Упорядоченность резистентности по отношению к МЕР следующая: более длинный вариант CNP (CNP-38) является более устойчивым по сравнению с более коротким вариантом CNP (CNP-34), который в свою очередь более устойчив, чем более короткий CNP-22. Порядок сайтов ПЭГ-присоединения следующий: кольцо N-конец > рядом с кольцом > кольцо. Поэтому N-концевое присоединение ПЭГ обеспечивает наивысшую устойчивость к протеолитическому расщеплению NEP для тестируемых конъюгатов. Стабильность CNP-38, ПЭГилированного при Lys26, может быть увеличена с увеличением размера ПЭГ.
Пример 22
Функциональная cGMP стимуляция в NIH-3T3 клетках CNP вариантами
Функциональную активность вариантов CNP определяли в ходе анализа на клетках с клетками NIH-3T3 (линия клеток фибробластов мышиного эмбриона). Эти клетки экспрессируют эндогенно NPR-B на поверхности клетки. Стимуляция NPR-B с помощью CNP приводит к внутриклеточной продукции второго мессенджера cGMP, который детектируется коммерчески доступным анализом cGMP. Клетки NIH-3T3 обычно культивировали в среде DMEM F-12 с 5% FBS и 5 мМ глутамина при 37°С и 5% CO2. Для каждого анализа 50000 клеток ресуспендировали в буфере стимуляции (Dulbecco’s PBS с IBMX) и инкубировали с вариантами CNP в разных концентрациях. CNP (разведения проводили в PBS с 0,2% BSA). После инкубации 30 мин при 37°С и 5% CO2 клетки лизировали, и уровни cGMP определяли с помощью коммерчески доступного теста cGMP TR-FRET (Cisbio, набор cGMP, номер по каталогу 62GM2PEB). ПЭГилированные варианты CNP всегда охарактеризовывали по сравнению с не-ПЭГилированным вариантов в том же эксперименте. Если возможно, оценка остаточной активности проводилась через параметр ЕС50 полученной кривой зависимости ответа от дозы (ограниченная модель с общей кривой).


Сравнивая протестированные сайты присоединения ПЭГ, присоединение при Lys26 (кольцо-лизин) показало наивысшее уменьшение функциональной активности, тогда как N-терминальное присоединение показало относительно высокие значения остаточной функциональной активности. Увеличение размера ПЭГ привело к более хорошему экранированию молекулы CNP и более низкой остаточной функциональной активности.
Пример 23
Исследование роста на FVB мышах через 5 недель обработки CNP-38 посредством ежедневной подкожной болюсной инъекции или путем непрерывной подкожной инфузии
Это исследование проводилось для того, чтобы протестировать эффект ежедневной подкожной болюсной инъекции по сравнению с непрерывной подкожной инфузией CNP-38 на рост животных. 21-22-дневным мышам FVB дикого типа (n=9/группа) давали 50 нмоль/кг/д CNP-38 или среду (30 мМ ацетат, рН 4, содержащий 5% сахарозу и 1% бензиловый спирт), либо посредством ежедневной подкожной болюсной инъекции, либо посредством непрерывной подкожной инфузии в лопаточной области в течение 35 дней. Непрерывная инфузия вводилась посредством модели 1002 для осмотических насосов Alzet в течение недели 1-2, а затем модели 1004 в течение недели 3-5. Концентрации CNP-38 в насосах регулировали относительно среднего веса животных в 7-й день исследования (модель насоса 1002) или на 25-й день исследования (модель насоса 1004). Рост определяли на день 35 путем измерения общей длины тела и рентгеновских измерений правого бедра и голени.
Результаты для животных, которым вводилась ежедневная подкожная болюсная инъекция: на день 35, общая длина тела животных, обработанных CNP-38 составила 110.2%, длина правой бедренной кости составила 105.6%, и длина правого голени составила 104.0% по сравнению с животными, обработанными средой.
Результаты для животных, которым вводилась непрерывная подкожная инфузия: на день 35, общая длина тела животных, обработанных CNP-38 составила 121.7%, длина правой бедренной кости составила 107.5%, и длина правого голени составила 112.2% по сравнению с животными, обработанными средой.
Сделали заключение, что непрерывная подкожная инфузия или композиции с относительно медленным высвобождением CNP-38 (например, медленно высвобождающие CNP-38 пролекарство) являются намного более эффективными, чем ежедневная подкожная болюсная инъекция в отношении вызова роста добавочного и осевого скелета.
Пример 24
Фармакокинетическое исследование перманентного Lys26 CNP-38 ПЭГ4х10 кДа конъюгата 12g на яванских макаках
Это исследование было выполнено для того, чтобы показать пригодность 12g в качестве модельного соединения для медленного высвобождения CNP-38 пролекарства на яванских макаках. Самки яванских макак (2-4 года, 3,5-4,1 кг) получали либо однократное внутривенное (n=3 животных), либо однократное подкожное (n=2 животных) введение 12g при дозе 0,146 мг CNP-38 экв./кг. Образцы крови собирали вплоть до 168 ч после введения дозы и получали плазму. Концентрации CNP-38 в плазме определяли путем количественного определения N-концевого сигнатурного пептида (последовательность LQEHPNAR) и С-концевого сигнатурного пептида (последовательность IGSMSGLGC) после трипсинового расщепления, как описано в части Вещества и Способы.
Результаты: введения доз хорошо переносились без видимых признаков дискомфорта во время введения и после введения. В течение всего исследования в любой момент времени не наблюдалось никаких местных реакций на дозу. После внутривенной инъекции CNP-38 tmax наблюдалось через 15 мин (наиболее ранний проанализированный момент времени), а затем медленный спад содержания CNP-38 с периодом полувысвобождения около 24 ч. После подкожной инъекции концентрация CNP-38 достигла максимума при tmax 48 часов. Через 168 часов концентрация CNP-38 все еще была выше, чем около 50% от cmax. Биодоступность составляла около 50%.
Аналогичные кривые PK получали для N- и С-концевого сигнатурного пептида вплоть до 168 ч после введения дозы, что указывает на присутствие интактного CNP-38 в конъюгате.
Благоприятная длительная фармакокинетика (PK) в течение нескольких дней и стабильность CNP-38 в конъюгате указывают на пригодность перманентного модельного Lys26 CNP-38 ПЭГ 4x10 кДа конъюгата 12g для медленного высвобождения CNP-38 пролекарства после подкожной инъекции. Можно сделать вывод, что подобные конъюгаты, имеющие временного связанный с Lys26 CNP-38 (например, 11i), являются подходящими CNP-38 пролекарствами, обеспечивающими длительные уровни высвобождаемого биоактивного CNP-38 в течение нескольких дней.
Пример 25
Фармакокинетическое исследование временного Lys26 CNP-38 ПЭГ4х10 кДа конъюгата 11i на яванских макаках
Исследование провели, чтобы показать пригодность 11i для медленного высвобождения CNP-38 пролекарства на яванских макаках. Исследование осуществили как описано в примере 24. Уровни в плазме всего содержащегося CNP-38 (конъюгированного и высвобожденного CNP-38) проанализировали, как описано в Примере 24. Чтобы проанализировать содержание в плазме свободного CNP-38, образцы крови подкислили после взятия (например, путем добавления 20 об % 0.5 М цитратно-натриевого буфера рН 4), чтобы остановить дальнейшее высвобождение CNP-38 из конъюгата. Уровни свободного CNP-38 в плазме могут, например, быть определены путем ELISA, применяя CNP антитело, которое связывается ч кольцевой областью CNP, как описано в ссылочных источниках (патент США 8,377,884 В2), или путем LC-MS/MS.
Пример 26
Фармакодинамическое исследование временного Lys26 CNP-38 ПЭГ4х10 кДа конъюгата Hi на яванских макаках
Влияния еженедельной обработки временным Lys26 CNP-38 ПЭГ4х10 кДа конъюгатом 11i на рост костной ткани и уровни биомаркеров, связанных с ростом костной ткани, оцениваются на яванских макаках. Восьми обычным малолетним самцам яванских макак (около 2 лет в начале исследования) делают подкожные инъекции один раз в неделю 16 или 56 нмоль/кг/неделю. Четырем таким макакам подкожно вводят ежедневную дозу 8 нмоль/кг/день CNP-38, в результате чего еженедельно накапливается доза 56 нмоль/кг/неделю. Четырем дополнительным макакам вводят среду в качестве контроля. Общая продолжительность обработки составляет 6 месяцев. Различные измерения расширения пластин роста и роста костной ткани производятся с помощью визуализации посредством цифровой рентгенограммы и магнитного резонанса и путем измерения длины конечностей и тела снаружи. Образцы крови и мочи периодически собираются для определения клинической патологии и измерения. В конце исследования определяется макропатология, и образцы тканей оцениваются гистологически для оценки эффективности и безопасности.
Аббревиатуры:
АСН ахондроплазия
ACN ацетонитрил
АсОН уксусная кислота
BN бензил
Boc трет-бутилоксикарбонил
BSA бычий сывороточный альбумин
cGMP циклический гуанозинмонофосфат
CNP натрийуретический пептид С-типа
COMU (1-циано-2-этокси-2-оксоэтилиденаминоокси)диметиламино-морфолино-карбения гексафторфосфат
конц. концентрированный
д день
DBU 1,3-диазабицикло[5.4.0]ундецен
DCC N,N’-дициклогексилкарбодиимид
DCM дихлорметан
DIC N,N’-диизопропилкарбодиимид
DIEA N,N-диизопропилэтиламин
DIPEA N,N-диизопропилэтиламин
DMAP диметиламино-пиридин
DMEM Модифицированная по способу Дульбекко среда Игла
Dmb 2,4-диметилбензил
DMEM Модифицированная по способу Дульбекко среда Игла
DMF N,N-диметилформамид
DMSO диметилсульфоксид
DTT дитиотреитол
ЕС50 полумаксимальная эффективная концентрация
EDC 1-этил-3-(3-диметиламинопропил)карбодиимид
EDTA этилендиаминтетрауксусная кислота
ELISA фермент-связанное иммуносорбентное исследование
экв стехиометрический эквивалент
ESI-MS масс-спектрометрия с ионизацией электрораспылением
Et этил
EtOAc этилацетат
EtOH этанол
FBS фетальная бычья сыворотка
FGFR3 рецептор фактора роста фибробластов 3
Fmoc 9-флуоренилметилоксикарбонил
ч час
HATU O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилуроний гексафторфосфат
НСН гипохондроплазии
HFIP гексафторизопропанол
HPLC высокоэффективная жидкостная хроматография
HOBt N-гидроксибензотриазол
IBMX 3-изобутил-1-метилксантин
iPrOH 2-пропанол
iv внутривенно
ivDde 4,4-диметил-2,6-диоксоциклогекс-1-илиден)-3-метилбутил
LC жидкостная хроматография
LTQ линейная квадрупольная ловушка
Mal 3-малеимидопропил
Me метил
МеОН метанол
мин минут
Mmt монометокситритил
MS масс-спектр / масс-спектрометрия
MSA метансульфоновая кислота
MW молекулярная масса
m/z отношение массы к заряду
NEP нейтральная эндопептидаза
NHS N-гидроксисукцинимид
NPR рецептор натрийуретического пептида
OtBu трет-бутилокси
PBS фосфатно-буферный солевой раствор
ПЭГ поли(этиленгликоль)
PFP пентафторфенол
рН potentia Hydrogenii
Pr пропил
РуВОР бензотриазол-1-ил-окситрипирролидинофосфония гексафторфосфат
Q-TOF квадрупольный времяпролетный
ОФ-ВЭЖХ обращено-фазовая высокоэффективная жидкостная хроматография
rpm оборотов в минуту
rt комнатная температура
SIM мониторинг избранных ионов
SEC эксклюзионная хроматография размеров
sc подкожная
t1/2 период полувысвобождения
ТСЕР трис(2-карбоксиэтил)фосфин
TCP тритилхлоридполистирол
TD танатофорическая дисплазия
TES триэтилсилан
TFA трифторуксусная кислота
THF тетрагидрофуран
TIPS триизопроилсилан
TMEDA N,N,N',N'-тетраметилэтилендиамин
Tmob 2,4,6-триметоксибензил
TR-FRET перенос энергии флуоресценции с временным разрешением
Trt трифенилметил, тритил
UPLC сверхвысокоэффективная жидкостная хроматография
UV ультрафиолет
vs. по сравнению
ZQ одноквадрупольный.
--->
Перечень последовательностей
<110> Ascendis Pharma A/S
<120> CNP ПРОЛЕКАРСТВА
<130> CPX69555PC
<160> 96
<170> PatentIn version 3.5
<210> 1
<211> 22
<212> PRT
<213> Homo sapiens
<220>
<221> DISULFID
<222> (6)..(22)
<400> 1
Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser
1 5 10 15
Met Ser Gly Leu Gly Cys
20
<210> 2
<211> 53
<212> PRT
<213> Homo sapiens
<220>
<221> DISULFID
<222> (37)..(53)
<400> 2
Asp Leu Arg Val Asp Thr Lys Ser Arg Ala Ala Trp Ala Arg Leu Leu
1 5 10 15
Gln Glu His Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Lys Lys Gly
20 25 30
Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met
35 40 45
Ser Gly Leu Gly Cys
50
<210> 3
<211> 54
<212> PRT
<213> Искусственная последовательность
<220>
<223> G-CNP-53
<220>
<221> DISULFID
<222> (38)..(54)
<400> 3
Gly Asp Leu Arg Val Asp Thr Lys Ser Arg Ala Ala Trp Ala Arg Leu
1 5 10 15
Leu Gln Glu His Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Lys Lys
20 25 30
Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser
35 40 45
Met Ser Gly Leu Gly Cys
50
<210> 4
<211> 54
<212> PRT
<213> Искусственная последовательность
<220>
<223> M-CNP-53
<220>
<221> DISULFID
<222> (38)..(54)
<400> 4
Met Asp Leu Arg Val Asp Thr Lys Ser Arg Ala Ala Trp Ala Arg Leu
1 5 10 15
Leu Gln Glu His Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Lys Lys
20 25 30
Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser
35 40 45
Met Ser Gly Leu Gly Cys
50
<210> 5
<211> 54
<212> PRT
<213> Искусственная последовательность
<220>
<223> P-CNP-53
<220>
<221> DISULFID
<222> (38)..(54)
<400> 5
Pro Asp Leu Arg Val Asp Thr Lys Ser Arg Ala Ala Trp Ala Arg Leu
1 5 10 15
Leu Gln Glu His Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Lys Lys
20 25 30
Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser
35 40 45
Met Ser Gly Leu Gly Cys
50
<210> 6
<211> 53
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-53 M48N
<220>
<221> DISULFID
<222> (37)..(53)
<400> 6
Asp Leu Arg Val Asp Thr Lys Ser Arg Ala Ala Trp Ala Arg Leu Leu
1 5 10 15
Gln Glu His Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Lys Lys Gly
20 25 30
Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Asn
35 40 45
Ser Gly Leu Gly Cys
50
<210> 7
<211> 36
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-53 с делецией аминокислот 15-31
<220>
<221> DISULFID
<222> (20)..(36)
<400> 7
Asp Leu Arg Val Asp Thr Lys Ser Arg Ala Ala Trp Ala Arg Gly Leu
1 5 10 15
Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met Ser
20 25 30
Gly Leu Gly Cys
35
<210> 8
<211> 52
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-52
<220>
<221> DISULFID
<222> (36)..(52)
<400> 8
Leu Arg Val Asp Thr Lys Ser Arg Ala Ala Trp Ala Arg Leu Leu Gln
1 5 10 15
Glu His Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Lys Lys Gly Leu
20 25 30
Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met Ser
35 40 45
Gly Leu Gly Cys
50
<210> 9
<211> 51
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-51
<220>
<221> DISULFID
<222> (35)..(51)
<400> 9
Arg Val Asp Thr Lys Ser Arg Ala Ala Trp Ala Arg Leu Leu Gln Glu
1 5 10 15
His Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Lys Lys Gly Leu Ser
20 25 30
Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met Ser Gly
35 40 45
Leu Gly Cys
50
<210> 10
<211> 50
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-50
<220>
<221> DISULFID
<222> (34)..(50)
<400> 10
Val Asp Thr Lys Ser Arg Ala Ala Trp Ala Arg Leu Leu Gln Glu His
1 5 10 15
Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Lys Lys Gly Leu Ser Lys
20 25 30
Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met Ser Gly Leu
35 40 45
Gly Cys
50
<210> 11
<211> 49
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-49
<220>
<221> DISULFID
<222> (33)..(49)
<400> 11
Asp Thr Lys Ser Arg Ala Ala Trp Ala Arg Leu Leu Gln Glu His Pro
1 5 10 15
Asn Ala Arg Lys Tyr Lys Gly Ala Asn Lys Lys Gly Leu Ser Lys Gly
20 25 30
Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met Ser Gly Leu Gly
35 40 45
Cys
<210> 12
<211> 48
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-48
<220>
<221> DISULFID
<222> (32)..(48)
<400> 12
Thr Lys Ser Arg Ala Ala Trp Ala Arg Leu Leu Gln Glu His Pro Asn
1 5 10 15
Ala Arg Lys Tyr Lys Gly Ala Asn Lys Lys Gly Leu Ser Lys Gly Cys
20 25 30
Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met Ser Gly Leu Gly Cys
35 40 45
<210> 13
<211> 47
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-47
<220>
<221> DISULFID
<222> (31)..(47)
<400> 13
Lys Ser Arg Ala Ala Trp Ala Arg Leu Leu Gln Glu His Pro Asn Ala
1 5 10 15
Arg Lys Tyr Lys Gly Ala Asn Lys Lys Gly Leu Ser Lys Gly Cys Phe
20 25 30
Gly Leu Lys Leu Asp Arg Ile Gly Ser Met Ser Gly Leu Gly Cys
35 40 45
<210> 14
<211> 46
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-46
<220>
<221> DISULFID
<222> (30)..(46)
<400> 14
Ser Arg Ala Ala Trp Ala Arg Leu Leu Gln Glu His Pro Asn Ala Arg
1 5 10 15
Lys Tyr Lys Gly Ala Asn Lys Lys Gly Leu Ser Lys Gly Cys Phe Gly
20 25 30
Leu Lys Leu Asp Arg Ile Gly Ser Met Ser Gly Leu Gly Cys
35 40 45
<210> 15
<211> 45
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-45
<220>
<221> DISULFID
<222> (29)..(45)
<400> 15
Arg Ala Ala Trp Ala Arg Leu Leu Gln Glu His Pro Asn Ala Arg Lys
1 5 10 15
Tyr Lys Gly Ala Asn Lys Lys Gly Leu Ser Lys Gly Cys Phe Gly Leu
20 25 30
Lys Leu Asp Arg Ile Gly Ser Met Ser Gly Leu Gly Cys
35 40 45
<210> 16
<211> 44
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-44
<220>
<221> DISULFID
<222> (28)..(44)
<400> 16
Ala Ala Trp Ala Arg Leu Leu Gln Glu His Pro Asn Ala Arg Lys Tyr
1 5 10 15
Lys Gly Ala Asn Lys Lys Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys
20 25 30
Leu Asp Arg Ile Gly Ser Met Ser Gly Leu Gly Cys
35 40
<210> 17
<211> 35
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-44 с делецией аминокислот 14-22
<220>
<221> DISULFID
<222> (19)..(35)
<400> 17
Ala Ala Trp Ala Arg Leu Leu Gln Glu His Pro Asn Ala Gly Leu Ser
1 5 10 15
Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met Ser Gly
20 25 30
Leu Gly Cys
35
<210> 18
<211> 36
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-44 с делецией аминокислот 15-22
<220>
<221> DISULFID
<222> (20)..(36)
<400> 18
Ala Ala Trp Ala Arg Leu Leu Gln Glu His Pro Asn Ala Arg Gly Leu
1 5 10 15
Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met Ser
20 25 30
Gly Leu Gly Cys
35
<210> 19
<211> 43
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-43
<220>
<221> DISULFID
<222> (27)..(43)
<400> 19
Ala Trp Ala Arg Leu Leu Gln Glu His Pro Asn Ala Arg Lys Tyr Lys
1 5 10 15
Gly Ala Asn Lys Lys Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu
20 25 30
Asp Arg Ile Gly Ser Met Ser Gly Leu Gly Cys
35 40
<210> 20
<211> 42
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-42
<220>
<221> DISULFID
<222> (26)..(42)
<400> 20
Trp Ala Arg Leu Leu Gln Glu His Pro Asn Ala Arg Lys Tyr Lys Gly
1 5 10 15
Ala Asn Lys Lys Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp
20 25 30
Arg Ile Gly Ser Met Ser Gly Leu Gly Cys
35 40
<210> 21
<211> 41
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-41
<220>
<221> DISULFID
<222> (25)..(41)
<400> 21
Ala Arg Leu Leu Gln Glu His Pro Asn Ala Arg Lys Tyr Lys Gly Ala
1 5 10 15
Asn Lys Lys Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg
20 25 30
Ile Gly Ser Met Ser Gly Leu Gly Cys
35 40
<210> 22
<211> 40
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-40
<220>
<221> DISULFID
<222> (24)..(40)
<400> 22
Arg Leu Leu Gln Glu His Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn
1 5 10 15
Lys Lys Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile
20 25 30
Gly Ser Met Ser Gly Leu Gly Cys
35 40
<210> 23
<211> 39
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-39
<220>
<221> DISULFID
<222> (23)..(39)
<400> 23
Leu Leu Gln Glu His Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Lys
1 5 10 15
Lys Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly
20 25 30
Ser Met Ser Gly Leu Gly Cys
35
<210> 24
<211> 38
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-38
<220>
<221> DISULFID
<222> (22)..(38)
<400> 24
Leu Gln Glu His Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Lys Lys
1 5 10 15
Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser
20 25 30
Met Ser Gly Leu Gly Cys
35
<210> 25
<211> 37
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-37
<220>
<221> DISULFID
<222> (21)..(37)
<400> 25
Gln Glu His Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Lys Lys Gly
1 5 10 15
Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met
20 25 30
Ser Gly Leu Gly Cys
35
<210> 26
<211> 37
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-37 cQ1pQ (pQ = пироглутамат)
<220>
<221> MISC_признак
<222> (1)..(1)
<223> X = пироглутамат
<220>
<221> DISULFID
<222> (21)..(37)
<400> 26
Xaa Glu His Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Lys Lys Gly
1 5 10 15
Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met
20 25 30
Ser Gly Leu Gly Cys
35
<210> 27
<211> 38
<212> PRT
<213> Искусственная последовательность
<220>
<223> G-CNP-37
<220>
<221> DISULFID
<222> (22)..(38)
<400> 27
Gly Gln Glu His Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Lys Lys
1 5 10 15
Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser
20 25 30
Met Ser Gly Leu Gly Cys
35
<210> 28
<211> 38
<212> PRT
<213> Искусственная последовательность
<220>
<223> P-CNP-37
<220>
<221> DISULFID
<222> (22)..(38)
<400> 28
Pro Gln Glu His Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Lys Lys
1 5 10 15
Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser
20 25 30
Met Ser Gly Leu Gly Cys
35
<210> 29
<211> 38
<212> PRT
<213> Искусственная последовательность
<220>
<223> M-CNP-37
<220>
<221> DISULFID
<222> (22)..(38)
<400> 29
Met Gln Glu His Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Lys Lys
1 5 10 15
Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser
20 25 30
Met Ser Gly Leu Gly Cys
35
<210> 30
<211> 39
<212> PRT
<213> Искусственная последовательность
<220>
<223> PG-CNP-37
<220>
<221> DISULFID
<222> (23)..(39)
<400> 30
Pro Gly Gln Glu His Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Lys
1 5 10 15
Lys Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly
20 25 30
Ser Met Ser Gly Leu Gly Cys
35
<210> 31
<211> 39
<212> PRT
<213> Искусственная последовательность
<220>
<223> MG-CNP-37
<220>
<221> DISULFID
<222> (23)..(39)
<400> 31
Met Gly Gln Glu His Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Lys
1 5 10 15
Lys Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly
20 25 30
Ser Met Ser Gly Leu Gly Cys
35
<210> 32
<211> 37
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-37 M32N
<220>
<221> DISULFID
<222> (21)..(37)
<400> 32
Gln Glu His Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Lys Lys Gly
1 5 10 15
Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Asn
20 25 30
Ser Gly Leu Gly Cys
35
<210> 33
<211> 38
<212> PRT
<213> Искусственная последовательность
<220>
<223> G-CNP-37 M32N
<220>
<221> DISULFID
<222> (22)..(38)
<400> 33
Gly Gln Glu His Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Lys Lys
1 5 10 15
Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser
20 25 30
Asn Ser Gly Leu Gly Cys
35
<210> 34
<211> 38
<212> PRT
<213> Искусственная последовательность
<220>
<223> G-CNP-37 K14Q
<220>
<221> DISULFID
<222> (22)..(38)
<400> 34
Gly Gln Glu His Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Gln Lys
1 5 10 15
Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser
20 25 30
Met Ser Gly Leu Gly Cys
35
<210> 35
<211> 38
<212> PRT
<213> Искусственная последовательность
<220>
<223> G-CNP-37 K14P
<220>
<221> DISULFID
<222> (22)..(38)
<400> 35
Gly Gln Glu His Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Pro Lys
1 5 10 15
Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser
20 25 30
Met Ser Gly Leu Gly Cys
35
<210> 36
<211> 37
<212> PRT
<213> Искусственная последовательность
<220>
<223> G-CNP-37 K14Q, делеция аминокислоты 15
<220>
<221> DISULFID
<222> (21)..(37)
<400> 36
Gly Gln Glu His Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Gln Gly
1 5 10 15
Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met
20 25 30
Ser Gly Leu Gly Cys
35
<210> 37
<211> 38
<212> PRT
<213> Искусственная последовательность
<220>
<223> G-CNP-37 K14Q, K15Q
<220>
<221> DISULFID
<222> (22)..(38)
<400> 37
Gly Gln Glu His Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Gln Gln
1 5 10 15
Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser
20 25 30
Met Ser Gly Leu Gly Cys
35
<210> 38
<211> 36
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-36
<220>
<221> DISULFID
<222> (20)..(36)
<400> 38
Glu His Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Lys Lys Gly Leu
1 5 10 15
Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met Ser
20 25 30
Gly Leu Gly Cys
35
<210> 39
<211> 35
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-35
<220>
<221> DISULFID
<222> (19)..(35)
<400> 39
His Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Lys Lys Gly Leu Ser
1 5 10 15
Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met Ser Gly
20 25 30
Leu Gly Cys
35
<210> 40
<211> 34
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-34
<220>
<221> DISULFID
<222> (18)..(34)
<400> 40
Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Lys Lys Gly Leu Ser Lys
1 5 10 15
Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met Ser Gly Leu
20 25 30
Gly Cys
<210> 41
<211> 33
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-33
<220>
<221> DISULFID
<222> (17)..(33)
<400> 41
Asn Ala Arg Lys Tyr Lys Gly Ala Asn Lys Lys Gly Leu Ser Lys Gly
1 5 10 15
Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met Ser Gly Leu Gly
20 25 30
Cys
<210> 42
<211> 32
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-32
<220>
<221> DISULFID
<222> (16)..(32)
<400> 42
Ala Arg Lys Tyr Lys Gly Ala Asn Lys Lys Gly Leu Ser Lys Gly Cys
1 5 10 15
Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met Ser Gly Leu Gly Cys
20 25 30
<210> 43
<211> 31
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-31
<220>
<221> DISULFID
<222> (15)..(31)
<400> 43
Arg Lys Tyr Lys Gly Ala Asn Lys Lys Gly Leu Ser Lys Gly Cys Phe
1 5 10 15
Gly Leu Lys Leu Asp Arg Ile Gly Ser Met Ser Gly Leu Gly Cys
20 25 30
<210> 44
<211> 30
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-30
<220>
<221> DISULFID
<222> (14)..(30)
<400> 44
Lys Tyr Lys Gly Ala Asn Lys Lys Gly Leu Ser Lys Gly Cys Phe Gly
1 5 10 15
Leu Lys Leu Asp Arg Ile Gly Ser Met Ser Gly Leu Gly Cys
20 25 30
<210> 45
<211> 29
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-29
<220>
<221> DISULFID
<222> (13)..(29)
<400> 45
Tyr Lys Gly Ala Asn Lys Lys Gly Leu Ser Lys Gly Cys Phe Gly Leu
1 5 10 15
Lys Leu Asp Arg Ile Gly Ser Met Ser Gly Leu Gly Cys
20 25
<210> 46
<211> 28
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-28
<220>
<221> DISULFID
<222> (12)..(28)
<400> 46
Lys Gly Ala Asn Lys Lys Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys
1 5 10 15
Leu Asp Arg Ile Gly Ser Met Ser Gly Leu Gly Cys
20 25
<210> 47
<211> 38
<212> PRT
<213> Искусственная последовательность
<220>
<223> GHKSEVAHRF-CNP-28
<220>
<221> DISULFID
<222> (22)..(38)
<400> 47
Gly His Lys Ser Glu Val Ala His Arg Phe Lys Gly Ala Asn Lys Lys
1 5 10 15
Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser
20 25 30
Met Ser Gly Leu Gly Cys
35
<210> 48
<211> 27
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-27
<220>
<221> DISULFID
<222> (11)..(27)
<400> 48
Gly Ala Asn Lys Lys Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu
1 5 10 15
Asp Arg Ile Gly Ser Met Ser Gly Leu Gly Cys
20 25
<210> 49
<211> 27
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-27 K4Q, K5Q
<220>
<221> DISULFID
<222> (11)..(27)
<400> 49
Gly Ala Asn Gln Gln Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu
1 5 10 15
Asp Arg Ile Gly Ser Met Ser Gly Leu Gly Cys
20 25
<210> 50
<211> 27
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-27 K4R, K5R
<220>
<221> DISULFID
<222> (11)..(27)
<400> 50
Gly Ala Asn Arg Arg Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu
1 5 10 15
Asp Arg Ile Gly Ser Met Ser Gly Leu Gly Cys
20 25
<210> 51
<211> 27
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-27 K4P, K5R
<220>
<221> DISULFID
<222> (11)..(27)
<400> 51
Gly Ala Asn Pro Arg Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu
1 5 10 15
Asp Arg Ile Gly Ser Met Ser Gly Leu Gly Cys
20 25
<210> 52
<211> 27
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-27 K4S, K5S
<220>
<221> DISULFID
<222> (11)..(27)
<400> 52
Gly Ala Asn Ser Ser Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu
1 5 10 15
Asp Arg Ile Gly Ser Met Ser Gly Leu Gly Cys
20 25
<210> 53
<211> 30
<212> PRT
<213> Искусственная последовательность
<220>
<223> GAN-CNP-27 K4P, K5R
<220>
<221> DISULFID
<222> (14)..(30)
<400> 53
Gly Ala Asn Gly Ala Asn Pro Arg Gly Leu Ser Arg Gly Cys Phe Gly
1 5 10 15
Leu Lys Leu Asp Arg Ile Gly Ser Met Ser Gly Leu Gly Cys
20 25 30
<210> 54
<211> 27
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-27 K4R, K5R, K9R
<220>
<221> DISULFID
<222> (11)..(27)
<400> 54
Gly Ala Asn Arg Arg Gly Leu Ser Arg Gly Cys Phe Gly Leu Lys Leu
1 5 10 15
Asp Arg Ile Gly Ser Met Ser Gly Leu Gly Cys
20 25
<210> 55
<211> 27
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-27 K4R, K5R, K9R, M22N
<220>
<221> DISULFID
<222> (11)..(27)
<400> 55
Gly Ala Asn Arg Arg Gly Leu Ser Arg Gly Cys Phe Gly Leu Lys Leu
1 5 10 15
Asp Arg Ile Gly Ser Asn Ser Gly Leu Gly Cys
20 25
<210> 56
<211> 28
<212> PRT
<213> Искусственная последовательность
<220>
<223> P-CNP-27 K4R, K5R, K9R
<220>
<221> DISULFID
<222> (12)..(28)
<400> 56
Pro Gly Ala Asn Arg Arg Gly Leu Ser Arg Gly Cys Phe Gly Leu Lys
1 5 10 15
Leu Asp Arg Ile Gly Ser Met Ser Gly Leu Gly Cys
20 25
<210> 57
<211> 28
<212> PRT
<213> Искусственная последовательность
<220>
<223> M-CNP-27 K4R, K5R, K9R
<220>
<221> DISULFID
<222> (12)..(28)
<400> 57
Met Gly Ala Asn Arg Arg Gly Leu Ser Arg Gly Cys Phe Gly Leu Lys
1 5 10 15
Leu Asp Arg Ile Gly Ser Met Ser Gly Leu Gly Cys
20 25
<210> 58
<211> 38
<212> PRT
<213> Искусственная последовательность
<220>
<223> Фрагмент человеческого сывороточного альбумина - CNP-27
<220>
<221> DISULFID
<222> (22)..(38)
<400> 58
Gly His Lys Ser Glu Val Ala His Arg Phe Lys Gly Ala Asn Lys Lys
1 5 10 15
Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser
20 25 30
Met Ser Gly Leu Gly Cys
35
<210> 59
<211> 38
<212> PRT
<213> Искусственная последовательность
<220>
<223> Фрагмент человеческого сывороточного альбумина - CNP-27 M22N
<220>
<221> DISULFID
<222> (22)..(38)
<400> 59
Gly His Lys Ser Glu Val Ala His Arg Phe Lys Gly Ala Asn Lys Lys
1 5 10 15
Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser
20 25 30
Asn Ser Gly Leu Gly Cys
35
<210> 60
<211> 39
<212> PRT
<213> Искусственная последовательность
<220>
<223> метионин- Фрагмент человеческого сывороточного альбумина - CNP-27
<220>
<221> DISULFID
<222> (23)..(39)
<400> 60
Met Gly His Lys Ser Glu Val Ala His Arg Phe Lys Gly Ala Asn Lys
1 5 10 15
Lys Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly
20 25 30
Ser Met Ser Gly Leu Gly Cys
35
<210> 61
<211> 39
<212> PRT
<213> Искусственная последовательность
<220>
<223> пролин- Фрагмент человеческого сывороточного альбумина - CNP-27
<220>
<221> DISULFID
<222> (23)..(39)
<400> 61
Pro Gly His Lys Ser Glu Val Ala His Arg Phe Lys Gly Ala Asn Lys
1 5 10 15
Lys Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly
20 25 30
Ser Met Ser Gly Leu Gly Cys
35
<210> 62
<211> 26
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-26
<220>
<221> DISULFID
<222> (10)..(26)
<400> 62
Ala Asn Lys Lys Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp
1 5 10 15
Arg Ile Gly Ser Met Ser Gly Leu Gly Cys
20 25
<210> 63
<211> 25
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-25
<220>
<221> DISULFID
<222> (9)..(25)
<400> 63
Asn Lys Lys Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg
1 5 10 15
Ile Gly Ser Met Ser Gly Leu Gly Cys
20 25
<210> 64
<211> 24
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-24
<220>
<221> DISULFID
<222> (8)..(24)
<400> 64
Lys Lys Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile
1 5 10 15
Gly Ser Met Ser Gly Leu Gly Cys
20
<210> 65
<211> 23
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-23
<220>
<221> DISULFID
<222> (7)..(23)
<400> 65
Lys Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly
1 5 10 15
Ser Met Ser Gly Leu Gly Cys
20
<210> 66
<211> 23
<212> PRT
<213> Искусственная последовательность
<220>
<223> R-CNP-22
<220>
<221> DISULFID
<222> (7)..(23)
<400> 66
Arg Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly
1 5 10 15
Ser Met Ser Gly Leu Gly Cys
20
<210> 67
<211> 24
<212> PRT
<213> Искусственная последовательность
<220>
<223> ER-CNP-22
<220>
<221> DISULFID
<222> (8)..(24)
<400> 67
Glu Arg Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile
1 5 10 15
Gly Ser Met Ser Gly Leu Gly Cys
20
<210> 68
<211> 23
<212> PRT
<213> Искусственная последовательность
<220>
<223> R-CNP-22 K4R
<220>
<221> DISULFID
<222> (7)..(23)
<400> 68
Arg Gly Leu Ser Arg Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly
1 5 10 15
Ser Met Ser Gly Leu Gly Cys
20
<210> 69
<211> 24
<212> PRT
<213> Искусственная последовательность
<220>
<223> ER-CNP-22 4KR
<220>
<221> DISULFID
<222> (8)..(24)
<400> 69
Glu Arg Gly Leu Ser Arg Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile
1 5 10 15
Gly Ser Met Ser Gly Leu Gly Cys
20
<210> 70
<211> 24
<212> PRT
<213> Искусственная последовательность
<220>
<223> RR-CNP-22
<220>
<221> DISULFID
<222> (8)..(24)
<400> 70
Arg Arg Gly Leu Ser Arg Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile
1 5 10 15
Gly Ser Met Ser Gly Leu Gly Cys
20
<210> 71
<211> 37
<212> PRT
<213> Искусственная последовательность
<220>
<223> HRGP фрагмент- CNP-22
<220>
<221> DISULFID
<222> (21)..(37)
<400> 71
Gly His His Ser His Glu Gln His Pro His Gly Ala Asn Gln Gln Gly
1 5 10 15
Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met
20 25 30
Ser Gly Leu Gly Cys
35
<210> 72
<211> 38
<212> PRT
<213> Искусственная последовательность
<220>
<223> HRGP фрагмент - CNP-22
<220>
<221> DISULFID
<222> (22)..(38)
<400> 72
Gly Ala His His Pro His Glu His Asp Thr His Gly Ala Asn Gln Gln
1 5 10 15
Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser
20 25 30
Met Ser Gly Leu Gly Cys
35
<210> 73
<211> 37
<212> PRT
<213> Искусственная последовательность
<220>
<223> HRGP фрагмент- CNP-22
<220>
<221> DISULFID
<222> (21)..(37)
<400> 73
Gly His His Ser His Glu Gln His Pro His Gly Ala Asn Pro Arg Gly
1 5 10 15
Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met
20 25 30
Ser Gly Leu Gly Cys
35
<210> 74
<211> 36
<212> PRT
<213> Искусственная последовательность
<220>
<223> IgG1(FC) фрагмент - CNP-22
<220>
<221> DISULFID
<222> (20)..(36)
<400> 74
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gly Leu
1 5 10 15
Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met Ser
20 25 30
Gly Leu Gly Cys
35
<210> 75
<211> 39
<212> PRT
<213> Искусственная последовательность
<220>
<223> человеческий сывороточный альбумин - CNP-22
<220>
<221> DISULFID
<222> (23)..(39)
<400> 75
Gly Gln His Lys Asp Asp Asn Pro Asn Leu Pro Arg Gly Ala Asn Pro
1 5 10 15
Arg Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly
20 25 30
Ser Met Ser Gly Leu Gly Cys
35
<210> 76
<211> 37
<212> PRT
<213> Искусственная последовательность
<220>
<223> человеческий сывороточный альбумин - CNP-22
<220>
<221> DISULFID
<222> (21)..(37)
<400> 76
Gly Glu Arg Ala Phe Lys Ala Trp Ala Val Ala Arg Leu Ser Gln Gly
1 5 10 15
Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met
20 25 30
Ser Gly Leu Gly Cys
35
<210> 77
<211> 35
<212> PRT
<213> Искусственная последовательность
<220>
<223> остеокрин NPR C фрагмент ингибитора - CNP-22
<220>
<221> DISULFID
<222> (19)..(35)
<400> 77
Phe Gly Ile Pro Met Asp Arg Ile Gly Arg Asn Pro Arg Gly Leu Ser
1 5 10 15
Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met Ser Gly
20 25 30
Leu Gly Cys
35
<210> 78
<211> 40
<212> PRT
<213> Искусственная последовательность
<220>
<223> FGF2 гепарин-связывающий домен фрагмент - CNP-22
<220>
<221> DISULFID
<222> (24)..(40)
<400> 78
Gly Lys Arg Thr Gly Gln Tyr Lys Leu Gly Ser Lys Thr Gly Pro Gly
1 5 10 15
Pro Lys Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile
20 25 30
Gly Ser Met Ser Gly Leu Gly Cys
35 40
<210> 79
<211> 37
<212> PRT
<213> Искусственная последовательность
<220>
<223> IgG1(FC) фрагмент- CNP-22 K4R
<220>
<221> DISULFID
<222> (21)..(37)
<400> 79
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Gly Ala Asn Gln Gln Gly
1 5 10 15
Leu Ser Arg Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met
20 25 30
Ser Gly Leu Gly Cys
35
<210> 80
<211> 36
<212> PRT
<213> Искусственная последовательность
<220>
<223> фрагмент человеческого сывороточного альбумина - CNP-22 K4R
<220>
<221> DISULFID
<222> (20)..(36)
<400> 80
Gly Val Pro Gln Val Ser Thr Ser Thr Gly Ala Asn Gln Gln Gly Leu
1 5 10 15
Ser Arg Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met Ser
20 25 30
Gly Leu Gly Cys
35
<210> 81
<211> 37
<212> PRT
<213> Искусственная последовательность
<220>
<223> фибронектиновый фрагмент - CNP-22
<220>
<221> DISULFID
<222> (21)..(37)
<400> 81
Gly Gln Pro Ser Ser Ser Ser Gln Ser Thr Gly Ala Asn Gln Gln Gly
1 5 10 15
Leu Ser Arg Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met
20 25 30
Ser Gly Leu Gly Cys
35
<210> 82
<211> 37
<212> PRT
<213> Искусственная последовательность
<220>
<223> фибронектиновый фрагмент - CNP-22 K4R
<220>
<221> DISULFID
<222> (21)..(37)
<400> 82
Gly Gln Thr His Ser Ser Gly Thr Gln Ser Gly Ala Asn Gln Gln Gly
1 5 10 15
Leu Ser Arg Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met
20 25 30
Ser Gly Leu Gly Cys
35
<210> 83
<211> 37
<212> PRT
<213> Искусственная последовательность
<220>
<223> фибронектиновый фрагмент - CNP-22 K4R
<220>
<221> DISULFID
<222> (21)..(37)
<400> 83
Gly Ser Thr Gly Gln Trp His Ser Glu Ser Gly Ala Asn Gln Gln Gly
1 5 10 15
Leu Ser Arg Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met
20 25 30
Ser Gly Leu Gly Cys
35
<210> 84
<211> 37
<212> PRT
<213> Искусственная последовательность
<220>
<223> фрагмент цинкового пальца - CNP-22 K4R
<220>
<221> DISULFID
<222> (21)..(37)
<400> 84
Gly Ser Ser Ser Ser Ser Ser Ser Ser Ser Gly Ala Asn Gln Gln Gly
1 5 10 15
Leu Ser Arg Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met
20 25 30
Ser Gly Leu Gly Cys
35
<210> 85
<211> 21
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-21
<220>
<221> DISULFID
<222> (5)..(21)
<400> 85
Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met
1 5 10 15
Ser Gly Leu Gly Cys
20
<210> 86
<211> 20
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-20
<220>
<221> DISULFID
<222> (4)..(20)
<400> 86
Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met Ser
1 5 10 15
Gly Leu Gly Cys
20
<210> 87
<211> 19
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-19
<220>
<221> DISULFID
<222> (3)..(19)
<400> 87
Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met Ser Gly
1 5 10 15
Leu Gly Cys
<210> 88
<211> 18
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-18
<220>
<221> DISULFID
<222> (2)..(18)
<400> 88
Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met Ser Gly Leu
1 5 10 15
Gly Cys
<210> 89
<211> 17
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-17
<220>
<221> DISULFID
<222> (1)..(17)
<400> 89
Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met Ser Gly Leu Gly
1 5 10 15
Cys
<210> 90
<211> 32
<212> PRT
<213> Искусственная последовательность
<220>
<223> BNP фрагмент- CNP-17 - BNP- фрагмент
<220>
<221> DISULFID
<222> (10)..(26)
<400> 90
Ser Pro Lys Met Val Gln Gly Ser Gly Cys Phe Gly Leu Lys Leu Asp
1 5 10 15
Arg Ile Gly Ser Met Ser Gly Leu Gly Cys Lys Val Leu Arg Arg His
20 25 30
<210> 91
<211> 38
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-38 L1G
<220>
<221> DISULFID
<222> (22)..(38)
<400> 91
Gly Gln Glu His Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Lys Lys
1 5 10 15
Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser
20 25 30
Met Ser Gly Leu Gly Cys
35
<210> 92
<211> 37
<212> PRT
<213> Искусственная последовательность
<220>
<223> Ac-CNP-37
<220>
<221> MOD_RES
<222> (1)..(1)
<223> ацетилирование
<220>
<221> DISULFID
<222> (21)..(37)
<400> 92
Gln Glu His Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Lys Lys Gly
1 5 10 15
Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met
20 25 30
Ser Gly Leu Gly Cys
35
<210> 93
<211> 37
<212> PRT
<213> Искусственная последовательность
<220>
<223> CNP-37, Xaa = K или R, при условии, что по меньшей мере один Xaa представляет собой R
<220>
<221> MISC_признак
<222> (8)..(8)
<223> Xaa = Lys, Arg, Pro, Ser или Gln, при условии, что по меньшей мере одну из аминокислот 8, 10, 14, 15, 19 или 25 выбирают
из группы, состоящей из Arg, Pro, Ser и Gln
<220>
<221> MISC_признак
<222> (10)..(10)
<223> Xaa = Lys, Arg, Pro, Ser или Gln, при условии, что по меньшей мере одну из аминокислот 8, 10, 14, 15, 19 или 25
выбирают из группы, состоящей из Arg, Pro, Ser и Gln
<220>
<221> MISC_признак
<222> (14)..(14)
<223> Xaa = Lys, Arg, Pro, Ser или Gln, при условии, что по меньшей мере одну из аминокислот 8, 10, 14, 15, 19 или 25
выбирают из группы, состоящей из Arg, Pro, Ser и Gln
<220>
<221> MISC_признак
<222> (15)..(15)
<223> Xaa = Lys, Arg, Pro, Ser или Gln, при условии, что по меньшей мере одну из аминокислот 8, 10, 14, 15, 19 или 25
выбирают из группы, состоящей из Arg, Pro, Ser и Gln
<220>
<221> MISC_признак
<222> (19)..(19)
<223> Xaa = Lys, Arg, Pro, Ser или Gln, при условии, что по меньшей мере одну из аминокислот 8, 10, 14, 15, 19 или 25
выбирают из группы, состоящей из Arg, Pro, Ser и Gln
<220>
<221> DISULFID
<222> (21)..(37)
<220>
<221> MISC_признак
<222> (25)..(25)
<223> Xaa = Lys, Arg, Pro, Ser или Gln, при условии, что по меньшей мере одну из аминокислот 8, 10, 14, 15, 19 или 25
выбирают из группы, состоящей из Arg, Pro, Ser и Gln
<400> 93
Gln Glu His Pro Asn Ala Arg Xaa Tyr Xaa Gly Ala Asn Xaa Xaa Gly
1 5 10 15
Leu Ser Xaa Gly Cys Phe Gly Leu Xaa Leu Asp Arg Ile Gly Ser Met
20 25 30
Ser Gly Leu Gly Cys
35
<210> 94
<211> 37
<212> PRT
<213> Искусственная последовательность
<220>
<223> мутированный CNP-37
<220>
<221> MISC_признак
<222> (14)..(14)
<223> X выбирают из группы, состоящей из Lys, Arg, Pro, Ser и
Gln, при условии, что по меньшей мере одну из аминокислот в положении 14, 15, 19 и 25
выбирают из группы, состоящей из Arg, Pro, Ser и Gln
<220>
<221> MISC_признак
<222> (15)..(15)
<223> X выбирают из группы, состоящей из Lys, Arg, Pro, Ser и
Gln, при условии, что по меньшей мере одну из аминокислот в положении
14, 15, 19 и 25 выбирают из группы, состоящей из Arg, Pro, Ser и Gln
<220>
<221> MISC_признак
<222> (19)..(19)
<223> X выбирают из группы, состоящей из Lys, Arg, Pro, Ser и
Gln, при условии, что по меньшей мере одну из аминокислот в положении
14, 15, 19 and 25 выбирают из группы, состоящей из Arg, Pro, Ser и Gln
<220>
<221> DISULFID
<222> (21)..(37)
<220>
<221> MISC_признак
<222> (25)..(25)
<223> X выбирают из группы, состоящей из Lys, Arg, Pro, Ser и
Gln, при условии, что по меньшей мере одну из аминокислот в положении 14, 15, 19 и 25
выбирают из группы, состоящей из Arg, Pro, Ser и Gln
<400> 94
Gln Glu His Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Xaa Xaa Gly
1 5 10 15
Leu Ser Xaa Gly Cys Phe Gly Leu Xaa Leu Asp Arg Ile Gly Ser Met
20 25 30
Ser Gly Leu Gly Cys
35
<210> 95
<211> 37
<212> PRT
<213> Искусственная последовательность
<220>
<223> мутированный CNP-37
<220>
<221> MISC_признак
<222> (14)..(15)
<223> Xaa Xaa выбирают из группы, состоящей из Lys Arg, Arg
Lys, Lys Pro, Pro Lys, Ser Ser, Arg Ser, Ser Arg, Gln Lys, Gln
Arg, Lys Gln, Arg Gln, Arg Arg и Gln Gln
<220>
<221> DISULFID
<222> (21)..(37)
<400> 95
Gln Glu His Pro Asn Ala Arg Lys Tyr Lys Gly Ala Asn Xaa Xaa Gly
1 5 10 15
Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met
20 25 30
Ser Gly Leu Gly Cys
35
<210> 96
<211> 15
<212> PRT
<213> Homo sapiens
<400> 96
Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser Met Ser Gly Leu Gly
1 5 10 15
<---