Результат интеллектуальной деятельности: Композиция на основе янтарной кислоты и аспарагина для повышения продуктивности клеточных линий-продуцентов рекомбинантных белков
Вид РИД
Изобретение
Область техники, к которой относится изобретение
Изобретение относится к биотехнологии, в частности к композиции на основе янтарной кислоты и аспарагина, и может быть использовано при культивировании клеток млекопитающих, а также для получения рекомбинантных антител IgG и IgA класса.
Уровень техники
Имеется несколько стратегий по улучшению свойств сред для культивирования клеток млекопитающих. Одной из них является комбинация стандартной базовой среды с разными композициями добавок с целью определения их влияния на клеточный рост и продуктивность. Важное значение в подборе компонентов добавок играет анализ роли незаменимых аминокислот в метаболизме клеток млекопитающих. (MINI-REVIEW, 2005, Michael Butler «Animal cell cultures: recent achievements and perspectives in the production of biopharmaceutical" Appl Microbiol Biotechnol.,vol. 68, p. 283-291).
Обычное содержание L-глутамина в средах, используемых при выращивании клеток яичника китайского хомячка (СНО) составляет 8 мМ. Такая концентрация глутамина способствует быстрому росту СНО клеток, но не является оптимальной при долгосрочном выращивании для получения продукта из-за накапливания продуктов распада. Замена глутамина на аспарагин для культуры СНО клеток улучшает клеточный рост и продуктивность (Kurano et al. "Growth behavior of Chinese hamster ovary cells in a compact loop bioreactor" Journal of Biotechnology 15(1-2): 113-28, August 1990). Глутамин и аспарагин играют интегрирующую роль в азотистом обмене. К ним относится так называемый феномен "перераспределения азота в организме". Помимо перераспределения азота в организме, наряду с глутаминовой кислотой, аспарагиновая кислота принимает участие в обезвреживании аммиака в организме. Метаболический фильтр подразумевает адаптацию клеток к росту в среде с заменой глутамина на аспарагин или янтарную кислоту, что в свою очередь уменьшает выход в среду лактата и аммония, и положительно сказывается на росте популяции клеток.
Однако увеличение плотности клеток и их жизнеспособности, а также продукции антител может быть достигнуто за счет иных факторов. Проведены исследования по изучению составляющих компонентов композиции при выращивании стабильных клеточных линий-продуцентов иммуноглобулинов, полученных на основе клеток СНО DG44 в бессывороточной суспензионной среде и их влиянию на продукцию рекомбинантных антител классов IgG и IgA. Однако сложности при культивировании клеток, экспрессирующих IgA связаны, вероятно, с составом бессывороточных сред, сильно отличающихся от природных и требуют дополнительных исследований и доработки по использованию различных добавок.
Известен состав питательной среды, включающий в том числе янтарную кислоту (RU 2558253 «Питательная среда для суспензионного культивирования клеток млекопитающих», 2014-02-10 или RU 2014104467А, 2015-08-20). Однако данная среда содержит глутамин, а содержание янтарной кислоты не превышает 0,06 м мМ, что не обеспечивает должных времени культивирования и продуктивности. Кроме того, в изобретении показано использование состава только для культивирования ВНК-21 (клетки почки сирийского хомячка).
Также известен способ, описывающий использование в качестве композиции к средам для культивирования гибридом, малат, сукцинат (янтарную кислоту), изоцитрат, ЭДТА, селенит натрия и диоксид селена. (US 5045468 A Grant «Protein-free culture medium which promotes hybridoma growth», Priority date 1991-09-03). Недостатком данного способа является его применение для культивирования гибридом и отличие состава от предложенной в заявке композиции.
Известна композиция для культивирования бактерий thiocapsa reseopersicina, в которой рассматривается влияние хлорида аммония и следовых количеств: Na2S.9H2O, Na2.EDTA, FeSO4.7H2O, CoCl2.6H2O, MnCl2.2H2O, ZnCl2, NiCl2.6H2O, Na2MoO4.2H2O, Н3ВО3, CuCl2.2H2O на рост бактерий. (КR 20080012083 A "Culture method for high concentration of thiocapsa reseopersicina" Priority date 2006-08-02). Однко данный состав нельзя использовать для выращивания клеток млекопитающих, включая клетки СНО.
Наиболее близким к заявленной композиции по техническому решению является способ, описывающий использование аспарагина в составе среды культивирования (US 20180148510 A1 «Production of proteins in glutamine-free cell culture media" Martin Gawlitzek, Shun Luo, Christina Teresa Petraglia. Priority date, 2009-08-11 US 9714293 B2, 2018 - US 15881308). Описанный способ принят за прототип изобретения. Данный способ рассматривает увеличение продуктивности за счет замещения глутамина на аргинин или аспарагин в составе среды культивирования. Недостатком прототипа является то, что в нем рассматривается замещение глутамина только на аспарагин, без использования янтарной кислоты в среде культивирования СНО клеток. Также используют другую концентрацию аргинина или аспарагина. Недостатком прототипа является и то, что замещают глутамин на аспарагин в концентрации от 7.5 mM до 15 mM в среде культивирования СНО клеток, при этом не используют янтарную кислоту в сочетании с фактором роста фибробластов, хлоридом цинка, хлоридом никеля, цитратом железа и молибдатом натрия.
Раскрытие изобретения
Композицию, предложенную в изобретении, используют для культивирования клеточных линий - продуцентов рекомбинантных антител IgG1, IgA1 и IgA2 - изотипов, созданных на основе клеток СНО.
Технической проблемой, решаемой изобретением, является создание композиции для базовой среды для повышения продуктивности клеточных линий-продуцентов рекомбинантных антител.
Технический результат заключается в повышении продуктивности клеточных линий-продуцентов рекомбинантных антител при увеличении продолжительности времени культивирования.
Технический результат достигается за счет использования композиции для среды культивирования на основе янтарной кислоты и аспарагина.
В одном из вариантов осуществления изобретения композиция включает янтарную кислоту, декстран сульфат, цитрат железа. В другом варианте осуществления изобретения состав содержит янтарную кислоту, аспарагин, фактор роста фибробластов (FGF-2), сульфат цинка, декстран сульфат и цитрат железа. Возможен вариант осуществления изобретения, согласно которому композиция содержит янтарную кислоту, аспарагин, фактор роста фибробластов, хлорид цинка, хлорид никеля, молибдат натрия и цитрат железа.
Наилучший результат достигается при использовании многокомпонентной композиции к базовой бессывороточной среде IMDM (среда Искова - модификация среды Дульбекко), которая включает в себя: водный раствор фактора роста фибробластов-2 (FGF-2) - 11.2-22.4 нг/мл, янтарную кислоту (бутандиовая кислота, этан-1,2-дикарбоновая кислота) - 2-8 мМ, аспарагин (амид аспарагиновой кислоты или 4-амид-2-аминобутандиовая кислота) - 2-6 мМ, и солевые добавки, в качестве которых используют декстран сульфат, хлорид цинка, хлорид никеля, цитрат железа, молибдат натрия, в конечной концентрации до 0.0015 мМ каждая. При этом солевые добавки используют в виде водных растворов.
Впервые было установлено, что использование предлагаемой многокомпонентной добавки к базовой среде позволяет повысить плотность, однородность культуры, а также время культивирования и продуктивность клеточных линий-продуцентов рекомбинантных антител клеток при их суспензионном культивировании.
Для повышения продуктивности клеточных линий - продуцентов рекомбинантных белков применяют в качестве замены глутамина янтарную кислоту и/или аспарагин. Однако используют меньшую концентрацию аспарагина (по сравнению с прототипом): от 2 мМ до 6 мМ как в одиночном использовании, так и при использовании в составе композиции с фактором роста фибробластов, янтарной кислотой и микроэлементами. Меньшая концентрация в сочетании с вышеупомянутыми компонентами способствует увеличению продуктивности стабильных клеточных линий. Кроме того, заявленная композиция повышает уровень продукции рекомбинантных антител не только класса IgG, но и антител IgA1- и IgA2-изотипов.
Краткое описание чертежей
Изобретение иллюстрируется следующими графическими материалами:
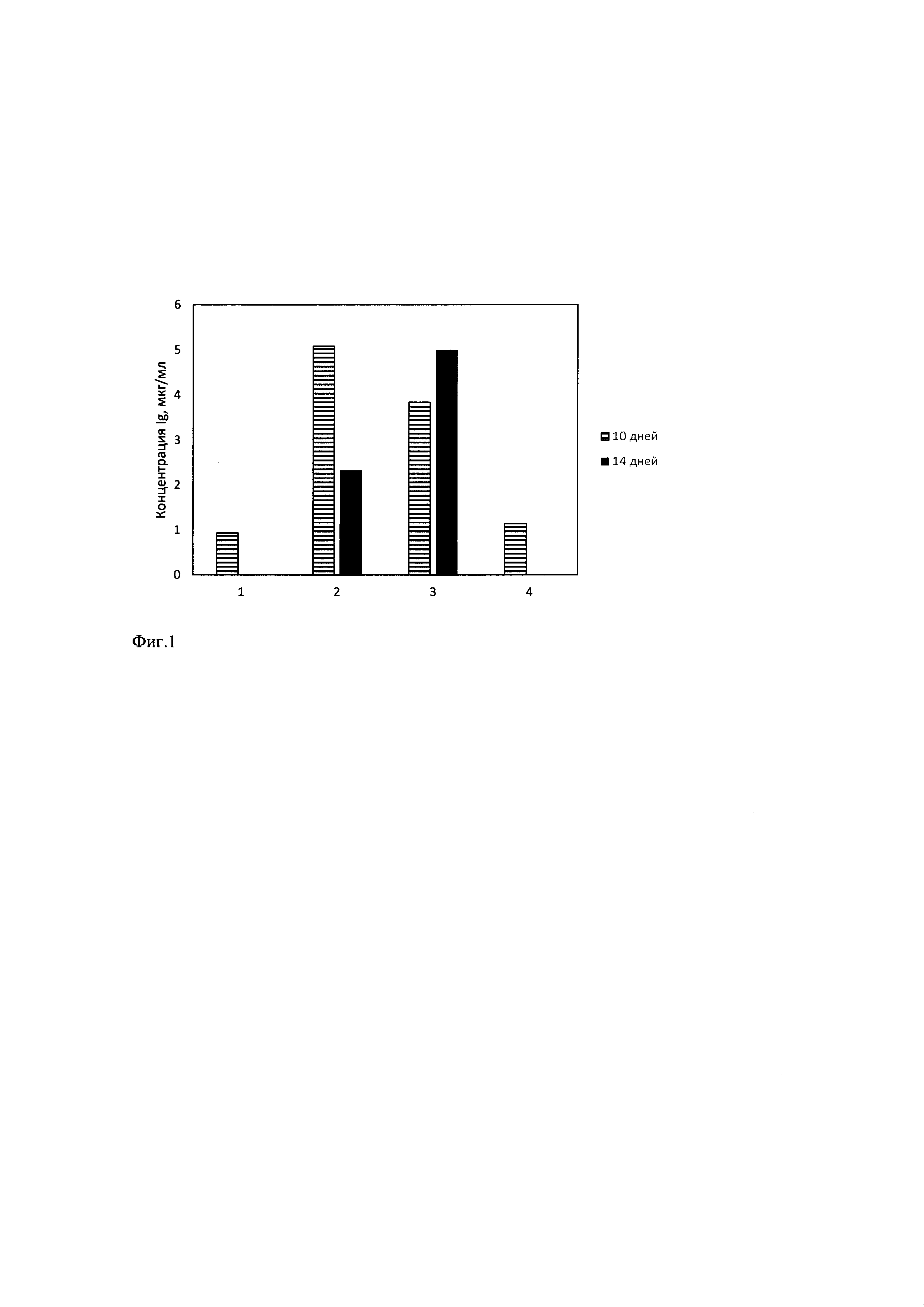
Фиг. 1 Влияние замены глутамина в среде на аспарагин и янтарную кислоту при культивировании стабильной клеточной линии- продуцента димера IgA1. 1 - Контроль: среда с 8 мМ L-глутамином; 2 - среда с 6 мМ янтарной кислотой; 3 - среда с 6 мМ аспарагином; 4 - среда с 6 мМ GlutaMax.
Фиг. 2 Влияние замены глутамина в среде на аспарагин и янтарную кислоту при культивировании стабильной клеточной линии- продуцента димера IgA2. 1 - Контроль: среда с 8 мМ L-глутамином; 2 - среда с 6 мМ янтарной кислотой; 3 - среда с 6 мМ аспарагином; 4 - среда с 6 мМ GlutaMax.
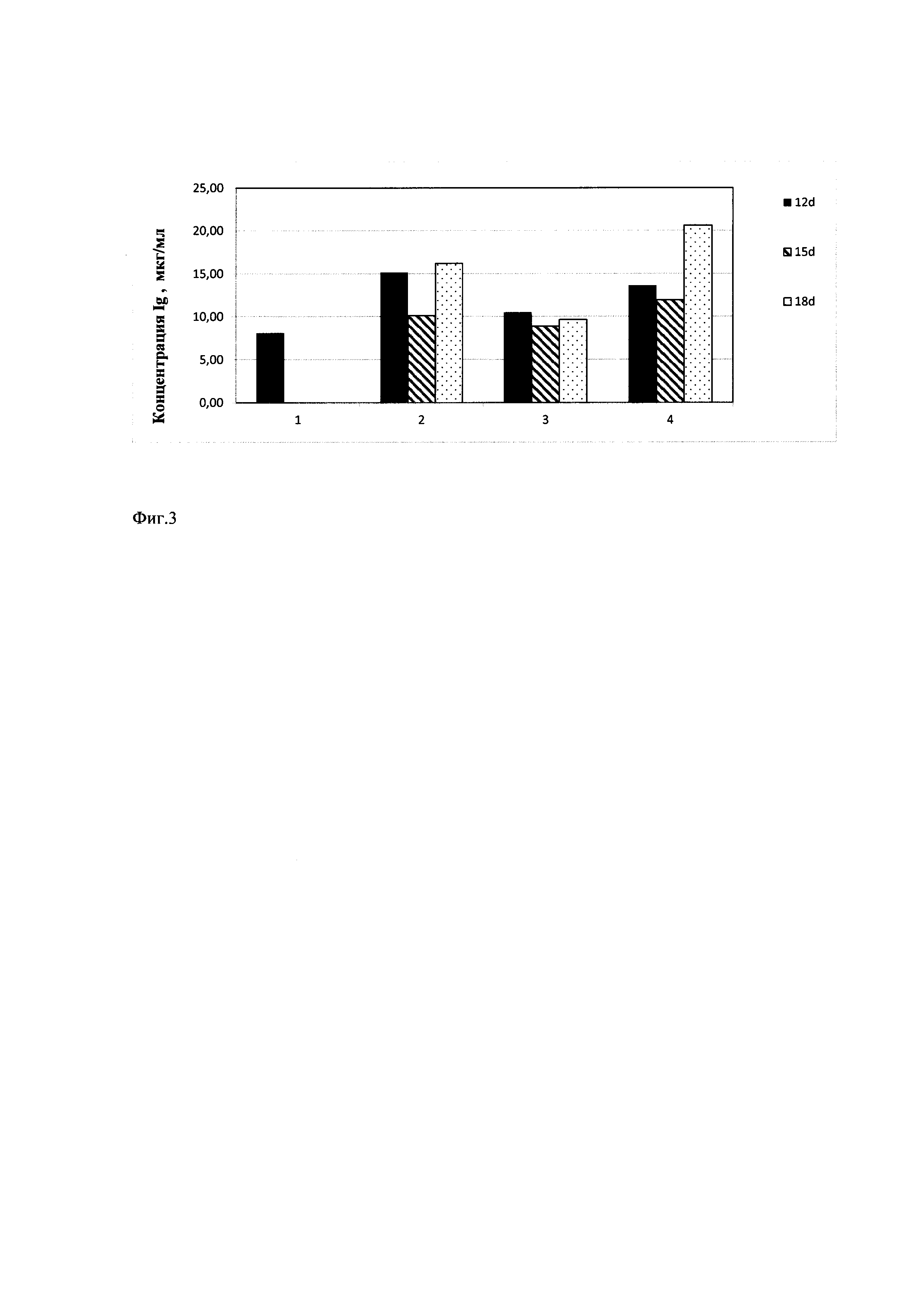
Фиг. 3 Влияние комплексных добавок, содержащих 6 мМ янтарную кислоту, FGF-2, декстран сульфат и цитрат железа на продолжительность и уровень продукции рекомбинантных антител. 1 - IMDM + 8 мМ L-глутамин - контроль; 2 - IMDM + 6 мМ янтарная кислота + FGF-2 + декстран сульфат + цитрат железа; 3 - IMDM + 6 мМ янтарная кислота + FGF-2 + сульфат цинка; 4 - IMDM + 6 мМ аспарагин + декстран сульфат + цитрат железа.
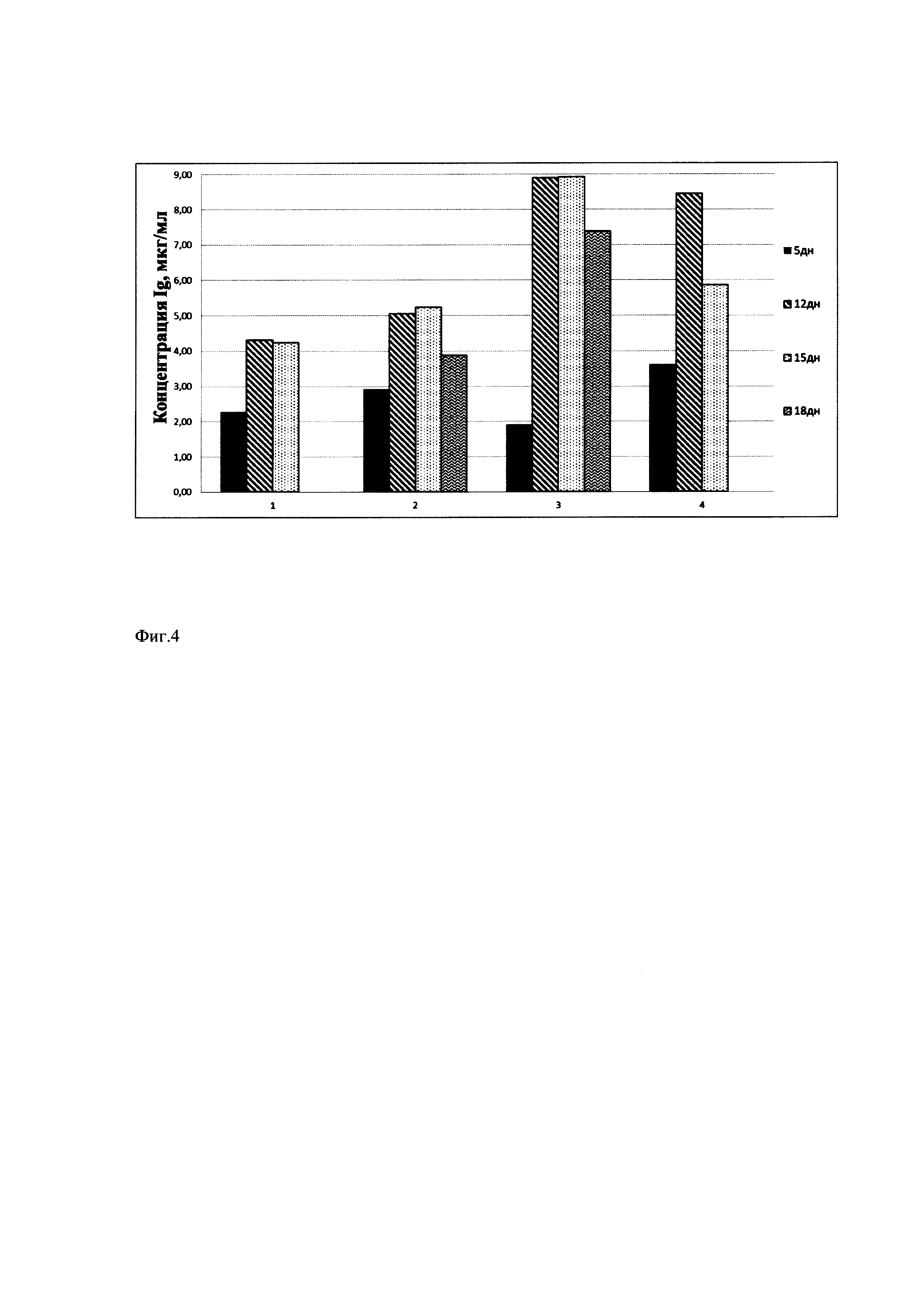
Фиг. 4 Влияние комплексных добавок, содержащих 6 мМ янтарную кислоту, 6 мМ аспарагин, FGF-2, сульфат цинка, декстран сульфат и цитрат железа на продолжительность и уровень продукции рекомбинантных антител. 1-IMDM + 8 мМ L-глутамин - контроль; 2- IMDM + 6 мМ янтарная кислота + FGF-2 + декстран сульфат + цитрат железа; 3 - IMDM + 6 мМ янтарная кислота + FGF-2 + сульфат цинка; 4 - IMDM + 6 мМ аспарагин + декстран сульфат + цитрат железа.
Фиг. 5 Влияние композиции янтарной кислоты и микроконцентраций солей на продолжительность и уровень продукции рекомбинантных антител IgG1. 1 - IMDM + 8 мМ L-глутамин-контроль; 2 - IMDM + 8 мМ L-глутамин + хлорид никеля + хлорид цинка + молибдат натрия; 3 - IMDM + 6 мМ янтарная кислота + хлорид никеля + хлорид цинка + молибдат натрия; 4 - IMDM + 8 мМ L-глутамин + хлорид никеля + хлорид цинка + хлорид железа(III); 5 - IMDM + 6 мМ янтарная кислота + хлорид никеля + хлорид цинка + молибдат натрия + цитрат железа
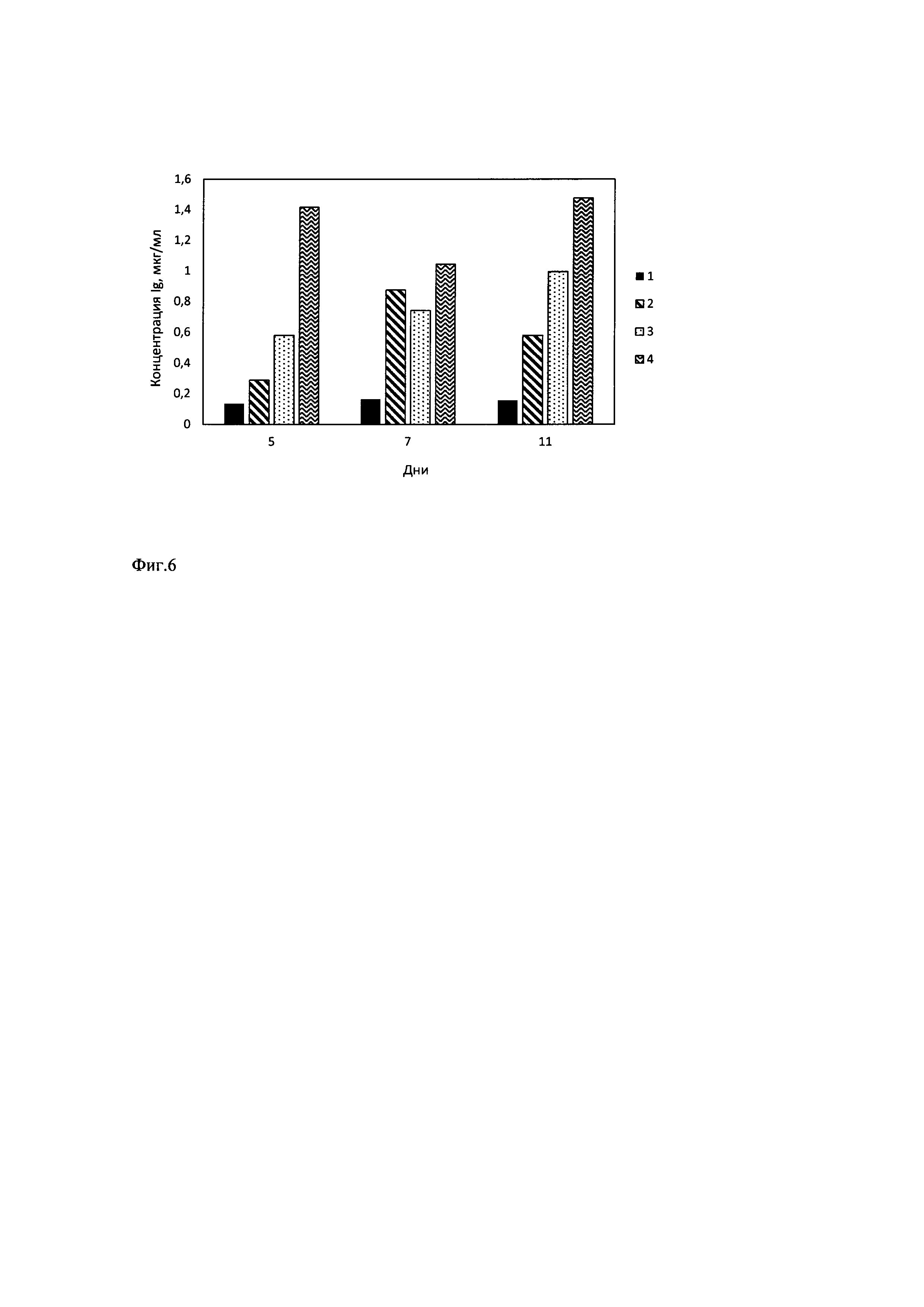
Фиг. 6 Влияние композиции янтарной кислоты и микроконцентраций солей на продолжительность и уровень продукции рекомбинантных антител димерной формы IgA1. 1 - OptiCHO + 8 мМ L-глутамин - контроль; 2 - IMDM + 8 мМ L-глутамин + хлорид никеля + хлорид цинка + молибдат натрия - контроль; 3 - IMDM + 6 мМ янтарная кислота + хлорид никеля + хлорид цинка + молибдат натрия; 4 - IMDM + 6 мМ янтарная кислота + хлорид никеля + хлорид цинка + молибдат натрия + цитратжелеза.
Осуществление изобретения
Изобретение иллюстрируется примерами конкретного выполнения, которые более подробно описывают возможность осуществления заявляемого изобретения с достижением заявляемого технического результата.
Пример 1. Сравнение влияния замены глутамина на янтарную кислоту и аспарагин в составе среды культивирования.
В экспериментах используют суспензионные стабильные клеточные линии -продуценты - рекомбинантных антител IgA1 и IgA2m1 - изотипов, на основе клеточной линии СНО DG44 (dhfr-). Клеточные культуры выращивают на бессывороточной базовой среде IMDM ("ПанЭко", РФ). Для определения влияния как на продуктивность, так и на плотность клеточных культур культивирования, эксперимент проводят в формате статических культур в 6-луночных планшетах при стандартных условиях выращивания при 37 С° и 8% CO2.
Для сравнения эффекта влияния на рост клеточных культур-продуцентов антител IgA-изотипа в качестве замещения 8 мМ L-глутамина используют 6 мМ янтарную кислоту, 6 мМ аспарагин и 6 мМ GlutaMax фирмы "Gibco". 6 мМ GlutaMax используют в качестве сравнения, так как предлагается фирмой в качестве добавки для увеличения продуктивности и содержит L-аланил-L-глутамин.
При культивировании стабильной клеточной линии - продуцента димера IgA1 с применением 6 мМ янтарной кислоты и 6 мМ аспарагина наблюдают увеличение продуктивности на 10 день культивирования по сравнению с контрольной средой с использованием 8 мМ глутамина в 5.5 и 4.2 раза соответственно, в то время как добавка 6 мМ GlutaMax фирмы "Gibco дает увеличение только в 1.25 раза (Фиг. 1).
На Фиг. 2 показано, что использование янтарной кислоты и аспарагина также увеличивает время культивирования: клеточные линии продолжают рост и экспрессию антител более 14 дней. Также использование 6 мМ аспарагина также увеличивает продуктивность.
При культивировании стабильной клеточной линии- продуцента димера IgA2 с применением 6 мМ янтарной кислоты и 6 мМ аспарагина наблюдают увеличение продуктивности на 14 и 19 день культивирования по сравнению с контрольной средой с использованием 8 мМ глутамина. При использовании 6 мМ янтарной кислоты увеличение составляет 1.66 и 2.25 раз на 14 и 19 день соответственно, а при использовании 6 мМ аспарагина - 1.5 раза на 14 день культивирования. (Фиг. 2)
Пример 2. Влияние комплексных добавок, содержащих 6 мМ янтарную кислоту, 6 мМ аспарагин, фактор роста фибробластов (FGF-2), сульфат цинка, декстран сульфат и цитрат железа на продолжительность и уровень продукции рекомбинантных антител.
При культивировании стабильной клеточной линии- продуцента IgG1 в базовой среде для увеличения времени и уровня продукции рекомбинантных антител используют замену глутамина на 6 мМ янтарную кислоту или 6 мМ аспарагин, фактор роста фибробластов (FGF-2), 0,0015 мМ цитрат железа и декстран сульфат. На Фиг. 3 продемонстрированы показатели по увеличению продукции рекомбинантных антител, которые получают на 12 и 18 день культивирования. Они составляют 15.1 и 16.21 мкг/мл при использовании в качестве добавки янтарной кислоты, 13.6 и 20.6 мкг/мл - при применении аспарагина.
Кроме того, использование янтарной кислоты и/или аспарагина позволяет также продлить время культивирования и продукции до 18 дней. Применение данной комплексной композиции позволяет увеличить продуктивность по сравнению с контролем в 1.8-2 раза для добавки, содержащей янтарную кислоту, и в 1.6-2.54 раза для добавки с аспарагином на 12 и 18 день, соответственно.
Также влияние данной добавки изучают при культивировании стабильной клеточной линии - продуцента димерной формы IgA1 в базовой среде. На Фиг. 4 продемонстрировано, что при культивировании стабильной клеточной линии- продуцента димерной формы IgA1 наибольшее влияние на продуктивность оказывает добавка, содержащая 6 мМ аспарагин, декстран сульфат и цитрат железа или 6 мМ янтарную кислоту, сульфат цинка и фактор роста фибробластов (FGF-2). Продукция рекомбинантных антител увеличивается примерно в 2 раза.
Пример 3. Изучение влияния композиции, содержащей 6 мМ янтарную кислоту, 6 мМ аспарагин, фактор роста фибробластов (FGF-2), хлорид цинка, хлорид никеля, молибдат натрия и цитрат железа на продолжительность и уровень продукции рекомбинантных антител.
Для сравнения эффекта влияния на рост клеточных культур-продуцентов антител IgG1 изотипа в качестве замещения 8 мМ L-глутамина используют 6 мМ янтарную кислоту, а в качестве микродобавок солей - хлорид цинка, хлорид никеля, молибдат натрия и цитрат железа (Фиг. 5). Все соли добавляют к базовой среде IMDM в конечной концентрации 0.0015 мМ. В качестве контролей используют клеточную линию, культивируемую на полной питательной бессывороточной среде OptiCHO ("Invitrogen", США), которая рекомендована производителем и содержит 8 мМ L-глутамин и базовую бессывороточную среду IMDM ("Биолот", РФ) с 8 мМ L-глутамином без микродобавок. При культивировании клеточных культур исключительно на базовой среде IMDM с 8 мМ L-глутамином без микродобавок происходит ухудшение роста и падение продуктивности. В связи с этим, в качестве 2-го контроля применяют культивирование на базовой среде IMDM с 8 мМ L-глутамином и микродобавками хлорида никеля, хлорида цинка, молибдата натрия или хлорида железа в конечной концентрации 0.0015 мМ. Произведено сравнение выращивания стабильных клеточных линий-продуцентов IgG1 и IgA1 при использовании базовой среды IMDM с 8 мМ L-глутамином и добавками хлорида цинка, хлорида никеля, молибдата натрия и при использовании базовой среды IMDM с замещением глутамина на 6 мМ янтарную кислоту с аналогичными солями.
На Фиг. 5 применение указанных микродобавок солей в сочетании с янтарной кислотой демонстрирует увеличение продуктивности рекомбинантных иммуноглобулинов. Применение добавки, содержащей 8 мМ L-глутамин и микродобавки хлорида никеля, хлорида цинка, хлорида железа показывает повышение продуктивности клеточной линии-продуцента антител IgG1, но проигрывает по показателям продуктивности при применении добавки, содержащей 6 мМ янтарную кислоту, хлорид никеля, хлорид цинка, молибдат натрия с цитратом железа или без него. На Фиг. 5 и Фиг. 6 показано, что по мере увеличения срока культивирования до 11 дней, наилучшие показатели по продуктивности получают при использовании добавки, содержащей 6 мМ янтарную кислоту, хлорид никеля, хлорид цинка, молибдат натрия или 6 мМ янтарную кислоту, хлорид никеля, хлорид цинка, молибдат натрия и цитрат железа для обеих стабильных клеточных линий - продуцентов. Культивирование в течение 11 дней стабильной клеточной линии - продуцента димера IgA1 с применением добавки 6 мМ янтарной кислоты, хлорида никеля, хлорида цинка, молибдата натрия с цитратом железа увеличивает продуктивность в 14 раз, а с применением 6 мМ янтарной кислоты, хлорида никеля, хлорида цинка, молибдата натрия - в 9 раз по сравнению с контролем.
Культивирование в течение 11 дней стабильной клеточной линии - продуцента димера IgA1 с применением добавки 6 мМ янтарной кислоты, хлорида никеля, хлорида цинка, молибдата натрия с цитратом железа увеличивает продуктивность в 7.6 раза, а с применением 6 мМ янтарной кислоты, хлорида никеля, хлорида цинка, молибдата натрия - в 9 раз по сравнению с контролем (Фиг. 5). Таким образом, применение указанных добавок к базовой среде дает увеличение продукции рекомбинантных иммуноглобулинов классов G и А.