Результат интеллектуальной деятельности: Способ получения активного материала катода на основе литий-обогащенного фосфата LiFePOсо структурой оливина, электродная масса и катод литий-ионного аккумулятора
Вид РИД
Изобретение
Область техники, к которой относится изобретение
Изобретение относится к электродным материалам на основе сложных фосфатов переходных металлов и лития и может быть использовано для получения катодного активного материала для литий-ионных аккумуляторов и батарей на основе такого материала.
Уровень техники
Литий-ионные аккумуляторы (ЛИА) являются наиболее эффективными электрохимическими источниками тока с точки зрения энергоемкости, безопасности, стабильности зарядно-разрядного циклирования и мощностных характеристик. Главный компонент ЛИА, определяющий его основные характеристики положительный электрод (катод). В настоящее время коммерческое применение нашли катодные материалы на основе слоистых оксидов LiCoO2, LiNiO2 и их производных; литий-марганцевая шпинели LiMn2O4 и фосфата лития-железа со структурой оливина LiFePO4.
Несмотря на десятилетие успешной коммерциализации, LiFePO4 и его производные продолжают оставаться важной частью научных исследований и технологических разработок в области литий-ионных батарей благодаря их богатой кристаллохимии и разнообразию электрохимических свойств. Необходимость поиска взаимосвязей между условиями синтеза, морфологией частиц, химией дефектов, электрохимическими характеристиками и фазовыми превращениями, происходящими в процессе (де)интеркаляции Li+ мотивирует интенсивные исследования в этой области. Влияние различных типов внутренних дефектов (антиструктурные Li/Fe дефекты, вакансии Li и/или Fe, гомо- и гетеровалентное легирование в позициях Li или Fe) на фазовый состав и электрохимические свойства материалов с структурой оливина описано и обсуждено в соответствующих экспериментальных, теоретических и обзорных работах [Chem. Rev. 2014, 114, 11414-11443; J. Power Sources 232 (2013) 357-369]. Имеющиеся в литературе данные указывают на то, что стехиометричный LiFePO4 с идеальным распределением катионов Li и Fe по кристаллографическим позициям не всегда является наилучшим составом для высокопроизводительного катодного материала [Nat. Mater. 1, 123-128 (2002); Nature 458, 190-193 (2009); Energy Environ. Sci., 2016, 9, 2902-2915].
Литий-обогащенные оливины как новое поколение высокоэффективных материалов для ЛИА были представлены в недавней работе Парка и соавторов, а также в последующей теоретической статье Зенга и соавторов [Energy Environ. Sci., 2016, 9, 2902-2915; Phys. Chem. Chem. Phys., 2018, 20, 17497-17503]. Показано, что присутствие небольшого количества Li в позициях Fe в материалах состава Li1+xFe1-yPO4 (0<х, у<0.1) приводит к уменьшению энергетического барьера спинодального распада, а также понижению барьеров диффузии Li+ вдоль кристаллографического направления [010]. Кроме того, наличие дефектов Li-Fe (Li в кристаллографической позиции Fe) энергетически дестабилизирует нежелательные Fe+Li (Fe в кристаллографической позиции Li) дефекты, улучшая тем самым транспорт Li+ в каналах структуры.
Кроме того, из уровня техники известен способ получения активного материала, раскрытый в US 9490483 В2, опубл. 08.11.2016, прототип. Способ получения активного материала, имеющего формулу LixFeyPO4, где 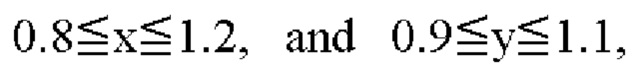 включает смешивание Fe-содержащего компонента, соли лития и соли фосфорной кислоты, с последующей термообработкой полученной смеси при температуре 650-850°С в восстановительной атмосфере.
включает смешивание Fe-содержащего компонента, соли лития и соли фосфорной кислоты, с последующей термообработкой полученной смеси при температуре 650-850°С в восстановительной атмосфере.
Раскрытие изобретения
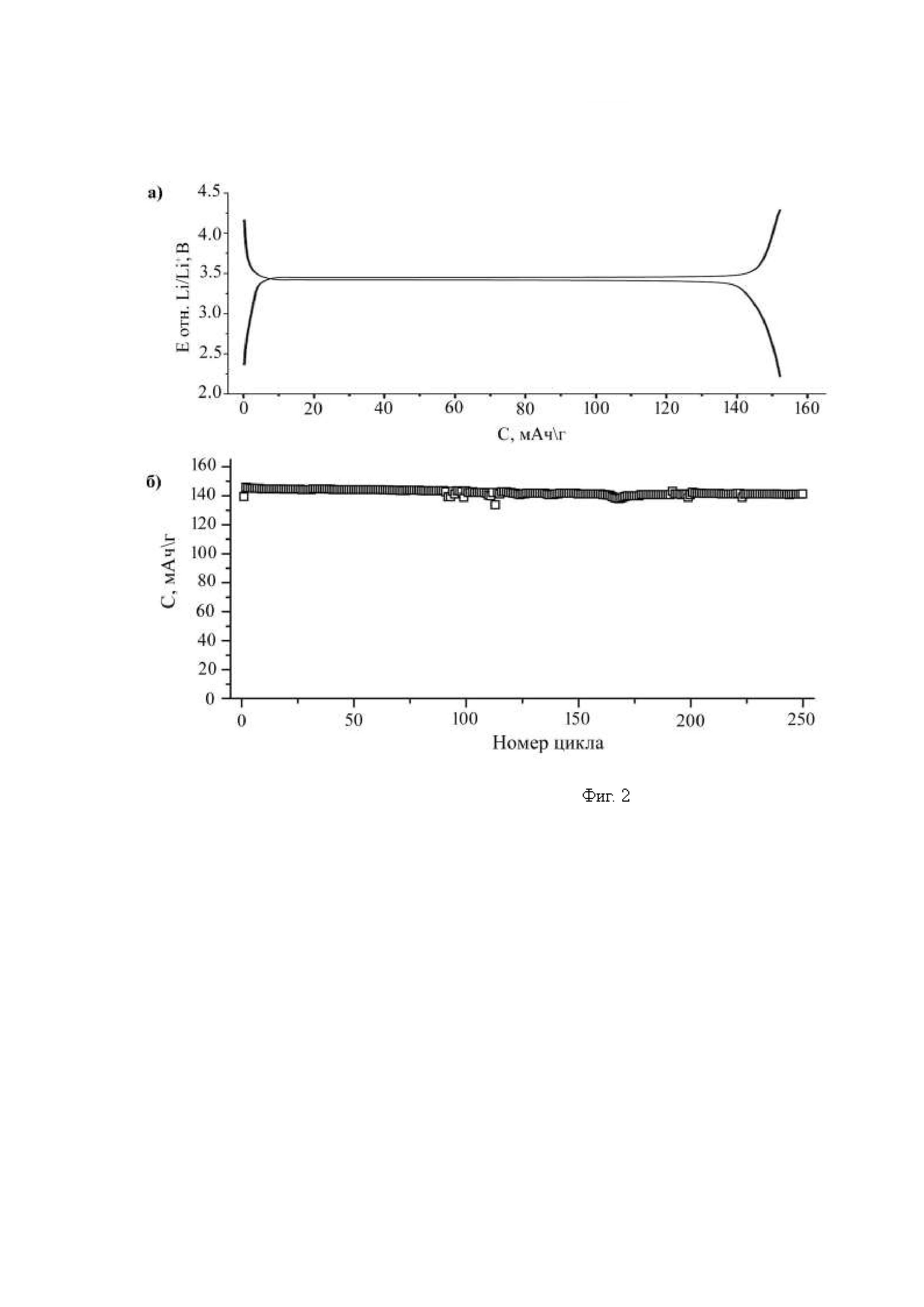
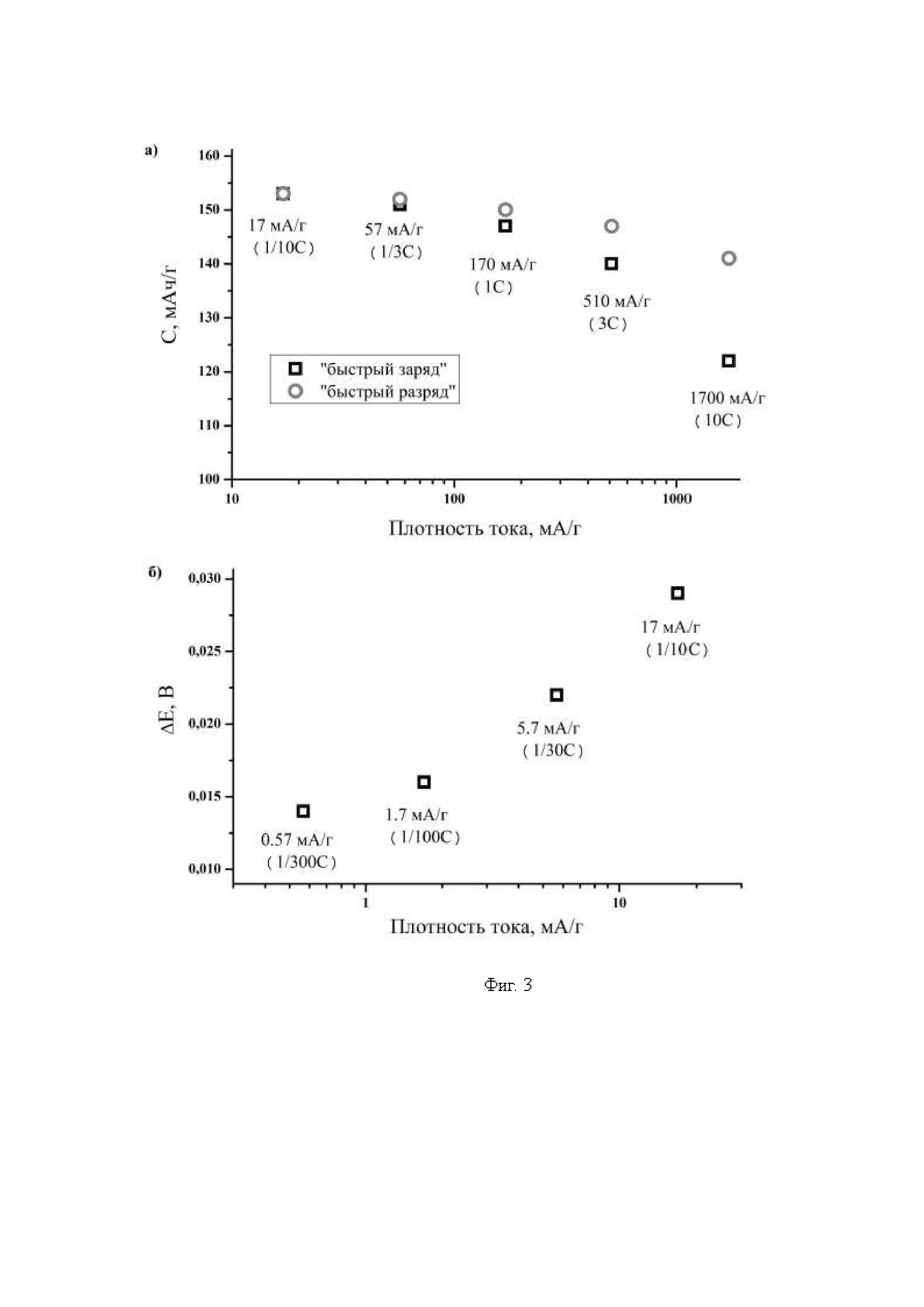
Авторы настоящего изобретения обнаружили, что фосфат железа и лития, получаемый в гидро- и сольвотермальных условиях с использованием Li3-zNazPO4 (0≤z<2) в качестве прекурсора (Фиг. 1-3), обладает рядом практически важных особенностей для применения в качестве катодного материала для ЛИА. Этот материал характеризуется высокой обратимой емкостью (более 150 мАч/г, Фиг. 2а) и очень высокими мощностными характеристиками (Фиг. 3а): так, при заряде током плотностью 1700 мА/г (скорость заряда 10С, что означает полный заряд за 6 минут) катодный материал демонстрирует более 140 мАч/г разрядной емкости. Этот материал демонстрирует очень низкие величины разности между средними потенциалами заряда и разряда (Фиг. 3б), что а) говорит о нетипично низких для LiFePO4 величинах энергетического барьера спинодального распада и б) улучшает энергетическую эффективность материала. Отличная циклическая устойчивость (падение емкости менее 2% за 250 циклов заряда-разряда, Фиг. 2б) позволяет утверждать о высокой коммерческой привлекательности материала.
При использовании в качестве прекурсора Li3PO4, комбинация данных порошкового рентгеноструктурного анализа и мессбауэровской спектроскопии (показавшей, что в материале содержится ≈96% катионов Fe2+ и ≈4% катионов Fe3+) позволила определить состав материала как Li1.04Fe0.96PO4. Данные элементного анализа, проведенного методом атомно-эмиссионной спектрометрии, подтверждают этот состав (атомное соотношение Li:Fe:P=1.02:0.95:1 с погрешностью порядка 1%). Эти результаты, в совокупности с повышенными мощностными характеристиками и нетипичными для LiFePO4 значениями гистерезиса потенциала на заряде и разряде находятся в полном соответствии с данными, опубликованными в приведенных выше литературных источниках для литий-обогащенных оливинов, за исключением того факта, что в них использовали твердофазный метод синтеза.
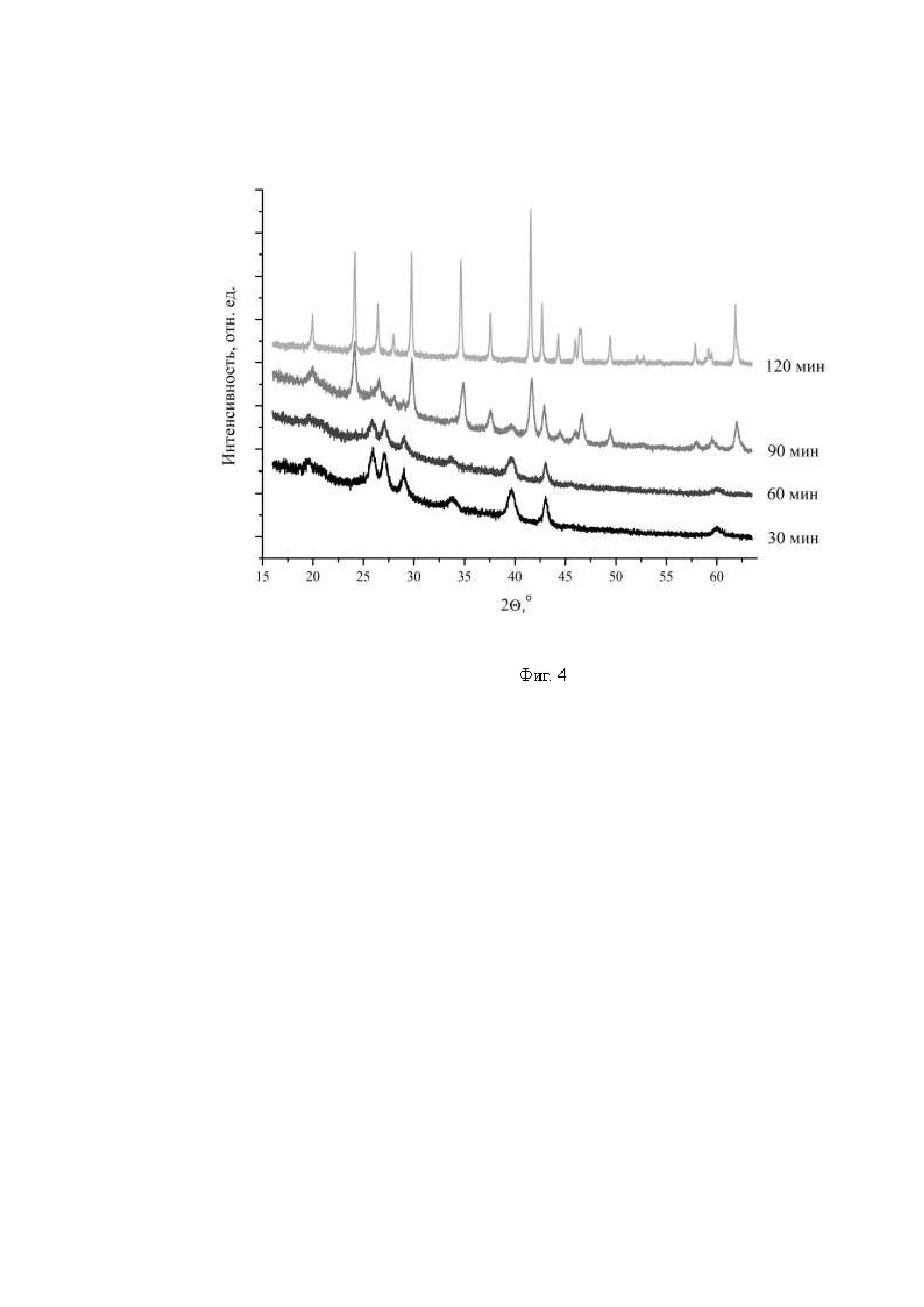
Авторы настоящего изобретения установили, что в процессе гидротермального синтеза фосфата лития-железа через прекурсор Li3PO4 отсутствуют промежуточные стадии. По данным рентгенофазового анализа образцов, отобранных на разных стадиях синтеза (Фиг. 4), образцы представляют собой либо однофазный фосфат лития β-Li3PO4 (30 мин), либо однофазный фосфат лития-железа со структурой оливина (120 мин), либо смесь этих фаз (60 мин и 90 мин). Таким образом, отсутствие промежуточных стадий в процессе гидротермального синтеза фосфата лития-железа, и избыток лития, имеющийся в реакционной системе, приводят к образованию Li-Fe дефектов, положительно влияющих на электрохимические свойства материала.
Кроме того, отсутствие промежуточных стадий в ходе синтеза позволяет сделать предположение о том, что состав прекурсора может отличаться от формулы Li3PO4 путем замены части лития на другие катионы. В соответствии с реакцией Li3PO4(твердый) + FeSO4(раствор)→ LiFePO4(твердый) + Li2SO4(раствор)
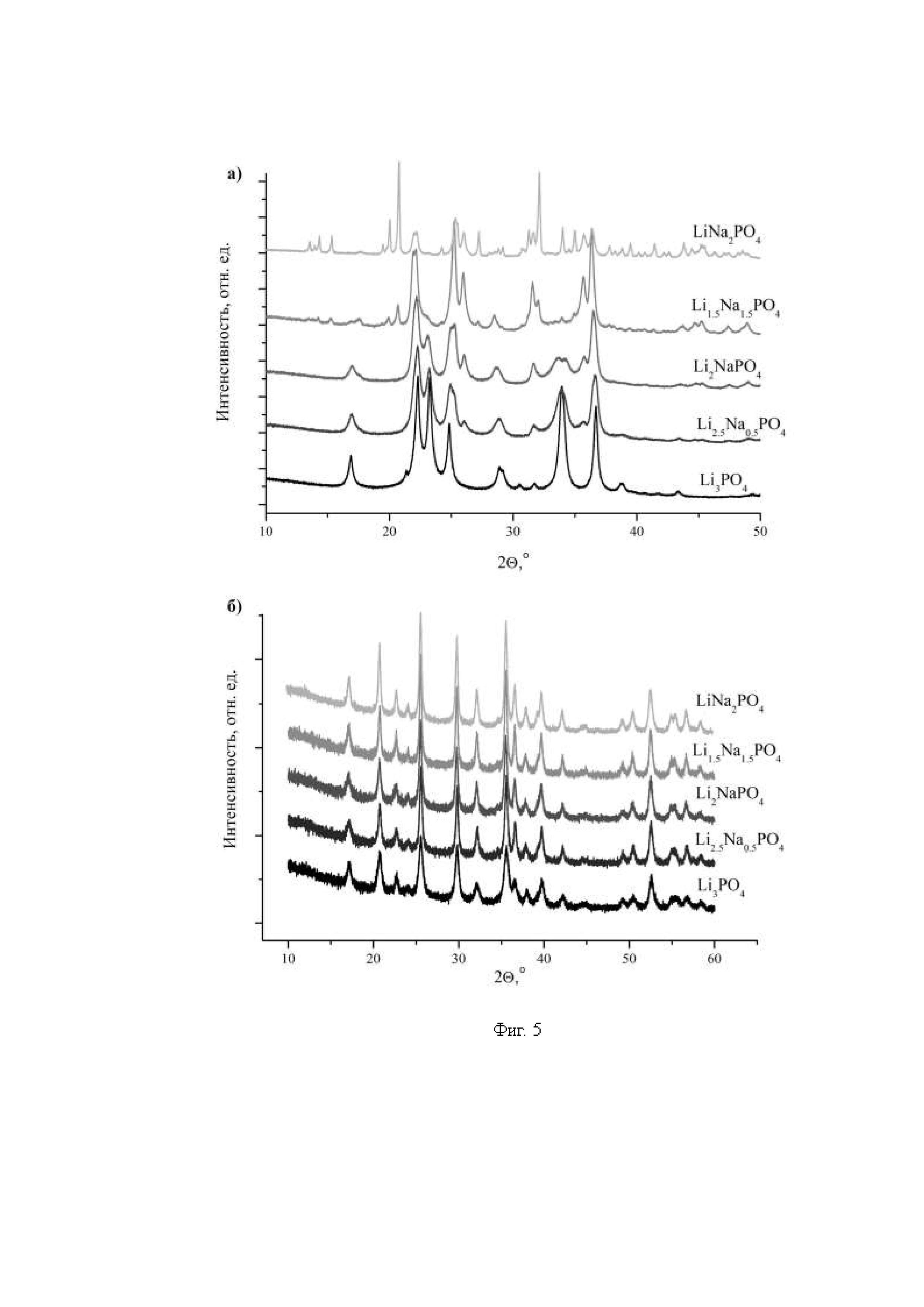
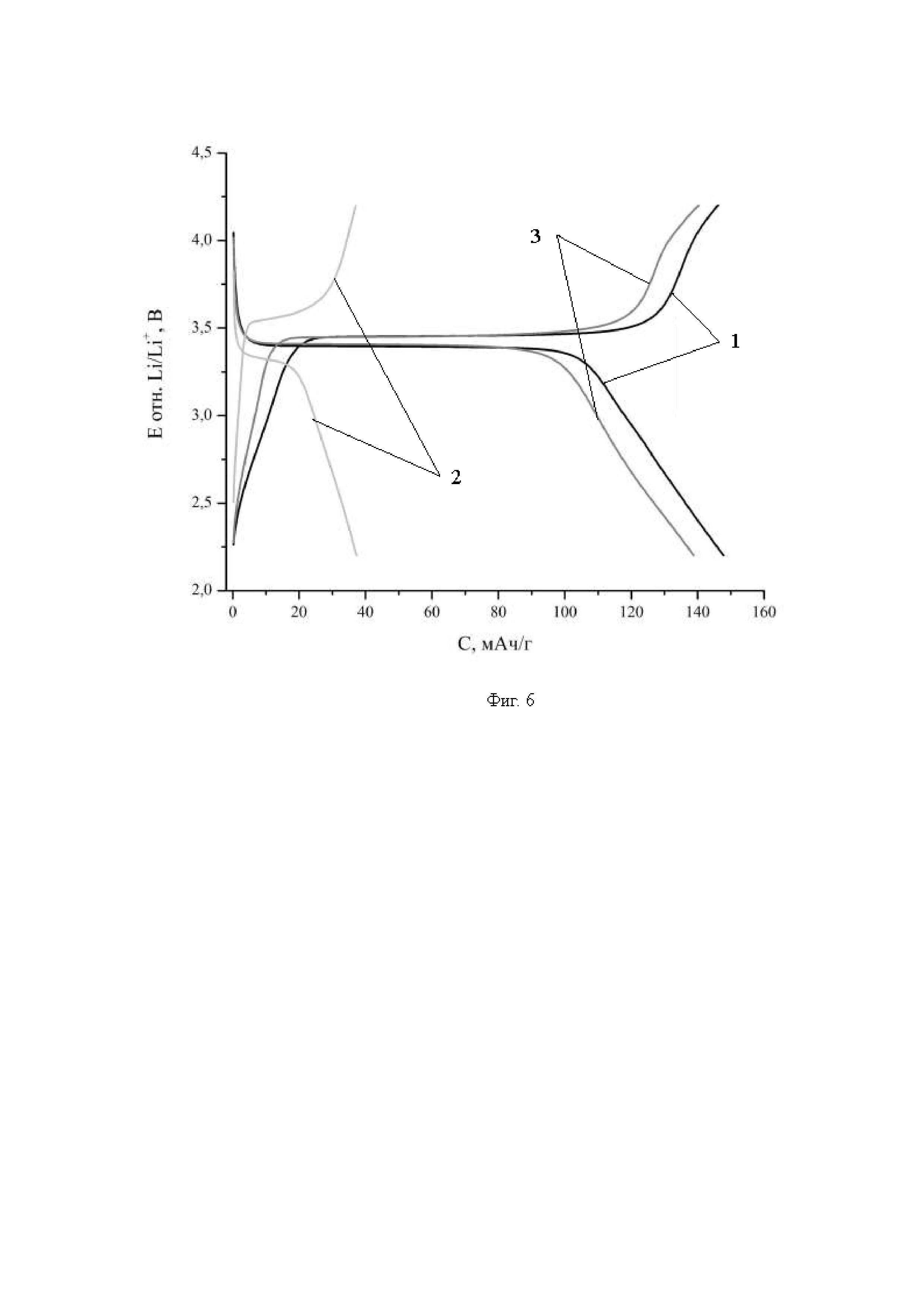
в маточном растворе остается порядка двух молей катионов лития из трех молей, присутствовавших изначально. Замена части катионов лития в исходном прекурсоре на другие катионы, например натрий, обладающие лучшей растворимостью солей (например, сульфатов) в реакционной среде, не должна влиять на фазовый состав образующегося продукта. Чтобы проверить это предположение, авторы настоящего изобретения осуществили синтез прекурсоров состава Li3-zNazPO4 (z=0, 0.5, 1, 1.5, 2) и последующую их гидротермальную обработку в присутствии сульфата железа. Дифрактограммы образцов состава Li3-zNazPO4 (z=0, 0.5, 1, 1.5, 2) представлены на Фиг. 5а. Дифрактограммы соответствующих продуктов гидротермального синтеза на Фиг. 5б. Можно видеть, что несмотря на значительное изменение фазового состава прекурсора с ростом содержания натрия (от однофазного β-Li3PO4 для состава Li:Na=3:0 до смеси Li2NaPO4 и Na3PO4 для состава Li:Na=1:2), гидротермальный синтез приводит к образованию одного и того же продукта однофазного фосфата железа-лития со структурой оливина. Отсутствие натрия в образцах после синтеза подтверждается данными локального рентгеноспектрального анализа. Электрохимические свойства получаемых материалов также соответствуют таковым для фосфата лития-железа со структурой оливина (Фиг. 6). Так, емкость материала, полученного из прекурсора состава Li2.5Na0.5PO4, составляет около 150 мАч/г. Стоит отметить, что образец, полученный из прекурсора состава LiNa2PO4 (т.е. с соотношением Li:Fe=1:1) демонстрирует низкие электрохимические характеристики (Фиг. 6). Это связано с тем, что при эквимолярном соотношении лития и железа литий-обогащенных оливинов не образуется, что приводит к резкому возрастанию вероятности образования нежелательных Fe+Li дефектов в ходе синтеза. Однако небольшое увеличение количества лития (до Li:Fe=1.1:1), т.е. использование прекурсора состава Li1.1Na1.9PO4, позволяет получать материал с высокой электрохимической емкостью (Фиг. 6), аналогичено образцам, полученных при высоком содержании лития в исходном фосфате.
Таким образом, синтез фосфата железа-лития через прекурсор общего состава Li3-zNazPO4 (0≤z<2) позволяет контролировать соотношение Li:Fe в ходе синтеза (а значит, и количество Li-Fe дефектов), а также значительно снижает стоимость производства материала, поскольку соли натрия гораздо дешевле литиевых аналогов.
Задачей настоящего изобретения является создание экономичного и масштабируемого способа получения катодного материала на основе структуры оливина, отличающегося высокой удельной энергоемкостью при средних и высоких скоростях заряда (более 1С) и стабильностью рабочих характеристик при длительной эксплуатации и ориентированного на использование в высокомощных источниках тока.
Технический результат настоящего изобретения заключается в экономичном и масштабируемом получении катодного материала, отличающегося высокой удельной энергоемкостью при циклировании на средних и высоких скоростях циклирования (более 1С) и стабильностью рабочих характеристик при длительной эксплуатации.
Указанный технический результат достигается за счет того, что способ получения активного материала для катода литий-ионного аккумулятора, имеющего формулу Li1+xFe1-yPO4, где 0<х, у<0,1, характеризующегося структурой оливина, включающий следующие стадии:
а) получают частицы Li3-zNazPO4 (0≤z<2) путем осаждения из раствора, полученного при растворении источников ионов Li+ или источников Li+ и Na+ в воде, с последующим добавлением источников ионов РО43- и органического сорастворителя, представляющего собой одноатомный и/или многоатомный спирты, содержащие 2-8 атомов углерода, при содержании сорастворителя в реакционной смеси указанных компонентов 20-80 масс. %.
б) смешивают источники катионов Fe2+ с частицами Li3-zNazPO4 (0≤z<2) при их мольном соотношении от 0,9:1 до 1,1: 1, соответственно, с последующим перемешиванием полученной смеси в атмосфере инертного газа в герметичном автоклаве при температуре в диапазоне 190-210°С в течение по меньшей мере 1 часа.
Такой способ представляет собой первый вариант осуществления настоящего изобретения.
Способ по изобретению характеризуется последовательностью стадий, ранее не использовавшейся для фосфатов данного состава, и позволяет получать однородные высокодисперсные порошки литий-обогащенного оливина Li1+xFe1-yPO4. Кроме того, способ позволяет снижать стоимость потенциального производства за счет уменьшения мольного соотношения Li:Fe от 3:1 до 1:1 за счет замены части лития на натрий.
В других вариантах осуществления способ может дополнительно включать нанесение электропроводного покрытия, позволяющее равномерно покрывать частицы слоем хорошо проводящего углеродного материала (например, сажи), что позволяет оптимизировать характеристики материала.
В частности, во втором варианте осуществления изобретения способ по изобретению используется для получения композитного активного материала для катода литий-ионного аккумулятора, имеющего формулу Li1+xFe1-yPO4/C, где 0<х, у<0,1, характеризующегося структурой оливина, включающий стадии, на которых:
а) получают частицы Li3-zNazPO4 (0≤z<2) путем осаждения из раствора, полученных при растворении источников ионов Li+ или источников Li+ и Na+ в воде, с последующим добавлением источников ионов РО43- органического сорастворителя, представляющего собой одноатомный и/или многоатомный спирты, при содержании сорастворителя в реакционной смеси указанных компонентов 20-80 масс. %;
б) смешивают источники катионов Fe2+ с частицами Li3-zNazPO4 (0≤z<2) при их мольном соотношении от 0,9:1 до 1,1: 1, соответственно, с последующим перемешиванием полученной смеси в атмосфере инертного газа в герметичном автоклаве при температуре в диапазоне 190-210°С в течение по меньшей мере 1 часа.
в) полученное в автоклаве вещество смешивают с источником углерода и отжигают при 600-700°С в течение по меньшей мере 1 часа в атмосфере инертного газа.
Изобретение также относится к электродной массе катода литий-ионного аккумулятора, содержащей активный материал, имеющий формулу Li1+xFe1-yPO4, где 0<х, у<0,1, полученный способом по п. 1, полимерное связующее и электропроводящую углеродную добавку, при следующем соотношении компонентов, масс. %: указанный активный компонент 60-94; полимерное связующее 3-20; электропроводящая углеродная добавка - 3-20.
Изобретение также относится к электродной массе катода литий-ионного аккумулятора, содержащей композитный активный материал, имеющий формулу Li1+xFe1-yPO4/С, где 0<х, у<0,1, полученный способом по п. 2, полимерное связующее и электропроводящую углеродную добавку, при следующем соотношении компонентов, масс. %: указанный активный компонент 60-94; полимерное связующее 3-20; электропроводящая углеродная добавка - 3-20.
Изобретение также относится к катоду литий-ионного аккумулятора, содержащий токосъемник, на поверхность которого нанесена вышеуказанная электродная масса на основе активного материала, имеющего формулу Li1+xFe1-yPO4, где 0<х, у<0,1, или вышеуказанная электродная масса на основе композитного активного материала, имеющего формулу Li1+xFe1-yPO4/C, где 0<х, у<0,1.
Другие варианты осуществления настоящего изобретения будут очевидны специалистам из нижеследующего описания и из прилагаемой формулы изобретения.
Не ограничивая себя какой-либо теорией, авторы изобретения полагают, что технический результат настоящего изобретения может быть связан с комбинацией факторов, позволяющих получать литий-обогащенные Li1+xFe1-yPO4, где 0<х, у<0.1, и в первую очередь обеспечивается получением прекурсора Li3-zNazPO4, где 0≤z<2, с использованием органического сорастворителя и последующим добавлением соли железа.
Краткое описание чертежей
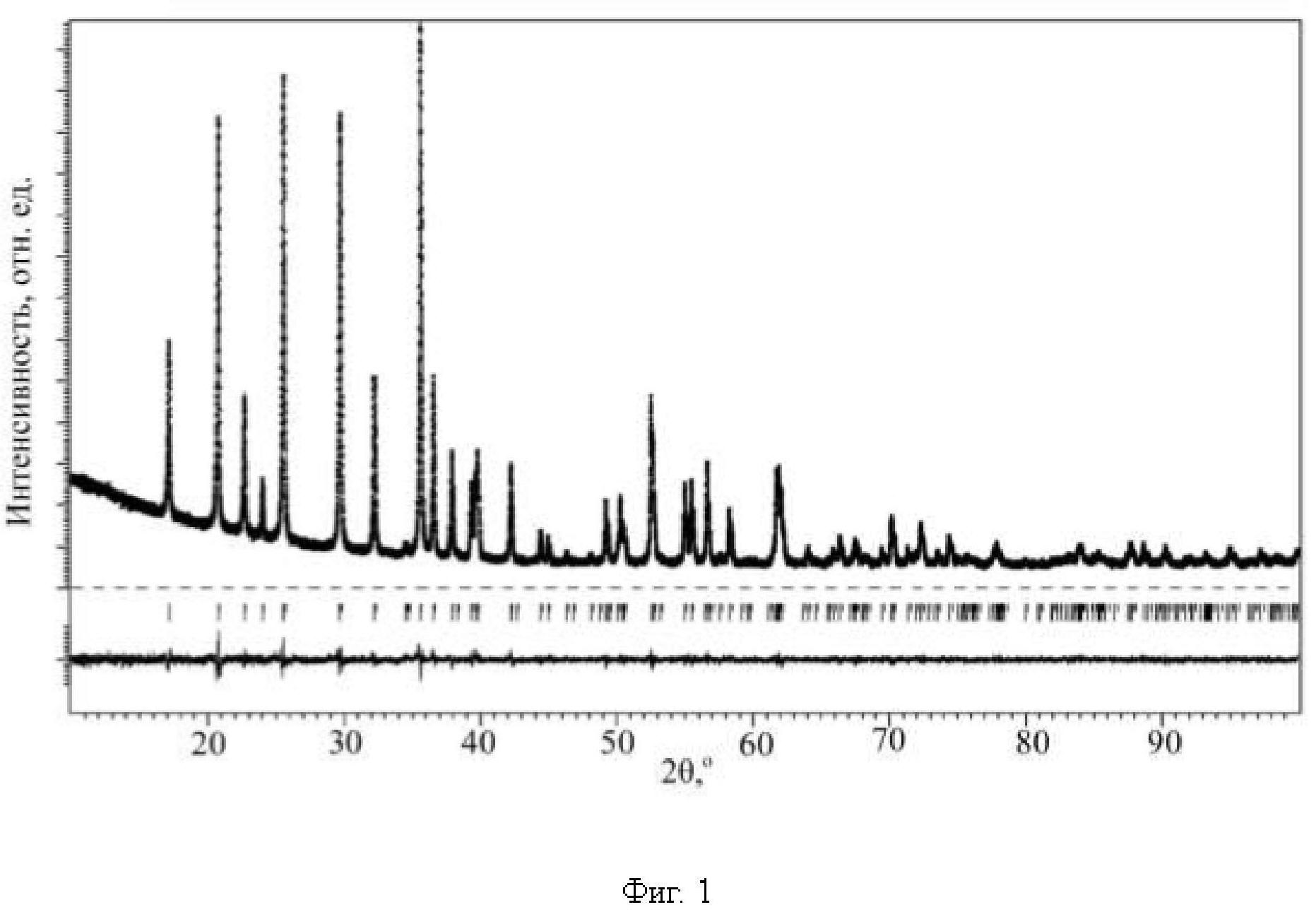
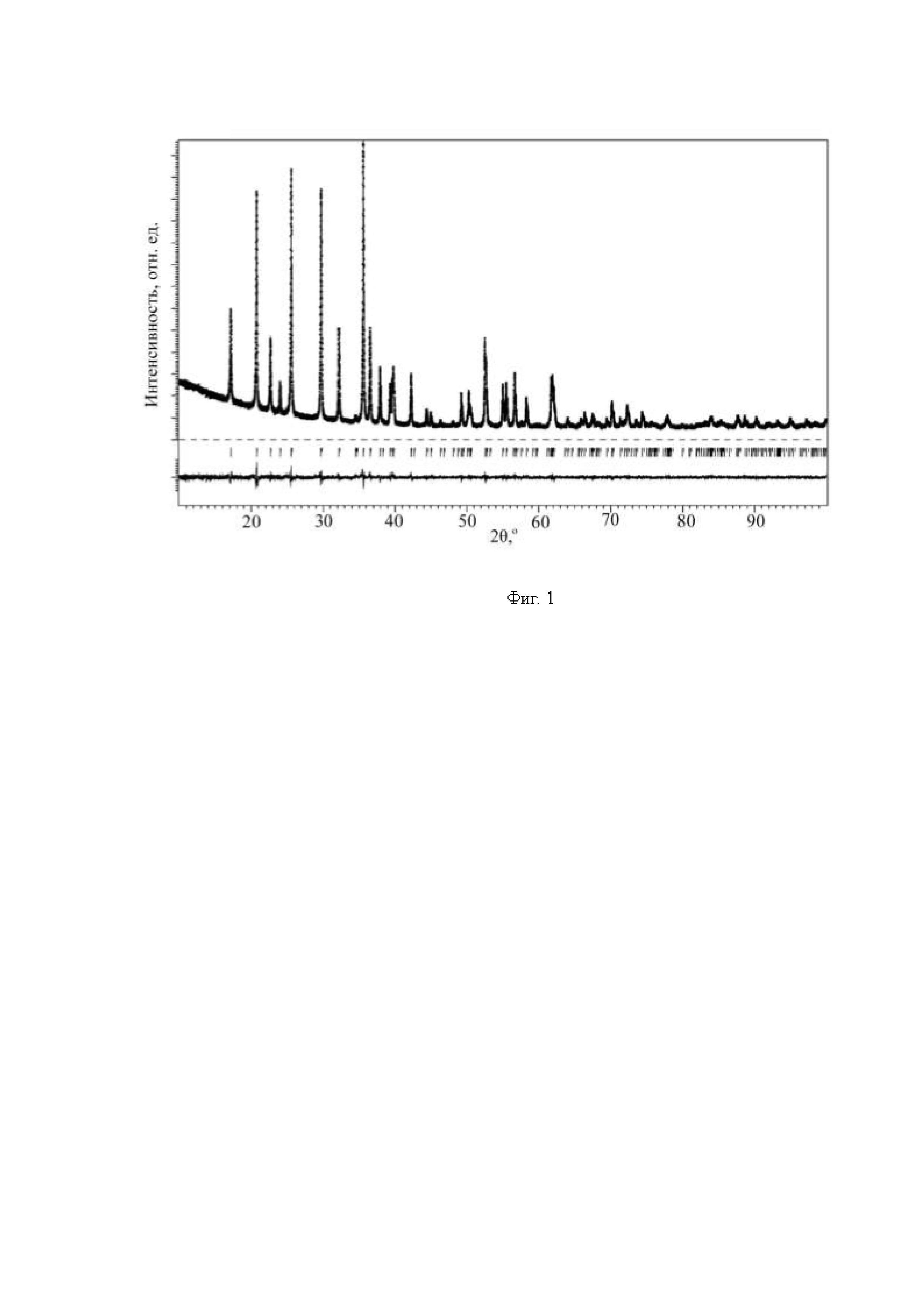
На Фиг. 1 представлена экспериментальная, расчетная и разностная дифрактограмма после уточнения методом Ритвельда кристаллической структуры образца Li1.04Fe0.96PO4, полученного из прекурсора Li3-zNazPO4, где z=0.
На Фиг. 2а представлена зарядо-разрядная гальваностатическая кривая для этого образца. На Фиг. 2б - зависимость разрядной емкости от номера цикла при заряде и разряде при плотности тока 170 мА/г для этого образца
На Фиг. 3а представлена зависимость разрядной емкости при заряде-разряде в режиме «быстрый заряд-медленный разряд» и «медленный заряд - быстрый разряд» для этого образца. На Фиг.36 зависимость среднего напряжения заряда и разряда от плотности тока.
На Фиг. 4 представлены дифрактограммы образцов, отобранных в ходе гидротермального синтеза Li1.04Fe0.96PO4.
На Фиг. 5а представлены дифрактограммы прекурсоров состава Li3-zNazPO4, z=0, 0.5, 1, 1.5, 2. На Фиг. 5б представлены дифрактограммы образцов Li1+xFe1-yPO4, полученных из прекурсоров тех же составов.
На Фиг. 6 представлены зарядо-разрядные гальваностатические кривые для образцов Li1+xFe1-yPO4, полученных из прекурсоров состава Li2.5Na0.5PO4 (кривые 1), LiNa2PO4 (кривые 2) и Li1.1Na1.9PO4 (кривые 3).
Осуществление изобретения
В настоящем изобретении выражения «содержит» и «включает» и их производные используются взаимозаменяемо и понимаются как неограничивающие, т.е. допускающие присутствие/использование других компонентов, стадий, условий и т.п., помимо тех, что перечислены в явном виде. Напротив, выражения «состоит из» и «составлен из» и их производные предназначены для указания на то, что перечисленные компоненты, стадии, условия и т.п.являются исчерпывающими.
В случае, когда какие-то признаки изобретения раскрыты в настоящем документе для одного варианта осуществления, эти признаки также могут быть использованы и во всех других вариантах осуществления изобретения, при условии, что это не противоречит смыслу изобретения.
В рамках настоящего изобретения термины в единственном числе охватывают также и соответствующие термины во множественном числе, и наоборот, при условии, что из контекста явно не следует иное.
За исключением экспериментальной части описания, все численные значения, выражающие какие-либо количества и условия в настоящем изобретении, являются приближенными, и их следует читать, как предваряемые термином «приблизительно» или «около», даже если эти термины и не приводятся в явном виде. Напротив, в экспериментальной части описания все численные величины приведены настолько точно, насколько это возможно, однако следует понимать, что любая экспериментально определенная величина по природе своей несет в себе некоторую погрешность. Таким образом, все численные величины, приведенные в экспериментальной части описания, следует воспринимать с учетом существования указанной экспериментальной погрешности и, по меньшей мере, с учетом количества приведенных значащих цифр и стандартных методик округления.
Под «электродной массой» в настоящем изобретении понимается активный материал, используемый в комбинации с электропроводящими добавками, связующими и, при необходимости, другими вспомогательными веществами для получения электродов литий-ионных аккумуляторов.
На стадии а) способа по настоящему изобретению получают осадок общего состава Li3-zNazPO4. Эту стадию осуществляют путем внесения в водный растворитель необходимых количеств источников ионов Li+, Na+, РО43- и по меньшей мере одного органического сорастворителя.
В настоящем изобретении в качестве источника ионов Li+ могут быть использованы гидроксид лития (LiOH), гидрат LiOH (LiOH*H2O) или соли лития или их гидраты, в том числе водные растворы этих веществ. Соли лития могут быть выбраны из известных специалистам органических и неорганических солей лития, таких как хлорид лития, бромид лития, сульфат лития, нитрат лития, ацетат лития и т.п.Также одним из источников лития может выступать дигидрофосфат лития (LiH2PO4) или его водный раствор. В предпочтительном варианте осуществления в качестве источника ионов Li+ используют LiOH или LiOH*H20.
В настоящем изобретении в качестве источника ионов Na+могут быть использованы гидроксид натрия (NaOH), или соли натрия или их гидраты, в том числе водные растворы этих веществ. Соли натрия могут быть выбраны из известных специалистам органических и неорганических солей натрия, таких как хлорид натрия, бромид натрия, сульфат натрия, нитрат натрия, ацетат натрия и т.п. Также одним из источников лития может выступать дигидрофосфат натрия (NaH2PO4) или его водный раствор. В предпочтительном варианте осуществления в качестве источника ионов Na+ используют NaOH.
В настоящем изобретении в качестве источника ионов РО43- могут быть использованы фосфорная кислота (Н3РО4) или дигидрофосфат лития (LiH2PO4), или дигидрофосфат натрия (NaH2PO4), в том числе их водные растворы.
В качестве органического сорастворителя в настоящем изобретении можно использовать органические растворители, имеющие одну, две или более гидроксильных групп (т.е. одноатомные и многоатомные спирты), а также их смеси. Предпочтительными органическими растворителями являются одноатомные или многоатомные спирты, включающие от 2 до 8 атомов углерода, а также их смеси. Примерами органических растворителей, подходящих для использования в настоящем изобретении, являются этиловый спирт, бензиловый спирт, этиленгликоль, пропиленгликоль и т.п., а также их смеси.
Количество органического сорастворителя в настоящем изобретении выбирают таким образом, чтобы массовое содержание сорастворителя в реакционной смеси составляло от 20% до 80%. В предпочтительном варианте осуществления массовое содержание сорастворителя в реакционной смеси составляет от 30% до 70%, например от 40 до 60%.
На стадии б) заявляемых способов в реакционную смесь, полученную на стадии а), вносят:
- по меньшей мере одно соединение, которое является источником катионов Fe2+, мольное количество источников катионов Fe к мольному количеству Li3-zNazPO4 составляет от 0,9:1 до 1,1: 1.
В предпочтительном варианте осуществления указанные компоненты вносят в смесь, полученную на стадии а) при перемешивании.
В настоящем изобретении соединениями, являющимися источниками катионов Fe2+, являются по крайней мере одно соединение, выбранное из группы: соли железа или гидраты таких солей, в том числе водные растворы этих веществ. В предпочтительном варианте осуществления соли железа содержат Fe(II), однако возможно также использование солей железа в других степенях окисления, при условии, что в раствор также добавляются восстановители, переводящие железо в степень окисления +2. Более того, в предпочтительном варианте осуществления восстановитель может добавляться и к солям Fe(II) с целью поддержания катионов железа, марганца и/или кобальта в степени окисления +2. В качестве восстанавливающего агента в настоящем изобретении могут быть использованы различные известные специалистам восстанавливающие агенты, например аскорбиновая кислота, щавелевая кислота, сульфат гидразина и т.п.
В качестве примера подходящих соединений, являющихся источниками ионов Fe2+, можно привести сульфат железа(II), нитрат железа(II), хлорид железа(II), бромид железа(II), ацетат железа(II) и т.д., а также гидраты этих солей.
Количество соединения(й), являющегося(ихся) источником(ами) катионов Fe2+, выбирается таким образом, чтобы сумма мольных количеств катионов Fe в смеси была приблизительно равна мольному количеству ионов PO43-. Например, отношение мольных количеств катионов Fe к мольному количеству Li3-zNazPO4 может лежать в диапазоне от 0.9:1 до 1.1:1, предпочтительно от 0.95:1 до 1.05:1, наиболее предпочтительно это отношение может быть равно 1:1.
После смешивания источников катионов Fe2+ с частицами Li3-zNazPO4 (0≤z<2), реакционную смесь нагревают при перемешивании в атмосфере инертного газа в герметичном автоклаве при температуре в диапазоне 190-210°С.
Под инертным газом в настоящем изобретении понимаются известные специалистам инертные газы, т.е. газы, не вступающие ни в какие в химические реакции в условиях, при которых осуществляются обсуждаемые способы. Примерами таких инертных газов могут быть азот, аргон и т.п.
Время нагрева реакционной смеси составляет по меньшей мере 1 час. В одном предпочтительном варианте осуществления нагрев осуществляют в течение по меньшей мере 2 часов, например в течение по меньшей мере 3 часов. Верхняя граница для диапазона подходящих времен нагрева в настоящем изобретении специально не ограничивается, но предпочтительно составляет менее 24 часов, более предпочтительно менее 6 часов, например, менее 4 часов.
В настоящем изобретении при смешивании реагентов и при сольвотермальной обработке используется механическое перемешивание реакционной смеси, что позволяет добиться хорошей однородности получаемых порошков.
Кроме того, в некоторых вариантах осуществления настоящего изобретения с целью обеспечения привлекательных электрохимических характеристик синтезируемого электродного материала в способ получения может быть включена стадия отжига с источником углерода в качестве дополнительной стадии синтетического процесса. В ходе такой дополнительной стадии в) отжига вещество, полученное на стадии б) способа по изобретению, выделяют, смешивают с источником углерода и отжигают при 600-700°С в течение по меньшей мере 1 часа в атмосфере инертного газа, в результате чего получают композитный материал, описывающийся формулой Li1+xFe1-yPO4/C, т.е. композитный материал, содержащий частицы Li1+xFe1-yPO4 и углерод.
Источником углерода на стадии отжига способа по изобретению могут служить известные специалистам источники углерода, такие как сажа, графит, углеродные нанотрубки, графен, восстановленный оксид графита и/или органические соединения, такие как аскорбиновая кислота, лимонная кислота, уксусная кислота, глюкоза, сахароза и т.п.
Время отжига, как уже было указано, составляет по меньшей мере 1 час. В предпочтительно варианте осуществления время отжига составляет по меньшей мере 2 часа, например по меньшей мере 3 часа. Верхняя граница для диапазона подходящих времен отжига в настоящем изобретении специально не ограничивается, но предпочтительно составляет менее 10 часов, более предпочтительно менее 6 часов, например менее 4 часов.
Содержание углерода в композитном материале Li1+xFe1-yPO4/C после отжига может составлять от 1 до 30 масс. %, предпочтительно от 1 до 20 масс. %, более предпочтительно от 1 до 10 масс. %, наиболее предпочтительно от 3 до 7 масс. %, например приблизительно 5 масс. %.
Для приготовления электродной массы (активной массы) катода литий-ионного аккумулятора, активный материал или композитный активный материал литий-ионного аккумулятора, полученный одним из способов по изобретению, смешивают с одной или несколькими электропроводящими добавками, одним или несколькими связующими и, при необходимости, с другими добавками, традиционно используемыми в данной области техники.
В качестве электропроводящей добавки могут использоваться, например, различные формы углерода, в т.ч. графит, сажа, углеродные нанотрубки и фуллерен, проводящие полимерные материалы (полианилин, полипиролл, полиэтилендиокситиофен) и т.п. Содержание электропроводящих добавок в электродной смеси по изобретению может варьироваться от 1 до 20 масс. %.
В качестве связующего могут быть использованы, например, раствор поливинилиденфторида в N-метилпирролидоне или суспензия перфторполиэтилена (фторопласт, тефлон) в воде. Содержание связующего в электродной смеси может варьироваться от 1 до 20 масс. %.
Катод для литий-ионного аккумулятора может быть изготовлен из электродного массы по изобретению известными в данной области техники методами.
Далее настоящее изобретение будет описано более подробно с приведением конкретных примеров осуществления. Следует понимать, что данные примеры приведены исключительно для иллюстрации изобретения, и они не ограничивают объем изобретения.
Примеры
Общая методика
Материал Li1+xFe1-yPO4 получают сольвотермальным синтезом с последующим отжигом для получения углерод содержащего композита Li1+xFe1-yPO4/C.
В рамках сольвотермального синтеза сначала готовят прекурсор (Li3-zNazPO4) смешением водных растворов LiOH, NaOH и Н3РО4 в мольном соотношении (3-z):z:1 (0≤z<2). На стадии получения прекурсора добавляют органический растворитель с целью получения его содержания в смеси 20-80 масс. %. Затем в реакционную смесь добавляют соль Fe2+ в необходимом количестве, а также восстанавливающий агент, например аскорбиновую кислоту, с целью поддержания степени окисления катионов железа +2 в ходе синтеза. Реакционную смесь помещают в гидротермальный реактор, который продувают аргоном, герметично закрывают и выдерживают при температуре 190-210°С в течение 1-3 часов при интенсивном перемешивании на магнитной мешалке.
В результате проведения синтеза получают материал, представляющий собой соединение формулы Li1+xFe1-yPO4, кристаллизующееся в ромбической сингонии с параметрами элементарной ячейки, которые несколько варьируются в зависимости от элементного состава 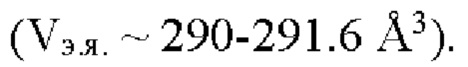
Для получения углеродсодержащего композита Li1+xFe1-yPO4/C готовят смесь Li1+xFe1-yPO4 и источника углерода. Полученную смесь тщательно перетирают в шаровой мельнице или ступке, а затем отжигают при 600-700°С в течение 1-10 часов в атмосфере аргона или азота. После осуществления отжига получают композит материала Li1+xFe1-yPO4 с углеродом (доля углерода приблизительно 5 масс. %).
Образцы электродного материала Li1+xFe1-yPO4 были охарактеризованы стандартным для данной области техники набором физико-химических методов исследования. Фазовый состав Li1+xFe1-yPO4 был установлен методом рентгенофазового анализа (рентгеновский дифрактометр Panalytical Aeris, излучение CuKα). Все полученные образцы Li1+xFe1-yPO4 оказались однофазными. Кристаллическая структура образца Li1.04Fe0.96PO4 уточнена методом Ритвельда по рентгеновским порошковым данным. Химический состав (соотношение Li:Fe:P) образца Li1.04Fe0.96PO4 был подтвержден методами атомно-эмиссионной спектроскопии с индуктивно связанной плазмой (масс-спектрометр ICP-AES Agilent 720). Доля катионов Fe3+ в образце Li1.04Fe0.96PO4 определялась с помощью Мессбауэровской спектроскопии (спектрометр MS-1104Em, работающий в режиме постоянных ускорений). Химический состав (соотношение Na:Fe:P) всех образцов подтвержден локальным рентгеноспектральным анализом (сканирующий электронный микроскоп JEOL JSM6490 LV с рентгеновским спектрометром INCA X-Sight). Морфология образцов была изучена с помощью сканирующей электронной микроскопии (сканирующий электронный микроскоп JEOL JSM6490 LV). Полученные частицы материала имеют форму пластин с линейными размерами 300-700 нм, толщиной 50-150 нм. Содержание углерода в образцах Li1+xFe1-yPO4/С, установленное методом термогравиметрии (термический анализатор Netzsch Jupiter STA-449, в атмосфере воздуха), не превышает 5 масс. %.
Для приготовления электродной массы полученное соединение тщательно смешивают с одной или несколькими электропроводящими добавками и одним или несколькими связующими. В качестве электропроводящей добавки могут использоваться различные формы углерода, в т.ч. графит, сажа, углеродные нанотрубки, фуллерен, проводящие полимерные материалы (полианилин, полипиролл, полиэтилендиокситиофен), в роли связующего используется поливинилиденфторид в N-метилпирролидоне или суспензия перфторполиэтилена (фторопласт, тефлон) в воде. Содержание электропроводящих добавок может варьироваться от 3 до 20% масс., связующего - так же от 3 до 20% масс.
Электрохимические испытания образцов Li1+xFe1-yPO4/С проводили методом гальваностатического циклирования в двухэлектродной ячейке относительно металлического лития в качестве анода с 1М раствором LiPF6 в этиленкарбонате:диметилкарбонате (1:1 по объему) в качестве электролита. В качестве сепаратора использовалось борсиликатное стекловолокно. Электрохимическая ячейка собиралась в боксе с атмосферой аргона MBraun. Электродную массу катода готовили смешением в ступке 80 масс. % активного материала или композитного активного материала по изобретению, 10 масс. % раствора поливинилидендифторида (ПВдФ) в N-метилпирролидоне и 10 масс. % ацетиленовой сажи (Timcal Super-C). Полученную пасту равномерно наносят на алюминиевую подложку (токосъемник), сушат и прокатывают на вальцах, затем вырезают электроды диаметром 16 мм, которые взвешивают и окончательно высушивают при пониженном давлении (10-2 атм) при 110°С в течение 12 часов для удаления остаточной воды и растворителя. Гальваностатические измерения полученных катодных материалов проводили на потенциостате Elins Р20Х8 (программное обеспечение ES8) при комнатной температуре.
Пример 1.
Активный материал катода Li1+xFe1-yPO4 синтезируют сольвотермальным методом с последующим отжигом с источником углерода.
Первоначально получают Li3-zNazPO4 где z=0, т.е. Li3PO4. Для этого исходный реагент LiOH*H20 в количестве 1.26 г растворяют в 10 мл дистиллированной воды при постоянном перемешивании при 80°С в автоклаве, затем к раствору добавляют 10 мл этиленгликоля и 1.15 г 85 масс. % Н3РО4. Образовавшийся осадок выдерживают в течение 1 часа. Далее, к осадку добавляют 0.2 г аскорбиновой кислоты и 2.78 г FeSO4*7H20. Автоклав продувается азотом и запечатывается. После запечатывания автоклав выдерживается в течение 3 часов при температуре 200°С и постоянном перемешивании.
По окончании процесса содержимое автоклава извлекают и промывают 4 раза дистиллированной водой с последующим центрифугированием для очистки от растворимых примесей. Полученный порошок сушат на воздухе.
Дифрактограмма полученного материала Li1+xFe1-yPO4 показана на Фиг. 1.
Для получения углерод-проводящего покрытия полученный Li1+xFe1-yPO4 смешивают с глюкозой (в массовом соотношении 0.8:0.2) и тщательно перетирают в ступке под спиртом или в планетарной мельнице. Полученную смесь отжигают в токе аргона в течение 3 часов при температуре 650°С.
На Фиг. 2 и 3 приведены результаты электрохимического тестирования Li1+xFe1-yPO4/С в литий-ионной полуячейке в интервале потенциалов 2,2-4,3 В отн. Li/Li+, при комнатной температуре при различных скоростях разряда и разряда. Электрохимическая разрядная емкость такого материала при плотности тока 17 мА/г составляет 153 мАч/г. Электрохимическая разрядная емкость такого материала при плотности тока заряда 1700 мА/г составляет 141 мАч/г.
Пример 2.
Композитный активный материал Li1+xFe1-yPO4/С синтезируют по схеме, описанной в примере 1, только в качестве исходных компонентов используют Li3-zNazPO4 где z=0.5, т.е. Li2.5Na0.5PO4 в количестве, соответствующем количеству молей катионов железа. В качестве источников Li и Na используют LiOH*H20 и NaOH в количествах 1.05 и 0.2 г, соответственно. Количества остальных реагентов и порядок их смешивания не отличается от описанного в Примере 1.
Дифрактограмма материала Li1+xFe1-yPO4, полученного таким методом, приведена на Фиг. 5б.
Электрохимическая разрядная емкость композита Li1+xFe1-yPO4/С при плотности тока 17 мА/г составляет 150 мАч/г.
Пример 3.
Композитный активный материал Li1+xFe1-yPO4/С синтезируют по схеме, описанной в примере 2, только в качестве исходных компонентов используют Li3-zNazPO4 где z=1.9, т.е. Li1.1Na1.9PO4 в количестве, соответствующем количеству молей катионов железа.
Дифрактограмма материала Li1+xFe1-yPO4, полученного таким методом, приведена на Фиг. 5б.
Электрохимическая разрядная емкость композита Li1+xFe1-yPO4/С при плотности тока 17 мА/г составляет 140 мАч/г.
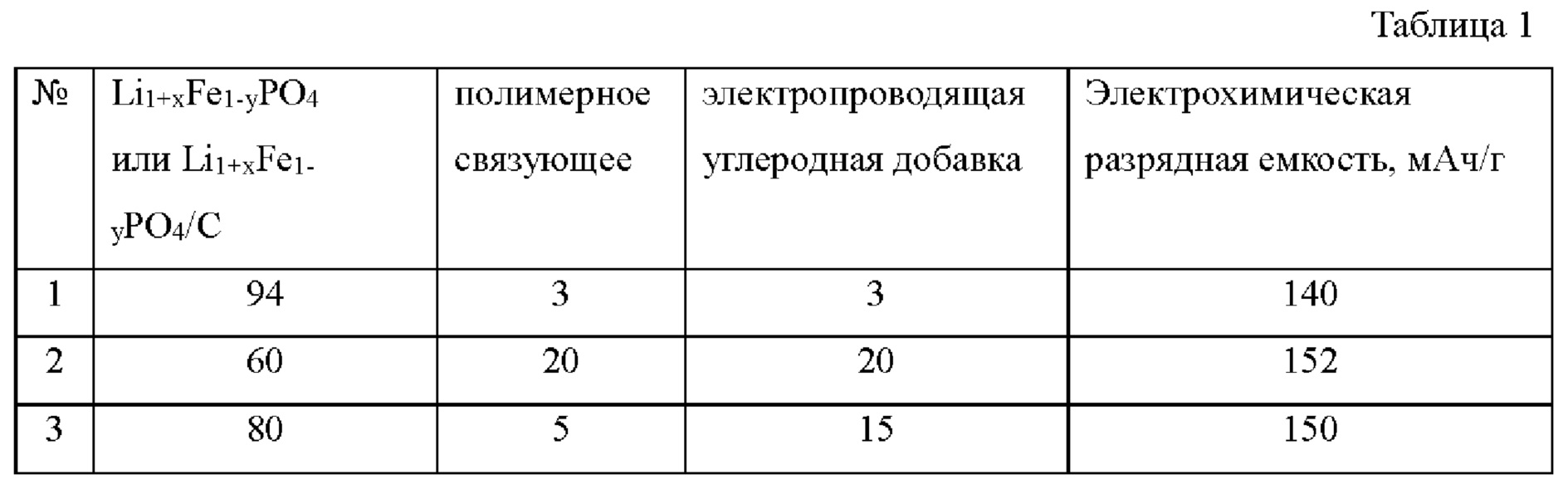
В таблице 1 представлена электрохимическая разрядная емкость при плотности тока 17 мА/г в зависимости от количественного содержания заявленных компонентов в заявленной электродной массе. Результаты актуальны для различные сочетания заявленных веществ, применяемых в качестве связующего и различные заявленные вещества, применяемые в качестве электропроводящей углеродной добавки.