Результат интеллектуальной деятельности: Интерполимерный носитель для пероральных систем контролируемой доставки активных фармацевтических ингредиентов
Вид РИД
Изобретение
Изобретение относится к медицине, в частности фармации, и касается носителя для пероральной системы с контролируемой доставкой лекарственных веществ в заданные отделы желудочно-кишечного тракта (ЖКТ) на основе интерполимерного комплекса (ИПК) с участием (мет)акриловых сополимеров. Изобретение может быть использовано в фармацевтической промышленности при получении лекарственных препаратов с контролируемой пероральной доставкой различных классов активных фармацевтических ингредиентов (АФИ) в заданные отделы желудочно-кишечного тракта (ЖКТ).
Задачей предлагаемого изобретения является разработка носителя для пероральной системы с контролируемой доставкой активных фармацевтических ингредиентов на основе интерполимерного комплекса, полученного при взаимодействии химически комплементарных сополимеров диметиламиноэтилметакрилата и эфиров метакриловой кислоты и метилметакрилата, метакриловой кислоты и этилакрилата в среде органического растворителя (этанол, изопропанол, метанол, ацетон, тетрагидрофуран и др.). Продукт характеризуется улучшенными фармакокинетическими параметрами и технологическими характеристиками. В зависимости от условий синтеза комплекса можно получить на его основе интерполимерные носители, обеспечивающие высвобождение АФИ как в верхних отделах ЖКТ (ципрофлоксацин, ацикловир, фуросемид, каптоприл, диазепам, метформин и др.), так и в толстом кишечнике (диклофенак натрия, окспренолол, метопролол, нифедипин, ибупрофен, индометацин, изосорбид, и др.), а также носители для систем с классическим пролонгированным высвобождением активных веществ (теофиллин, парацетамол, пироксикам и др.).
Известны носители на основе интерполимерных комплексов линейной поли(мет)акриловой кислоты с полиэтиленгликолем или поливинилпирролидоном, стабилизированные кооперативной системой водородных связей (А.с. №895036, C08F 291/06, 1981).
Известен способ получения протививовоспалительного средства пролонгированного действия на основе диклофенака натрия, где в качестве полимерного носителя используют ИПК с участием редкосшитой полиакриловой кислоты (Патент РФ №2070034, МПК А61К 9/22, А61К 31/135, 1996). Известны также способы получения пролонгированных антиаритмического препарата этмозина и антиангинального препарата изосорбидадинитрата, где в качестве носителя используется ИПК между редкосшитой полиакриловой или полиметакриловой кислотой и полиэтиленгликолем (Патент РФ №2267321 С1 МПК А61К 31/5415 А61К 9/22 А61Р 9/06,2006; патент РФ №2267318 С1 МПК А61К 31/34 А61К 9/22 А61Р 9/06, 2006), способ получения антиангинального пролонгированного препарата триметазидина гидрохлорида на основе интерполимерного комплекса (ИПК) между полиакриловой кислотой и полиэтиленгликолем (Патент РФ №2435584 С2 МПК А61К 31/495 А61К 9/22 А61К 9/36 А61Р 9/10, 2011). Во всех этих случаях в качестве носителей использовались ИПК, стабилизированные системой водородных связей, недостатком которых является то, что они применимы в желудочно-нерастворимых пероральных системах с достаточно быстрым высвобождением АФИ при достижении верхних отделов кишечника.
Известна пероральная система доставки АФИ в область кишечника, где в качестве носителя предлагается интерполиэлектролитный комплекс на основе редкосшитой полиакриловой кислоты и сополимера диметиаминоэтилметакрилата и нейтральных эфиров метакриловой кислоты (Патент РФ №2445118 С2 МПК А61К 47/34 C08G 81/02 А61К 9/22, 2012; патент РФ №2467766 С1 МПК А61К 47/30 А61К 31/196 А61К 31/405, 2012). Данные носители обеспечивают как классическое высвобождение теофиллина, так и высвобождение диклофенака натрия и индометацина в дальних отделах желудочно-кишечного тракта.
В качестве прототипа для данного изобретения использовали поликомплекс, образованный желудочно-растворимым Eudragit® E100 (сополимер на основе диметиламиноэтилметакрилата и нейтральных эфиров метакриловой кислоты) и кишечнорастворимым Eudragit® L100 (сополимер на основе метакриловой кислоты метилметакрилата), который охарактеризован с целью возможности использования его в качестве носителя лекарственных веществ в таблетированных лекарственных формах (R.I. Moustafine, T.V. Kabanova, V.A. Kemenova, and G. Van den Mooter, J. Control. Release, 103, 191-198 (2005)). Синтез данного поликомплекса осуществлялся смешением растворов полимеров при фиксированном значении рН (5,5 или 6,0). В результате были получены и охарактеризованы поликомплексы, обеспечивающие пролонгированное высвобождение лекарственных веществ (ЛВ). Недостатком данных носителей является сложность воспроизведения получения поликомплекса в промышленных условиях за счет использования водных растворов полимеров и необходимости доведения рН растворов до определенного значения.
Раскрытие изобретения.
Для решения задачи разработан носитель для пероральной системы контролируемой доставки АФИ (ацикловир, пропранолол, метронидазол, диклофенак натрия, ибупрофен, индометацин, теофиллин и др.) на основе интерполимерных комплексов, полученных при взаимодействии химически комплементарных сополимеров диметиламиноэтилметакрилата и эфиров метакриловой кислоты и метилметакрилата, метакриловой кислоты и этилакрилата в органических растворителях (этанол, изопропанол, метанол, ацетон, тетрагидрофуран и др.). В зависимости от условий получения носителей можно получить матричные системы с доставкой АФИ в толстый кишечник, либо системы с внутрижелудочной доставкой, либо системы с пролонгированным высвобождением АФИ.
Заявленный интерполимерный носитель обладает заданными биофармацевтическими свойствами (обеспечение высвобождения активного вещества в заданном отделе ЖКТ), а также необходимыми для промышленного производства технологическими свойствами (сыпучесть, прессуемость), что достигается рядом подобранных условий получения интерполимерного комплекса (концентрация исходных сополимеров, их соотношение, выбор растворителя).
Изобретение подтверждается следующими графическими материалами, на которых представлено:
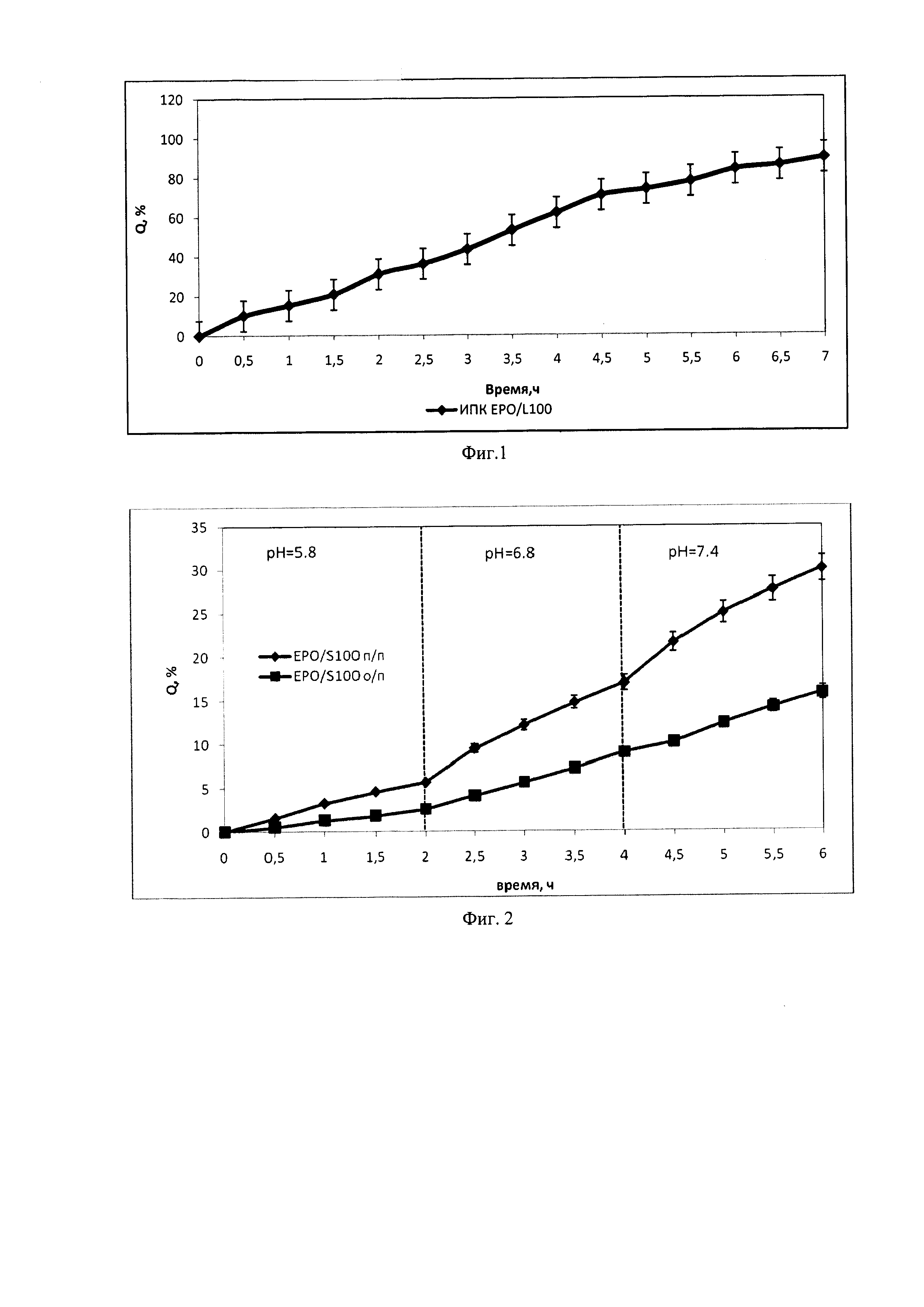
На фиг. 1 - высвобождение пропранолола в условиях нахождения в желудке из матриц, содержащих ИПК Eudragit® EPO/L100.
На фиг. 2 - высвобождение диклофенака натрия в условиях продвижения по ЖКТ из матриц, содержащих ИПК Eudragit® EPO/S100.
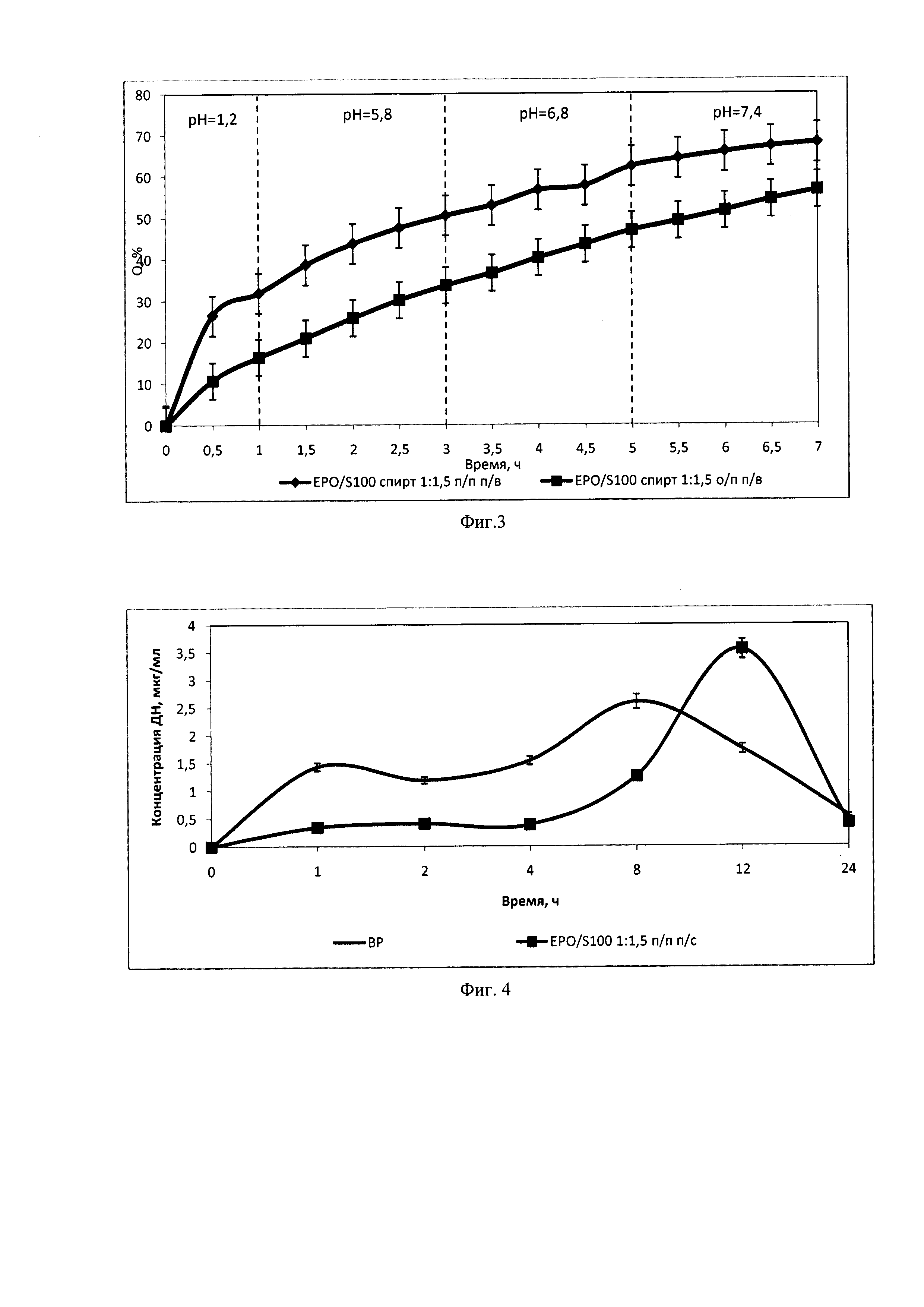
На фиг. 3 - высвобождение теофиллина в условиях продвижения по ЖКТ из матриц, содержащих ИПК Eudragit® EPO/S100.
Изобретение иллюстрируется следующими примерами.
Пример 1. Были получены носители на основе ИПК Eudragit® EPO/(L100, S100, L100-55) путем смешения растворов сополимеров в органическом растворителе (этиловый спирт, смесь изопропанол-ацетон (60-40)) с концентрацией каждого раствора 0,03 М. Смешение растворов проводили таким образом, чтобы молярное соотношение сополимеров ЕРО:L100 составило 1:2, EPO:S100 - 1:1,5 и ЕРО:L100-55 - 1:2 при постоянном перемешивании на магнитной мешалке. После выпадения и отделения осадка центрифугированием, осадок промывали водой очищенной до удаления запаха растворителя и высушивали в вакуум-сушильном шкафу при температуре 40°С до постоянной массы. Измельчали полученный продукт до размера частиц 150-500 мкм. Методами ИК-спектроскопии, элементного органического анализа, дифференциальной сканирующей калориметрии с моделируемой температурой и газовой хроматографии доказали, что получаемые интерполимерные комплексы представляют собой индивидуальные соединения, не содержащие примесей исходных веществ их синтеза (индивидуальных сополимеров) и остаточных органических растворителей.
Путем смешения ИПК с пропранололоми карбонатом натрия в соотношении 1:1:0,5 по массе прессовали таблетки массой 150 мг (80 мг ИПК, 40 мг ЛВ и 30 мг карбоната натрия) и диаметром 8 мм.
Высвобождение пропранолола определяли в условиях нахождения в желудке в 0,1 н растворе хлористоводородной кислоты со значением рН раствора 1,2 в течение 7 часов на приборе ErwekaDT 626 (Германия) методом 2 согласно ГФ XIII «вращающаяся лопасть» при следующих условиях: объем среды растворения - 900 мл; скорость вращения лопасти - 50 об/мин; температура среды - 37±0,5°С. Концентрацию лекарственного вещества определяли УФ-спектрофотометрически. На основании полученных данных строили кривые Q-t, где Q - количество лекарственного вещества, t - время. Профили высвобождения пропранолола представлены на фигуре 1 и показывают классическое пролонгированное высвобождение лекарственного вещества в условиях имитации нахождения в желудке, таким образом обеспечивается высвобождение пропранолола в течение длительного времени в желудке, что может быть использовано для систем внутрижелудочной пролонгированной доставки лекарственных веществ.
Пример 2. Получали носители на основе ИПК Eudragit® EPO/(L100, S100, L100-55) как описано в примере 1. Путем смешивания ИПК с диклофенаком натрия в соотношении 1:2 по массе прессовали таблетки массой 150 мг (100 мг ЛВ и 50 мг ИПК) и диаметром 8 мм. Высвобождение диклофенака натрия определяли в условиях продвижения по желудочно-кишечному тракту на приборе ErwekaDT 626 (Германия) методом 1 согласно ГФ XIII «вращающаяся корзинка» в течении 7 часов в различных средах: 1 час в среде 0,1 н хлористоводородной кислоты с рН=1,2; 2 часа в фосфатном буфере со значением рН=5,8; 2 часа в фосфатном буфере со значением рН=6,8 и 2 часа в фосфатном буфере со значением рН=7,4. Условия определения: объем среды растворения - 900 мл; скорость вращения корзинки - 100 об/мин; температура среды - 37±0,5°С. Концентрацию высвободившегося диклофенака натрия определяли УФ-спектрофотометрически. На основании полученных данных строили кривые Q-t, где Q - количество лекарственного вещества, t - время. Профили высвобождения диклофенака натрия из образцов ИПК Eudragit® EPO/S100, представленные на фигуре 2, показывают, что высвобождение лекарственного вещества происходит по «кишечному типу» с низким количеством высвобождающегося вещества в первых двух средах с последующим увеличением концентрации диклофенака натрия в средах, имитирующих дальние отделы ЖКТ (рН=6,8 и рН=7,4). Таким образом, полученные ИПК могут быть использованы как носители в системах с контролируемой доставкой АФИ в дальние отделы желудочно-кишечного тракта, в том числе и в толстый кишечник.
Пример 3. Получали матричные таблетки с теофиллином массой 150 мг и диаметром 8 мм путем прессования ИПК Eudragit® EPO/(L100, S100, L100-55) и теофиллина в соотношении 1:2 по массе (100 мг теофиллина и 50 мг ИПК). Высвобождение теофиллина определяли в условиях продвижения по желудочно-кишечному тракту на приборе ErwekaDT 626 (Германия) методом 1 согласно ГФ XIII «вращающаяся корзинка» в течении 7 часов в различных средах: 1 час в среде 0,1 н хлористоводородной кислоты с рН=1,2; 2 часа в фосфатном буфере со значением рН=5,8; 2 часа в фосфатном буфере со значением рН=6,8 и 2 часа в фосфатном буфере со значением рН=7,4. Условия определения: объем среды растворения - 900 мл; скорость вращения корзинки - 100 об/мин; температура среды - 37±0,5°С. Концентрацию высвободившегося теофиллина определяли УФ-спектрофотометрически. На основании полученных данных строили кривые Q-t, где Q - количество лекарственного вещества, t - время. Профили высвобождения теофиллина из образцов ИПК Eudragit® EPO/S100 представлены на фигуре 3. ИПК обеспечивают замедленный профиль с постепенным во времени высвобождением ЛВ, что позволяет использовать данные ИПК в классических системах с пролонгированным высвобождением лекарственных веществ.
Пример 4. Определяли технологические свойства ИПК Eudragit® EPO/S100: сыпучесть, насыпную плотность и прессуемость в сравнении с индивидуальными сополимерами (Таблица 1).
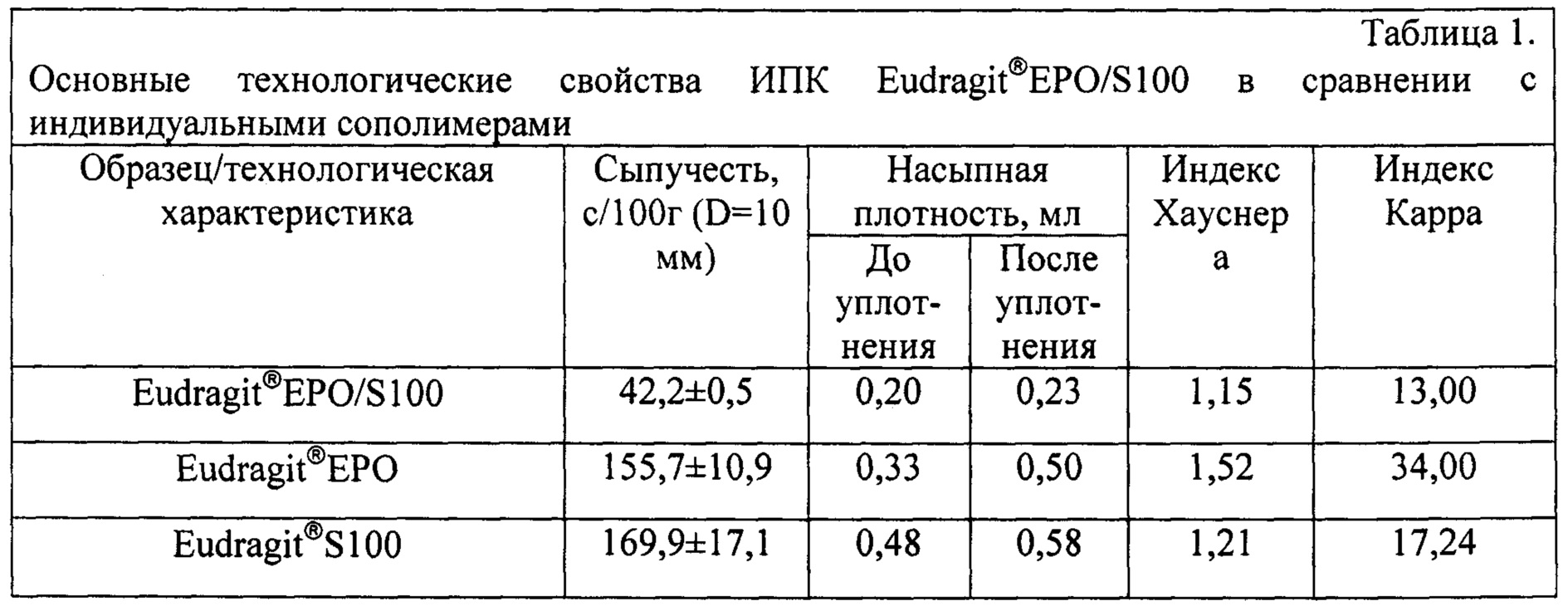
ИПК Eudragit® EPO/S100 обладает лучшей сыпучестью (время истечения 100 г порошка из воронки с диаметром отверстия 10 мм), а также лучшей сжимаемостью, а соответственно, и прессуемостью. Исходя из значений индексов Хауснера и Карра сжимаемость ИПК можно охарактеризовать как «хорошая», в то время как сжимаемость порошков индивидуальных сополимеров характеризуется как «средняя» для Eudragit® S100 и «очень плохая» для Eudragit® EPO. Таким образом, носители на основе ИПК обладают улучшенными технологическими характеристиками по сравнению с индивидуальными полимерами, что обеспечивает, наряду с упрощенной схемой синтеза данных носителей, их дальнейшее применение в промышленном производстве лекарственных форм.
Пример 5. Фармакологические исследования по определению «острой» токсичности и токсикологических характеристик полученных лабораторных образцов композиций ИПК проведены на 145 белых беспородных мышах-самцах массой 17-25 г. До начала экспериментов все животные содержались в стандартных условиях вивария с естественным световым режимом на полнорационной сбалансированной диете (ГОСТ Р 50258-92) с соблюдением Международных рекомендаций Европейской конвенции по защите позвоночных животных, используемых при экспериментальных исследованиях (1997), а также правил лабораторной практики при проведении доклинических исследований в РФ (ГОСТ З 51000.3-96 и 51000.4-96). Все исследования были согласованы с комитетом по этической экспертизе. Опытные образцы композиций и индивидуальные сополимеры сравнения вводили в дозах 1000, 2000 и 3000 мг/кг в желудок в крахмальной слизи с использованием специального зонда. Каждая доза вводилась 6 мышам. Одновременно контрольным группам из 6 мышей вводили крахмальную слизь в том же объеме. Проводили анализ картины общего действия (наличие угнетающего или возбуждающего действия со стороны центральной нервной системы, отличительные особенности в поведении в сравнении с животными контрольной группы). Результаты исследований показали, что при введении всех исследуемых доз поликомплексов животные оставались живы, и их поведение не отличалось от такового у контрольной группы. 3000 мг/кг - максимальная доза, которую можно было ввести экспериментальным животным, поэтому ЛД50 определить не удалось, что может свидетельствовать о безопасности поликомплексов.
Пример 6. Определение фармакокинетических параметров in vivo. Эксперимент проводили на 12 кроликах. Для исследования отбирали кроликов-самцов породы Шиншилла со средним весом 3.50 кг после ночного 12-часового голодания. Утром натощак животным вводили перорально 1 таблетку, содержащую 100 мг диклофенака натрия и 50 мг интерполимерного комплекса Eudragit® EPO/S100. Через 1; 2; 4; 8; 12 и 24 часа с момента введения таблетки у кроликов из краевой ушной вены отбирали пробы крови по 0,5 мл. Получали плазму путем центрифугирования в течение 20 мин при 5000 об/мин. К 0,2 мл сыворотки прибавляли 0,2 мл 0,1 н раствора хлористоводородной кислоты, встряхивали в течение 30 с. К смеси добавляли 3 мл хлороформа, встряхивали в течение 2 мин, центрифугировали в течение 10 мин при 5000 об/мин. После центрифугирования к 2,6 мл нижнего органического слоя добавляли 150 мкл 0,1 М раствора едкого натра, встряхивали 30 с, центрифугировали 10 мин при 5000 об/мин. После отстаивания в течение 10 мин отбирали 25 мкл верхнего щелочного реэкстракта. Хроматографировали на приборе LC-20 Prominence (Shimadzu, Япония) с УФ-детектором, подвижная фаза - этанол (96%):0.15 М раствор фосфата натрия : уксусная кислота. На фигуре 4 представлены кривые зависимости концентрации диклофенака натрия в плазме крови кроликов в зависимости от времени для препарата «Вольтарен ретард» (Novartis, Швейцария) и системы на основе ИПК Eudragit® EPO/S100. Согласно полученным результатам системы на основе ИПК обеспечивают иные фармакокинетические профили в сравнении с оригинальным препаратом «Вольтарен ретард» и системой-прототипом. Как и в эксперименте по высвобождению диклофенака натрия invitro система показала характерный «кишечный» характер поведения.