Результат интеллектуальной деятельности: ГЕТЕРОАРИЛЬНЫЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ТЕРАПЕВТИЧЕСКИХ ЛЕКАРСТВЕННЫХ СРЕДСТВ
Вид РИД
Изобретение
Область техники
[1] Данная заявка испрашивает преимущество приоритета согласно 119(e) U.S.C. по предварительной заявке на патент США № 62/212520, поданной 31 августа 2015 года, которая включена в данный документ посредством ссылки.
[2] Настоящее изобретение относится к новым гетероциклическим соединениям, обладающим ингибирующей активностью в отношении Mer-киназы, их стереоизомеру, их энантиомеру или их фармацевтически приемлемой соли, к применению для получения фармацевтических композиций, фармацевтическим композициям, содержащим их, способам лечения заболеваний с применением данных композиций.
Предпосылки создания изобретения
[3] Трансмембранные рецепторные тирозинкиназы (RTK) относятся к эволюционно консервативному семейству структурно связанных белков. Ген Mer является представителем семейства рецепторных киназ Tyro3/Axl/Mer (TAM) и протоонкогеном. Его аномальная экспрессия и активация обнаруживаются в связи с формами рака у человека, такими как формы аденомы гипофиза, формы лимфомы из клеток мантийной зоны и T-клеточный острый лимфобластный лейкоз.
[4] Сайт связывания АТФ является подобным для всех протеинкиназ. По этой причине сложно найти ингибитор, специфичный по отношению к Mer. Соединение-52, 2,6,9-трехзамещенный пурин, который занимает сайт связывания АТФ, фактически был первой молекулой, которая, как было обнаружено, обеспечивала успешное ингибирование Mer (J Struct Biol. 2009 Feb; 165(2): 88-96). Однако данный ингибитор обладает ограниченной активностью и недостаточной селективностью. Позднее было открыто несколько соединений, главным образом посредством модифицирования соединения-52, в том числе UNC-569, UNC-1062 и UNC-2025 (ACS Med Chem Lett. 2012 Feb 9;3(2):129-134, Eur J Med Chem. 2013 Jul;65:83-93, J Med Chem. 2014 Aug 28;57(16):7031-41).
[5] Целью настоящего изобретения является обеспечение реагентов и способов регуляции рецепторной тирозинкиназы Mer. Данная цель и другие цели настоящего изобретения достигаются с помощью одного или нескольких вариантов осуществления, описанных ниже.
Раскрытие сущности изобретения
Техническая задача
[6] Несколько ингибиторов Mer-киназы были описаны ранее, но они содержат фрагменты в остове, отличные от таковых согласно настоящему изобретению. Описываются высоко активные и селективные ингибиторы Mer-киназы на основе аминопиридинового или аминопиримидинового остовов.
[7] Настоящее изобретение относится к соединениям, способным к ингибированию активности Mer, при этом соединения являются пригодными для предупреждения и/или лечения рака и других заболеваний, связанных с иммунной системой, таких как инфекция и сепсис.
Решение задачи
[8] Новые ингибиторы Mer-киназы
[9] Настоящее изобретение относится к гетероциклическому соединению, представленному следующей формулой I, его стереоизомеру, его энантиомеру или его фармацевтически приемлемой соли:
[10] [формула I],
[11] 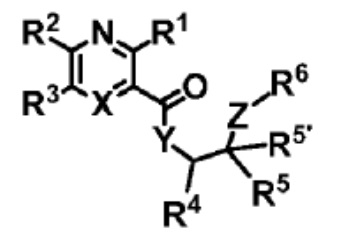 ,
,
[12] где
[13] X представляет собой CR7 или N;
[14] Y представляет собой CHR8, NR8 или O;
[15] Z представляет собой CH2, CH2O, C(=O), C(=O)O, C(=O)NH, NR8, NHC(=O), O или O(C=O);
[16] R1 представляет собой H, галоген, C1-3алкил, NHR8 или OR8;
[17] R2 представляет собой H, галоген, C1-4алкил, C1-2алкиларил, C1-2алкилгетероарил, C1-2алкилгетероциклил или -L-арил, при этом C1-2алкиларил, C1-2алкилгетероарил, C1-2алкилгетероциклил или -L-арил необязательно могут быть замещены одним или несколькими R9;
[18] R3 представляет собой H, галоген, CN, C1-3алкил, циклоалкенил, C2-6алкенил, арил, биарил, гетероарил, гетеробиарил, гетероциклил, C1-2алкиларил, C1-2алкилгетероарил или C1-2алкилгетероциклил, при этом арил, биарил, гетероарил, гетеробиарил, гетероциклил, C1-2алкиларил, C1-2алкилгетероарил или C1-2алкилгетероциклил необязательно могут быть замещены одним или несколькими R9;
[19] каждый из R4 и R5 независимо представляет собой H, C1-6алкил, C1-6алкокси, C3-10циклоалкил, C(=O)R6, C1-2алкиларил, арил; или
[20] R4 и R5 могут быть объединены друг с другом с образованием 3-7-членного циклического кольца или гетероциклического кольца, содержащего 1 или 2 из NR8, O или S, и циклическое или гетероциклическое кольцо необязательно может быть замещено 1 или 2 атомами галогена, C1-4алкилами или C1-4алкокси;
[21] R5' представляет собой H, или R5 и R5' могут быть объединены друг с другом с образованием карбонила;
[22] R6 представляет собой H, C1-4алкил, C1-6алкокси, -NR15R16, арил, биарил, гетероарил, гетеробиарил, гетероциклил, C1-2алкиларил, C1-2алкилгетероарил, C1-2алкилгетероциклил, C1-2алкилбиарил, -L-арил или -L-биарил, при этом C1-4алкил, арил, биарил, гетероарил, гетеробиарил, гетероциклил, C1-2алкиларил, C1-2алкилгетероарил, C1-2алкилгетероциклил, C1-2алкилбиарил, -L-арил или -L-биарил необязательно могут быть замещены одним или несколькими R9;
[23] R7 представляет собой H, галоген или C1-3алкил;
[24] R8 представляет собой H, C1-6алкил, C1-4фторалкил, C1-4гидроксиалкил, C1-3алкиларил или C(=O)R10, при этом C1-6алкил или C1-3алкиларил необязательно может быть замещен одним или несколькими R9;
[25] если Z представляет собой NR8, то R8 и R6 могут быть объединены друг с другом с образованием 3-7-членного гетероциклического кольца, содержащего 1-2 гетероатома N или 0-2 гетероатома O;
[26] R9 представляет собой галоген, гидроксил, -CN, -NO2, -COOH, -(C=O)H, C1-6алкил, C2-6алкенил, C2-6алкинил, C3-10циклоалкил, C1-4гидроксиалкил, C1-6алкокси, циклоалкенил, арил, гетероциклил, гетероарил, -NR15R16, -L-NR15R16, -L-COOR17, -L-алкил, -L-C3-10циклоалкил, -L-гетероциклил, -L-гетероарил или -L-арил, при этом C1-6алкил, C2-6алкенил, C2-6алкинил, C3-10циклоалкил, C1-4гидроксиалкил, C1-6алкокси, циклоалкенил, арил, гетероциклил, гетероарил, -L-алкил, -L-C3-10циклоалкил, -L-гетероциклил, -L-гетероарил или -L-арил могут быть замещены галогеном, гидроксилом, -CN, -NR15R16, C1-6алкилом, C3-10циклоалкилом, C1-4гидроксиалкилом, C2-6алкенилом, арилом, гетероциклилом, -L-гетероциклилом или -(CH2)l-C(=O)-NR15R16;
[27] R10 представляет собой C1-3алкил или C1-3алкиларил;
[28] каждый из R15 и R16 независимо представляет собой H, C1-6алкил, C3-10циклоалкил или SO2R17;
[29] R17 представляет собой H, C1-3алкил или C1-3алкиларил;
[30] L представляет собой C1-3алкил, C1-3алкил-O, C2-6алкинил, C3-10циклоалкил, -(CH2)l-C(=O)-(CH2)m-, C(=O)O, -(CH2)l-C(=O)NH-(CH2)m-, -(CH2)l-NHC(=O)-(CH2)m-, -(CH2)l-NH-(CH2)m-, NR8, -NH-C(=O)-CR15R16-NH-C(=O)-, NHC(=O), O, O(C=O)S, S(=O) или SO2; и
[31] каждый из l и m независимо представляет собой целое число от 0 до 2.
[32] В соответствии со вторым вариантом осуществления настоящего изобретения предусмотренное гетероциклическое соединение, представленное формулой I, представлено следующей формулой Ia:
[33] [формула Ia],
[34] 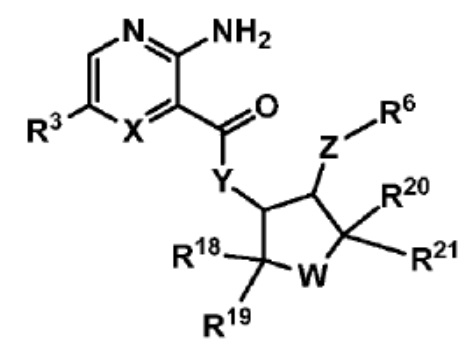 ,
,
[35] где
[36] X представляет собой CH или N;
[37] Y представляет собой NR8 или O;
[38] W представляет собой CH2, (CH2)2, NR11 или O;
[39] Z представляет собой CH2, CH2O, C(=O), C(=O)O, C(=O)NH, NR8, NHC(=O), O или O(C=O);
[40] R3 представляет собой H, галоген, CN, C1-3алкил, циклоалкенил, C2-6алкенил, арил, биарил, гетероарил, гетеробиарил, гетероциклил, C1-2алкиларил, C1-2алкилгетероарил или C1-2алкилгетероциклил, при этом арил, биарил, гетероарил, гетеробиарил, гетероциклил, C1-2алкиларил, C1-2алкилгетероарил или C1-2алкилгетероциклил необязательно могут быть замещены одним или несколькими R9;
[41] R6 представляет собой H, C1-4алкил, C1-6алкокси, -NR15R16, арил, биарил, гетероарил, гетеробиарил, гетероциклил, C1-2алкиларил, C1-2алкилгетероарил, C1-2алкилгетероциклил, C1-2алкилбиарил, -L-арил или -L-биарил, при этом C1-4алкил, арил, биарил, гетероарил, гетеробиарил, гетероциклил, C1-2алкиларил, C1-2алкилгетероарил, C1-2алкилгетероциклил, C1-2алкилбиарил, -L-арил или -L-биарил необязательно могут быть замещены одним или несколькими R9;
[42] R8 представляет собой H, C1-6алкил, C1-4фторалкил, C1-4гидроксиалкил, C1-3алкиларил или C(=O)R10, при этом C1-6алкил или C1-3алкиларил необязательно может быть замещен одним или несколькими R9;
[43] если Z представляет собой NR8, то R8 и R6 могут быть объединены друг с другом с образованием 3-7-членного гетероциклического кольца, содержащего 1-2 гетероатома N или 0-2 гетероатома O;
[44] R9 представляет собой галоген, гидроксил, -CN, -NO2, -COOH, -(C=O)H, C1-6алкил, C2-6алкенил, C2-6алкинил, C3-10циклоалкил, C1-4гидроксиалкил, C1-6алкокси, циклоалкенил, арил, гетероциклил, гетероарил, -NR15R16, -L-NR15R16, -L-COOR17, -L-алкил, -L-C3-10циклоалкил, -L-гетероциклил, -L-гетероарил или -L-арил, при этом C1-6алкил, C2-6алкенил, C2-6алкинил, C3-10циклоалкил, C1-4гидроксиалкил, C1-6алкокси, циклоалкенил, арил, гетероциклил, гетероарил, -L-алкил, -L-C3-10циклоалкил, -L-гетероциклил, -L-гетероарил или -L-арил могут быть замещены галогеном, гидроксилом, -CN, -NR15R16, C1-6алкилом, C3-10циклоалкилом, C1-4гидроксиалкилом, C2-6алкенилом, арилом, гетероциклилом, -L-гетероциклилом или -(CH2)l-C(=O)-NR15R16;
[45] R10 представляет собой C1-3алкил или C1-3алкиларил;
[46] R11 представляет собой H, C1-6алкил, C1-4фторалкил, C1-4гидроксиалкил, C1-3алкиларил или C(=O)R10, при этом C1-6алкил или C1-3алкиларил необязательно могут быть замещены одним или несколькими R9;
[47] каждый из R15 и R16 независимо представляет собой H, C1-6алкил, C3-10циклоалкил или SO2R17;
[48] R17 представляет собой H, C1-3алкил или C1-3алкиларил;
[49] R18-R21 являются одинаковыми или отличными друг от друга, и каждый из них независимо представляет собой H или галоген; или
[50] R18 и R19 или R20 и R21 могут быть объединены друг с другом с образованием 3-7-членного циклического кольца или гетероциклического кольца, содержащего 1 или 2 из NR8, O или S, и циклическое или гетероциклическое кольцо необязательно может быть замещено 1 или 2 атомами галогена, C1-4алкилами или C1-4алкокси;
[51] L представляет собой C1-3алкил, C1-3алкил-O, C2-6алкинил, C3-10циклоалкил, -(CH2)l-C(=O)-(CH2)m-, C(=O)O, -(CH2)l-C(=O)NH-(CH2)m-, -(CH2)l-NHC(=O)-(CH2)m-, -(CH2)l-NH-(CH2)m-, NR8, -NH-C(=O)-CR15R16-NH-C(=O)-, NHC(=O), O, O(C=O)S, S, S(=O) или SO2; и
[52] каждый из l и m независимо представляет собой целое число от 0 до 2.
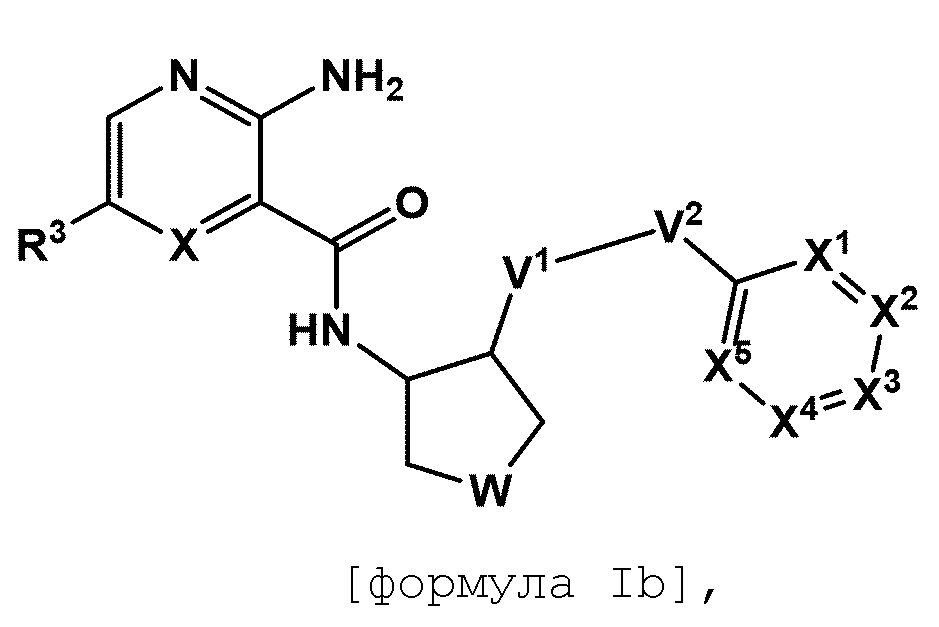
[53] В соответствии с третьим вариантом осуществления настоящего изобретения предусмотренное гетероциклическое соединение, представленное формулой I, представлено следующей формулой Ib:
[54] [формула Ib]
[55] 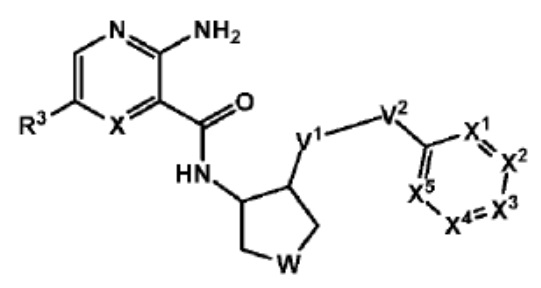 ,
,
[56] где
[57] X представляет собой CH или N;
[58] W представляет собой CH2, NR11 или O;
[59] каждый из V1 и V2 независимо представляет собой CR13R13', NR13 или O;
[60] по меньшей мере один из V1 и V2 представляет собой CR13R13';
[61] X1-X5 являются одинаковыми или отличными друг от друга и каждый из них независимо представляет собой CR14 или N;
[62] по меньшей мере один из X1-X5 представляет собой CR14;
[63] R3 представляет собой H, галоген, CN, C1-3алкил, циклоалкенил, C2-6алкенил, арил, биарил, гетероарил, гетеробиарил, гетероциклил, C1-2алкиларил, C1-2алкилгетероарил или C1-2алкилгетероциклил, при этом арил, биарил, гетероарил, гетеробиарил, гетероциклил, C1-2алкиларил, C1-2алкилгетероарил или C1-2алкилгетероциклил необязательно могут быть замещены одним или несколькими R9;
[64] R9 представляет собой галоген, гидроксил, -CN, -NO2, -COOH, -(C=O)H, C1-6алкил, C2-6алкенил, C2-6алкинил, C3-10циклоалкил, C1-4гидроксиалкил, C1-6алкокси, циклоалкенил, арил, гетероциклил, гетероарил, -NR15R16, -L-NR15R16, -L-COOR17, -L-алкил, -L-C3-10циклоалкил, -L-гетероциклил, -L-гетероарил или -L-арил, при этом C1-6алкил, C2-6алкенил, C2-6алкинил, C3-10циклоалкил, C1-4гидроксиалкил, C1-6алкокси, циклоалкенил, арил, гетероциклил, гетероарил, -L-алкил, -L-C3-10циклоалкил, -L-гетероциклил, -L-гетероарил или -L-арил могут быть замещены галогеном, гидроксилом, -CN, -NR15R16, C1-6алкилом, C3-10циклоалкилом, C1-4гидроксиалкилом, C2-6алкенилом, арилом, гетероциклилом, -L-гетероциклилом или -(CH2)l-C(=O)-NR15R16;
[65] R10 представляет собой C1-3алкил или C1-3алкиларил;
[66] R11 представляет собой H, C1-6алкил, C1-4фторалкил, C1-4гидроксиалкил, C1-3алкиларил или C(=O)R10, при этом C1-6алкил или C1-3алкиларил необязательно может быть замещен одним или несколькими R9;
[67] каждый из R13 и R13' независимо представляет собой H, C1-3алкил, C2-3гидроксиалкил;
[68] каждый R14 независимо выбран из H, галогена, гидроксила, -CN, -NO2, C1-6алкила, C2-6алкенила, C2-6алкинила, C3-10циклоалкила, циклоалкенила, арила, гетероциклила, гетероарила, -NR15R16, -L-алкила, -L-гетероциклила, -L-гетероарила или -L-арила, при этом C1-6алкил, арил, гетероарил, гетероциклил необязательно могут быть замещены одним или несколькими R9; или прилежащие группы среди множества R14 связаны друг с другом с образованием 3-7-членного циклического кольца или гетероциклического кольца, содержащего 1 или 2 из NR11, O или S, и циклическое или гетероциклическое кольцо необязательно может быть замещено 1 или 2 атомами галогена, C1-4алкилами или C1-4алкокси;
[69] каждый из R15 и R16 независимо представляет собой H, C1-6алкил, C3-10циклоалкил или SO2R17;
[70] R17 представляет собой H, C1-3алкил или C1-3алкиларил;
[71] L представляет собой C1-3алкил, C1-3алкил-O, C2-6алкинил, C3-10циклоалкил, -(CH2)l-C(=O)-(CH2)m-, C(=O)O, -(CH2)l-C(=O)NH-(CH2)m-, -(CH2)l-NHC(=O)-(CH2)m-, -(CH2)l-NH-(CH2)m-, NR8, -NH-C(=O)-CR15R16-NH-C(=O)-, NHC(=O), O, O(C=O)S, S, S(=O) или SO2; и
[72] каждый из l и m независимо представляет собой целое число от 0 до 2.
[73] В настоящем изобретении галоген может представлять собой фтор, хлор, бром или йод.
[74] В настоящем изобретении алкил может быть с прямой или разветвленной цепью, и количество атомов углерода в нем конкретно не ограничивается, но предпочтительно составляет от 1 до 6. Его конкретные примеры включают метильную группу, этильную группу, пропильную группу, изопропильную группу, бутильную группу, пентильную группу, гексильную группу и т. п. или группы с разветвленной цепью, но не ограничиваются этим.
[75] В настоящем изобретении циклоалкил конкретно не ограничивается, но содержит предпочтительно 3-10 атомов углерода. Его конкретные примеры включают циклопропильную, циклобутильную, циклопентильную, циклогексильную, циклогептильную, циклооктильную, норборнильную группу, адамантильную группу и т. п., но не ограничиваются этим.
[76] В настоящем изобретении алкокси может быть с прямой, разветвленной цепью или циклическим. Количество атомов углерода алкоксигруппы конкретно не ограничивается, но предпочтительно составляет от 1 до 6. Ее конкретные примеры включают метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси и т. п., но не ограничиваются этим.
[77] В настоящем изобретении алкенил может быть с прямой или разветвленной цепью, и количество атомов углерода в нем конкретно не ограничивается, но предпочтительно составляет от 2 до 6. Его конкретные примеры включают винил, 1-пропенил, изопропенил, 1-бутенил, 2-бутенил, 3-бутенил, 1-пентенил, 2-пентенил, 3-пентенил, 3-метил-1-бутенил, 1,3-бутадиенил и т. п., но не ограничиваются этим.
[78] В настоящем изобретении арил может быть моноциклическим или полициклическим, и количество атомов углерода конкретно не ограничивается, но предпочтительно составляет от 6 до 60. Конкретные примеры арильной группы включают моноциклическую ароматическую группу, такую как фенильная группа, и полициклическую ароматическую группу, такую как нафтильная группа, антраценильная группа, фенантренильная группа, пиренильная группа, периленильная группа, тетраценильная группа, хризенильная группа, фторенильная группа, аценафтаценильная группа, трифениленовая группа и флуорантеновая группа и т. п., но не ограничиваются этим.
[79] В настоящем изобретении биарил может содержать две или более моноциклических и/или полициклических групп, соединенных друг с другом.
[80] В настоящем изобретении арил в алкилариле и биариле является таким же, как в вышеописанных примерах арильной группы.
[81] В настоящем изобретении гетероциклил или гетероарил содержит один или несколько гетероатомов, например гетероциклическая группа, содержащая один или несколько из O, N, S, Si, Se и т. п. Примеры гетероциклической группы включают тиофеновую группу, фурановую группу, пиррольную группу, имидазольную группу, тиазольную группу, оксазольную группу, оксадиазольную группу, триазольную группу, пиридильную группу, бипиридильную группу, триазиновую группу, акридильную группу, пиридазиновую группу, пирролидиновую группу, морфолиновую группу, пиперазиновую группу, пиперидиновую группу, тетрагидрофурановую группу, пиразольную группу, хинолинильную группу, изохинолиновую группу, индольную группу, карбазольную группу, бензоксазольную группу, бензимидазольную группу, бензотиазольную группу, бензокарбазольную группу, бензотиофеновую группу, дибензотиофеновую группу, бензофуранильную группу, фенантролиновую группу, дибензофуранильную группу и т. п., но не ограничиваются этим.
[82] В настоящем изобретении «прилежащая» группа может означать заместитель, замещенный атомом, непосредственно соединенным с атомом, при котором соответствующий заместитель является замещенным, заместитель, расположенный пространственно наиболее близко к соответствующему заместителю, или другой заместитель, замещенный атомом, при котором соответствующий заместитель является замещенным. Например, два заместителя, замещенные в орто-положении в бензольном кольце, и два заместителя, замещенные одним и тем же атомом углерода в алифатическом кольце, могут быть интерпретированы как группы, «прилежащие» друг к другу.
[83] В настоящем изобретении циклическое кольцо или гетероциклическое кольцо, образованное посредством связывания двух или более R14, включает циклоалкил, циклоалкенил, арил, гетероцикл, гетероарил. В соответствии с четвертым вариантом осуществления настоящего изобретения предусмотренное гетероциклическое соединение, представленное формулой I, представлено любым из следующих соединений.
|
[84]
|
[85]
|
[86]
|
[87]
|
[88]
|
[89]
|
[90]
|
[91]
|
[92]
|
[93]
|
[94]
|
[95]
|
[96]
|
[97]
|
[98]
|
[99]
|
[100]
|
[101]
|
[102]
|
[103]
|
[104]
|
[105]
|
[106]
|
[107]
|
[108]
|
[109]
|
[110]
|
[111]
|
[112]
|
[113]
|
[114]
|
[115]
|
[116]
|
[117]
|
[118]
|
[119]
|
[120]
|
[121]
|
[122]
|
[123]
|
[124]
|
[125]
|
[126]
|
[127]
|
[128]
|
[129]
[130] Фармацевтические композиции, содержащие новые ингибиторы Mer-киназы
[131] Настоящее изобретение предусматривает фармацевтические композиции, содержащие гетероциклические соединения, их стереоизомер, их энантиомер или их фармацевтически приемлемую соль вместе с фармацевтически приемлемыми носителями.
[132] Носители, которые применяются в настоящем изобретении, могут представлять собой носители, которые обычно применяются в данной области техники, и их примеры включают без ограничения сахар, крахмал, микрокристаллическую целлюлозу, лактозу (гидрат лактозы), глюкозу, D-маннит, альгинат, соли щелочноземельных металлов, глину, полиэтиленгликоль, безводный гидроортофосфат кальция или их смеси.
[133] Кроме того, в соответствии с другим вариантом осуществления настоящего изобретения фармацевтические композиции могут содержать добавки, такие как связующие вещества, разрыхлители, смазывающие вещества, средства, регулирующие pH, антиоксиданты и т. п.
[134] Примеры связующих веществ, которые можно применять в настоящем изобретении, включают без ограничения крахмал, микрокристаллическую целлюлозу, высокодисперсный диоксид кремния, маннит, D-маннит, сахарозу, гидрат лактозы, полиэтиленгликоль, поливинилпирролидон (повидон), сополимер поливинилпирролидона (коповидон), гипромеллозу, гидроксипропилцеллюлозу, природную камедь, синтетическую камедь, коповидон, желатин, или их смеси.
[135] Примеры разрыхлителей, которые можно применять в настоящем изобретении, включают без ограничения виды крахмала или модифицированные виды крахмала, такие как натрия крахмалгликолят, кукурузный крахмал, картофельный крахмал или прежелатинизированный крахмал; виды глины, такие как бентонит, монтмориллонит или вигум; разновидности целлюлозы, такие как микрокристаллическая целлюлоза, гидроксипропилцеллюлоза или карбоксиметилцеллюлоза; альгины, такие как альгинат натрия или альгиновая кислота; разновидности сшитой целлюлозы, такие как кроскармеллоза натрия; камеди, такие как гуаровая камедь или ксантановая камедь; сшитые полимеры, такие как сшитый поливинилпирролидон (кросповидон); шипучие составы, такие как бикарбонат натрия или лимонная кислота; или их смеси.
[136] Примеры смазывающих веществ, которые можно применять в настоящем изобретении, включают без ограничения тальк, стеариновую кислоту, стеарат магния, стеарат кальция, лаурилсульфат натрия, гидрогенизированное растительное масло, бензоат натрия, стеарилфумарат натрия, глицерилбегенат, глицерилмоноолеат, глицерилмоностеарат, глицерилпальмитостеарат, коллоидный диоксид кремния или их смеси.
[137] Примеры средств, регулирующих pH, которые можно применять в настоящем изобретении, включают без ограничения подкисляющие средства, такие как уксусная кислота, адипиновая кислота, аскорбиновая кислота, аскорбат натрия, эфират натрия, яблочная кислота, янтарная кислота, винная кислота, фумаровая кислота или лимонная кислота, и подщелачивающие средства, такие как осажденный карбонат кальция, водный раствор аммиака, меглюмин, карбонат натрия, оксид магния, карбонат магния, цитрат натрия или трикальцийфосфат.
[138] Примеры антиоксидантов, которые можно применять в настоящем изобретении, включают без ограничения дибутилгидрокситолуол, бутилированный гидроксианизол, токоферола ацетат, токоферол, пропилгаллат, гидросульфит натрия, пиросульфит натрия и т. п.
[139] Предусмотренные в настоящем изобретении фармацевтические композиции содержат в качестве активных ингредиентов гетероциклические соединения, их стереоизомер, их энантиомер или их фармацевтически приемлемую соль и применяются для предупреждения или лечения заболевания, на которое можно оказать воздействие посредством ингибирования Mer-киназы.
[140] Предусмотренное в настоящем изобретении заболевание, на которое можно оказать воздействие посредством ингибирования Mer-киназы, представляет собой рак или заболевания, связанные с иммунной системой.
[141] Рак выбран из группы, состоящей из глиомы, глиосаркомы, анапластической астроцитомы, медуллобластомы, рака легкого, мелкоклеточной карциномы легкого, карциномы шейки матки, рака толстой кишки, рака прямой кишки, хордомы, рака горла, саркомы Капоши, лимфангиосаркомы, лимфангиоэндотелиосаркомы, рака ободочной и прямой кишки, рака эндометрия, рака яичника, рака молочной железы, рака поджелудочной железы, рака предстательной железы, почечно-клеточной карциномы, гепатокарциномы, карциномы желчного протока, хориокарциномы, семиномы, опухоли яичка, опухоли Вильмса, опухоли Юинга, карциномы мочевого пузыря, ангиосаркомы, эндотелиосаркомы, аденокарциномы, карциномы потовых желез, саркомы сальных желез, сосочковой саркомы, сосочковой аденосаркомы, цистаденосаркомы, бронхогенной карциномы, медуллярной карциномы, мастоцитомы, мезотелиомы, синовиомы, меланомы, лейомиосаркомы, рабдомиосаркомы, нейробластомы, ретинобластомы, олигодендроглиомы, невриномы слухового нерва, гемангиобластомы, менингиомы, пинеаломы, эпендимомы, краниофарингиомы, эпителиальной карциномы, эмбриональной карциномы, плоскоклеточной карциномы, базалиомы, фибросаркомы, миксомы, миксосаркомы, липосаркомы, хондросаркомы, остеогенной саркомы, лейкоза и метастатических очагов, вторичных по отношению к этим первичным опухолям.
[142] Заболевание, связанное с иммунной системой, выбрано из группы, состоящей из инфекции и сепсиса.
[143] Термин «лечение» используется для обозначения как предупреждения заболеваний, так и лечения уже существующих состояний.
[144] Терапевтическое количество варьирует в зависимости от конкретного заболевания и может быть определено специалистом в данной области без чрезмерных усилий.
[145] Помимо этого, субъект в способе предупреждения или лечения согласно настоящему изобретению включает млекопитающих, в частности людей.
[146] Доза варьирует в зависимости от конкретного применяемого соединения, конкретного заболевания, состояния пациента и т. д. Обычно терапевтическая доза является достаточной для уменьшения нежелательной популяции клеток в ткани-мишени, в то время как жизнеспособность пациента сохраняется. Лечение, как правило, продолжается до тех пор, пока не произойдет значительное снижение, например снижение клеточной нагрузки по меньшей мере на 50%, и может продолжаться до тех пор, пока в организме фактически не перестанут обнаруживаться нежелательные клетки.
[147] Способ предупреждения или лечения заболеваний, связанных с иммунной системой, или рака
[148] Настоящее изобретение предусматривает способ лечения или предупреждения заболеваний, связанных с иммунной системой, или рака, причем способ включает введение млекопитающим, в том числе людям, нуждающимся в этом, композиций, содержащих в качестве активных ингредиентов гетероциклические соединения, их изомеры или их фармацевтически приемлемые соли.
[149] Композиция, которая применяется в способе согласно настоящему изобретению для предупреждения или лечения заболеваний, связанных с иммунной системой, или рака, предусматривает фармацевтическую композицию, охарактеризованную в описании.
[150] Настоящее изобретение предусматривает применение композиций, содержащих в качестве активных ингредиентов гетероциклические соединения, их стереоизомер, их энантиомер или их фармацевтически приемлемую соль для получения лекарственных препаратов для предупреждения или лечения рака или заболеваний, связанных с иммунной системой.
[151] Способы получения новых ингибиторов Mer-киназы
[152] Соединения согласно настоящему изобретению можно получать в соответствии с одной или несколькими схемами, описанными ниже.
[153] Данные способы можно применять либо непосредственно, либо с изменениями, очевидными для подготовленных в области химии специалистов, для получения ключевых промежуточных соединений и определенных соединений согласно настоящему изобретению.
[154] Подходящие последовательности синтеза легко подбираются к конкретным структурам согласно настоящему изобретению, но в пределах уровня техники, известного специалистам в области органического синтеза, как, например, способы, кратко изложенные в доступных химических базах данных, а именно в CAS Scifinder и Elesevier Reaxys. Исходя из данных общих способов получение соединений согласно настоящему изобретению является несложным в реализации и его можно осуществлять в рамках общих профессиональных знаний. Некоторые общие способы синтеза для получения соединений согласно настоящему изобретению проиллюстрированы ниже на схемах 1-2 (неограничивающие, только для иллюстрации).
[155] Один общий подход в отношении соединений согласно настоящему изобретению проиллюстрирован на общей схеме 1.
[156] 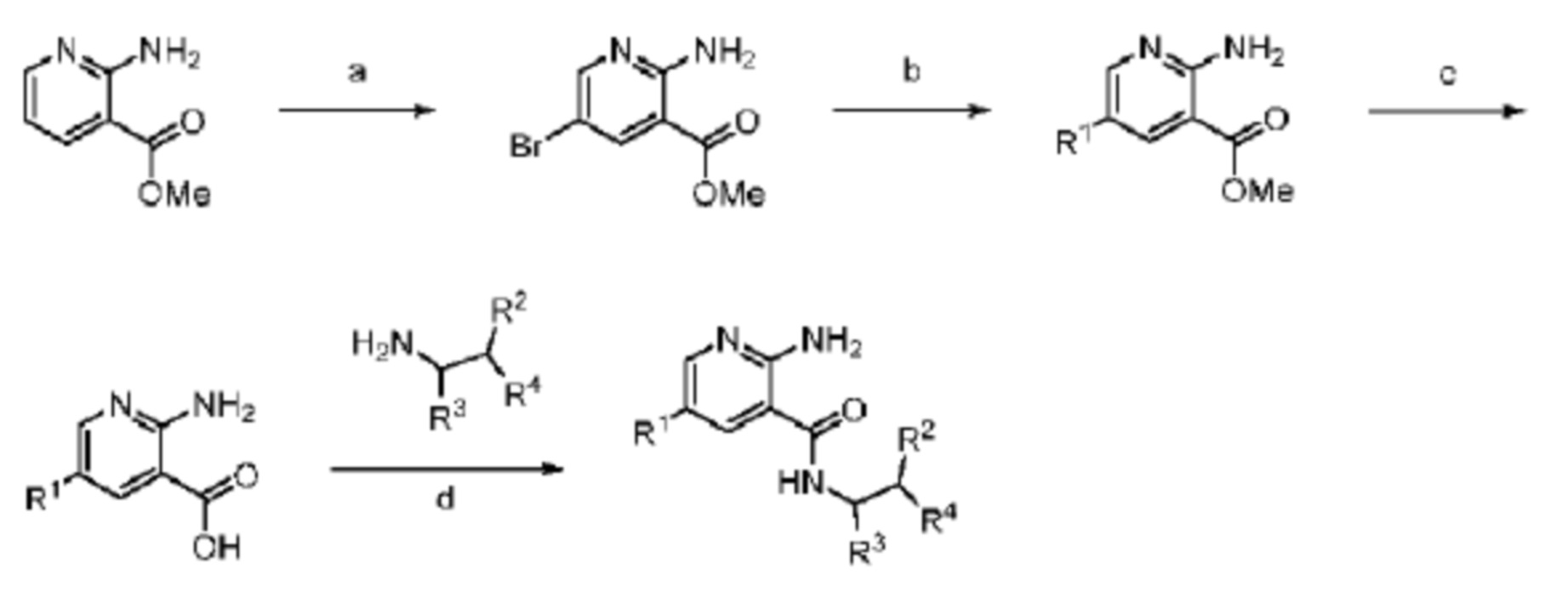
[157] Схема 1. Общая процедура A
[158] a) NBS, CH3CN, H2O; b) R1-B(OH)2 или его пинаколиновый сложный эфир, Pd(PPh3)4, водн. K3PO4, диоксан, нагрев; c) NaOH, MeOH, нагрев; d) HATU, TEA, DMF.
[159] Другой общий подход в отношении соединений согласно настоящему изобретению проиллюстрирован на общей схеме 2.
[160] 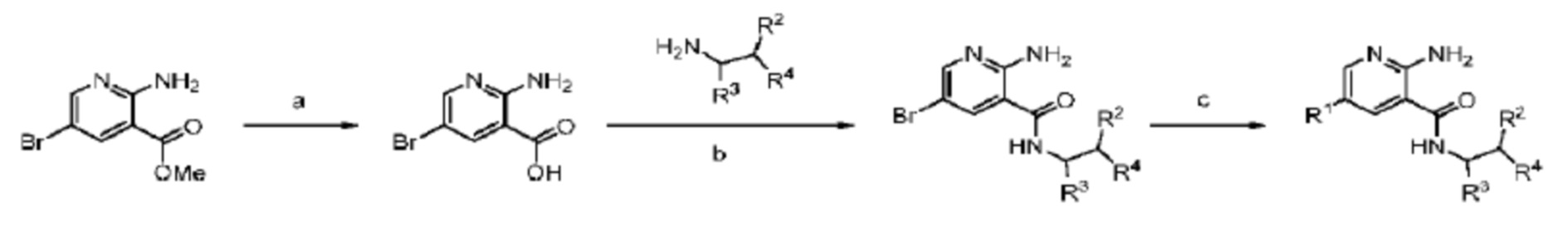
[161] Схема 2. Общая процедура B
[162] a) NaOH, MeOH, нагрев; b) HATU, TEA, DMF; c) R1-B(OH)2 или его пинаколиновый сложный эфир, Pd(PPh3)4, водн. K3PO4, диоксан, нагрев.
Полезные эффекты настоящего изобретения
[163] Новые гетероциклические соединения согласно настоящему изобретению, их стереоизомер, их энантиомер или их фармацевтически приемлемая соль проявляют эффект эффективного ингибирования Mer-киназы.
[164] Новые гетероциклические соединения согласно настоящему изобретению, их стереоизомер, их энантиомер или фармацевтически приемлемую соль можно применять для предупреждения или лечения рака или заболевания, связанного с иммунной системой.
Способ согласно настоящему изобретению
[165] На основании проведенных исследований и полученных до настоящего времени результатов считается, что следующие соединения (под номерами от 1 до 458), включая изомеры, смеси изомеров, а также их фармацевтически приемлемые соли и сольваты, особенно интересны.
[166] Общие способы синтеза
[167] Примеры
[168] Варианты осуществления настоящего изобретения описаны в следующих примерах, которые предполагаются как иллюстрирующие, а не ограничивающие объем настоящего изобретения. Общие сокращения, хорошо известные специалистам в области синтеза, используются во всем документе.
[169] Все химические реагенты коммерчески доступны. Колоночная флэш-хроматография означает хроматографию на силикагеле, если не указано иное, которую проводили на системе Teledyne Combiflash-RF200. Спектры 1H-ЯМР (δ, ppm) записывали на приборе при 400 МГц или 600 МГц. Представлены данные масс-спектроскопии для метода положительной ионизации. Препаративную HPLC проводили на Agilent technologies G1361A.
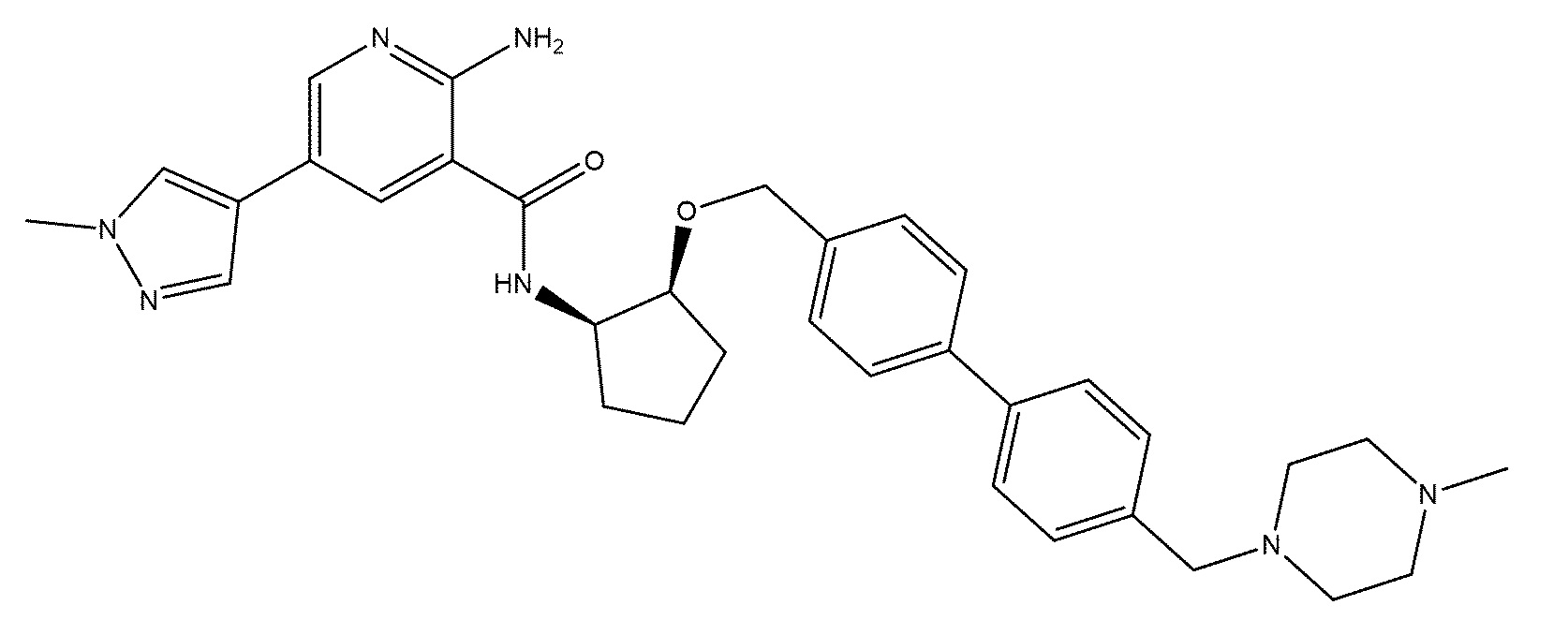
[170] Пример 1. 2-амино-N-((1S,2S)-2-(бензилокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[171] Схема получения соединения из примера 1:
[172]
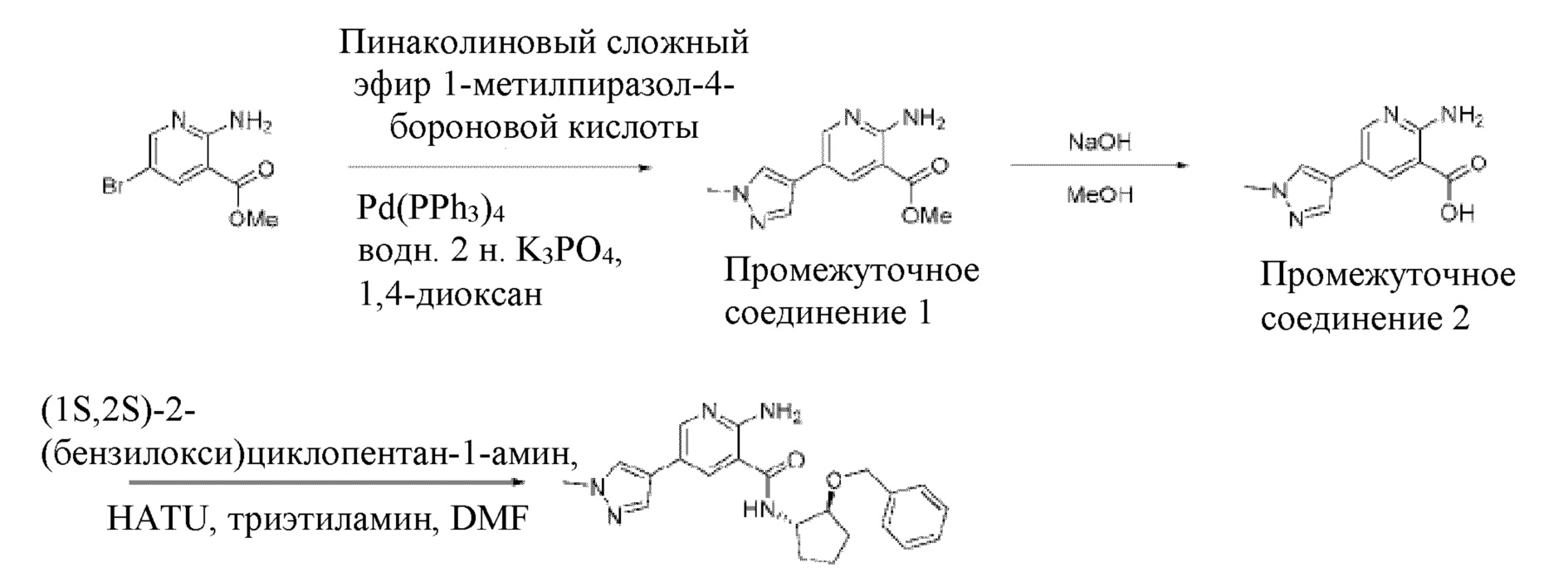
[173] Промежуточное соединение 1. В смесь метил-2-амино-5-бромникотината (1,5 г, 6,5 ммоль) и пинаколинового сложного эфира 1-метилпиразол-4-бороновой кислоты (1,76 г, 8,5 ммоль) в 24 мл 1,4-диоксана добавляли 8 мл водн. 2 н. K3PO4, а затем Pd(PPh3)4 (370 мг, 0,32 ммоль). Реакционную смесь нагревали при 100°C в течение 3 часов, охлаждали до комнатной температуры и экстрагировали при помощи EtOAc, сушили над безводным MgSO4 и концентрировали под вакуумом. Неочищенный продукт очищали колоночной хроматографией на силикагеле с получением 1,25 г грязно-белого твердого вещества.
[174] 1H-ЯМР (400 МГц, CD3OD) δ 3,90(s, 3H), 3,91(s, 3H), 7,74(s, 1H), 7,91(s, 1H), 8,29(d, J=2,4 Гц, 1H), 8,35(d, J=2,4 Гц, 1H);
[175] MS (ESI, масса/заряд): 233,1 [M+H]+
[176] Промежуточное соединение 2. В суспензию промежуточного соединения 1 (1,2 г, 5,17 ммоль) в 26 мл MeOH добавляли 2 н. NaOH (4,3 мл, 8,63 ммоль), и смесь нагревали при 65°C в течение 1 часа, охлаждали до комнатной температуры, нейтрализовали (4,3 мл 2 н. HCl), и полученный осадок отфильтровывали, промывали при помощи MeOH и сушили с получением 0,97 г грязно-белого твердого вещества.
[177] 1H-ЯМР (600 MГц, DMSO-d6) δ ppm 3,82(s, 3H), 5,73(s, 2H), 7,77(s, 1H), 8,05(s, 1H), 8,13(d, J=2,4 Гц, 1H), 8,42(d, J=2,4 Гц, 1H);
[178] MS (ESI, масса/заряд): 219,1 [M+H]+
[179] Пример 1. 2-амино-N-((1S,2S)-2-(бензилокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[180] В смесь промежуточного соединения 2 (43 мг, 0,2 ммоль) и триэтиламина (24 мг, 0,24 ммоль) в 2 мл DMF добавляли HATU (91 мг, 0,24 ммоль), а затем (1S,2S)-2-(бензилокси)циклопентан-1-амин (38 мг, 0,2 ммоль). Смесь перемешивали при комнатной температуре в течение 1 часа, а затем добавляли насыщенный раствор бикарбоната натрия. Смесь экстрагировали при помощи EtOAc, промывали солевым раствором, сушили над MgSO4 и концентрировали in vacuo. Неочищенный остаток очищали препаративной HPLC с получением 46 мг названого соединения.
[181] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,57-1,69 (m, 1 H) 1,72-1,86 (m, 3 H) 1,90-2,08 (m, 1 H) 2,11-2,21 (m, 1 H) 3,93 (s, 3 H) 3,96 (dt, J=6,75, 4,26 Гц, 1 H) 4,39 (td, J=7,34, 4,11 Гц, 1 H) 4,61 (s, 2 H) 7,13-7,24 (m, 1 H) 7,27 (t, J=7,46 Гц, 2 H) 7,32 (d, J=7,04 Гц, 2 H) 7,79-7,90 (m, 1 H) 8,00 (s, 1 H) 8,23 (d, J=1,76 Гц, 1 H) 8,46 (d, J=2,35 Гц, 1 H);
[182] MS (ESI, масса/заряд): 392,2 [M+H]+
[183] Пример 2. 2-амино-N-((1R,2R)-2-(бензилокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[184] Используя (1R,2R)-2-(бензилокси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[185] MS (ESI, масса/заряд): 392,2 [M+H]+
[186] Пример 3. 2-амино-N-(транс-2-(бензилокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[187] Используя транс-2-(бензилокси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[188] MS (ESI, масса/заряд): 392,2 [M+H]+
[189] Пример 4. 2-амино-N-((1R,2S)-2-(бензилокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[190] Используя (1R,2S)-2-(бензилокси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[191] 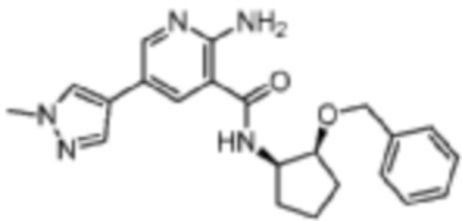
[192] MS (ESI, масса/заряд): 392,2 [M+H]+
[193] Пример 5. 2-амино-N-(цис-2-(бензилокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[194] Используя цис-2-(бензилокси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[195] 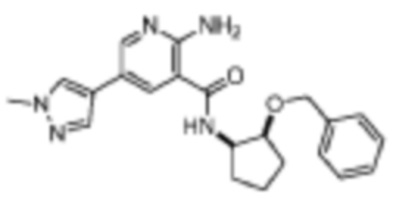
[196] MS (ESI, масса/заряд): 392,2 [M+H]+
[197] Пример 6. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((2-метилбензил)окси)циклопентил)никотинамид
[198] Используя (1S,2S)-2-((2-метилбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[199] 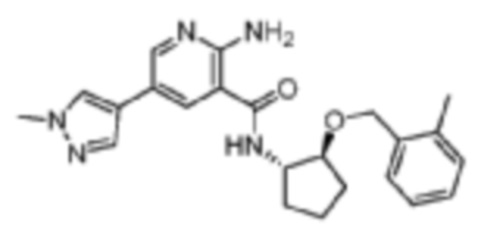
[200] Пример 7. 2-амино-N-((1S,2S)-2-((3-этилбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[201] Используя (1S,2S)-2-((3-этилбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[202] 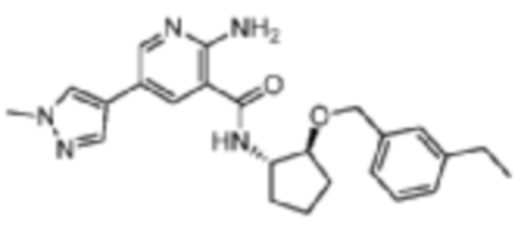
[203] MS (ESI, масса/заряд): 420,2 [M+H]+
[204] Пример 8. 2-амино-N-((1S,2S)-2-((4-этилбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[205] Используя (1S,2S)-2-((4-этилбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[206] 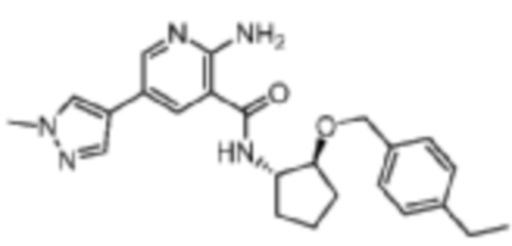
[207] MS (ESI, масса/заряд): 420,2 [M+H]+
[208] Пример 9. 2-амино-N-(транс-2-((4-этилбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[209] Используя транс-2-((4-этилбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[210] 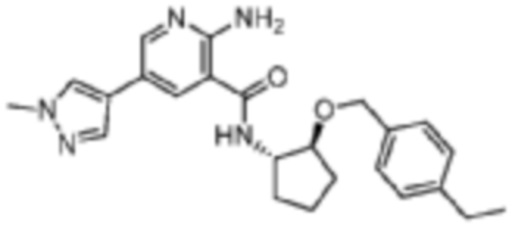
[211] MS (ESI, масса/заряд): 420,2 [M+H]+
[212] Пример 10. 2-амино-N-((1S,2S)-2-((4-изопропилбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[213] Используя (1S,2S)-2-((4-изопропилбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[214] 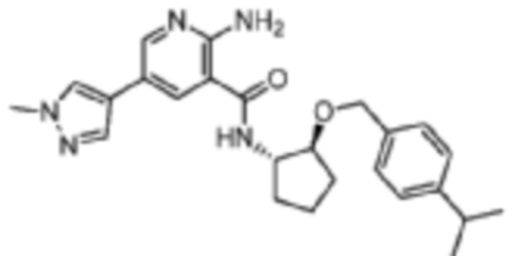
[215] MS (ESI, масса/заряд): 434,3 [M+H]+
[216] Пример 11. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[217] Используя (1S,2S)-2-((2,3-диметилбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[218] 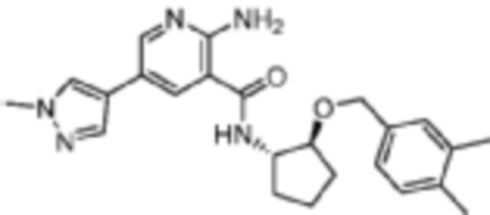
[219] MS (ESI, масса/заряд): 420,2 [M+H]+
[220] Пример 12. 2-амино-N-((1R,2R)-2-((3,4-диметилбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[221] Используя (1R,2R)-2-((3,4-диметилбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[222] 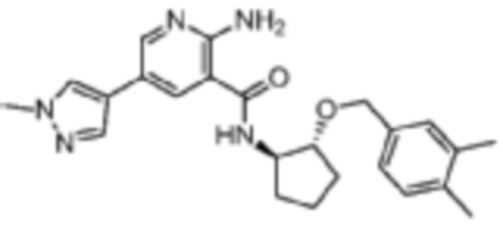
[223] MS (ESI, масса/заряд): 420,2 [M+H]+
[224] Пример 13. 2-амино-N-(транс-2-((3,4-диметилбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[225] Используя транс-2-((3,4-диметилбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[226] 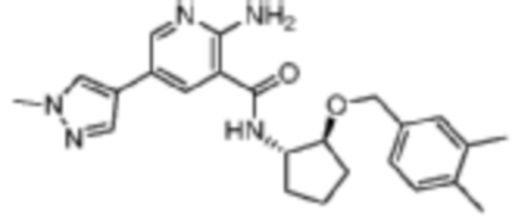
[227] MS (ESI, масса/заряд): 420,2 [M+H]+
[228] Пример 14. 2-амино-N-((1S,2S)-2-((2,3-диметилбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[229] Используя (1S,2S)-2-((2,3-диметилбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[230] 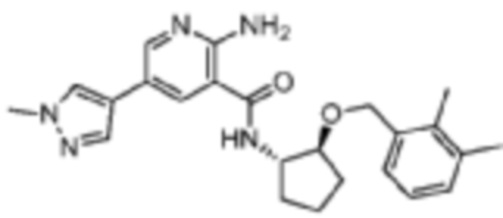
[231] MS (ESI, масса/заряд): 420,2 [M+H]+
[232] Пример 15. 2-амино-N-((1S,2S)-2-((2,6-диметилбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[233] Используя (1S,2S)-2-((2,6-диметилбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[234] 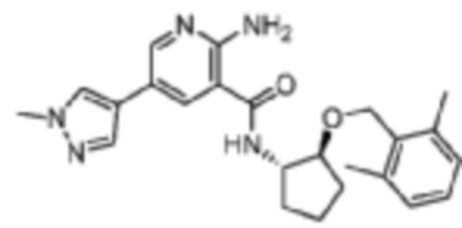
[235] MS (ESI, масса/заряд): 420,2 [M+H]+
[236] Пример 16. 2-амино-N-((1S,2S)-2-((2,5-диметилбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[237] Используя (1S,2S)-2-((2,5-диметилбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[238] 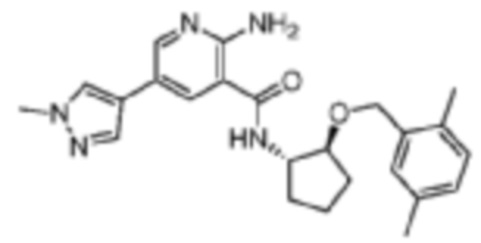
[239] MS (ESI, масса/заряд): 420,2 [M+H]+
[240] Пример 17. 2-амино-N-((1S,2S)-2-((3,5-диметилбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[241] Используя (1S,2S)-2-((3,5-диметилбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[242] 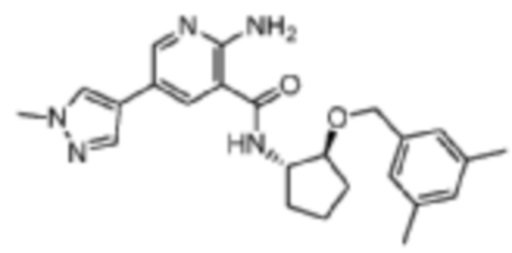
[243] MS (ESI, масса/заряд): 420,2 [M+H]+
[244] Пример 18. 2-амино-N-((1S,2S)-2-((2,4-диметилбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[245] Используя (1S,2S)-2-((2,4-диметилбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[246] 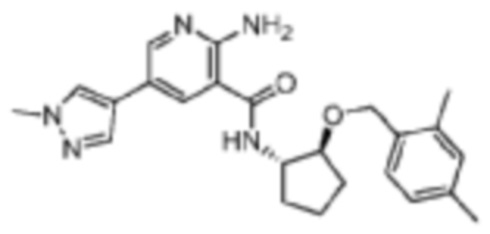
[247] MS (ESI, масса/заряд): 420,2 [M+H]+
[248] Пример 19. 2-амино-N-((1S,2S)-2-((4-этил-3-метилбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[249] Используя (1S,2S)-2-((4-этил-3-метилбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[250] 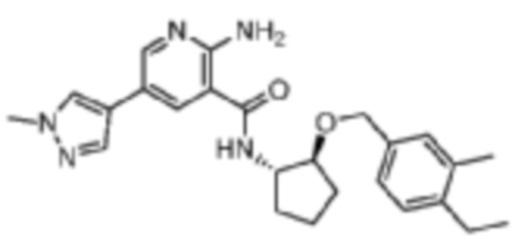
[251] MS (ESI, масса/заряд): 434,3 [M+H]+
[252] Пример 20. 2-амино-N-((1S,2S)-2-((3,4-диэтилбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[253] Используя (1S,2S)-2-((3,4-диэтилбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[254] 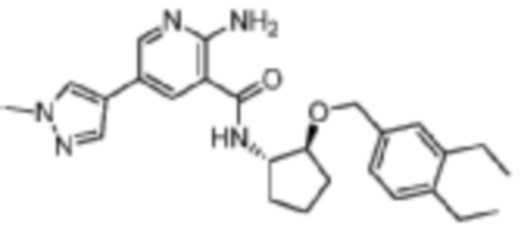
[255] MS (ESI, масса/заряд): 448,3 [M+H]+
[256] Пример 21. 2-амино-N-((1S,2S)-2-((3-этил-4-метилбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[257] Используя (1S,2S)-2-((3-этил-4-метилбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[258] 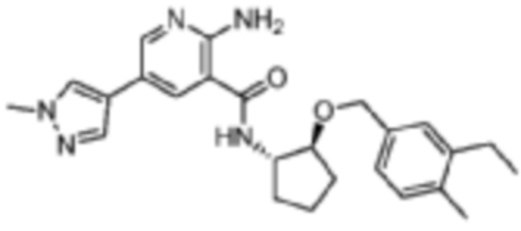
[259] MS (ESI, масса/заряд): 434,3 [M+H]+
[260] Пример 22. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((3-пропилбензил)окси)циклопентил)никотинамид
[261] Используя (1S,2S)-2-((3-пропилбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[262] 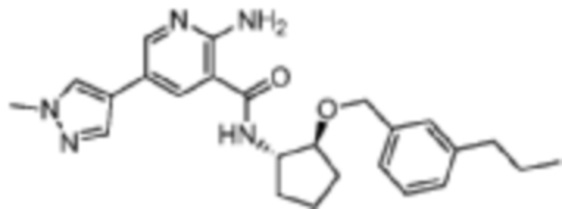
[263] MS (ESI, масса/заряд): 434,3 [M+H]+
[264]
[265] Пример 23. 2-амино-N-((1S,2S)-2-((3-циклопентилбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[266] Используя (1S,2S)-2-((3-циклопентилбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[267] 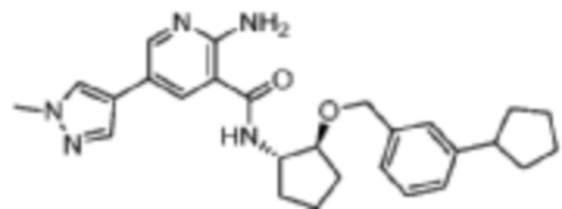
[268] MS (ESI, масса/заряд): 460,3 [M+H]+
[269] Пример 24. 2-амино-N-((1S,2S)-2-((3-изопропилбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[270] Используя (1S,2S)-2-((3-изопропилбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[271] 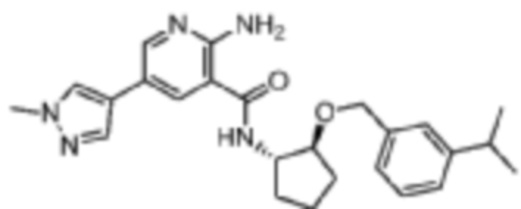
[272] MS (ESI, масса/заряд): 434,3 [M+H]+
[273] Пример 25. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((3-(проп-1-ен-2-ил)бензил)окси)циклопентил)никотинамид
[274] Используя (1S,2S)-2-((3-(проп-1-ен-2-ил)бензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[275] 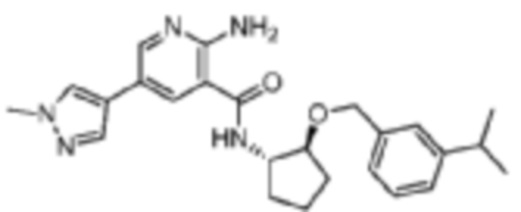
[276] MS (ESI, масса/заряд): 432,2 [M+H]+
[277] Пример 26. 2-амино-N-((1S,2S)-2-((3-циклопропилбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[278] Используя (1S,2S)-2-((3-циклопропилбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[279] 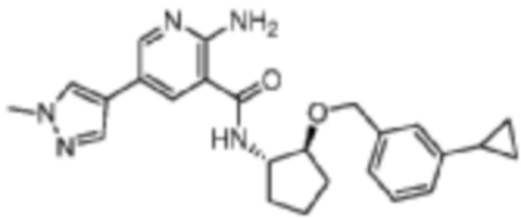
[280] MS (ESI, масса/заряд): 432,2 [M+H]+
[281] Пример 27. 2-амино-N-((1S,2S)-2-((3-циклобутилбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[282] Используя (1S,2S)-2-((3-циклобутилбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[283] 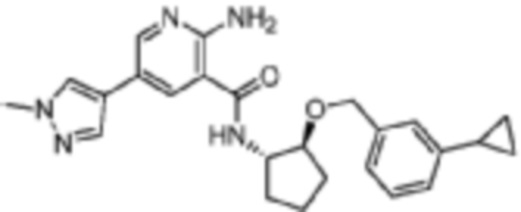
[284] MS (ESI, масса/заряд): 446,3 [M+H]+
[285] Пример 28. 2-амино-N-((1S,2S)-2-((3-этинилбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[286] Используя (1S,2S)-2-((3-этинилбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[287] 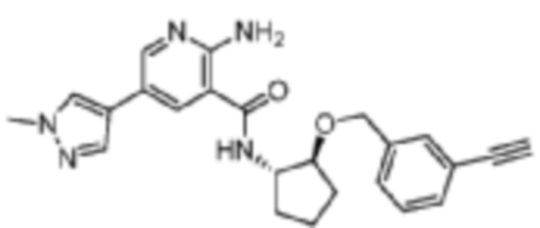
[288] MS (ESI, масса/заряд): 416,2 [M+H]+
[289] Пример 29. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4-(трифторметил)бензил)окси)циклопентил)никотинамид
[290] Используя (1S,2S)-2-((4-(трифторметил)бензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[291] 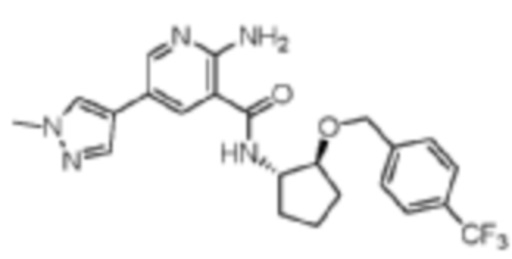
[292] MS (ESI, масса/заряд): 460,2 [M+H]+
[293] Пример 30. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((3-нитробензил)окси)циклопентил)никотинамид
[294] Используя (1S,2S)-2-((3-нитробензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[295] 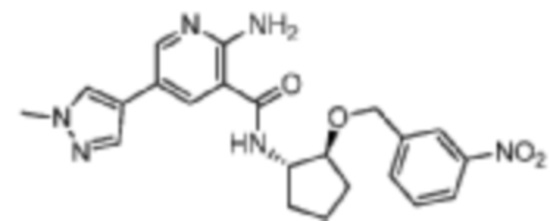
[296] MS (ESI, масса/заряд): 437,2 [M+H]+
[297] Пример 31. 2-амино-N-((1S,2S)-2-((3-цианобензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[298] Используя 3-((((1S,2S)-2-аминоциклопентил)окси)метил)бензонитрил, названное соединение получали, как описано для примера 1.
[299] 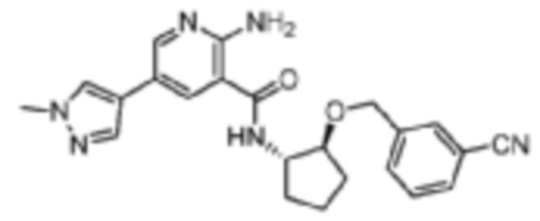
[300] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,58-1,70 (m, 1 H) 1,73-1,90 (m, 3 H) 1,95-2,07 (m, 1 H) 2,11-2,22 (m, 1 H) 3,88-3,98 (m, 4 H) 4,36-4,44 (m, 1 H) 4,61-4,72 (m, 2 H) 7,43-7,51 (m, 1 H) 7,57 (br d, J=7,43 Гц, 1 H) 7,63 (br d, J=7,43 Гц, 1 H) 7,70 (s, 1 H) 7,85 (s, 1 H) 7,99 (s, 1 H) 8,23 (d, J=1,96 Гц, 1 H) 8,45 (d, J=1,96 Гц, 1 H);
[301] MS (ESI, масса/заряд): 417,2 [M+H]+
[302] Пример 32. 2-амино-N-((1S,2S)-2-((3-гидроксибензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[303] Используя (1S,2S)-2-((3-гидроксибензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[304] 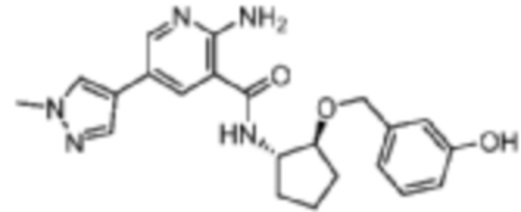
[305] MS (ESI, масса/заряд): 408,2 [M+H]+
[306] Пример 33. 2-амино-N-((1S,2S)-2-((3-метилоксибензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[307] Используя (1S,2S)-2-((3-метилоксибензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[308] 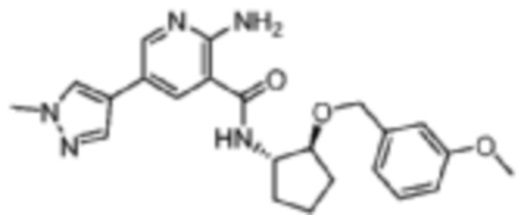
[309] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,54-1,65 (m, 1 H) 1,68-1,88 (m, 3 H) 1,95-2,07 (m, 1 H) 2,09-2,22 (m, 1 H) 3,65-3,74 (m, 3 H) 3,88-3,98 (m, 4 H) 4,33-4,43 (m, 1 H) 4,51-4,66 (m, 2 H) 6,74 (dd, J=8,41, 1,76 Гц, 1 H) 6,83-6,93 (m, 2 H) 7,12-7,22 (m, 1 H) 7,85 (s, 1 H) 7,99 (s, 1 H) 8,22 (d, J=1,96 Гц, 1 H) 8,45 (d, J=1,96 Гц, 1 H);
[310] MS (ESI, масса/заряд): 422,2 [M+H]+
[311] Пример 34. 2-амино-N-((1R,2R)-2-((3-метоксибензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[312] Используя (1R,2R)-2-((3-метоксибензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[313] 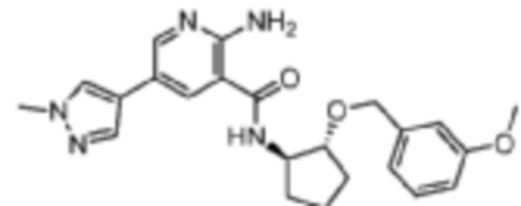
[314] MS (ESI, масса/заряд): 422,2 [M+H]+
[315] Пример 35. 2-амино-N-((1S,2S)-2-((4-метоксибензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[316] Используя (1S,2S)-2-((4-метоксибензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[317] 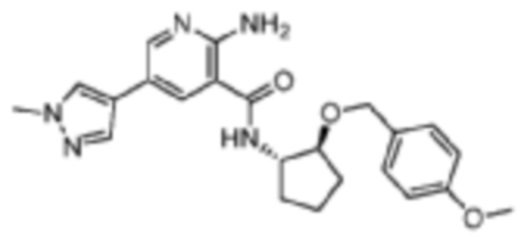
[318] MS (ESI, масса/заряд): 422,2 [M+H]+
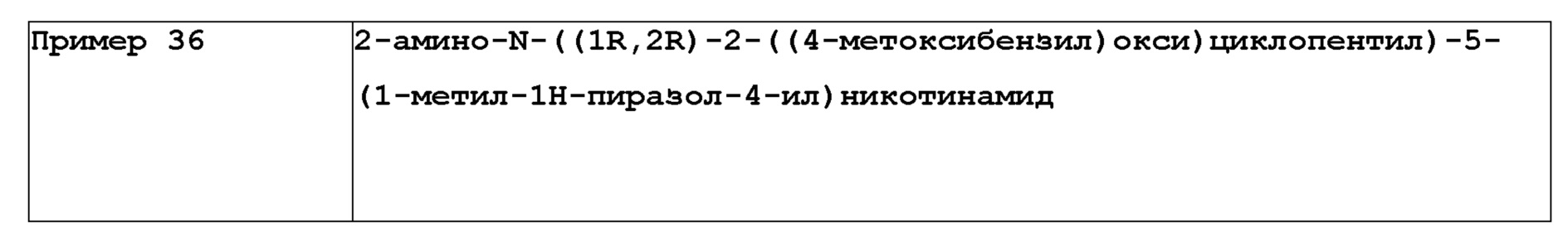
[319] Пример 36. 2-амино-N-((1R,2R)-2-((4-метоксибензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[320] Используя (1R,2R)-2-((4-метоксибензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[321] 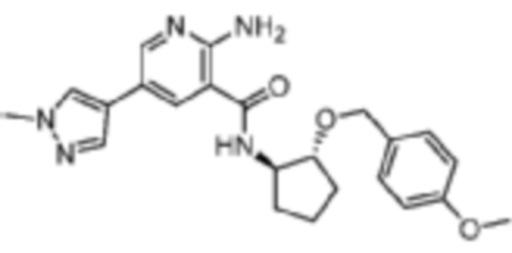
[322] MS (ESI, масса/заряд): 422,2 [M+H]+
[323] Пример 37. 2-амино-N-(транс-2-((3,5-диметоксибензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[324] Используя транс-2-((3,5-диметоксибензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[325] 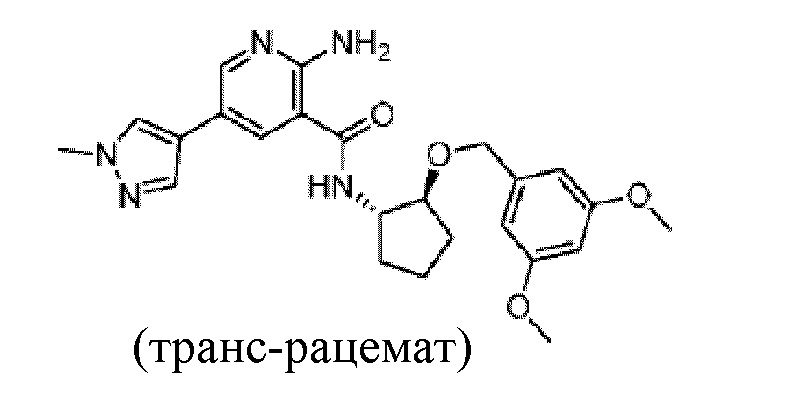
[326] MS (ESI, масса/заряд): 452,2 [M+H]+
[327] Пример 38. 2-амино-N-((1S,2S)-2-((2,3-диметоксибензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[328] Используя (1S,2S)-2-((2,3-диметоксибензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[329] 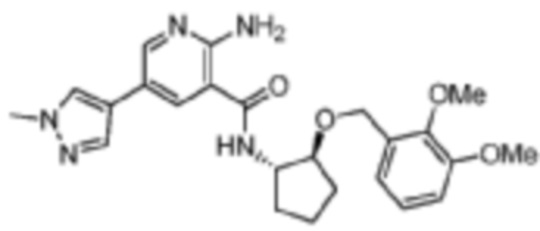
[330] MS (ESI, масса/заряд): 452,2 [M+H]+
[331] Пример 39. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((3-феноксибензил)окси)циклопентил)никотинамид
[332] Используя (1S,2S)-2-((3-феноксибензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[333] 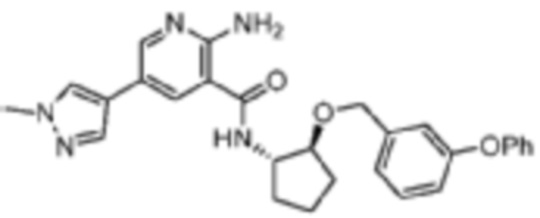
[334] MS (ESI, масса/заряд): 484,2 [M+H]+
[335] Пример 40. 2-амино-N-((1S,2S)-2-(бензо[d][1,3]диоксол-5-илметокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[336] Используя (1S,2S)-2-(бензо[d][1,3]диоксол-5-илметокси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[337] 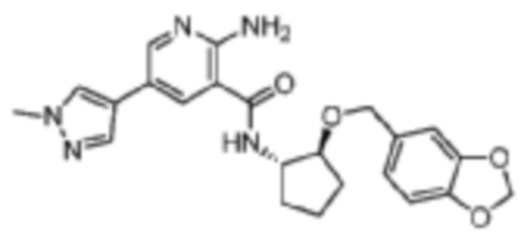
[338] MS (ESI, масса/заряд): 436,2 [M+H]+
[339] Пример 41. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4-(метилтио)бензил)окси)циклопентил)никотинамид
[340] Используя (1S,2S)-2-((4-(метилтио)бензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[341] 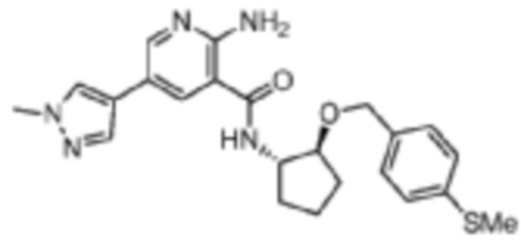
[342] MS (ESI, масса/заряд): 438,2 [M+H]+
[343] Пример 42. метил-3-((((1S,2S)-2-(2-амино-5-(1-метил-1H-пиразол-4-ил)никотинамидо)циклопентил)окси)метил)бензоат
[344] Используя метил-3-((((1S,2S)-2-аминоциклопентил)окси)метил)бензоат, названное соединение получали, как описано для примера 1.
[345] 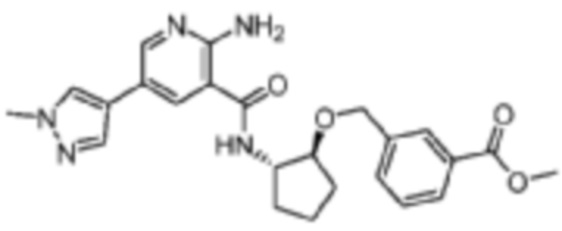
[346] MS (ESI, масса/заряд): 450,2 [M+H]+
[347] Пример 43. 2-амино-N-((1S,2S)-2-((3-хлорбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[348] Используя (1S,2S)-2-((3-хлорбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[349] 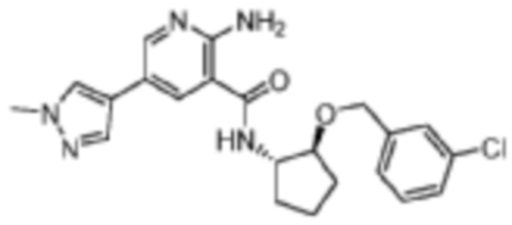
[350] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,62 (br dd, J=13,50, 6,46 Гц, 1 H) 1,72-1,87 (m, 3 H) 1,94-2,05 (m, 1 H) 2,16 (br d, J=6,65 Гц, 1 H) 3,89-3,97 (m, 4 H) 4,38 (br d, J=4,70 Гц, 1 H) 4,55-4,66 (m, 2 H) 7,20 (br s, 1 H) 7,22-7,28 (m, 2 H) 7,34 (s, 1 H) 7,85 (s, 1 H) 7,99 (s, 1 H) 8,22 (d, J=2,35 Гц, 1 H) 8,44 (br d, J=2,35 Гц, 1 H);
[351] MS (ESI, масса/заряд): 426,2 [M+H]+
[352] Пример 44. 2-амино-N-(транс-2-((3-хлорбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[353] Используя транс-2-((3-хлорбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[354] 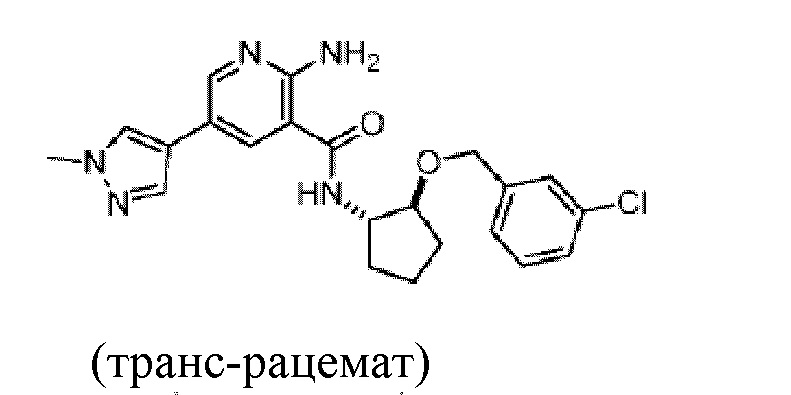
[355] MS (ESI, масса/заряд): 426,2 [M+H]+
[356] Пример 45. 2-амино-N-(транс-2-((4-хлорбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[357] Используя транс-2-((4-хлорбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[358] 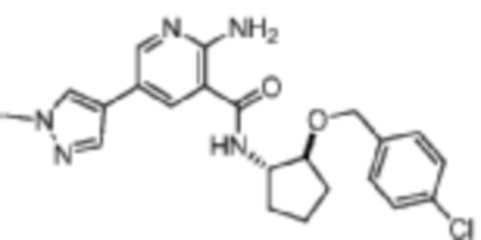
[359] MS (ESI, масса/заряд): 426,2 [M+H]+
[360] Пример 46. 2-амино-N-(транс-2-((3,4-дихлорбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[361] Используя транс-2-((3,4-дихлорбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[362] 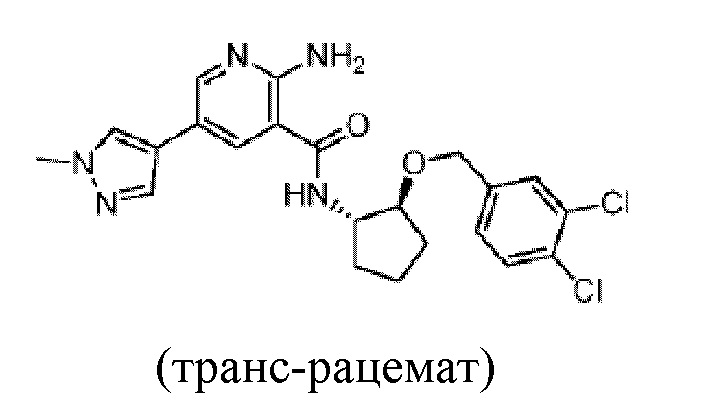
[363] MS (ESI, масса/заряд): 460,1 [M+H]+
[364] Пример 47. 2-амино-N-(транс-2-((2-фторбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[365] Используя транс-2-((2-фторбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[366] 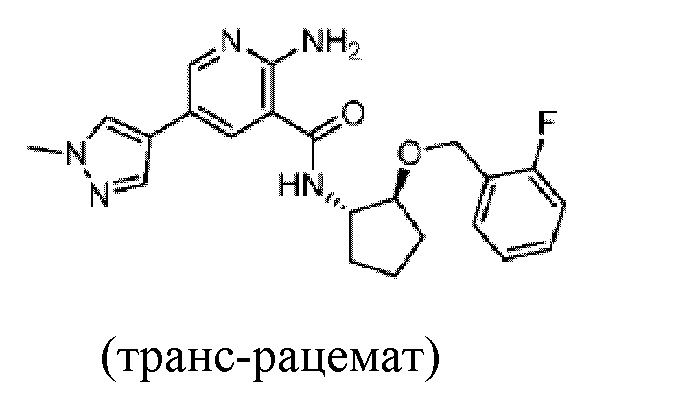
[367] Пример 48. 2-амино-N-((1S,2S)-2-((3-фторбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[368] Используя (1S,2S)-2-((3-фторбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[369] 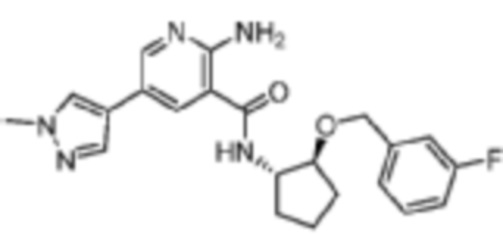
[370] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,63 (dq, J=13,69, 7,17 Гц, 1 H) 1,70-1,88 (m, 3 H) 1,93-2,06 (m, 1 H) 2,15 (dt, J=13,69, 6,85 Гц, 1 H) 3,87-4,00 (m, 4 H) 4,34-4,42 (m, 1 H) 4,62 (s, 2 H) 6,92 (td, J=8,61, 1,96 Гц, 1 H) 7,03-7,16 (m, 2 H) 7,27 (dd, J=8,02, 6,06 Гц, 1 H) 7,85 (s, 1 H) 8,00 (s, 1 H) 8,22 (d, J=1,96 Гц, 1 H) 8,49 (d, J=1,96 Гц, 1 H); MS (ESI, масса/заряд): 410,2 [M+H]+
[371] Пример 49. 2-амино-N-(транс-2-((4-бром-2-фторбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[372] Используя транс-2-((4-бром-2-фторбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[373] 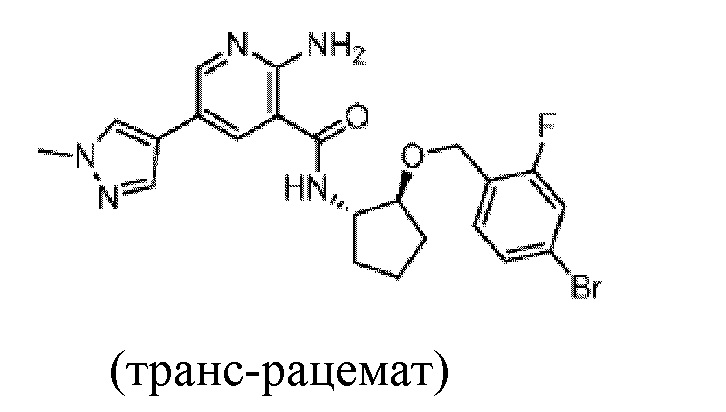
[374] MS (ESI, масса/заряд): 488,1/490,1 [M+H]+
[375] Пример 50. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-(транс-2-((2,4,5-трифторбензил)окси)циклопентил)никотинамид
[376] Используя транс-2-((2,4,5-трифторбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[377] 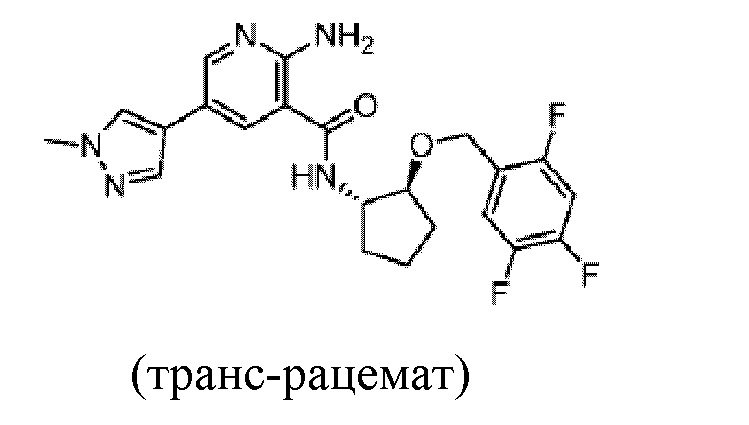
[378] MS (ESI, масса/заряд): 446,2 [M+H]+
[379] Пример 51. 2-амино-N-((1S,2S)-2-((3-бромбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[380] Используя (1S,2S)-2-((3-бромбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[381] 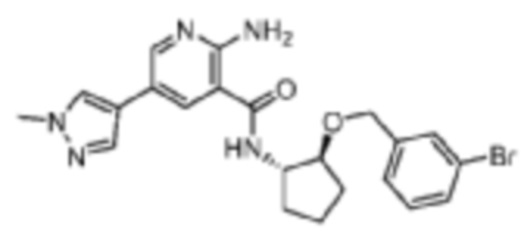
[382] MS (ESI, масса/заряд): 470,1/472,1 [M+H]+
[383] Пример 52. 2-амино-N-(транс-2-((3-бром-4-фторбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[384] Используя транс-2-((3-бром-4-фторбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[385] 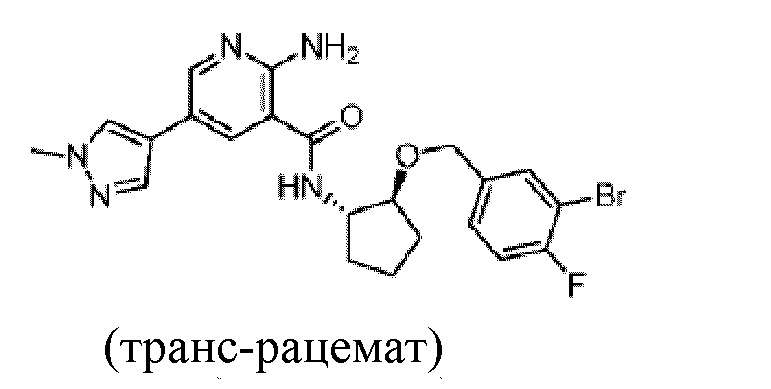
[386] MS (ESI, масса/заряд): 488,1/490,1 [M+H]+
[387] Пример 53. 2-амино-N-((1R,2R)-2-((3-бром-4-фторбензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[388] Используя (1R,2R)-2-((3-бром-4-фторбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[389] 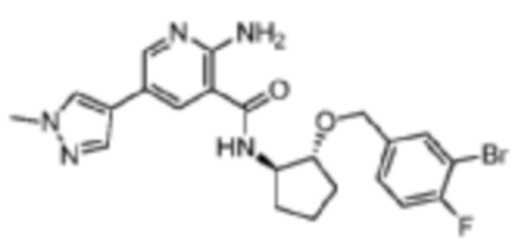
[390] MS (ESI, масса/заряд): 488,1/490,1 [M+H]+
[391] Пример 54. 2-амино-N-((1S,2S)-2-(1-(4-бромфенил)этокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[392] Используя (1S,2S)-2-(1-(4-бромфенил)этокси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[393] 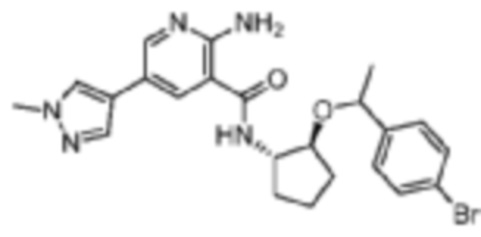
[394] MS (ESI, масса/заряд): 484,1/486,1 [M+H]+
[395] Пример 55. метил-(3-((((1S,2S)-2-(2-амино-5-(1-метил-1H-пиразол-4-ил)никотинамидо)циклопентил)окси)метил)бензоил)глицинат
[396] Используя метил-(3-((((1S,2S)-2-аминоциклопентил)окси)метил)бензоил)глицинат, названное соединение получали, как описано для примера 1.
[397] 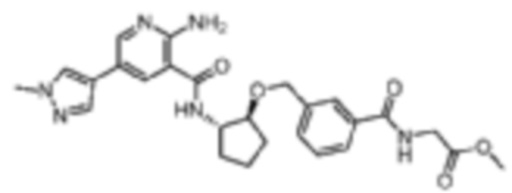
[398] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,58-1,70 (m, 1 H) 1,73-1,90 (m, 3 H) 1,95-2,07 (m, 1 H) 2,11-2,22 (m, 1 H) 3,88-3,98 (m, 4 H) 4,36-4,44 (m, 1 H) 4,61-4,72 (m, 2 H) 7,43-7,51 (m, 1 H) 7,57 (br d, J=7,43 Гц, 1 H) 7,63 (br d, J=7,43 Гц, 1 H) 7,70 (s, 1 H) 7,85 (s, 1 H) 7,99 (s, 1 H) 8,23 (d, J=1,96 Гц, 1 H) 8,45 (d, J=1,96 Гц, 1 H);
[399] MS (ESI, масса/заряд): 507,2 [M+H]+
[400] Пример 56. 2-амино-N-((1S,2S)-2-((3-((2-гидроксиэтил)карбамоил)бензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[401] Используя метил-(3-((((1S,2S)-2-аминоциклопентил)окси)метил)-N-(2-гидроксиэтил)бензамид, названное соединение получали, как описано для примера 1.
[402] 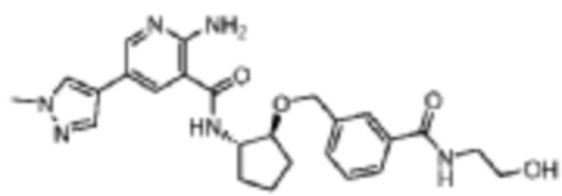
[403] MS (ESI, масса/заряд): 479,2 [M+H]+
[404] Пример 57. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((3-(пиперидин-4-карбоксамидо)бензил)окси)циклопентил)никотинамид
[405] Используя трет-бутил-4-((3-((((1S,2S)-2-аминоциклопентил)окси)метил)фенил)карбамоил)пиперидин-1-карбоксилат, названное соединение получали, как описано для примера 1 и после снятия защитных групп при помощи TFA.
[406] 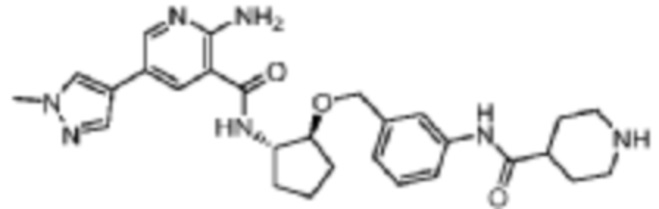
[407] MS (ESI, масса/заряд): 518,3 [M+H]+
[408] Пример 58. 2-амино-N-((1S,2S)-2-((3-((S)-2-аминопропанамидо)бензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[409] Используя трет-бутил-((S)-1-((3-((((1S,2S)-2-аминоциклопентил)окси)метил)фенил)амино)-1-оксопропан-2-ил)карбамат, названное соединение получали, как описано для примера 1 и после снятия защитных групп при помощи TFA.
[410] 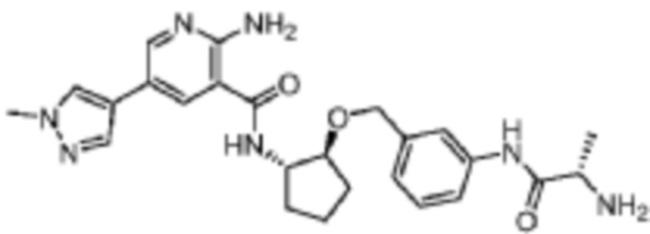
[411] MS (ESI, масса/заряд): 478,3 [M+H]+
[412] Пример 59. N-((1S,2S)-2-((3-((S)-2-ацетамидопропанамидо)бензил)окси)циклопентил)-2-амино-5-(1-метил-1H-пиразол-4-ил)никотинамид
[413] Используя (S)-2-ацетамидо-N-(3-((((1S,2S)-2-аминоциклопентил)окси)метил)фенил)пропанамид, названное соединение получали, как описано для примера 1.
[414] 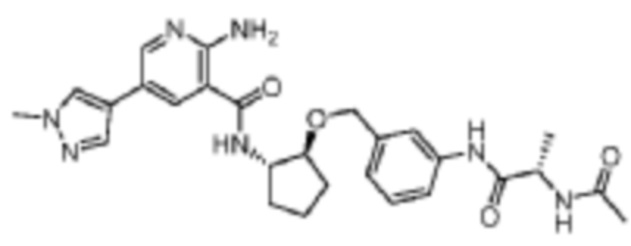
[415] MS (ESI, масса/заряд): 520,3 [M+H]+
[416] Пример 60. 2-амино-N-((1S,2S)-2-((3-(3-аминопропанамидо)бензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[417] Используя трет-бутитл-(3-((3-((((1S,2S)-2-аминоциклопентил)окси)метил)фенил)амино)-3-оксопропил)карбамат, названное соединение получали, как описано для примера 1 и после снятия защитных групп при помощи TFA.
[418] 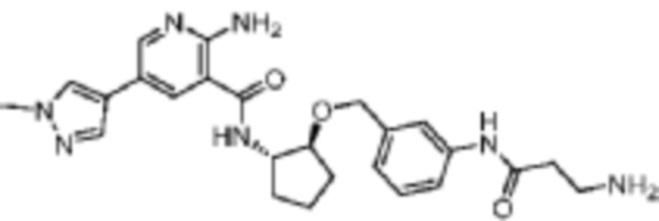
[419] MS (ESI, масса/заряд): 478,3 [M+H]+
[420] Пример 61. N-((1S,2S)-2-((3-(2H-1,2,3-триазол-2-ил)бензил)окси)циклопентил)-2-амино-5-(1-метил-1H-пиразол-4-ил)никотинамид
[421] Используя (1S,2S)-2-((3-(2H-1,2,3-триазол-2-ил)бензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[422] 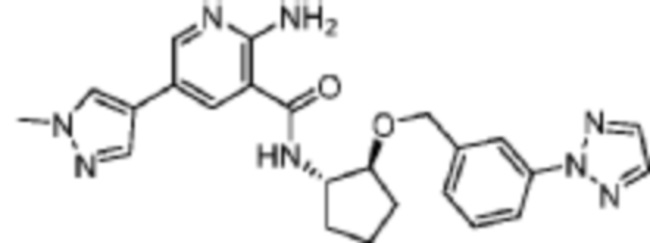
[423] MS (ESI, масса/заряд): 459,2 [M+H]+
[424] Пример 62. N-((1S,2S)-2-((4-(2H-1,2,3-триазол-2-ил)бензил)окси)циклопентил)-2-амино-5-(1-метил-1H-пиразол-4-ил)никотинамид
[425] Используя (1S,2S)-2-((4-(2H-1,2,3-триазол-2-ил)бензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[426] 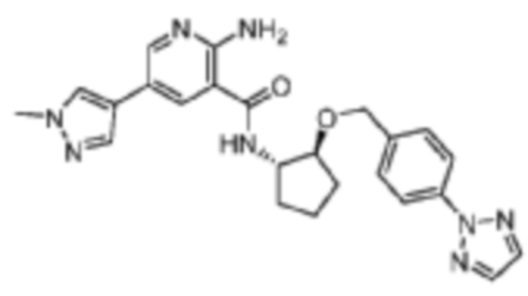
[427] MS (ESI, масса/заряд): 459,2 [M+H]+
[428] Пример 63. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-(нафталин-2-илметокси)циклопентил)никотинамид
[429] Используя (1S,2S)-2-(нафталин-2-илметокси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[430] 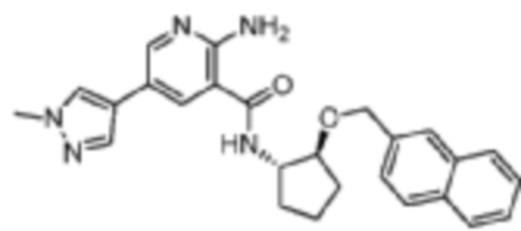
[431] MS (ESI, масса/заряд): 442,2 [M+H]+
[432] Пример 64. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-(хинолин-8-илметокси)циклопентил)никотинамид
[433] Используя (1S,2S)-2-(хинолин-8-илметокси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[434] 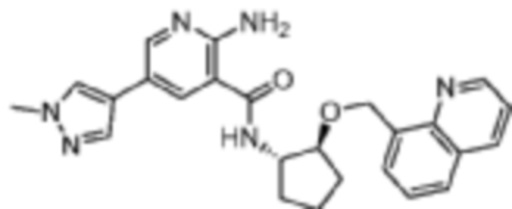
[435] MS (ESI, масса/заряд): 443,2 [M+H]+
[436] Пример 65. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((2',3',4',5'-тетрагидро-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[437] Используя (1S,2S)-2-((2',3',4',5'-тетрагидро-[1,1'-бифенил]-4-ил)метокси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[438] 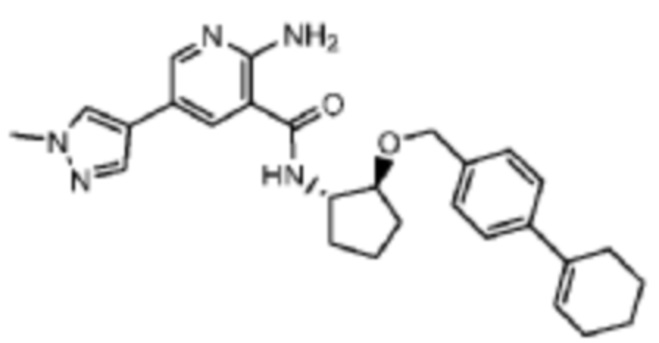
[439] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,62 (br d, J=5,87 Гц, 2 H) 1,67-1,87 (m, 5 H) 1,93-2,09 (m, 2 H) 2,14 (br s, 3 H) 2,28 (br s, 2 H) 3,92 (s, 3 H) 4,37 (br d, J=5,48 Гц, 1 H) 4,49-4,65 (m, 2 H) 6,00 (br s, 1 H) 7,18-7,30 (m, 2 H) 7,54 (br s, 1 H) 7,59-7,69 (m, 1 H) 7,84 (s, 1 H) 7,98 (s, 1 H) 8,23 (s, 1 H) 8,38 (s, 1 H);
[440] MS (ESI, масса/заряд): 472,3 [M+H]+
[441] Пример 66. N-(транс-2-([1,1'-бифенил]-2-илметокси)циклопентил)-2-амино-5-(1-метил-1H-пиразол-4-ил)никотинамид
[442] Используя транс-2-([1,1'-бифенил]-2-илметокси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[443]
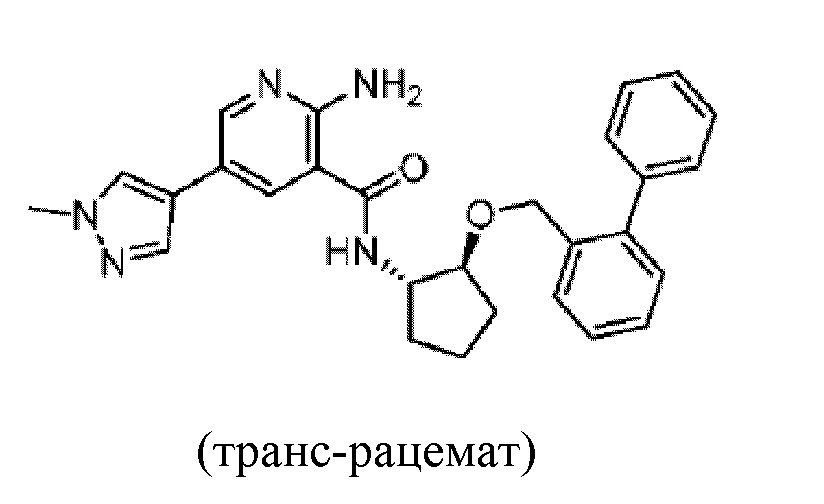
[444] MS (ESI, масса/заряд): 468,2 [M+H]+
[445] Пример 67. N-((1S,2S)-2-([1,1'-бифенил]-3-илметокси)циклопентил)-2-амино-5-(1-метил-1H-пиразол-4-ил)никотинамид
[446] Используя (1S,2S)-2-([1,1'-бифенил]-3-илметокси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[447] 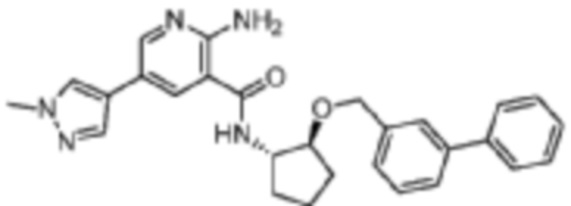
[448] MS (ESI, масса/заряд): 468,2 [M+H]+
[449] Пример 68. N-((1S,2S)-2-([1,1'-бифенил]-4-илметокси)циклопентил)-2-амино-5-(1-метил-1H-пиразол-4-ил)никотинамид
[450] Используя (1S,2S)-3-([1,1'-бифенил]-4-илметокси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[451] 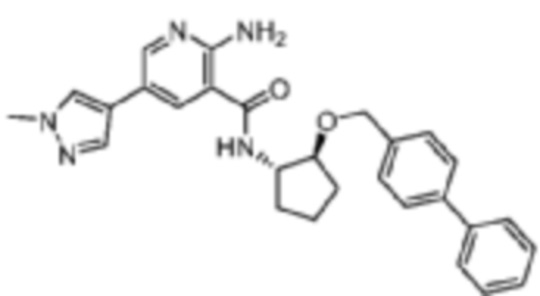
[452] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,59 (br d, J=1,17 Гц, 1 H) 1,79 (br s, 3 H) 1,97 (br s, 1 H) 2,11-2,21 (m, 1 H) 3,62 (s, 2 H) 3,87 (s, 3 H) 3,97 (br s, 1 H) 4,39 (br s, 1 H) 4,65 (br d, J=13,69 Гц, 2 H) 7,34-7,42 (m, 2 H) 7,50 (br t, J=7,43 Гц, 2 H) 7,80 (s, 1 H) 7,90 (s, 1 H) 8,17 (br s, 1 H) 8,29-8,34 (m, 1 H);
[453] MS (ESI, масса/заряд): 468,2 [M+H]+
[454] Пример 69. 2-амино-N-((1S,2S)-2-гидроксициклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[455] Используя (1S,2S)-2-аминоциклопентан-1-ол, названное соединение получали, как описано для примера 1.
[456] 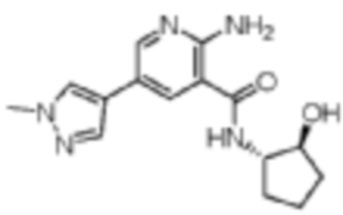
[457] MS (ESI, масса/заряд): 302,2 [M+H]+
[458] Пример 70. 2-амино-N-(цис-2-гидроксициклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[459] Используя цис-2-аминоциклопентан-1-ол, названное соединение получали, как описано для примера 1.
[460] 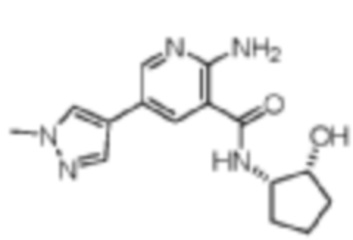
[461] MS (ESI, масса/заряд): 302,2 [M+H]+
[462] Пример 71. N-((1S,2S)-2-(бензилокси)циклопентил)-2-(этиламино)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[463] Используя 2-(этиламино)-5-(1-метил-1H-пиразол-4-ил)никотиновую кислоту, названное соединение получали, как описано для примера 1.
[464] 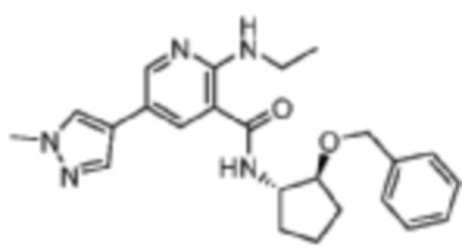
[465] MS (ESI, масса/заряд): 420,2 [M+H]+
[466] Пример 72. N-((1S,2S)-2-(бензилокси)циклопентил)-2-((3,4-диметилбензил)амино)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[467] Используя 2-((3,4-диметилбензил)амино)-5-(1-метил-1H-пиразол-4-ил)никотиновую кислоту, названное соединение получали, как описано для примера 1.
[468] 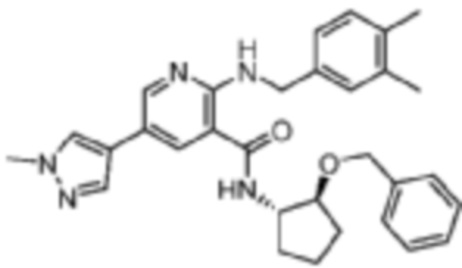
[469] MS (ESI, масса/заряд): 510,3 [M+H]+
[470] Пример 73. 2-амино-N-((6R,7S)-6-(бензилокси)-1,4-диоксаспиро[4.4]нонан-7-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[471] Используя (6R,7S)-6-(бензилокси)-1,4-диоксаспиро[4.4]нонан-7-амин, названное соединение получали, как описано для примера 1.
[472] 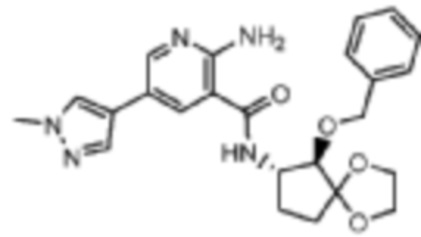
[473] MS (ESI, масса/заряд): 450,2 [M+H]+
[474] Пример 74. 2-амино-N-(транс-2-(бензилокси)циклогексил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[475] Используя транс-2-(бензилокси)циклогексан-1-амин, названное соединение получали, как описано для примера 1.
[476] 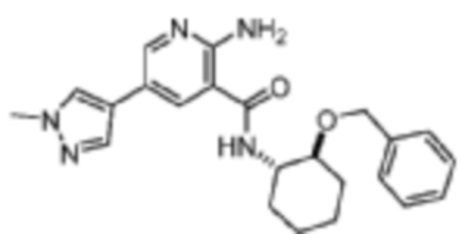
[477] MS (ESI, масса/заряд): 406,2 [M+H]+
[478] Пример 75. 2-амино-N-((1S,2S)-2-(бензилокси)циклогексил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[479] Используя (1S,2S)-2-(бензилокси)циклогексан-1-амин, названное соединение получали, как описано для примера 1.
[480] 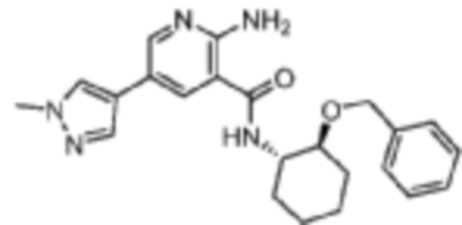
[481] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,28-1,47 (m, 4 H) 1,77 (br s, 1 H) 1,83 (br s, 1 H) 1,97 (s, 1 H) 2,29 (br s, 1 H) 3,38 (br d, J=9,39 Гц, 1 H) 3,92 (s, 3 H) 3,99 (br d, J=10,17 Гц, 1 H) 4,41-4,47 (m, 1 H) 4,68 (br d, J=12,13 Гц, 1 H) 7,13 (dt, J=14,57, 6,99 Гц, 3 H) 7,25 (br d, J=7,43 Гц, 2 H) 7,77 (s, 1 H) 7,89 (s, 1 H) 8,21 (s, 1 H) 8,25 (br s, 1 H);
[482] MS (ESI, масса/заряд): 406,2 [M+H]+
[483] Пример 76. 2-амино-N-(транс-2-(бензил(метил)амино)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[484] Используя транс-N1-бензил-N1-метилциклопентан-1,2-диамин, названное соединение получали, как описано для примера 1.
[485] 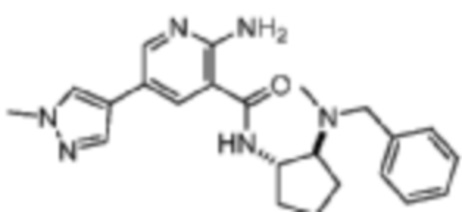
[486] MS (ESI, масса/заряд): 405,2 [M+H]+
[487] Пример 77. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-(феноксиметил)циклопентил)никотинамид
[488] Используя (1S,2S)-2-(феноксиметил)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[489] 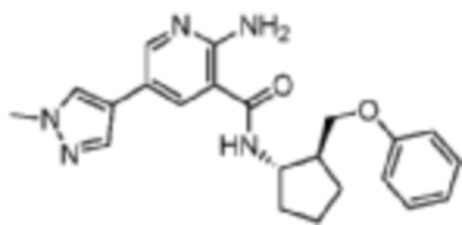
[490] MS (ESI, масса/заряд): 392,2 [M+H]+
[491] Пример 78. 2-амино-N-((1S,2S)-2-((3,4-диметилфенокси)метил)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[492] Используя (1S,2S)-2-((3,4-диметилфенокси)метил)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[493] 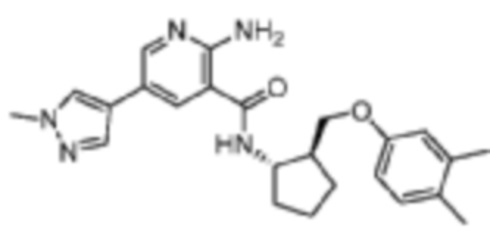
[494] MS (ESI, масса/заряд): 420,2 [M+H]+
[495] Пример 79. 2-амино-N-(транс-2,2-дифтор-5-(феноксиметил)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[496] Используя (транс-2,2-дифтор-5-(феноксиметил)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[497] 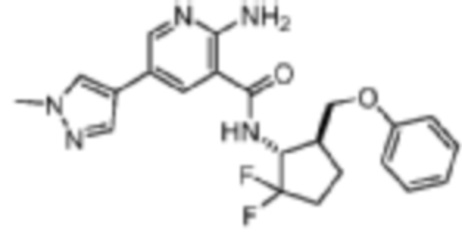
[498] MS (ESI, масса/заряд): 428,2 [M+H]+
[499] Пример 80. 2-амино-N-((1S,2S)-2-(((2,3-дигидро-1H-инден-5-ил)окси)метил)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[500] Используя (1S,2S)-2-(((2,3-дигидро-1H-инден-5-ил)окси)метил)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[501] 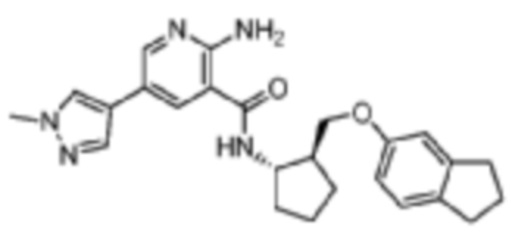
[502] MS (ESI, масса/заряд): 432,2 [M+H]+
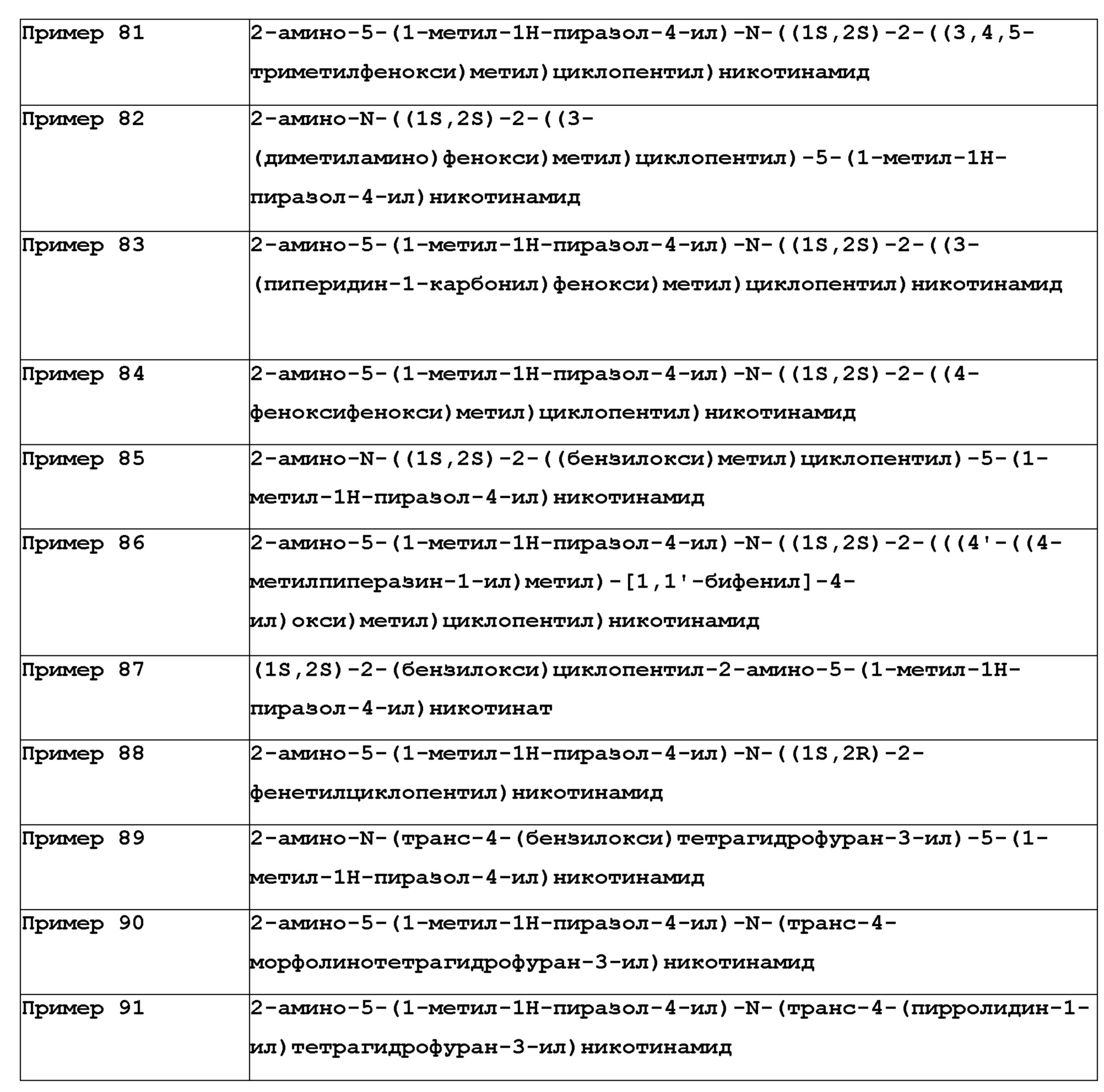
[503] Пример 81. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((3,4,5-триметилфенокси)метил)циклопентил)никотинамид
[504] Используя (1S,2S)-2-((3,4,5-триметилфенокси)метил)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[505] 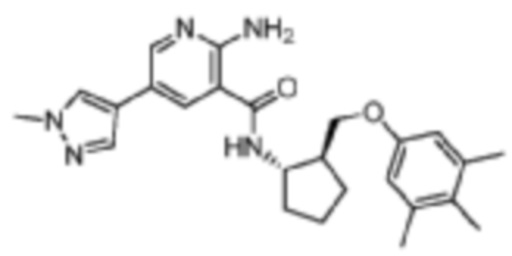
[506] MS (ESI, масса/заряд): 434,3 [M+H]+
[507] Пример 82. 2-амино-N-((1S,2S)-2-((3-(диметиламино)фенокси)метил)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[508] Используя 3-(((1S,2S)-2-аминоциклопентил)метокси)-N,N-диметиланилин, названное соединение получали, как описано для примера 1.
[509] 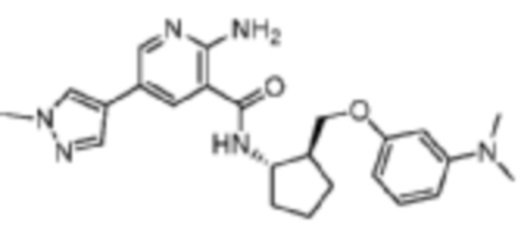
[510] MS (ESI, масса/заряд): 435,2 [M+H]+
[511] Пример 83. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((3-(пиперидин-1-карбонил)фенокси)метил)циклопентил)никотинамид
[512] Используя (3-(((1S,2S)-2-аминоциклопентил)метокси)фенил)(пиперидин-1-ил)метанон, названное соединение получали, как описано для примера 1.
[513] 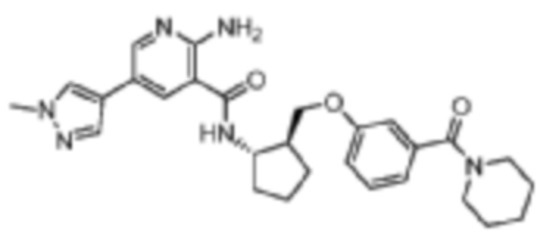
[514] MS (ESI, масса/заряд): 503,3 [M+H]+
[515] Пример 84. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4-феноксифенокси)метил)циклопентил)никотинамид
[516] Используя (1S,2S)-2-((4-феноксифенокси)метил)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[517] 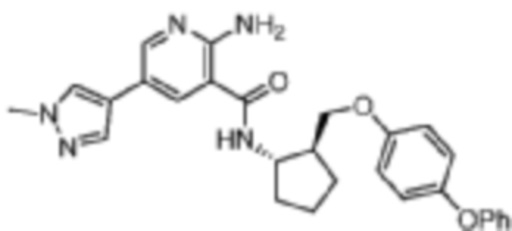
[518] MS (ESI, масса/заряд): 484,2 [M+H]+
[519] Пример 85. 2-амино-N-((1S,2S)-2-((бензилокси)метил)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[520] Используя (1S,2S)-2-((бензилокси)метил)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[521] 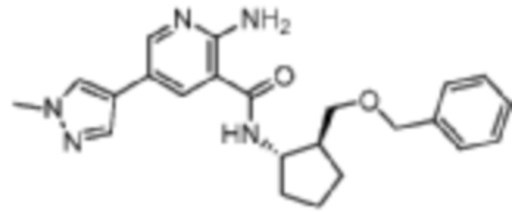
[522] MS (ESI, масса/заряд): 406,2 [M+H]+
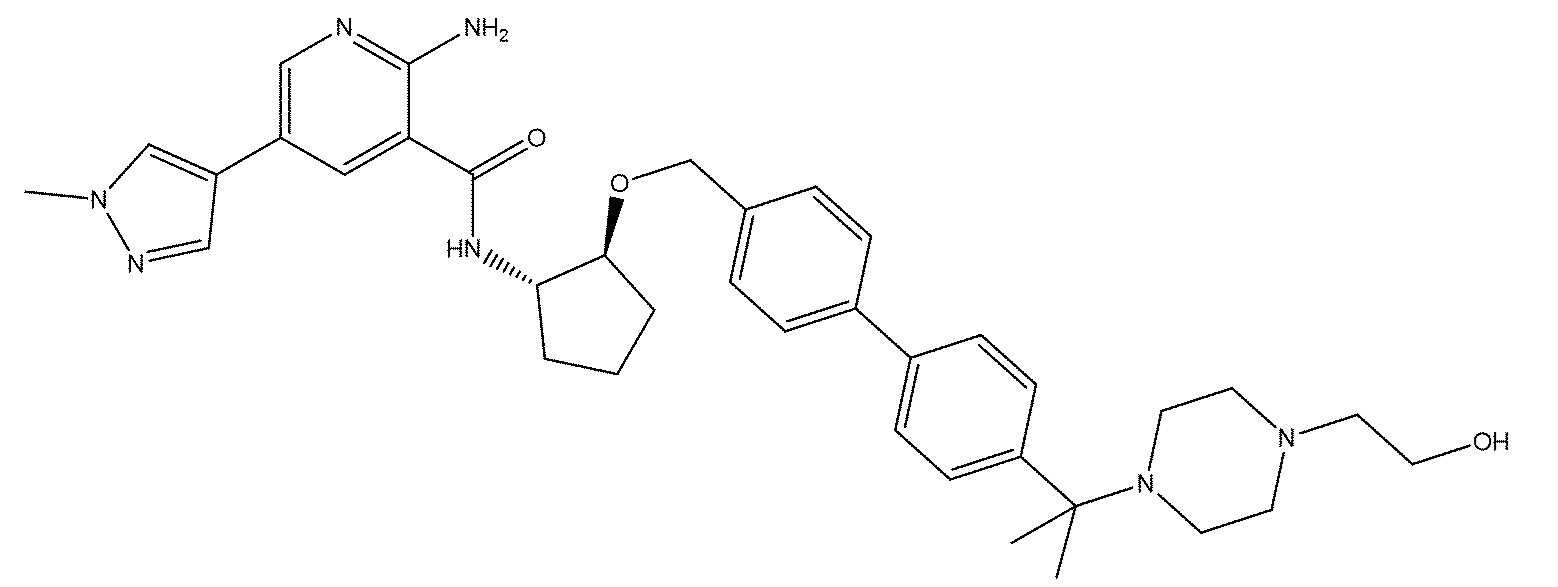
[523] Пример 86. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-(((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)окси)метил)циклопентил)никотинамид
[524] Используя (1S,2S)-2-(((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)окси)метил)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[525] 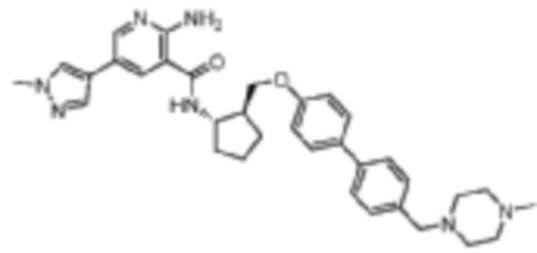
[526] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,56-1,65 (m, 1 H) 1,67-1,75 (m, 1 H) 1,79 (br d, J=6,46 Гц, 1 H) 1,85 (br d, J=8,80 Гц, 1 H) 2,03-2,12 (m, 1 H) 2,16 (br dd, J=12,91, 5,87 Гц, 1 H) 2,43-2,51 (m, 1 H) 2,84 (s, 3 H) 3,75 (s, 2 H) 3,89 (s, 3 H) 4,10 (d, J=5,87 Гц, 2 H) 4,30-4,38 (m, 1 H) 6,96 (d, J=8,80 Гц, 2 H) 7,38 (br d, J=8,22 Гц, 2 H) 7,50 (dd, J=16,43, 8,22 Гц, 4 H) 7,86 (s, 1 H) 7,98 (s, 1 H) 8,21 (d, J=2,35 Гц, 1 H) 8,51 (d, J=2,35 Гц, 1 H);
[527] MS (ESI, масса/заряд): 580,3 [M+H]+
[528] Пример 87. (1S,2S)-2-(бензилокси)циклопентил-2-амино-5-(1-метил-1H-пиразол-4-ил)никотинат
[529] Используя (1S,2S)-2-(бензилокси)циклопентан-1-ол, названное соединение получали, как описано для примера 1.
[530] 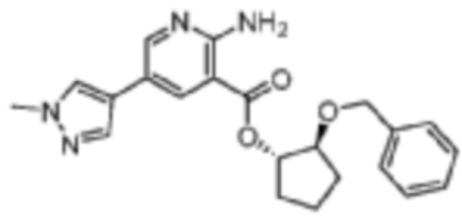
[531] MS (ESI, масса/заряд): 393,2 [M+H]+
[532] Пример 88. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2R)-2-фенетилциклопентил)никотинамид
[533] Используя (1S,2R)-2-фенетилциклопентан-1-амин, названное соединение получали, как описано для примера 1.
[534] 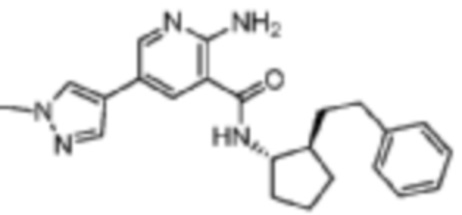
[535] MS (ESI, масса/заряд): 390,2 [M+H]+
[536] Пример 89. 2-амино-N-(транс-4-(бензилокси)тетрагидрофуран-3-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[537] Используя транс-4-(бензилокси)тетрагидрофуран-3-амин, названное соединение получали, как описано для примера 1.
[538] 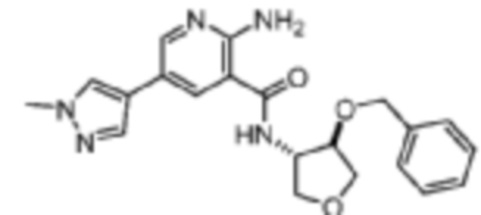
[539] MS (ESI, масса/заряд): 394,2 [M+H]+
[540] Пример 90. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-(транс-4-морфолинотетрагидрофуран-3-ил)никотинамид
[541] Используя транс-4-морфолинотетрагидрофуран-3-амин, названное соединение получали, как описано для примера 1.
[542] 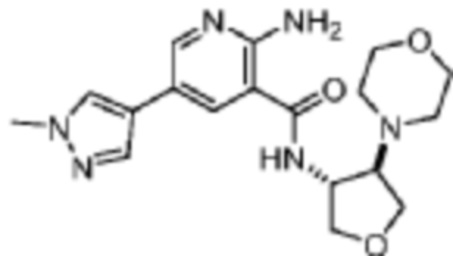
[543] MS (ESI, масса/заряд): 373,2 [M+H]+
[544] Пример 91. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-(транс-4-(пирролидин-1-ил)тетрагидрофуран-3-ил)никотинамид
[545] Используя транс-4-(пирролидин-1-ил)тетрагидрофуран-3-амин, названное соединение получали, как описано для примера 1.
[546] 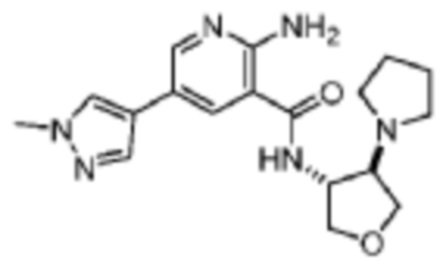
[547] MS (ESI, масса/заряд): 357,2 [M+H]+
[548] Пример 92. 2-амино-N-(цис-4-гидрокситетрагидрофуран-3-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[549] Используя цис-4-аминотетрагидрофуран-3-ол, названное соединение получали, как описано для примера 1.
[550] 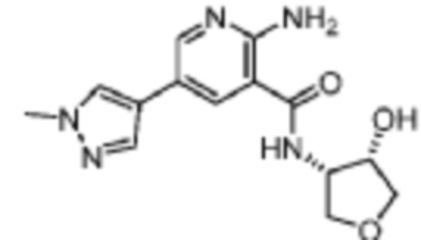
[551] MS (ESI, масса/заряд): 304,1 [M+H]+
[552] Пример 93. 2-амино-N-(4-(бензилокси)-1-метилпирролидин-3-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[553] Используя транс-4-(бензилокси)-1-метилпирролидин-3-амин, названное соединение получали, как описано для примера 1.
[554] 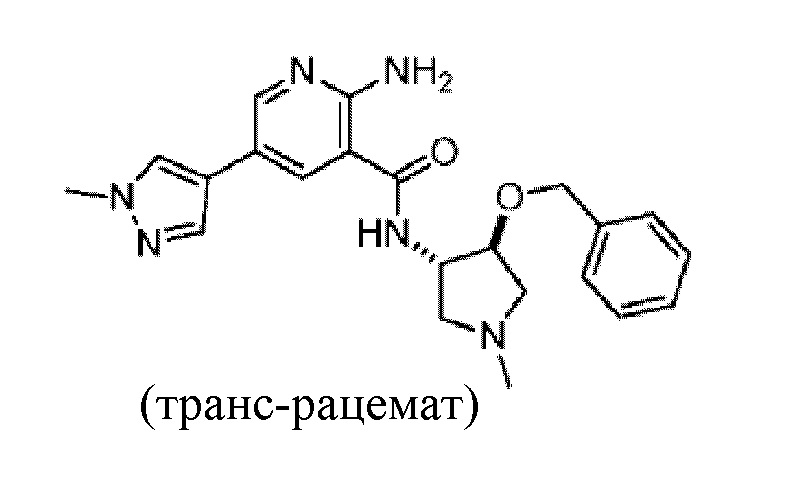
[555] MS (ESI, масса/заряд): 407,2 [M+H]+
[556] Пример 94. 2-амино-N-(транс-4-(бензилокси)-1-изопропилпирролидин-3-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[557] Используя транс-4-(бензилокси)-1-изопропилпирролидин-3-амин, названное соединение получали, как описано для примера 1.
[558] 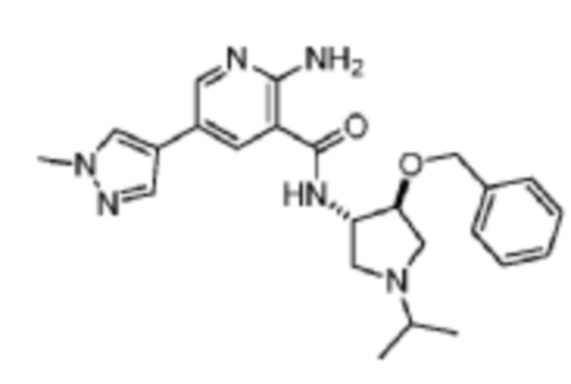
[559] MS (ESI, масса/заряд): 435,2 [M+H]+
[560] Пример 95. (R)-2-амино-N-(2-(бензилокси)пропил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[561] Используя (R)-2-(бензилокси)пропан-1-амин, названное соединение получали, как описано для примера 1.
[562] 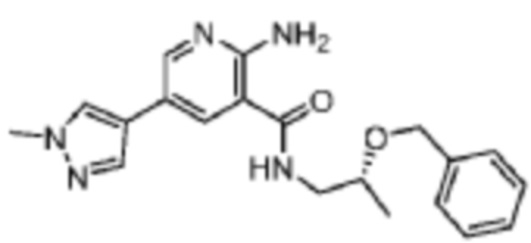
[563] MS (ESI, масса/заряд): 366,2 [M+H]+
[564] Пример 96. (S)-2-амино-N-(2-(бензилокси)пропил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[565] Используя (S)-2-(бензилокси)пропан-1-амин, названное соединение получали, как описано для примера 1.
[566] 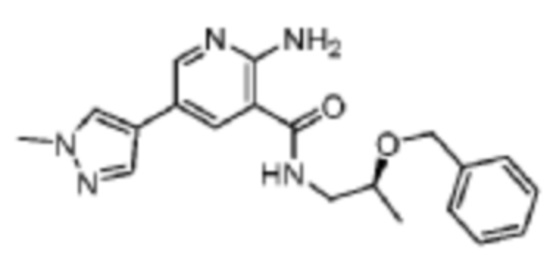
[567] MS (ESI, масса/заряд): 366,2 [M+H]+
[568] Пример 97. (S)-2-амино-N-(1-(бензилокси)пропан-2-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[569] Используя (S)-1-(бензилокси)пропан-2-амин, названное соединение получали, как описано для примера 1.
[570] 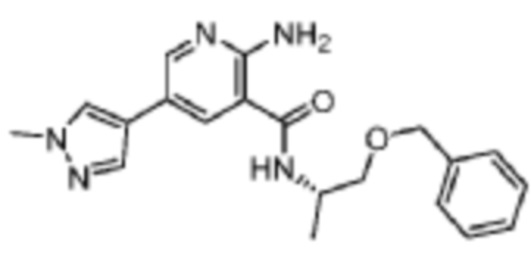
[571] MS (ESI, масса/заряд): 366,2 [M+H]+
[572] Пример 98. (R)-2-амино-N-(1-(бензилокси)пропан-2-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[573] Используя (R)-1-(бензилокси)пропан-2-амин, названное соединение получали, как описано для примера 1.
[574] 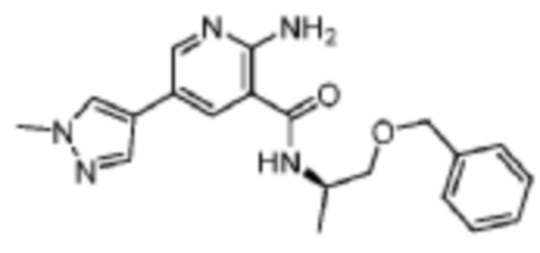
[575] MS (ESI, масса/заряд): 366,2 [M+H]+
[576] Пример 99. 2-амино-N-(1-(бензилокси)-2-метилпропан-2-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[577] Используя 1-(бензилокси)-2-метилпропан-2-амин, названное соединение получали, как описано для примера 1.
[578] 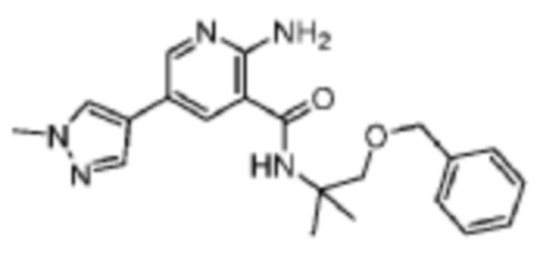
[579] MS (ESI, масса/заряд): 380,2 [M+H]+
[580] Пример 100. (R)-2-амино-N-(1-((3,4-диметилбензил)окси)пропан-2-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[581] Используя (R)-1-((3,4-диметилбензил)окси)пропан-2-амин, названное соединение получали, как описано для примера 1.
[582] 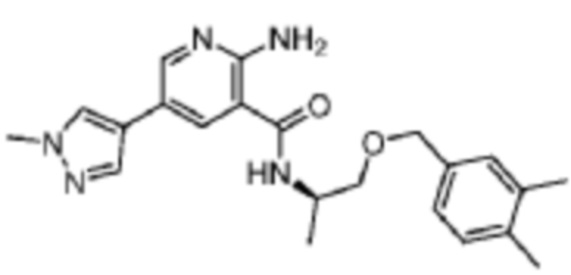
[583] MS (ESI, масса/заряд): 394,2 [M+H]+
[584] Пример 101. (S)-2-амино-N-(2-((3,4-диметилбензил)окси)пропил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[585] Используя (S)-2-((3,4-диметилбензил)окси)пропан-1-амин, названное соединение получали, как описано для примера 1.
[586] 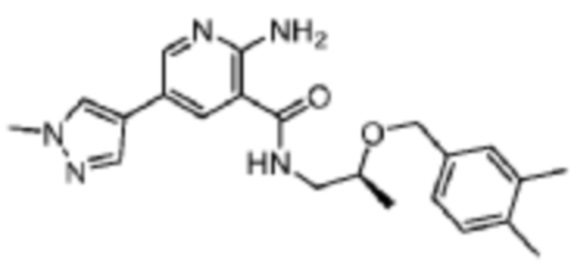
[587] MS (ESI, масса/заряд): 394,2 [M+H]+
[588] Пример 102. (R)-2-амино-N-(1-((4-хлорбензил)окси)пропан-2-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[589] Используя (R)-1-((4-хлорбензил)окси)пропан-2-амин, названное соединение получали, как описано для примера 1.
[590] 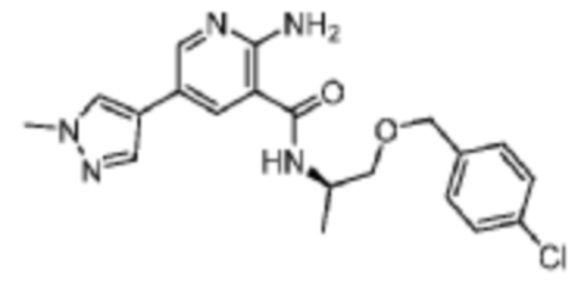
[591] MS (ESI, масса/заряд): 400,2 [M+H]+
[592] Пример 103. (S)-2-амино-N-(2-((4-хлорбензил)окси)пропил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[593] Используя (S)-2-((4-хлорбензил)окси)пропан-1-амин, названное соединение получали, как описано для примера 1.
[594] 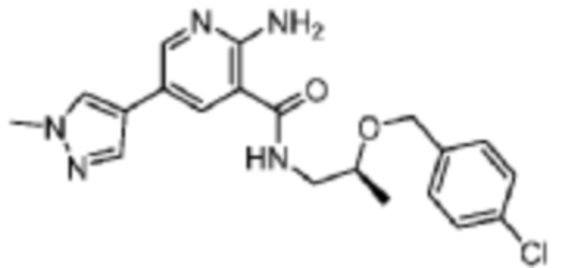
[595] MS (ESI, масса/заряд): 400,2 [M+H]+
[596] Пример 104. (R)-2-амино-N-(1-((3,4-дихлорбензил)окси)пропан-2-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[597] Используя (R)-1-((3,4-дихлорбензил)окси)пропан-2-амин, названное соединение получали, как описано для примера 1.
[598] 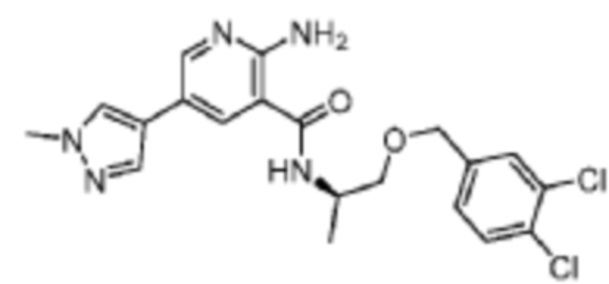
[599] MS (ESI, масса/заряд): 434,1 [M+H]+
[600] Пример 105. (S)-2-амино-N-(2-((3,4-дихлорбензил)окси)пропил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[601] Используя (S)-2-((3,4-дихлорбензил)окси)пропан-1-амин, названное соединение получали, как описано для примера 1.
[602] 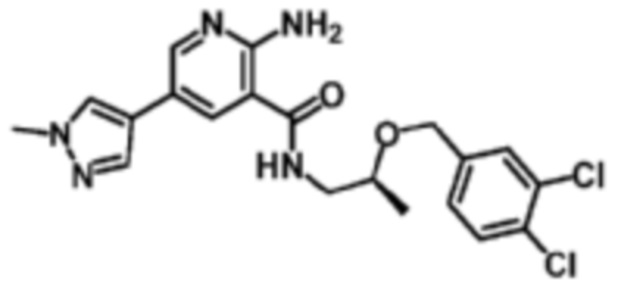
[603] MS (ESI, масса/заряд): 419,1 [M+H]+
[604] Пример 106. (R)-2-амино-N-(1-((3-метоксибензил)окси)пропан-2-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[605] Используя (R)-1-((3-метоксибензил)окси)пропан-2-амин, названное соединение получали, как описано для примера 1.
[606] 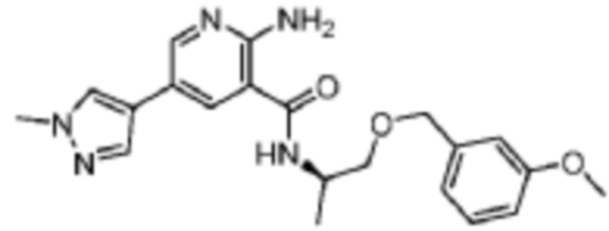
[607] MS (ESI, масса/заряд): 396,2 [M+H]+.
[608] Пример 107. (S)-2-амино-N-(2-((3-метоксибензил)окси)пропил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[609] Используя (S)-2-((3-метоксибензил)окси)пропан-1-амин, названное соединение получали, как описано для примера 1.
[610] 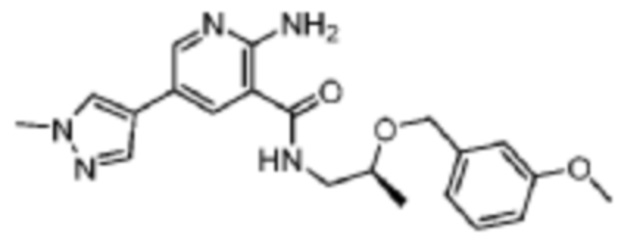
[611] MS (ESI, масса/заряд): 396,2 [M+H]+
[612] Пример 108. (R)-2-амино-N-(1-(бензилокси)бутан-2-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[613] Используя (R)-1-(бензилокси)бутан-2-амин, названное соединение получали, как описано для примера 1.
[614] 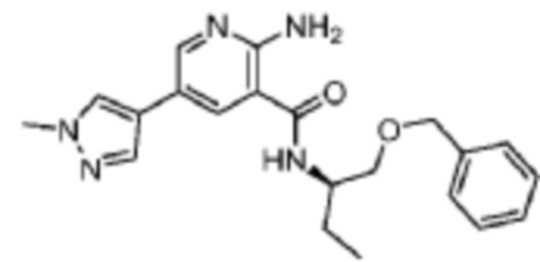
[615] MS (ESI, масса/заряд): 380,2 [M+H]+
[616] Пример 109. (S)-2-амино-N-(1-(бензилокси)-3-метилбутан-2-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[617] Используя (S)-1-(бензилокси)-3-метилбутан-2-амин, названное соединение получали, как описано для примера 1.
[618] 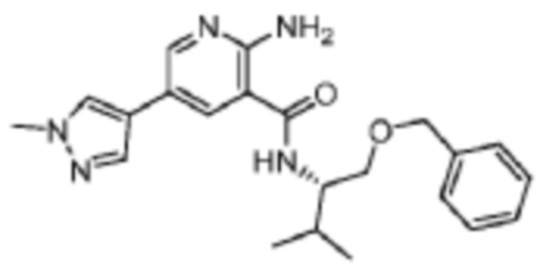
[619] MS (ESI, масса/заряд): 394,2 [M+H]+
[620] Пример 110. (R)-2-амино-N-(1-(бензилокси)-3-метилбутан-2-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[621] Используя (R)-1-(бензилокси)-3-метилбутан-2-амин, названное соединение получали, как описано для примера 1.
[622] 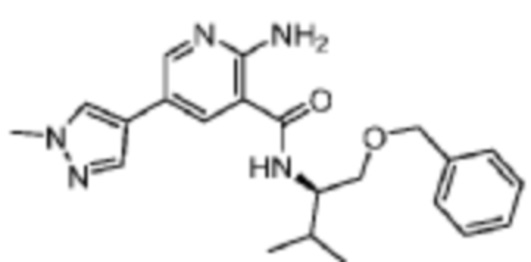
[623] MS (ESI, масса/заряд): 394,2 [M+H]+
[624] Пример 111. (S)-2-амино-N-(1-(бензилокси)-4-метилпентан-2-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[625] Используя (S)-1-(бензилокси)-4-метилпентан-2-амин, названное соединение получали, как описано для примера 1.
[626] 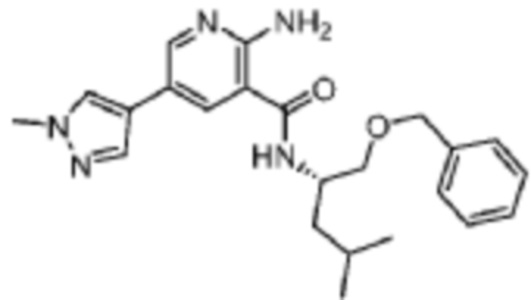
[627] MS (ESI, масса/заряд): 408,2 [M+H]+
[628] Пример 112. (R)-2-амино-N-(1-(бензилокси)-4-метилпентан-2-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[629] Используя (R)-1-(бензилокси)-4-метилпентан-2-амин, названное соединение получали, как описано для примера 1.
[630] 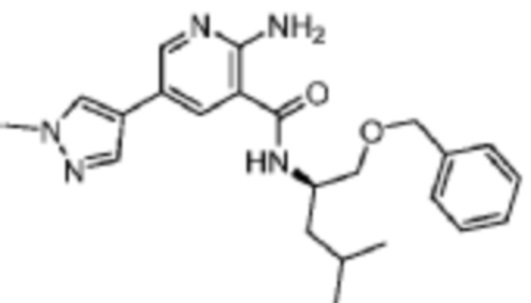
[631] MS (ESI, масса/заряд): 408,2 [M+H]+
[632] Пример 113. (R)-2-амино-N-(2-(бензилокси)-1-циклогексилэтил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[633] Используя (R)-2-(бензилокси)-1-циклогексилэтан-1-амин, названное соединение получали, как описано для примера 1.
[634] 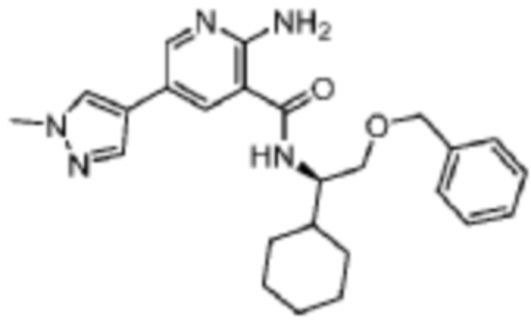
[635] MS (ESI, масса/заряд): 434,3 [M+H]+
[636] Пример 114. (R)-2-амино-N-(1-циклогексил-2-гидроксиэтил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[637] Используя (R)-2-амино-2-циклогексилэтан-1-ол, названное соединение получали, как описано для примера 1.
[638] 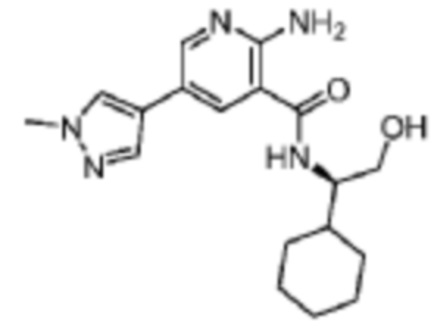
[639] MS (ESI, масса/заряд): 344,3 [M+H]+
[640] Пример 115. (S)-2-амино-N-(2-(бензилокси)-1-фенилэтил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
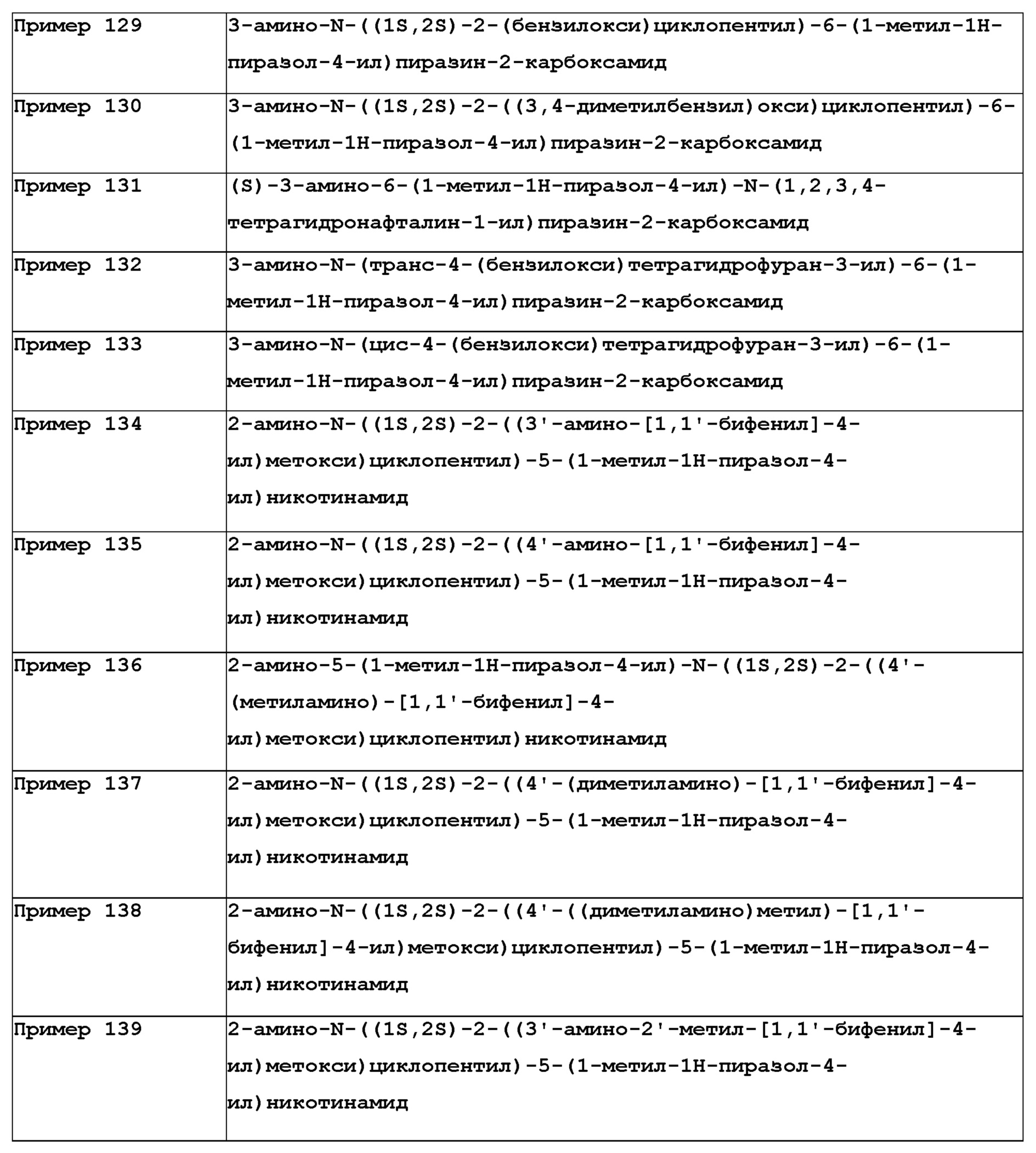
[641] Используя (S)-2-(бензилокси)-1-фенилэтан-1-амин, названное соединение получали, как описано для примера 1.
[642] 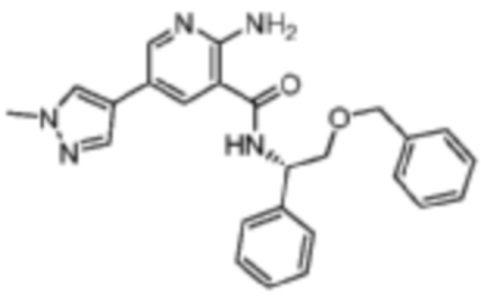
[643] MS (ESI, масса/заряд): 428,2 [M+H]+
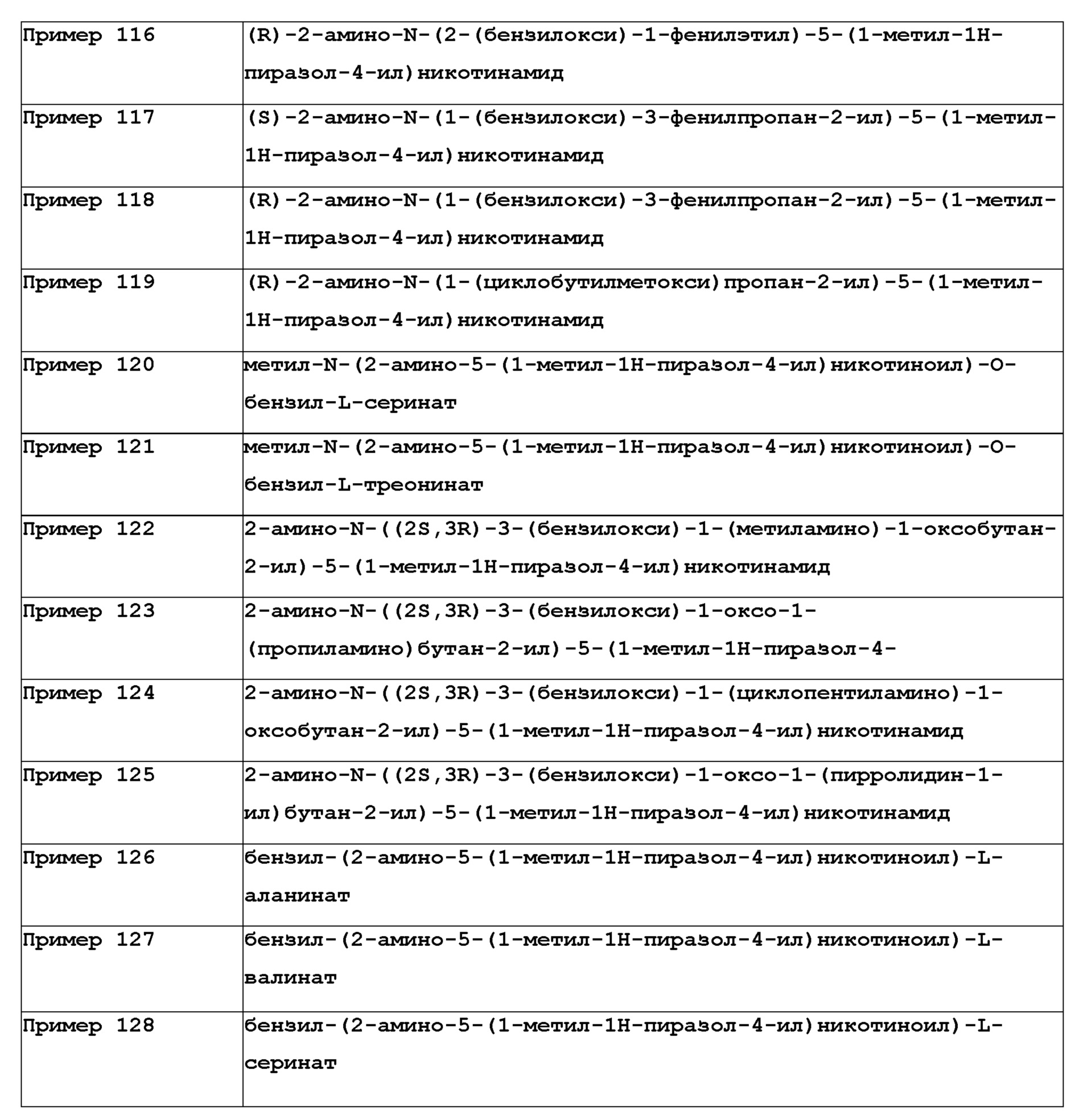
[644] Пример 116. (R)-2-амино-N-(2-(бензилокси)-1-фенилэтил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[645] Используя (R)-2-(бензилокси)-1-фенилэтан-1-амин, названное соединение получали, как описано для примера 1.
[646] 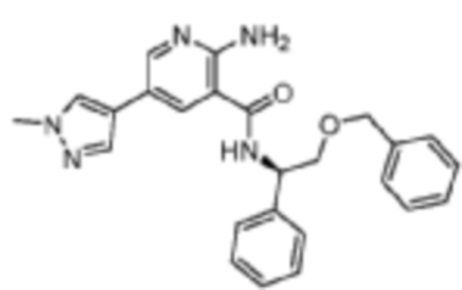
[647] MS (ESI, масса/заряд): 428,2 [M+H]+
[648] Пример 117. (S)-2-амино-N-(1-(бензилокси)-3-фенилпропан-2-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[649] Используя (S)-1-(бензилокси)-3-фенилпропан-2-амин, названное соединение получали, как описано для примера 1.
[650] 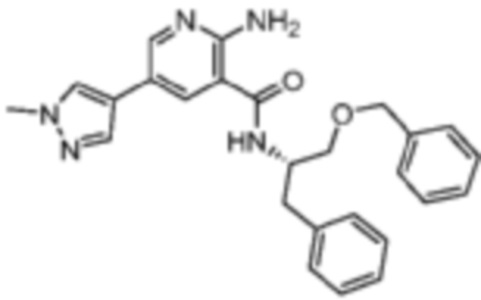
[651] MS (ESI, масса/заряд): 442,2 [M+H]+
[652] Пример 118. (R)-2-амино-N-(1-(бензилокси)-3-фенилпропан-2-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[653] Используя (R)-1-(бензилокси)-3-фенилпропан-2-амин, названное соединение получали, как описано для примера 1.
[654] 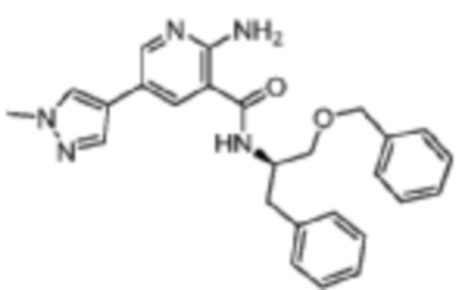
[655] MS (ESI, масса/заряд): 442,2 [M+H]+
[656] Пример 119. (R)-2-амино-N-(1-(циклобутилметокси)пропан-2-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[657] Используя (R)-1-(циклобутилметокси)пропан-2-амин, названное соединение получали, как описано для примера 1.
[658] 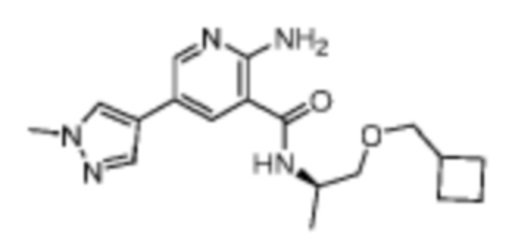
[659] MS (ESI, масса/заряд): 344,2 [M+H]+
[660] Пример 120. метил-N-(2-амино-5-(1-метил-1H-пиразол-4-ил)никотиноил)-O-бензил-L-серинат
[661] Используя метил-O-бензил-L-серинат, названное соединение получали, как описано для примера 1.
[662] 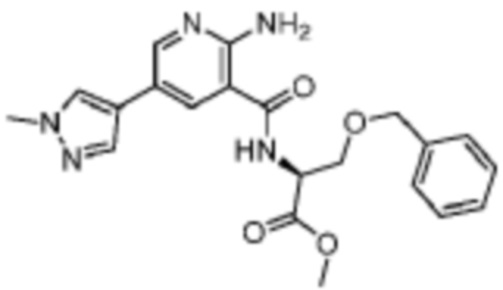
[663] MS (ESI, масса/заряд): 410,2 [M+H]+
[664] Пример 121. метил-N-(2-амино-5-(1-метил-1H-пиразол-4-ил)никотиноил)-O-бензил-L-треонинат
[665] Используя метил-O-бензил-L-треонинат, названное соединение получали, как описано для примера 1.
[666] 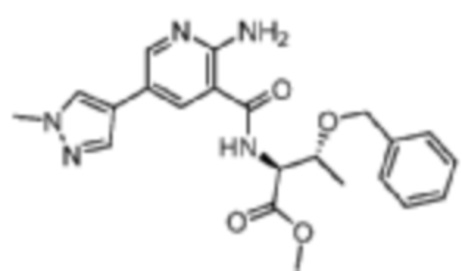
[667] MS (ESI, масса/заряд): 424,2 [M+H]+
[668] Пример 122. 2-амино-N-((2S,3R)-3-(бензилокси)-1-(метиламино)-1-оксобутан-2-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[669] Используя (2S,3R)-2-амино-3-(бензилокси)-N-метилбутанамид, названное соединение получали, как описано для примера 1.
[670] 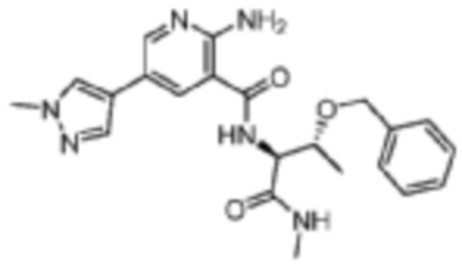
[671] MS (ESI, масса/заряд): 423,2 [M+H]+
[672] Пример 123. 2-амино-N-((2S,3R)-3-(бензилокси)-1-оксо-1-(пропиламино)бутан-2-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[673] Используя (2S,3R)-2-амино-3-(бензилокси)-N-пропилбутанамид, названное соединение получали, как описано для примера 1.
[674] 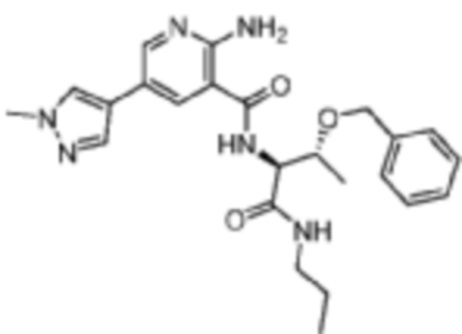
[675] MS (ESI, масса/заряд): 451,2 [M+H]+
[676] Пример 124. 2-амино-N-((2S,3R)-3-(бензилокси)-1-(циклопентиламино)-1-оксобутан-2-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[677] Используя (2S,3R)-2-амино-3-(бензилокси)-N-циклопентилбутанамид, названное соединение получали, как описано для примера 1.
[678] 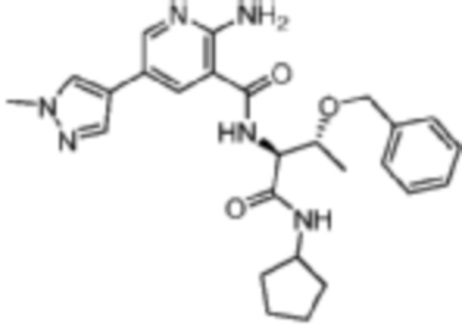
[679] MS (ESI, масса/заряд): 477,3 [M+H]+
[680] Пример 125. 2-амино-N-((2S,3R)-3-(бензилокси)-1-оксо-1-(пирролидин-1-ил)бутан-2-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[681] Используя (2S,3R)-2-амино-3-(бензилокси)-1-(пирролидин-1-ил)бутан-1-он, названное соединение получали, как описано для примера 1.
[682] 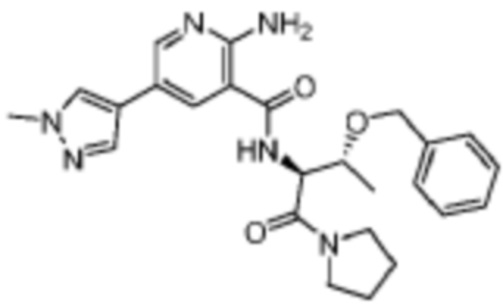
[683] MS (ESI, масса/заряд): 463,2 [M+H]+
[684] Пример 126. бензил-(2-амино-5-(1-метил-1H-пиразол-4-ил)никотиноил)-L-аланинат
[685] Используя бензил-L-аланинат, названное соединение получали, как описано для примера 1.
[686] 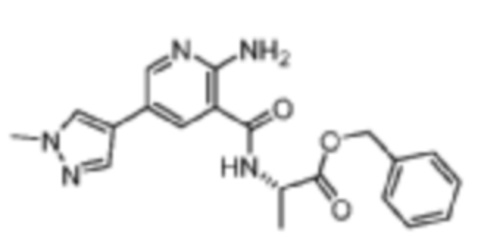
[687] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,51 (d, J=7,43 Гц, 3 H) 3,92 (s, 3 H) 4,64 (d, J=7,43 Гц, 1 H) 5,12-5,25 (m, 2 H) 7,21-7,42 (m, 5 H) 7,84 (s, 1 H) 7,96-8,00 (m, 1 H) 8,21-8,27 (m, 1 H) 8,54 (d, J=2,35 Гц, 1 H);
[688] MS (ESI, масса/заряд): 380,2 [M+H]+
[689] Пример 127. бензил-(2-амино-5-(1-метил-1H-пиразол-4-ил)никотиноил)-L-валинат
[690] Используя бензил-L-валинат, названное соединение получали, как описано для примера 1.
[691] 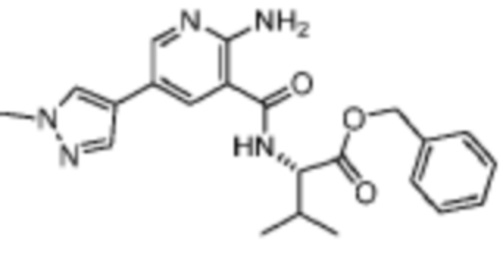
[692] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,00 (dd, J=9,19, 6,85 Гц, 6 H) 2,16-2,36 (m, 1 H) 4,46-4,55 (m, 1 H) 5,10-5,30 (m, 2 H) 7,22-7,41 (m, 5 H) 7,84 (d, J=0,78 Гц, 1 H) 7,98 (s, 1 H) 8,24 (d, J=1,96 Гц, 1 H) 8,48 (d, J=2,35 Гц, 1 H);
[693] MS (ESI, масса/заряд): 408,2 [M+H]+
[694] Пример 128. бензил-(2-амино-5-(1-метил-1H-пиразол-4-ил)никотиноил)-L-серинат
[695] Используя бензил L-серинат, названное соединение получали, как описано для примера 1.
[696] 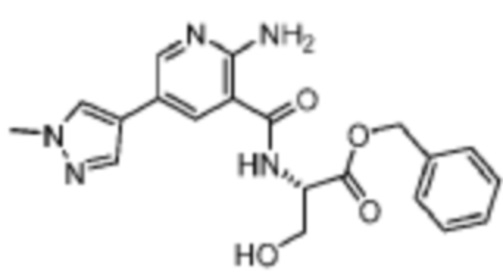
[697] 1H-ЯМР (400 MГц, CD3OD) δ ppm 3,94-4,07 (m, 2 H) 4,78 (dd, J=5,48, 4,30 Гц, 1 H) 5,21 (s, 2 H) 7,23-7,43 (m, 5 H) 7,86 (d, J=0,78 Гц, 1 H) 8,01 (s, 1 H) 8,24 (d, J=1,96 Гц, 1 H) 8,64 (d, J=1,96 Гц, 1 H);
[698] MS (ESI, масса/заряд): 396,2 [M+H]+
[699] Пример 129. 3-амино-N-((1S,2S)-2-(бензилокси)циклопентил)-6-(1-метил-1H-пиразол-4-ил)пиразин-2-карбоксамид
[700] Используя 3-амино-6-(1-метил-1H-пиразол-4-ил)пиразин-2-карбоновую кислоту и (1S,2S)-2-(бензилокси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[701] 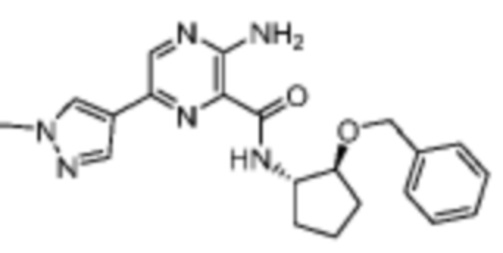
[702] MS (ESI, масса/заряд): 393,2 [M+H]+
[703] Пример 130. 3-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-6-(1-метил-1H-пиразол-4-ил)пиразин-2-карбоксамид
[704] Используя 3-амино-6-(1-метил-1H-пиразол-4-ил)пиразин-2-карбоновую кислоту и (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для примера 1.
[705] 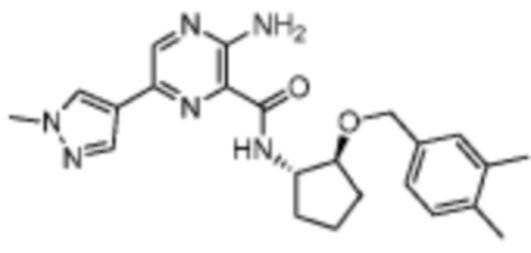
[706] MS (ESI, масса/заряд): 421,2 [M+H]+
[707] Пример 131. (S)-3-амино-6-(1-метил-1H-пиразол-4-ил)-N-(1,2,3,4-тетрагидронафталин-1-ил)пиразин-2-карбоксамид
[708] Используя 3-амино-6-(1-метил-1H-пиразол-4-ил)пиразин-2-карбоновую кислоту и (S)-1,2,3,4-тетрагидронафталин-1-амин, названное соединение получали, как описано для примера 1.
[709] 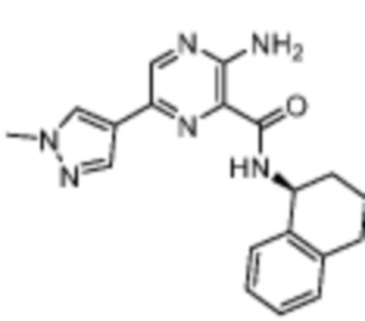
[710] MS (ESI, масса/заряд): 349,2 [M+H]+
[711] Пример 132. 3-амино-N-(транс-4-(бензилокси)тетрагидрофуран-3-ил)-6-(1-метил-1H-пиразол-4-ил)пиразин-2-карбоксамид
[712] Используя 3-амино-6-(1-метил-1H-пиразол-4-ил)пиразин-2-карбоновую кислоту и транс-4-(бензилокси)тетрагидрофуран-3-амин, названное соединение получали, как описано для примера 1.
[713] 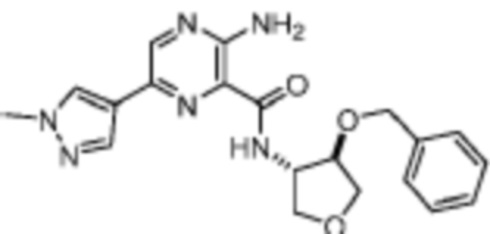
[714] MS (ESI, масса/заряд): 395,2 [M+H]+
[715] Пример 133. 3-амино-N-(цис-4-(бензилокси)тетрагидрофуран-3-ил)-6-(1-метил-1H-пиразол-4-ил)пиразин-2-карбоксамид
[716] Используя 3-амино-6-(1-метил-1H-пиразол-4-ил)пиразин-2-карбоновую кислоту и цис-4-(бензилокси)тетрагидрофуран-3-амин, названное соединение получали, как описано для примера 1.
[717] 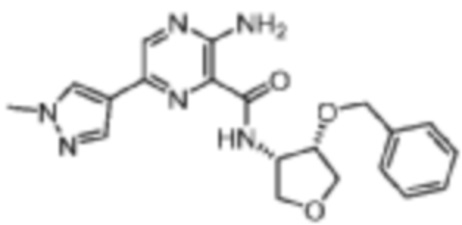
[718] MS (ESI, масса/заряд): 395,2 [M+H]+
[719] Пример 134. 2-амино-N-((1S,2S)-2-((3'-амино-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[720] Схема получения соединения примера 134:
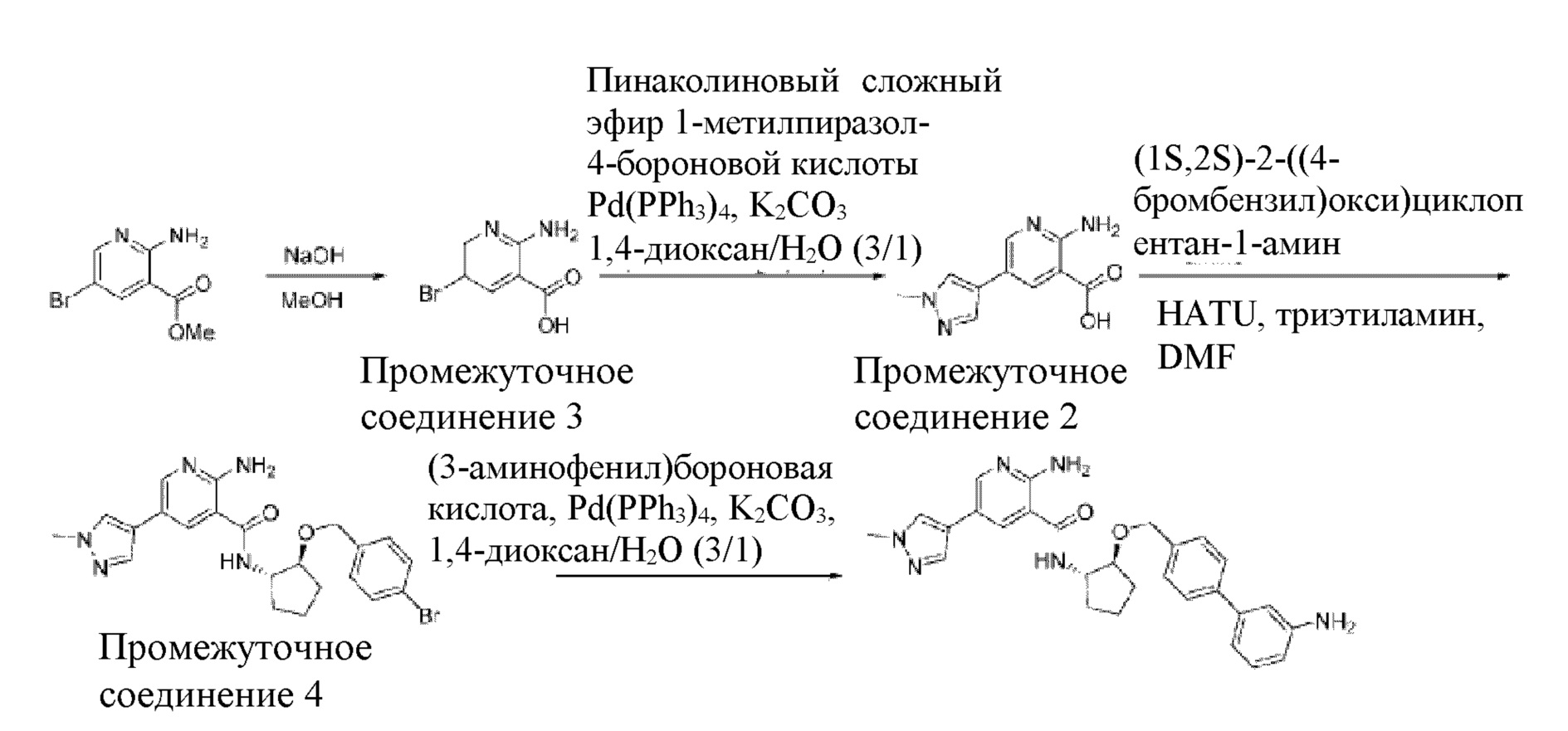
[721]
[722] Промежуточное соединение 3. В раствор метил-2-амино-5-бромникотината (560 мг, 2,42 ммоль) в 10 мл MeOH добавляли 2 н. NaOH (2 мл, 4 ммоль) и смесь нагревали при 65°C в течение 1 часа, охлаждали до комнатной температуры, нейтрализовали (2 мл 2 н. HCl) и полученный осадок отфильтровывали, промывали при помощи MeOH и сушили с получением 0,35 г белого твердого вещества.
[723] 1H-ЯМР (400 MГц, CD3OD) δ ppm 8,17 (d, J=2,4 Гц, 1H), 8,23 (d, J=2,4 Гц, 1H);
[724] MS (ESI, масса/заряд): 217,0 [M+H]+
[725] Промежуточное соединение 2. В смесь промежуточного соединения 3 (4,48 г, 20,6 ммоль) и пинаколинового сложного эфира 1-метилпиразол-4-бороновой кислоты (5,5 г, 26,8 ммоль) в 100 мл 1,4-диоксана/воды (3/1) добавляли K2CO3 (8,5 г, 61,9 ммоль), а затем Pd(PPh3)4 (1,19 г, 1,03 ммоль). Реакционную смесь нагревали при 100°C в течение 3 часов, охлаждали до комнатной температуры и разделяли между водой и EtOAc. Водный слой отделяли и доводили до значения pH от 4 до 5. Осадок собирали фильтрованием и сушили с получением 4 г названного соединения. Неочищенный продукт использовали для следующей стадии без дополнительной очистки.
[726] 1H-ЯМР (600 MГц, DMSO-d6) δ ppm 3,82(s, 3H), 5,73(s, 2H), 7,77(s, 1H), 8,05(s, 1H), 8,13(d, J=2,4 Гц, 1H), 8,42(d, J=2,4 Гц, 1H);
[727] MS (ESI, масса/заряд): 219,1 [M+H]+
[728] Промежуточное соединение 4. В смесь промежуточного соединения 2 (350 мг, 1,60 ммоль) и триэтиламина (0,34 мл, 2,41 ммоль) в 4 мл DMF добавляли HATU (732 мг, 1,92 ммоль), а затем (1S,2S)-2-((4-бромбензил)окси)циклопентан-1-амин (475 мг, 1,76 ммоль). Смесь перемешивали при комнатной температуре в течение 1 часа, а затем добавляли насыщенный раствор бикарбоната натрия. Смесь экстрагировали при помощи EtOAc, промывали солевым раствором, сушили над MgSO4 и концентрировали in vacuo. Неочищенный продукт очищали колоночной хроматографией на силикагеле с получением 650 мг грязно-белого твердого вещества.
[729] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,59-1,69 (m, 1 H) 1,72-1,78 (m, 1 H) 1,78-1,86 (m, 2 H) 1,96-2,07 (m, 1 H) 2,16 (dq, J=13,50, 6,85 Гц, 1 H) 3,94 (s, 3 H) 3,95 (br d, J=1,76 Гц, 1 H) 4,33-4,42 (m, 1 H) 4,53-4,62 (m, 2 H) 7,25 (m, J=8,22 Гц, 2 H) 7,41 (m, J=8,22 Гц, 2 H) 7,87 (s, 1 H) 8,01 (s, 1 H) 8,22 (d, J=1,76 Гц, 1 H) 8,52 (d, J=1,76 Гц, 1 H);
[730] MS (ESI, масса/заряд): 470,1/472,1 [M+H]+
[731] Пример 134. 2-амино-N-((1S,2S)-2-((3'-амино-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[732] В смесь промежуточного соединения 4 (33 мг, 0,07 ммоль) и (3-аминофенил)бороновой кислоты (11 мг, 0,08 ммоль) в 0,4 мл 1,4-диоксана/воды (3/1) добавляли K2CO3 (29 мг, 0,21 ммоль), а затем Pd(PPh3)4 (4 мг, 0,003 ммоль). Реакционную смесь нагревали при 100°C в течение 3 часов, охлаждали до комнатной температуры и экстрагировали при помощи EtOAc, сушили над безводным MgSO4 и концентрировали под вакуумом. После концентрирования под вакуумом неочищенный остаток очищали препаративной HPLC с получением 30 мг названого соединения.
[733] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,60-1,69 (m, 1 H) 1,73-1,90 (m, 3 H) 2,05 (br d, J=7,04 Гц, 1 H) 2,17 (s, 1 H) 3,89 (s, 3 H) 4,00 (br d, J=4,30 Гц, 1 H) 4,36-4,46 (m, 2 H) 4,67 (s, 2 H) 7,24 (br d, J=7,43 Гц, 1 H) 7,42-7,59 (m, 7 H) 7,84 (s, 1 H) 7,97 (s, 1 H) 8,20 (d, J=2,35 Гц, 1 H) 8,48 (d, J=2,35 Гц, 1 H);
[734] MS (ESI, масса/заряд): 483,2 [M+H]+
[735] Пример 135. 2-амино-N-((1S,2S)-2-((4'-амино-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[736] Используя (4-аминофенил)бороновую кислоту, названное соединение получали, как описано для примера 134.
[737] 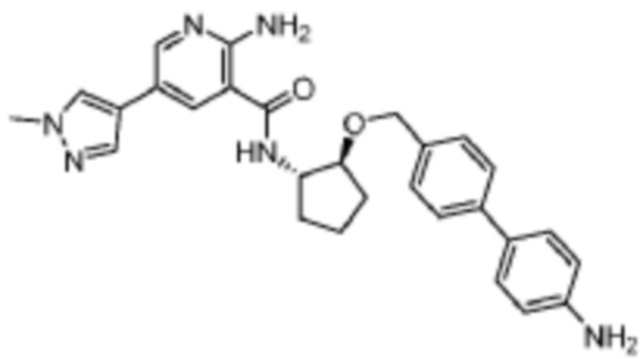
[738] MS (ESI, масса/заряд): 483,2 [M+H]+
[739] Пример 136. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-(метиламино)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[740] Используя (4-(метиламино)фенил)бороновую кислоту, названное соединение получали, как описано для примера 134.
[741] 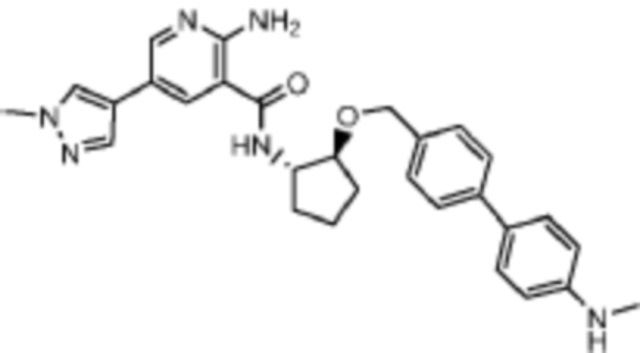
[742] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,64 (br d, J=5,87 Гц, 1 H) 1,73-1,94 (m, 3 H) 2,05 (br s, 1 H) 2,17 (br s, 1 H) 3,55 (br t, J=11,15 Гц, 3 H) 3,90 (s, 3 H) 4,00 (br s, 1 H) 4,43 (s, 4 H) 4,67 (s, 2 H) 7,45 (br d, J=8,22 Гц, 2 H) 7,55 (br d, J=7,83 Гц, 2 H) 7,60 (br d, J=7,83 Гц, 2 H) 7,71 (br d, J=7,83 Гц, 2 H) 7,85 (s, 1 H) 7,98 (s, 1 H) 8,21 (s, 1 H) 8,52 (s, 1 H);
[743] MS (ESI, масса/заряд): 497,3 [M+H]+
[744] Пример 137. 2-амино-N-((1S,2S)-2-((4'-(диметиламино)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[745] Используя (4-(диметиламино)фенил)бороновую кислоту, названное соединение получали, как описано для примера 134.
[746] 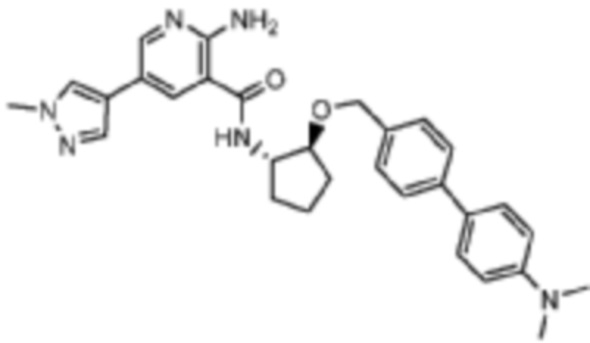
[747] MS (ESI, масса/заряд): 511,3 [M+H]+
[748] Пример 138. 2-амино-N-((1S,2S)-2-((4'-((диметиламино)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[749] Используя ((4-((диметиламино)метил)фенил)бороновую кислоту, названное соединение получали, как описано для примера 134.
[750] 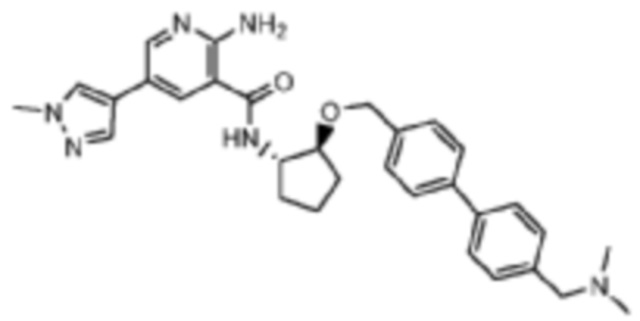
[751] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,55-1,68 (m, 1 H) 1,80 (br s, 3 H) 2,04 (br d, J=7,43 Гц, 1 H) 2,15 (br s, 1 H) 3,49 (br s, 3 H) 3,62 (br s, 3 H) 3,75 (br s, 2 H) 3,89 (s, 3 H) 3,97 (br s, 1 H) 4,39 (br s, 1 H) 4,62 (br d, J=12,91 Гц,1 H) 4,66-4,73 (m, 1 H) 7,44 (br t, J=9,19 Гц, 4 H) 7,56 (br d, J=8,22 Гц, 2 H) 7,62 (br d, J=7,83 Гц, 2 H) 7,82 (s, 1 H) 7,94 (s, 1 H) 8,16 (s, 1 H) 8,42 (s, 1 H);
[752] MS (ESI, масса/заряд): 525,3 [M+H]+
[753] Пример 139. 2-амино-N-((1S,2S)-2-((3'-амино-2'-метил-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[754] Используя (3-амино-2-метилфенил)бороновую кислоту, названное соединение получали, как описано для примера 134.
[755] 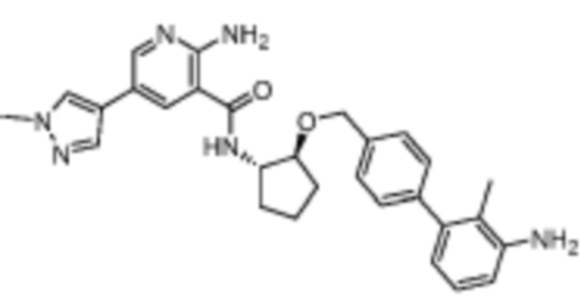
[756] MS (ESI, масса/заряд): 497,2 [M+H]+
[757] Пример 140. 2-амино-N-((1S,2S)-2-((3'-гидрокси-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[758] Используя (3-гидроксифенил)бороновую кислоту, названное соединение получали, как описано для примера 134.
[759] 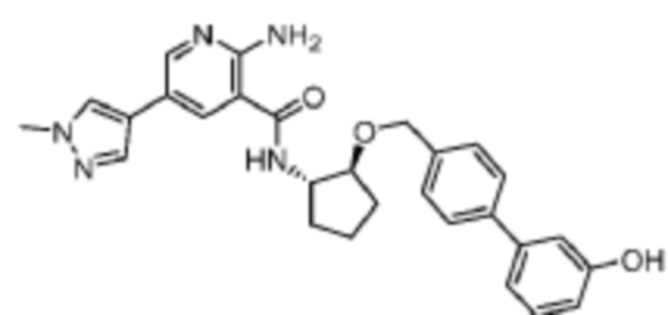
[760] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,61 (br d, J=7,43 Гц, 1 H) 1,72-1,86 (m, 3 H) 1,95-2,08 (m, 1 H) 2,09-2,20 (m, 1 H) 3,87 (s, 3 H) 3,97 (br s, 1 H) 4,40 (br d, J=18,00 Гц, 1 H) 4,56-4,71 (m, 2 H) 6,70-6,75 (m, 1 H) 6,90 (br s, 1 H) 6,95 (br d, J=7,83 Гц, 1 H) 7,14-7,21 (m, 1 H) 7,32-7,41 (m, 2 H) 7,42-7,50 (m, 2 H) 7,78-7,83 (m, 1 H) 7,88-7,93 (m, 1 H) 8,16 (br d, J=1,96 Гц, 1 H) 8,36 (br d, J=2,35 Гц, 1 H);
[761] MS (ESI, масса/заряд): 484,2 [M+H]+
[762] Пример 141. 2-амино-N-((1S,2S)-2-((3'-(гидроксиметил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[763] Используя (3-(гидроксиметил)фенил)бороновую кислоту, названное соединение получали, как описано для примера 134.
[764] 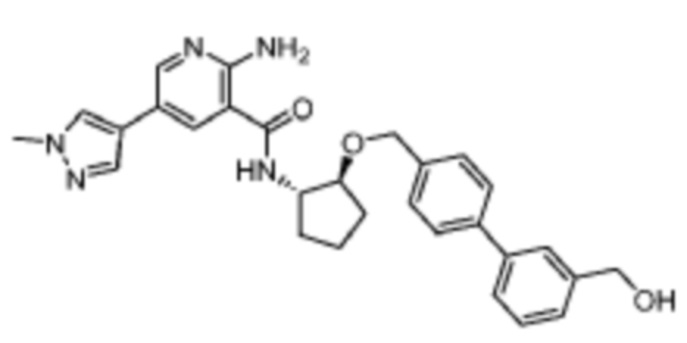
[765] MS (ESI, масса/заряд): 498,2 [M+H]+
[766] Пример 142. 2-амино-N-((1S,2S)-2-((4'-(гидроксиметил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[767] Используя ((4-(гидроксиметил)фенил)бороновую кислоту, названное соединение получали, как описано для примера 134.
[768] 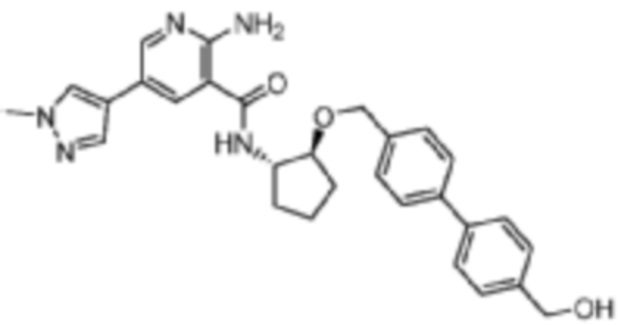
[769] MS (ESI, масса/заряд): 498,2 [M+H]+
[770] Пример 143. 2-амино-N-((1S,2S)-2-((3'-(аминометил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[771] Используя (3-(аминометил)фенил)бороновую кислоту, названное соединение получали, как описано для примера 134.
[772] 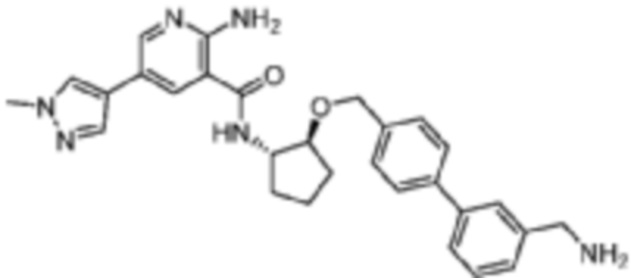
[773] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,54-1,67 (m, 1 H) 1,71-1,90 (m, 3 H) 2,03 (br dd, J=12,33, 7,04 Гц, 1 H) 2,11-2,21 (m, 1 H) 3,88 (s, 3 H) 3,96-4,03 (m, 1 H) 4,16 (s, 2 H) 4,35-4,47 (m, 1 H) 4,67 (s, 2 H) 7,40 (br d, J=7,63 Гц, 1 H) 7,44 (d, J=8,22 Гц, 1 H) 7,49 (br t, J=7,63 Гц, 2 H) 7,58 (d, J=7,63 Гц, 1 H) 7,59-7,62 (m, 2 H) 7,61 (br d, J=7,63 Гц, 1 H) 7,66 (s, 1 H) 7,80 (s, 1 H) 7,92 (s, 1 H) 8,21 (d, J=2,35 Гц, 1 H) 8,29 (br s, 1 H);
[774] MS (ESI, масса/заряд): 497,3 [M+H]+
[775] Пример 144. 2-амино-N-((1S,2S)-2-((4'-(аминометил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[776] Используя (4-(аминометил)фенил)бороновую кислоту, названное соединение получали, как описано для примера 134.
[777] 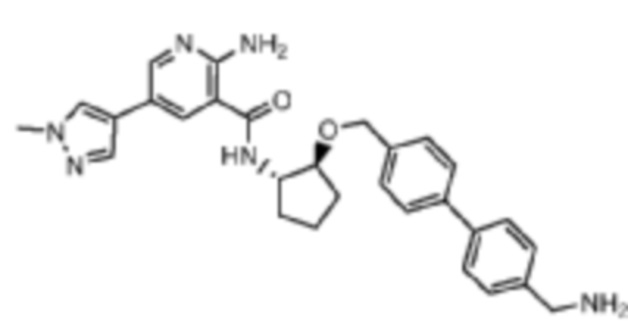
[778] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,64 (br dd, J=14,09, 7,04 Гц, 1 H) 1,72-1,90 (m, 3 H) 2,03 (br dd, J=13,21, 6,16 Гц, 1 H) 2,14-2,23 (m, 1 H) 3,90 (s, 3 H) 4,01 (br d, J=7,04 Гц, 1 H) 4,14 (s, 2 H) 4,40-4,45 (m, 1 H) 4,63-4,70 (m, 2 H) 7,43 (d, J=8,22 Гц, 2 H) 7,49 (d, J=7,63 Гц, 2 H) 7,57 (d, J=7,63 Гц, 2 H) 7,65 (d, J=8,22 Гц, 2 H) 7,85 (s, 1 H) 7,97 (s, 1 H) 8,21 (d, J=1,76 Гц, 1 H) 8,49 (br s, 1 H);
[779] MS (ESI, масса/заряд): 497,3 [M+H]+
[780] Пример 145. 2-амино-N-((1S,2S)-2-((4'-(2-аминоэтил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[781] Используя (4-(2-аминоэтил)фенил)бороновую кислоту, названное соединение получали, как описано для примера 134.
[782] 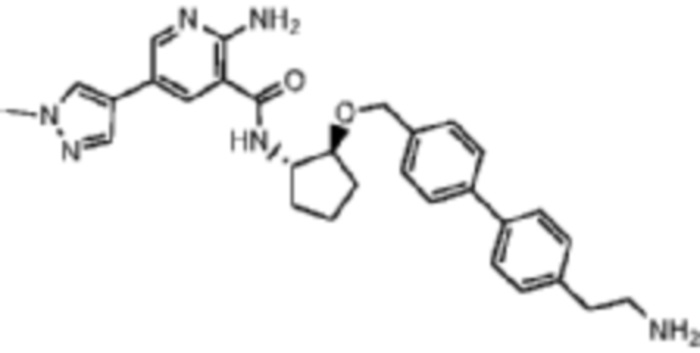
[783] MS (ESI, масса/заряд): 511,3 [M+H]+
[784] Пример 146. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-(4-метилпиперазин-1-ил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[785] Используя (4-(4-метилпиперазин-1-ил)фенил)бороновую кислоту, названное соединение получали, как описано для примера 134.
[786] 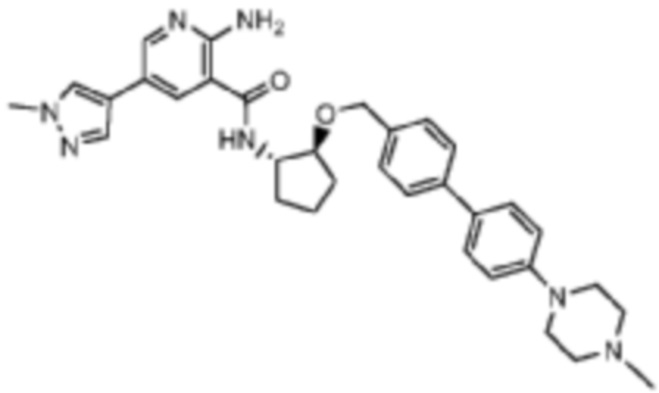
[787] MS (ESI, масса/заряд): 566,3 [M+H]+
[788] Пример 147. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4-(6-(пиперазин-1-ил)пиридин-3-ил)бензил)окси)циклопентил)никотинамид
[789] Используя (6-(пиперазин-1-ил)пиридин-3-ил)бороновую кислоту, названное соединение получали, как описано для примера 134.
[790] 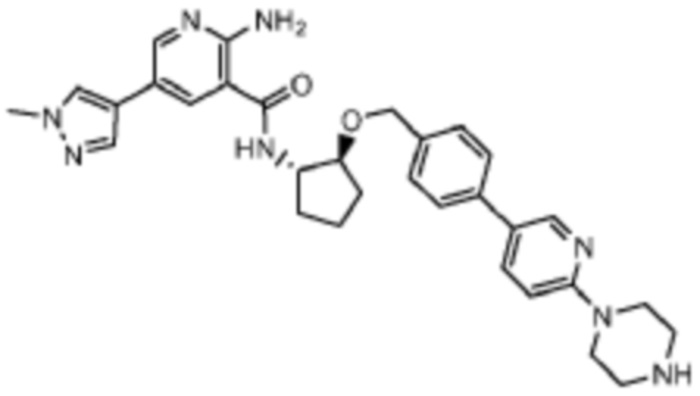
[791] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,64 (br d, J=7,83 Гц, 1 H) 1,81 (br d, J=7,83 Гц, 3 H) 2,04 (br s, 1 H) 2,18 (br s, 1 H) 3,32-3,40 (m, 4 H) 3,84 (br s, 4 H) 3,90 (s, 3 H) 3,98 (br s, 1 H) 4,40 (br s, 1 H) 4,65 (s, 2 H) 6,98-7,02 (m, 1 H) 7,41 (br d, J=7,04 Гц, 2 H) 7,50 (br d, J=7,83 Гц, 2 H) 7,83-7,89 (m, 2 H) 7,96 (s, 1 H) 8,20 (s, 1 H) 8,35 (s, 1 H) 8,48 (s, 1 H);
[792] MS (ESI, масса/заряд): 553,3 [M+H]+
[793] Пример 148. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4-(6-(4-метилпиперазин-1-ил)пиридин-3-ил)бензил)окси)циклопентил)никотинамид
[794] Используя (6-(4-метилпиперазин-1-ил)пиридин-3-ил)бороновую кислоту, названное соединение получали, как описано для примера 134.
[795] 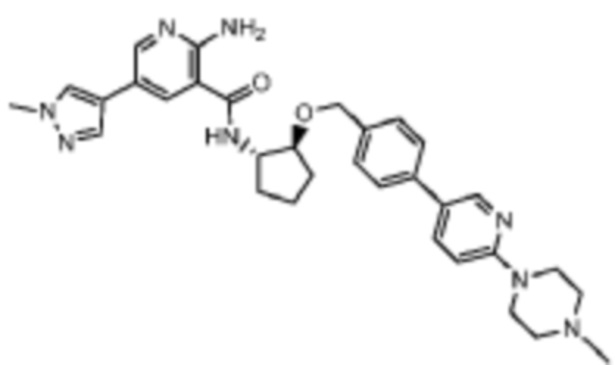
[796] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,58-1,66 (m, 1 H) 1,73-1,87 (m, 3 H) 2,04 (dq, J=13,72, 6,77 Гц, 1 H) 2,16 (dt, J=13,35, 6,53 Гц, 1 H) 2,96 (s, 3 H) 3,90 (s, 3 H) 3,96-4,01 (m, 1 H) 4,37-4,45 (m, 1 H) 4,60-4,69 (m, 2 H) 6,99 (d, J=8,80 Гц, 1 H) 7,41 (d, J=8,22 Гц, 2 H) 7,50 (d, J=8,22 Гц, 2 H) 7,83 (s, 1 H) 7,85 (d, J=2,35 Гц, 1 H) 7,96 (s, 1 H) 8,20 (d, J=2,35 Гц, 1 H) 8,36 (d, J=2,35 Гц, 1 H) 8,45 (s, 1 H);
[797] MS (ESI, масса/заряд): 567,3 [M+H]+
[798] Пример 149. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((3'-(пиперазин-1-ил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[799] Используя (3-(пиперазин-1-ил)фенил)бороновую кислоту, названное соединение получали, как описано для примера 134.
[800] 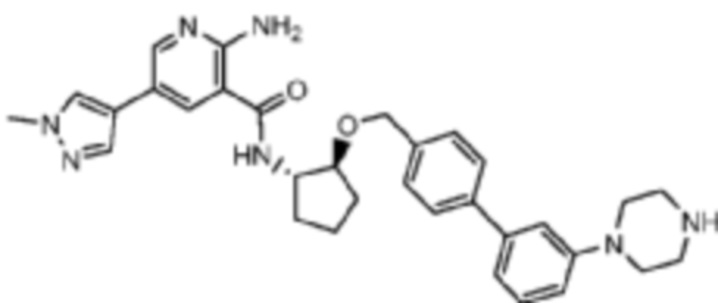
[801] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,62 (br d, J=5,87 Гц, 2 H) 1,81 (br d, J=6,65 Гц, 3 H) 1,96-2,07 (m, 1 H) 2,17 (br s, 1 H) 3,40 (br dd, J=19,95, 5,87 Гц, 8 H) 3,88 (s, 3 H) 4,00 (br s, 1 H) 4,40 (br s, 1 H) 4,65 (s, 2 H) 6,99 (br d, J=7,43 Гц, 1 H) 7,10 (br d, J=6,65 Гц, 1 H) 7,16 (s, 1 H) 7,32 (t, J=7,60 Гц, 1 H) 7,40 (d, J=7,83 Гц, 2 H) 7,53 (d, J=8,61 Гц, 2 H) 7,84 (s, 1 H) 7,95 (s, 1 H) 8,19 (s, 1 H) 8,46 (s, 1 H);
[802] MS (ESI, масса/заряд): 552,3 [M+H]+
[803] Пример 150. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((3'-(4-метилпиперазин-1-ил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[804] Используя (3-(4-метилпиперазин-1-ил)фенил)бороновую кислоту, названное соединение получали, как описано для примера 134.
[805] 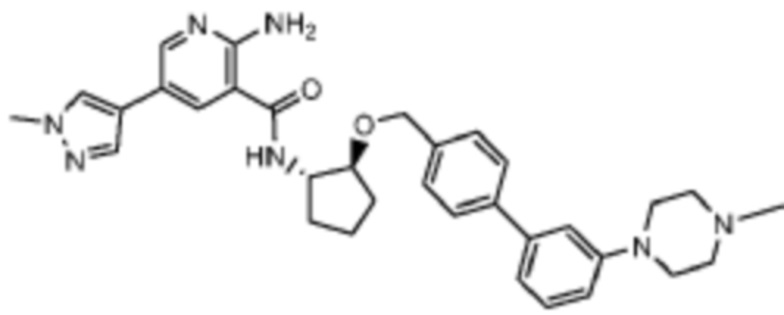
[806] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,66 (s, 1 H) 1,73-1,88 (m, 3 H) 1,99-2,08 (m, 1 H) 2,17 (br dd, J=13,50, 5,87 Гц, 1 H) 2,97 (s, 3 H) 3,06 (br s, 2 H) 3,60 (br s, 2 H) 3,88 (s, 3 H) 3,96-4,03 (m, 1 H) 4,41 (br d, J=4,70 Гц, 1 H) 4,61-4,70 (m, 2 H) 6,99 (br d, J=8,80 Гц, 1 H) 7,10 (br d, J=7,63 Гц, 1 H) 7,16 (s, 1 H) 7,32 (t, J=7,92 Гц, 1 H) 7,41 (d, J=8,22 Гц, 2 H) 7,53 (d, J=8,22 Гц, 2 H) 7,82 (s, 1 H) 7,93 (s, 1 H) 8,19 (d, J=1,76 Гц, 1 H) 8,35-8,41 (m, 1 H);
[807] MS (ESI, масса/заряд): 566,3 [M+H]+
[808] Пример 151. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((3'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[809] Используя пинаколиновый сложный эфир (3-((4-метилпиперазин-1-ил)метил)фенил)бороновой кислоты, названное соединение получали, как описано для примера 134.
[810] 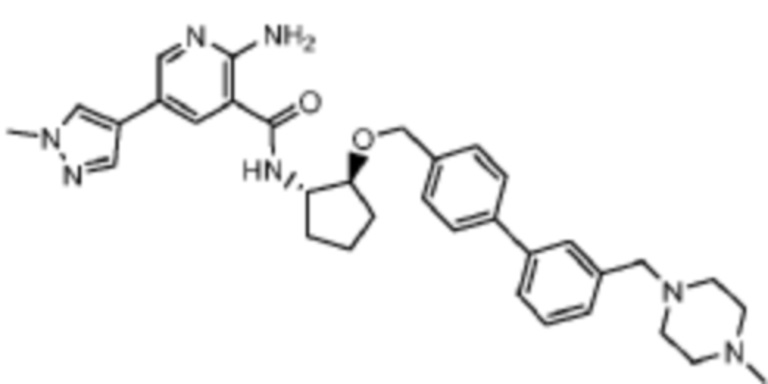
[811] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,65 (br dd, J=13,30, 6,26 Гц, 1 H) 1,76-1,90 (m, 3 H) 1,99-2,10 (m, 1 H) 2,18 (br dd, J=14,09, 6,65 Гц, 1 H) 2,85 (s, 3 H) 3,78 (s, 2 H) 3,91 (s, 3 H) 4,02 (br s, 1 H) 4,43 (br dd, J=10,96, 7,83 Гц, 1 H) 4,68 (s, 2 H) 7,34 (br d, J=7,43 Гц, 1 H) 7,38-7,45 (m, 3 H) 7,51 (br d, J=7,83 Гц, 1 H) 7,54-7,60 (m, 3 H) 7,86 (s, 1 H) 7,99 (s, 1 H) 8,21 (d, J=1,96 Гц, 1 H) 8,51 (d, J=1,96 Гц, 1 H);
[812] MS (ESI, масса/заряд): 579,3 [M+H]+
[813] Пример 152. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-(морфолин-4-карбонил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[814] Используя (4-(морфолин-4-карбонил)фенил)бороновую кислоту, названное соединение получали, как описано для примера 134.
[815] 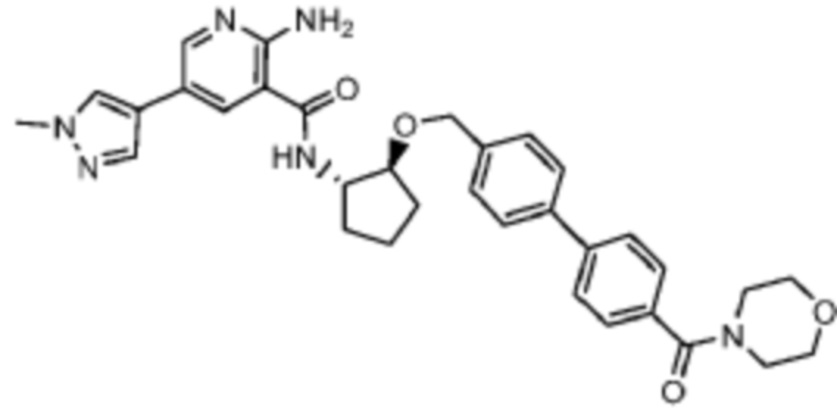
[816] MS (ESI, масса/заряд): 581,3 [M+H]+
[817] Пример 153. 2-амино-N-((1S,2S)-2-((4'-этил-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[818] Используя (4-этилфенил)бороновую кислоту, названное соединение получали, как описано для примера 134.
[819] 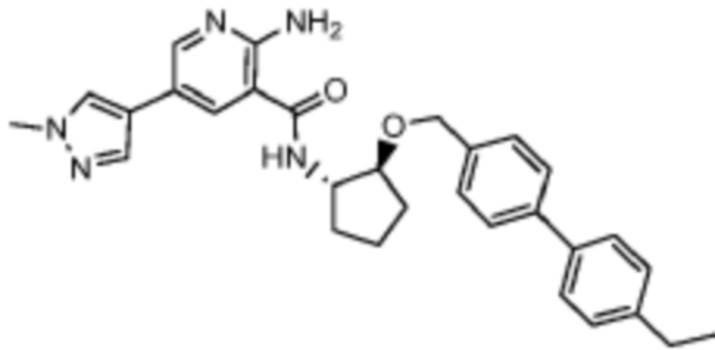
[820] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,24 (t, J=7,63 Гц, 3 H) 1,55-1,67 (m, 1 H) 1,73-1,86 (m, 3 H) 2,01-2,08 (m, 1 H) 2,16 (br dd, J=13,21, 5,58 Гц, 1 H) 2,66 (q, J=7,63 Гц, 2 H) 3,87 (s, 3 H) 3,93-3,99 (m, 1 H) 4,38-4,42 (m, 1 H) 4,61 (d, J=12,91 Гц, 1 H) 4,65-4,71 (m, 1 H) 7,21 (d, J=7,63 Гц, 2 H) 7,38 (d, J=8,22 Гц, 2 H) 7,41 (d, J=8,22 Гц, 2 H) 7,50 (d, J=8,22 Гц, 2 H) 7,82 (s, 1 H) 7,91 (s, 1 H) 8,16 (d, J=1,76 Гц, 1 H) 8,42 (d, J=2,35 Гц, 1 H);
[821] MS (ESI, масса/заряд): 496,3 [M+H]+
[822] Пример 154. 2-амино-N-((1S,2S)-2-((4'-(цианометил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[823] Используя (4-(цианометил)фенил)бороновую кислоту, названное соединение получали, как описано для примера 134.
[824] 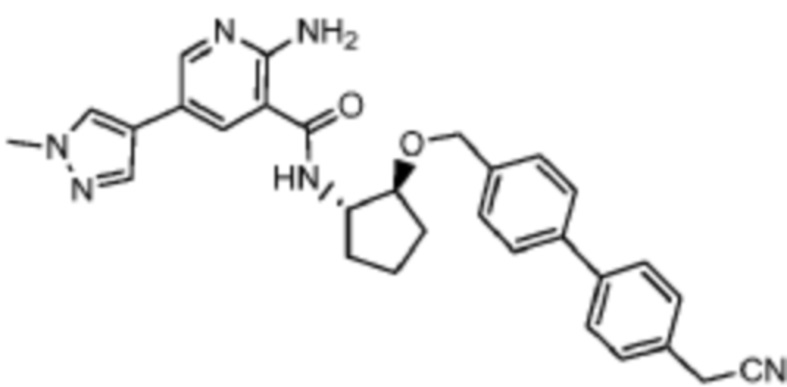
[825] MS (ESI, масса/заряд): 507,2 [M+H]+
[826] Пример 155. 2-амино-N-((1S,2S)-2-((4'-карбамоил-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[827] Используя (4-карбамоилфенил)бороновую кислоту, названное соединение получали, как описано для примера 134.
[828] 
[829] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,62 (s, 1 H) 1,70-1,88 (m, 3 H) 2,05 (s, 1 H) 2,16 (td, J=13,06, 7,92 Гц, 1 H) 3,88 (s, 3 H) 3,98 (br d, J=6,46 Гц, 1 H) 4,40 (br d, J=4,70 Гц, 1 H) 4,63 (d, J=12,33 Гц, 1 H) 4,70 (d, J=12,91 Гц, 1 H) 7,44 (d, J=8,22 Гц, 2 H) 7,58 (d, J=8,22 Гц, 2 H) 7,61 (d, J=8,80 Гц, 2 H) 7,81 (s, 1 H) 7,89 (d, J=8,22 Гц, 2 H) 7,92 (s, 1 H) 8,17 (d, J=2,35 Гц, 1 H) 8,38 (d, J=1,76 Гц, 1 H);
[830] MS (ESI, масса/заряд): 511,2 [M+H]+
[831] Пример 156. 2-амино-N-((1S,2S)-2-((3-фтор-4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[832] Используя (1S,2S)-2-((4-бром-2-фторбензил)окси)циклопентан-1-амин и пинаколиновый сложный эфир 4-(4-метилпиперазинo)метилфенилбороновой кислоты, названное соединение получали, как описано для примера 134.
[833] 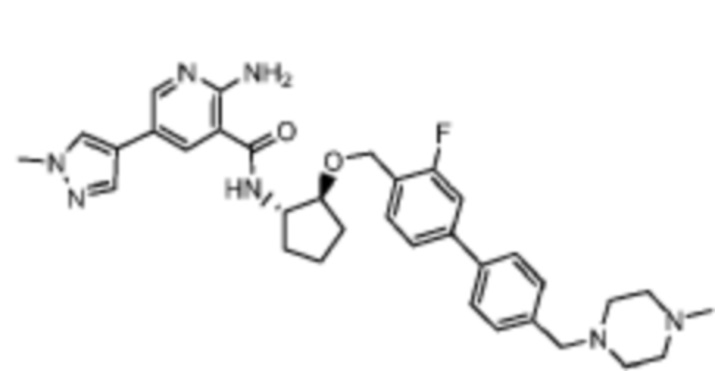
[834] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,64 (br dd, J=13,30, 7,04 Гц, 1 H) 1,74-1,92 (m, 3 H) 2,04 (br dd, J=12,72, 6,06 Гц, 1 H) 2,17 (br dd, J=13,50, 6,46 Гц, 1 H) 2,91 (s, 3 H) 3,25 (br s, 4 H) 3,47 (br s, 4 H) 3,90 (s, 3 H) 3,96-4,08 (m, 1 H) 4,12 (s, 2 H) 4,34-4,45 (m, 1 H) 4,64-4,78 (m, 2 H) 5,47 (s, 1 H) 7,32 (br d, J=11,35 Гц, 1 H) 7,40 (br d, J=7,83 Гц, 1 H) 7,47-7,57 (m, 3 H) 7,62 (br d, J=7,83 Гц, 2 H) 7,85 (s, 1 H) 7,99 (s, 1 H) 8,18 (s, 1 H) 8,55 (s, 1 H);
[835] MS (ESI, масса/заряд): 598,4 [M+H]+
[836] Пример 157. 2-амино-N-((1S,2S)-2-((3-фтор-4'-((цис-3,4,5-триметилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[837] Используя (1S,2S)-2-((4-бром-2-фторбензил)окси)циклопентан-1-амин и пинаколиновый сложный эфир (4-((цис-3,4,5-триметилпиперазин-1-ил)метил)фенил)бороновой кислоты, названное соединение получали, как описано для примера 134.
[838] 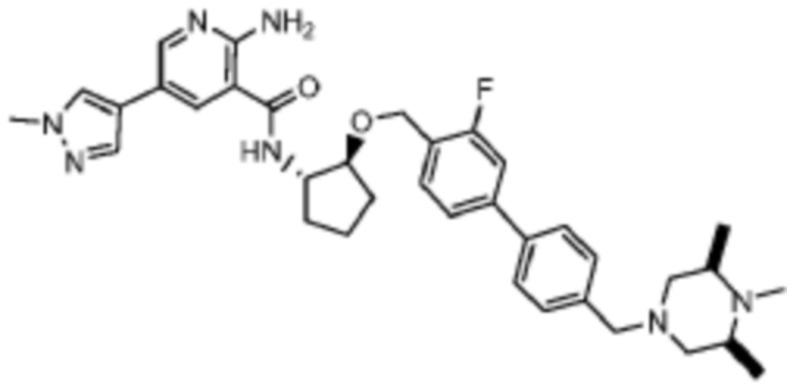
[839] MS (ESI, масса/заряд): 626,4 [M+H]+
[840] Пример 158. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-3-(трифторметил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[841] Используя (1S,2S)-2-((4-бром-2-(трифторметил)бензил)окси)циклопентан-1-амин и пинаколиновый сложный эфир 4-(4-метилпиперазинo)метилфенилбороновой кислоты, названное соединение получали, как описано для примера 134.
[842] 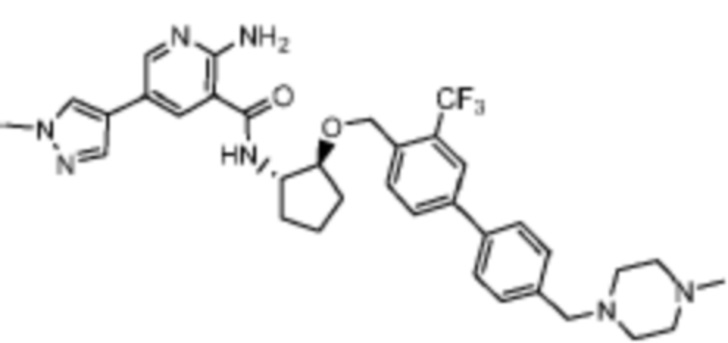
[843] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,69 (dt, J=13,89, 6,75 Гц, 1 H) 1,77-1,93 (m, 3 H) 2,01-2,12 (m, 1 H) 2,13-2,30 (m, 1 H) 2,87 (s, 3 H) 3,75 (s, 2 H) 3,92 (s, 3 H) 4,00-4,08 (m, 1 H) 4,45 (br dd, J=11,54, 7,24 Гц, 1 H) 7,47 (d, J=8,22 Гц, 2 H) 7,62 (m, J=8,22 Гц, 2 H) 7,81-7,84 (m, 2 H) 7,86 (d, J=5,09 Гц, 2 H) 8,00 (s, 1 H) 8,23 (d, J=1,96 Гц, 1 H) 8,56 (d, J=2,35 Гц, 1 H);
[844] MS (ESI, масса/заряд): 648,3 [M+H]+
[845] Пример 159. 2-амино-N-((1S,2S)-2-((2-хлор-4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[846] Используя (1S,2S)-2-((4-бром-3-хлорбензил)окси)циклопентан-1-амин и пинаколиновый сложный эфир 4-(4-метилпиперазинo)метилфенилбороновой кислоты, названное соединение получали, как описано для примера 134.
[847] 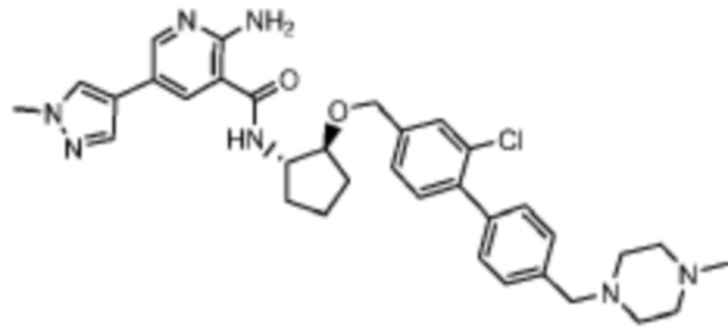
[848] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,65 (br dd, J=13,50, 7,04 Гц, 1 H) 1,74-1,89 (m, 3H) 1,97-2,11 (m, 1 H) 2,15-2,22 (m, 1 H) 2,85 (s, 3 H) 3,72 (s, 2 H) 3,92 (s, 3 H) 3,98 (dt, J=6,46, 4,11 Гц, 1 H) 4,42 (td, J=7,34, 4,11 Гц, 1 H) 4,66 (d, J=2,35 Гц, 2 H) 7,27 (d, J=7,63 Гц, 1 H) 7,30-7,37 (m, 3 H) 7,40 (d, J=8,22 Гц, 2 H) 7,47 (d, J=1,17 Гц, 1 H) 7,86 (s, 1 H) 7,99 (s, 1 H) 8,22 (d, J=2,35 Гц, 1 H) 8,49 (d, J=2,35 Гц, 1 H);
[849] MS (ESI, масса/заряд): 614,3 [M+H]+
[850] Пример 160. 2-амино-N-((1S,2S)-2-((3-фтор-4'-((цис-4-(2-гидроксиэтил)-3,5-диметилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[851] Используя (1S,2S)-2-((4-бром-2-фторбензил)окси)циклопентан-1-амин и пинаколиновый сложный эфир (4-((цис-4-(2-гидроксиэтил)-3,5-диметилпиперазин-1-ил)метил)фенил)бороновой кислоты, названное соединение получали, как описано для примера 134.
[852] 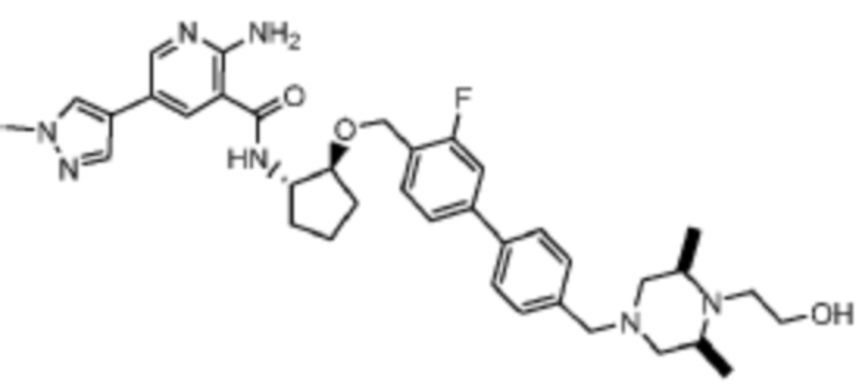
[853] MS (ESI, масса/заряд): 656,4 [M+H]+
[854] Пример 161. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-(2-(4-метилпиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[855] Используя пинаколиновый сложный эфир 4-(2-(4-метилпиперазинo)этил)фенилбороновой кислоты, названное соединение получали, как описано для примера 134.
[856] 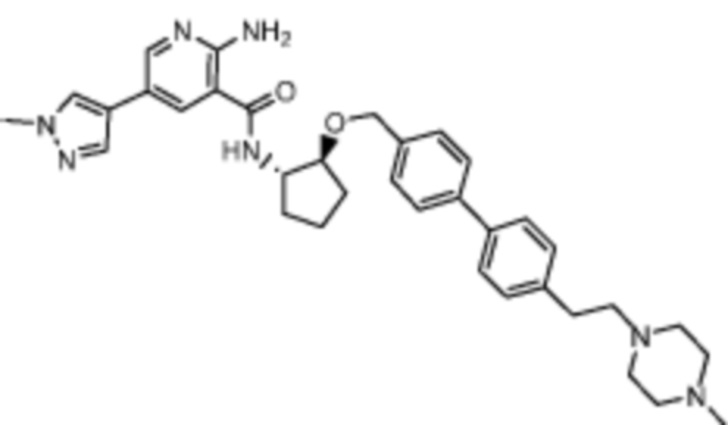
[857] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,63 (br dd, J=13,79, 6,75 Гц, 1 H) 1,74-1,87 (m, 3 H) 2,00-2,11 (m, 1 H) 2,11-2,23 (m, 1 H) 2,79-2,96 (m, 2 H) 3,02 (br s, 2 H) 3,24 (s, 2 H) 3,41 (br s, 4 H) 3,89 (s, 3 H) 3,97-4,03 (m, 1 H) 4,41 (br s, 1 H) 4,61-4,71 (m, 2 H) 7,31 (br d, J=8,22 Гц, 2 H) 7,40 (d, J=7,63 Гц, 2 H) 7,50 (br d, J=8,22 Гц, 2 H) 7,51-7,57 (m, 2 H) 7,84 (br d, J=2,93 Гц, 1 H) 7,96 (s, 1 H) 8,16-8,21 (m, 1 H) 8,50 (br d, J=4,70 Гц, 1 H);
[858] MS (ESI, масса/заряд): 594,4 [M+H]+
[859] Пример 162. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4-(1-(пиперидин-4-ил)-1H-пиразол-4-ил)бензил)окси)циклопентил)никотинамид
[860] Используя трет-бутил-4-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1H-пиразол-1-ил)пиперидин-1-карбоксилат, названное соединение получали, как описано для примера 134 и после снятия защитных групп при помощи TFA.
[861] 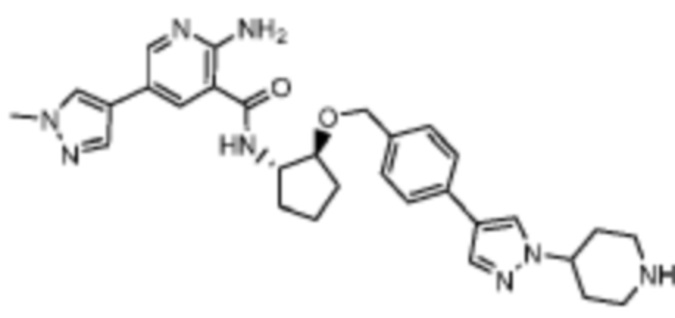
[862] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,62 (br s, 1 H) 1,80 (br d, J=6,65 Гц, 3 H) 2,03 (br s, 1 H) 2,15 (br s, 1 H) 2,28 (br d, J=13,69 Гц, 4 H) 3,14-3,25 (m, 2 H) 3,56 (br d, J=11,35 Гц, 2 H) 3,90 (s, 3 H) 3,97 (br s, 1 H) 4,39 (br s, 1 H) 4,53 (br s, 1 H) 4,60 (s, 2 H) 7,32 (br d, J=7,83 Гц, 2 H) 7,47 (br d, J=7,83 Гц, 2 H) 7,79 (s, 1 H) 7,85 (s, 1 H) 7,97 (br s, 2 H) 8,20 (br s, 1 H) 8,48 (s, 1 H);
[863] MS (ESI, масса/заряд): 541,3 [M+H]+
[864] Пример 163. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4-(1-(1-метилпиперидин-4-ил)-1H-пиразол-4-ил)бензил)окси)циклопентил)никотинамид
[865] Используя (1-метил-4-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1H-пиразол-1-ил)пиперидин, названное соединение получали, как описано для примера 134.
[866] 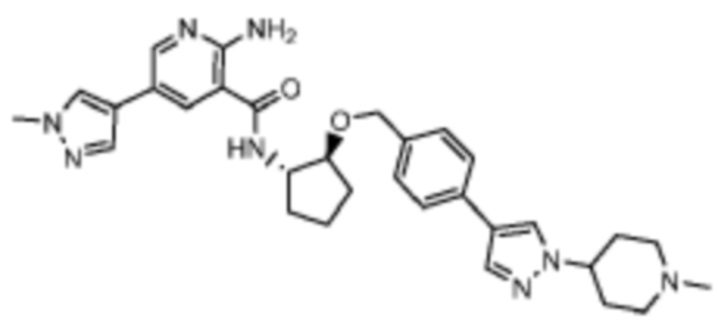
[867] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,57-1,66 (m, 1 H) 1,72-1,87 (m, 3 H) 2,03 (br dd, J=12,62, 6,75 Гц, 1 H) 2,17 (br s, 1 H) 2,24-2,42 (m, 4 H) 2,94 (s, 3 H) 3,19-3,27 (m, 2 H) 3,48 (br s, 1 H) 3,90 (s, 3 H) 3,98 (br d, J=6,46 Гц, 1 H) 4,36-4,45 (m, 1 H) 4,46-4,55 (m, 1 H) 4,57-4,64 (m, 2 H) 7,33 (br d, J=8,22 Гц, 2 H) 7,47 (br d, J=8,22 Гц, 2 H) 7,79 (br s, 1 H) 7,84 (s, 1 H) 7,97 (d, J=5,87 Гц, 2 H) 8,20 (br d, J=1,76 Гц, 1 H) 8,47 (s, 1 H);
[868] MS (ESI, масса/заряд): 555,3 [M+H]+
[869] Пример 164. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2R)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[870] Используя (1S,2R)-2-((4-бромбензил)окси)циклопентан-1-амин и пинаколиновый сложный эфир (4-((4-метилпиперазин-1-ил)метил)фенил)бороновой кислоты, названное соединение получали, как описано для примера 134.
[871] 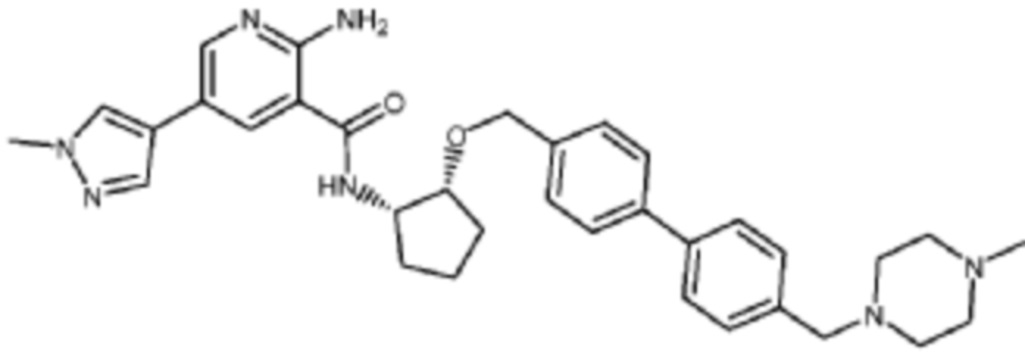
[872] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,58-1,69 (m, 1 H) 1,82-1,97 (m, 4 H) 2,00-2,07 (m, 1 H) 2,83-2,90 (m, 3 H) 3,79 (s, 3 H) 3,80-3,87 (m, 2 H) 4,11-4,18 (m, 1 H) 4,36-4,43 (m, 1 H) 4,45 (d, J=11,74 Гц, 1 H) 4,67 (d, J=11,74 Гц, 1 H) 7,38 (d, J=8,22 Гц, 2 H) 7,40-7,44 (m, 2 H) 7,46 (d, J=8,22 Гц, 2 H) 7,49 (d, J=8,22 Гц, 2 H) 7,78 (s, 1 H) 7,83 (s, 1 H) 8,12-8,19 (m, 1 H) 8,44 (s, 1 H);
[873] MS (ESI, масса/заряд): 580,3 [M+H]+
[874] Пример 165. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1R,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[875] Используя (1R,2S)-2-((4-бромбензил)окси)циклопентан-1-амин и пинаколиновый сложный эфир (4-((4-метилпиперазин-1-ил)метил)фенил)бороновой кислоты, названное соединение получали, как описано для примера 134.
[876] 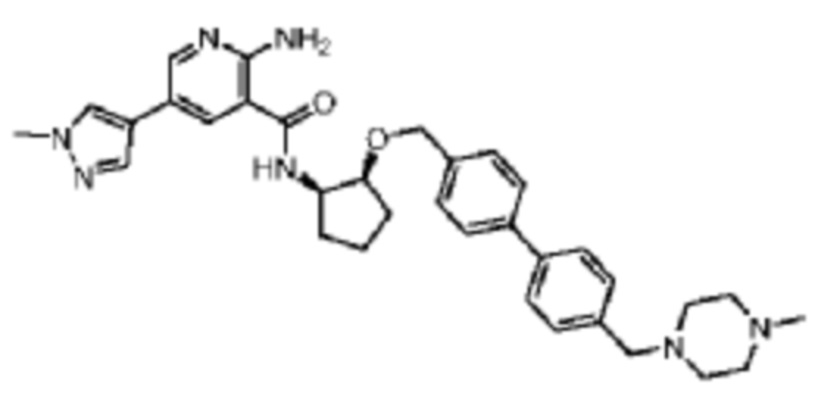
[877] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,60-1,70 (m, 1 H) 1,81-1,98 (m, 4 H) 2,00-2,09 (m, 1 H) 2,87 (s, 3 H) 3,79 (s, 3 H) 3,80-3,85 (m, 2 H) 4,15 (d, J=4,70 Гц, 1 H) 4,36-4,42 (m, 1 H) 4,45 (d, J=11,74 Гц, 1 H) 4,67 (d, J=12,33 Гц, 1 H) 7,38 (d, J=8,22 Гц, 2 H) 7,42 (d, J=7,04 Гц, 2 H) 7,46 (d, J=8,22 Гц, 2 H) 7,48-7,50 (m, 2 H) 7,78 (s, 1 H) 7,83 (s, 1 H) 8,15 (d, J=1,76 Гц, 1 H) 8,44 (d, J=2,35 Гц, 1 H);
[878] MS (ESI, масса/заряд): 580,3 [M+H]+
[879] Пример 166. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклогексил)никотинамид
[880] Используя (1S,2S)-2-((4-бромбензил)окси)циклогексан-1-амин и пинаколиновый сложный эфир(4-((4-метилпиперазин-1-ил)метил)фенил)бороновой кислоты, названное соединение получали, как описано для примера 134.
[881] 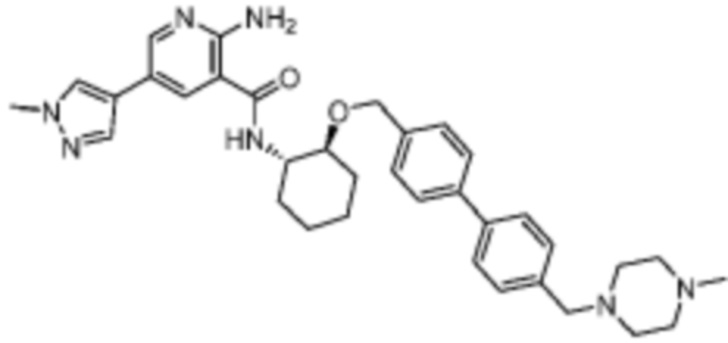
[882] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,43 (br s, 4 H) 1,97-2,07 (m, 2 H) 2,18 (br s, 2 H) 2,32 (s, 3 H) 3,40-3,48 (m, 1 H) 3,58 (s, 2 H) 3,80-3,89 (m, 1 H) 3,90 (s, 3 H) 4,61 (s, 2 H) 7,41 (dd, J=14,09, 8,22 Гц, 4 H) 7,55-7,62 (m, 4 H) 7,78 (s, 1 H) 7,89 (s, 1 H) 8,03 (d, J=1,76 Гц, 1 H) 8,23 (br s, 1 H);
[883] MS (ESI, масса/заряд): 594,4 [M+H]+
[884] Пример 167. 2-амино-N-((1S,2S)-2-((4'-(2-(4-метилпиперазин-1-ил)пропан-2-ил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[885] Используя 2-аминоникотиновую кислоту и пинаколиновый сложный эфир (4-(2-(4-метилпиперазин-1-ил)пропан-2-ил)фенил)бороновой кислоты, названное соединение получали, как описано для примера 134.
[886] 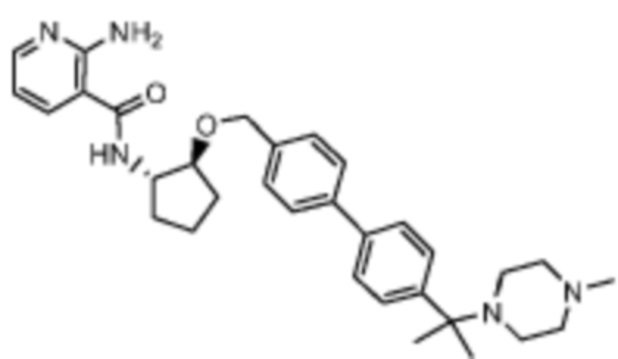
[887] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,47 (s, 6 H) 1,55-1,70 (m, 1 H) 1,82 (br d, J=7,04 Гц, 3 H) 2,03 (br s, 1 H) 2,12-2,25 (m, 1 H) 2,86 (s, 3 H) 4,00 (br s, 1 H) 4,40 (br s, 1 H) 4,66 (s, 2 H) 6,90-6,99 (m, 1 H) 7,38-7,46 (m, 2 H) 7,59 (br dd, J=10,96, 7,83 Гц, 6 H) 8,01 (d, J=5,09 Гц, 1 H) 8,33 (d, J=7,83 Гц, 1 H);
[888] MS (ESI, масса/заряд): 528,3 [M+H]+
[889] Пример 168. 2-амино-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-3-(трифторметил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[890] Используя 2-аминоникотиновую кислоту, (1S,2S)-2-((4-бром-2-(трифторметил)бензил)окси)циклопентан-1-амин и пинаколиновый сложный эфир 4-(4-метилпиперазинo)метилфенилбороновой кислоты, названное соединение получали, как описано для примера 134.
[891] 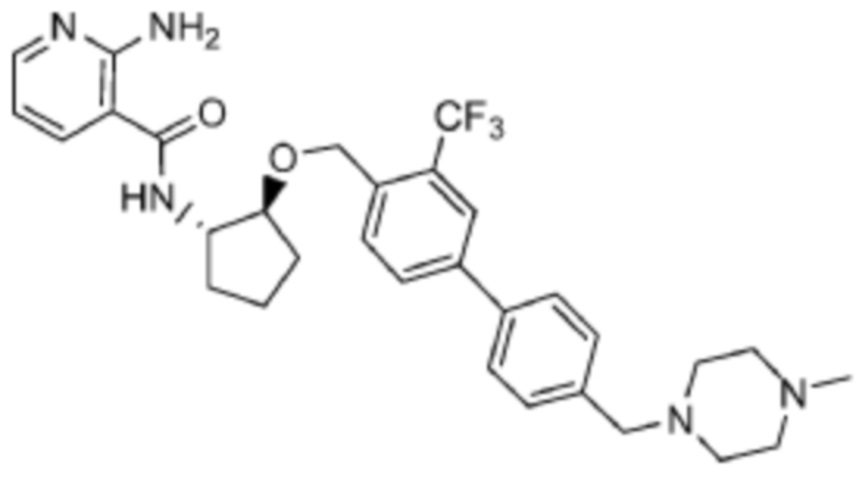
[892] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,66 (dt, J=13,60, 6,70 Гц, 1 H) 1,78-1,93 (m, 3 H) 1,97-2,12 (m, 1 H) 2,13-2,26 (m, 1 H) 2,87 (s, 3 H) 3,77 (s, 2 H) 4,00-4,05 (m, 1 H) 4,43 (br dd, J=10,76, 7,63 Гц, 1 H) 6,98 (dd, J=7,43, 6,26 Гц, 1 H) 7,48 (d, J=8,22 Гц, 2 H) 7,65 (d, J=8,22 Гц, 2 H) 7,77-7,93 (m, 3 H) 8,02 (br dd, J=6,26, 1,57 Гц, 1 H) 8,37 (dd, J=7,43, 1,57 Гц, 1 H):
[893] MS (ESI, масса/заряд): 568,3 [M+H]+
[894] Пример 169. амино-N-((1S,2S)-2-((3'-гидрокси-[1,1'-бифенил]-3-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[895] Схема получения соединения из примера 169:
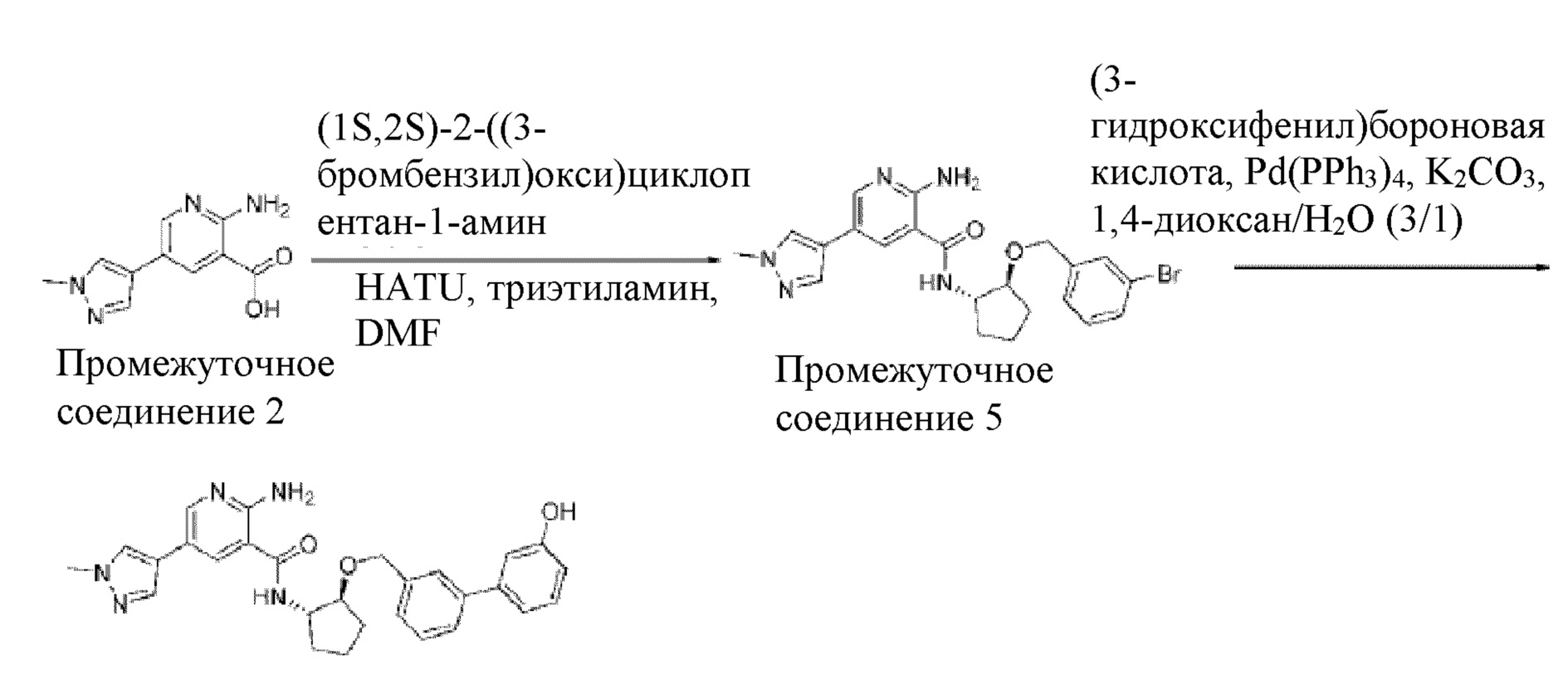
[896]
[897] Промежуточное соединение 5. В смесь промежуточного соединения 2 (350 мг, 1,60 ммоль) и триэтиламина (0,34 мл, 2,41 ммоль) в 4 мл DMF добавляли HATU (732 мг, 1,92 ммоль), а затем (1S,2S)-2-((3-бромбензил)окси)циклопентан-1-амин (475 мг, 1,76 ммоль). Смесь перемешивали при комнатной температуре в течение 1 часа, а затем добавляли насыщенный раствор бикарбоната натрия. Смесь экстрагировали при помощи EtOAc, промывали солевым раствором, сушили над MgSO4 и концентрировали in vacuo. Неочищенный продукт очищали колоночной хроматографией на силикагеле с получением 680 мг грязно-белого твердого вещества.
[898] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,58-1,69 (m, 1 H) 1,72-1,88 (m, 3 H) 1,96-2,08 (m, 1 H) 2,16 (td, J=13,35, 7,92 Гц, 1 H) 3,86-4,00 (m, 3 H) 4,39 (td, J=7,48, 4,40 Гц, 1 H) 4,60 (q, J=12,72 Гц, 2 H) 7,20 (t, J=7,92 Гц, 1 H) 7,29 (d, J=7,63 Гц, 1 H) 7,35 (d, J=7,63 Гц, 1 H) 7,50 (s, 1 H) 7,45-7,53 (m, 1 H) 7,86 (s, 1 H) 8,00 (s, 1 H) 8,23 (d, J=2,35 Гц, 1 H) 8,46 (d, J=1,76 Гц, 1 H):
[899] MS (ESI, масса/заряд): 470,1/472,1 [M+H]+
[900] Пример 169. 2-амино-N-((1S,2S)-2-((3'-гидрокси-[1,1'-бифенил]-3-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[901] В смесь промежуточного соединения 5 (33 мг, 0,07 ммоль) и (3-гидроксифенил)бороновой кислоты (11 мг, 0,08 ммоль) в 0,4 мл 1,4-диоксана/воды (3/1) добавляли K2CO3 (29 мг, 0,21 ммоль), а затем Pd(PPh3)4 (4 мг, 0,003 ммоль). Реакционную смесь нагревали при 100°C в течение 3 часов, охлаждали до комнатной температуры и экстрагировали при помощи EtOAc, сушили над безводным MgSO4 и концентрировали под вакуумом. Неочищенный остаток растворяли в 0,5 мл CH2Cl2/TFA (10/1) и смесь перемешивали в течение 2 ч. После концентрирования под вакуумом неочищенный остаток очищали препаративной HPLC с получением 27 мг названного соединения.
[902] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,62 (br dd, J=12,62, 6,75 Гц, 1 H) 1,81 (br d, J=4,70 Гц, 3 H) 2,03 (br d, J=11,74 Гц, 1 H) 2,16 (br s, 1 H) 3,92 (s, 3 H) 3,94-4,01 (m, 1 H) 4,43 (br s, 1 H) 4,64-4,74 (m, 2 H) 7,13 (br d, J=6,46 Гц, 2 H) 7,34-7,43 (m, 3 H) 7,47 (br d, J=7,63 Гц, 2 H) 7,58-7,62 (m, 1 H) 7,81 (s, 1 H) 7,96 (s, 1 H) 8,17 (br d, J=1,76 Гц, 1 H) 8,36 (br d, J=2,35 Гц, 1 H);
[903] MS (ESI, масса/заряд): 484,2 [M+H]+
[904] Пример 170. 2-амино-N-((1S,2S)-2-((3'-амино-[1,1'-бифенил]-3-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[905] Используя (3-аминофенил)бороновую кислоту, названное соединение получали, как описано для примера 169.
[906] 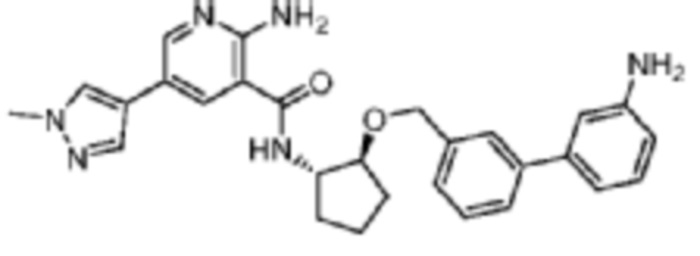
[907] MS (ESI, масса/заряд): 483,2 [M+H]+
[908] Пример 171. 2-амино-N-((1S,2S)-2-((3'-(гидроксиметил)-[1,1'-бифенил]-3-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[909] Используя (3-(гидроксиметил)фенил)бороновую кислоту, названное соединение получали, как описано для примера 169.
[910] 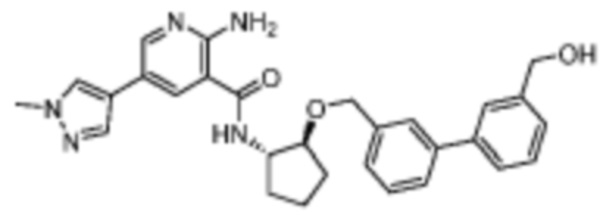
[911] MS (ESI, масса/заряд): 498,2 [M+H]+
[912] Пример 172. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[913] Схема получения соединения из примера 172:
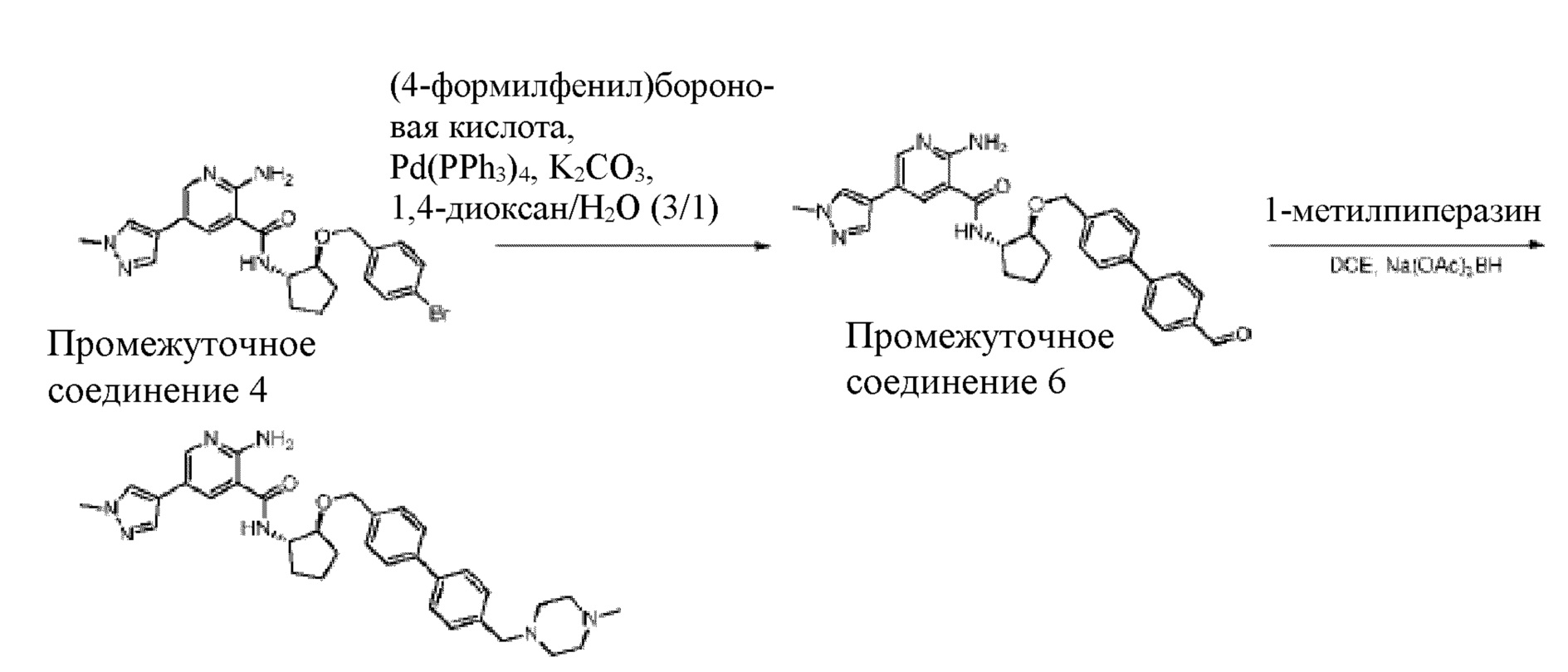
[914]
[915] Промежуточное соединение 6. В смесь промежуточного соединения 4 (33 мг, 0,07 ммоль) и (4-формилфенил)бороновой кислоты (12 мг, 0,08 ммоль) в 0,4 мл 1,4-диоксана/воды (3/1) добавляли K2CO3 (29 мг, 0,21 ммоль), а затем Pd(PPh3)4 (4 мг, 0,003 ммоль). Реакционную смесь нагревали при 100°C в течение 3 часов, охлаждали до комнатной температуры и экстрагировали при помощи EtOAc, сушили над безводным MgSO4. После концентрирования под вакуумом неочищенный остаток очищали препаративной HPLC с получением 30 мг названого соединения.
[916] 1H-ЯМР (400 MГц, CDCl3) δ ppm 1,52-1,62 (m, 1 H) 1,74-1,85 (m, 3 H) 1,85-1,93 (m, 1 H) 1,97-2,06 (m, 1 H) 2,27 (br dd, J=13,30, 5,48 Гц, 1 H) 3,87 (s, 3 H) 3,97-4,03 (m, 1 H) 4,36-4,46 (m, 1 H) 4,69 (s, 2 H) 6,90 (br s, 1 H) 7,12 (br s, 1 H) 7,16-7,19 (m, 1 H) 7,43-7,48 (m, 2 H) 7,50 (s, 1 H) 7,54-7,60 (m, 2 H) 7,68 (m, J=8,22 Гц, 2 H) 7,79 (s, 1 H) 7,90 (m, J=8,22 Гц, 2 H) 7,98 (s, 1 H) 10,02 (s, 1 H); MS (ESI, масса/заряд): 496,2 [M+H]+
[917] Пример 172. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[918] В промежуточное соединение 6 (30 мг, 0,06 ммоль) в 0,4 мл дихлорэтана добавляли 1-метилпиперазин (12 мг, 0,12 ммоль), а затем NaBH(OAc)3 (26 мг, 0,18 ммоль). Смесь перемешивали при комнатной температуре в течение 4 часов, а затем добавляли воду. Смесь экстрагировали при помощи EtOAc, промывали солевым раствором, сушили над MgSO4. После концентрирования под вакуумом неочищенный остаток очищали препаративной HPLC с получением 27 мг названого соединения.
[919] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,52-1,67 (m, 1 H) 1,69-1,86 (m, 3 H) 2,01 (br dd, J=12,52, 5,87 Гц, 1 H) 2,08-2,21 (m, 1 H) 2,28 (s, 3 H) 2,51 (br s, 8 H) 3,54 (s, 2 H) 3,84 (s, 3 H) 3,91-3,99 (m, 1 H) 4,40 (br d, J=4,70 Гц, 1 H) 4,64 (br d, J=3,13 Гц, 2 H) 7,34 (br d, J=7,83 Гц, 2 H) 7,39 (br d, J=8,22 Гц, 2 H) 7,47 (br d, J=7,83 Гц, 1 H) 7,50 (br d, J=7,83 Гц, 2 H) 7,73 (s, 1 H) 7,81 (s, 1 H) 7,96 (s, 1 H) 8,23 (s, 1 H);
[920] MS (ESI, масса/заряд): 580,3 [M+H]+
[921] Пример 173. 2-амино-N-((1S,2S)-2-((4'-(((2-гидроксиэтил)амино)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[922] Используя 2-аминоэтан-1-ол, названное соединение получали, как описано для примера 172.
[923] 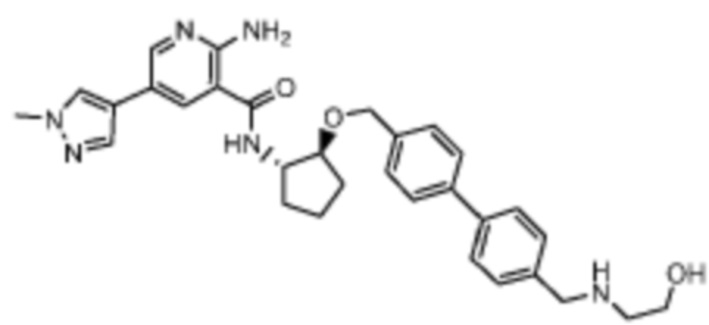
[924] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,59-1,69 (m, 1 H) 1,74-1,88 (m, 3 H) 1,99-2,11 (m, 1 H) 2,18 (td, J=12,91, 7,04 Гц, 1 H) 3,11-3,12 (m, 1 H) 3,11-3,16 (m, 1 H) 3,77-3,86 (m, 2 H) 3,90 (s, 3 H) 3,93 (br d, J=5,87 Гц, 1 H) 3,97-4,05 (m, 1 H) 4,26 (s, 2 H) 4,39-4,48 (m, 1 H) 4,67 (s, 2 H) 7,44 (d, J=8,22 Гц, 2 H) 7,53 (m, J=8,22 Гц, 2 H) 7,55-7,62 (m, 2 H) 7,66 (d, J=8,22 Гц, 2 H) 7,85 (s, 1 H) 7,97 (s, 1 H) 8,20 (s, 1 H) 8,49 (br s, 1 H);
[925] MS (ESI, масса/заряд): 541,3 [M+H]+
[926] Пример 174. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-(морфолинометил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[927] Используя морфолин, названное соединение получали, как описано для примера 172.
[928] 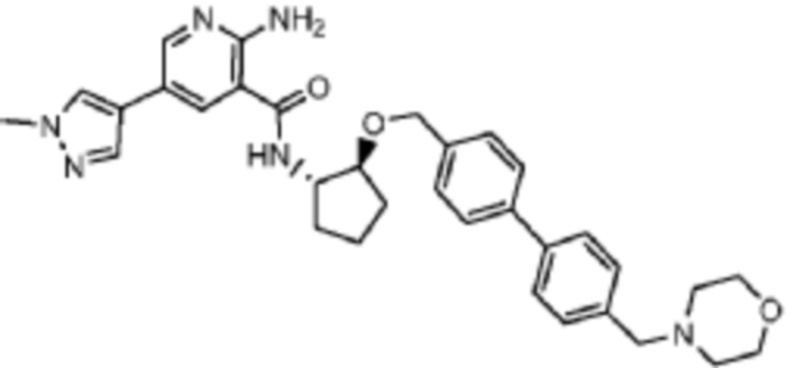
[929] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,57-1,69 (m, 1 H) 1,74-1,90 (m, 3 H) 2,04 (s, 1 H) 2,14-2,23 (m, 1 H) 2,19 (br d, J=7,63 Гц, 1 H) 3,31-3,46 (m, 2 H) 3,90 (s, 3 H) 3,99-4,03 (m, 1 H) 4,39 (s, 2 H) 4,42 (br d, J=5,28 Гц, 1 H) 4,67 (d, J=3,52 Гц, 2 H) 7,45 (d, J=8,22 Гц, 2 H) 7,56 (d, J=8,22 Гц, 2 H) 7,59 (d, J=8,22 Гц, 2 H) 7,71 (d, J=7,63 Гц, 2 H) 7,85 (s, 1 H) 7,98 (s, 1 H) 8,21 (d, J=1,76 Гц, 1 H) 8,49 (br s, 1 H);
[930] MS (ESI, масса/заряд): 567,3 [M+H]+
[931] Пример 175. 2-амино-N-((1S,2S)-2-((4'-((3,3-дифторпиперидин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[932] Используя 3,3-дифторпиперидин, названное соединение получали, как описано для примера 172.
[933] 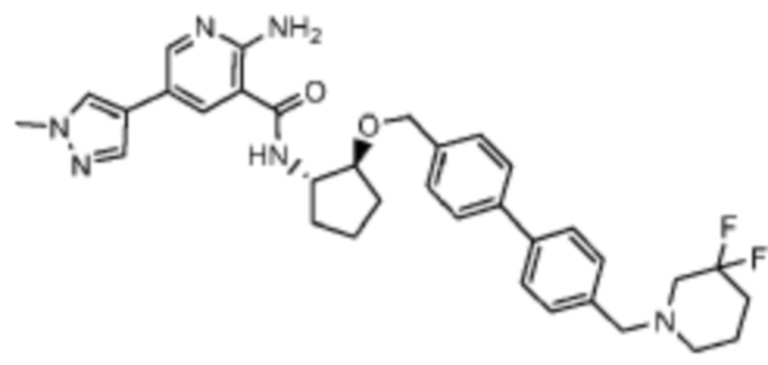
[934] MS (ESI, масса/заряд): 601,3 [M+H]+
[935] Пример 176. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-((4-метилпиперидин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[936] Используя 4-метилпиперидин, названное соединение получали, как описано для примера 172.
[937] 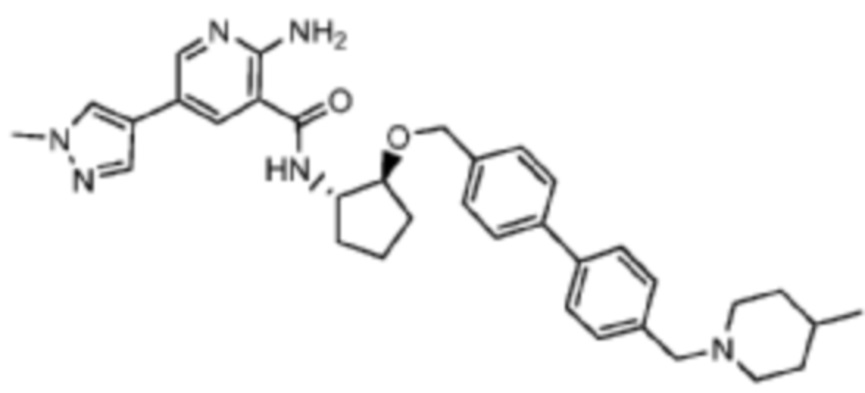
[938] MS (ESI, масса/заряд): 579,3 [M+H]+
[939] Пример 177. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-(пиперазин-1-илметил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[940] Используя пиперазин, названное соединение получали, как описано для примера 172.
[941] 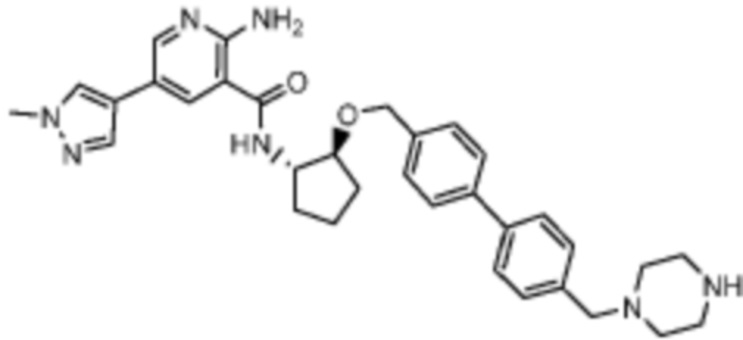
[942] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,63 (br dd, J=13,50, 7,04 Гц, 1 H) 1,73-1,88 (m, 3 H) 2,00-2,08 (m, 1 H) 2,13-2,22 (m, 1 H) 2,96 (br s, 4 H) 3,32 (br d, J=9,98 Гц, 4 H) 3,50 (s, 1 H) 3,84-3,89 (m, 2 H) 3,90 (s, 3 H) 4,00 (br s, 1 H) 4,38-4,44 (m, 1 H) 4,66 (d, J=2,93 Гц, 2 H) 7,38-7,47 (m, 4 H) 7,52-7,60 (m, 4 H) 7,85 (s, 1 H) 7,97 (s, 1 H) 8,19 (d, J=2,35 Гц, 1 H) 8,50 (d, J=2,35 Гц, 1 H);
[943] MS (ESI, масса/заряд): 566,3 [M+H]+
[944] Пример 178. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-((4-фенилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[945] Используя 1-фенилпиперазин, названное соединение получали, как описано для примера 172.
[946] 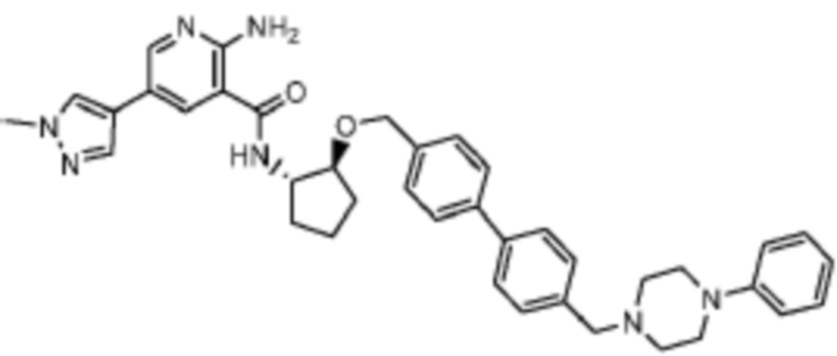
[947] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,61-1,69 (m, 1 H) 1,76-1,87 (m, 3 H) 2,00-2,07 (m, 1 H) 2,15-2,23 (m, 1 H) 3,90 (s, 3 H) 3,98-4,04 (m, 1 H) 4,39-4,44 (m, 1 H) 4,45 (s, 2 H) 4,68 (s, 2 H) 6,92 (t, J=7,34 Гц, 1 H) 7,00 (d, J=8,22 Гц, 2 H) 7,27 (t, J=7,92 Гц, 2 H) 7,45 (d, J=8,22 Гц, 2 H) 7,60 (dd, J=9,68, 8,51 Гц, 4 H) 7,72 (br d, J=8,22 Гц, 2 H) 7,85 (s, 1 H) 7,98 (s, 1 H) 8,21 (d, J=1,76 Гц, 1 H) 8,51 (d, J=1,76 Гц, 1 H);
[948] MS (ESI, масса/заряд): 642,4 [M+H]+
[949] Пример 179. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-((4-(пирролидин-1-ил)пиперидин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[950] Используя 4-(пирролидин-1-ил)пиперидин, названное соединение получали, как описано для примера 172.
[951] 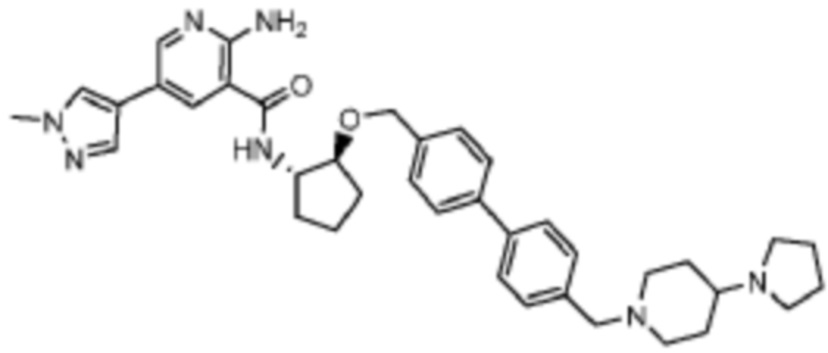
[952] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,60-1,69 (m, 1 H) 1,74-1,88 (m, 3 H) 1,96-2,23 (m, 8 H) 2,43 (br d, J=13,50 Гц, 2 H) 3,06-3,21 (m, 4 H) 3,44 (br s, 2 H) 3,66 (br d, J=12,91 Гц, 4 H) 3,90 (s, 3 H) 3,99-4,03 (m, 1 H) 4,37 (s, 2 H) 4,39-4,45 (m, 1 H) 4,67 (s, 2 H) 7,41-7,48 (m, 2 H) 7,51-7,57 (m, 2 H) 7,58 (d, J=8,22 Гц, 2 H) 7,68 (br d, J=8,22 Гц, 2 H) 7,85 (s, 1 H) 7,98 (s, 1 H) 8,20 (d, J=2,35 Гц, 1 H) 8,50 (d, J=1,76 Гц, 1 H);
[953] MS (ESI, масса/заряд): 634,4 [M+H]+
[954] Пример 180. 2-амино-N-((1S,2S)-2-((4'-((4-гидроксипиперидин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[955] Используя пиперидин-4-ол, названное соединение получали, как описано для примера 172.
[956] 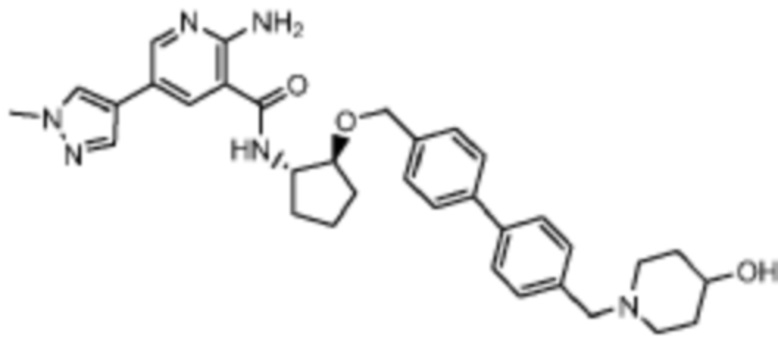
[957] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,59-1,68 (m, 1 H) 1,74-1,87 (m, 3 H) 1,92 (br s, 1 H) 2,03 (dt, J=13,35, 6,53 Гц, 1 H) 2,10-2,23 (m, 1 H) 3,07 (br s, 1 H) 3,51 (br d, J=10,56 Гц, 1 H) 3,82 (br s, 1 H) 3,89-3,92 (m, 3 H) 3,98-4,03 (m, 1 H) 4,08 (br s, 1 H) 4,34 (br s, 2 H) 4,39-4,45 (m, 1 H) 4,67 (s, 2 H) 7,45 (d, J=8,22 Гц, 2 H) 7,54 (br s, 2 H) 7,57-7,61 (m, 2 H) 7,59 (d, J=8,22 Гц, 2 H) 7,69 (br d, J=8,22 Гц, 2 H) 7,85 (s, 1 H) 7,99 (s, 1 H) 8,21 (s, 1 H) 8,52 (d, J=1,76 Гц, 1 H);
[958] MS (ESI, масса/заряд): 581,3 [M+H]+
[959] Пример 181. 2-амино-N-((1S,2S)-2-((4'-((4-(2-гидроксиэтил)пиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[960] Используя 2-(пиперазин-1-ил)этан-1-ол, названное соединение получали, как описано для примера 172.
[961] 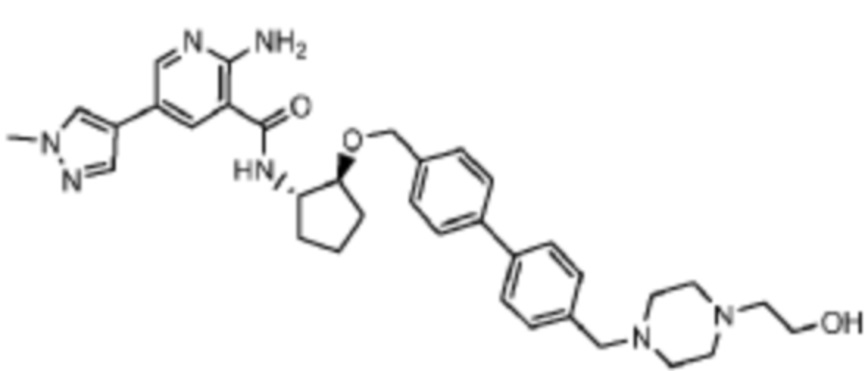
[962] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,64 (br dd, J=13,50, 7,04 Гц, 1 H) 1,76-1,86 (m, 3 H) 2,00-2,08 (m, 1 H) 2,14-2,22 (m, 1 H) 3,19 (br s, 2 H) 3,82-3,85 (m, 2 H) 3,90 (s, 3 H) 3,98-4,02 (m, 1 H) 4,39-4,44 (m, 1 H) 4,66 (s, 2 H) 7,40-7,47 (m, 4 H) 7,53-7,61 (m, 4 H) 7,85 (s, 1 H) 7,97 (s, 1 H) 8,20 (d, J=2,35 Гц, 1 H) 8,52 (d, J=2,35 Гц, 1 H);
[963] MS (ESI, масса/заряд): 610,3 [M+H]+
[964] Пример 182. 2-амино-N-((1S,2S)-2-((4'-((4-(2-гидрокси-2-метилпропил)пиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[965] Используя 2-метил-1-(пиперазин-1-ил)пропан-2-ол, названное соединение получали, как описано для примера 172.
[966] 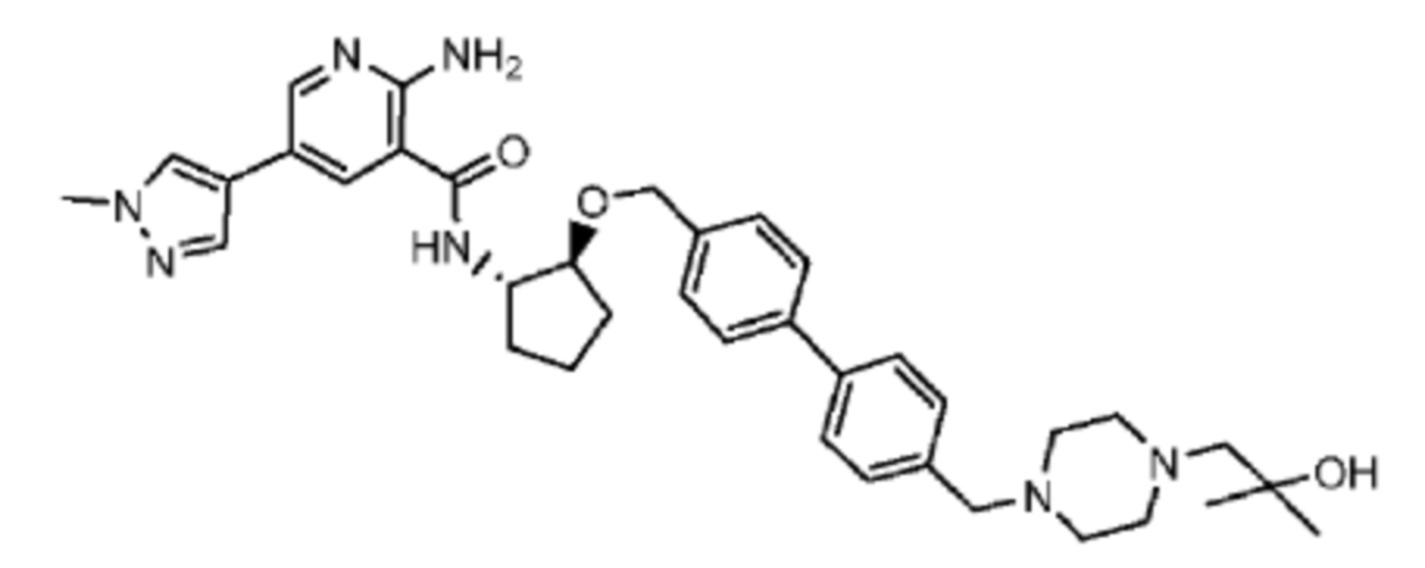
[967] MS (ESI, масса/заряд): 638,4 [M+H]+
[968] Пример 183. 2-амино-N-((1S,2S)-2-((4'-((4-этилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[969] Используя 1-этилпиперазин, названное соединение получали, как описано для примера 172.
[970] 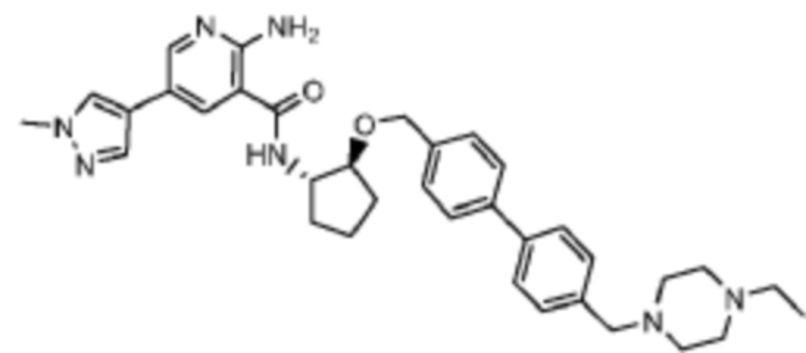
[971] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,32 (t, J=7,34 Гц, 3 H) 1,59-1,68 (m, 1 H) 1,74-1,88 (m, 3 H) 2,04 (dq, J=13,50, 6,85 Гц, 1 H) 2,13-2,21 (m, 1 H) 3,18 (br d, J=7,63 Гц, 2 H) 3,78-3,87 (m, 2 H) 3,90 (s, 3 H) 3,98-4,02 (m, 1 H) 4,38-4,44 (m, 1 H) 4,66 (d, J=1,76 Гц, 2 H) 7,38-7,46 (m, 4 H) 7,51-7,60 (m, 4 H) 7,85 (s, 1 H) 7,97 (s, 1 H) 8,19 (d, J=2,35 Гц, 1 H) 8,51 (d, J=2,35 Гц, 1 H); MS (ESI, масса/заряд): 594,4 [M+H]+
[972] Пример 184. 2-амино-N-((1S,2S)-2-((4'-((4-циклопропилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[973] Используя 1-циклопропилпиперазин, названное соединение получали, как описано для примера 172.
[974] 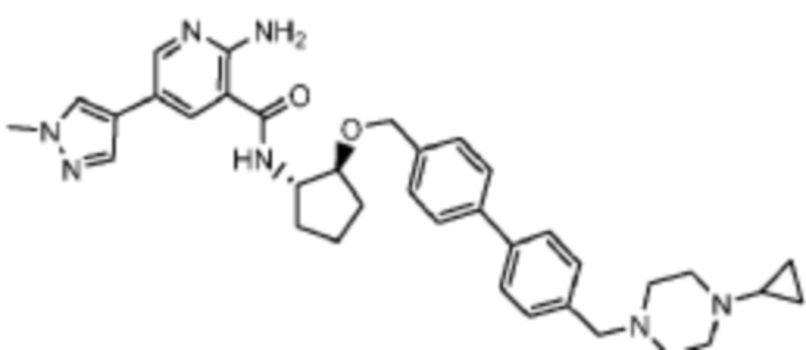
[975] MS (ESI, масса/заряд): 606,4 [M+H]+
[976] Пример 185. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-(((R)-3-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[977] Используя трет-бутил-(R)-2-метилпиперазин-1-карбоксилат, названное соединение получали, как описано для примера 172 и после снятия защитных групп при помощи TFA.
[978] 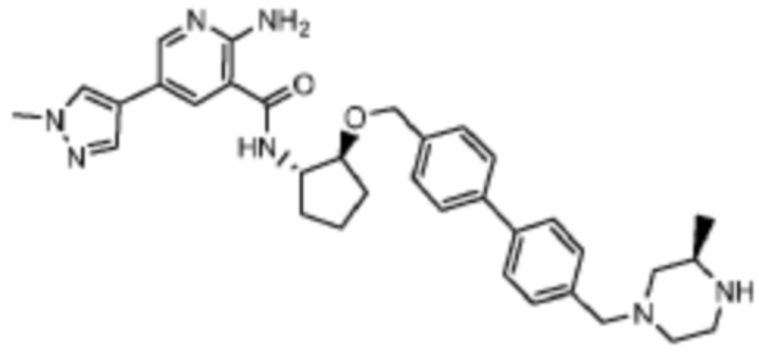
[979] MS (ESI, масса/заряд): 580,3 [M+H]+
[980] Пример 186. 2-амино-N-((1S,2S)-2-((4'-(((R)-3,4-диметилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[981] Используя (R)-1,2-диметилпиперазин, названное соединение получали, как описано для примера 172.
[982] 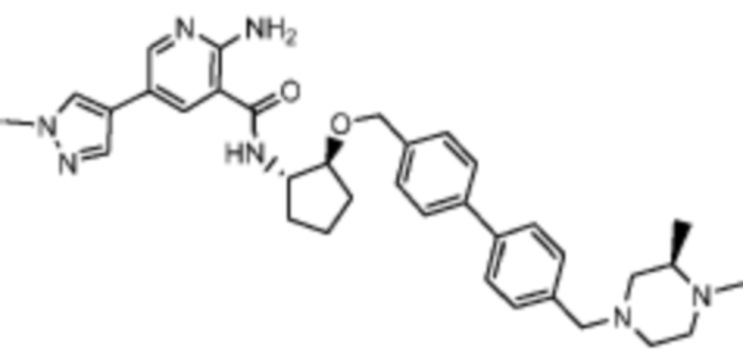
[983] MS (ESI, масса/заряд): 594,4 [M+H]+
[984] Пример 187. 2-амино-N-((1S,2S)-2-((4'-(((R)-2,4-диметилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[985] Используя (R)-1,3-диметилпиперазин, названное соединение получали, как описано для примера 172.
[986] 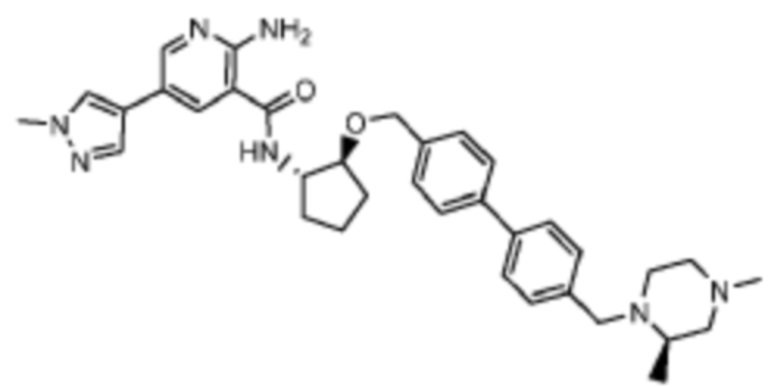
[987] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,34 (br d, J=5,09 Гц, 3 H) 1,63 (br dd, J=15,06, 6,46 Гц, 1 H) 1,81 (br d, J=7,43 Гц, 3 H) 2,03 (br d, J=6,26 Гц, 1 H) 2,18 (s, 1 H) 2,55 (br s, 1 H) 2,82 (s, 3 H) 2,92 (br s, 1 H) 3,02 (br d, J=12,52 Гц, 1 H) 3,89 (s, 3 H) 4,00 (br s, 1 H) 4,30 (br d, J=11,35 Гц, 1 H) 4,42 (br s, 1 H) 4,65 (s, 2 H) 7,41 (br d, J=7,43 Гц, 4 H) 7,54 (br dd, J=7,63, 3,33 Гц, 4 H) 7,84 (s, 1 H) 7,96 (s, 1 H) 8,19 (s, 1 H) 8,50 (s, 1 H);
[988] MS (ESI, масса/заряд): 594,4 [M+H]+
[989] Пример 188. 2-амино-N-((1S,2S)-2-((4'-((3-этил-4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[990] Используя 2-этил-1-метилпиперазин, названное соединение получали, как описано для примера 172.
[991] 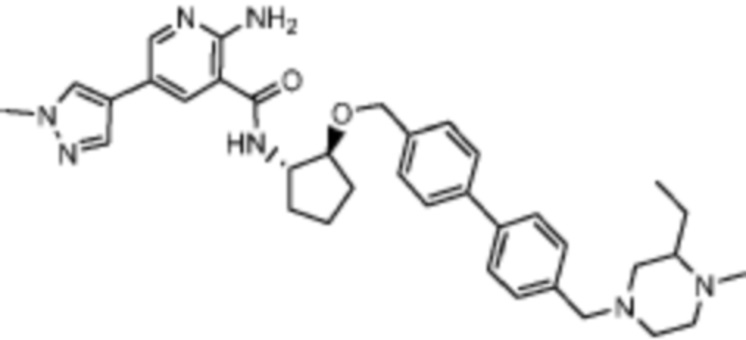
[992] 1H-ЯМР (400 MГц, CD3OD) δ ppm 0,96 (br t, J=7,24 Гц, 3 H) 1,62 (br d, J=14,48 Гц, 3 H) 1,81 (br d, J=7,43 Гц, 3 H) 1,92 (br s, 1 H) 2,04 (br s, 1 H) 2,16 (br d, J=7,04 Гц, 1 H) 2,87 (s, 3 H) 3,20 (br d, J=14,09 Гц, 1 H) 3,45 (br d, J=13,30 Гц, 1 H) 3,70 (br d, J=13,30 Гц, 1 H) 3,81 (br d, J=12,91 Гц, 1 H) 3,89 (s, 3 H) 3,99 (br s, 1 H) 4,42 (br s, 1 H) 4,65 (s, 2 H) 7,41 (br d, J=8,22 Гц, 4 H) 7,55 (br d, J=7,43 Гц, 4 H) 7,85 (s, 1 H) 7,97 (s, 1 H) 8,19 (s, 1 H) 8,51 (s, 1 H);
[993] MS (ESI, масса/заряд): 608,4 [M+H]+
[994] Пример 189. 2-амино-N-((1S,2S)-2-((4'-((цис-3,5-диметилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[995] Используя трет-бутил-цис-2,6-диметилпиперазин-1-карбоксилат, названное соединение получали, как описано для примера 172 и после снятия защитных групп при помощи TFA.
[996] 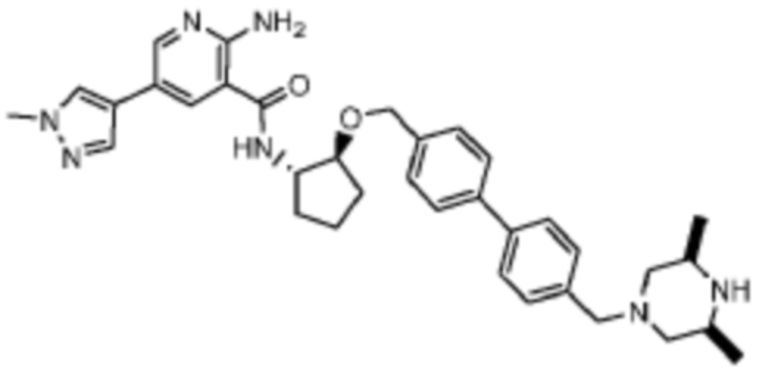
[997] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,27 (br d, J=6,26 Гц, 6 H) 1,64 (br d, J=5,87 Гц, 1 H) 1,81 (br d, J=7,04 Гц, 3 H) 1,96-2,24 (m, 3 H) 3,09 (d, J=12,91 Гц, 2 H) 3,62 (br s, 5 H) 3,68 (s, 3 H) 3,89 (s, 3 H) 4,00 (br s, 1 H) 4,37-4,45 (m, 1 H) 4,65 (s, 2 H) 7,34-7,46 (m, 4 H) 7,53 (br d, J=7,43 Гц, 4 H) 7,83 (s, 1 H) 7,95 (s, 1 H) 8,20 (s, 1 H) 8,45 (s, 1 H);
[998] MS (ESI, масса/заряд): 594,4 [M+H]+
[999] Пример 190. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-((цис-3,4,5-триметилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1000] Используя цис-1,2,6-триметилпиперазин, названное соединение получали, как описано для примера 172.
[1001] 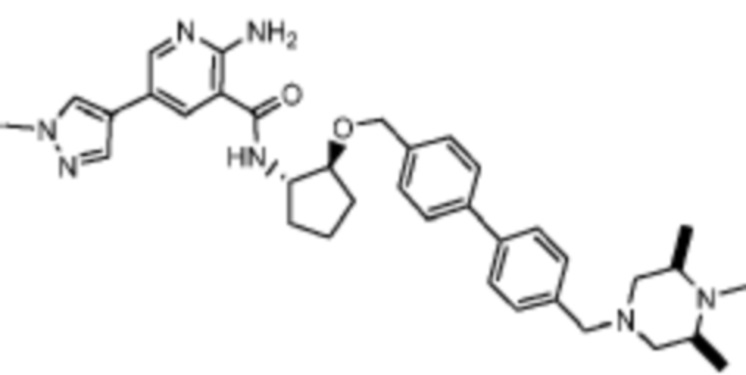
[1002] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,30 (br d, J=6,46 Гц, 6 H) 1,64 (br dd, J=13,50, 7,04 Гц, 1 H) 1,74-1,90 (m, 3 H) 2,00-2,09 (m, 1 H) 2,18 (br dd, J=12,91, 5,87 Гц, 1 H) 2,30 (br d, J=12,91 Гц, 3 H) 3,22 (br s, 3 H) 3,45 (br s, 2 H) 3,84 (br d, J=19,37 Гц, 2 H) 3,90 (s, 3 H) 3,97-4,03 (m, 1 H) 4,38-4,45 (m, 1 H) 4,66 (s, 2 H) 4,69 (s, 1 H) 7,42 (br d, J=7,63 Гц, 4 H) 7,49-7,62 (m, 4 H) 7,85 (s, 1 H) 7,97 (s, 1 H) 8,20 (d, J=2,35 Гц, 1 H) 8,52 (d, J=1,76 Гц, 1 H);
[1003] MS (ESI, масса/заряд): 608,4 [M+H]+
[1004] Пример 191. 2-амино-N-((1S,2S)-2-((4'-((транс-2,5-диметилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[1005] Используя транс-2,5-диметилпиперазин, названное соединение получали, как описано для примера 172.
[1006] 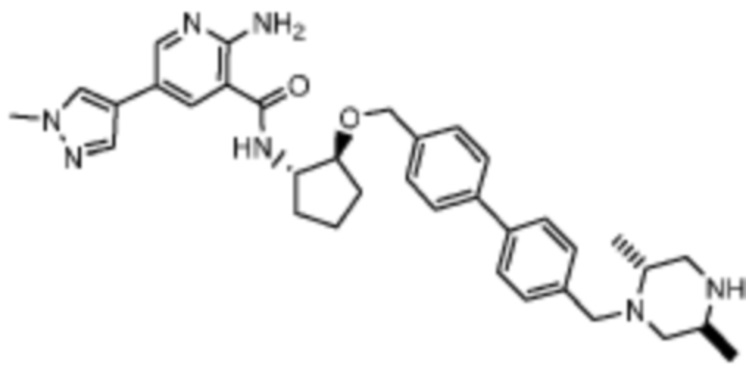
[1007] MS (ESI, масса/заряд): 594,4 [M+H]+
[1008] Пример 192. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-(((2R,5S)-2,4,5-триметилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1009] Используя транс-1,2,5-триметилпиперазин, названное соединение получали, как описано для примера 172.
[1010] 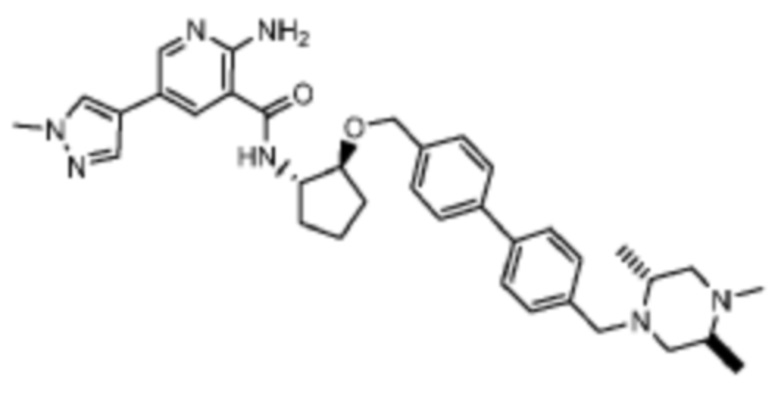
[1011] MS (ESI, масса/заряд): 608,4 [M+H]+
[1012] Пример 193. 2-амино-N-((1S,2S)-2-((4'-((3-(диметиламино)пирролидин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[1013] Используя N,N-диметил-3-пирролидинамин, названное соединение получали, как описано для примера 172.
[1014] 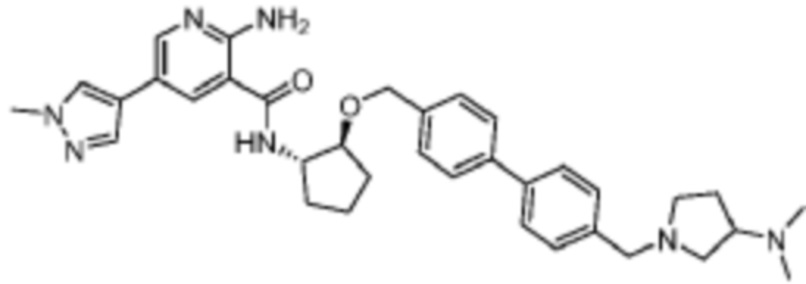
[1015] MS (ESI, масса/заряд): 594,4 [M+H]+
[1016] Пример 194. 3-амино-6-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)пиразин-2-карбоксамид
[1017] Используя 3-амино-6-(1-метил-1H-пиразол-4-ил)пиразин-2-карбоновую кислоту, названное соединение получали, как описано для примера 172.
[1018] 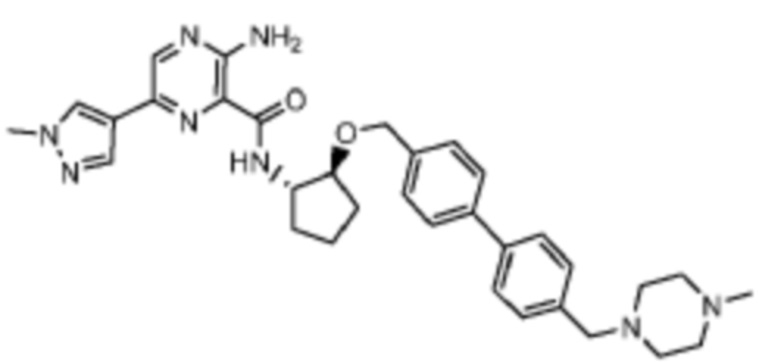
[1019] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,60-1,69 (m, 1 H) 1,70-1,78 (m, 1 H) 1,78-1,87 (m, 2 H) 2,03-2,20 (m, 3 H) 2,88 (d, J=1,76 Гц, 3 H) 3,00 (br s, 4 H) 3,34 (br d, J=11,74 Гц, 3 H) 3,85 (s, 3 H) 3,91 (br d, J=11,74 Гц, 2 H) 3,99-4,06 (m, 1 H) 4,33-4,40 (m, 1 H) 4,59-4,70 (m, 2 H) 7,38 (d, J=8,22 Гц, 2 H) 7,42 (br d, J=8,22 Гц, 2 H) 7,47 (d, J=8,22 Гц, 2 H) 7,52 (br d, J=8,22 Гц, 2 H) 7,99 (s, 1 H) 8,12 (s, 1 H) 8,41 (s, 1 H);
[1020] MS (ESI, масса/заряд): 581,3 [M+H]+
[1021] Пример 195. 2-амино-N-((1S,2S)-2-((3'-фтор-4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[1022] Используя пинаколиновый сложный эфир (3-фтор-4-формилфенил)бороновой кислоты, названное соединение получали, как описано для примера 172.
[1023] 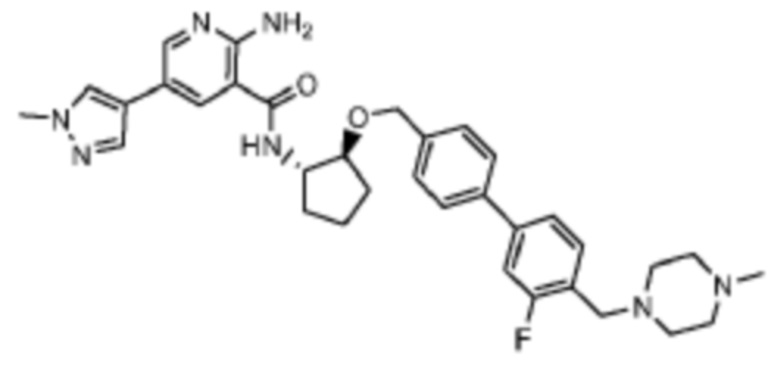
[1024] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,63 (br dd, J=13,69, 7,04 Гц, 1 H) 1,72-1,90 (m, 3 H) 1,96-2,09 (m, 1 H) 2,10-2,23 (m, 1 H) 2,90 (s, 3 H) 3,05-3,27 (m, 4 H) 3,34-3,51 (m, 4 H) 3,89 (s, 3 H) 3,94-4,01 (m, 1 H) 4,07 (s, 2 H) 4,34-4,47 (m, 1 H) 4,60-4,73 (m, 2 H) 5,47 (s, 1 H) 7,35 (br d, J=11,35 Гц, 1 H) 7,42 (br d, J=7,83 Гц, 3 H) 7,50 (br t, J=7,83 Гц, 1 H) 7,55 (d, J=8,22 Гц, 2 H) 7,83 (s, 1 H) 7,97 (s, 1 H) 8,17 (d, J=1,96 Гц, 1 H) 8,50 (d, J=1,96 Гц, 1 H);
[1025] MS (ESI, масса/заряд): 598,7 [M+H]+
[1026] Пример 196. 2-амино-N-((1S,2S)-2-((3',5'-дифтор-4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[1027] Используя пинаколиновый сложный эфир ((3,5-дифтор-4-формилфенил)бороновой кислоты, названное соединение получали, как описано для примера 172.
[1028] 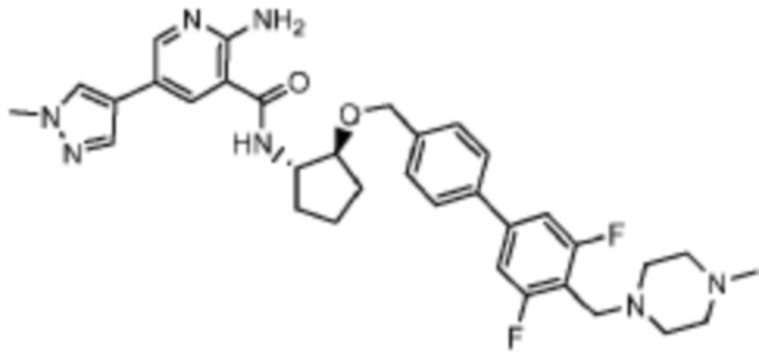
[1029] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,63 (br dd, J=13,30, 7,04 Гц, 1 H) 1,71-1,91 (m, 3 H) 2,03 (br dd, J=12,91, 5,48 Гц, 1 H) 2,12-2,23 (m, 1 H) 2,87 (s, 3 H) 2,94 (br d, J=18,00 Гц, 3 H) 3,32 (br s, 4 H) 3,90 (s, 3 H) 3,99 (br s, 1 H) 4,40 (br d, J=3,91 Гц, 1 H) 4,62-4,77 (m, 2 H) 7,24 (br d, J=8,61 Гц, 2 H) 7,44 (m, J=7,83 Гц, 2 H) 7,57 (m, J=7,83 Гц, 2 H) 7,83 (s, 1 H) 7,98 (s, 1 H) 8,19 (s, 1 H) 8,50 (s, 1 H);
[1030] MS (ESI, масса/заряд): 616,8 [M+H]+
[1031] Пример 197. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-3'-(трифторметил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1032] Используя пинаколиновый сложный эфир (4-формил-3-(трифторметил)фенил)бороновой кислоты, названное соединение получали, как описано для примера 172.
[1033] 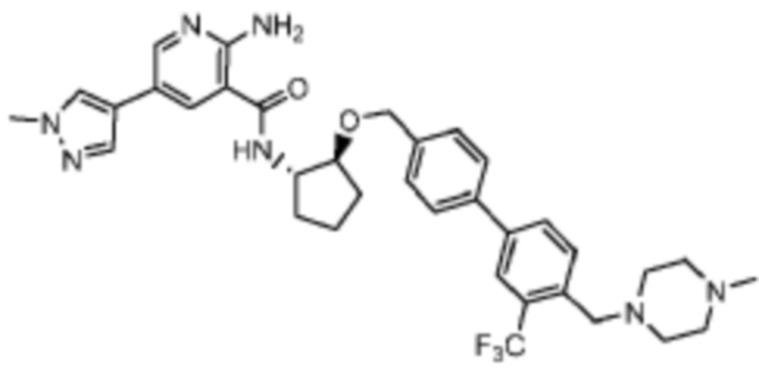
[1034] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,59-1,71 (m, 1 H) 1,75-1,89 (m, 3 H) 1,99-2,10 (m, 1 H) 2,13-2,25 (m, 1 H) 2,91 (s, 3 H) 3,47 (br d, J=1,57 Гц, 2 H) 3,81 (s, 2 H) 3,91 (s, 3 H) 4,02 (br d, J=4,30 Гц, 1 H) 4,39-4,46 (m, 1 H) 4,69 (s, 2 H) 7,47 (m, J=8,22 Гц, 2 H) 7,60 (m, J=8,22 Гц, 2 H) 7,83 (d, J=8,22 Гц, 4 H) 7,98 (s, 1 H) 8,21 (d, J=1,96 Гц, 1 H) 8,50 (d, J=2,35 Гц, 1 H);
[1035] MS (ESI, масса/заряд): 648,32 [M+H]+
[1036] Пример 198. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((3'-метил-4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1037] Используя пинаколиновый сложный эфир (4-формил-3-метилфенил)бороновой кислоты, названное соединение получали, как описано для примера 172.
[1038] 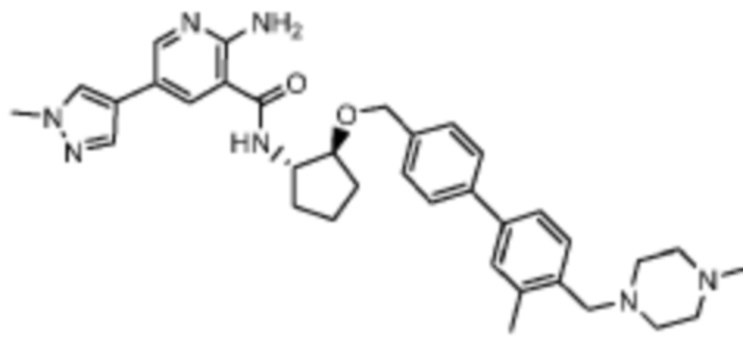
[1039] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,64 (br dd, J=13,11, 6,85 Гц, 2 H) 1,72-1,90 (m, 3 H) 1,82 (br s, 1 H) 1,94-2,09 (m, 2 H) 2,10-2,24 (m, 2 H) 2,43 (s, 1 H) 2,88 (s, 3 H) 3,29-3,31 (m, 11 H) 3,69 (s, 1 H) 3,90 (s, 2 H) 3,93-3,96 (m, 1 H) 4,01 (br d, J=4,70 Гц, 1 H) 4,16 (s, 1 H) 4,37-4,47 (m, 1 H) 4,66 (d, J=3,13 Гц, 1 H) 7,37-7,43 (m, 2 H) 7,51-7,55 (m, 1 H) 7,52-7,59 (m, 1 H) 7,85 (d, J=0,78 Гц, 1 H) 7,96 (s, 1 H) 8,19 (d, J=1,96 Гц, 1 H) 8,49 (d, J=2,35 Гц, 1 H);
[1040] MS (ESI, масса/заряд): 594,4 [M+H]+
[1041] Пример 199. 2-амино-N-((1S,2S)-2-((3'-гидрокси-4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[1042] Используя пинаколиновый сложный эфир (4-формил-3-гидроксифенил)бороновой кислоты, названное соединение получали, как описано для примера 172.
[1043] 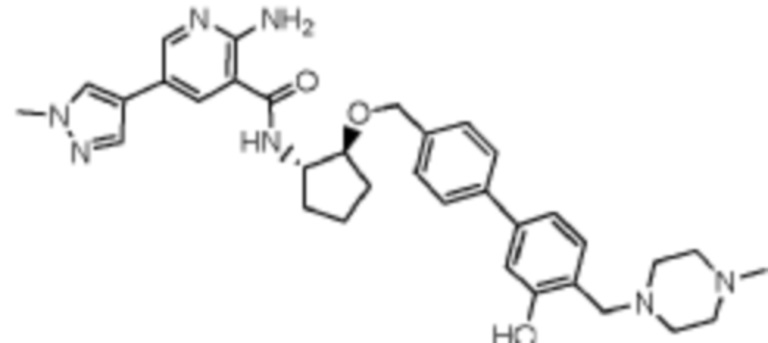
[1044] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,64 (br dd, J=12,72, 6,85 Гц, 1 H) 1,74-1,90 (m, 3 H) 2,05 (br s, 1 H) 2,12-2,26 (m, 1 H) 2,82 (d, J=3,13 Гц, 3 H) 3,13 (br s, 5 H) 3,91 (s, 3 H) 4,01 (br d, J=6,26 Гц, 1 H) 4,05 (s, 1 H) 4,08 (s, 1 H) 4,38-4,46 (m, 1 H) 4,66 (s, 2 H) 7,05 (s, 1 H) 7,28 (br d, J=8,61 Гц, 1 H) 7,25-7,34 (m, 1 H) 7,32 (br d, J=7,83 Гц, 1 H) 7,41 (d, J=8,22 Гц, 2 H) 7,52 (d, J=8,22 Гц, 2 H) 7,54-7,59 (m, 1 H) 7,85 (s, 1 H) 7,97 (s, 1 H) 8,20 (d, J=2,35 Гц, 1 H) 8,48 (d, J=2,35 Гц, 1 H);
[1045] MS (ESI, масса/заряд): 596,3 [M+H]+
[1046] Пример 200. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-3'-нитро-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1047] Используя пинаколиновый сложный эфир (4-формил-3-нитрофенил)бороновой кислоты, названное соединение получали, как описано для примера 172.
[1048] 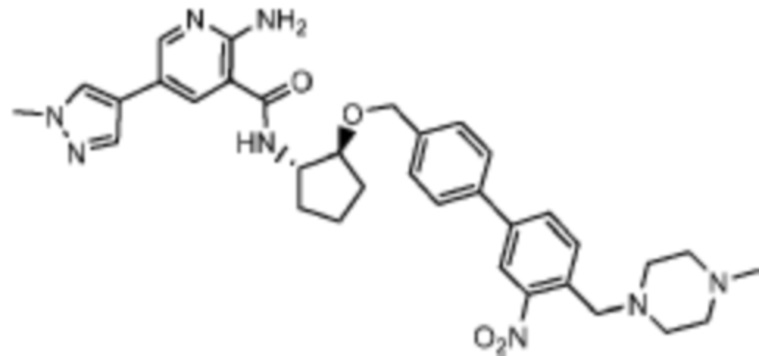
[1049] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,64 (dt, J=13,89, 7,14 Гц, 1 H) 1,74-1,91 (m, 3 H) 2,00-2,10 (m, 1 H) 2,13-2,24 (m, 1 H) 2,88 (s, 3 H) 3,35-3,39 (m, 2 H) 3,91 (s, 3 H) 3,92-3,95 (m, 2 H) 3,99-4,03 (m, 1 H) 4,39-4,47 (m, 1 H) 4,69 (d, J=3,13 Гц, 2 H) 7,48 (d, J=8,22 Гц, 2 H) 7,60-7,65 (m, 4 H) 7,83 (s, 1 H) 7,97 (s, 1 H) 8,02 (d, J=1,96 Гц, 1 H) 8,21 (d, J=2,35 Гц, 1 H) 8,48 (d, J=2,35 Гц, 1 H);
[1050] MS (ESI, масса/заряд): 625,3 [M+H]+
[1051] Пример 201. 2-амино-N-((1S,2S)-2-((3'-метокси-4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[1052] Используя пинаколиновый сложный эфир (4-формил-3-метоксифенил)бороновой кислоты, названное соединение получали, как описано для примера 172.
[1053] 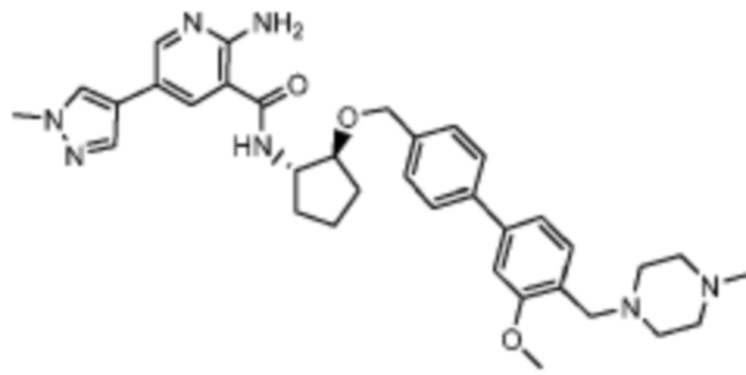
[1054] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,65 (br dd, J=13,50, 6,46 Гц, 1 H) 1,74-1,91 (m, 3 H) 1,99-2,10 (m, 1 H) 2,19 (br d, J=6,65 Гц, 1 H) 2,81 (s, 3 H) 3,91 (s, 3 H) 3,92 (s, 3 H) 3,98-4,07 (m, 1 H) 4,43 (br d, J=3,52 Гц, 1 H) 4,68 (s, 2 H) 7,15-7,24 (m, 2 H) 7,37-7,47 (m, 3 H) 7,59 (d, J=8,22 Гц, 2 H) 7,86 (s, 1 H) 7,98 (s, 1 H) 8,21 (d, J=1,96 Гц, 1 H) 8,51 (d, J=2,35 Гц, 1 H);
[1055] MS (ESI, масса/заряд): 610,3 [M+H]+
[1056] Пример 202. 2-амино-N-((1S,2S)-2-((2'-хлор-4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[1057] Используя пинаколиновый сложный эфир (2-хлор-4-формилфенил)бороновой кислоты, названное соединение получали, как описано для примера 172.
[1058] 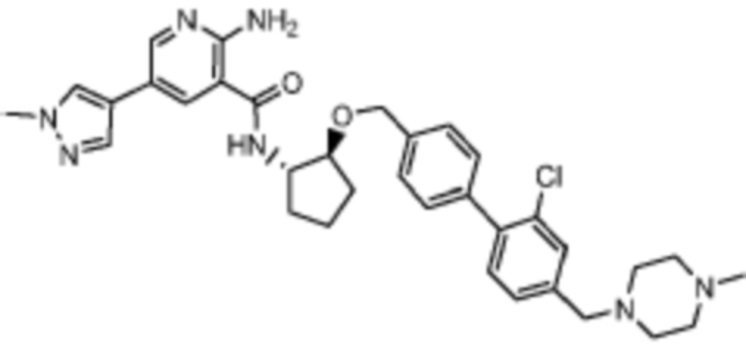
[1059] MS (ESI, масса/заряд): 614,3 [M+H]+
[1060] Пример 203. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4-(6-((4-метилпиперазин-1-ил)метил)пиридин-3-ил)бензил)окси)циклопентил)никотинамид
[1061] Используя пинаколиновый сложный эфир ((6-формилпиридин-3-ил)бороновой кислоты, названное соединение получали, как описано для примера 172.
[1062] 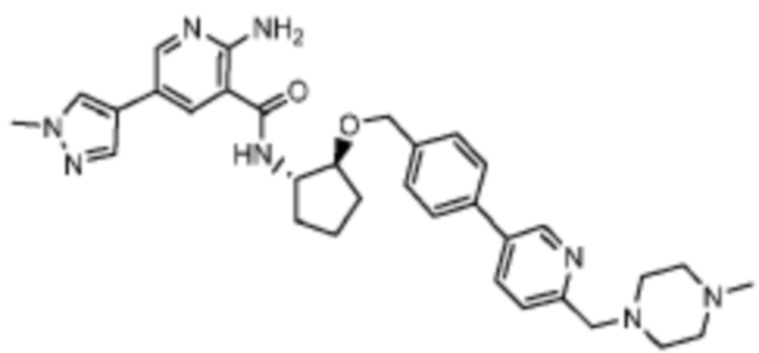
[1063] 1H-ЯМР (400 МГц, CD3OD) δ ppm 1,65 (dt, J=13,60, 7,09 Гц, 1 H) 1,74-1,90 (m, 3 H) 2,05 (br dd, J=13,11, 6,46 Гц, 1 H) 2,13-2,26 (m, 1 H) 2,90 (s, 3 H) 3,91-3,94 (m, 3 H) 3,99-4,06 (m, 1 H) 4,43 (br dd, J=11,93, 6,85 Гц, 1 H) 7,52 (d, J=8,22 Гц, 2 H) 7,64-7,68 (m, 2 H) 7,72 (br dd, J=12,33, 8,41 Гц, 2 H) 7,85 (s, 1 H) 7,99 (s, 1 H) 8,22 (d, J=2,35 Гц, 1 H) 8,51 (d, J=1,96 Гц, 1 H) 8,82 (d, J=2,35 Гц, 1 H);
[1064] MS (ESI, масса/заряд): 581,3 [M+H]+
[1065] Пример 204. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4-(5-((4-метилпиперазин-1-ил)метил)пиридин-2-ил)бензил)окси)циклопентил)никотинамид
[1066] Используя пинаколиновый сложный эфир (5-формилпиридин-2-ил)бороновой кислоты, названное соединение получали, как описано для примера 172.
[1067] 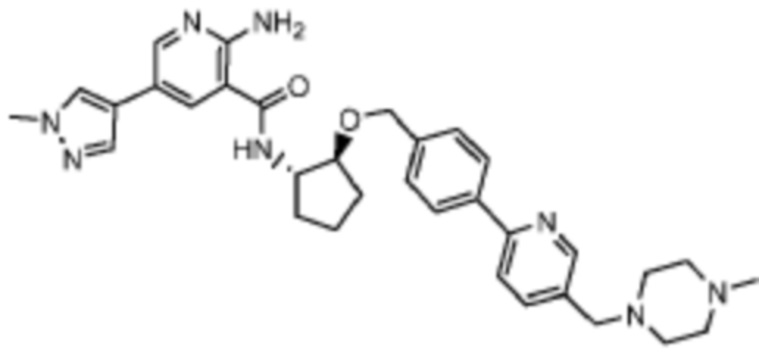
[1068] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,66 (td, J=14,09, 7,04 Гц, 1 H) 1,76-1,92 (m, 3 H) 1,98-2,11 (m, 1 H) 2,19 (br s, 1 H) 2,90 (s, 3 H) 3,64 (s, 1 H) 3,76 (s, 3 H) 3,98-4,07 (m, 1 H) 4,38-4,48 (m, 1 H) 7,52 (d, J=8,22 Гц, 2 H) 7,84 (s, 1 H) 7,90 (dd, J=8,41, 1,76 Гц, 3 H) 7,98 (s, 1 H) 8,02 (br d, J=8,61 Гц, 1 H) 8,21 (d, J=1,96 Гц, 1 H) 8,50 (d, J=1,96 Гц, 1 H) 8,60 (s, 1 H);
[1069] MS (ESI, масса/заряд): 581,3 [M+H]+
[1070] Пример 205. 2-амино-N-((1S,2S)-2-((4'-((4-(2-гидроксиэтил)пиперазин-1-ил)метил)-3'-(трифторметил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[1071] Используя пинаколиновый сложный эфир (4-формил-3-(трифторметил)фенил)бороновой кислоты и 2-(пиперазин-1-ил)этан-1-ол, названное соединение получали, как описано для примера 172.
[1072] 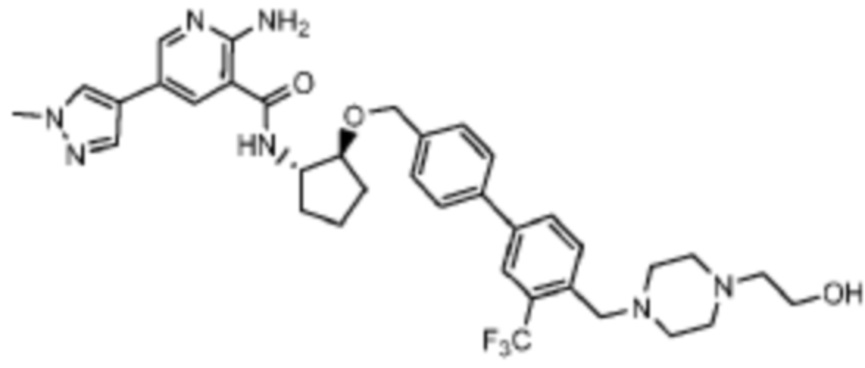
[1073] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,57-1,72 (m, 1 H) 1,75-1,90 (m, 3 H) 2,04 (dt, J=12,81, 6,70 Гц, 1 H) 2,13-2,26 (m, 1 H) 3,82 (s, 2 H) 3,86-3,90 (m, 2 H) 3,91 (s, 3 H) 3,97-4,05 (m, 1 H) 4,43 (br dd, J=11,93, 6,46 Гц, 1 H) 4,69 (s, 2 H) 7,48 (d, J=8,22 Гц, 2 H) 7,60 (d, J=8,22 Гц, 2 H) 7,81-7,87 (m, 3 H) 7,99 (s, 1 H) 8,22 (d, J=2,35 Гц, 1 H) 8,51 (d, J=1,96 Гц, 1 H);
[1074] MS (ESI, масса/заряд): 678,3 [M+H]+
[1075] Пример 206. 2-амино-N-((1S,2S)-2-((2'-хлор-4'-((4-(2-гидроксиэтил)пиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[1076] Используя пинаколиновый сложный эфир (2-хлор-4-формилфенил)бороновой кислоты и 2-(пиперазин-1-ил)этан-1-ол, названное соединение получали, как описано для примера 172.
[1077] 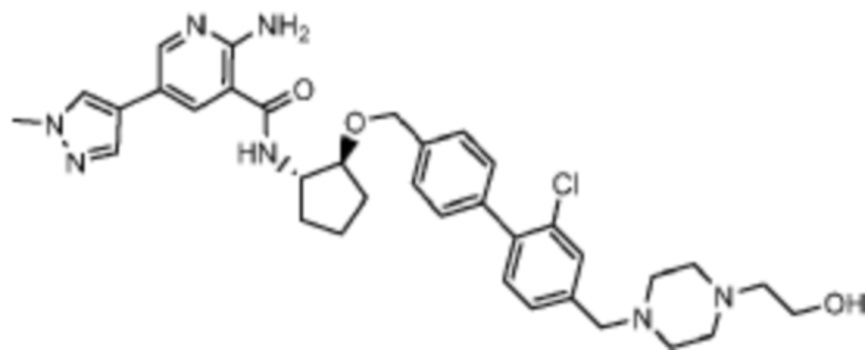
[1078] MS (ESI, масса/заряд): 644,3 [M+H]+
[1079] Пример 207. 2-амино-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-3'-(трифторметил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1080] Используя 2-аминоникотиновую кислоту и пинаколиновый сложный эфир (4-формил-3-(трифторметил)фенил)бороновой кислоты, названное соединение получали, как описано для примера 172.
[1081] 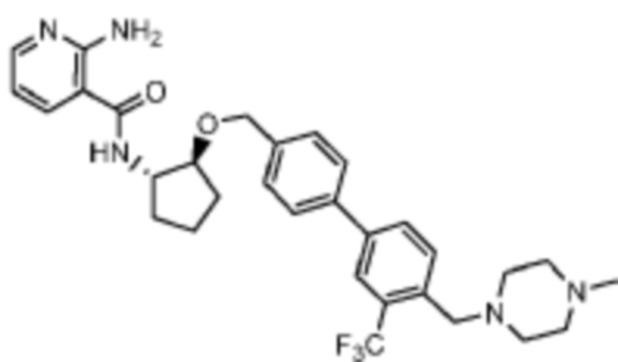
[1082] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,53-1,69 (m, 1 H) 1,76-1,89 (m,3 H) 2,01 (s, 1 H) 2,18 (br dd, J=13,30, 5,87 Гц, 1 H) 2,48 (br s, 2 H) 2,91 (s, 3 H) 3,82 (s, 2 H) 3,99 (br d, J=4,30 Гц, 1 H) 4,40 (br d, J=5,09 Гц, 1 H) 4,68 (d, J=4,30 Гц, 2 H) 6,95 (dd, J=7,43, 6,26 Гц, 1 H) 7,47 (d, J=8,22 Гц, 2 H) 7,62 (d, J=8,22 Гц, 2 H) 7,84-7,92 (m, 3 H) 7,98-8,05 (m, 1 H) 8,32 (dd, J=7,43, 1,56 Гц, 1 H);
[1083] MS (ESI, масса/заряд): 568,3 [M+H]+
[1084] Пример 208. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-(1-(4-метилпиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1085] Схема получения соединения из примера 208:
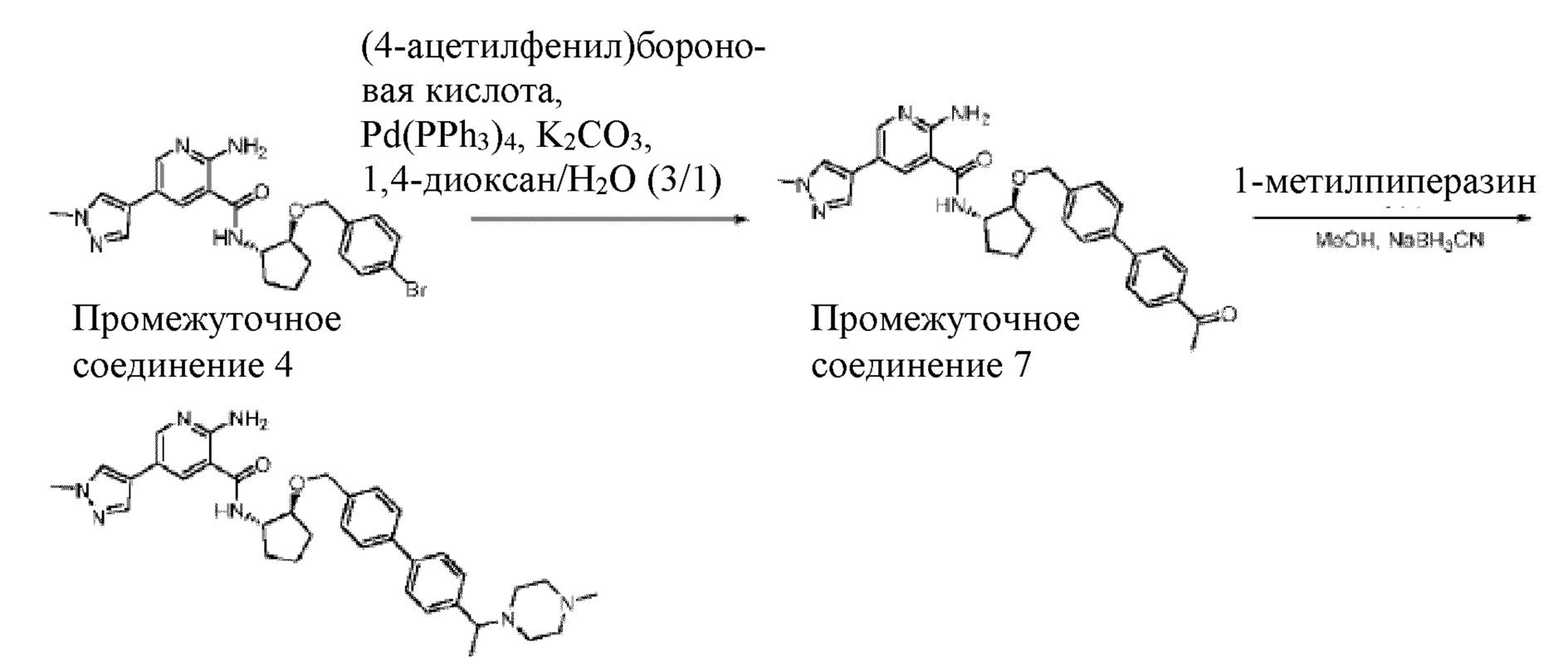
[1086]
[1087] Промежуточное соединение 7. В смесь промежуточного соединения 4 (100 мг, 0,21 ммоль) и (4-ацетилфенил)бороновой кислоты (52 мг, 0,32 ммоль) в 1,2 мл 1,4-диоксана/воды (3/1) добавляли K2CO3 (88 мг, 0,64 ммоль), а затем Pd(PPh3)4 (12 мг, 0,01 ммоль). Реакционную смесь нагревали при 100°C в течение 3 часов, охлаждали до комнатной температуры и экстрагировали при помощи EtOAc, сушили над безводным MgSO4. После концентрирования под вакуумом неочищенный продукт очищали колоночной хроматографией на силикагеле с получением 80 мг грязно-белого твердого вещества
[1088] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,62 (br dd, J=13,21, 7,34 Гц, 1 H) 1,74-1,88 (m, 3 H) 2,05 (br dd, J=12,62, 7,34 Гц, 1 H) 2,17 (br dd, J=13,21, 5,58 Гц, 1 H) 2,62 (s, 3 H) 3,89 (s, 3 H) 3,96-4,01 (m, 1 H) 4,38-4,45 (m, 1 H) 4,61-4,73 (m, 2 H) 7,45 (d, J=8,22 Гц, 2 H) 7,60 (d, J=8,22 Гц, 2 H) 7,66 (d, J=8,22 Гц, 2 H) 7,82 (s, 1 H) 7,94 (s, 1 H) 8,01 (d, J=8,22 Гц, 2 H) 8,18 (d, J=1,76 Гц, 1 H) 8,44 (d, J=1,76 Гц, 1 H);
[1089] MS (ESI, масса/заряд): 510,8 [M+H]+
[1090] Пример 208. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-(1-(4-метилпиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1091] В смесь промежуточного соединения 7 (30 мг, 0,06 ммоль) в 0,4 мл метанола добавляли 1-метилпиперазин (14 мкл, 0,12 ммоль), а затем NaBH3CN (11 мг, 0,18 ммоль). Смесь перемешивали при комнатной температуре в течение 4 часов, а затем добавляли воду. Смесь экстрагировали при помощи EtOAc, промывали солевым раствором, сушили над MgSO4. После концентрирования под вакуумом неочищенный остаток очищали препаративной HPLC с получением 17 мг названого соединения.
[1092] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,40 (d, J=6,46 Гц, 3 H) 1,59 (br dd, J=13,21, 7,34 Гц, 1 H) 1,73-1,85 (m, 3 H) 1,98-2,05 (m, 1 H) 2,15 (br dd, J=13,21, 5,58 Гц, 1 H) 2,31 (s, 3 H) 2,35-2,77 (m, 8 H) 3,41-3,48 (m, 1 H) 3,86 (s, 3 H) 3,90-3,99 (m, 1 H) 4,37-4,44 (m, 1 H) 4,61-4,70 (m, 2 H) 7,34 (d, J=7,63 Гц, 2 H) 7,39 (br d, J=7,63 Гц, 2 H) 7,48 (br d, J=7,63 Гц, 2 H) 7,50 (br d, J=8,22 Гц, 2 H) 7,74 (s, 1 H) 7,82 (d, J=2,93 Гц, 1 H) 7,96 (s, 1 H) 8,22-8,26 (m, 1 H);
[1093] MS (ESI, масса/заряд): 594,7 [M+H]+
[1094] Пример 209. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-(1-((3S,5R)-3,4,5-триметилпиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1095] Используя (2S,6R)-1,2,6-триметилпиперазин, названное соединение получали, как описано для примера 208.
[1096] 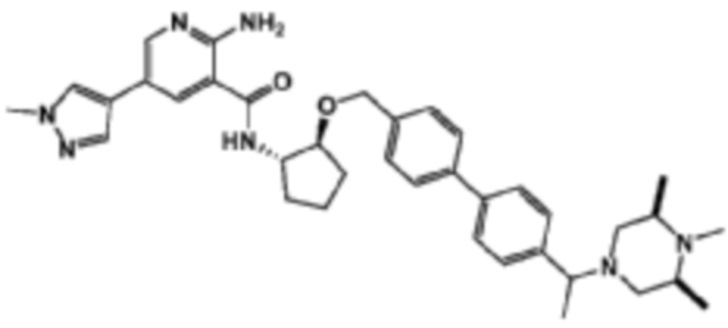
[1097] MS (ESI, масса/заряд): 622,4 [M+H]+
[1098] Пример 210. 2-амино-N-((1S,2S)-2-((4'-(1-(4-(2-гидроксиэтил)пиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[1099] Используя 1-(2-гидроксиэтил)пиперазин, названное соединение получали, как описано для примера 208.
[1100] 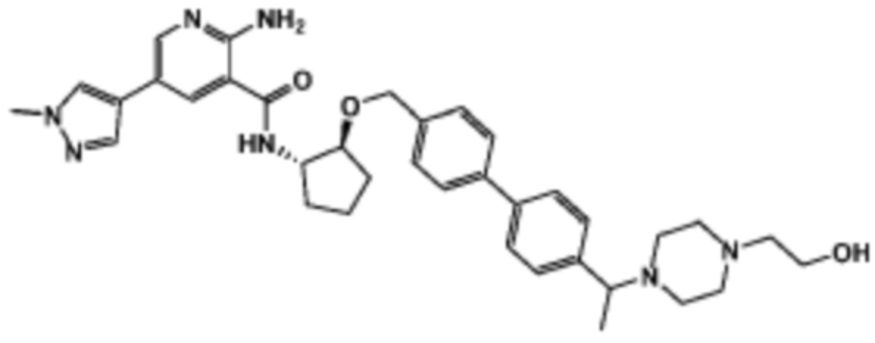
[1101] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,64 (br dd, J=13,50, 7,04 Гц, 1 H) 1,69 (d, J=7,04 Гц, 3 H) 1,75-1,88 (m, 3 H) 2,00-2,08 (m, 1 H) 2,18 (br dd, J=13,50, 5,87 Гц, 1 H) 3,16-3,23 (m, 2 H) 3,23-3,27 (m, 2 H) 3,53 (br s, 4 H) 3,84 (br t, J=4,99 Гц, 2 H) 3,90 (s, 3 H) 3,98-4,03 (m, 1 H) 4,25 (br d, J=7,04 Гц, 1 H) 4,38-4,45 (m, 1 H) 4,64-4,70 (m, 2 H) 7,43 (d, J=7,63 Гц, 2 H) 7,51 (m, J=8,22 Гц, 2 H) 7,56 (m, J=8,22 Гц, 2 H) 7,64 (d, J=8,22 Гц, 2 H) 7,85 (s, 1 H) 7,98 (s, 1 H) 8,19 (s, 1 H) 8,53 (s, 1 H);
[1102] MS (ESI, масса/заряд): 624,4 [M+H]+
[1103] Пример 211. 2-амино-N-((1S,2S)-2-((4'-(1-((3S,5R)-4-(2-гидроксиэтил)-3,5-диметилпиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[1104] Используя 2-(цис-2,6-диметилпиперазин-1-ил)этан-1-ол, названное соединение получали, как описано для примера 208.
[1105] 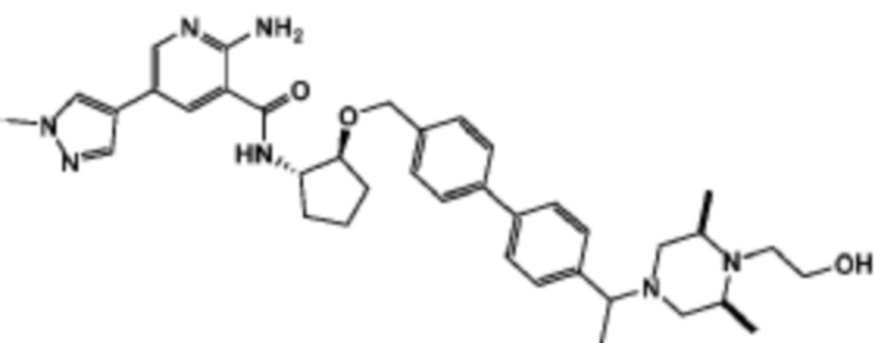
[1106] MS (ESI, масса/заряд): 652,4 [M+H]+
[1107] Пример 212. 2-амино-N-((1S,2S)-2-((3',5'-дифтор-4'-(1-(4-(2-гидроксиэтил)пиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[1108] Используя пинаколиновый сложный эфир (4-ацетил-3,5-дифторфенил)бороновой кислоты и 2-(пиперазин-1-ил)этан-1-ол, названное соединение получали, как описано для примера 208.
[1109] 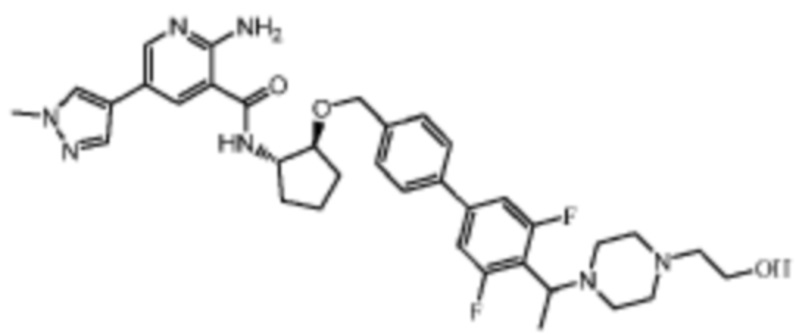
[1110] MS (ESI, масса/заряд): 660,32 [M+H]+
[1111] Схема получения промежуточного соединения 9:
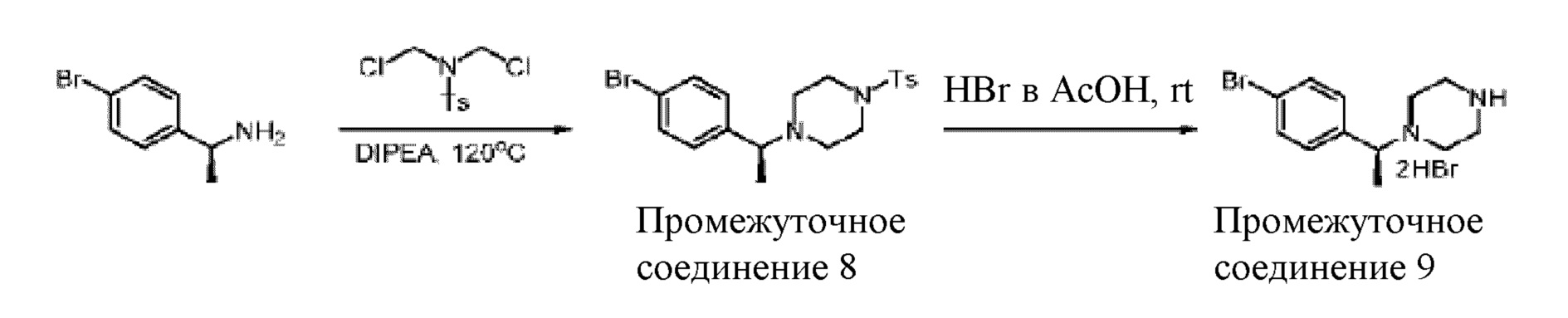
[1112]
[1113] Промежуточное соединение 8. Смесь (S)-1-(4-бромфенил)этиламина (300 мг, 1,50 ммоль) и (N,N-бис(2-хлорэтил)-4-метилбензолсульфонамида (533 мг, 1,80 ммоль) в 3 мл DIPEA нагревали при 120°C в течение 24 ч., охлаждали до комнатной температуры и экстрагировали при помощи EtOAc, сушили над безводным MgSO4. После концентрирования под вакуумом неочищенный продукт очищали колоночной хроматографией на силикагеле с получением 500 мг грязно-белого твердого вещества
[1114] 1H-ЯМР (600 MГц, DMSO-d6) δ ppm 1,16 (d, J=6,46 Гц, 3 H) 2,27-2,33 (m, 2 H) 2,39 (s, 5 H) 2,78 (br s, 4 H) 3,37-3,44 (m, 1 H) 7,16 (d, J=7,87 Гц, 2 H) 7,43 (t, J=7,59 Гц, 4 H) 7,55-7,60 (m, 2 H):
[1115] MS (ESI, масса/заряд): 423,1/ 425,2 [M+H]+
[1116] Промежуточное соединение 9. (S)-1-(1-(4-бромфенил)этил)пиперазин
[1117] Промежуточное соединение 8 (0,5 г, 1,1 ммоль) в 5 мл HBr в AcOH перемешивали при комнатной температуре в течение 24 ч. После концентрирования под вакуумом неочищенный продукт разбавляли при помощи EtOAC и твердое вещество собирали фильтрацией с получением 0,5 г грязно-белого твердого вещества
[1118] 1H-ЯМР (600 MГц, DMSO-d6) δ ppm 1,63 (br s, 3 H) 3,40 (br s, 1 H) 3,47-3,72 (br s, 8 H) 7,54 (br s, 2 H) 7,69 (br d, J=7,63 Гц, 2 H);
[1119] MS (ESI, масса/заряд): 269,1/ 271,4 [M+H]+
[1120] Промежуточное соединение 10. (R)-1-(1-(4-бромфенил)этил)пиперазин
[1121] Используя (R)-1-(4-бромфенил)этиламин, названное соединение получали, как описано для промежуточного соединения 9.
[1122] 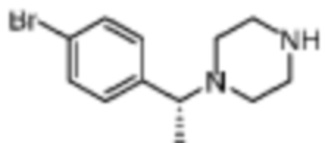
[1123] MS (ESI, масса/заряд): 269,1/ 271,4 [M+H]+
[1124] Промежуточное соединение 11. 1-(1-(4-бромфенил)циклопропил)пиперазин
[1125] Используя 1-(4-бромфенил)циклопропан-1-амин, названное соединение получали, как описано для промежуточного соединения 9.
[1126] 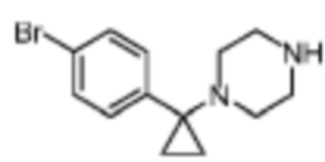
[1127] MS (ESI, масса/заряд): 281,1/ 283,4 [M+H]+
[1128] Промежуточное соединение 12. 1-(2-(4-бромфенил)пропан-2-ил)пиперазин
[1129] Используя 2-(4-бромфенил)пропан-2-амин, названное соединение получали, как описано для промежуточного соединения 9.
[1130] 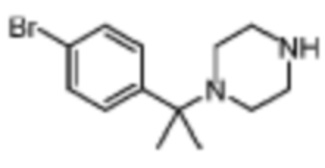
[1131] MS (ESI, масса/заряд): 283,1/ 285,4 [M+H]+
[1132] Пример 213 и 214.
[1133] Схема получения соединений из примера 213 и 214;
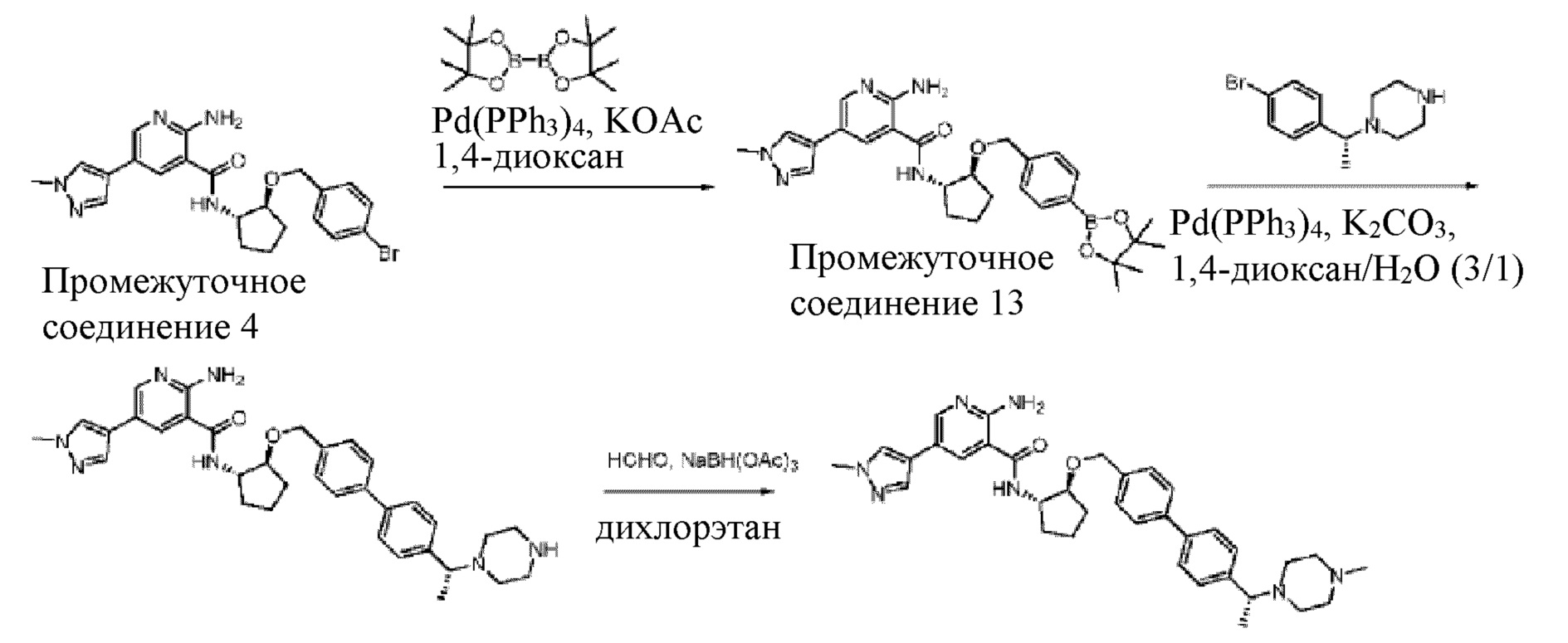
[1134]
[1135] Промежуточное соединение 13. В смесь промежуточного соединения 4 (0,56 г, 1,19 ммоль) и бис(пинаколато)дибора (0,6 г, 2,38 ммоль) в 6 мл 1,4-диоксана добавляли KOAc (0,35 г, 3,57 ммоль), а затем Pd(PPh3)4 (69 мг, 0,06 ммоль). Реакционную смесь нагревали при 110°C в течение 5 часов, охлаждали до комнатной температуры и разделяли между водой и EtOAc, сушили над безводным MgSO4. После концентрирования под вакуумом неочищенный продукт очищали колоночной хроматографией на силикагеле с получением 0,5 г светло-желтого твердого вещества.
[1136] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,19 (s, 6 H) 1,30 (s, 6 H) 1,60 (br dd, J=13,30, 7,04 Гц, 1 H) 1,68-1,88 (m, 3 H) 1,93-2,06 (m, 1 H) 2,15 (br dd, J=13,11, 6,06 Гц, 1 H) 3,90 (s, 3 H) 3,92-3,99 (m, 1 H) 4,32-4,44 (m, 1 H) 4,64 (s, 2 H) 7,33 (m, J=7,83 Гц, 2 H) 7,66 (m, J=7,83 Гц, 2 H) 7,75 (s, 1 H) 7,85 (s, 1 H) 7,97 (d, J=1,96 Гц, 1 H) 8,20-8,30 (m, 1 H);
[1137] MS (ESI, масса/заряд): 518,3 [M+H]+
[1138] Пример 213. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-((R)-1-(пиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1139] В смесь промежуточного соединения 13 (150 мг, 0,29 ммоль) и промежуточного соединения 10 (100 мг, 0,29 ммоль) в 1,5 мл 1,4-диоксана/воды (3/1) добавляли K2CO3 (120 мг, 0,87 ммоль), а затем Pd(PPh3)4 (17 мг, 0,01 ммоль). Реакционную смесь нагревали при 100°C в течение 3 часов, охлаждали до комнатной температуры и экстрагировали при помощи EtOAc, сушили над безводным MgSO4. После концентрирования под вакуумом неочищенный продукт очищали колоночной хроматографией на силикагеле с получением 130 мг грязно-белого твердого вещества
[1140] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,40 (d, J=6,46 Гц, 3 H) 1,54-1,63 (m, 1 H) 1,73-1,86 (m, 3 H) 1,98-2,05 (m, 1 H) 2,12-2,19 (m, 1 H) 2,40 (br s, 2 H) 2,82 (t, J=4,99 Гц, 4 H) 3,40 (q, J=6,46 Гц, 1 H) 3,86 (s, 3 H) 3,95 (dt, J=6,90, 4,48 Гц, 1 H) 4,41 (td, J=7,63, 4,70 Гц, 1 H) 4,61-4,70 (m, 2 H) 5,48 (s, 1 H) 7,33 (d, J=8,22 Гц, 2 H) 7,39 (d, J=8,22 Гц, 2 H) 7,44-7,49 (m, 2 H) 7,49-7,55 (m, 2 H) 7,74 (s, 1 H) 7,83 (s, 1 H) 7,97 (d, J=2,35 Гц, 1 H) 8,23 (d, J=2,35 Гц, 1 H);
[1141] MS (ESI, масса/заряд): 580,6 [M+H]+
[1142] Пример 214. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-((R)-1-(4-метилпиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1143] 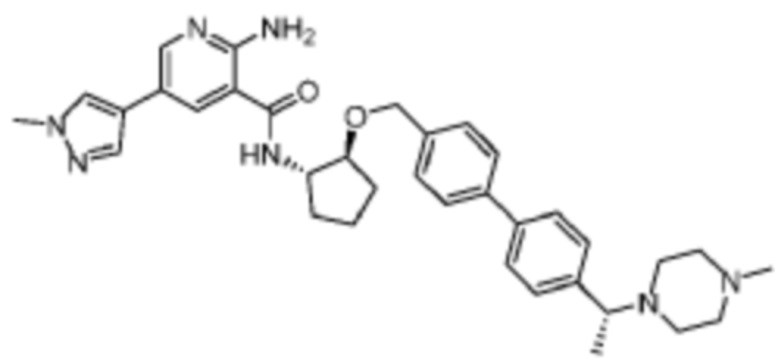
[1144] В соединение 213 (20 мг, 0,03 ммоль) в 0,2 мл 1,2-дихлорэтана добавляли формальдегид (0,005 мл, 0,06 ммоль), а затем NaBH(OAc)3 (13 мг, 0,09 ммоль). Смесь перемешивали при комнатной температуре в течение 1 часа, а затем добавляли воду. Смесь экстрагировали при помощи EtOAc, промывали солевым раствором, сушили над MgSO4 и концентрировали in vacuo. Неочищенный остаток очищали препаративной HPLC с получением 15 мг названого соединения.
[1145] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,64 (dd, J=13,50, 7,04 Гц, 1 H) 1,71 (d, J=7,04 Гц, 3 H) 1,75-1,88 (m, 3 H) 2,00-2,10 (m, 1 H) 2,12-2,23 (m, 1 H) 2,91 (s, 3 H) 3,20-3,28 (m, 2 H) 3,52 (br s, 4 H) 3,90 (s, 3 H) 4,00 (dt, J=6,46, 4,40 Гц, 1 H) 4,32 (q, J=6,65 Гц, 1 H) 4,42 (td, J=7,34, 4,11 Гц, 1 H) 4,63-4,71 (m, 2 H) 7,43 (d, J=8,22 Гц, 2 H) 7,52 (d, J=8,22 Гц, 2 H) 7,56 (d, J=8,22 Гц, 2 H) 7,64 (d, J=8,22 Гц, 2 H) 7,85 (s, 1 H) 7,98 (s, 1 H) 8,20 (d, J=1,76 Гц, 1 H) 8,53 (d, J=2,35 Гц, 1 H);
[1146] MS (ESI, масса/заряд): 594,8 [M+H]+
[1147] Пример 215. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-((S)-1-(4-метилпиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1148] Используя промежуточное соединение 9, названное соединение получали, как описано для примера 214.
[1149] 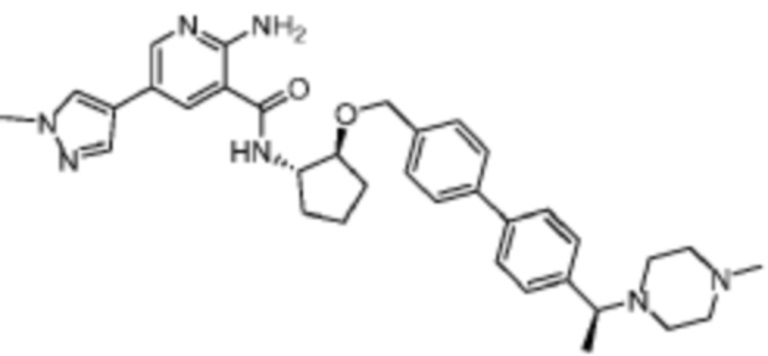
[1150] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,51 (d, J=7,04 Гц, 3 H) 1,64 (br dd, J=13,21, 6,75 Гц, 1 H) 1,76-1,85 (m, 3 H) 2,01-2,06 (m, 1 H) 2,14 (s, 1 H) 2,15-2,20 (m, 1 H) 2,84 (s, 3 H) 3,82 (br d, J=6,46 Гц, 1 H) 3,90 (s, 3 H) 3,98-4,02 (m, 1 H) 4,42 (br dd, J=6,75, 3,23 Гц, 1 H) 4,66 (s, 2 H) 7,42 (dd, J=8,22, 1,76 Гц, 4 H) 7,54-7,59 (m, 4 H) 7,86 (s, 1 H) 7,98 (s, 1 H) 8,20 (d, J=2,35 Гц, 1 H) 8,53 (d, J=1,76 Гц, 1 H);
[1151] MS (ESI, масса/заряд): 594,8 [M+H]+
[1152] Пример 216. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-(1-(4-метилпиперазин-1-ил)циклопропил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1153] Используя промежуточное соединение 11, названное соединение получали, как описано для примера 214.
[1154] 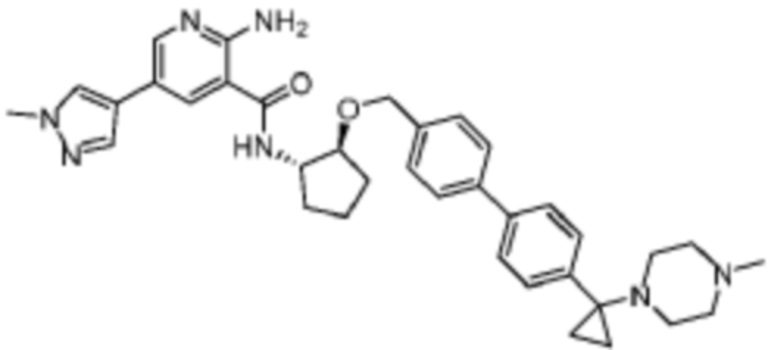
[1155] 1H-ЯМР (600 MГц, CD3OD) δ ppm 0,85-0,88 (m, 1 H) 0,89-0,92 (m, 1 H) 0,99-1,01 (m, 1 H) 1,01-1,04 (m, 1 H) 1,64 (br dd, J=13,50, 6,46 Гц, 1 H) 1,75-1,88 (m, 3 H) 2,01-2,07 (m, 1 H) 2,16-2,24 (m, 2 H) 2,79 (d, J=1,76 Гц, 3 H) 3,00 (br s, 2 H) 3,15-3,21 (m, 2 H) 3,34-3,43 (m, 4 H) 3,90 (s, 3 H) 4,00 (dt, J=6,46, 4,11 Гц, 1 H) 4,42 (td, J=7,34, 4,70 Гц, 1 H) 4,66 (s, 2 H) 7,26 (d, J=8,31 Гц, 2 H) 7,37-7,40 (m, 2 H) 7,40-7,43 (m, 2 H) 7,49-7,52 (m, 1 H) 7,86 (s, 1 H) 7,98 (s, 1 H) 8,20 (d, J=1,76 Гц, 1 H) 8,54 (d, J=2,35 Гц, 1 H);
[1156] MS (ESI, масса/заряд): 606,3 [M+H]+
[1157] Пример 217. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-(2-(4-метилпиперазин-1-ил)пропан-2-ил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1158] Используя промежуточное соединение 12, названное соединение получали, как описано для примера 214.
[1159] 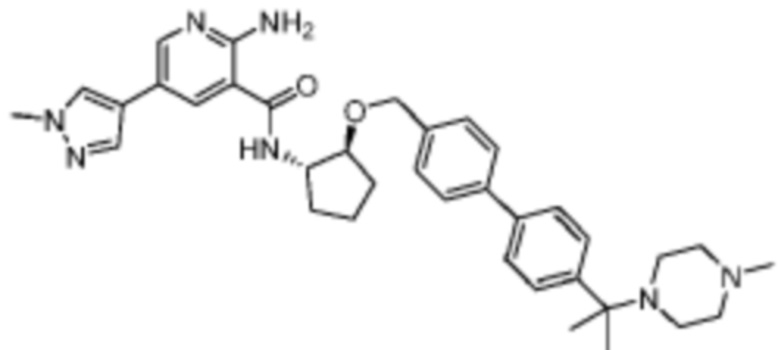
[1160] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,49 (s, 5 H) 1,60-1,61 (m, 1 H) 1,60-1,66 (m, 1 H) 1,80-1,88 (m, 3 H) 2,02-2,08 (m, 1 H) 2,17 (br s, 1 H) 2,87 (s, 3 H) 3,90 (s, 3 H) 4,02 (br s, 1 H) 4,40-4,47 (m, 1 H) 4,67 (s, 2 H) 7,42 (d, J=8,22 Гц, 2 H) 7,51-7,58 (m, 4 H) 7,58-7,62 (m, 2 H) 7,85 (d, J=0,78 Гц, 1 H) 7,98 (s, 1 H) 8,20 (d, J=2,35 Гц, 1 H) 8,51 (d, J=1,96 Гц, 1 H);
[1161] MS (ESI, масса/заряд): 608,2 [M+H]+
[1162] Пример 218. 2-амино-N-((1S,2S)-2-((4'-((R)-1-(4-(2-гидроксиэтил)пиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[1163] Схема получения соединения из примера 218;
[1164] 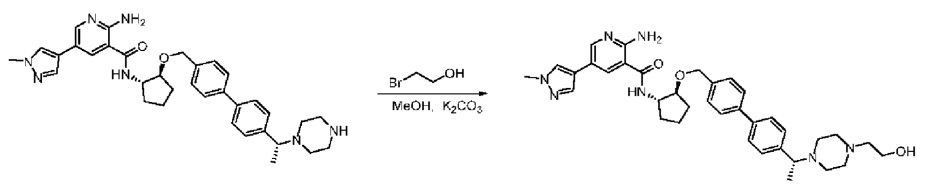
[1165] В смесь соединения 213 (20 мг, 0,03 ммоль) и K2CO3 (14 мг, 0,1 ммоль) в 0,3 мл метанола добавляли 2-бромэтанол (4 мкл, 0,05 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 3 часов, после концентрирования под вакуумом, неочищенный продукт очищали при помощи HPLC с получением 10 мг грязно-белого твердого вещества
[1166] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,60-1,71 (m, 1 H) 1,75 (d, J=7,04 Гц, 3 H) 1,76-1,85 (m, 3 H) 2,00-2,09 (m, 1 H) 2,14-2,23 (m, 1 H) 3,33-3,44 (m, 2 H) 3,56-3,73 (m, 4 H) 3,83-3,87 (m, 2 H) 3,90 (s, 3 H) 4,00 (dt, J=6,60, 4,33 Гц, 1 H) 4,38-4,45 (m, 2 H) 4,64-4,70 (m, 2 H) 7,43 (d, J=8,22 Гц, 2 H) 7,54 (d, J=8,22 Гц, 2 H) 7,56-7,61 (m, 2 H) 7,64-7,71 (m, 2 H) 7,85 (s, 1 H) 7,98 (s, 1 H) 8,20 (d, J=1,76 Гц, 1 H) 8,53 (s, 1 H);
[1167] MS (ESI, масса/заряд): 624,8 [M+H]+
[1168] Пример 219. 2-амино-N-((1S,2S)-2-((4'-((S)-1-(4-(2-гидроксиэтил)пиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[1169] Используя промежуточное соединение 9, названное соединение получали, как описано для примера 213 и 218.
[1170] 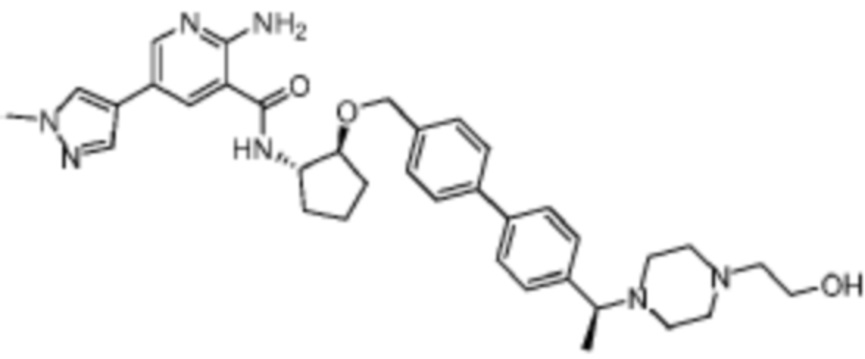
[1171] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,58 (d, J=7,04 Гц, 3 H) 1,64 (br dd, J=13,21, 6,75 Гц, 1 H) 1,72-1,87 (m, 3 H) 2,00-2,07 (m, 1 H) 2,15-2,23 (m, 1 H) 2,99 (br s, 2 H) 3,17-3,22 (m, 3 H) 3,35-3,44 (m, 4 H) 3,80-3,85 (m, 3 H) 3,90 (s, 3 H) 3,96-4,03 (m, 2 H) 4,42 (td, J=7,34, 4,11 Гц, 1 H) 4,66 (s, 2 H) 7,42 (d, J=8,22 Гц, 2 H) 7,46 (d, J=8,22 Гц, 2 H) 7,55-7,57 (m, 2 H) 7,60 (d, J=8,22 Гц, 2 H) 7,86 (s, 1 H) 7,98 (s, 1 H) 8,20 (d, J=2,35 Гц, 1 H) 8,52 (d, J=2,35 Гц, 1 H);
[1172] MS (ESI, масса/заряд): 624,8 [M+H]+
[1173] Пример 220. 2-амино-N-((1S,2S)-2-((4'-(1-(4-(2-гидроксиэтил)пиперазин-1-ил)циклопропил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[1174] Используя промежуточное соединение 11, названное соединение получали, как описано для примера 213 и 218.
[1175] 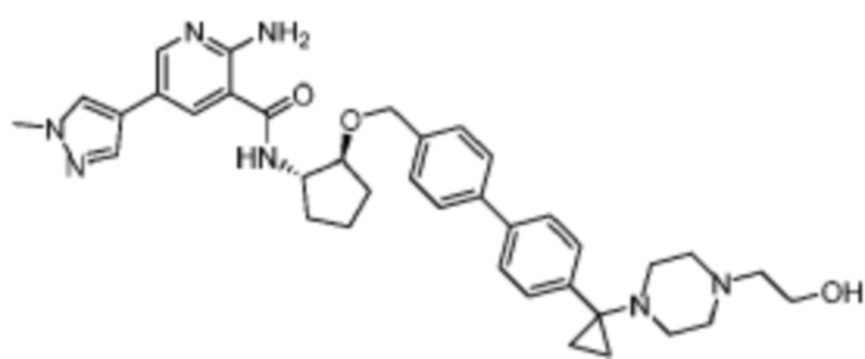
[1176] 1H-ЯМР (600 MГц, CD3OD) δ ppm 0,85-0,88 (m, 1 H) 0,91-0,94 (m, 1 H) 1,00-1,03 (m, 1 H) 1,05-1,07 (m, 1 H) 1,64 (dd, J=13,21, 6,75 Гц, 1 H) 1,74-1,86 (m, 2 H) 1,99-2,07 (m, 1 H) 2,15-2,21 (m, 1 H) 3,13-3,18 (m, 3 H) 3,76-3,81 (m, 2 H) 3,90 (s, 3 H) 3,97-4,04 (m, 1 H) 4,39-4,45 (m, 1 H) 4,61-4,71 (m, 2 H) 7,25-7,28 (m, 1 H) 7,35-7,43 (m, 3 H) 7,49-7,58 (m, 4 H) 7,85 (s, 1 H) 7,98 (s, 1 H) 8,19 (d, J=1,76 Гц, 1 H) 8,53 (d, J=1,76 Гц, 1 H);
[1177] MS (ESI, масса/заряд): 636,5 [M+H]+
[1178] Пример 221. 2-амино-N-((1S,2S)-2-((4'-(2-(4-(2-гидроксиэтил)пиперазин-1-ил)пропан-2-ил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[1179] Используя промежуточное соединение 12, названное соединение получали, как описано для примера 213 и 218.
[1180] 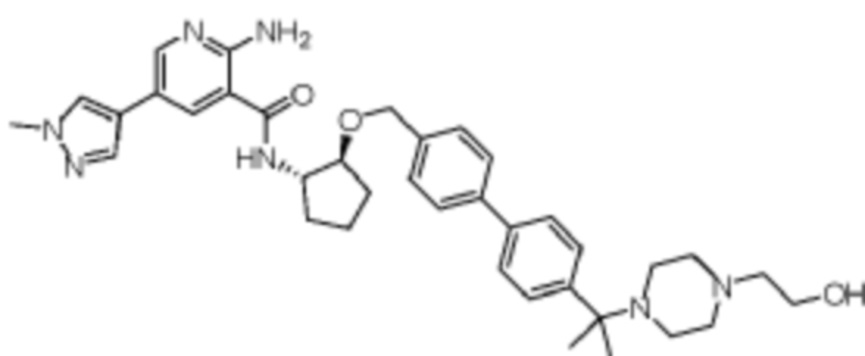
[1181] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,35-1,44 (m, 6 H) 1,60 (br dd, J=12,91, 7,43 Гц, 1 H) 1,73-1,89 (m, 3 H) 2,03 (br dd, J=13,50, 6,46 Гц, 1 H) 2,11-2,21 (m, 1 H) 2,48-2,62 (m, 9 H) 3,67 (t, J=6,06 Гц, 2 H) 3,86 (s, 3 H) 3,96 (dt, J=6,95, 4,55 Гц, 1 H) 4,36-4,46 (m, 1 H) 4,59-4,72 (m, 2 H) 7,40 (d, J=7,83 Гц, 2 H) 7,43-7,49 (m, 2 H) 7,53 (dd, J=12,72, 8,41 Гц, 4 H) 7,75 (s, 1 H) 7,83 (s, 1 H) 7,97 (d, J=2,35 Гц, 1 H) 8,24 (d, J=1,96 Гц, 1 H);
[1182] MS (ESI, масса/заряд): 624,8 [M+H]+
[1183] Пример 222. 6-амино-6'-фтор-N-((1S,2S)-2-((4'-((S)-1-(4-метилпиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-[3,3'-бипиридин]-5-карбоксамид
[1184] Схема получения соединения из примера 222:
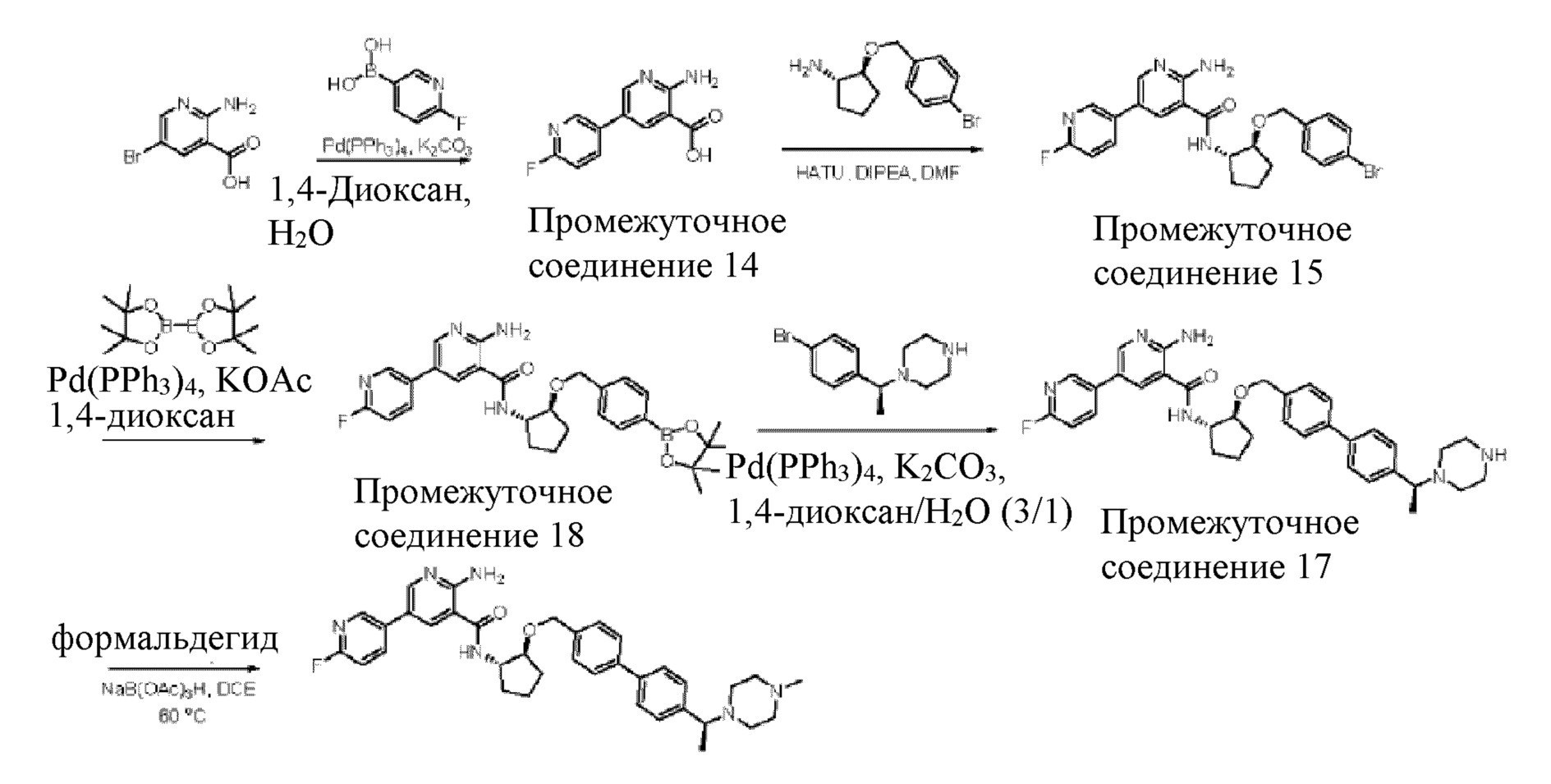
[1185]
[1186] Промежуточное соединение 14.
[1187] Используя 6-фторпиридин-3-бороновую кислоту, названное соединение получали, как описано для промежуточного соединения 2.
[1188] 1H-ЯМР (600 MГц, DMSO-d6) δ ppm 7,20 (dd, J=8,51, 2,64 Гц, 1 H) 8,20 (td, J=8,22, 2,35 Гц, 1 H) 8,27 (d, J=2,93 Гц, 1 H) 8,45 (d, J=2,93 Гц, 1 H) 8,48 (d, J=2,35 Гц, 1 H);
[1189] MS (ESI+) масса/заряд 234,1 [M+H]+
[1190] Промежуточное соединение 15.
[1191] Используя промежуточное соединение 14, названное соединение получали, как описано для промежуточного соединения 4.
[1192] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,60 (br dd, J=13,30, 7,04 Гц, 1 H) 1,71-1,84 (m, 3 H) 2,00 (br dd, J=13,30, 6,26 Гц, 1 H) 2,10-2,21 (m, 1 H) 3,92 (dt, J=6,55, 4,35 Гц, 1 H) 4,39 (td, J=7,34, 4,50 Гц, 1 H) 4,58 (s, 2 H) 7,15 (dd, J=8,41, 2,54 Гц, 1 H) 7,26 (d, J=8,22 Гц, 2 H) 7,38-7,43 (m, 2 H) 8,08 (d, J=2,35 Гц, 1 H) 8,12-8,21 (m, 1 H) 8,35 (d, J=2,35 Гц, 1 H) 8,43 (d, J=2,35 Гц, 1 H);
[1193] MS (ESI+) масса/заряд 485,2/ 487,3 [M+H]+
[1194] Промежуточное соединение 16.
[1195] Используя промежуточное соединение 15, названное соединение получали, как описано для промежуточного соединения 13.
[1196] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,18 (s, 12 H) 1,58 (br dd, J=13,21, 7,34 Гц, 1 H) 1,69-1,84 (m, 3 H) 1,96-2,03 (m, 1 H) 2,15 (br d, J=7,63 Гц, 1 H) 3,93 (br d, J=6,46 Гц, 1 H) 4,39 (br d, J=4,70 Гц, 1 H) 4,63 (s, 2 H) 7,13 (dd, J=8,51, 2,64 Гц, 1 H) 7,32 (d, J=7,63 Гц, 2 H) 7,49-7,57 (m, 1 H) 7,64 (d, J=7,63 Гц, 2 H) 8,07 (d, J=2,35 Гц, 1 H) 8,10-8,18 (m, 1 H) 8,33 (d, J=1,76 Гц, 1 H) 8,41 (d, J=2,35 Гц, 1 H);
[1197] MS (ESI+) масса/заряд 533,3 [M+H]+
[1198] Промежуточное соединение 17.
[1199] Используя промежуточное соединение 16, названное соединение получали, как описано для соединения 213.
[1200] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,61 (d, J=6,65 Гц, 3 H) 1,64 (br s, 1 H) 1,77-1,86 (m, 3 H) 2,02-2,08 (m, 1 H) 2,16-2,22 (m, 1 H) 3,02 (br s, 2 H) 3,13 (br s, 2 H) 3,32-3,40 (m, 4 H) 3,97-4,02 (m, 2 H) 4,05 (br d, J=6,26 Гц, 1 H) 4,41-4,46 (m, 1 H) 4,67 (d, J=3,91 Гц, 2 H) 7,16 (br dd, J=8,41, 2,54 Гц, 1 H) 7,43 (br d, J=8,22 Гц, 2 H) 7,48 (d, J=8,22 Гц, 2 H) 7,55 (d, J=7,83 Гц, 2 H) 7,60 (d, J=7,83 Гц, 2 H) 8,19 (td, J=8,02, 2,74 Гц, 1 H) 8,35 (d, J=2,35 Гц, 1 H) 8,47 (br d, J=2,74 Гц, 1 H) 8,52 (d, J=2,35 Гц, 1 H);
[1201] MS (ESI+) масса/заряд 595,3 [M+H]+
[1202] Пример 222. 6-амино-6'-фтор-N-((1S,2S)-2-((4'-((S)-1-(4-метилпиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-[3,3'-бипиридин]-5-карбоксамид
[1203] Используя промежуточное соединение 17, названное соединение получали, как описано для примера 214.
[1204] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,57 (d, J=6,65 Гц, 3 H) 1,63 (br dd, J=13,50, 6,85 Гц, 1 H) 1,72-1,89 (m, 3 H) 2,00-2,08 (m, 1 H) 2,14-2,23 (m, 1 H) 2,87 (s, 3 H) 3,90-3,97 (m, 1 H) 3,97-4,05 (m, 1 H) 4,40-4,47 (m, 1 H) 4,63-4,71 (m, 2 H) 7,16 (dd, J=8,61, 2,74 Гц, 1 H) 7,32-7,50 (m, 4 H) 7,55 (br d, J=8,22 Гц, 2 H) 7,58 (br d, J=8,22 Гц, 2 H) 8,19 (ddd, J=8,61, 7,43, 2,74 Гц, 1 H) 8,35 (d, J=2,35 Гц, 1 H) 8,48 (d, J=2,74 Гц, 1 H) 8,56 (d, J=2,35 Гц, 1 H);
[1205] MS (ESI+) масса/заряд 609,3 [M+H]+
[1206] Пример 223. 6-амино-6'-фтор-N-((1S,2S)-2-((4'-((R)-1-(4-метилпиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-[3,3'-бипиридин]-5-карбоксамид
[1207] Используя промежуточное соединение 10, названное соединение получали, как описано для примера 222.
[1208] 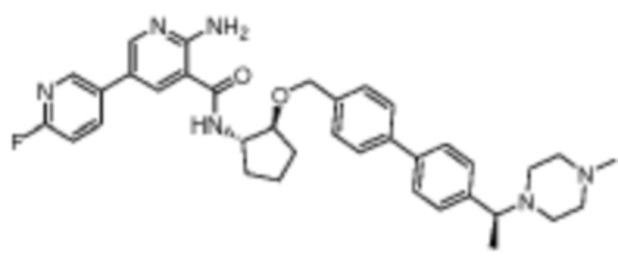
[1209] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,49 (d, J=7,04 Гц, 3 H) 1,63 (br d, J=6,65 Гц, 1 H) 1,84 (br d, J=15,65 Гц, 3 H) 2,06 (br s, 1 H) 2,19 (br d, J=8,61 Гц, 1 H) 2,84 (s, 3 H) 3,74 (br d, J=6,26 Гц, 1 H) 4,00 (br s, 1 H) 4,43 (br s, 1 H) 4,67 (d, J=3,13 Гц, 2 H) 7,15 (br dd, J=9,00, 2,74 Гц, 1 H) 7,42 (dd, J=7,83, 3,52 Гц, 4 H) 7,54 (br dd, J=7,83, 5,09 Гц, 4 H) 8,15-8,22 (m, 1 H) 8,35 (br d, J=2,35 Гц, 1 H) 8,46 (s, 1 H) 8,50 (br d, J=1,96 Гц, 1 H);
[1210] MS (ESI+) масса/заряд 609,4 [M+H]+
[1211] Пример 224. 6-амино-6'-фтор-N-((1S,2S)-2-((4'-(1-(4-метилпиперазин-1-ил)циклопропил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-[3,3'-бипиридин]-5-карбоксамид
[1212] Используя промежуточное соединение 11, названное соединение получали, как описано для примера 222.
[1213] 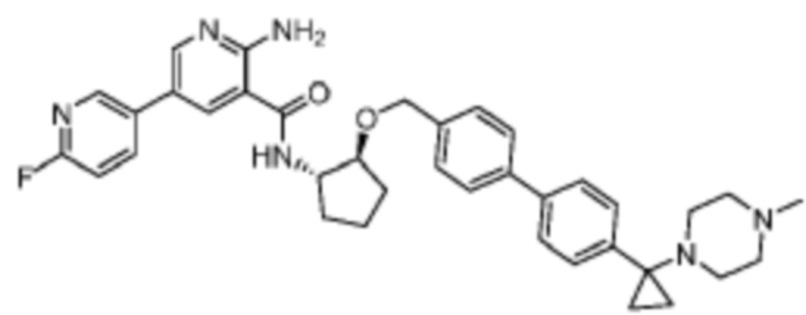
[1214] 1H-ЯМР (400 MГц, CD3OD) δ ppm 0,91-0,95 (m, 2 H) 1,01-1,06 (m, 2 H) 1,64 (br dd, J=13,21, 6,75 Гц, 1 H) 1,76-1,85 (m, 3 H) 2,01-2,06 (m, 1 H) 2,14 (s, 1 H) 2,15-2,20 (m, 1 H) 2,80 (s, 3 H) 3,34 (s, 2 H) 3,99 (br d, J=4,30 Гц, 1 H) 4,43 (br d, J=4,70 Гц, 1 H) 4,67 (d, J=3,52 Гц, 2 H) 7,12-7,16 (m, 1 H) 7,40 (dd, J=14,28, 8,41 Гц, 4 H) 7,52 (br dd, J=8,22, 3,91 Гц, 4 H) 8,18 (s, 1 H) 8,35 (d, J=2,35 Гц, 1 H) 8,42 (d, J=2,35 Гц, 1 H) 8,45 (s, 1 H);
[1215] MS (ESI+) масса/заряд 621,5 [M+H]+
[1216] Пример 225. 6-амино-6'-фтор-N-((1S,2S)-2-((4'-(2-(4-метилпиперазин-1-ил)пропан-2-ил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-[3,3'-бипиридин]-5-карбоксамид
[1217] Используя промежуточное соединение 12, названное соединение получали, как описано для примера 222.
[1218] 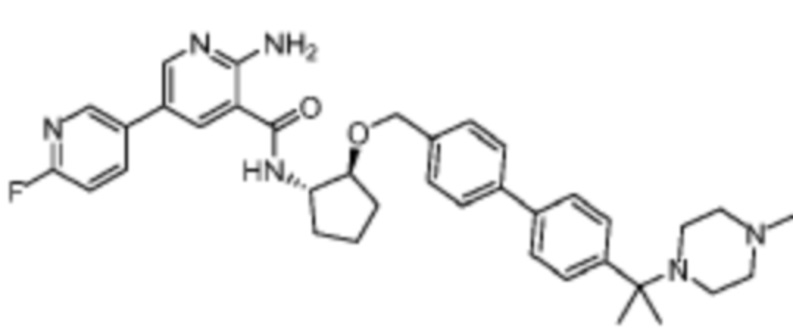
[1219] MS (ESI+) масса/заряд 623,3 [M+H]+
[1220] Пример 226. 6-амино-6'-фтор-N-((1S,2S)-2-((4'-((S)-1-(4-(2-гидроксиэтил)пиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-[3,3'-бипиридин]-5-карбоксамид
[1221] Схема получения соединения из примера 226:
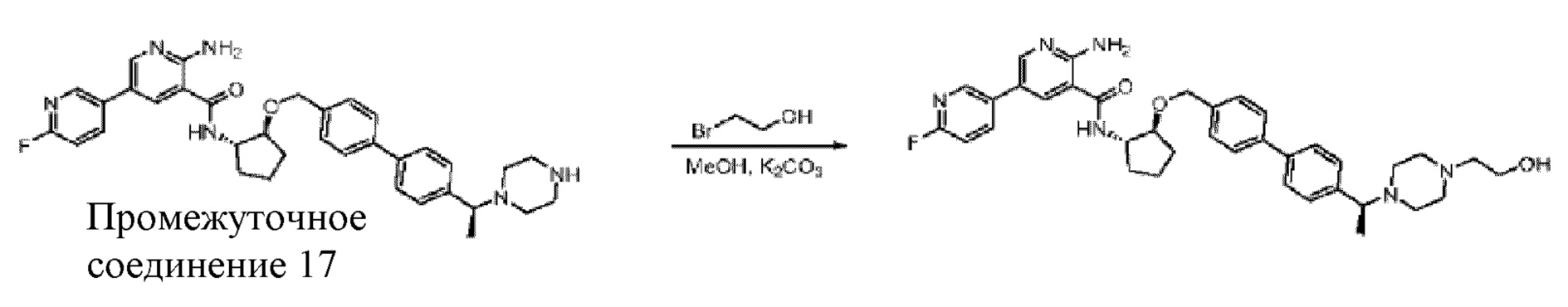
[1222]
[1223] Используя промежуточное соединение 17, названное соединение получали, как описано для примера 218.
[1224] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,58-1,68 (m, 4 H) 1,77-1,87 (m, 3 H) 2,02-2,09 (m, 1 H) 2,15-2,23 (m, 1 H) 3,13 (br s, 2 H) 3,17-3,26 (m, 2 H) 3,46 (br s, 4 H) 3,77 (br s, 1 H) 3,82-3,87 (m, 2 H) 4,02 (br d, J=4,70 Гц, 2 H) 4,11 (br d, J=6,26 Гц, 1 H) 4,44 (br dd, J=11,74, 7,43 Гц, 1 H) 4,67 (d, J=2,74 Гц, 2 H) 7,17 (dd, J=8,61, 2,74 Гц, 1 H) 7,43 (d, J=8,22 Гц, 2 H) 7,49 (d, J=8,22 Гц, 2 H) 7,56 (d, J=8,22 Гц, 2 H) 7,62 (d, J=8,61 Гц, 2 H) 8,20 (td, J=8,02, 2,74 Гц, 1 H) 8,36 (d, J=2,35 Гц, 1 H) 8,48 (br d, J=2,74 Гц, 1 H) 8,57 (d, J=1,96 Гц, 1 H);
[1225] MS (ESI+) масса/заряд 639,4 [M+H]+
[1226] Пример 227. 6-амино-6'-фтор-N-((1S,2S)-2-((4'-((R)-1-(4-(2-гидроксиэтил)пиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-[3,3'-бипиридин]-5-карбоксамид
[1227] Используя промежуточное соединение 10, названное соединение получали, как описано для примера 226.
[1228] 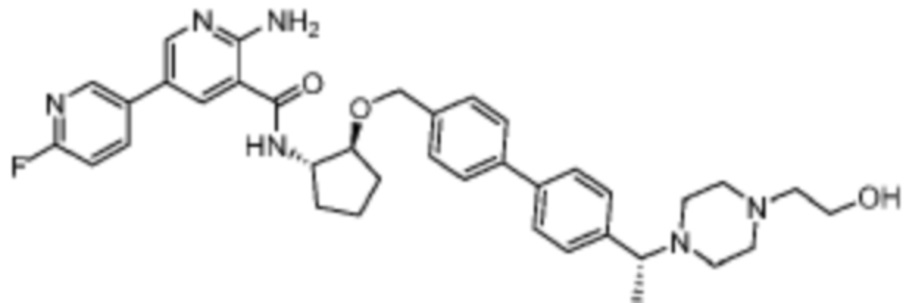
[1229] MS (ESI+) масса/заряд 639,1 [M+H]+
[1230] Пример 228. 6-амино-6'-фтор-N-((1S,2S)-2-((4'-(1-(4-(2-гидроксиэтил)пиперазин-1-ил)циклопропил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-[3,3'-бипиридин]-5-карбоксамид
[1231] Используя промежуточное соединение 11, названное соединение получали, как описано для примера 226.
[1232] 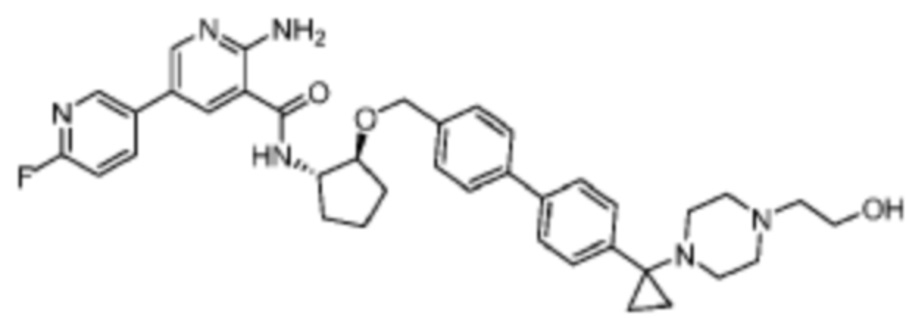
[1233] MS (ESI+) масса/заряд 651,6 [M+H]+
[1234] Пример 229. 6-амино-6'-фтор-N-((1S,2S)-2-((4'-(2-(4-(2-гидроксиэтил)пиперазин-1-ил)пропан-2-ил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-[3,3'-бипиридин]-5-карбоксамид
[1235] Используя промежуточное соединение 12, названное соединение получали, как описано для примера 226.
[1236] 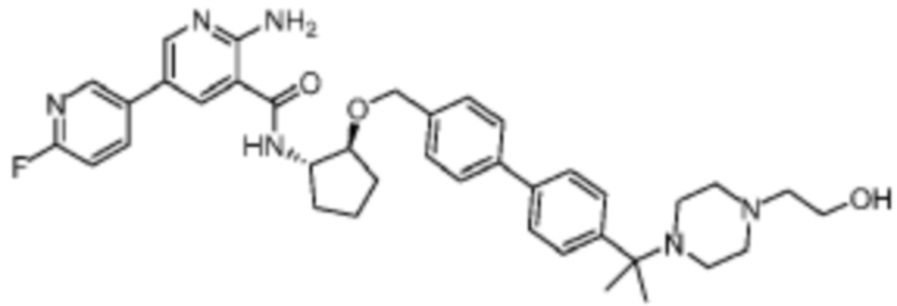
[1237] MS (ESI+) масса/заряд 653,4 [M+H]+
[1238] Пример 230. 6-амино-5'-фтор-N-((1S,2S)-2-((4'-(1-(4-метилпиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-[3,3'-бипиридин]-5-карбоксамид
[1239] Схема получения соединения из примера 230:
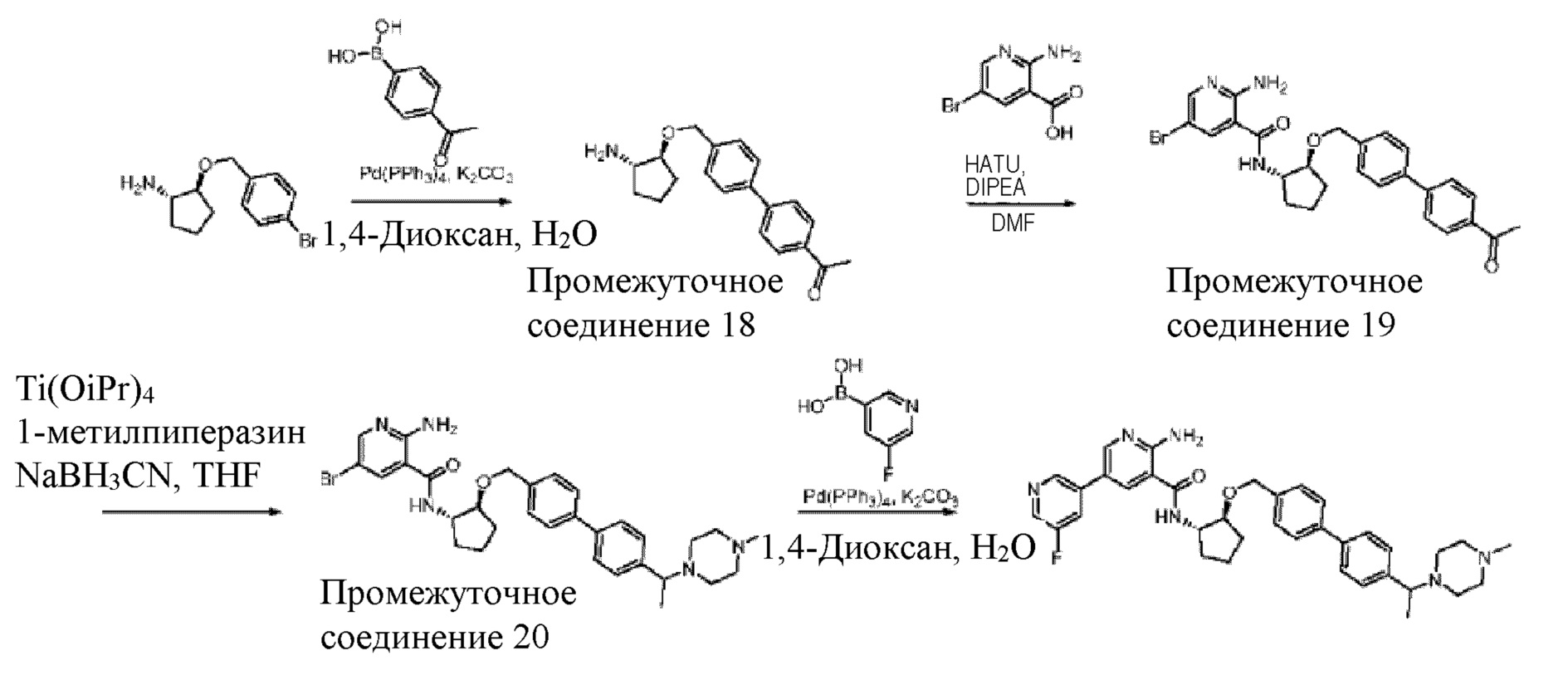
[1240]
[1241] Промежуточное соединение 18.
[1242] Используя (1S,2S)-2-((4-бромбензил)окси)циклопентан-1-амин, названное соединение получали, как описано для промежуточного соединения 7.
[1243] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,58-1,65 (m, 1 H) 1,74-1,85 (m, 3 H) 2,01-2,08 (m, 1 H) 2,12-2,18 (m, 1 H) 2,60 (s, 3 H) 3,41-3,48 (m, 1 H) 3,92 (q, J=5,87 Гц, 1 H) 4,45-4,55 (m, 2 H) 7,27 (d, J=8,22 Гц, 2 H) 7,43-7,50 (m, 3 H) 7,65 (d, J=8,22 Гц, 1 H) 7,73 (d, J=8,22 Гц, 1 H) 8,03 (d, J=8,22 Гц, 1 H);
[1244] MS (ESI+) масса/заряд 310,1 [M+H]+
[1245] Промежуточное соединение 19.
[1246] Используя промежуточное соединение 18, названное соединение получали, как описано для промежуточного соединения 4.
[1247] 1H-ЯМР (600 MГц, CDCl3) δ ppm 1,45-1,54 (m, 1 H) 1,71-1,82 (m, 2 H) 1,84-1,92 (m, 1 H) 1,92-2,02 (m, 1 H) 2,23-2,33 (m, 1 H) 2,63 (s, 3 H) 3,81-3,91 (m, 1 H) 4,29-4,44 (m, 1 H) 4,63-4,75 (m, 2 H) 5,90 (br d, J=6,46 Гц, 1 H) 6,35 (br s, 2 H) 7,44 (d, J=8,22 Гц, 2 H) 7,56-7,62 (m, 3 H) 7,66 (d, J=8,22 Гц, 2 H) 8,01 (d, J=8,22 Гц, 2 H) 8,15 (d, J=1,76 Гц, 1 H);
[1248] MS (ESI+) масса/заряд 508,1/510,2 [M+H]+
[1249] Промежуточное соединение 20.
[1250] В промежуточное соединение 19 (300 мг, 0,59 ммоль) в 3 мл THF добавляли 1-метилпиперазин (0,13 мл, 1,18 ммоль), а затем Ti(OiPr)4 (0,7 мл, 2,36 ммоль). Смесь перемешивали при 60°C в течение 4 ч., а затем добавляли NaBH3CN (0,11 г, 1,18 ммоль). Смесь перемешивали в течение 1 часа и экстрагировали при помощи EtOAc, промывали солевым раствором, сушили над MgSO4. После концентрирования под вакуумом неочищенный продукт очищали колоночной хроматографией на силикагеле с получением 200 мг грязно-белого твердого вещества
[1251] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,55-1,61 (m, 1 H) 1,64 (d, J=7,04 Гц, 3 H) 1,72-1,84 (m, 3 H) 1,97-2,05 (m, 1 H) 2,09-2,17 (m, 1 H) 2,88 (s, 3 H) 3,11 (br s, 2 H) 3,36-3,49 (m, 4 H) 3,95 (dt, J=6,75, 4,26 Гц, 1 H) 4,14 (br d, J=6,46 Гц, 1 H) 4,35 (td, J=7,34, 4,70 Гц, 1 H) 4,61-4,68 (m, 2 H) 7,42 (d, J=8,22 Гц, 2 H) 7,50 (d, J=8,22 Гц, 2 H) 7,57 (d, J=8,22 Гц, 2 H) 7,65 (d, J=8,22 Гц, 2 H) 8,13 (d, J=2,35 Гц, 1 H) 8,20 (d, J=2,35 Гц, 1 H);
[1252] MS (ESI+) масса/заряд 592,2/594,3 [M+H]+
[1253] Пример 230. 6-амино-5'-фтор-N-((1S,2S)-2-((4'-(1-(4-метилпиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-[3,3'-бипиридин]-5-карбоксамид
[1254] Используя промежуточное соединение 20 и 5-фторпиридин-3-бороновую кислоту, названное соединение получали, как описано для промежуточного соединения 14.
[1255] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,54 (d, J=7,04 Гц, 3 H) 1,63 (br dd, J=13,21, 6,75 Гц, 1 H) 1,77-1,86 (m, 3 H) 2,04 (br dd, J=12,91, 7,04 Гц, 1 H) 2,16-2,23 (m, 1 H) 2,85 (s, 3 H) 3,88 (br d, J=7,04 Гц, 1 H) 3,97-4,03 (m, 1 H) 4,43 (br d, J=4,70 Гц, 1 H) 4,64-4,70 (m, 2 H) 7,42 (br dd, J=8,22, 4,11 Гц, 4 H) 7,53 (br d, J=8,22 Гц, 2 H) 7,56 (br d, J=8,22 Гц, 2 H) 7,96 (br d, J=9,39 Гц, 1 H) 8,42 (s, 1 H) 8,50 (d, J=2,35 Гц, 1 H) 8,56 (s, 1 H) 8,70 (br s, 1 H);
[1256] MS (ESI+) масса/заряд 609,3 [M+H]+
[1257] Пример 231. 2-амино-5-хлор-N-((1S,2S)-2-((4'-(1-(4-метилпиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1258] Используя 2-амино-5-хлорникотиновую кислоту, названное соединение получали, как описано для синтеза промежуточного соединения 20.
[1259] 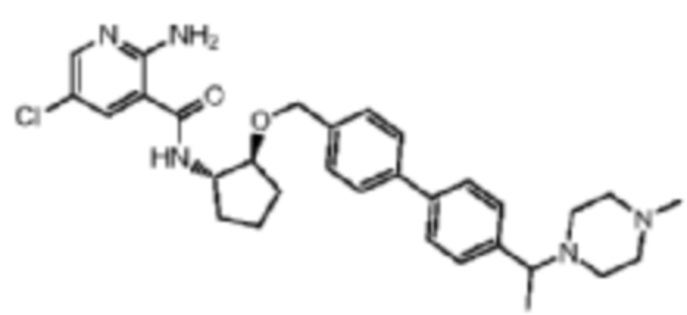
[1260] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,60 (dt, J=13,60, 7,09 Гц, 1 H) 1,66 (d, J=6,65 Гц, 3 H) 1,73-1,87 (m, 3 H) 1,98-2,06 (m, 1 H) 2,10-2,20 (m, 1 H) 2,90 (s, 2 H) 3,15 (br s, 2 H) 3,45 (br s, 4 H) 3,96 (dt, J=6,65, 4,30 Гц, 1 H) 4,18 (q, J=6,65 Гц, 1 H) 4,37 (td, J=7,24, 4,30 Гц, 1 H) 4,61-4,71 (m, 2 H) 7,43 (m, J=8,22 Гц, 2 H) 7,52 (d, J=8,22 Гц, 2 H) 7,59 (d, J=8,22 Гц, 2 H) 7,67 (m, J=8,22 Гц, 2 H) 8,09 (d, J=2,74 Гц, 1 H) 8,14 (d, J=2,74 Гц, 1 H);
[1261] MS (ESI+) масса/заряд 548,3 [M+H]+
[1262] Пример 232. 2-амино-5-фтор-N-((1S,2S)-2-((4'-(1-(4-метилпиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1263] Используя 2-амино-5-фторникотиновую кислоту, названное соединение получали, как описано для синтеза промежуточного соединения 20.
[1264] 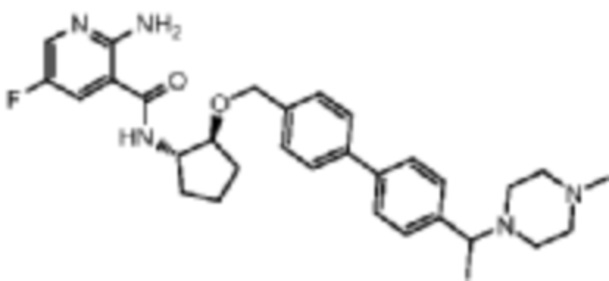
[1265] MS (ESI, масса/заряд): 532,3 [M+H]+
[1266] Пример 233. 2-амино-5-циано-N-((1S,2S)-2-((4'-(1-(4-метилпиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1267] Используя 2-амино-5-цианоникотиновую кислоту, названное соединение получали, как описано для синтеза промежуточного соединения 20.
[1268] 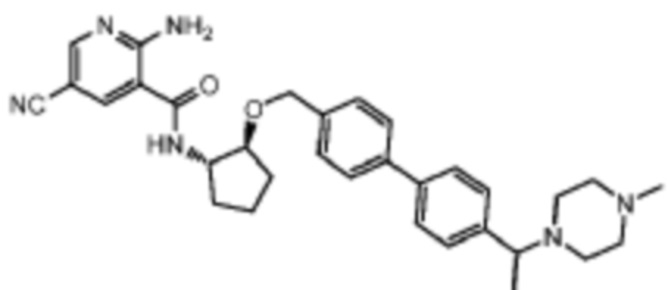
[1269] MS (ESI, масса/заряд): 539,3 [M+H]+
[1270] Пример 234. 2-амино-6-хлор-N-((1S,2S)-2-((4'-(1-(4-метилпиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1271] Используя 2-амино-6-хлорникотиновую кислоту, названное соединение получали, как описано для синтеза промежуточного соединения 20.
[1272] 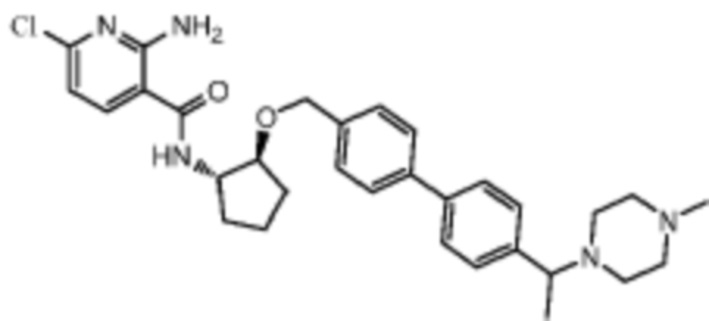
[1273] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,56 (br dd, J=13,11, 7,24 Гц, 1 H) 1,66 (d, J=7,04 Гц, 3 H) 1,70-1,85 (m, 3 H) 2,01 (br dd, J=13,11, 6,46 Гц, 1 H) 2,07-2,19 (m, 2 H) 2,90 (s, 3 H) 3,09-3,21 (m, 2 H) 3,39-3,58 (m, 4 H) 3,87-3,96 (m, 1 H) 4,19 (br d, J=6,65 Гц, 1 H) 4,35 (br d, J=4,70 Гц, 1 H) 4,57-4,73 (m, 2 H) 6,56 (d, J=7,83 Гц, 1 H) 7,42 (m, J=8,22 Гц, 2 H) 7,52 (d, J=8,22 Гц, 2 H) 7,56 (d, J=8,22 Гц, 2 H) 7,66 (m, J=8,22 Гц, 2 H) 7,73 (d, J=8,22 Гц, 1 H) ;
[1274] MS (ESI, масса/заряд): 548,3 [M+H]+
[1275] Пример 235. 2-амино-N-((1S,2S)-2-((4'-(1-(4-метилпиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1276] Используя 2-аминоникотиновую кислоту, названное соединение получали, как описано для синтеза промежуточного соединения 20.
[1277] 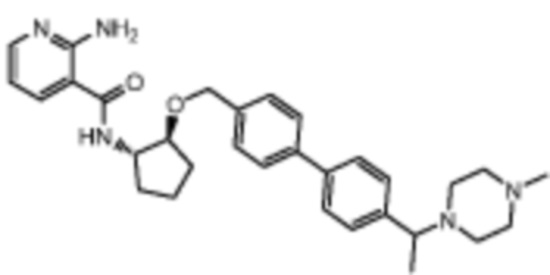
[1278] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,58-1,64 (m, 1 H) 1,66 (d, J=7,04 Гц, 3 H) 1,74-1,85 (m, 3 H) 1,97-2,05 (m, 1 H) 2,13-2,20 (m, 1 H) 2,89 (s, 3 H) 3,02-3,27 (m, 4 H) 3,46 (br s, 4 H) 3,93-4,00 (m, 1 H) 4,20 (q, J=6,46 Гц, 1 H) 4,35-4,42 (m, 1 H) 4,65 (s, 2 H) 6,95 (t, J=6,75 Гц, 1 H) 7,43 (d, J=8,22 Гц, 2 H) 7,52 (m, J=8,22 Гц, 2 H) 7,58 (m, J=8,22 Гц, 2 H) 7,67 (d, J=8,22 Гц, 2 H) 7,99 (dd, J=6,46, 1,17 Гц, 1 H) 8,33 (dd, J=7,34, 1,47 Гц, 1 H) ;
[1279] MS (ESI, масса/заряд): 514,3 [M+H]+
[1280] Пример 236. 6-амино-5'-фтор-N-((1S,2S)-2-((4'-(1-(4-(2-гидроксиэтил)пиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-[3,3'-бипиридин]-5-карбоксамид
[1281] Схема получения соединения из примера 236:
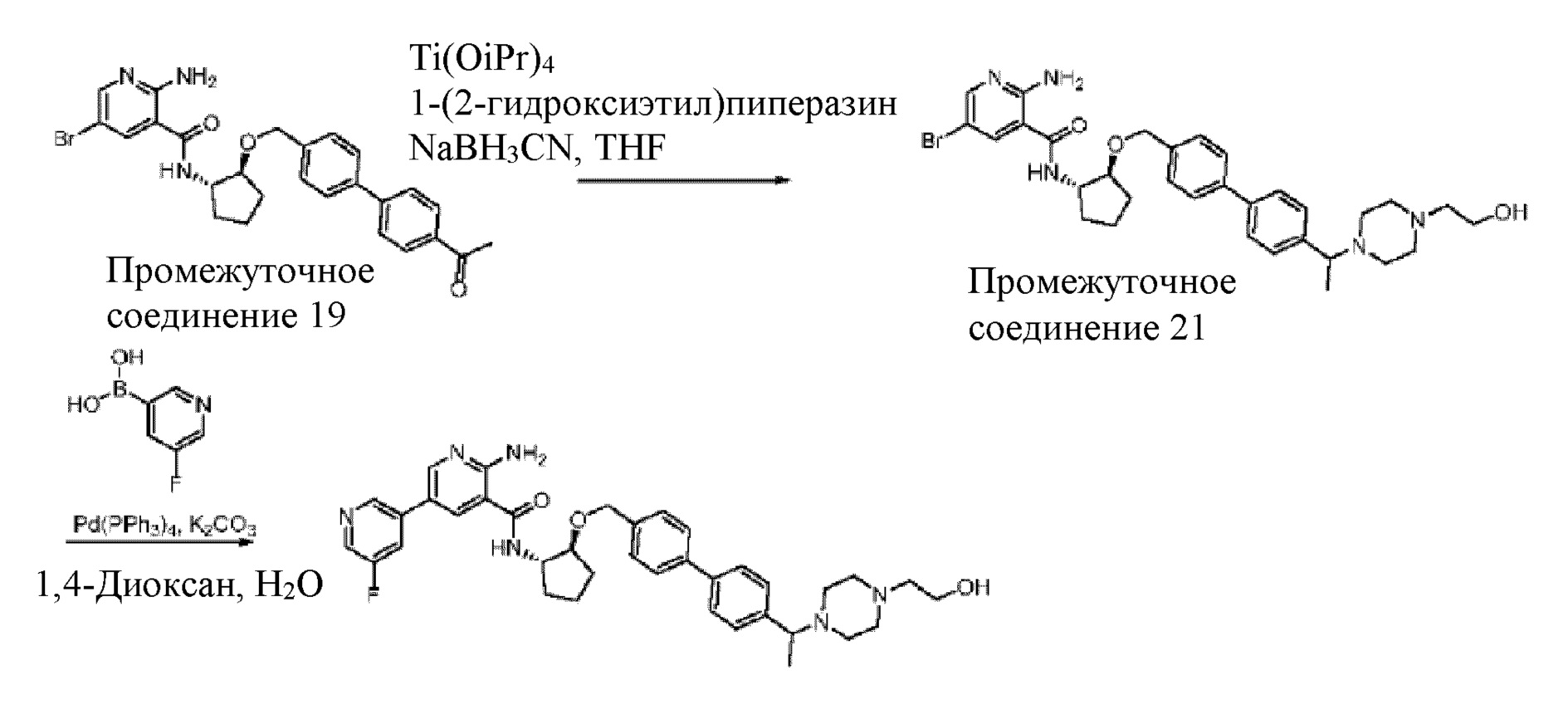
[1282]
[1283] Промежуточное соединение 21. Используя 1-(2-гидроксиэтил)пиперазин, названное соединение получали, как описано для промежуточного соединения 20.
[1284] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,42 (d, J=6,46 Гц, 2 H) 1,51-1,58 (m, 1 H) 1,71-1,81 (m, 3 H) 1,97-2,04 (m, 1 H) 2,08-2,15 (m, 1 H) 2,61 (br s, 2 H) 3,47 (br d, J=5,28 Гц, 1 H) 3,67 (t, J=5,87 Гц, 2 H) 3,91 (dt, J=6,46, 4,70 Гц, 1 H) 4,35 (td, J=7,34, 4,70 Гц, 1 H) 4,59-4,67 (m, 2 H) 7,37 (br d, J=8,22 Гц, 2 H) 7,39 (br d, J=8,22 Гц, 2 H) 7,54 (d, J=7,63 Гц, 4 H) 7,90 (d, J=2,35 Гц, 1 H) 8,05 (d, J=2,35 Гц, 1 H);
[1285] MS (ESI+) масса/заряд 622,2/624,2 [M+H]+
[1286] Пример 236. 6-амино-5'-фтор-N-((1S,2S)-2-((4'-(1-(4-(2-гидроксиэтил)пиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-[3,3'-бипиридин]-5-карбоксамид
[1287] Используя промежуточное соединение 21, названное соединение получали, как описано для примера 230.
[1288] 1H-ЯМР (400 МГц, CD3OD) δ ppm 1,63 (br dd, J=13,89, 6,85 Гц, 1 H) 1,72 (br d, J=6,65 Гц, 3 H) 1,76-1,87 (m, 3 H) 2,04 (br dd, J=12,72, 6,46 Гц, 1 H) 2,13-2,23 (m, 1 H) 3,52-3,68 (m, 4 H) 3,84 (br t, J=4,89 Гц, 2 H) 4,00 (br d, J=3,91 Гц, 1 H) 4,35 (br d, J=6,65 Гц, 1 H) 4,39-4,49 (m, 2 H) 4,61-4,73 (m, 2 H) 7,43 (br d, J=7,83 Гц, 2 H) 7,53 (br t, J=9,39 Гц, 4 H) 7,63 (br d, J=8,22 Гц, 2 H) 7,98 (br d, J=9,78 Гц, 1 H) 8,43 (s, 1 H) 8,52 (s, 1 H) 8,61 (s, 1 H) 8,71 (s, 1 H);
[1289] MS (ESI+) масса/заряд 639,3 [M+H]+
[1290] Пример 237. 6-амино-6'-фтор-N-((1S,2S)-2-((4'-(1-(4-(2-гидроксиэтил)пиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-[3,3'-бипиридин]-5-карбоксамид
[1291] Используя 6-фторпиридин-3-бороновую кислоту, названное соединение получали, как описано для примера 236.
[1292] 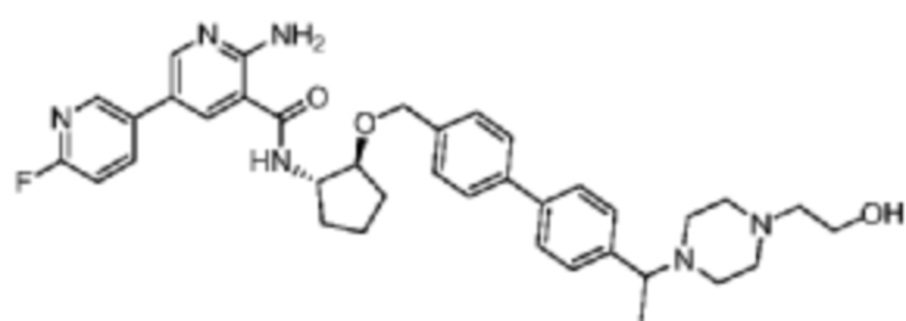
[1293] 1H-ЯМР (400 МГц, CD3OD) δ ppm 1,62 (br dd, J=13,30, 6,65 Гц, 1 H) 1,68 (br d, J=7,04 Гц, 3 H) 1,81 (br d, J=7,43 Гц, 3 H) 1,98-2,08 (m, 1 H) 2,12-2,23 (m, 1 H) 3,17-3,28 (m, 4 H) 3,53 (br s, 4 H) 3,84 (br d, J=4,30 Гц, 2 H) 3,99 (br s, 1 H) 4,25 (br d, J=7,04 Гц, 1 H) 4,42 (br d, J=4,70 Гц, 1 H) 4,62-4,72 (m, 2 H) 7,16 (br d, J=7,83 Гц, 1 H) 7,42 (br d, J=7,83 Гц, 2 H) 7,47-7,59 (m, 4 H) 7,62 (br d, J=7,83 Гц, 2 H) 8,19 (br t, J=8,02 Гц, 1 H) 8,34 (s, 1 H) 8,47 (br s, 1 H) 8,56 (s, 1 H);
[1294] MS (ESI+) масса/заряд 639,3 [M+H]+
[1295] Пример 238. 6-амино-2'-фтор-N-((1S,2S)-2-((4'-(1-(4-(2-гидроксиэтил)пиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-[3,3'-бипиридин]-5-карбоксамид
[1296] Используя 2-фторпиридин-3-бороновую кислоту, названное соединение получали, как описано для примера 236.
[1297] 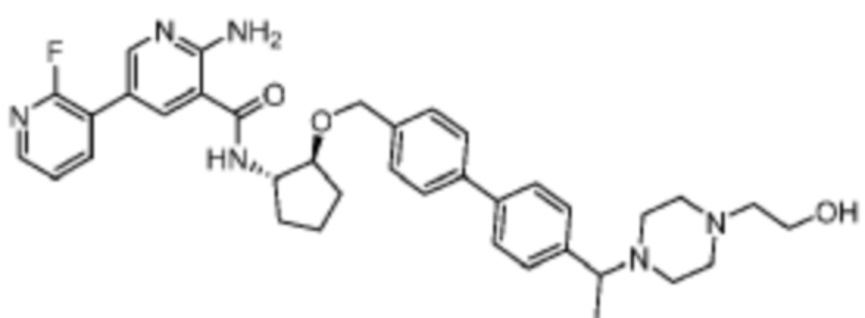
[1298] MS (ESI+) масса/заряд 639,3 [M+H]+
[1299] Пример 239. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-((1-метилпиперидин-4-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1300] Схема получения соединения из примера 239:
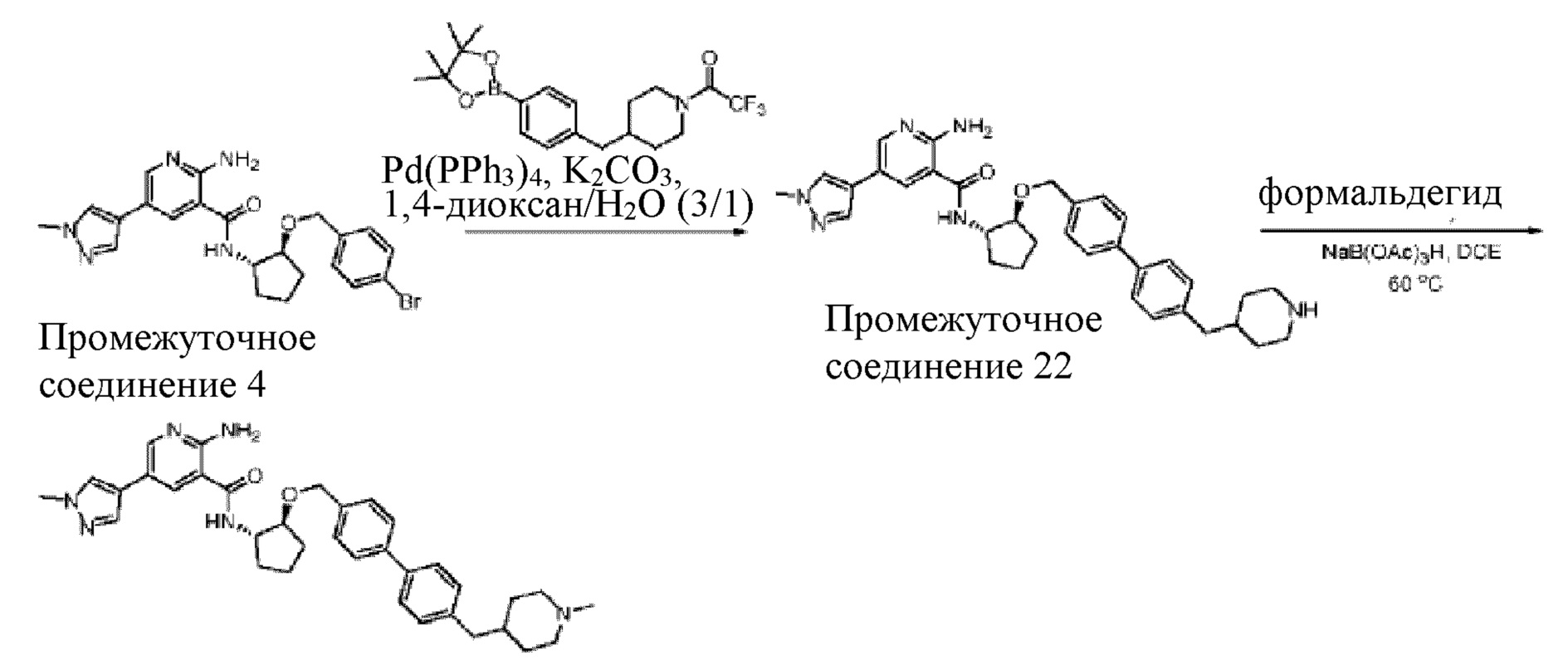
[1301]
[1302] Промежуточное соединение 22.
[1303] Используя пинаколиновый сложный эфи 4-(4-(1-трифторацетилпиперидинo)метил)фенилбороновой кислоты, названное соединение получали, как описано для примера 134.
[1304] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,39-1,48 (m, 2 H) 1,63 (br dd, J=13,50, 7,04 Гц, 1 H) 1,76-1,86 (m, 4 H) 1,86-1,95 (m, 3 H) 2,04 (br dd, J=13,21, 6,75 Гц, 1 H) 2,18 (br dd, J=13,50, 5,87 Гц, 1 H) 2,64 (br d, J=6,46 Гц, 2 H) 2,90-2,98 (m, 2 H) 3,33 (s, 3 H) 3,36 (br d, J=12,33 Гц, 3 H) 3,89 (s, 3 H) 3,97-4,03 (m, 1 H) 4,37-4,45 (m, 1 H) 4,63-4,70 (m, 2 H) 7,23 (br d, J=8,22 Гц, 2 H) 7,40 (d, J=8,22 Гц, 2 H) 7,48 (d, J=8,22 Гц, 2 H) 7,52 (d, J=8,22 Гц, 2 H) 7,85 (s, 1 H) 7,97 (s, 1 H) 8,19 (d, J=1,76 Гц, 1 H) 8,51 (d, J=2,35 Гц, 1 H);
[1305] MS (ESI, масса/заряд): 564,8 [M+H]+
[1306] Пример 239. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-((1-метилпиперидин-4-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1307] Используя промежуточное соединение 22 и формальдегид, названное соединение получали, как описано для примера 214.
[1308] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,42-1,54 (m, 2 H) 1,63 (br dd, J=13,50, 7,04 Гц, 1 H) 1,75-1,88 (m, 4 H) 1,92 (br d, J=14,67 Гц, 2 H) 2,00-2,08 (m, 1 H) 2,17 (br dd, J=13,50, 5,87 Гц, 1 H) 2,64 (br d, J=7,04 Гц, 2 H) 2,82 (s, 3 H) 2,89-2,98 (m, 2 H) 3,47 (br d, J=12,33 Гц, 2 H) 3,89 (s, 3 H) 3,94-4,05 (m, 1 H) 4,36-4,46 (m, 1 H) 4,61-4,69 (m, 2 H) 7,22 (d, J=8,22 Гц, 2 H) 7,39 (br d, J=8,22 Гц, 2 H) 7,47 (br d, J=8,22 Гц, 2 H) 7,51 (br d, J=8,22 Гц, 2 H) 7,84 (s, 1 H) 7,96 (s, 1 H) 8,18 (d, J=1,76 Гц, 1 H) 8,49 (d, J=2,35 Гц, 1 H);
[1309] MS (ESI, масса/заряд): 579,8 [M+H]+
[1310] Пример 240. 2-амино-N-((1S,2S)-2-((4'-((1-(2-гидроксиэтил)пиперидин-4-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[1311] Схема получения соединения из примера 240:
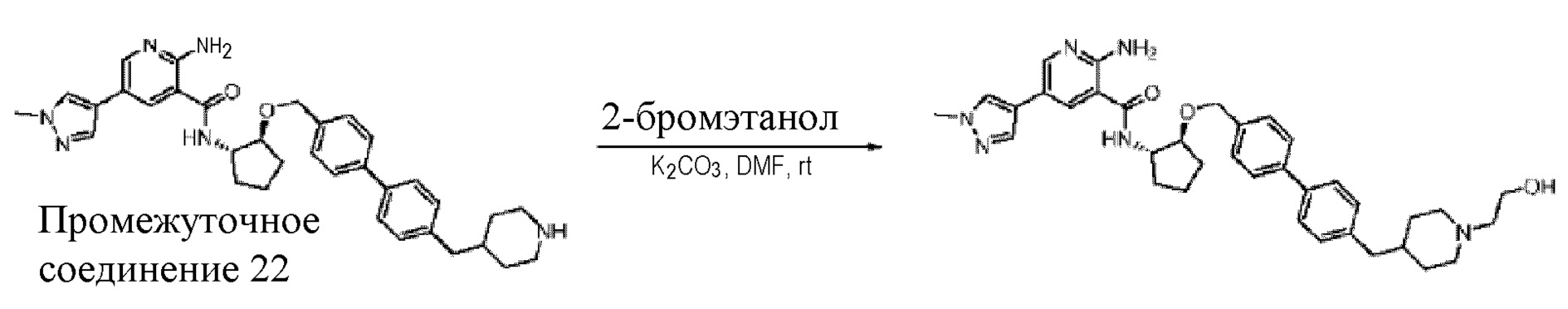
[1312]
[1313] В смесь промежуточного соединения 22 (30 мг, 0,05 ммоль) и K2CO3 (22 мг, 0,16 ммоль) в 0,4 мл DMF добавляли 2-бромэтанол (6 мкл, 0,08 ммоль). Смесь перемешивали при комнатной температуре в течение 4 часов, а затем добавляли воду. Смесь экстрагировали при помощи EtOAc, промывали солевым раствором, сушили над MgSO4. После концентрирования под вакуумом неочищенный остаток очищали препаративной HPLC с получением 27 мг названого соединения.
[1314] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,26 (br d, J=13,50 Гц, 2 H) 1,56-1,74 (m, 4 H) 1,74-1,89 (m, 4 H) 2,04 (br dd, J=13,21, 6,16 Гц, 1 H) 2,20 (br dd, J=13,50, 7,04 Гц, 1 H) 2,64 (br d, J=7,04 Гц, 2 H) 2,77 (br t, J=12,62 Гц, 2 H) 3,05-3,13 (m, 2 H) 3,47 (br d, J=12,33 Гц, 2 H) 3,75-3,81 (m, 2 H) 3,92 (s, 3 H) 4,01-4,07 (m, 1 H) 4,40-4,47 (m, 1 H) 4,62-4,72 (m, 2 H) 7,10 (br d, J=7,63 Гц, 1 H) 7,20-7,26 (m, 3 H) 7,27-7,33 (m, 2 H) 7,41 (br d, J=7,63 Гц, 2 H) 7,87-7,90 (m, 1 H) 7,88 (s, 1 H) 8,03 (s, 1 H) 8,23 (d, J=1,76 Гц, 1 H) 8,60 (br s, 1 H);
[1315] MS (ESI, масса/заряд): 609,8 [M+H]+
[1316] Пример 241. метил-2-(4-((4'-((((1S,2S)-2-(2-амино-5-(1-метил-1H-пиразол-4-ил)никотинамидо)циклопентил)окси)метил)-[1,1'-бифенил]-4-ил)метил)пиперидин-1-ил)ацетат
[1317] Используя промежуточное соединение 22 и метилбромацетат, названное соединение получали, как описано для примера 240.
[1318] 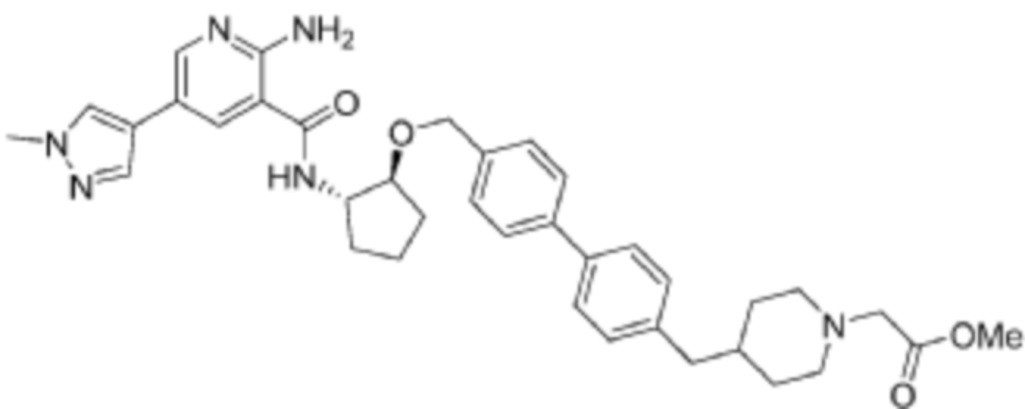
[1319] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,32 (br s, 2 H) 1,61-1,71 (m, 4 H) 1,79-1,89 (m, 4 H) 2,01-2,06 (m, 1 H) 2,20 (br dd, J=13,79, 6,75 Гц, 1 H) 2,66 (br s, 2 H) 2,85 (br s, 2 H) 3,49 (br s, 2 H) 3,79 (s, 3 H) 3,92 (s, 3 H) 4,01 (br s, 2 H) 4,02-4,06 (m, 1 H) 4,44 (br dd, J=11,15, 7,04 Гц, 1 H) 4,63-4,73 (m, 2 H) 7,11 (br d, J=7,63 Гц, 1 H) 7,23-7,30 (m, 4 H) 7,41 (br d, J=8,22 Гц, 2 H) 7,88 (s, 1 H) 8,02-8,04 (m, 1 H) 8,23 (d, J=1,76 Гц, 1 H) 8,60 (s, 1 H);
[1320] MS (ESI, масса/заряд): 637,7 [M+H]+
[1321] Пример 242. 2-амино-N-((1S,2S)-2-((4'-((1-(2-амино-2-оксоэтил)пиперидин-4-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[1322] Используя промежуточное соединение 22 и бромацетамид, названное соединение получали, как описано для примера 240.
[1323] 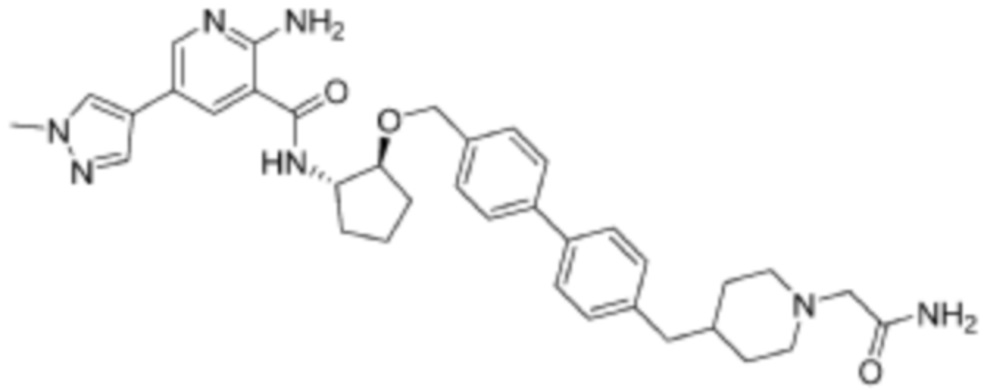
[1324] MS (ESI, масса/заряд): 622,8 [M+H]+
[1325] Пример 243. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4-(3-(4-метилпиперазин-1-ил)пропил)бензил)окси)циклопентил)никотинамид
[1326] Схема получения соединения из примера 243
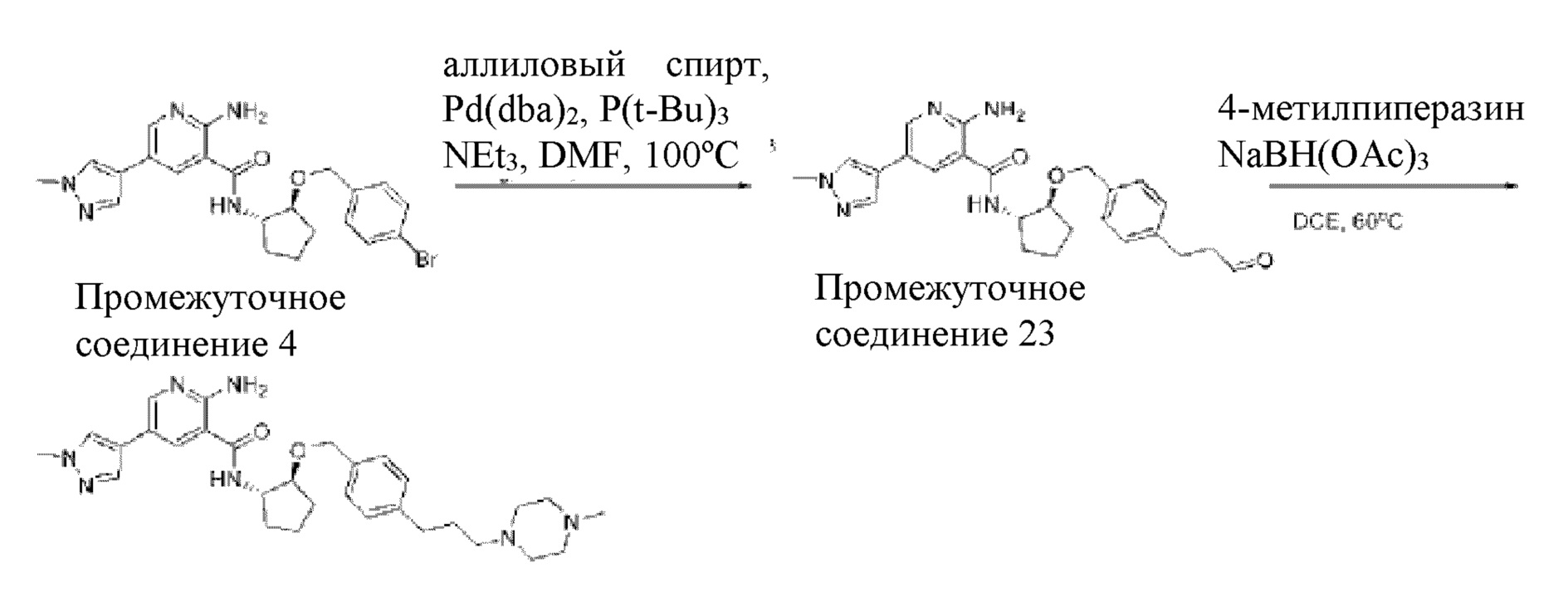
[1327]
[1328] Промежуточное соединение 23.
[1329] Смесь промежуточного соединения 4 (300 мг, 0,64 ммоль), Pd(dba)2 (7 мг, 0,01 ммоль), P(t-bu)3 (8 мг, 0,04 ммоль) в DMF (3 мл) дегазировали азотом и TEA (0,133 мл, 0,96 ммоль), добавляли аллиловый спирт (0,11 мл, 1,28 ммоль). Смесь нагревали при 100°C в течение 1 ч. После охлаждения смесь разделяли между EA и водой. Органический слой отделяли и промывали водой, солевым раствором, сушили над MgSO4 и концентрировали in vacuo. Неочищенный материал очищали флэш-хроматографией на силикагеле при помощи смеси Et2O-гексана в качестве элюентов с получением 150 мг грязно-белого твердого вещества.
[1330] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,64 (br dd, J=13,21, 6,75 Гц, 1 H) 1,75 (br d, J=7,63 Гц, 1 H) 1,79-1,85 (m, 2 H) 1,94-2,04 (m, 3 H) 2,16 (br d, J=6,46 Гц, 1 H) 2,64 (br t, J=7,63 Гц, 2 H) 2,89 (s, 3 H) 3,02-3,07 (m, 2 H) 3,40 (br s, 2 H) 3,46 (br s, 4 H) 3,93 (s, 3 H) 3,96-4,00 (m, 1 H) 4,36-4,42 (m, 1 H) 4,54-4,65 (m, 3 H) 7,16 (d, J=8,22 Гц, 2 H) 7,27 (d, J=8,22 Гц, 2 H) 7,84-7,89 (m, 1 H) 8,03 (s, 1 H) 8,23 (d, J=1,76 Гц, 1 H) 8,56 (d, J=2,35 Гц, 1 H);
[1331] MS (ESI, масса/заряд): 532,5 [M+H]+
[1332] Пример 243. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4-(3-(4-метилпиперазин-1-ил)пропил)бензил)окси)циклопентил)никотинамид
[1333] Используя промежуточное соединение 23, названное соединение получали, как описано для примера 172.
[1334] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,64 (br dd, J=13,21, 6,75 Гц, 1 H) 1,75 (br d, J=7,63 Гц, 1 H) 1,79-1,85 (m, 2 H) 1,94-2,04 (m, 3 H) 2,16 (br d, J=6,46 Гц, 1 H) 2,64 (br t, J=7,63 Гц, 2 H) 2,89 (s, 3 H) 3,02-3,07 (m, 2 H) 3,40 (br s, 2 H) 3,46 (br s, 4 H) 3,93 (s, 3 H) 3,96-4,00 (m, 1 H) 4,36-4,42 (m, 1 H) 4,54-4,65 (m, 3 H) 7,16 (d, J=8,22 Гц, 2 H) 7,27 (d, J=8,22 Гц, 2 H) 7,84-7,89 (m, 1 H) 8,03 (s, 1 H) 8,23 (d, J=1,76 Гц, 1 H) 8,56 (d, J=2,35 Гц, 1 H);
[1335] MS (ESI, масса/заряд): 532,4 [M+H]+
[1336] Пример 244. 2-амино-N-((1S,2S)-2-((4-(3-(диметиламино)пропил)бензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[1337] Используя промежуточное соединение 23 и диметиламин (50% в THF), названное соединение получали, как описано для примера 243.
[1338] 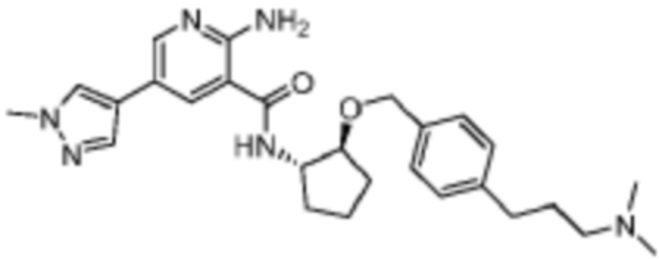
[1339] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,63-1,68 (m, 1 H) 1,73-1,78 (m, 1 H) 1,80-1,83 (m, 3 H) 1,96-2,05 (m, 3 H) 2,17 (br d, J=6,46 Гц, 1 H) 2,65 (br t, J=7,63 Гц, 2 H) 2,84 (s, 6 H) 3,06-3,14 (m, 2 H) 3,94 (s, 3 H) 3,98 (br s, 1 H) 4,39 (br s, 1 H) 4,55-4,67 (m, 3 H) 7,18 (br d, J=7,63 Гц, 2 H) 7,29 (br d, J=7,63 Гц, 2 H) 7,87-7,89 (m, 1 H) 8,04 (s, 1 H) 8,23 (d, J=1,76 Гц, 1 H) 8,57 (d, J=2,35 Гц, 1 H);
[1340] MS (ESI, масса/заряд): 477,5 [M+H]+
[1341] Пример 245. 2-амино-N-((1S,2S)-2-((4'-(2-(диметиламино)этокси)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[1342] Схема получения соединения из примера 245
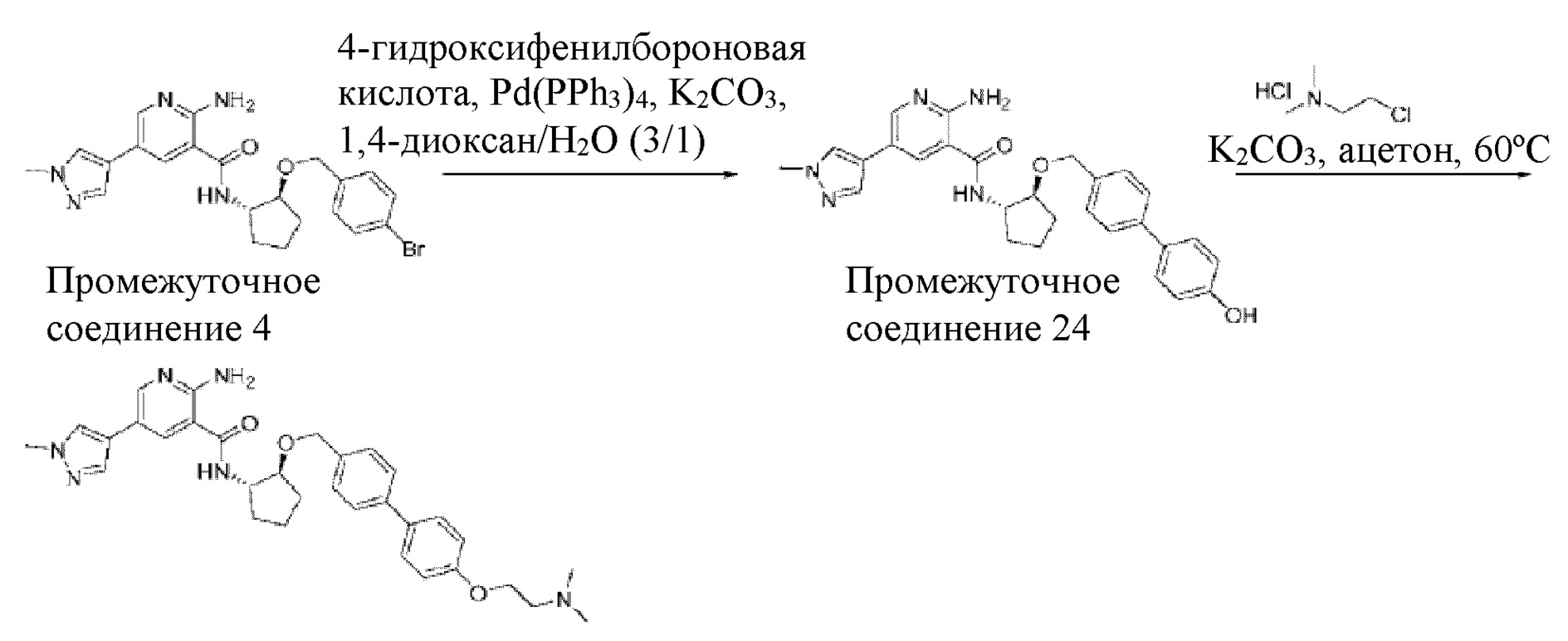
[1343]
[1344] Промежуточное соединение 24.
[1345] В смесь промежуточного соединения 4 (300 мг, 0,64 ммоль) и (4-гидроксифенил)бороновой кислоты (132 мг, 0,96 ммоль) в 4 мл 1,4-диоксана/воды (3/1) добавляли K2CO3 (264 мг, 1,91 ммоль), а затем Pd(PPh3)4 (37 мг, 0,03 ммоль). Реакционную смесь нагревали при 100°C в течение 3 часов, охлаждали до комнатной температуры и экстрагировали при помощи EtOAc, сушили над безводным MgSO4 и концентрировали под вакуумом. После концентрирования под вакуумом неочищенный материал очищали флэш-хроматографией на силикагеле при помощи смесей DCM-MeOH в качестве элюентов с получением 250 мг грязно-белого твердого вещества.
[1346] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,60 (br dd, J=13,21, 7,34 Гц, 1 H) 1,74-1,87 (m, 3 H) 2,04 (br dd, J=12,62, 7,34 Гц, 1 H) 2,10-2,20 (m, 1 H) 3,88 (s, 3 H) 3,92-4,00 (m, 1 H) 4,35-4,44 (m, 1 H) 4,57 (d, J=12,33 Гц, 1 H) 4,66 (d, J=12,33 Гц, 2 H) 6,78 (m, J=8,22 Гц, 2 H) 7,33 (t, J=9,10 Гц, 4 H) 7,43 (m, J=8,22 Гц, 2 H) 7,82 (s, 1 H) 7,91 (s, 1 H) 8,15 (d, J=2,35 Гц, 1 H) 8,43 (d, J=1,76 Гц, 1 H);
[1347] MS (ESI, масса/заряд): 484,3 [M+H]+
[1348] Пример 245. 2-амино-N-((1S,2S)-2-((4'-(2-(диметиламино)этокси)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[1349] Смесь промежуточного соединения 24 (30 мг, 0,06 ммоль) и K2CO3 (43 мг, 0,31 ммоль) нагревали при 60°C в течение 12 ч., охлаждали до комнатной температуры и экстрагировали при помощи EtOAc, сушили над безводным MgSO4 и концентрировали под вакуумом. После концентрирования под вакуумом неочищенный остаток очищали препаративной HPLC с получением 30 мг названного соединения.
[1350] 1H-ЯМР (400 МГц, CD3OD) δ ppm 1,57-1,68 (m, 1 H) 1,81 (br d, J=7,83 Гц, 3 H) 2,01 (br d, J=19,56 Гц, 1 H) 2,16 (br d, J=12,91 Гц, 1 H) 2,99 (s, 6 H) 3,61 (br s, 2 H) 3,89 (s, 3 H) 3,99 (br s, 1 H) 4,37 (br d, J=3,52 Гц, 3 H) 4,64 (s, 2 H) 7,05 (br d, J=8,22 Гц, 2 H) 7,38 (br d, J=7,83 Гц, 2 H) 7,50 (br t, J=7,43 Гц, 3 H) 7,84 (s, 1 H) 7,96 (s, 1 H) 8,19 (br s, 1 H) 8,48 (s, 1 H);
[1351] MS (ESI, масса/заряд): 555,4 [M+H]+
[1352] Пример 246. 2-амино-N-((1S,2S)-2-((4'-(3-(диметиламино)пропокси)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[1353] Используя (3-хлорпропил)диметиламин, названное соединение получали, как описано для примера 245.
[1354] 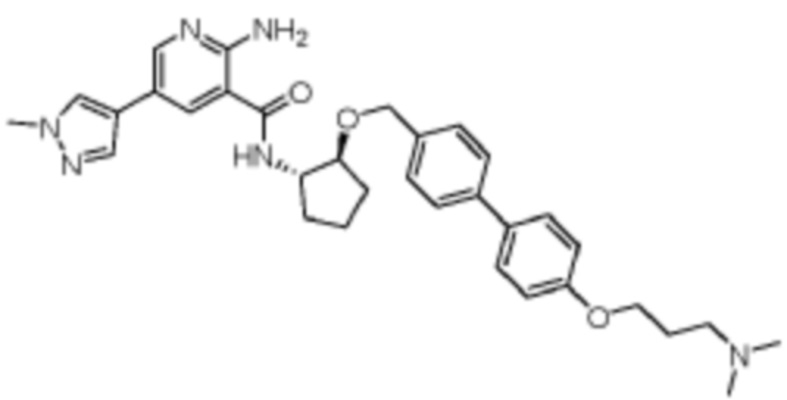
[1355] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,62 (br dd, J=13,21, 7,34 Гц, 1 H) 1,73-1,86 (m, 3 H) 2,04 (br dd, J=12,91, 7,63 Гц, 1 H) 2,16 (br dd, J=13,21, 6,16 Гц, 1 H) 2,19-2,28 (m, 2 H) 2,94 (s, 6 H) 3,32-3,41 (m, 2 H) 3,88 (s, 3 H) 3,93-4,05 (m, 1 H) 4,13 (t, J=5,87 Гц, 2 H) 4,36-4,43 (m, 1 H) 4,58-4,68 (m, 2 H) 6,97 (d, J=8,80 Гц, 2 H) 7,37 (d, J=8,22 Гц, 2 H) 7,46 (t, J=8,51 Гц, 4 H) 7,82 (s, 1 H) 7,93 (s, 1 H) 8,17 (d, J=2,35 Гц, 1 H) 8,43 (d, J=1,76 Гц, 1 H);
[1356] MS (ESI, масса/заряд): 569,4 [M+H]+
[1357] Пример 247. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4'-((1-метилпиперидин-4-ил)окси)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1358] Используя 4-бром-1-метилпиперидин, названное соединение получали, как описано для примера 245.
[1359] 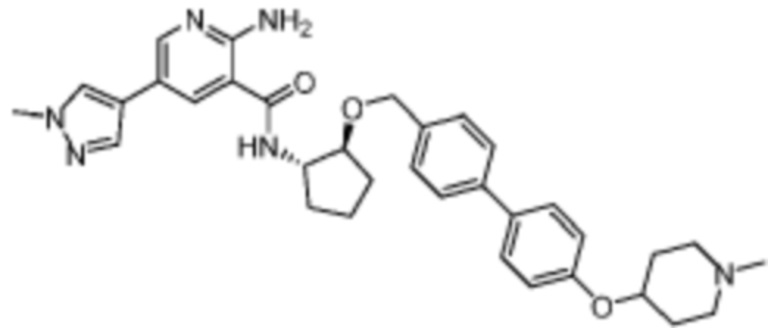
[1360] MS (ESI, масса/заряд): 581,5 [M+H]+
[1361] Пример 248. 2-амино-N-((1S,2S)-2-((4-(3-(диметиламино)проп-1-ин-1-ил)бензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[1362] Схема получения соединения из примера 248
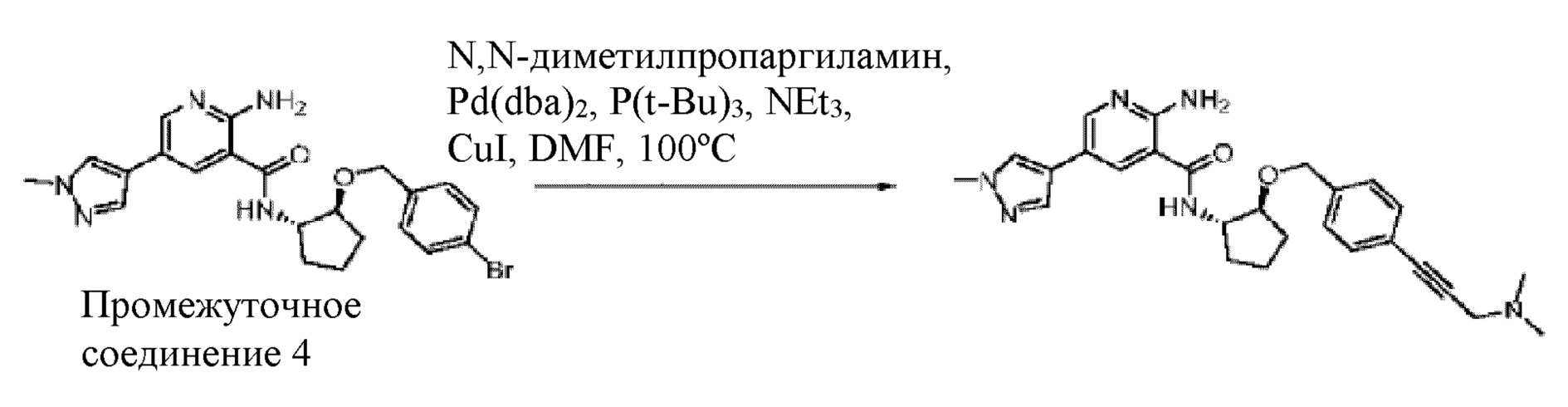
[1363]
[1364] Смесь промежуточного соединения 4 (40 мг, 0,09 ммоль), Pd(dba)2 (1 мг, 2 мольн. %), P(t-bu)3 (1 мг, 6 мольн. %) в DMF (3 мл) дегазировали азотом и TEA (0,018 мл, 0,13 ммоль), добавляли N,N-диметилпропаргиламин (0,016 мл, 0,17 ммоль). Смесь нагревали при 100°C в течение 12 ч. После охлаждения смесь разделяли между EA и водой. Органический слой отделяли и промывали водой, солевым раствором, сушили над MgSO4 и концентрировали in vacuo. После концентрирования под вакуумом неочищенный остаток очищали препаративной HPLC с получением 10 мг названного соединения.
[1365] 1H-ЯМР (400 МГц, CD3OD) δ ppm 1,63 (s, 2 H) 1,78 (br dd, J=14,28, 6,85 Гц, 2 H) 1,99 (br dd, J=12,91, 6,65 Гц, 1 H) 2,09-2,18 (m, 1 H) 2,35 (s, 3 H) 3,12-3,18 (m, 1 H) 3,32-3,34 (m, 4 H) 3,42-3,50 (m, 2 H) 3,58 (br d, J=7,04 Гц, 1 H) 3,90 (s, 3 H) 4,32-4,42 (m, 1 H) 4,61 (s, 2 H) 7,27-7,40 (m, 4 H) 7,76 (s, 1 H) 7,87 (s, 1 H) 7,98 (s, 1 H) 8,24 (s, 1 H);
[1366] MS (ESI, масса/заряд): 473,4 [M+H]+
[1367] Пример 249. 2-амино-N-((1S,2S)-2-((4-(4-гидроксибут-1-ин-1-ил)бензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[1368] Используя 3-бутин-1-ол, названное соединение получали, как описано для примера 248.
[1369] 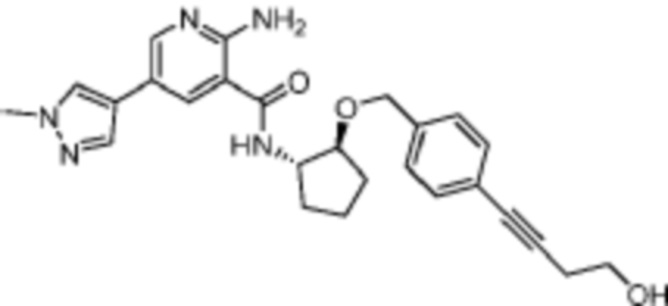
[1370] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,62 (br dd, J=13,21, 7,34 Гц, 1 H) 1,70-1,77 (m, 1 H) 1,77-1,84 (m, 3 H) 2,01 (br dd, J=12,62, 7,34 Гц, 1 H) 2,15 (br dd, J=13,21, 6,16 Гц, 1 H) 2,57 (t, J=6,75 Гц, 2 H) 3,69 (t, J=6,75 Гц, 2 H) 3,94 (s, 3 H) 4,32-4,40 (m, 1 H) 4,54-4,63 (m, 2 H) 7,23-7,31 (m, 4 H) 7,87 (s, 1 H) 8,01 (s, 1 H) 8,23 (d, J=2,35 Гц, 1 H) 8,50 (d, J=1,76 Гц, 1 H);
[1371] MS (ESI, масса/заряд): 460,6 [M+H]+
[1372] Пример 250. 2-амино-N-((1S,2S)-2-((4-(5-гидроксипент-1-ин-1-ил)бензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[1373] Используя 4-пентин-1-ол, названное соединение получали, как описано для примера 248.
[1374] 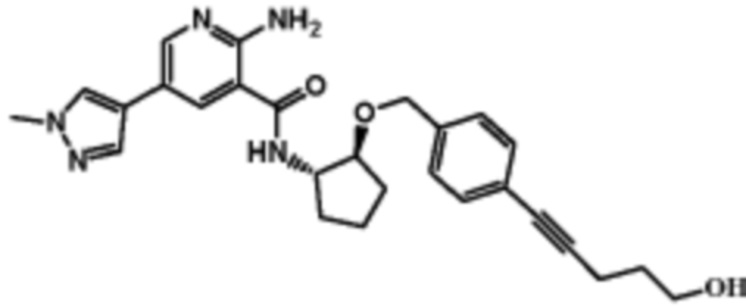
[1375] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,62 (br dd, J=12,91, 7,04 Гц, 1 H) 1,69-1,78 (m, 3 H) 1,78-1,86 (m, 2 H) 2,01 (br dd, J=12,91, 7,63 Гц, 1 H) 2,16 (br d, J=5,87 Гц, 1 H) 2,45 (t, J=7,04 Гц, 2 H) 3,66 (t, J=6,46 Гц, 2 H) 3,88-4,00 (m, 4 H) 4,31-4,41 (m, 1 H) 4,51-4,65 (m, 2 H) 7,26 (s, 4 H) 7,87 (s, 1 H) 8,01 (s, 1 H) 8,23 (d, J=1,76 Гц, 1 H) 8,51 (d, J=2,35 Гц, 1 H);
[1376] MS (ESI, масса/заряд): 474,2 [M+H]+
[1377] Пример 251. 2-амино-N-((1S,2S)-2-((4-(6-гидроксигекс-1-ин-1-ил)бензил)окси)циклопентил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[1378] Используя 5-гексин-1-ол, названное соединение получали, как описано для примера 248.
[1379] 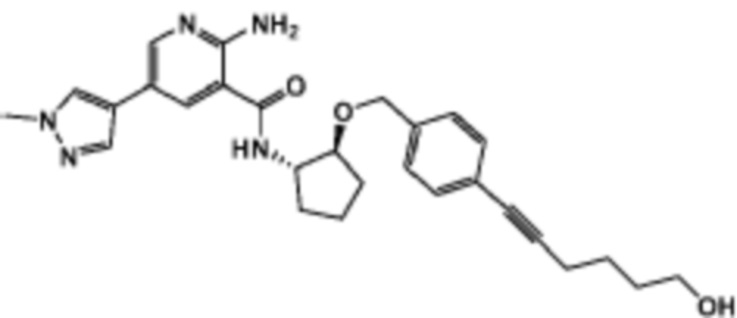
[1380] 1H-ЯМР (600 MГц, CD3OD) δ ppm 0,00-0,00 (m, 1 H) 1,54-1,69 (m, 8 H) 1,72-1,78 (m, 1 H) 1,78-1,86 (m, 3 H) 1,91 (br d, J=7,63 Гц, 1 H) 1,97-2,05 (m, 1 H) 2,12-2,20 (m, 1 H) 2,24-2,30 (m, 2 H) 2,32 (br d, J=3,52 Гц, 1 H) 2,40 (t, J=7,04 Гц, 1 H) 2,45 (t, J=6,75 Гц, 1 H) 2,43-2,43 (m, 1 H) 3,55 (t, J=6,46 Гц, 2 H) 3,56-3,60 (m, 1 H) 3,94 (d, J=1,17 Гц, 3 H) 4,35-4,41 (m, 2 H) 4,43 (t, J=6,46 Гц, 1 H) 4,54-4,65 (m, 2 H) 4,68-4,68 (m, 1 H) 4,69-4,69 (m, 1 H) 7,26 (d, J=7,04 Гц, 3 H) 7,87 (s, 1 H) 8,01 (s, 1 H) 8,19-8,26 (m, 1 H) 8,48-8,53 (m, 1 H);
[1381] MS (ESI, масса/заряд): 488,3 [M+H]+
[1382] Пример 252. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((4-(4-(4-метилпиперазин-1-ил)бут-1-ин-1-ил)бензил)окси)циклопентил)никотинамид
[1383] Схема получения соединения из примера 252
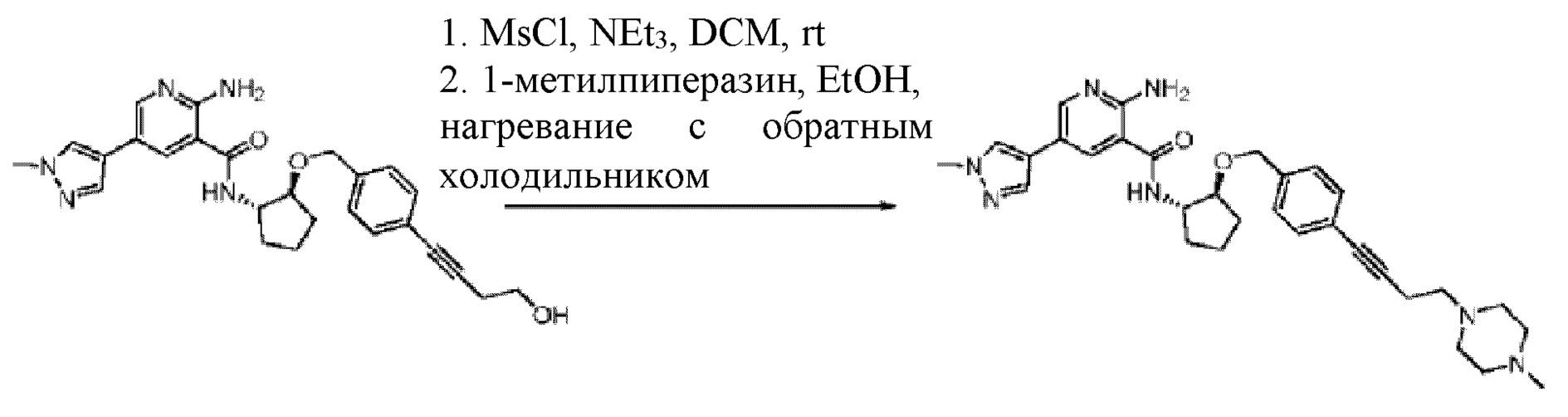
[1384]
[1385] В смесь соединения 249 (30 мг, 0,07 ммоль) и триэтиламина (27 мкл, 0,2 ммоль) в DCM (0,3 мл) добавляли метансульфонилхлорид (12 мкл, 0,16 ммоль). Смесь перемешивали при комнатной температуре в течение 2 ч. После завершения превращения летучие вещества удаляли под пониженным давлением. Неочищенный остаток разбавляли при помощи EtOH (0,3 мл) и добавляли 1-метилпиперазин (16 мкл, 0,13 ммоль). Смесь нагревали с обратным холодильником в течение 2 ч. После охлаждения неочищенный остаток очищали препаративной HPLC с получением 20 мг названного соединения.
[1386] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,63 (br dd, J=13,21, 6,75 Гц, 1 H) 1,75 (br d, J=5,28 Гц, 1 H) 1,80-1,84 (m, 2 H) 1,98-2,02 (m, 1 H) 2,16 (br dd, J=13,79, 6,75 Гц, 1 H) 2,78 (br s, 2 H) 2,89-2,93 (m, 3 H) 3,44 (br s, 4 H) 3,55 (br s, 2 H) 3,94 (s, 3 H) 3,95-3,99 (m, 1 H) 4,38 (br dd, J=11,15, 7,04 Гц, 1 H) 4,60 (s, 2 H) 7,26-7,35 (m, 4 H) 7,88 (s, 1 H) 8,02 (s, 1 H) 8,23 (d, J=2,35 Гц, 1 H) 8,55 (d, J=1,76 Гц, 1 H);
[1387] MS (ESI, масса/заряд): 542,5 [M+H]+
[1388] Пример 253. 2-амино-N-((1S,2S)-2-(бензилокси)циклопентил)-5-(4-((4-метилпиперазин-1-ил)метил)фенил)никотинамид
[1389] Схема получения соединения из примера 253:
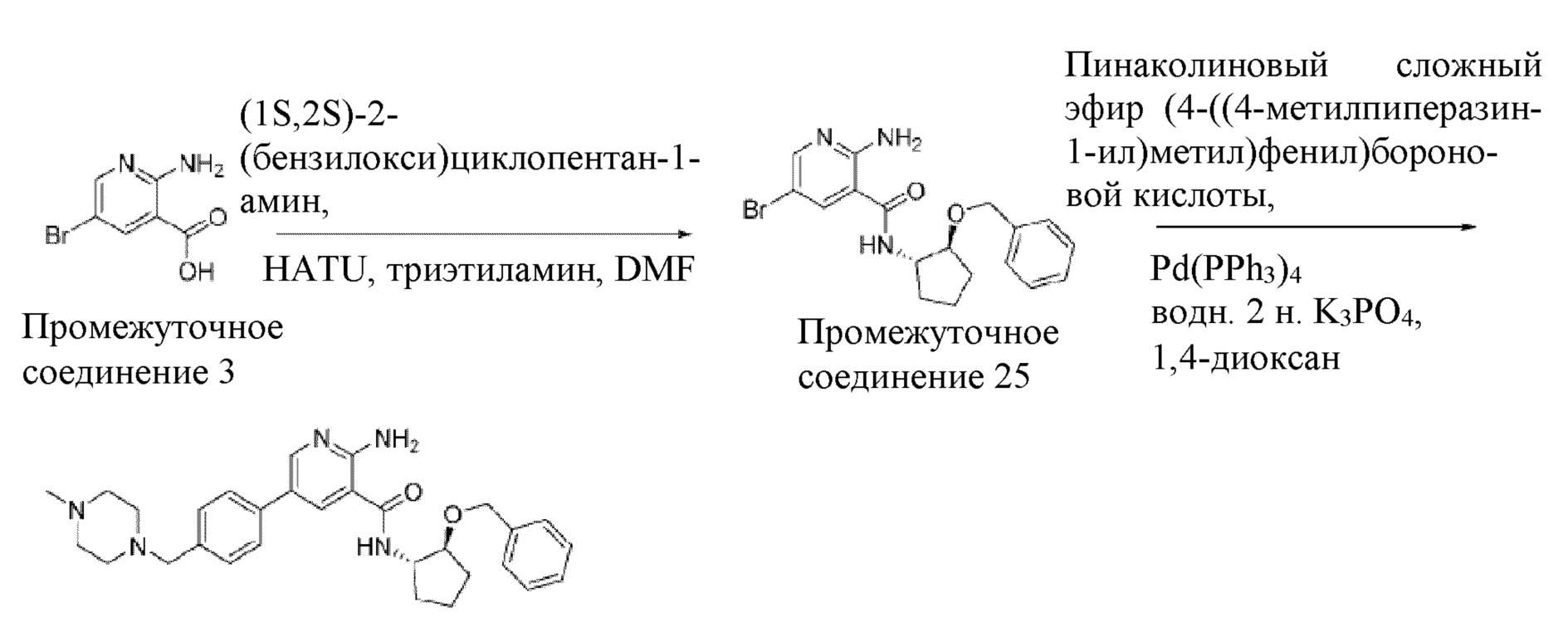
[1390]
[1391] Промежуточное соединение 25.
[1392] В смесь промежуточного соединения 3 (300 мг, 1,38 ммоль) и триэтиламина (168 мг, 1,66 ммоль) в 7 мл DMF добавляли HATU (524 мг, 1,66 ммоль), а затем (1S,2S)-2-(бензилокси)циклопентан-1-амин (263 мг, 1,38 ммоль). Смесь перемешивали при комнатной температуре в течение 1 часа, а затем добавляли насыщенный раствор бикарбоната натрия. Смесь экстрагировали при помощи EtOAc, промывали солевым раствором, сушили над MgSO4 и концентрировали in vacuo. Неочищенный продукт очищали колоночной хроматографией на силикагеле с получением 326 мг грязно-белого твердого вещества.
[1393] 1H-ЯМР (400 МГц, CDCl3) δ ppm 1,47 (dt, J=13,99, 6,90 Гц, 1 H) 1,72-1,82 (m, 2 H) 1,83-1,92 (m, 1 H) 1,92-2,01 (m, 2 H) 2,22-2,34 (m, 1 H) 3,79-3,88 (m, 1 H) 4,32 (dd, J=7,04, 4,70 Гц, 1 H) 4,56-4,68 (m, 2 H) 5,81 (br d, J=6,65 Гц, 1 H) 6,35 (br s, 2 H) 7,26-7,38 (m, 4 H) 7,53 (d, J=2,35 Гц, 1 H) 8,17 (d, J=2,35 Гц, 1 H);
[1394] MS (ESI, масса/заряд): 390,2/392,2 [M+H]+
[1395] Пример 253. 2-амино-N-((1S,2S)-2-(бензилокси)циклопентил)-5-(4-((4-метилпиперазин-1-ил)метил)фенил)никотинамид
[1396] В смесь промежуточного соединения 25 (40 мг, 0,1 ммоль) и пинаколинового сложного эфира (4-((4-метилпиперазин-1-ил)метил)фенил)бороновой кислоты (51 мг, 0,16 ммоль) в 1 мл 1,4-диоксана добавляли 0,15 мл водн. 2 н. K3PO4, а затем Pd(PPh3)4 (8 мг, 0,007 ммоль). Реакционную смесь нагревали при 100°C в течение 3 часов, охлаждали до комнатной температуры и экстрагировали при помощи EtOAc, сушили над безводным MgSO4 и концентрировали под вакуумом. Неочищенный остаток очищали препаративной HPLC с получением 23 мг названого соединения.
[1397] 1H-ЯМР (400 МГц, метанол-d4) δ ppm 1,57 (br dd, J=13,30, 7,04 Гц, 1 H) 1,66-1,87 (m, 3 H) 1,97 (dt, J=13,01, 6,60 Гц, 1 H) 2,13 (br dd, J=13,11, 6,85 Гц, 1 H) 2,95 (s, 3 H) 3,44-3,62 (m, 4 H) 3,87-3,97 (m, 1 H) 4,17 (s, 2 H) 4,31-4,39 (m, 1 H) 4,60 (s, 2 H) 6,25 (d, J=9,00 Гц, 1 H) 7,21-7,35 (m, 5 H) 7,43 (d, J=8,22 Гц, 2 H) 7,58 (d, J=8,61 Гц, 2 H) 8,08 (d, J=9,00 Гц, 1 H);
[1398] MS (ESI, масса/заряд): 500,3 [M+H]+
[1399] Пример 254. 2-амино-N-((1S,2S)-2-(бензилокси)циклопентил)-5-(1-(пиперидин-4-ил)-1H-пиразол-4-ил)никотинамид
[1400] Используя пинаколиновый сложный эфир (1-(пиперидин-4-ил)-1H-пиразол-4-ил)бороновой кислоты, названное соединение получали, как описано для примера 201.
[1401] 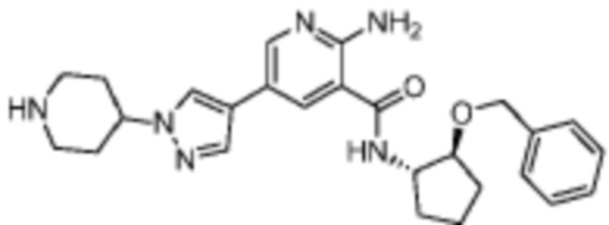
[1402] MS (ESI, масса/заряд): 461,3 [M+H]+
[1403] Пример 255. 2-амино-N-((1S,2S)-2-(бензилокси)циклопентил)-5-(1-(1-метилпиперидин-4-ил)-1H-пиразол-4-ил)никотинамид
[1404] Используя пинаколиновый сложный эфир (1-(1-метилпиперидин-4-ил)-1H-пиразол-4-ил)бороновой кислоты, названное соединение получали, как описано для примера 253.
[1405] 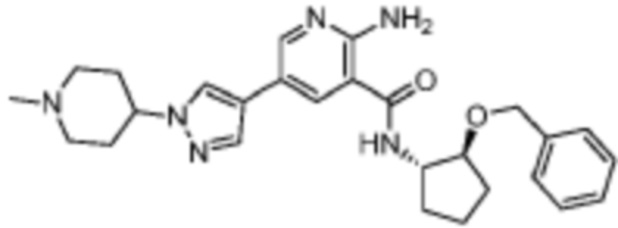
[1406] MS (ESI, масса/заряд): 475,3 [M+H]+
[1407] Пример 256. 2-амино-N-((1S,2S)-2-(бензилокси)циклопентил)-5-(1-(1-этилпиперидин-4-ил)-1H-пиразол-4-ил)никотинамид
[1408] Используя пинаколиновый сложный эфир (1-(1-этилпиперидин-4-ил)-1H-пиразол-4-ил)бороновой кислоты, названное соединение получали, как описано для примера 253.
[1409] 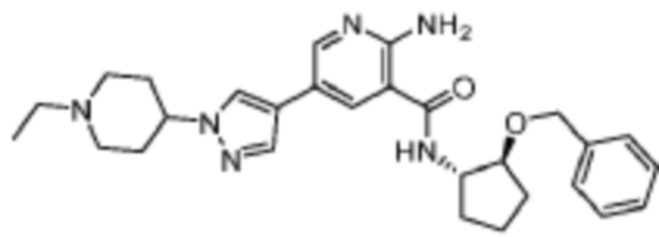
[1410] MS (ESI, масса/заряд): 489,3 [M+H]+
[1411] Пример 257. 2-амино-N-((1S,2S)-2-(бензилокси)циклопентил)-5-(1-(1-изопропилпиперидин-4-ил)-1H-пиразол-4-ил)никотинамид
[1412] Используя пинаколиновый сложный эфир (1-(1-изопропилпиперидин-4-ил)-1H-пиразол-4-ил)бороновой кислоты, названное соединение получали, как описано для примера 253.
[1413] 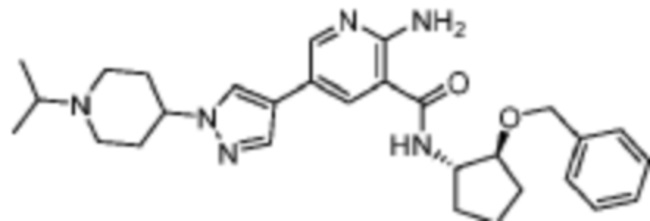
[1414] MS (ESI, масса/заряд): 503,3 [M+H]+
[1415] Пример 258. 2-амино-N-((1S,2S)-2-(бензилокси)циклопентил)-5-(1-(1-(пирролидин-3-илметил)пиперидин-4-ил)-1H-пиразол-4-ил)никотинамид
[1416] Используя пинаколиновый сложный эфир (1-(1-(пирролидин-3-илметил)пиперидин-4-ил)-1H-пиразол-4-ил)бороновой кислоты, названное соединение получали, как описано для примера 253.
[1417] 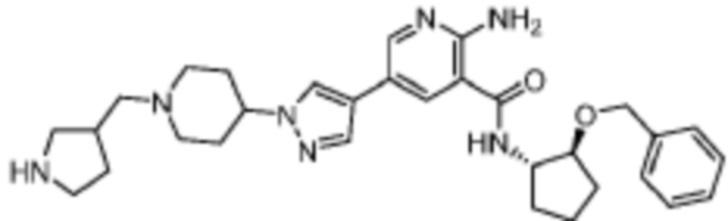
[1418] MS (ESI, масса/заряд): 544,3 [M+H]+
[1419] Пример 259. 2-амино-N-((1R,2R)-2-(бензилокси)циклопентил)-5-(1-(пиперидин-4-ил)-1H-пиразол-4-ил)никотинамид
[1420] Используя (1R,2R)-2-(бензилокси)циклопентан-1-амин и пинаколиновый сложный эфир (1-(пиперидин-4-ил)-1H-пиразол-4-ил)бороновой кислоты, названное соединение получали, как описано для примера 253.
[1421] 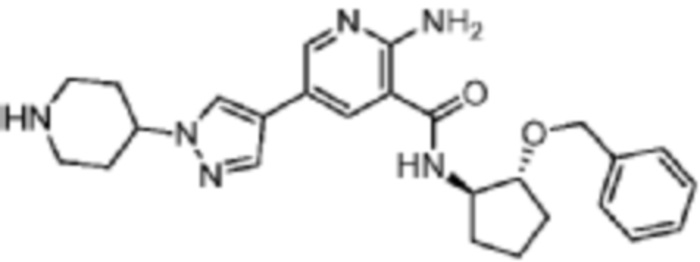
[1422] MS (ESI, масса/заряд): 461,3 [M+H]+
[1423] Пример 260. 2-амино-N-((1S,2S)-2-((3,4-дихлорбензил)окси)циклопентил)-5-(1-(пиперидин-4-ил)-1H-пиразол-4-ил)никотинамид
[1424] Используя (1S,2S)-2-((3,4-дихлорбензил)окси)циклопентан-1-амин и пинаколиновый сложный эфир (1-(пиперидин-4-ил)-1H-пиразол-4-ил)бороновой кислоты, названное соединение получали, как описано для примера 253.
[1425] 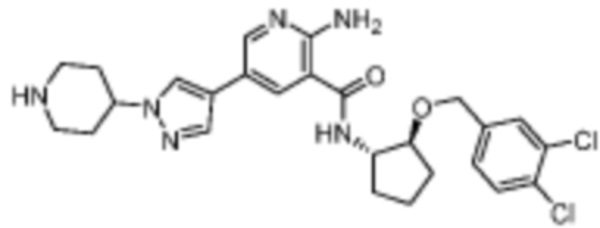
[1426] MS (ESI, масса/заряд): 529,2 [M+H]+
[1427] Пример 261. 2-амино-N-((1S,2S)-2-(бензилокси)циклопентил)-5-(3-(гидроксиметил)-1-метил-1H-пиразол-4-ил)никотинамид
[1428] Используя пинаколиновый сложный эфир (3-(гидроксиметил)-1-метил-1H-пиразол-4-ил)бороновой кислоты, названное соединение получали, как описано для примера 253.
[1429] 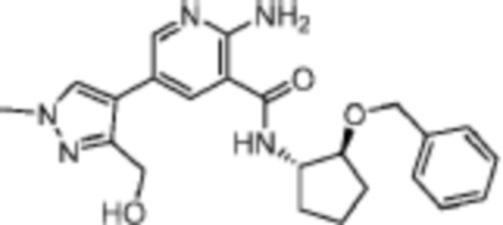
[1430] MS (ESI, масса/заряд): 422,2 [M+H]+
[1431] Пример 262. 2-амино-N-((1S,2S)-2-(бензилокси)циклопентил)-5-(3-(((2-гидроксиэтил)амино)метил)-1-метил-1H-пиразол-4-ил)никотинамид
[1432] Используя пинаколиновый сложный эфир (3-(((2-гидроксиэтил)амино)метил)-1-метил-1H-пиразол-4-ил)бороновой кислоты, названное соединение получали, как описано для примера 253.
[1433] 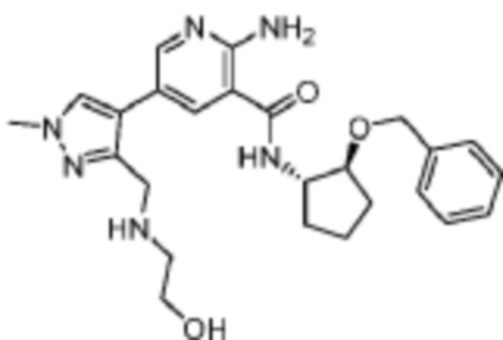
[1434] MS (ESI, масса/заряд): 465,3 [M+H]+
[1435] Пример 263. 2-амино-N-((1S,2S)-2-(бензилокси)циклопентил)-5-(3-((3-гидроксипиперидин-1-ил)метил)-1-метил-1H-пиразол-4-ил)никотинамид
[1436] Используя пинаколиновый сложный эфир (3-((3-гидроксипиперидин-1-ил)метил)-1-метил-1H-пиразол-4-ил)бороновой кислоты, названное соединение получали, как описано для примера 253.
[1437] 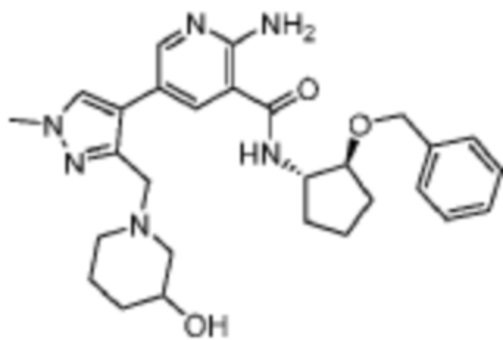
[1438] MS (ESI, масса/заряд): 505,3 [M+H]+
[1439] Пример 264. 2-амино-N-((1S,2S)-2-(бензилокси)циклопентил)-5-(4-цианофенил)никотинамид
[1440] Используя (4-цианофенил)бороновую кислоту, названное соединение получали, как описано для примера 253.
[1441] 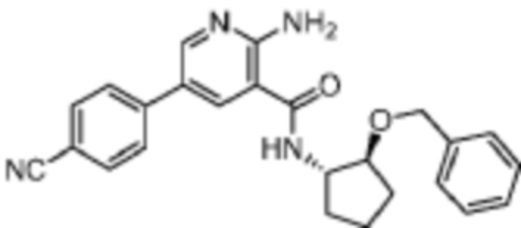
[1442] 1H-ЯМР (400 МГц, CDCl3) 1,59 (m, 2 H) 1,85 (m, 4 H) 2,10 (m, 2 H) 2,24 (m, 1 H) 4,17 (br d, J=7,04 Гц, 1 H) 4,28 (br d, J=7,04 Гц, 1 H) 4,43-4,54 (m, 1 H) 4,56-4,67 (m, 2 H) 7,13-7,19 (m, 1 H) 7,13-7,19 (m, 1 H) 7,13-7,19 (m, 2 H) 7,19-7,24 (m, 2 H) 7,35 (br d, J=7,43 Гц, 2 H) 7,64 (m, J=8,22 Гц, 2 H) 7,73 (m, J=8,22 Гц, 2 H) 7,80 (s, 1 H) 7,85-7,91 (m, 1 H) 8,27 (s, 1 H) 8,58 (br s, 2 H) 11,76-11,97 (m, 2 H);
[1443] MS (ESI, масса/заряд): 413,2 [M+H]+
[1444] Пример 265. 2-амино-N-((1S,2S)-2-(бензилокси)циклопентил)-5-(3-цианофенил)никотинамид
[1445] Используя (3-цианофенил)бороновую кислоту, названное соединение получали, как описано для примера 253.
[1446] 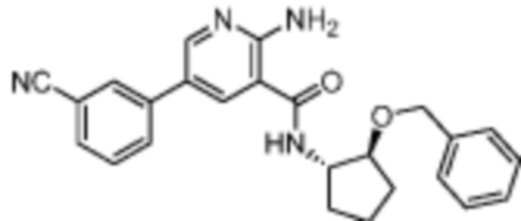
[1447] 1H-ЯМР (400 МГц, CDCl3) 1,54-1,70 (m, 2 H) 1,70-1,95 (m, 4 H) 2,07 (br s, 2 H) 2,23 (br s, 2 H) 4,08 (br d, J=5,87 Гц, 1 H) 4,33 (br s, 1 H) 4,61 (q, J=11,74 Гц, 2 H) 7,14-7,20 (m, 1 H) 7,20-7,29 (m, 2 H) 7,29-7,38 (m, 2 H) 7,53-7,63 (m, 1 H) 7,70 (br d, J=7,43 Гц, 1 H) 7,75 (br d, J=7,43 Гц, 1 H) 7,87 (s, 1 H) 7,91 (s, 1 H) 8,26 (s, 1 H) 8,87 (br s, 2 H) 11,40-11,54 (m, 1 H);
[1448] MS (ESI, масса/заряд): 413,2 [M+H]+
[1449] Пример 266. 2-амино-N-((1S,2S)-2-(бензилокси)циклопентил)-5-(4-(цианометил)фенил)никотинамид
[1450] Используя (4-(цианометил)фенил)бороновую кислоту, названное соединение получали, как описано для примера 253.
[1451] 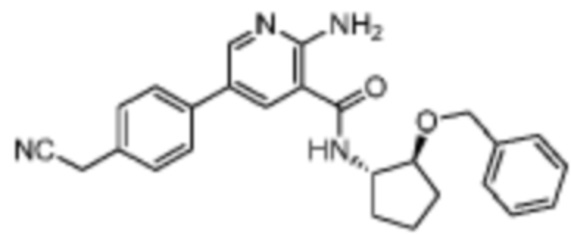
[1452] 1H-ЯМР (400 МГц, CDCl3) 1,54-1,64 (m, 1 H) 1,70 (br s, 1 H) 1,83 (br s, 2 H) 1,97-2,05 (m, 2 H) 3,11 (br s, 1 H) 3,79 (s, 2 H) 4,35 (br s, 1 H) 4,64 (s, 2 H) 7,14 (br s, 1 H) 7,18-7,24 (m, 3 H) 7,39 (br t, J=7,83 Гц, 2 H) 7,55 (br d, J=7,83 Гц, 1 H) 7,59 (s, 1 H) 8,00 (br s, 1 H) 8,34 (s, 1 H) 8,55-8,67 (m, 1 H);
[1453] MS (ESI, масса/заряд): 427,2 [M+H]+
[1454] Пример 267. 2-амино-N-((1S,2S)-2-(бензилокси)циклопентил)-5-(4-феноксифенил)никотинамид
[1455] Используя (4-феноксифенил)бороновую кислоту, названное соединение получали, как описано для примера 253.
[1456] 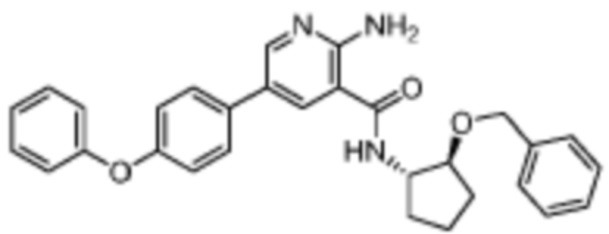
[1457] 1H-ЯМР (400 МГц, CDCl3) 1,23 (m, 2 H) 1,56 (m, 2 H) 1,75 (m, 4 H) 2,07 (br s, 2 H) 2,24 (br s, 2 H) 4,12 (br d, J=5,87 Гц, 1 H) 4,29 (br s, 1 H) 4,56-4,66 (m, 2 H) 7,04 (br t, J=6,85 Гц, 3 H) 7,17 (br d, J=7,43 Гц, 1 H) 7,22-7,26 (m, 4 H) 7,30-7,39 (m, 3 H) 7,39-7,44 (m, 2 H) 7,50 (s, 1 H) 7,74 (s, 1 H) 8,18 (s, 1 H) 8,45 (br s, 2 H) 11,28 (br s, 1 H);
[1458] MS (ESI, масса/заряд): 480,2 [M+H]+
[1459] Пример 268. 2-амино-N-((1S,2S)-2-(бензилокси)циклопентил)-5-(3-((1-метилпиперидин-4-ил)карбамоил)фенил)никотинамид
[1460] Используя (3-((1-метилпиперидин-4-ил)карбамоил)фенил)бороновую кислоту, названное соединение получали, как описано для примера 253.
[1461] 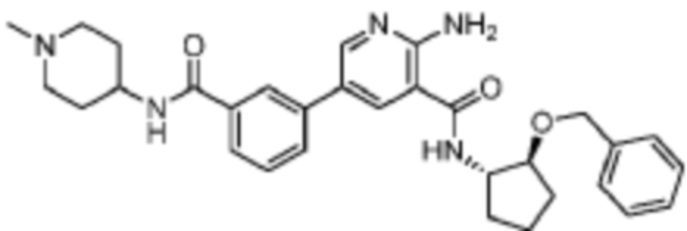
[1462] MS (ESI, масса/заряд): 528,3 [M+H]+
[1463] Пример 269. 6-амино-N-((1S,2S)-2-(бензилокси)циклопентил)-6'-(гидроксиметил)-[3,3'-бипиридин]-5-карбоксамид
[1464] Используя (6-(гидроксиметил)пиридин-3-ил)бороновую кислоту, названное соединение получали, как описано для примера 253.
[1465] 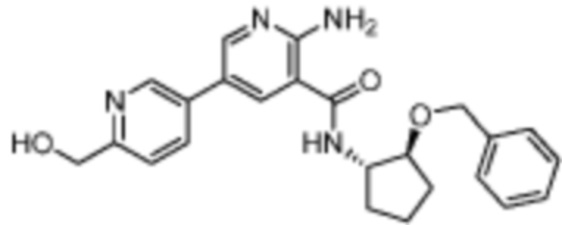
[1466] MS (ESI, масса/заряд): 420,2 [M+H]+
[1467] Пример 270. 2-амино-N-((1S,2S)-2-((3-метилбензил)окси)циклопентил)-5-(4-((4-метилпиперазин-1-ил)метил)фенил)никотинамид
[1468] Используя (1S,2S)-2-((3-метилбензил)окси)циклопентан-1-амин и пинаколиновый сложный эфир (4-((4-метилпиперазин-1-ил)метил)фенил)бороновой кислоты, названное соединение получали, как описано для примера 253.
[1469] 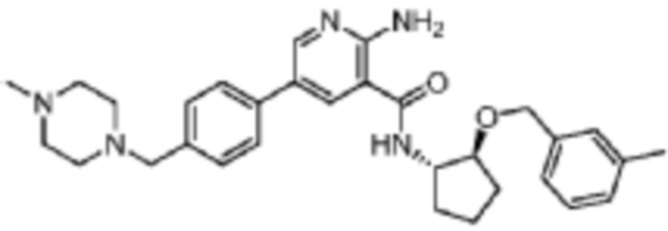
[1470] MS (ESI, масса/заряд): 514,3 [M+H]+
[1471] Пример 271. 2-амино-N-((1S,2S)-2-((3-метилбензил)окси)циклопентил)-5-(3-(4-метилпиперазин-1-карбонил)фенил)никотинамид
[1472] Используя (1S,2S)-2-((3-метилбензил)окси)циклопентан-1-амин и (4-метилпиперазин-1-ил)(3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил)метанон, названное соединение получали, как описано для примера 253.
[1473] 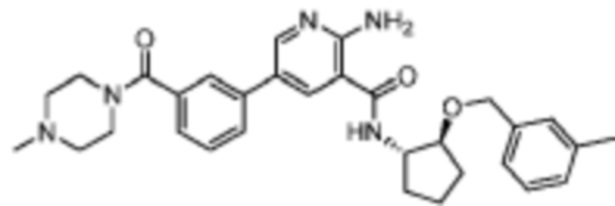
[1474] MS (ESI, масса/заряд): 528,3 [M+H]+
[1475] Пример 272. 2-амино-N-((1S,2S)-2-((3-метилбензил)окси)циклопентил)-5-(3-(4-(пирролидин-1-ил)пиперидин-1-карбонил)фенил)никотинамид
[1476] Используя (1S,2S)-2-((3-метилбензил)окси)циклопентан-1-амин и (4-(пирролидин-1-ил)пиперидин-1-ил)(3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил)метанон, названное соединение получали, как описано для примера 253.
[1477] 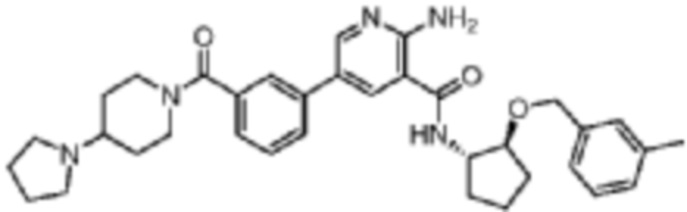
[1478] MS (ESI, масса/заряд): 582,3 [M+H]+
[1479] Пример 273. 2-амино-N-((1S,2S)-2-((3-метилбензил)окси)циклопентил)-5-(3-((4-метилпиперазин-1-ил)метил)фенил)никотинамид
[1480] Используя (1S,2S)-2-((3-метилбензил)окси)циклопентан-1-амин и 1-метил-4-(3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)пиперазин, названное соединение получали, как описано для примера 253.
[1481] 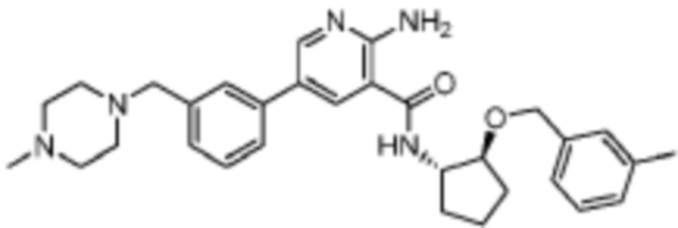
[1482] MS (ESI, масса/заряд): 514,3 [M+H]+
[1483] Пример 274. 2-амино-5-(3-фтор-4-((4-метилпиперазин-1-ил)метил)фенил)-N-((1S,2S)-2-((3-метилбензил)окси)циклопентил)никотинамид
[1484] Используя (1S,2S)-2-((3-метилбензил)окси)циклопентан-1-амин и 1-(2-фтор-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)-4-метилпиперазин, названное соединение получали, как описано для примера 253.
[1485] 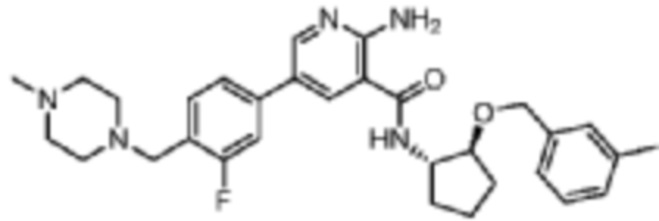
[1486] MS (ESI, масса/заряд): 532,3 [M+H]+
[1487] Пример 275. 2-амино-N-((1S,2S)-2-((3-метилбензил)окси)циклопентил)-5-(4-((4-(пирролидин-1-ил)пиперидин-1-ил)метил)фенил)никотинамид
[1488] Используя (1S,2S)-2-((3-метилбензил)окси)циклопентан-1-амин и 4-(пирролидин-1-ил)-1-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)пиперидин, названное соединение получали, как описано для примера 253.
[1489] 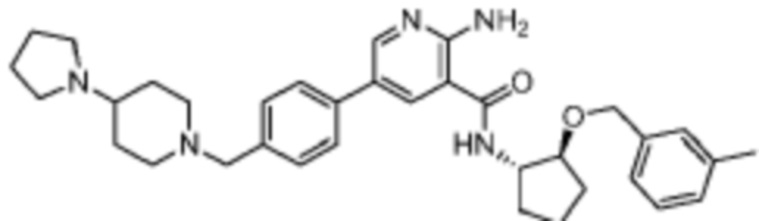
[1490] MS (ESI, масса/заряд): 568,4 [M+H]+
[1491] Пример 276. 2-амино-N-((1S,2S)-2-((3-метилбензил)окси)циклопентил)-5-(4-(4-метилпиперазин-1-карбонил)фенил)никотинамид
[1492] Используя (1S,2S)-2-((3-метилбензил)окси)циклопентан-1-амин и (4-метилпиперазин-1-ил)(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил)метанон, названное соединение получали, как описано для примера 253.
[1493] 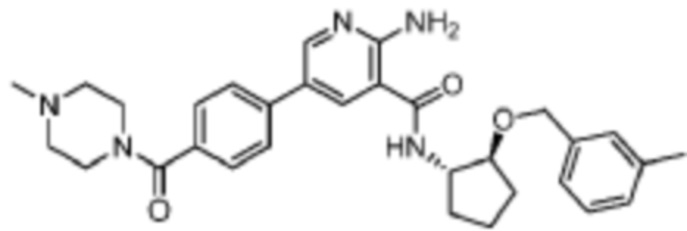
[1494] MS (ESI, масса/заряд): 528,3 [M+H]+
[1495] Пример 277. 2-амино-N-((1S,2S)-2-((3-метилбензил)окси)циклопентил)-5-(4-(4-(пирролидин-1-ил)пиперидин-1-карбонил)фенил)никотинамид
[1496] Используя (1S,2S)-2-((3-метилбензил)окси)циклопентан-1-амин и (4-(пирролидин-1-ил)пиперидин-1-ил)(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил)метанон, названное соединение получали, как описано для примера 253.
[1497] 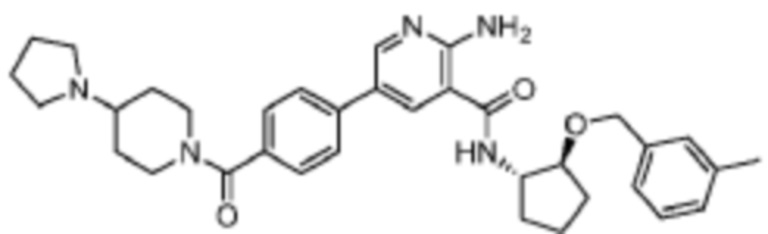
[1498] MS (ESI, масса/заряд): 582,3 [M+H]+
[1499] Пример 278. 2-амино-N-((1S,2S)-2-((3-метилбензил)окси)циклопентил)-5-(4-(2-((1-метилпиперидин-4-ил)амино)-2-оксоэтил)фенил)никотинамид
[1500] Используя (1S,2S)-2-((3-метилбензил)окси)циклопентан-1-амин и N-(1-метилпиперидин-4-ил)-2-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил)ацетамид, названное соединение получали, как описано для примера 253.
[1501] 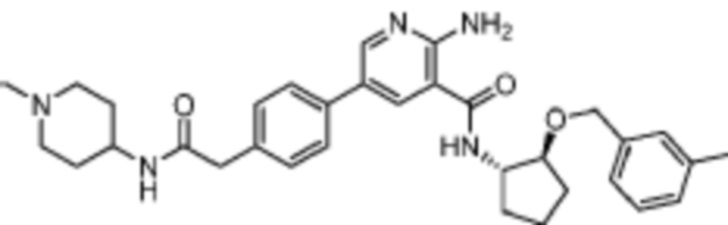
[1502] MS (ESI, масса/заряд): 556,3 [M+H]+
[1503] Пример 279. 2-амино-N-((1S,2S)-2-((3-метилбензил)окси)циклопентил)-5-(4-(2-(4-метилпиперазин-1-ил)ацетил)фенил)никотинамид
[1504] Используя (1S,2S)-2-((3-метилбензил)окси)циклопентан-1-амин и 2-(4-метилпиперазин-1-ил)-1-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил)этан-1-он, названное соединение получали, как описано для примера 253.
[1505] 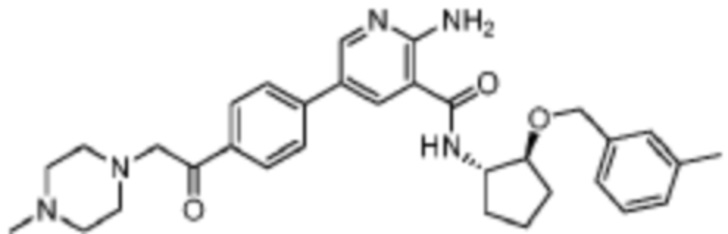
[1506]
[1507] MS (ESI, масса/заряд): 542,3 [M+H]+
[1508] Пример 280. 2-амино-5-(3-фтор-4-((4-(пирролидин-1-ил)пиперидин-1-ил)метил)фенил)-N-((1S,2S)-2-((3-метилбензил)окси)циклопентил)никотинамид
[1509] (1S,2S)-2-((3-метилбензил)окси)циклопентан-1-амин и 1-(2-фтор-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)-4-(пирролидин-1-ил)пиперидин, названное соединение получали, как описано для примера 253.
[1510] 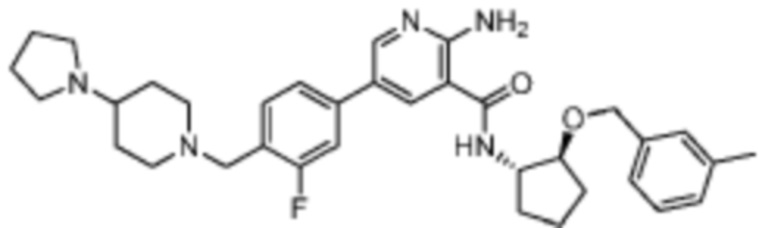
[1511] MS (ESI, масса/заряд): 586,4 [M+H]+
[1512] Пример 281. 2-амино-N-((1S,2S)-2-((3-метилбензил)окси)циклопентил)-5-(4-(4-(4-метилпиперазин-1-ил)пиперидин-1-карбонил)фенил)никотинамид
[1513] Используя (1S,2S)-2-((3-метилбензил)окси)циклопентан-1-амин и (4-(4-метилпиперазин-1-ил)пиперидин-1-ил)(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил)метанон, названное соединение получали, как описано для примера 253.
[1514] 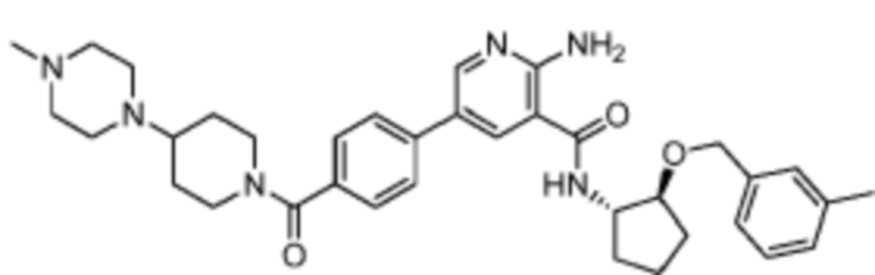
[1515] MS (ESI, масса/заряд): 611,4 [M+H]+
[1516] Пример 282. 2-амино-N-((1S,2S)-2-((3-метилбензил)окси)циклопентил)-5-(4-(пиперазин-1-илметил)фенил)никотинамид
[1517] Используя (1S,2S)-2-((3-метилбензил)окси)циклопентан-1-амин и 1-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)пиперазин, названное соединение получали, как описано для примера 253.
[1518] 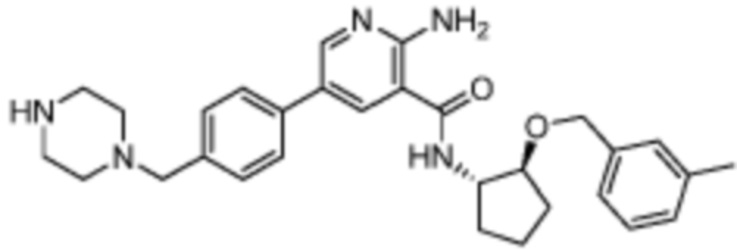
[1519] MS (ESI, масса/заряд): 500,3 [M+H]+
[1520] Пример 283. 2-амино-N-((1S,2S)-2-((4-метилбензил)окси)циклопентил)-5-(4-(4-метилпиперазин-1-карбонил)фенил)никотинамид
[1521] Используя (1S,2S)-2-((4-метилбензил)окси)циклопентан-1-амин и (4-метилпиперазин-1-ил)(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил)метанон, названное соединение получали, как описано для примера 253.
[1522] 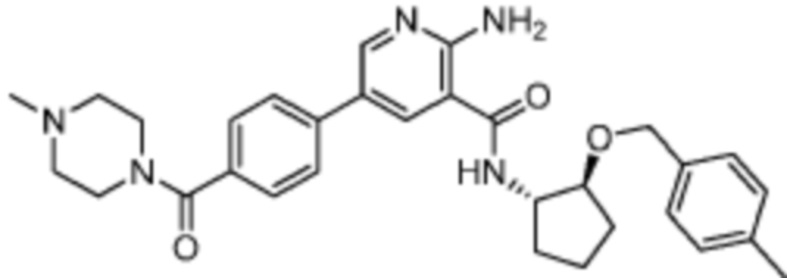
[1523] MS (ESI, масса/заряд): 528,3 [M+H]+
[1524] Пример 284. 2-амино-N-((1S,2S)-2-((4-метилбензил)окси)циклопентил)-5-(4-(4-(пирролидин-1-ил)пиперидин-1-карбонил)фенил)никотинамид
[1525] Используя (1S,2S)-2-((4-метилбензил)окси)циклопентан-1-амин и (4-(пирролидин-1-ил)пиперидин-1-ил)(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил)метанон, названное соединение получали, как описано для примера 253.
[1526] 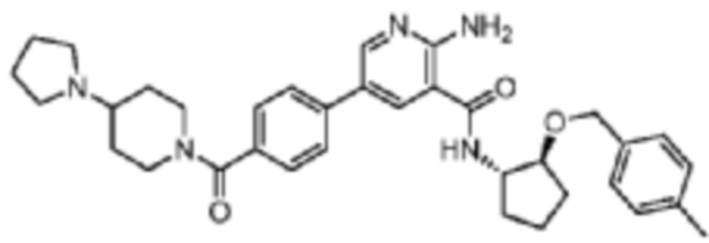
[1527] MS (ESI, масса/заряд): 582,3 [M+H]+
[1528] Пример 285. 2-амино-5-(1,5-диметил-1H-пиразол-4-ил)-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)никотинамид
[1529] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и пинаколиновый сложный эфир (1,5-диметил-1H-пиразол-4-ил)бороновой кислоты, названное соединение получали, как описано для примера 253.
[1530] 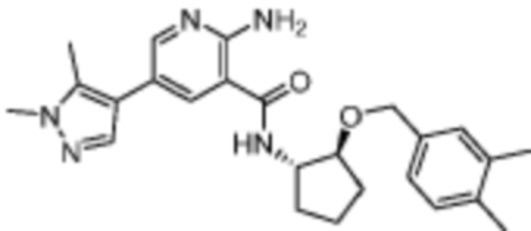
[1531] MS (ESI, масса/заряд): 434,3 [M+H]+
[1532] Пример 286. 2-амино-5-(1,3-диметил-1H-пиразол-4-ил)-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)никотинамид
[1533] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и пинаколиновый сложный эфир (1,3-диметил-1H-пиразол-4-ил)бороновой кислоты, названное соединение получали, как описано для примера 253.
[1534] 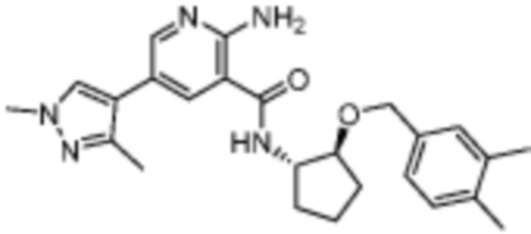
[1535] MS (ESI, масса/заряд): 434,3 [M+H]+
[1536] Пример 287. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(2-(2-гидроксипропан-2-ил)-4-метилтиазол-5-ил)никотинамид
[1537] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и пинаколиновый сложный эфир (2-(2-гидроксипропан-2-ил)-4-метилтиазол-5-ил)бороновой кислоты, названное соединение получали, как описано для примера 253.
[1538] 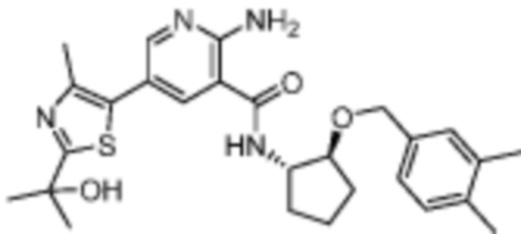
[1539] MS (ESI, масса/заряд): 495,2 [M+H]+
[1540] Пример 288. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(2-(3-гидрокситетрагидрофуран-3-ил)-4-метилтиазол-5-ил)никотинамид
[1541] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и пинаколиновый сложный эфир (2-(3-гидрокситетрагидрофуран-3-ил)-4-метилтиазол-5-ил)бороновой кислоты, названное соединение получали, как описано для примера 253.
[1542] 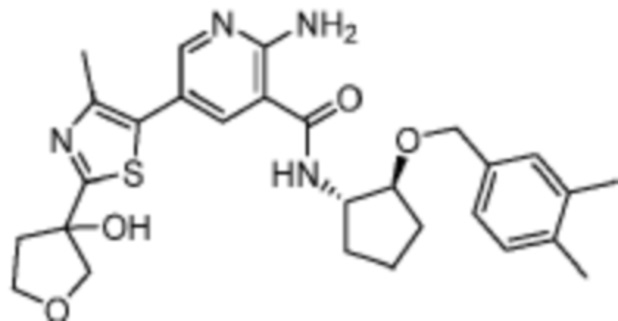
[1543] MS (ESI, масса/заряд): 523,2 [M+H]+
[1544] Пример 289. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(4-((4-метилпиперазин-1-ил)метил)фенил)никотинамид
[1545] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и пинаколиновый сложный эфир (4-((4-метилпиперазин-1-ил)метил)фенил)бороновой кислоты, названное соединение получали, как описано для примера 253.
[1546] 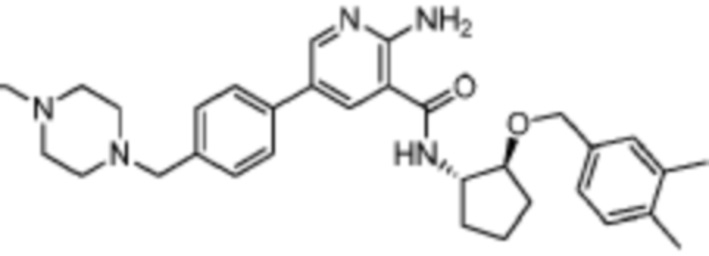
[1547] MS (ESI, масса/заряд): 528,3 [M+H]+
[1548] Пример 290. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(4-(2-(4-метилпиперазин-1-ил)-2-оксоэтил)фенил)никотинамид
[1549] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и 1-(4-метилпиперазин-1-ил)-2-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил)этан-1-он, названное соединение получали, как описано для примера 253.
[1550] 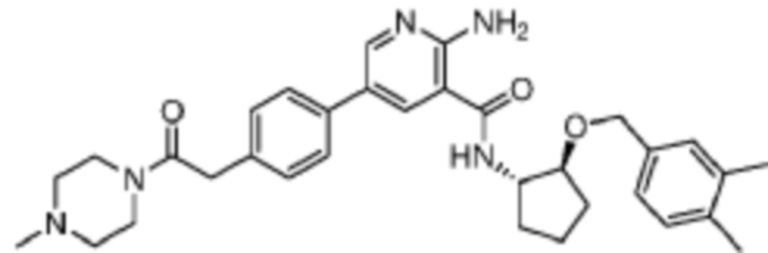
[1551] MS (ESI, масса/заряд): 556,3 [M+H]+
[1552] Пример 291. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(4-(морфолинометил)фенил)никотинамид
[1553] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и 4-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)морфолин, названное соединение получали, как описано для примера 253.
[1554] 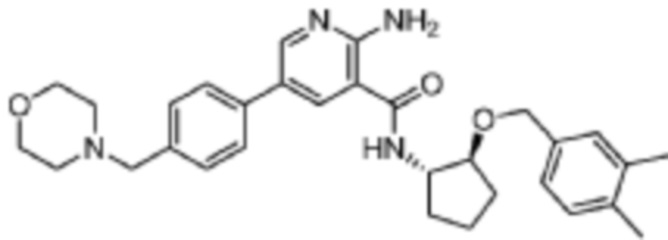
[1555] MS (ESI, масса/заряд): 515,3 [M+H]+
[1556] Пример 292. 2-амино-5-(4-((диметиламино)метил)фенил)-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)никотинамид
[1557] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (4-((диметиламино)метил)фенил)бороновую кислоту, названное соединение получали, как описано для примера 253.
[1558] 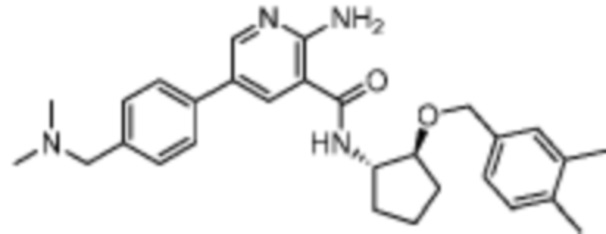
[1559] MS (ESI, масса/заряд): 473,3 [M+H]+
[1560] Пример 293. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(4-((4-(2-гидроксиэтил)пиперазин-1-ил)метил)фенил)никотинамид
[1561] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и 2-(4-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)пиперазин-1-ил)этан-1-ол, названное соединение получали, как описано для примера 253.
[1562] 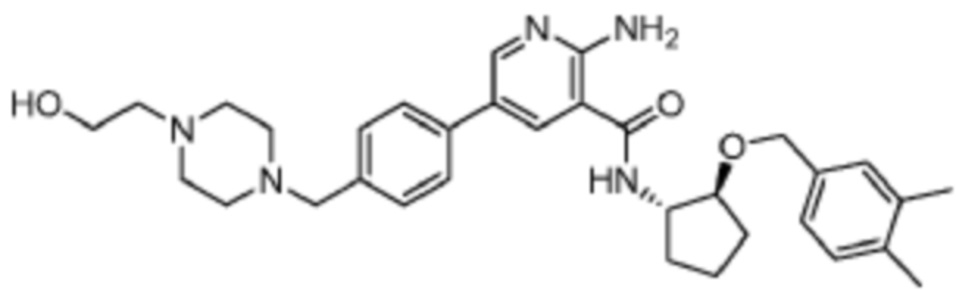
[1563] MS (ESI, масса/заряд): 558,3 [M+H]+
[1564] Пример 294. 6-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-2'-метокси-[3,3'-бипиридин]-5-карбоксамид
[1565] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (2-метоксипиридин-3-ил)бороновую кислоту, названное соединение получали, как описано для примера 253.
[1566] 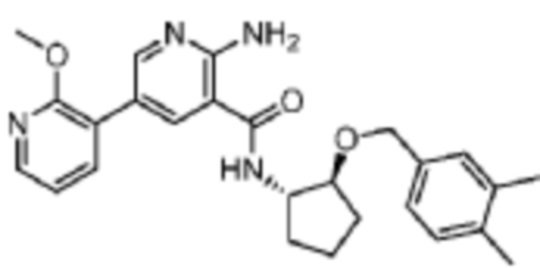
[1567] MS (ESI, масса/заряд): 447,2 [M+H]+
[1568] Пример 295. 2-амино-5-(4-(диметиламино)фенил)-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)никотинамид
[1569] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (4-(диметиламино)фенил)бороновую кислоту, названное соединение получали, как описано для примера 253.
[1570] 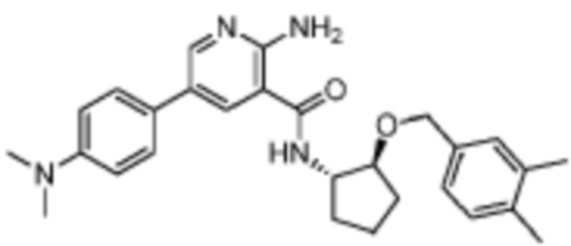
[1571] MS (ESI, масса/заряд): 459,3 [M+H]+
[1572] Пример 296. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(3-гидроксифенил)никотинамид
[1573] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (3-гидроксифенил)бороновую кислоту, названное соединение получали, как описано для примера 253.
[1574] 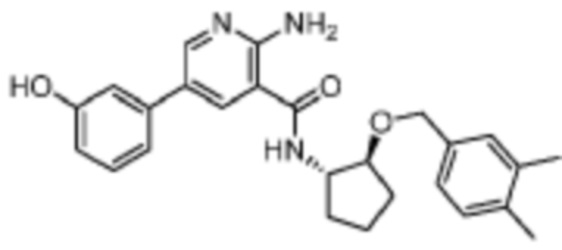
[1575] MS (ESI, масса/заряд): 432,2 [M+H]+
[1576] Пример 297. 2-амино-5-(3-аминофенил)-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)никотинамид
[1577] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (3-аминофенил)бороновую кислоту, названное соединение получали, как описано для примера 253.
[1578] 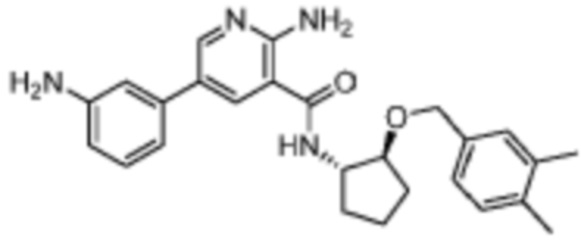
[1579] MS (ESI, масса/заряд): 431,2 [M+H]+
[1580] Пример 298. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(3-(метилсульфонамидо)фенил)никотинамид
[1581] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (3-(метилсульфонамидо)фенил)бороновую кислоту, названное соединение получали, как описано для примера 253.
[1582] 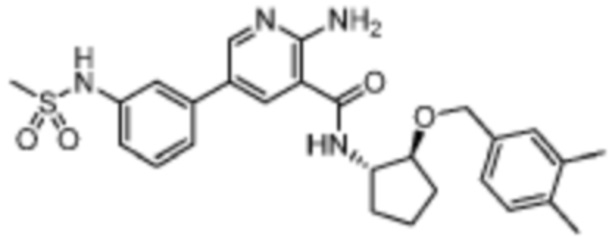
[1583] MS (ESI, масса/заряд): 509,2 [M+H]+
[1584] Пример 299. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(3-(гидроксиметил)фенил)никотинамид
[1585] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (3-(гидроксиметил)фенил)бороновую кислоту, названное соединение получали, как описано для примера 253.
[1586] 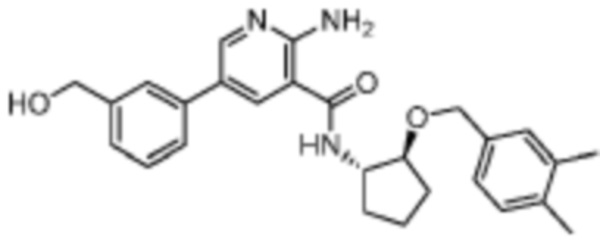
[1587] MS (ESI, масса/заряд): 446,2 [M+H]+
[1588] Пример 300. 2-амино-5-(3-(аминометил)фенил)-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)никотинамид
[1589] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (3-(аминометил)фенил)бороновую кислоту, названное соединение получали, как описано для примера 253.
[1590] 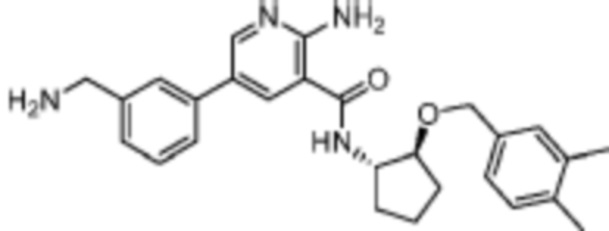
[1591] MS (ESI, масса/заряд): 445,3 [M+H]+
[1592] Пример 301. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(3-(3-гидроксипропил)фенил)никотинамид
[1593] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (3-(3-гидроксипропил)фенил)бороновую кислоту, названное соединение получали, как описано для примера 253.
[1594] 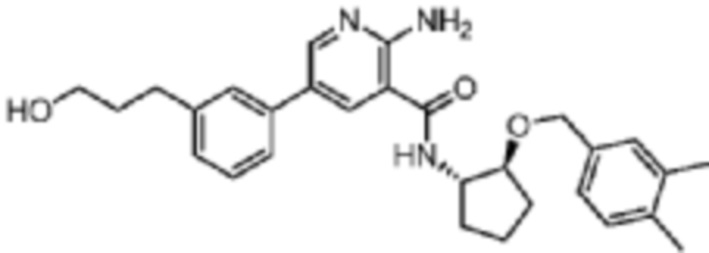
[1595] MS (ESI, масса/заряд): 474,3 [M+H]+
[1596] Пример 302. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(3-((((1r,4S)-4-гидроксициклогексил)амино)метил)фенил)никотинамид
[1597] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (1r,4r)-4-((3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)амино)циклогексан-1-ол, названное соединение получали, как описано для примера 253
[1598] 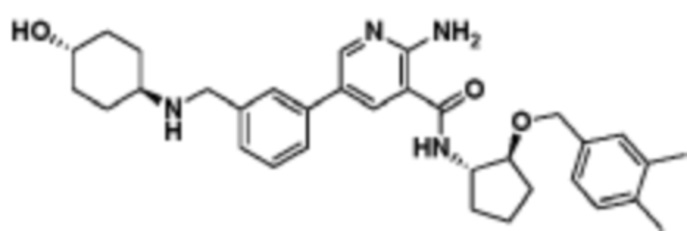
[1599] MS (ESI, масса/заряд): 543,3 [M+H]+
[1600] Пример 303. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(3-(((1-метилпиперидин-4-ил)амино)метил)фенил)никотинамид
[1601] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и 1-метил-N-(3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)пиперидин-4-амин, названное соединение получали, как описано для примера 253.
[1602] 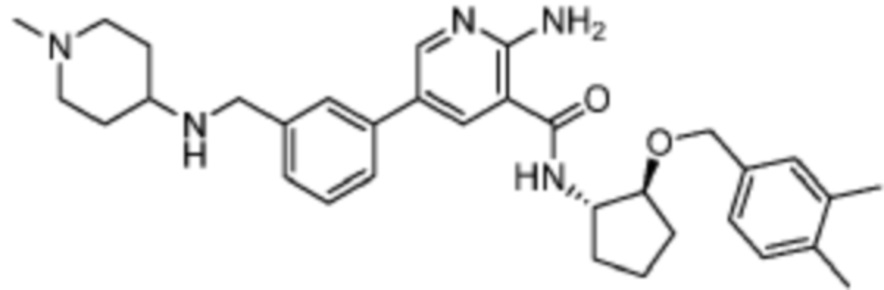
[1603] MS (ESI, масса/заряд): 542,3 [M+H]+
[1604] Пример 304. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(3-((((S)-пиперидин-3-ил)амино)метил)фенил)никотинамид
[1605] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (S)-N-(3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)пиперидин-3-амин, названное соединение получали, как описано для примера 253.
[1606] 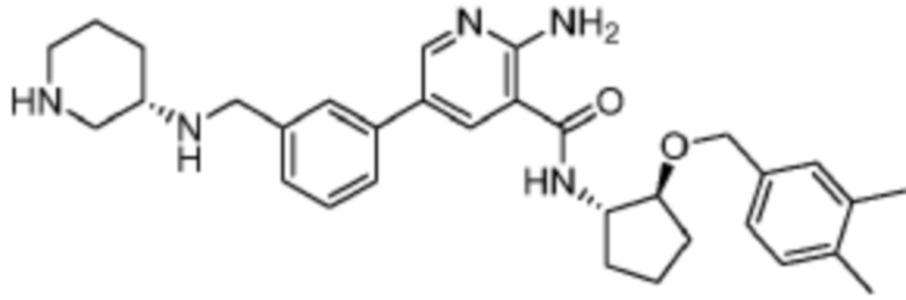
[1607] MS (ESI, масса/заряд): 528,3 [M+H]+
[1608] Пример 305. 3-(6-амино-5-(((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)карбамоил)пиридин-3-ил)-5-гидроксибензойная кислота
[1609] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и 3-бор-5-гидроксибензойную кислоту, названное соединение получали, как описано для примера 253.
[1610] 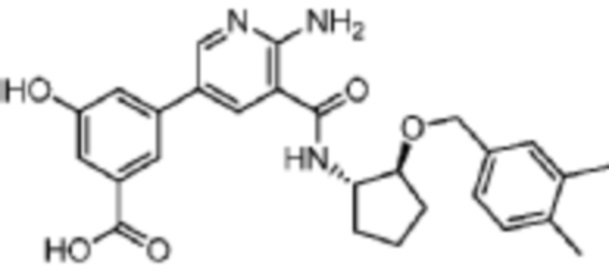
[1611] MS (ESI, масса/заряд): 476,2 [M+H]+
[1612] Пример 306. 4-(6-амино-5-(((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)карбамоил)пиридин-3-ил)-2-метилбензойная кислота
[1613] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и 4-бор-2-метилбензойную кислоту, названное соединение получали, как описано для примера 253.
[1614] 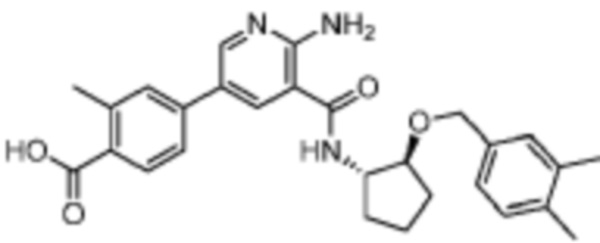
[1615] MS (ESI, масса/заряд): 474,2 [M+H]+
[1616] Пример 307. 2-амино-5-(4-аминофенил)-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)никотинамид
[1617] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (4-аминофенил)бороновую кислоту, названное соединение получали, как описано для примера 253.
[1618] 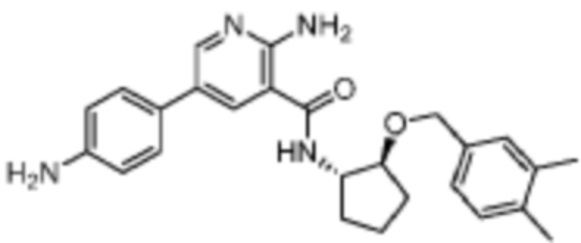
[1619] MS (ESI, масса/заряд): 431,2 [M+H]+
[1620] Пример 308. 3-(6-амино-5-(((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)карбамоил)пиридин-3-ил)бензойная кислота
[1621] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и 3-борбензойную кислоту, названное соединение получали, как описано для примера 253.
[1622] 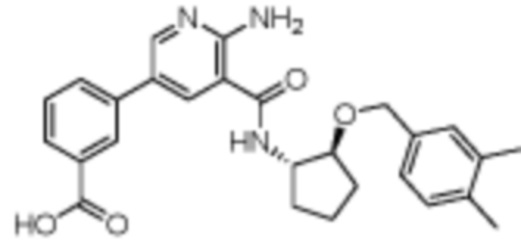
[1623] MS (ESI, масса/заряд): 460,2 [M+H]+
[1624] Пример 309. 3-амино-5-(6-амино-5-(((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)карбамоил)пиридин-3-ил)бензойная кислота
[1625] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и 3-амино-5-борбензойную кислоту, названное соединение получали, как описано для примера 253.
[1626] 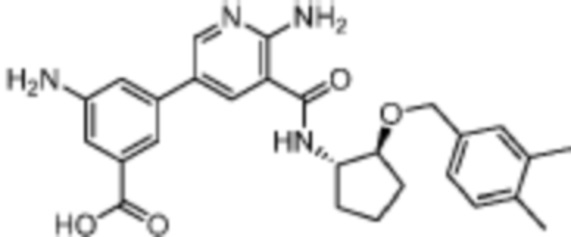
[1627] MS (ESI, масса/заряд): 475,2 [M+H]+
[1628] Пример 310. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(2-метил-5-(4-(пирролидин-1-ил)пиперидин-1-карбонил)фенил)никотинамид
[1629] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (4-метил-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил)(4-(пирролидин-1-ил)пиперидин-1-ил)метанон, названное соединение получали, как описано для примера 253.
[1630] 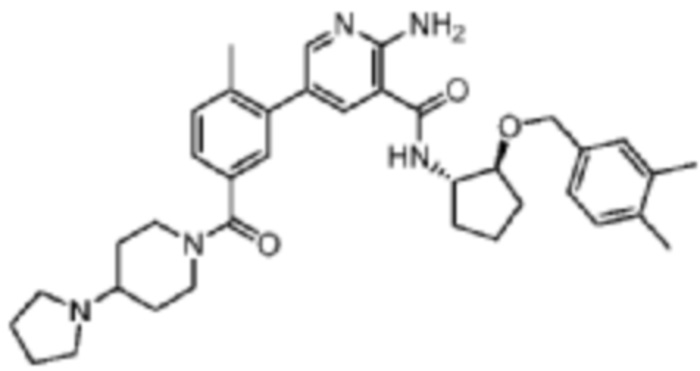
[1631] MS (ESI, масса/заряд): 610,4 [M+H]+
[1632] Пример 311. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(3-метил-4-(4-метилпиперазин-1-карбонил)фенил)никотинамид
[1633] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (2-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил)(4-метилпиперазин-1-ил)метанон, названное соединение получали, как описано для примера 253.
[1634] 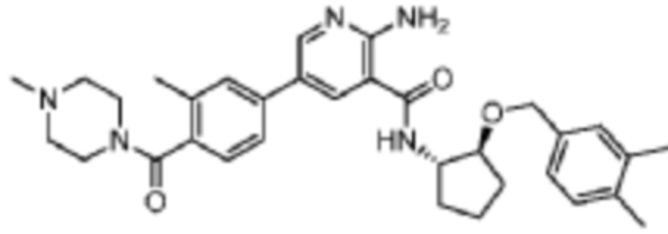
[1635] MS (ESI, масса/заряд): 556,3 [M+H]+
[1636] Пример 312. 2-амино-5-(3-амино-5-(4-(пирролидин-1-ил)пиперидин-1-карбонил)фенил)-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)никотинамид
[1637] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (3-амино-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил)(4-(пирролидин-1-ил)пиперидин-1-ил)метанон, названное соединение получали, как описано для примера 253.
[1638] 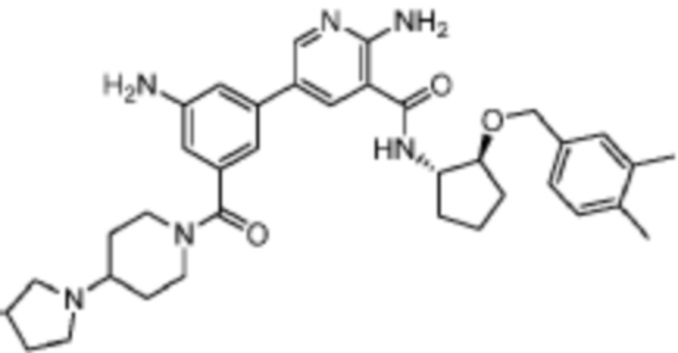
[1639] MS (ESI, масса/заряд): 611,4 [M+H]+
[1640] Пример 313. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(4-(гидроксиметил)фенил)никотинамид
[1641] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (4-(гидроксиметил)фенил)бороновую кислоту, названное соединение получали, как описано для примера 253.
[1642] 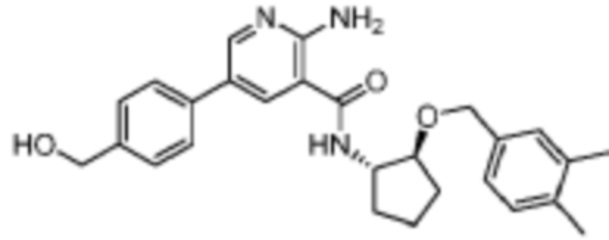
[1643] MS (ESI, масса/заряд): 446,2 [M+H]+
[1644] Пример 314. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(4-формилфенил)никотинамид
[1645] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (4-формилфенил)бороновую кислоту, названное соединение получали, как описано для примера 253.
[1646] 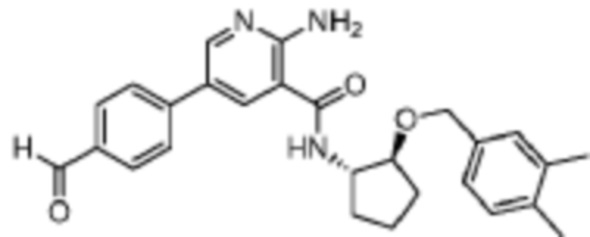
[1647] MS (ESI, масса/заряд): 444,2 [M+H]+
[1648] Пример 315. 4-(6-амино-5-(((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)карбамоил)пиридин-3-ил)бензойная кислота
[1649] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и 4-борбензойную кислоту, названное соединение получали, как описано для примера 253.
[1650] 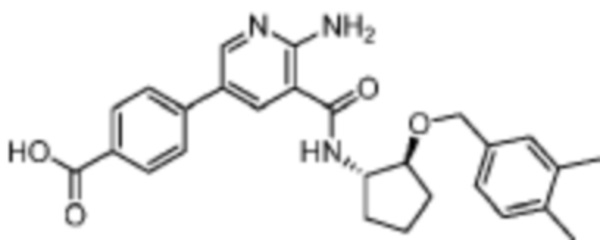
[1651] MS (ESI, масса/заряд): 460,2 [M+H]+
[1652] Пример 316. 3-(4-(6-амино-5-(((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)карбамоил)пиридин-3-ил)фенил)пропановая кислота
[1653] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и 3-(4-борфенил)пропановую кислоту, названное соединение получали, как описано для примера 253.
[1654] 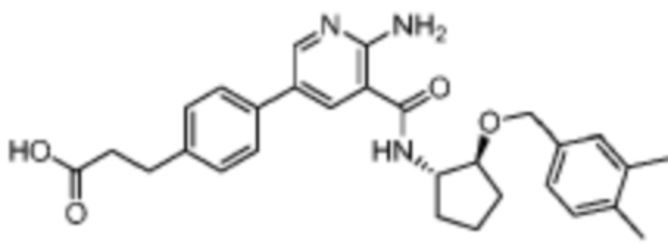
[1655] MS (ESI, масса/заряд): 488,3 [M+H]+
[1656] Пример 317. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(2-гидроксифенил)никотинамид
[1657] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (2-гидроксифенил)бороновую кислоту, названное соединение получали, как описано для примера 253.
[1658] 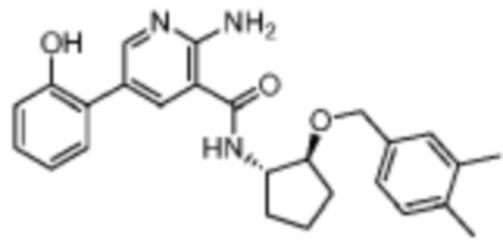
[1659] MS (ESI, масса/заряд): 432,22 [M+H]+
[1660] Пример 318. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(4-((1-метилпиперидин-4-ил)карбамоил)фенил)никотинамид
[1661] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и N-(1-метилпиперидин-4-ил)-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензамид, названное соединение получали, как описано для примера 253.
[1662] 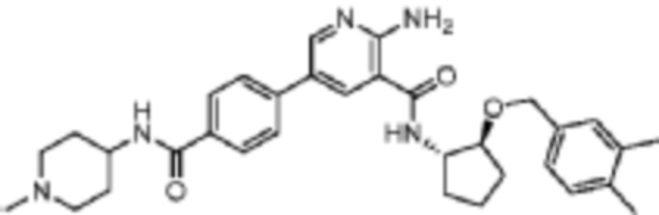
[1663] MS (ESI, масса/заряд): 556,3 [M+H]+
[1664] Пример 319. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(4-(диметилкарбамоил)фенил)никотинамид
[1665] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (4-(диметилкарбамоил)фенил)бороновую кислоту, названное соединение получали, как описано для примера 253.
[1666] 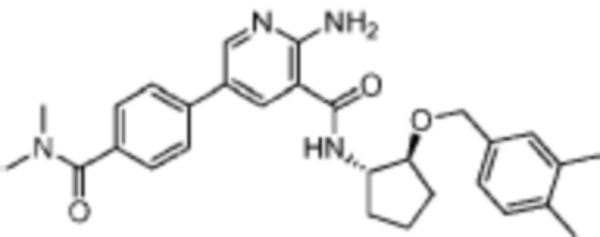
[1667] MS (ESI, масса/заряд): 487,3 [M+H]+
[1668] Пример 320. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(4-(((1-метилпиперидин-4-ил)амино)метил)фенил)никотинамид
[1669] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и 1-метил-N-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)пиперидин-4-амин, названное соединение получали, как описано для примера 253.
[1670] 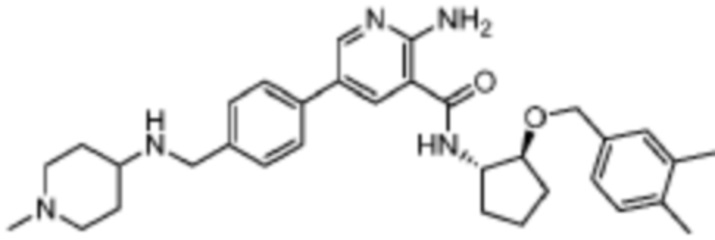
[1671] MS (ESI, масса/заряд): 542,3 [M+H]+
[1672] Пример 321. 6-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-6'-(гидроксиметил)-[3,3'-бипиридин]-5-карбоксамид
[1673] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (6-(гидроксиметил)пиридин-3-ил)бороновую кислоту, названное соединение получали, как описано для примера 253.
[1674] 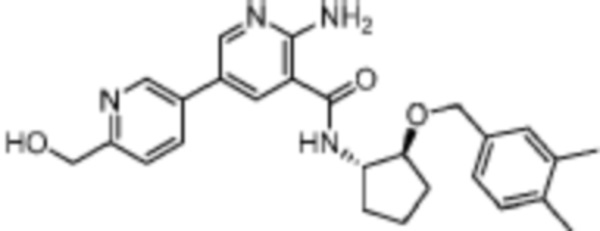
[1675] MS (ESI, масса/заряд): 447,2 [M+H]+
[1676] Пример 322. 2-амино-4-(6-амино-5-(((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)карбамоил)пиридин-3-ил)бензойная кислота
[1677] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и 2-амино-4-борбензойную кислоту, названное соединение получали, как описано для примера 253.
[1678] 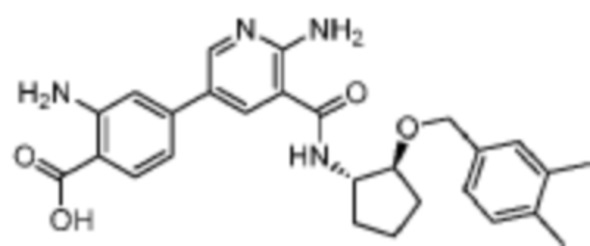
[1679] MS (ESI, масса/заряд): 475,2 [M+H]+
[1680] Пример 323. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(4-(гидроксиметил)-3-метоксифенил)никотинамид
[1681] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (2-метокси-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил)метанол, названное соединение получали, как описано для примера 253.
[1682] 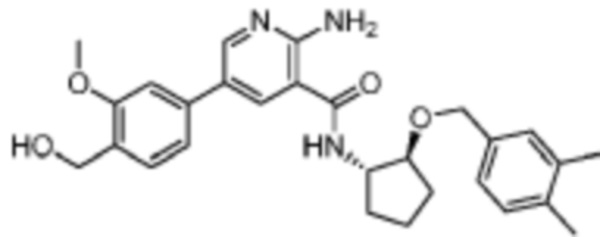
[1683] MS (ESI, масса/заряд): 476,3 [M+H]+
[1684] Пример 324. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(3-фтор-4-(гидроксиметил)фенил)никотинамид
[1685] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (3-фтор-4-(гидроксиметил)фенил)бороновую кислоту, названное соединение получали, как описано для примера 253.
[1686] 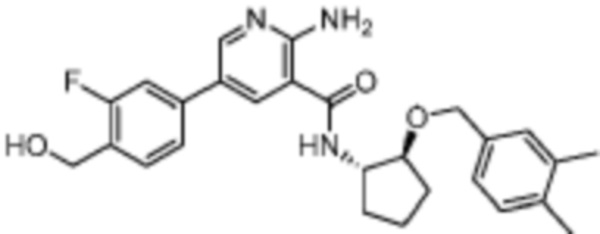
[1687] MS (ESI, масса/заряд): 464,2 [M+H]+
[1688] Пример 325. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(3-фтор-4-((4-(пирролидин-1-ил)пиперидин-1-ил)метил)фенил)никотинамид
[1689] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и 1-(2-фтор-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)-4-(пирролидин-1-ил)пиперидин, названное соединение получали, как описано для примера 253.
[1690] 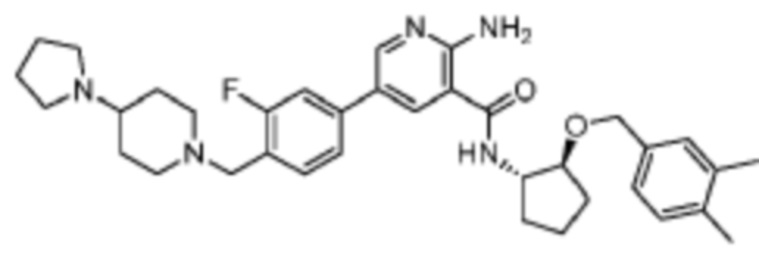
[1691] MS (ESI, масса/заряд): 600,4 [M+H]+
[1692] Пример 326. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(4-(1-гидроксиэтил)фенил)никотинамид
[1693] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (4-(1-гидроксиэтил)фенил)бороновую кислоту, названное соединение получали, как описано для примера 253.
[1694] 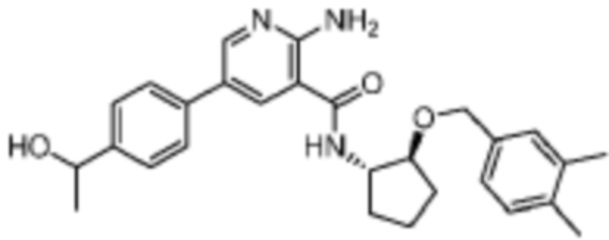
[1695] MS (ESI, масса/заряд): 460,3 [M+H]+
[1696] Пример 327. 2-амино-5-(4-((3-(диметиламино)пирролидин-1-ил)метил)фенил)-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)никотинамид
[1697] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и N,N-диметил-1-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)пирролидин-3-амин, названное соединение получали, как описано для примера 253.
[1698] 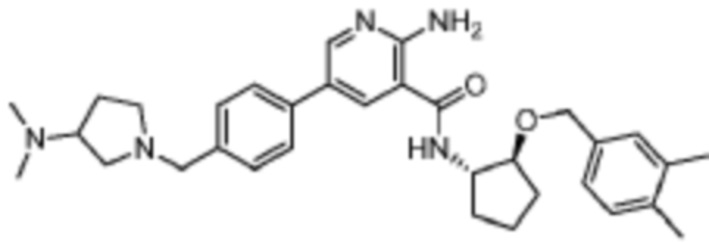
[1699] MS (ESI, масса/заряд): 542,3 [M+H]+
[1700] Пример 328. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(4-((4-гидроксипиперидин-1-ил)метил)фенил)никотинамид
[1701] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и 1-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)пиперидин-4-ол, названное соединение получали, как описано для примера 253.
[1702] 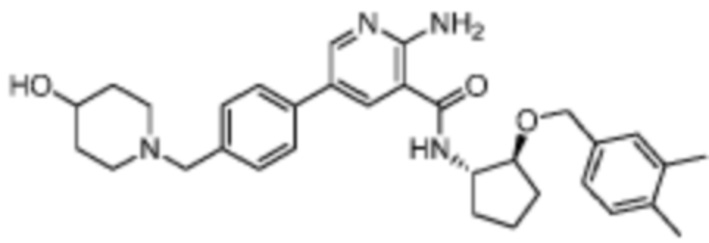
[1703] MS (ESI, масса/заряд): 529,3 [M+H]+
[1704] Пример 329. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(4-((((1-метилпиперидин-4-ил)метил)амино)метил)фенил)никотинамид
[1705] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и 1-(1-метилпиперидин-4-ил)-N-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)метанамин, названное соединение получали, как описано для примера 253.
[1706] 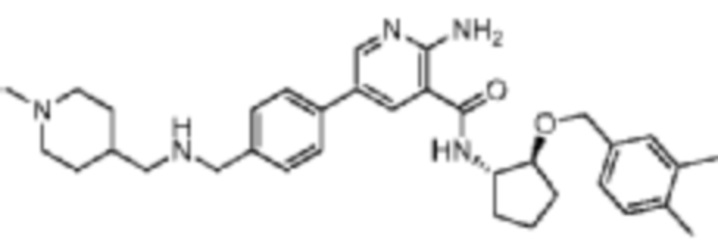
[1707] MS (ESI, масса/заряд): 556,4 [M+H]+
[1708] Пример 330. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(3-метил-4-(4-(пирролидин-1-ил)пиперидин-1-карбонил)фенил)никотинамид
[1709] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (2-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил)(4-(пирролидин-1-ил)пиперидин-1-ил)метанон, названное соединение получали, как описано для примера 253.
[1710] 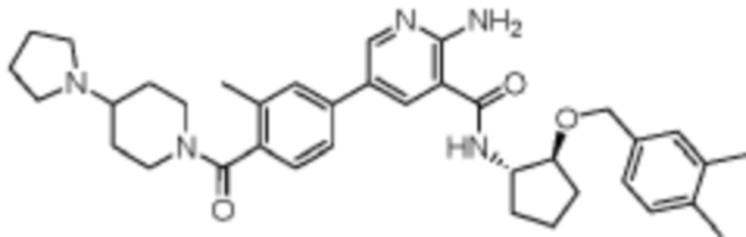
[1711] MS (ESI, масса/заряд): 610,4 [M+H]+
[1712] Пример 331. 2-амино-5-(3-амино-4-(4-(пирролидин-1-ил)пиперидин-1-карбонил)фенил)-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)никотинамид
[1713] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (2-амино-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил)(4-(пирролидин-1-ил)пиперидин-1-ил)метанон, названное соединение получали, как описано для примера 253.
[1714] 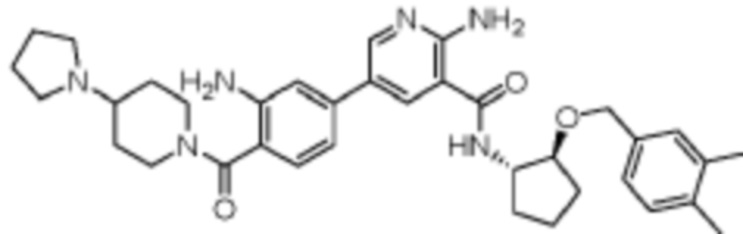
[1715] MS (ESI, масса/заряд): 611,4 [M+H]+
[1716] Пример 332. 2-амино-5-(3-амино-4-((4-(пирролидин-1-ил)пиперидин-1-ил)метил)фенил)-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)никотинамид
[1717] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и 2-((4-(пирролидин-1-ил)пиперидин-1-ил)метил)-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)анилин, названное соединение получали, как описано для примера 253.
[1718] 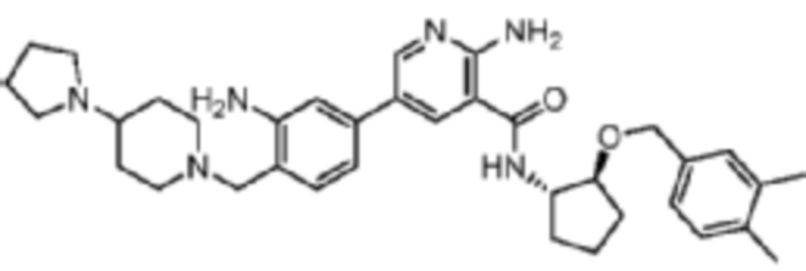
[1719] MS (ESI, масса/заряд): 597,4 [M+H]+
[1720] Пример 333. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(4-(гидроксиметил)-3-метилфенил)никотинамид
[1721] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (2-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил)метанол, названное соединение получали, как описано для примера 253.
[1722] 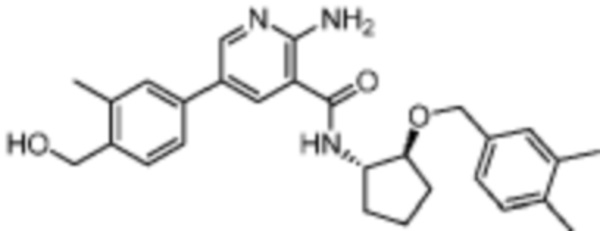
[1723] MS (ESI, масса/заряд): 460,3 [M+H]+
[1724] Пример 334. 2-амино-5-(3-хлорфенил)-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)никотинамид
[1725] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (3-хлорфенил)бороновую кислоту, названное соединение получали, как описано для примера 253.
[1726] 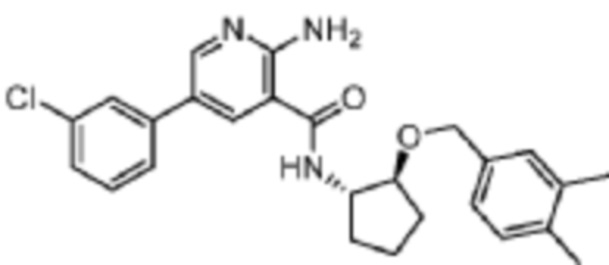
[1727] MS (ESI, масса/заряд): 450 [M+H]+
[1728] Пример 335. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(м-толил)никотинамид
[1729] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и м-толилбороновую кислоту, названное соединение получали, как описано для примера 253.
[1730] 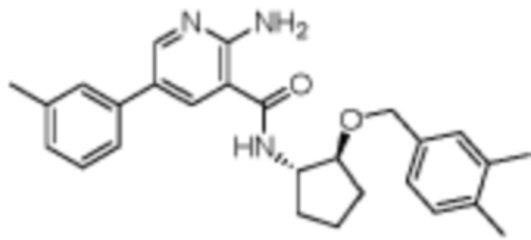
[1731] MS (ESI, масса/заряд): 430,2 [M+H]+
[1732] Пример 336. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(3,5-диметилфенил)никотинамид
[1733] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (3,5-диметилфенил)бороновую кислоту, названное соединение получали, как описано для примера 253.
[1734] 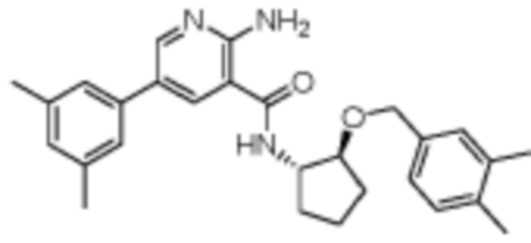
[1735] MS (ESI, масса/заряд): 444,3 [M+H]+
[1736] Пример 337. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(4-((3-морфолинопирролидин-1-ил)метил)фенил)никотинамид
[1737] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и 4-(1-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)пирролидин-3-ил)морфолин, названное соединение получали, как описано для примера 253.
[1738] 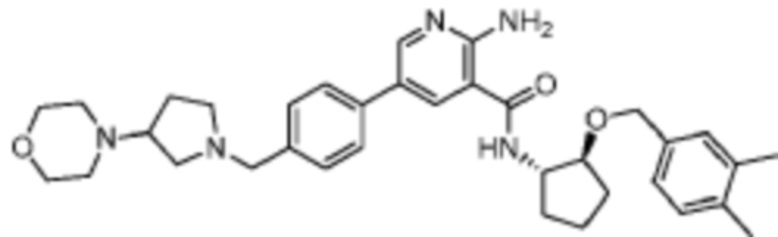
[1739] MS (ESI, масса/заряд): 584,4 [M+H]+
[1740] Пример 338. 2-амино-5-(4-((4-аминопиперидин-1-ил)метил)фенил)-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)никотинамид
[1741] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и 1-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)пиперидин-4-амин, названное соединение получали, как описано для примера 253.
[1742] 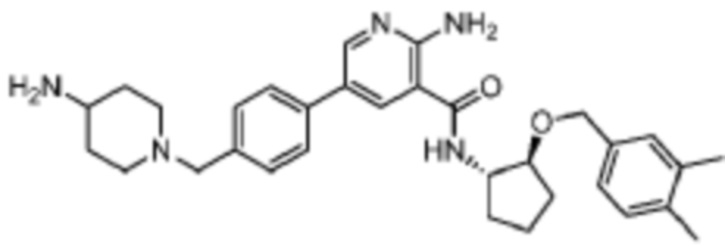
[1743] MS (ESI, масса/заряд): 528,3 [M+H]+
[1744] Пример 339. 2-амино-5-(4-((3-аминопиперидин-1-ил)метил)фенил)-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)никотинамид
[1745] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и 1-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)пиперидин-3-амин, названное соединение получали, как описано для примера 253.
[1746] 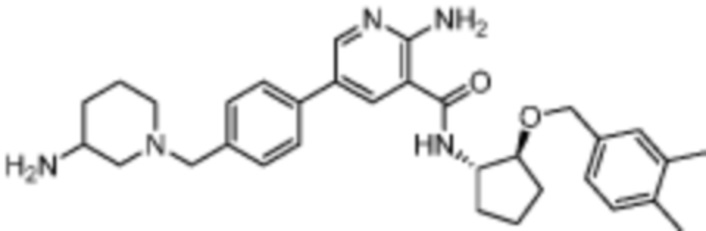
[1747] MS (ESI, масса/заряд): 528,3 [M+H]+
[1748] Пример 340. 2-амино-5-(4-((3-аминопирролидин-1-ил)метил)фенил)-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)никотинамид
[1749] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и 1-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)пирролидин-3-амин, названное соединение получали, как описано для примера 253.
[1750] 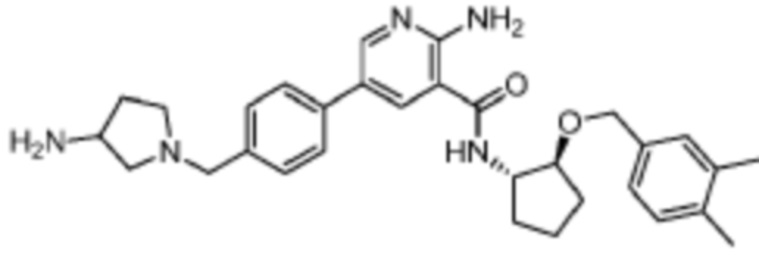
[1751] MS (ESI, масса/заряд): 514,3 [M+H]+
[1752] Пример 341. 2-амино-5-(4-((3-аминопирролидин-1-ил)метил)-3-фторфенил)-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)никотинамид
[1753] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и 1-(2-фтор-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)пирролидин-3-амин, названное соединение получали, как описано для примера 253.
[1754] 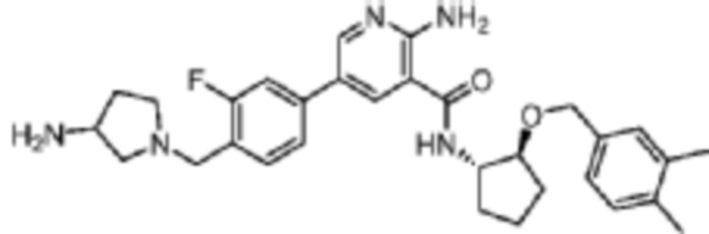
[1755] MS (ESI, масса/заряд): 532,3 [M+H]+
[1756] Пример 342. 2-амино-5-(4-((3-аминопирролидин-1-ил)метил)-3,5-дифторфенил)-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)никотинамид
[1757] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и 1-(2,6-дифтор-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)пирролидин-3-амин, названное соединение получали, как описано для примера 253.
[1758] 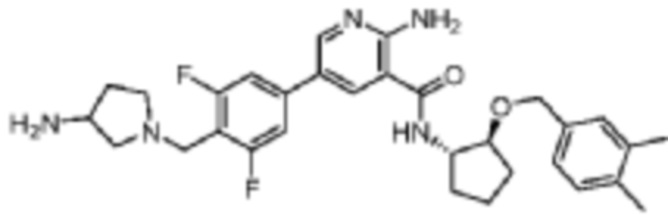
[1759] MS (ESI, масса/заряд): 550,3 [M+H]+
[1760] Пример 343. 2-амино-5-(3-((3-(диметиламино)пирролидин-1-ил)метил)фенил)-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)никотинамид
[1761] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и N,N-диметил-1-(3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)пирролидин-3-амин, названное соединение получали, как описано для примера 253.
[1762] 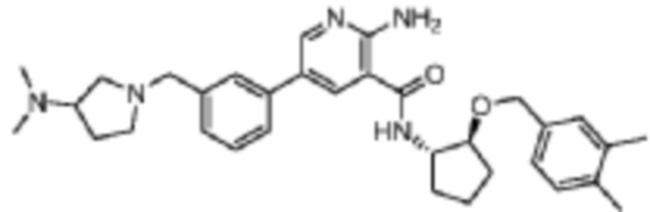
[1763] MS (ESI, масса/заряд): 542,3 [M+H]+
[1764] Пример 344. 2-амино-5-(3-((3-(диметиламино)пирролидин-1-ил)метил)-4-метоксифенил)-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)никотинамид
[1765] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и 1-(2-метокси-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)-N,N-диметилпирролидин-3-амин, названное соединение получали, как описано для примера 253.
[1766] 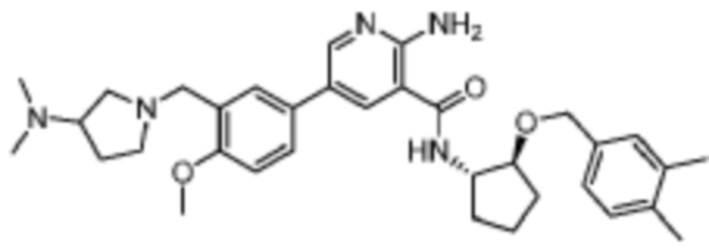
[1767] MS (ESI, масса/заряд): 572,4 [M+H]+
[1768] Пример 345. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(4-((3-гидроксиазетидин-1-ил)метил)фенил)никотинамид
[1769] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и 1-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)азетидин-3-ол, названное соединение получали, как описано для примера 253.
[1770] 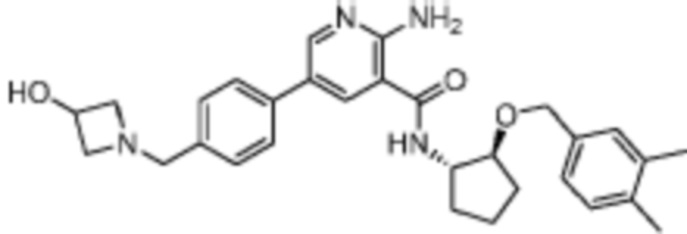
[1771] MS (ESI, масса/заряд): 501,3 [M+H]+
[1772] Пример 346. 2-амино-5-(4-(((R)-3-(диметиламино)пирролидин-1-ил)метил)фенил)-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)никотинамид
[1773] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (R)-N,N-диметил-1-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)пирролидин-3-амин, названное соединение получали, как описано для примера 253.
[1774] 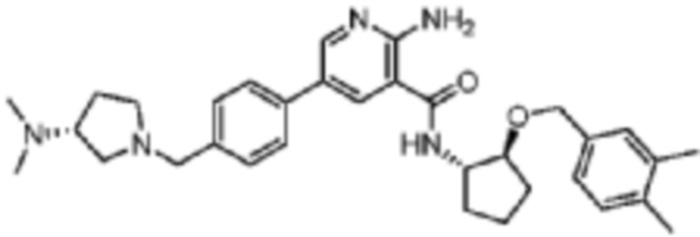
[1775] MS (ESI, масса/заряд): 542,3 [M+H]+
[1776] Пример 347. 2-амино-5-(4-(((S)-3-(диметиламино)пирролидин-1-ил)метил)фенил)-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)никотинамид
[1777] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (S)-N,N-диметил-1-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)пирролидин-3-амин, названное соединение получали, как описано для примера 253.
[1778] 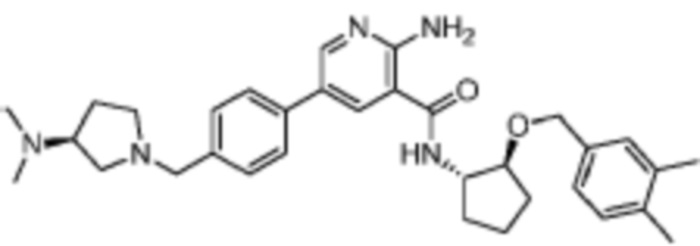
[1779] MS (ESI, масса/заряд): 542,3 [M+H]+
[1780] Пример 348. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(4-(((R)-3-гидроксипирролидин-1-ил)метил)фенил)никотинамид
[1781] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (R)-1-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)пирролидин-3-ол, названное соединение получали, как описано для примера 253.
[1782] 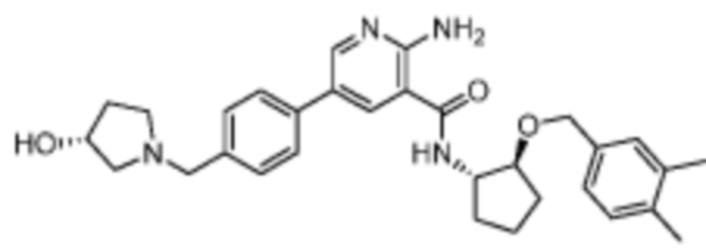
[1783] MS (ESI, масса/заряд): 515,3 [M+H]+
[1784] Пример 349. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(4-(((S)-3-гидроксипирролидин-1-ил)метил)фенил)никотинамид
[1785] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (S)-1-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)пирролидин-3-ол, названное соединение получали, как описано для примера 253.
[1786] 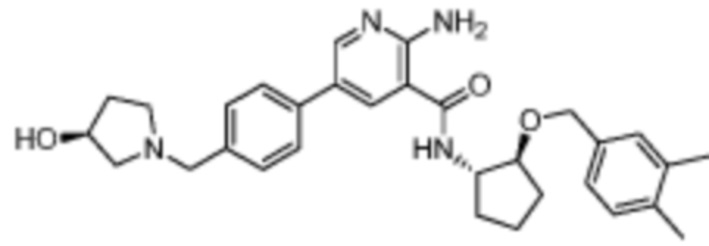
[1787] MS (ESI, масса/заряд): 515,3 [M+H]+
[1788] Пример 350. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(4-((3-гидроксипиперидин-1-ил)метил)фенил)никотинамид
[1789] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и 1-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)пиперидин-3-ол, названное соединение получали, как описано для примера 253.
[1790] 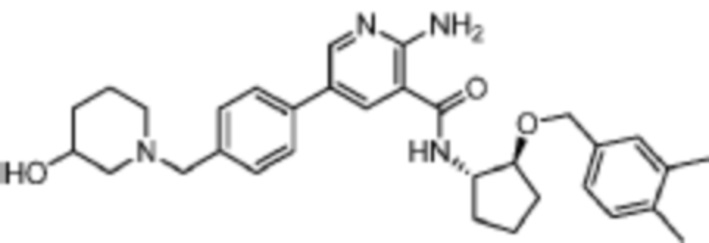
[1791] MS (ESI, масса/заряд): 529,3 [M+H]+
[1792] Пример 351. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(4-гидроксифенил)никотинамид
[1793] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (4-гидроксифенил)бороновую кислоту, названное соединение получали, как описано для примера 253.
[1794] 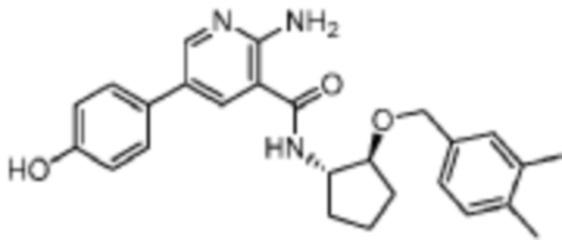
[1795] MS (ESI, масса/заряд): 432,2 [M+H]+
[1796] Пример 352. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(4-гидрокси-3-метоксифенил)никотинамид
[1797] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (4-гидрокси-3-метоксифенил)бороновую кислоту, названное соединение получали, как описано для примера 253.
[1798] 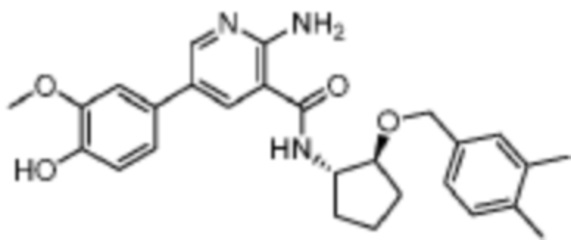
[1799] MS (ESI, масса/заряд): 462,23 [M+H]+
[1800] Пример 353. 2-амино-5-(3,4-диметоксифенил)-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)никотинамид
[1801] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и (3,4-диметоксифенил)бороновую кислоту, названное соединение получали, как описано для примера 253.
[1802] 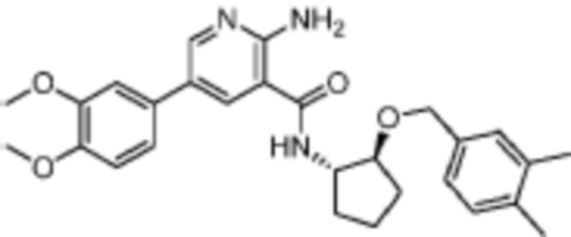
[1803] MS (ESI, масса/заряд): 476,3 [M+H]+
[1804] Пример 354. 2-амино-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)-5-(3-(пирролидин-1-ил)фенил)никотинамид
[1805] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и пинаколиновый сложный эфир (3-(пирролидин-1-ил)фенил)бороновой кислоты, названное соединение получали, как описано для примера 253.
[1806] 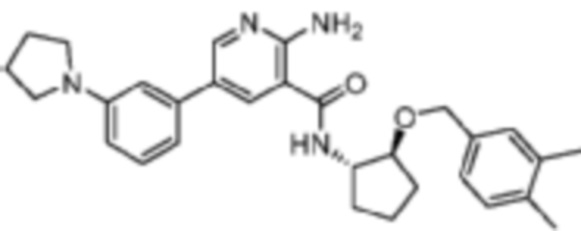
[1807] MS (ESI, масса/заряд): 485,3 [M+H]+
[1808] Пример 355. 2-амино-5-(5-амино-1-метил-1H-пиразол-4-ил)-N-((1S,2S)-2-((3,4-диметилбензил)окси)циклопентил)никотинамид
[1809] Используя (1S,2S)-2-((3,4-диметилбензил)окси)циклопентан-1-амин и 1-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1H-пиразол-5-амин, названное соединение получали, как описано для примера 253.
[1810] 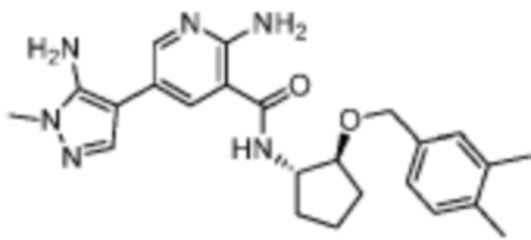
[1811] MS (ESI, масса/заряд): 435,2 [M+H]+
[1812] Пример 356. 2-амино-N-((1S,2S)-2-((3-этил-4-метилбензил)окси)циклопентил)-5-(4-(гидроксиметил)фенил)никотинамид
[1813] Используя (1S,2S)-2-((3-этил-4-метилбензил)окси)циклопентан-1-амин и (4-(гидроксиметил)фенил)бороновую кислоту, названное соединение получали, как описано для примера 253.
[1814] 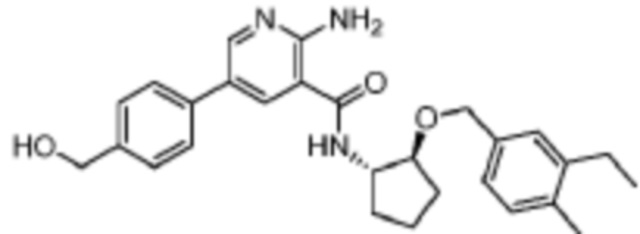
[1815] MS (ESI, масса/заряд): 460,3 [M+H]+
[1816] Пример 357. 2-амино-5-(4-((3-(диметиламино)пирролидин-1-ил)метил)фенил)-N-((1S,2S)-2-((3-этил-4-метилбензил)окси)циклопентил)никотинамид
[1817] Используя (1S,2S)-2-((3-этил-4-метилбензил)окси)циклопентан-1-амин и N,N-диметил-1-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)пирролидин-3-амин, названное соединение получали, как описано для примера 253.
[1818] 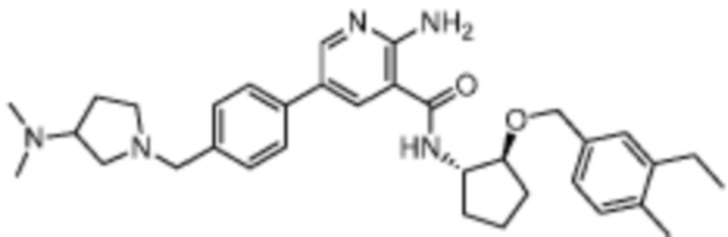
[1819] MS (ESI, масса/заряд): 556,4 [M+H]+
[1820] Пример 358. 2-амино-N-((1S,2S)-2-((3-этил-4-метилбензил)окси)циклопентил)-5-(4-((3-гидроксипирролидин-1-ил)метил)фенил)никотинамид
[1821] Используя (1S,2S)-2-((3-этил-4-метилбензил)окси)циклопентан-1-амин и 1-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)пирролидин-3-ол, названное соединение получали, как описано для примера 253.
[1822] 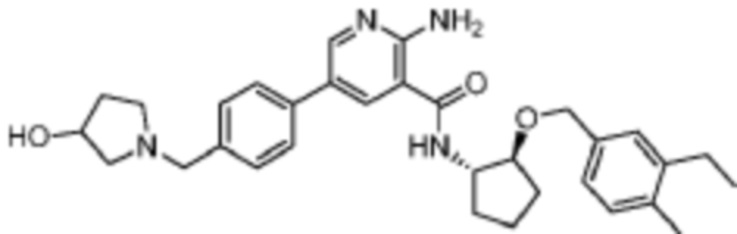
[1823] MS (ESI, масса/заряд): 529,3 [M+H]+
[1824] Пример 359. 2-амино-N-((1S,2S)-2-((3-этил-4-метилбензил)окси)циклопентил)-5-(4-(2-(пиперазин-1-ил)пропан-2-ил)фенил)никотинамид
[1825] Используя (1S,2S)-2-((3-этил-4-метилбензил)окси)циклопентан-1-амин и 1-(2-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил)пропан-2-ил)пиперазин, названное соединение получали, как описано для примера 253.
[1826] 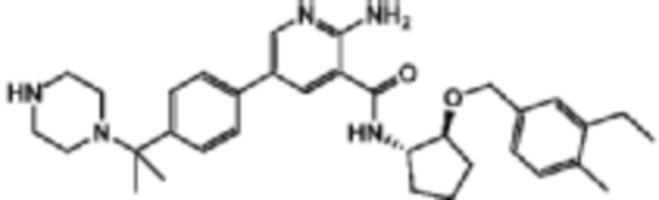
[1827] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,11 (t, J=7,63 Гц, 3 H) 1,50 (s, 6 H) 1,58-1,67 (m, 1 H) 1,70-1,88 (m, 3 H) 1,98-2,06 (m, 1 H) 2,10-2,17 (m, 1H) 2,17 (s, 3 H) 2,49-2,57 (q, J=7,63 Гц, 2 H) 2,84 (br s, 4 H) 3,24 (t, J=4,70 Гц, 4 H) 3,91-4,00 (m, 1 H) 4,40 (br d, J=4,70 Гц, 1 H) 4,49-4,61 (m, 2 H) 6,98-7,05 (m, 2 H) 7,09 (s, 1 H) 7,64-7,80 (m, 4 H) 8,31 (d, J=2,35 Гц, 1 H) 8,57 (d, J=1,96 Гц, 1 H);
[1828] MS (ESI, масса/заряд): 556,4 [M+H]+
[1829] Пример 360. 2-амино-N-((1S,2S)-2-((3-этил-4-метилбензил)окси)циклопентил)-5-(4-(2-(4-(2-гидроксиэтил)пиперазин-1-ил)пропан-2-ил)фенил)никотинамид
[1830] Используя (1S,2S)-2-((3-этил-4-метилбензил)окси)циклопентан-1-амин и 2-(4-(2-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил)пропан-2-ил)пиперазин-1-ил)этан-1-ол, названное соединение получали, как описано для примера 253.
[1831] 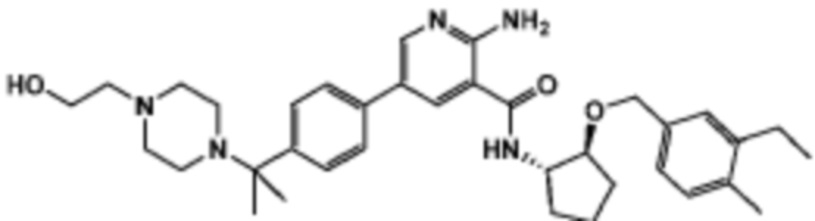
[1832] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,11 (t, J=7,43 Гц, 3 H) 1,57 (s, 3 H) 1,61-1,64 (m, 1H) 1,64 (s, 3 H) 1,69-1,89 (m, 3 H) 2,01 (br dd, J=13,11, 6,06 Гц, 1 H) 2,10-2,29 (m, 4 H) 2,53 (q, J=7,56 Гц, 2 H) 2,88-3,13 (m, 4 H) 3,22-3,28 (m, 1 H) 3,33-3,39 (m, 2 H) 3,43 (br s, 2 H) 3,83-3,90 (m, 1 H) 3,92-4,00 (m, 1 H) 4,35-4,45 (m, 1 H) 4,47-4,62 (m, 2 H) 6,95-7,07 (m, 2 H) 7,09 (s, 1 H) 7,65-7,84 (m, 4 H) 8,29-8,36 (m, 1 H) 8,56-8,64 (m, 1 H);
[1833] MS (ESI, масса/заряд): 600,3 [M+H]+
[1834] Пример 361. 3-амино-N-((1S,2S)-2-(бензилокси)циклопентил)-6-(1-(пиперидин-4-ил)-1H-пиразол-4-ил)пиразин-2-карбоксамид
[1835] Используя 3-амино-N-((1S,2S)-2-(бензилокси)циклопентил)-6-бромпиразин-2-карбоксамид и пинаколиновый сложный эфир (1-(пиперидин-4-ил)-1H-пиразол-4-ил)бороновой кислоты, названное соединение получали, как описано для примера 253.
[1836] 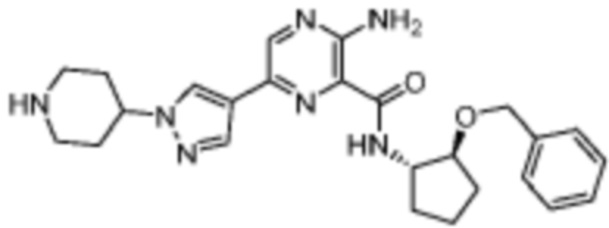
[1837] MS (ESI, масса/заряд): 462,3 [M+H]+
[1838] Пример 362. (S)-3-амино-6-(1-(пиперидин-4-ил)-1H-пиразол-4-ил)-N-(1,2,3,4-тетрагидронафталин-1-ил)пиразин-2-карбоксамид
[1839] Используя (S)-3-амино-6-бром-N-(1,2,3,4-тетрагидронафталин-1-ил)пиразин-2-карбоксамид и пинаколиновый сложный эфир (1-(пиперидин-4-ил)-1H-пиразол-4-ил)бороновой кислоты, названное соединение получали, как описано для примера 253.
[1840] 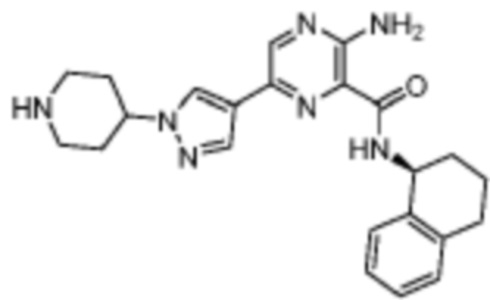
[1841] MS (ESI, масса/заряд): 418,2 [M+H]+
[1842] Пример 363. 2-амино-5-(4-фторфенил)-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1843] Схема получения соединения из примера 363:
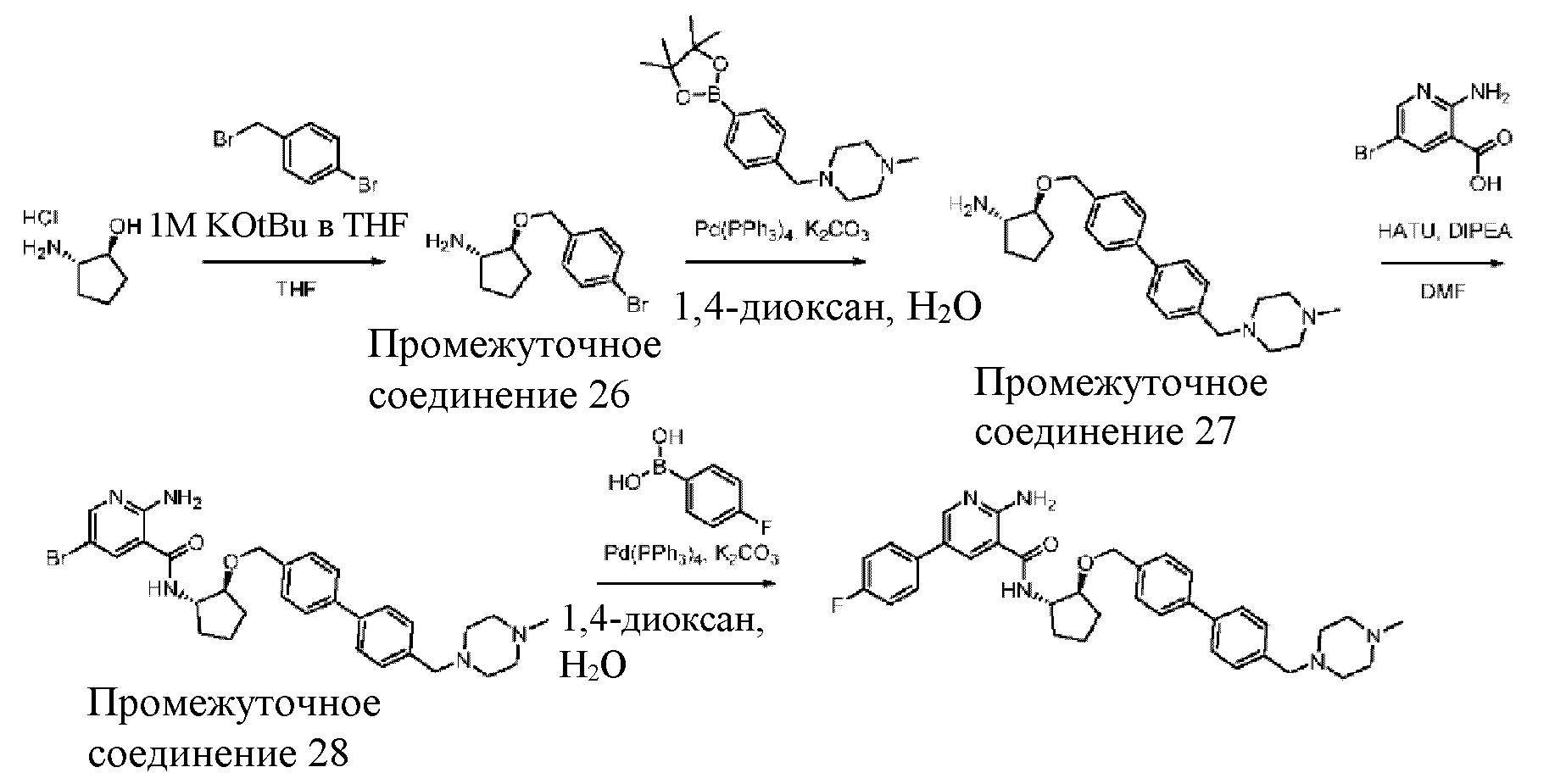
[1844]
[1845] Промежуточное соединение 26.
[1846] В раствор гидрохлорида транс-(1S,2S)-2-аминоциклопентанола (8,0 ммоль) в DMF (5 мл) добавляли 1M трет-бутоксид калия в THF (20 мл) при комнатной температуре. Смесь оставляли перемешиваться в течение 30 мин. После обеспечения перемешивания в течение 30 мин. в смесь добавляли 4-бромбензилбромид (9,6 ммоль), а затем оставляли перемешиваться в течение дополнительных 2 ч при комнатной температуре. Затем реакционную смесь гасили водой и экстрагировали при помощи EtOAc. Отделенный органический слой сушили над MgSO4, фильтровали и концентрировали in vacuo. Концентрированный остаток использовали на следующей стадии без дополнительной очистки.
[1847] 1H-ЯМР (600 MГц, CDCl3) δ ppm 1,29-1,35 (m, 1 H) 1,57-1,65 (m, 1 H) 1,65-1,77 (m, 2 H) 1,96 (br dd, J=12,62, 6,75 Гц, 2 H) 3,20-3,27 (m, 1 H) 3,51 (br d, J=5,28 Гц, 1 H) 4,40-4,46 (m, 1 H) 4,46-4,54 (m, 1 H) 7,21 (br t, J=7,63 Гц, 2 H) 7,40-7,48 (m, 2 H);
[1848] MS (ESI+) масса/заряд 270 [M+H]+
[1849] Промежуточное соединение 27.
[1850] В раствор промежуточного соединения 26 (0,851 ммоль) в 1,4-диоксане (4 мл) и воде (1 мл) добавляли 1-метил-4-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил)пиперазин (0,851 ммоль), тетракис(трифенилфосфин)палладий (0) (0,0851 ммоль) и карбонат калия (0,851 ммоль). Смесь нагревали до 100°C и оставляли перемешиваться на протяжении ночи. После охлаждения до комнатной температуры реакционную смесь разбавляли водой (10 мл) и экстрагировали при помощи этилацетата (10 мл). Отделенный органический слой сушили над MgSO4, фильтровали и концентрировали in vacuo. Концентрированный остаток очищали колоночной флэш-хроматографией с получением требуемого соединения (265 мг, 0,7 ммоль).
[1851] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,36-1,45 (m, 1 H) 1,63-1,78 (m, 3 H) 1,97-2,07 (m, 2 H) 2,26 (s, 3 H) 2,30-2,71 (br s, 8 H) 3,24 (td, J=7,48, 4,99 Гц, 1 H) 3,55 (s, 2 H) 3,67-3,74 (m, 1 H) 4,53 (d, J=11,74 Гц, 1 H) 4,60 (d, J=11,74 Гц, 1 H) 7,38 (d, J=8,22 Гц, 2 H) 7,42 (d, J=8,22 Гц, 2 H) 7,55-7,58 (m, 2 H) 7,58-7,61 (m, 2 H);
[1852] MS (ESI+) масса/заряд 380 [M+H]+
[1853] Промежуточное соединение 28.
[1854] В раствор промежуточного соединения 27 (0,685 ммоль) и 2-амино-5-бромникотиновой кислоты (0,685 ммоль) в N,N-диметилформамиде (5 мл) добавляли диизопропилэтиламин (3,425 ммоль) и HATU (1,027 ммоль) при комнатной температуре. Реакционную смесь оставляли перемешиваться на протяжении ночи, концентрировали in vacuo, разбавляли при помощи EtOAc и промывали солевым раствором. Отделенный органический слой сушили над MgSO4, фильтровали и концентрировали in vacuo. Концентрированный остаток очищали колоночной флэш-хроматографией с получением требуемого соединения (0,653 ммоль) в виде бледно-желтого масла.
[1855] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,49-1,57 (m, 1 H) 1,68-1,78 (m, 3 H) 1,95-2,01 (m, 1 H) 2,07-2,13 (m, 1 H) 2,41 (s, 3 H) 2,49-2,79 (br s, 8 H) 3,56 (s, 2 H) 3,91 (dt, J=6,90, 4,48 Гц, 1 H) 4,34 (td, J=7,48, 4,40 Гц, 1 H) 4,57-4,65 (m, 2 H) 7,35 (br d, J=8,22 Гц, 2 H) 7,37 (br d, J=8,22 Гц, 2 H) 7,52 (d, J=7,63 Гц, 4 H) 7,90 (d, J=2,35 Гц, 1 H) 8,04 (d, J=2,35 Гц, 1 H);
[1856] MS (ESI+) масса/заряд 579 [M+H]+
[1857] Пример 363. 2-амино-5-(4-фторфенил)-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1858] В раствор промежуточного соединения 28 (0,076 ммоль) в 1,4-диоксане (4 мл) и воде (1 мл) добавляли (4-фторфенил)бороновую кислоту (0,076 ммоль), тетракис(трифенилфосфин)палладий (0) (0,0076 ммоль) и карбонат калия (0,076 ммоль). Смесь нагревали до 100°C и оставляли перемешиваться на протяжении ночи. После охлаждения до комнатной температуры реакционную смесь разбавляли водой (10 мл) и экстрагировали при помощи этилацетата (10 мл). Отделенный органический слой сушили над MgSO4, фильтровали и концентрировали in vacuo. Концентрированный остаток очищали препаративной HPLC с получением соединения из примера 363.
[1859] 1H-ЯМР (400 MГц, CD3OD) δ 8,57 (s, 1H), 8,23 (s, 1H), 7,64-7,47 (m, 8H), 7,42 (d, 2H), 7,17 (t, 2H), 4,66 (qd, 2H), 4,45-4,39 (m, 1H), 4,25 (s, 1H), 4,09-3,90 (m, 1H), 3,62 (s, 1H), 3,53 (br s, 2H), 3,39 (br s, 2H), 2,94 (s, 3H), 2,19-2,12 (m, 1H), 2,05-1,97 (m, 1H), 1,83-1,75 (m, 3H), 1,66-1,57 (m, 1H);
[1860] MS (ESI+) масса/заряд 594 [M+H]+
[1861] Пример 364. 2-амино-5-(3,4-дифторфенил)-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1862] Используя 3,4-дифторфенилбороновую кислоту, названное соединение получали, как описано для примера 363.
[1863] 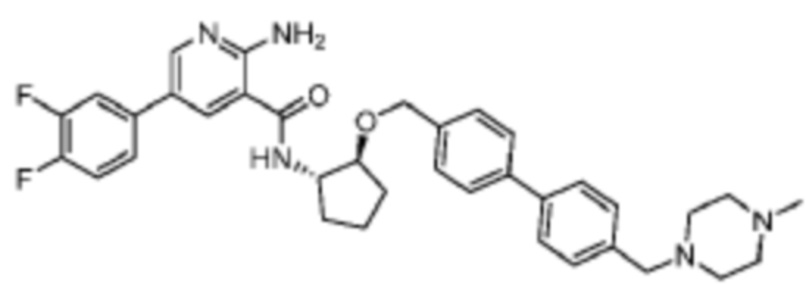
[1864] 1H-ЯМР (400 MГц, CD3OD) δ 8,54 (s, 1H), 8,26 (s, 1H), 7,71-7,52 (m, 8H), 7,42-7,33 (m, 3H), 4,65 (qd, 2H), 4,41 (m, 1H), 4,32 (s, 2H), 3,98 (m, 1H), 3,57 (br s, 2H), 3,48 (br s, 2H), 2,94 (s, 3H), 2,18-2,05 (m, 1H), 2,04-1,99 (m, 1H), 1,81-1,73 (m, 3H), 1,66-1,59 (m, 1H);
[1865] MS (ESI+) масса/заряд 612 [M+H]+
[1866] Пример 365. 2-амино-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(4-(трифторметил)фенил)никотинамид
[1867] Используя 4-трифторметилфенилбороновую кислоту, названное соединение получали, как описано для примера 363.
[1868] 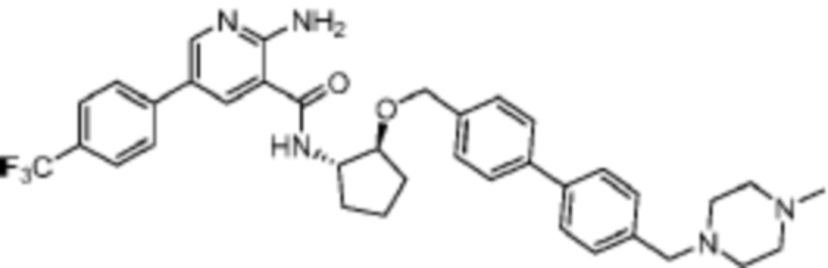
[1869] 1H-ЯМР (400 MГц, CD3OD) δ 8,65 (s, 1H), 8,36 (s, 1H), 7,83 (d, J=8,0 Гц, 2H), 7,75 (d, J=12,0 Гц, 2H), 7,62 (d, J=8,0 Гц, 2H), 7,54-7,50 (m, 4H), 7,42 (d, J=8,0 Гц, 2H), 4,69-4,62 (qd, 2H), 4,44-4,39 (m, 1H), 4,27 (s, 2H), 4,02-4,00 (m, 1H), 3,54 (br s, 2H), 3,42 (br s, 2H), 2,94 (s, 3H), 2,21-2,05 (m, 1H), 2,05-1,97 (m, 1H), 1,87-1,76 (m, 3H), 1,68-1,59 (m, 1H);
[1870] MS (ESI+) масса/заряд 644 [M+H]+
[1871] Пример 366. 2-амино-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-(1-метилпиперидин-4-ил)-1H-пиразол-4-ил)никотинамид
[1872] Используя 1-метил-4-[4-(тетраметил-1,3,2-диоксаборолан-2-ил)-1H-пиразол-1-ил]пиперидин, названное соединение получали, как описано для примера 363.
[1873] 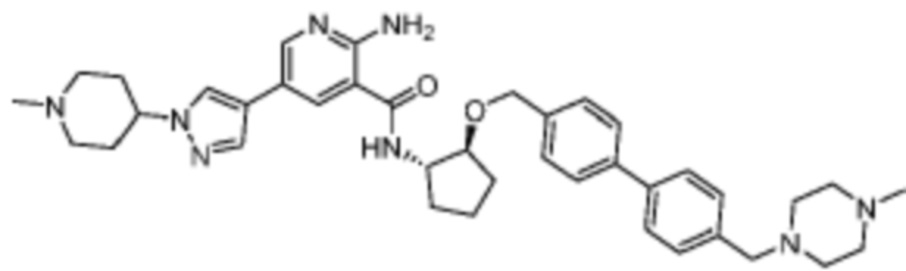
[1874] 1H-ЯМР (400 MГц, CD3OD) δ 8,57 (s, 1H), 8,21 (s, 1H), 8,15 (s, 1H), 7,92 (s, 1H), 7,63 (d, J=8,0 Гц, 2H), 7,57-7,50 (m, 4H), 7,42 (d, J=8,0 Гц, 2H), 4,66 (s, 2H), 4,59-4,53 (m, 1H), 4,43-4,38 (m, 1H), 4,25 (s, 2H), 4,12-4,01 (m, 2H), 3,69-3,66 (d, 2H), 3,53 (br s, 2H), 3,39 (br s, 2H), 3,25-3,20 (m, 1H), 2,93 (s, 3H), 2,92 (s, 3H), 2,41-2,33 (m, 4H), 2,19-1,97 (m, 2H), 1,84-1,76 (m, 3H), 1,69-1,60 (m, 1H);
[1875] MS (ESI+) масса/заряд 663 [M+H]+
[1876] Пример 367. 2-амино-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(4-(4-метилпиперазин-1-ил)фенил)никотинамид
[1877] Используя 4-(4-метилпиперазин-1-ил)фенилбороновую кислоту, названное соединение получали, как описано для примера 363.
[1878] 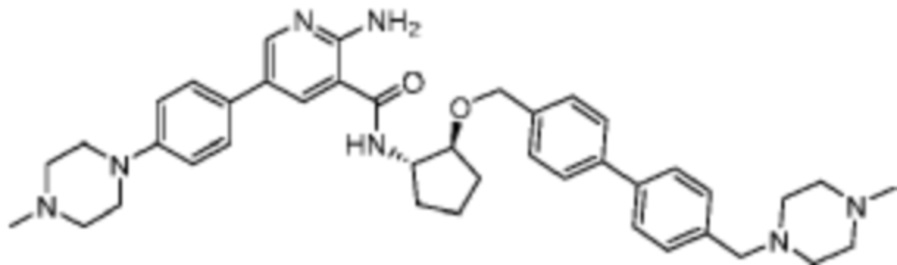
[1879] 1H-ЯМР (400 MГц, CD3OD) δ 8,59 (s, 1H), 8,18 (s, 1H), 7,64-7,50 (m, 8H), 7,43 (d, J=8,0 Гц, 2H), 7,11 (d, J=8,0 Гц, 2H), 4,66 (s, 2H), 4,43-4,39 (m, 1H), 4,25 (s, 2H), 4,03-4,00 (m, 1H), 3,92 (d, J=1,2 Гц, 2H), 3,62 (d, J=1,2 Гц, 2H), 3,52 (br s, 2H), 3,39 (br s, 2H), 3,26-3,20 (m, 2H), 3,12-3,06 (m, 2H), 2,96 (s, 3H), 2,93 (s, 3H), 2,18-2,13 (m, 1H), 2,05-1,92 (m, 1H), 1,83-1,76 (m, 3H), 1,66-1,59 (m, 1H);
[1880] MS (ESI+) масса/заряд 674 [M+H]+
[1881] Пример 368. 2-амино-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(4-((4-метилпиперазин-1-ил)метил)фенил)никотинамид
[1882] Используя 4-((4-метилпиперазин-1-ил)метил)фенилбороновую кислоту, названное соединение получали, как описано для примера 363.
[1883] 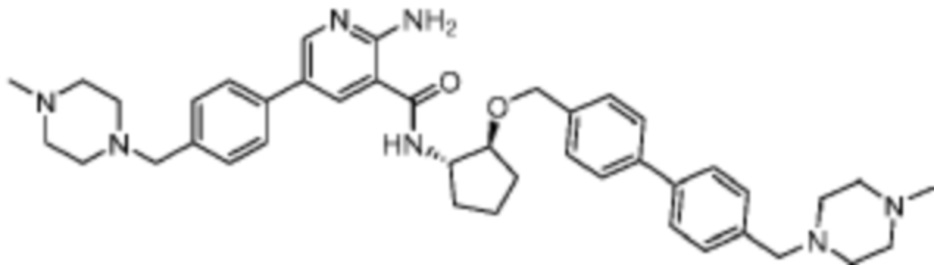
[1884] 1H-ЯМР (400 MГц, CD3OD) δ 8,66 (s, 1H), 8,29 (s, 1H), 7,73 (d, J=8,0 Гц, 2H), 7,65-7,52 (m, 8H), 7,43 (d, J=8,0 Гц, 2H), 4,66 (s, 2H), 4,42 (m, 1H), 4,31 (s, 2H), 4,21 (s, 2H), 4,02 (m, 1H), 3,53 (br, 8H), 3,46 (br, 4H), 3,29 (br, 4H), 2,94 (s, 3H), 2,93 (s, 3H), 2,23-2,10 (m, 1H), 2,04-1,98 (m, 1H), 1,88-1,75 (m, 3H), 1,67-1,60 (m, 1H);
[1885] MS (ESI+) масса/заряд 688 [M+H]+
[1886] Пример 369. 2-амино-5-(4-(гидроксиметил)фенил)-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1887] Используя 4-(гидроксиметил)фенилбороновую кислоту, названное соединение получали, как описано для примера 363.
[1888] 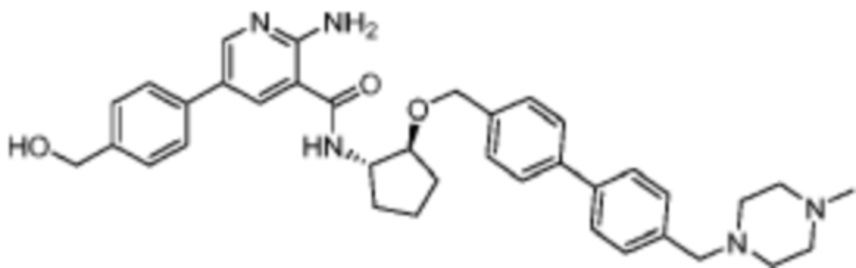
[1889] 1H-ЯМР (400 MГц, CD3OD) δ 8,63 (s, 1H), 8,26 (s, 1H), 7,70 (d, J=8,0 Гц, 1H), 7,61-7,53 (m, 5H), 7,46-7,41 (m, 6H), 4,66 (s, 2H), 4,64 (s, 2H), 4,42 (m, 1H), 3,99 (m, 1H), 3,91 (s, 2H), 3,35 (br s, 2H), 3,00 (br s, 2H), 2,88 (s, 3H), 2,22-2,10 (m, 1H), 2,04 (m, 1H), 1,85-1,74 (m, 3H), 1,63 (m, 1H);
[1890] MS (ESI+) масса/заряд 606 [M+H]+
[1891] Пример 370. 2-амино-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(м-толил)никотинамид
[1892] Используя 3-толилбороновую кислоту, названное соединение получали, как описано для примера 363.
[1893] 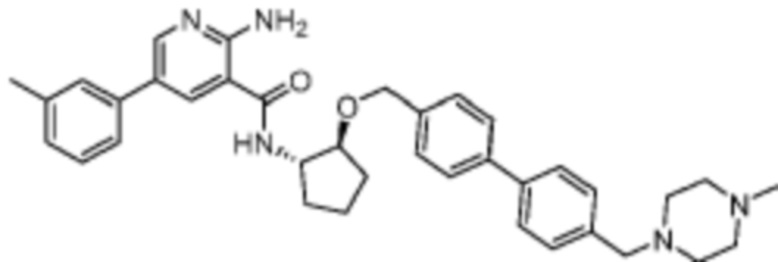
[1894] 1H-ЯМР (400 MГц, CD3OD) δ 8,62 (s, 1H), 8,23 (s, 1H), 7,72-7,32 (m, 11H), 7,24 (d, J=8,0 Гц, 1H), 4,66 (s, 2H), 4,41 (m, 1H), 4,06 (s, 2H), 4,00 (m, 1H), 3,43 (br s, 2H), 3,17 (br s, 2H), 2,90 (s, 3H), 2,39 (s, 3H), 2,18 (m, 1H), 2,04 (m, 1H), 1,89-1,75 (m, 3H), 1,65-1,60 (m, 1H);
[1895] MS (ESI+) масса/заряд 590 [M+H]+
[1896] Пример 371. 2-амино-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-фенилникотинамид
[1897] Используя фенилбороновую кислоту, названное соединение получали, как описано для примера 363.
[1898] 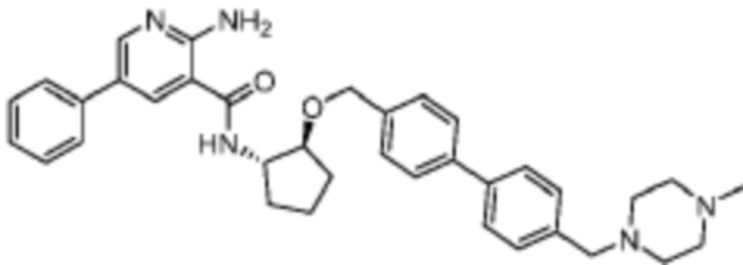
[1899] MS (ESI+) масса/заряд 576 [M+H]+
[1900] Пример 372. 2-амино-5-(4-гидроксифенил)-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1901] Используя 4-гидроксифенилбороновую кислоту, названное соединение получали, как описано для примера 363.
[1902] 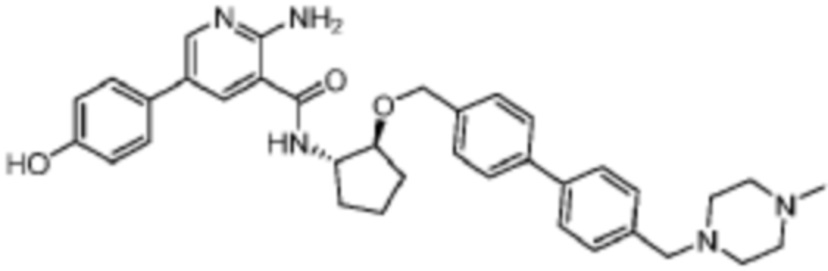
[1903] MS (ESI+) масса/заряд 592 [M+H]+
[1904] Пример 373. 2-амино-5-(4-хлор-3-фторфенил)-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1905] Используя 4-хлор-3-фторфенилбороновую кислоту, названное соединение получали, как описано для примера 363.
[1906] 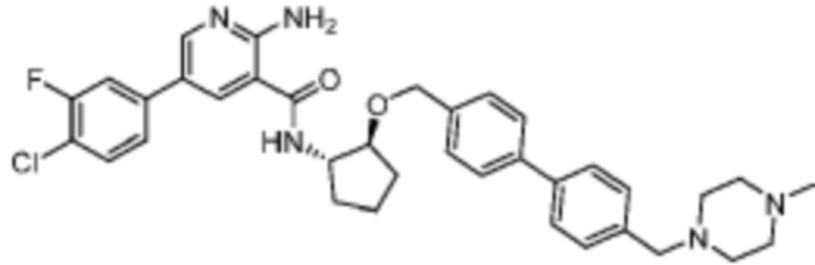
[1907] MS (ESI+) масса/заряд 629 [M+H]+
[1908] Пример 374. 2-амино-5-метил-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1909] Используя триметилбороксин, названное соединение получали, как описано для примера 363.
[1910] 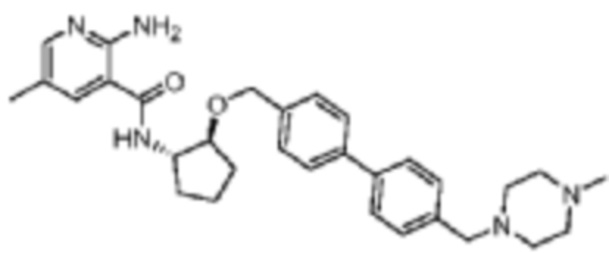
[1911] MS (ESI+) масса/заряд 514 [M+H]+
[1912] Пример 375. 6-амино-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-[3,3'-бипиридин]-5-карбоксамид
[1913] Используя 3-пиридилбороновую кислоту, названное соединение получали, как описано для примера 363.
[1914] 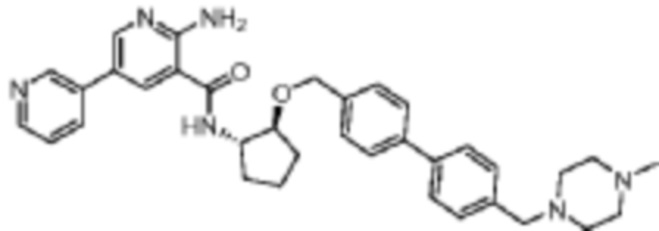
[1915] MS (ESI+) масса/заряд 577 [M+H]+
[1916] Пример 376. 2-амино-5-(4-метоксифенил)-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1917] Используя 4-метоксифенилбороновую кислоту, названное соединение получали, как описано для примера 363.
[1918] 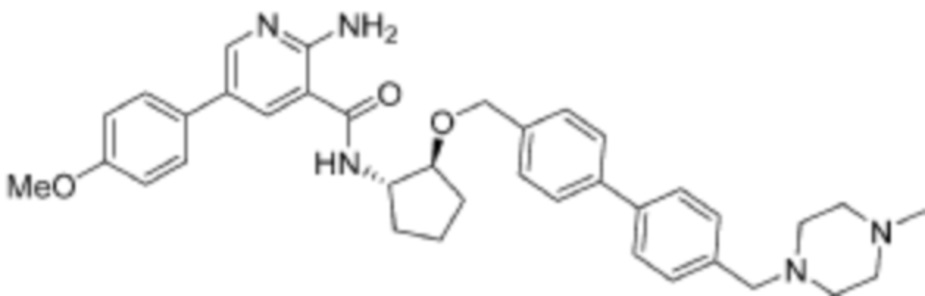
[1919] MS (ESI+) масса/заряд 606 [M+H]+
[1920] Пример 377. 6-амино-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-[3,4'-бипиридин]-5-карбоксамид
[1921] Используя 4-пиридилбороновую кислоту, названное соединение получали, как описано для примера 363.
[1922] 
[1923] MS (ESI+) масса/заряд 577 [M+H]+
[1924] Пример 378. 2-амино-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(4-((4-метилпиперидин-1-ил)метил)фенил)никотинамид
[1925] Используя (4-((4-метилпиперидин-1-ил)метил)фенил)бороновую кислоту, названное соединение получали, как описано для примера 363.
[1926] 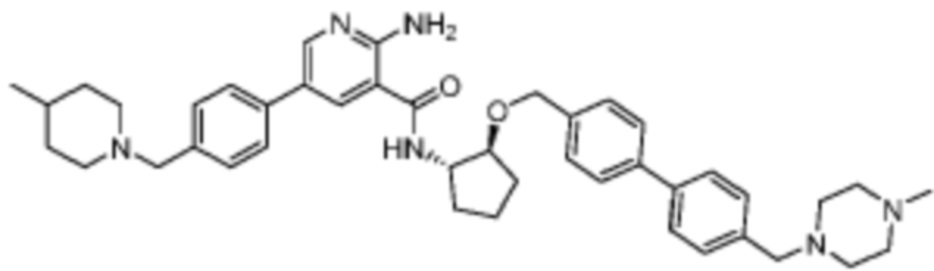
[1927] MS (ESI+) масса/заряд 687 [M+H]+
[1928] Пример 379. 2-амино-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(4-(морфолинометил)фенил)никотинамид
[1929] Используя (4-(морфолинометил)фенил)бороновую кислоту, названное соединение получали, как описано для примера 363.
[1930] 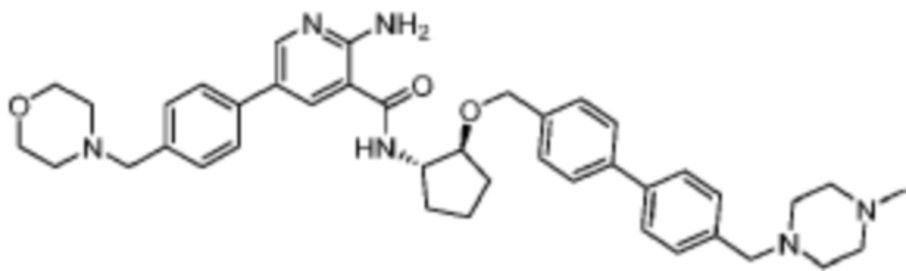
[1931] MS (ESI+) масса/заряд 675 [M+H]+
[1932] Пример 380. 2-амино-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-(тетрагидро-2H-пиран-4-ил)-1H-пиразол-4-ил)никотинамид
[1933] Используя пинаколиновый сложный эфир 1-(тетрагидропиран-4-ил)-1H-пиразол-4-бороновой кислоты, названное соединение получали, как описано для примера 363.
[1934] 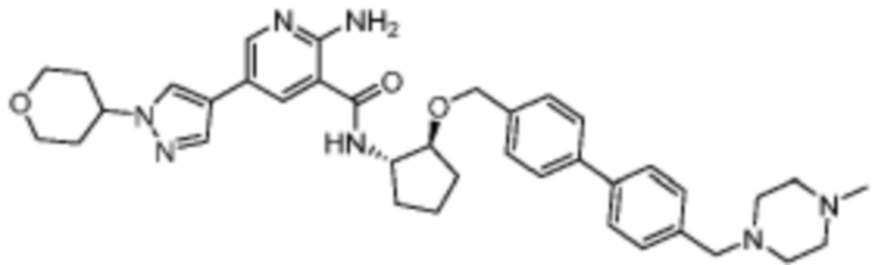
[1935] MS (ESI+) масса/заряд 650 [M+H]+
[1936] Пример 381. 2-амино-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(4-морфолинофенил)никотинамид
[1937] Используя 4-морфолинофенилбороновую кислоту, названное соединение получали, как описано для примера 363.
[1938] 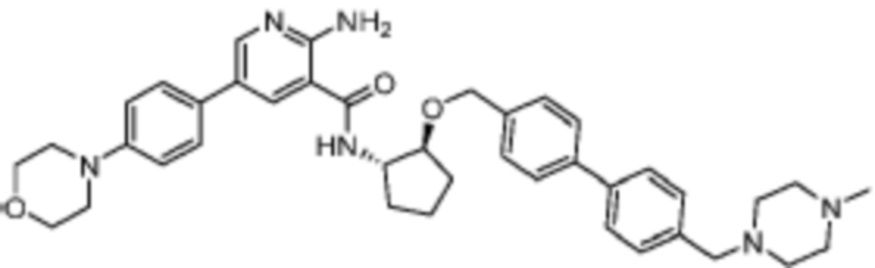
[1939] MS (ESI+) масса/заряд 661 [M+H]+
[1940] Пример 382. 2-амино-5-(циклогекс-1-ен-1-ил)-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1941] Используя 1-циклогексенилбороновую кислоту, названное соединение получали, как описано для примера 363.
[1942] 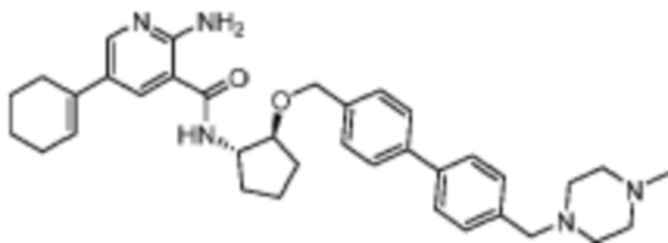
[1943] MS (ESI+) масса/заряд 580 [M+H]+
[1944] Пример 383. 2-амино-5-(3,4-диметоксифенил)-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)никотинамид
[1945] Используя 3,4-диметоксифенилбороновую кислоту, названное соединение получали, как описано для примера 363.
[1946] 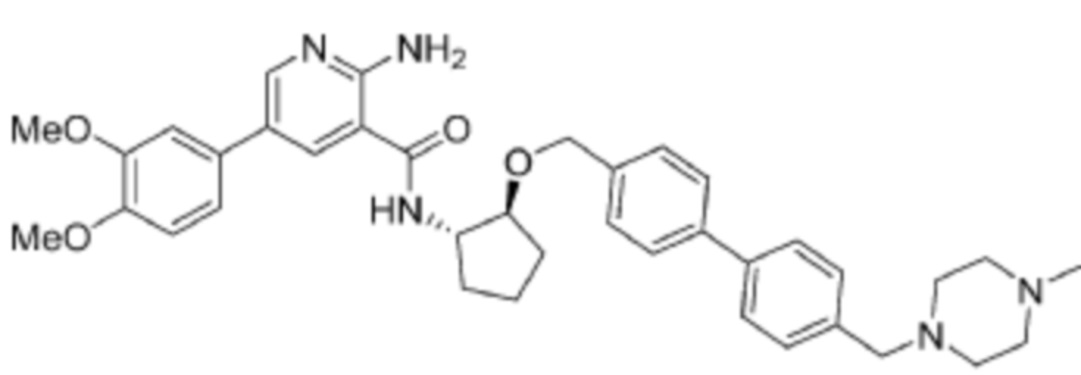
[1947] MS (ESI+) масса/заряд 636 [M+H]+
[1948] Пример 384. 6-амино-2',6'-дифтор-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-[3,4'-бипиридин]-5-карбоксамид
[1949] Используя 2,6-дифторпиридин-4-бороновую кислоту, названное соединение получали, как описано для примера 363.
[1950] 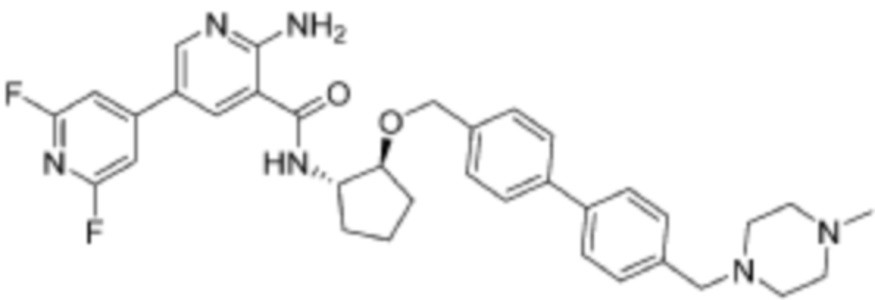
[1951] MS (ESI+) масса/заряд 613 [M+H]+
[1952] Пример 385. 2-амино-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(4-метилтиофен-3-ил)никотинамид
[1953] Используя 4-метил-3-тиенилбороновую кислоту, названное соединение получали, как описано для примера 363.
[1954] 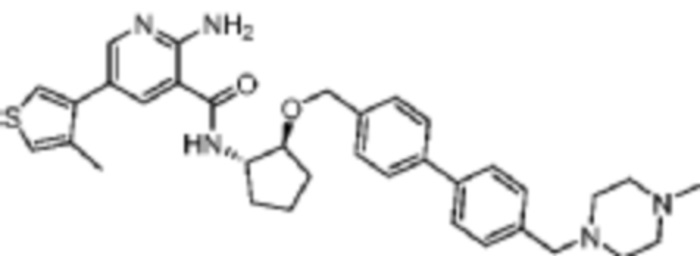
[1955] MS (ESI+) масса/заряд 596 [M+H]+
[1956] Пример 386. 6-амино-6'-фтор-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-[3,3'-бипиридин]-5-карбоксамид
[1957] Используя 6-фтор-3-пиридинилбороновую кислоту, названное соединение получали, как описано для примера 363.
[1958] 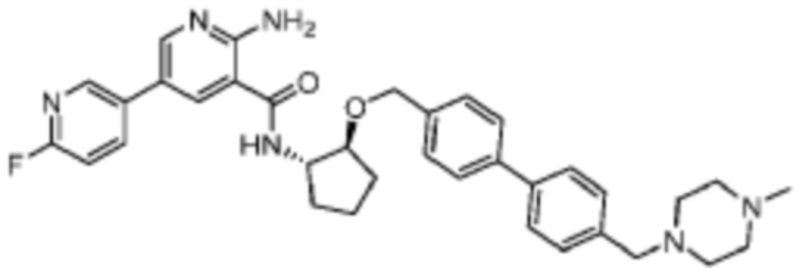
[1959] MS (ESI+) масса/заряд 595 [M+H]+
[1960] Пример 387. 2-амино-N-((1S,2S)-2-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)циклопентил)-5-(1-(1,1,2,2-тетрафторэтил)-1H-пиразол-4-ил)никотинамид
[1961] Используя (1-(1,1,2,2-тетрафторэтил)-1H-пиразол-4-ил)бороновую кислоту, названное соединение получали, как описано для примера 363.
[1962] 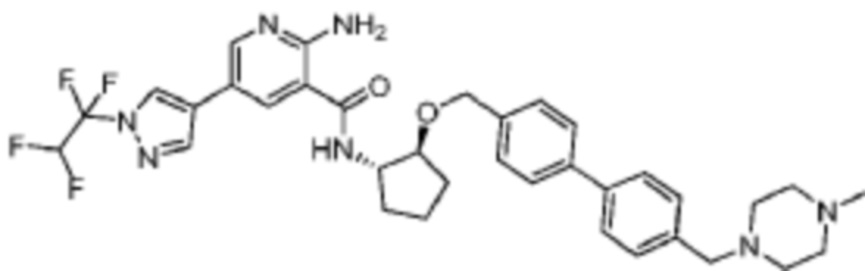
[1963] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,64 (br dd, J=14,09, 7,04 Гц, 1 H) 1,75-1,88 (m, 3 H) 2,04 (br dd, J=12,33, 7,63 Гц, 1 H) 2,15-2,23 (m, 1 H) 2,87 (s, 3 H) 2,90-3,06 (m, 4 H) 3,33 (br s, 4 H) 3,86 (s, 2 H) 3,98-4,04 (m, 1 H) 4,39-4,44 (m, 1 H) 4,62-4,69 (m, 2 H) 6,75-6,98 (m, 1 H) 7,39-7,45 (m, 4 H) 7,55 (br d, J=8,22 Гц, 2 H) 7,57 (br d, J=8,22 Гц, 2 H) 8,20 (s, 1 H) 8,33 (d, J=1,76 Гц, 1 H) 8,58 (d, J=1,76 Гц, 1 H) 8,60 (s, 1 H);
[1964] MS (ESI+) масса/заряд 666,3 [M+H]+
[1965] Пример 388. 2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[1966] Схема получения соединения из примера 388:
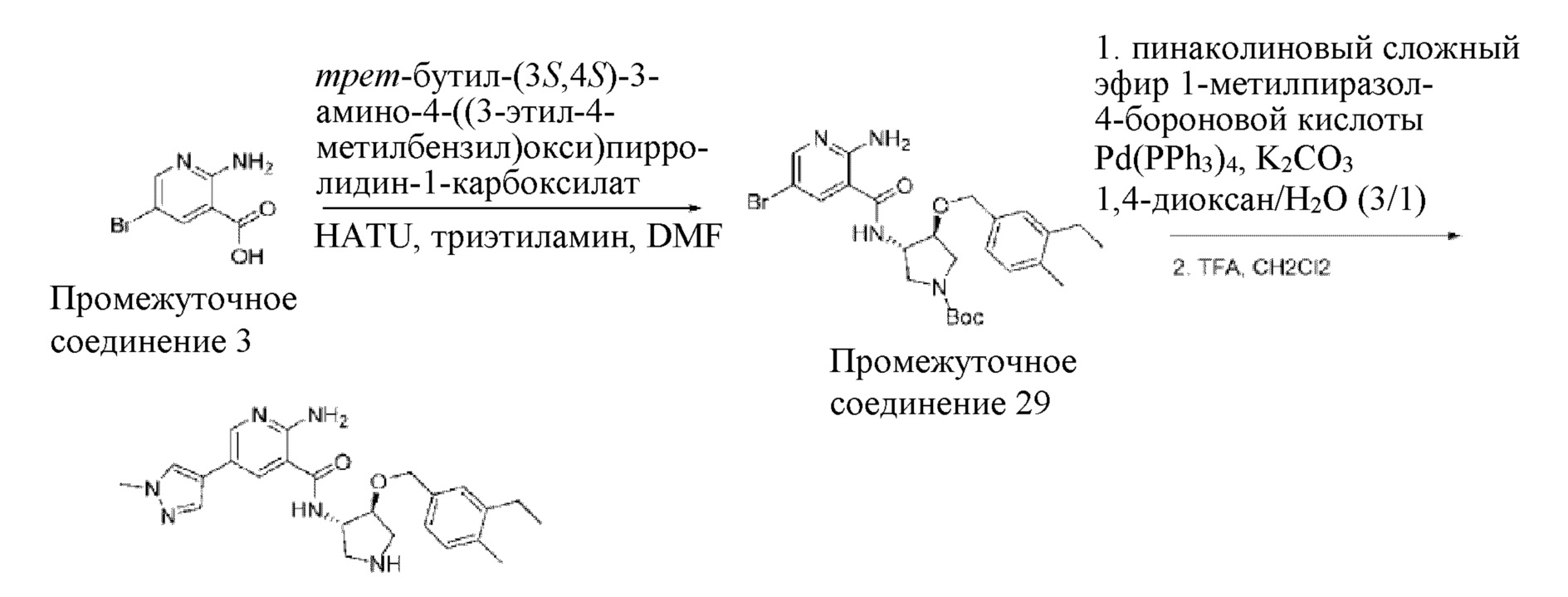
[1967]
[1968] Промежуточное соединение 29.
[1969] В смесь промежуточного соединения 3 (420 мг, 1,94 ммоль) и триэтиламина (0,40 мл, 2,90 ммоль) в 10 мл DMF добавляли HATU (884 мг, 2,32 ммоль), а затем трет-бутил-(3S,4S)-3-амино-4-((3-этил-4-метилбензил)окси)пирролидин-1-карбоксилат (647 мг, 1,94 ммоль). Смесь перемешивали при комнатной температуре в течение 1 часа, а затем добавляли насыщенный раствор бикарбоната натрия. Смесь экстрагировали при помощи EtOAc, промывали солевым раствором, сушили над MgSO4 и концентрировали in vacuo. Неочищенный продукт очищали колоночной хроматографией на силикагеле с получением 800 мг грязно-белого твердого вещества.
[1970] 1H-ЯМР (600 MГц, CDCl3) δ ppm 1,14-1,22 (t, 3 H) 1,41 (br s, 9 H) 2,27 (s, 3 H) 2,55-2,64 (q, 2 H) 3,37-3,66 (m, 4 H) 3,78 (dd, J=12,03, 5,58 Гц, 1 H) 4,10 (br s, 1 H) 4,50-4,79 (m, 2 H) 6,74 (br s, 2 H) 7,04-7,15 (m, 3 H) 7,98 (d, J=1,76 Гц, 1 H) 8,43 (br s, 1 H);
[1971] MS (ESI, масса/заряд): 534,3 [M+H]+
[1972] Пример 388. 2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[1973] В смесь промежуточного соединения 29 (40 мг, 0,07 ммоль) и пинаколинового сложного эфира 1-метилпиразол-4-бороновой кислоты (23 мг, 0,11 ммоль) в 0,4 мл 1,4-диоксана/воды (3/1) добавляли K2CO3 (31 мг, 0,22 ммоль), а затем Pd(PPh3)4 (4 мг, 0,003 ммоль). Реакционную смесь нагревали при 100°C в течение 3 часов, охлаждали до комнатной температуры и экстрагировали при помощи EtOAc, сушили над безводным MgSO4 и концентрировали под вакуумом. Неочищенный остаток растворяли в 0,5 мл CH2Cl2/TFA (10/1) и смесь перемешивали в течение 2 часов. После концентрирования под вакуумом неочищенный остаток очищали препаративной HPLC с получением 23 мг названного соединения.
[1974] 1H-ЯМР (600 MГц, CD3OD) ppm 1,13 (t, J=7,34 Гц, 3 H) 2,23 (s, 2 H) 2,57 (q, J=7,24 Гц, 2 H) 2,91 (dd, J=12,03, 4,40 Гц, 1 H) 2,97-3,04 (m, 1 H) 3,16-3,22 (m, 1 H) 3,36-3,43 (m, 1 H) 3,91 (s, 3 H) 4,05-4,10 (m, 1 H) 4,48 (br s, 1 H) 4,57 (d, J=11,74 Гц, 1 H) 4,65 (d, J=11,74 Гц, 1 H) 7,06 (s, 2 H) 7,12 (s, 1 H) 7,76 (s, 1 H) 7,89 (s, 1 H) 8,02 (d, J=2,35 Гц, 1 H) 8,26 (d, J=2,35 Гц, 1 H),
[1975] MS (ESI, масса/заряд): 435,5 [M+H]+
[1976] Пример 389. 2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)-5-(4-(гидроксиметил)фенил)никотинамид
[1977] Используя 4-гидроксиметилфенилбороновую кислоту, названное соединение получали, как описано для примера 388.
[1978] 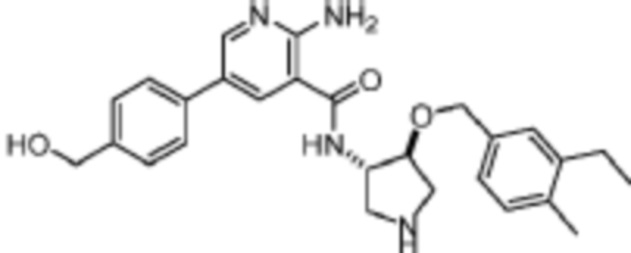
[1979] MS (ESI, масса/заряд): 461,6 [M+H]+
[1980] Пример 390. 2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)-5-(4-((4-метилпиперазин-1-ил)метил)фенил)никотинамид
[1981] Используя (4-((4-метилпиперазин-1-ил)метил)фенил)бороновую кислоту, названное соединение получали, как описано для примера 388.
[1982] 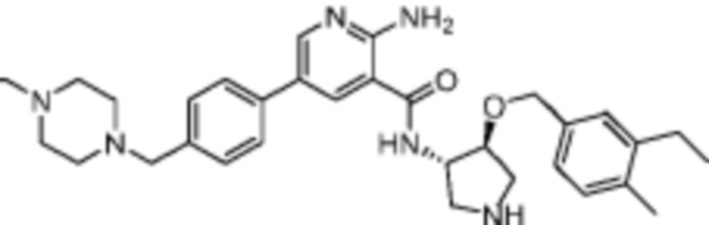
[1983] MS (ESI, масса/заряд): 543,4 [M+H]+
[1984] Пример 391. 2-амино-5-(4-карбамоилфенил)-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)никотинамид
[1985] Используя (4-карбамоилфенил)бороновую кислоту, названное соединение получали, как описано для примера 388.
[1986] 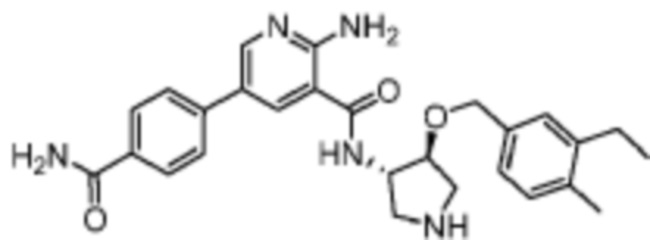
[1987] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,16 (t, J=7,63 Гц, 3 H) 2,25 (s, 3 H) 2,19-2,19 (m, 1 H) 2,60 (q, J=7,70 Гц, 2 H) 3,33-3,35 (m, 1 H) 3,43-3,64 (m, 2 H) 3,77 (br dd, J=12,72, 7,24 Гц, 1 H) 4,36 (br s, 1 H) 4,55-4,73 (m, 3 H) 7,10 (s, 2 H) 7,17 (s, 1 H) 7,78 (d, J=8,22 Гц, 2 H) 7,99 (d, J=8,61 Гц, 2 H) 8,44 (d, J=2,35 Гц, 1 H) 8,62 (d, J=1,96 Гц, 1 H);
[1988] MS (ESI, масса/заряд): 474,5 [M+H]+
[1989] Пример 392. 2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)-5-(м-толил)никотинамид
[1990] Используя м-толилбороновую кислоту, названное соединение получали, как описано для примера 388.
[1991] 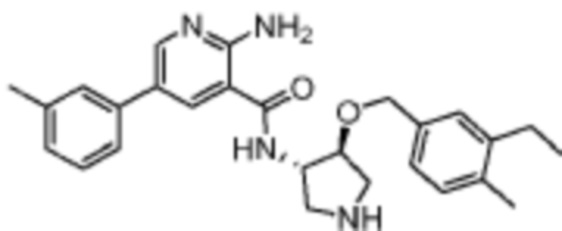
[1992] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,16 (t, J=7,43 Гц, 3 H) 2,25 (s, 3 H) 2,41 (s, 3 H) 2,60 (q, J=7,56 Гц, 2 H) 3,43-3,65 (m, 3 H) 3,77 (dd, J=12,52, 7,04 Гц, 1 H) 4,35 (br d, J=4,30 Гц, 1 H) 4,62-4,74 (m, 3 H) 7,09 (s, 2 H) 7,16 (s, 1 H) 7,25 (br d, J=7,43 Гц, 1 H) 7,36 (t, J=7,63 Гц, 1 H) 7,42-7,51 (m, 2 H) 8,31 (d, J=1,96 Гц, 1 H) 8,65 (d, J=1,96 Гц, 1 H);
[1993] MS (ESI, масса/заряд): 445,3 [M+H]+
[1994] Пример 393. 4-(6-амино-5-(((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)карбамоил)пиридин-3-ил)бензойная кислота
[1995] Используя 4-карбоксифенилбороновую кислоту, названное соединение получали, как описано для примера 388.
[1996] 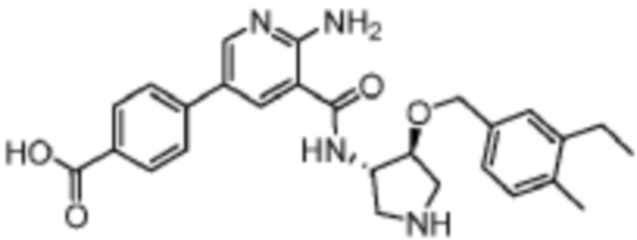
[1997] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,16 (t, J=7,43 Гц, 3 H) 2,23 (s, 3 H) 2,59 (q, J=7,56 Гц, 2 H) 3,34-3,51 (m, 2 H) 3,52-3,67 (m, 1 H) 3,76 (br d, J=7,43 Гц, 1 H) 4,13 (br s, 1 H) 4,57-4,69 (m, 3 H) 7,02-7,10 (m, 2 H) 7,14 (s, 1 H) 7,79 (br d, J=8,22 Гц, 2 H) 8,13 (br d, J=8,22 Гц, 2 H) 8,37-8,45 (m, 1 H) 8,73 (d, J=1,56 Гц, 1 H); MS (ESI, масса/заряд): 475,4 [M+H]+
[1998] Пример 394. 2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)-5-фенилникотинамид
[1999] Используя фенилбороновую кислоту, названное соединение получали, как описано для примера 388.
[2000] 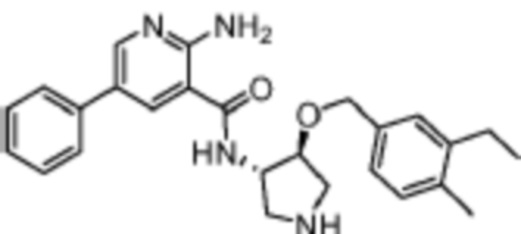
[2001] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,16 (t, J=7,63 Гц, 3 H) 2,25 (s, 3 H) 2,61 (q, J=7,43 Гц, 2 H) 3,42-3,51 (m, 1 H) 3,51-3,65 (m, 2 H) 3,77 (dd, J=12,91, 7,04 Гц, 1 H) 4,35 (br d, J=4,30 Гц, 1 H) 4,57-4,76 (m, 3 H) 7,06-7,13 (m, 2 H) 7,17 (s, 1 H) 7,35-7,58 (m, 3 H) 7,68 (d, J=7,04 Гц, 2 H) 8,33 (d, J=2,35 Гц, 1 H) 8,74 (d, J=2,35 Гц, 1 H);
[2002] MS (ESI, масса/заряд): 431,5 [M+H]+
[2003] Пример 395. 6-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)-[3,4'-бипиридин]-5-карбоксамид
[2004] Используя пиридин-4-бороновую кислоту, названное соединение получали, как описано для примера 388.
[2005] 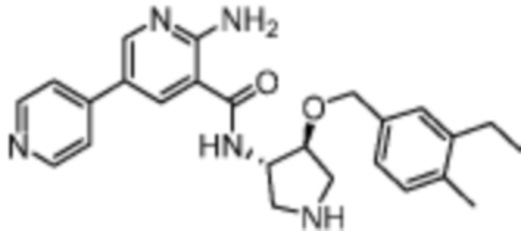
[2006] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,17 (t, J=7,63 Гц, 3 H) 2,26 (s, 3 H) 2,62 (q, J=7,56 Гц, 2 H) 3,47 (br d, J=12,52 Гц, 1 H) 3,52-3,67 (m, 2 H) 3,77 (br dd, J=12,72, 6,85 Гц, 1 H) 4,34 (br d, J=3,91 Гц, 1 H) 4,61-4,78 (m, 3 H) 7,07-7,13 (m, 2 H) 7,13-7,19 (m, 1 H) 7,99 (dd, J=8,02, 5,67 Гц, 1 H) 8,56 (d, J=1,96 Гц, 1 H) 8,68-8,82 (m, 3 H) 9,14 (s, 1 H);
[2007] MS (ESI, масса/заряд): 432,3 [M+H]+
[2008] Пример 396. 6-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)-[3,3'-бипиридин]-5-карбоксамид
[2009] Используя пиридин-3-бороновую кислоту, названное соединение получали, как описано для примера 388.
[2010] 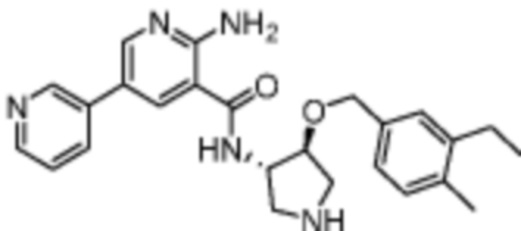
[2011] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,17 (t, J=7,63 Гц, 3 H) 2,26 (s, 3 H) 2,62 (q, J=7,56 Гц, 2 H) 3,47 (br d, J=12,52 Гц, 1 H) 3,52-3,67 (m, 2 H) 3,77 (br dd, J=12,72, 6,85 Гц, 1 H) 4,34 (br d, J=3,91 Гц, 1 H) 4,60-4,78 (m, 3 H) 7,07-7,13 (m, 2 H) 7,17 (d, J=7,06 Гц, 1 H) 7,18 (s, 1 H) 7,99 (dd, J=8,02, 5,67 Гц, 1 H) 8,56 (d, J=1,96 Гц, 1 H) 8,67-8,83 (m, 3 H) 9,14 (s, 1 H);
[2012] MS (ESI, масса/заряд): 432,3 [M+H]+
[2013] Пример 397. 2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)-5-винилникотинамид
[2014] Используя винилтрифторборат калия, названное соединение получали, как описано для примера 388.
[2015] 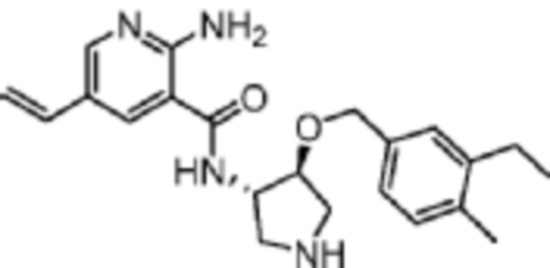
[2016] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,17 (t, J=7,43 Гц, 3 H) 2,26 (s, 3 H) 2,61 (q, J=7,56 Гц, 2 H) 3,44-3,65 (m, 3 H) 3,76 (br dd, J=12,91, 7,04 Гц, 1 H) 4,33 (br d, J=3,91 Гц, 1 H) 4,59-4,74 (m, 3 H) 5,42 (d, J=10,96 Гц, 1 H) 5,94 (d, J=17,61 Гц, 1 H) 6,66 (dd, J=17,80, 11,15 Гц, 1 H) 7,10 (s, 2 H) 7,16 (s, 1 H) 8,02-8,08 (m, 1 H) 8,66 (d, J=1,96 Гц, 1 H);
[2017] MS (ESI, масса/заряд): 381,3 [M+H]+
[2018] Пример 398. 2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)-5-(4-фторфенил)никотинамид
[2019] Используя 4-фторфенилбороновую кислоту, названное соединение получали, как описано для примера 388.
[2020] 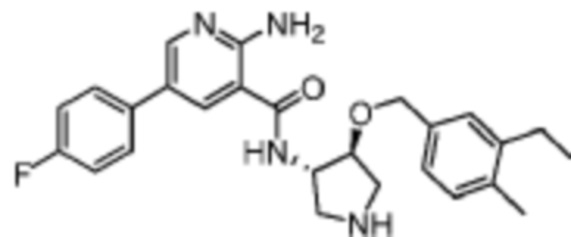
[2021] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,16 (t, J=7,63 Гц, 3 H) 2,25 (s, 3 H) 2,60 (q, J=7,63 Гц, 2 H) 3,44-3,59 (m, 2 H) 3,76 (dd, J=12,62, 7,34 Гц, 2 H) 4,25-4,38 (m, 1 H) 4,61-4,71 (m, 3 H) 7,03-7,12 (m, 2 H) 7,14-7,24 (m, 3 H) 7,60-7,69 (m, 2 H) 8,32 (d, J=2,35 Гц, 1 H) 8,48 (d, J=2,35 Гц, 1 H);
[2022] MS (ESI, масса/заряд): 499,3 [M+H]+
[2023] Пример 399. 2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)-5-(4-формилфенил)никотинамид
[2024] Используя 4-формилфенилбороновую кислоту, названное соединение получали, как описано для примера 388.
[2025] 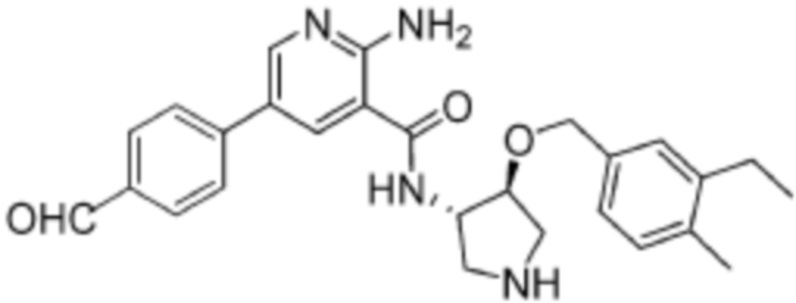
[2026] 1H-ЯМР (600 MГц, CDCl3) δ ppm 1,30 (t, J=7,63 Гц, 3 H) 2,26 (br s, 3 H) 2,58 (q, J=7,63 Гц, 2 H), 3,43-3,49 (m, 1 H) 3,50-3,65 (m, 2 H) 3,77 (dd, J=12,62, 6,75 Гц, 1 H) 4,17 (br s, 1 H) 4,64 (br s, 2 H) 4,77 (br s, 1 H) 6,59 (br s, 2 H) 7,05-7,20 (m, 3 H) 7,55-7,73 (m, 2 H) 7,86 (br d, J=5,28 Гц, 2 H) 8,04 (br s, 1 H) 8,46 (br s, 1 H) 9,86 (br s, 1 H);
[2027] MS (ESI, масса/заряд): 459,5 [M+H]+
[2028] Пример 400. 2-амино-5-(4-цианофенил)-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)никотинамид
[2029] Используя 4-цианофенилбороновую кислоту, названное соединение получали, как описано для примера 388.
[2030] 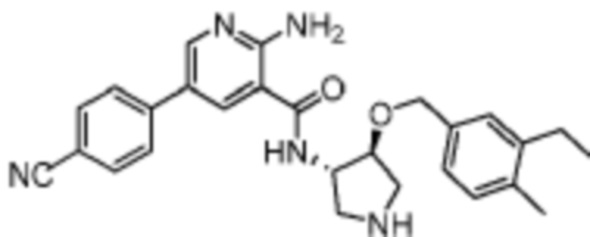
[2031] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,16 (t, J=7,34 Гц, 3 H) 2,25 (s, 3 H) 2,60 (q, J=7,63 Гц, 2 H) 3,43-3,49 (m, 1 H) 3,50-3,65 (m, 2 H) 3,77 (dd, J=12,62, 6,75 Гц, 1 H) 4,35 (br d, J=4,11 Гц, 1 H) 4,62-4,74 (m, 3 H) 7,04-7,14 (m, 2 H) 7,16 (s, 1 H) 7,78-7,84 (m, 2 H) 7,84-7,88 (m, 2 H) 8,39-8,52 (m, 1 H) 8,59 (d, J=1,76 Гц, 1 H);
[2032] MS (ESI, масса/заряд): 456,3 [M+H]+
[2033] Пример 401. 2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)-5-(4-(метилсульфонамидо)фенил)никотинамид
[2034] Используя 4-метилсульфонилфенилбороновую кислоту, названное соединение получали, как описано для примера 388.
[2035] 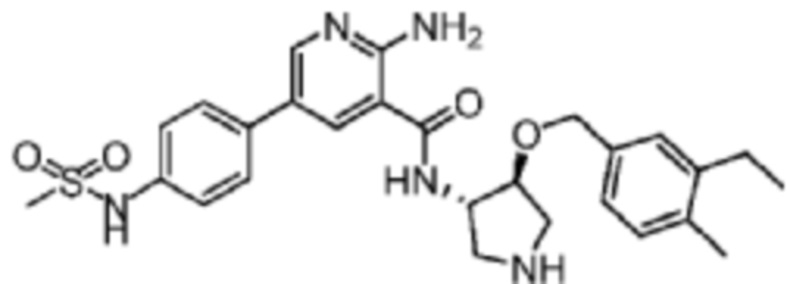
[2036] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,16 (t, J=7,34 Гц, 3 H) 2,25 (s, 3 H) 2,60 (q, J=7,63 Гц, 2 H) 2,98 (s, 3 H) 3,43-3,49 (m, 1 H) 3,50-3,65 (m, 2 H) 3,76 (dd, J=12,62, 7,34 Гц, 1 H) 4,33-4,38 (m, 1 H) 4,62-4,71 (m, 3 H) 7,05-7,13 (m, 2 H) 7,16 (s, 1 H) 7,36 (d, J=8,80 Гц, 2 H) 7,65 (d, J=8,22 Гц, 2 H) 8,32 (d, J=1,76 Гц, 1 H) 8,59 (d, J=1,76 Гц, 1 H);
[2037] MS (ESI, масса/заряд):524,6 [M+H]+
[2038] Пример 402. 2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)-5-(4-феноксифенил)никотинамид
[2039] Используя 4-феноксифенилбороновую кислоту, названное соединение получали, как описано для примера 388.
[2040] 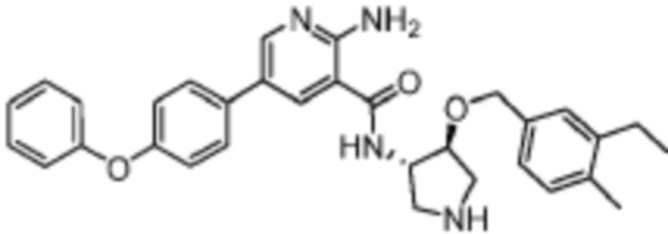
[2041] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,16 (t, J=7,63 Гц, 3 H) 2,25 (s, 3 H) 2,56-2,65 (m, 2 H) 3,46 (br d, J=12,33 Гц, 1 H) 3,52-3,61 (m, 2 H) 3,76 (s, 1 H) 4,32-4,40 (m, 1 H) 4,62-4,73 (m, 3 H) 7,02 (d, J=7,63 Гц, 2 H) 7,04-7,12 (m, 4 H) 7,13-7,19 (m, 2 H) 7,38 (t, J=7,92 Гц, 2 H) 7,66 (d, J=8,80 Гц, 2 H) 8,29-8,34 (m, 1 H) 8,68 (d, J=1,76 Гц, 1 H);
[2042] MS (ESI, масса/заряд):523,7 [M+H]+
[2043] Пример 403. 5-([1,1'-бифенил]-4-ил)-2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)никотинамид
[2044] Используя 4-бифенилбороновую кислоту, названное соединение получали, как описано для примера 388,
[2045] 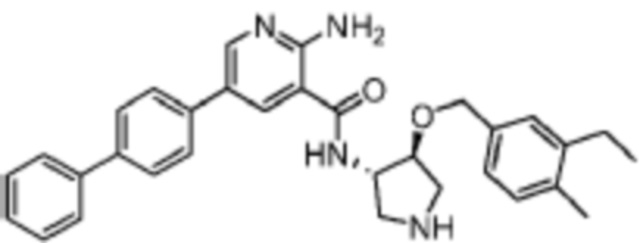
[2046] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,16 (t, J=7,63 Гц, 3 H) 2,25 (s, 3 H) 2,60 (q, J=7,63 Гц, 2 H) 3,47 (br d, J=12,91 Гц, 1 H) 3,51-3,62 (m, 2 H) 3,77 (dd, J=12,33, 7,04 Гц, 1 H) 4,31-4,40 (m, 1 H) 4,63-4,73 (m, 3 H) 7,05-7,14 (m, 2 H) 7,17 (s, 1 H) 7,34 (s, 1 H) 7,36 (br d, J=7,63 Гц, 1 H) 7,45 (t, J=7,63 Гц, 2 H) 7,64 (d, J=7,63 Гц, 2 H) 7,70-7,79 (m, 3 H) 8,40 (d, J=1,76 Гц, 1 H) 8,64 (d, J=2,35 Гц, 1 H);
[2047] MS (ESI, масса/заряд):507,4 [M+H]+
[2048] Пример 404. 2-амино-5-(4-(бензилокси)фенил)-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)никотинамид
[2049] Используя 4-бензилоксифенилбороновую кислоту, названное соединение получали, как описано для примера 388.
[2050] 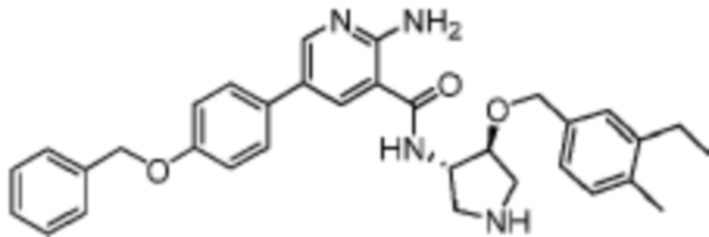
[2051] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,16 (t, J=7,63 Гц, 3 H) 2,24 (s, 3 H) 2,60 (q, J=7,63 Гц, 2 H) 3,46 (br d, J=12,91 Гц, 1 H) 3,49-3,60 (m, 2 H) 3,76 (dd, J=12,91, 7,04 Гц, 1 H) 4,28-4,36 (m, 1 H) 4,60-4,73 (m, 3 H) 5,13 (s, 2 H) 7,03-7,13 (m, 4 H) 7,16 (s, 1 H) 7,23-7,32 (m, 1 H) 7,36 (t, J=7,63 Гц, 2 H) 7,43 (d, J=7,04 Гц, 2 H) 7,59 (d, J=8,80 Гц, 2 H) 8,23-8,29 (m, 1 H) 8,60 (d, J=1,76 Гц, 1 H);
[2052] MS (ESI, масса/заряд): 537,8 [M+H]+
[2053] Пример 405. 2-амино-5-(4-(диметиламино)фенил)-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)никотинамид
[2054] 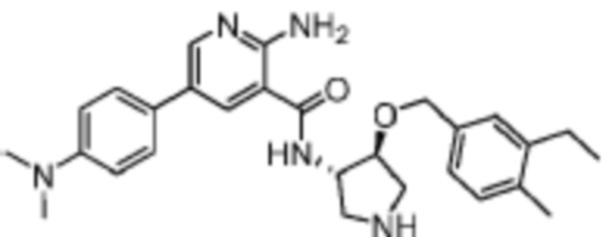
[2055] Используя 4-диметиламинофенилбороновую кислоту, названное соединение получали, как описано для примера 388.
[2056] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,16 (t, J=7,63 Гц, 3 H) 2,25 (s, 3 H) 2,60 (q, J=7,24 Гц, 2 H) 3,07 (s, 6 H) 3,47 (br d, J=12,91 Гц, 1 H) 3,57 (ddd, J=18,78, 12,91, 3,52 Гц, 2 H) 3,76 (br dd, J=12,91, 7,04 Гц, 1 H) 4,32-4,37 (m, 1 H) 4,61-4,72 (m, 3 H) 7,02-7,12 (m, 4 H) 7,16 (s, 1 H) 7,62 (d, J=8,80 Гц, 2 H) 8,26 (d, J=1,76 Гц, 1 H) 8,69 (d, J=1,76 Гц, 1 H);
[2057] MS (ESI, масса/заряд): 474,4 [M+H]+
[2058] Пример 406. 2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)-5-(хинолин-3-ил)никотинамид
[2059] 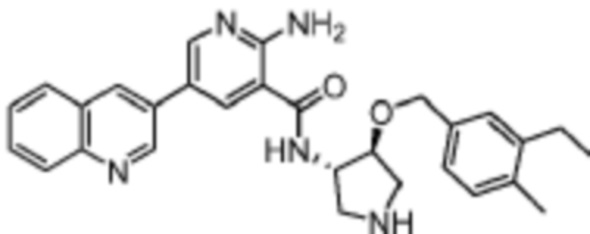
[2060] Используя хинолин-3-бороновую кислоту, названное соединение получали, как описано для примера 388.
[2061] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,17 (t, J=7,34 Гц, 3 H) 2,25 (s, 3 H) 2,61 (q, J=7,24 Гц, 2 H) 3,48 (br d, J=12,91 Гц, 1 H) 3,57-3,69 (m, 2 H) 3,78 (br dd, J=12,91, 7,04 Гц, 1 H) 4,34-4,42 (m, 1 H) 4,61-4,75 (m, 3 H) 7,05-7,15 (m, 2 H) 7,18 (s, 1 H) 7,78-7,93 (m, 1 H) 7,93-8,09 (m, 1 H) 8,18 (br dd, J=8,22, 3,52 Гц, 2 H) 8,63 (d, J=1,76 Гц, 1 H) 8,86 (d, J=2,35 Гц, 1 H) 8,99-9,07 (m, 1 H) 9,37 (d, J=1,76 Гц, 1 H); MS (ESI, масса/заряд): 482,6 [M+H]+
[2062] Пример 407. 2-амино-5-(бензофуран-2-ил)-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)никотинамид
[2063] 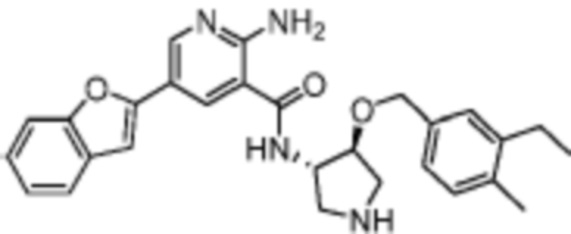
[2064] Используя бензо[b]фуран-2-бороновую кислоту, названное соединение получали, как описано для примера 388.
[2065] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,16 (t, J=7,63 Гц, 3 H) 2,25 (s, 3 H) 2,61 (q, J=7,63 Гц, 2 H) 3,48 (br d, J=12,33 Гц, 1 H) 3,53 (br dd, J=12,91, 2,93 Гц, 1 H) 3,60 (br dd, J=12,91, 4,70 Гц, 1 H) 3,78 (br dd, J=12,62, 7,34 Гц, 1 H) 4,37 (br s, 1 H) 4,63-4,72 (m, 3 H) 7,04-7,14 (m, 2 H) 7,15-7,20 (m, 2 H) 7,20-7,26 (m, 1 H) 7,29 (br t, J=7,63 Гц, 1 H) 7,51 (d, J=8,22 Гц, 1 H) 7,58 (br d, J=7,63 Гц, 1 H) 8,57 (d, J=1,76 Гц, 1 H) 8,60 (d, J=1,76 Гц, 1 H);
[2066] MS (ESI, масса/заряд): 471,5 [M+H]+
[2067] Пример 408. 2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)-5-(нафталин-1-ил)никотинамид
[2068] Используя 2-нафтиленбороновую кислоту, названное соединение получали, как описано для примера 388.
[2069] 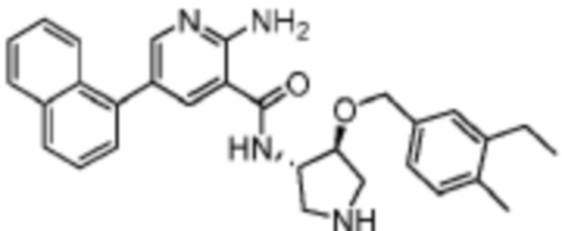
[2070] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,16 (t, J=7,63 Гц, 3 H) 2,24 (s, 3 H) 2,60 (q, J=7,43 Гц, 2 H) 3,48 (br d, J=12,91 Гц, 1 H) 3,53-3,69 (m, 2 H) 3,78 (dd, J=12,91, 7,04 Гц, 1 H) 4,31-4,46 (m, 1 H) 4,55-4,72 (m, 3 H) 7,05-7,14 (m, 2 H) 7,17 (s, 1 H) 7,47-7,58 (m, 2 H) 7,79 (dd, J=8,22, 1,76 Гц, 1 H) 7,85-8,02 (m, 3 H) 8,16 (s, 1 H) 8,47 (d, J=1,76 Гц, 1 H) 8,78 (d, J=1,76 Гц, 1 H);
[2071] MS (ESI, масса/заряд): 481,4 [M+H]+
[2072] Пример 409. 2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)-5-(4-(трифторметил)фенил)никотинамид
[2073] Используя 4-трифторметилбензолбороновую кислоту, названное соединение получали, как описано для примера 388.
[2074] 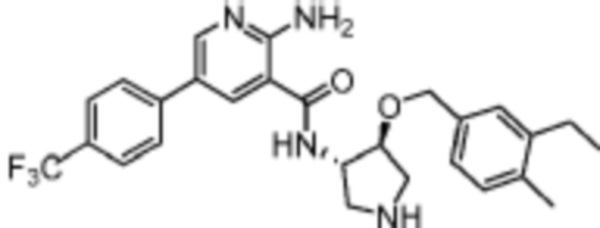
[2075] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,16 (t, J=7,63 Гц, 3 H) 2,25 (s, 3 H) 2,61 (q, J=7,24 Гц, 2 H) 3,45 (br d, J=12,32 Гц, 1 H) 3,49-3,62 (m, 2 H) 3,75 (dd, J=12,62, 6,75 Гц, 1 H) 4,26-4,38 (m, 1 H) 4,61-4,72 (m, 3 H) 7,03-7,13 (m, 2 H) 7,16 (s, 1 H) 7,33 (td, J=10,12, 6,75 Гц, 2 H) 7,53-7,69 (m, 2 H) 8,29 (s, 1 H) 8,48 (d, J=1,76 Гц, 1 H);
[2076] MS (ESI, масса/заряд): 499,6 [M+H]+
[2077] Пример 410. 2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)-5-(2,4,5-трифторфенил)никотинамид
[2078] Используя 2,4,5-трифторфенилбороновую кислоту, названное соединение получали, как описано для примера 388.
[2079] 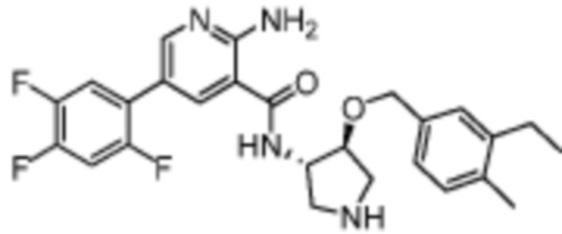
[2080] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,16 (t, J=7,63 Гц, 3 H) 2,25 (s, 3 H) 2,61 (q, J=7,24 Гц, 2 H) 3,45 (br d, J=12,32 Гц, 1 H) 3,49-3,62 (m, 2 H) 3,75 (dd, J=12,62, 6,75 Гц, 1 H) 4,26-4,38 (m, 1 H) 4,61-4,72 (m, 3 H) 7,03-7,13 (m, 2 H) 7,16 (s, 1 H) 7,33 (td, J=10,12, 6,75 Гц, 1 H) 7,53-7,63 (m, 1 H) 8,29 (s, 1 H) 8,48 (d, J=1,76 Гц, 1 H);
[2081] MS (ESI, масса/заряд): 485,3 [M+H]+
[2082] Пример 411. 2-амино-5-(4-(цианометил)фенил)-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)никотинамид
[2083] Используя 4-цианометилфенилбороновую кислоту, названное соединение получали, как описано для примера 388.
[2084] 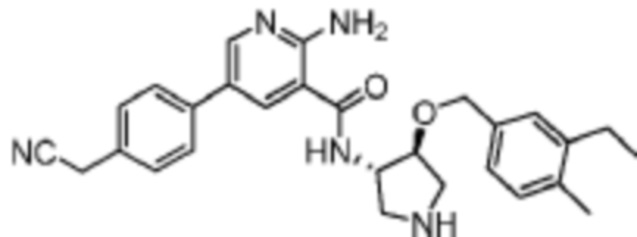
[2085] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,16 (td, J=7,63, 2,35 Гц, 3 H) 2,24 (d, J=4,11 Гц, 3 H) 2,59 (qd, J=7,53, 3,23 Гц, 2 H) 3,45-3,56 (m, 1 H) 3,67-3,74 (m, 1 H) 3,77-3,88 (m, 1 H) 3,93 (s, 2 H) 3,98 (br dd, J=11,44, 6,16 Гц, 1 H) 4,11-4,28 (m, 1 H) 4,58-4,70 (m, 3 H) 7,07 (s, 2 H) 7,14 (s, 1 H) 7,86 (d, J=2,93 Гц, 1 H) 8,02 (s, 1 H) 8,19 (d, J=11,15 Гц, 1 H) 8,24 (d, J=1,76 Гц, 1 H) 8,59 (dd, J=7,04, 2,35 Гц, 1 H);
[2086] MS (ESI, масса/заряд): 470,8 [M+H]+
[2087] Пример 412. 2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)-5-(1-(пиперидин-4-ил)-1H-пиразол-4-ил)никотинамид
[2088] Используя 1-(4-N-Boc-пиперидин)пиразол-4-бороновую кислоту, названное соединение получали, как описано для примера 388 и после снятия защитных групп при помощи TFA.
[2089] 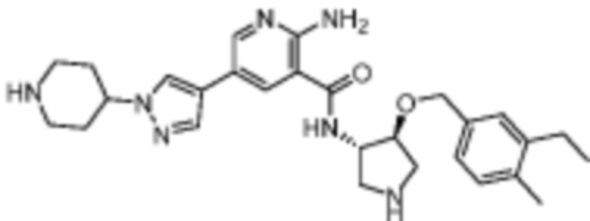
[2090] MS (ESI, масса/заряд): 504,3 [M+H]+
[2091] Пример 413. 2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)-5-(1-(1-метилпиперидин-4-ил)-1H-пиразол-4-ил)никотинамид
[2092] Используя 1-(4-N-метилпиперидин)пиразол-4-бороновую кислоту, названное соединение получали, как описано для примера 388.
[2093] 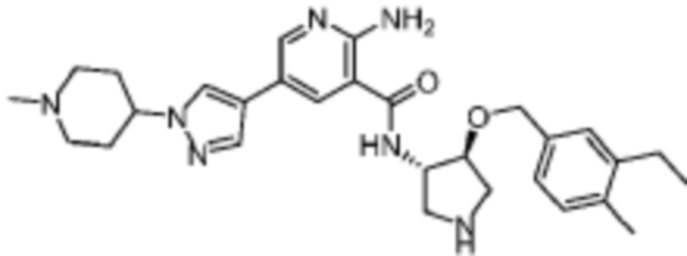
[2094] MS (ESI, масса/заряд): 518,3 [M+H]+
[2095] Пример 414. 2-амино-N-((3S,4S)-4-(бензилокси)пирролидин-3-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[2096] Используя трет-бутил-(3S,4S)-3-амино-4-(бензилокси)пирролидин-1-карбоксилат, названное соединение получали, как описано для примера 388.
[2097] 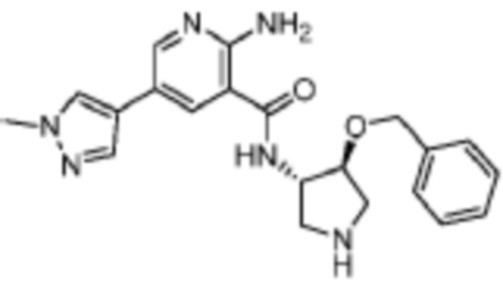
[2098] MS (ESI, масса/заряд): 393,2 [M+H]+
[2099] Пример 415. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((3S,4S)-4-((4-метилбензил)окси)пирролидин-3-ил)никотинамид
[2100] Используя трет-бутил-(3S,4S)-3-амино-4-((4-метилбензил)окси)пирролидин-1-карбоксилат, названное соединение получали, как описано для примера 388.
[2101] 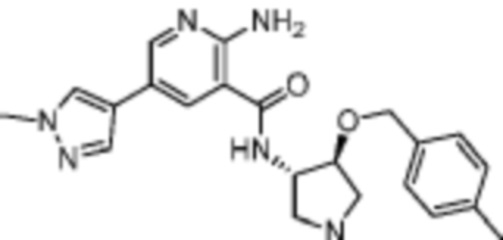
[2102] MS (ESI, масса/заряд): 407,2 [M+H]+
[2103] Пример 416. 2-амино-N-((3S,4S)-4-((3-этилбензил)окси)пирролидин-3-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[2104] Используя трет-бутил-(3S,4S)-3-амино-4-((3-этилбензил)окси)пирролидин-1-карбоксилат, названное соединение получали, как описано для примера 388.
[2105] 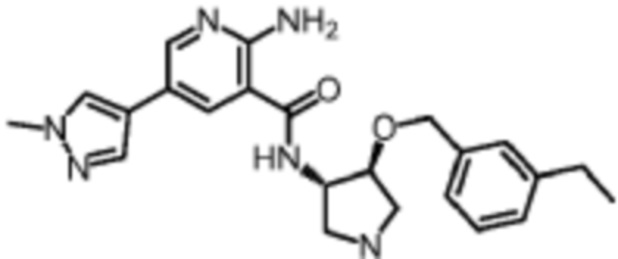
[2106] MS (ESI, масса/заряд): 421,2 [M+H]+
[2107] Пример 417. 2-амино-N-((3S,4S)-4-((3-этил-4-фторбензил)окси)пирролидин-3-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[2108] Используя трет-бутил-(3S,4S)-3-амино-4-((3-этил-4-фторбензил)окси)пирролидин-1-карбоксилат, названное соединение получали, как описано для примера 388.
[2109] 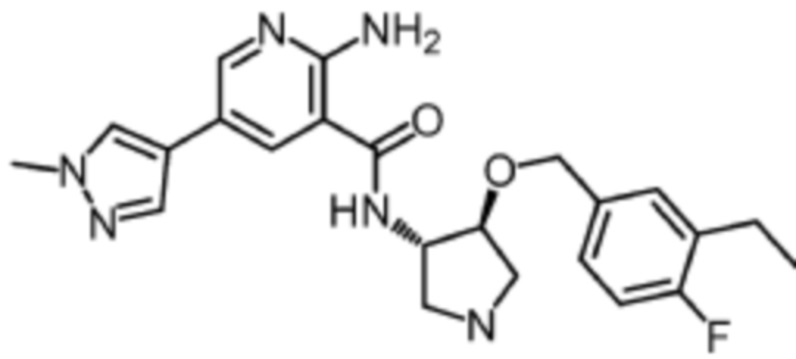
[2110] MS (ESI, масса/заряд): 439,2 [M+H]+
[2111] Пример 418. 2-амино-N-((3S,4S)-4-((4-хлор-3-этилбензил)окси)пирролидин-3-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[2112] Используя трет-бутил-(3S,4S)-3-амино-4-((4-хлор-3-этилбензил)окси)пирролидин-1-карбоксилат, названное соединение получали, как описано для примера 388.
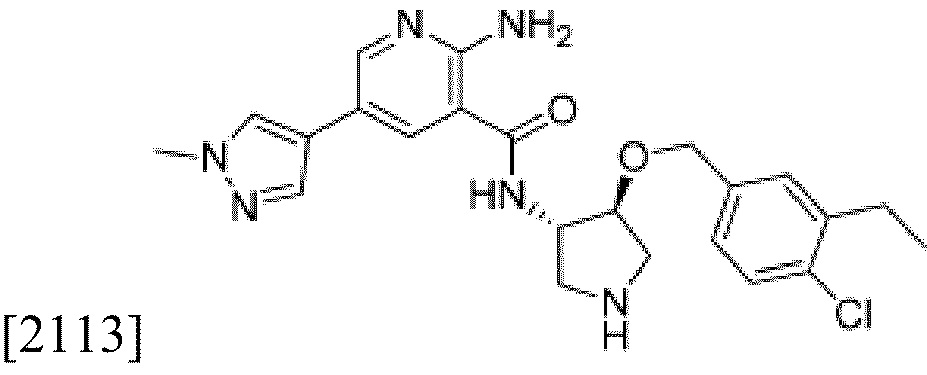
[2114] MS (ESI, масса/заряд): 455,2 [M+H]+
[2115] Пример 419. 2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)-5-(4-((1-метилпиперидин-4-ил)карбамоил)фенил)никотинамид
[2116] Схема получения соединения из примера 419:
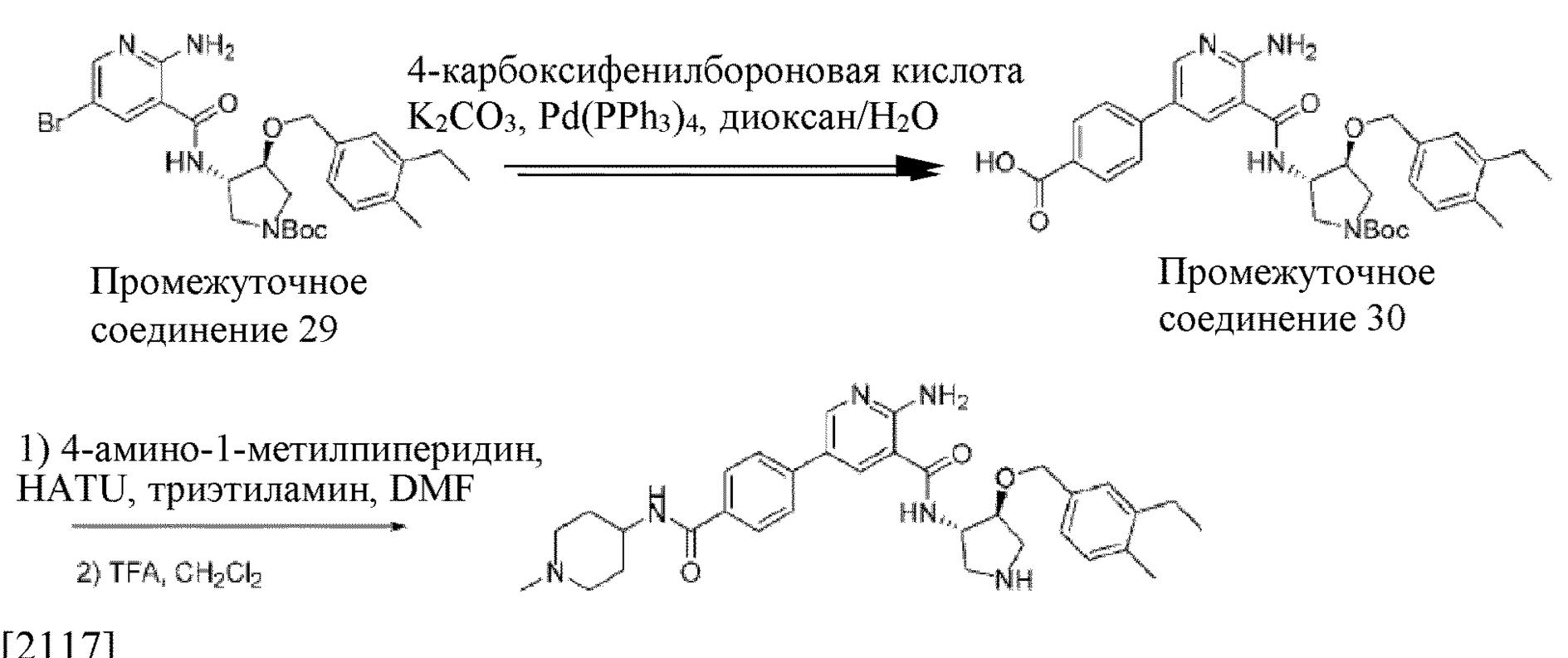
[2118] Промежуточное соединение 30.
[2119] В смесь промежуточного соединения 29 (400 мг, 0,7 ммоль) и 4-карбоксифенилбороновой кислоты (230 мг, 1,10 ммоль) в 4 мл 1,4-диоксана/воды (3/1) добавляли K2CO3 (310 мг, 2,2 ммоль), а затем Pd(PPh3)4 (40 мг, 0,03 ммоль). Реакционную смесь нагревали при 100°C в течение 3 часов, охлаждали до комнатной температуры и экстрагировали при помощи EtOAc, сушили над безводным MgSO4 и концентрировали под вакуумом. Неочищенный продукт очищали колоночной хроматографией на силикагеле с получением 350 мг грязно-белого твердого вещества
[2120] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,16 (t, J=7,43 Гц, 3 H) 1,46 (br d, J=1,96 Гц, 9 H) 2,23 (s, 3 H) 2,59 (q, J=7,56 Гц, 2 H) 3,40-3,51 (m, 2 H) 3,52-3,65 (m, 1 H) 3,76 (br d, J=7,43 Гц, 1 H) 4,13 (br s, 1 H) 4,57-4,74 (m, 3 H) 7,06 (s, 2 H) 7,14 (s, 1 H) 7,79 (br d, J=8,22 Гц, 2 H) 8,13 (br d, J=8,22 Гц, 2 H) 8,37-8,45 (m, 1 H) 8,73 (d, J=1,56 Гц, 1 H);
[2121] MS (ESI, масса/заряд): 575,3 [M+H]+
[2122] Пример 419. 2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)-5-(4-((1-метилпиперидин-4-ил)карбамоил)фенил)никотинамид
[2123] В смесь промежуточного соединения 30 (12 мг, 0,02 ммоль) и триэтиламина (0,04 мл, 0,03 ммоль) в 0,2 мл DMF добавляли HATU (10 мг, 0,03 ммоль), а затем 4-амино-1-метилпиперидин (0,03 мл, 0,02 ммоль). Смесь перемешивали при комнатной температуре в течение 1 часа, а затем добавляли насыщенный раствор бикарбоната натрия. Смесь экстрагировали при помощи EtOAc, промывали солевым раствором, сушили над MgSO4 и концентрировали in vacuo. Неочищенный остаток растворяли в 0,5 мл CH2Cl2/TFA (10/1) и смесь перемешивали в течение 2 часов. После концентрирования под вакуумом неочищенный остаток очищали препаративной HPLC с получением 10 мг названного соединения.
[2124] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,16 (t, J=7,63 Гц, 3 H) 1,86-1,98 (m, 2 H) 2,23 (br s, 3 H) 2,25 (s, 3 H) 2,61 (q, J=7,70 Гц, 2 H) 2,89 (s, 3 H) 3,10-3,26 (m, 2 H) 3,47 (br d, J=12,52 Гц, 1 H) 3,52-3,66 (m, 3 H) 3,77 (dd, J=12,72, 6,85 Гц, 1 H) 4,11-4,23 (m, 1 H) 4,32-4,43 (m, 1 H) 4,53-4,77 (m, 3 H) 7,05-7,14 (m, 2 H) 7,17 (s, 1 H) 7,81 (d, J=8,22 Гц, 2 H) 7,88-7,99 (m, 2 H) 8,42 (d, J=1,96 Гц, 1 H) 8,74 (d, J=1,96 Гц, 1 H);
[2125] MS (ESI, масса/заряд): 571,4 [M+H]+
[2126] Пример 420. 2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)-5-(4-((4-метилциклогексил)карбамоил)фенил)никотинамид
[2127] Используя 4-метилциклогексиламин, названное соединение получали, как описано для примера 419.
[2128] 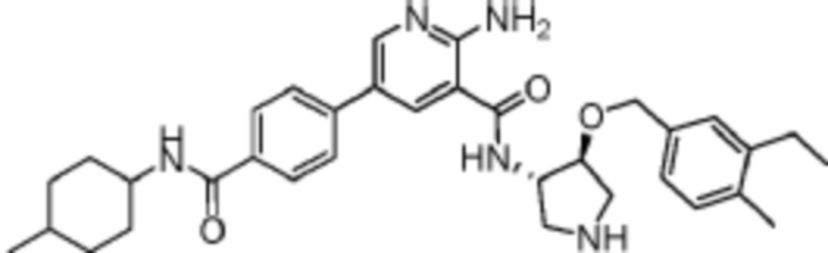
[2129] 1H-ЯМР (600 MГц, CD3OD) δ ppm 0,93 (d, J=6,46 Гц, 1 H) 1,00 (d, J=6,46 Гц, 2 H) 1,09 (br d, J=14,09 Гц, 1 H) 1,16 (t, J=7,63 Гц, 3 H) 1,38-1,48 (m, 2 H) 1,59-1,73 (m, 3 H) 1,75-1,84 (m, 2 H) 1,96 (br d, J=11,15 Гц, 1 H) 2,25 (s, 3 H) 2,60 (q, J=7,63 Гц, 2 H) 3,32-3,36 (m, 1 H) 3,47 (br d, J=12,91 Гц, 1 H) 3,51-3,61 (m, 2 H) 3,76 (dd, J=12,91, 7,04 Гц, 2 H) 3,99 (br s, 1 H) 4,35 (br s, 1 H) 4,62-4,72 (m, 3 H) 7,03-7,14 (m, 2 H) 7,16 (s, 1 H) 7,76 (dd, J=8,51, 4,40 Гц, 2 H) 7,91 (dd, J=8,22, 2,35 Гц, 2 H) 8,42 (d, J=2,35 Гц, 1 H) 8,58-8,62 (m, 1 H);
[2130] MS (ESI, масса/заряд): 570,5 [M+H]+
[2131] Пример 421. 2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)-5-(4-(4-метилпиперидин-1-карбонил)фенил)никотинамид
[2132] Используя 4-метилпиперидин, названное соединение получали, как описано для примера 419.
[2133] 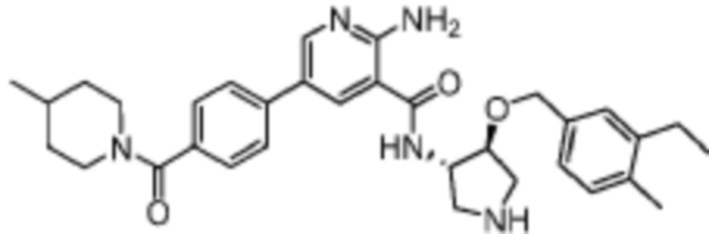
[2134] 1H-ЯМР (600 MГц, CD3OD) δ ppm 0,98 (d, J=6,46 Гц, 3 H) 1,09-1,22 (m, 3H) 1,16 (t, J=7,63, 3 H) 1,62 (br d, J=11,74 Гц, 1 H) 1,66-1,74 (m, 2 H) 1,79 (br d, J=12,91 Гц, 1 H) 2,23 (s, 3 H) 2,53-2,63 (q, J=7,63 Гц, 2 H) 2,85 (br t, J=12,33 Гц, 1 H) 3,11 (br t, J=12,33 Гц, 1 H) 3,39-3,49 (m, 2 H) 3,55-3,61 (m, 1 H) 3,68 (br d, J=12,91 Гц, 1 H) 3,75 (td, J=11,74, 7,04 Гц, 1 H) 4,12 (br s, 1 H) 4,58-4,64 (m, 3 H) 7,02-7,11 (m, 2 H) 7,13 (s, 1 H) 7,51 (d, J=8,22 Гц, 2 H) 7,76 (d, J=8,22 Гц, 2 H) 8,36 (d, J=1,76 Гц, 1 H) 8,70 (d, J=1,76 Гц, 1 H);
[2135] MS (ESI, масса/заряд): 556,5 [M+H]+
[2136] Пример 422. 2-амино-5-(4-(диметилкарбамоил)фенил)-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)никотинамид
[2137] Используя диметиламин, названное соединение получали, как описано для примера 419.
[2138] 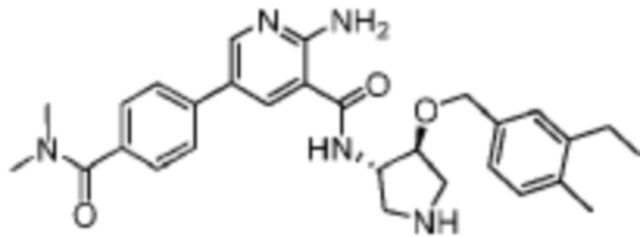
[2139] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,15 (t, J=7,63 Гц, 3 H) 2,22 (s, 3 H) 2,58 (q, J=7,63 Гц, 2 H) 3,01 (s, 3 H) 3,11 (s, 3 H) 3,38-3,50 (m, 2 H) 3,52-3,66 (m, 1 H) 3,67-3,81 (m, 1 H) 4,12 (br s, 1 H) 4,57-4,68 (m, 3 H) 7,05 (s, 2 H) 7,13 (s, 1 H) 7,54 (d, J=8,80 Гц, 2 H) 7,75 (d, J=8,22 Гц, 2 H) 8,36 (d, J=1,76 Гц, 1 H) 8,68 (d, J=2,35 Гц, 1 H);
[2140] MS (ESI, масса/заряд): 502,4 [M+H]+
[2141] Пример 423. 2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)-5-(4-((4-метилпиперидин-1-ил)метил)фенил)никотинамид
[2142] Схема получения соединения из примера 423:
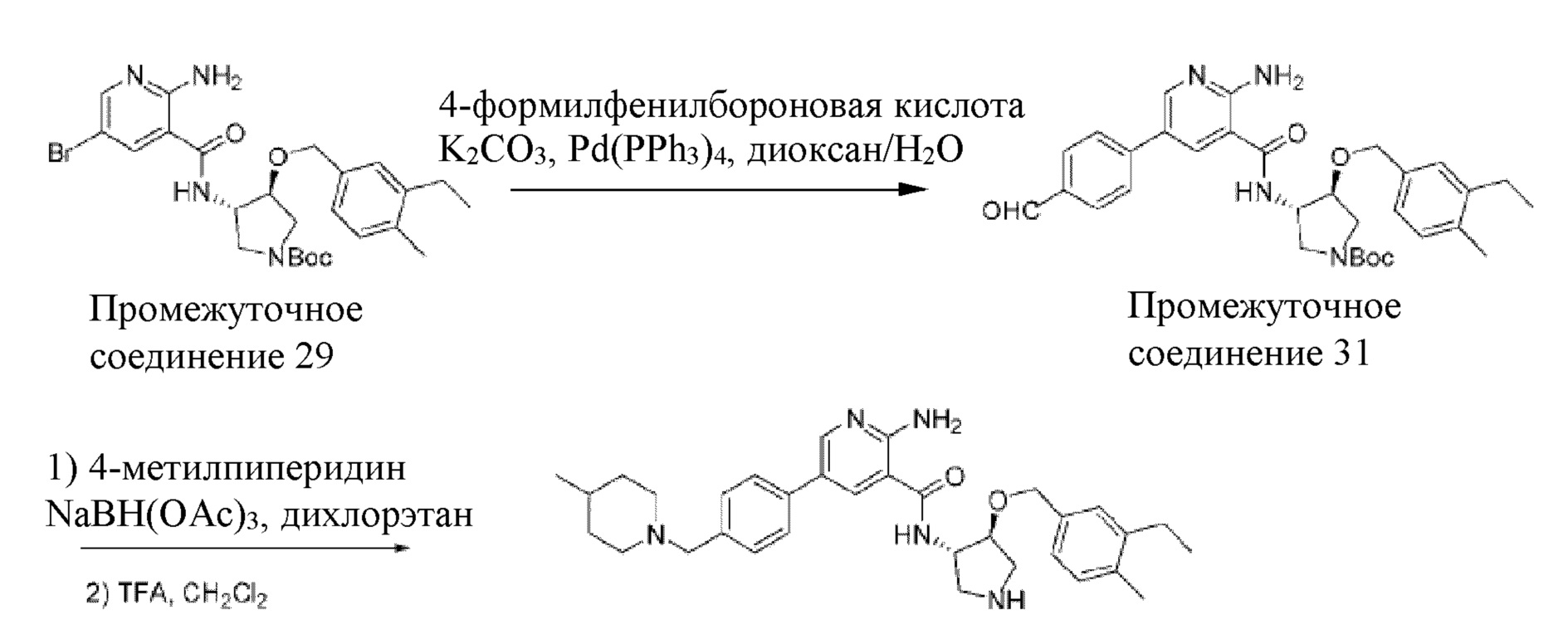
[2143]
[2144] Промежуточное соединение 31.
[2145] Используя промежуточное соединение 29 и 4-формилфенилбороновую кислоту, названное соединение получали, как описано для синтеза промежуточного соединения 30.
[2146] 1H-ЯМР (600 MГц, CDCl3)
[2147] ppm 1,30 (t, J=7,63 Гц, 3 H), 1,42 (s, 9 H), 2,26 (br s, 3 H) 2,58 (q, J=7,63 Гц, 2 H) 3,37-3,84 (m, 4H) 4,17 (br s, 1 H) 4,64 (br s, 2 H) 4,77 (br s, 1 H) 6,59 (br s, 2 H) 7,05-7,20 (m, 3 H) 7,55-7,73 (m, 2 H) 7,86 (br d, J=5,28 Гц, 2 H) 8,04 (br s, 1 H) 8,46 (br s, 1 H) 9,86 (br s, 1 H);
[2148] MS (ESI, масса/заряд): 559,4 [M+H]+
[2149] Пример 423. 2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)-5-(4-((4-метилпиперидин-1-ил)метил)фенил)никотинамид
[2150] В смесь промежуточного соединения 31 (40 мг, 0,07 ммоль) в 0,4 мл дихлорэтана добавляли 4-метилпиперидин (0,017 мл, 0,14 ммоль), а затем NaBH(OAc)3 (30 мг, 0,21 ммоль). Смесь перемешивали при комнатной температуре в течение 4 часов, а затем добавляли воду. Смесь экстрагировали при помощи EtOAc, промывали солевым раствором, сушили над MgSO4 и концентрировали in vacuo. Неочищенный остаток растворяли в 0,5 мл CH2Cl2/TFA (10/1) и смесь перемешивали в течение 2 часов. После концентрирования под вакуумом неочищенный остаток очищали препаративной HPLC с получением 10 мг названного соединения.
[2151] 1H-ЯМР (600 MГц, CD3OD) δ ppm 0,99 (d, J=6,46 Гц, 3 H) 1,16 (t, J=7,34 Гц, 3 H) 1,34-1,46 (m, 2 H) 1,91 (br d, J=14,09 Гц, 2 H) 2,25 (s, 3 H) 2,61 (q, J=7,63 Гц, 2 H) 2,93-3,07 (m, 2 H) 3,43-3,49 (m, 3 H) 3,57 (ddd, J=16,43, 12,91, 3,52 Гц, 2 H) 3,76 (dd, J=12,62, 6,75 Гц, 2 H) 4,27-4,39 (m, 3 H) 4,59-4,76 (m, 3 H) 7,05-7,14 (m, 2 H) 7,17 (s, 1 H) 7,60 (d, J=8,22 Гц, 2 H) 7,80 (d, J=8,22 Гц, 2 H) 8,39 (d, J=1,76 Гц, 1 H) 8,67 (d, J=1,76 Гц, 1 H);
[2152] MS (ESI, масса/заряд): 542,3 [M+H]+
[2153] Пример 424. 2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)-5-(4-(морфолинометил)фенил)никотинамид
[2154] Используя морфолин, названное соединение получали, как описано для примера 423.
[2155] 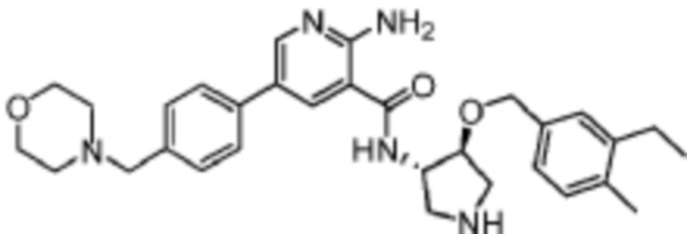
[2156] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,16 (t, J=7,63 Гц, 3 H) 2,25 (s, 3 H) 2,61 (q, J=7,63 Гц, 2 H) 3,09-3,27 (m, 2 H) 3,31-3,40 (m, 2 H) 3,46 (d, J=12,33 Гц, 1 H) 3,52-3,67 (m, 2 H) 3,76 (br dd, J=12,91, 7,04 Гц, 1 H) 3,77 (br s, 2 H) 4,03 (br s, 2 H) 4,35 (br d, J=4,11 Гц, 1 H) 4,41 (s, 2 H) 4,63-4,71 (m, 2 H) 4,72 (br d, J=6,46 Гц, 1 H) 7,06-7,12 (m, 2 H) 7,17 (s, 1 H) 7,63 (d, J=8,22 Гц, 2 H) 7,82 (d, J=8,22 Гц, 2 H) 8,40 (d, J=2,35 Гц, 1 H) 8,66-8,70 (m, 1 H);
[2157] MS (ESI, масса/заряд): 530,3 [M+H]+
[2158] Пример 425. 2-амино-5-(4-((3,3-дифторпиперидин-1-ил)метил)фенил)-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)никотинамид
[2159] Используя 3,3-дифторпиперидин, названное соединение получали, как описано для примера 423.
[2160] 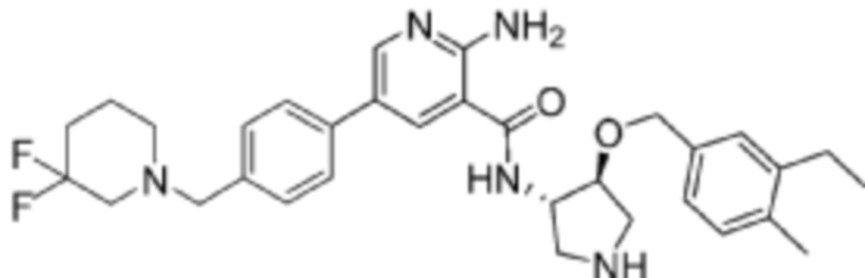
[2161] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,16 (t, J=7,63 Гц, 3 H) 1,97-2,09 (m, 2 H) 2,15 (br s, 2 H) 2,25 (s, 3 H) 2,61 (q, J=7,63 Гц, 2 H) 3,22-3,28 (m, 2 H) 3,38-3,49 (m, 4 H) 3,50-3,66 (m, 2 H) 3,76 (dd, J=12,33, 7,04 Гц, 1 H) 4,35 (br d, J=4,70 Гц, 1 H) 4,40 (s, 2 H) 4,62-4,73 (m, 3 H) 7,07-7,12 (m, 2 H) 7,17 (s, 1 H) 7,61 (d, J=8,22 Гц, 2 H) 7,81 (d, J=8,22 Гц, 2 H) 8,40 (d, J=2,35 Гц, 1 H) 8,61 (d, J=1,76 Гц, 1 H);
[2162] MS (ESI, масса/заряд): 564,3 [M+H]+
[2163] Пример 426. 2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)-1-метилпирролидин-3-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[2164] Схема получения соединения из примера 426:
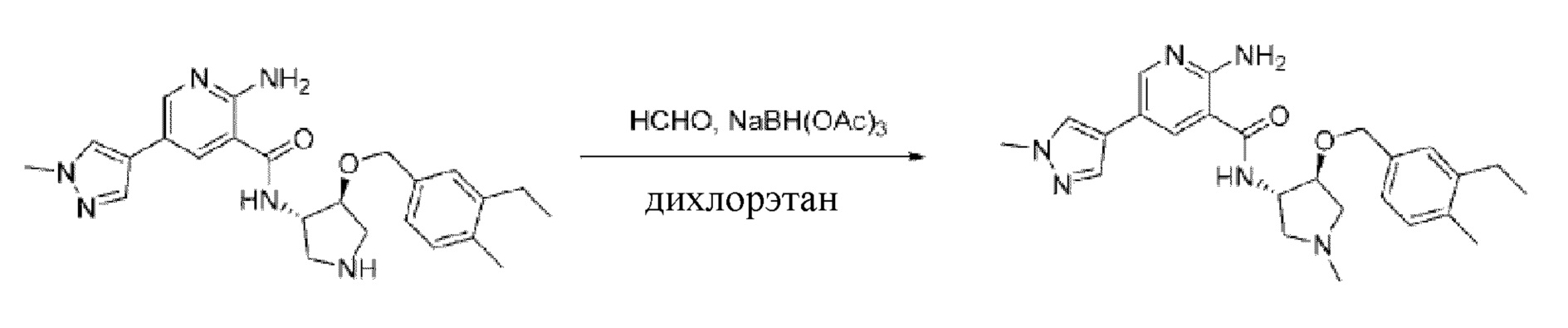
[2165]
[2166] В соединение 388 (40 мг, 0,09 ммоль) в 0,4 мл 1,2-дихлорэтана добавляли формальдегид (0,015 мл, 0,18 ммоль), а затем NaBH(OAc)3 (38 мг, 0,28 ммоль). Смесь перемешивали при комнатной температуре в течение 1 часа, а затем добавляли воду. Смесь экстрагировали при помощи EtOAc, промывали солевым раствором, сушили над MgSO4 и концентрировали in vacuo. Неочищенный остаток очищали препаративной HPLC с получением 30 мг названого соединения.
[2167] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,12-1,17 (m, 3 H) 2,23 (s, 3 H) 2,55-2,65 (m, 2 H) 3,01 (s, 3 H) 3,43-3,54 (m, 1 H) 3,60-3,71 (m, 1 H) 3,73-3,84 (m, 1 H) 3,92 (s, 3 H) 4,08-4,23 (m, 1 H) 4,31-4,45 (m, 1 H) 4,62-4,70 (m, 2 H) 4,72 (br d, J=5,87 Гц, 1 H) 7,04-7,11 (m, 2 H) 7,15 (s, 1 H) 7,88 (s, 1 H) 8,05 (s, 1 H) 8,26 (d, J=2,35 Гц, 1 H) 8,66 (d, J=1,76 Гц, 1 H);
[2168] MS (ESI, масса/заряд): 449,3 [M+H]+
[2169] Пример 427. 2-амино-N-((3S,4S)-1-бензил-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[2170] Используя бензальдегид, названное соединение получали, как описано для примера 426.
[2171] 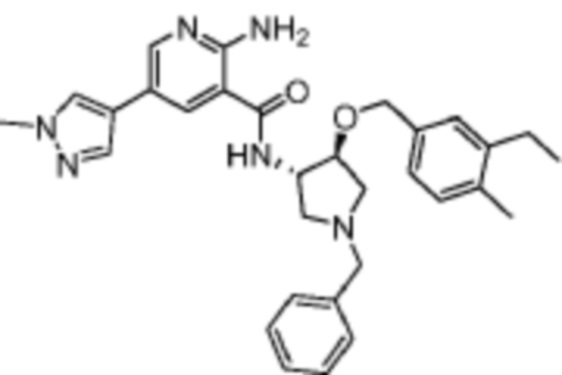
[2172] MS (ESI, масса/заряд): 525,7 [M+H]+
[2173] Пример 428. 2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)-1-(3-фенилпропил)пирролидин-3-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[2174] Используя 3-фенилпропаналь, названное соединение получали, как описано для примера 426.
[2175] 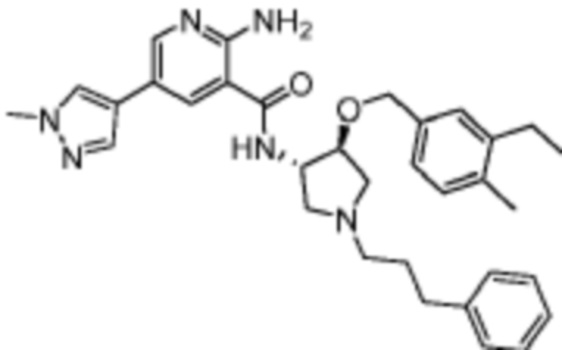
[2176] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,14 (t, J=7,63 Гц, 3 H) 1,97-2,13 (m, 2 H) 2,22 (s, 3 H) 2,58 (q, J=7,63 Гц, 2 H) 2,70 (t, J=7,63 Гц, 2 H) 3,27 (t, J=7,63 Гц, 2 H) 3,43-3,54 (m, 1 H) 3,60-3,71 (m, 1 H) 3,73-3,84 (m, 1 H) 3,92 (s, 3 H) 4,08-4,23 (m, 1 H) 4,36 (br s, 1 H) 4,6 -4,72 (m, 3 H) 7,01-7,10 (m, 2 H) 7,12-7,15 (m, 1 H) 7,15-7,30 (m, 5 H) 7,87 (s, 1 H) 8,04 (s, 1 H) 8,25 (d, J=1,76 Гц, 1 H) 8,64 (br s, 1 H);
[2177] MS (ESI, масса/заряд): 553,3 [M+H]+
[2178] Пример 429. 2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)-1-фенетилпирролидин-3-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[2179] Используя фенилацетальдегид, названное соединение получали, как описано для примера 426.
[2180] 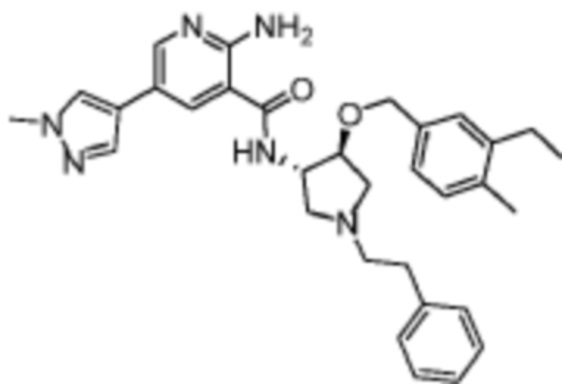
[2181] MS (ESI, масса/заряд): 539,3 [M+H]+
[2182] Пример 430. 2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)-1-изобутилпирролидин-3-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[2183] Используя изобутиральдегид, названное соединение получали, как описано для примера 426.
[2184] 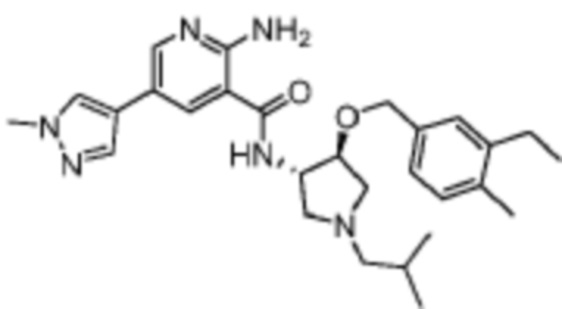
[2185] 1H-ЯМР (600 MГц, CD3OD) δ ppm 1,04 (br d, J=3,52 Гц, 6 H) 1,14 (t, J=7,63 Гц, 3 H) 2,10 (dt, J=13,65, 6,97 Гц, 1 H) 2,22 (s, 3 H) 2,58 (q, J=7,63 Гц, 2 H) 3,14 (br d, J=6,46 Гц, 2 H) 3,32-3,42 (m, 1 H) 3,52 (br s, 1 H) 3,70-3,83 (m, 1 H) 3,93 (s, 3 H) 3,99-4,17 (m, 1 H) 4,41 (br d, J=16,43 Гц, 1 H) 4,59-4,75 (m, 3 H) 7,02-7,12 (m, 2 H) 7,15 (br s, 1 H) 7,87 (br s, 1 H) 8,05 (br d, J=11,15 Гц, 1 H) 8,28 (d, J=1,76 Гц, 1 H) 8,59 (br s, 1 H);
[2186] MS (ESI, масса/заряд): 491,3 [M+H]+
[2187] Пример 431. 2-амино-N-((3S,4S)-1-бутил-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[2188] Используя бутиральдегид, названное соединение получали, как описано для примера 426.
[2189] 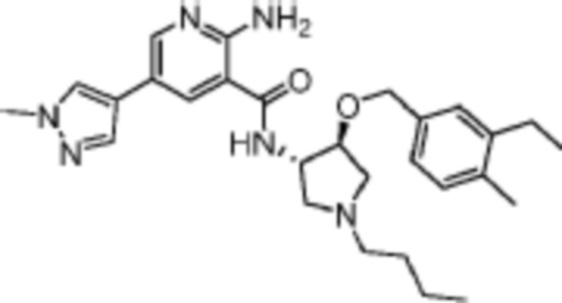
[2190] MS (ESI, масса/заряд): 491,4 [M+H]+
[2191] Пример 432. 2-амино-N-((3S,4S)-1-этил-4-((3-этил-4-метилбензил)окси)пирролидин-3-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[2192] Используя ацетальдегид, названное соединение получали, как описано для примера 426.
[2193] 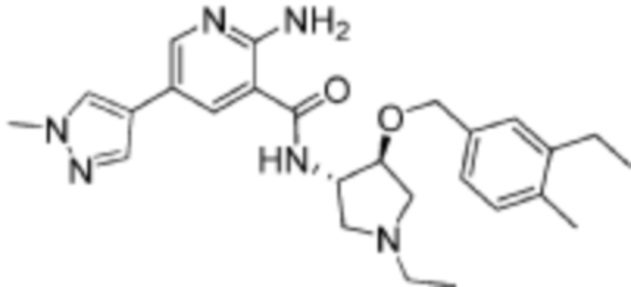
[2194] MS (ESI, масса/заряд): 463,3 [M+H]+
[2195] Пример 433. 2-амино-N-((3S,4S)-4-((3-этил-4-метилбензил)окси)-1-метилпирролидин-3-ил)-5-(1-(1-метилпиперидин-4-ил)-1H-пиразол-4-ил)никотинамид
[2196] Названное соединение получали из соединения 359, как описано для примера 426.
[2197] 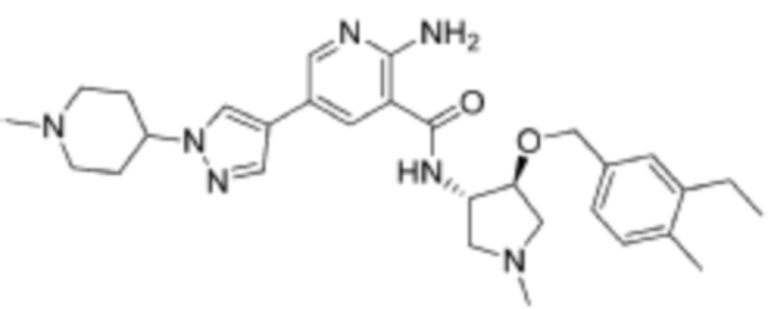
[2198] MS (ESI, масса/заряд): 532,3 [M+H]+
[2199] Пример 434 и пример 435.
[2200] Схема получения соединений из примера 434 и 435:
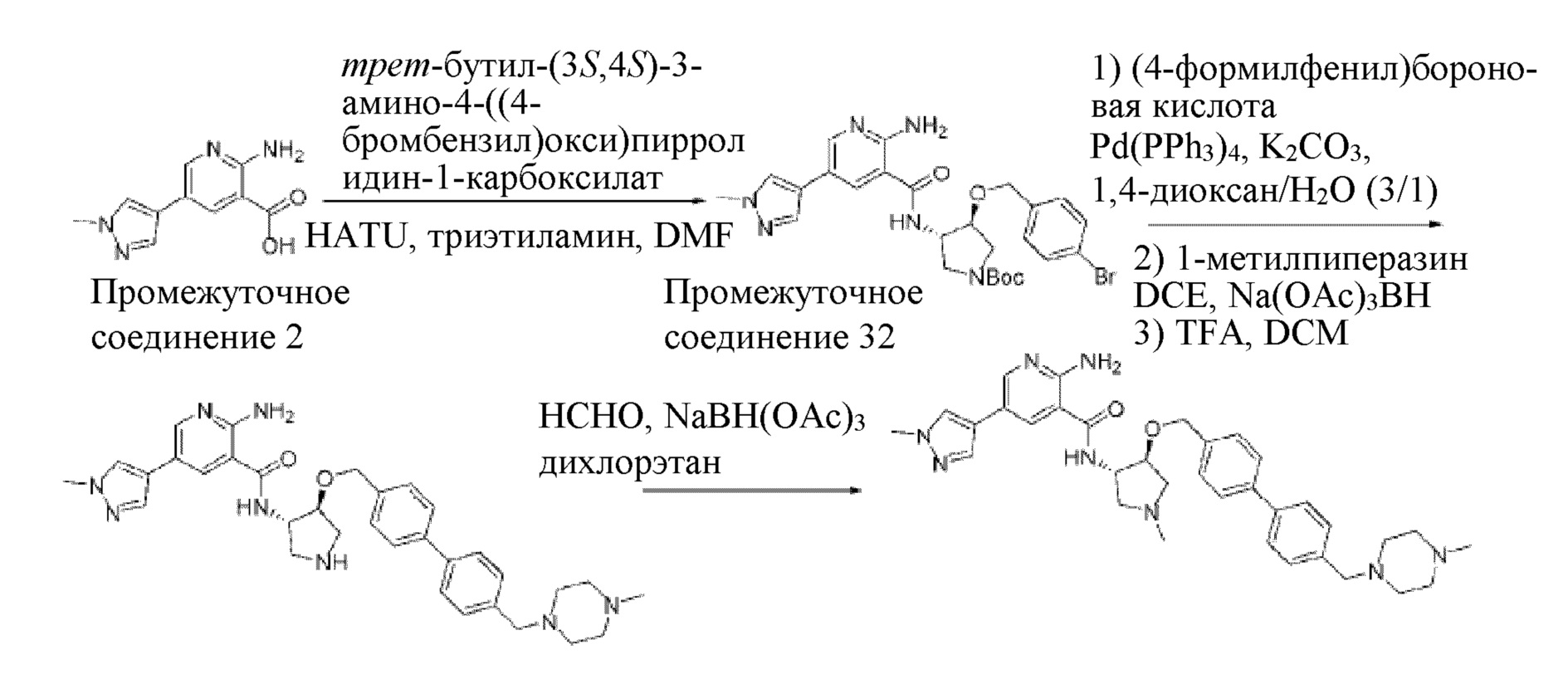
[2201]
[2202] Промежуточное соединение 32.
[2203] В смесь промежуточного соединения 2 (350 мг, 1,60 ммоль) и триэтиламина (0,34 мл, 2,41 ммоль) в 4 мл DMF добавляли HATU (732 мг, 1,92 ммоль), а затем трет-бутил (3S,4S)-3-амино-4-((4-бромбензил)окси)пирролидин-1-карбоксилат (657 мг, 1,76 ммоль). Смесь перемешивали при комнатной температуре в течение 1 часа, а затем добавляли насыщенный раствор бикарбоната натрия. Смесь экстрагировали при помощи EtOAc, промывали солевым раствором, сушили над MgSO4 и концентрировали in vacuo. Неочищенный продукт очищали колоночной хроматографией на силикагеле с получением 700 мг грязно-белого твердого вещества
[2204] 1H-ЯМР (600 MГц, CDCl3)
[2205] ppm 1,43 (br s, 9 H) 3,42 (br d, J=10,56 Гц, 1 H) 3,51-3,65 (m, 2 H) 3,80 (dd, J=12,03, 5,58 Гц, 1 H) 3,89 (s, 3 H) 4,03-4,20 (m, 1 H) 4,54-4,77 (m, 3 H) 6,29 (br s, 2 H) 7,25 (br d, J=8,22 Гц, 2 H) 7,46 (br d, J=8,22 Гц, 2 H) 7,53 (br s, 1 H) 7,57-7,67 (m, 2 H) 8,29 (d, J=1,76 Гц, 1 H);
[2206] MS (ESI, масса/заряд): 571,2 [M+H]+
[2207] Пример 434. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((3S,4S)-4-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)пирролидин-3-ил)никотинамид
[2208] В смесь промежуточного соединения 32 (40 мг, 0,07 ммоль) и пинаколинового сложного эфира 4-((4-метилпиперазин-1-ил)метилфенилбороновой кислоты (27 мг, 0,08 ммоль) в 0,4 мл 1,4-диоксана/воды (3/1) добавляли K2CO3 (29 мг, 0,21 ммоль), а затем Pd(PPh3)4 (4 мг, 0,003 ммоль) Pd(PPh3)4. Реакционную смесь нагревали при 100°C в течение 3 часов, охлаждали до комнатной температуры и экстрагировали при помощи EtOAc, сушили над безводным MgSO4 и концентрировали под вакуумом. Неочищенный остаток растворяли в 0,5 мл CH2Cl2/TFA (10/1) и смесь перемешивали в течение 2 часов. После концентрирования под вакуумом неочищенный остаток очищали препаративной HPLC с получением 30 мг названного соединения.
[2209] 1H-ЯМР (600 MГц, CD3OD) δ ppm 2,88 (s, 3 H) 2,91-3,13 (m, 4 H) 3,31-3,46 (m, 4 H) 3,52-3,65 (m, 3 H) 3,80 (dd, J=12,91, 7,04 Гц, 1 H) 3,87-3,96 (m, 5 H) 4,39-4,45 (m, 1 H) 4,71-4,83 (m, 3 H) 7,46 (br d, J=8,22 Гц, 2 H) 7,49 (br d, J=8,22 Гц, 2 H) 7,62 (dd, J=8,22, 2,35 Гц, 4 H) 7,87 (s, 1 H) 8,04 (s, 1 H) 8,25 (d, J=1,76 Гц, 1 H) 8,65 (d, J=1,76 Гц, 1 H);
[2210] MS (ESI, масса/заряд): 581,4 [M+H]+
[2211] Пример 435. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((3S,4S)-1-метил-4-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)пирролидин-3-ил)никотинамид
[2212] В смесь соединения 434 (52 мг, 0,09 ммоль) в 0,4 мл 1,2-дихлорэтана добавляли формальдегид (0,015 мл, 0,18 ммоль), а затем NaBH(OAc)3 (38 мг, 0,28 ммоль). Смесь перемешивали при комнатной температуре в течение 1 часа, а затем добавляли воду. Смесь экстрагировали при помощи EtOAc, промывали солевым раствором, сушили над MgSO4 и концентрировали in vacuo. Неочищенный остаток очищали препаративной HPLC с получением 35 мг названого соединения.
[2213] 1H-ЯМР (600 MГц, CD3OD) δ ppm 2,94 (s, 3 H) 3,04 (s, 3 H) 3,36-3,47 (m, 6 H) 3,48-3,58 (m, 6 H) 3,91 (s, 3 H) 4,27 (s, 2 H) 4,44 (br s, 1 H) 4,72-4,83 (m, 3 H) 7,49 (d, J=8,22 Гц, 2 H) 7,53 (d, J=8,22 Гц, 2 H) 7,61 (d, J=8,22 Гц, 2 H) 7,66 (d, J=8,22 Гц, 2 H) 7,86 (s, 1 H) 8,03 (s, 1 H) 8,22 (d, J=1,76 Гц, 1 H) 8,67 (d, J=2,35 Гц, 1 H);
[2214] MS (ESI, масса/заряд): 595,3 [M+H]+
[2215] Пример 436. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((3S,4S)-4-((4'-((4-метилпиперазин-1-ил)метил)-3'-(трифторметил)-[1,1'-бифенил]-4-ил)метокси)пирролидин-3-ил)никотинамид
[2216] Используя пинаколиновый сложный эфир (4-формил-3-(трифторметил)фенил)бороновой кислоты, названное соединение получали, как описано для примера 434.
[2217] 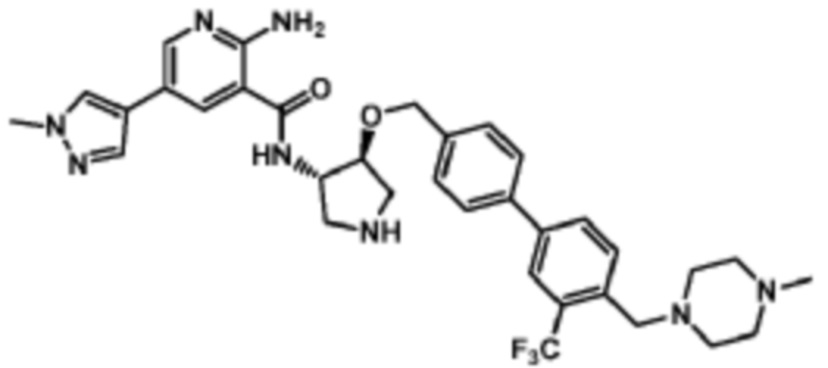
[2218] MS (ESI, масса/заряд): 649,3 [M+H]+
[2219] Пример 437. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((3S,4S)-1-метил-4-((4'-((4-метилпиперазин-1-ил)метил)-3'-(трифторметил)-[1,1'-бифенил]-4-ил)метокси)пирролидин-3-ил)никотинамид
[2220] Названное соединение получали из соединения 436, как описано для примера 435.
[2221] 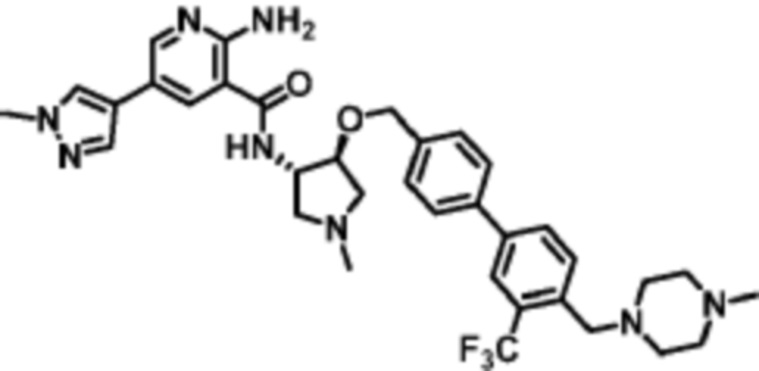
[2222] MS (ESI, масса/заряд): 663,3 [M+H]+
[2223] Пример 438. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((3S,4S)-4-((4'-(1-(4-метилпиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)пирролидин-3-ил)никотинамид
[2224] Используя (4-ацетилфенил)бороновую кислоту, названное соединение получали, как описано для примера 434.
[2225] 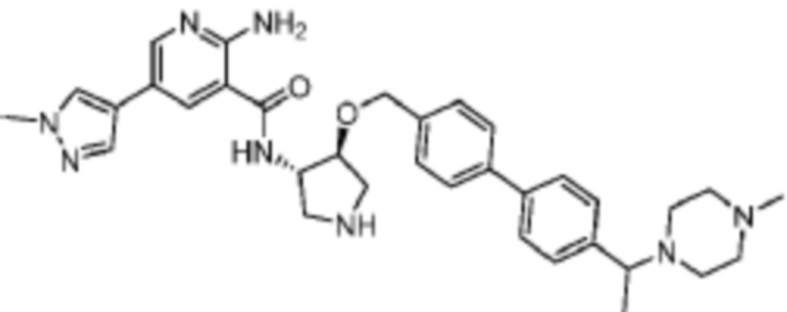
[2226] MS (ESI+) масса/заряд 595,3 [M+H]+
[2227] Пример 439. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((3S,4S)-1-метил-4-((4'-(1-(4-метилпиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)пирролидин-3-ил)никотинамид
[2228] Названное соединение получали из соединения 438, как описано для примера 435.
[2229] 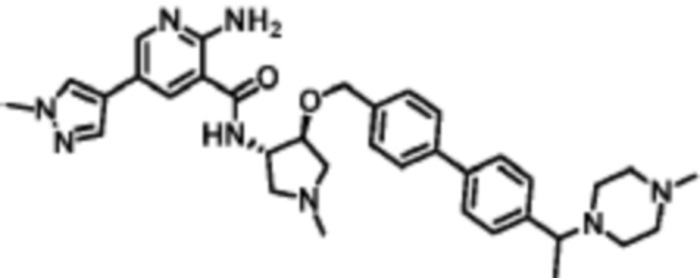
[2230] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,65 (d, J=7,04 Гц, 3 H) 2,90 (s, 3 H) 3,05 (s, 3 H) 3,08-3,17 (m, 2 H) 3,46 (br s, 4 H) 3,93 (s, 3 H) 4,16 (br d, J=6,65 Гц, 2 H) 4,49 (s, 1 H) 4,75-4,87 (m, 3 H) 7,51 (dd, J=8,22, 4,70 Гц, 4 H) 7,57-7,70 (m, 4 H) 7,88 (s, 1 H) 8,05 (s, 1 H) 8,26 (d, J=1,96 Гц, 1 H) 8,68 (d, J=1,96 Гц, 1 H); MS (ESI+) масса/заряд 609,4 [M+H]+
[2231] Пример 440. 2-амино-N-((3S,4S)-4-((4'-(2-(4-(2-гидроксиэтил)пиперазин-1-ил)пропан-2-ил)-[1,1'-бифенил]-4-ил)метокси)пирролидин-3-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[2232] Используя пинаколиновый сложный эфир (4-(2-(4-(2-гидроксиэтил)пиперазин-1-ил)пропан-2-ил)фенил)бороновой кислоты, названное соединение получали, как описано для примера 434.
[2233] 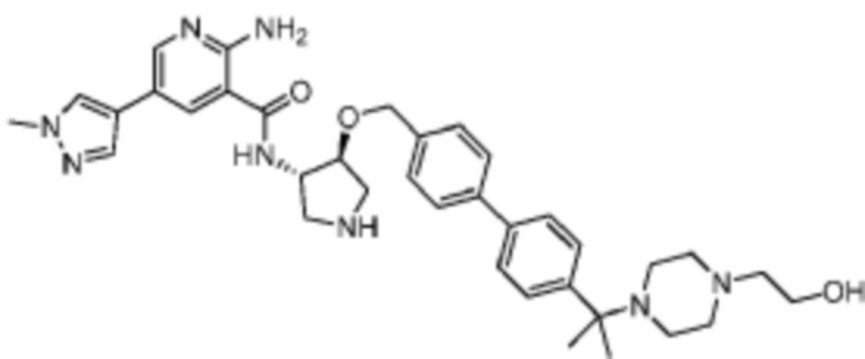
[2234] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,77 (s, 6 H) 3,50-3,68 (m, 6 H) 3,80 (s, 1 H) 3,83-3,89 (m, 2 H) 3,92 (s, 3 H) 4,42 (br d, J=4,30 Гц, 1 H) 4,73-4,88 (m, 3 H) 7,52 (d, J=8,22 Гц, 2 H) 7,65 (d, J=8,22 Гц, 2 H) 7,67-7,84 (m, 3 H) 7,86-7,92 (m, 1 H) 8,06 (s, 1 H) 8,26 (d, J=2,35 Гц, 1 H) 8,70 (d, J=2,35 Гц, 1 H);
[2235] MS (ESI, масса/заряд): 639,4 [M+H]+
[2236] Пример 441. 2-амино-N-((3S,4S)-4-((4'-(2-(4-(2-гидроксиэтил)пиперазин-1-ил)пропан-2-ил)-[1,1'-бифенил]-4-ил)метокси)-1-метилпирролидин-3-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[2237] Названное соединение получали из соединения 440, как описано для примера 435.
[2238] 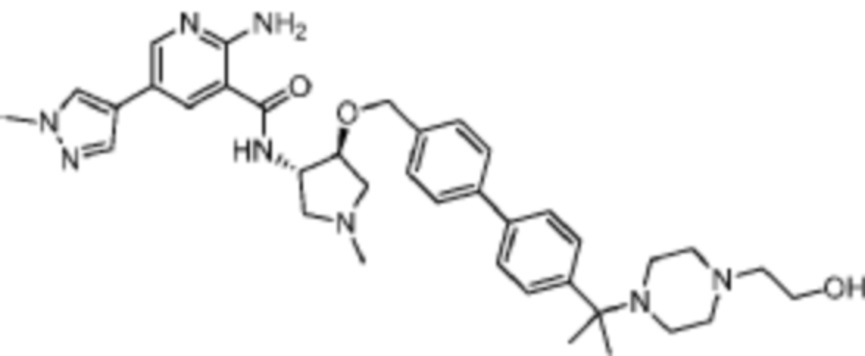
[2239] MS (ESI, масса/заряд): 653,4 [M+H]+
[2240] Пример 442. 2-амино-N-((3S,4S)-4-((4'-(1-(4-(2-гидроксиэтил)пиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)пирролидин-3-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[2241] Используя пинаколиновый сложный эфир (4-(1-(4-(2-гидроксиэтил)пиперазин-1-ил)этил)фенил)бороновой кислоты, названное соединение получали, как описано для примера 434.
[2242] 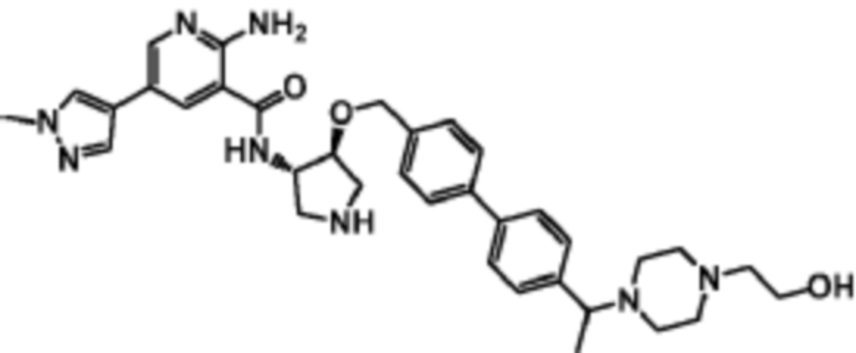
[2243] MS (ESI, масса/заряд): 625,4 [M+H]+
[2244] Пример 443. 2-амино-N-((3S,4S)-4-((4'-(1-(4-(2-гидроксиэтил)пиперазин-1-ил)этил)-[1,1'-бифенил]-4-ил)метокси)-1-метилпирролидин-3-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[2245] Названное соединение получали из соединения 442, как описано для примера 435.
[2246] 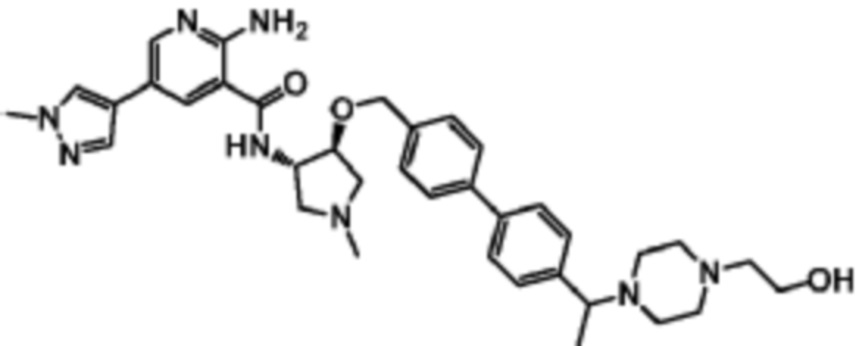
[2247] MS (ESI, масса/заряд): 639,4 [M+H]+
[2248] Пример 444. 2-амино-N-((3S,4S)-4-((4'-((4-(2-гидроксиэтил)пиперазин-1-ил)метил)-3'-(трифторметил)-[1,1'-бифенил]-4-ил)метокси)пирролидин-3-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[2249] Используя пинаколиновый сложный эфир (4-((4-(2-гидроксиэтил)пиперазин-1-ил)метил)-3-(трифторметил)фенил)бороновой кислоты, названное соединение получали, как описано для примера 434.
[2250] 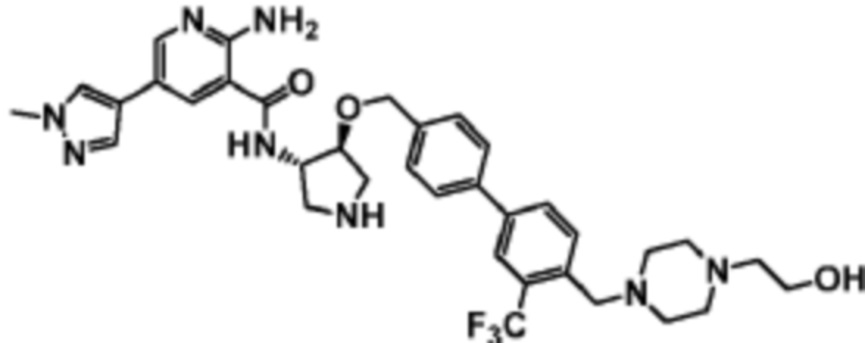
[2251] MS (ESI, масса/заряд): 679,3 [M+H]+
[2252] Пример 445. 2-амино-N-((3S,4S)-4-((4'-((4-(2-гидроксиэтил)пиперазин-1-ил)метил)-3'-(трифторметил)-[1,1'-бифенил]-4-ил)метокси)-1-метилпирролидин-3-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[2253] Используя 1-(4-бром-2-(трифторметил)бензил)пиперазин, названное соединение получали, как описано для примера 435.
[2254] 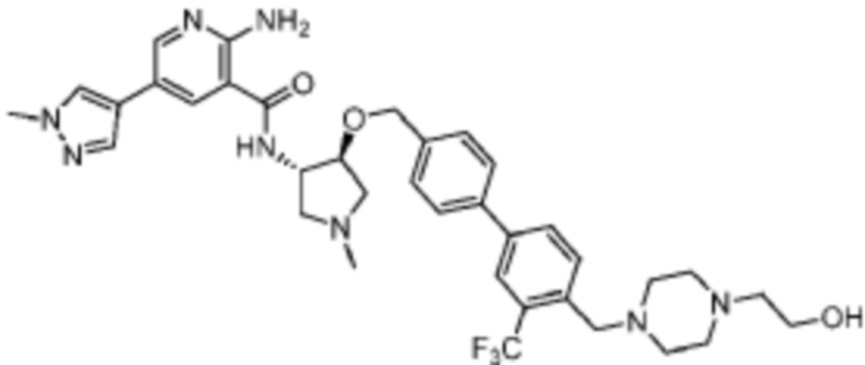
[2255] MS (ESI, масса/заряд): 693,3 [M+H]+
[2256] Пример 446. 2-амино-N-((3S,4S)-4-((4'-((4-(2-гидроксиэтил)пиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)пирролидин-3-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[2257] Используя пинаколиновый сложный эфир (4-((4-(2-гидроксиэтил)пиперазин-1-ил)метил)фенил)бороновой кислоты, названное соединение получали, как описано для примера 434.
[2258] 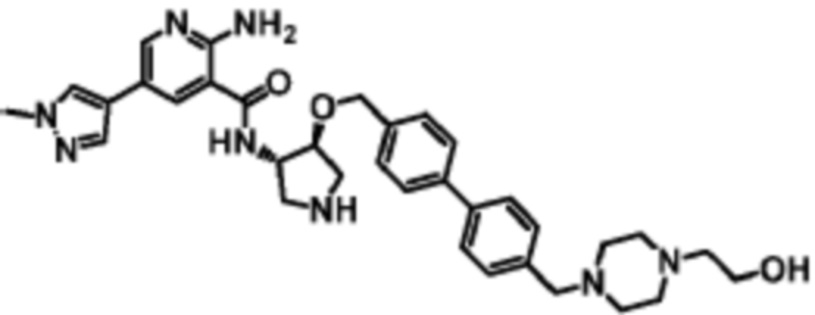
[2259] MS (ESI, масса/заряд): 611,3 [M+H]+
[2260] Пример 447. 2-амино-N-((3S,4S)-4-((4'-((4-(2-гидроксиэтил)пиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)-1-метилпирролидин-3-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[2261] Названное соединение получали из соединения 446, как описано для примера 435.
[2262] 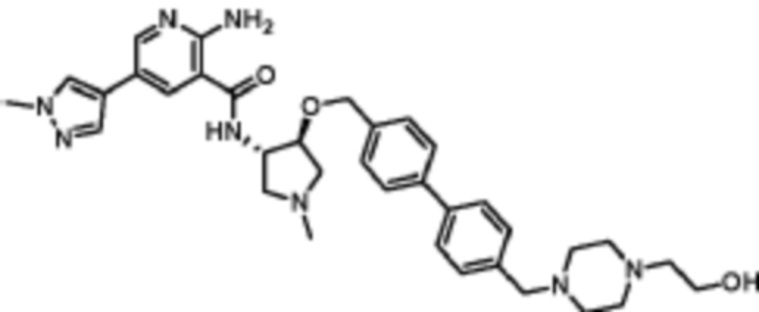
[2263] MS (ESI, масса/заряд): 625,4 [M+H]+
[2264] Пример 448. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((3S,4R)-4-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)тетрагидрофуран-3-ил)никотинамид
[2265] Схема получения соединения из примера 448:
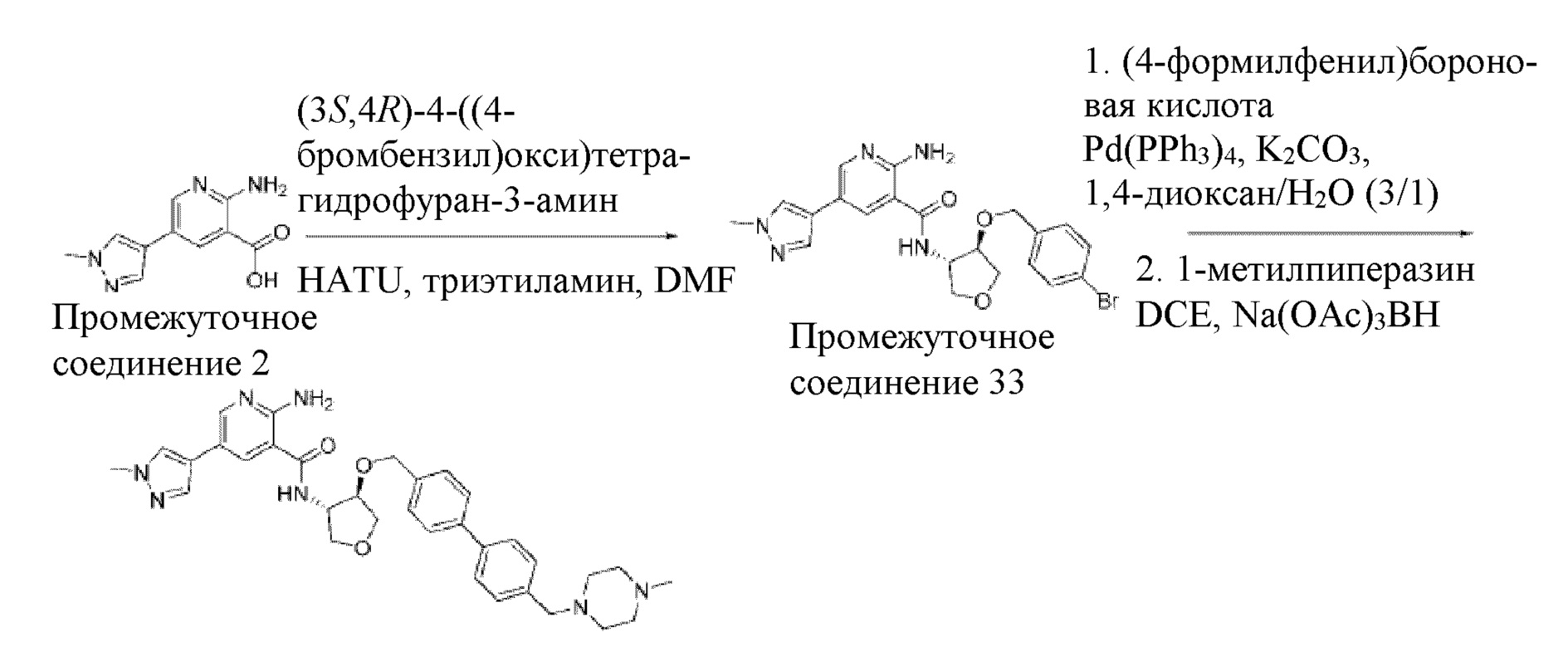
[2266]
[2267] Промежуточное соединение 33.
[2268] Используя промежуточное соединение 2 и (3S,4R)-4-((4-бромбензил)окси)тетрагидрофуран-3-амин, названное соединение получали, как описано для промежуточного соединения 4.
[2269] 1H-ЯМР (600 MГц, CD3OD) δ ppm 3,81 (td, J=10,27, 2,35 Гц, 2 H) 3,91 (s, 3 H) 4,05 (dd, J=9,98, 5,28 Гц, 1 H) 4,11 (dd, J=9,39, 5,87 Гц, 1 H) 4,13-4,16 (m, 1 H) 4,55 (dd, J=3,81, 2,05 Гц, 1 H) 4,60 (s, 2 H) 4,63 (d, J=12,33 Гц, 1 H) 4,74 (d, J=12,33 Гц, 1 H) 7,30 (m, J=8,22 Гц, 2 H) 7,45-7,49 (m, 2 H) 7,78 (s, 1 H) 7,90 (s, 1 H) 8,07 (d, J=2,35 Гц, 1 H) 8,26 (d, J=1,76 Гц, 1 H);
[2270] MS (ESI, масса/заряд): 472,1 [M+H]+
[2271] Пример 448. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((3S,4R)-4-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)тетрагидрофуран-3-ил)никотинамид
[2272] Используя промежуточное соединение 33, названное соединение получали, как описано для примера 172.
[2273] 1H-ЯМР (600 MГц, CD3OD) δ ppm 2,87 (s, 3 H) 3,80-3,89 (m, 4 H) 3,92 (s, 3 H) 4,04-4,15 (m, 2 H) 4,19-4,25 (m, 1 H) 4,57-4,63 (m, 1 H) 4,71 (d, J=11,74 Гц, 1 H) 4,82 (d, J=11,74 Гц, 1 H) 7,40-7,51 (m, 4 H) 7,57-7,63 (m, 4 H) 7,88 (s, 1 H) 8,02 (s, 1 H) 8,23 (s, 1 H) 8,62 (s, 1 H);
[2274] MS (ESI, масса/заряд): 582,3 [M+H]+
[2275] Пример 449. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((3S,4R)-4-((4'-((4-метилпиперазин-1-ил)метил)-3'-(трифторметил)-[1,1'-бифенил]-4-ил)метокси)тетрагидрофуран-3-ил)никотинамид
[2276] Используя пинаколиновый сложный эфир (4-формил-3-(трифторметил)фенил)бороновой кислоты, названное соединение получали, как описано для примера 448.
[2277] 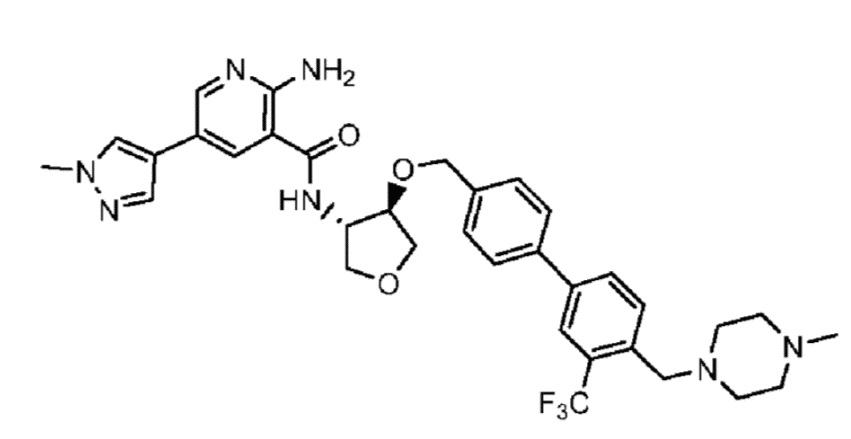
[2278] 1H-ЯМР (400 MГц, CD3OD) δ ppm 2,91 (s, 3 H) 3,80-3,91 (m, 3 H) 3,94 (s, 2 H) 4,12 (td, J=9,59, 5,48 Гц, 2 H) 4,23 (br s, 1 H) 4,62 (br s, 1 H) 4,74 (d, J=12,13 Гц, 1 H) 7,52 (d, J=8,61 Гц, 2 H) 7,65 (d, J=8,22 Гц, 2 H) 7,88 (d, J=13,30 Гц, 4 H) 8,03 (s, 1 H) 8,25 (d, J=1,96 Гц, 1 H) 8,63 (d, J=1,96 Гц, 1 H);
[2279] MS (ESI, масса/заряд): 650,3 [M+H]+
[2280] Пример 450. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-((3S,4R)-4-((4'-(2-(4-метилпиперазин-1-ил)пропан-2-ил)-[1,1'-бифенил]-4-ил)метокси)тетрагидрофуран-3-ил)никотинамид
[2281] Используя пинаколиновый сложный эфир (4-формил-3-(трифторметил)фенил)бороновой кислоты, названное соединение получали, как описано для примера 448.
[2282] 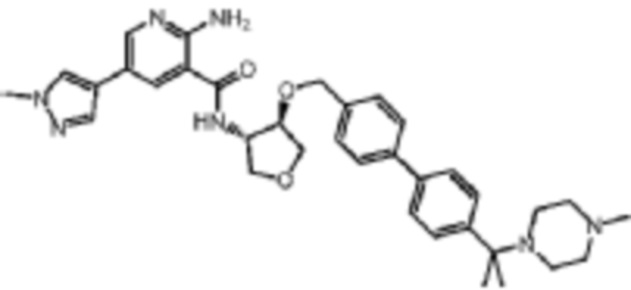
[2283] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,62 (s, 6 H) 2,89 (s, 3 H) 3,04 (br s, 2 H) 3,34-3,47 (m, 4 H) 3,82-3,91 (m, 2 H) 3,93 (s, 3 H) 4,12 (td, J=10,56, 5,48 Гц, 2 H) 4,22 (br s, 1 H) 4,61 (br s, 1 H) 4,66-4,77 (m, 1 H) 4,81-4,88 (m, 1 H) 7,47 (d, J=7,83 Гц, 2 H) 7,58-7,70 (m, 6 H) 7,89 (s, 1 H) 8,03 (s, 1 H) 8,24 (d, J=1,96 Гц, 1 H) 8,65 (d, J=1,96 Гц, 1 H);
[2284] MS (ESI, масса/заряд): 610,2 [M+H]+
[2285] Пример 451. 2-амино-N-((3S,4R)-4-((4'-((4-(2-гидроксиэтил)пиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)тетрагидрофуран-3-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[2286] Используя пинаколиновый сложный эфир (4-((4-(2-гидроксиэтил)пиперазин-1-ил)метил)фенил)бороновой кислоты, названное соединение получали, как описано для примера 448.
[2287] 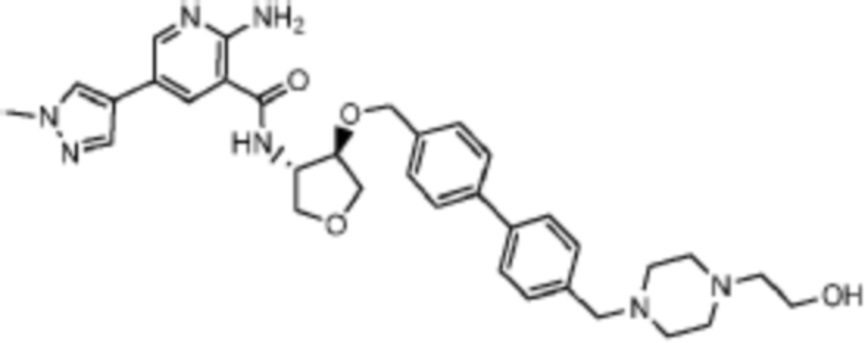
[2288] MS (ESI, масса/заряд): 612,3 [M+H]+
[2289] Пример 452. 2-амино-N-((3S,4R)-4-((4'-((4-(2-гидроксиэтил)пиперазин-1-ил)метил)-3'-(трифторметил)-[1,1'-бифенил]-4-ил)метокси)тетрагидрофуран-3-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[2290] Используя пинаколиновый сложный эфир (4-((4-(2-гидроксиэтил)пиперазин-1-ил)метил)-3-(трифторметил)фенил)бороновой кислоты, названное соединение получали, как описано для примера 448.
[2291] 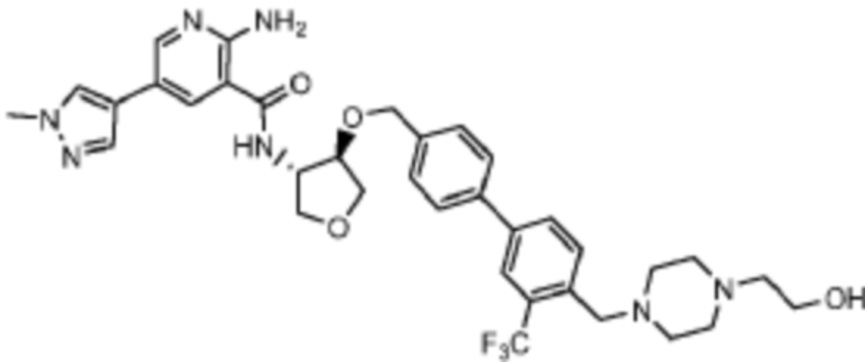
[2292] 1H-ЯМР (400 MГц, CD3OD) δ ppm 2,62 (br s, 4 H) 3,25-3,29 (m, 2 H) 3,34-3,40 (m, 2 H) 3,82-3,84 (m, 2 H) 3,85-3,91 (m, 2 H) 3,94 (s, 2 H) 4,06-4,17 (m, 2 H) 4,23 (br s, 1 H) 4,62 (br s, 1 H) 4,74 (m, 1 H) 7,52 (m, J=8,22 Гц, 2 H) 7,65 (m, J=8,22 Гц, 2 H) 7,86 (s, 2 H) 7,89 (s, 2 H) 8,03 (s, 1 H) 8,25 (d, J=1,96 Гц, 1 H) 8,63 (d, J=1,96 Гц, 1 H);
[2293] MS (ESI, масса/заряд): 680,3 [M+H]+
[2294] Пример 453. 2-амино-N-((3S,4R)-4-((4'-(2-(4-(2-гидроксиэтил)пиперазин-1-ил)пропан-2-ил)-[1,1'-бифенил]-4-ил)метокси)тетрагидрофуран-3-ил)-5-(1-метил-1H-пиразол-4-ил)никотинамид
[2295] Используя пинаколиновый сложный эфир (4-(2-(4-(2-гидроксиэтил)пиперазин-1-ил)пропан-2-ил)фенил)бороновой кислоты, названное соединение получали, как описано для примера 448.
[2296] 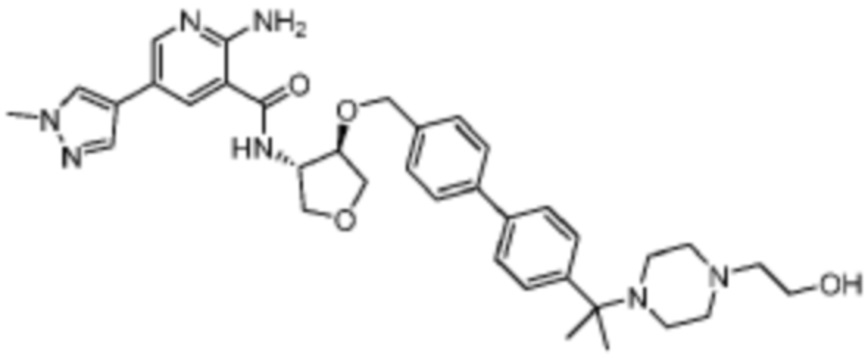
[2297] MS (ESI, масса/заряд): 640,2 [M+H]+
[2298] Пример 454. 2-амино-5-(1-метил-1H-пиразол-4-ил)-N-(транс-4-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)тетрагидрофуран-3-ил)никотинамид
[2299] Используя транс-4-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)тетрагидрофуран-3-амин, названное соединение получали, как описано для примера 448.
[2300] 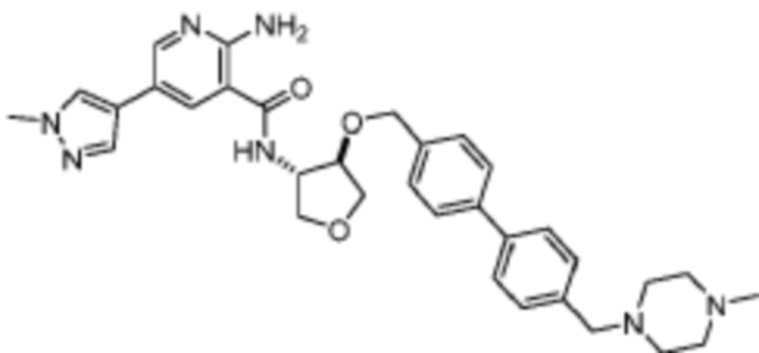
[2301] 1H-ЯМР (400 MГц, CD3OD) δ ppm 2,88 (s, 3 H) 3,76-3,89 (m, 4 H) 4,09 (ddd, J=16,92, 9,88, 5,28 Гц, 2 H) 4,20 (br d, J=4,70 Гц, 1 H) 4,57 (br s, 1 H) 4,70 (br d, J=11,74 Гц, 1 H) 6,98 (dd, J=7,43, 6,26 Гц, 1 H) 7,46 (d, J=8,22 Гц, 4 H) 7,56-7,67 (m, 4 H) 7,99-8,06 (m, 1 H) 8,40 (dd, J=7,43, 1,56 Гц, 1 H);
[2302] MS (ESI, масса/заряд): 582,3 [M+H]+
[2303] Пример 455. 2-амино-N-(транс-4-((4'-((4-метилпиперазин-1-ил)метил)-[1,1'-бифенил]-4-ил)метокси)тетрагидрофуран-3-ил)никотинамид
[2304] Используя 2-аминоникотиновую кислоту и транс-4-((4-бромбензил)окси)тетрагидрофуран-3-амин, названное соединение получали, как описано для примера 448.
[2305] 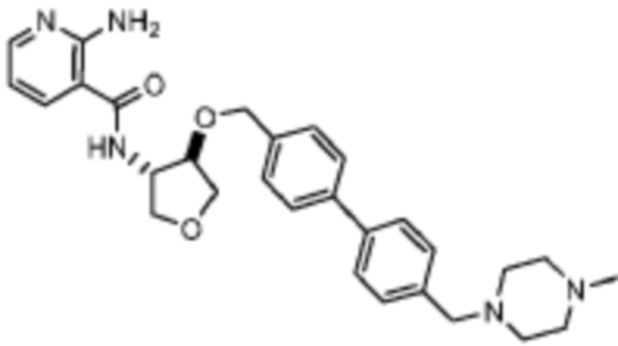
[2306] 1H-ЯМР (400 MГц, CD3OD) δ ppm 2,88 (s, 3 H) 3,76-3,89 (m, 4 H) 4,09 (ddd, J=16,92, 9,88, 5,28 Гц, 2 H) 4,20 (br d, J=4,70 Гц, 1 H) 4,57 (br s, 1 H) 4,70 (br d, J=11,74 Гц, 1 H) 6,98 (dd, J=7,43, 6,26 Гц, 1 H) 7,46 (d, J=8,22 Гц, 4 H) 7,56-7,67 (m, 4 H) 7,99-8,06 (m, 1 H) 8,40 (dd, J=7,43, 1,56 Гц, 1 H);
[2307] MS (ESI, масса/заряд): 502,3 [M+H]+
[2308] Пример 456. 2-амино-N-((1S,2S)-2-(бензилокси)циклопентил)-6-((4-((4-метилпиперазин-1-ил)метил)фенил)амино)никотинамид
[2309] Схема получения соединения из примера 456:
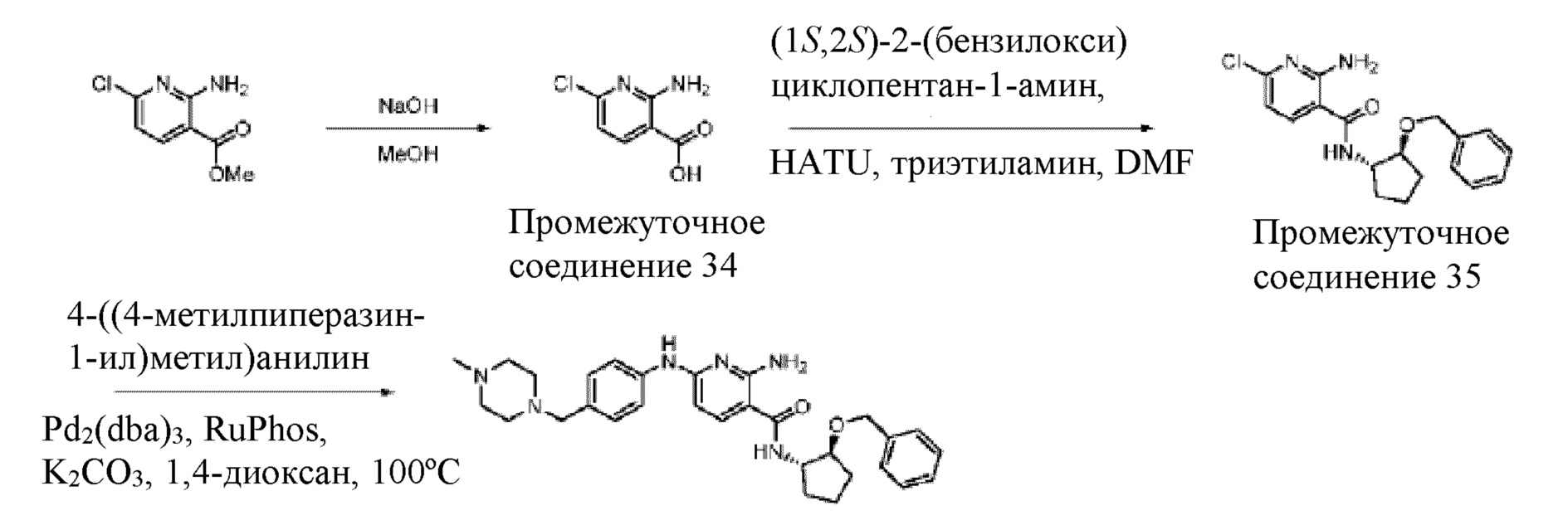
[2310]
[2311] Промежуточное соединение 34.
[2312] В суспензию метил-2-амино-6-хлорникотината (100 мг, 0,54 ммоль) в 3 мл MeOH добавляли 2 н. NaOH (1 мл, 2 ммоль) и смесь нагревали при 65°C в течение 1 часа, охлаждали до комнатной температуры, нейтрализовали (1 мл 2 н. HCl), и полученный осадок отфильтровывали, промывали при помощи MeOH и сушили с получением 80 мг грязно-белого твердого вещества.
[2313] 1H-ЯМР (400 MГц, DMSO-d6) δ ppm 6,61 (d, J=7,83 Гц, 1 H) 7,53 (br s, 2 H) 8,01 (d, J=8,22 Гц, 1 H);
[2314] MS (ESI, масса/заряд): 173,2 [M+H]+
[2315] Промежуточное соединение 35.
[2316] В смесь промежуточного соединения 34 (50 мг, 0,29 ммоль) и триэтиламина (0,061 мл, 0,43 ммоль) в 2 мл DMF добавляли HATU (132 мг, 0,35 ммоль), а затем (1S,2S)-2-(бензилокси)циклопентан-1-амин (55 мг, 0,29 ммоль). Смесь перемешивали при комнатной температуре в течение 1 часа, а затем добавляли насыщенный раствор бикарбоната натрия. Смесь экстрагировали при помощи EtOAc, промывали солевым раствором, сушили над MgSO4 и концентрировали in vacuo. Неочищенный остаток очищали препаративной HPLC с получением 80 мг названого соединения.
[2317] 1H-ЯМР (400 MГц, CDCl3) δ ppm 1,39-1,52 (m, 1 H) 1,68-1,81 (m, 2 H) 1,83-1,89 (m, 1 H) 1,89-2,02 (m, 1 H) 2,27 (td, J=13,69, 7,83 Гц, 1 H) 3,80-3,87 (m, 1 H) 4,27-4,37 (m, 1 H) 4,58-4,67 (m, 2 H) 5,79 (br d, J=6,26 Гц, 1 H) 6,51 (br s, 2H) 6,56 (d, J=7,83 Гц, 1 H) 7,25-7,37 (m, 5 H) 7,39 (d, J=7,83 Гц, 1 H);
[2318] MS (ESI, масса/заряд): 345,3 [M+H]+
[2319] Пример 456. 2-амино-N-((1S,2S)-2-(бензилокси)циклопентил)-6-((4-((4-метилпиперазин-1-ил)метил)фенил)амино)никотинамид
[2320] В смесь промежуточного соединения 35 (186 мг, 1 ммоль) и 4-((4-метилпиперазин-1-ил)метил)анилина (240 мг, 1,2 ммоль) в 5 мл 1,4-диоксана добавляли 480 мг K2CO3, а затем Pd2(dba)3 (30 мг, 0,3 ммоль). Реакционную смесь нагревали при 100°C в течение 3 часов, охлаждали до комнатной температуры и экстрагировали при помощи EtOAc, сушили над безводным MgSO4 и концентрировали под вакуумом. Неочищенный продукт очищали колоночной хроматографией на силикагеле с получением 170 мг грязно-белого твердого вещества.
[2321] 1H-ЯМР (400 MГц, CD3OD) δ ppm 1,57 (br dd, J=13,30, 7,04 Гц, 1 H) 1,66-1,87 (m, 3 H) 1,97 (dt, J=13,01, 6,60 Гц, 1 H) 2,13 (br dd, J=13,11, 6,85 Гц, 1 H) 2,95 (s, 3 H) 3,44-3,62 (m, 4 H) 3,87-3,97 (m, 1 H) 4,17 (s, 2 H) 4,31-4,39 (m, 1 H) 4,60 (s, 2 H) 6,25 (d, J=9,00 Гц, 1 H) 7,21-7,35 (m, 4 H) 7,43 (d, J=8,22 Гц, 2 H) 7,58 (d, J=8,61 Гц, 2 H) 8,08 (d, J=9,00 Гц, 1 H); MS (ESI, масса/заряд): 515,3 [M+H]+
[2322] Пример 457. 2-амино-N-((1S,2S)-2-(бензилокси)циклопентил)-6-(фениламино)никотинамид
[2323] Используя анилин, названное соединение получали, как описано для примера 456.
[2324] 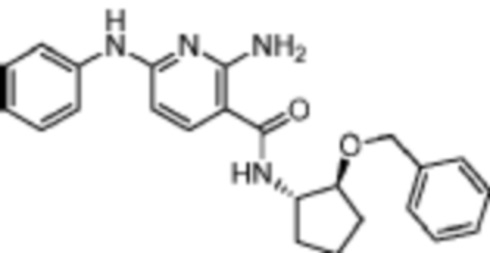
[2325] MS (ESI, масса/заряд): 403,2 [M+H]+
[2326] Пример 458. 2-амино-N-((1S,2S)-2-(бензилокси)циклопентил)-6-((4-(4-метилпиперазин-1-ил)фенил)амино)никотинамид
[2327] Используя 4-(4-метилпиперазин-1-ил)анилин, названное соединение получали, как описано для примера 456.
[2328] 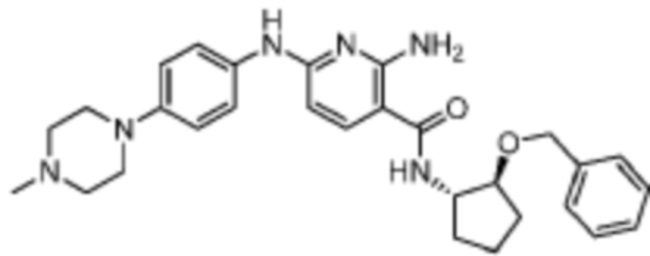
[2329] MS (ESI, масса/заряд): 501,3 [M+H]+
[2330] Биохимический анализ
[2331] Для анализа SAR (зависимости активности от структуры) и скрининга соединений использовали анализ LanthaScreen™ TR-FRET (перенос энергии флуоресценции с временным разрешением), используя меченное тербием (Tb) специфичное к фосфотирозину антитело и меченный флуоресцеином поли-GT (глутамат-тирозин) в качестве субстрата. После возбуждения при 340 нм под действием УФ-излучения энергия от Tb-донора на антителе переносится к флуоресцеину на субстрате на основе фосфорилированного поли-GT, и флуоресцеин излучает свет при 520 нм. Отношение между интенсивностью первичного излучения при 495 нм и интенсивностью вторичного излучения при 520 нм применяли для оценки уровня киназной активности. Рекомбинантные белки из c-MER человека и каталитических доменов AXL, субстрат на основе меченного флуоресцеином поли-GT, меченные Tb антитела к фосфорилированному тирозину, буфер для анализа киназы и 0,5 M раствор EDTA приобретали (Life technologies, США). Анализы TR-FRET проводили в белом 384-луночном планшете малого объема (Corning, США). Для измерения опосредованного соединением ингибирования киназной активности рекомбинантные киназы предварительно инкубировали с тестируемыми соединениями в течение 20 минут перед добавлением 200 нM субстратов на основе меченного флуоресцеином поли-GT и 10 мкM ATP, и затем реакцию проводили в течение 1 часа при комнатной температуре. Для остановки ферментативной реакции добавляли 10 мM EDTA и уровень фосфорилирования субстрата на основе поли-GT определяли после 30 мин. инкубирования с 2 нM меченного Tb антитела. Интенсивность флуоресценции измеряли при помощи планшет-ридера EnvisionTM (PerkinElmer, США).
[2332] Внутриклеточный анализ киназы MER с использованием клеточной системы BaF3
[2333] CD8-MerTK представляет собой химерный слитый белок, состоящий из внеклеточного и трансмембранного доменов CD8α человека (аминокислоты 1-209) на его N-конце и киназного домена и внутриклеточных частей MerTK (аминокислоты 521-994) на его C-конце. Для обеспечения внутриклеточного анализа киназы в отношении киназы MerTK IL-3-зависимые клетки Ba/F3, происходящие из лимфатической системы мышей, трансфицировали при помощи CD8-MerTK. Полученную линию Ba/F3-CDM затем проверяли в отношении того, что пролиферация клеток Ba/F3-CDM полностью зависит от активности киназы MerTK при выращивании в отсутствие IL-3. Для традиционного клеточного анализа клетки Ba/F3-CDM высевали в концентрации 2000 клеток на лунку в 384-луночный планшет для клеточных культур, содержащий питательную среду DMEM/10% FBS, и инкубировали в течение 24 часов перед добавлением соединений, предварительно разбавленных в питательной среде. После обработки соединениями клетки дополнительно инкубировали в течение 48 часов и измеряли пролиферацию. Чтобы отличить ингибирование роста Ba/F3 вследствие специфичного ингибирования киназы MerTK после обработки соединениями от ингибирования роста из-за неспецифичной нежелательной цитотоксичности соединений, традиционно параллельно обеспечивали контрольные группы клеток Ba/F3, которые выращивали в дополненных IL3 средах для выращивания. В присутствии IL-3 пролиферация Ba/F3 более не зависит от активности MerTK. Рост и пролиферацию клеток измеряли при помощи системы Celltiter-Glo™ (Promega, США) согласно инструкции производителя. Значение концентрации полумаксимального ингибирования роста (GI50) рассчитывали при помощи программного обеспечения Prism6.0 (GraphPad, США).
[2334] Таблица 1. Значения биохимического ингибирования IC50 и ингибирования роста клеток GI50.
[2335]
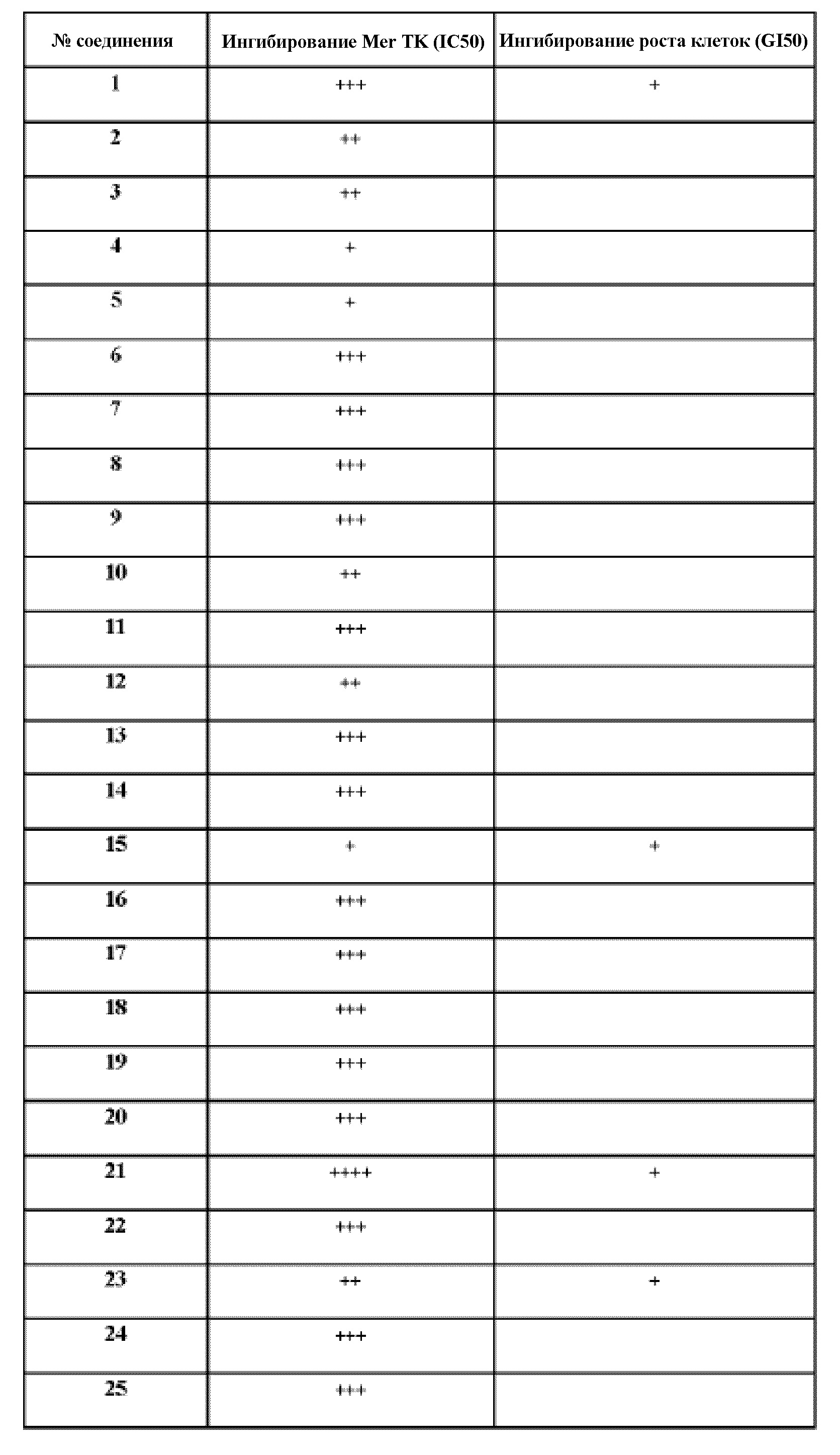
[2336]
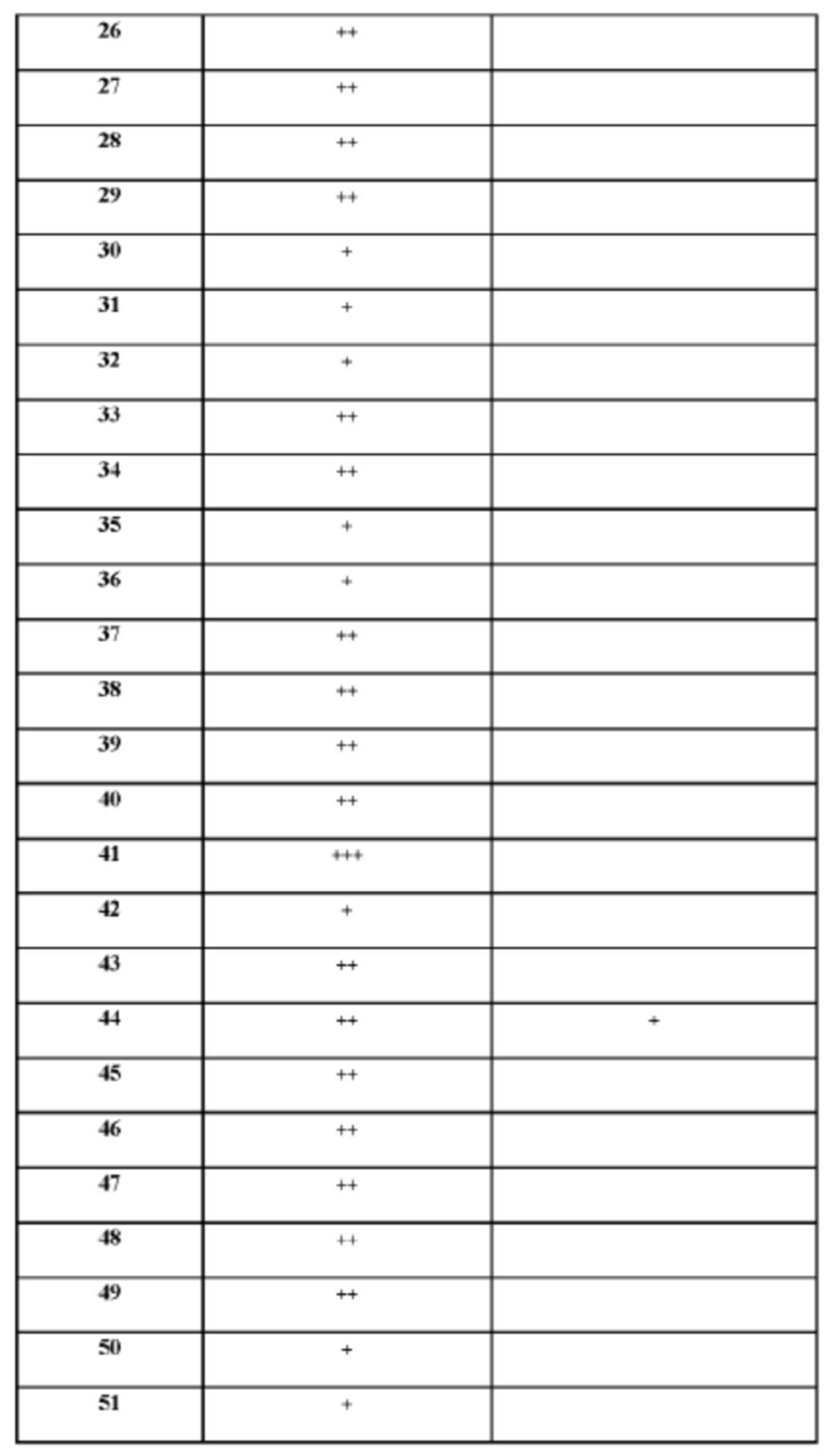
[2337]
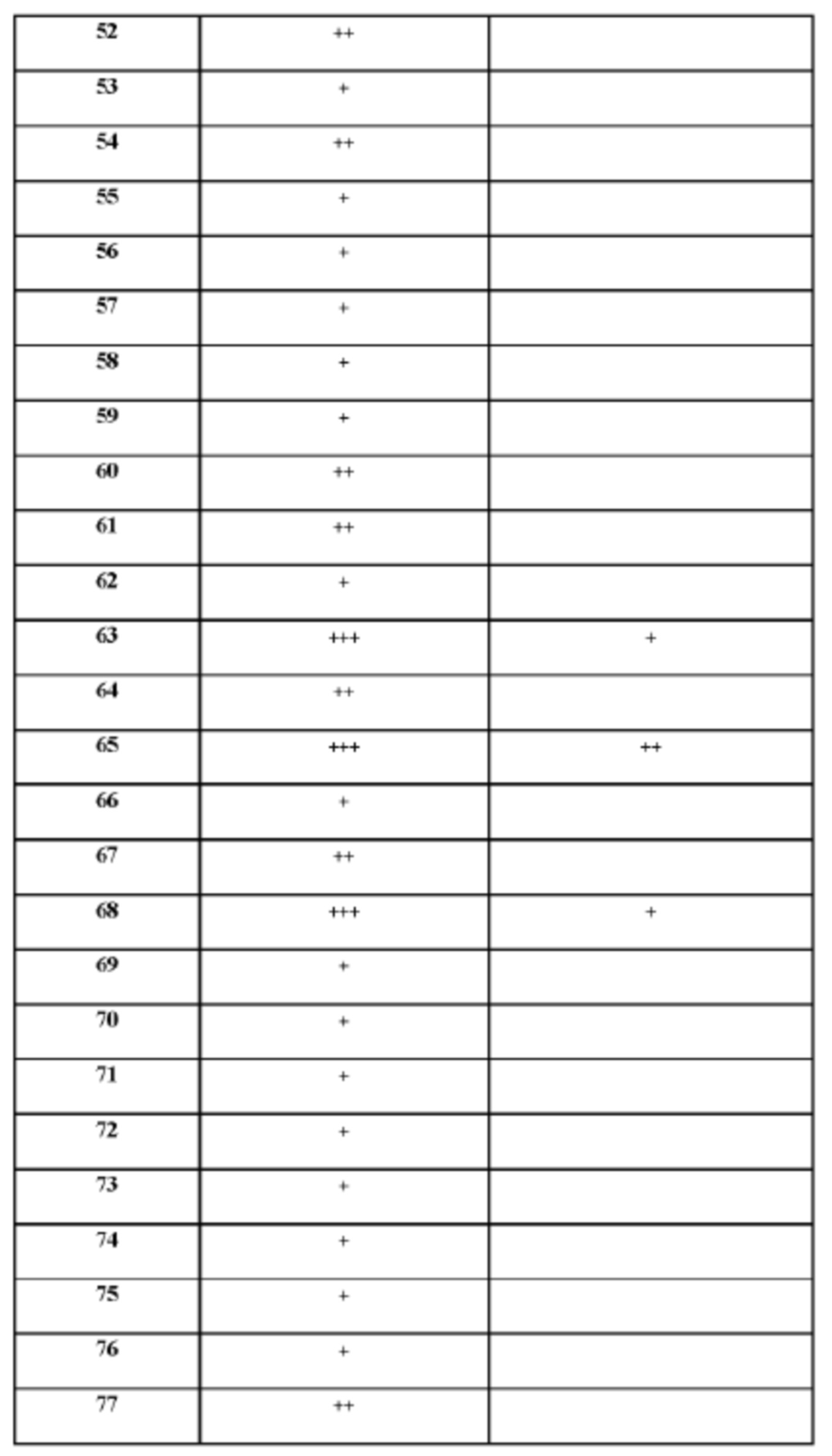
[2338]
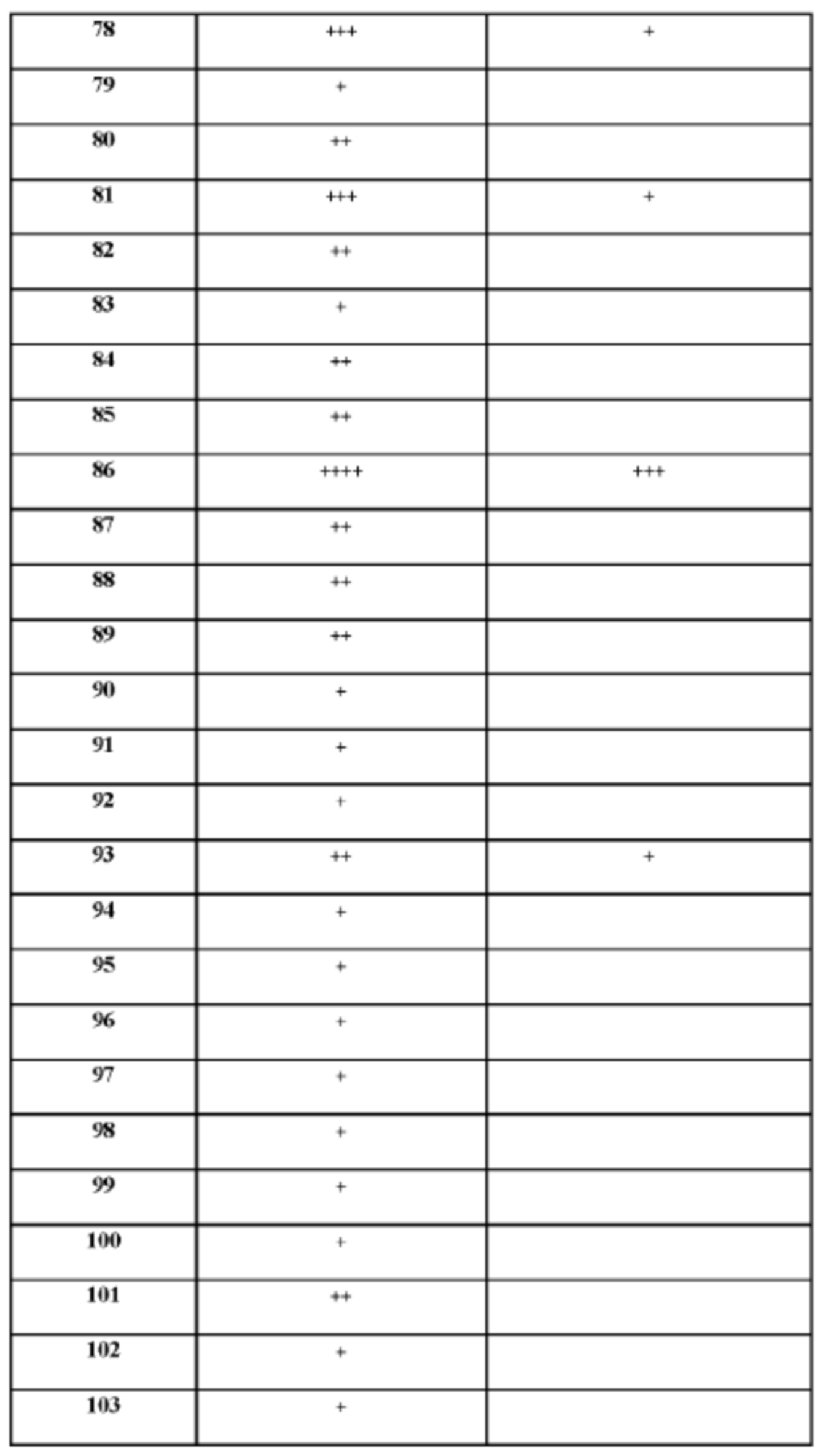
[2339]
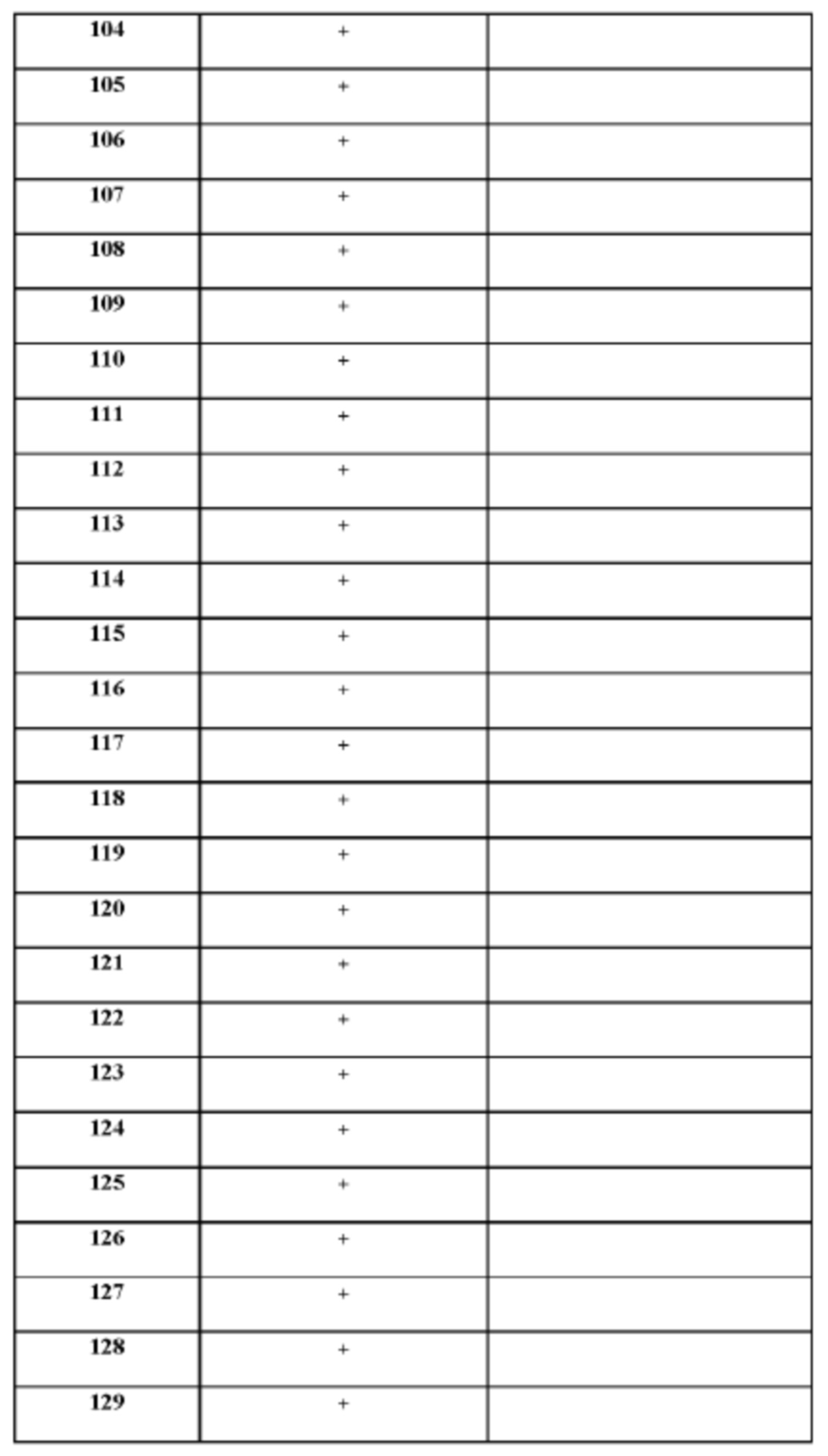
[2340]
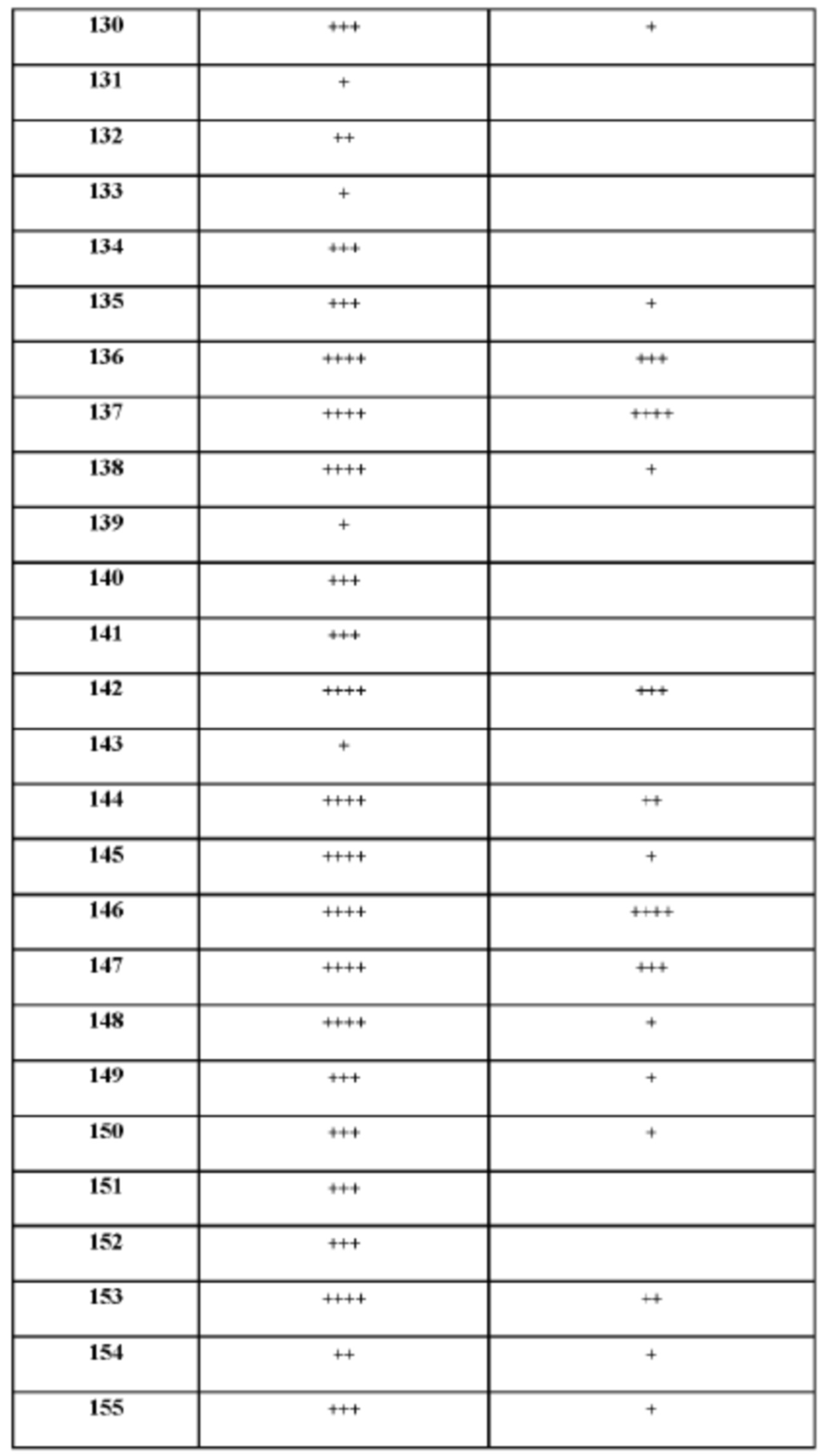
[2341]
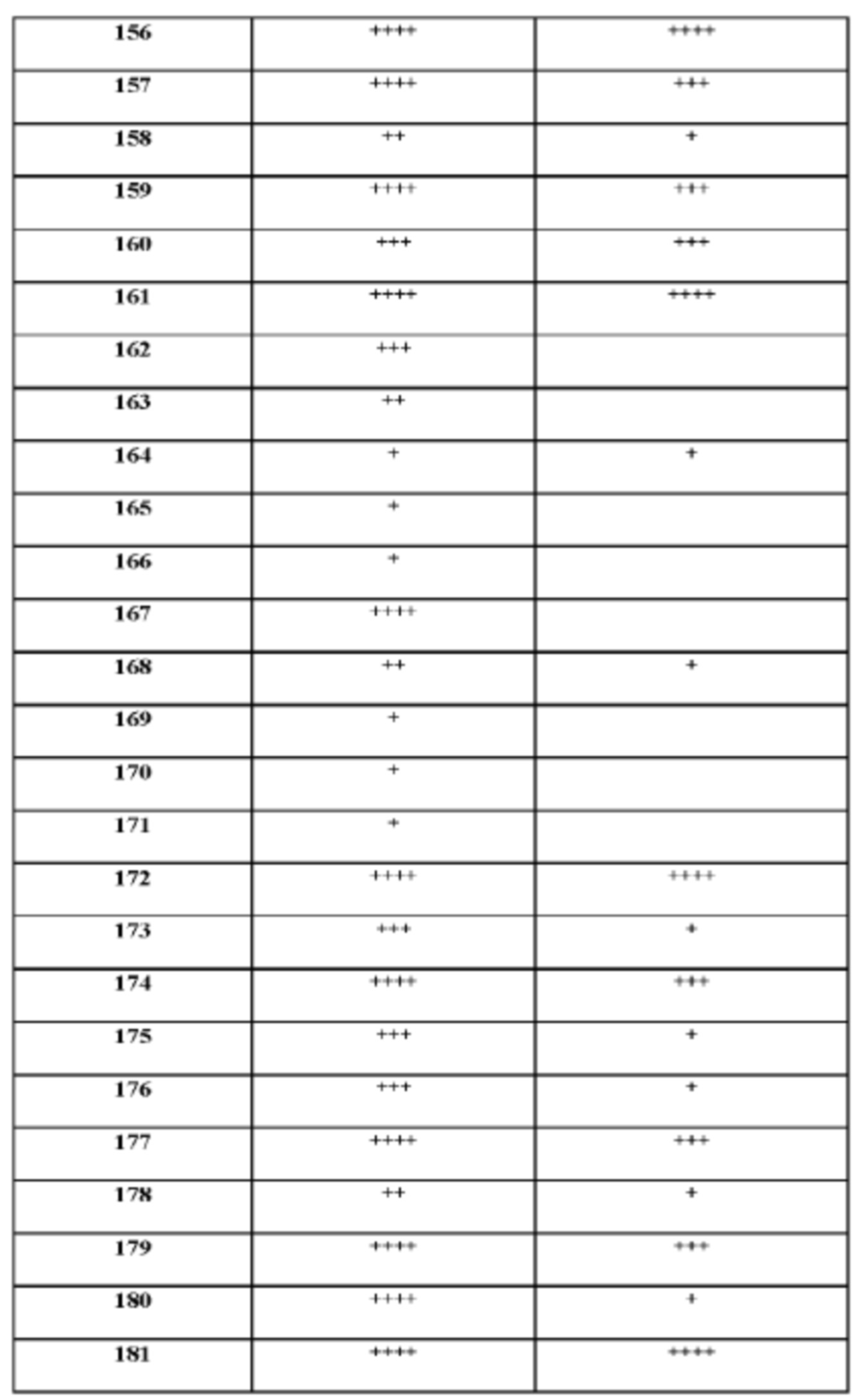
[2342]
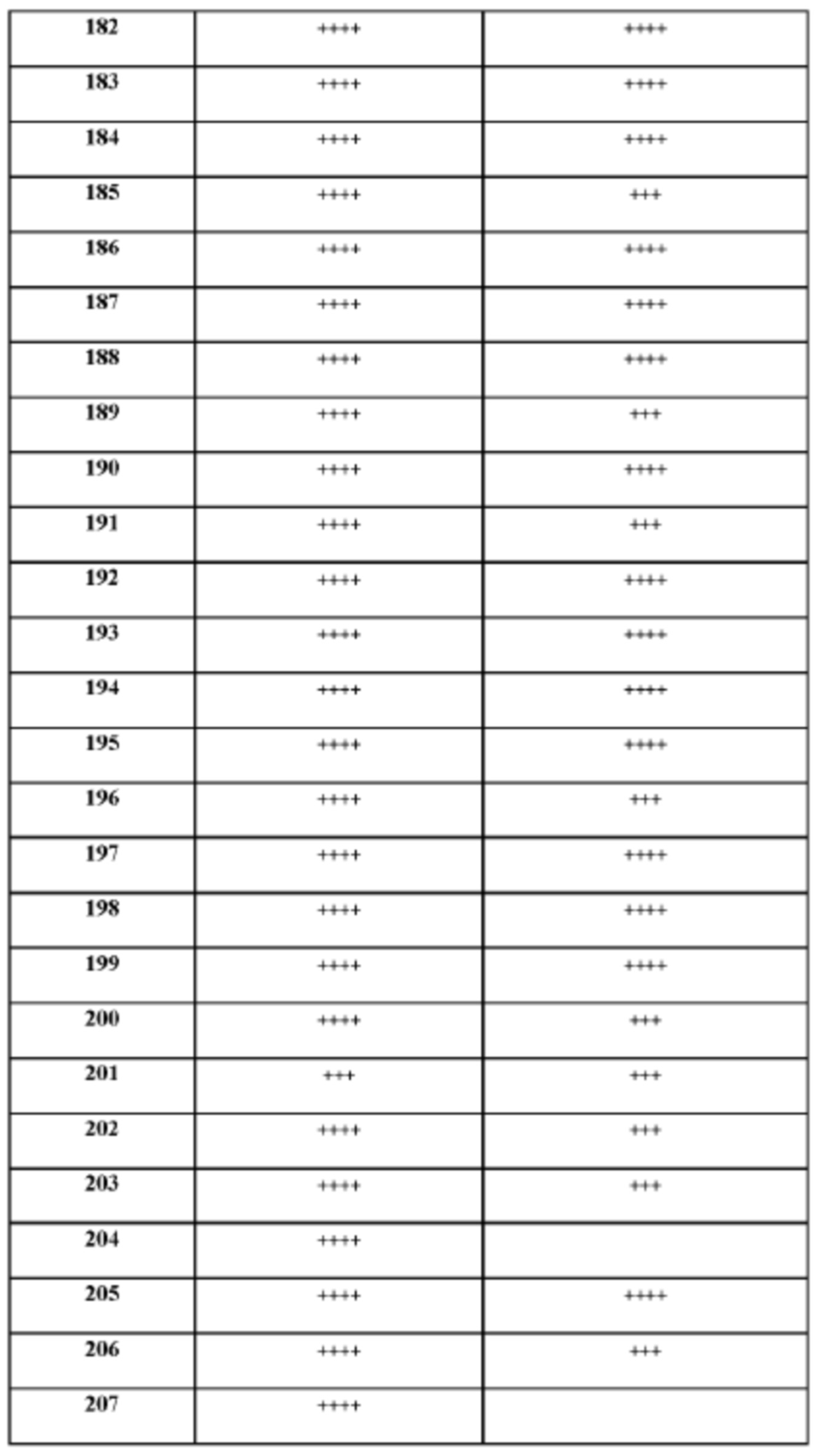
[2343]
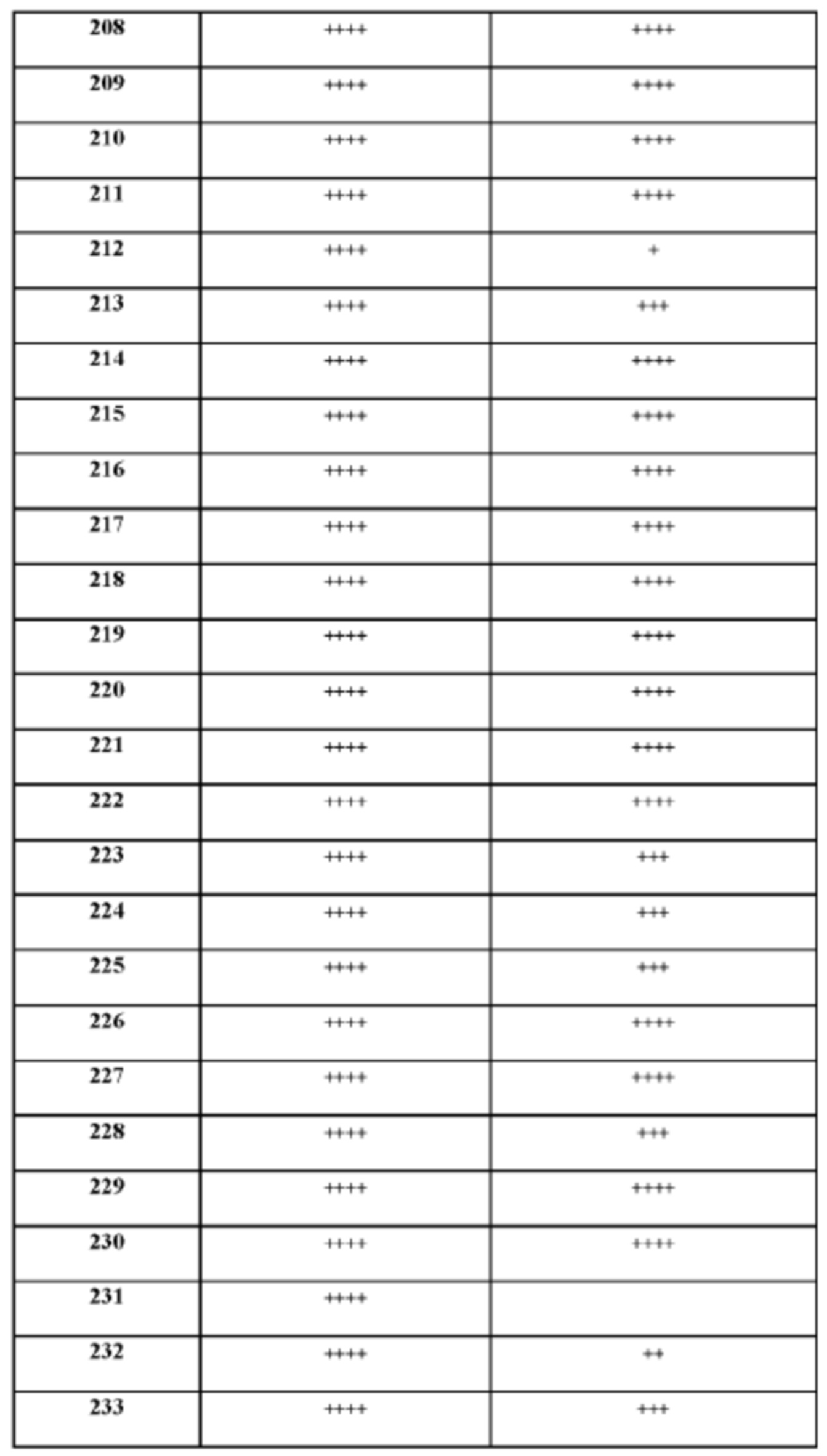
[2344]
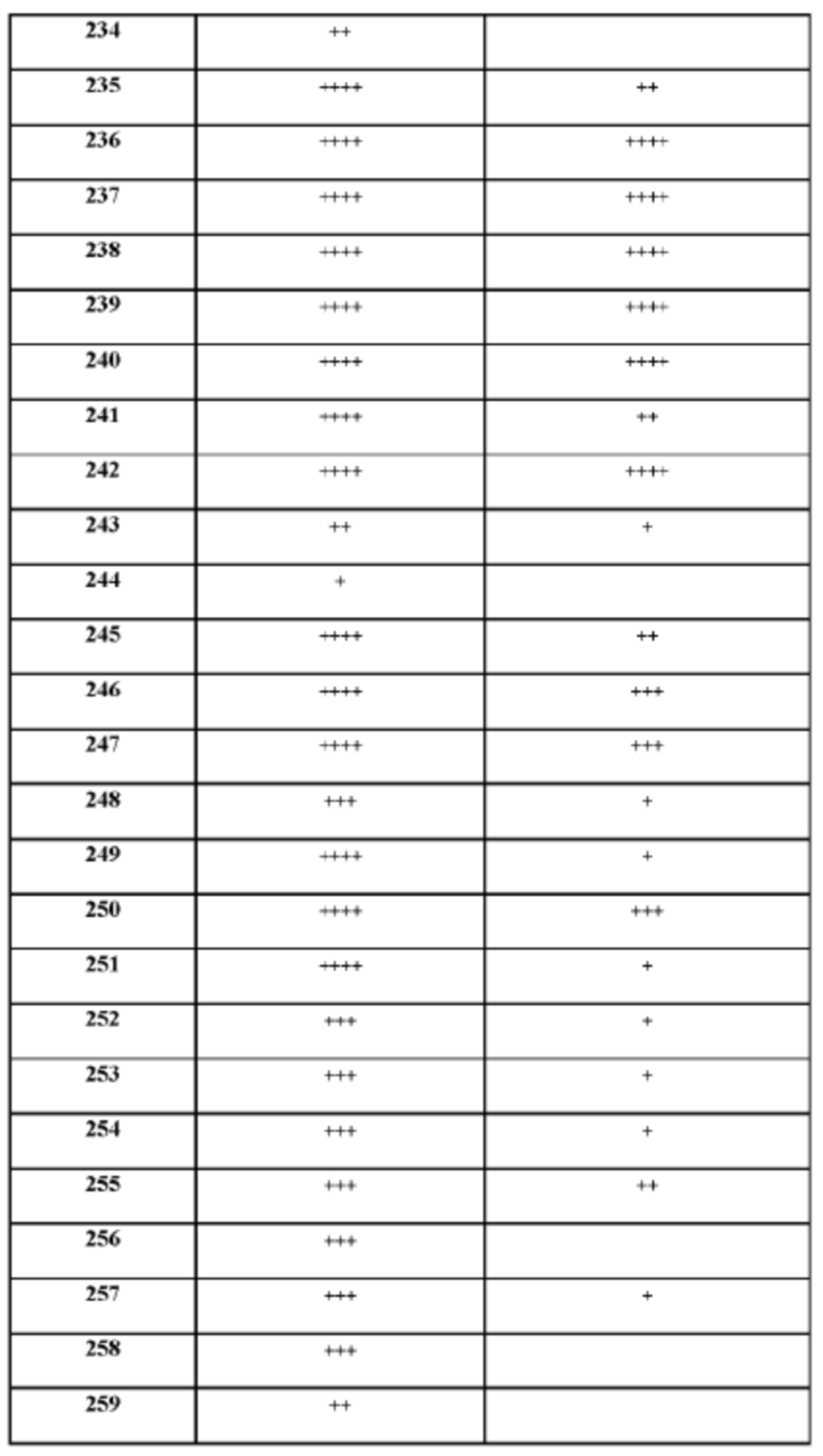
[2345]
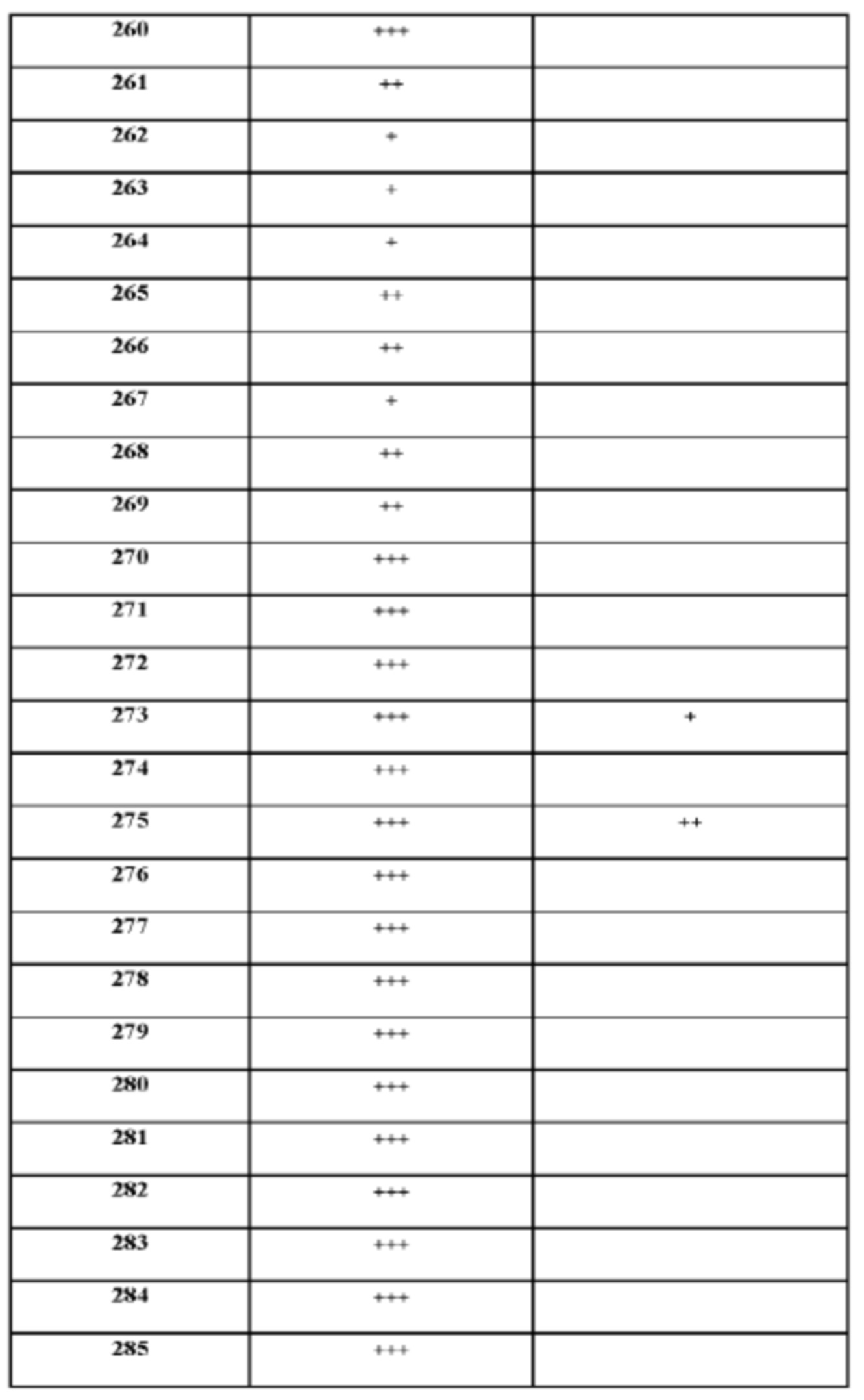
[2346]
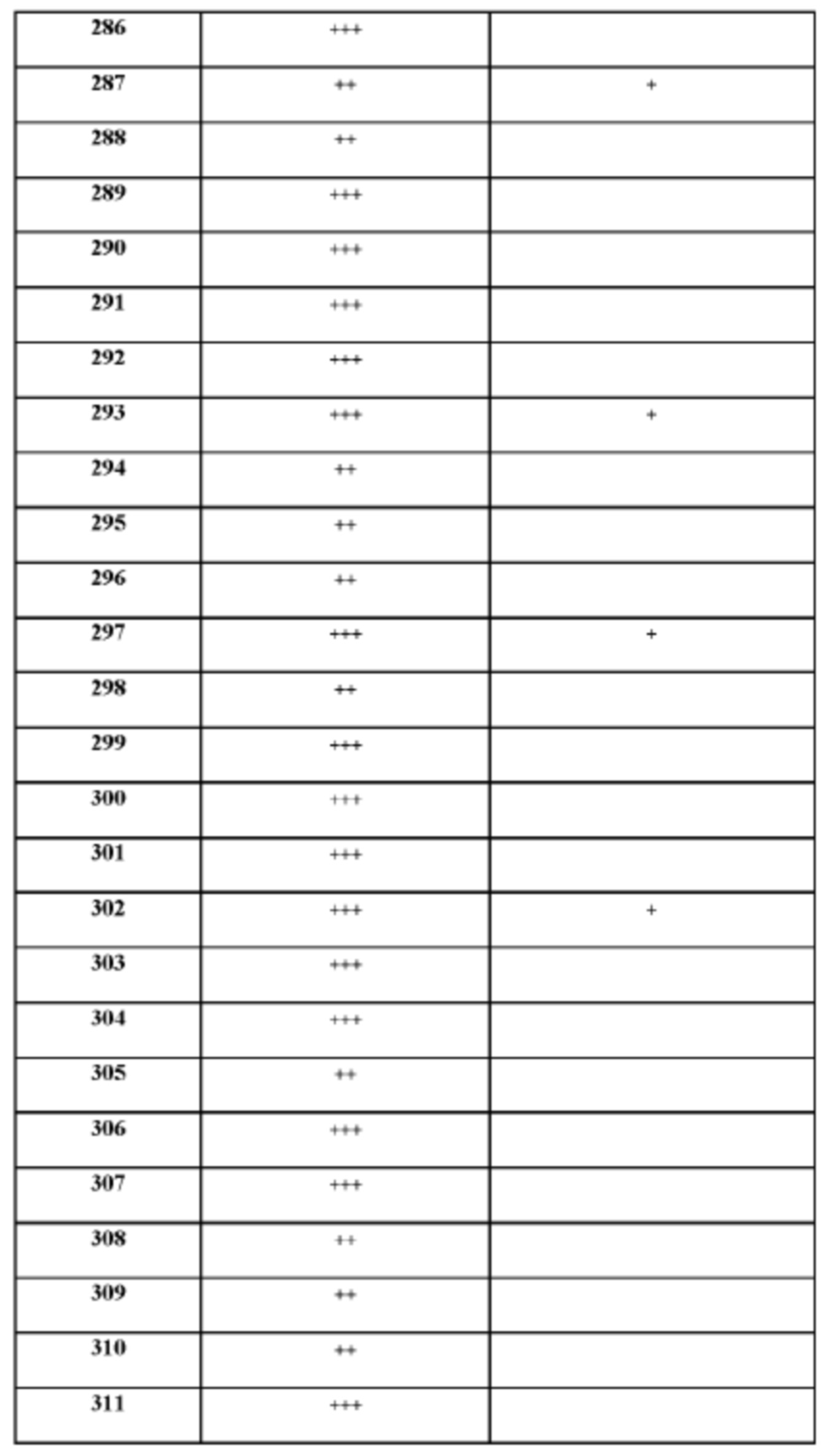
[2347]
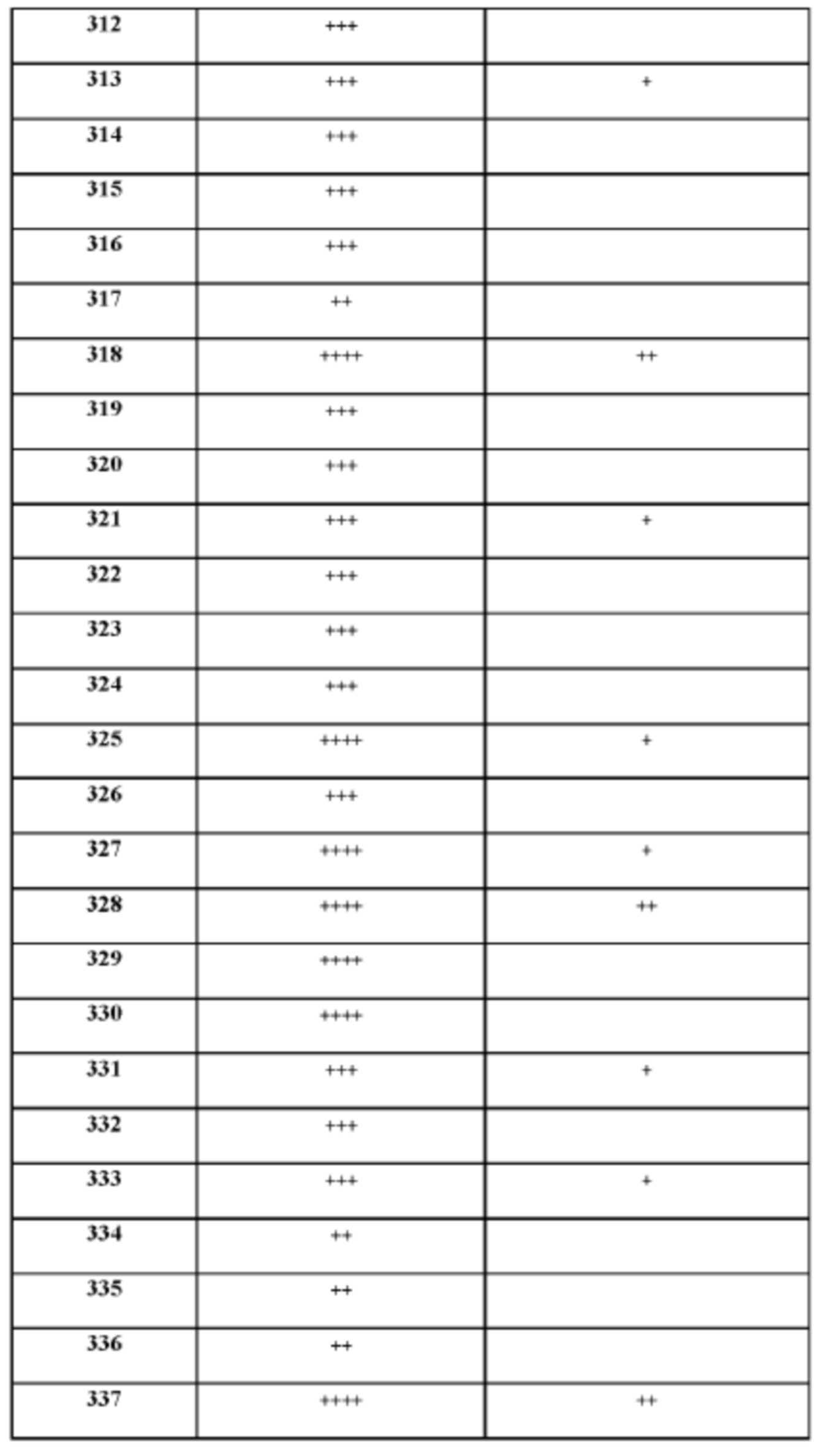
[2348]
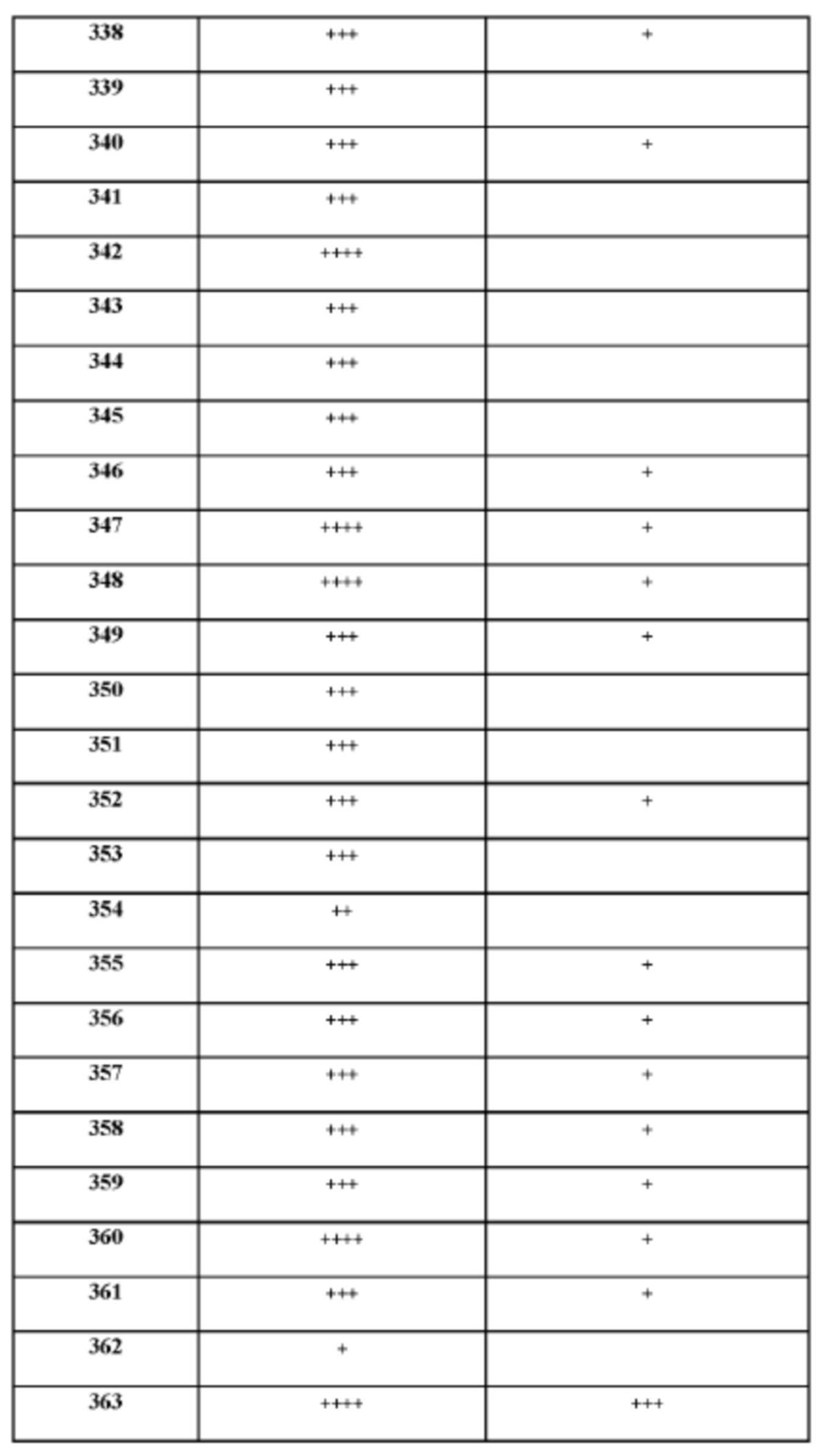
[2349]
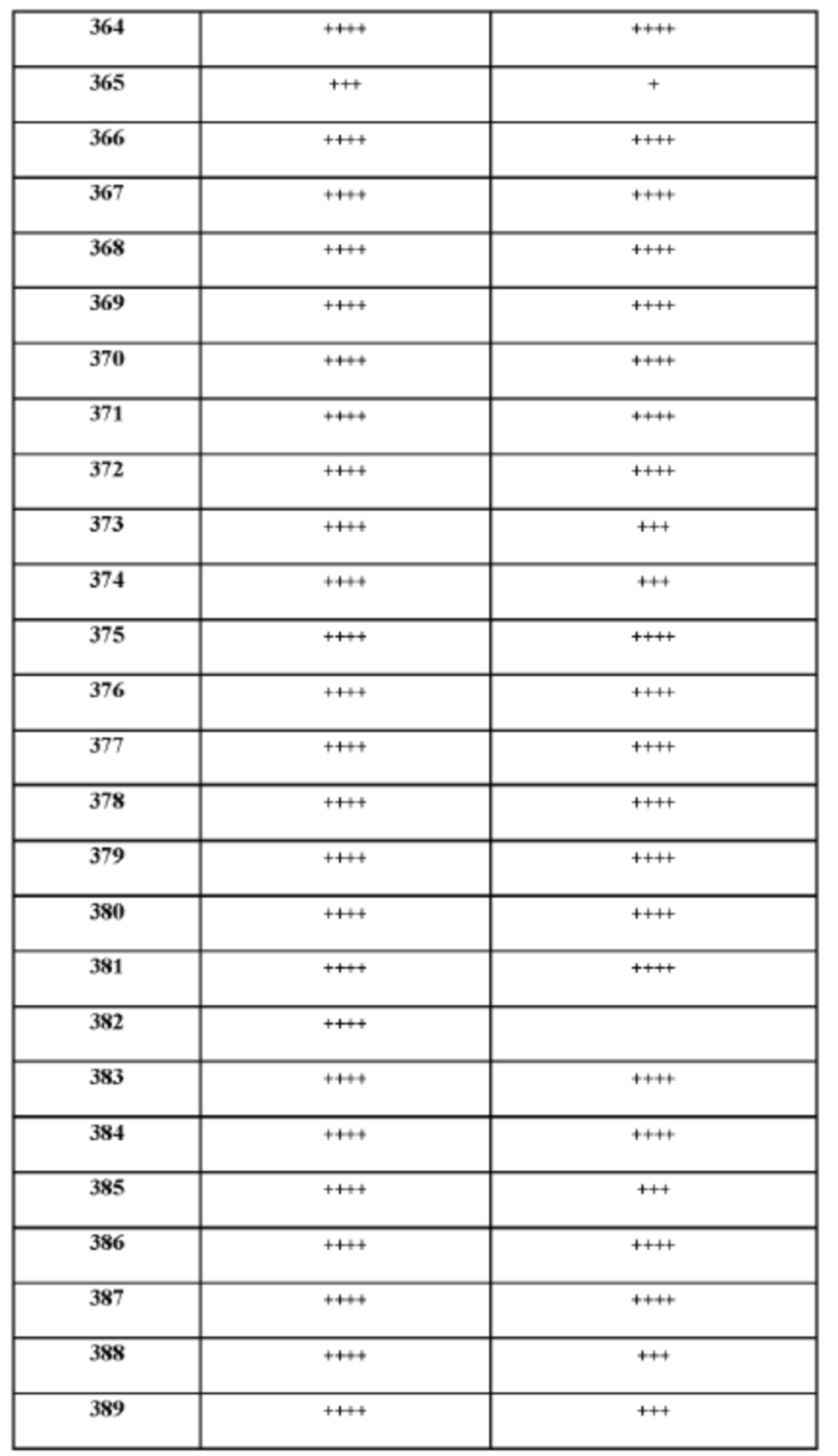
[2350]
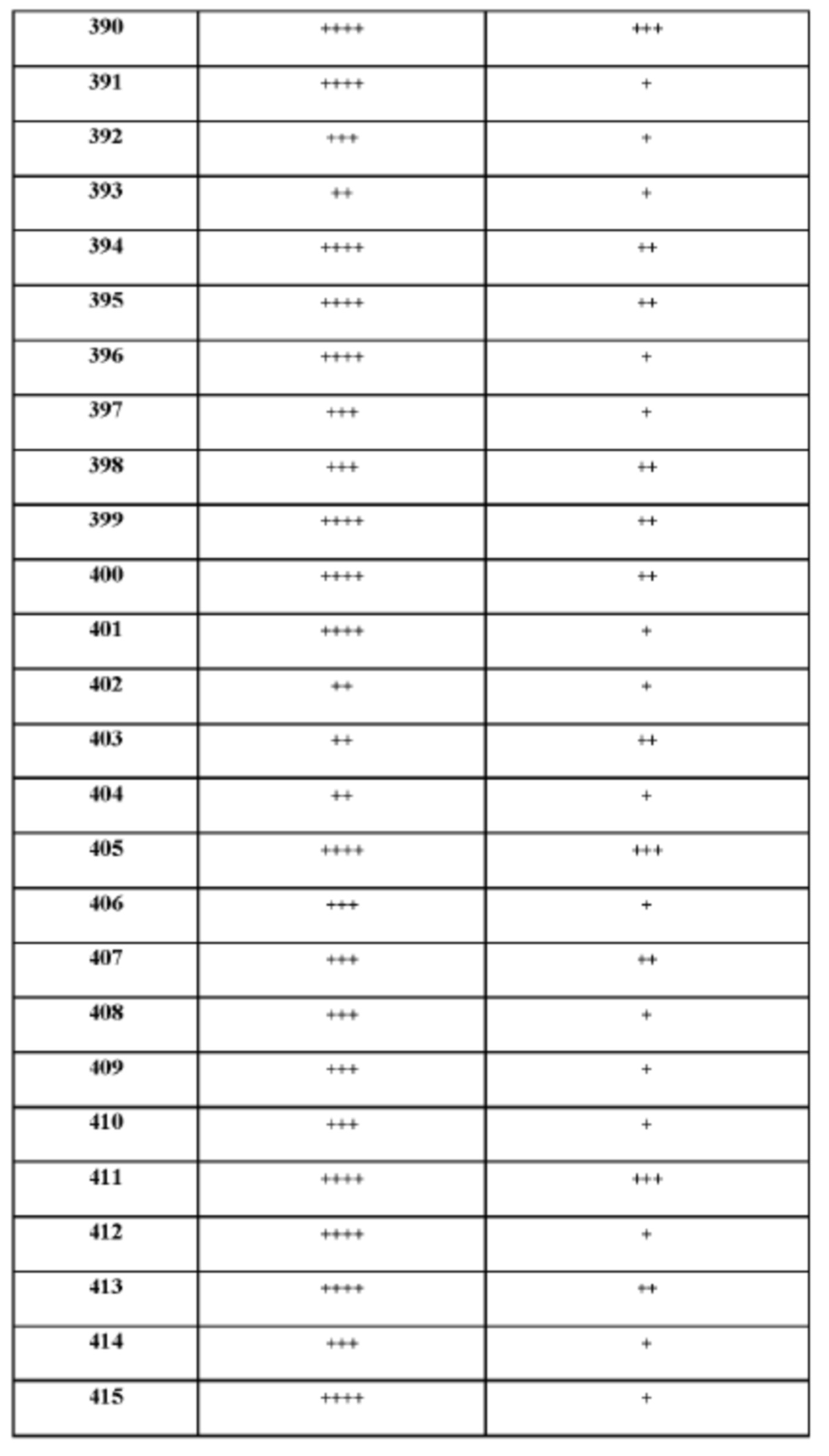
[2351]
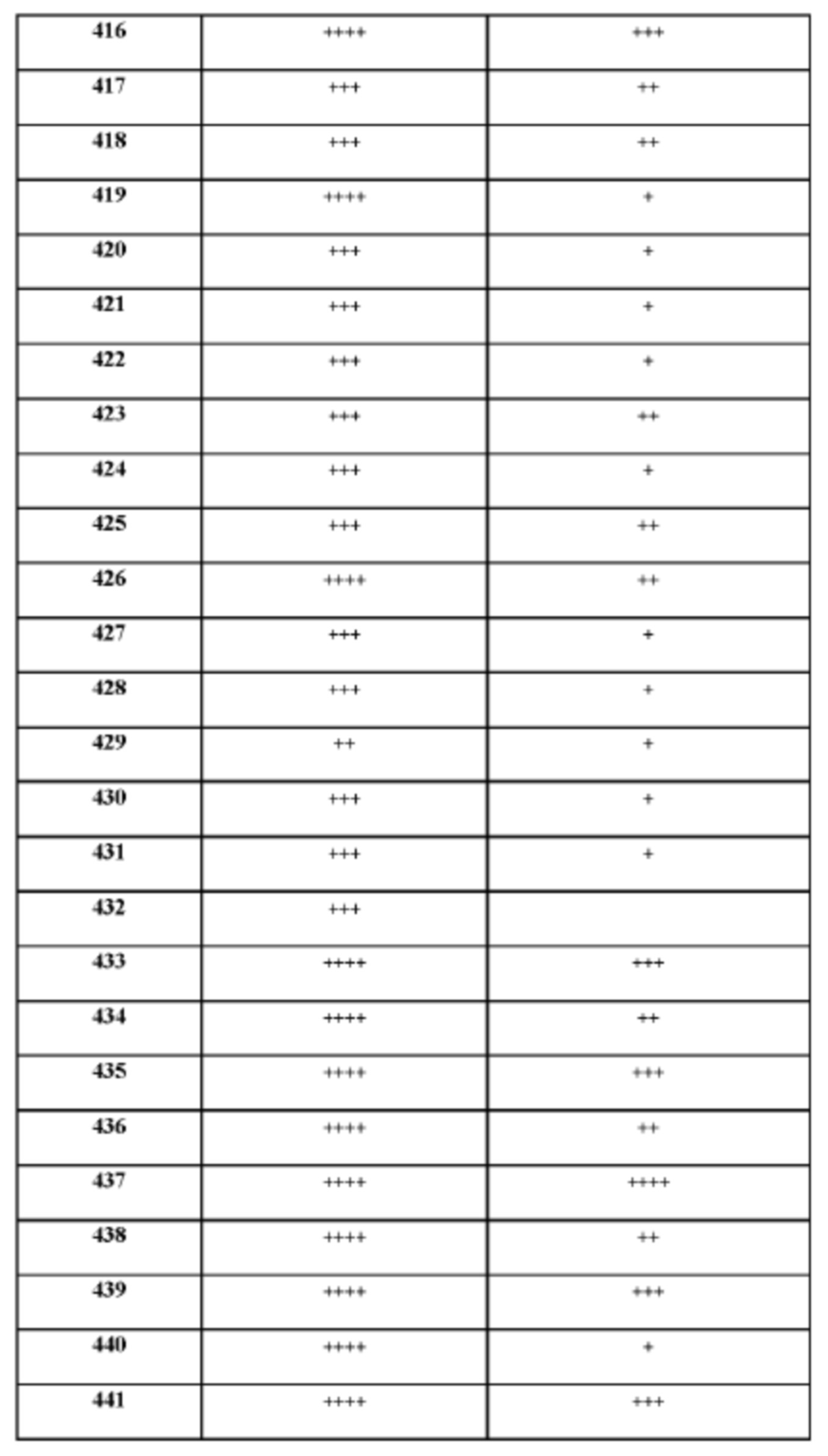
[2352]
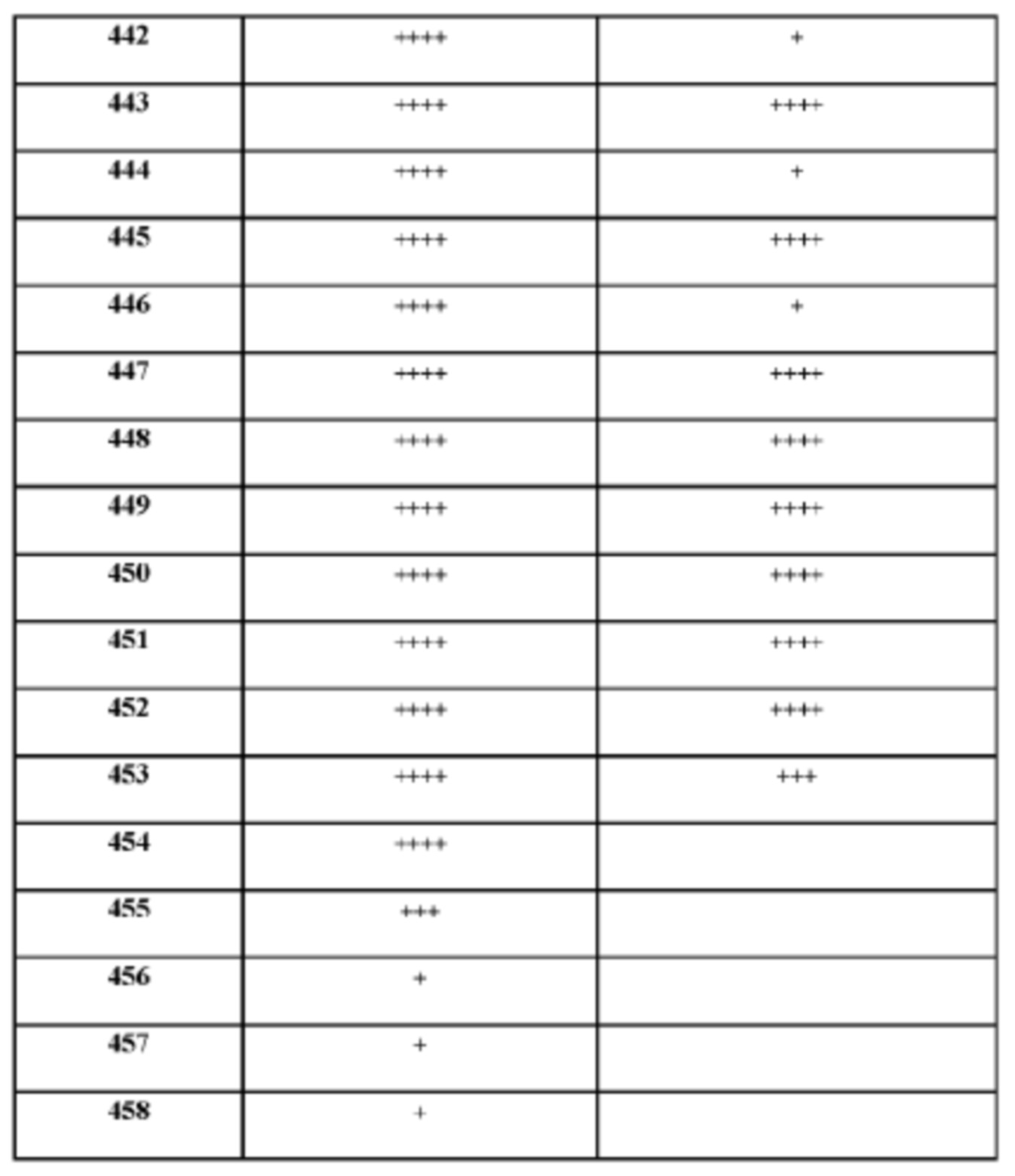
[2353] ++++: IC50<10, +++: 10≤IC50<100, ++: 100≤IC50<1000, +: IC50≥1000 нM
[2354] ++++: GI50<100, +++: 100≤GI50<500, ++: 500≤GI50<1000, +: GI50≥1000 нM
[2355] Как можно видеть из таблицы 1 выше, гетероциклические соединения согласно настоящему изобретению показывали активность в отношении Mer, это означает, что данные соединения пригодны для предупреждения и/или лечения рака.