Результат интеллектуальной деятельности: ОРГАНИЗАЦИЯ ХИМИЧЕСКИХ ЦИКЛОВ
Вид РИД
Изобретение
[0001] Настоящая заявка относится к способу организации химических циклов с использованием нестехиометрических соединений с переменной степенью нестереохимичности. Одним из применений этих способов является сдвиг равновесия реакции водяного газа при получении H2. Способы согласно данному изобретению могут преодолеть ограничения, например, ограничения, связанные с химическим равновесием, которые препятствуют протеканию химических реакций до полной степени конверсии исходных веществ в конечные продукты.
УРОВЕНЬ ТЕХНИКИ
[0002] Многие химические реакции обратимы по своей природе. Прохождение таких химических реакций в основном ограничено химическим равновесием, которое устанавливается, когда реагенты смешиваются и вступают в реакцию. Ограничения на условия равновесия приводят к неполной конверсии реагентов, необходимости сложных процессов разделения и рециклинга неиспользованных реагентов.
[0003] Одной такой обратимой реакцией является реакция сдвига равновесия в системе вода-газ (WGS), когда монооксид углерода (СО) реагирует с водой (H2О) с получением водорода (H2) и диоксида углерода (СО2). Эта реакция является важной в процессах получения H2 и при этом обычно расходуются вода и CO-содержащий исходный поток, например, из потока углеводородов процесса риформинга, осуществляемого при температурах около 800°С или выше. Обратимая экзотермическая природа реакции WGS означает, что для производства H2 требуется сложный многостадийный процесс. H2 и СО2 обычно разделяются с использованием короткоцикловой безнагревной адсорбции. В то время как риформинг при низкой температуре или сдвиг могут быть реализуемыми, технически прогрессивные процессы для увеличения конверсии при кинетически выгодных высоких температурах были сосредоточены на способах удаления одного из продуктов реакции in-situ. Такие способы включали применение палладиевых мембран для выделения H2 и применение так называемого усовершенствованного процесса WGS для удаления СО2 через образование карбоната кальция.
[0004] Организация химических циклов (CL) представляет собой динамический процесс, в котором соединение, например, оксид металла (который действует как переносчик кислорода или ОСМ) используется для обеспечения элемента, такого как кислород, для реакции, во время которой вещество само подвергается восстановлению (см. 'Chemical looping and oxygen permeable ceramic membranes for hydrogen production - a review'; Thursfield et al; Energy Environ. Sci., 2012, 5, 7421-59). Восстановленный оксид или металл затем снова окисляется или во втором реакторе, или на второй стадии, если используется неподвижный слой. Результат заключается в том, что процесс CL физически (или временно) делит весь процесс на его отдельные стадии окисления и восстановления при применении твердофазного материала, который сам способен подвергаться окислению и восстановлению. CL ранее применялась для конверсии энергии, риформинга и процессов WGS. Важно, что окисляющий и восстанавливающий потоки, подаваемые при осуществлении CL, никогда не смешиваются друг с другом и, таким образом, осуществляется 'реакция несмешиваемых реагентов'.
[0005] Организация химических циклов в противотоке имеет место, когда окисляющие и восстанавливающие газы проходят через реактор в противоположных направлениях. В частности, сдвиг равновесия реакции водяного пара осуществляется с использованием оксида железа в качестве ОСМ ('Thermodynamic analysis of a cyclic water gas-shift reactor (CWGSR) for hydrogen production'; Heidebrecht et al.; Chemical Engineering Science, 2009, 64, 5057-5065).
[0006] В химических реакциях сдвига равновесия в водяном газе использовали нестехиометрические соединения ('A chemical looping process for hydrogen production using iron-containing perovskites'; Murugan et al; Energy Environ. Sci.; 2011, 4, 4639-4649).
КРАТКОЕ РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
[0007] В соответствии с настоящим изобретением предусмотрен способ осуществления химической реакции, который включает передачу элемента или группы X от одной химической молекулы вещества к другой, при этом этот способ включает последовательно:
A) пропускание химической частицы Р через реактор с неподвижным слоем, причем химическая частица Р поступает из первого положения в реакторе с неподвижным слоем во второе положение в реакторе с неподвижным слоем, и извлечение полученного химического соединения РХy из второго положения в реакторе с неподвижным слоем; и затем
B) пропускание химической частицы QXz через реактор с неподвижным слоем, причем химическая частица QXz, поступает из второго положения в реакторе с неподвижным слоем в первое положение в реакторе с неподвижным слоем, и извлечение полученного химического соединения из первого положения в реакторе с неподвижным слоем;
С) необязательное последовательное повторение стадий А) и В) по меньшей мере один раз;
причем Р и Q представляют собой химические частицы, которые выбирают таким образом, что обе Р и Q могут принимать элемент или группу X и оба соединения РХy и QXz могут отдавать элемент или группу X; y и z обозначают целые числа; и реактор с неподвижным слоем содержит по меньшей мере одно нестехиометрическое соединение, которое имеет формулу MnXp(1-q), где n и p обозначают целые числа, требующееся для стехиометрического соединения между М и X, и 0<q<1 или 0>q>-1; при этом соединение способно содержать величины q в интервале; и М может обозначать один элемент или смесь более одного элементов.
[0008] Переменно нестехиометрическое соединение должно обладать способностью отдавать и принимать элемент или группу X в условиях реакции. Нестехиометрические оксиды согласно изобретению обычно будут обладать способностью передавать элемент или группу X. Таким образом, ионы элемента или группы X должны быть способны диффундировать в такое соединение.
[0009] М может обозначать один металлический элемент или смесь более, чем одного металлического элемента.
[0010] Данные изобретатели установили, что, когда обратимые реакции осуществляются с использованием системы организации химических циклов в противотоке при наличии неподвижного слоя или переменно нестехиометрического соединения, может быть получен поток практически чистого продукта, при этом исключается необходимость расхода энергии, больших расходов экономических для разделения равновесных смесей.
[0011] Не желая ограничиваться какой-либо теорией, полагают, что образуется градиент через неподвижный слой во время осуществления как стадии А), так и стадии В), при этом градиент представляет собой потенциал нестехиометрического соединения принимать или отдавать X. Таким образом, градиент может быть описан как градиент химического потенциала. Таким образом, после стадии А) первое положение в реакторе с неподвижным слоем имеет самую высокую величину потенциала акцептора X, и второе положение в реакторе с неподвижным слоем имеет самую низкую величину потенциала донора X. На стадии В), когда поток QXz подвергается действию низкого потенциала акцепторного типа во втором положении, только небольшие количества X акцептируются нестехиометрическим соединением, но как только смесь Q и QXz проходит градиент химического потенциала, равновесие смещается по направлению к Q до первого положения, смесь, которая имеет относительно низкое содержание QXz подвергается действию самого высокого потенциала акцептора X, что эффективно сдвигает реакцию к положению завершения. После стадии В) первое положение в реакторе с неподвижным слоем имеет самую низкую величину потенциала донора X и второе положение в реакторе с неподвижным слоем имеет самую высокую величину потенциала донора X. На стадии А), когда поток Р подвергается действию низкого потенциала донорного типа в первом положении, только небольшие количества X отдаются стехиометрическим соединением, но как только смесь Р и РХy проходит градиент потенциала, равновесие смещается в сторону РХy до второго положения, смесь, которая содержит относительно небольшое количество Р, подвергается действию самого высокого потенциала донорного типа, что эффективно сдвигает реакцию в сторону завершения. Таким образом, способ по изобретению может преодолеть ограничения для равновесия и позволяет реакции осуществляться с практически полной конверсией исходных соединений в конечные продукты.
[0012] Таким образом, соединения РХy и Q получаются с высокой степенью чистоты как на стадии А), так и на стадии В), соответственно. При организации химических циклов, которые не используют как противоток, так и переменно нестехиометрическое соединение, будет необходим избыток Р для того, чтобы получить достаточно высокую степень конверсии QXz в Q. В этом соединении РХy будет превращаться только небольшое количество Р и поэтому при получении Q с высокой степенью чистоты, большое количество Р останется непрореагировавшим. Таким образом, при осуществлении известных процессов или степень конверсии с передачей для одной реакции (или превращение Р в РХy или QXz в Q) является очень низкой и степень чистоты продукта другой реакции является высокой, или степень конверсии с передачей для одной реакции является хорошей, но степень чистоты продукта другой реакции является низкой, и необходимы последующие стадии разделения. При осуществлении способов согласно данному изобретению, как реакция Р с получением РХy, так и реакция QXz с получением Q протекают с высокими степенями конверсии. Следовательно, в случае таких реакций и степени конверсии при реакциях передачи X, и степень чистоты продуктов являются высокими.
[0013] Таким образом, может быть, что более 50% и QXz, и Р превращаются в Q и РХy, соответственно. Может быть, что более 75% и QXz, и Р превращаются в Q и РХy, соответственно, или более 90% и QXz, и Р превращаются в Q и РХy, соответственно.
[0014] Обычно первое положение в реакторе с неподвижным слоем является первым концом в реакторе с неподвижным слоем и второе положение является вторым концом. Объем данного изобретения охватывает реактор с неподвижным слоем, который является циркуляционным или реактор в виде пучка труб или другой формы, которую нельзя считать реактором, имеющим конец. Реактор с неподвижным слоем обычно включает корпус. Следовательно, газы обычно подаются и выводятся из реактора с неподвижным слоем через первое входное отверстие и второе входное отверстие в корпусе, при этом эти отверстия расположены в первом положении или вблизи первого положения или конца реактора с неподвижным слоем и во втором положении или конце реактора с неподвижным слоем. Может быть множество первых отверстий и/или множество вторых отверстий вблизи первого положения и второго положения, соответственно.
[0015] Нестехиометрическое соединение обычно является твердым. Как исключение, нестехиометрическое соединение может представлять собой жидкость. Когда нестехиометрическое соединение представляет собой жидкость, оно обычно иммобилизовано, например, при использовании пористых твердых гранул с жидким нестехиометрическим соединением, абсорбированным в порах. Это будет ограничивать количество смешиваемой жидкости до количества, которое помещается внутри самой гранулы и таким образом по длине слоя может поддерживаться потенциал донора или акцептора X.
[0016] Химические частицы Р и Q могут каждый независимо быть одним атомом или они могут быть более, чем одним атомом. Когда химические чР или Q обозначают более, чем один атом, атомы, из которых образованы химические вещества Р или Q, могут быть одними и теми же элементами или другими элементами. Когда химические частицы Р или Q обозначают более, чем один атом, может быть так, что связи между атомами химических частиц Р и Q будут разорваны во время образования РХy и QXz (это, например, может быть в случае, когда Q обозначает H2 и QXz обозначает H2O), или может быть так, что связи остаются целыми (это, например, может быть в случае, когда Р обозначает СО и РХy обозначает СО2). Связывание, в терминах количества и связности ковалентных связей, между атомами, составляющими Р, может быть одинаковым в Р и РХy (это, например, может быть в случае, когда Р обозначает СО и РХy обозначает СО2), или может быть разным. Связывание, в терминах количества и связности ковалентных связей, между атомами, составляющими Q может быть одинаковым в Q и QXz или может быть разным (это, например, может быть в случае, когда Q обозначает H2 и QXz обозначает H2O). Когда химические частицы Р или Q обозначают более, чем один атом, это обычно бывает в случае, когда они каждая образуют одну молекулу, но можно представить, что в одной из форм (а именно: Р или РХy; или Q или QXz) Р и/или Q представляют собой множество молекул (это может быть случай, когда Р представляет собой смесь СО и H2 и РХy представляет собой смесь СО2 и H2О). Таким образом, может быть так, что QXz превращается в Q1 и Q2, где Q1 и Q2 вместе содержат все атомы Q. Может быть так, что Q1 и Q2Xz превращаются в Q, где Q1 и Q2 вместе содержат все атомы Q. Таким образом, может быть так, что частица Р превращается в Р1Хy и Р2, где Р1 и Р2 вместе содержат все атомы Р (это может быть случай, когда Р представляет собой углеводород и РХy является смесью СО и H2). Может быть так, что Р1 и Р2 превращаются в РХУ, где Р1 и Р2 вместе содержат все атомы Р. Атомы, которые содержит Р, могут включать X, в форме, которая не передается в условиях реакции. Подобным образом, атомы, которые содержит Q, могут включать элемент X, в форме, которая не передается в условиях реакции.
[0017] В действительности, реакция может быть реакцией, приводящей к очистке. В этом случае Р и Q являются одинаковыми и РХy и QXz являются одинаковыми, но потоки Р и РХy содержат значительные количества примесей (которые отличаются от Р и РХy), в то время как потоки Q и QXz по существу являются чистыми (по существу не содержащими ничего кроме Q и QXz).
[0018] Р, РХy, Q и QXz обычно все являются газами в температурных пределах реакции. Однако возможно, что любое одно или более из соединений Р, РХy, Q и QXz является другой формой текучей среды, например, жидкостью или даже порошком.
[0019] Может быть так, что Р пропускают через реактор на стадии А) в виде смеси с другими компонентами. Например, может быть так, что смесь, содержащую Р и РХy, пропускают через реактор на стадии А). Вначале смесь будет обычно содержать больше Р, чем РХy. Так, может быть, что смесь содержит более 70 мол. % Р, остальное представляет собой РХy и/или другие примеси. Может быть так, что смесь содержит более 80 мол. % Р. Может быть так, что смесь содержит более 90 мол. % Р. Другие примеси, которые могут присутствовать, включают примеси, появившиеся при образовании Р. Р, или упомянутая смесь, содержащая Р, могут пропускаться через реактор в виде смеси с инертным разбавителем (например, N2).
[0020] Можно пропускать QXz через реактор на стадии В) в виде смеси с другими компонентами. Таким образом, может быть случай, когда смесь, содержащая QXz и Q, пропускается через реактор на стадии В). Вначале смесь обычно содержит больше QXz, чем Q. Таким образом, может быть, что смесь содержит больше 70 мол. % QXz, а остальное составляют Q и/или другие примеси. Может быть, что смесь содержит больше 80 мол. % QXz. Может быть, что смесь содержит больше 90 мол. % QXz. Другие примеси, которые могут присутствовать, включают примеси, образовавшиеся при получении QXz. QXz или упомянутая смесь, содержащая QXz, может пропускаться через реактор в виде смеси с инертным разбавителем (например, N2). Может быть так, что смесь Р и РХy выводится из реактора на стадии А). Такая смесь обычно содержит больше РХy, чем Р. Таким образом, может быть, что смесь содержит больше 70 мол. % РХy, остальное составляют Р и/или другие примеси. Может быть, что смесь содержит больше 80 мол. % РХy. Может быть, что смесь содержит больше 90 мол. % РХy. РХy, выходящий из реактора на стадии А), может также содержать небольшие (а именно: в общем менее 5 мол. %) количества Q и/или QXz.
[0021] Может быть так, что смесь Q и QXz выводится из реактора на стадии В). Такая смесь обычно содержит больше Q, чем QXz. Таким образом, может быть, что смесь содержит больше 70 мол. % Q, а остальное составляет QXz и/или другие примеси. Может быть, что смесь содержит больше 80 мол. % Q. Может быть, что смесь содержит больше 90 мол. % Q. Q, выходящий из реактора на стадии А), может также содержать небольшие (а именно: в общем менее 5 мол. %) количества Р и/или РХy.
[0022] Эта степень, чистоты, обсуждавшаяся в предыдущих двух параграфах, представляет собой степень чистоты, полученную сразу же после реакции, то есть, перед любой дальнейшей стадией очистки.
[0023] Может быть случай, когда Q и/или РХy подвергаются очистке, как только такое соединение выводится из реактора.
[0024] Величины скоростей реакции конверсии Р с получением РХy обычно отличаются от величин скоростей реакции конверсии QXz в Q.
[0025] Таким образом, может быть, что величины продолжительности стадии А) и стадии В) отличаются друг от друга. Альтернативно, может быть, что величины продолжительности стадии А) и стадии В) являются одинаковыми.
[0026] Может быть, что величины объемной скорости потока Р и QXy одинаковы или эти скорости могут быть разными.
[0027] Может быть так, что два или более реакторов работают параллельно. Таким образом, в одном или более реакторах может осуществляться стадия А) в то же время, как в одном или более реакторах может осуществляться стадия В). Это позволяет получать постоянные потоки РХy и Q. Когда скорость реакции при конверсии Р в РХy отличается от скорости реакции конверсии QXz в Q, это может быть компенсировано тем, что стадию А осуществляют в большем количестве реакторов в любой данный момент времени или тем, что стадию В осуществляют в большем количестве реакторов в любой данный момент времени. Альтернативно, может быть так, что в одном и том же количестве реакторов осуществляют стадию А и стадию В в любой данный момент времени.
[0028] Можно после стадии В и перед стадией А осуществлять стадию D. Стадия D включает пропускание еще одного донора X через слой в реакторе, при этом еще один донор X поступает из второго положения в реакторе с неподвижным слоем в первое положение в реакторе с неподвижным слоем. Можно после стадии А и перед стадией В осуществлять стадию Е. Стадия Е включает пропускание еще одного акцептора X через слой в реакторе. Этот прием может быть использован для увеличения активности системы и/или для получения тепла для запуска эндотермической реакции. Еще один акцептор X может поступать из первого положения в реакторе с неподвижным слоем во второе положение в реакторе с неподвижным слоем.
[0029] Реактор может работать при температуре от 300°С до 1200°С, например, от 500°С до 1100°С. Реактор может работать при температуре от 600°С до 1000°С. Реактор может работать при температуре от 750°С до 950°С. Реактор может работать при температуре от 800°С до 900°С.
[0030] Величины температур в реакторе на стадии А и на стадии В могут быть разными или они могут быть одинаковыми. Величины давления в реакторе на стадии А и на стадии В могут быть разными или они могут быть одинаковыми.
[0031] Способ согласно изобретению может быть непрерывным. Альтернативно, способы по изобретению могут осуществляться периодически.
[0032] Способ по изобретению является окислительно-восстановительным процессом, но не следует считать, что он всегда включает передачу кислорода: процессы окисления-восстановления могут также включать передачу других элементов, например, водорода. X может обозначать какую-либо группу, например, гидроксильную группу, но чаще является элементом. Элемент X обычно является неметаллом (например, элементом, выбранным из Н, В, С, N, О, F, Si, Р, S, Cl, As, Se, Br, Те, I). X может быть серой. X может быть азотом. X может быть водородом. X может быть галогеном. Предпочтительно, когда X является кислородом.
[0033] Q может быть Н2, в этом случае QXz будет являться Н2О. Согласно этому варианту Р может быть СО (в этом случае РХy обозначает СО2), Н2 (в этом случае РХy обозначает Н2О), органическим соединением (в этом случае РХy является смесью Н2, СО и возможно, Н2О и СО2) или их смесями.
Процесс I - реакция конверсии водяного газа
[0034] Способ по изобретению может представлять собой способ осуществления реакции сдвига фаз вода-газ при получении Н2. Согласно этим вариантам X обозначает кислород, Р обозначает СО, РХy обозначает СО2, QXz обозначает Н2О и Q обозначает Н2. Таким образом, это может быть способ получения Н2, при этом способ последовательно включает:
A) пропускание СО через реактор с неподвижным слоем, при этом СО поступает из первого положения в реакторе с неподвижным слоем во второе положение в реакторе с неподвижным слоем, и извлечение полученного СО2 из второго положения в реакторе с неподвижным слоем; и затем
B) пропускание Н2О через реактор с неподвижным слоем, при этом Н2О поступает из второго положения в реакторе с неподвижным слоем в первое положение в реакторе с неподвижным слоем, и извлечение полученного Н2 из первого положения в реакторе с неподвижным слоем;
C) необязательное последовательное повторение стадий А) и В) по меньшей мере один раз;
причем в реакторе с неподвижным слоем содержится по меньшей мере одно нестехиометрическое соединение, которое имеет формулу MnOp(1-q), где n и p обозначают целые числа, что требуется для стехиометрического связывания между М и О, и 0<q<1 или 0>q>-1; и это соединение способно принимать диапазон величин q; и при этом М может являться одним элементом или смесью более, чем одного элемента.
[0035] Как показатель общего подхода к первому аспекту изобретения, можно отметить, что способ обеспечивает получение Н2 по реакции сдвига фаз вода-газ с использованием нестехиометрического носителя кислорода. Была достигнута степень конверсии Н2О в Н2 равная 85%, что является значительным улучшением по сравнению с величиной 70%, которая была получена Heidebrecht et al с использованием оксида железа. Следует отметить, что высокая степень конверсии Н2О в Н2 была достигнута без использования большого избытка СО (степень конверсии СО в СО2 была также равна 85%), таким образом, при проведении этой реакции достигаются как высокий выход переносчика кислорода, так и высокая чистота продукта. Еще одно преимущество заключается в том, что нестехиометрические соединения согласно изобретению обладают увеличенным сроком службы по сравнению с соединениями, применявшимися при осуществлении известных способов.
Процесс II - окисление смеси Н2/СО
[0036] Способ по изобретению может представлять собой способ окисления газообразного продукта риформинга и получения Н2. В соответствии с этими вариантами X обозначает кислород, Р является смесью Н2 и СО, РХy является смесью Н2О и СО2, QXz является Н2О и Q является Н2. Таким образом, это может быть способ получения Н2, при этом этот способ последовательно включает:
A) пропускание смеси Н2 и СО через реактор с неподвижным слоем, при этом Н2 и СО поступают из первого положения в реакторе с неподвижным слоем во второе положение в реакторе с неподвижным слоем, и извлечение полученных Н2О и СО2 из второго положения в реакторе с неподвижным слоем; и затем
B) пропускание смеси Н2О через реактор с неподвижным слоем, при этом Н2О поступает из второго положения в реакторе с неподвижным слоем в первое положение в реакторе с неподвижным слоем, и извлечение полученного Н2 из первого положения в реакторе с неподвижным слоем;
C) необязательное последовательное повторение стадий А) и В) по меньшей мере один раз;
причем в реакторе с неподвижным слоем содержится по меньшей мере одно нестехиометрическое соединение, которое имеет формулу MnOp(1-q), где n и p обозначают целые числа, что требуется для стехиометрического связывания между М и О, и 0<q<1 или 0>q>-1; и это соединение способно принимать дапазон величин q; и при этом М может являться одним элементом или смесью более, чем одного элемента.
[0037] Этот способ перед стадией А может включать стадию F, при этом стадия F включает получение смеси Н2 и СО путем риформинга, например, парового риформинга, по меньшей мере одного органического соединения, например, метана. Стадия F может включать осуществление процесса, как описано ниже в разделе Процесс III.
[0038] И СО, и Н2, присутствующие в газообразном продукте риформинга, получают кислород из нестехиометрического соединения и, таким образом, сила восстановительного действия как Н2, так и СО используется для удаления кислорода из Н2О для получения потока чистого Н.
Процесс III - риформинг органического соединения
[0039] Способ по изобретению может представлять собой способ риформинга по меньшей мере одного органического соединения, например, метана, а также получения Н2. Таким образом, Р может обозначать по меньшей мере одну органическую частицу, РХy является смесью СО и Н2, QXz является Н2О и Q является Н2. Когда органическое соединение представляет собой метан, X является кислородом, Р является СН4, РХy является СО и 2Н2, QXz является Н2О и Q является Н2. Таким образом, это может быть способ получения Н2, который последовательно включает:
A) пропускание по меньшей мере одного органического соединения (например, метана) через реактор с неподвижным слоем, при этом по меньшей мере одно органическое соединение поступает из первого положения в реакторе с неподвижным слоем во второе положение в реакторе с неподвижным слоем, и извлечение полученной смеси Н2 и СО из второго положения в реакторе с неподвижным слоем; и затем
B) пропускание Н2О через реактор с неподвижным слоем, при этом Н2О поступает из второго положения в реакторе с неподвижным слоем в первое положение в реакторе с неподвижным слоем, и извлечение полученного Н2 из первого положения в реакторе с неподвижным слоем;
C) необязательное последовательное повторение стадий А) и В) по меньшей мере один раз;
причем в реакторе с неподвижным слоем содержится по меньшей мере одно нестехиометрическое соединение, которое имеет формулу MnOp(1-q), где n и p обозначают целые числа, что требуется для стехиометрического связывания между М и О, и 0<q<1 или 0>q>-1; и это соединение способно принимать диапазон величин q; и при этом М может являться одним элементом или смесью более, чем одного элемента.
[0040] Этот способ может включать стадию D, осуществляемую после стадии В и перед стадией А, при этом стадия D включает пропускание О2 через слой в реакторе, и О2 поступает из второго положения в реакторе с неподвижным слоем в первое положение в реакторе с неподвижным слоем.
[0041] Продукт на стадии А представляет собой газообразный продукт риформинга, который затем может быть использован как восстанавливающий газ сам по себе в процессе превращения Н2О в Н2, как описано выше в разделе Процесс II. Эти оба процесса (первый процесс представляет собой образование газообразного продукта риформинга и первое превращение Н2О в Н2 и второй процесс является окислением полученного газообразного продукта риформинга и второе превращение Н2О в Н2) могут осуществляться в отдельных реакторах (см. Процесс V ниже) или они могут осуществляться в одном и том же реакторе (см. Процесс VI ниже).
Процесс IV - риформинг органического соединения с последующим окислением газообразного продукта риформинга и рециклингом полученного тепла
[0042] После преобразования по меньшей мере одного органического соединения при осуществлении способов согласно данному изобретению (например, Процесса III) смесь Н2 и СО, полученная на стадии А, может быть затем окислена, например, путем воздействия О2 или другого окислителя, с получением СО2 или Н2О. Это окисление обычно является экзотермическим и может генерировать тепло, которое может быть передано обычными средствами в реактор с неподвижным слоем, в котором осуществляется эндотермическая реакция преобразования, для запуска реакции.
[0043] Примером способа по изобретению может быть способ получения Н2, который последовательно включает:
A) пропускание по меньшей мере одного органического соединения (например, метана) через первый реактор с неподвижным слоем, при этом по меньшей мере одно органическое соединение поступает из первого положения в реакторе с неподвижным слоем во второе положение в реакторе с неподвижным слоем, и извлечение полученной смеси Н2 и СО из второго положения в реакторе с неподвижным слоем; и затем
B) пропускание Н2О через первый реактор с неподвижным слоем, при этом Н2О поступает из второго положения в реакторе с неподвижным слоем в первое положение в реакторе с неподвижным слоем, и извлечение полученного Н2 из первого положения в реакторе с неподвижным слоем;
C) необязательное последовательное повторение стадий А) и В) по меньшей мере один раз;
K) пропускание смеси Н2 и СО, полученной на стадии А), через второй реактор и удаление полученных Н2О и СО2 из второго реактора; и
L) пропускание О2 через второй реактор;
М) необязательное последовательное повторение стадий K) и L) по меньшей мере один раз;
N) передачу тепла, удаленного из второго реактора с неподвижным слоем, в первый реактор с неподвижным слоем;
причем в первом реакторе с неподвижным слоем содержится по меньшей мере одно нестехиометрическое соединение, которое имеет формулу MnOp(1-q), где n и p обозначают целые числа, что требуется для стехиометрического связывания между М и О, и 0<q<1 или 0>q>-1; и это соединение способно принимать диапазон величин q в интервале; и при этом М может являться одним элементом или смесью более, чем одного элемента.
[0044] Стадии K) и L) могут осуществляться одновременно. Альтернативно, они могут осуществляться последовательно.
[0045] Стадии K) и L) могут выполняться следующим образом:
K) пропускание смеси Н2 и СО, полученной на стадии А), через второй реактор с неподвижным слоем, при этом Н2 и СО поступают из первого положения во втором реакторе с неподвижным слоем во второе положение во втором реакторе с неподвижным слоем, и извлечение полученных Н2О и СО2 из второго положения во втором реакторе с неподвижным слоем; и затем
L) пропускание О2 через второй реактор с неподвижным слоем, при этом О2 поступает из второго положения во втором реакторе с неподвижным слоем в первое положение во втором реакторе с неподвижным слоем, извлечение избытка О2 из первого положения во втором реакторе с неподвижным слоем и удаление тепла из второго реактора с неподвижным слоем;
и второй реактор содержит по меньшей мере одно нестехиометрическое соединение, которое имеет формулу MnOp(1-q), где n и p обозначают целые числа, что требуется для стехиометрического связывания между М и О, и 0<q<1 или 0>q>-1; и это соединение способно принимать диапазон величин q; и при этом М может являться одним элементом или смесью более, чем одного элемента, при этом соединения в первом реакторе и во втором реакторе могут быть одинаковыми или разными.
Процесс V - процесс II и процесс III осуществляются в отдельных реакторах
[0046] Способ по изобретению может представлять собой способ получения Н2, который последовательно включает:
А) пропускание по меньшей мере одного органического соединения (например, метана) через первый реактор с неподвижным слоем, при этом по меньшей мере одно органическое соединение поступает из первого положения в первом реакторе с неподвижным слоем во второе положение в первом реакторе с неподвижным слоем, и извлечение полученной смеси Н2 и СО из второго положения в первом реакторе с неподвижным слоем; и затем
B) пропускание Н2О через первый реактор с неподвижным слоем, при этом Н2О поступает из второго положения в первом реакторе с неподвижным слоем в первое положение в первом реакторе с неподвижным слоем и извлечение полученного Н2 из первого положения в первом реакторе с неподвижным слоем;
C) необязательное последовательное повторение стадий А) и В) по меньшей мере один раз;
G) пропускание смеси Н2 и СО, полученной на стадии А), через второй реактор с неподвижным слоем, при этом Н2 и СО поступают из первого положения во втором реакторе с неподвижным слоем во второе положение во втором реакторе с неподвижным слоем, и извлечение полученных Н2О и СО2 из второго положения во втором реакторе с неподвижным слоем; и затем
H) пропускание Н2О через второй реактор с неподвижным слоем, при этом Н2О поступает из второго положения во втором реакторе с неподвижным слоем в первое положение во втором реакторе с неподвижным слоем, и извлечение полученного Н2 из первого положения во втором реакторе с неподвижным слоем; а
I) необязательное последовательное повторение стадий G) и Н) по меньшей мере один раз;
причем первый и второй реакторы с неподвижным слоем каждый независимо содержит по меньшей мере одно нестехиометрическое соединение, которое имеет формулу MnOp(1-q), где n и p обозначают целые числа, что требуется для стехиометрического связывания между М и О, и 0<q<1 или 0>q>-1; и это соединение способно принимать диапазон величин q; и при этом М может являться одним элементом или смесью более, чем одного элемента.
[0047] Этот способ может включать стадию D, осуществляемую после стадии В и перед стадией А, при этом стадия D включает пропускание О2 через слой в реакторе, и О2 поступает из второго положения в реакторе с неподвижным слоем в первое положение в реакторе с неподвижным слоем.
Процесс VI - процесс II и процесс III осуществляются в одном и том же реакторе
[0048] Способ согласно изобретению может быть способом получения Н2, который последовательно включает:
A) пропускание по меньшей мере одного органического соединения (например, метана) через реактор с неподвижным слоем, при этом по меньшей мере одно органическое соединение поступает из первого положения в реакторе с неподвижным слоем во второе положение в реакторе с неподвижным слоем, и извлечение полученной смеси Н2 и СО из второго положения в реакторе с неподвижным слоем; и затем
B) пропускание Н2О через реактор с неподвижным слоем, при этом Н2О поступает из второго положения в реакторе с неподвижным слоем в первое положение в реакторе с неподвижным слоем, и извлечение полученного Н2 из первого положения в реакторе с неподвижным слоем;
C) необязательное последовательное повторение стадий А) и В) по меньшей мере один раз;
причем в реакторе с неподвижным слоем содержится по меньшей мере одно нестехиометрическое соединение, которое имеет формулу MnOp(1-q), где n и p обозначают целые числа, что требуется для стехиометрического связывания между М и О, и 0<q<1 или 0>q>-1; и это соединение способно принимать диапазон величин q; и при этом М может являться одним элементом или смесью более, чем одного элемента.
[0049] Этот способ может включать стадию D, осуществляемую после стадии В и перед стадией А, при этом стадия D включает пропускание О2 через слой в реакторе, и О2 поступает из второго положения в реакторе с неподвижным слоем в первое положение в реакторе с неподвижным слоем.
[0050] Примеры других конкретных способов, которые могут осуществляться согласно общему подходу к первому аспекту данного изобретения, включают способ получения частично ненасыщенных углеводородов (например, бутана; тогда, X обозначает водород, Р обозначает О2, РХy является Н2О, QXz является С4H10 и Q является С4Н8), и способ конверсии H2S в Н2 (тогда X обозначает серу, Р является СО, РХy является COS, QXz является H2S и Q является Н2).
Вещества
[0051] При осуществлении способов может быть случай, когда 0<q<1.
[0052] Нестехиометрические соединения, пригодные для осуществления способов согласно настоящему изобретению, имеют свойства, одинаковые со свойствами, используемыми в ионопроводящих мембранах. Поэтому при осуществлении способов согласно данному изобретению применение соединений, описанных в публикации Sunarso et al; Journal of Membrane Science, 320, 2008, 13-41, однозначно включено в данную заявку посредством отсылки.
[0053] Нестехиометрические соединения, пригодные для осуществления способов, в которых X обозначает кислород (например, способа сдвига равновесия реакции в системе вода-газ, описанного выше), включают оксиды на основе структуры кристаллического флюорита (а именно: AO2(1-q)); перовскиты (а именно: АВО3(1-q)); оксиды на основе структуры кристаллического пирохлора (А2В2O7(1-q)); и оксиды на основе структуры кристаллического браунмиллерита (А2В2O5(1-q)) (где А и В обозначают металлические элементы). Следовательно, соединение может быть перовскитом.
[0054] Примеры перовскитов включают: BaBi0.5 Сo0.2 Fe0.3O3-δ; BaBi0.4Co0.2Fe0.4O3-δ; BaBi0.2Co0.2 Fe0.6O3-δ; ВаСе0.4Fе0.6О3-δ; BaCe0.2Fe0.8O3-δ; BaCe0.15Fe0.85O3-δ; BaCo0.4Fe0.5Zr0.1O3-δ; Ba0.5Sr0.5Co0.8Fe0.2O3-δ; Ba0.5Sr0.5Zn0.2Fe0.8O3-δ; BaTi0.2Co0.4Fe0.4O3-δ; BaTi0.2Со0.5Fe0.3O3-δ; CaTi0.8Fe0.2O3-δ; Gd0.6Sr0.4CoO3-δ; Lа0.6Ва0.4Со0.8Fе0.2О3-δ; La0.4Ba0.6Co0.2Fe0.8O3-δ; La0.2Ba0.8Co0.2Fe0.8O3-δ; Lа0.6Са0.4Со0.8Fе0.2О3-δ; La0.4Ca0.6Co0.2Fe0.8O3-δ; LаСо0.8Fе0.2О3-δ; LaCo0.8Fe0.2O3-δ; LаСо0.4Fе0.6О3-δ; LaCo0.8Fe0.1Ni0.1O3-δ; LaCo0.7Fe0.1Ni0.2O3-δ; LaCo0.6Fe0.2Ni0.2O3-δ; LaCo0.5Fe0.2Ni0.3O3-δ; LaCo0.4Ga0.4Mg0.2O3-δ; LaCo0.6Ga0.3Mg0.1O3-δ; LaCo0.9Mg0.1O3-δ; LaCo0.8W0.2O3-δ; LaFe0.8Ni0.2O3-δ; LaFe0.7Ni0.3O3-δ; LaFe0.6Ni0.4O3-δ; LaFe0.5Ni0.5O3-δ; LaGa0.8Ni0.2O3-δ; LaGa0.7Ni0.3O3-δ; LaGa0.6Ni0.4O3-δ; LaGa0.5Ni0.5O3-δ; LaGa0.4Ni0.6O3-δ; La0.6Na0.4Co0.8Fe0.2O3-δ; La0.6Sr0.4CoO3-δ; La0.6Sr0.4Co0.8Cr0.2O3-δ; La0.6Sr0.4Co0.8Cu0.2O3-δ; La0.6Sr0.4Co0.2Fe0.2O3-δ; La0.6Sr0.4Co0.2Fe0.6O3-δ; La0.6Sr0.4Co0.8Fe0.2O3-δ; La0.6Sr0.4Co0.8Fe0.2O3-δ; La0.4Sr0.6Co0.2Fe0.8O3-δ; La0.2Sr0.8Co0.2Fe0.8O3-δ; La0.2Sr0.4Co0.8Fe0.6O3-δ; La0.6Sr0.4Co0.8Mn0.2O3-δ; La0.6Sr0.4Co0.8Ni0.2O3-δ; La0.9Sr0.1FeO3-δ; La0.8Sr0.2FeO3-δ; La0.7Sr0.3FeO3-δ; La0.6Sr0.4FeO3-δ; Lа0.8Sr0.2Gа0.7Со0.3O3-δ; La0.8Sr0.2Ga0.7Fe0.3O3-δ; La0.8Sr0.2Ga0.7Ni0.3O3-δ; Nd0.6Sr0.4CoO3-8; Pr0.6Sr0.4CoO3-δ; Sm0.6Sr0.4CoO3-δ; Sr0.5Bi0.5FeO3-δ; SrCoO3-δ; SrCo0.4Fe0.6O3-δ; SrCo0.8Fe0.2O3-δ; SrCo0.8Fe0.2O3-δ; SrCo0.89Fe0.1Cr0.01O3-δ; SrCo0.85Fe0.1Cr0.05O3-δ; SrCo0.95Ti0.05O3-δ; SrCo0.8Ti0.2O3-δ; Sr0.7Gd0.3CoO3-δ; Sr0.7La0.3СоО3-δ; Sr0.65La0.35CoO3-δ; Sr0.6La0.4CoO3-δ; Sr0.55La0.45CoO3-δ; Sr0.65La0.35CoO3-δ; Sr0.7Nd0.3CoO3-δ; Sr0.7Sm0.3CoO3-δ; Y0.85Ва0.95СоО3-δ; Y0.1Ba0.9CoO3-δ; и Y0.33Ва0.67СоО3-δ.
[0055] Примеры оксидов флюоритного типа включают: (Bi2 О3)0.73(СаО)0.27; (Bi2 О3)0.75(Er2 О3)0.25; (Bi2 О3)0.6(Tb2O3.5)0.4; (Bi2 О3)0.75(Y2 О3)0.25; Bi1.25Y0.5Cu0.25O3; Bi0.5Cu0.5O3; Bi0.75Y0.5Cu0.75O3; Bi1.5Y0.3Sm0.2O3; Bi2.02 Со0.13 V0.85Oz; Се0.8Pr0.2O2-δ; Gd0.15Ce0.65Pr0.2O2-δ; Gd0.2Ce0.6Pr0.2O2-δ; (ZrO2)0.85(CaO)0.15; (ZrO2)0.84(CaO)0.16; [(ZrO2)0.9(CeO2)0.1]0.9(CaO)0.1; [(ZrO2)0.8(CeO2)0.2]0.9(CaO)0.1; [(ZrO2)0.7(CeO2)0.3]0.9(CaO)0.1; [(ZrO2)0.6(CeO2)0.4]0.9(CaO)0.1; (ZrO2)0.7(Tb2O3.5)0.3; (ZrO2)0.7(Тb2О3.5)0.25(Y2О3)0.05; (ZrO2)0.7(Тb2О3.5)0.228(Y2О3)0.072; (ZrO2)0.8(Y2O3)0.20; [(ZrO2)0.89(Y2O3)0.11]0.96(CeO2)0.04; [(ZrO2)0.89(Y2O3)0.11]0.87(CeO2)0.13; и [(ZrO2)0.89(Y2O3)0.11]0.77(CeO2)0.23.
[0056] Примеры жидких носителей оксидов включают расплавленные смеси нитратов и нитритов лития, натрия и/или калия. Смесь солей щелочных металлов снижает температуру плавления и тем самым позволяет оперировать в более широком интервале температур. Смесь нитратов и нитритов позволяет хранить кислород. Химический потенциал кислорода в смеси солей зависит, таким образом, от отношения нитрата к нитриту и способен непрерывно меняться по мере изменения состава соли. Таким образом, такие соли могут вести себя аналогично нестехиометрическим твердым соединениям.
[0057] Нестехиометрическое соединение может включать лантан. Нестехиометрическое соединение может включать стронций. Нестехиометрическое соединение может включать железо. Нестехиометрическое соединение может включать кислород. Нестехиометрическое соединение может включать по меньшей мере два элемента, выбранные из лантана, стронция, железа и алюминия. Нестехиометрическое соединение может включать по меньшей мере три элемента, выбранные из лантана, стронция, железа и алюминия. Нестехиометрическое соединение может включать лантан, стронций и железо и необязательно алюминий. Таким образом, нестехиометрическое соединение может включать лантан, стронций, железо и кислород и необязательно алюминий. Согласно некоторым конкретным вариантам соединение выбрано из La0.8Sr0.2FeO3-δ, La0.8Sr0.2Fe0.94Al0.06O3-δ, La0.7Sr0.3FeO3-δ, La0.7Sr0.3Fe0.94Al0.06O3-δ, La0.6Sr0.4FeO3-δ, La0.6Sr0.4Fe0.94Al0.06O3-δ и La0.5Sr0.5FeO3-δ. Согласно некоторым конкретным вариантам соединение представляет собой La0.7Sr0.3FeO3-δ (LSF).
[0058] Нестехиометрические соединения, подходящие для осуществления способов, в которых X обозначает серу, включают соединения, имеющие формулу Fe(1-a)S, где а обозначает величину между 0.1 и 0.9.
[0059] Нестехиометрические соединения, подходящие для осуществления способов, в которых X обозначает водород, включают соединения, имеющие формулу PdHb, где 0.02<b<0.58.
КРАТКОЕ ОПИСАНИЕ РИСУНКОВ
[0060] Ниже описаны варианты данного изобретения со ссылкой на прилагаемые рисунки, на которых:
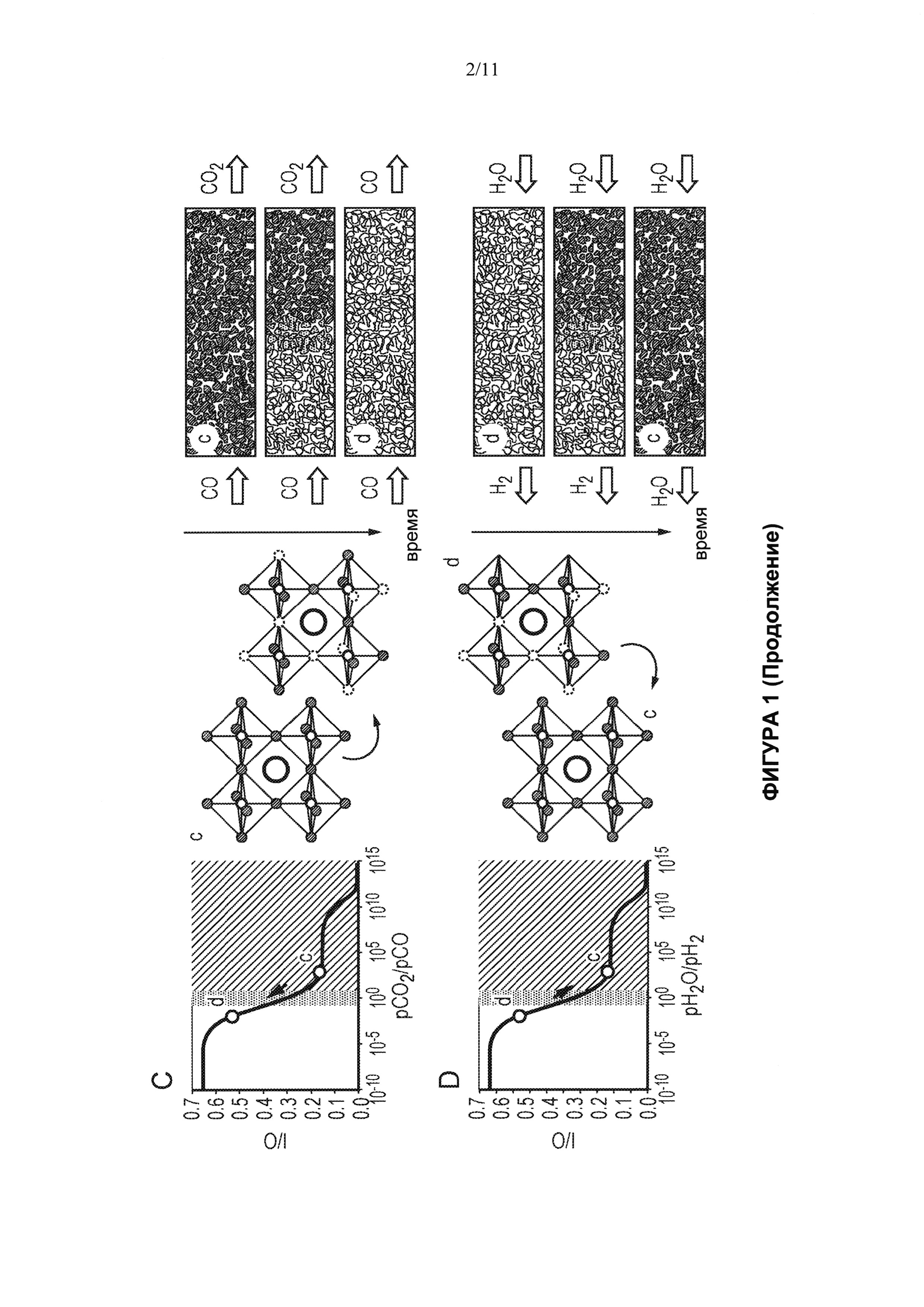
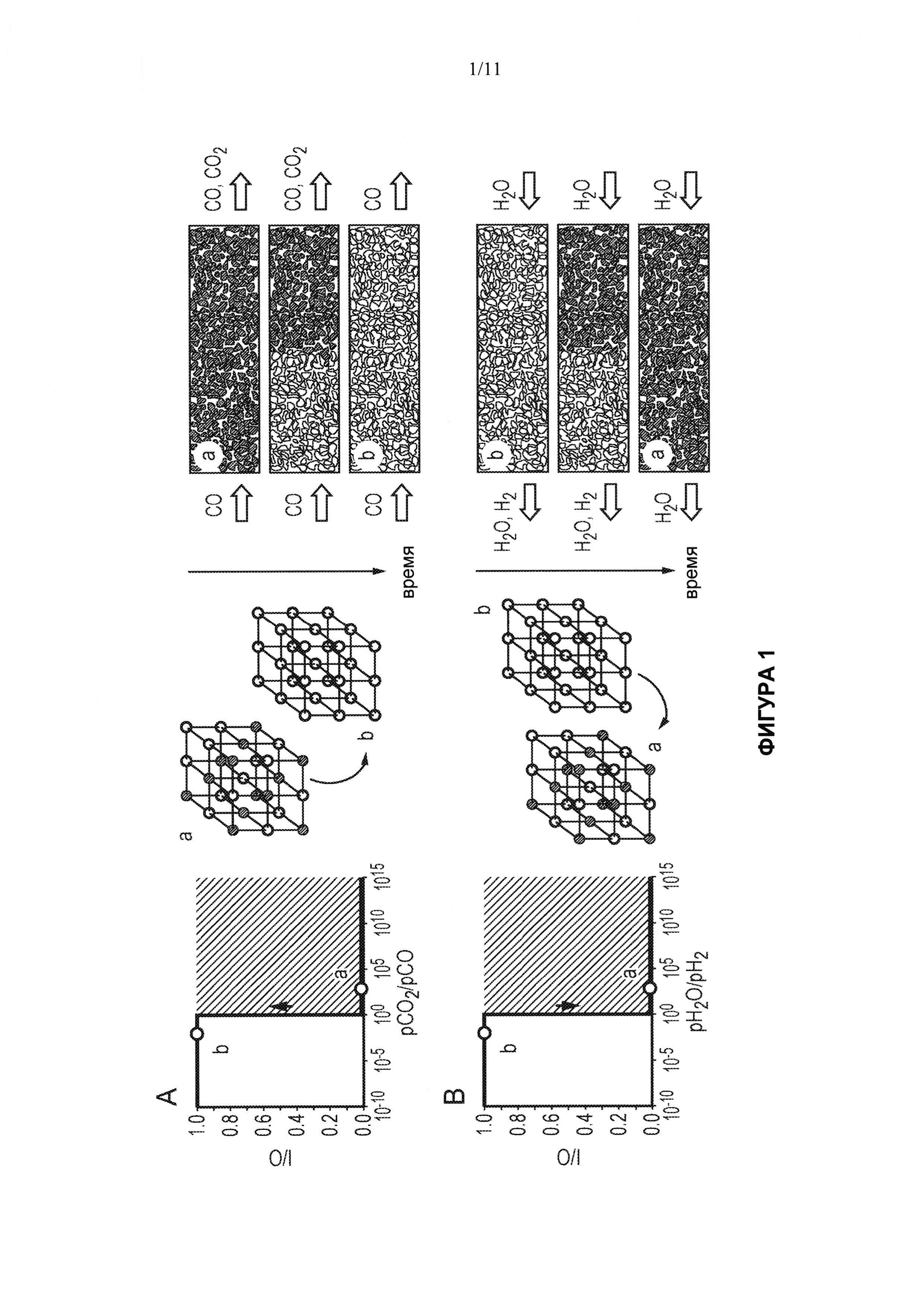
[0061] Фигура 1 отражает реакцию сдвига равновесия в системе вода-газ, протекающую в реакторе противоточного типа с использованием (А и В) гипотетического носителя кислорода - металла-оксида металла общей формулы MO1-δ, который подвергается фазовому изменению при парциальном давлении воды к водороду равном единице и (С и D) нестехиометрического соединения - носителя кислорода (La0.7Sr0.3FeO3-δ). Следует отметить, что при 817°С константа равновесия реакции в системе вода-газ равна единице и термодинамически отношение воды к водороду эквивалентно отношению диоксида углерода к монооксиду углерода. В левой колонке равновесная степень восстановления носителя кислорода, δ, показана как функция условий газовой фазы. В правой колонке представлена структура носителя кислорода. Система металл - оксид металла никогда не может характеризоваться низкими (меньше единицы) отношениями воды к водороду в поступающем потоке воды. (А) Монооксид углерода, подаваемый к слою оксида металла, вызывает восстановление соединения оксида металла до металла, а к b, и увеличение δ. Отношение диоксида углерода к монооксиду углерода в выходящем газе будет равно единице в равновесном состоянии до тех пор, пока в слое остается некоторое количество оксида металла. (В) Когда вода подается в противоположный конец слоя, металл начинает снова окисляться с получением а из b. В выходящем газе будет достигаться отношение воды к водороду равное единице. (С) Монооксид углерода, подаваемый к нестехиометрическому соединению - носителю кислорода, вызывает восстановление этого соединения с получением d из с и увеличение δ. Так как первоначально выходящие газы выходят в контакте с окисленным нестехиометрическим соединением, они характеризуются высоким отношением диоксида углерода к монооксиду углерода (значительно больше единицы). (D) Когда к противоположному концу слоя подается вода, указанное соединение начинает снова окисляться с получением с из d. Снова, так как выходящие газы выходят в контакте с окисленным нестехиометрическим соединением, они характеризуются низким отношением диоксида углерода к монооксиду углерода (значительно меньше единицы).
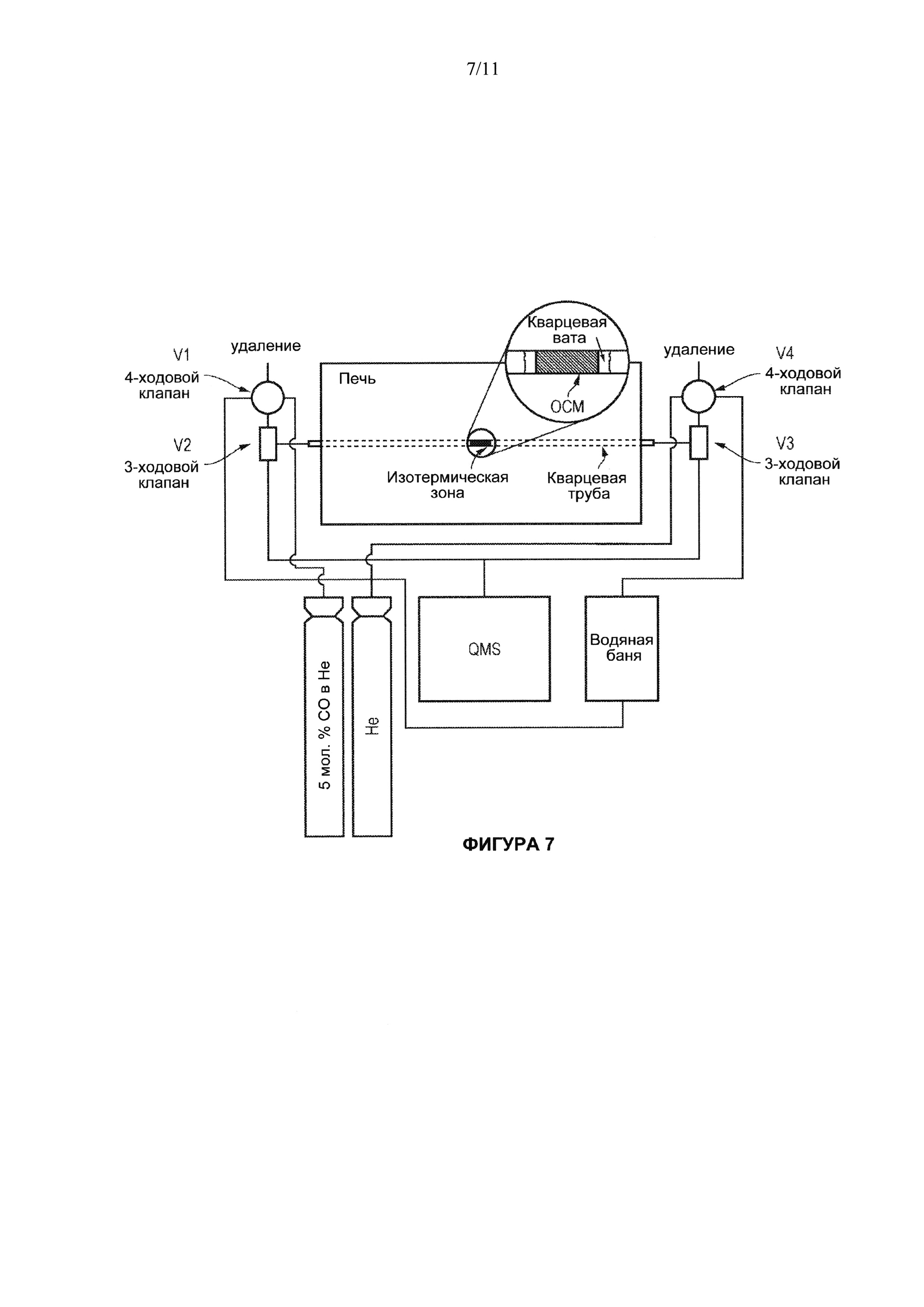
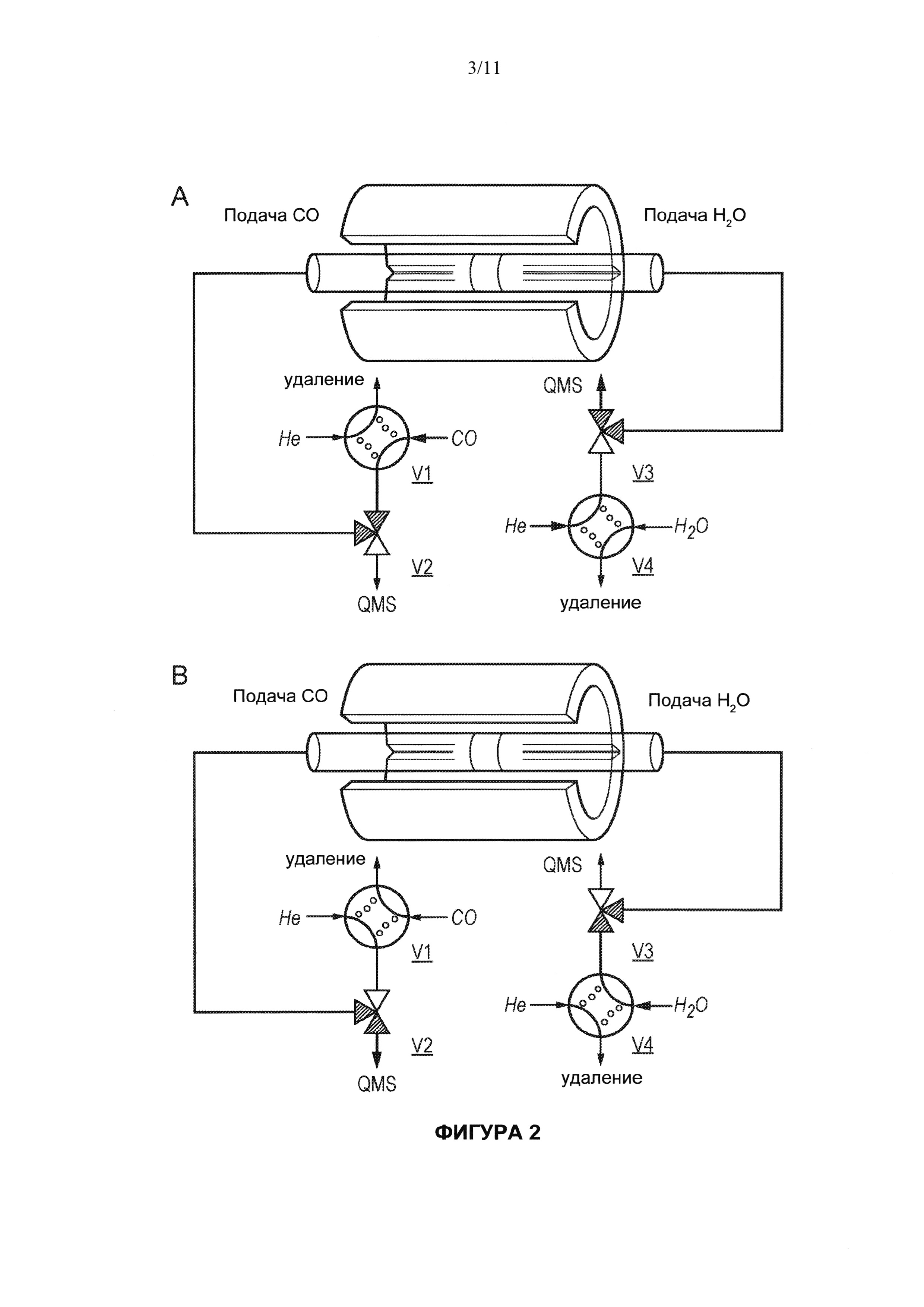
[0062] На Фигуре 2 схематически показан интегральный реактор противоточного типа с неподвижным слоем, включающий кварцевую трубку со слоем носителя кислорода, удерживаемого на месте при помощи кварцевой ваты. Носитель кислорода помещали в центре изотермической печи и полностью размещали в ее изотермической зоне. (А) показывает положения клапанов для доставки монооксида углерода, (В) показывает положения клапанов для доставки воды. Следует отметить, что четырехходовые клапаны обеспечивают непрерывное поступление реагентов, даже если они не доставляются в реактор.
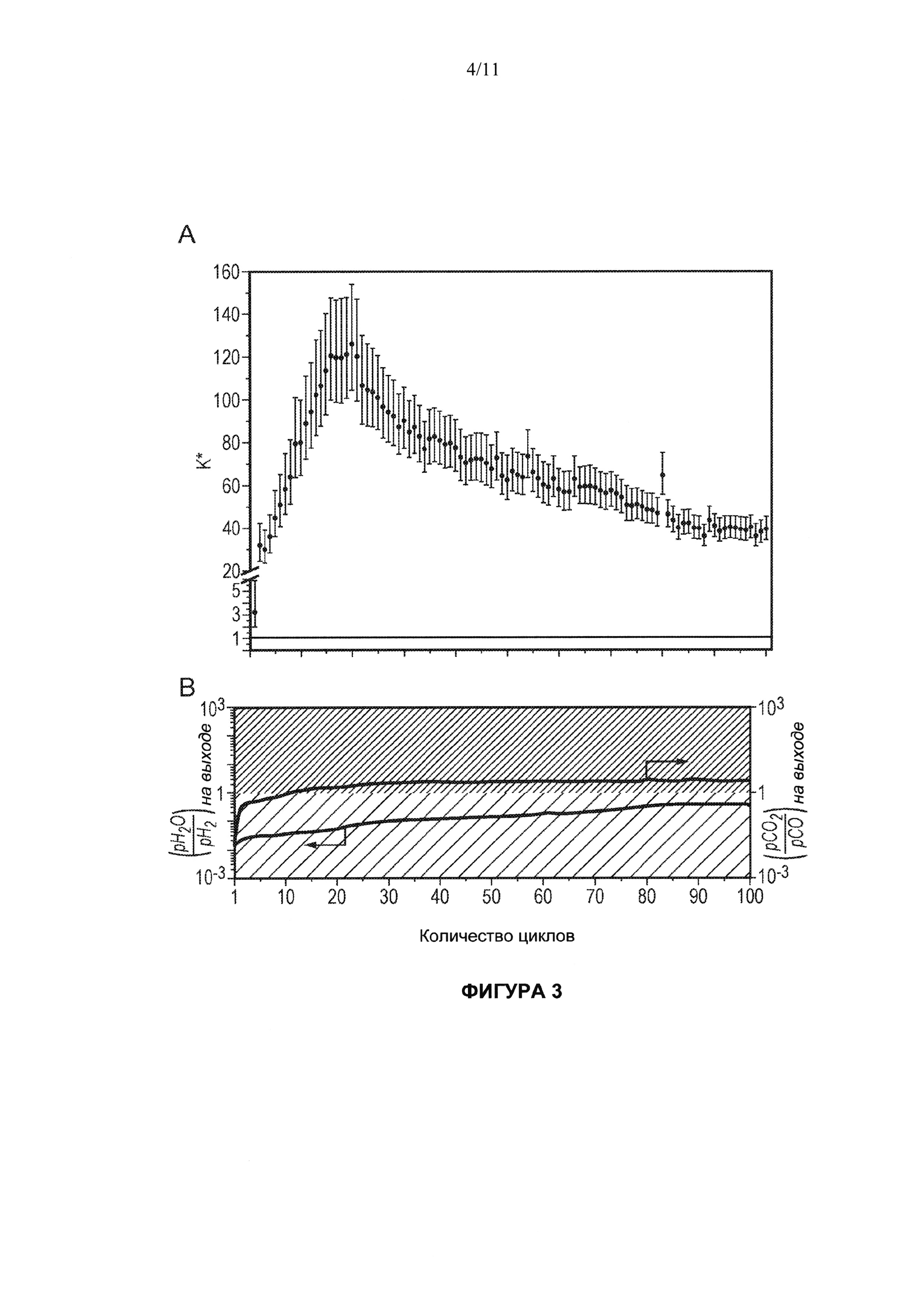
[0063] Фигура 3 показывает процесс изменения K* (определение дано ниже) в зависимости от числа циклов (обратите внимание на прерванную ось y) для первоначально предварительно восстановленного носителя кислорода LSF. Полуциклы восстановления используют 5 мол. % монооксида углерода в среде гелия в течение промежутка времени в 60 с. Полуциклы окисления используют 5 мол. % воды в среде гелия в течение промежутка времени в 60 с. Между полуциклами реактор продували гелием (120 с). Использовалась температура равная 820°С. Общая скорость потока была на всем протяжении постоянной - 3.7×10-5 моль/с (50 мл (STP)/мин). (В) показывает процесс изменения отношений конечного парциального давления на выходе (логарифмическая шкала) при проведении полуциклов в зависимости от количества циклов.
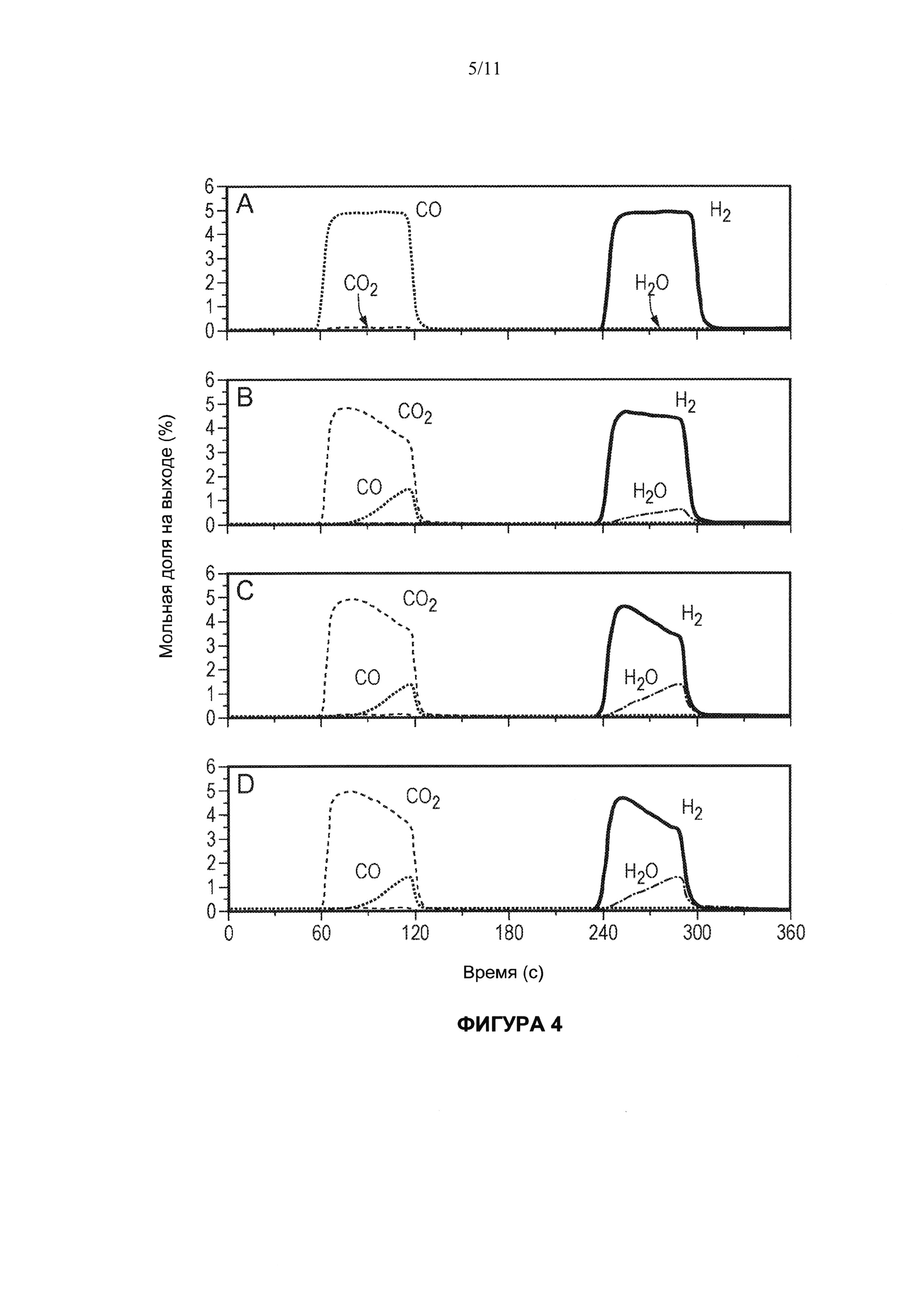
[0064] На Фигуре 4 показан процесс изменения молярной концентрации компонентов на выходе в зависимости от времени при использовании предварительно восстановленного LSF. На Фигуре (А) показаны молярные концентрации компонентов на выходе для Цикла 1; (В) для Цикла 50; (С) для Цикла 90; и (D) для Цикла 99. Циклы 90 и 99 не отличаются друг от друга и воспроизводятся. В полуциклах восстановления используют 5% (мол.) монооксида углерода в гелии в течение 60 секунд. В полуциклах окисления используют 5% (мол.) воды в гелии в течение 60 секунд. Между полуциклами реактор продували гелием, чтобы гарантировать, что эффекты полуциклов не накладываются друг на друга. Использовалась температура 820°С. Скорость потока была все время постоянной и составляла 3.7×10-5 моль/с (50 мл (STP)/мин).
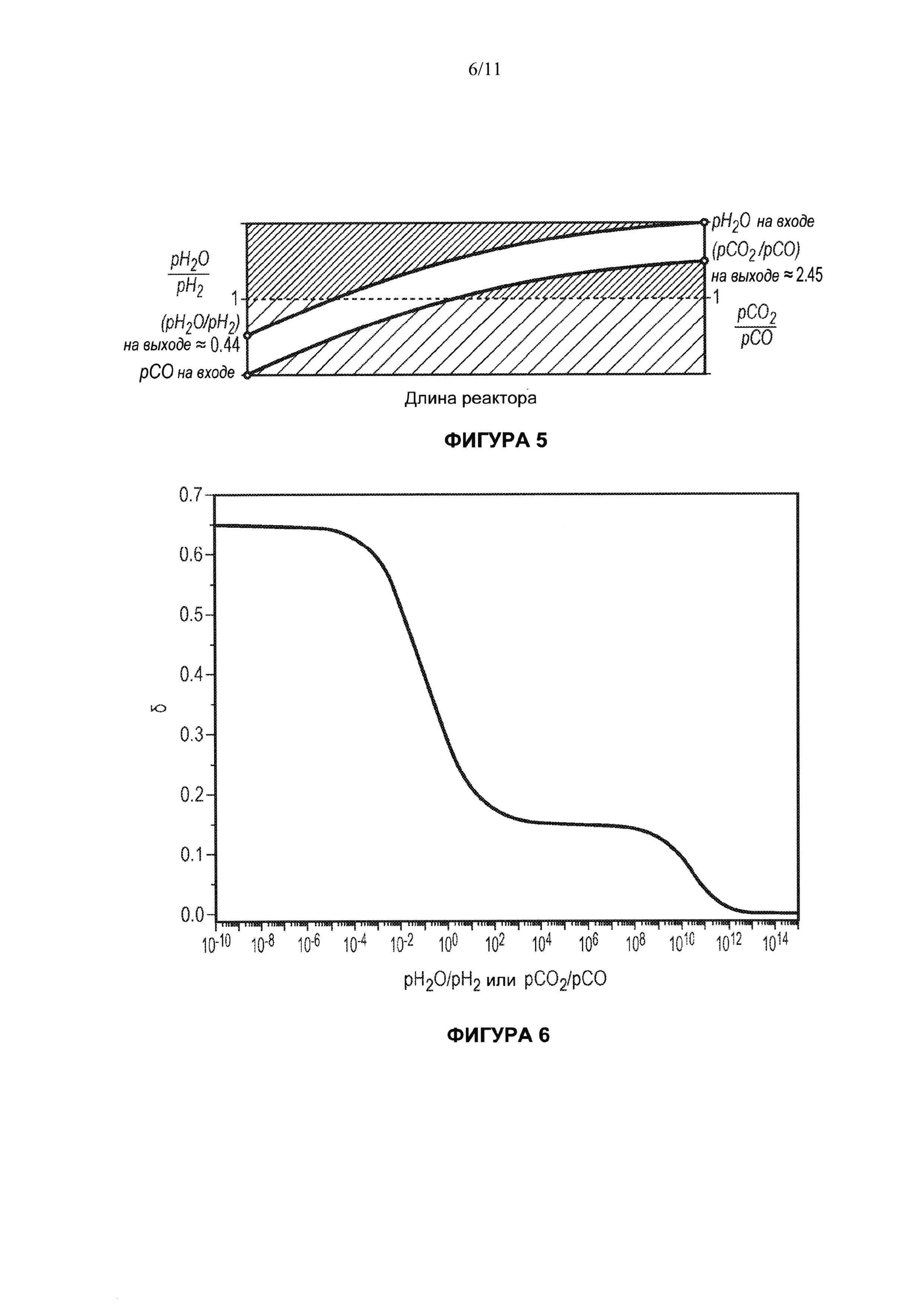
[0065] На Фигуре 5 схематически показано состояние материала носителя кислорода в конце полуциклов восстановления-окисления в процессе многократного периодического повторения циклов. Подача восстановителя осуществляется слева, а окислителя справа. Числовые значения, относящиеся к соотношениям в составе газа (в логарифмической шкале), представляют собой значения, соответствующие конечному составу газа на выходе, и, соответственно, предполагается, что твердое вещество находится в равновесии с газовой фазой. Следует отметить, что условия на входе нечетко охарактеризованы с точки зрения термодинамики и являются лишь типическими. Более "быстрая кинетика" (скорость реакции) процесса окисления воды по сравнению с кинетикой восстановления монооксида углерода (см. Пример 3) означает, что степень окисления (неподвижного) слоя в целом выше, чем вообще-то ожидалось, и объясняет изгибы в профилях.
[0066] На Фигуре 6 показана зависимость равновесного значения δ при 817°С для La0.7Sr0.3FeO3-δ от отношения парциального давления воды к парциальному давлению водорода или парциального давления монооксида углерода к парциальному давлению диоксида углерода.
[0067] На Фигуре 7 представлена принципиальная схема работы интегрального реактора. Клапаны V1, V2, V3 и V4 регулируют характер и направление газового потока к интегральному реактору с уплотненным слоем. Поток, содержащий 5 мол. % монооксида углерода в гелии, доставляется непосредственно из сертифицированного баллона (5.03 мол. % монооксида углерода, ВОС, UK) к уплотненному слою реактора. Поток, содержащий 5 мол. % воды в гелии, доставляется с помощью гелия (чистота 99.996%, ВОС, UK), насыщение которым осуществляется в сатураторной системе на водяной бане. Материал носителя кислорода удерживается в центральной изотермической зоне печи с помощью кварцевой ваты.
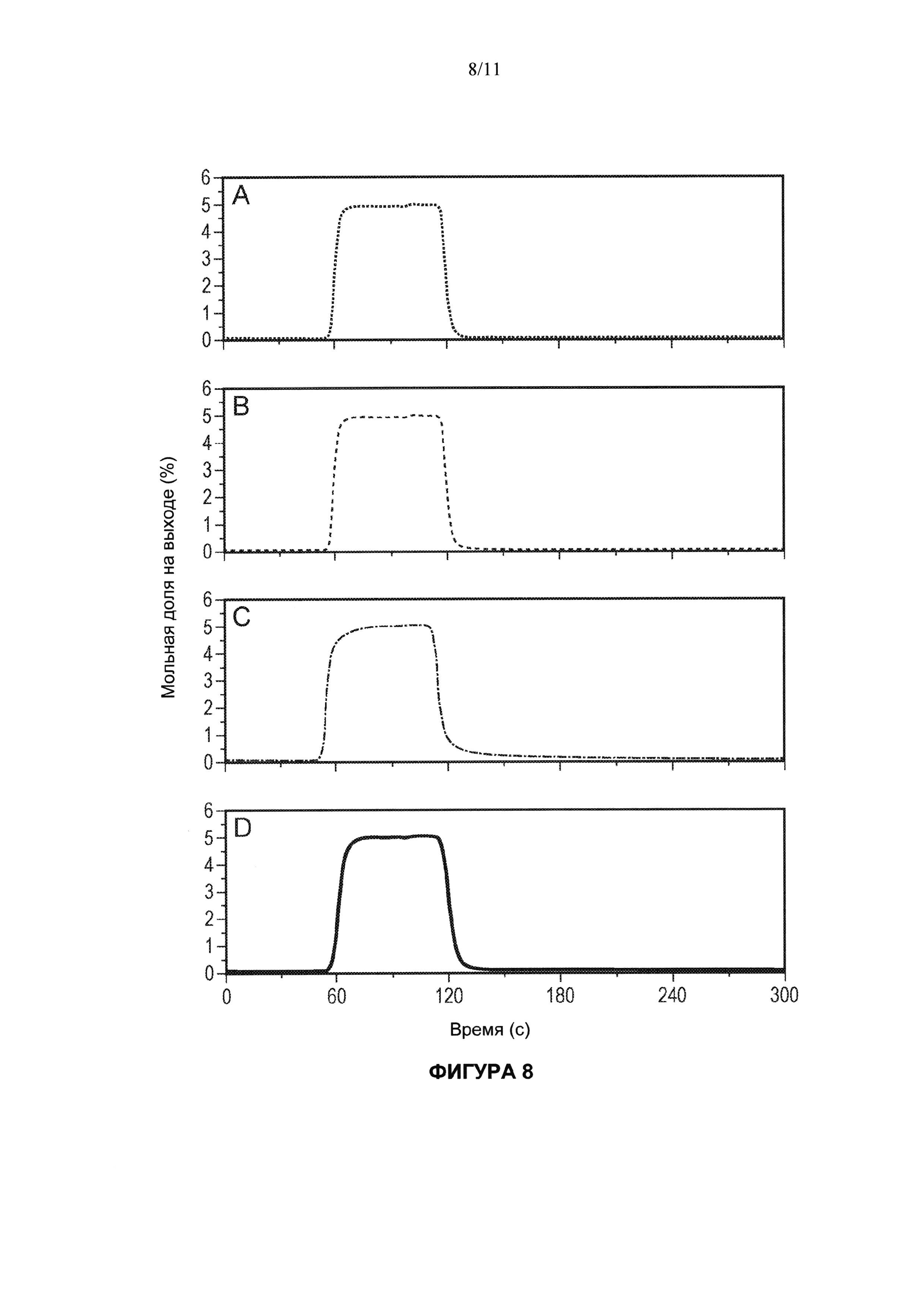
[0068] На Фигуре 8 показаны результаты экспериментов по распределению времени пребывания для (А) 5 мол. % монооксида углерода в гелии, (В) 5 моль. % диоксида углерода в гелии, (С) 5 мол. % воды в гелии и (D) 5 мол. % водорода в гелии. Химически активный газ вводили на время 60 с за 30 с; общая скорость потока была постоянной все время и составляла 3.7×10-5 моль/с (50 мл (STP)/мин) при 820°С. Протяженность неподвижного слоя была 6 см (~6 г) LSF. Перед экспериментами по распределению времени пребывания с монооксидом и водородом (А и D) неподвижный слой полностью восстанавливали, а перед экспериментами по распределению времени пребывания с диоксидом и водой (В и С) неподвижный слой подвергали полному окислению.
[0069] На Фигуре 9 представлены изображения, полученные с помощью SEM (растрового (сканирующего) электронного микроскопа, РЭМ, СЭМ) при двух различных увеличениях. На снимках (А) и (В) показан свежий материал LSF-носителя кислорода после обжига на воздухе, на снимках (С) и (D) показан материал LSF-носителя кислорода после предварительного восстановления 5 мол. % монооксидом углерода в гелии в течение 4.32×104 с (12 часов) при 820°С, и на рисунках (Е) и (F) показана центральный участок (из пяти участков равной длины) слоя материала LSF-носителя кислорода в реакторе после предварительного восстановления 5 мол. % монооксидом углерода в гелии в течение 4.32×104 с (12 часов) и последующих ста редокс-циклов с использованием 5 мол. % монооксида углерода в гелии и 5 мол. % воды в гелии при 820°С.
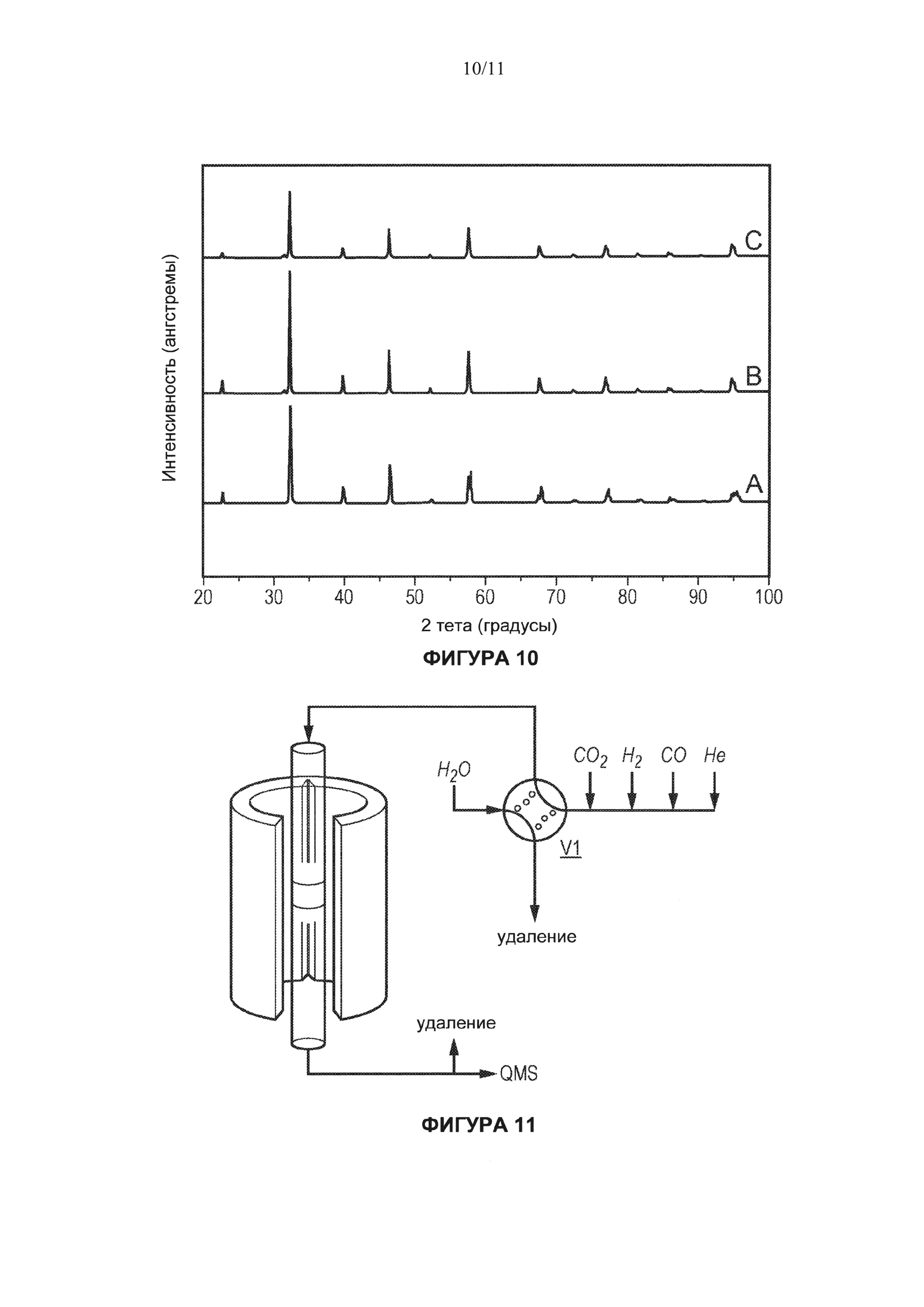
[0070] На Фигуре 10 показан дифракционный (рентгеновский) спектр образца LSF на различных стадиях эксперимента. На рисунке (А) показан спектр свежего материала LSF-носителя кислорода после обжига на воздухе, на снимке (В) показан материал LSF-носителя кислорода после предварительного восстановления 5 мол. % монооксидом углерода в гелии в течение 4.32×104 с (12 часов) при 820°С, и на рисунке (С) показан центральный участок (из пяти участков равной длины) слоя материала LSF-носителя кислорода в реакторе после предварительного восстановления 5 мол. % монооксидом углерода в гелии в течение 4.32×104 с (12 часов) и последующих ста редокс-циклов с использованием 5 мол. % монооксида углерода в гелии и 5 мол. % воды в гелии при 820°С.
[0071] На Фигуре 11 показан реактор дифференциального типа, применяемый для кинетических исследований. Поток направляется в реактор с помощью двухпозиционного четырехходового Клапана V1. Вода поступает постоянно, тогда как подача других газов является периодической. Протяженность неподвижного слоя обычно составляла 0.3 см (50 мг материала LSF носителя кислорода), а внутренний диаметр трубки с образцом был равен примерно 0.38 см. Вес процесс пропускания по трубке проводили при нагревании до 120°С с помощью сетевого нагревателя с целью избежать конденсации воды.
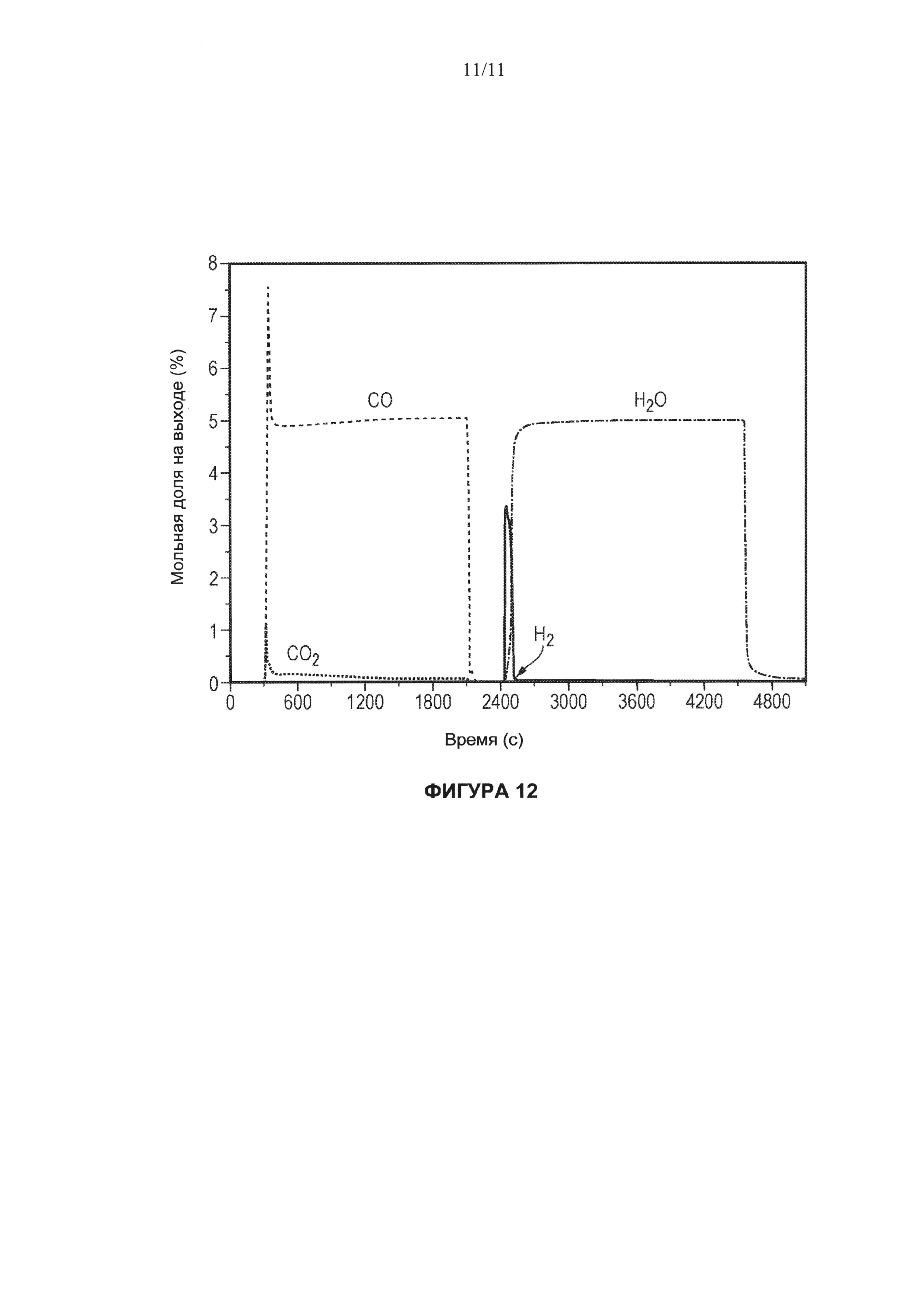
[0072] На Фигуре 12 показан состав, в мольных долях, на выходе в зависимости от времени в процессе работы 'дифференциального' реактора. Для процесса восстановления пропускают 5 мол. % монооксида углерода в гелии в течение 1800 с (30 минут). Для процесса окисления пропускают 5 мол. % воду в гелии в течение 1800 с (30 минут). Между процессами окисления и восстановления реактор продували гелием. Температура составляла 850°С. Скорость потока была постоянной все время и составляла 7.4×10-5 моль/с (100 мл (STP)/мин). Масса образца LSF составляла примерно 50 мг.
ОСУЩЕСТВЛЕНИЕ ИЗОБРЕТЕНИЯ
[0073] Нестехиометрическое соединение означает соединение, в котором содержание элемента X выражается не целочисленной величиной. Нестехиометрические материалы, пригодные для применения в способах по данному изобретению, имеют переменную степень нестехиометричности. Так они имеют общую формулу MnXp(1-q), где n и p обозначают целые числа, необходимые для стехиометрического связывания между М и X и 0<q<1 или 0>q>-1; при этом соединение способно принимать диапазон значений q; и М может независимо в каждом случае может представлять собой один элемент или смесь более чем одного элемента. Соединение выбирают таким образом, что значение q меняется в соответствии с химическим окружением, с которым это соединение экспонируется.
[0074] Так, степень нестехиометричности X может быть непрерывной. Другими словами, может быть таким образом, что градиент на кривой содержания X в зависимости от химического потенциала X никогда не будет бесконечной величиной. Например, это может быть соединение, которое не претерпевает никаких фазовых переходов оттого, что оно принимает или отдает больше элемента X. Или же это может быть соединение, которое претерпевает большое число фазовых переходов в связи с тем, что оно принимает или отдает элемент X. Так, возможно, что соединение претерпевает четыре или более фазовых переходов в связи с тем, что оно принимает или отдает элемент X (например, 6 или более фазовых переходов или 10 или более фазовых переходов). Следовательно, возможно, что нестехиометрическое соединение, применяемое в способах по изобретению, либо не претерпевают никаких фазовых переходов в связи с тем, что оно принимает или отдает элемент X, или оно претерпевает четыре или более фазовых переходов.
[0075] Из объема изобретения исключается нестехиометричность, которая в природных условиях является результатом случайных термодинамических дефектов в объемном кристалле. Возможно, что q имеет значение от 0.01 до 0.99. Возможно, что q имеет значение от 0.05 до 0.95. Возможно, что q имеет значение от 0.1 до 0.9.
[0076] Если М представляет собой несколько элементов, может случиться так, что эти элементы присутствуют в целочисленным отношении друг к другу, или может случиться так, что эти элементы присутствуют в нецелочисленным отношении друг к другу. Так, если М представляет собой два различных элемента Ма и Мb, то Мn можно было бы представить как Man1Mbn2, где n1 и n2 обозначают целые числа и сумма n1 и n2 равна n. Или же может случиться так, что, n1 and n2 не являются целыми числами и сумма n1 и n2 равна 1. Аналогично, если М обозначает смесь трех элементов Мс, Md и Ме, Мn можно представить как Mcn3Mdn4Men5, где n3 обозначает целое число и сумма n4 и n5 обозначает целое число, и где сумма n3, n4 и n5 равна n. М может представлять собой два или более различных элементов. М может представлять собой вплоть до четырех различных элементов.
[0077] Элементы, представляющие собой металлы, включают: Li, Be, Na, Mg, K, Ca, Sc, Ti, V, Cr, Mn, Fe, Co, Ni, Cu, Zn, Al, Rb, Sr, Y, Zr, Nb, Mo, Ru, Rh, Pd, Ag, Cd, In, Sn, Sb, Cs, Ba, La, Ce, Pr, Nd, Sm, Eu, Gd, Tb, Dy, Ho, Er, Th, Yb, Lu, Hf, Та, W, Re, Os, Ir, Pt, Au, Hg, Tl, Pb и Bi.
[0078] Типичные перовскиты имеют структуру формулы АВО3, где А и В представляют собой металлы. А может быть лантанидом, а В может представлять собой переходный металл. Лантанид, или редкоземельный элемент, представляет собой элемент с атомным номером в диапазоне от 57 (лантан) и до 71 (лютеций) в Периодической таблице элементов в соответствии с указаниями ИЮПАК (IUPАС). Обычно в группу лантанидов включают иттрий (атомный номер 39). Типичным лантанидом является лантан. Примеры переходных металлов включают титан, ванадий, хром, марганец, железо, кобальт, никель, медь и цинк.
[0079] Компонент А и/или компонент В перовскита может иметь примеси других элементов для повышения устойчивости и активности. Так, компонент А может быть дополнен примесью щелочноземельного металла, например, стронция. Компонент В может содержать в качестве примеси алюминий.
[0080] Термин 'органическая молекула' относится к любому соединению, содержащему как углерод, так и водород. Органические молекулы могут также содержать другие элементы, например, кислород, азот и серу. Примеры органических молекул включают углеводороды, спирты (например, метанол), карбоновые кислоты (например, уксусную кислоту или жирные кислоты), ароматические соединения (например, бензол, толуол), кетоны (ацетон), альдегиды и т.д. Способы по данному изобретению можно применять к смесям органических молекул, например, смесям нефтепродуктов или продуктов реакций в биореакторе.
[0081] Термин 'углеводород' относится к соединению, имеющему общую формулу СаН2а+2. Углеводород может представлять собой C1-С6 углеводород, т.е. углеводород вышеуказанной общей формулы, в которой а обозначает от 1 до 6, или С1-С4 углеводород, т.е. углеводород вышеуказанной общей формулы, в которой а обозначает от 1 до 4. Примеры углеводородов включает метан, этан и пропан.
[0082] Теоретически 'несмешанные' реакционные процессы по изобретению не подпадают под действие ограничений, накладываемых условиями равновесия, ассоциируемыми с обычными смешанными реакциями.
[0083] Носитель кислорода, который демонстрирует один фазовый переход, никогда не сможет применяться для преодоления ограничений, накладываемых условиями равновесия. На Фигуре 1В (левый рисунок) показано равновесное содержание кислорода в системе металл/оксид металла в зависимости от отношения воды к водороду в газовой фазе, действию которой эта система подвергается. Фазовый переход и, следовательно, поглощение и высвобождение кислорода происходит всего при одном значении отношения воды к водороду, т.е. имеется разрыв (нарушение непрерывности) в содержании кислорода материала - носителя кислорода как функция химического потенциала кислорода. Повышенный восстановительный потенциал потока поступающего монооксида углерода расходуется за счет материала, который не может соответствовать этому восстановительному потенциалу; у материала отсутствует память об условиях его соответствия, и реализуется термодинамическая необратимость. Для того, чтобы преодолеть ограничения, накладываемые условиями равновесия, требуется материал, у которого не наблюдается такого нарушения непрерывности в содержании кислорода в зависимости от химического потенциала кислорода. Таким образом, этот материал будет обладать 'памятью' о природе, например, восстановительного газа, с которым он экспонировался. В результате отсутствует утрата информации о реакции. Такие материалы можно найти, и примером являются нестехиометрические твердые вещества, или, в данном случае, нестехиометрические оксиды. На Фигуре 1D (левый рисунок) показано значение δ (степени нестехиометричности) для La0.7Sr0.3FeO3-δ (LSF) в зависимости от отношения воды к водороду при 817°С. Как можно видеть, δ непрерывно меняется при изменении валентности железа, отвечающей степени окисления в кристаллической решетке перовскита. Это означает, что если восстановительный газ использовать при конкретном отношении воды к водороду, то в принципе мы обязательно сумеем добиться (восстановить) такого же отношения воды к водороду в продукте (см. более подробный термодинамический анализ в Примере 1).
[0084] Конверсию водяного газа осуществляли в реакторе с неподвижным слоем (Фигура 2), находящимся непосредственно рядом с потоком, движущимся в поршневом пробковом режиме (т.е. с временной постоянной, значительно меньше обусловленной смешением в газовой фазе, нежели продолжительностью импульсов (подачи) реагентов), и упакованным с нестехиометрическим LSF носителем кислорода (см. Пример 2). Следует подчеркнуть, что применяют реактор с неподвижным слоем (отсутствует перемешивание твердых веществ). В реакторе с псевдоожиженным слоем (обычный способ осуществления организации химических циклов) наблюдается интенсивное перемешивание твердых веществ, нежелательное в данном случае, так как такое перемешивание стирает 'память' твердого вещества о газовой фазе, с которой оно экспонировалось. Носитель кислорода многократно восстанавливался в монооксиде углерода (Фигура 2А) и окислялся в воде после изменения направления потока на обратный (Фигура 2В). Сто полных редокс-циклов с 5 мол. % монооксида углерода в инертном носителе, гелии, и 5 мол. % воды в гелии при 820°С (эта температура является достаточно близкой к 817°С, поэтому имеется в виду, что константа равновесия реакции конверсии водяного газа равна примерно единице) и атмосферном давлении проводили над предварительно восстановленным LSF. В промышленных масштабах эту реакцию было бы лучше проводить при более высоком парциальном давлении монооксида углерода и воды. Однако константа равновесия не зависит от давления, поэтому мы можем продемонстрировать принцип преодоления ограничений, накладываемых условиями равновесия, при любом давлении и при любой молярной концентрации на входе.
[0085] В качестве показателя того, что равновесие удалось преодолеть, мы определяем для каждого цикла величину K*, которая представляет собой минимальную константу равновесия, которая потребовалась бы для достижения усредненных по времени (усредненных в течение полного цикла) значений парциального давления, 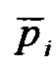 , или молярных концентраций,
, или молярных концентраций, 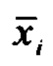 ,
,
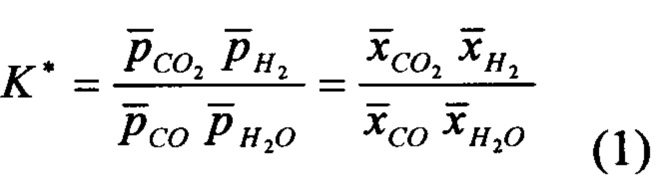
[0086] Для обычного реактора с перемешиванием реагентов величина K* никогда не сможет превысить константу равновесия реакции конверсии водяного газа, которая при этой температуре равна единице. Аналогично, величина K* никогда не сможет превысить единицу для носителя кислорода с одним фазовым переходом. Тем не менее возможно достичь значений K* больше единицы в интегральном реакторе с реверсируемыми потоками, содержащем LSF носитель кислорода, в результате осуществления многократных циклов (см. Фигуру 3А). Ожидается, что в первом цикле величина K* близка к единице с учетом того, что слой перед этим был восстановлен до однородного химического потенциала кислорода. Когда вводят воду, начинается окисление на поверхности по фронту воды; водный поток приходит в равновесие или близко к равновесию с неподвижным слоем (поскольку неподвижный слой был предварительно восстановлен, это соответствует высокой степени превращения (конверсии) в водород). Таким образом, за изменением состояния носителя кислорода могут последовать отношения воды к водороду и диоксида углерода к монооксиду углерода на выходе (Фигура 3В). На Фигуре 4А показаны молярные концентрации доли воды и водорода, полученные в первом цикле. Когда монооксид углерода вводят с одного конца неподвижного слоя, может образоваться небольшое количество диоксида углерода (Фигура 4А) вследствие восстановленного характера носителя кислорода. При повторных циклах слой, близкий ко входу воды, будет постепенно становиться окисленным, что приводит к заметной конверсии монооксида углерода, когда поток меняет направление (например, Цикл 50, Фигура 4В), в то же время все еще сохраняется высокая степень конверсии воды. В этих условиях ожидается максимальное значение K* (высокая степень конверсии воды при увеличивающейся конверсии активатора) в соответствии с Фигурой 3А. По мере продолжения осуществления циклов состояние неподвижного слоя, близкого к выходу воды, начинает становиться более окисленным и степень конверсии воды падает. Наконец, когда циклы становятся многократными (например, Цикл 90, Фигура 4С, и Цикл 99, Фигура 4D), конверсия воды и монооксида углерода становятся аналогичными (поскольку количественное окисление в ходе полуцикла воды должно быть равно восстановлению в полуцикле монооксида углерода) и K* имеет стабильное значение. Конверсия в водород составляет примерно 85%, в то же время конверсия монооксида углерода также составляет примерно 85% (например, Цикл 90, Фигура 4С, и Цикл 99, Фигура 4D). Стабильное значение K* здесь равно 40 (например, Циклы 90-100, Фигура 3), и совершенно ясно, что ограничения, накладываемые условиями равновесия, здесь преодолены. Фактически K* больше единицы для каждого индивидуального цикла.
[0087] С практической точки зрения стабильность носителей кислорода - это важный вопрос, который может ограничивать внедрение способов организации химических циклов. Причиной нестабильности материала носителя кислорода является обычное применение материалов, которые претерпевают фазовый переход. Однако согласно настоящему изобретению материал носителя кислорода LSF предназначен для того, чтобы оставаться в фазе перовскита. Действительно, изображения SEM и спектры XRD носителя кислорода LSF до и после осуществления повторных циклов (Фигуры 9 и 10) не показывают никакого заметного изменения в структуре. Помимо этого, деление конечного неподвижного слоя материала LSF носителя кислорода на пять равных участков не показало никакого изменения свойств LSF носителя кислорода вдоль оси материала (см. Пример 2).
[0088] На Фигуре 5 наглядно представлено потенциальное изменение состояния материала носителя кислорода между восстановительными и окислительными циклами. Изменение средней степени нестехиометричности (средней вдоль всего неподвижного слоя) LSF в направлении от окисленного слоя до восстановленного слоя можно рассчитать из баланса кислорода на газовую фазу. После того, как циклы стали многократными, примерно, в ходе Цикла 90, изменение средней степени нестехиометричности между окислением и восстановлением стабилизируется при значении примерно 0.003. Отсюда следует, что используется относительно малая доля кислорода, имеющегося в неподвижном слое. Эту долю можно повысить за счет использования материала с большей площадью поверхности или условий, в которых перенос кислорода твердым веществом происходит быстрее, тем самым быстрее удаляется кислород с поверхности носителя. Кроме того, увеличение времени пребывания на неподвижном слое обеспечило бы более высокую степень конверсии в водород за счет большей продолжительности.
[0089] По всему описанию и в формуле настоящего изобретения слова "включать" и "содержать" и их варианты означают "включать, но без ограничения", и они не предназначены для того, чтобы исключить (и не исключают) другие молекулы, добавки, компоненты, целые числа или стадии. По всему описанию и в формуле настоящего изобретения существительные в единственном числе охватывают существительные во множественном числе, если по контексту не подразумевается иное. В частности, следует понимать, что, если по контексту не требуется иное, вспомогательные слова, характеризующие единственное число, относятся к описанию как в единственном, так и во множественном числе, если по контексту не требуется иное.
[0090] Следует отдавать отчет, что признаки, целые числа, характеристики, соединения, химические молекулы или группы, описанные в отношении конкретного аспекта, варианта или примера по изобретению, применимы к любому другому аспекту, варианту или примеру по данному описанию, если только они не являются несовместимыми. Все признаки, раскрываемые в данной заявке (включая прилагаемые формулу изобретения, реферат и фигуры), и/или все стадии любого способа или процесса, раскрываемые при этом, можно объединять в любой комбинации за исключением комбинаций, в которых по меньшей мере некоторые из таких признаков и/или стадий являются взаимоисключающими. Изобретение не ограничено элементами каких-либо вышеприведенных вариантов. Изобретение распространяется на любой новый признак или на любую новую комбинацию признаков, раскрываемых в настоящей заявке (включая прилагаемые формулу изобретения, реферат и фигуры), или к любой новой стадии или к любой новой комбинации стадий любого способа или процесса, раскрываемого в настоящей заявке.
[0091] Вниманию читателя предлагаются все статьи и документы, которые поданы одновременно с данной заявкой или до данной заявки вместе с данной заявкой, и которые выложены для всеобщего ознакомления с помощью данного описания, и содержание всех этих статей и документов включено в настоящее изобретение посредством отсылки.
ПРИМЕР 1 - ТЕРМОДИНАМИЧЕСКИЙ АНАЛИЗ
[0092] Монооксид углерода и вода смешивались и подавались в обычный реактор, где происходила реакция конверсии водяного газа,
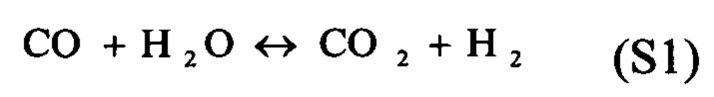
[0093] Если скорость (кинетика) реакции достаточно "быстрая", чтобы газы достигли равновесия, тогда
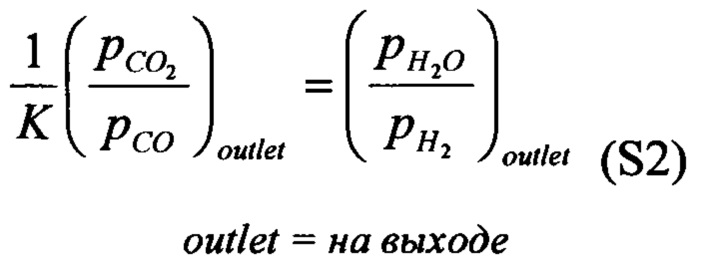
где значения парциального давления, pi, определяемые на выходе, регулируются соотношением равновесия для реакции конверсии водяного газа.
[0094] В том случае, когда реакция конверсии водяного газа осуществляется методом организации химических циклов, схема реакции включает:
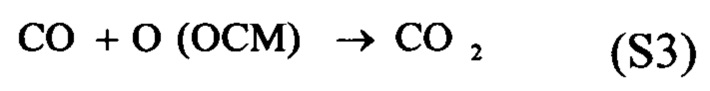

где О (ОСМ) обозначает кислород, ассоциированный с материалом носителя кислорода. Образуются раздельные потоки водорода (в воде) и диоксида углерода (в монооксиде углерода).
[0095] В том случае, когда носителем кислорода является соединение, у которого наблюдается один фазовый переход, значения парциального давления на выходе из реактора для проведения химических циклов регулируются соотношением равновесия
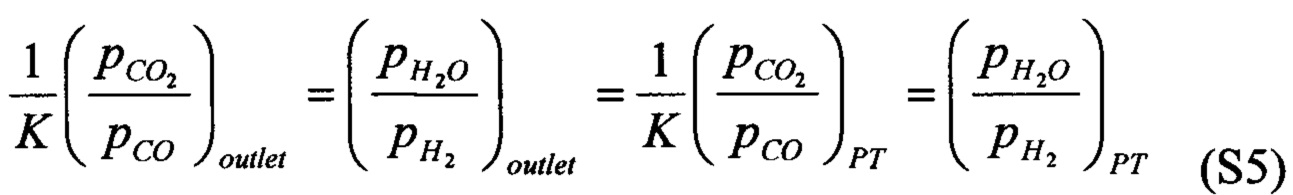
а при 817°С, когда константа равновесия равна единице,
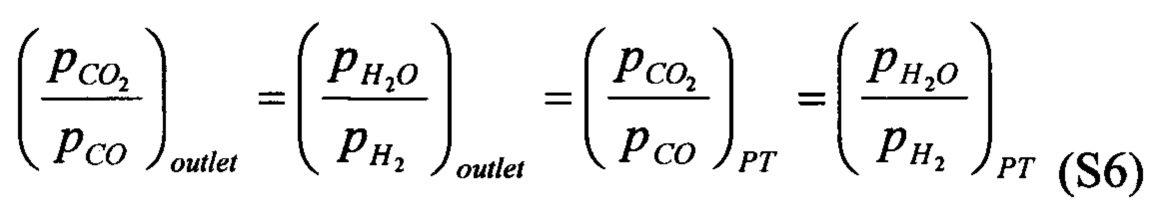
где РТ обозначает фазовый переход, относящийся к материалу носителя кислорода. Уравнения (S2) и (S5) содержат общие элементы, и соответственно, нельзя преодолеть ограничения, накладываемые условиями равновесия в случае, когда носитель кислорода имеет один фазовый переход.
[0096] Теперь рассмотрим конверсию водяного газа, осуществляемую методом организации химических циклов в реакторе с неподвижным слоем, заполненным нестехиометрическим оксидом. Если равновесие между газом и твердым веществом достигается на входе в слой при восстановлении и на выходе из слоя при окислении (одно и то же место в реакторе), тогда
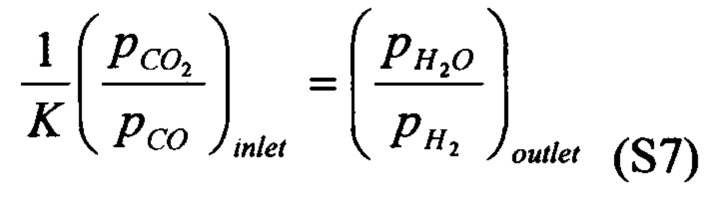
и при 817°С,
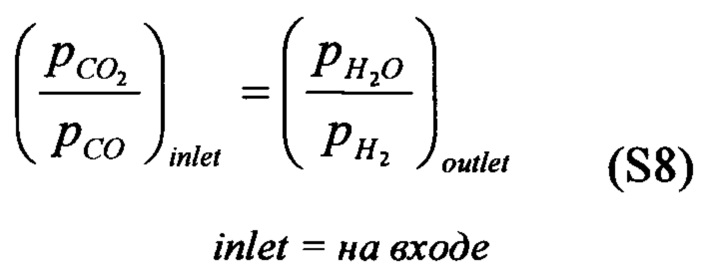
[0097] Следует обратить внимание на разницу между Уравнением (S7) и Уравнениями (S2), (S5). Когда мы смешиваем восстановительный и окислительный газы, все газы на выходе находятся в равновесии друг с другом (Уравнение (S2)). Аналогично, если мы используем носитель кислорода с одним фазовым переходом, самое лучшее, на что мы можем надеяться, это то, что выходящие газы находятся в равновесии друг с другом (Уравнение (S2)). Если мы используем обратный поток с нестехиометрическим носителем кислорода, наш выходящий газ в начале окислительной фазы находится в равновесии со входящим газом из восстановительной фазы (Уравнение (S7)). Это означает, что, если мы имеем низкое значение отношения диоксида углерода к оксиду углерода в подаваемом восстановителе, мы можем достичь такого же низкого значения отношения воды к водороду в нашем потоке продукта, выходящего из окислительной фазы. Не допуская смешения газов, используя процесс с обратным потоком на неподвижном слое (никакого перемешивания твердых веществ) и используя материал с непрерывным изменением нестехиометричности с отношением воды к водороду, мы способны достичь более высоких молярных концентраций водорода в потоке продукта, стремящихся к полной конверсии.
ПРИМЕР 2 - МАТЕРИАЛЫ И МЕТОДЫ
[0098] Нестехиометрическое соединение перовскитного типа лантан - стронциевый феррит (La0.7Sr0.3FeO3-δ или LSF) использовали в качестве носителя кислорода. Это соединение является нестехиометрическим со степенью нестехиометричности в равновесном состоянии, δ, определяемой отношением парциального давления воды к парциальному давлению водорода, с которыми это соединение экспонируется. Две реакции, которые регулируют степень нестехиометричности в LSF, это окисление и диспропорционирование Fe(III) в Fe(II) и Fe(IV). Используя систему Крёгера-Винка (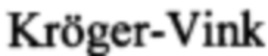 ), эти реакции можно представить как
), эти реакции можно представить как
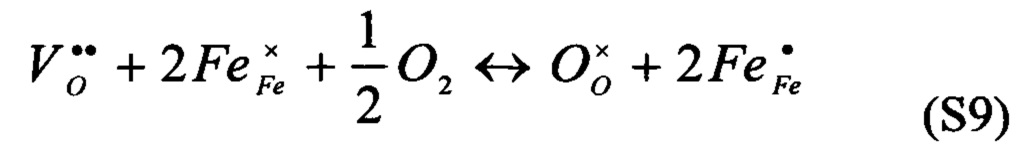
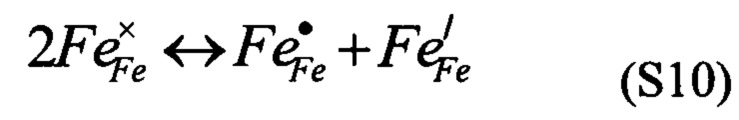
[0099] А константы равновесия для этих реакций можно определять как
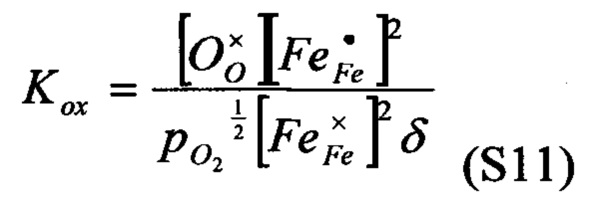
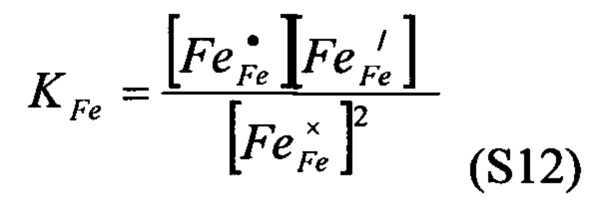
где в квадратных скобках приводится среднее число молекул на элементарную ячейку. Вместо того, чтобы использовать парциальное давление кислорода, можно использовать отношение парциального давления воды к парциальному давлению водорода, которое может быть в равновесии с этим парциальным давлением кислорода,
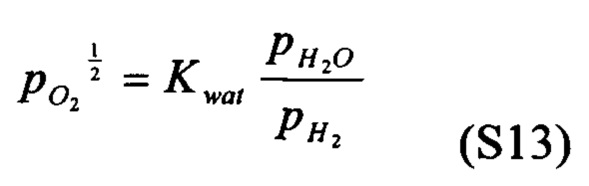
где Kwat обозначает константу равновесия для диссоциации воды:
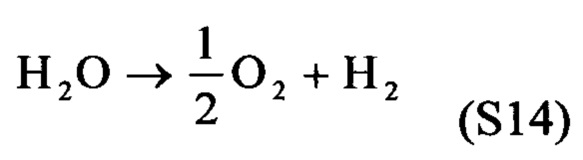
[00100] Применяя уравнения с (S11) до (S14), можно показать, что
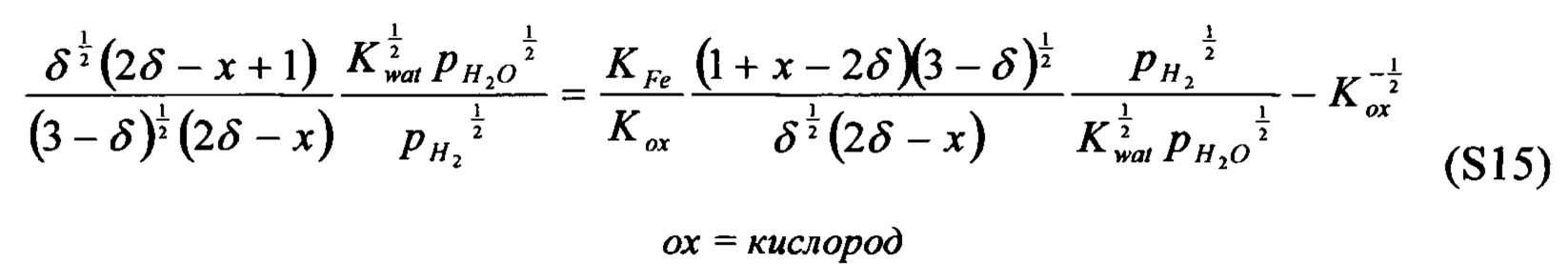
[00101] Это уравнение применяли с использованием констант равновесия для построения кривой на Фигуре 6.
[00102] Продажные порошки LSF (Praxair Speciality Ceramics, LSF имеет молекулярный вес 227.4 г/моль и плотность 1.26×103 кг/м3) гранулировали с использованием гидравлического пресса с последующим обжигом при 1250°С в течение 4.32×104 с (12 часов) на воздухе. Затем эти гранулы измельчали и просеивали, получая частицы (гранулы) нужного размера (80-160 мкм). Полученные частицы называют свежеполученными частицами (гранулами). Затем эти частицы (6 г (2.62×10-2 моля)) помещали в кварцевую трубку длиной 1 м с внутренним диаметром 8 мм; частицы удерживались на месте с помощью кварцевой ваты. Частицы располагали в изотермической зоне (температуру и изотермичность которой подтверждали с помощью дополнительной подвижной термопары) печи (как показано на Фигуре 7).
[00103] Выходящие газы, содержащие монооксид углерода, диоксид углерода, воду, водород и гелий, поступали в квадрупольный масс-спектрометр (QMS) с "мягкой ионизацией" (QGA Quantitative Gas Analysis unit, Hiden Analytical Ltd., UK) no капиллярной линии с обогревом для непрерывного анализа в реальном времени. QMS калибровали по воде по сравнению с конденсационным гигрометром с охлаждаемым зеркальцем (СМН-1, 182 Alpha Moisture Systems, UK). Погрешность в определяемых мольных долях (молярных концентрациях) по оценке составляла ±2% от определяемой мольной доли. Разрешение QMS было равно примерно 100 м. д.
[00104] Перед началом осуществления циклов частицы восстанавливали в смеси 5 мол. % монооксида углерода в гелии (сертифицированный стандарт 5.03 мол. % монооксида углерода в гелии, ВОС, UK) в течение 4.32×104 с (12 часов) при 820°С. Поскольку LSF предварительно прокаливали на воздухе при 1250°С, а затем охлаждали до комнатной температуры, мы рассчитывали, что после прокаливания (перед восстановлением) величина δ для LSF будет постоянной, равной, примерно, 0.15, на основании плато на кривой зависимости δ от 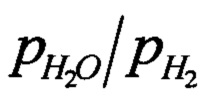 (например, для воздуха эффективное отношение
(например, для воздуха эффективное отношение 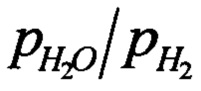 составляет 4.7×108 при 820°С). Мы полагали, что после предварительного восстановления δ может иметь значение примерно 0.5 или выше, поскольку в первом цикле полученное отношение
составляет 4.7×108 при 820°С). Мы полагали, что после предварительного восстановления δ может иметь значение примерно 0.5 или выше, поскольку в первом цикле полученное отношение 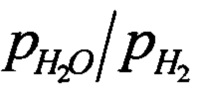 было примерно 0.01. На основании этого мы ожидали, что после предварительного восстановления изменение степени нестехиометричности, Δδ, будет выше +0.35. Баланс кислорода, достигнутый за этот период предварительного восстановления с использованием молярных концентраций выходящего диоксида углерода, введенного за время полуцикла, дал величину Δδ+0.09±0.002. Этот факт указывает на то, что не весь LSF участвует в редокс-процессах, некоторое количество материала кинетически исключено из проходящей реакции.
было примерно 0.01. На основании этого мы ожидали, что после предварительного восстановления изменение степени нестехиометричности, Δδ, будет выше +0.35. Баланс кислорода, достигнутый за этот период предварительного восстановления с использованием молярных концентраций выходящего диоксида углерода, введенного за время полуцикла, дал величину Δδ+0.09±0.002. Этот факт указывает на то, что не весь LSF участвует в редокс-процессах, некоторое количество материала кинетически исключено из проходящей реакции.
[00105] После восстановления LSF использовали в течение 100 циклов для осуществления многократных циклов методом реверсирования потока. Восстанавливающий (монооксид углерода) и окисляющий (вода) агенты подавали в виде дискретных полуциклов с продувкой гелием для разделения полуциклов (в промышленных масштабах продувку инертным газом не используют, но очень важно гарантировать, чтобы смешивание в газовой фазе было минимальным). Эксперименты проводили при 820°С. На протяжении всего эксперимента молярные концентрации (мольные доли) монооксида углерода и воды на входе составляли 5 мол. % в балансе гелия при скорости потока 3.7×10-5 моль/с (50 мл (STP)/мин). Давление на выходе из реактора было примерно 1 бар (0.01 кПа). Давление на входе было примерно 1.2 бар вследствие падения давления в неподвижном слое (давление не влияет на константу равновесия в реакции конверсии водяного газа). Вода доставляется с помощью сатураторной системы (Grant, 179 UK) с применением гелия (с чистотой 99.996%, ВОС, UK) в качестве носителя. Циклы проводили в виде полуциклов продолжительностью 60 секунд. Продувку гелием (чистота 99.996%, ВОС, UK) проводили в течение 120 секунд.
[00106] Переключение газовых потоков в цикле осуществляли с помощью трех- и четырехходовых клапанов, поддерживая постоянный ток всех газов, участвующих в реакции, как показано на Фигуре 2. Протокол переключения цикла начинали с Клапанов V1 и V2, расположенных с возможностью пропускать гелий в реактор со стороны подачи монооксида углерода, и Клапана V3, расположенного с возможностью пропускать гелий, уходящий из реактора к QMS. Через 60 с Клапан VI переключали на подачу монооксида углерода в течение 60 с, а затем поворачивали обратно для подачи гелия. Еще через 60 с подачу гелия к Клапану V1 прекращали; начинали подачу гелия к Клапану V4; а Клапаны V2 и V3 поворачивали одновременно для изменения направления потока гелия с целью его подачи со стороны входа воды. Через 60 с Клапан V4 поворачивали для доставки воды в реактор в течение 60 с, затем поворачивали обратно для подачи гелия еще с течение 60 с перед тем, как снова переключить направление потока гелия и повторить цикл. В результате осуществления этого протокола поочередно реализуются 60-секундные импульсы (полуциклы) подачи монооксида углерода и воды, разделенные подачей гелия в течение 120 с.
[00107] Эксперименты по распределению времени пребывания (показанные на Фигуре 8) проводили для каждого из газообразных реагентов и продуктов в концентрации 5 мол. % для того, чтобы подтвердить, что их полуциклы остаются дискретными в процессе работы. Следует отметить, что форма этих кривых, показывающих молярные концентрации на выходе относительно времени, аналогичны за исключением того, что кривая для воды, которая, по-видимому, реагирует более активно с носителем кислорода, имеет более 'округлую' форму для молярной концентрации на выходе.
[00108] После того, как циклы стали многократными, примерно, в ходе Цикла 90, изменение средней степени нестехиометричности, 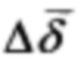 , между восстановительным и окислительным полуциклами стабилизировалось при значении ±0.003 (здесь мы имеем информацию только об изменении средней степени нестехиометричности,
, между восстановительным и окислительным полуциклами стабилизировалось при значении ±0.003 (здесь мы имеем информацию только об изменении средней степени нестехиометричности, 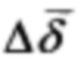 , поскольку степень нестехиометричности неподвижного слоя больше не является постоянной). Перед тем, как воспроизведение циклов стало повторяться, степень окисления LSF была выше степени восстановления в течение одного цикла, как можно было ожидать, если исходить из восстановленного материала (носителя кислорода). Осуществление кислородного баланса в ходе всех циклов приводит к изменению
, поскольку степень нестехиометричности неподвижного слоя больше не является постоянной). Перед тем, как воспроизведение циклов стало повторяться, степень окисления LSF была выше степени восстановления в течение одного цикла, как можно было ожидать, если исходить из восстановленного материала (носителя кислорода). Осуществление кислородного баланса в ходе всех циклов приводит к изменению 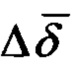 на величину -0.09±0.02, которая аналогична величине изменения δ на предварительно восстановленном носителе и указывает на то, что значительная часть неподвижного слоя имеет величину δ примерно 0.15 с восстановленным участком неподвижного слоя, предположительно, вблизи выхода воды.
на величину -0.09±0.02, которая аналогична величине изменения δ на предварительно восстановленном носителе и указывает на то, что значительная часть неподвижного слоя имеет величину δ примерно 0.15 с восстановленным участком неподвижного слоя, предположительно, вблизи выхода воды.
[00109] Частицы материала носителя кислорода, свежие, после предварительного восстановления и после предварительного восстановления с последующим проведением ста редокс-циклов, были охарактеризованы методами SEM-EDX и XRD. После проведения редокс-циклов неподвижный слой делили на пять участков примерно равной длины для того, чтобы посмотреть, имеются ли какие-либо различия микроструктуры, композиционных свойств или фазового состава в аксиальном направлении (вдоль оси). Никаких таких аксиальных изменений не наблюдали, и поэтому в данном описании мы приводим данные только для центрального отрезка материала носителя кислорода (в случае изображений SEMs и спектров XRDs). Площади поверхности BET определяли адсорбцией/десорбцией азота при 77 K на приборе Beckman Coulter SA3100. Площадь поверхности BET для LSF составляла примерно 0.1 м2/г. Для изучения микроструктуры свежих частиц носителя кислорода и влияния процесса (работы) на микроструктуру применяли сканирующую электронную микроскопию (SEM) (XL30 ESEM-FEG). Как можно видеть на Фигуре 9А, свежие частицы имели неправильную форму. При большем увеличении (Фигура 9В) наблюдали гладкую поверхность с некоторым явно неполным оплавлением поверхности. После предварительного восстановления и последующих 100 циклов никаких заметных изменений в образцах LSF не было замечено (Фигуры 9С, 9D, 9Е и 9F). Частицы сохраняли свою форму и размер, и не наблюдалось ни никакого значительного образования мелкодисперсного материала, ни потерь материала (носителя кислорода) из реактора. Дифракцию рентгеновских лучей (PAN analytical  Pro) изучали с целью определить кристаллические фазы в свежем материале носителя кислорода LSF (Фигура 10А); носитель кислорода LSF после предварительного восстановления с помощью 5 мол. % монооксида углерода в гелии в течение 4.32×104 с (12 часов) (Фигура 10В); и носитель кислорода LSF после предварительного восстановления с помощью 5 мол. % монооксида углерода в гелии в течение 4.32×104 с (12 часов) и последующих ста редокс-циклов с использованием 5 мол. % монооксида углерода в гелии и 5 мол. % воды в гелии с 820°С (Фигура 10С). Во всех случаях единственная имеющаяся кристаллическая фаза соответствовала перовскитной фазе. Не было отмечено никаких заметных изменений в материале при восстановлении и при проведении циклических реакций.
Pro) изучали с целью определить кристаллические фазы в свежем материале носителя кислорода LSF (Фигура 10А); носитель кислорода LSF после предварительного восстановления с помощью 5 мол. % монооксида углерода в гелии в течение 4.32×104 с (12 часов) (Фигура 10В); и носитель кислорода LSF после предварительного восстановления с помощью 5 мол. % монооксида углерода в гелии в течение 4.32×104 с (12 часов) и последующих ста редокс-циклов с использованием 5 мол. % монооксида углерода в гелии и 5 мол. % воды в гелии с 820°С (Фигура 10С). Во всех случаях единственная имеющаяся кристаллическая фаза соответствовала перовскитной фазе. Не было отмечено никаких заметных изменений в материале при восстановлении и при проведении циклических реакций.
ПРИМЕР 3: ДИФФЕРЕНЦИАЛЬНАЯ КИНЕТИКА
[00110] Дифференциальные кинетические измерения проводили в полностью автоматическом и программируемом микрореакторе (CATLAB, Hiden Analytical Ltd., UK) с соединенным с ним квадрупольным масс-спектрометром (QMS) с "мягкой ионизацией" (QMS) (QIC-20 Bench-top Gas Analysis unit, Hiden Analytical Ltd., UK) при давлении примерно 1 бар (0.01 кПа) и при немного более высокой температуре 850°С (Фигура 6). Реактор работал преимущественно дифференциально, то есть конверсия реагентов была низкой (менее 10% за исключением тех случаев, когда имели место высокие начальные скорости получения водорода). Температуру образца проверяли и регулировали с помощью внутренней термопары K-типа, помещенной в защитный чехол из инертного оксида алюминия. Сначала свежий образец (~50 мг) после обжига помещали в реактор, затем промывали струей гелия со скоростью потока 7.4×10-5 моль/с (100 мл (STP)/мин) перед началом испытаний. После этого носитель кислорода подвергали изотермическому восстановлению под действием 5 мол. % монооксида углерода в гелии и изотермическому окислению под действием 5 мол. % воды в гелии при скорости потока 7.4×10-5 моль/с (100 мл (STP)/мин). Стадии восстановления и окисления продолжались 1800 с (30 минут). Гелий продували в течение 300 с (5 минут) после восстановления и 900 с (15 минут) после окисления, чтобы освободить реактор от любого реакционноспособного газа или любого продукта и не допустить смешения восстановительного и окислительного газов.
[00111] На Фигуре 12 показаны молярные концентрации на выходе в процессе полного цикла восстановления и окисления LSF. Каждый полуцикл продолжался примерно 1800 с (30 минут), но полуцикл окисления с использованием 5 мол. % воды в гелии продолжался немного дольше 1800 с (30 минут), поскольку при переключении Клапана Valve V1 (Фигура 11), который регулирует доставку воды, наблюдалась задержка. Для полуцикла восстановления наблюдается острый пик на кривой молярной концентрации монооксида углерода на короткий период времени с величиной, намного превышающей 5 мол. % доставляемого монооксида углерода. Этот пик следует игнорировать, поскольку он является аномалией системы, вызываемой изменениями давления при открытии и закрытии регуляторов массового расхода для гелия, монооксида углерода, водорода и диоксида водорода. Когда в реактор доставляется вода, такой пик не наблюдается, поскольку вода течет непрерывно и при необходимости подается в реактор с помощью двухпозиционного четырехходового Клапана V1.
[00112] Начальная производительность по диоксиду углерода составляла ≈0.75 мкмоль/с, но она быстро снижалась до ≈0.1 мкмоль/с в первые 120 с (2 минуты) полуцикла восстановления. В течение остальных 1680 с (28 минут) скорость продуцирования диоксида углерода продолжала неизменно падать до конечного значения ≈0.05 мкмоль/с. С другой стороны начальная производительность по водороду составляла ≈2.5 мкмоль/с (имеется значительная неопределенность относительно этой скорости, поскольку микрореактор при таких высоких скоростях реакции не работает в дифференциальном режиме). Эта скорость сохранялась в течение примерно 100 с. После этой начальной высокой скорости продуцирования водорода скорость падает до не поддающегося измерению уровня. Ясно, что окисление водорода протекает намного легче, чем восстановление монооксида углерода
ПРИМЕР 4: ДРУГИЕ МАТЕРИАЛЫ
[00113] Описанную выше реакцию конверсии водяного газа повторяли с целым рядом нестехиометрических соединений. Результаты представлены в Таблице 1:
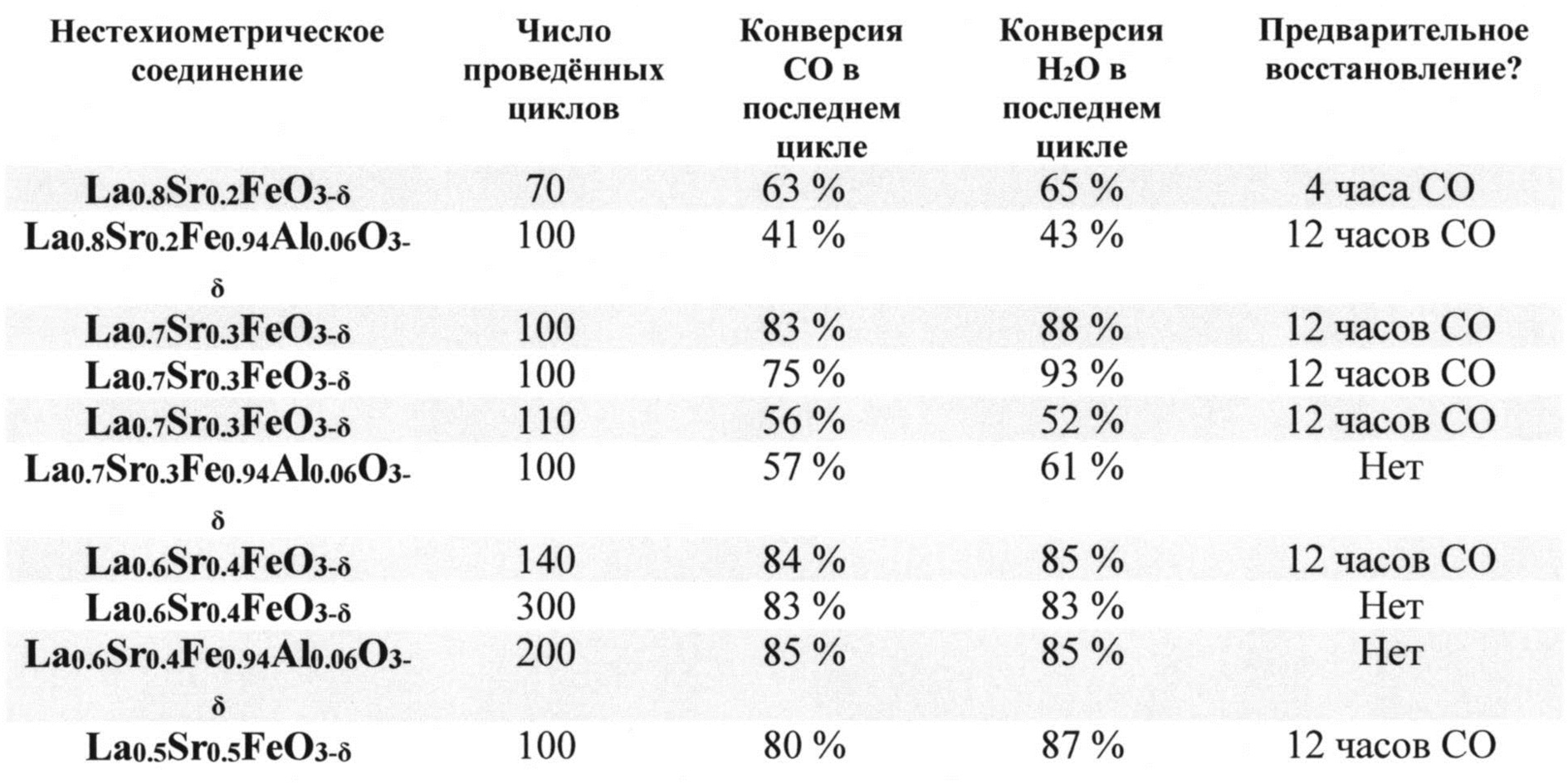
Для всех этих соединений, за исключением La0.8Sr0.2Fe0.94Al0.06O3-δ, наблюдается конверсия превышающая 50% как в СО, так и в Н2О циклах, т.е. K* выше единицы.
ПРИМЕР 5: ПАРОВОЙ РИФОРМИНГ МЕТАНА
[00114] Также проводили автотермический риформинг метана посредством химических циклов. Реакция метана с водой не имеет ограничений, накладываемых условиями равновесия, в общем смысле, но, тем не менее, до сих пор трудно добиться высокого отношения водорода к воде с помощью химических циклов из-за термодинамических свойств материала носителя кислорода. Носители различной степени нестехиометричности по своей природе являются значительно более гибкими применительно к процессам, в которых их можно применять для получения высокочистых раздельных потоков даже при отсутствии общих ограничений, накладываемых условиями равновесия.
[00115] После восстановления LSF использовали в 50 циклах в режиме реверсирования потока. Восстановительный (метан) и окислительный (вода и кислород) агенты подавали в виде дискретных циклов с продувкой гелием для разделения циклов. Порядок подачи: подача метана через устройство для впуска восстановителя с последующей подачей воды через устройство для впуска окислителя и, наконец, подача кислорода через устройство для впуска окислителя. Эксперименты проводили при 850°С. В продолжение всех экспериментов молярные концентрации метана, воды и кислорода на входе составляли 5 мол. % в балансе гелия (в балансе аргона в случае кислорода) при скорости потока 2.2×10-5 моль/с (30 мл (STP)/мин). Продолжительность циклов была 15 минут для подачи метана, 6 минут для подачи воды и 30 секунд для подачи кислорода. Применяли продувку гелием (чистота 99.996%, ВОС, UK) в течение 90 секунд. Общая конверсия достигала 35% для метана (давая смесь монооксида углерода, диоксида углерода, водорода и воды), 85% для воды и 100% для кислорода.