Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ БИОРЕЗОРБИРУЕМОЙ ТРУБКИ НА ОСНОВЕ МЕТАКРИЛИРОВАННОГО ЖЕЛАТИНА И МЕТАКРИЛИРОВАННОГО ФИБРОИНА И СПОСОБ ВОССТАНОВЛЕНИЯ СТЕНКИ ТОНКОЙ КИШКИ В ЭКСПЕРИМЕНТЕ С ПОМОЩЬЮ ТАКОЙ ТРУБКИ
Вид РИД
Изобретение
Область техники
Изобретение относится к биотехнологии и медицине. Более подробно изобретение относится к области хирургии, регенеративной медицине и тканевой инженерии, а именно к способам восстановления стенок полых органов желудочно-кишечного тракта, включающих применение биорезорбируемых имплантатов для закрытия области дефекта, обеспечивающих полное структурное и функциональное восстановление стенки кишки.
Уровень техники
Синдром короткого кишечника (СКК) развивается в результате обширной резекции тонкой кишки [doi: 10.1016/j.cgh.2005.10.002]. Такая процедура может потребоваться при воспалительных заболеваниях (болезнь Крона), завороте кишок, травмах и врожденных патологиях. В педиатрической практике причиной может служить гастрошизис или некротический энтероколит новорожденных [doi: 10.1053/j.gastro.2005.12.002]. При СКК площадь всасывающей питательные вещества поверхности слишком мала, чтобы обеспечить организм требуемым количеством энергии. В конечном итоге развивается обезвоживание, диарея и хроническое недоедание. Традиционная терапия предусматривает перевод больного на парентеральное питание, способное значительно улучшить его состояние, однако подобное решение зачастую приводит к развитию многочисленных осложнений [doi: 10.1016/S0016-5085(99)70388-4].
Для лечения СКК применяются и хирургические методы двух основных категорий. Первая, не предусматривающая трансплантации, направлена на улучшение абсорбции воды и питательных веществ путем либо замедления прохождения пищи по кишечнику, например, установка клапанов, фрагментальная инверсия [doi: 10.1007/BF02385811], увеличение площади всасывания (например, удлинение кишки продольным механическим натяжением [doi: 10.1136/gut.2004.061481], последовательная поперечная энтеропластика [doi: 10.1016/j.jpedsurg.2005.03.020]). Другая категория - пересадка кишечника от донора - показала себя очень эффективной при строгом соблюдении правил ухода и применении иммуносупрессии [doi: 10.1056/NEJMra0804605]. Однако имеются сложности с подбором донора, проблема отторжения трансплантата, осложнения на фоне лекарственное терапии, риск заражения вирусными инфекциями и прочее [doi: 10.5500/wjt.v6.i1.1].
Современным перспективным подходом является применение тканеинженерных конструкций, имеющих, как и кишка, форму трубки. Классическим материалом для таких трансплантатов является децеллюляризованный внеклеточный матрикс. Являясь продуктом секреции клеток, он состоит из структурных и функциональных соединений, а потому играет не просто роль каркаса, но биоактивной субстанции, влияющей на многие тканеассоциированные процессы в организме [doi: 10.1016/В978-0-12-800548-4.00002-4]. Скаффолды на основе внеклеточного матрикса показали себя крайне эффективными в экспериментах in situ, причем ткани кишки полностью восстанавливали свою структуру без каких-либо серьезных нарушений [doi: 10.1038/nrm3902].
Из уровня техники известен патент на изобретение US 6312474 В1 «Resorbable implant materials» («Рассасывающиеся материалы для имплантатов»). В документе раскрыто использование в качестве имплантируемого биорезорбируемого материала децеллюляризованной и очищенной ткани млекопитающих (например, бычий перикард). Материал обрабатывают путем алкилирования его первичных аминогрупп таким образом, чтобы снизить антигенность ткани, позволяя использовать обработанную ткань in vivo и без ковалентного перешивания, что обеспечивает возможность биорезорбции такого материала. Материал может быть использован в хирургии при восстановлении дефектов мягких тканей в течение определенного периода времени, в то время как сам имплантат постепенно ремоделируется и биорезорбируется. Также предоставлен способ подготовки такого материала и способ использования такого материала для восстановления дефектов тканей.
Также из уровня техники известен документ US 20030225355 A1 «Composite material for wound repair» («Композитный материал для заживления ран»), в котором раскрыт композитный материал, содержащий барьерный материал и материал подложки, используемый для заживления ран или тканей. Преимущества включают снижение адгезии к органам или другим структурам, прилегающим к месту дефекта, снижение отечности тканей, усиление васкуляризации и клеточной инфильтрации, уменьшение воспаления и уменьшение образования рубцовой ткани.
Наиболее близкое решение по отношению к заявляемому способу, известное из уровня техники, раскрыто в патентном документе US 20060173471 A1 «Tissue Repair Fabric» («Материал для восстановления тканей») раскрыт протез, содержащий два или более наложенных связанных слоев коллагеновой ткани, которые сшиты перешивающим агентом, где указанная коллагеновая ткань выделена из подслизистой оболочки тонкой кишки, где два или более слоев коллагеновой ткани полностью биорезорбируемы, и при имплантации пациенту-млекопитающему полностью биодеградируют, замещаясь тканью пациента. При этом протез не является антигенным, стерилен и предназначен для восстановления, увеличения или замены больных, или поврежденных органов, выбранных из группы, состоящей из брюшной стенки, перикарда, грыж, костей, надкостницы, перихондрия, межпозвонкового диска, суставного хряща, дермы, эпидермиса, кишечника, связок и сухожилий.
Недостатками указанных выше изобретений являются использование материалов животного происхождения, что может привести к дополнительному инфицированию, в том числе такими опасными возбудителями, как вирусы гепатита и ВИЧ, а также другими осложнениям. Кроме того, забор у пациента донорского материала предполагает дополнительное травмирование пациента, дополнительный риск инфицирования, повреждение нервов, большую потерю крови и, как следствие, необходимость переливания крови, сопровождающуюся дополнительными рисками для пациента. Также существуют ограничения в максимальном объеме тканей, который можно взять у пациента. Иной подход базируется на использовании в качестве материала биорезорбируемых искусственных и натуральных полимеров. Последние имеют особое преимущество, поскольку родственны организму, многие из них обладают биоактивностью, способствующей более быстрому восстановлению нативной структуры поврежденных тканей и органов, а при их естественной деградации образуются нетоксичные соединения, которые могут стать питательным субстратом для клеток.
Раскрытие изобретения
Предлагается использование биодеградируемого имплантата на основе метакрилированного желатина и метакрилированного фиброина шелка как перспективный метод восстановления полых органов ЖКТ. Биодеградиремый имплантат представляет собой трубку, соответствующую по диаметру кишечнику, с армированными краями для обеспечения состоятельности швов, выполненную фотополимеризацией смеси метакрилированного желатина и метакрилированного фиброина и обладающую такими свойствами как: программируемая скорость деградация, низкая иммуногенность, легкость модификации, особенность строения позволяет витализировать данный имплантат.
Предлагается новый подход к решению проблемы восстановления повреждений полых органов ЖКТ, в том числе обширных, а также увеличения длины кишечной трубки, где имплантат не только обеспечивает герметичность закрытия дефекта, но и стимулирует процессы регенерации, являясь субстратом для адгезии, пролиферации и миграции тканеспецифичных и прогенеторных клеток. В экспериментальных исследованиях на крысах показана полная регенерация стенки кишки с сохранением архитектоники и функции органа.
Задачей группы изобретений является разработка способа применения имплантатов на основе фиброина восстановления стенок полых органов ЖКТ
Техническим результатом, достигаемым при использовании заявляемой группы изобретений, является обеспечение возможности снижения послеоперационных осложнений до полного их отсутствия и полного восстановлении циркулярного дефекта стенки тонкой кишки. При этом эффект обеспечивается за счет коррекции циркулярного дефекта кишки трубчатым биодеградируемым имплантатом, выполненным из метакрилированных производных фиброина шелка и желатина, представляющим собой трубку с армированными хирургическими шелковыми нитями краями. Армирование краев трубки препятствует прорезыванию имплантата при пришивании и обеспечивает тем самым герметичность кишечника. При этом имплантат обеспечивает герметичность кишечника в течение всего периода заживления дефекта и является основой для формирования грануляционной ткани и привлечения тканеспецифичных и прогенеторных клеток в область дефекта, обеспечивая полное восстановление стенки тонкой кишки, включая все структурные и функциональные элемента. Кроме того, имплантат обеспечивает быстрое восстановление обширных дефектов стенки тонкой кишки в эксперименте на крысах линии Wistar. Так, в модели циркулярного дефекта стенки тонкой кишки с расстоянием между отводящим и приводящим отделом кишечника 3 мм, уже через 1 месяц после имплантации биорезорбируемой трубки в область дефекта наблюдается полное восстановление всех структурных и функциональных слоев стенки кишки. А в модели циркулярного дефекта стенки тонкой кишки с расстоянием между отводящим и приводящим отделом кишечника 10 мм при имплантации биорезорбируемой трубки в область дефекта также наблюдается полное восстановление всех структурных и функциональных слоев стенки кишки через 6 месяцев.
Заявляемый способ характеризуется простотой, низкой стоимостью, отсутствием необходимости дополнительных расходных материалов и специальных навыков, что позволит быстро и широко внедрить его в клиническую практику.
Поставленная задача решается тем, что способ повышения состоятельности кишечного анастомоза, согласно техническому решению, включает 2 стадии:
1. Получение биорезорбируемой трубки на основе метакрилированного желатина и метакрилированного фиброина, обладающей следующими параметрами: толщина стенки трубки: от 150 мкм до 700 мкм, длина армированных участков 2-15 мм, длина неармированного участка: 3-150 мм, количество армированных участков: 2, расположение армированных участков: по краям трубки на расстоянии 1-6 мм от края, внутренний диаметр: от 2 мм до 15 см. Получение заявленной биорезорбируемой трубки включает несколько этапов:
а) растворение в гексафторизопропаноле макромономеров: метакрилированного желатина (ЖМА) из расчета 10 масс. % и метакрилированного фиброина (ФМА) из расчета 4 масс. % при 55°С±5 в течение 18-36 часов, преимущественно растворение ЖМА и ФМА проводят в течение 24 часов при 50°С;
б) получение смеси макромономеров, включающей равные части растворов ЖМА и ФМА, и фотоинициатор дифенил(2,4,6-триметилбензоил)фосфин оксид из расчета 5 масс. % от массы макромономеров;
в) подготовка направляющей для формирования трубки - стеклянной палочки с круглым сечением диаметром 2-15 см, преимущественно 4 мм. Поверхность стеклянной палочки обезжиривают, преимущественно 70%-ым этанолом и высушивают. На 10-30 секунд погружают стеклянную палочку в раствор вакуумной смазки в хлороформе (5 мг/мл) и высушивают 30-60 минут.
г) подготовка армировочной нити посредством выдерживания шелковой некрученой нити 8/0-4/0 в смеси, полученной на шаге б);
д) формирование первых слоев биорезорбируемой трубки на направляющей. Направляющую, подготовленную на этапе в), погружают в смесь макромономеров с фотоинициатором, полученную на этапе б), на 5-10 секунд, извлекают и вращая со скоростью 10-20 об./мин. экспонируют в свете УФ-лампы (мощность 36 Вт) не менее 2 минут. Процедуру повторяют 4-6 раз в зависимости от желаемого количества слоев. Направляющую вращают со скоростью 10-20 об./мин. Преимущественно направляющую выдерживают в смеси макромономеров в течение 7 секунд, экспонируют в свете ультрафиолетовой лампы мощностью 36 Вт в течение 2 мин, вращая направляющую со скоростью 15 об./мин.;
е) армирование нитью концевых участков трубки посредством укладывания нити витками на расстоянии 2-5 мм от концов формируемой трубки на заготовку, полученную на шаге д) из расчета 10-15 витков на 3 мм. Количество витков определяют исходя из требований к длине армированного участка и расстоянию между армированными участками. Преимущественно армирование нитью концевых участков трубки проводят посредством равномерного укладывания по 10 витков нити на концевые участки трубки длиной 2,5 мм, отступив от одного края 2 мм и 7,5 мм;
ж) формирование наружных слоев биорезорбируемой трубки посредством погружения полученной на шаге е) заготовки в смесь, полученную на шаге б), на 5-10 секунд, с последующим вращением и экспонированием полученной трубки в свете ультрафиолетовой лампы не менее 2 минут. Процедуру повторяют 4-20 раз в зависимости от желаемого количества слоев. Направляющую вращают со скоростью 10-20 об./мин;
з) обработка сформированной трубки выдерживанием в дистиллированной воде в течение 1-1.5 часа, с последующим выдерживанием в 96%-ом этаноле в течение 12-18 часов и повторным выдерживанием в дистиллированной воде в течение 1-1.5 часа, обработкой внутренней поверхности сформированной трубки хлороформом. Преимущественно сформированную трубку выдерживают в дистиллированной воде в течение 1 часа, затем 12 часов выдерживают в 96%-ом этаноле и еще 1 час в дистиллированной воде
2. Восстановление стенки тонкой кишки, включающее следующие шаги:
а) подготовка биорезорбируемой трубки для закрытия анастомоза посредством ее инкубации в стерильном физиологическом растворе в течение 15-30 минут с многократной заменой физиологического раствора. При этом биорезорбируемая трубка преимущественно имеет следующие параметры: внутренний диаметр - 4 мм, длина неармированного участка - 3 мм, длина армированных участков - 2,5 мм, толщина стенки - 300 мкм;
б) предоперационная подготовка экспериментальных животных посредством питания 10% раствором глюкозы без ограничения в течение 2 суток;
в) закрытие анастомоза трубкой. Для чего животных наркотизируют, преимущественно смесью Золетил+Ксилазин, фиксируют в положении на спине, внутримышечно вводят цефтриаксон из расчета 100 мг/кг массы тела и атропина сульфат в дозе 0.04 мг/кг, подкожно за 15 мин до начала хирургического вмешательства. Операционное поле ограничивают стерильными марлевыми салфетками, выполняют лапаротомию, в операционную рану выводят участок тонкой кишки, формируют операционную рану, в которую выводят участок тонкой кишки, после чего с противобрыжеечного края кишки выполняют разрез на половину диаметра кишечной трубки, вводят в просвет кишечника биорезорбируемую трубку и фиксируют с помощью хирургической нити, после чего в месте имплантации удаляют участок кишечной трубки длиной 3-10 мм, преимущественно 3 или 10 мм, и проводят послойное ушивание полости с помещением кишки брюшную полость;
г) послеоперационный уход посредством ежедневных инъекций цефтриаксона из расчета 50 мг/кг массы тела в течение 4-х суток.
В заявляемом изобретении может быть использован фиброин шелка каркасной нити пауков, фиброин шелка тутового шелкопряда и других видов шелкопрядов, фиброин рекомбинантного шелка, а также искусственные аналоги шелка.
В качестве фотоинициатора был выбран дифенил(2,4,6-триметилбензоил)фосфин оксид (97%), являющийся высокореактивным, нерастворимым в воде соединением, применяемым для быстрого фотоотверждения, например, для лазерной стереолитографии. Биорезорбируемой трубки, полученные в соответствии с заявляемым изобретением могут применяться для восстановления дефектов полых органов ЖКТ.
Краткое описание чертежей
Изобретение поясняется чертежами.
На фиг. 1 представлена биорезорбируемая трубка, полученная заявляемым способом.
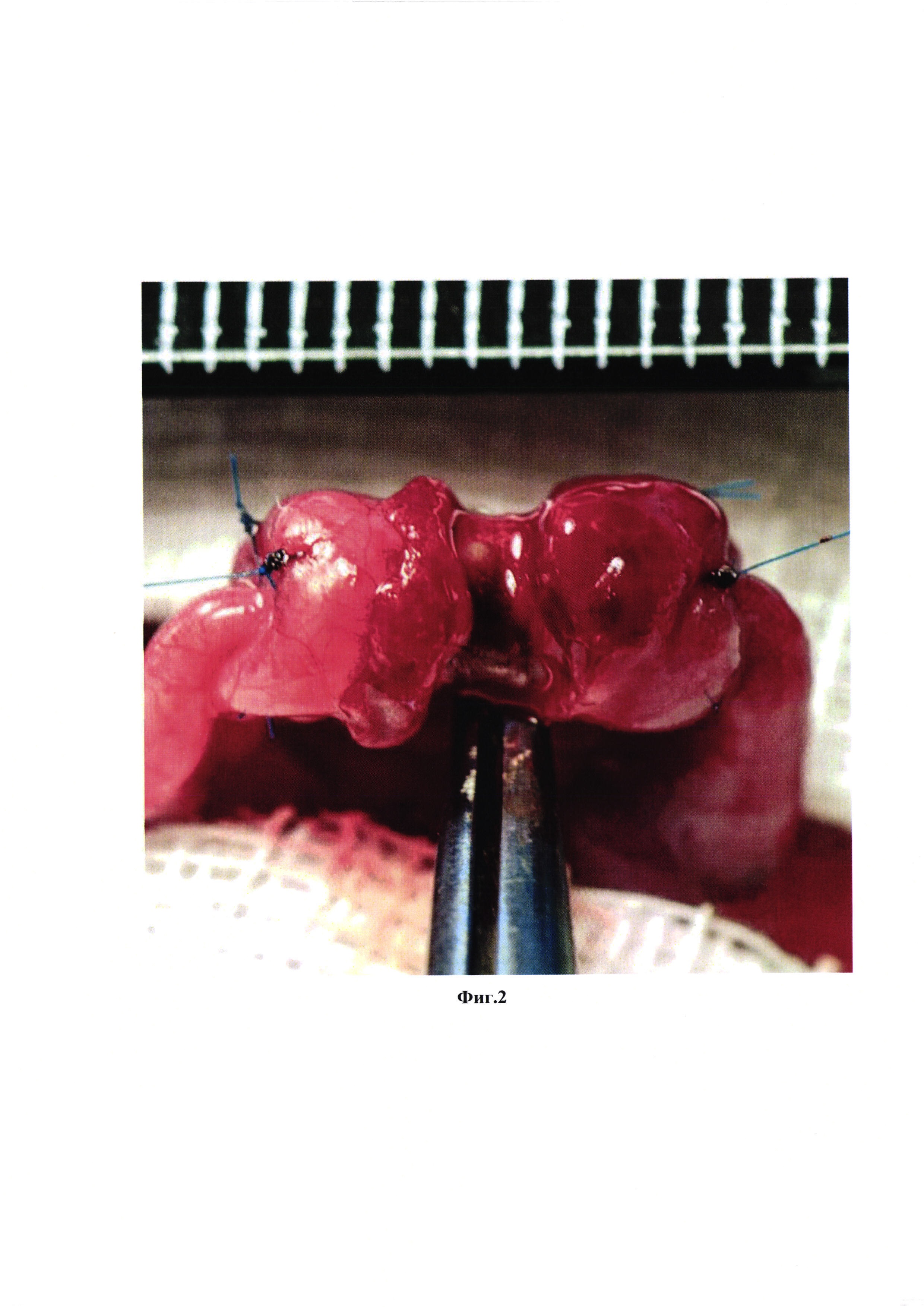
На фиг. 2 представлено изображение имплантированной биодеградируемой трубки на место циркулярного дефекта тонкой кишки с диастазом 3 мм.
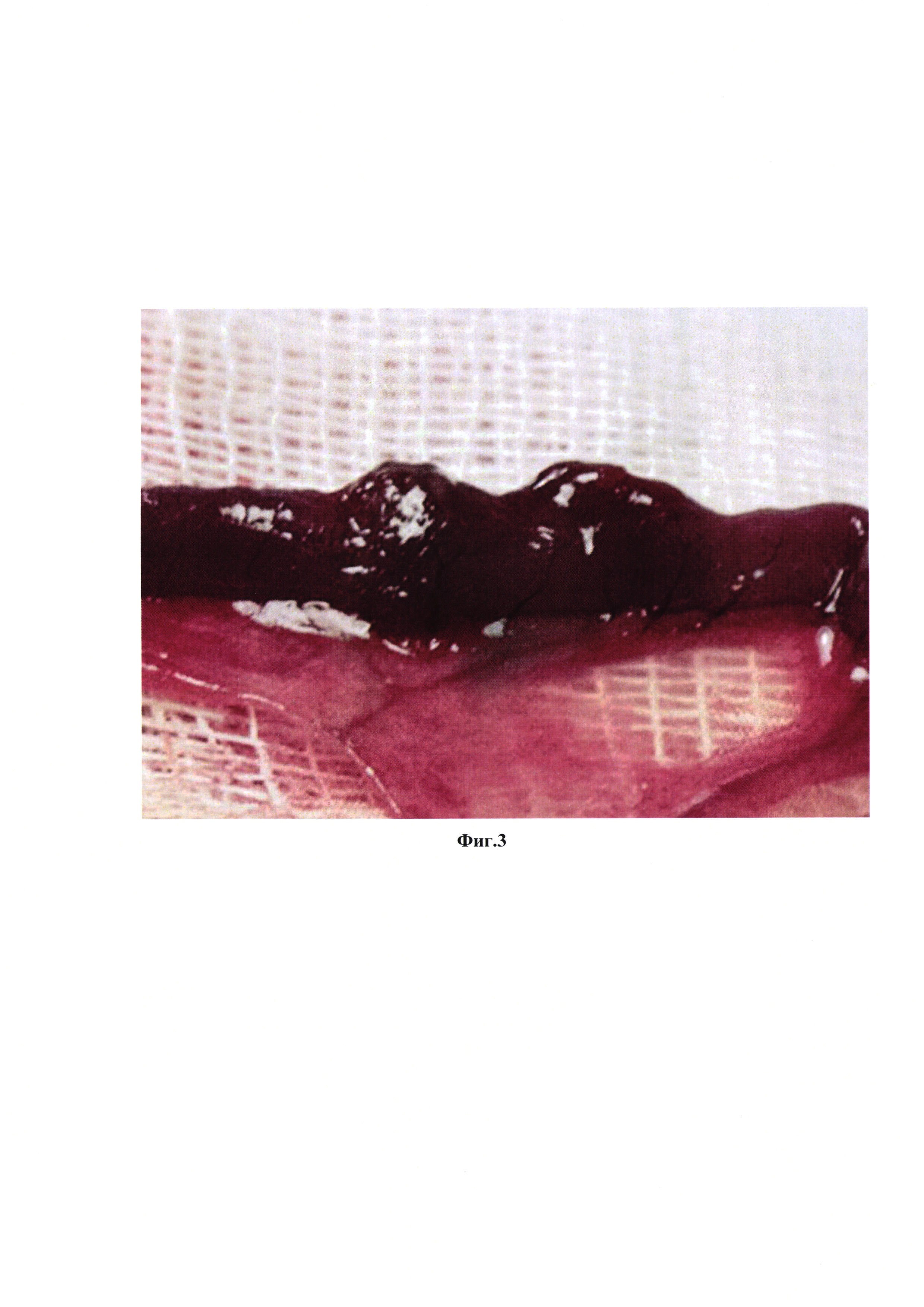
На фиг. 3 представлено состояние кишечника через 1 месяц после имплантации биодеградируемой трубки на место циркулярного дефекта тонкой кишки с диастазом 3 мм.
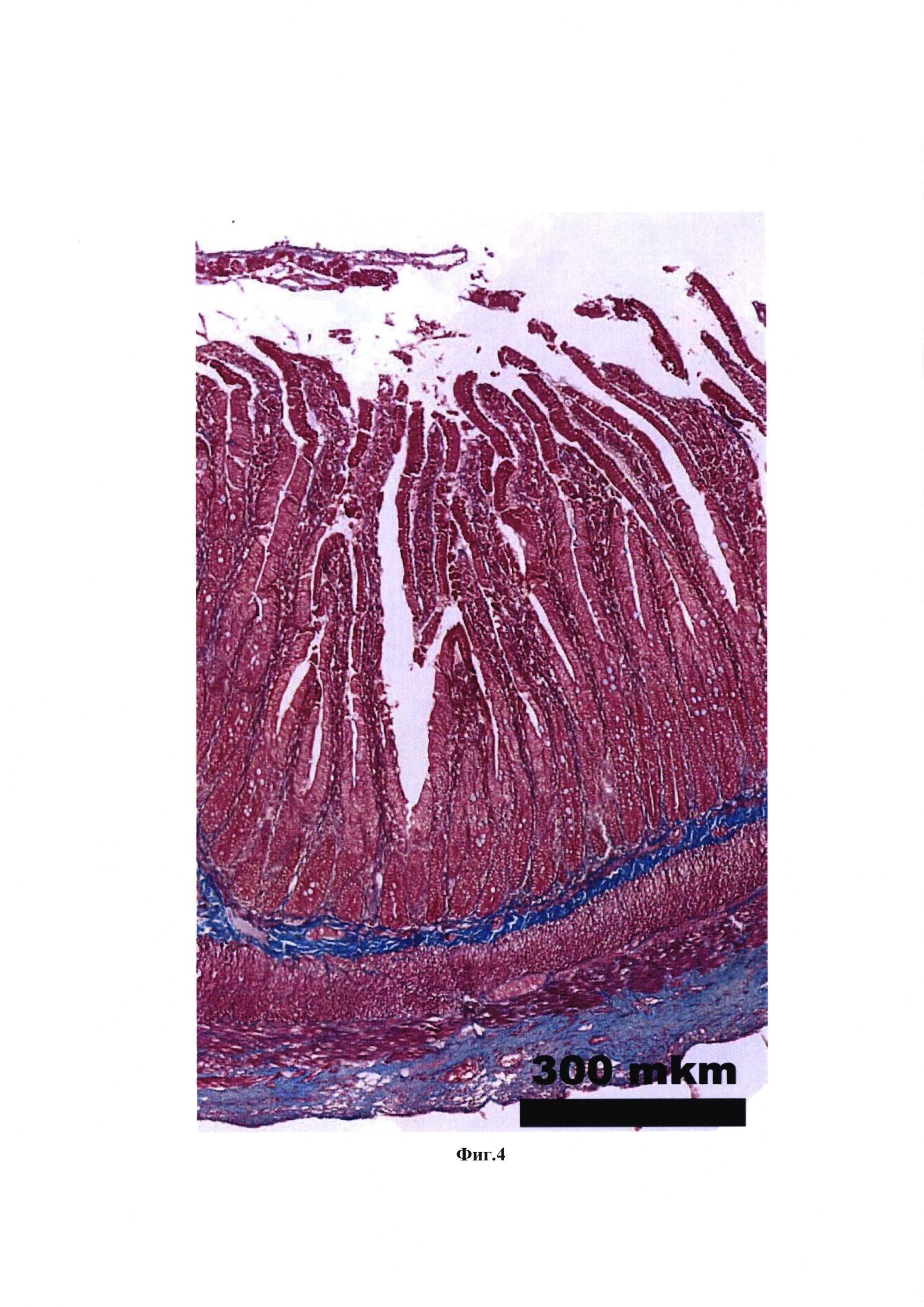
На фиг. 4 представлен гистологический анализ тканей, сформированных через 1 месяц на месте циркулярного дефекта тонкой кишки, закрытого биодеградируемой трубкой с диастазом 3 мм. Окраска по Маллори.
На фиг. 5 представлено изображение имплантированной биодеградируемой трубки на место циркулярного дефекта тонкой кишки с диастазом 10 мм.
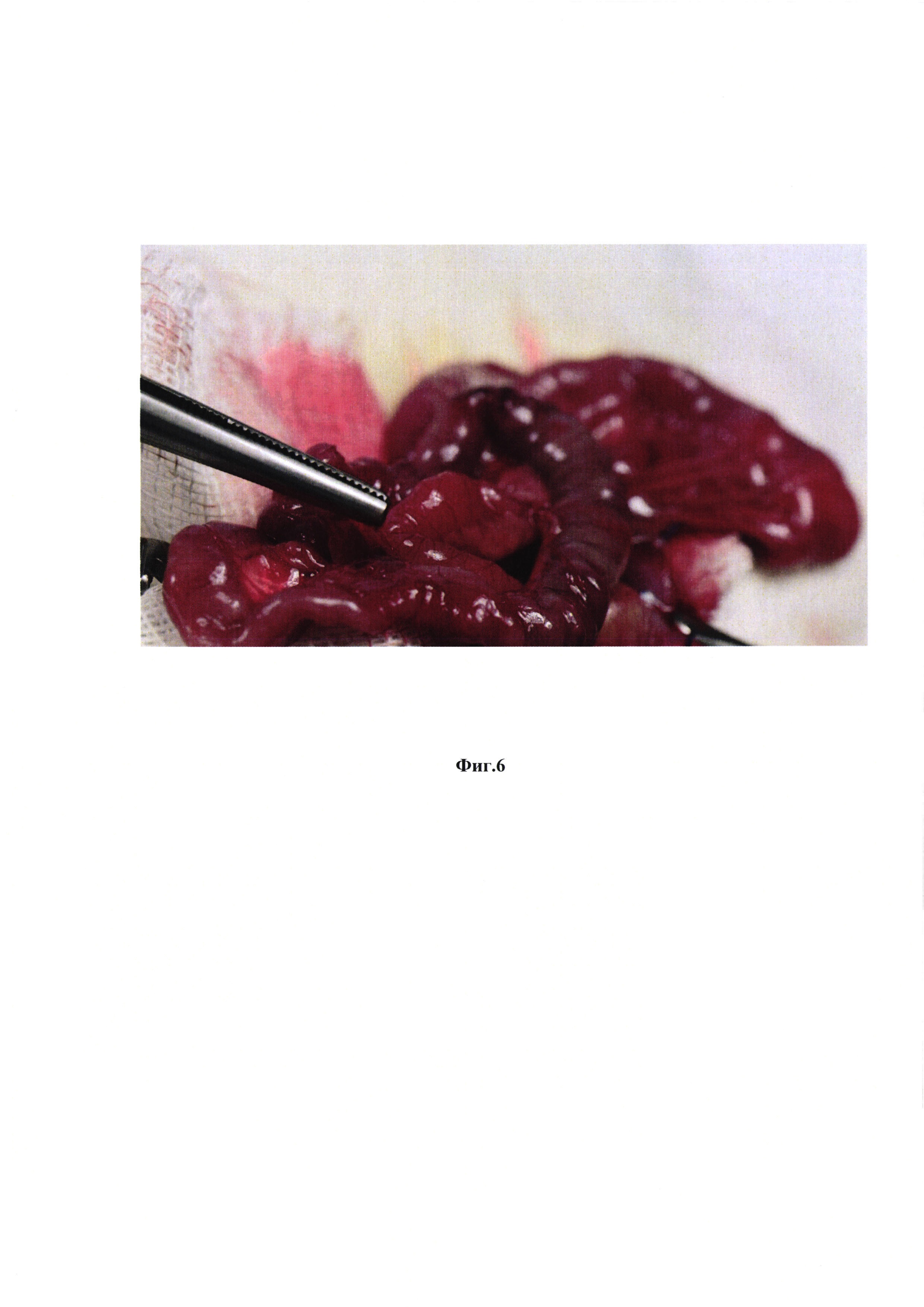
На фиг. 6 представлено состояние кишечника через 6 месяцев после имплантации биодеградируемой трубки на место циркулярного дефекта тонкой кишки с диастазом 10 мм.
На фиг. 7 представлен гистологический анализ тканей, сформированных через 6 месяцев на месте циркулярного дефекта тонкой кишки, закрытого биодеградируемой трубкой с диастазом 10 мм. Окраска гематоксилин-эозин.
Осуществление изобретения
Навеску метакрилированного желатина (ЖМА) растворяют в гексафторизопропаноле на водяной бане при 55°С±5 в течение 18-36 часов из расчета 10 масс. %. Навеску метакрилированного фиброина (ФМА) растворяют в гексафторизопропаноле на водяной бане при 55°С±5 в течение 18-36 часов из расчета 4 масс. %. Полученные растворы ЖМА и ФМА смешивают в равных объемных соотношениях и вносят фотоинициатор дифенил(2,4,6-триметилбензоил)фосфин оксид (ТРО) в количестве 5% от массы макромономеров: ЖМА и ФМА. Формирование трубки диаметром 2-15 мм и длиной 4-36 мм выполняют на предварительно обработанной стеклянной палочке с круглым сечением соответствующей длины и диаметра. Обработка стеклянной палочки включает обезжиривание 70% этанолом, высушивание и обработку вакуумной смазкой, растворенной в хлороформе (5 мг/мл). Для этого палочку погружают в раствор вакуумной смазки в хлороформе на 10-30 секунд и затем высушивают на воздухе при комнатной температуре 30-60 минут. Далее формируют на направляющей - обработанной соответствующей стеклянной полочке, первые 4-6 слоев. Для этого погружают ее в смесь ЖМА/ФМА/ТРО на 5-10 секунд, извлекают и проводят фотополимеризацию нанесенного на направляющую слоя смеси ЖМА/ФМА/ТРО посредством экспонирования в свете УФ-лампы (мощность 36 Вт) не менее 2 минут. Направляющую при этом вращают со скоростью 10-20 об. мин. В зависимости от требуемого количества слоев процедуру повторяют 4-6 раз. Затем осуществляют армирование концевых участков формируемой трубки нанесением витков некрученой шелковой нити, предварительно обработанной в смеси ЖМА/ФМА/ТРО не менее 2 минут, из расчета 10 -15 витков на 3 мм на расстоянии 2-5 мм от края. При этом количество витков и расстояние между ними определяется требуемыми параметрами получаемой трубки: длина армированного участка и длина неармированного участка. Далее формируют наружные слои трубки. Количество наружных слоев определяют исходя из требуемой толщины стенки трубки, считая, что каждый слой составляет 30 мкм. Заготовку помещают в смесь ЖМА/ФМА/ТРО на 5-10 секунд, извлекают и вращая со скоростью 10-20 обУмин. экспонируют в свете УФ-лампы (мощность 36 Вт) не менее 2 минут. Сформированную трубку на оправке переносят в дистиллированную воду на 1-1.5 часа, затем 12-18 часов выдерживают в 96%-ом этаноле и еще 1-1.5 часа в дистиллированной воде. Полученную трубку снимают с направляющей, обрабатывают внутреннюю поверхность хлороформом и переносят в 96%-ый этанол для хранения.
Полученную биорезорбируемую трубку используют для закрытия циркулярного дефекта тонкой кишки крысы. Для крыс линии Wistar массой 190-230 г используют трубку со следующими параметрами: диаметр - 4 мм, длина неармированного участка - 3-10 мм, длина армированных участков - 2,5 мм, толщина стенки - 280-320 мкм. Перед операцией трубку отмывают от этанола. Для этого переносят трубку из 96%-ого этанола в стерильный физиологический раствор, инкубируют при 37°С 15-30 минут, заменяют физиологический раствор на свежий и выдерживают трубку в нем еще 30 минут. Процедуру повторяют 3 раза. Животных начинают готовить к операции за 2 суток до хирургического вмешательства. За 2 суток до операции животных лишают твердой пищи и дают им 10% раствор глюкозы без ограничения (per os). Операция проводят под общей анестезией (Золетил+Ксилазин), премедикация - атропина сульфат в дозе 0.04 мг/кг, подкожно за 15 мин до начала хирургического вмешательства. Животных фиксируют в положении на спине. В начале операции внутримышечно вводят цефтриаксон из расчета 100 мг/кг массы тела. Операционное поле ограничивают стерильными марлевыми салфетками, выполняют лапаротомию. В операционную рану выводят участок тонкой кишки (7 см дистальнее желудка), после чего с противобрыжеечного края кишки выполняют разрез на половину диаметра кишечной трубки, вводят в просвет кишечника стерильную трубку и узловыми швами герметично фиксируют имплантат с помощью хирургической нити (полиэстер, 4/0). После чего в месте имплантации удаляют участок кишечной трубки длиной 3-10 мм. Кишку помещают в брюшную полость и проводят послойное ушивание полости. В течение 4-х суток после операции выполняют ежедневные инъекции цефтриаксона из расчета 50 мг/кг массы тела. В течение 2-х суток животные получают 10-% раствор глюкозы, твердую пищу не получают, на третьи сутки их переводят на стандартную диету.
Таким образом применение заявленной биорезорбируемрй трубки обеспечивает полное восстановлении циркулярного дефекта стенки тонкой кишки и снижает вероятность послеоперационных осложнений до полного их отсутствия. При этом армирование краев трубки препятствует прорезыванию имплантата при пришивании и обеспечивает тем самым герметичность кишечника в течение всего периода заживления дефекта и является основой для формирования грануляционной ткани и привлечения тканеспецифичных и прогенеторных клеток в область дефекта, обеспечивая полное восстановление стенки тонкой кишки, включая все структурные и функциональные элемента. Кроме того, применение заявленной биорезорбируемой трубки в качестве имплантат позволяет быстро восстановить обширные дефекты стенки тонкой кишки в эксперименте на крысах линии Wistar. Ниже приведены примеры конкретного выполнения. Специалисту в данной области техники понятно, что данные примеры не являются ограничивающими изобретение, а лишь показывают возможность его реализации.
Пример 1.
Получение трубки. Навеску лиофилизированного метакрилированного желатина (ЖМА) помещают в 1,5 мл гексафторизопропанола (ГФИП) из расчета 4 масс. % и помещают в закрытой посуде на водяную баню. Инкубируют смесь ЖМА с ГФИП до полного растворения в течение 24 часов при 50°С. Навеску лиофилизированного метакрилированного фиброина (ФМА) помещают в 1,5 мл ГФИП из расчета 10 масс. % и помещают в закрытой посуде на водяную баню. Инкубируют смесь ЖМА с ГФИП до полного растворения в течение 24 часов при 50°С. Смешивают растворы макромономеров: 1,5 мл ЖМА и 1,5 мл ФМА и добавляют к ним фотоинициатор дифенил(2,4,6-триметилбензоил)фосфин оксид (ТРО) в количестве 5% от массы макромономеров. Поверхность стеклянной палочки диаметром 4 мм обезжиривают 70%-ым этиловым спиртом. Далее готовят смазку для оправки - стеклянной палочки диаметром 4 мм: в 1 мл хлороформа вносят 5 мг вакуумной смазки и растворяют на водяной бане при 50°С. Сухую стеклянную палочку диаметром 4 мм, обезжиренную спиртом, погружают в смазку на 20 секунд и затем высушивают на воздухе при комнатной температуре 30 минут. Обработанную смазкой стеклянную палочку используют в качестве направляющей для формирования трубки. Направляющую погружают в смесь ЖМА/ФМА/ТРО на 7 секунд, извлекают из раствора и облучают в свете УФ-лампы (мощность 36 Вт) в течение 2 мин, вращая направляющую со скоростью 15 об./мин. Повторяют процедуру погружения-экспонирования 4 раза. Для армирования концевых участков трубки используют хирургическую некрученую шелковую нить, смоченную в растворе ЖМА/ФМА/ТРО. Равномерно укладывают по 10 витков нити на концевые участки трубки длиной 2,5 мм, отступив от одного края 2 мм и 10,5 мм. Таким образом получают заготовку со следующими параметрами: длина армированных участков - 2,5 мм, длина неармированного участка - 6 мм. Вновь погружают заготовку в раствор ЖМА/ФМА/ТРО на 5 секунд, извлекают и вращая со скоростью 15 об./мин. экспонируют в свете УФ-лампы (мощность 36 Вт) 2 минуты. Повторяют процедуру еще 4 раза. Сформированную трубку на оправке переносят в дистиллированную воду на 1 час, затем 12 часов выдерживают в 96%-ом этаноле и еще 1 час в дистиллированной воде. Полученную трубку снимают с направляющей, обрабатывают внутреннюю поверхность хлороформом для удаления остатков смазки и переносят в 96%-ый этанол для хранения. Сформированная таким образом трубка представлена на фиг. 1.
Пример 2.
Восстановление дефекта стенки тонкой кишки крысы биодеградируемой трубкой (диастаз 3 мм).
Биорезорбируемую трубку со следующими параметрами: диаметр - 4 мм, длина неармированного участка - 3 мм, длина армированных участков - 2,5 мм, толщина стенки - 300 мкм, отмывают от этанола: переносят трубку из 96%-ого этанола в стерильный физиологический раствор, инкубируют при 37°С 20 минут, заменяют физиологический раствор на свежий и выдерживают трубку в нем еще 30 минут. Процедуру повторяют 3 раза. Крыс линии Wistar массой 190-230 г начинают готовить к операции за 2 суток до хирургического вмешательства. За 2 суток до операции животных лишают твердой пищи и дают им 10% раствор глюкозы без ограничения (per os). Операцию проводят под общей анестезией (Золетил+Ксилазин), премедикация -атропина сульфат в дозе 0.04 мг/кг, подкожно за 15 мин до начала хирургического вмешательства. Животных фиксируют в положении на спине. В начале операции внутримышечно вводят цефтриаксон из расчета 100 мг/кг массы тела. Операционное поле ограничивают стерильными марлевыми салфетками, выполняют лапаротомию. В операционную рану выводят участок тонкой кишки (7 см дистальнее желудка), после чего с противобрыжеечного края кишки выполняют разрез на половину диаметра кишечной трубки, вводят в просвет кишечника стерильную трубку и узловыми швами герметично фиксируют имплантат с помощью хирургической нити (полиэстер, 4/0). После чего в месте имплантации удаляют участок кишечной трубки длиной 3 мм. Кишку помещают в брюшную полость и проводят послойное ушивание полости. В течение 4-х суток после операции выполняют ежедневные инъекции цефтриаксона из расчета 50 мг/кг массы тела. В течение 2-х суток животные получают 10-% раствор глюкозы, твердую пищу не получают, на третьи сутки их переводят на стандартную диету. Закрытый биодеградируемой трубкой циркулярный дефект тонкой кишки крысы с диастазом 3 мм представлен на фиг. 2. Через 1 месяц после имплантации животных выводили из эксперимента. Состояние кишечника в области операции через 1 месяц представлено на фиг. 3. Выраженного спаечного процесса и других патологий не наблюдалось. Далее проводили гистологический анализ тканей, сформированных на месте трубки через 1 месяц (фиг. 4). Через 1 месяц после операции на месте дефекта наблюдалась полностью восстановленная стенка тонкой кишки, включая все характерные анатомические слои: слизистую, подслизистую, мышечную (слои продольных и циркулярных мышц) и серозную оболочки. Таким образом применение биорезорбируемых трубок, описанных в настоящем изобретении, обеспечивает полное восстановление циркулярного дефекта тонкой кишки крысы с диастазом 3 мм через 1 месяц.
Пример 3.
Восстановление дефекта стенки тонкой кишки крысы биодеградируемой трубкой (диастаз 10 мм).
Биорезорбируемую трубку со следующими параметрами: диаметр - 4 мм, длина неармированного участка - 10 мм, длина армированных участков - 2,5 мм, толщина стенки - 300 мкм, отмывают от этанола: переносят трубку из 96%-ого этанола в стерильный физиологический раствор, инкубируют при 37°С 20 минут, заменяют физиологический раствор на свежий и выдерживают трубку в нем еще 30 минут. Процедуру повторяют 3 раза. Крыс линии Wistar массой 190-230 г начинают готовить к операции за 2 суток до хирургического вмешательства. За 2 суток до операции животных лишают твердой пищи и дают им 10% раствор глюкозы без ограничения (per os). Операцию проводят под общей анестезией (Золетил+Ксилазин), премедикация - атропина сульфат в дозе 0.04 мг/кг, подкожно за 15 мин до начала хирургического вмешательства. Животных фиксируют в положении на спине. В начале операции внутримышечно вводят цефтриаксон из расчета 100 мг/кг массы тела. Операционное поле ограничивают стерильными марлевыми салфетками, выполняют лапаротомию. В операционную рану выводят участок тонкой кишки (7 см дистальнее желудка), после чего с противобрыжеечного края кишки выполняют разрез на половину диаметра кишечной трубки, вводят в просвет кишечника стерильную трубку и узловыми швами герметично фиксируют имплантат с помощью хирургической нити (полиэстер, 4/0). После чего в месте имплантации удаляют участок кишечной трубки длиной 3 мм. Кишку помещают в брюшную полость и проводят послойное ушивание полости. В течение 4-х суток после операции выполняют ежедневные инъекции цефтриаксона из расчета 50 мг/кг массы тела. В течение 2-х суток животные получают 10-% раствор глюкозы, твердую пищу не получают, на третьи сутки их переводят на стандартную диету. Закрытый биодеградируемой трубкой циркулярный дефект тонкой кишки крысы с диастазом 10 мм представлен на фиг. 5. Через 6 месяцев после имплантации животных выводили из эксперимента. Состояние кишечника в области операции через 6 месяцев представлено на фиг. 6. Выраженного спаечного процесса и других патологий не наблюдалось. Далее проводили гистологический анализ тканей, сформированных на месте трубки через 6 месяцев (фиг. 7). Через 6 месяцев после операции на месте дефекта наблюдалась полностью восстановленная стенка тонкой кишки, включая все характерные анатомические слои: слизистую, подслизистую, мышечную (слои продольных и циркулярных мышц) и серозную оболочки. Таким образом применение биорезорбируемых трубок, описанных в настоящем изобретении, обеспечивает полное восстановление циркулярного дефекта тонкой кишки крысы с диастазом 10 мм.