Результат интеллектуальной деятельности: Лекарственный препарат для лечения нарушений мозгового кровообращения и восстановления утраченных функций мозга
Вид РИД
Изобретение
Изобретение относится к области фармакологии, неврологии, в том числе детской.
Проблема цереброваскулярных болезней имеет высокую значимость во многих странах мира. Инсульт является ведущей причиной инвалидизации населения, вероятность его развития у больных артериальной гипертензией повышается в 3-4 раза. Ежегодно в мире диагностируется около 10 миллионов случаев инсульта, из которых на долю России приходится более 450 тысяч. Смертность от инсульта в России составляет 1,23 на 1000 населения, в течение года после перенесенного инсульта умирает около 50% больных. Ишемические инсульты составляют 70-85% от общего числа инсультов, внутримозговые кровоизлияния - 20-25%, нетравматические субарахноидальные кровоизлияния - 5%. Достоверных данных о числе больных с хроническими нарушениями мозгового кровообращения в России нет, однако, по оценкам, заболеваемость хронической ишемией головного мозга превышает 700 на 100000 населения
(https://ru.wikipedia.org/wiki/Цереброваскулярные_болезни). Разработка новых эффективных препаратов для лечения цереброваскулярных болезней является важной научно - технической задачей.
Из уровня техники известно лекарственное средство "Церебрал" для лечения инсульта (Патент РФ 2151605), представляющий собой аминокислотно - пептидный комплекс, содержащий пептиды с молекулярным весом до 1500 Да и свободные аминокислоты. Недостатком данного изобретения является низкая эффективность при лечении ишемического инсульта (патент РФ 2470650).
Ближайшим аналогом заявленного изобретения является препарат для лечения ишемического и геморрагического инсульта, выделенный из мозга свиней, подвергшихся моделированию геморрагического инсульта (патент RU 2470650). Однако данный препарат является недостаточно эффективным и, при этом, сложным в получении. В частности, для получения указанного препарата необходимо моделирование геморрагического полушарного инсульта после окклюзии общей сонной артерии на этой же стороне (ишемического инсульта)
Таким образом, задачей заявленного изобретения является создание лекарственного препарата для лечения нарушений мозгового кровообращения и восстановления утраченных функций мозга, обладающим эффективностью при лечении как ишемического, так и геморрагического инсульта и при этом технически простого в получении.
Решение поставленной задачи обеспечивает пептидно-белковый комплекс, обладающий нейропротекторными и нейрорегенеративными свойствами, содержащий белковые молекулы и пептиды, синтез которых избирательно возрастает после повреждения ткани головного мозга животного и/или принимающих участие в механизмах нейропротекции и нейрорегенерации.
Авторами было показано, что после повреждения ткани мозга в ней избирательно возрастает содержание таких белков, как, например, Complexin-1, Heat shock 70 kDa protein, Peroxiredoxin-6, Actin, Prothymosin alpha, S100-A6, Parathymosin, S-phase kinase-associated protein 1, Transaldolase, Carbonic anhydrase 2, Neurofilament light polypeptide, Tubulin alpha-4A chain, Tubulin alpha-ID chain, Tubulin beta-2B chain, Microtubule-associated proteins 1A/1B light chain 3А, ADP-ribosylation factor 1, Tubulin beta-3 chain, Alpha-synuclein, Beta-synuclein, S100-A1, Cystatin-B, Macrophage migration inhibitory factor, Heat shock 90-alpha protein, Phosphatidylethanolamine-binding protein 1 (предшественник Hippocampal cholinergic neurostimulating peptide), Rab GDP dissociation inhibitor alpha, Alpha-enolase, Fatty acid-binding protein (brain), Thioredoxin, 14-3-3, Calmodulin, L-lactate dehydrogenase В chain, Phosphoglycerate kinase 1, Triosephosphate isomerase, Dihydropyrimidinase-related protein 2, Purine nucleoside phosphorylase, Ras-related proteins Rab-11A, 1A, 3А, 3С, 7a. Однако, есть основания полагать, что далеко не все белки, содержание которых повышается в мозге после его повреждения, участвуют в механизмах нейропротекции и нейрорегенерации.
Предположительно, белковые молекулы и пептиды, синтез которых избирательно возрастает после повреждения ткани головного мозга животного и/или принимающих участие в механизмах нейропротекции и нейрорегенерации, имеют молекулярную массу менее 200000 Дальтон.
Одной из наиболее оптимальных комбинаций указанных пептидов и белков, представляющих собой заявляемый препарат, может быть следующая: Complexin-1; Heat shock 70 kDa protein; 14-3-3; Alpha-synuclein, Beta-synuclein; Fatty acid-binding protein, brain; Phosphatidylethanolamine-binding protein 1 (или Hippocampal cholinergic neurostimulating peptide, предшественником которого он является), Dihydropyrimidinase-related protein 2, Cystatin-B, Tenascin, Cell division cycle 5-like protein, Macrophage migration inhibitory factor.

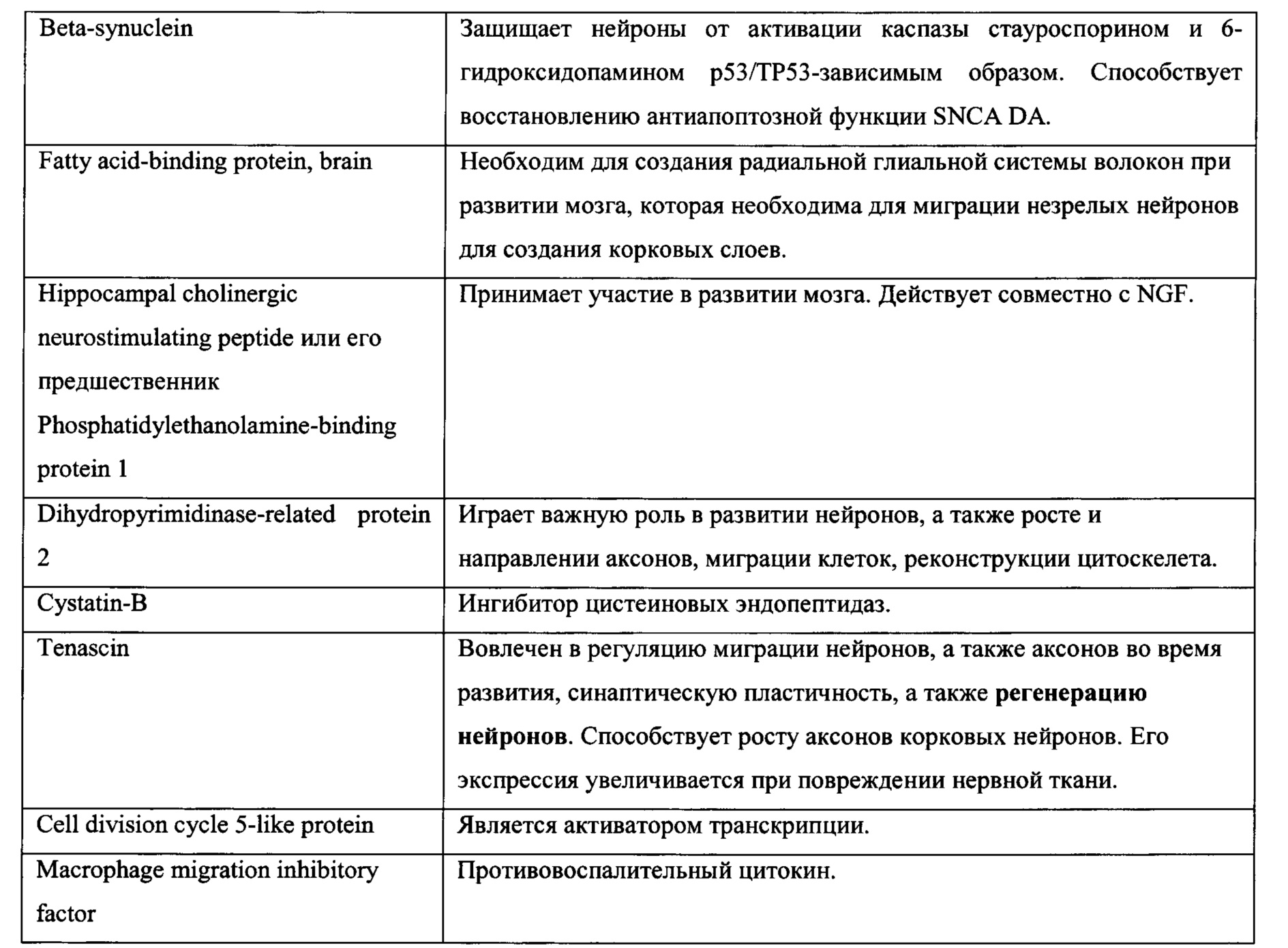
Таблица 1. Состав заявленного пептидно - белкового комплекса.
Дополнительно в препарат могут быть добавлены белки с нейропротекторными свойствами, такие как Aspartate aminotransferase, cytoplasmic; Glucose-6-phosphate isomerase, Protein DJ-1 (таблица 2).

Таблица 2. Дополнительные компоненты заявленного пептидно - белкового комплекса.
При этом, повреждение ткани головного мозга животного может осуществляться как путем физического, так и химического воздействия.
В качестве животных предпочтительно могут быть использованы млекопитающие, например, свиньи.
В немалой степени решение поставленной задачи обеспечивает способ получения указанного выше пептидно-белкового комплекса, включающий в себя:
- повреждающее воздействие на ткани головного мозга животного; -дробление тканей головного мозга животного с получением раздробленных частей тканей мозга животного;
- гомогенизацию раздробленных частей тканей головного мозга животного при рН 7,3-7,6 с получением гомогената мозга животного; -центрифугирование полученного гомогената головного мозга животного;
-очистка гомогената головного мозга животного от твердых компонентов с получением супернананта;
-очистку полученного супернатанта от липидных компонентов путем экстракции с получением неосветленного пептидно-белкового комплекса;
-удаление из полученного неосветленного пептидно-белкового комплекса молекул массой более 200000 Дальтон с получением заявленного пептидно-белкового комплекса;
При этом дробление тканей головного мозга животного с получением раздробленных частей тканей мозга животного осуществляется по прошествии 1-70 суток после повреждающего воздействия на ткани головного мозга животного, а в качестве повреждающего воздействия на ткани головного мозга животного может быть оказано как химическое, так и физическое воздействие.
В качестве животных предпочтительно могут быть использованы млекопитающие, например, свиньи.
Как вариант, полученный пептидно-белкововый комплекс дополнительно подвергается заморозке и последующей лиофилизации.
Заявленный пептидно-белкового комплекс может быть получен следующим образом:
На первом этапе, на ткани головного мозга животного (свиньи) оказывается повреждающее воздействие (производится моделирование двустороннего геморагического инсульта). Через 24 часа после повреждающего воздействия производится дробление тканей головного мозга животного с получением раздробленных частей тканей мозга животного, гомогенизацию раздробленных частей тканей головного мозга животного при рН 7,3-7,6 с получением гомогената мозга животного. Полученный гомогенат центрифугируется в течение в течение 25 минут (10000 g) и очищается от твердых компонентов путем декантации. Полученный супернатант очищается от липидных компонентов путем экстракции. Используют гексан (в смеси с супернатантом 1 к 3 по объему), экстракцию проводят двукратно. Из полученного неосветленного пептидно-белкового комплекса производится удаление молекул массой более 200000 Дальтон (посредством пропускания комплекса через фильтр с размером пор 0,48 мкм в течение 2 ч) с получением заявленного пептидно-белкового комплекса. Полученный препарат замораживают при температуре ниже -30°С, а затем подвергают лиофилизации.
Определение белкового состава полученного пептидно-белкового комплекса осуществляли методом масс-спектрометрии во фронтальном зависимом тандемном режиме сканирования на времяпролетном квадрупольном масс-спектрометре с использованием разделения пептидов, полученных после ферментативного расщепления белковых молекул, на системе высокоэффективной жидкостной хроматографии.
Поиск и идентификацию белков в полученных данных проводили с использованием алгоритма MASCOT / Andromeda против базы данных Uniprot 2.2014, валидацию данных против базы декойных произвольных последовательностей с макисмально допустимым пороговым значением ложных позитивных значений посика не более FDR=1% при вероятности р=0.05.
Относительный количественный анализ проводили по алгоритму iBRQ (intensity-based relative quantification) с измерением коэффициента emPAI, отражающего повторяемость и вырожденность идентифицированных и зарегистрированных протеотипических пептидов для каждого белка, идентифицированного в анализе.
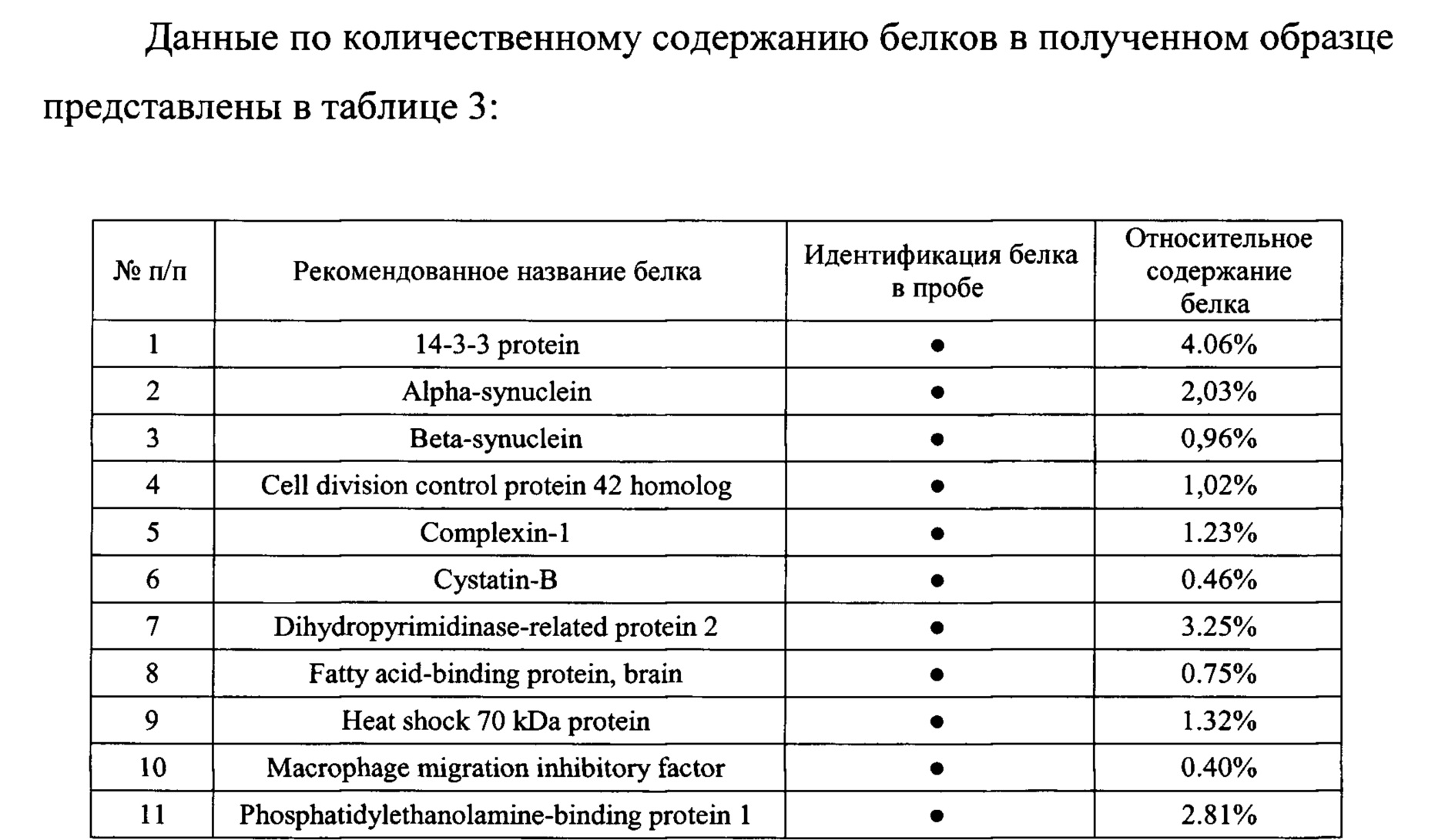
Таблица 3. Список белков, идентифицированных в полученном пептидно-белкового комплексе панорамным методом масс-спектрометрического анализа по пептидным продуктам ферментативного расщепления.
Решение поставленной задачи также обеспечивает лекарственное средство для лечения цереброваскулярных заболеваний, содержащее заявленный пептидно-белковый комплекс и фармацевтически приемлемые добавки, а также способ лечения цереброваскулярных заболеваний, включающий в себя введение больному указанного лекарственного средства.
Эффективность заявленного пептидно-белкового комплекса иллюстрируется нижеследующим примером.
Пример 1. Эффективность заявленного пептидно-белкового комплекса.
Материалы и методы
Для определения эффективности заявленного пептидно-белкового комплекса проводили эксперименты на крысах-самцах линии Вистар массой 200-300 г. У животных моделировали геморрагический инсульт по методу А.Н. Макаренко (2001) и ишемический инсульт - методом фототромбоза.
Исследуемые животные были разделены на 6 групп. Из них 2 контрольные группы (с модельным геморрагическим и ишемическим инсультом) и 4 опытные (2 с геморрагическим и 2 с ишемическим инсультом). Заявленный пептидно-белковый комплекс (далее - препарат) получала 1 группа с геморрагическим и 1 группа с ишемическим инсультом. Группы сравнения получали препарат для лечения ишемического и геморрагического инсульта, выделенный из мозга свиней, подвергшихся моделированию геморрагического инсульта, и представляющий собой аминокислотно-пептидный комплекс, отличающийся тем, что он выделен из мозга свиней, подвергшихся моделированию геморрагического полушарного инсульта после окклюзии общей сонной артерии на этой же стороне (ишемического инсульта), полученный в соответствии с текстом патента RU 2470650 (далее - аналог). Оценивалась летальность животных во всех группах.
Через 3 дня после воспроизведения модельного инсульта выжившим животным вводили образцы в течение 5 дней. Контрольные группы получали интраназально в каждую ноздрю по 2 капли 0,9% раствора NaCl. Опытные группы получали по 2 капли в каждую ноздрю заявленный препарат, содержащий 0,2 мг препарата, а группы сравнения - аналог в одинаковой дозировке. По шкале Stroke-index McGrow в модификации И.В. Ганнушкиной проводилось неврологическое тестирование функций выживших животных.
Статистические расчеты выполнялись методом дисперсионного анализа с повторными измерениями в программе R v.3.4.2. Отличия считались статистически значимыми при р<0,05 Результаты исследования

Таблица 4. Летальность животных (крыс) с модельным геморрагическим и ишемическим инсультом.
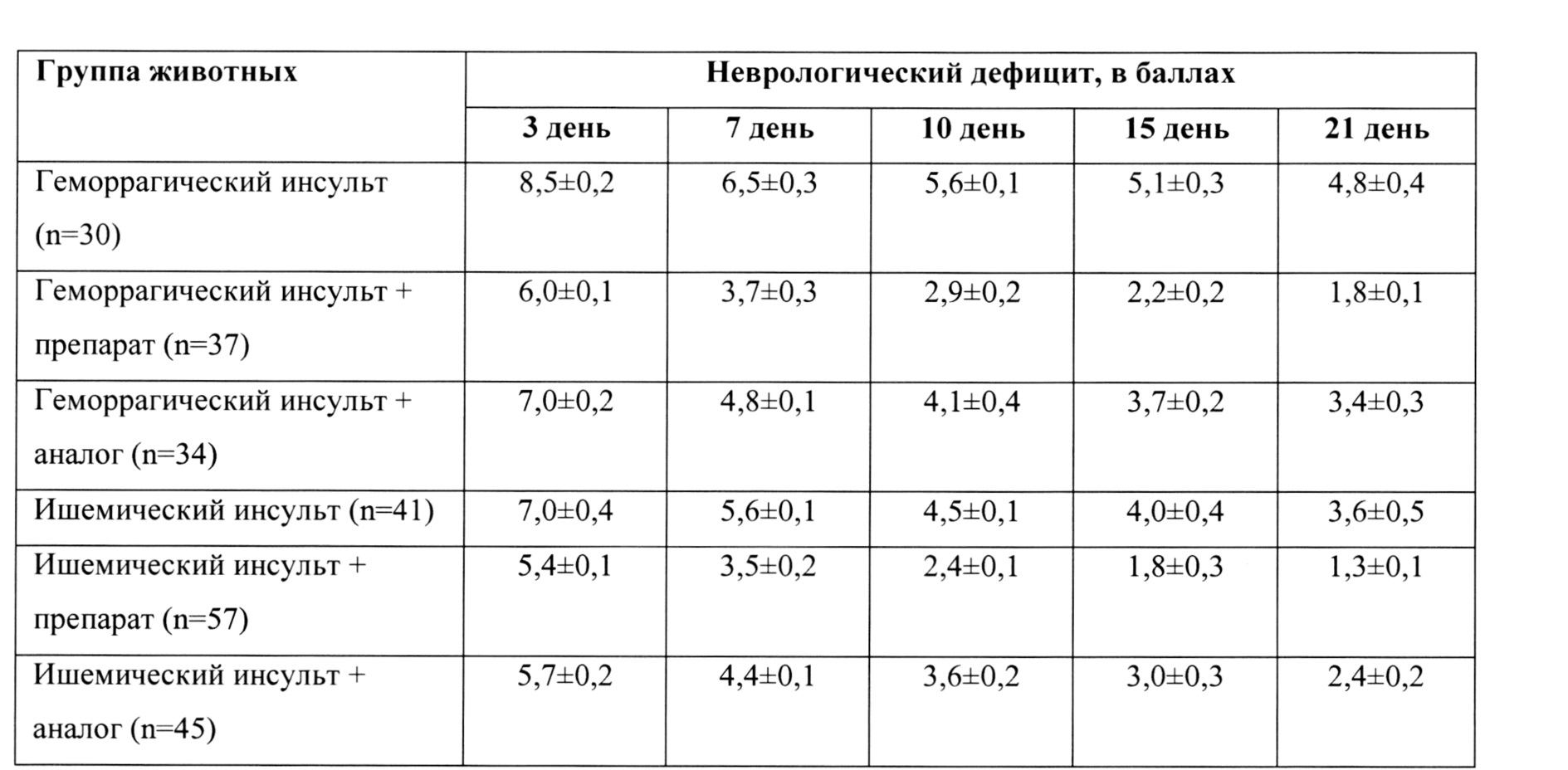
Таблица 5. Неврологический дефицит у животных (крыс) с модельным геморрагическим и ишемическим инсультом
Обсуждение результатов
Изучение выживаемости животных после модельного инсульта показало, что применение заявленного пептидно-белкового комплекса достоверно (р<0,05) повышает выживаемость по сравнению с препаратами сравнения. На каждый представленный в таблице 5 день тестирования при применении заявленного пептидно-белкового комплекса неврологический дефицит был менее выражен по сравнению с группами, где применяли препарат-аналог (р<0,05). Неврологический дефицит, возникавший у крыс после моделирования геморрагического и ишемического инсульта, снижался достоверно (р<0,05) быстрее у животных, получавших заявленный пептидно-белковый комплекс, по сравнению с группами сравнения.
На основании вышеуказанного можно сделать вывод об эффективности заявленного петидно-белкового комплекса для лечения нарушений мозгового кровообращения и восстановления утраченных функций мозга, а также вывод о том, что заявленный препарат обладает высокой эффективностью при лечении как ишемического, так и геморрагического инсульта.

