Результат интеллектуальной деятельности: Способ получения производных фуро[3,2-c]изохинолин-5(4Н)-она
Вид РИД
Изобретение
Предлагаемое изобретение относится к органической химии, а точнее к способам получения новых гетероциклических соединений ряда изохинолинона, которые могут представлять интерес как биологически активные вещества или полупродукты для их синтеза.
Известен способ получения бензофуро[3,2-с]изохинолин-5(6Н)-онов IV осуществляемый в две стадии: вначале проводят конденсацию салицилонитрила I с 2-(хлорметил)бензоатом II в присутствии безводного поташа в среде диметилформамида при 50-55°С, далее при обработке III трет-бутилатом калия происходит циклизация в соответствии со схемой:
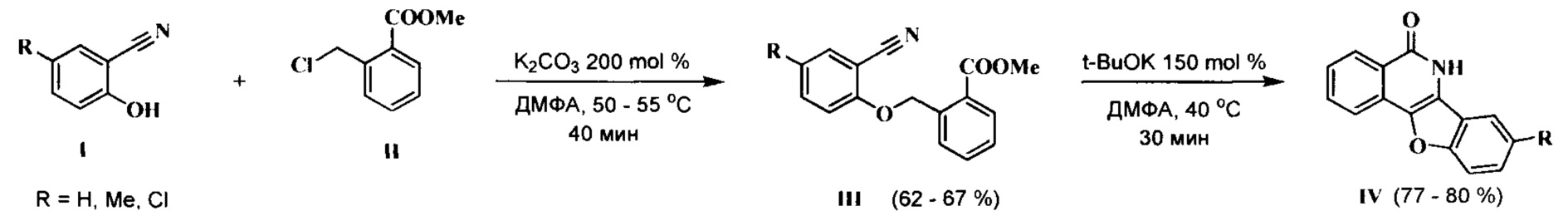
(V.E. Kalugin, A.M. Shestopalov. A convenient synthesis of benzofuro[3,2-c]isoquinolines and naphto[l'.2':4,5]furo[3,2-c]isoquimolines. Tetrahedron Letters, 2011, vol. 52, p. 1557-1560).
Практически в тоже время был предложен аналогичный способ получения бензофуро[3,2-с]изохинолин-5(6Н)-онов IV, отличающийся лишь тем, что вместо 2-(хлорметил)бензоата II используется 2-(бромметил)бензоат, а также тем, что основанием и для стадии конденсации и для стадии циклизации служит трет-бутилат калия (III), позволяющий осуществлять процесс one-pot.
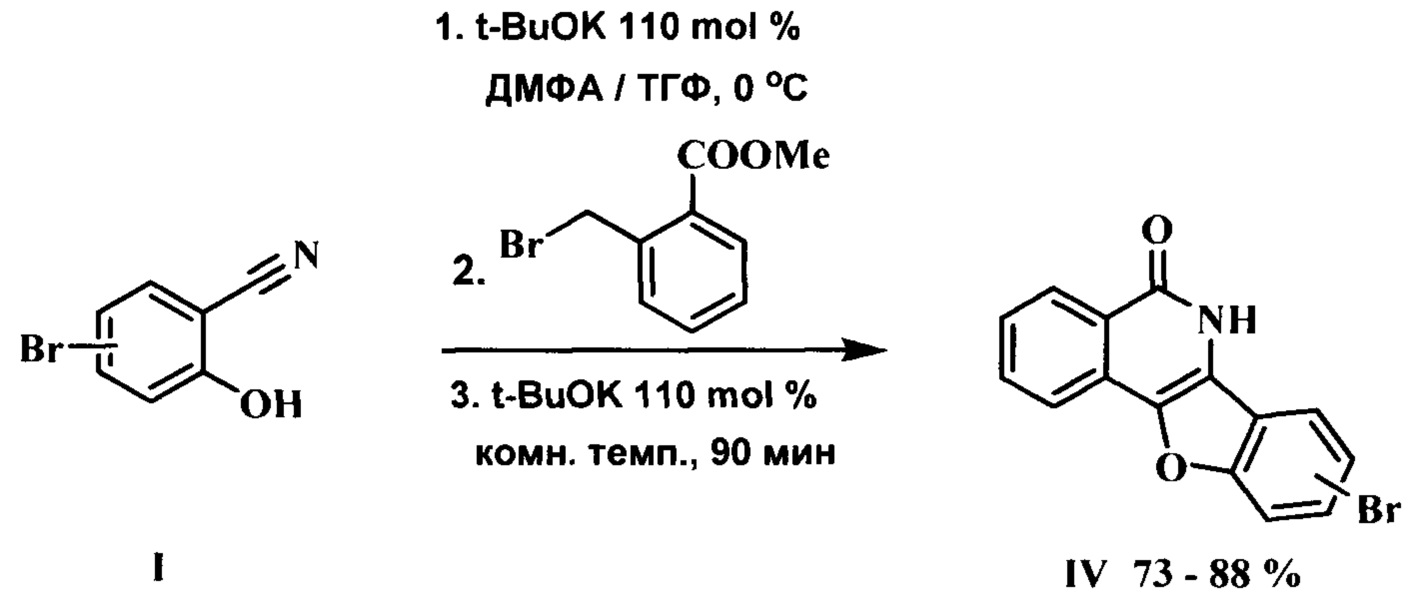
(L. Li, W.K.S. Chua. One-pot multistep synthesis of 3.4-fused isoquinolin-1(2H)-one analogs. Tetrahedron Letters, 2011, Vol. 52, p. 1574-1577).
Описаны аналогичные способы получения бензофуро[3,2-с]изохинолин-5(6Н)-она IV по реакции алкилирования салицилонитрила, в котором в качестве алкилирующего реагента используют бромгомофталат V.

Отличия способов состоят в используемых растворителях и основаниях:
- в случае применения поташа в среде ацетона целевой продукт образуется с низким выходом от 15 до 27% (направление А на схеме) (S. Yamaguchi, М. Yoshida, I. Miyajima, Т. Araki, Y. Hirai. The synthesis of benzofuroquinolines. X. Some benzofuro[3.2-c]isoquinoline derivatives. J. Heterocyclic Chem., 1995, Vol. 32, p. 1517-1519);
- гораздо эффективнее применение триэтиламина в среде ацетонитрила, что позволяет увеличить выход IV до умеренного (направление В на схеме) (P.G. Jagtap, Е. Baloglu, G. Southan, W. Williams, A. Roy, A. Nivorozhkin, N. Landrau, K. Desisto, A. L. Salzman,  Facile and Convenient Syntheses of 6,1l-Dihydro-5H-indeno[l,2-c]isoquinolin-5-ones and 6,1l-Dihydro-5H-indolo[3,2-c]isoquinolin-5-one. Organic Letters, 2005, Vol. 7, p. 1753-1756.).
Facile and Convenient Syntheses of 6,1l-Dihydro-5H-indeno[l,2-c]isoquinolin-5-ones and 6,1l-Dihydro-5H-indolo[3,2-c]isoquinolin-5-one. Organic Letters, 2005, Vol. 7, p. 1753-1756.).
Эффективность этого способа удалось увеличить, выделяя промежуточно образующийся продукт алкилирования салицилонитрила VI и осуществляя циклизацию действием гидрида натрия в среде толуола в соответствии со схемой:
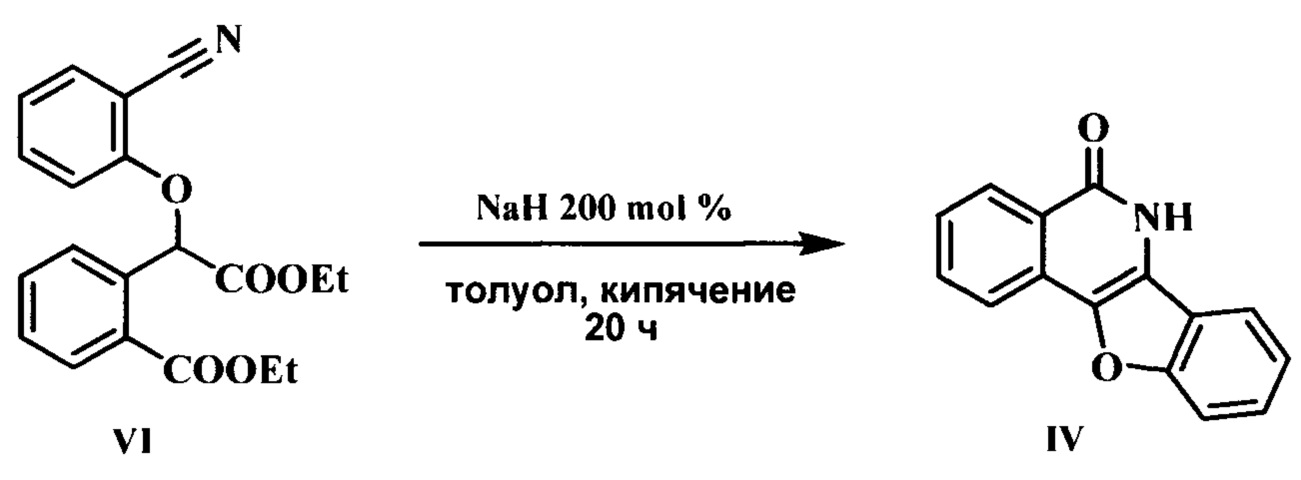
(S. Yamaguchi, М. Yoshida, I. Miyajima, Т. Araki, Y. Hirai. The synthesis of benzofuroquinolines. X. Some benzofuro[3.2-c]isoquinoline derivatives. J. Heterocyclic Chem., 1995, Vol. 32, p. 1517-1519).
Известен способ получения бензофуро[3,2-с]изохинолин-5(6Н)-она IV путем амминолиза 5Н-бензофуро[3,2-с]изохромен-5-она VII, который осуществляют при избыточном давлении в запаянной стеклянной трубке в соответствии со схемой:

(S. Yamaguchi, Y. Uchiuzoh, К|. Sanada. The synthesis of benzofuroquinolines. IX. A benzofuroisoquinolinone and benzofuroisocoumarin. J. Heterocyclic Chem., 1995, Vol. 32, p. 419-423).
Известен способ получения бензофуро[3,2-с]изохинолин-5(6Н)-она, включающий последовательность трех реакций: на первой стадии, используя в качестве исходного соединения гетероциклическую иодониевую соль VIII получают бензофуро[3,2-с]изохинолин IX, который далее окисляют мета-хлорпербензойной кислотой в соответствующий N-оксид X, обработка которого метансульфонилхлоридом дает целевое соединение с общим выходом 42%:

(D. Zhu, Z. Wu, В. Luo, Y. Du, P. Liu, Y. Chen, Y. Hu, P. Huang, .S. Wen. Heterocyclic Iodoniums for the Assembly of Oxygen-Bridged Polycyclic Heteroarenes with Water as the Oxygen Source. Organic Letters, 2018, Vol. 20, p. 4815-4818.).
Все описанные способы позволяют получать соединения, содержащие фуро[3,2-с]изохинолин-5(4Н)-оновый фрагмент, в котором фурановое кольцо аннелировано к арильному кольцу.
Однако сведения о способах получения соединений, в которых фуро[3,2-с]изохинолин-5(4Н)-оновый фрагмент содержит во втором положении фуранового кольца какой-либо заместитель, а в третьем положении водород, отсутствуют.
Задача изобретения - разработка эффективного способа получения производных фуро[3,2-с]изохинолин-5(4Н)-она, которые представляют интерес в качестве аналогов биологически активных веществ.
Техническим результатом является создание простого и эффективного способа получения производных фуро[3,2-с]изохинолин-5(4Н)-она с использованием коммерчески доступных соединений, позволяющих варьировать заместитель в положении 2 фуранового кольца.
Технический результат достигается проведением реакции 2-имино-1Н-инден-1,3(2Н)-дионов с 1-алкинами в среде хлорированных растворителей в присутствии трифторуксусной кислоты при комнатной температуре в соответствии со схемой:
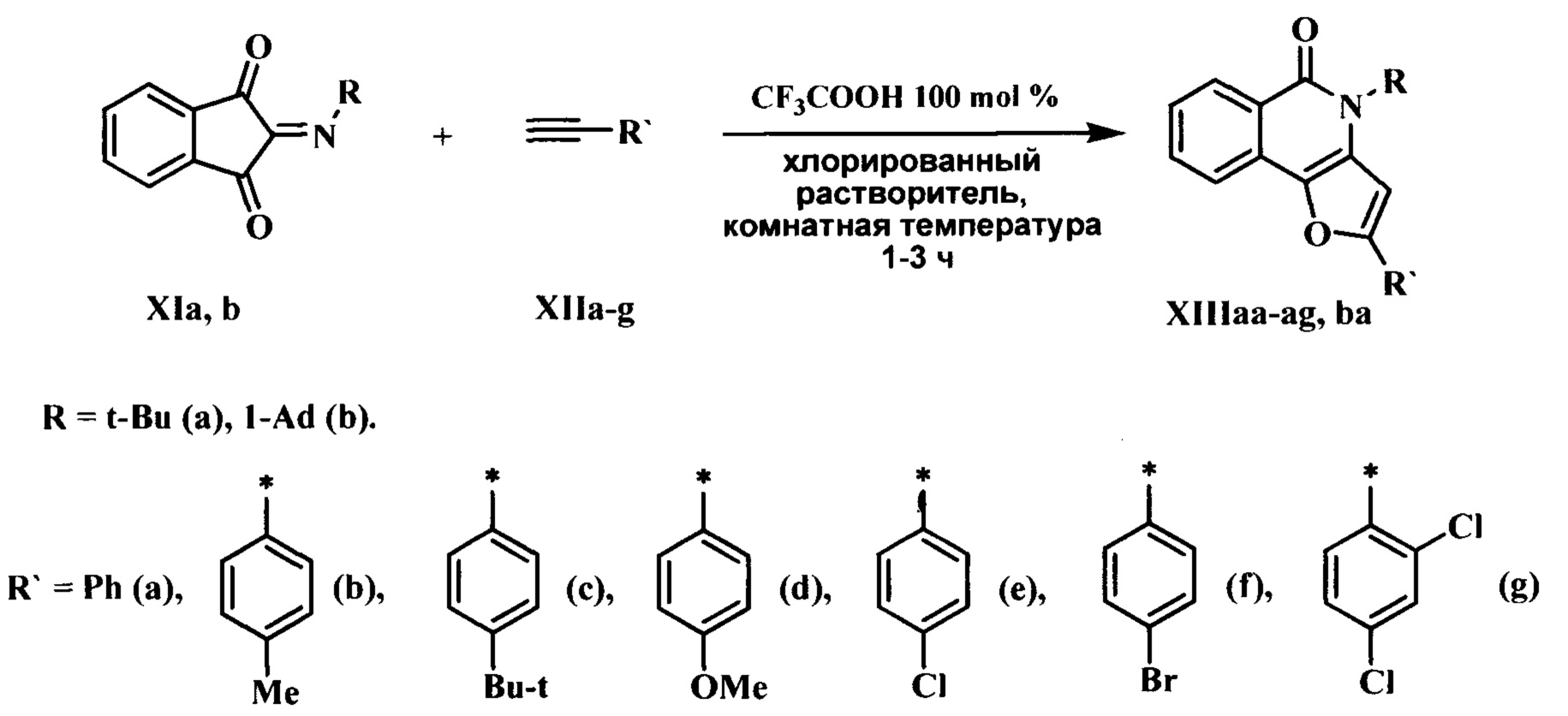
Используемые 2-имино-1Н-инден-1,3(2Н)-дионы XI являются легко доступными соединениями, они могут быть получены с высокими выходами при взаимодействии нингидрина или продукта его дегидратации - индантриона с аминами. (Р.А. Crooks. Synthesis of 2-amino-1.3-dihydroxyindanes. Chemistry and industry. 1980, p. 467-468.).
Выбор оптимальных условий получения производных фуро[3,2-с]изохинолин-5(4Н)-она с заместителем в положении 2 фуранового кольца, проводили на модельной реакции 2-(трет-бутилимино)-1Н-инден-1,3(2Н)-диона XIa с фенилацетиленом XIIa, ход которой контролировали тонкослойной хроматографией. 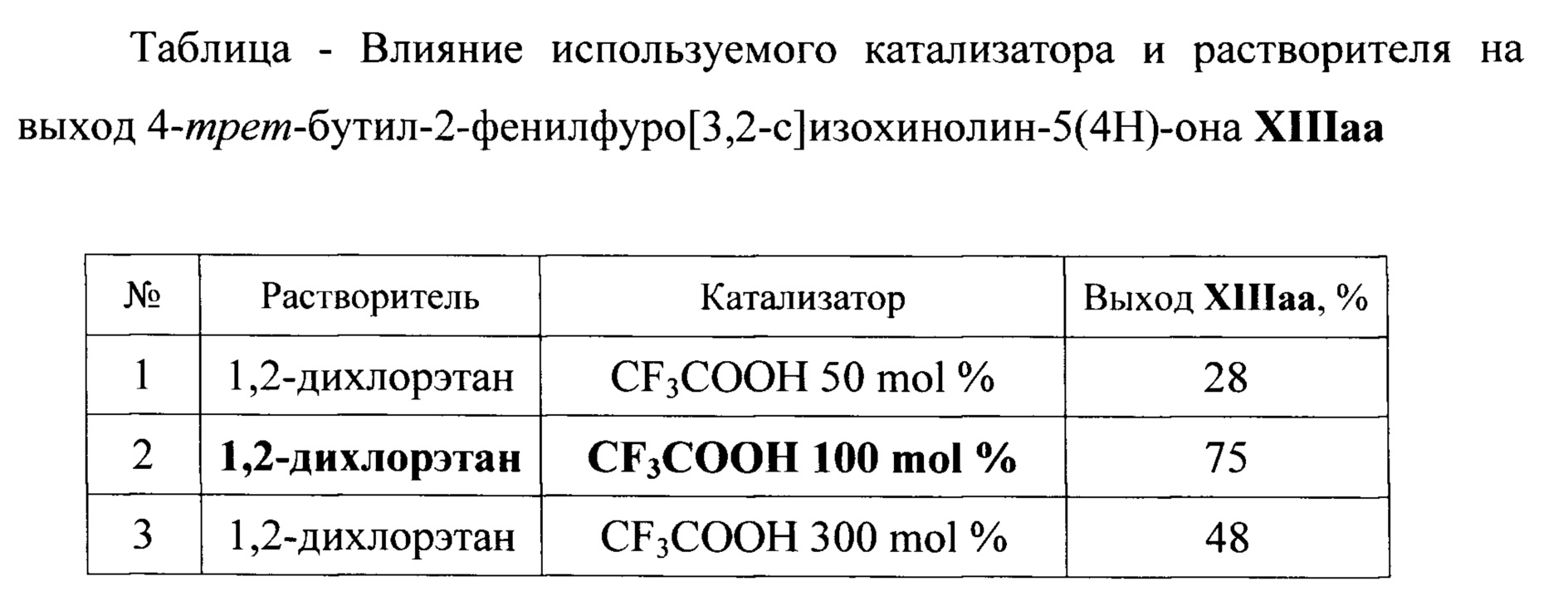
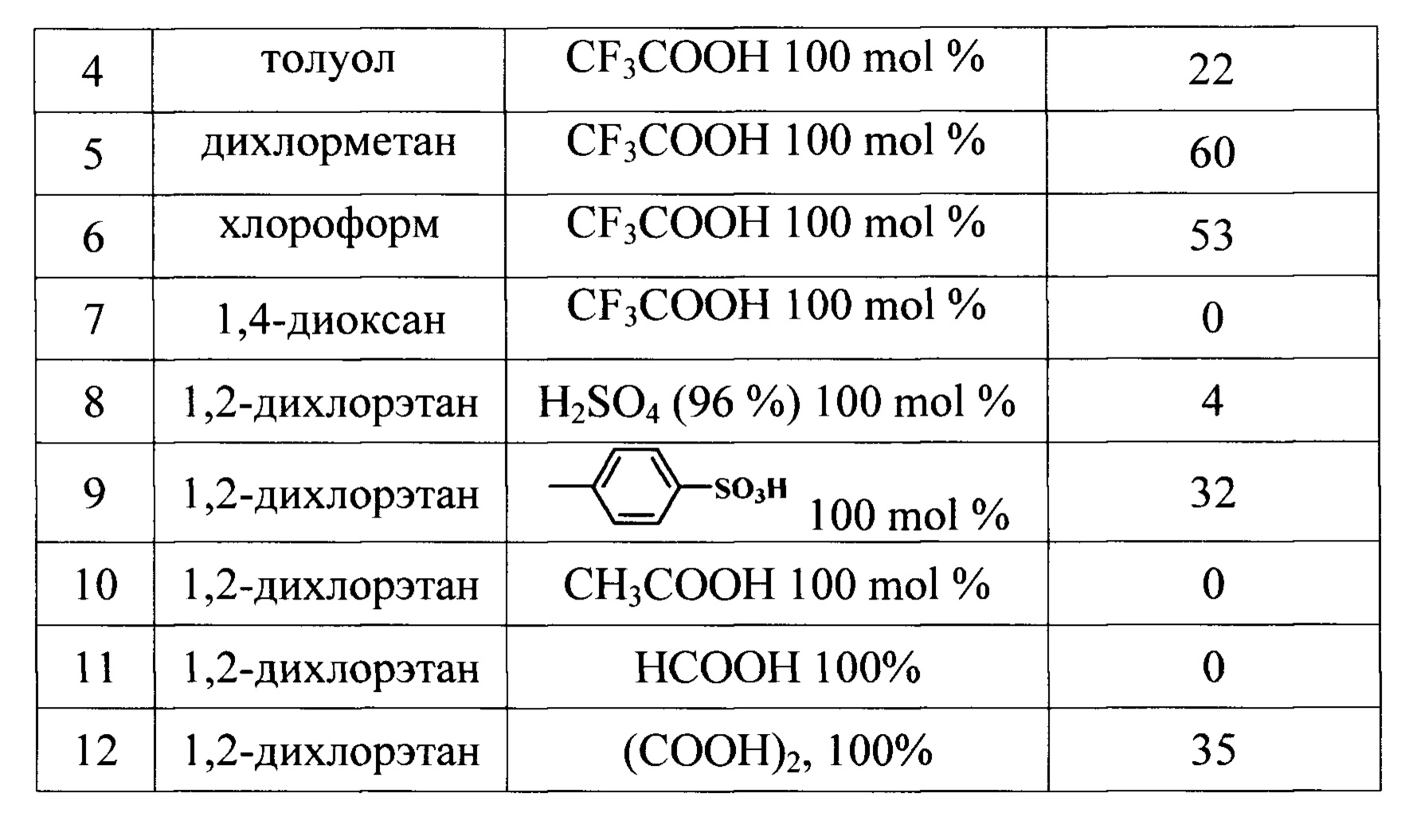
Как видно из данных таблицы, наилучшую активность показала трифторуксусная кислота, использованная в количестве 100-300 мольных % в среде хлорированных растворителей, таких как 1,2-дихлорэтан, дихлорметан или хлороформ.
Экспериментально было выявлено, что время реакции зависит от природы 1-алкина и составляет от 1 до 3 часов, и отражено в примерах конкретного выполнения.
Пример 1. Получение 4-трет-бутил-2-фенилфуро[3,2-с]изохинолин-5(4Н)-она.
В реакционную виалу, снабженную магнитным перемешивающим элементом, помещают 3 мл 1,2-дихлорэтана, 0,129 г (0,0006 моль) 2-(трет-бутилимино)-1Н-инден-1,3(2Н)-диона и прибавляют 0,046 мл (0,0006 моль) трифторуксусной кислоты. Реакционную массу перемешивают 5 минут при комнатной температуре и прибавляют 0,079 мл (0,00072 моль) фенилацетилена. После перемешивания при комнатной температуре в течение 3 ч реакционную массу переносят в делительную воронку, содержащую 25 мл насыщенного раствора гидрокарбоната натрия и экстрагируют этил ацетатом 3 раза по 15 мл. Объединенные экстракты упаривают, остаток очищают флеш-хроматографией на силикагеле, проводя элюирование смесью гексана и этилацетата (10: 2). Выход 75%. Желтые кристаллы. Тпл 116-117°С.
ИК-спектр (KBr), ν/см-1: 3074, 3053, 3020 (Csp2-H), 2978, 2933 (Csp3-H), 1643 (С=О), 1624, 1606,1500 (Csp2-Csp2).
Спектр ЯМР 1Н (399.78 МГц, CDCl3, δ, м.д.): 1.90 (с., 9Н, СН3), 7.14 (с., 1H, СН), 7.32-7.35 (м, 1Н, СН), 7.39-7.46 (м, 3Н, СН), 7.65-7.69 (м, 1Н, СН), 7.79-7.81 (м, 2Н, СН), 7.88-7.90 (м, 1Н, СН), 8.37-8.39 (м, 1Н, СН).
Спектр ЯМР 13С (CDCl3), δ, м.д.: 30.4 (СН3), 62.6 (С), 101.0 (СН), 118.2, 124.1, 125.4, 125.9, 126.9, 128.3, 128.8, 128.9, 129.2, 129.9, 132.2, 136.8, 152.9 (С), 163.4 (С).
Пример 2. Получение 4-трет-бутил-2-(4-метилфенил)фуро[3,2-с]изохинолин-5(4Н)-она.
В реакционную виалу, снабженную магнитным перемешивающим элементом, помещают 3 мл 1,2-дихлорэтана, 0,129 г (0,0006 моль) 2-(трет-бутилимино)-1Н-инден-1,3(2Н)-диона и прибавляют 0,046 мл (0,0006 моль) трифторуксусной кислоты. Реакционную массу перемешивают 5 минут при комнатной температуре и прибавляют 0,084 г (0,00072 моль) 4-этинилтолуола. После перемешивания при комнатной температуре в течение 2 ч реакционную массу переносят в делительную воронку, содержащую 25 мл насыщенного раствора гидрокарбоната натрия и экстрагируют этилацетатом 3 раза по 15 мл. Объединенные экстракты упаривают, остаток очищают флеш-хроматографией на силикагеле, проводя элюирование смесью гексана и этилацетата. Выход 70%. Желтые кристаллы. Тпл 139-140°С.
ИК-спектр (KBr), ν/см-1: 3055, 3020 (Csp2-H), 2972, 2922 (Csp3-H), 1643 (С=О), 1624,1508 (Csp2-Csp2).
Спектр ЯМР 1Н (399.78 МГц, CDC13, δ, м.д.): 1.90 (с, 9Н, СН3), 2.39 (с., 3Н, СН3), 7.08 (с., 1Н, СН), 7.23-7.26 (м, 2Н, СН), 7.37-7.41 (м, 1Н, СН), 7.64-7.69 (м, 3Н, СН), 7.88 (д, J=8 Гц, 1Н, СН), 8.38 (д, J=8 Гц, 1Н, СН).
Спектр ЯМР 13С (CDCl3), δ, м.д.: 21.4 (СН3), 30.4 (СН3), 62.6 (С), 100.4 (СН), 118.2, 124.1, 125.2, 125.7, 127.0, 127.2, 129.0, 129.2, 129.5, 132.2, 136.5, 138.4, 153.2 (С), 163.4 (С).
Пример 3. Получение 4-трет-бутил-2-(4-трет-бутилфенил)фуро[3,2-с]изохинолин-5(4Н)-она.
В реакционную виалу, снабженную магнитным перемешивающим элементом, помещают 3 мл 1,2-дихлорэтана, 0,129 г (0,0006 моль) 2-(трет-бутилимино)-1Н-инден-1,3(2Н)-диона и прибавляют 0,046 мл (0,0006 моль) трифторуксусной кислоты. Реакционную массу перемешивают 5 мин при комнатной температуре и прибавляют 0,114 г (0,00072 моль) 4-трет-бутилфенилацетилена. После перемешивания при комнатной температуре в течение 1 ч реакционную массу переносят в делительную воронку, содержащую 25 мл насыщенного раствора гидрокарбоната натрия и экстрагируют этилацетатом 3 раза по 15 мл. Объединенные экстракты упаривают, остаток очищают флеш-хроматографией на силикагеле, проводя элюирование смесью гексана и этилацетата. Выход 74%. Желтые кристаллы. Тпл 147-148°С.
ИК-спектр (KBr), ν/см-1: 3062, 3032 (Csp2-H), 2954, 2904, 2868 (Csp3-H), 1645 (С=О), 1624, 1508 (Csp2-Csp2).
Спектр ЯМР 1Н (399.78 МГц, CDC13, δ, м.д.): 1.36 (с, 9Н, СН3), 1.90 (с., 9Н, СН3), 7.09 (с., 1Н, СН), 7.38-7.42 (м, 1Н, СН), 7.46-7.48 (м, 2Н, СН), 7.65-7.68 (м, 1Н, СН), 7.72-7.74 (м, 2Н, СН), 7.89 (д, J=7 Гц, 1Н, СН), 8.38 (д, J=7.6 Гц, 1Н, СН).
Спектр ЯМР 13С (CDCl3), δ, м.д.: 30.4 (СН3), 31.2 (СН3), 34.7 (С), 62.6 (С), 100.5 (СН), 118.2, 124.0, 125.3, 125.7, 125.8, 127.0, 127.2, 129.0, 129.2, 132.2, 136.6, 151.7 (С), 153.2 (С), 163.4 (С).
Пример 4. Получение 4-трет-бутил-2-(4-метоксифенил)фуро[3,2-с]изохинолин-5(4Н)-она.
В реакционную виалу, снабженную магнитным перемешивающим элементом, помещают 3 мл 1,2-дихлорэтана, 0,129 г (0,0006 моль) 2-трет-бутилимино)-1Н-инден-1,3(2Н)-диона и прибавляют 0,046 мл (0,0006 моль) трифторуксусной кислоты. Реакционную массу перемешивают 5 мин при комнатной температуре и прибавляют 0,095 г (0,00072 моль) 4-метоксифенилацетилена. После перемешивания при комнатной температуре в течение 1 ч реакционную массу переносят в делительную воронку, содержащую 25 мл насыщенного раствора гидрокарбоната натрия и экстрагируют этилацетатом 3 раза по 15 мл. Объединенные экстракты упаривают, остаток очищают флеш-хроматографией на силикагеле, проводя элюирование смесью гексана и этилацетата. Выход 67%. Желтое масло.
ИК-спектр (KBr), ν/см-1: 3064, 3018 (Csp2-H), 2954, 2920, 2841 (Csp3-H), 1639 (С=О), 1624, 1506 (Csp2-Csp2).
Спектр ЯМР 1Н (399.78 МГц, CDCl3, δ, м.д.): 1.89 (с., 9Н, СН3), 3.84 (с., 3Н, СН3), 6.94-6.97 (м, 2Н, СН), 7.00 (с., 1Н, СН), 7.35-7.39 (м, 1Н, СН), 7.62-7.66 (м, 1Н, СН), 7.69-7.73 (м, 2Н, СН), 7.84-7.86 (м, 1Н, СН), 8.35-8.37 (м, 1Н, СН).
Спектр ЯМР 13С (CDCl3), δ, м.д.: 30.4 (СН3), 55.3 (СН3), 62.6 (С), 99.6 (СН), 114.3, 118.0, 122.8, 125.0, 125.5, 125.6, 127.0, 129.0, 129.2, 132.1, 136.2, 153.1 (С), 159.8 (С), 163.4 (С).
Пример 5. Получение 4-трет-бутил-2-(4-хлорфенил)фуро[3,2-с]изохинолин-5(4Н)-она.
В реакционную виалу, снабженную магнитным перемешивающим элементом, помещают 3 мл 1,2-дихлорэтана, 0,129 г (0,0006 моль) 2-(трет-бутилимино)-1Н-инден-1,3(2Н)-диона и прибавляют 0,046 мл (0,0006 моль) трифторуксусной кислоты. Реакционную массу перемешивают 5 мин при комнатной температуре и прибавляют 0,098 г (0,00072 моль) 4-хлорфенилацетилена. После перемешивания при комнатной температуре в течение 3 ч реакционную массу переносят в делительную воронку, содержащую 25 мл насыщенного раствора гидрокарбоната натрия и экстрагируют этилацетатом 3 раза по 15 мл. Объединенные экстракты упаривают, остаток очищают флеш-хроматографией на силикагеле, проводя элюирование смесью гексана и этилацетата. Выход 64%. Желтые кристаллы. Тпл 157-158°С.
ИК-спектр (KBr), ν/см-1: 3055, 3028 (Csp2-H), 2972, 2958, 2922 (Csp3-H), 1645 (С=О), 1625, 1500 (Csp2-Csp2).
Спектр ЯМР 1Н (399.78 МГц, CDCl3, δ, м.д.): 1.89 (с., 9Н, СН3), 7.12 (с., 1Н, СН), 7.38-7.43 (м, 3, СН), 7.64-7.68 (м, 1Н, СН), 7.69-7.72 (м, 2Н, СН), 7.86 (д, J=8 Гц, 1Н, СН), 8.37 (д, J=8.2 Гц, 1Н, СН).
Спектр ЯМР 13C (CDCl3), δ, м.д.: 30.4 (СН3), 62.6 (С), 101.3 (СН), 118.2, 125.3, 125.5, 126.1, 126.8, 128.4, 128.8, 129.1, 129.3, 132.2, 134.1, 137.0, 151.7 (С), 163.3 (С).
Пример 6. Получение 2-(4-бромфенил)-4-трет-бутилфуро[3,2-с]изохинолин-5(4Н)-она.
В реакционную виалу, снабженную магнитным перемешивающим элементом, помещают 3 мл 1,2-дихлорэтана, 0,129 г (0,0006 моль) 2-(трет-бутилимино)-1Н-инден-1,3(2Н)-диона и прибавляют 0,046 мл (0,0006 моль) трифторуксусной кислоты. Реакционную массу перемешивают 5 мин при комнатной температуре и прибавляют 0,13 г (0,00072 моль) 4-бромфенилацетилена. После перемешивания при комнатной температуре в течение 3 ч реакционную массу переносят в делительную воронку, содержащую 25 мл насыщенного раствора гидрокарбоната натрия и экстрагируют этилацетатом 3 раза по 15 мл. Объединенные экстракты упаривают, остаток очищают флеш-хроматографией на силикагеле, проводя элюирование смесью гексана и этилацетата. Выход 65%. Желтые кристаллы. Тпл 149-150°С.
ИК-спектр (KBr), ν/см-1: 3064, 3055, 3012 (Csp2-H), 2972, 2958, 2922 (Csp3-H), 1643 (С=О), 1624, 1498 (Csp2-Csp2).
Спектр ЯМР 1Н (399.78 МГц, CDCl3, δ, м.д.): 1.89 (с., 9Н, СН3), 7.13 (с., 1Н, СН), 7.39-7.43 (м, 1Н, СН), 7.53-7.57 (м, 2Н, СН), 7.63-7.68 (м, 3Н, СН), 7.86 (д, J=8 Гц, 1Н, СН), 8.37 (д, J=8 Гц, 1Н, СН).
Спектр ЯМР 13С (CDCl3), δ, м.д.: 30.4 (СН3), 62.7 (С), 101.4 (СН), 118.32, 122.23, 125.5, 126.2, 126.8, 128.9, 129.3, 132.0, 132.3, 137.1, 151.8 (С), 163.4 (С).
Пример 7. Получение 4-трет-бутил-2-(2,4-дихлорфенил)фуро[3,2-с]изохинолин-5(4Н)-она.
В реакционную виалу, снабженную магнитным перемешивающим элементом, помещают 3 мл 1,2-дихлорэтана, 0,129 г (0,0006 моль) 2-(трет-бутилимино)-1Н-инден-1,3(2Н)-диона и прибавляют 0,046 мл (0,0006 моль) трифторуксусной кислоты. Реакционную массу перемешивают 5 мин при комнатной температуре и прибавляют 0,123 г (0,00072 моль) 2,4-дихлорфенилацетилена. После перемешивания при комнатной температуре в течение 3 ч реакционную массу переносят в делительную воронку, содержащую 25 мл насыщенного раствора гидрокарбоната натрия и экстрагируют этилацетатом 3 раза по 15 мл. Объединенные экстракты упаривают, остаток очищают флеш-хроматографией на силикагеле, проводя элюирование смесью гексана и этилацетата. Выход 57%. Желтоватые кристаллы. Тпл 136-137°С.
ИК-спектр (KBr), ν/см-1: 3074, 3016 (Csp2-H), 2970, 2954, 2918 (Csp3-H), 1641 (С=О), 1624, 1496 (Csp2-Csp2).
Спектр ЯМР 1Н (399.78 МГц, CDCl3, δ, м.д.): 1.89 (с., 9Н, СН3), 7.34-7.36 (м, 1Н, СН), 7.41-7.45 (м, 1Н, СН), 7.48 (д, J=8.2 Гц, 1Н, СН), 7.65-7,69 (м, 2Н, СН+СН), 7.86 (д, J=8 Гц, 1Н, СН).
Спектр ЯМР 13С (CDCl3), δ, м.д.: 30.4 (СН3), 62.6 (С), 106.8 (СН), 118.4, 125.9, 126.5, 126.6, 127.0, 127.5, 128.5, 128.8, 129.3, 130.7, 132.3, 134.0, 136.8, 148.0 (С), 163.3 (С).
Пример 8. Получение 4-(1-адамантил)-2-фенилфуро[3,2-с]изохинолин-5(4Н)-она.
В реакционную виалу, снабженную магнитным перемешивающим элементом, помещают 3 мл 1,2-дихлорэтана, 0,176 г (0,0006 моль) 2-(1-адамантилимино)-1Н-инден-1,3(2Н)-диона и прибавляют 0,46 мл (0,0006) трифторуксусной кислоты. Реакционную массу перемешивают 5 мин при комнатной температуре и прибавляют 0,079 мл (0,00072) фенилацетилена. После перемешивания при комнатной температуре в течение 3 ч реакционную массу переносят в делительную воронку, содержащую 25 мл насыщенного раствора гидрокарбоната натрия и экстрагируют этилацетатом 3 раза по 15 мл. Объединенные экстракты упаривают, остаток очищают флеш-хроматографией на силикагеле, проводя элюирование смесью гексана и этилацетата. Выход 63%. Желтые кристаллы. Тпл 220-221°С.
ИК-спектр (KBr), ν/см-1: 3057, 3007 (Csp2-H), 2908, 2881, 2846 (Csp3-H), 1631 (С=O), 1602, 1498 (Csp2-Csp2).
Спектр ЯМР 1Н (399.78 МГц, CDCl3, δ, м.д.): 1.73-1.90 (м., 6Н, СН2), 2.28 (уш.с, 3Н, СН), 2.71-2.75 (м., 6Н, СН2), 7.26 (с, 1Н, СН), 7.31-7.36 (м, 1Н, СН), 7.38-7.46 (м, 3Н, СН), 7.64-7.68 (м, 1Н, СН), 7.79-7.68 (м, 2Н, СН), 7.87-7.89 (м, 1Н, СН), 8.36-8.38 (м, 1Н, СН).
Спектр ЯМР 13С (CDCl3), δ, м.д.: 30.5 (СН), 36.3 (СН2), 40.9 (СН2), 65.9 (С), 101.5 (СН), 118.2, 124.1, 125.6, 126.0, 126.8, 128.3, 128.5, 128.8, 129.3, 130.0, 132.2, 137.2, 152.6 (С), 163.5 (С).
Таким образом, предлагается простой и эффективный способ получения новых производных фуро[3,2-с]изохинолин-5(4Н)-она, позволяющий варьировать заместитель в положении 2 фуранового кольца. Способ обеспечивает получение целевых веществ с хорошим выходом, при этом используют коммерчески доступные реагенты, что делает его промышленно применимым. Заявляемый способ удовлетворяет условиям патентоспособности.
![Способ получения производных фуро[3,2-c]изохинолин-5(4Н)-она](https://fips.edrid.ru/images/rid/7f/b5/68/3890fa6715977563042809c251589ad2.jpg)
![Способ получения производных фуро[3,2-c]изохинолин-5(4Н)-она](https://fips.edrid.ru/images/rid/7f/b5/68/081bf057d5ae0d2108fa3aec44ac3f7e.jpg)

