Результат интеллектуальной деятельности: СПОСОБ ОПРЕДЕЛЕНИЯ ВЕЛИЧИНЫ АДСОРБЦИИ ВИНПОЦЕТИНА ЛИПОСОМАМИ
Вид РИД
Изобретение
Изобретение относится к области исследования и анализа веществ и может быть использовано для определения концентрации исследуемого вещества при разработке новых сложных лекарственных форм фармацевтических препаратов с использованием спектрофотометрического метода.
Известен способ, который заключается в дезинтеграции липосомальных везикул нагреванием до температуры 90-100°С [Gardner S.C. "Delipidation treatment for large-scale protein purification processing" Thesis for MS in Chem. Engineering, Virginia Polytechnic Inst., 1996].
Недостатком этого способа является относительно низкая точность, поскольку возникает обратная интеграция везикул при остывании смеси. В результате липосомальные везикулы и мицеллы формируются заново и часть препарата попадает обратно в липосомы, поэтому в водном растворе можно измерить лишь оставшуюся часть реальной концентрации препарата.
Заслуживает внимания способ осаждения липосом, нагруженных препаратом с помощью протамина сульфата, с последующим спектрофотометрическим определением неинкапсулированного вещества в полученном супернатанте [V.Torchilin and V. Weissig, "Liposomes 2nd eds., A Practical Approach" ed. Oxford Univercity Press, 2003, 384 pp].
Однако метод имеет существенные ограничения, связанные с возможностью соосаждения определяемого вещества.
Наиболее близким по своей сущности к предлагаемому является способ определения концентрации липосомально инкапсулированных фармацевтических препаратов цитостатиков гидрофильной природы, включающий разрушение липосомальных везикул и последующее измерение концентрации вышедшего в раствор цитостатика [Патент на изобретение №2337358 РФ/ Некоммерческое организация Учреждение «Прогрессивные медицинские исследования». - №2007112306; заявлено 03.04.07; опубл. 27.10.2009; Бюл. №30. - 10 с]. Данный способ отличается тем, что липосомальные везикулы разрушают добавлением к липосомальной суспензии, разбавленной 2 М раствором хлорида натрия в соотношении 1:1, 3-кратного объема хлороформа, после чего пробы нагревают до 50-60°С, центрифугируют при 5000 g в течение 5 мин, концентрацию вышедшего в водную фазу цитостатика определяют спектрофотометрически.
Недостатком способа является образование различных мицеллярных форм определяемого препарата, что приводит к серьезным погрешностям в измерениях и вызывает трудности в интерпретации получаемых результатов.
Технический результат заключается в разработке неразрушающего способа, количественного определения винпоцетина на поверхности липосом, полученных из соевого лецитина.
Технический результат достигается тем, что в способе определения величины адсорбции винпоцетина липосомами, включающем количественное определение винпоцетина методом спектрофотометрии, согласно изобретению, проводится диализ при температуре 37°С в течение 12 ч в диализаторе с 12 мл коллоидного раствора липосом с массовой долей липосом 0,1342±0,02881% из соевого лецитина или с 12 мл водного раствора кислоты хлористоводородной 0,01 М; куда помещается диализная пробирка, заполненная 3 мл водного раствора кислоты хлористоводородной 0,01 М, содержащего винпоцетин в концентрации 0,24 мг/мл, для проведения диализа используется мембрана, характеристика пропускания которой 14 кДа; после достижения равнения концентрация винпоцетина измеряется в диализной пробирке, погруженной в диализатор с раствором липосом и диализатор, заполненный раствором кислоты хлористоводородной 0,01 М; определение величины адсорбции винпоцетина липосомами осуществляется по разности концентраций винпоцетина, вышедшего в диализную среду диализатора с водным раствором кислоты хлористоводородной 0,01 М и диализатора с раствором липосом.
Для изучения характеристик адсорбции винпоцетина на поверхности липосом был использован метод равновесного диализа. Выбор данного метода обусловлен тем, что количественный анализ равновесной концентрации винпоцетина в дисперсионной среде, необходимый для определения величины адсорбции, затруднен присутствием дисперсной фазы - липосом. Полупроницаемая мембрана, с диаметром пор, достаточным для проникновения молекул винпоцетина, но не пропускающая липосомы, позволяет получить раствор винпоцетина с концентрацией, достаточно близкой к концентрации в дисперсионной среде липосом. Получаемый таким образом раствор может быть подвергнут количественному анализу с использованием спектрофотометрии.
Липосомы из соевого лецитина получали методом гидратации/регидратации.
Пример.
Приготовление образцов липосом из соевого лецитина
Для получения липосом из соевого лецитина был использован метод гидратации/регидратации. Раствор соевого лецитина (Sigma) в этиловом спирте испаряли в роторном испарителе при температуре 45°С и давлении -0,085 МПа. Затем добавляли раствор кислоты хлористоводородной 0,01 М (рН=2,0). Для получения липосом растворы были подвержены облучению на ультразвуковом дезинтеграторе в течение 15 минут. Далее липосомы были отфильтрованы через стеклянный фильтр с диаметром пор 16 мкм.
Приготовление рабочего стандартного образца (РСО) винпоцетина
Точную навеску винпоцетина 12 мг растворяли в водном растворе кислоты хлористоводородной 0,01 М в мерной колбе объемом 50,00 мл и доводили растворителем до метки.
Определение массовой доли коллоидного раствора липосом
В сушильном шкафу при температуре 80°С высушивали чашку Петри и производили ее взвешивание на аналитических весах Radwag 220/С/2 с точностью до 4-го знака после десятичной запятой в граммах. В чашку Петри помещали коллоидный раствор липосом и взвешивали. Далее чашку Петри с раствором липосом помещали в сушильный шкаф при температуре 80°С и высушивали ее содержимое до постоянной массы. Массовую долю коллоидного раствора липосом определяли по формуле:

где
mпуст. - масса пустой чашки Петри, г;
mжидк. - масса чашки Петри с коллоидным раствором, г;
mсух. - масса чашки Петри с сухим остатком коллоидного раствора, г.
Для проведения равновесного диализа использовались диализные пробирки Easy Dial-L с полупроницаемой мембраной с характеристикой пропускания 14 кДа. Для определения величины адсорбции винпоцетина липосомами проводился основной опыт (диализатор А), в котором наблюдалась адсорбция в процессе диализа, опыт сравнения (диализатор Б), в котором происходил диализ, но отсутствовали липосомы и опыт для измерения содержания свободного лецитина в дисперсионной среде (диализатор В). В диализатор А помещали 12 мл раствора липосом и диализную пробирку. В диализную пробирку помещали 3 мл раствора винпоцетина с концентрацией С0. В диализатор Б помещали 12 мл 0,01 М раствора кислоты хлористоводородной 0,01 М и диализную пробирку. В диализную пробирку помещали 3 мл раствора винпоцетина с концентрацией С0. В диализатор В помещали 12 мл раствора липосом и диализную пробирку. В диализную пробирку помещали 3 мл раствора кислоты хлористоводородной 0,01 М. Диализ проводили в термостате при температуре 37°С в течение 12 ч. После этого измеряли оптическую плотность при длине волны 313 нм растворов из диализных пробирок в диализаторах А, Б и В (DА, DБ и DВ соответственно). Для определения концентрации винпоцетина в диализной пробирке А использовалась разница оптических плотностей D=DА-DВ.
Расчет молярной концентрации винпоцетина по результатам спектрофотометрии производился по формуле:

где
 - коэффициент молярного поглощения винпоцетина, М-1 см-1;
- коэффициент молярного поглощения винпоцетина, М-1 см-1;
D - оптическая плотность;
1 - толщина кюветы, см.
С использованием приведенной формулы определялась концентрация винпоцетина в диализной пробирке А (основной опыт) и Б (опыт сравнения). Для данных концентраций были введены обозначения СА и СБ соответственно.
Величина адсорбции винпоцетина определялась по формуле:

где
А - величина адсорбции винпоцетина липосомами, моль/кг;
СА и СБ - равновесные концентрации винпоцетина в диализных пробирках для основного опыта и опыта сравнения, моль/л;
V - суммарный объем жидкости в диализаторе, мл;
m - масса липосом в диализаторе, кг.
Массу липосом в диализаторе определяли с учетом их массовой доли в коллоидном растворе и объема данного раствора по формуле:

где
ω% - массовая доля коллоидного раствора липосом, %
Vлип. - объем раствора липосом, помещенный в диализатор, мл;
m - масса липосом, кг.
Для определения характеристик адсорбции винпоцетина на липосомах была приготовлена серия растворов винпоцетина с различными концентрациями и проводился диализ по приведенной выше методике.
На фиг. 1 приведены равновесные концентраций винпоцетина в диализаторах А и Б, которые рассчитывались с использованием коэффициента молярного поглощения.
На фиг. 2 приведены результаты расчета величины адсорбции винпоцетина на липосомах.
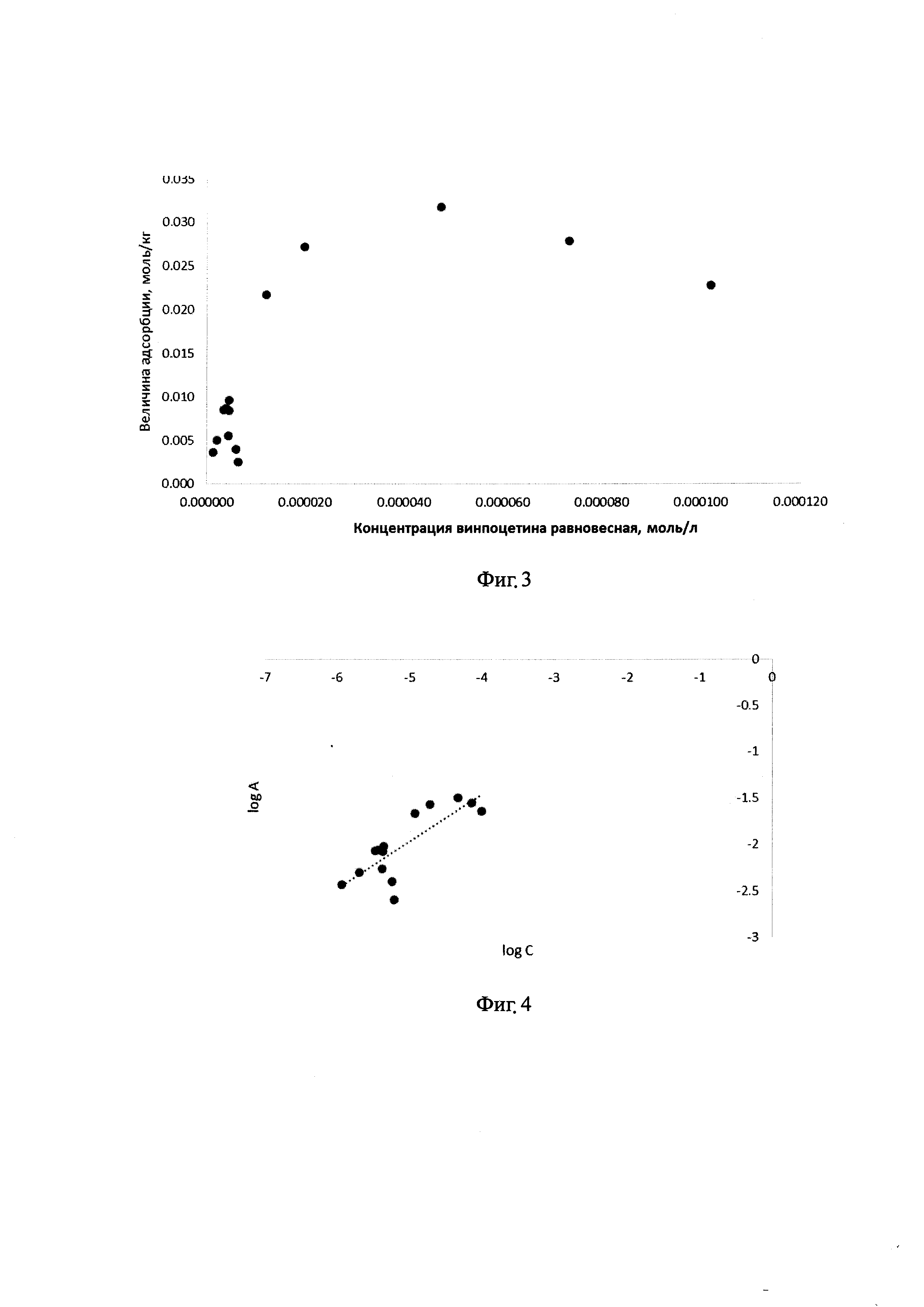
На фиг. 3, 4 - изображена зависимость величины адсорбции винпоцетина на липосомах от равновесной концентрации.
На фиг 5. приведены результаты определения характеристик адсорбции винпоцетина на липосомах.
При повышении концентрации винпоцетина величина адсорбции возрастает и достигает максимума в районе 0,030-0,035 моль/кг.
По величинам адсорбции винпоцетина на липосомах были определены константы уравнений Фрейндлиха и Ленгмюра:


где
А - величина адсорбции, моль/кг,
С - концентрация адсорбтива, моль/л,
k - константа уравнения Фрейндлиха, моль/кг,
1/n - константа уравнения Фрейндлиха,
A∞ - предельная адсорбция, моль/кг,
b - концентрация адсорбтива, при которой достигается половина предельной адсорбции, моль/л.
Для определения констант уравнения Фрейндлиха был построен график зависимости величины адсорбции от равновесной концентрации винпоцетина в логарифмических координатах и определены коэффициенты уравнения линейной зависимости методом наименьших квадратов, показанные на фиг. 4.
Для полученной зависимости были определены коэффициенты линейной регрессии
log А=(0,505919±0,108038364)* log С+(0,558169262±0,551738074).
Коэффициент 1/n=0,505919±0,108038364.
Коэффициент k=10(0,558169262±0,551738074).
Для оценки погрешности коэффициента k воспользуемся формулой связывающей погрешность функции с погрешностью ее аргумента

Для расчета коэффициента k используется показательная функция, таким образом, расчет погрешности данной константы можно выполнить по формуле

Таким образом, получаем коэффициент k=3,615507457±1.163161619 моль/кг.
Для определения констант уравнения Ленгмюра методом наименьших квадратов был найден свободный член уравнения линейной регрессии равный 1/А∞=81,30940761±36,26474441.
Для оценки погрешности коэффициента А∞ воспользуемся формулой связывающей погрешность функции с погрешностью ее аргумента

тогда погрешность 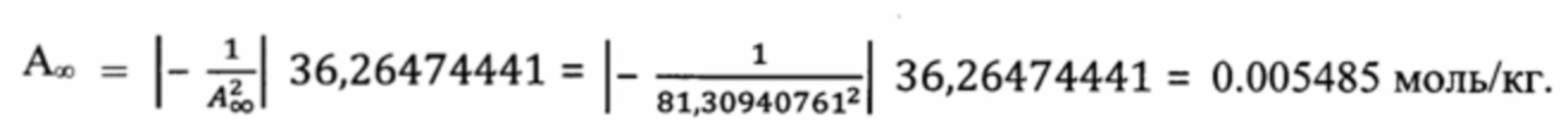
Предельная адсорбция А∞=(1/81,30940761)±0,005485=0,0122987±0,005485 моль/кг.
Для определения константы b уравнения Ленгмюра величина 1/А∞ удваивалась
2/А∞=162,6188152±72,52948882.
Константа b уравнения Ленгмюра (концентрация, при которой достигается половина предельной адсорбции) подтверждает достаточно эффективную адсорбцию винпоцетина липосомами при низкой концентрации.
Способ определения величины адсорбции винпоцетина липосомами, включающий количественное определение винпоцетина методом спектрофотометрии, отличающийся тем, что проводится диализ при температуре 37°С в течение 12 ч в диализаторе с 12 мл коллоидного раствора липосом с массовой долей липосом 0,1342±0,02881% из соевого лецитина или водным раствором кислоты хлористоводородной 0,01 М; куда помещается диализная пробирка, заполненная 3 мл водного раствора кислоты хлористо-водородной 0,01 М, содержащего винпоцетин в концентрации 0,24 мг/мл, для проведения диализа используется мембрана, характеристика пропускания которой 14 кДа; после достижения выравнивания концентрация винпоцетина измеряется в диализной пробирке, погруженной в диализатор с раствором липосом и диализатор, заполненный раствором кислоты хлористоводородной 0,01 М; определение величины адсорбции винпоцетина липосомами осуществляется по разности концентраций винпоцетина, вышедшего в диализную среду диализатора с водным раствором хлористоводородной 0,01 М кислоты и диализатора с раствором липосом.