Результат интеллектуальной деятельности: ЛИОФИЛИЗИРОВАННЫЕ КОМПОЗИЦИИ АНТИБАКТЕРИАЛЬНОГО БЕЛКА
Вид РИД
Изобретение
Настоящая заявка заявляет приоритет по первоначальной заявке США 62/277588, поданной 12 января 2016 года, которая включена посредством ссылки для всех целей, как если бы она была полностью изложена в данном документе.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Область изобретения
Настоящее изобретение относится к лиофилизированным композициям антибактериального белка, конкретнее антибактериального белка, специфичного по меньшей мере в отношении одного из или всех следующих видов: Staphylococcus arlettae, Staphylococcus aureus, Staphylococcus auricularis, Staphylococcus carnosus, Staphylococcus carprae, Staphylococcus chromogenes, Staphylococcus cohnii, Staphylococcus delphini, Staphylococcus epidermidis, Staphylococcus equorum, Staphylococcus gallinarum, Staphylococcus haemolyticus, Staphylococcus hominis, Staphylococcus intermedius, Staphylococcus kloosii, Staphylococcus lentus, Staphylococcus lugdunensis, Staphylococcus muscae, Staphylococcus pasteuri, Staphylococcus saprophyticus, Staphylococcus warneri и Staphylococcus xylosus.
Обсуждение родственной области
Бактериофаг представляет собой любой из целого ряда вирусоподобных микроорганизмов, которые инфицируют бактерии, и данный термин обычно используется в своей сокращенной форме, "фаг". Бактериофаг, обладающий способностью к уничтожению клеток, специфичный в отношении Staphylococcus aureus, был выделен и депонирован в корейской коллекции сельскохозяйственных культур (KACC), государственного института сельскохозяйственной биотехнологии (NIAB) 14 июня 2006 года (учетный номер: KACC 97001Р). Несмотря на то, что данный бактериофаг является эффективным в отношении предупреждения и лечения инфекций Staphylococcus aureus, применение этого бактериофага имеет некоторые недостатки.
Антибактериальный белок, обладающий способностью к уничтожению клеток Staphylococcus aureus, получали из данного бактериофага, и данный антибактериальный белок можно использовать для предупреждения и лечения заболевания, вызываемого Staphylococcus aureus. См., Патент США 8232370.
Кроме того, данный антибактериальный белок демонстрировал антибактериальную активность, специфичную ко всем следующим видам: Staphylococcus arlettae, Staphylococcus aureus, Staphylococcus auricularis, Staphylococcus carnosus, Staphylococcus carprae, Staphylococcus chromogenes, Staphylococcus cohnii, Staphylococcus delphini, Staphylococcus epidermidis, Staphylococcus equorum, Staphylococcus gallinarum, Staphylococcus haemolyticus, Staphylococcus hominis, Staphylococcus intermedius, Staphylococcus kloosii, Staphylococcus lentus, Staphylococcus lugdunensis, Staphylococcus muscae, Staphylococcus pasteuri, Staphylococcus saprophyticus, Staphylococcus warneri и Staphylococcus xylosus.
При получении фармацевтической композиции, содержащей антибактериальный белок, композиция должна быть изготовлена таким образом, чтобы активность антибактериального белка поддерживалась в течение соответствующего периода времени. Потеря активности или стабильности антибактериального белка может быть результатом химической или физической нестабильности белка, например, вследствие денатурации, агрегации или окисления. Композиция может таким образом быть фармацевтически неприемлемой. Применение эксципиентов, как известно, повышает стабильность биологически активного белка, но стабилизирующие эффекты данных эксципиентов непредсказуемы и сильно зависят от природы биологически активного белка и данных эксципиентов.
Остается потребность в композициях, содержащих антибактериальный белок в качестве активного ингредиента, и чтобы данные композиции были стабильными в течение соответствующего периода времени и подходящими для инъекции. Композиции будет полезны для введения при лечении заболевания, вызываемого бактериальной инфекцией.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Согласно настоящему изобретению предложена лиофилизированная композиция, включающая антибактериальный белок, обладающий способностью к уничтожению клеток, специфичной в отношении по меньшей мере одного из или всех следующих видов: Staphylococcus arlettae, Staphylococcus aureus, Staphylococcus auricularis, Staphylococcus carnosus, Staphylococcus carprae, Staphylococcus chromogenes, Staphylococcus cohnii, Staphylococcus delphini, Staphylococcus epidermidis, Staphylococcus equorum, Staphylococcus gallinarum, Staphylococcus haemolyticus, Staphylococcus hominis, Staphylococcus intermedius, Staphylococcus kloosii, Staphylococcus lentus, Staphylococcus lugdunensis, Staphylococcus muscae, Staphylococcus pasteuri, Staphylococcus saprophyticus, Staphylococcus warneri и Staphylococcus xylosus; полоксамер; сахар; и аминокислоту.
В одном из аспектов концентрация антибактериального белка в растворе перед лиофилизацией составляет от примерно 0,1 мг/мл до примерно 30 мг/мл.
В другом аспекте антибактериальный белок состоит из аминокислотной последовательности SEQ ID NO: 1.
В другом аспекте антибактериальный белок состоит из аминокислотной последовательности SEQ ID NO: 2.
В другом аспекте антибактериальный белок представляет собой смесь первого антибактериального белка, состоящего из аминокислотной последовательности SEQ ID NO: 1, и второго антибактериального белка, состоящего из аминокислотной последовательности SEQ ID NO: 2.
В другом аспекте антибактериальный белок включает 15-35 мол. % первого антибактериального белка и 65-85 мол. % второго антибактериального белка.
В другом аспекте антибактериальный белок включает 25 мол. % первого антибактериального белка и 75 мол. % второго антибактериального белка.
В другом аспекте концентрация полоксамера в растворе перед лиофилизацией составляет от примерно 0,1 г/л до примерно 10 г/л.
В другом аспекте полоксамер представляет собой полоксамер 188.
В другом аспекте сахар представляет собой D-сорбит.
В другом аспекте концентрация сахара в растворе перед лиофилизацией составляет от примерно 1 г/л до примерно 600 г/л.
В другом аспекте аминокислота представляет собой L-гистидин.
В другом аспекте концентрация аминокислоты в растворе перед лиофилизацией составляет от примерно 0,1 г/л до примерно 10 г/л.
Согласно настоящему изобретению предложена антибактериальная композиция, включающая антибактериальный белок, обладающий способностью к уничтожению клеток, специфичной в отношении по меньшей мере одного из или всех следующих видов: Staphylococcus arlettae, Staphylococcus aureus, Staphylococcus auricularis, Staphylococcus carnosus, Staphylococcus carprae, Staphylococcus chromogenes, Staphylococcus cohnii, Staphylococcus delphini, Staphylococcus epidermidis, Staphylococcus equorum, Staphylococcus gallinarum, Staphylococcus haemolyticus, Staphylococcus hominis, Staphylococcus intermedius, Staphylococcus kloosii, Staphylococcus lentus, Staphylococcus lugdunensis, Staphylococcus muscae, Staphylococcus pasteuri, Staphylococcus saprophyticus, Staphylococcus warneri и Staphylococcus xylosus; полоксамер; сахар; аминокислоту и воду. Антибактериальный белок состоит из аминокислотной последовательности SEQ ID NO: 1, и концентрация антибактериального белка составляет от примерно 0,1 мг/мл до примерно 30 мг/мл.
Согласно настоящему изобретению предложена антибактериальная композиция, включающая антибактериальный белок, обладающий способностью к уничтожению клеток, специфичной в отношении по меньшей мере одного из или всех следующих видов: Staphylococcus arlettae, Staphylococcus aureus, Staphylococcus auricularis, Staphylococcus carnosus, Staphylococcus carprae, Staphylococcus chromogenes, Staphylococcus cohnii, Staphylococcus delphini, Staphylococcus epidermidis, Staphylococcus equorum, Staphylococcus gallinarum, Staphylococcus haemolyticus, Staphylococcus hominis, Staphylococcus intermedius, Staphylococcus kloosii, Staphylococcus lentus, Staphylococcus lugdunensis, Staphylococcus muscae, Staphylococcus pasteuri, Staphylococcus saprophyticus, Staphylococcus warneri и Staphylococcus xylosus; полоксамер; сахар; аминокислоту и воду. Антибактериальный белок состоит из аминокислотной последовательности SEQ ID NO: 2, и концентрация антибактериального белка составляет от примерно 0,1 мг/мл до примерно 30 мг/мл.
Согласно настоящему изобретению предложена антибактериальная композиция, включающая антибактериальный белок, обладающий способностью к уничтожению клеток, специфичной в отношении по меньшей мере одного из или всех следующих видов: Staphylococcus arlettae, Staphylococcus aureus, Staphylococcus auricularis, Staphylococcus carnosus, Staphylococcus carprae, Staphylococcus chromogenes, Staphylococcus cohnii, Staphylococcus delphini, Staphylococcus epidermidis, Staphylococcus equorum, Staphylococcus gallinarum, Staphylococcus haemolyticus, Staphylococcus hominis, Staphylococcus intermedius, Staphylococcus kloosii, Staphylococcus lentus, Staphylococcus lugdunensis, Staphylococcus muscae, Staphylococcus pasteuri, Staphylococcus saprophyticus, Staphylococcus warneri и Staphylococcus xylosus; полоксамер; сахар; аминокислоту и воду. Антибактериальный белок включает первый антибактериальный белок, состоящий из аминокислотной последовательности SEQ ID NO: 1, и второй антибактериальный белок, состоящий из аминокислотной последовательности SEQ ID NO: 2, и концентрация антибактериального белка составляет от примерно 0,1 мг/мл до примерно 30 мг/мл.
В одном из аспектов антибактериальный белок включает 15-35 мол. % первого антибактериального белка и 65-85 мол. % второго антибактериального белка.
В другом аспекте антибактериальный белок включает 25 мол. % первого антибактериального белка и 75 мол. % второго антибактериального белка.
В другом аспекте полоксамер представляет собой полоксамер 188. В другом аспекте концентрация полоксамера составляет от примерно 0,1 г/л до примерно 10 г/л.
В другом аспекте сахар представляет собой D-сорбит.
В другом аспекте концентрация сахара составляет от примерно 1 г/л до примерно 600 г/л.
В другом аспекте аминокислота представляет собой L-гистидин. В другом аспекте концентрация аминокислоты составляет от примерно 0,1 г/л до примерно 10 г/л.
Согласно настоящей заявке предложен способ изготовления лиофилизированной композиции, включающий образование смеси, состоящей из антибактериального белка, обладающего киллинговой активностью, специфичной к по меньшей мере одному из или всем следующим видам: Staphylococcus arlettae, Staphylococcus aureus, Staphylococcus auricularis, Staphylococcus carnosus, Staphylococcus carprae, Staphylococcus chromogenes, Staphylococcus cohnii, Staphylococcus delphini, Staphylococcus epidermidis, Staphylococcus equorum, Staphylococcus gallinarum, Staphylococcus haemolyticus, Staphylococcus hominis, Staphylococcus intermedius, Staphylococcus kloosii, Staphylococcus lentus, Staphylococcus lugdunensis, Staphylococcus muscae, Staphylococcus pasteuri, Staphylococcus saprophyticus, Staphylococcus warneri и Staphylococcus xylosus; полоксамера; сахара и аминокислоты, и подвергание данной смеси лиофилизации.
В одном из аспектов концентрация антибактериального белка в смеси перед лиофилизацией составляет примерно от 0,1 мг/мл до 30 мг/мл.
В другом аспекте антибактериальный белок состоит из аминокислотной последовательности SEQ ID NO: 1.
В другом аспекте антибактериальный белок состоит из аминокислотной последовательности SEQ ID NO: 2.
В другом аспекте антибактериальный белок представляет собой смесь первого антибактериального белка, состоящего из аминокислотной последовательности SEQ ID NO: 1, и второго антибактериального белка, состоящего из аминокислотной последовательности SEQ ID NO: 2.
В другом аспекте антибактериальный белок включает 15-35 мол. % первого антибактериального белка и 65-85 мол. % второго антибактериального белка.
В другом аспекте антибактериальный белок включает 25 мол. % первого антибактериального белка и 75 мол. % второго антибактериального белка.
В другом аспекте концентрация полоксамера в смеси перед лиофилизацией составляет от примерно 0,1 г/л до примерно 10 г/л.
В другом аспекте полоксамер представляет собой полоксамер 188. В другом аспекте сахар представляет собой D-сорбит.
В другом аспекте концентрация сахара в смеси перед лиофилизацией составляет от примерно 1 г/л до примерно 600 г/л.
В другом аспекте аминокислота представляет собой L-гистидин.
В другом аспекте концентрация аминокислоты в смеси перед лиофилизацией составляет от примерно 0,1 г/л до примерно 10 г/л.
Следует понимать, что как приведенное выше общее описание, так и последующее подробное описание приведены в качестве примера и являются пояснительными и предназначены для обеспечения дополнительного объяснения заявленного изобретения.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Сопровождающие графические материалы, которые включены для обеспечения дополнительного понимания изобретения и включены в и составляют часть данного описания, иллюстрируют воплощения изобретения и совместно с описанием служат для объяснения принципов данного изобретения. В графических материалах:
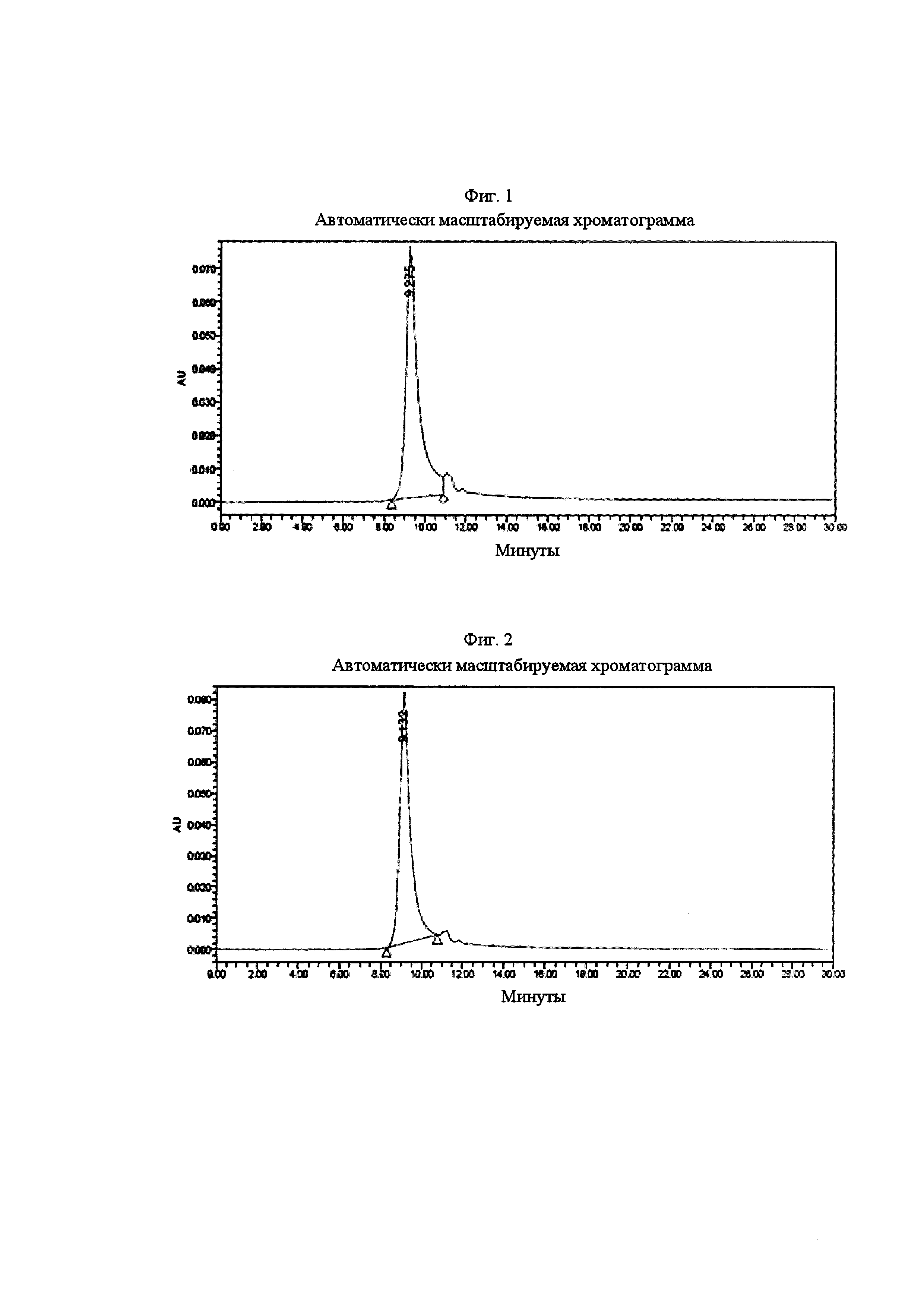
Фиг. 1 представляет собой результат эксклюзионной высокоэффективной жидкостной хроматографии, анализируемой в момент времени ноль для лиофилизированной композиции.
Фиг. 2 представляет собой результат эксклюзионной высокоэффективной жидкостной хроматографии, анализируемой спустя 1 месяц хранения лиофилизированной композиции.
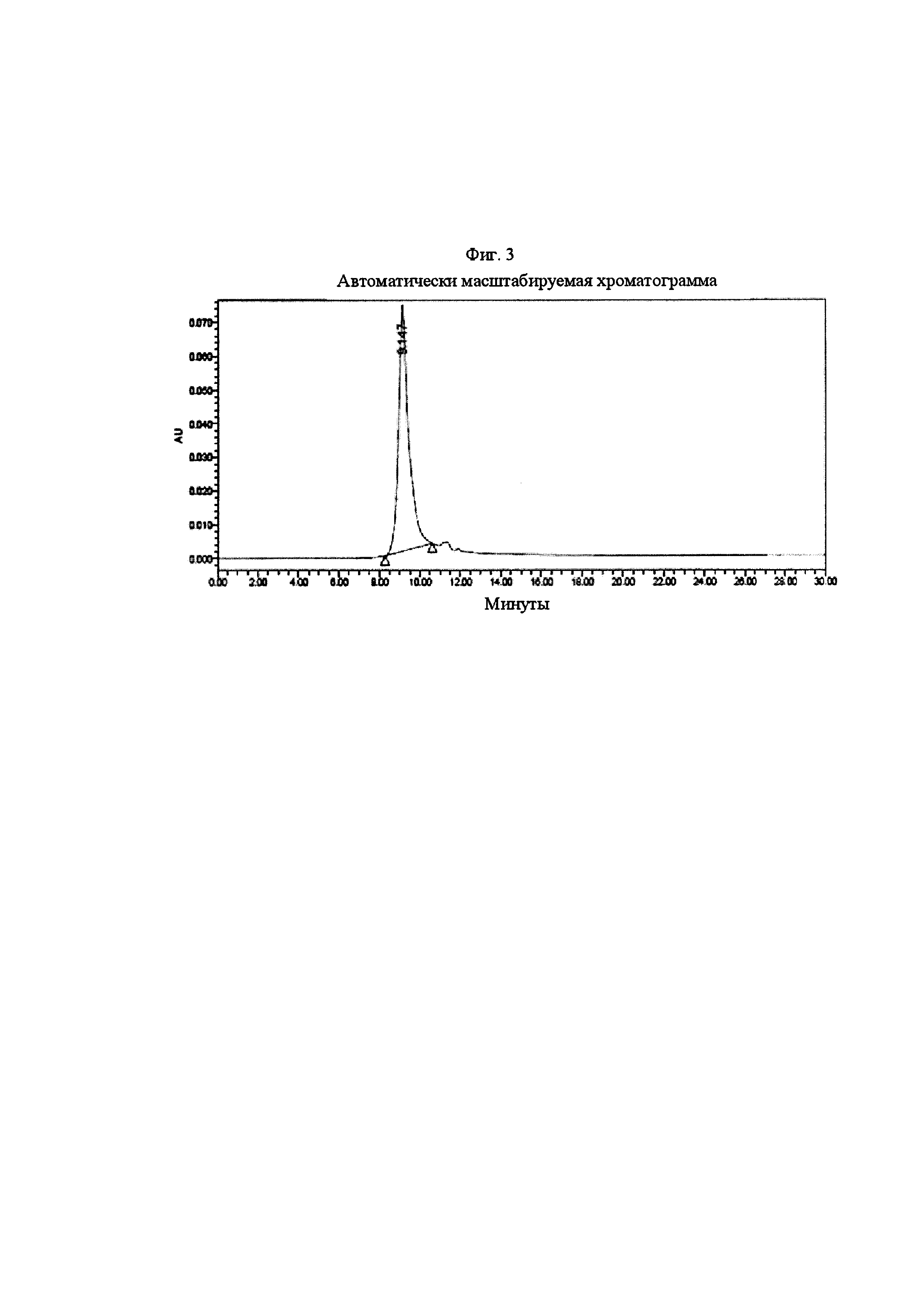
Фиг. 3 представляет собой результат эксклюзионной высокоэффективной жидкостной хроматографии, анализируемой спустя 6 месяцев хранения лиофилизированной композиции.
ПОДРОБНОЕ ОПИСАНИЕ ПРОИЛЛЮСТРИРОВАННЫХ ВОПЛОЩЕНИЙ
Сейчас подробно будет сделана ссылка на воплощения настоящего изобретения, пример которых проиллюстрирован в сопровождающих графических материалах.
Используемое здесь выражение "по меньшей мере один из или все следующие виды стафилококка" означает любой один, два, три, четыре, пять, шесть … вплоть до двадцати двух видов стафилококка, выбранных из группы, состоящей из Staphylococcus arlettae, Staphylococcus aureus, Staphylococcus auricularis, Staphylococcus carnosus, Staphylococcus carprae, Staphylococcus chromogenes, Staphylococcus cohnii, Staphylococcus delphini, Staphylococcus epidermidis, Staphylococcus equorum, Staphylococcus gallinarum, Staphylococcus haemolyticus, Staphylococcus hominis, Staphylococcus intermedius, Staphylococcus kloosii, Staphylococcus lentus, Staphylococcus lugdunensis, Staphylococcus muscae, Staphylococcus pasteuri, Staphylococcus saprophyticus, Staphylococcus warneri и Staphylococcus xylosus.
Известно, что белки являются относительно нестабильными в водном состоянии и подвергаются химической и физической деградации, приводящей к потере биологической активности во время обработки и хранения. Лиофилизация (известная также как лиофильная сушка) представляет собой способ защиты белков во время хранения.
Лиофилизированная композиция включает антибактериальный белок, обладающий способностью к уничтожению клеток, специфичной в отношении по меньшей мере одного из или всех следующих видов: Staphylococcus arlettae, Staphylococcus aureus, Staphylococcus auricularis, Staphylococcus carnosus, Staphylococcus carprae, Staphylococcus chromogenes, Staphylococcus cohnii, Staphylococcus delphini, Staphylococcus epidermidis, Staphylococcus equorum, Staphylococcus gallinarum, Staphylococcus haemolyticus, Staphylococcus hominis, Staphylococcus intermedius, Staphylococcus kloosii, Staphylococcus lentus, Staphylococcus lugdunensis, Staphylococcus muscae, Staphylococcus pasteuri, Staphylococcus saprophyticus, Staphylococcus warneri и Staphylococcus xylosus; полоксамер; сахар и аминокислоту.
Способ производства лиофилизированной композиции включает образование смеси, состоящей из антибактериального белка, обладающего способностью к уничтожению клеток, специфичной к по меньшей мере одному из или всем следующим видам: Staphylococcus arlettae, Staphylococcus aureus, Staphylococcus auricularis, Staphylococcus carnosus, Staphylococcus carprae, Staphylococcus chromogenes, Staphylococcus cohnii, Staphylococcus delphini, Staphylococcus epidermidis, Staphylococcus equorum, Staphylococcus gallinarum, Staphylococcus haemolyticus, Staphylococcus hominis, Staphylococcus intermedius, Staphylococcus kloosii, Staphylococcus lentus, Staphylococcus lugdunensis, Staphylococcus muscae, Staphylococcus pasteuri, Staphylococcus saprophyticus, Staphylococcus warneri и Staphylococcus xylosus; полоксамера; сахара и аминокислоты, и подвергание данной смеси лиофилизации.
Концентрация антибактериального белка в растворе перед лиофилизацией может составлять от примерно 0,1 мг/мл до примерно 30 мг/мл, от 0,1 мг/мл до 30 мг/мл, от 0,5 мг/мл до 30 мг/мл, от 1,0 мг/мл до 30 мг/мл, от 1,5 мг/мл до 30 мг/мл, от 5 мг/мл до 30 мг/мл, от 0,1 мг/мл до 25 мг/мл, от 0,1 мг/мл до 20 мг/мл, от 0,5 мг/мл до 25 мг/мл, от 0,5 мг/мл до 20 мг/мл или от 1,0 мг/мл до 20 мг/мл.
Антибактериальный белок состоит из аминокислотной последовательности SEQ ID NO: 1, состоит из аминокислотной последовательности SEQ ID NO: 2 или представляет собой смесь первого антибактериального белка, состоящего из аминокислотной последовательности SEQ ID NO: 1, и второго антибактериального белка, состоящего из аминокислотной последовательности SEQ ID NO: 2.
Когда антибактериальный белок представляет собой смесь первого антибактериального белка и второго антибактериального белка, антибактериальный белок может включать 15-35 мол. % первого антибактериального белка и 65-85 мол. % второго антибактериального белка. Например, антибактериальный белок включает 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34 или 35 мол. % первого антибактериального белка и 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84 или 85 мол. % второго антибактериального белка.
Полоксамеры представляют собой неионные триблоксополимеры, состоящие из центральной гидрофобной цепи полиоксипропилена (поли(пропиленоксида)) и двух гидрофильных цепей полиоксиэтилена (поли(этиленоксида)). Концентрация полоксамера в растворе перед лиофилизацией может составлять от примерно 0,1 г/л до примерно 10 г/л, от 0,1 г/л до 10 г/л, от 0,2 г/л до 10 г/л, от 0,1 г/л до 8 г/л, от 0,2 г/л до 8 г/л, от 0,1 г/л до 6 г/л или от 0,2 г/л до 6 г/л. Предпочтительно, полоксамер представляет собой полоксамер 188.
Предпочтительными сахарами, используемыми в лиофилизированной композиции, являются, например, D-сорбит, сахароза, глюкоза, лактоза, трегалоза, глицерин, этиленгликоль, маннит, ксилит и инозит. Более предпочтительно, сахаром является D-сорбит. Концентрация сахара в растворе перед лиофилизацией может составлять от примерно 1 г/л до примерно 600 г/л, от 1 г/л до 600 г/л, от 5 г/л до 600 г/л, от 1 г/л до 500 г/л, от 5 г/л до 500 г/л, от 1 г/л до 400 г/л или от 5 г/л до 400 г/л.
Предпочтительными аминокислотами, используемыми в лиофилизированной композиции, являются, например, L-гистидин, L-глицин и L-аргинин. Более предпочтительно, аминокислотой является L-гистидин. Концентрация аминокислоты в растворе перед лиофилизацией может составлять от примерно 0,1 г/л до примерно 10 г/л, от 0,1 г/л до 10 г/л, от 0,5 г/л до 10 г/л, от 0,1 г/л до 8 г/л, от 0,5 г/л до 8 г/л, от 0,1 г/л до 6 г/л или от 0,5 г/л до 6 г/л.
Антибактериальные композиции включают антибактериальный белок, обладающий способностью к уничтожению клеток, специфичной к по меньшей мере одному из или всем следующим видам: Staphylococcus arlettae, Staphylococcus aureus, Staphylococcus auricularis, Staphylococcus carnosus, Staphylococcus carprae, Staphylococcus chromogenes, Staphylococcus cohnii, Staphylococcus delphini, Staphylococcus epidermidis, Staphylococcus equorum, Staphylococcus gallinarum, Staphylococcus haemolyticus, Staphylococcus hominis, Staphylococcus intermedius, Staphylococcus kloosii, Staphylococcus lentus, Staphylococcus lugdunensis, Staphylococcus muscae, Staphylococcus pasteuri, Staphylococcus saprophyticus, Staphylococcus warneri и Staphylococcus xylosus; полоксамер; сахар; аминокислоту и воду. Антибактериальный белок состоит из аминокислотной последовательности SEQ ID NO: 1, состоит из аминокислотной последовательности SEQ ID NO: 2 или включает первый антибактериальный белок, состоящий из аминокислотной последовательности SEQ ID NO: 1, и второй антибактериальный белок, состоящий из аминокислотной последовательности SEQ ID NO: 2.
Концентрация антибактериального белка в антибактериальной композиции может составлять от примерно 0,1 мг/мл до примерно 30 мг/мл, от 0,1 мг/мл до 30 мг/мл, от 0,5 мг/мл до 30 мг/мл, от 1,0 мг/мл до 30 мг/мл, от 1,5 мг/мл до 30 мг/мл, от 5 мг/мл до 30 мг/мл, от 0,1 мг/мл до 25 мг/мл, от 0,1 мг/мл до 20 мг/мл, от 0,5 мг/мл до 25 мг/мл, от 0,5 мг/мл до 20 мг/мл или от 1,0 мг/мл до 20 мг/мл.
Когда антибактериальный белок представляет собой смесь первого антибактериального белка и второго антибактериального белка, антибактериальный белок может включать 15-35 мол. % первого антибактериального белка и 65-85 мол. % второго антибактериального белка. Например, антибактериальный белок включает 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34 или 35 мол. % первого антибактериального белка и 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84 или 85 мол. % второго антибактериального белка.
Концентрация полоксамера в антибактериальной композиции может составлять от примерно 0,1 г/л до примерно 10 г/л, от 0,1 г/л до 10 г/л, от 0,2 г/л до 10 г/л, от 0,1 г/л до 8 г/л, от 0,2 г/л до 8 г/л, от 0,1 г/л до 6 г/л или от 0,2 г/л до 6 г/л. Предпочтительно, полоксамер представляет собой полоксамер 188.
Предпочтительными сахарами, используемыми в антибактериальной композиции, являются, например, D-сорбит, сахароза, глюкоза, лактоза, трегалоза, глицерин, этиленгликоль, маннит, ксилит и инозит. Концентрация сахара в антибактериальной композиции может составлять от примерно 1 г/л до примерно 600 г/л, от 1 г/л до 600 г/л, от 5 г/л до 600 г/л, от 1 г/л до 500 г/л, от 5 г/л до 500 г/л, от 1 г/л до 400 г/л или от 5 г/л до 400 г/л.
Предпочтительные аминокислоты, используемые в антибактериальной композиции, представляют собой, например, L-гистидин, L-глицин и L-аргинин. Более предпочтительно, аминокислота представляет собой L-гистидин. Концентрация аминокислоты в антибактериальной композиции может составлять от примерно 0,1 г/л до примерно 10 г/л, от 0,1 г/л до 10 г/л, от 0,5 г/л до 10 г/л, 0,1 г/л до 8 г/л, от 0,5 г/л до 8 г/л, от 0,1 г/л до 6 г/л или от 0,5 г/л до 6 г/л.
Способ изготовления лиофилизированной композиции включает образование смеси, состоящей из антибактериального белка, обладающего способностью к уничтожению клеток, специфичной к по меньшей мере одному из или всем следующим видам: Staphylococcus arlettae, Staphylococcus aureus, Staphylococcus auricularis, Staphylococcus carnosus, Staphylococcus carprae, Staphylococcus chromogenes, Staphylococcus cohnii, Staphylococcus delphini, Staphylococcus epidermidis, Staphylococcus equorum, Staphylococcus gallinarum, Staphylococcus haemolyticus, Staphylococcus hominis, Staphylococcus intermedius, Staphylococcus kloosii, Staphylococcus lentus, Staphylococcus lugdunensis, Staphylococcus muscae, Staphylococcus pasteuri, Staphylococcus saprophyticus, Staphylococcus warneri и Staphylococcus xylosus; полоксамера; сахара и аминокислоты, и подвергание данной смеси лиофилизации.
Практические и в настоящее время предпочтительные воплощения настоящего изобретения являются иллюстративными, как показано в следующих примерах.
Однако, понятно, что специалисты в данной области, на основании данного описания могут осуществить модификации и улучшения в пределах сущности и объема настоящего изобретения.
Пример 1: Получение антибактериального белка
Экспрессионную плазмиду антибактериального белка по настоящему изобретению конструировали посредством общепринятого субклонирования гена, кодирующего антибактериальный белок по настоящему изобретению, который представлен SEQ ID NO: 3, в вектор pBAD-TOPO (Invitrogen). Клетку Escherichia coli BL21, трансформированную полученной плазмидой, использовали в качестве хозяина-продуцента антибактериального белка по настоящему изобретению.
Экспрессию антибактериального белка по настоящему изобретению индуцировали 0,2% арабинозой при оптической плотности при 600 нм (OD600) 2,0, и индуцированные бактериальные клетки затем инкубировали в течение еще 10 часов при 19°С. Бактериальные клетки выделяли посредством центрифугирования (6000×g в течение 20 минут), и полученный осадок клеток ресуспендировали в лизирующем буфере [50 мМ Na2HPO4 (pH 7,5), 10 мМ этилендиаминтетрауксусная кислота (EDTA), 1 мМ дитиотреитол (DTT)] и разрушали с использованием традиционной ультразвуковой обработки в течение 5 минут (импульс 1 секунда с перерывом между импульсами 3 секунды). После центрифугирования (13000×g в течение 20 минут) супернатант выделяли и подвергали двухстадийной хроматографии, включающей ионообменную хроматографию (колонка быстрого потока SP; GE Healthcare) и хроматографию гидрофобного взаимодействия (колонка Toyopearl PPG-600M; Tosoh Bioscience).
Для большей информативности, полученного хозяина-продуцента инокулировали в среду TSB (триптиказо-соевый бульон) (гидролизат казеина, 17 г/л; гидролизат сои, 3 г/л; декстроза, 2,5 г/л; NaCl, 5 г/л; гидроортофосфат калия, 2,5 г/л) и инкубировали при 37°С. Когда концентрация клеток достигала 2,0 OD600, добавляли L-арабинозу в конечной концентрации 0,2% для индукции экспрессии антибактериального белка. Клетки культивировали при 19°С в течение еще 10 часов с момента индукции. Культуральный бульон центрифугировали при 6000×g в течение 20 минут с получением клеточного осадка. Осадок суспендировали в 50 мМ буфере Na2HPO4 (рН 7,5), содержащем 10 мМ EDTA и 1 мМ DTT (10 мл буфера на 1 г клеток). Клетки в суспензии разрушали посредством общепринятой обработки ультразвуком. Клеточный лизат центрифугировали при 13000×g в течение 20 минут для удаления клеточного дебриса. Супернатант подвергали двухстадийной хроматографии, включая ионообменную хроматографию (Буфер А: 25 мМ Na2HPO4 (рН 7,5), 10 мМ EDTA; Буфер В: 25 мМ Na2HPO4 (рН 7,5), 10 мМ EDTA, 1 М NaCl; Буфер С: 25 мМ Na2HPO4 (рН 7,5), 10 мМ EDTA, 50 мМ NaCl, 0,5% Triton Х-100; Процедура: загрузка образца → 1,6 CV (объем колонки) буфера А → 30 CV буфера С → 20 CV буфера А → 5 CV 22% буфера В → градиентное элюирование (20 CV 22-100% буфера В)) и хроматографию гидрофобного взаимодействия (Буфер А: 10 мМ L-гистидин (рН 7,5), 1 М NaCl; Буфер В: 10 мМ L-гистидин (рН 7,5), 1 М мочевина; Процедура: загрузка образца (образец, очищенный посредством ионообменной хроматографии) → 10 CV буфера А → градиентное элюирование (10 CV 0-100% буфера В)). Раствор белка затем фильтровали с помощью 0,2 мкм фильтра.
Для определения состава антибактериальных белков, состоящих из аминокислотной последовательности SEQ ID NO: 1 и SEQ ID NO: 2, проводили двухстадийный анализ. Сначала, жидкостную хроматографию (LC)-Macc спектрометрию (MS) осуществляли с использованием образца белка, обработанного протеазой. Раствор белка, полученный согласно способу, описанному выше, подвергали замене буфера через фильтрование на центрифуге в 50 мМ буфера Tris-HCl (рН 7,6) и разбавляли до концентрации 2,5 мг/мл 6 М раствором мочевины. Разбавленный раствор белка подвергали обработке протеазой. В качестве протеазы использовали модифицированную свиную Glu-C протеазу со степенью чистоты для секвенирования (Promega, Madison, WI, США), и обработку протеазой проводили в соответствии с протоколом производителя. После обработки протеазой раствор белка, обработанный протеазой, подвергали обращенно-фазовой HPLC (высокоэффективная жидкостная хроматография) и Q-TOF-MS (квадрупольная-времяпролетная масс-спектрометрия). Посредством анализа пиков, пики HPLC и MS, соответствующие пептидному фрагменту MAKTQAE, происходящему из антибактериального белка, состоящего из аминокислотной последовательности SEQ ID NO: 1, и пептидному фрагменту AKTQAE, происходящему из антибактериального белка, состоящего из аминокислотной последовательности SEQ ID NO: 2, идентифицировали на основе оцениваемой картины протеазного расщепления и расчетов массы. Дополнительно, пики HPLC и MS подтверждали сравнением профиля пиков, полученного при использовании в качестве образцов химически синтезированных пептидов (MAKTQAE и AKTQAE). Затем, долю в составе антибактериального белка, состоящего из аминокислотной последовательности SEQ ID NO: 1, в композиции антибактериального белка определяли посредством анализа обращенно-фазовой HPLC с образцом белка, обработанным протеазой, и химически синтезированными пептидами (MAKTQAE и AKTQAE) на основе корреляции концентрации пептида с соответствующей ей площадью пика. В результате анализа с тремя партиями антибактериального белка определяли, что доля в составе антибактериального белка, состоящего из аминокислотной последовательности SEQ ID NO: 1, составляла 25, 27 и 29 мол. %.
Пример 2: Получение фармацевтической композиции с лиофилизированной композицией
Фармацевтическую композицию для лечения стафилококковых инфекций, содержащую антибактериальные белки по настоящему изобретению, получали посредством лиофилизации. Получали лиофилизированную композицию, имеющую следующий состав:

Способ изготовления заключается в замене буфера раствора белка, полученного в Примере 1, на буфер, содержащий указанные ингредиенты, концентрировании полученного раствора, регулировании концентрации антибактериального белка в растворе, фильтровании раствора с отрегулированной концентрацией и лиофилизировании фильтрата.
Описание каждой стадии способа приведено ниже:
Замена буфера раствора белка, полученного в Примере 1, на буфер (1,56 г/л L-гистидина (рН 6,0), 50 г/л D-сорбита, 1,47 г/л CaCl2⋅Н2О и 1 г/л полоксамера 188) с использованием стандартной диафильтрации.
Концентрирование полученного раствора с использованием центрифужного фильтра (10 K).
Регулирование концентрации антибактериального белка с помощью буфера (1,56 г/л L-гистидина (рН 6,0), 50 г/л D-сорбита, 1,47 г/л CaCl2⋅Н2О и 1 г/л полоксамера 188) с получением 18 мг/мл, исходя из концентрации белка, определенной традиционным анализом на основе бицинхониновой кислоты (ВСА).
Фильтрование раствора с отрегулированной концентрацией с использованием 0,2 мкм фильтра.
Добавление 1 мл фильтрованного раствора в 3 мл стеклянную пробирку и помещение наполненной пробирки в планшет из нержавеющей стали.
Загрузка планшета в лиофилизатор и лиофилизация продукта с использованием следующего цикла лиофилизации:
Уравновешивание при 4°С в течение примерно 20 минут.
Доведение температуры полки до -40°С и поддержание в течение 12 часов.
Доведение температуры в конденсаторе до -50°С.
Вакуумирование камеры.
При достижении вакуумом значения 1500 мторр, повышение температуры полки вплоть до -20°С и поддержание в течение 16 часов.
Повышение температуры полки вплоть до 20°С в режиме повышения на 10°С в 1 час и поддержание в течение 4 часов.
Снятие вакуума.
Закупоривание и герметизация закупоренных пробирок соответствующими съемными обжимными колпачками.
Лиофилизированную композицию хранили при 4°С и тестировали на стабильность и биологическую активность, как указано ниже. Перед анализом композиции ее растворяли с использованием воды для инъекции (0,92 мл). Стабильность определяли с использованием эксклюзионной высокоэффективной жидкостной хроматографии (SEC-HPLC). SEC-HPLC осуществляли с помощью колонки BioSep™-SEC-S 2000 (Phenomenex, Torrance, СА). Подвижную фазу (10 мМ Tris, 0,5 М NaCl, 1 М мочевина, рН 7,5) наносили при скорости потока 1,0 мл/мин. Инъецировали 50 мкл образца, и за элюированием образца наблюдали в течение 30 мин посредством измерения поглощения при 280 нм. Результаты показаны на Фиг. 1-3.
Биологическую активность оценивали с использованием анализа уменьшения помутнения. Анализ уменьшения помутнения осуществляли следующим образом: образец добавляли к суспензии штамма Staphylococcus aureus АТСС 33591 (CD600 равна 0,5) в 10 мМ фосфатно-солевом буферном растворе (PBS) (рН 7,2) до конечной концентрации антибактериального белка 0,1 мкг/мл. Изменения в плотности бактериальных клеток (CD600) записывали каждые 30 секунд в течение 15 минут. Из данного эксперимента получали TOD50 (полу-log падение в исходной концентрации жизнеспособных бактерий в минутах).
В Таблице 2 обобщены результаты аналитических тестов, связанные со стабильностью и биологической активностью композиции. Значения определяли в 4 контрольных точках: в момент времени ноль, спустя 1 месяц, 3 месяца и 6 месяцев хранения, при температуре хранения 4°С. В тесте на стабильность количество интактного белка в момент времени ноль рассматривали как 100%. В тесте на биологическую активность анализировали отличие от значения TOD50, определенного в момент времени ноль.
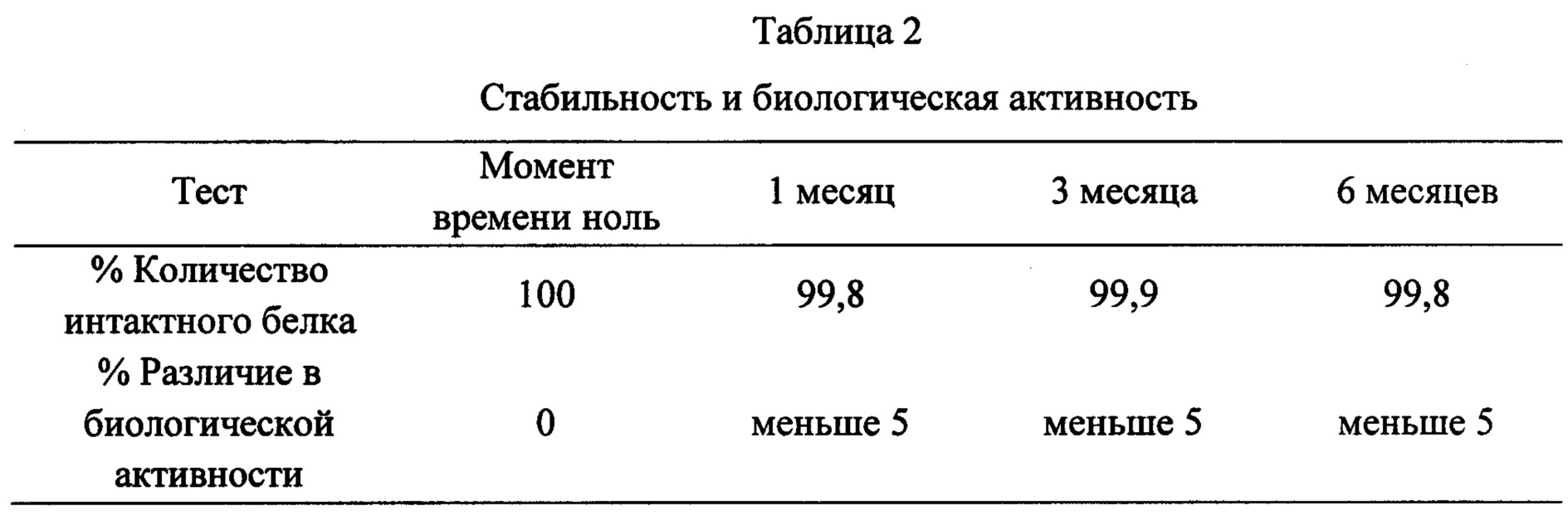
Из таблицы 2 можно сделать вывод о том, стабильность и биологическая активность лиофилизированной композиции по настоящему изобретению хорошо сохранялись после 6 месяцев хранения.
Пример 3: Сравнение лиофилизированной композиции и жидкой композиции Биологическую активность лиофилизированной композиции и жидкой композиции сравнивали с использованием анализа уменьшения помутнения в Примере 2. В качестве лиофилизированной композиции использовали лиофилизированную композицию, хранившуюся 1 месяц. Перед анализом биологической активности ее ресуспендировали с использованием воды для инъекции (0,92 мл). В качестве жидкой композиции использовали фильтрованный раствор, свежеприготовленный в соответствии с процедурой, описанной в Примере 2. В данном эксперименте использовали следующие штаммы.
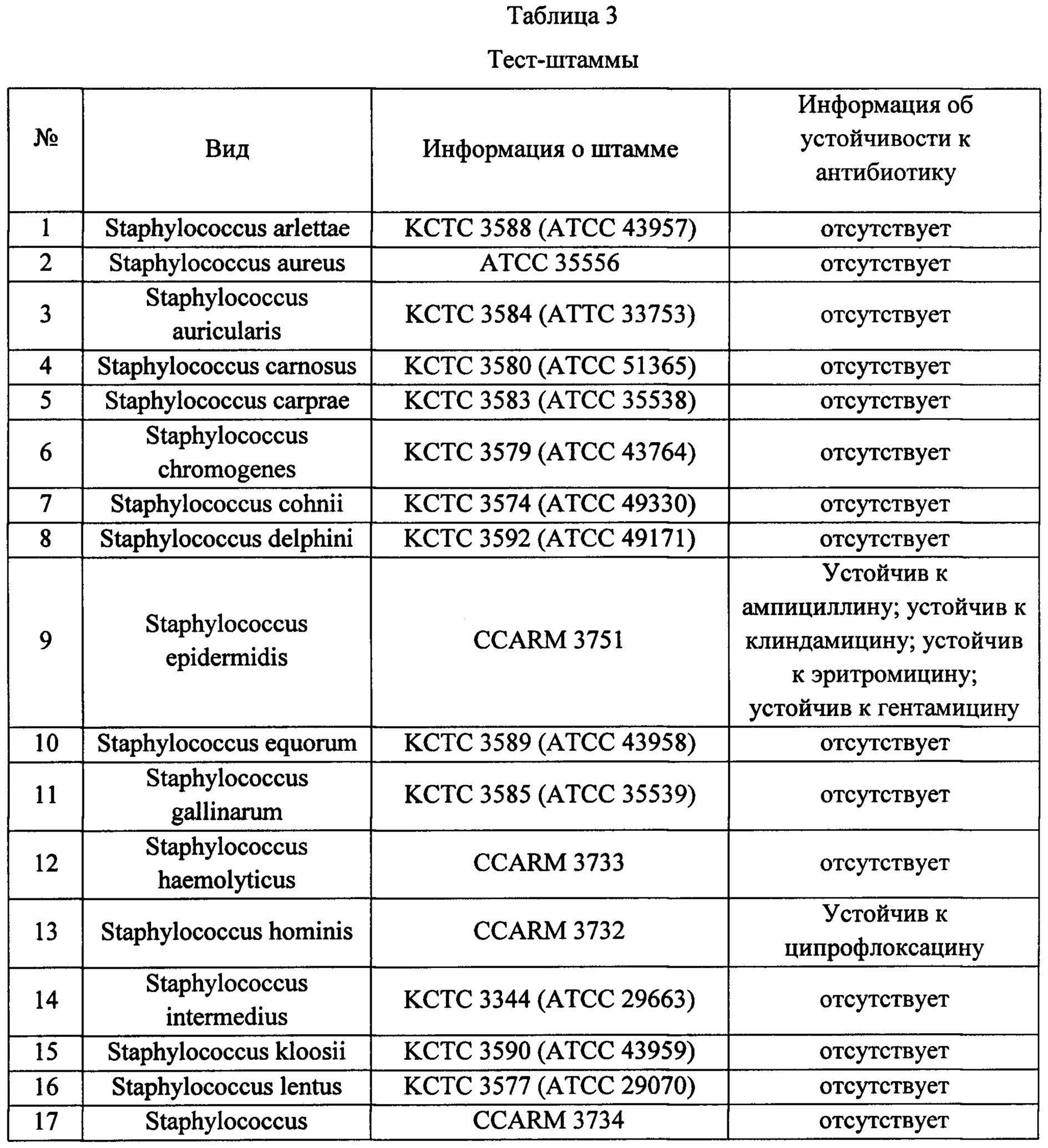
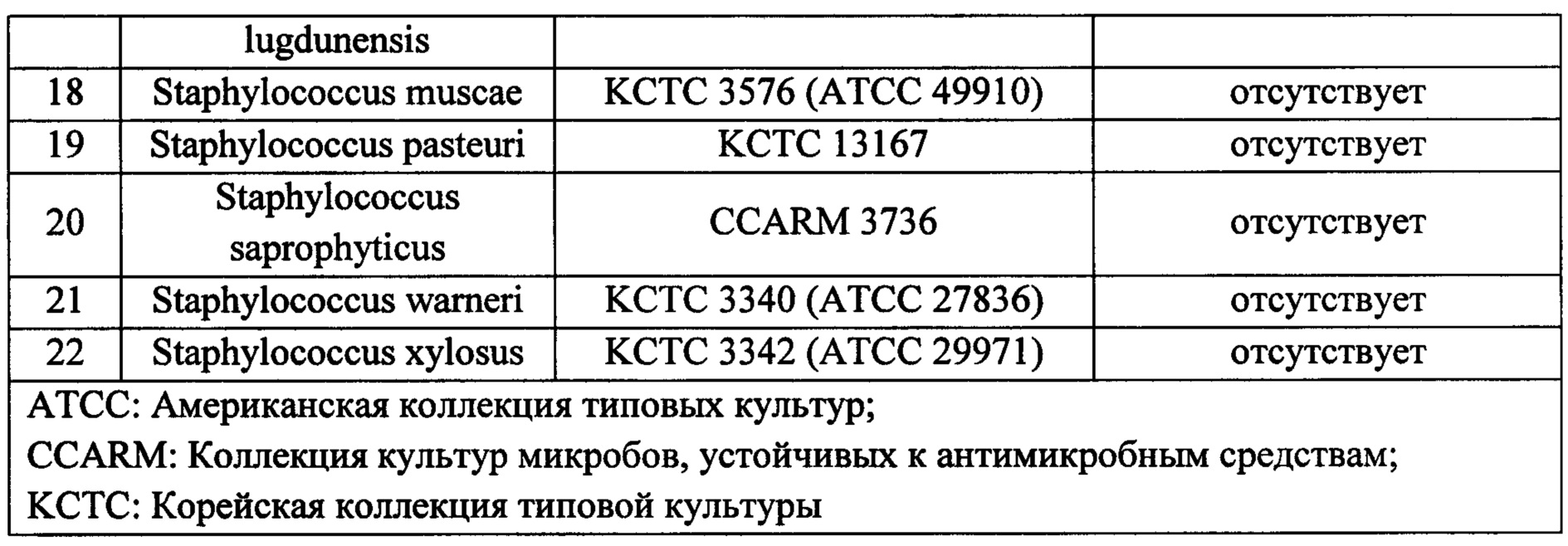
В анализе на уменьшение помутнения применяемая конечная концентрация антибактериального белка составляла 0,1 мкг/мл для следующих штаммов: Staphylococcus aureus, Staphylococcus auricularis, Staphylococcus carnosus, Staphylococcus carprae, Staphylococcus chromogenes, Staphylococcus delphini, Staphylococcus epidermidis, Staphylococcus equorum, Staphylococcus gallinarum, Staphylococcus haemolyticus, Staphylococcus hominis, Staphylococcus kloosii, Staphylococcus lugdunensis, Staphylococcus muscae, Staphylococcus saprophyticus,and Staphylococcus xylosus. For the testing against Staphylococcus arlettae, Staphylococcus cohnii, Staphylococcus intermedius, Staphylococcus lentus и Staphylococcus warneri, применяемая конечная концентрация антибактериального белка составляла 0,5 мкг/мл. Для тестирования против Staphylococcus pasteuri применяемая конечная концентрация антибактериального белка составляла 1,0 мкг/мл. Разницу значений TOD50 сравнивали у двух композиций. Результат представлен в Таблице 4.
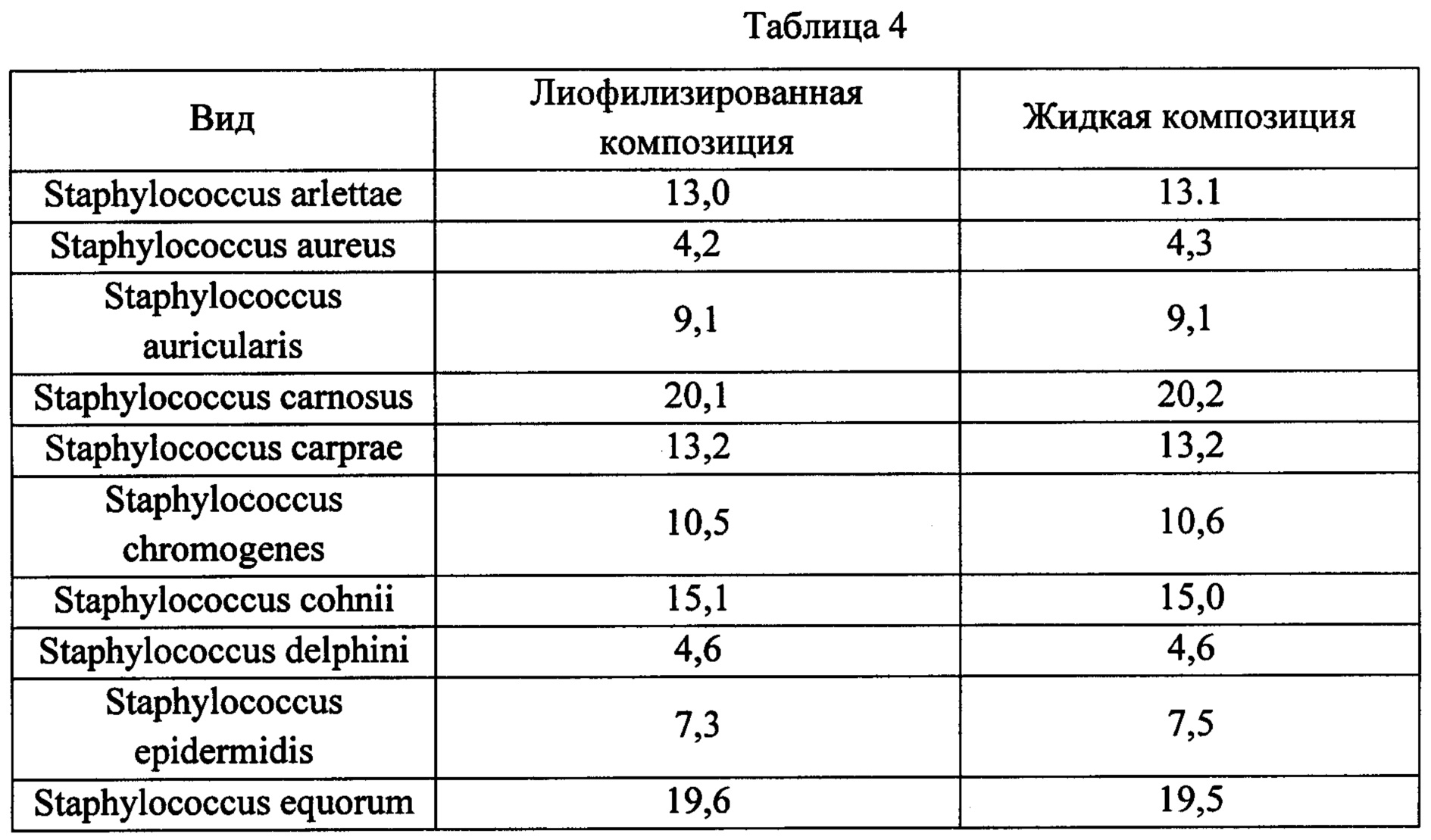
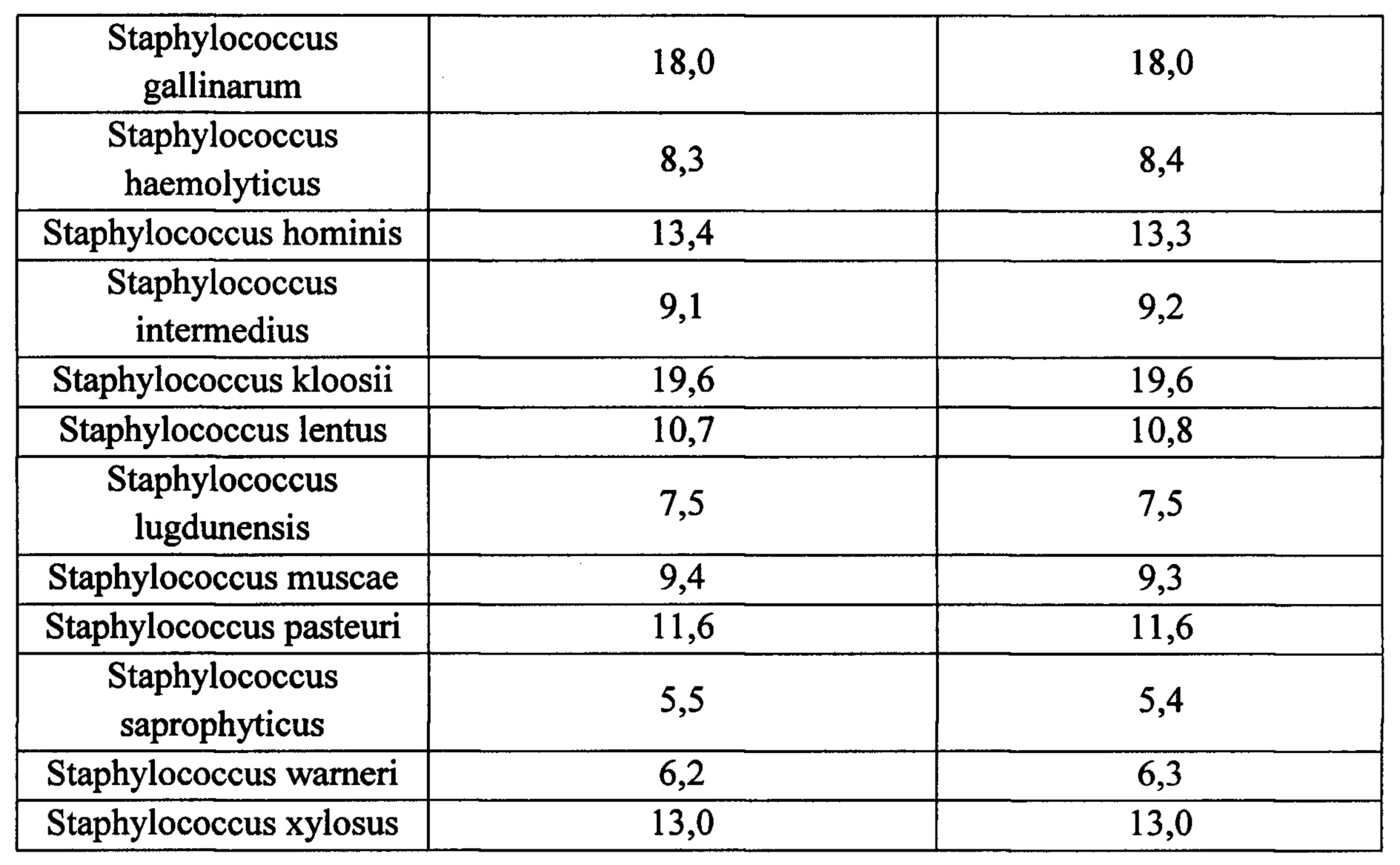
Результат, показанный в Таблице 4, очевидно указывает на то, что лиофилизированная композиция по настоящему изобретению может обеспечивать очень похожую антибактериальную активность и эффективность антибактериальных свойств с жидкой композицией. Кроме того, результат, показанный в Таблице 4, показывает, что лиофилизрованная композиция по настоящему изобретению обладает быстрой и эффективной бактерицидной активности против разных штаммов Staphylococcus. TOD50 лиофилизированной композиции по настоящему изобретению составляло меньше чем 20 минут против почти всех тестируемых штаммов Staphylococcus.
В то же время исследовали антибактериальную активность лиофилизированной композиции по настоящему изобретению против штаммов, отличных от Staphylococcus. В качестве штаммов, отличных от Staphylococcus, тестировали 2 штамма Enterococcus faecalis, 3 штамма Enterococcus faecium, 2 штамма Streptococcus mitis, 1 штамм Streptococcus uberis, 5 штаммов Escherichia coli, 2 штамма Clostridium perfringens и 3 штамма Salmonella. В результате лиофилизированная композиция по настоящему изобретению не обладала антибактериальной активностью в отношении данных тестируемых штаммов, отличных от Staphylococcus (Таблица 5). Данный результат указывает на то, что антибактериальная активность лиофилизированной композиции по настоящему изобретению является специфичной в отношении Staphylococcus.
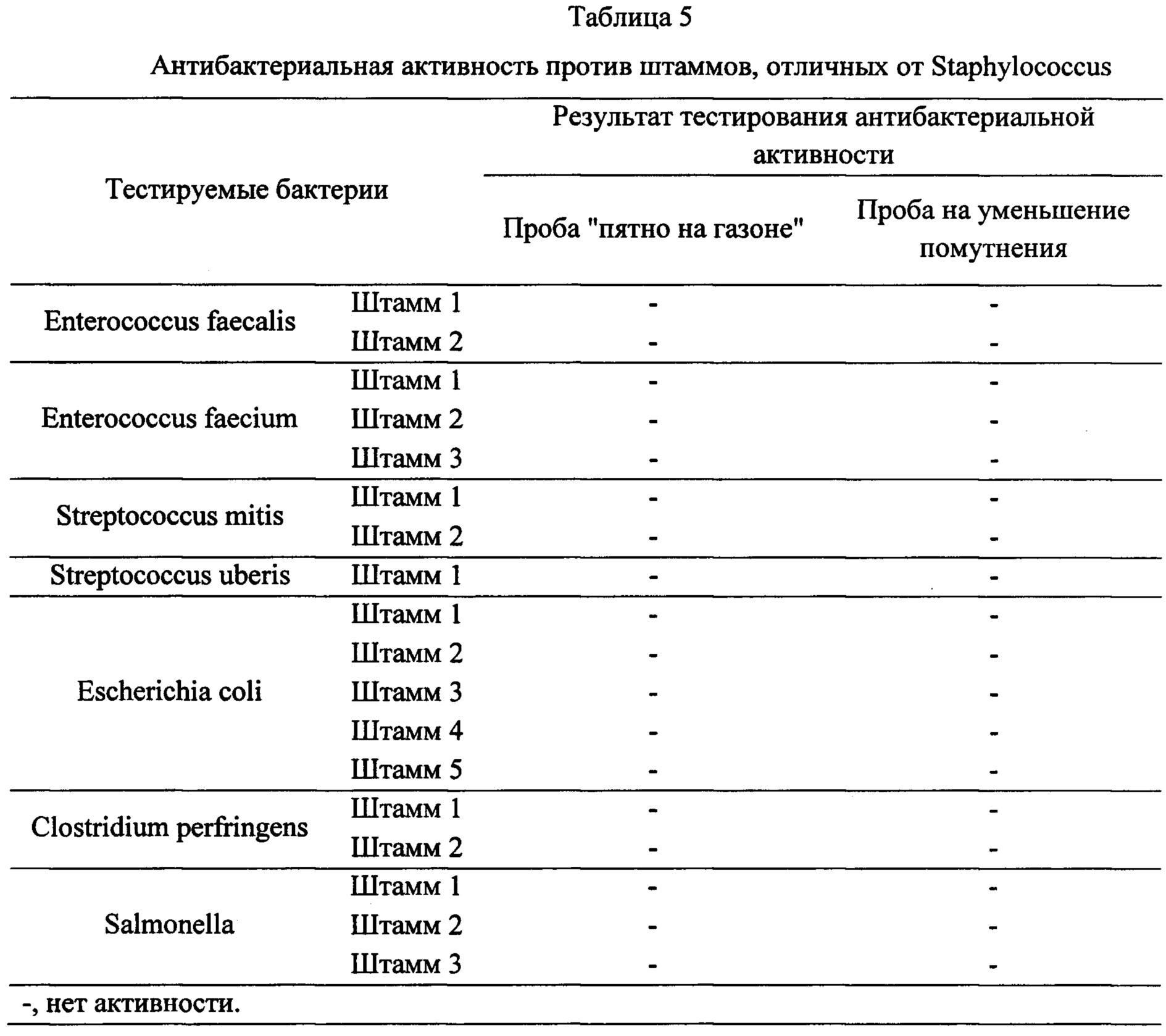
Таким образом, сделан вывод о том, что лиофилизированная композиция по настоящему изобретению была специфична в отношении Staphylococcus и обладает широким антибактериальным спектром в пределах Staphylococcus, указывая на то, что лиофилизированная композиция по настоящему изобретению может быть использована в качестве терапевтического агента при стафилококковых инфекциях.
Пример 4: Терапевтический эффект лиофилизированной композиции на одиночную стафилококковую инфекцию
Терапевтический эффект лиофилизированной композиции по настоящему изобретению на одиночные стафилококковые инфекции исследовали с использованием животной модели. В данном эксперименте в качестве модельных штаммов Staphylococcus отбирали Staphylococcus epidermidis и Staphylococcus haemolyticus. В качестве лиофилизированной композиции использовали лиофилизированную композицию после 1 месяца хранения. Перед применением в эксперименте с животными ее ресуспендировали с использованием воды для инъекции (0,92 мл). В качестве жидкой композиции использовали фильтрованный раствор, свежеприготовленный в соответствии с процедурой, описанной в Примере 2.
Для эксперимента с Staphylococcus epidermidis использовали самок мышей ICR [линия, свободная от специфической патогенной микрофлоры (SPF)], массой 23 г плюс/минус 20% (возраст 5 недель). В итоге, 30 мышам, разделенным на три группы (10 мышей на группу) внутривенно инъецировали инокуляты штамма Staphylococcus epidermidis CCARM 3751 (1×108 КОЕ (колониеобразующая единица)/мышь). Животному первой группы (т.е., контрольной группы), вводили внутривенно три раза только буфер (1,56 г/л L-гистидина (рН 6,0), 50 г/л D-сорбита, 1,47 г/л CaCl2⋅Н2О и 1 г/л полоксамера 188) в моменты времени 30 минут, 12 часов и 24 часа после бактериального заражения. Животному из группы обработки восстановленным раствором лиофилизированной композиции внутривенно три раза вводили восстановленный раствор лиофилизированной композиции (доза: 25 мг/кг) в моменты времени 30 минут, 12 часов и 24 часа после бактериального заражения. Животному из группы обработки жидкой композицией внутривенно три раза вводили жидкую композицию (доза: 25 мг/кг) в моменты времени 30 минут, 12 часов и 24 часа после бактериального заражения. Ежедневно регистрировали число мертвых мышей и наблюдали за клиническими признаками. Способность восстановленного раствора лиофилизированной композиции и жидкой композиции избавляться от бактерий в кровяном русле исследовали с использованием крови, собранной через 5 суток после бактериального заражения (экспериментальная конечная точка), путем стандартного подсчета колоний.
Для эксперимента со Staphylococcus haemolyticus использовали самок мышей ICR [линия, свободная от специфической патогенной микрофлоры (SPF)], массой 22 г плюс/минус 20% (возраст 5 недель). В итоге, 30 мышам, разделенным на три группы (10 мышей на группу), внутривенно инъецировали инокуляты штамма Staphylococcus haemolyticus CCARM 3733 (1×108 КОЕ/мышь). Животному первой группы (т.е. контрольной группы) вводили три раза внутривенно только буфер (1,56 г/л L-гистидина (рН 6,0), 50 г/л D-сорбита, 1,47 г/л CaCl2⋅Н2О и 1 г/л полоксамера 188) в моменты времени 30 минут, 12 часов и 24 часа после бактериального заражения. Животному из группы обработки восстановленным раствором лиофилизированной композиции внутривенно вводили восстановленный раствор лиофилизированной композиции (доза: 25 мг/кг) три раза в моменты времени 30 минут, 12 часов и 24 часа после бактериального заражения. Животному из группы обработки жидкой композицией внутривенно три раза вводили жидкую композицию (доза: 25 мг/кг) в моменты времени 30 минут, 12 часов и 24 часа после бактериального заражения. Ежедневно регистрировали число мертвых мышей и наблюдали за клиническими признаками. Способность восстановленного раствора лиофилизированной композиции и жидкой композиции избавляться от бактерий в кровяном русле исследовали с использованием крови, собранной через 5 суток после бактериального заражения (экспериментальная конечная точка), путем стандартного подсчета колоний.
В результате, наблюдали очевидные терапевтические эффекты. Два эксперимента продемонстрировали похожие результаты. В отношении клинических признаков, несмотря на то, что мыши в группах обработки были нормальными в течение всего экспериментального периода, мыши в контрольных группах демонстрировали разные клинические признаки, начиная с 2 суток после бактериального заражения, включая эритему края века, пониженную локомоторную активность, потерю шерсти, пилоэрекцию и вращательное поведение. Внутривенные инъекции восстановленного раствора лиофилизированной композиции и жидкой композиции значимо повышали выживаемость (Таблица 6).
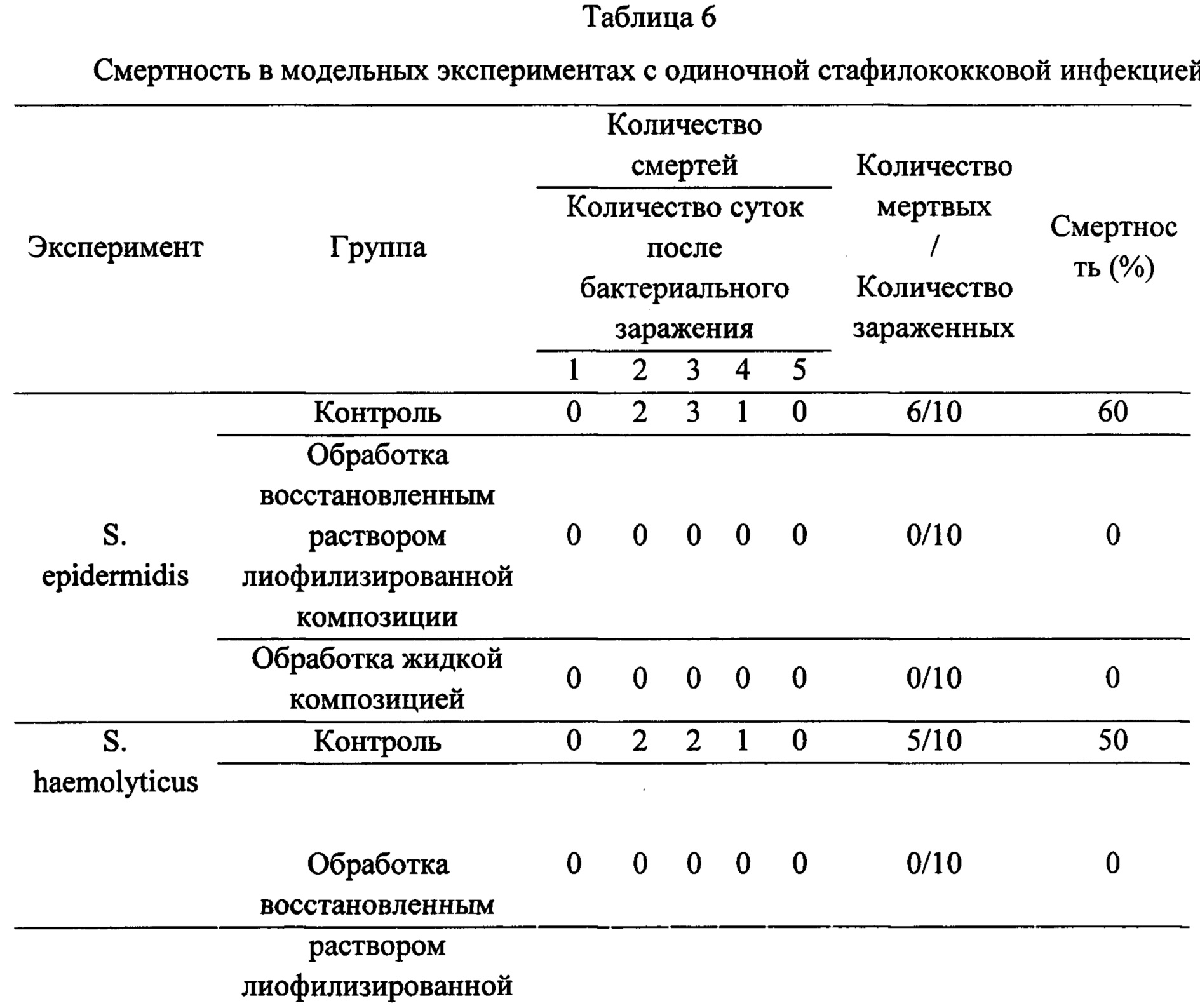
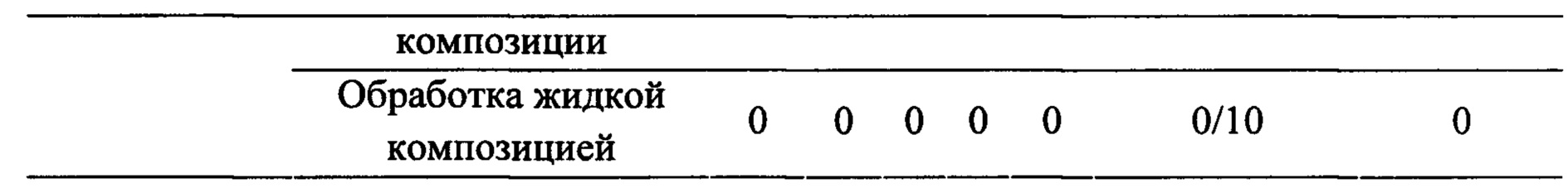
Более того, внутривенные инъекции восстановленного раствора лиофилизированной композиции и жидкой композиции значительно уменьшали количество бактерий в крови. Среднее значение КОЕ/мл составляло больше 1×106 в сыворотке, собранной у мышей контрольной группы в эксперименте со Staphylococcus epidermidis, и больше 1×105 в сыворотке, собранной у мышей контрольной группы в эксперименте со Staphylococcus haemolyticus, тогда как у мышей всех групп обработки не наблюдалось бактериальных колоний.
Исходя из вышеуказанных результатов, было подтверждено, что лиофилизированная композиция по настоящему изобретению может обеспечивать очень похожий терапевтический эффект в лечении одиночных стафилококковых инфекций с жидкой композицией. Кроме того, результат, показанный в Таблице 6, демонстрирует, что лиофилизированную композицию по настоящему изобретению можно эффективно использовать для лечения стафилококковых инфекций.
Пример 5: Терапевтический эффект лиофилизированной композиции на множественную стафилококковую инфекцию
Терапевтический эффект лиофилизированной композиции по настоящему изобретению на множественные стафилококковые инфекции исследовали с использованием животной модели. В данном эксперименте в качестве модельных штаммов Staphylococcus отбирали Staphylococcus epidermidis, Staphylococcus lugdunensis и Staphylococcus warneri. В качестве лиофилизированной композиции использовали лиофилизированную композицию, хранившуюся 1 месяц. Перед применением в эксперименте с животными ее ресуспендировали с использованием воды для инъекции (0,92 мл). В качестве жидкой композиции использовали фильтрованный раствор, свежеприготовленный в соответствии с процедурой, описанной в Примере 2.
Использовали самок мышей ICR [линия, свободная от специфической патогенной микрофлоры (SPF)], массой 22 г плюс/минус 20% (возраст 5 недель). В итоге, 30 мышам, разделенным на три группы (10 мышей на группу), внутривенно инъецировали смешанные инокуляты Staphylococcus epidermidis CCARM 3751, Staphylococcus lugdunensis CCARM 3734 и Staphylococcus warneri KCTC 3340 (ATCC 27836) (1×108 КОЕ каждого/мышь). Животному первой группы (т.е. контрольной группы) три раза внутривенно вводили только буфер (1,56 г/л L-гистидина (рН 6,0), 50 г/л D-сорбита, 1,47 г/л CaCl2⋅Н2О и 1 г/л полоксамера 188) в моменты времени 30 минут, 12 часов и 24 часа после бактериального заражения. Животному из группы обработки восстановленным раствором лиофилизированной композиции три раза внутривенно вводили восстановленный раствор лиофилизированной композиции (доза: 25 мг/кг) в моменты времени 30 минут, 12 часов и 24 часа после бактериального заражения. Животному из группы обработки жидкой композицией три раза внутривенно вводили жидкую композицию (доза: 25 мг/кг) в моменты времени 30 минут, 12 часов и 24 часа после бактериального заражения. Ежедневно регистрировали число мертвых мышей и наблюдали за клиническими признаками. Способность восстановленного раствора лиофилизированной композиции и жидкой композиции избавляться от бактерий в кровяном русле исследовали с использованием крови, собранной через 5 суток после бактериального заражения (экспериментальная конечная точка), путем стандартного подсчета колоний.
В результате, наблюдали очевидные терапевтические эффекты. В отношении клинических признаков, несмотря на то, что мыши в группах обработки были нормальными в течение всего экспериментального периода, мыши в контрольной группе демонстрировали разные клинические признаки, включая эритему края века, пониженную локомоторную активность, потерю шерсти, птоз и пилоэрекцию. Внутривенные инъекции восстановленного раствора лиофилизированной композиции и жидкой композиции значимо повышали выживаемость (Таблица 7).
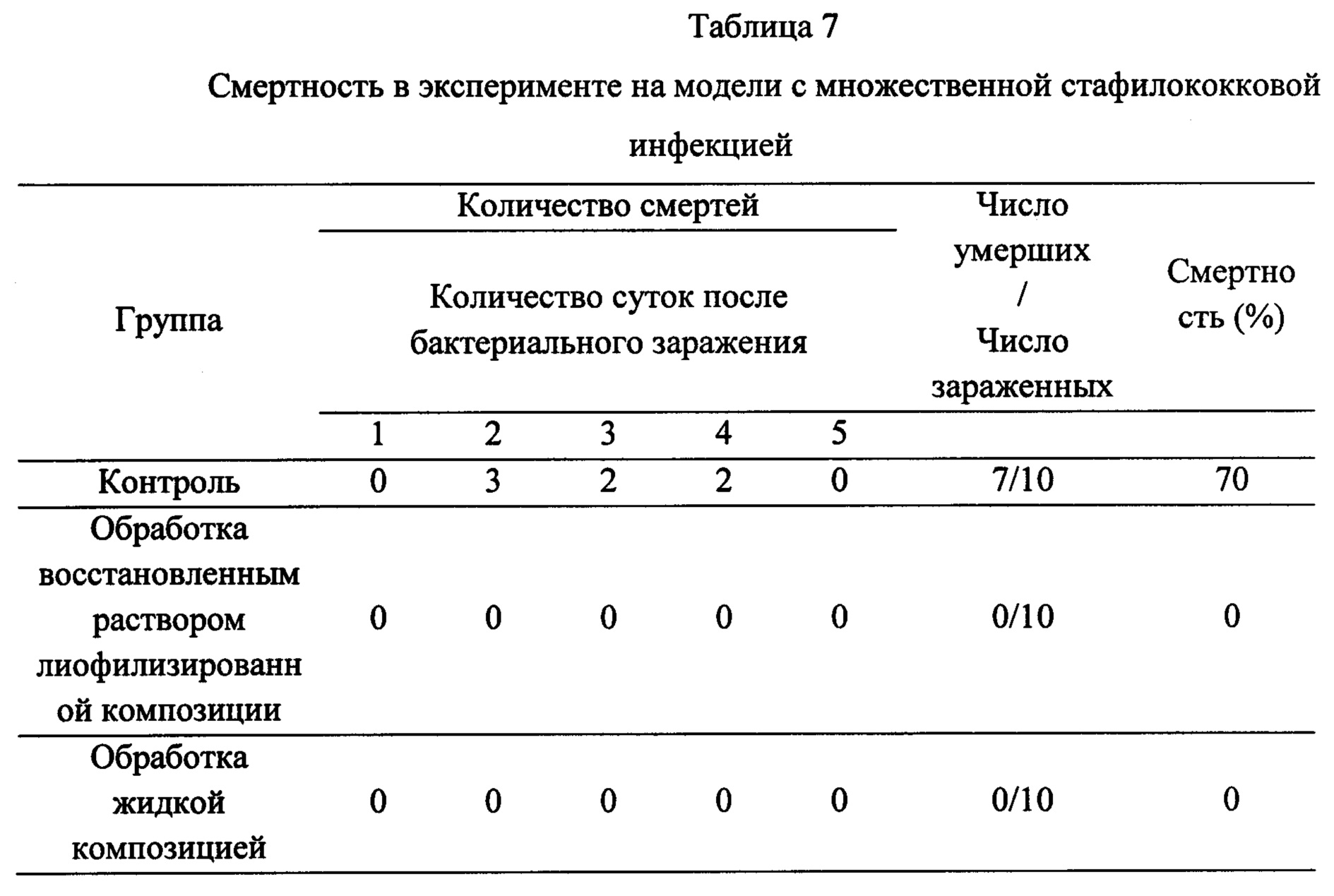
Кроме того, внутривенные инъекции восстановленного раствора лиофилизированной композиции и жидкой композиции значимо уменьшали бактериальное число в крови. Среднее значение КОЕ/мл составляло больше 1×106 в сыворотке, собранной у мышей контрольной группы, тогда как у мышей всех групп обработки не наблюдалось бактериальных колоний.
Исходя из вышеуказанных результатов, было подтверждено, что лиофилизированная композиция по настоящему изобретению может обеспечивать очень похожий терапевтический эффект в лечении множественных стафилококковых инфекций с жидкой композицией. Кроме того, результат, показанный в Таблице 7, демонстрирует, что лиофилизированную композицию по настоящему изобретению можно эффективно использовать для лечения стафилококковых инфекций.
Специалистам в данной области будет очевидно, что в настоящем изобретении могут быть сделаны разные модификации и варианты, не отступая от сущности и объема изобретения. Таким образом, предполагается, что настоящее изобретение охватывает модификации и варианты данного изобретения, при условии, что они попадают в пределы объема прилагаемой формулы изобретения и ее эквивалентов.