Результат интеллектуальной деятельности: НОВАЯ ОФТАЛЬМОЛОГИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ РЕБАМИПИД, И СПОСОБ ЕЕ ПОЛУЧЕНИЯ
Вид РИД
Изобретение
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее раскрытие относится к офтальмологической композиции, содержащей ребамипид, которая сохраняет свою прозрачность, имеет превосходную стабильность и является простой для получения, и способу ее получения.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Ребамипид [2-(4-хлорбензоиламино)-3-(2-хинолон-4-ил)пропионовая кислота] представляет собой производное хинолона, представленное следующей формулой I.
[Формула I]
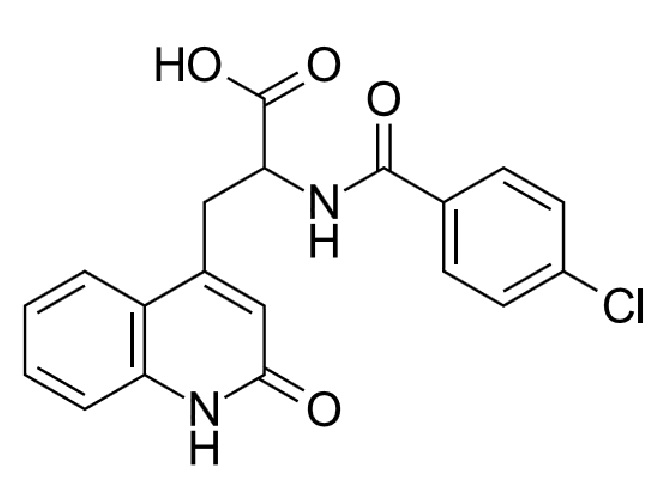
Известно, что ребамипид увеличивает желудочный муцин, обладая противовоспалительным и противоязвенным действием на пищеварительный тракт, и, таким образом, он применялся в качестве перорального терапевтического средства для лечения язвенной болезни желудка с 1990 г. Кроме того, была доказано действие ребамипида на увеличение плотности бокаловидных клеток в глазах, увеличение муцина в глазах и увеличение слезной жидкости, и, таким образом, ребамипид был разработан и поставлялся в виде терапевтического средства для лечения синдрома сухого глаза в форме офтальмологического раствора в Японии.
Однако ребамипид имеет низкую растворимость в интервале рН, где он является применимым для глаз, что создает трудности для поддержания стабильного и прозрачного водного раствора во время длительного хранения и для производства в форме прозрачного офтальмологического раствора, и таким образом, он является доступным в форме офтальмологической суспензии. Кроме того, в доступных для приобретения офтальмологических суспензиях лекарственное средство диспергировано в виде частиц, которые вызывают ощущение раздражения в глазах, а также местную боль. Исследования, нацеленные на разработку прозрачного офтальмологического раствора, содержащего ребамипид, продолжают развиваться; однако полагают, что пока является трудным разработать водный препарат, содержащий ребамипид, и продукты, разработанные до настоящего времени, находятся в форме офтальмологической суспензии.
Публикация Международной заявки на патент № WO 97/013515 раскрывает водную суспензию, содержащую ребамипид. Однако эта суспензия может образовывать флокулированную суспензию при выдерживании в течение длительного времени. Следовательно, необходимо хорошее встряхивание суспензии, чтобы диспергировать образованный осадок. Кроме того, вышеуказанная суспензия представляет собой белую суспензию и, таким образом, может ограничивать видимость.
Публикация Международной заявки на патент № WO 2008/050896 раскрывает содержащую ребамипид водную суспензию с улучшенной суспензированностью, которая может поддерживать стабильным состояние мелкодисперсных частиц ребамипида без агглютинации мелких частиц, в сравнении с водной суспензией вышеуказанной Публикации Международной заявки на патент № WO 97/013515. Однако эта суспензии может также образовывать осадок при выдерживании в течение длительного времени и является белой суспензией, которая ограничивает видимость.
Публикация Международной заявки на патент № WO 2006/052018 раскрывает водную суспензию, содержащую кристаллический ребамипид, которая имеет улучшенную прозрачность, по сравнению с вышеуказанными двумя водными суспензиями. Однако для реализации данного изобретения в процессе производства требуется дорогостоящее оборудование, такое как гомогенизатор высокого давления, коллоидная мельница, ультразвуковое устройство, и т.д., производственный процесс является очень трудным и осложненным, и время производства является длительным, что приводит к высоким производственным затратам. Кроме того, она также имеет проблему с образованием осадка, при выдерживании в течение длительного времени.
Публикация Международной заявки на патент № WO 2009/154304 и Публикация Международной заявки на патент № WO 2014/051163 раскрывают прозрачные офтальмологические композиции ребамипида. Однако эти офтальмологические растворы имеют высокий pH, равный 8 или выше, и не подходят для пациента, страдающего от повреждения в роговице и конъюнктиве, такого как сухость глаз.
Кроме того, Публикация Международной заявки на патент № WO 2008/074853 раскрывает композицию, в которой используют усилитель вязкости и буфер для поддержания стабильности водного раствора, содержащего ребамипид. Однако эта композиция также имеет проблему с образованием осадка при выдерживании в течение длительного времени.
Следовательно, необходимо разработать фармацевтическую композицию, содержащую ребамипид, которая поддерживает свою прозрачность в течение длительного времени даже в интервале рН от физиологически нейтрального до слабоосновного (ниже 8), которая не повреждает роговицу и конъюнктиву пациента, страдающего от сухости глаз, и которая имеет улучшенную стабильность таким образом, чтобы повторно не диспергироваться.
Описание
Техническая проблема
Цель настоящего раскрытия состоит в том, чтобы предоставить офтальмологическую композицию, содержащую ребамипид, которая является прозрачной в интервале рН от 7 до 8. Более конкретно, целью настоящего раскрытия является предоставить офтальмологическую композицию, содержащую ребамипид, которая поддерживает свою прозрачность в течение длительного времени даже в интервале рН от физиологически нейтрального до слабоосновного, которая не повреждает кератоконъюнктиву пациента, страдающего от сухости глаз, и которая имеет улучшенную стабильность, таким образом, чтобы повторно не диспергироваться.
Кроме того, еще одной целью настоящего раскрытия является предоставить способ получения офтальмологической композиции настоящего раскрытия простым образом, без какого-либо осложненного процесса.
Техническое решение
Чтобы достичь целей настоящего раскрытия, настоящее раскрытие предоставляет новую офтальмологическую композицию, содержащую ребамипид, и способ ее получения, которые ниже будут описаны подробно.
Офтальмологическая композиция, содержащая ребамипид
Офтальмологическая композиция согласно настоящему раскрытию содержит (1) ребамипид, (2) средство против перекристаллизации, выбранное из группы, состоящей из производного циклодекстрина, аминокислоты и их смесей и (3) буферного агента.
Ребамипид может быть получен непосредственно общеизвестным способом или является доступным для приобретения.
В настоящем раскрытии концентрация ребамипида может составлять от 0,1 до 1,5 масс./об.%, предпочтительно от 0,2 до 1,0 масс./об.%.
Средство против перекристаллизации, применяемое в настоящем раскрытии, является добавкой для предотвращения неспособности раствора, который является достаточно прозрачным, но присутствует в супернасыщенном состоянии, поддерживать прозрачный внешний вид без образования какого-либо осадка в процессе длительного хранения. Средство против перекристаллизации, которое может применяться в настоящем раскрытии, включает производное циклодекстрина и/или аминокислоту.
Примеры производного циклодекстрина, применяемого в качестве средства против перекристаллизации в настоящем раскрытии, включают альфа-, бета- и гамма-циклодекстрин и их замещенные производные, такие как диметил-, гидроксиэтил-, гидроксипропил- или сульфобутиловый эфир-бета-циклодекстрин. Предпочтительно может применяться гидроксипропилбетадекс. Кроме того, концентрация производного циклодекстрина может предпочтительно составлять от 1,0 до 10,0 масс./об.%.
Аминокислота, которая является другим средством против перекристаллизации согласно настоящему раскрытию, может содержать по меньшей мере одну аминокислоту, выбранную из группы, состоящей из основных аминокислот, таких как аргинин, лизин, гистидин, и т.д., и нейтральных аминокислот, таких как глицин, аланин, валин и т.д. Кроме того, концентрация аминокислот может предпочтительно составлять от 0,1 до 5,0 масс./об.%.
В настоящем раскрытии буферный агент может содержать по меньшей мере один агент, выбранный из группы, состоящей из бората, фосфата, трометамина и их смесей. Борат может предпочтительно применяться в качестве буферного агента. Кроме того, концентрация буферного агента может предпочтительно составлять от 0,05 до 2,0 масс./об.%.
Кроме того, офтальмологическая композиция согласно настоящему раскрытию может дополнительно включать по меньшей мере одну добавку, выбранную из группы, состоящей из загустителя, солюбилизирующего средства, изотонического агента, и регулятора рН.
Загуститель представляет собой добавку, которая продлевает период времени, в течение которого лекарственное средство остается в организме во время клинического применения, и может содержать по меньшей мере один загуститель, выбранный из группы, состоящей из поливинилпирролидона, гидроксипропилметилцеллюлозы, и поливинилового спирта, но ими не ограничивается. Предпочтительно может применяться поливинилпирролидон.
Солюбилизирующее средство представляет собой добавку для увеличения растворимости лекарственного средства и может содержать по меньшей мере одно средство, выбранное из группы, состоящей из гидрогенизированного касторового масла полиоксил 35, полоксамера и полисорбата.
Изотонический агент может добавляться в количестве, которое создает осмотическое давление офтальмологического раствора, сходное осмотическому давлению в слезах, и может содержать хлориды, сахариды, пропиленгликоль и глицерин.
Регулятор рН является добавкой для регуляции pH в интервале, который является применимым в организме (глазах) и не повреждает роговицу и конъюнктиву, и может содержать неорганические кислоты или органические кислоты. Предпочтительно может применяться неорганическая кислота, такая как фосфорная кислота или фосфат.
Офтальмологическая композиция согласно настоящему раскрытию может предпочтительно иметь pH от 7 до 8, который находится в интервале рН от физиологически нейтрального до слабоосновного, который не повреждает роговицу и конъюнктиву пациента, страдающего от сухости глаз.
Кроме того, офтальмологическая композиция согласно настоящему раскрытию обладает превосходной прозрачностью в вышеуказанном интервале рН (pH 7-8), поддерживает свою прозрачность даже после выдержки в течение длительного времени и имеет улучшенную стабильность таким образом, чтобы повторно не диспергироваться.
В соответствии с предпочтительным вариантом осуществления настоящего раскрытия, офтальмологическая композиция настоящего раскрытия представляет собой состав в виде раствора, а не существующую водную суспензию. Офтальмологическая композиция согласно настоящему раскрытию решила проблему трудности производства в форме раствора вследствие низкой растворимости, и в то же время обладает гарантированной превосходной прозрачностью и стабильностью. Следовательно, офтальмологическая композиция согласно настоящему раскрытию может быть очень полезной в качестве офтальмологического раствора для пациентов, страдающих от сухости глаз.
Способ получения офтальмологической композиции, содержащей ребамипид
Способ получения офтальмологической композиции согласно настоящему раскрытию включает: первую стадию (S-1) получения раствора посредством растворения ребамипида в буферном растворе; вторую стадию (S-2) добавления и растворения средства против перекристаллизации, выбранного из группы, состоящей из производного циклодекстрина, аминокислоты и их смесей в раствор, полученный на первой стадии; и третью стадию (S-3) фильтрации раствора, полученного на второй стадии, через стерильный фильтр.
Кроме того, вторая стадия может дополнительно включать, после растворения средства против перекристаллизации, стадию добавления и растворения по меньшей мере одной добавки, выбранной из группы, состоящей из загустителя, солюбилизирующего средства, изотонического агента и регулятора рН.
Конкретно, буферный раствор с подходящей концентрацией получают посредством добавления буферного агента, а затем добавляют ребамипид и растворяют его в буферном растворе при перемешивании. Регулятор рН может добавляться при необходимости, и средство против перекристаллизации добавляют и растворяют в прозрачном растворе ребамипида при перемешивании. Загуститель, солюбилизирующее средство, регулятор рН и изотонический агент могут добавляться при соответствующих концентрациях в соответствии с обстоятельствами. Кроме того, все из этих процессов достигаются простым перемешиванием, а фильтрацию выполняют, используя стерильный фильтр 0,22 мкм для достижения стерилизации.
В способе производства согласно настоящему раскрытию применяют средство против перекристаллизации ребамипида, такое как производное циклодекстрина и/или аминокислота, и буферный агент, чтобы достаточным образом поддерживать прозрачность и предотвратить образование слоя осадка даже во время длительного хранения, и этим способом можно производить офтальмологическую композицию, содержащую ребамипид, путем простого перемешивания без применения дорогостоящего оборудования.
Фармацевтическая композиция и способ предотвращения или лечения синдрома сухого глаза
Настоящее раскрытие предоставляет фармацевтическую композицию, содержащую офтальмологическую композицию согласно настоящему раскрытию.
Настоящее раскрытие также предоставляет фармацевтическую композицию для лечения синдрома сухого глаза, содержащую офтальмологическую композицию согласно настоящему раскрытию.
Настоящее раскрытие также предоставляет способ лечения синдрома сухого глаза, включающий введение офтальмологической композиции согласно настоящему раскрытию пациентам.
Положительные эффекты
Офтальмологическую композицию согласно настоящему раскрытию получают посредством смешивания средства против перекристаллизации с композицией, содержащей ребамипид и буферный раствор, и, таким образом, является возможным улучшить прозрачность офтальмологической композиции и поддерживать ее прозрачность без агрегации или осаждения растворенных частиц даже в процессе длительного хранения.
Кроме того, согласно настоящему раскрытию, является возможным производить прозрачный офтальмологический раствор ребамипида посредством простого перемешивания без необходимости применять затруднительные процессы производства, такие как гомогенизация под высоким давлением, ультразвуковое диспергирование, и т.д., посредством выбора буферного агента, пригодного для композиции, и регуляции концентрации буферного раствора. Кроме того, является возможным удалять бактерии только посредством фильтрации, используя стерильный фильтр 0,22 мкм, что приводит к сниженным производственным затратам.
Способ осуществления изобретения
Далее в данном документе ниже будут описаны Примеры и Экспериментальные Примеры согласно настоящему раскрытию для лучшего понимания настоящего раскрытия, но объем настоящего раскрытия не ограничивается Примерами и Экспериментальными Примерами.
Примеры 1-13 и Сравнительные примеры 1-5
Согласно композиции и отношению компонентов, показанных в следующих таблицах 1 и 2, к очищенной воде, имеющей соответствующий объем, при перемешивании добавляли буферный агент. При перемешивании к буферному раствору добавляли и растворяли ребамипид, и затем к нему добавляли гидроксипропилбетадекс. После полного растворения ребамипида и гидроксипропилбетадекса добавляли регулятор рН и изотонический агент для регуляции уровня pH и осмотического давления. Полученный в результате раствор ребамипида отфильтровывали, используя стерильный фильтр 0,22 мкм, для получения бесцветных прозрачных офтальмологических композиций Примеров 1-13.
Согласно композиции и отношению компонентов, показанных в следующих таблицах 1 и 2, композиции Сравнительных примеров 1-5 получали тем же способом получения, который описан в Примерах 1-13, за исключением процесса добавления гидроксипропилбетадекса.
[Таблица 1] Композиции I согласно композиции буферного агента и гидроксипропилбетадекса
|
[Таблица 2] Композиции II согласно композиции буферного агента и гидроксипропилбетадекса
|
Примеры 14-21
Композиции примеров 14-21 получали тем же способом получения, который описан в Примерах 1-13, за исключением варьирования композиции и отношения аминокислот, как показано в следующей таблице 3.
[Таблица 3] Композиции согласно композиции и отношению аминокислот
|
Примеры 22-29
Композиции Примеров 22-29 получали тем же способом получения, который описан в Примерах 1-13, за исключением варьирования отношения загустителя, который может быть дополнительно добавлен к офтальмологической композиции, содержащей средство против перекристаллизации и буферного агента, как показано в следующей таблице 4.
[Таблица 4] Композиции согласно отношению загустителей
|
Примеры 30-34
Композиции примеров 30-34 получали тем же способом получения, который описан в Примерах 1-13, за исключением варьирования отношения солюбилизирующего средства, которое может быть дополнительно добавлено к композиции, содержащей средство против перекристаллизации и буферного агента, как показано в следующей таблице 5.
[Таблица 5] Композиции согласно отношению солюбилизирующих средств
|
Экспериментальный Пример 1
Чтобы оценить прозрачность и стабильность в зависимости от наличия или отсутствия средства против перекристаллизации, композиции, полученные в Примерах 1-13 и Сравнительных примерах 1-5, хранили при комнатной температуре и в условиях низких температур, а затем определяли наличие или отсутствие осаждения кристаллов с течением времени, что показано в следующих таблицах 6-9.
Прозрачность композиций наблюдали невооруженным глазом, используя тестирующее устройство для Теста на нерастворимые твердые частицы для офтальмологических растворов из Фармакопеи Республики Корея.
[Таблица 6] Оценка стабильности композиций Примеров 1-13 при комнатной температуре
|
[Таблица 7] Оценка стабильности композиций Сравнительных Примеров 1-5 при комнатной температуре
|
[Таблица 8] Оценка стабильности Композиций Примеров 1-13 в условиях низких температур
|
[Таблица 9] Оценка стабильности композиций Сравнительных Примеров 1-3 в условиях низких температур
|
Как показано в таблицах 6-9, офтальмологические композиции Примеров 1-13, содержащие производное циклодекстрина (гидроксипропилбетадекс), которое является средством против перекристаллизации, были бесцветными и прозрачными даже после выдерживания в течение длительного времени, в то время как в композициях Сравнительных Примеров 1-5, которые не содержали средства против перекристаллизации, через 2 недели образовались осадки.
Экспериментальный Пример 2
Чтобы определить доступность аминокислот в качестве средства против перекристаллизации, композиции, полученные в Примерах 14-21, хранили при комнатной температуре и в условиях низких температур, а затем наличие или отсутствие осаждения кристаллов с течением времени определяли тем же методом, что в Экспериментальном Примере 1, что показано в следующих таблицах 10 и 11.
[Таблица 10] Оценка стабильности композиций Примеров 14-21 при комнатной температуре
|
[Таблица 11] Оценка стабильности композиций Примеров 14-21 в условиях низких температур
|
В результате эксперимента офтальмологические композиции примеров 14-21, дополнительно содержащие аминокислоту, также поддерживали прозрачность (бесцветность) без образования какого-либо осадка.
Экспериментальный Пример 3
Чтобы определить эффект от добавления загустителя, композиции, полученные в Примерах 22-29, хранили при комнатной температуре и в условиях низких температур, а затем наличие или отсутствие осаждения кристаллов с течением времени определяли тем же методом, что в Экспериментальном Примере 1, что показано в следующих таблицах 12 и 13.
[Таблица 12] Оценка стабильности композиций примеров 22-29 при комнатной температуре
|
[Таблица 13] Оценка стабильности композиций Примеров 22-29в условиях низких температур
|
В результате эксперимента наблюдали, что композиции, дополнительно содержащие загуститель, также поддерживали прозрачность (бесцветность) и стабильность во время периода наблюдения.
Экспериментальный Пример 4
Чтобы определить эффект от добавления солюбилизирующего средства, композиции, полученные в Примерах 30-34, хранили при комнатной температуре и в условиях низких температур, и затем наличие или отсутствие осаждения кристаллов с течением времени определяли тем же методом, что в Экспериментальном Примере 1, что показано в следующих таблицах 14 и 15.
[Таблица 14] Оценка стабильности композиций Примеров 30-34 при комнатной температуре
|
[Таблица 15] Оценка стабильности композиций Примеров 30-34 в условиях низких температур
|
В результате эксперимента наблюдали, что композиции, дополнительно содержащие солюбилизирующее средство, также поддерживали прозрачность (бесцветность) и стабильность во время периода наблюдения.

