Результат интеллектуальной деятельности: 2-замещенные 5-гидроксипирано[2,3-d][1,3]оксазин-4,7-дионы и способ их получения
Вид РИД
Изобретение
Группа изобретений относится к области органической и медицинской химии, а именно: к новым, неописанным в литературе полифункциональным гетероциклическим соединениям с общей структурной формулой I и к способу их получения, которые могут быть использованы для синтеза новых гетероциклических соединений и в медицине в качестве потенциального антимикробного средства.
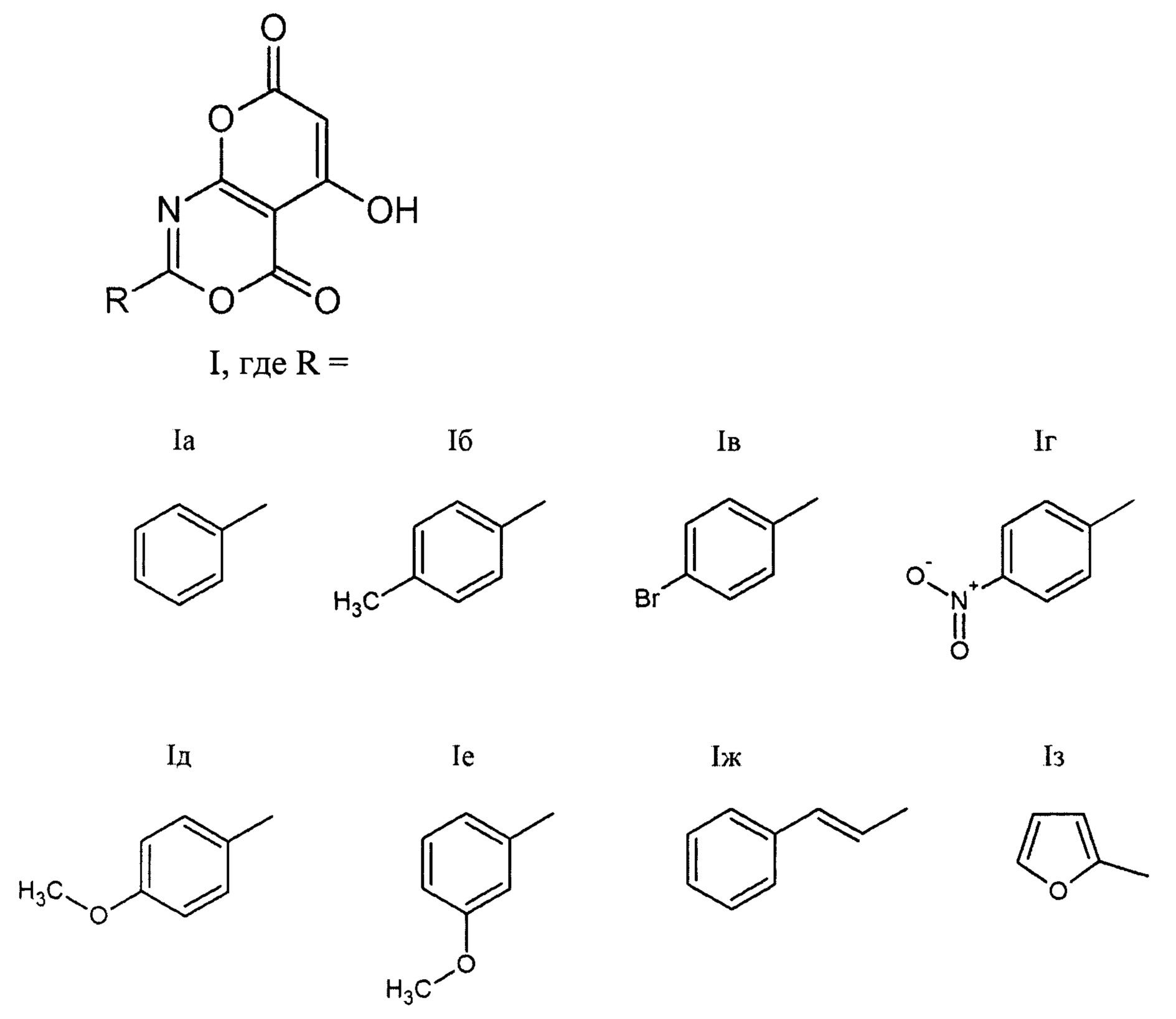
R = фенил, (Ia - 2-фенил-5-гидроксипирано[2,3-d][1,3]оксазин-4,7-дион),
R = 4-метилфенил, (Iб - 2-(4-метилфенил)-5-гидроксипирано[2,3-d][1,3]оксазин-4,7-дион),
R = 4-бромфенил, (Iв - 2-(4-бромфенил)-5-гидроксипирано[2,3-d][1,3]оксазин-4,7-дион),
R = 4-нитрофенил, (Iг - 2-(4-нитрофенил)-5-гидроксипирано[2,3-d][1,3]оксазин-4,7-дион),
R = 4-метоксифенил, (Iд - 2-(4-метоксифенил)-5-гидроксипирано[2,3-d][1,3]оксазин-4,7-дион),
R = 3-метоксифенил, (Ie - 2-(3-метоксифенил)-5-гидроксипирано[2,3-d][1,3]оксазин-4,7-дион),
R = стирил, (Iж - 2-стирил-5-гидроксипирано[2,3-d][1,3]оксазин-4,7-дион),
R = фуран-2-ил, (Iз - 2-(фуран-2-ил)-5-гидроксипирано[2,3-d][1,3]оксазин-4,7-дион).
Известен 7-хлоро-4,5-диоксо-2-фенилпирано[3,4-е][1,3]оксазин IV, который был получен взаимодействием бензонитрила II с малонилхлоридом III в соотношении 1:2 без растворителя при 100°С [5-oxopyrano[3,4-е][1,3] 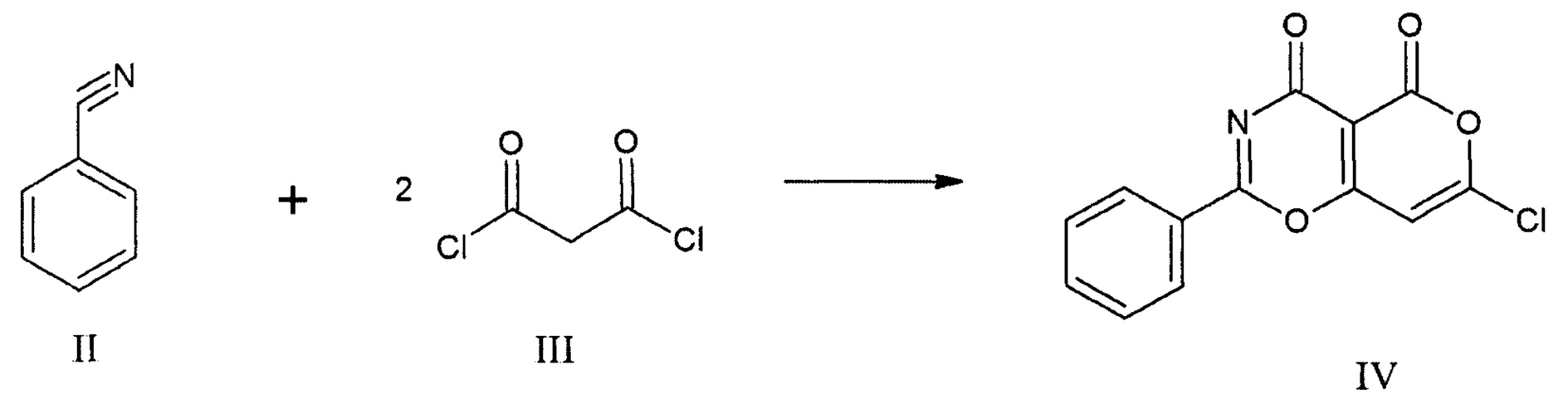 oxazines from nitriles, and their degradation to4-oxo-1,3-oxazines and other products / S.J. Davis and J.A. Elvidge, J. Chem. Soc., 1962, 3553].
oxazines from nitriles, and their degradation to4-oxo-1,3-oxazines and other products / S.J. Davis and J.A. Elvidge, J. Chem. Soc., 1962, 3553].
В литературе также описаны 4-арил-3,4-дигидро-2Н,5Н-пирано[3,4-e][1,3]оксазин-2,5-дионы VIII, образующиеся в результате взаимодействия 1-хлоробензилизоцианатов V с 4-гидроксипиран-2-оном VI в толуоле VII при 60°С [Вовк М.В., Сукач В.А., Дорохов В.И. // ЖОХ. - 2007. - Т. 43, №8 - С. 1192-1195].
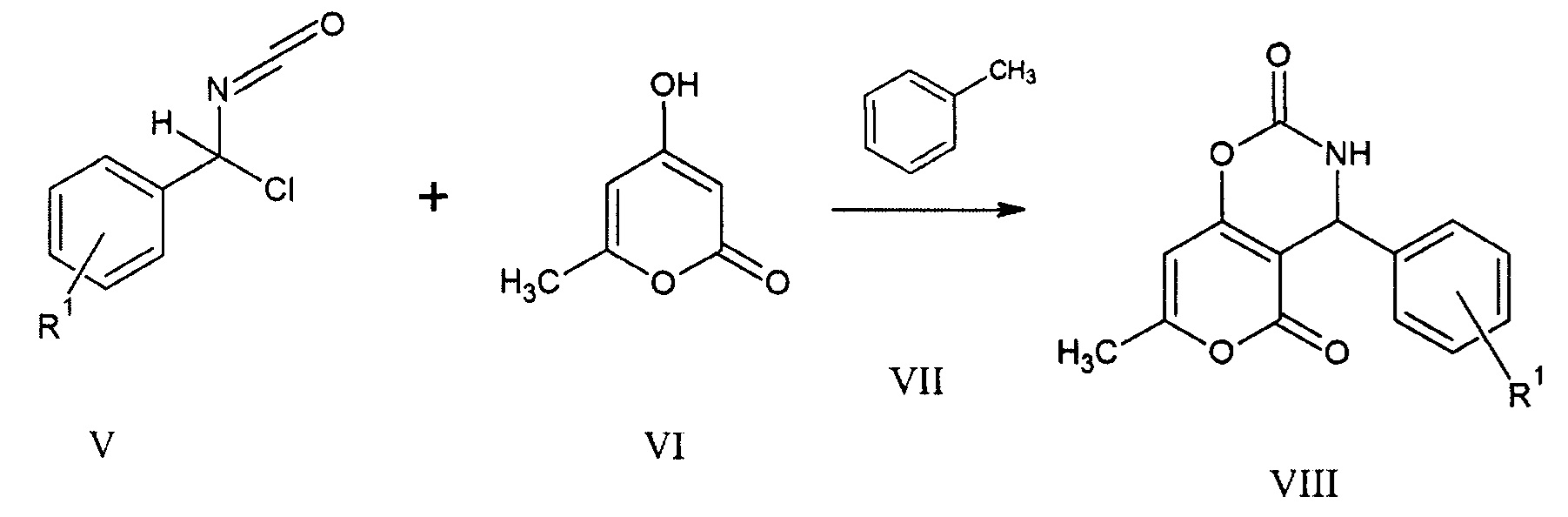
R1=4-H; 2-F; 3-Br; 4-NO2; 3,4-Cl.
Из патентной и научно-технической литературы не выявлены ни способ получения нового, заявляемого авторами соединения, ни сама структура.
Задачей предполагаемой группы изобретений является создание новых неописанных в литературе соединений - 2-замещенных 5-гидроксипирано[2,3-d][1,3]оксазин-4,7-дионов (I).
Техническими результатами, на решение которых направлена группа изобретений, являются получение новых гетероциклических соединений формулы I, которые могут быть использованы в качестве исходных продуктов для синтеза новых гетероциклических систем и в медицине, например, в качестве антимикробного средства; разработка простого способа их получения с высоким выходом продукта.
Поставленная задача осуществляется путем взаимодействия амидов соответствующих карбоновых кислот, выбранных из группы: бензамида, п-метилбензамида, п-бромбензамида, п-нитробензамида, п-метоксибензамида, м-метоксибензамида, стириламида, фуриламида, - с малонилхлоридом в мольном соотношении 1:2 в среде безводного полярного органического растворителя (тетрагидрофуран), реакционную массу перемешивают в течение 12-25 часов при комнатной температуре, полученный осадок целевого продукта отфильтровывают.
Выделяют чистое вещество по схеме:
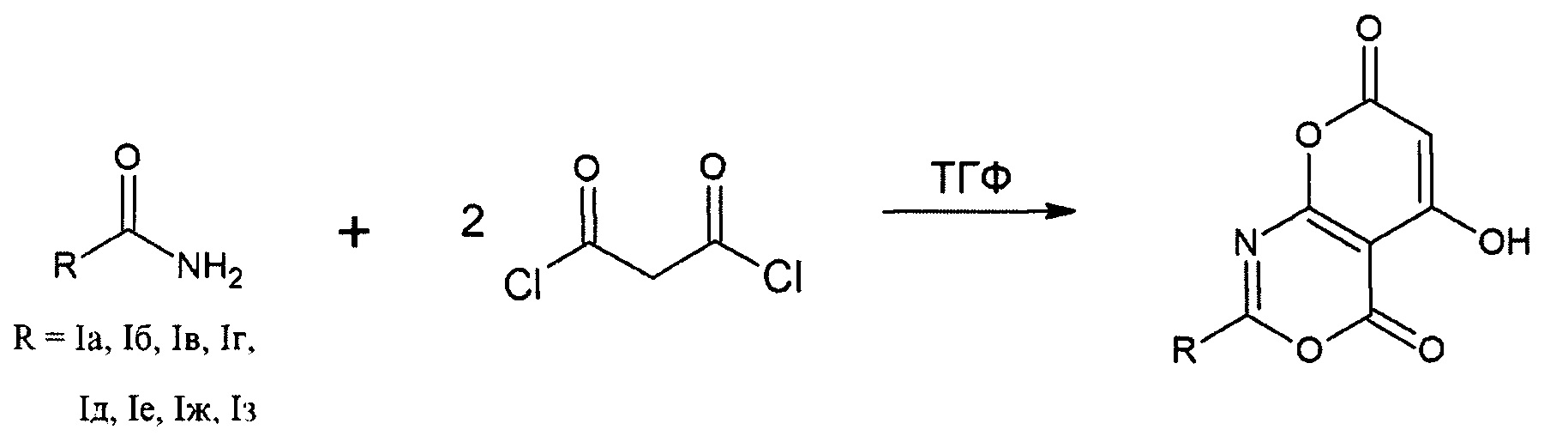
Способ получения 2-замещенных 5-гидроксипирано[2,3-d][1,3]оксазин-4,7-дионов изучен и проведен в лабораторных условиях на стандартном товарном сырье.
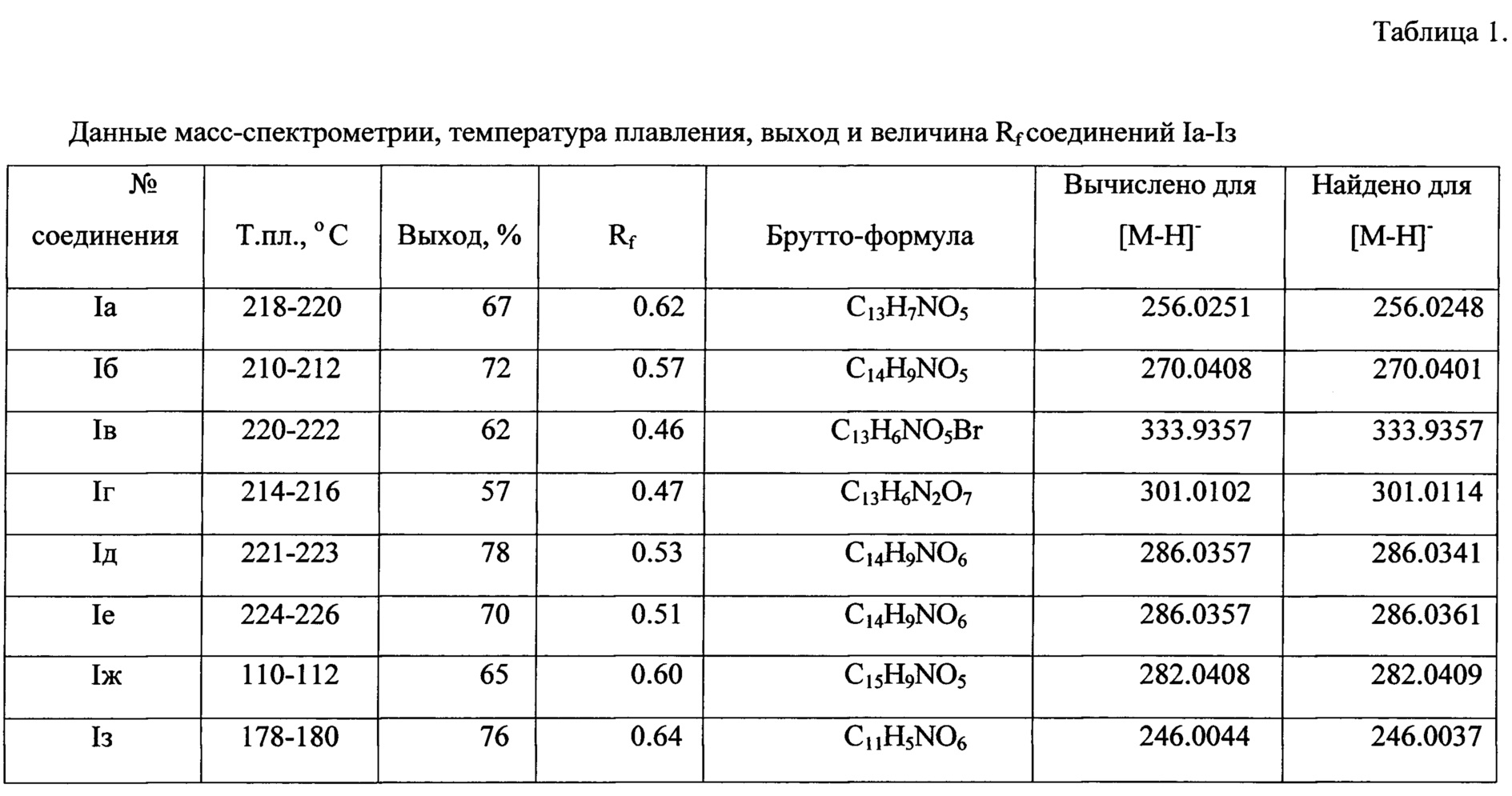
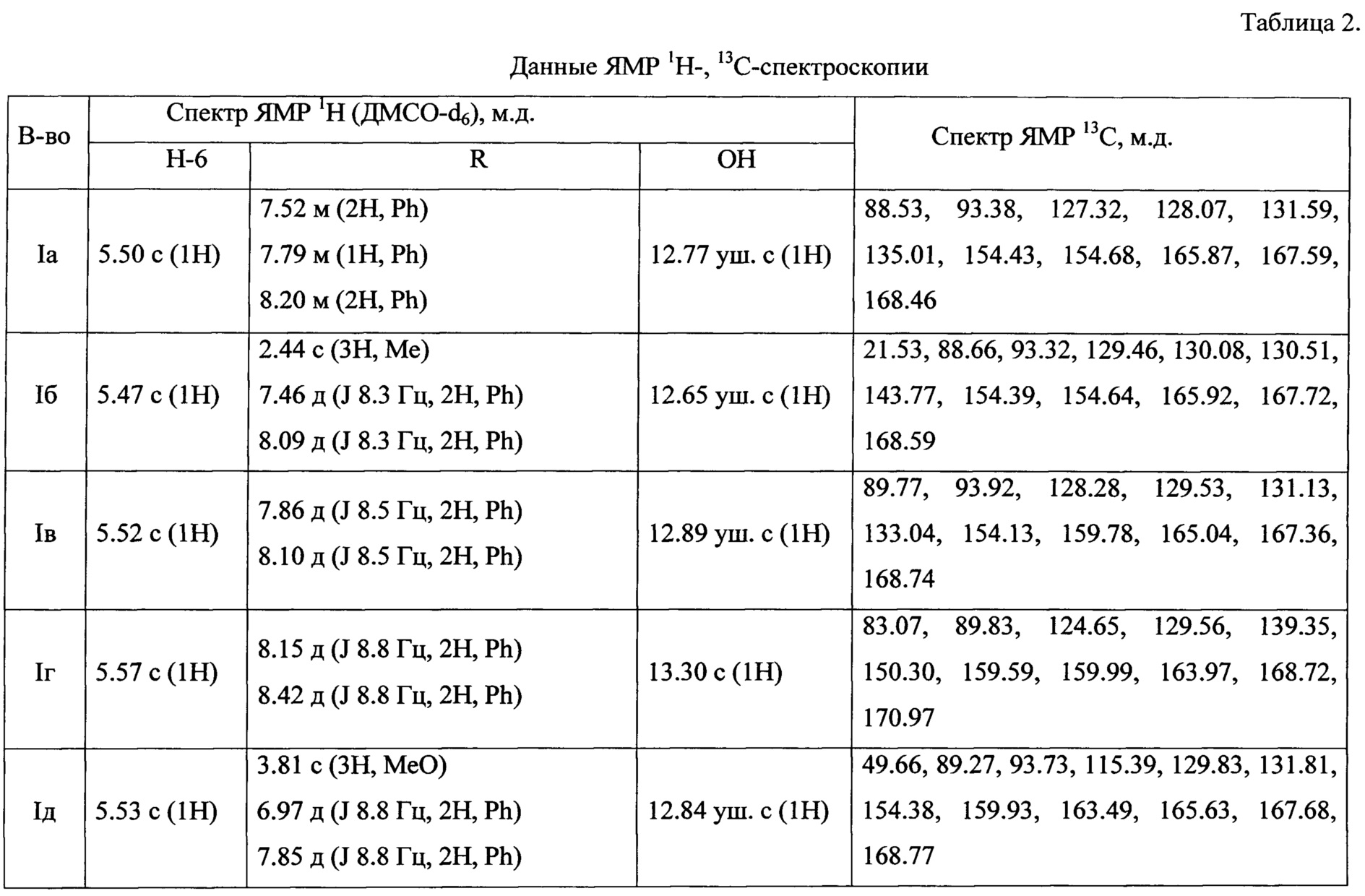
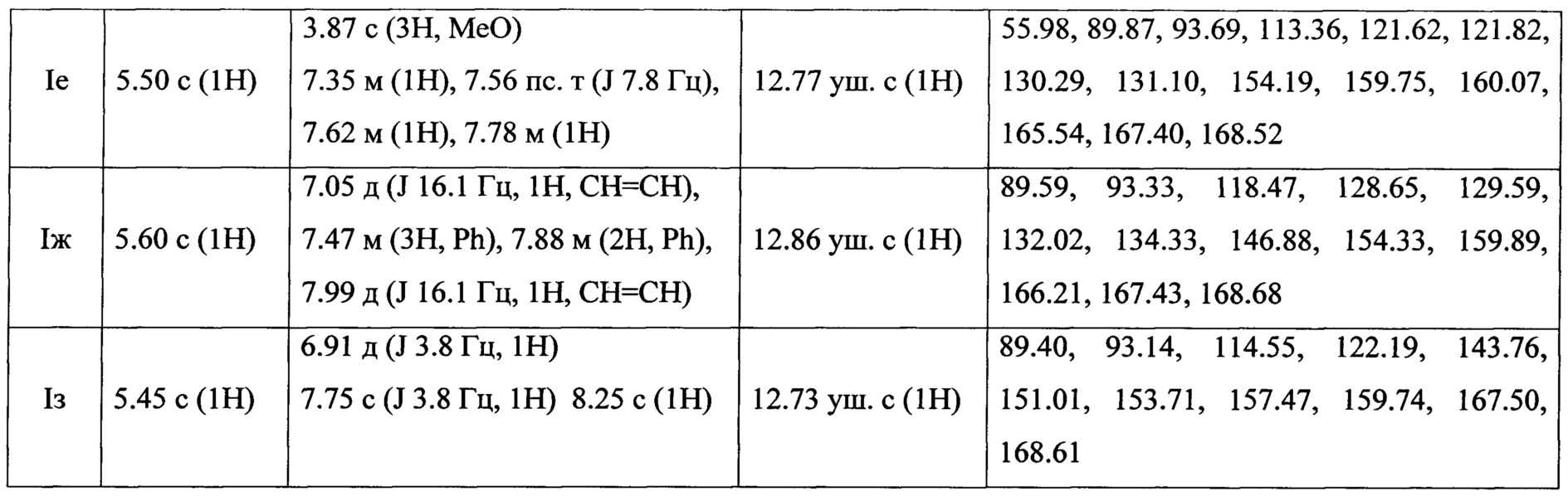
Данные масс-спектрометрии, температура плавления, выход и величина Rf приведены в табл. 1, данные ЯМР 1Н-, 13С-спектроскопии приведены в табл. 2.
Пример 1. Получение 2-фенил-5-гидроксипирано[2,3-d][1,3]оксазин-4,7-диона (Iа).
В плоскодонную колбу емкостью 100 мл загружают 4 г (0,01 моль) бензамида и 25 мл безводного тетрагидрофурана. К полученной суспензии при перемешивании и охлаждении холодной водой прикапывают раствор 9,4 мл малонилхлорида (0,02 моль) в 25 мл тетрагидрофурана, бензамид при этом растворяется. Реакционную смесь перемешивают в течение 18 часов при комнатной температуре. Образовавшийся осадок отфильтровывают под вакуумом и сушат.
Выделенный продукт желтого цвета составляет 5,695 г, 67% от теоретического из расчета на бензамид. Температура плавления 218-220°С. Хроматографическая однородность целевого продукта подтверждалась хроматографированием раствора его в ацетонитриле в системе этанол : этилацетат 4:1. Rf=0,62.
Строение синтезированного вещества было доказано физико-химическими методами идентификации органических соединений: ЯМР 1Н и 13С и масс-спектрометрией.
Пример 2. Получение 2-(4-метилфенил)-5-гидроксипирано[2,3-d][1,3]оксазин-4,7-диона (I6).
В плоскодонную колбу емкостью 100 мл загружают 4 г (0,012 моль) п-метилбензамида и 25 мл безводного тетрагидрофурана. К полученной суспензии при перемешивании и охлаждении холодной водой прикапывают раствор 8,4 мл малонилхлорида (0,024 моль) в 25 мл тетрагидрофурана, п-метилбензамид при этом растворяется. Реакционную смесь перемешивают в течение 15 часов при комнатной температуре. Образовавшийся осадок отфильтровывают под вакуумом и сушат.
Выделенный продукт желтого цвета составляет 5,786 г, 72% от теоретического из расчета на п-метилбензамид. Температура плавления 210-212°С. Хроматографическая однороднсть целевого продукта подтверждалась хроматографированием раствора его в ацетонитриле в системе этанол : этилацетат 4:1. Rf=0,57.
Строение синтезированного вещества было доказано физико-химическими методами идентификации органических соединений: ЯМР 1Н и 13С и масс-спектрометрией.
Пример 3. Получение 2-(4-бромфенил)-5-гидроксипирано[2,3-d][1,3]оксазин-4,7-диона (Iв).
В плоскодонную колбу емкостью 100 мл загружают 4 г (0,011 моль) п-бромбензамида и 25 мл безводного тетрагидрофурана. К полученной суспензии при перемешивании и охлаждении холодной водой прикапывают раствор 5,7 мл малонилхлорида (0,022 моль) в 20 мл тетрагидрофурана, п-бромбензамид при этом растворяется. Реакционную смесь перемешивают в течение 23 часов при комнатной температуре. Образовавшийся осадок отфильтровывают под вакуумом и сушат.
Выделенный продукт ярко-желтого цвета составляет 4,147 г, 62% от теоретического из расчета на п-бромбензамид. Температура плавления 220-222°С. Хроматографическая однородность целевого продукта подтверждалась хроматографированием раствора его в ацетонитриле в системе этанол : этилацетат 4:1. Rf=0,46.
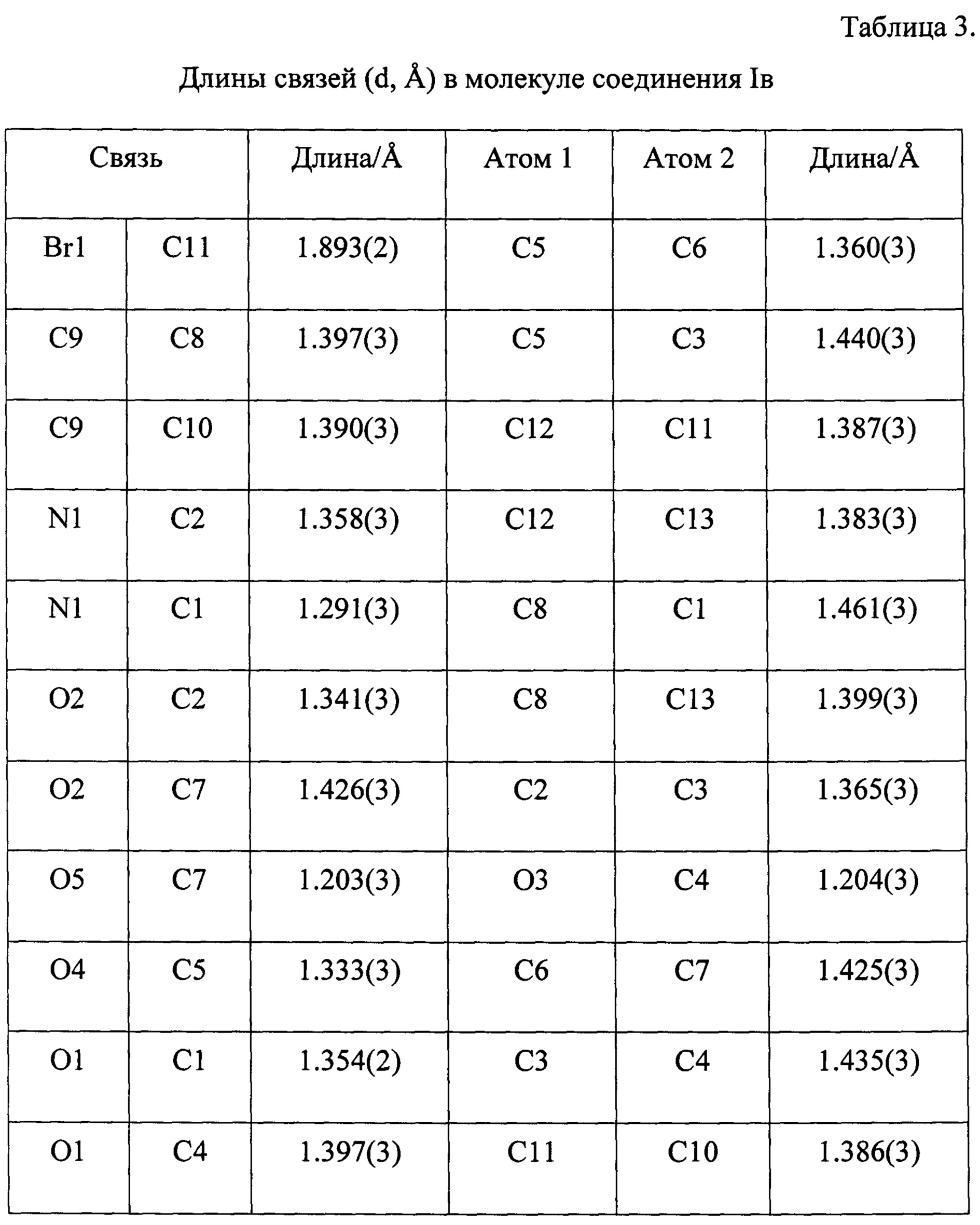
Строение синтезированного вещества было доказано физико-химическими методами идентификации органических соединений: ЯМР 1Н и 13С и масс-спектрометрией, а также рентгеноструктурным анализом.
В спектре ЯМР 1Н полученного соединения в ДМСО-d6присутствуют сигналы протонов бензольных колец (δ 7.86-8.10), сигналы протона СН группы пиранового кольца δ 5.52 и уширенный сигнал протона ОН группы δ 12.89.
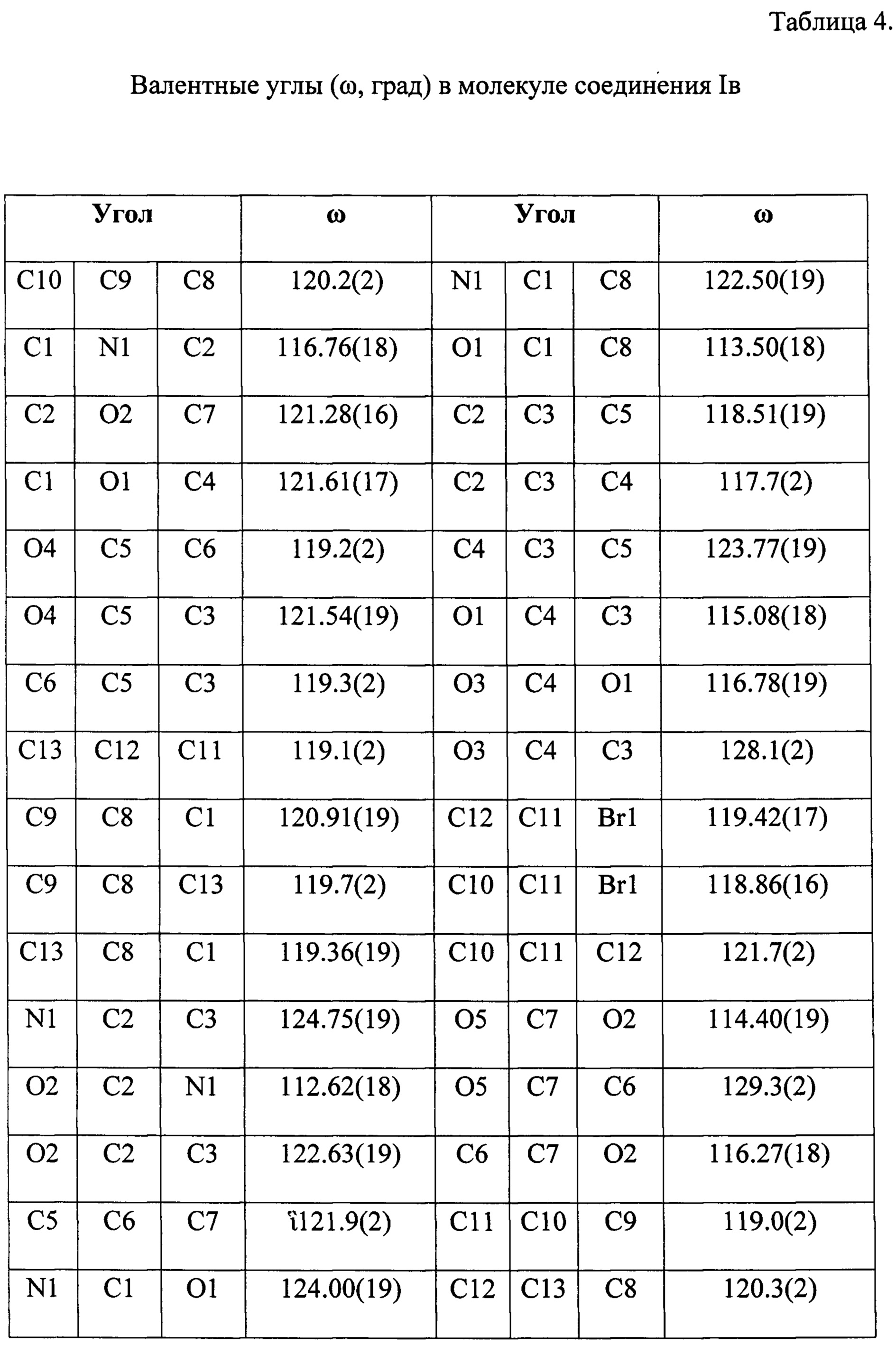
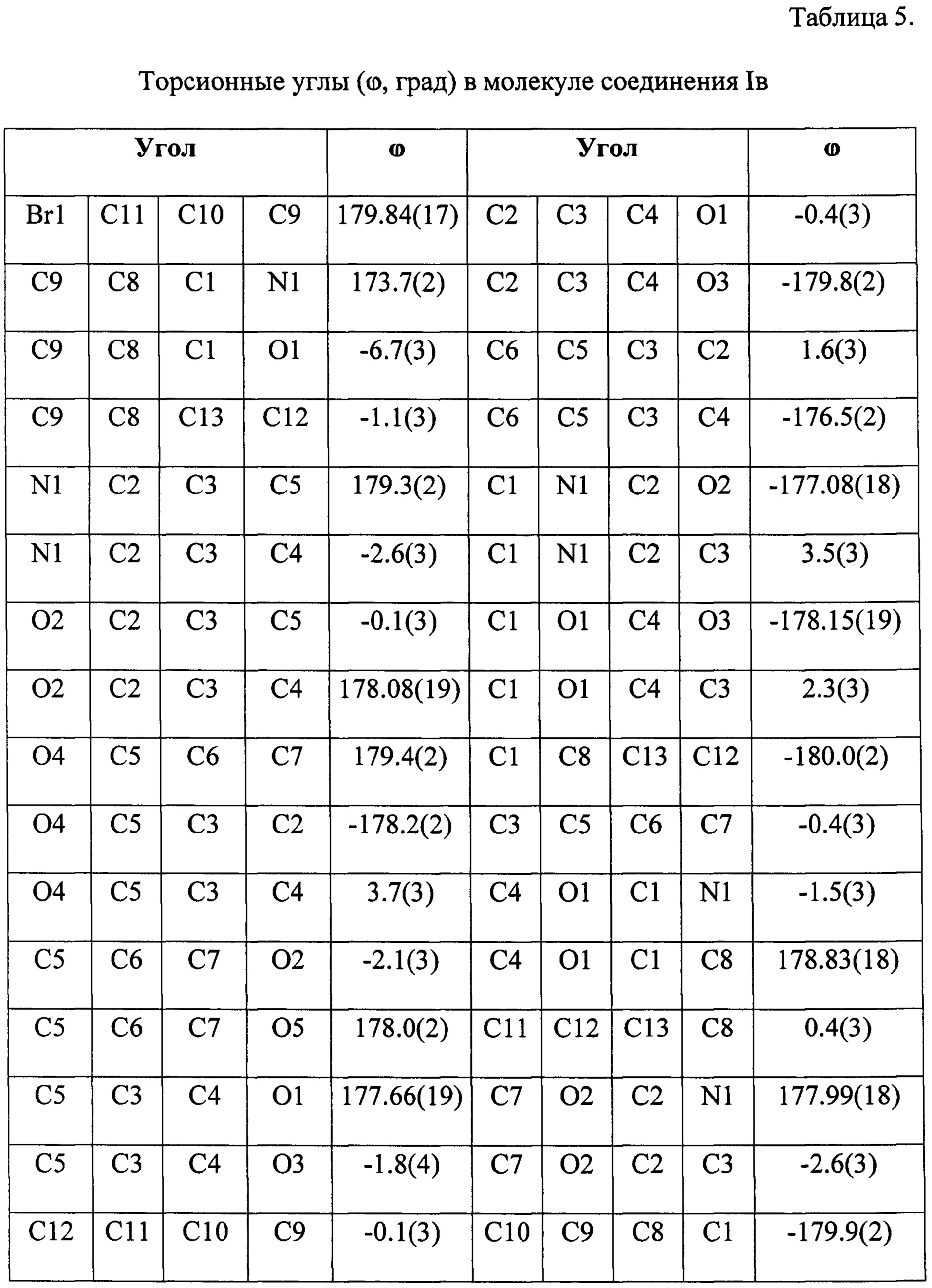
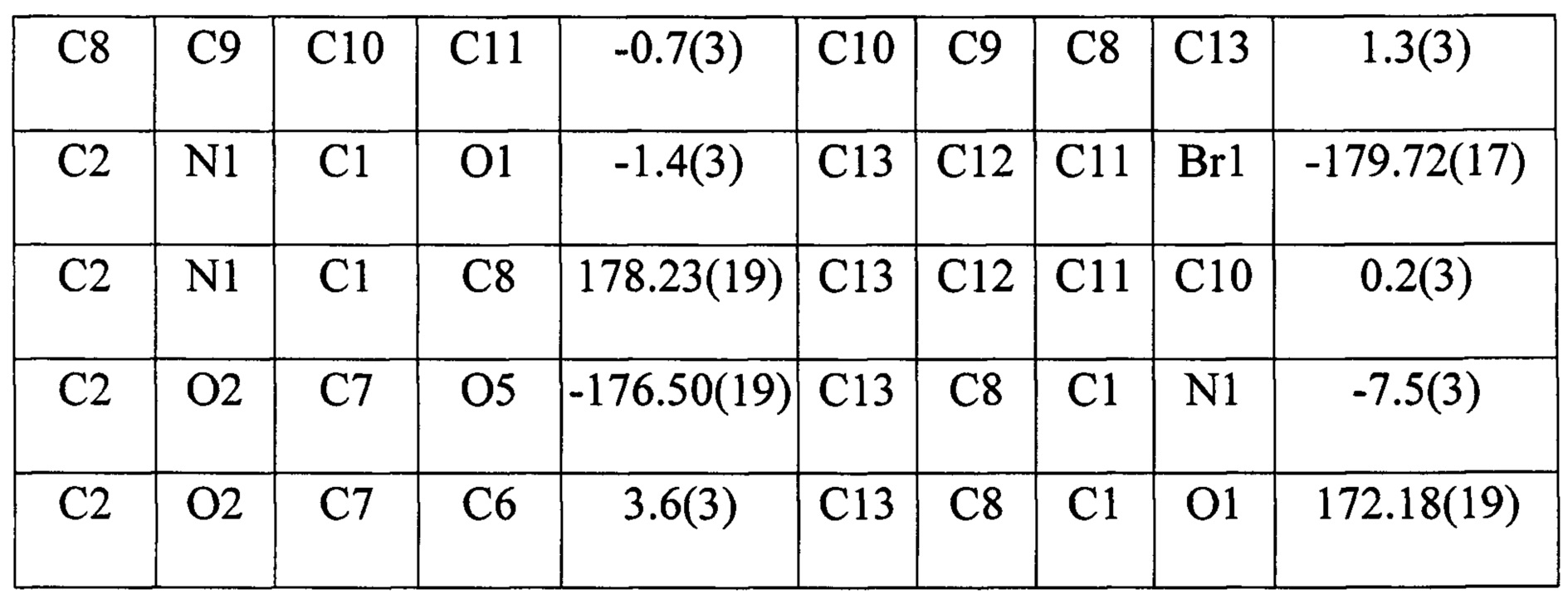
Гетероциклический скелет был однозначно установлен на основании данных рентгеноструктурного анализа. Значения длин связей, валентных и торсионных углов находятся в таблицах 3, 4 и 5 соответственно.
Пример 4. Получение 2-(4-нитрофенил)-5-гидроксипирано[2,3-d][1,3]оксазин-4,7-диона (Iг).
В плоскодонную колбу емкостью 100 мл загружают 4 г (0,012 моль) п-нитробензамида и 25 мл безводного тетрагидрофурана. К полученной суспензии при перемешивании и охлаждении холодной водой прикапывают раствор 6,8 мл малонилхлорида (0,024 моль) в 20 мл тетрагидрофурана, п-нитробензамид при этом растворяется. Реакционную смесь перемешивают в течение 25 часов при комнатной температуре. Образовавшийся осадок отфильтровывают под вакуумом и сушат.
Выделенный продукт ярко-желтого цвета составляет 4,151 г, 57% от теоретического из расчета на п-нитробензамид. Температура плавления 214-216°С. Хроматографическая однородность целевого продукта подтверждалась хроматографированием раствора его в системе этанол : этилацетат 4:1. Rf=0,47.
Строение синтезированного вещества было доказано физико-химическими методами идентификации органических соединений: ЯМР 1Н и 13С и масс-спектрометрией.
Пример 5. Получение 2-(4-метоксифенил)-5-гидроксипирано[2,3-d][1,3]оксазин-4,7-диона (Iд).
В плоскодонную колбу емкостью 100 мл загружают 4 г (0,01 моль) п-метоксибензамида и 25 мл безводного тетрагидрофурана. К полученной суспензии при перемешивании и охлаждении холодной водой прикапывают раствор 7,5 мл малонилхлорида (0,02 моль) в 25 мл тетрагидрофурана, п-метоксибензамид при этом растворяется. Реакционную смесь перемешивают в течение 14 часов при комнатной температуре. Образовавшийся осадок отфильтровывают под вакуумом и сушат.
Выделенный продукт желтого цвета составляет 5,935 г, 78% от теоретического из расчета на п-метоксибензамид. Температура плавления 221-223°С. Хроматографическая однородность целевого продукта подтверждалась хроматографированием раствора его в ацетонитриле в системе этанол : этилацетат 4:1. Rf=0,53.
Строение синтезированного вещества было доказано физико-химическими методами идентификации органических соединений: ЯМР 1Н и 13С и масс-спектрометрией.
Пример 6. Получение 2-(3-метоксифенил)-5-гидроксипирано[2,3-d][1,3]оксазин-4,7-диона (Iе).
В плоскодонную колбу емкостью 100 мл загружают 4 г (0,015 моль) м-метоксибензамида и 25 мл безводного тетрагидрофурана. К полученной суспензии при перемешивании и охлаждении холодной водой прикапывают раствор 7,5 мл малонилхлорида (0,03 моль) в 25 мл тетрагидрофурана, м-метоксибензамид при этом растворяется. Реакционную смесь перемешивают в течение 17 часов при комнатной температуре. Образовавшийся осадок отфильтровывают под вакуумом и сушат.
Выделенный продукт желтого цвета составляет 5,326 г, 70% от теоретического из расчета на м-метоксибензамид. Температура плавления 224-226°С. Хроматографическая однородность целевого продукта подтверждалась хроматографированием раствора его в ацетонитриле в системе этанол : этилацетат 4:1. Rf=0,51.
Строение синтезированного вещества было доказано физико-химическими методами идентификации органических соединений: ЯМР 1Н и 13С и масс-спектрометрией.
Пример 7. Получение 2-стирил-5-гидроксипирано[2,3-d][1,3]оксазин-4,7-диона (Iж).
В плоскодонную колбу емкостью 100 мл загружают 4 г (0,013 моль) стириламида и 25 мл безводного тетрагидрофурана. К полученной суспензии при перемешивании и охлаждении холодной водой прикапывают раствор 8,2 мл малонилхлорида (0,026 моль) в 25 мл тетрагидрофурана, стириламид при этом растворяется. Реакционную смесь перемешивают в течение 22 часов при комнатной температуре. Образовавшийся осадок отфильтровывают под вакуумом и сушат.
Выделенный продукт светло-желтого цвета составляет 5,044 г, 65% от теоретического из расчета на стириламид. Температура плавления 110-112°С. Хроматографическая однородность целевого продукта подтверждалась хроматографированием раствора его в ацетонитриле в системе этанол : этилацетат 4:1. Rf=0,6.
Строение синтезированного вещества было доказано физико-химическими методами идентификации органических соединений: ЯМР 1Н и 13С и масс-спектрометрией.
Пример 8. Получение 2-(фуран-2-ил)-5-гидроксипирано[2,3-d][1,3]оксазин-4,7-диона (Iз).
В плоскодонную колбу емкостью 100 мл загружают 4 г (0,01 моль) фуриламида и 25 мл безводного тетрагидрофурана. К полученной суспензии при перемешивании и охлаждении холодной водой прикапывают раствор 10,2 мл малонилхлорида (0,02 моль) в 25 мл тетрагидрофурана, фуриламид при этом растворяется. Реакционную смесь перемешивают в течение 18 часов при комнатной температуре. Образовавшийся осадок отфильтровывают под вакуумом и сушат.
Выделенный продукт зеленовато-желтого цвета составляет 6,769 г, 76% от теоретического из расчета на фуриламид. Температура плавления 178-180°С. Хроматографическая однородность целевого продукта подтверждалась хроматографированием раствора его в ацетонитриле в системе этанол : этилацетат 4:1. Rf=0,64.
Строение синтезированного вещества было доказано физико-химическими методами идентификации органических соединений: ЯМР 1Н и 13С и масс-спектрометрией.
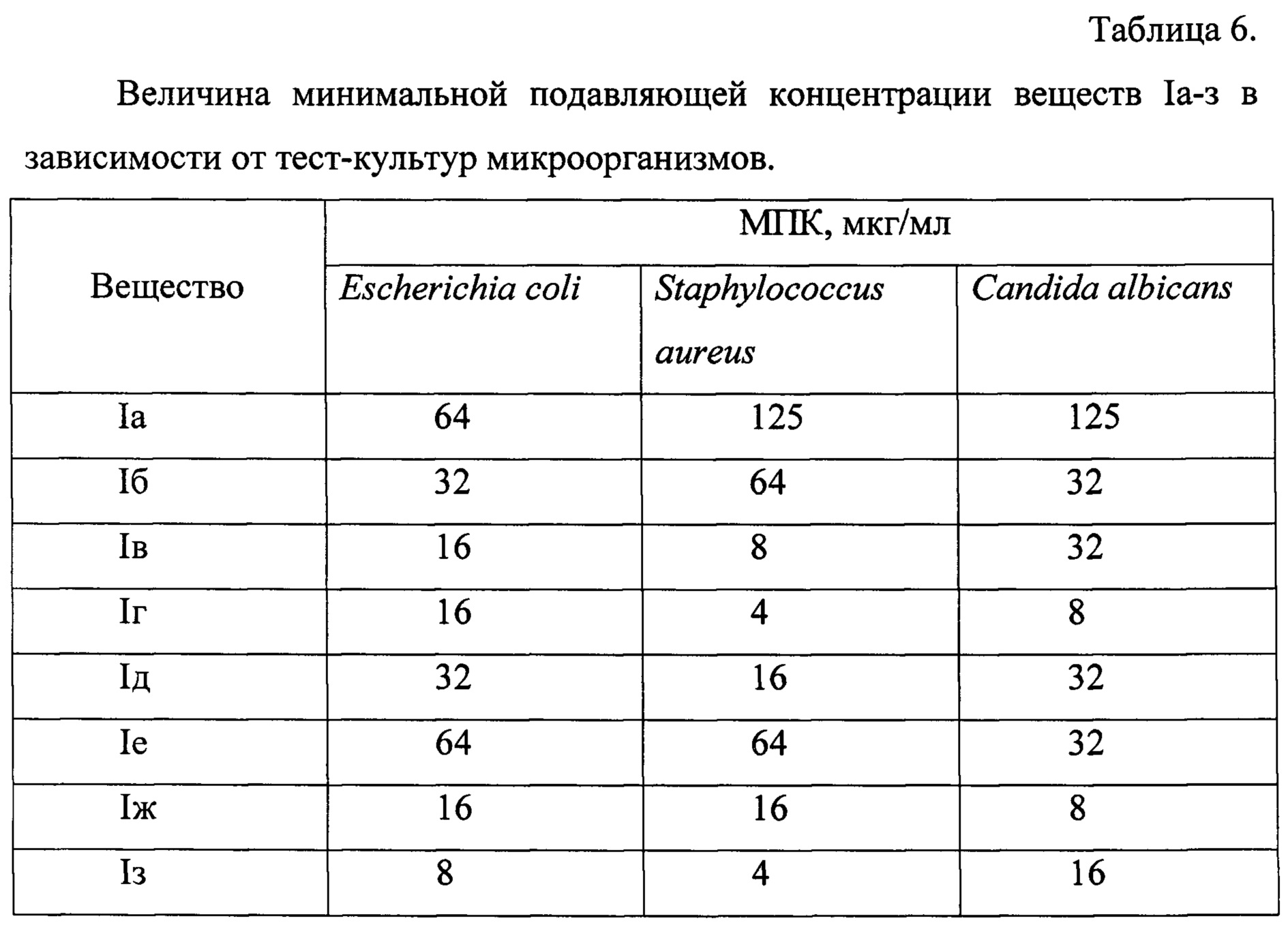
Пример 9. Соединения формулы I (Iа, Iб, Iв, Iг, Iд, Iе, Iж, Iз) обладают антимикробной активностью. Определение минимальных подавляющих концентраций (МПК) проводили методом серийных разведений в мясопептонном бульоне в отношении тест-культур Staphylococcus aureus АТСС 6538-Р и Escherichia coli АТСС и в жидкой среде Сабуро в отношении тест-культуры Candida albicans NCTC 885-653, рекомендованных Государственной Фармакопеей [Государственная фармакопея. - 12-е изд. - М., 2007. - Ч. 1. - 312 с.] (табл. 6). Исследуемые соединения ограниченно растворяются в воде, поэтому в качестве растворителя использовали 50% раствор ДМСО, не подавляющий роста ни одной из использованных тест-культур в условиях эксперимента. Величина МПК соединений Iв, Iг и Iз в отношении St. aureus составляет 8 мкг/мл, 4 мкг/мл и 4 мкг/мл соответственно, что находится на уровне широко используемых на практике антибиотиков (ванкомицин и тейкопланин - 0,3-12,5 мкг/мл).
Получена новая группа соединений формулы I - 2-замещенные 5-гидроксипирано[2,3-d][1,3]оксазин-4,7-дионы, которые могут быть использованы для синтеза новых гетероциклических соединений и в медицине в качестве потенциального антимикробного средства; разработан простой способ их синтеза.
![2-замещенные 5-гидроксипирано[2,3-d][1,3]оксазин-4,7-дионы и способ их получения](https://fips.edrid.ru/images/rid/12/f5/29/710ddb161e5d45de60b42c7d4747565f.jpg)
![2-замещенные 5-гидроксипирано[2,3-d][1,3]оксазин-4,7-дионы и способ их получения](https://fips.edrid.ru/images/rid/12/f5/29/33333ab384969648dd8b378063b35700.jpg)
![2-замещенные 5-гидроксипирано[2,3-d][1,3]оксазин-4,7-дионы и способ их получения](https://fips.edrid.ru/images/rid/12/f5/29/203a56b6e2ef65a9dae38791b3f99862.jpg)

