Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ ПРОДУКТА ДЛЯ РЕГЕНЕРАЦИИ ВОЗДУХА
Вид РИД
Изобретение
Изобретение относится к способам получения продуктов для регенерации воздуха на основе надпероксида калия, используемых в изолирующих дыхательных аппаратах (ИДА).
Известен способ получения продукта для регенерации воздуха [патент РФ №2599664 МПК A62D 9/00, 2016 г.]. Способ получения продукта для регенерации воздуха осуществляют следующим образом. Готовят исходный щелочной раствор пероксида водорода, для чего в раствор пероксида водорода с концентрацией от 50 до 85% массовых при интенсивном перемешивании вводят сульфат магния. После его полного растворения (примерно 1-3 минуты) в жидкую фазу вводят тетрабораты щелочных металлов, гидроксид натрия и гидроксид калия. Гидроксид калия вводят в систему через 10-15 минут после введения гидроксида натрия. Мольное соотношение исходных компонентов должно составлять следующие величины: пероксид водорода/сульфат магния (H2O2/MgSO4)=450÷670; пероксид водорода/тетраборат щелочного металла (Н2О2/Ме2В4O7)=160÷1000; пероксид водорода/гидроксид натрия (H2O2/NaOH)=7,0÷66,7; пероксид водорода/гидроксид калия (Н2О2/КОН)=1,60÷2,00. Добавление гидроксидов натрия и калия проводят таким образом, чтобы температура жидкой фазы тройной системы МеОН-H2O2-H2O (щелочной раствор пероксида водорода) не превышала 50°С. Далее щелочной раствор пероксида водорода не менее чем через 10-15 минут равномерно наносят на индифферентную пористую матрицу необходимых геометрических размеров любым известным способом (пропитка, аэрозольное напыление и др.) и проводят дегидратацию либо сушкой в вакууме при температуре 30÷150°С, либо в потоке осушенного декарбонизованного газа при атмосферном давлении при температуре 60÷220°С. По окончании дегидратации готовый продукт собирают в специальный контейнер.
Однако продукт для регенерации воздуха, полученный известным способом, характеризуется недостаточно высокой степенью отработки по диоксиду углерода, что приводит к увеличению массогабаритных параметров индивидуальных дыхательных аппаратов. Последнее крайне неудобно при эксплуатации ИДА пользователями, вынужденными в силу специфики условий труда постоянно носить их (например, шахтеры). Кроме того, данный способ недостаточно экономичен и безопасен.
Задачей изобретения является разработка способа получения продукта для регенерации воздуха, имеющего улучшенные эксплуатационные характеристик при его работе в составе индивидуальных дыхательных аппаратов.
Технический результат заключается в получении продукта для регенерации воздуха, имеющего высокую степень отработки по диоксиду углерода при его эксплуатации в индивидуальных дыхательных аппаратах.
Дополнительным техническим результатом является повышение экономичности и безопасности процесса.
Технический результат достигается тем, что в способе получения продукта для регенерации воздуха путем смешения раствора пероксида водорода с сульфатом магния и гидроксидами натрия и калия, нанесение полученного щелочного раствора пероксида водорода на индифферентную пористую матрицу и последующую дегидратацию жидкой фазы, в раствор пероксида водорода после его смешения с сульфатом магния при мольном соотношении пероксид водорода/сульфат магния (H2O2/MgSO4)=450÷700 через 1-3 минуты вводят ортоборную кислоту при мольном соотношении пероксид водорода/ортоборная кислота (H2O2/Н3ВО3)=285÷850.
При этом гидроксиды натрия и калия вводят в жидкую фазу одновременно двумя порциями с интервалом 6-10 минут таким образом, чтобы температура в зоне синтеза не превышала 60°С.
Изобретение позволяет достигнуть заявленный технический результат по следующим обстоятельствам. Как хорошо известно специалистам, работающим в технике процессов хемосорбции и регенерации воздуха, поглощение из газообразной фазы сорбата (CO2) происходит в тонком слое жидкой фазы, образующейся на поверхности хемосорбентов. Часто лимитирующей стадией процессов хемосорбции является внутренняя диффузия молекул сорбата в объем жидкой фазы и образование в ней ионизированных молекул, вступающих в химические реакции. При нейтрализации ортоборной кислоты щелочами в водных растворах не образуются ортобораты, содержащие ион (ВО3)3-, поскольку ортобораты практически полностью гидролизуются вследствие слишком малой константы образования [В(ОН)4]-. В растворе образуются тетрабораты, метабораты и соли других полиборных кислот (nB2O2⋅mH2O), не существующие в свободном состоянии (и которые по этой причине невозможно ввести в жидкую фазу в виде исходных соединений), что хорошо известно из курса неорганической химии [Карапетьянц М.X., Дракин С.И. Общая и неорганическая химия. М.: Химия 1994]. Присутствие в жидкой фазе в указанном количестве солей щелочных металлов полиборных кислот приводит к снижению вязкости поверхностной пленки водного раствора, образующейся на поверхности продукта для регенерации воздуха, что приводит к усилению диффузионных процессов на границах раздела фаз, в жидкой фазе и повышению растворимости и ионизации диоксида углерода в водном растворе поверхностной пленки. В результате за счет интенсификации массообменных процессов на границах газ - жидкость и жидкость - твердая фаза повышается степень отработки продукта для регенерации воздуха по диоксиду углерода при его эксплуатации в ИДА.
Необходимо отметить, что взаимодействие пероксида водорода и гидроксидов щелочных металлов при нормальных условиях - ярко выраженный экзотермический процесс, сопровождающийся каталитическим разложением пероксидных продуктов под воздействием гидроксид - анионов [У. Шамб, Ч. Сеттерфилд, Р. Вентворс. Перекись водорода, - М.: Иностранная литература, - 1958. - 578 с.] и выделением атомарного кислорода. Это не только приводит к снижению содержания пероксидных соединений в продукте синтеза, но и создает дополнительную угрозу возникновения «кислородного» пожара, локализовать который практически невозможно. Поэтому следует отметить, что полученный щелочной раствор пероксида водорода при температуре 60°С за 8 часов (продолжительность технологического цикла) теряет не более 180 л активного кислорода, т.е. меньше, чем щелочной раствор пероксида водорода, приготовленный с использованием технологических приемов и соотношения компонентов, описанных в патенте РФ №2599664, где щелочной раствор пероксида водорода при температуре 25°С за 8 часов (как следует из примеров 1÷6) теряет в среднем 199,2 л активного кислорода. Таким образом, здесь абсолютно уместно говорить об увеличении стабилизирующего влияния присутствующих в щелочном растворе пероксида водорода ионов на химическую устойчивость жидкой фазы тройной системы МеОН-H2O2-H2O при более высокой температуре в зоне синтеза и повышении безопасности процесса получения продукта для регенерации воздуха. Механизм стабилизации различных растворов пероксида водорода неизвестен [Г.А. Серышев. Химия и технология перекиси водорода, - Л.: Химия, - 1984. - С. 182.]. Поэтому сложно однозначно оценить влияние того или иного иона или их ассоциатов, содержащихся в многокомпонентном растворе, на стабильность системы в целом. Нахождение стабилизатора для конкретной цели - задача, которая решается только эмпирическим путем. Но было отмечено, что в раствор пероксида водорода в первую очередь следует вводить сульфат магния, после его растворения вводить в полученный раствор ортоборную кислоту, а гидроксиды щелочных металлов следует вводить двумя порциями с интервалом 6-10 минут.
Кроме того, использование ортоборной кислоты позволяет ускорить процесс приготовления щелочного раствора пероксида водорода (раздельная загрузка щелочей предполагает наличие или 2 бункеров, или поочередную засыпку щелочей в бункеры, что, apriory, занимает больше времени) и осуществлять его приготовление и хранение в течение производственного цикла при более высокой температуре (что приведет к отказу от охлаждения щелочного раствора пероксида водорода). Перечисленные выше аспекты положительно отражаются на экономичности способа получения продукта для регенерации воздуха.
Способ получения продукта для регенерации воздуха осуществляют следующим образом. В раствор пероксида водорода с концентрацией от 50 до 85% массовых при интенсивном перемешивании вводят сульфат магния при мольном соотношении пероксид водорода/сульфат магния (H2O2/MgSO4)=450÷700. После его полного растворения (примерно 1÷3 минуты) в жидкую фазу вводят ортоборную кислоту при мольном соотношении пероксид водорода/ортоборная кислота (H2O2/Н3ВО3)=285÷850, гидроксид натрия и гидроксид калия. Гидроксиды натрия и калия вводят в систему одновременно двумя порциями с интервалом 6-10 минут таким образом, чтобы температура в зоне реакции не превышала 60°С. Такой режим позволяет максимально нивелировать влияние температурного фактора на разложение пероксидных продуктов. Полученный щелочной раствор пероксида водорода равномерно наносят на индифферентную пористую матрицу необходимых геометрических размеров любым известным способом (пропитка, аэрозольное напыление и др.) и проводят дегидратацию. Дегидратацию пропитанной исходным щелочным раствором пероксида водорода индифферентной пористой матрицы осуществляют либо сушкой в вакууме при температуре 30÷150°С, либо в потоке осушенного декарбонизованного газа при атмосферном давлении и при температуре 60÷220°С. По окончании дегидратации готовый продукт собирают в специальный контейнер. Далее полученный продукт формуют различными способами для придания определенной геометрической формы (гранулы, блоки, таблетки и др.) и размещают в патроне ИДА.
В примерах 1-6 приведены данные о получении заявляемым способом продукта для регенерации воздуха и потере жидкой фазой тройной системы МеОН-H2O2-H2O (щелочным раствором пероксида водорода) активного кислорода за 8 часов (время производственной смены) при 60°С.
Пример 1.
К 56,82 л водного 50% раствора пероксида водорода при непрерывном перемешивании добавляют 267 г сульфата магния (H2O2/MgSO4=450). После растворения MgSO4 примерно через 3 минуты в жидкую фазу вводят 73,0 г ортоборной кислоты (H2O2/H3BO3=850), затем одновременно 66,7 г твердого 90% гидроксида натрия и 3,1 кг твердого 90% гидроксида калия. Примерно через 6 минут после прохождения реакции нейтрализации и равномерного распределения всех введенных компонентов по объему жидкой фазы одновременно добавляют 600,3 г гидроксида натрия (H2O2/NaOH=66,7) и 28,0 кг твердого 90% гидроксида калия (H2O2/КОН=2,0). Добавление второй порции щелочей производят таким образом, чтобы температура жидкой фазы не превышала 60°С. Полученный щелочной раствор пероксида водорода наносят аэрозольным напылением на индифферентную пористую матрицу необходимых размеров и проводят дегидратацию жидкой фазы на матрице сушкой в вакууме при температуре 30÷150°С и остаточном давлении 0,95 атм.
Получают 38,8 кг продукта, содержащего 74,06% КO2, 14,68% КОН, 4,6% матрицы, 1,28% Na2O2, 0,41% NaOH, 3,83% H2O, 0,46% полиборатов лития и натрия и 0,68% MgSO4. Потеря щелочным раствором пероксида водорода активного кислорода за 8 часов составила 176 л.
Пример 2.
К 51,7 л водного 50% раствора пероксида водорода при непрерывном перемешивании добавляют 210 г сульфата магния (H2O2/MgSO4=520). После растворения MgSO4 примерно через 2,5 минуты в жидкую фазу вводят 75,3 г ортоборной кислоты (H2O2/Н3ВО3=750), затем одновременно 133,4 г твердого 90% гидроксида натрия и 3,1 кг твердого 90% гидроксида калия. Примерно через 7 минут после прохождения реакции нейтрализации и равномерного распределения всех введенных компонентов по объему жидкой фазы одновременно добавляют 1,2 кг гидроксида натрия (H2O2/NaOH=15,2) и 28,0 кг твердого 90% гидроксида калия (H2O2/КОН=1,82). Добавление второй порции щелочей производят таким образом, чтобы температура жидкой фазы не превышала 60°С. Полученный щелочной раствор пероксида водорода наносят аэрозольным напылением на индифферентную пористую матрицу необходимых размеров и проводят дегидратацию жидкой фазы на матрице сушкой в вакууме при температуре 30÷150°С и остаточном давлении 0,95 атм. Получают 40,50 кг продукта, содержащего 69,46% КO2, 15,61% КОН, 3,95% Na2O2, 4,4% матрицы, 1,60% NaOH, 3,90% H2O, 0,48% полиборатов натрия и калия и 0,6% MgSO4. Потеря щелочным раствором пероксида водорода активного кислорода за 8 часов составила 173 л.
Пример 3.
К 45,45 л водного 50% раствора пероксида водорода при непрерывном перемешивании добавляют 160 г сульфата магния (H2O2/MgSO4=600). После растворения MgSO4 примерно через 2 минуты в жидкую фазу вводят 76,4 г ортоборной кислоты (H2O2/Н3ВО3=650), затем одновременно 445 г твердого 90% гидроксида натрия и 3,1 кг твердого 90% гидроксида калия. Примерно через 7,5 минут после прохождения реакции нейтрализации и равномерного распределения всех введенных компонентов по объему жидкой фазы одновременно добавляют 4,0 кг гидроксида натрия (H2O2/NaOH=8) и 28,0 кг твердого 90% гидроксида калия (H2O2/КОН=1,6). Добавление второй порции щелочей производят таким образом, чтобы температура жидкой фазы не превышала 60°С. Полученный щелочной раствор пероксида водорода наносят аэрозольным напылением на индифферентную пористую матрицу необходимых размеров и проводят дегидратацию жидкой фазы на матрице сушкой в потоке осушенного декарбонизованного воздуха при температуре 200°С. Получают 42,34 кг продукта, содержащего 64,88% КO2, 16,37% КОН, 8,0% Na2O2, 3,9% матрицы, 2,12% NaOH, 3,31% H2O, 0,83% полиборатов натрия и калия и 0,6% MgSO4. Потеря щелочным раствором пероксида водорода активного кислорода за 8 часов составила 168 л.
Пример 4.
К 27,23 л водного 85% раствора пероксида водорода при непрерывном перемешивании добавляют 166,6 г сульфата магния (H2O2/MgSO4=670). После растворения MgSO4 примерно через 3 минуты в жидкую фазу вводят 115,3 г ортоборной кислоты (H2O2/Н3ВО3=500), затем одновременно 445 г твердого 90% гидроксида натрия и 3,1 кг твердого 90% гидроксида калия. Примерно через 10 минут после прохождения реакции нейтрализации и равномерного распределения всех введенных компонентов по объему жидкой фазы одновременно добавляют 5,32 кг гидроксида натрия (H2O2/NaOH=7) и 28,0 кг твердого 90% гидроксида калия (H2O2/КОН=1,86). Добавление второй порции щелочей производят таким образом, чтобы температура жидкой фазы не превышала 60°С. Полученный щелочной раствор пероксида водорода наносят аэрозольным напылением на индифферентную пористую матрицу необходимых размеров и проводят дегидратацию жидкой фазы на матрице сушкой в потоке осушенного декарбонизованного воздуха при температуре 180°С. Получают 43,76 кг продукта, содержащего 66,15% КO2, 12,7% КОН, 9,43% Na2O2, 3,7% матрицы, 2,74% NaOH, 3,11% H2O, 1,65% полиборатов натрия и калия и 0,52% MgSO4. Потеря щелочным раствором пероксида водорода активного кислорода за 8 часов составила 174 л.
Пример 5.
К 46,88 л водного 50% раствора пероксида водорода при непрерывном перемешивании добавляют 171 г сульфата магния (H2O2/MgSO4=580). После растворения MgSO4 примерно через 2,5 минуты в жидкую фазу вводят 170,7 г ортоборной кислоты (H2O2/Н3ВО3=300), затем одновременно 122 г твердого 90% гидроксида натрия и 3,1 кг твердого 90% гидроксида калия. Примерно через 9 минут после прохождения реакции нейтрализации и равномерного распределения всех введенных компонентов по объему жидкой фазы одновременно добавляют 1,1 кг гидроксида натрия (H2O2/NaOH=30) и 28,0 кг твердого 90% гидроксида калия (H2O2/КОН=1,65). Добавление второй порции щелочей производят таким образом, чтобы температура жидкой фазы не превышала 60°С. Полученный щелочной раствор пероксида водорода наносят аэрозольным напылением на индифферентную пористую матрицу необходимых размеров и проводят дегидратацию жидкой фазы на матрице сушкой в вакууме при температуре 30÷150°С и остаточном давлении 0,95 атм. Получают 40,11 кг продукта, содержащего 73,85% КO2, 13,37% КОН, 2,52% Na2O2, 3,85% матрицы, 0,91% NaOH, 3,57% H2O, 1,54% полиборатов натрия и калия и 0,39% MgSO4. Потеря щелочным раствором пероксида водорода активного кислорода за 8 часов составила 180 л.
Пример 6.
К 48,9 л водного 50% раствора пероксида водорода при непрерывном перемешивании добавляют 147,7 г сульфата магния (H2O2/MgSO4=700). После растворения MgSO4 примерно через 2,5 минуты в жидкую фазу вводят 187,4 г ортоборной кислоты (H2O2/H3BO3=285), затем одновременно 76 г твердого 90% гидроксида натрия и 3,1 кг твердого 90% гидроксида калия. Примерно через 10 минут после прохождения реакции нейтрализации и равномерного распределения всех введенных компонентов по объему жидкой фазы одновременно добавляют 689 г гидроксида натрия (H2O2/NaOH=50) и 28,0 кг твердого 90% гидроксида калия (H2O2/КОН=1,72). Добавление второй порции щелочей производят таким образом, чтобы температура жидкой фазы не превышала 60°С. Полученный щелочной раствор пероксида водорода наносят аэрозольным напылением на индифферентную пористую матрицу необходимых размеров и проводят дегидратацию жидкой фазы на матрице сушкой в вакууме при температуре 30÷150°С и остаточном давлении 0,95 атм. Получают 39,0 кг продукта, содержащего 74,84% КO2, 12,59% КОН, 4,1% матрицы, 1,38% Na2O2, 0,48% NaOH, 4,12% H2O, 2,03% полиборатов натрия и калия и 0,46% MgSO4. Потеря щелочным раствором пероксида водорода активного кислорода за 8 часов составила 166 л.
Продукт для регенерации воздуха, полученный заявляемым способом, испытан в патроне серийного индивидуального дыхательного аппарата СПИ - 20, используемого гражданским населением, на установке «Искусственные легкие».
Испытания на установке «Искусственные легкие» проводили при следующих условиях:
|
Объемы кислорода и диоксида углерода указаны при 10°С и 101,3 кПа, легочная вентиляция - при 37°С и 101,3 кПа.
Для сравнения в тех же условиях испытывался продукт для регенерации воздуха, специально изготовленный по способу, описанному в патенте РФ №2599664 (пример 3). Все продукты для регенерации воздуха имели форму одинакового размера и плотности. Время защитного действия ИДА определяли как время от начала его работы до того момента, когда концентрация СО2 в потоке газо-воздушной смеси на линии «вдоха» установки «Искусственные легкие» достигала 3%. Результаты испытаний представлены в таблице. В таблице так же представлены данные о потере жидкой фазой активного кислорода за 8 часов при н.у. в процессе синтеза продукта для регенерации воздуха (данные о 6 этом параметре продукта для регенерации воздуха по примеру 3 патента РФ №2599664 взяты из описания патента).
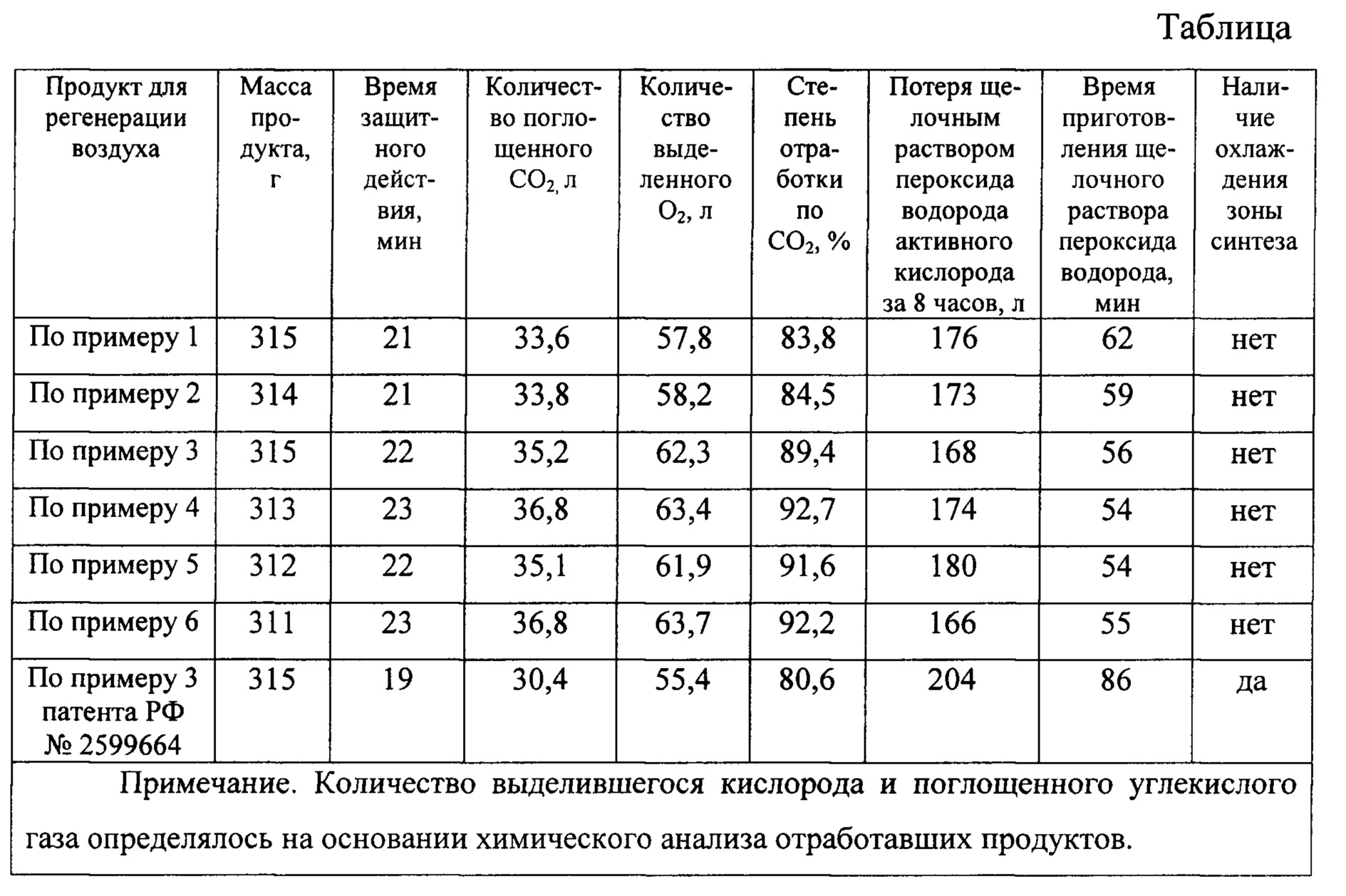
Из представленных в таблице данных следует, что продукт для регенерации воздуха, полученный по изобретению, по таким важным эксплуатационным характеристикам, как степень отработки по диоксиду углерода и время защитного действия, превосходит аналогичные показатели продукта для регенерации воздуха, полученного по патенту РФ №2599664.
Перечисленные выше позитивные аспекты, связанные с процессом регенерации воздуха в патроне ИДА, обусловлены наличием в продукте для регенерации воздуха в указанном количестве солей щелочных металлов полиборных кислот и способом их введения в продукт. Это приводит к снижению вязкости поверхностной пленки водного раствора, образующейся на поверхности продукта, что, в свою очередь, приводит к усилению диффузионных процессов на границах раздела фаз, в жидкой фазе и повышению растворимости и ионизации реагирующих веществ в водном растворе поверхностной пленки. В результате за счет интенсификации массообменных процессов на границах газ - жидкость и жидкость - твердая фаза повышается степень отработки по диоксиду углерода продукта для регенерации воздуха при его эксплуатации в индивидуальных дыхательных аппаратах, что позволяет снизить массогабаритные параметры изделия.
Кроме того, присутствие в щелочном растворе пероксида водорода в указанном количестве солей щелочных металлов полиборных кислот и последовательность введения в жидкую фазу исходных компонентов позволяют сократить время приготовления щелочного раствора пероксида водорода, повысить температуру в зоне синтеза (т.е. снизить затраты на охлаждение зоны реакции) и снизить в течение производственного цикла выделение атомарного кислорода, т.е. повысить экономичность и безопасность процесса.
Способ получения продукта для регенерации воздуха путем смешения раствора пероксида водорода с сульфатом магния и гидроксидами натрия и калия, нанесением полученного щелочного раствора пероксида водорода на индифферентную пористую матрицу с последующей дегидратацией жидкой фазы, отличающийся тем, что в раствор пероксида водорода после его смешения с сульфатом магния при мольном соотношении пероксид водорода/сульфат магния, равном (HO/MgSO)=450÷700, через 1-3 минуты вводят ортоборную кислоту при мольном соотношении пероксид водорода/ортоборная кислота, равном (НО/НВО)=285÷850, при этом гидроксиды натрия и калия вводят в жидкую фазу одновременно двумя порциями с интервалом 6-10 минут таким образом, чтобы температура в зоне синтеза не превышала 60°С.
