Результат интеллектуальной деятельности: Способ формирования межпротезного анастомоза в хирургии грудной аорты
Вид РИД
Изобретение
Изобретение относится к медицине, в частности, к сердечно-сосудистой хирургии и может быть использовано с целью минимизации интра- и послеоперационной кровопотери, а также сокращении времени искусственного кровообращения.
Кровотечения после операций на грудной аорте относят к тяжелым осложнениям, которые в 9-13% случаев требуют проведения повторного вмешательства. Реоперация по поводу кровотечения, в свою очередь, ассоциируется с осложненным течением послеоперационного периода, что влияет на исход лечения [1-4]. Так. в работе Ranucci М. et al. [4] отражено достоверное увеличение дыхательных, почечных осложнений, а также госпитальной летальности в раннем послеоперационном периоде у пациентов, которым потребовалась реоперация по поводу кровотечения по сравнению с теми, у кого не было показаний для ревизии послеоперационной раны. Более того, Zindovic I. et al. [2] опубликовали сведения о том, что послеоперационные кровотечения в значительной степени влияют и на среднесрочную выживаемость повторно оперированных пациентов. К примеру, 5-летняя выживаемость больных с геморрагическими осложнениями находится на уровне 53,9±6,9%, в то время как у пациентов без кровотечения выживаемость достигает 82,1±3,3% (р=0,001). Таким образом, решение проблемы кровотечения - это в значительной мере вопрос сокращения послеоперационной летальности.
Профилактика геморрагических осложнений в послеоперационном периоде включает в применение кровесберегающих технологий, а также проведение фармакологической и трансфузионной поддержки. Однако основное значение имеет формирование герметичного анастомоза.
Известен способ, при котором для формирования анастомозов между сосудистым протезом и аортой используют фетровую полоску [5]. Таким образом, укрепляется линия формируемого анастомоза и снимается излишнее напряжение на швы с одновременной профилактикой кровотечения из проколов. Однако, при формировании протезо-протезных анастомозов данная техника является излишней, поскольку нет необходимости укреплять линию шва данных анастомозов вследствие высокой прочности сосудистых протезов. Более того, использование фетровых прокладок при формировании протезо-протезных анастомозов увеличивает время его формирования и потенциально несет в себе риски стенозирования данного анастомоза вследствие отсутствия достаточной эластичности протеза.
В проанализированной патентной и научно-медицинской литературе адекватного прототипа не найдено.
Задачей изобретения является создание способа формирования межпротезного анастомоза при реконструкции грудной аорты, обеспечивающего минимальную кровопотерю через проколы линии анастомоза, а также позволяющего сократить время аппроксимации протезов, что опосредованно способствует сокращению времени искусственного кровообращения.
Поставленная задача решается выполнением аппроксимации анастомозируемых аортальных протезов непрерывным П-образным швом, затем дополнительно герметизируют линию межпротезного анастомоза полоской из аутоперикарда шириной 1 см, которую фиксируют непрерывным обвивным швом.
Новым в предлагаемом способе является формирование межпротезного анастомоза с одновременным сокращением времени искусственного кровообращения.
Техническим результатом является практически полное исключение потери крови через линию межпротезного анастомоза, а также сокращение времени искусственного кровообращения.
Новые свойства проявили в заявляемой совокупности новые свойства явным образом не вытекающие из уровня техники в данной области и не очевидны для специалиста. Идентичной совокупности свойств не обнаружено в патентной и научно-медицинской литературе. Предлагаемый способ может быть использован в практическом здравоохранении для сокращения интра- и послеоперационной кровопотери через линию межпротезного анастомоза.
Исходя из вышеизложенного, следует считать предлагаемое изобретение соответствующим условиям патентоспособности «новизна», «изобретательский уровень», «промышленная применимость».
Изобретение будет понятно из следующего описания и приложенных к нему рисунков.
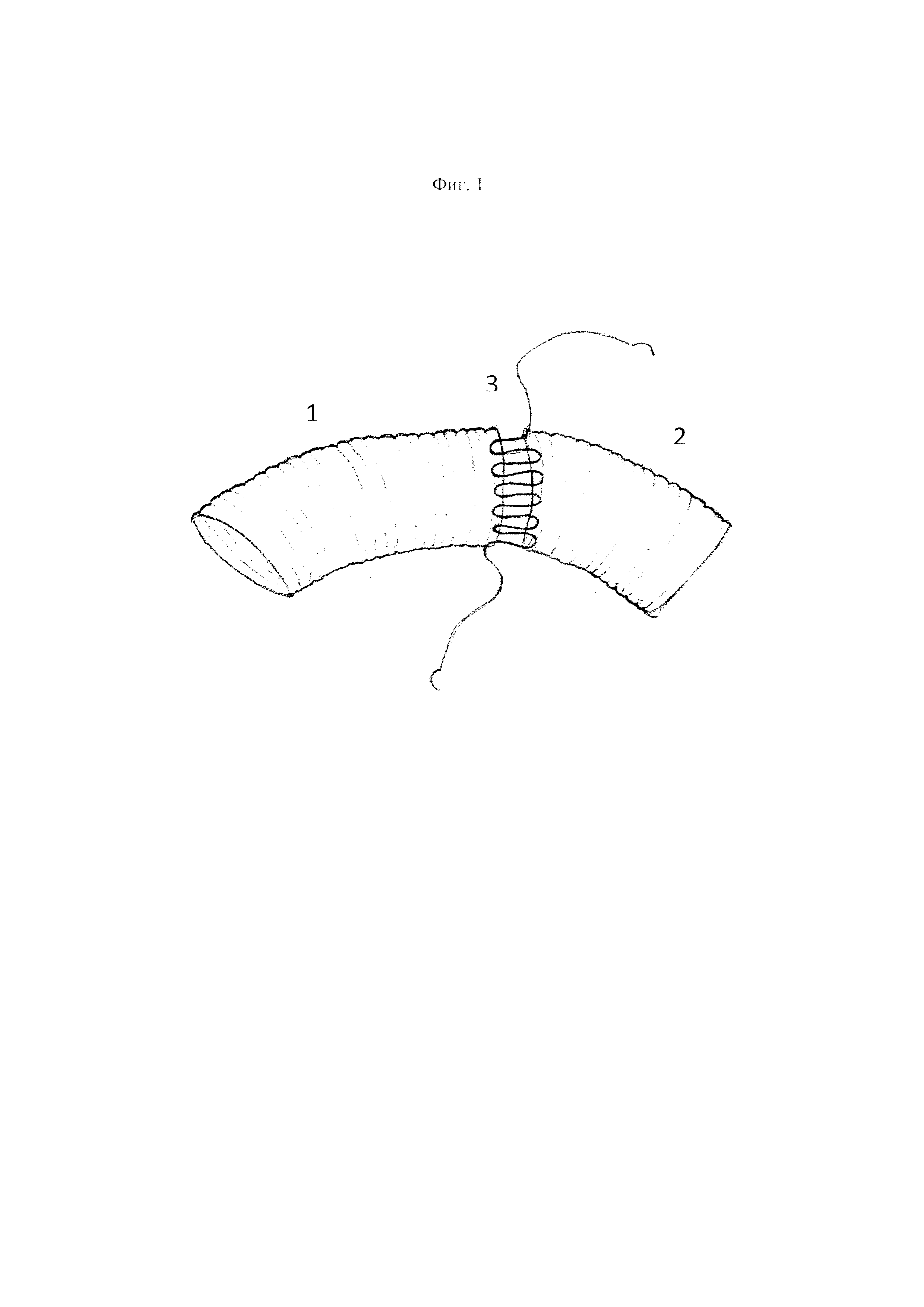
На фиг. 1 изображено два аортальных протеза, анастомозируемые друг с другом непрерывным П-образным швом, где 1 - протез №1, 2 - протез №2, 3 - непрерывный П-образный шов.
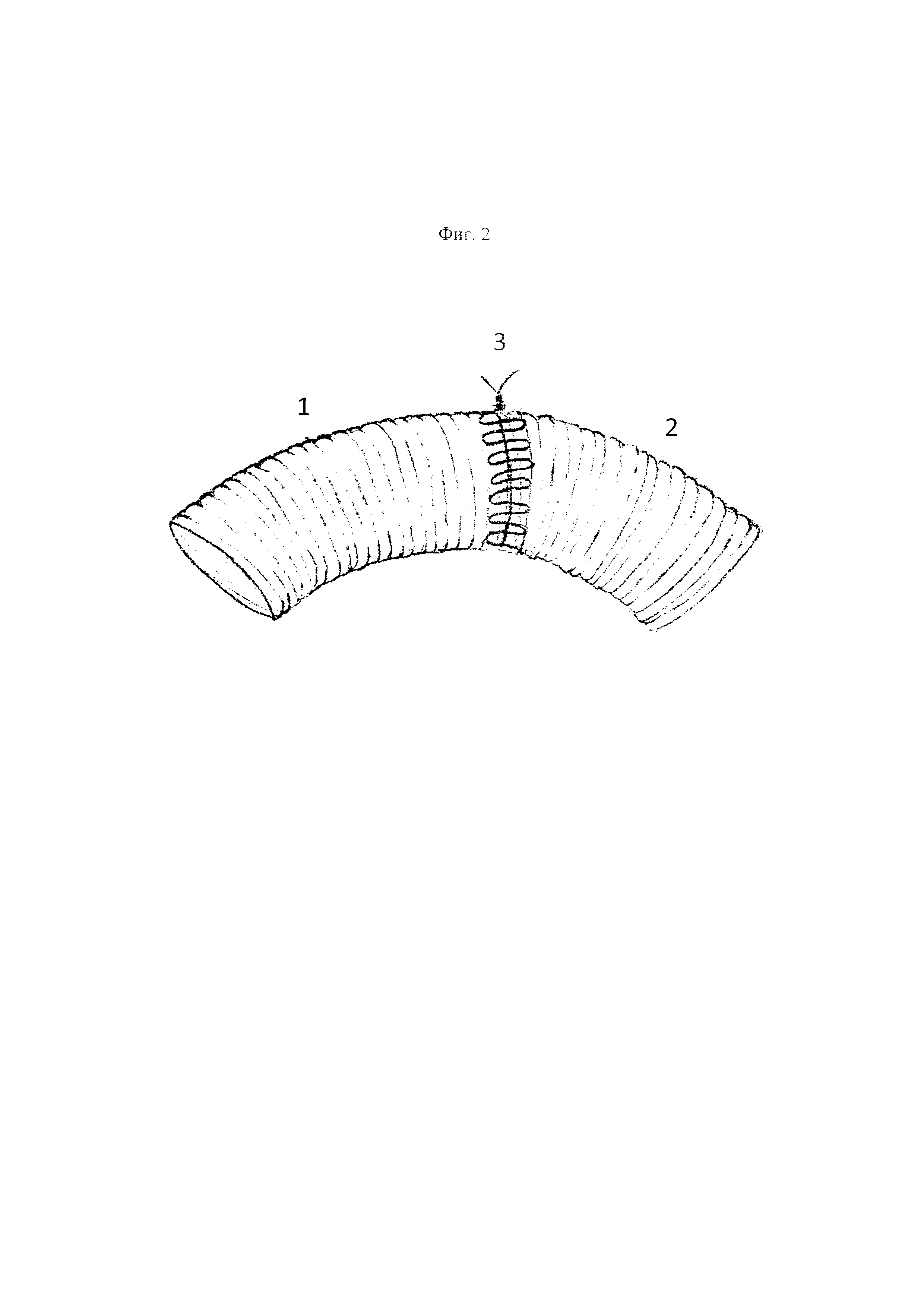
На фиг. 2 изображено два аортальных протеза, плотно подведенные друг к другу в результате затягивания непрерывного П-образного шва, где 1 - протез №1, 2 - протез №2, 3 - непрерывный П-образный шов.
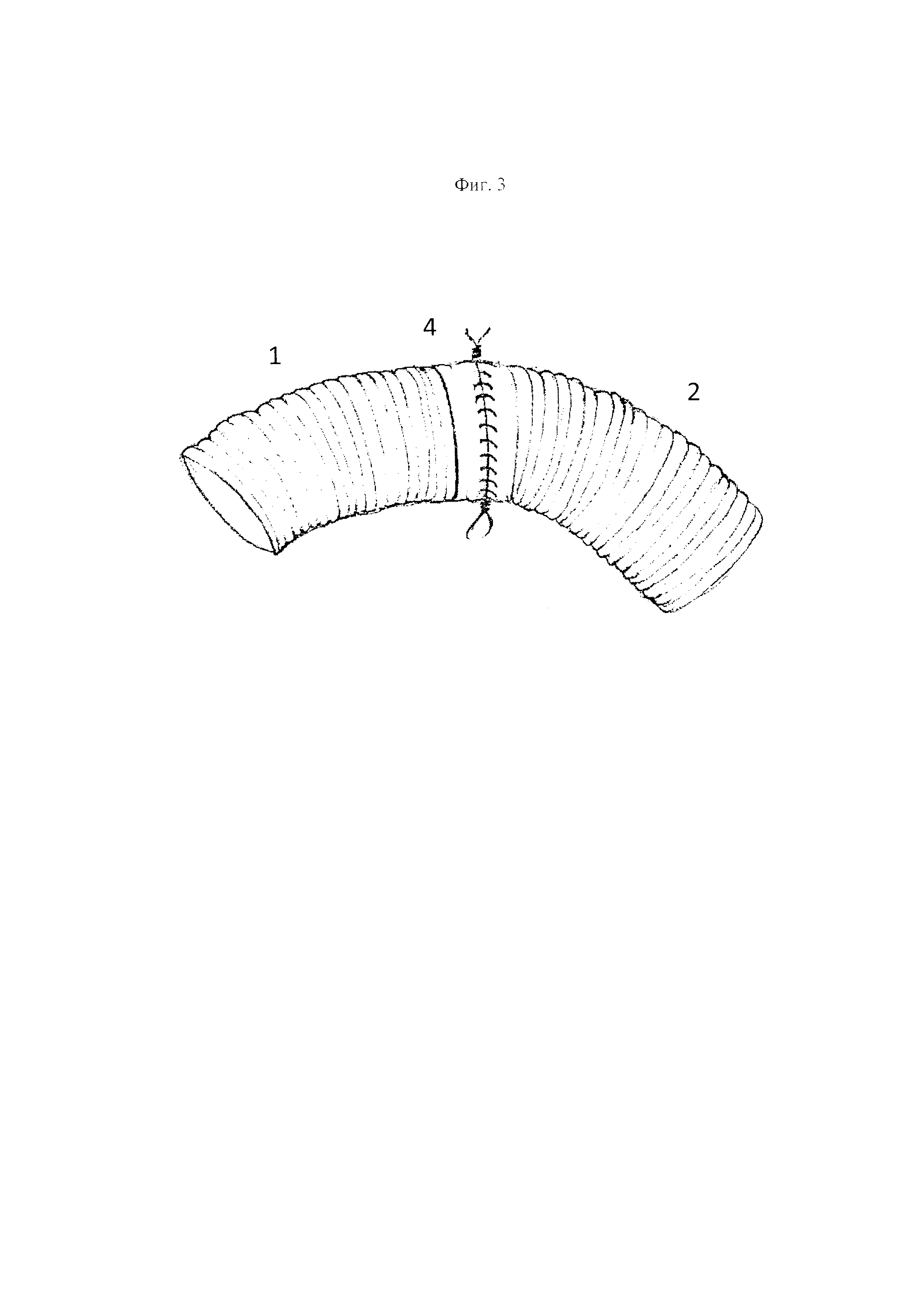
На фиг.3 изображено два аортальных протеза, анастомозированных друг с другом непрерывным П-образным швом с дополнительным укрыванием линии шва полоской из аутоперикарда шириной 1 см и фиксацией ее непрерывным обвивным швом, где 1 - протез №1 2 - протез №2, 4 - аутоперикардиальная полоска шириной 1 см.
Способ осуществляют следующим образом. Выполняют аппроксимацию анастомозируемых друг с другом сосудистых протезов грудной аорты 1,2 по типу «конец в конец» непрерывным П-образным швом 3 монофиламентной нитью 4/0 по всей окружности. После пуска кровотока по протезам циркулярно оборачивают линию сформированного межпротезного анастомоза полоской из аутоперикарда 4 шириной 1 см. После чего обшивают всю линию анастомоза непрерывным обвивным швом с захватом краев протезов 1,2 и аутоперикардиальной заплаты 4, таким образом, чтобы аутоперикардиальная заплата укутывала линию сформированного межпротезного анастомоза, дополнительно обеспечивая ее герметизацию.
Пример.
Пациент П., 49 лет, поступил в кардиохирургическое отделение с диагнозом: Расслоение аорты тип А по Stanford. Недостаточность аортального клапана 4 степени.
Согласно данным проведенной спиральной компьютерной томографии аорты с контрастированием был подтвержден диагноз диссекции грудной аорты, а по данным ЭхоКГ верифицирована полная несостоятельность аортального клапана.
Пациенту запланировано оперативное лечение в объеме протезирования аортального клапана и грудной аорты с имплантацией гибридного стент-графта «Е-vita open plus» в нисходящую аорту в условиях искусственного кровообращения, фармакохолодовой кардиоплегии, антеградной унилатеральной перфузии головного мозга, циркуляторного ареста и умеренной гипотермии.
Основной этап операции протекал в следующей последовательности. После канюляции начато охлаждение пациента до целевой температуры тела 25 С. По достижении заданной температуры начат циркуляторный арест с унилатеральной перфузией головного мозга. Имплантирован гибридный стент-графт «Е-vita open plus» в нисходящую аорту с фиксацией к дуге аорты. Реконструированы сосуды дуги путем раздельного протезирования и реплантацией в нестентированную часть гибридного стент-графта с восстановлением физиологического кровотока в головном мозге. Выполнена процедура Бенталл-ДеБоно. Протезы дуги аорты и корня аорты соединены с использованием описанного способа формирования межпротезного анастомоза.
Операция завершена стандартно. Продолжительность искусственного кровообращения составила 250 минут, время сердечного ареста - 195 минут, время циркуляторного ареста - 52 минут. Пациент переведен в палату интенсивной терапии.
Через 12 часов после окончания операции пациент пришел в сознание, доступен контакту, выполняет простые просьбы. Неврологический статус без очаговой симптоматики со стороны головного и спинного мозга. Пациент находился на искусственной вентиляции легких в течение 15 часов. Общее время пребывания больного в палате интенсивной терапии составило 3 суток. По данным спиральной компьютерной томографии аорты с контрастированием в послеоперационном периоде все анастомозы проходимы, герметичны. Пациент выписан из стационара в удовлетворительном состоянии на 31-е сутки после операции.
Способ применен у 17 взрослых больных. Подготовка к операции и анестезиологическое обеспечение у всех пациентов были одинаковыми. Всем пациентам требовалась сложная реконструкция грудной аорты в связи с чем было необходимо формирование межпротезных анастомозов.
Применение предлагаемого способа позволило исключить потерю крови через линию межпротезного анастомоза, а также позволило сократить время искусственного кровообращения за счет быстрой аппроксимации протезов аорты.
Список литературы
1. Whitson ВА, Huddleston SJ, Savik K, et al. Bloodless cardiac surgery is associated with decreased morbidity and mortality. Card Surg 2007; 22:373-378. doi: 10.1111/j.1540-191.2007.00428.x.
2. Zindovic I, Sjogren O, Bjursten P, et al. Predictors and impact of massive bleeding in acute type A aortic dissection. Interactive Cardio Vascular and Thoracic Surgery. 2017; 24:498-505. doi:10.1093/icvts/ivw425.
3. Ма W-G, Ziganshin BA, Guo C-F, et al. Does BioGlue contribute to anastomotic pseudoaneurysm after thoracic aortic surgery? J Thorac Dis. 2017; 9(8):2491-2497. doi: 10.21037/jtd.2017.06.120.
4. Ranucci M, Bozzetti G. Ditta A, et al. Surgical reexploration after cardiac operations: why a worse outcome? Ann Thorac Surg. 2008; 86:1557-1562. doi: 10.1016/j.athoracsur.2008.07.114.
5. Белов Ю.В., Алексеев И.А, Чарчян Э.Р. Способы формирования герметичного анастомоза в хирургии аорты. Кардиология и сердечно-сосудистая хирургия. 2009; 6:38-41.
Способ формирования межпротезного анастомоза в хирургии грудной аорты, характеризующийся тем, что выполняют аппроксимацию анастомозируемых аортальных протезов непрерывным П-образным швом, затем дополнительно герметизируют линию межпротезного анастомоза полоской из аутоперикарда шириной 1 см, которую фиксируют непрерывным обвивным швом.