Результат интеллектуальной деятельности: НОВАЯ ПОЛИКРИСТАЛЛИЧЕСКАЯ ФОРМА ПРОЛЕКАРСТВА ТЕНОФОВИРА И СПОСОБ ЕЕ ПОЛУЧЕНИЯ И ЕЕ ПРИМЕНЕНИЕ
Вид РИД
Изобретение
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к области медицинской химии и, в частности, относится к новой кристаллической форме пролекарства тенофовира 9-[(R)-2-[[(S)-[[[1-(изопропоксикарбонил)-1-метил]этил]амино]феноксифосфинил]метокси]пропил]аденин фумарата, способу его получения, фармацевтической композиции, содержащей терапевтически эффективное количество этого соединения и медицинскому применению указанного вещества.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
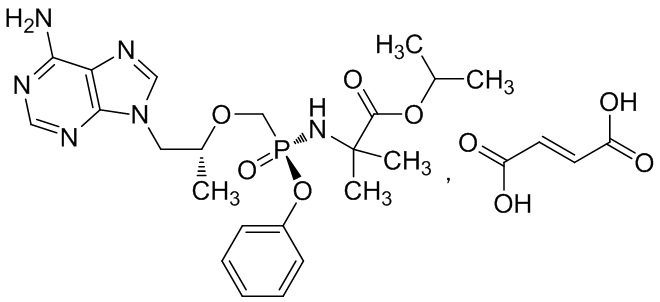
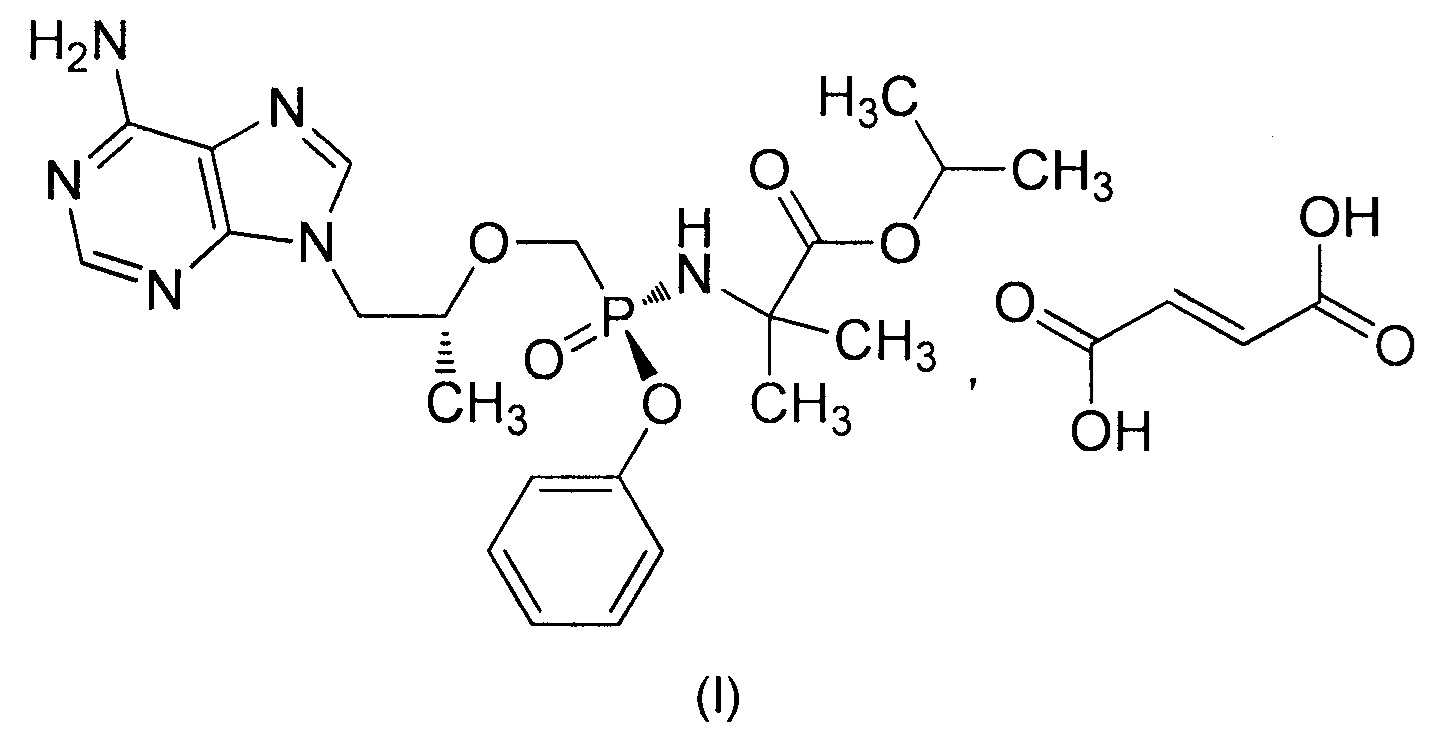
9-[(R)-2-[[(S)-[[[1-(изопропоксикарбонил)-1-метил]этил]амино]феноксифосфинил]метокси]пропил]аденин фумарат (I) имеет следующую структуру:
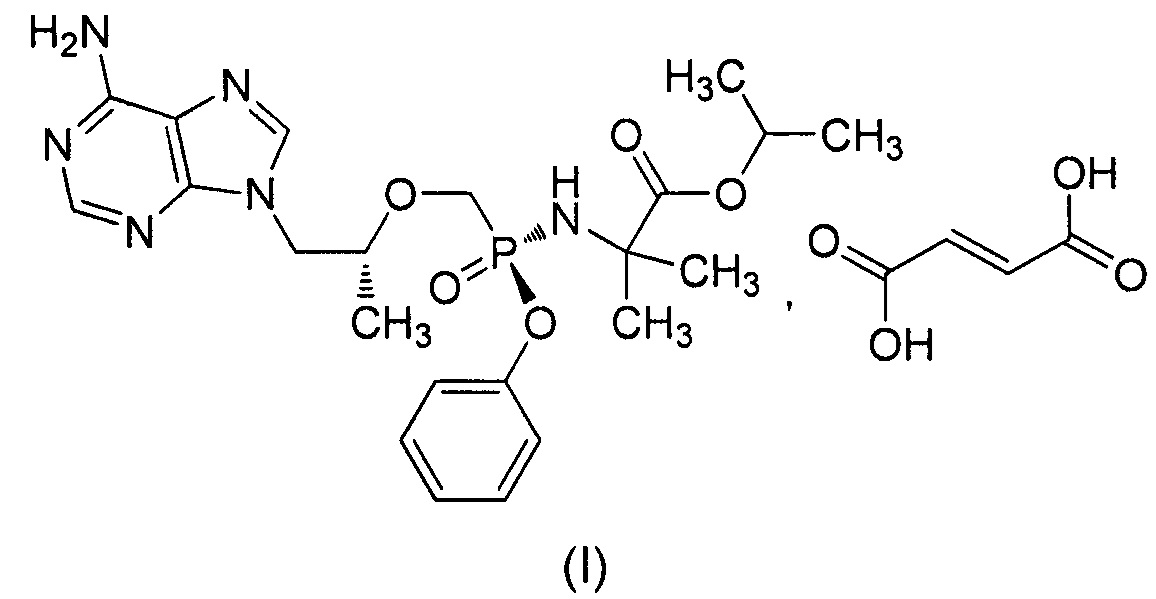
9-[(R)-2-[[(S)-[[[1-(изопропоксикарбонил)-1-метил]этил]амино]феноксифосфинил]метокси]пропил]аденин фумарат (I) представляет собой нуклеозидный ингибитор обратной транскриптазы и пролекарство тенофовира РМРА. РМРА подобен естественному нуклеозидмонофосфату по структуре и в организме быстро превращается в активный метаболит РМРА дифосфат (РМРАрр). РМРАрр конкурирует с природным дезоксиаденозин-5'-трифосфатом и включается в цепь ДНК вируса. Однако РМРАрр не может выполнить реакцию сочетания 5',3'-фосфодиэфирной связи в связи с отсутствием 3'-ОН группы, таким образом расширение цепи ДНК блокируется, и репликация вируса в конечном счете заблокирована (Фиг. 1). Доказано, что РМРА обладает противовирусной активностью в отношении вируса иммунодефицита человека (ВИЧ) и противовирусной активностью в отношении вируса гепатита В (HBV, от англ. Hepatitis В virus).
Тем не менее, РМРА содержит фосфатную группу, которая, как правило, отрицательно заряжена при физиологическом рН, и ее полярность слишком высока, чтобы пройти через биопленку, что приводит к плохой биодоступности при пероральном введении, низкому коэффициенту распределения в ткани, а также некоторой нефротоксичности. Таким образом, при разработке таких лекарственных средств необходимо использовать принцип пролекарств, чтобы замаскировать отрицательный заряд фосфатных групп для устранения недостатков подобных лекарственных средств. Диэфирное пролекарство РМРА, тенофовир дизопроксил фумарат (ТДФ), разработанный компанией Gilead, был одобрен FDA (Управлением по контролю за продуктами питания и лекарственными средствами США) в 2001 году для лечения ВИЧ-инфекции.
ТДФ значительно улучшил фармакокинетические свойства РМРА до некоторой степени, но он быстро гидролизуется в организме неспецифическими эстеразами, которые широко представлены в плазме, в частности в присутствии карбонат-эстераз в клетках эпителиалия кишечника с высвобождением РМРА. Высокая концентрация РМРА в плазме быстро выводится из организма из-за его плохой мембранной проницаемости, что приводит к сложности в поддержании адекватной концентрации в пораженном месте. Кроме того, РМРА является субстратом транспортера органических анионов (hOAT) в эпителиальных клетках проксимальных почечных канальцев, и высокая концентрация РМРА в плазме легко накапливается в эпителиальных клетках проксимальных почечных канальцев, что приводит к определенному риску почечной токсичности.
Новое поколение монофосфамидного моноэфирного пролекарства преодолевает вышеупомянутые недостатки ТДФ, является очень стабильным в плазме и не так легко гидролизуется эстеразами. Когда оно поглощается клетками, оно сразу же превращается в РМРА в присутствии сериновых протеаз (катепсин А) и специфической амидазы. Таким образом, оно имеет лучшую тканевую проницаемость и направленное воздействие на лимфоидную ткань и клетки. Монофосфамидное моноэфирное пролекарство GS7340 (см. патентную заявку WO 2013052094 A2), разработанное компанией Gilead, успешно вступило в фазу III клинических испытаний, и результаты показывают, что GS7340 имеет более высокий противовирусный потенциал и более высокий уровень безопасности по сравнению с 30-кратной дозой ТДФ.
9-[(R)-2-[[(S)-[[[1-(изопропоксикарбонил)-1-метил]этил]амино]феноксиф осфинил]метокси]пропил]аденин фумарат (I), подобно GS7340, может высвобождать активный ингредиент РМРА в клетках. Его добавочная группа тщательно продумана, ее структура отличается от GS7340 только одной метильной группой, и поведение и схема удаления добавочной группы в клетках почти такие же, как и у GS7340. Можно ожидать, что HS-10234 будет более эффективно, чем ТДФ и другие пролекарства, воспроизводить эффективность активного ингредиента РМРА из-за преимуществ в абсорбции и распределении. В качестве наиболее перспективного нового поколения пролекарств РМРА, HS-10234 принесет пользу большинству пациентов.
Специалисту в данной области техники известно, что полиморфная форма лекарственного средства стала неотъемлемой частью фармацевтического процесса исследования и контроля качества и выявления дефектов готового лекарственного продукта. Изучение полиморфизма лекарственных средств является полезным для выбора биоактивности нового лекарственного соединения, для улучшения биодоступности, для улучшения клинического лечебного эффекта, для выбора и разработки пути введения лекарственного средства, и для определения параметров фармацевтического способа получения, улучшая таким образом качество производства лекарственных средств. Биодоступность может существенно различаться для различных кристаллических форм одного и того же лекарственного средства. Для одного лекарственного средства некоторые кристаллические формы могут иметь более высокую биологическую активность, чем другие кристаллические формы. Получение кристаллической формы пролекарства тенофовира с более высокой биоактивностью и более подходящим медицинским применением является технической задачей, решения которой с большим интересом ожидают специалисты в сфере медицины.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Задачей настоящего изобретения является решение вышеуказанной технической задачи, а также получение новой кристаллической формы пролекарства тенофовира 9-[(R)-2-[[(S)-[[[1-(изопропоксикарбонил)-1-метил]этил]амино]феноксифосфинил]метокси]пропил]аденин фумарата, который в настоящем изобретении называется кристаллической формой А.
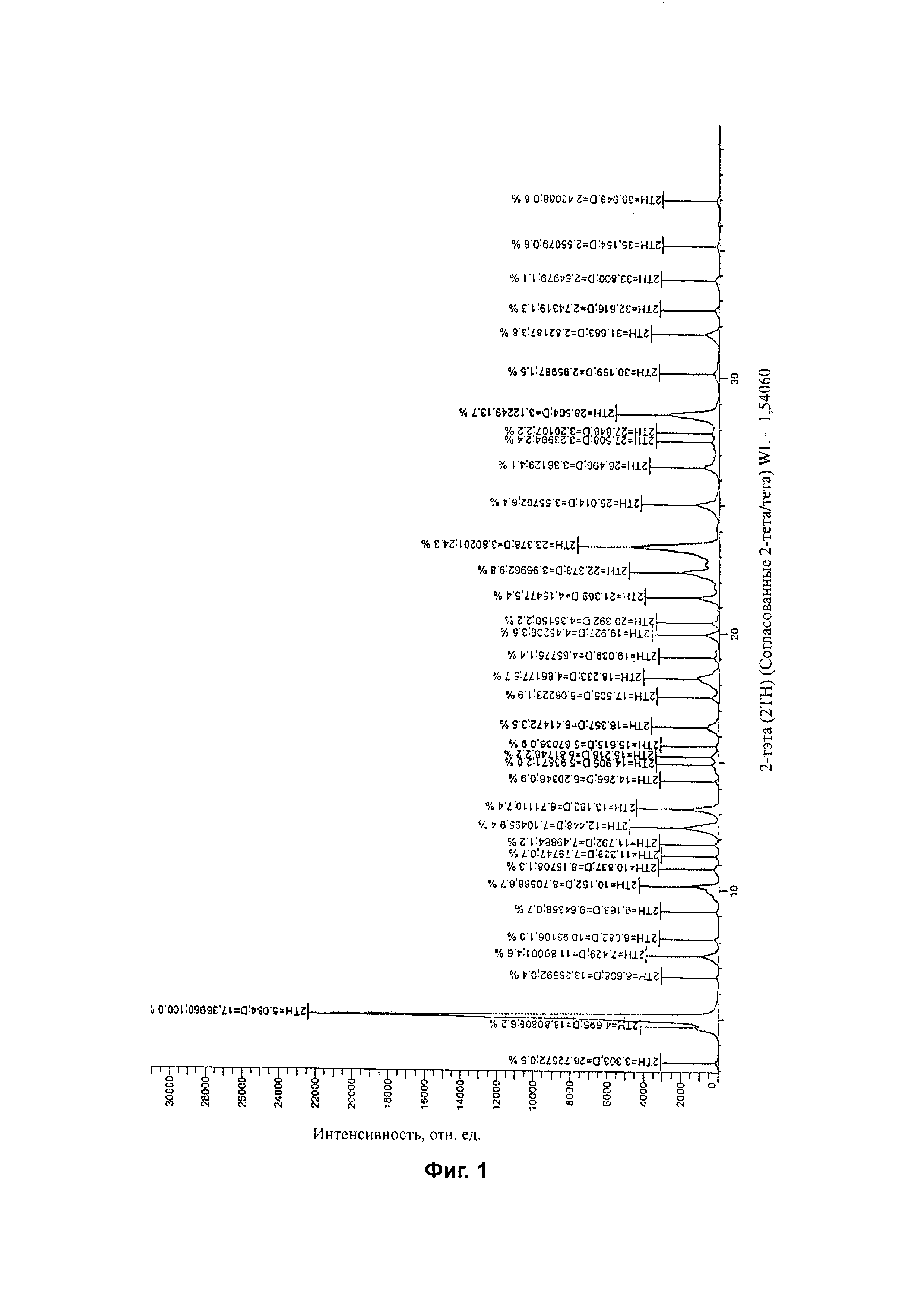
Рентгеновская порошковая дифрактограмма кристаллической формы А в соответствии с настоящим изобретением содержит по меньшей мере следующие дифракционные пики при 2θ ±0,20°: 5,08, 12,44, 13,18, 22,37, 23,37 и 28,56.
Предпочтительно, рентгеновская порошковая дифрактограмма кристаллической формы А 9-[(R)-2-[[(5)-[[[1-(изопропоксикарбонил)-1-метил]этил]амино]феноксифосфинил]метокси]пропил]аденин фумарата содержит по меньшей мере следующие дифракционные пики при 2θ±0,20°: 5,08, 7,42, 10,15, 12,44, 13.18, 22.37, 23,37 и 28,56, более предпочтительно дополнительно содержит следующие дифракционные пики при 2θ ±0,20°: 16,35, 18,23, 21,36, 25,00 и 31,68.
Особенно предпочтительная рентгеновская порошковая дифрактограмма кристаллической формы А представляет собой такой, как показано на Фиг. 1.
Результат дифференциального термического анализа кристаллической формы А 9-[(R)-2-[(S)-[[[1-(изопропоксикарбонил)-1-метил]этил]амино]феноксифосфинил]метокси]пропил]аденин фумарата в соответствии с настоящим изобретением демонстрирует острый эндотермический пик плавления при 110,9°С.
Другой задачей настоящего изобретения является получение способа получения кристаллической формы A 9-[(R)-2-[(S)-[[[1-(изопропоксикарбонил)1-метил]этил]амино]феноксифосфинил]метокси]пропил]аденин фумарата, включающий следующие стадии:
(1) растворение любых форм 9-[(R)-2-[(S)-[[[1-(изопропоксикарбонил)-1-метил]этил]амино]феноксифосфинил]метокси]пропил]аденин фумарата в органическом растворителе при нагревании;
(2) охлаждение раствора 9-[(R)-2-[(S)-[[[1-(изопропоксикарбонил)-1-метил]этил]амино]феноксифосфинил]метокси]пропил]аденин фумарата для осаждения кристалла;
(3) отфильтровывание кристалла с получением кристаллической формы А.
Предпочтительно органический растворитель выбирают из группы, состоящей из ацетонитрила, безводного метанола, безводного этанола, изопропанола, безводного метанола/н-гептана, безводного этанола/н-гептана, изопропанола/н-гептана, безводного метанола/метил-трет-бутилового эфира, безводного этанола/метил-трет-бутилового эфира, изопропанола/метил-трет-бутилового эфира, безводного метанола/изопропилового эфира, безводного этанола/изопропилового эфира, изопропанола/изопропилового эфира, безводного метанола/диэтилового эфира, безводного этанола/диэтилового эфира и изопропанола/диэтилового эфира, более предпочтительно безводного метанола/н-гептана.
Предпочтительно температура нагрева органического растворителя обычно составляет от 30°С до температуры кипения, предпочтительно представляет собой температуру кипения; температура кристаллизации предпочтительно составляет от -40°С до 40°С, наиболее предпочтительно от 0°С до 10°С.
Еще одной задачей настоящего изобретения является получение фармацевтической композиции, содержащей эффективное количество указанной кристаллической формы А, фармацевтическая композиция необязательно дополнительно содержит фармацевтически приемлемый носитель.
Композицию в соответствии с настоящим изобретением вводят подходящим путем, включающим пероральный и инъекционный путь и т.д., предпочтительно оральным путем. Подходящие лекарственные формы включают таблетки, капсулы, дисперсии и суспензии, предпочтительно таблетки.
Другой задачей настоящего изобретения является обеспечение применения указанной кристаллической формы А и фармацевтической композиции, содержащей кристаллическую форму А, при получении лекарственного средства для лечения СПИДа или вируса гепатита В.
Новая кристаллическая форма А в соответствии с настоящим изобретением имеет преимущества высокой биодоступности, значительной эффективности, хорошей стабильности, высокого выхода и высокой степени чистоты, и т.д. Новая кристаллическая форма в соответствии с настоящим изобретением является полезной для выбора и разработки пути введения лекарственного средства и определения параметров фармацевтического способа получения, улучшая тем самым качество производства лекарственных средств.
ОПИСАНИЕ ФИГУР
Фиг. 1 представляет собой рентгеновскую порошковую дифрактограмму новой кристаллической формы 9-[(R)-2-[(S)-[[[1-(изопропоксикарбонил)-1-метил]этил]амино]феноксифосфинил]метокси]пропил]аденин фумарата в соответствии с настоящим изобретением.
Фиг. 2 представляет собой профиль ДСК (дифференциальной сканирующей калориметрии) новой кристаллической формы 9-[(R)-2-[(S)-[[[1-(изопропоксикарбонил)-1-метил]этил]амино]феноксифосфинил]метокси]пропил]аденин фумарата в соответствии с настоящим изобретением.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Чтобы проиллюстрировать техническое решение по настоящему изобретению и полученный таким образом результат, настоящее изобретение будет описано далее со ссылкой на конкретные примеры ниже, но следует понимать, что объем настоящего изобретения не ограничивается этими конкретными примерами.
Пример 1
5,0 г 9-[(R)-2-[(S)-[[[1-(изопропоксикарбонил)-1-метил]этил]амино]феноксифосфинил]метокси]пропил]аденин фумарата, 20,0 мл безводного метанола и 5 мл н-гептана помещали в реакционную колбу, и затем нагревали с обратным холодильником до тех пор, пока твердое вещество не было полностью растворено. Нагревание прекращали и раствор охлаждали до 0~10°С и перемешивали в течение 2 ч, чтобы осадить кристаллы. Твердое вещество отфильтровывали с получением кристаллической формы А
После тестирования и верификации, ее рентгеновская порошковая дифрактограмма представляла собой такую, как показано на Фиг. 1, и ее профиль ДСК соответствовал Фиг. 2, что свидетельствовало о том, что полученная кристаллическая форма представляла собой кристаллическую форму А.
Пример 2
5,0 г 9-[(R)-2-[(S)-[[[1-(изопропоксикарбонил)-1-метил]этил]амино]феноксифосфинил]метокси]пропил]аденин фумарата и 20,0 мл безводного этанола помещали в реакционную колбу, и затем нагревали с обратным холодильником до тех пор, пока твердое вещество не было полностью растворено. Нагревание прекращали и раствор охлаждали до 0~10°С и перемешивали в течение 2 ч для осаждения кристаллов. Твердое вещество отфильтровывали с получением кристаллической формы А.
После исследования и проверки ее рентгеновская порошковая дифрактограмма соответствовала Фиг. 1, и ее профиль ДСК соответствовал Фиг. 2, что свидетельствовало о том, что полученная кристаллическая форма представляла собой кристаллическую форму А.
Пример 3
5,0 г 9-[(R)-2-[(S)-[[[1-(изопропоксикарбонил)-1-метил]этил]амино]феноксифосфинил]метокси]пропил]аденин фумарата, 20,0 мл изопропанола и 5 мл метил-трет-бутилового эфира помещали в реакционную колбу, и затем нагревали с обратным холодильником до тех пор, пока твердое вещество не было полностью растворено. Нагревание прекращали и раствор охлаждали до 0~10°С и перемешивали в течение 2 ч для осаждения кристаллов. Твердое вещество отфильтровывали с получением кристаллической формы А
После исследования и проверки ее рентгеновская порошковая дифрактограмма соответствовала Фиг. 1, и ее профиль ДСК соответствовал Фиг. 2, что свидетельствовало о том, что полученная кристаллическая форма представляла собой кристаллическую форму А.
Экспериментальный пример: исследование стабильности
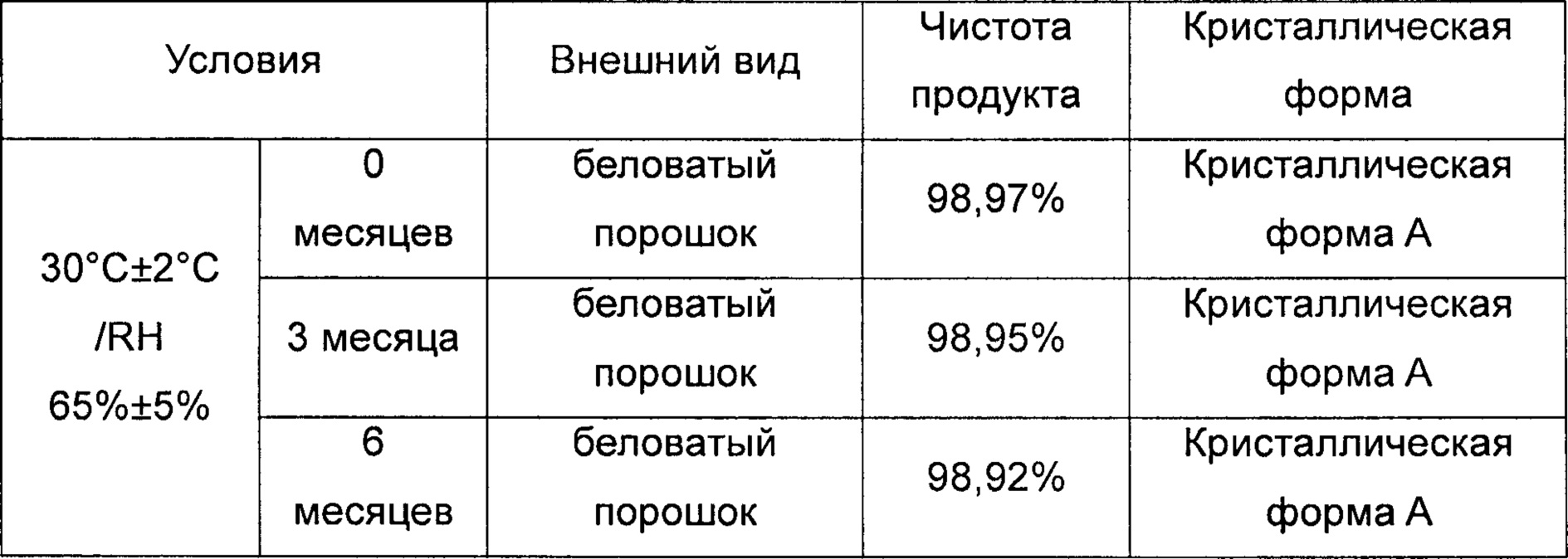
Была изучена стабильность новой кристаллической формы, полученной способом согласно Примеру 1 по настоящему изобретению. Результаты показали, что новая кристаллическая форма А по настоящему изобретению не претерпевала трансформацию в тесте на стабильность и не подвергалась химическому разложению, являась стабильной при комнатной температуре и находилась в соответствии с требованиями к лекарственным средствам и их получению. Подробности исследования приведены в таблице ниже:
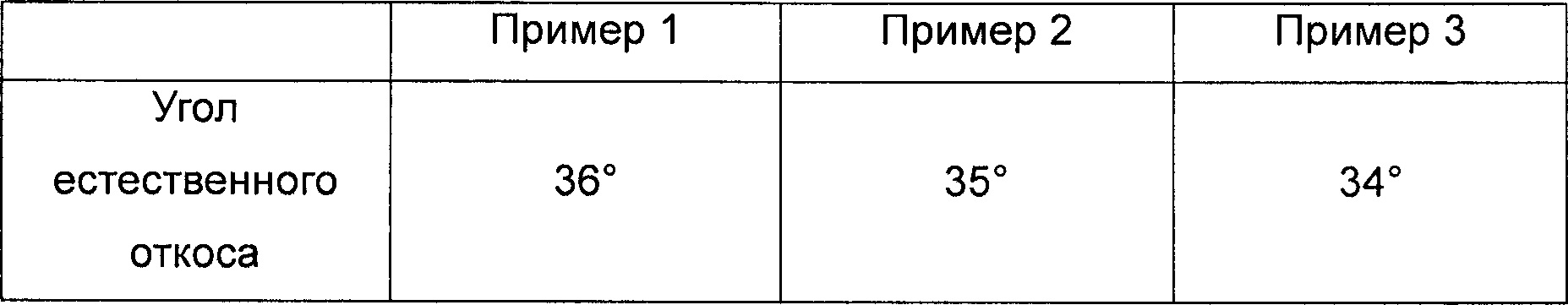
Экспериментальный пример: исследование текучести
Была изучена текучесть новой кристаллической формы, полученной в Примерах 1, 2 и 3 настоящего изобретения. Результаты показали, что новая кристаллическая форма А по настоящему изобретению имеет хорошую текучесть.
Экспериментальный пример: Определение абсолютной биодоступности Абсолютная биодоступность новой кристаллической формы А, полученной в соответствии с настоящим изобретением, как было измерено путем внутривенного введения и перорального введения крысам, составила 81%. Результаты показали, что новая кристаллическая форма, полученная в соответствии с настоящим изобретением, имела высокую биодоступность.