Результат интеллектуальной деятельности: АНТИВИРУСНАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ
Вид РИД
Изобретение
Настоящее изобретение относится к фармацевтической области, в частности к фармацевтической композиция в форме, подходящей для введения в нос, глаза или влагалище.
Также изобретение относится к фармацевтическому продукту, содержащему йотта-каррагенан и бета-глюкан, представленные в виде аэрозольной композиции для доставки посредством дозирующего ингалятора в виде назального или вагинального спрея. Такая комбинация активных компонентов приводит к их взаимному улучшению стабильности, а также обеспечивает улучшенную эффективность.
Настоящее изобретение относится к фармацевтическим продуктам и композициям. Особенно настоящее изобретение относится к фармацевтическим продуктам и композициям, применимым для предотвращения или минимизации проявлений и последствий вирусных заболеваний. В частности, но не исключительно, настоящее изобретение относится к фармацевтическим продуктам и композициям для назального, вагинального и офтальмологического применения.
Вирусные заболевания обычно включают в себя локальне симптомы, связанные с активацией вирусных частиц, обусловленной снижением, в том числе локального, иммунитета, и, как правило вазомоторные симптомы (гипериемия, отечность, зуд, эксудативные выделения). Обычно эти симптомы не зависят от вида вируса и являются общими для вирусного поражения.
Из области техники, известно применение противовирусных препаратов для локального воздействия в виде мазей, кремов, гелей. Как правило, это химические вещества, имеющие различный механизм действия.
Например, широкоизвестные противовирусные препараты - ацикловир, бонафтон, ремантадин, иодоскуридин применяются в виде локальних аппликаций, например в виде мазей.
Однако эти вещества фактически не применяютсяв виде спреев, поскольку или они нерастворимы в воде и растворителях, использующихся в форме для спрея, или сложно дозируются, или не стабильны в таком виде.
Из заявки СА, 1273576 А1 известен способ применения антивирусного агента (антисептика) и анестетика для лечения заболеваний, вызванных вирусом герпеса. Однако их применение возможно толко для локального накожного применения, поскольку могут повреждать слизистые оболочки носовой, ротовой полостей, влагалища (opcit.. Author(s): М. Azim Khan. EffectsofPhenol, Benzalkonium Chloride, Oxymetazoline, Tobacco and Formalin on Nasal Mucosa of Albino Rat//Journal of the Anatomical Society of India, Vol. 55, No. 1 (2006-01 - 2006-07). Meggs WJ (1994). "RADS and RUDS--the toxic induction of asthma and rhinitis". J. Toxicol. Clin. Toxicol. 32 (5): 487-501.)
Существующие проблемы побуждают к поиску и разработке эффективных и безопасных средств, эффективных в отношениии вирусных возбудителей, особенно передающихся воздушно-капельным путем или прямым контактным путем.
Так, из международной заявки WO 2005/039623 А1 известно применение в виде спрея для лечения и профилактики вирусных заболеваний интерферона, в особенности типа альфа.
Однако такое применение интерферона может сопровождаться рядом нежелательных побочных эффектов, связанных с системными проявлениями его действия, такими как - боль в мышцах или повышение температуры тела.
Поэтому актуальными являются попытки разработки средств местного действия, которые бы препятствовали вирусному проникновению из места локального внедрения.
Сравнительно недавно было неожиданно установлено, что подобным свойством обладает бета-глюкан.
Опыт применения бета-глюкана для профшактики вирусных заболеваний известен с конца XX столетия (Wakshull Е., D. Brunke-Reese, J. Lindermuth, L. Fisette, R.S. Nathans, J.J. Crowley, J.C. Zimmermann, W. Mackin, S. Adams, PGG-glucana soluble beta (1-3)-glucan enhances the oxidative burst response, microbicidal activity, and activates an N1-Kappa Blike factor in human PMN: evidence for a glycosphigolipid beta(1-3)-glucan receptor Immunopharmacology 1999; 41: 89-107).
Бета-глюканы представляют собой семейство полисахаридов мономеров D-глюкозы, соединенных посредством бета-гликозидных связей, отличающихся за счет этого между собой молекулярной массой, плотностью и трехмерной структурой и некоторыми терапевтическими свойствами.
Известны бета-глюканы (1-3), бета-глюканы (1-3/1-6), бета-глюканы (1-3/1-4). Цифры в скобках указывают на характер бета-гликозидной связи. Наиболее активной в биологическом отношении формой бета-глюканов считается бета-1,3/1,6-глюкан, в молекуле которого глюкоза привязана к позициям 1 и 3, а также молекула которого имеет ответвления в позициях 1 и 6 (Bohn J.A., BeMille J.N., 1995).
Однако, бета-глюканы 1,3/1,6 и 1-3/1-4 плохо растворимы в воде, что создает определенные трудности в разработке фармацевтических форм, направленных для местного воздействия.
Бета-глюкан с преимущественным содержанием 1-3 связей лучше растворим в воде, однако он менее эффективен для противовирусной защиты.
Поэтому делаются попытки усилить эффективность бета-глюкана другими ингредиентами.
Так, из международной заявки WO 2010095158 А1 известна комбинация бета-глюкана и микроколлодного серебра для лечения заболеваний слизистой оболочки носа.
Однако доктор медицины Стивен Баррет (Stephen Barrett, MD), который уделяет большое внимание защите прав потребителей, медицинской этике и научному скептицизму, в своей работе "Коллоидное серебро: бесполезный риск» (Alternative Medicine Digest) пришел к следующим выводам: «…слишком мало данных о реальности лечебных эффектов, приписываемых коллоидном серебру, риск подвергнуться токсическому воздействию серебра превышает ценность попытки необоснованного его назначения, включая использование антибактериального действия серебра. Следует прекратить незаконное распространение коллоидных серебряных продуктов, которое становится существенной проблемой для здоровья населения.». Такая же точка зрения следует из публикаций Fung МС, Bowen DL. Silver products for medical indications: risk-benefit assessment. Journal of Toxicology and Clinical Toxicology 34:119-26, 1996.
Данное утверждение нашло подтверждение в Своде регуляторных актов, регламентирующих применение коллоидного серебра (Regulation of colloidal silver and related products. Therapeutic Goods Administration Web site, Aug 19, 2003 иобзор FDA. Final rule: Over-the-counter drug products containing colloidal silver ingredients or silver salts. Federal Register 64:44653-44658, 1999.
Таким образом, к недостаткам известного средства можно отнести то, что возможен риск для здоровья и относительно дорогая цена на препарат.
Делаются попытки применять карбоксиметилированную форму 1,3/1,6 бета-глюканов.
Известно средство на основе бета-глюкана, применяемого в виде назального спрея, под торговой маркой "Immuwash".
Однако сам по себе бета-глюкан, будучи абсолютно безопасным средством при местном воздействии не может в полной мере решить проблему профилактики и, тем более лечения, вирусных заболеваний, хотя и демонстрирует значительный терапевтический потенциал.
Так, известно, (Curr Med Res Opin. 2014 Oct; 30(10):1931-5. doi: 10.1185/03007995.2014.938731. Epub 2014 Jul 7.), что добавление к карбоксиметилированной форме 1,3/1,6 бета-глюкана антиоксиданта ресвератрола существенно уменынаает выраженность симптомов, связанных с острым вирусным заболеванием у детей.
Однако известно, что и ресвератрол может вызывать ряд серьезных побочных эффектов. Так, в 2011 году компания «GlaxoSmithKline», занимавшаяся разработкой и продвижением лекарственного препарата на основе ресвератрола, заявила о прекращении дальнейшей работы над препаратом в связи с рядом выявленных негативных последствий при его применения («GSK Abandons Resveratrol, Focuses on Next Generation Compounds»).
Поэтому существует необходимость поиска средств, которые могут усиливать защитное противовирусное действие бета-глюкана.
Задача настоящего изобретения, заключается в создании эффективного противовирусного средства для наружного применения, обладающего широким спектром действия.
В заявляемом препарате отсутствуют токсические компоненты, а присутствующие активные ингредиенты стимулируют репаративные процессы, восстанавливая морфологически и биохимически нормальные структуры тканей. При этом данные вещества добавляют в незначительном количестве, что сводит практически к нулю вероятность токсической или аллергической реакции на него со стороны организма.
Авторами в ходе экспериментов неожиданно было установлено, что добавление йотта-каррагенана к бета-глюкану приводит к выраженному усилению противовирусной защиты.
Согласно заявляемого технического решения противовирусная фармацевтическая композиция дополнительно к бета-глюкану, преимуществено в виде карбоксиметил бета-глюкана натриевой соли содержит йотта-каррагенан в весовом соотношении от приблизительно 1 к 0,5 до приблизительно 1 к 5 и в предпочтительном варианте осуществления представлена в виде аэрозоля для доставки посредством дозирующего ингалятора или в виде назального или вагинального спрея, порошка для инсуфляций в полости тела, а так же геля.
Как будет далее показано на примерах, композиция может обеспечивать при однократном введении или режиме дозирования противовирусные свойства без какого-либо значительного взаимовлияния между компонентами или побочной реакции в месте применения.
Предпочтительными формами композиций согласно изобретению являються капли в нос, глазные капли, назальные спреи, растворы или аэрозоли для назальной ингаляции или инсуффляционные порошки.
Предпочтительные варианты воплощения изобретения могут включать в себя стабильные водные растворы карбоксиметилбета-глюкана или одну или более его солей в комбинации с йота-каррагенаном, которые могут быть использованы в форме раствора для ингаляций, герметизированного аэрозоля, глазных капель или капель в нос и в определенных предпочтительных вариантах воплощения изобретения в форме спрея (предпочтительно назального спрея).
Спрей может, например, быть создан посредством применения обычного флакона для сжатия, спрея или насосного пульверизатора. Кроме того, также возможно использовать аэрозоли сжатого газа. В предпочтительном варианте воплощения изобретения от 0,03 до 3 мг бета-глюкана и от 0,05 до 0,15 мг йота-карагенана должны высвобождаться при однократном срабатывании.
Композиции предпочтительно содержат консервант и/или стабилизатор. Они включают в себя, например, этилендиаминтетрауксусную кислоту (эдетовую кислоту) и ее щелочные соли (например, дищелочные соли, такие как соль динатрия, соль кальция, соль кальция-натрия), п-гидроксибензоаты низших алкилов, хлоргексидин (например, в форме ацетата или глюконата) и борат фенилртути.
Другими подходящими консервантами являются фармацевтически применимые четвертичные соединения аммония, например хлорид цетилпиридина, бромид тетрадецилтриметиламмония, обычно известный как «цетримид», хлорид бензилдиметил-[2-[2-[п-(1,1,3,3-тетраметилбутил)фенокси]этокси] аммония, обычно известный как «хлорид бензэтония», и хлорид миристилпиколина. Каждое из этих соединений может быть использовано в концентрации, стандартной для достижения консервирующего эффекта.
Предпочтительными консервантами среди четвертичных соединений аммония являються хлорид алкилбензилдиметиламмония и его смеси, например соединения, обычно известные как «хлорид бензалкония».
В случае консервантов следующие количества отдельных веществ могут, например, быть использованы: тимеросал 0,002-0,02%; хлорид бензалкония от 0,002 до 0,02% (в комбинации с тимеросалом, количество тимеросала составляет, например, от 0,002 до 0,005%); ацетат или глюконат хлоргексидина от 0,01 до 0,02%; нитрат, борат, ацетат фенилртути 0,002-0,004%; сложный эфир п-гидроксибензойной кислоты (например, смесь метилового эфира и пропилового эфира в соотношении 7:3, предпочтительно 0,05-0,15, более предпочтительно 0,1%.
В случае растворов/суспензий обычно указывают процентное отношение мас./об., в случае твердых или полутвердых композиций -процентное отношение мас./мас. композиции.
Следующими вспомогательными веществами, которые могут, например, быть использованы для композиций согласно изобретению, являются поливинилпирролидон, сложные эфиры сорбита и жирной кислоты, такие как триолеат сорбита, полиэтоксилированные эфиры сорбита и жирной кислоты (например, полиэтоксилированный триолеат сорбита), олеат сорбимакрогола, синтетические амфотензиды (тритоны), этиленоксидные эфиры продуктов конденсации октилфенолформальдегида, фосфатиды, такие как лецитин, полиэтоксилированные жиры, полиэтоксилированные олеотриглицерилы и полиэтоксилированные жирные спирты.
В данном контексте полиэтоксилированный означает, что подходящие вещества содержат полиоксиэтиленовые цепи, степень полимеризации которых обычно составляет от 2 до 40, в частности между 10 и 20. Такие вещества предпочтительно используют для улучшения растворимости бета-глюканового компонента.
Необязательно является возможным использовать дополнительные изотонические агенты. Изотоническими агентами, которые могут, например, быть использованы, являются сахароза, глюкоза, глицерин, сорбит, 1,2-пропиленгликоль или NaCl.
Изотонические агенты доводят осмотическое давление композиций до такого же осмотического давления, как у выделяемого из носа. С этой целью такие вещества в каждом случае должны использоваться в таких количествах, посредством которых, например, в случае раствора, достигается снижение температуры замерзания от 0,50 до 0,56 градусов С по сравнению с чистой водой.
Также возможно добавлять к композициям буферные вещества, такие как лимонной кислоты/гидросульфата натрия боратный буфер, фосфаты (гидроортофосфат натрия, гидрофосфат динатрия), трометамол или равноценные обычные буферы с целью, например, доведения композиций до значения рН от 3 до 7, предпочтительно от 4,5 до 6,5.
В примере 1 можно использовать вместо NaCl на 100 мл раствора, например, глюкозу 1Н2O 3,81 г; сахарозу 6,35 г; глицерин 2,2 г; 1,2-пропиленгликоль 1,617 г; сорбит 3,84 г (в случае смесей таких веществ они, соответственно, при желании могут быть использованы в меньших количествах).
Более того, возможно добавлять загустители к растворам в соответствии с настоящим изобретением для предотвращения слишком быстрого вытекания раствора из носа и для придания раствору вязкости около 1,5-3 мПа, предпочтительно 2 мПа.
Такими загустителями могут, например, быть производные целлюлозы (например, эфир целлюлозы), в которых гидроксигруппы целлюлозы частично этерифицированы низшими ненасыщенными алифатическими спиртами и/или низшими ненасыщенными алифатическими оксиспиртами (например, метилцеллюлоза, карбоксиметилцеллюлоза, гидроксипропилметилцеллюлоза), желатин, поливинилпирролидон, трагакант, этоксоза (водорастворимые вяжущие и сгущающие вещества на основании этилцеллюлозы), альгиновая кислота, поливиниловый спирт, полиакриловая кислота, пектин и равноценные агенты. Если такие вещества содержат кислотные группы, соответствующие физиологически приемлемые соли также могут быть использованы.
В случае использования гидроксипропилцеллюлозы для этой цели используют, например, 0,1 мас. % композиции.
В случае использования Avicel RC 591 или CLII для этой цели используют, например, 0,65-3,0 мас. % композиции.
Для назального применения может предпочтительно быть использован раствор или суспензия, который применяют в виде аэрозоля, т.е. в форме мелкой дисперсии в воздухе или в другом обычном газе-носителе, например, посредством обычного насосного пульверизатора.
Применение заявляемой композиции в виде дозированного аэрозоля также является возможным.
Дозированные аэрозоли определяют как аэрозольные упаковки, которые содержат бета-глюкан или его соли или эфиры в комбинации с йота-каррагенаном, растворенные преимущественно в воде в так называемом пропелленте.
Пропеллентом может быть находящийся под давлением жидкий хлорированный, фторированный углеводород или смесь различных хлорированных, фторированных углеводородов, а также пропан, бутан, изобутен или их смеси друг с другом или с хлорированными, фторированными углеводородами, которые являются газообразными при атмосферном давлении и комнатной температуре. Гидрофторуглероды (ГФУ), такие как ГФУ 134а и ГФУ 227а, также могут быть использованы и являются предпочтительными по причинам защиты окружающей среды.
Аэрозольная упаковка имеет дозатор или дозирующий клапан, которые при срабатывании высвобождают определенное количество раствора или суспензии лекарственного средства. В результате очень быстрое парообразование пропеллента разрывает раствор или суспензию азеластина на мелкие капельки или мельчайшие частицы, которые могут быть распылены в нос или которые доступны для вдыхания в нос. Определенные пластиковые аппликаторы могут быть использованы для приведения в действие клапана и для переноса распыленной суспензии в нос.
В случае применения композизии согласно изобретению в виде аэрозоля также возможно использование обычного соединительного устройства.
Особенно предпочтительные варианты воплощения настоящего изобретения описаны ниже, и, конечно, необходимо понимать, что предыдущее описание подходящих ингредиентов и характеристик композиции также может быть применимо к следующим продуктам и композициям, которые обеспечиваются настоящим изобретением.
Необходимо понимать, следовательно, что настоящее изобретение, кроме того, обеспечивает фармацевтический продукт, включающий в себя (i) бета-глюкан или его фармацевтически приемлемую соль, сольват или физиологически функциональное производное, представленный в аэрозольной композиции, предпочтительно вместе с пропеллентом, обычно подходящим для доставки посредством MDI, и (ii) по меньшей мере один йотта-каррагенан или его фармацевтически приемлемую соль, сольват или физиологически функциональное производное, представленное в аэрозольной композиции, предпочтительно вместе с пропеллентом, обычно подходящим для доставки с помощью MDI, в качестве комбинированного препарата для одновременного, раздельного или последовательного применения в лечении состояний, вызванных вирусами.
Настоящее изобретение также обеспечивает композицию аэрозоля, предпочтительно подходящую для доставки посредством MDI, включающую в себя (i) азеластин или его фармацевтически приемлемую соль, сольват или физиологически функциональное производное, и (ii) по меньшей мере один стероид или его фармацевтически приемлемую соль, сольват или физиологически функциональное производное, вместе с пропеллентом.
Также, необходимо учитывать, что соответствующие терапевтические агенты комбинированного препарата могут вводиться одновременно, в одной и той же или различных фармацевтических композициях, или раздельно или последовательно. Если имеет место раздельное или последовательное введение, также необходимо понимать, что последовательно вводимые терапевтические агенты должны вводиться пациенту в течение временного промежутка, таким образом, чтобы достичь или, в особенности, оптимизировать вышеописанный полезный синергический терапевтический эффект комбинированного препарата, который присутствует в фармацевтическом продукте в соответствии с настоящим изобретением.
Предпочтительно фармацевтическая аэрозольная композиция согласно изобретению дополнительно включает в себя полярный сорастворитель, такой как С2-6-алифатические спирты и полиолы, например этанол, изопропанол и пропиленгликоль, причем этанол часто является предпочтительным. Предпочтительно концентрация сорастворителя заключена в диапазоне примерно от 2 до 10 мас. %, обычно примерно до 5% общей композиции.
Фармацевтическая аэрозольная композиция согласно изобретению может, кроме того, включать в себя одно или более поверхностно-активных веществ. Такие поверхностно-активные вещества могут быть включены для стабилизации композиций и для смазывания клапанной системы. Наиболее предпочтительные поверхностно-активные вещества в аэрозольных композициях включают масла, полученные из естественных источников, такие как кукурузное масло, оливковое масло, хлопковое масло и подсолнечное масло, а также фосфолипиды. Подходящие поверхностно-активные вещества могут включать в себя лецитин, олеиновую кислоту и олеат сорбита.
Следующим предпочтительным вариантом воплощения настоящего изобретения может быть такой вариант, при котором композиция или продукт представлен в форме инсуффлируемого порошка, где предпочтительным является максимальный размер частиц вещества, соответственно, не более 10 мкм. Бета-глюкан или его соли и йотта-карагенан могут быть смешаны с инертными веществами-носителями или помещены на инертные вещества-носители. Веществами-носителями, которые могут быть использованы, являются, например, сахара, такие как глюкоза, сахароза, лактоза и фруктоза. Также такими веществами могут быть крахмалы или производные крахмала, олигосахариды, такие как декстрины, циклодекстрины и их производные, поливинилпирролидон, альгиновая кислота, тилоза, кремниевая кислота, целлюлоза, производные целлюлозы (например, эфир целлюлозы), сахарные спирты, такие как маннит или сорбит, карбонат кальция, фосфат кальция и др.
В одном из вариантов воплощения изобретения применяемые терапевтические агенты имеют размер частиц менее, чем примерно 10 мкм, предпочтительно менее чем 5 мкм.
Применение инсуффляционных порошков может представлять собой предпочтительный вариант воплощения настоящего изобретения. Настоящим изобретением обеспечивается фармацевтический продукт, включающий в себя (i) бета-глюкан или его фармацевтически приемлемую соль, сольват или физиологически функциональное производное, представленный в виде инсуффляционного порошка, и (ii) йотта-каррагенан, сольват или физиологически функциональное производное, представленное в виде инсуффляционного порошка, в качестве комбинированного препарата для одновременного, раздельного или последовательного применения при лечении состояний, спровоцированных вирусной интоксикацией.
Композиции сухого инсуффляционного порошка согласно настоящему изобретению могут быть полезными в случае, когда требуется, чтобы терапевтические агенты удерживались в носовой полости, а системные побочные эффекты были минимизированы или устранены. Более того, композиции инсуффляционного порошка могут быть полезны за счет того, что удерживание бета-глюкана или его фармацевтически приемлемой соли, сольвата или физиологически функционального производного на слизистой оболочке носа улучшено, и неприятный привкус, связанный с жидкими противовирусными композициями, значительно уменьшается, при этом такие композиции также проявляют синергический терапевтический эффект, связанный с комбинациями бета-глюкана/йотта-каррагенана, предлагаемыми настоящим изобретением.
Путем обеспечения композиции сухого инсуффляционного порошка бета-глюкана вместе с йотта-каррагенаном, имеющей средний размер частиц примерно менее 10 мкм, терапевтические агенты могут быть направлены главным образом на желаемый орган-мишень, слизистую оболочку носа, полости рта или влагалища.
Композиция сухого инсуффляционного порошка в соответствии с настоящим изобретением может быть введена при использовании инсуффлятора, который может давать мелкораспыленное облако сухого порошка. Предпочтительно инсуффлятор снабжен средствами для обеспечения введения по существу заранее определенного количества композиции или продукта, обеспечиваемых настоящим изобретением. Порошок может быть использован непосредственно с инсуффлятором, который снабжен флаконом или контейнером для порошка, или порошок может быть помещен в капсулу или картридж, такой как желатиновая капсула, или другое устройство для однократной дозы, приспособленное для введения. Инсуффлятор предпочтительно имеет средства для открывания капсулы или другого дозирующего устройства.
Следующим предпочтительным вариантом воплощения настоящего изобретения может быть такой вариант, при котором композиция представлена в форме геля. В одном варианте воплощения изобретения в применяемые сольватированные терапевтические агенты добавляют загустители, обеспечивающего стабильную гелевую основу. В качестве гелеобразователей предпочтительно, но не обязательно использовать карбополы и/или карбоксиметилцеллюлозу предпочтительно в виде натриевой соли в среде липофильного сольвата, в этом варианте предпочтительно глицерина или его уксусного эфира.
Композиция в соответствии с настоящим изобретением может быть нанесена локально на кожу, слизнете, введена в наружные полости тела.
Предпочтительные комбинации терапевтических агентов, применяемых в фармацевтических продуктах и композициях в соответствии с настоящим изобретением (в частности, назальных спреях или каплях, аэрозоле, геле или инсуффляционных продуктах и композициях, как описано выше), и включают в себя любую из следующих комбинаций.
Настоящее изобретение, кроме того, обеспечивает, следовательно, фармацевтический продукт, включающий в себя (i) бета-глюкан или его фармацевтически приемлемую соль и (ii) йотта-каррагенан в виде комбинированного препарата для одновременного, отдельного или последовательного применения в лечении состояний, для которых показано введение одного или более противовирусного средства.
Настоящее изобретение также обеспечивает фармацевтическую композицию, содержащую (i) бета-глюкан или его фармацевтически приемлемую соль и (ii) йотта-каррагенан, вместе с фармацевтически приемлемым для них носителем или вспомогательным веществом.
В случае назального спрея особенно предпочтительной композицией согласно изобретению является назальный спрей, содержащий предпочтительно карбоксиметилбета-глюкан натрия или его другую фармацевтически приемлемую соль, вместе с йотта-каррагенаном в водной среде осмотического агента, стабилизатора, предпочтительно этилендиаминтетра уксусной кислоты динатриевой соли, консерванта, предпочтительно тиомерсала, и буфера водородных ионов, предпочтительно фосфата натрия и/или калия для достижения рН 6,0-7,0.
Также настоящее изобретение обеспечивает способ профилактики или лечения у млекопитающего, такого как человек, состояний, вызванных вирусными агентами, данный способ включает в себя введение терапевтически эффективного количества фармацевтического продукта, по существу, как описано ниже, в виде комбинированного препарата для одновременного, раздельного или последовательного применения в полости тела.
Настоящее изобретение также обеспечивает способ получения фармацевтической композиции, по существу, как описано выше, данный способ включает в себя смешивание фармацевтически приемлемого носителя или вспомогательного вещества с (i) бета-глюканом или его фармацевтически приемлемой солью, сольватом или физиологически функциональным производным и (ii) йотта-карагенаном, сольватом или физиологически функциональным производным. Предпочтительно фармацевтические композиции в соответствии с настоящим изобретением могут включать в себя композиции инсуффляционного порошка, назальных спреев, растворов или аэрозолей для назальной ингаляции, для влагалищных ирригаций и введения по существу, как описано выше.
Далее настоящее изобретение проиллюстрировано следующими примерами, которые не ограничивают рамки изобретения каким-либо образом. В примерах, где только перечислены ингредиенты композиций согласно изобретению, такие композиции получают с помощью методик, хорошо известных в данной области.
ПРИМЕРЫ
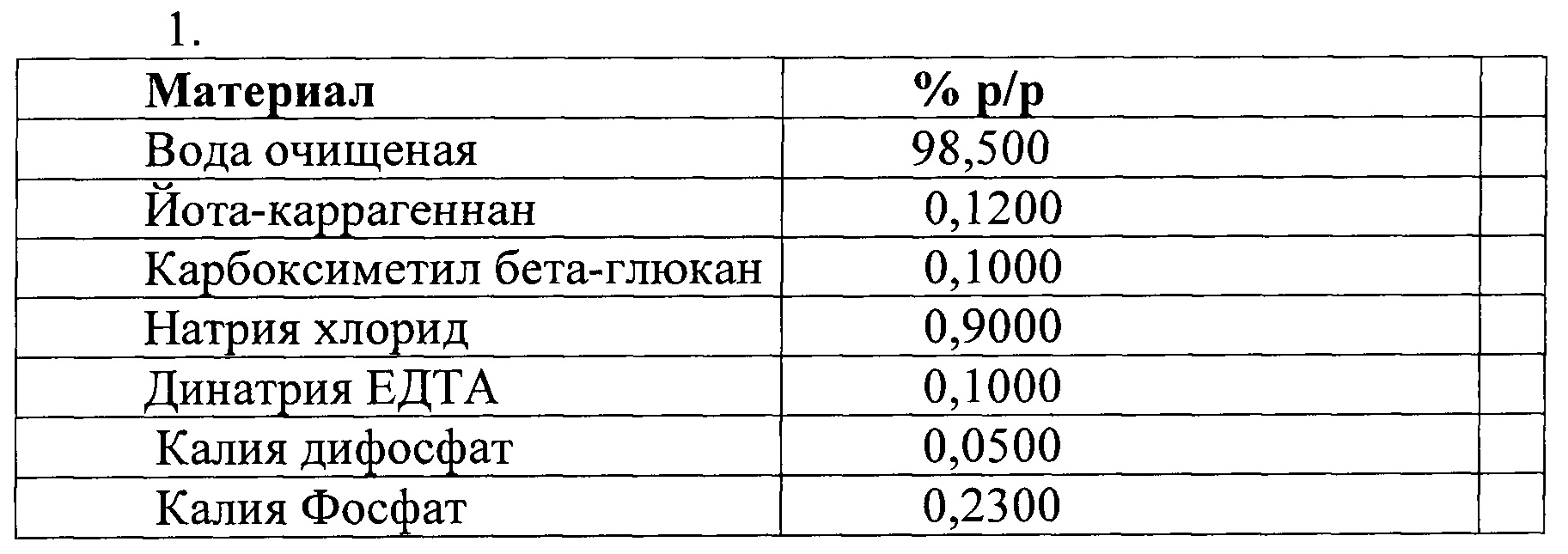
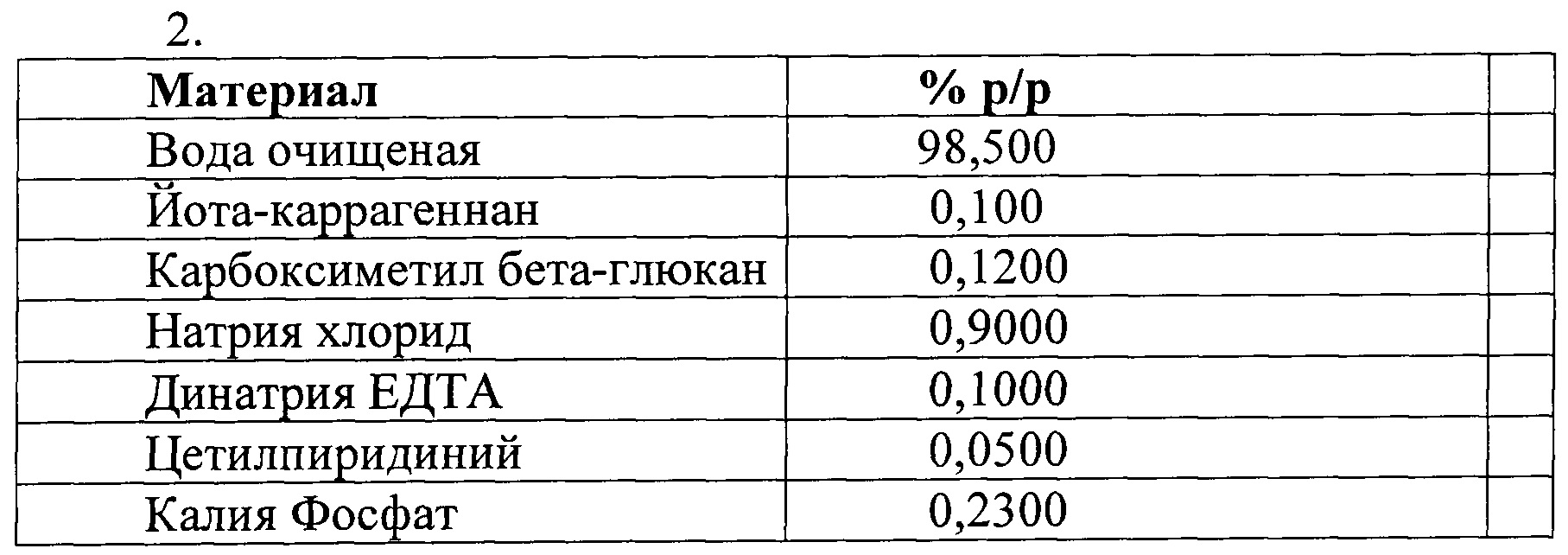
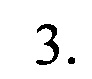
Примеры изучения антивирусного действия:
Изучение противовирусной активности бета-глюкана и каррагенана, полученных предлагаемым способом.
Для изучения противовирусной активности фармацевтической композиции использовали цитопатогенный для культур клеток почки эмбриона свиньи (СПЭВ) вариант вируса герпеса, изолированный из сыворотки крови больного герпетической инфекцией. Вирусосодержащий материал представлял собой культуральную жидкость, собранную из зараженных вирусом герпеса культур клеток СПЭВ на высоте развития цитопатических проявлений. Исходный титр вируса - 7,51 g ТЦЦ50/100 мкл.
В опытах использовали дозу вируса герпеса равную 10,0 и 1,0 ТЦД50.
Культуры клеток. Исследования противовирусной активности препарата проводили в чувствительных для репликации вируса герпеса культурах клеток СПЭВ, выращенных в виде однодневного монослоя клеток в 24-луночных панелях на среде 199 с добавлением 7% сыворотки крупного рогатого скота, пенициллина и стрептомицина по 100 ЕД/мл.
Фармацевтические композиции в различных концентрациях добавляли в питательную среду культур клеток СПЭВ, после чего на протяжении 4-х суток наблюдали за жизнеспособностью и пролиферативной активностью клеток. Учет результатов проводили по регистрации % жизнеспособных клеток и их пролиферативной активности.

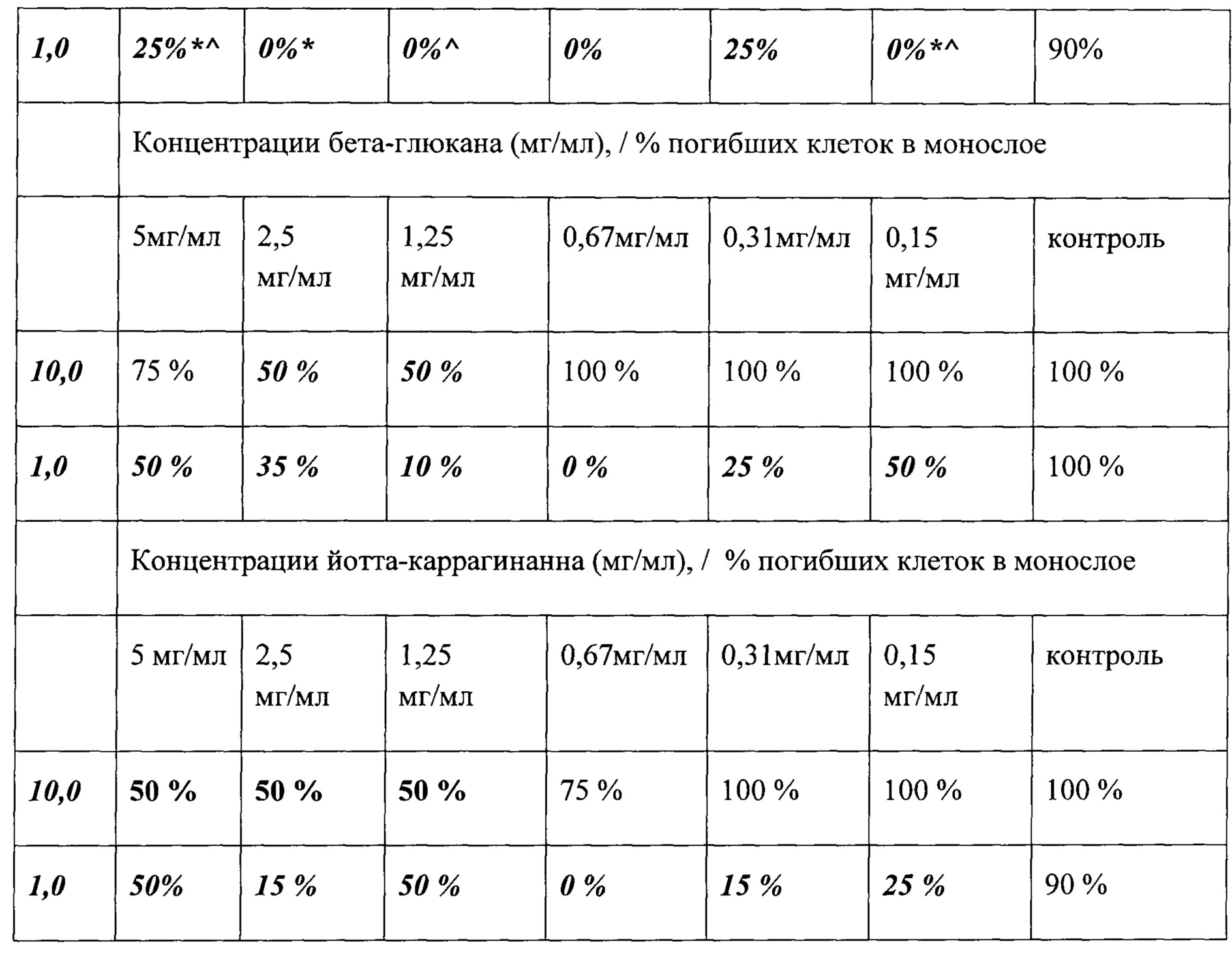
Примечание: Жирные цифры - разница достоверна с контролем (р<0,05), * - разница достоверна с группой бета-глюкана(р<0,05), ^ - разница достоверна с группой каррагенана(р<0,05)
При использовании высокой дозы вируса герпеса для заражения клеток СПЭВ (10,0 ТЦЦ50) был отмечен выраженный противовирусный эффект при использовании достаточных доз фармацевтической композиции. В отличие от раздельного применения бета-глюкана и каррагенана, которые по отдельности оказывали всего лишь незначительное действие, причем более выраженное у каррагенанана.
При использовании низкой дозы вируса герпеса для заражения клеток СПЭВ (1,0 ТЦЦ50) был отмечен практически полный противовирусный эффект фармацевтической композиции.
Приведенные данные свидетельствуют о вираженном аддитивном действии компонентов фармацевтической композиции.

