Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ ОПТИЧЕСКОГО ИЗОБРАЖЕНИЯ МЕЖФАЛАНГОВЫХ СУСТАВОВ И ОПТИЧЕСКИЙ СЕНСОР ДЛЯ ЕГО РЕАЛИЗАЦИИ
Вид РИД
Изобретение
Группа изобретений относится к медицине, а именно к методу биомедицинской визуализации и устройству для его реализации, в частности, оптической визуализации изображений, и может быть использовано для неинвазивной диагностики заболеваний суставов, в том числе ревматоидного артрита.
Одним из наиболее перспективных методов визуализации является оптический метод получения изображений благодаря своей абсолютной безопасности, высокой чувствительности и уникальной специфичности по сравнению с другими методами биомедицинской визуализации. Оптическая визуализация в биомедицине определяется взаимодействием света с микроскопическими и макроскопическими составляющими среды в результате поглощения и рассеяния света. Поэтому характеристики поглощения и рассеяния света тканями человека могут коррелировать с развитием заболевания. Просвечивание является одним из перспективных методов оптической визуализации внутренней структуры биологической ткани.
Известен способ получения оптического изображения и устройство оптической томографии для получения изображений суставов пальцев и рук (см. заявку WO 2014/028594 по МПК А61В 8/13, опуб. 20.02.2014). Способ включает получение оптического томографического изображения для диагностики медицинских состояний, таких как ревматоидный артрит, путем облучения точек на поверхности суставов, таких как пальцы человека в плоскости поперечного сечения и детектирования отраженного сигнала. Устройство включает множество источников и детекторов оптического излучения, расположенных вокруг суставов. В вариантах осуществления обеспечивается удобное расположение источников и детекторов и быстрое получение анатомической геометрии поверхности.
Однако устройство и способ основаны на получении томографических изображений, что существенно затрудняет изучение межфаланговых суставов пальцев и не обеспечивает необходимого пространственного разрешения. В результате способ трудоёмок, а конструкция устройства достаточно сложна из-за наличия множества источников и детекторов, приводящих к многообразию связей между ними, требующих наличия специальных сотрудников, обеспечивающих работу устройства, а также разработки специального программного обеспечения для управления и решения сложных обратных задач по реконструкции изображения.
Известен также биосенсор для неинвазивного оптического мониторинга патологии биологических тканей (см. патент РФ № 2633494, МПК A61B 5/05, опуб. 25.07.2017), реализующий метод просвечивания. Биосенсор содержит источник и приемник излучения; аппликатор, изготовленный в виде сосуда с биосовместимым иммерсионным агентом (оптическим просветляющим агентом (ОПА); излучающий световод, подключенный одним концом к источнику излучения, принимающий световод, подключенный одним концом к приемнику излучения, при этом дистальные концы световодов расположены внутри аппликатора.
Способ для неинвазивного оптического мониторинга патологии биологических тканей, согласно патенту № 2633494, заключается в нанесении на исследуемую биологическую ткань биосовместимого иммерсионного агента, вызывающего изменение во времени коэффициента оптического отражения и/или пропускания ткани за счет ее дегидратации и проникновения в нее молекул агента, облучении биологической ткани, определение степени гликированности ткани, по которой судят о развитии заболевания, при этом облучение осуществляют на одной или несколькихдлинах волн в диапазоне 400-2300 нм после нанесения агента, измеряют временную зависимость изменения коэффициента оптического отражения/пропускания в течение 5-30 минут, определяют коэффициент диффузии иммерсионного агента в ткани, и по величине этого коэффициента судят о наличии или развитии патологии исследуемой ткани, а также тканей внутренних жизненно важных органов труднодоступных для светового излучения.
Однако данное устройство и способ, лежащий в его основе, реализуют не прямой, а косвенный характер получения информации о патологии, изучается состояние кожи и только по одному патологическому параметру – степени гликированности белков при сахарном диабете предсказывается состояние внутренних (недоступных непосредственно) органов. Сам сенсор предназначен только для исследования оптических свойств кожи и неприменим для исследования суставов из-за отсутствия специальных приспособлений для их просвечивания и получения изображений.
Наиболее близким к заявляемому является способ получения оптического изображения межфаланговых суставов и оптический сенсор для его реализации (см. E. A. Kolesnikova et al., Optical clearing of human skin for the enhancement of optical imaging of proximal interphalangeal joints, Optical Technologies in Biophysics and Medicine XV; and Laser Physics and Photonics XV, edited by E. A. Genina et al., Proc. of SPIE Vol. 9031, 90310Cdoi: 10.1117/12.2049525).Способ получения оптического изображения межфаланговых суставов заключается в воздействии на сустав пальца биосовместимым иммерсионным агентом, обладающим гиперосмотическим действием и показателем преломления, равным или большим среднего показателя преломления кожи, просвечивании сустава оптическим излучением последовательно на нескольких длинах волн, лежащих в области окна прозрачности биологических тканей, регистрации соответствующих изображений с помощью цифровой камеры, располагающейся по другую сторону от источника света по отношению к положению сустава, определении контраста изображения в рамках статистики первого или второго порядка.
Оптический сенсор для реализации способа содержит, по крайней мере, один источник лазерного излучения, обеспечивающий три или более длины волны лазерного излучения(670, 820 и 904 нм), световод, цифровую монохромную камеру с линзой и ИК-корректирующей линзой для регистрации изображения проксимальных и дистальных межфаланговых суставов пальцев человека, расположенную с противоположной стороны от источника излучения по отношению к положению сустава, опору для пальца, программируемый блок управления источником лазерного изучения и цифровой монохромной камерой, выполненный с возможностью получения изображения пальца в режиме просвечивания в реальном времени на мониторе компьютера.
Однако контраст получаемого изображения невелик за счёт наличия значительного рассеяния лазерного пучка на входе в кожу пальца и выходе из него. Кроме того, расположение сустава недостаточно хорошо ориентировано относительно направления пучка лазерного излучения, что существенно снижает эффект от иммерсии подповерхностных структур кожи пальца. Иммерсия кожи просветляющими агентами также неэффективна из-за отсутствия физических и химических усилителей проницаемости кожи.
Технической проблемой заявляемой группы изобретений является получение контрастного оптического изображения путём просвечивания лазерным излучением межфаланговых суставов для обеспечения возможности диагностики заболеваний суставов, в частности ревматоидного артрита.
Техническим результатом является повышение контраста оптического изображения за счёт выявленного нового свойства иммерсионного агента и особой формы аппликатора для его размещения, обеспечивающих процесс натяжения кожи в течение определённого времени и иммерсию неоднородной границы и подповерхностных структур кожи пальца, что существенно повышает эффективность ввода излучения в ткань пальца за счет минимизации рассеяния на входе лазерного пучка в кожу и на выходе из кожи с обратной стороны.
Техническая проблема и заявляемый технический результат достигается тем, что в способе получения оптического изображения межфаланговых суставов, включающем воздействие на сустав пальца биосовместимым иммерсионным агентом, обладающим гиперосмотическим действием и показателем преломления, равным или большим среднего показателя преломления кожи, просвечивание сустава оптическим излучением последовательно на нескольких длинах волн, лежащих в области окна прозрачности биологических тканей, регистрацию соответствующих изображений с помощью цифровой камеры, располагающейся по другую сторону от источника света по отношению к положению сустава, определение контраста изображения осуществляют в рамках статистики первого порядка, согласно изобретению, перед просвечиванием исследуемую область погружают в иммерсионный агент на 8-10 минут до достижения натяжения кожи, при этом иммерсионный агент помещают в сосуд с двумя плоскими стенками, расположенными напротив друг друга, через которые осуществляют просвечивание.
Для комфортного проведения процедуры иммерсионный агент подогревают до физиологической температуры поверхности пальца и выше, в частности до 33-39°С.
В качестве иммерсионного агента могут быть использованы: дегидратированный глицерин с концентрацией не ниже 99%, либо водный раствор глицерина с концентрацией 70- 99%, либо лосьон для рук с 1-30%-ным содержанием мочевины, в состав которого также входит глицерин, либо водный раствор глюкозы с концентрацией 40-60%, либо водный раствор фруктозы с концентрацией 40-80%, либо водный раствор сахарозы с концентрацией 40-70%, либо водные растворы мальтозы и маннитола с концентрациями 40-50%, либо пропиленгликоль с концентрациями 80-100%, либо полиэтиленгликоль (ПЭГ) с молекулярной массой 300-600.
В качестве иммерсионного агента могут быть также использованы смеси растворов, в частности - раствор, содержащий 50% глюкозы, 20% воды и 30% этанола, либо водно-спиртовые растворы глюкозы, сахарозы, фруктозы, мальтозы с концентрациями 50% при содержании спирта до 30%.
Для усиления проницаемости кожи могут быть использованы химические усилители проницаемости кожи, такие как этиловый спирт, диметилсульфоксид, олеиновая кислота, гиалуроновая кислота, тиазон.
Для усиления проницаемости кожи могут быть использованы физические усилители проницаемости кожи, такие как сонофорез, электрофорез, лазерофорез.
Для усиления проницаемости кожи с одновременным достижением терапевтического эффекта в качестве иммерсионного агента может быть использован раствор, состоящий из 45% глицерина, 45 % диметилсульфоксида и 10% воды.
При осуществлении просвечивания сустава выбирают длины волн, лежащие в видимом и инфракрасном диапазонах длин волн, а именно 670-975 нм, 1100-1350 нм, 1600-1870 нм и 2100-2300 нм, которые соответствуют “оптическим окнам прозрачности” мягких и твердых биологических тканей [В.В. Тучин, Оптика биологических тканей. Методы рассеяния света в медицинской диагностике, 2-е издание, Физматлит, 2012, 811 с.]. Такие “окна” определяются спектрами поглощения основных хромофоров биотканей, таких как гемоглобин крови, вода и липиды.
Оптический сенсор для реализации способа получения оптического изображения межфаланговых суставов содержит, по крайней мере, один источник лазерного излучения, обеспечивающий три или более длины волны лазерного излучения, световод, цифровую монохромную камеру с линзой и ИК-корректирующей линзой для регистрации изображения проксимальных и дистальных межфаланговых суставов пальцев человека, расположенную с противоположной стороны от источника излучения по отношению к положению сустава, опору кисти руки, программируемый блок управления источником лазерного изучения и цифровой монохромной камерой, выполненный с возможностью получения изображения пальца в режиме просвечивания в реальном времени на мониторе компьютера. Согласно изобретению, оптический сенсор дополнительно содержит камеру-аппликатор из прозрачного стекла или пластика для иммерсионного агента, охватывающего палец со всех сторон, камера-аппликатор имеет две плоские и две закругленные стенки, опора для пальца выполнена в виде корпуса симметричной сферической формы, источник лазерного излучения и камера установлены в корпусе, корпус имеет окно напротив камеры и дополнительное отверстие для обеспечения возможности вертикального размещения пальца в аппликаторе с просветляющим агентом, один конец световода закреплен на корпусе шарнирным соединением с возможностью поворота на 90°, а другой снабжен разъемом, установленным напротив плоских стенок камеры-аппликатора, цифровая камера выполнена с возможностью изменения положения по вертикали и горизонтали, при этом камера-аппликатор расположена на корпусе напротив окна и выполнена с возможностью перемещения.
Камера-аппликатор может быть установлена на передвижном столике с микрометрическим винтом, либо на сильфоне с фиксатором
Камера-аппликатор закреплена на корпусе с помощью разъемных монтажных колец.
Цифровая камера связана с линзой с фокальным расстоянием 12 мм посредством крепления CS-Mount.
Группа изобретений поясняется иллюстрациями, где представлены:
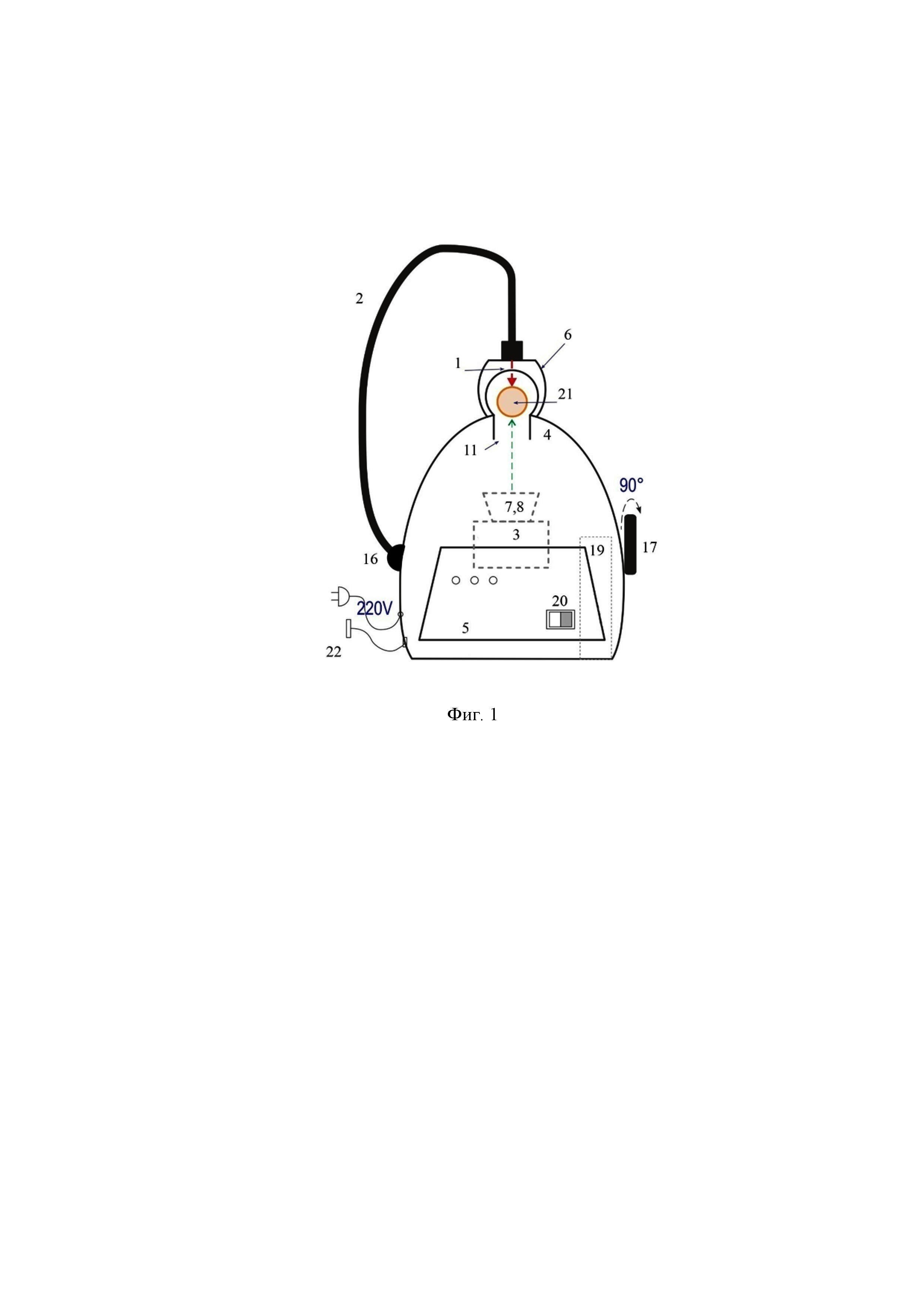
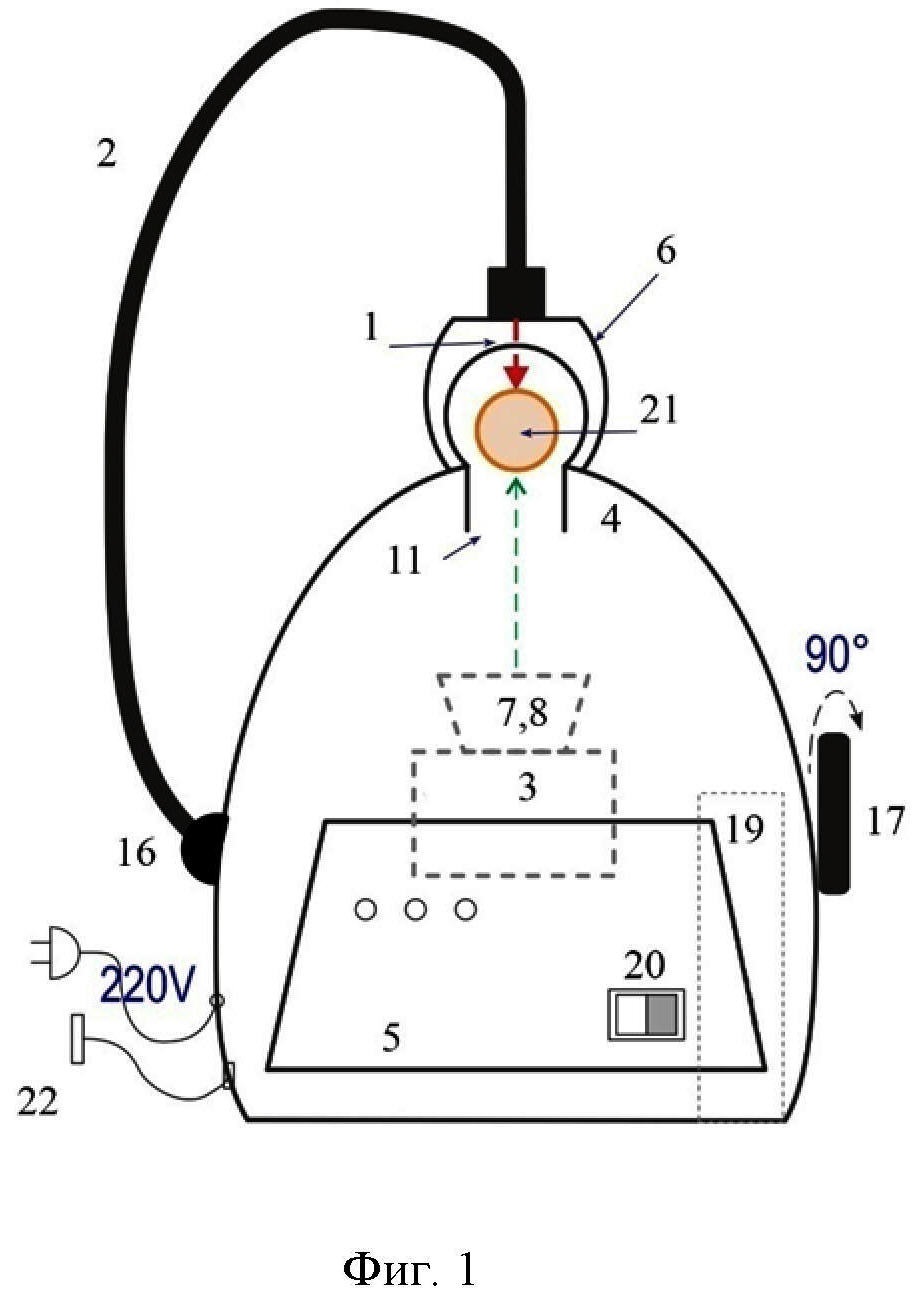
на фиг. 1 –оптический сенсор для реализации способа получения оптического изображения межфаланговых суставов (вид спереди);
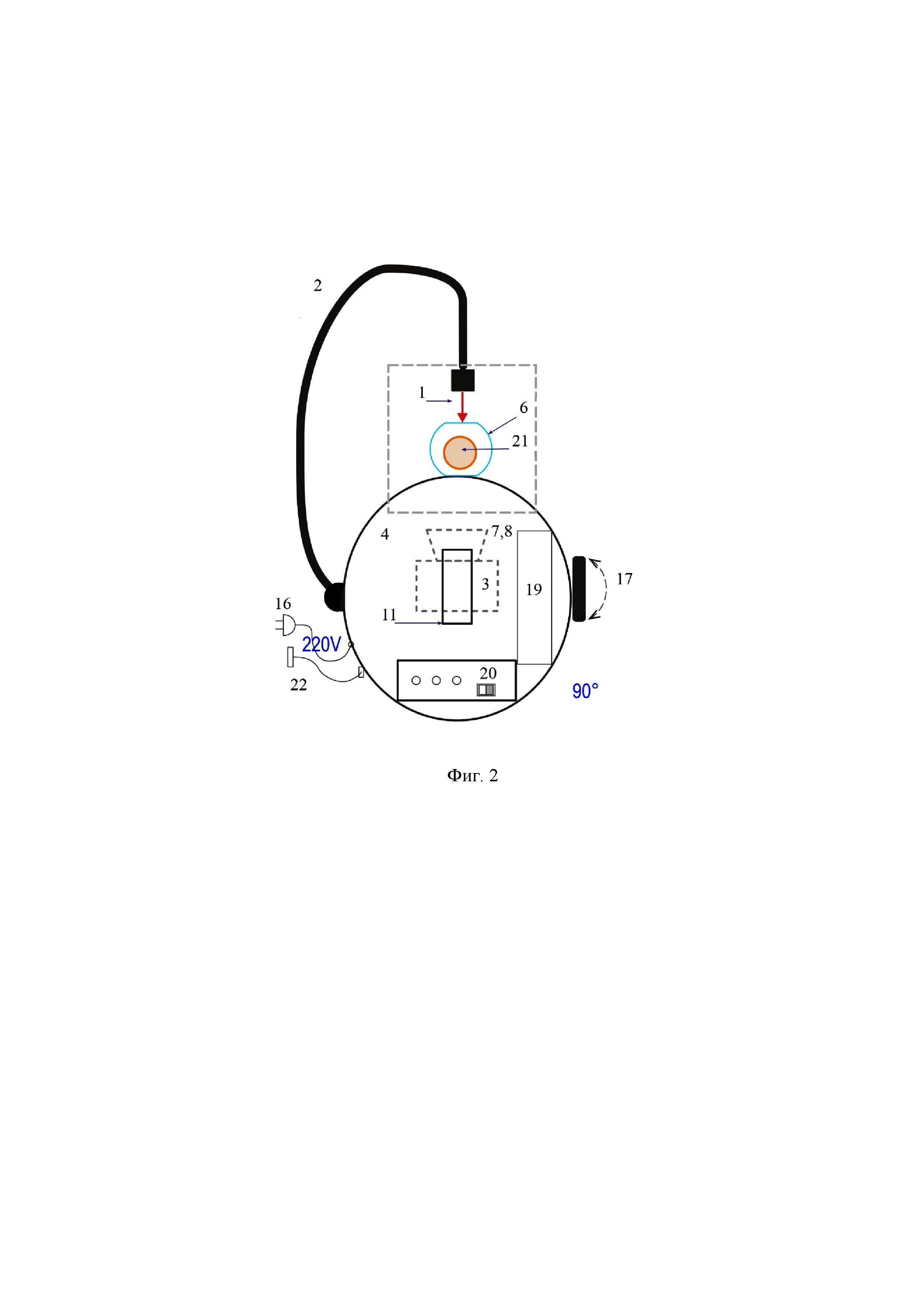
на фиг. 2 –оптический сенсор (вид сверху);
на фиг. 3 –схема расположения камеры-аппликатора;
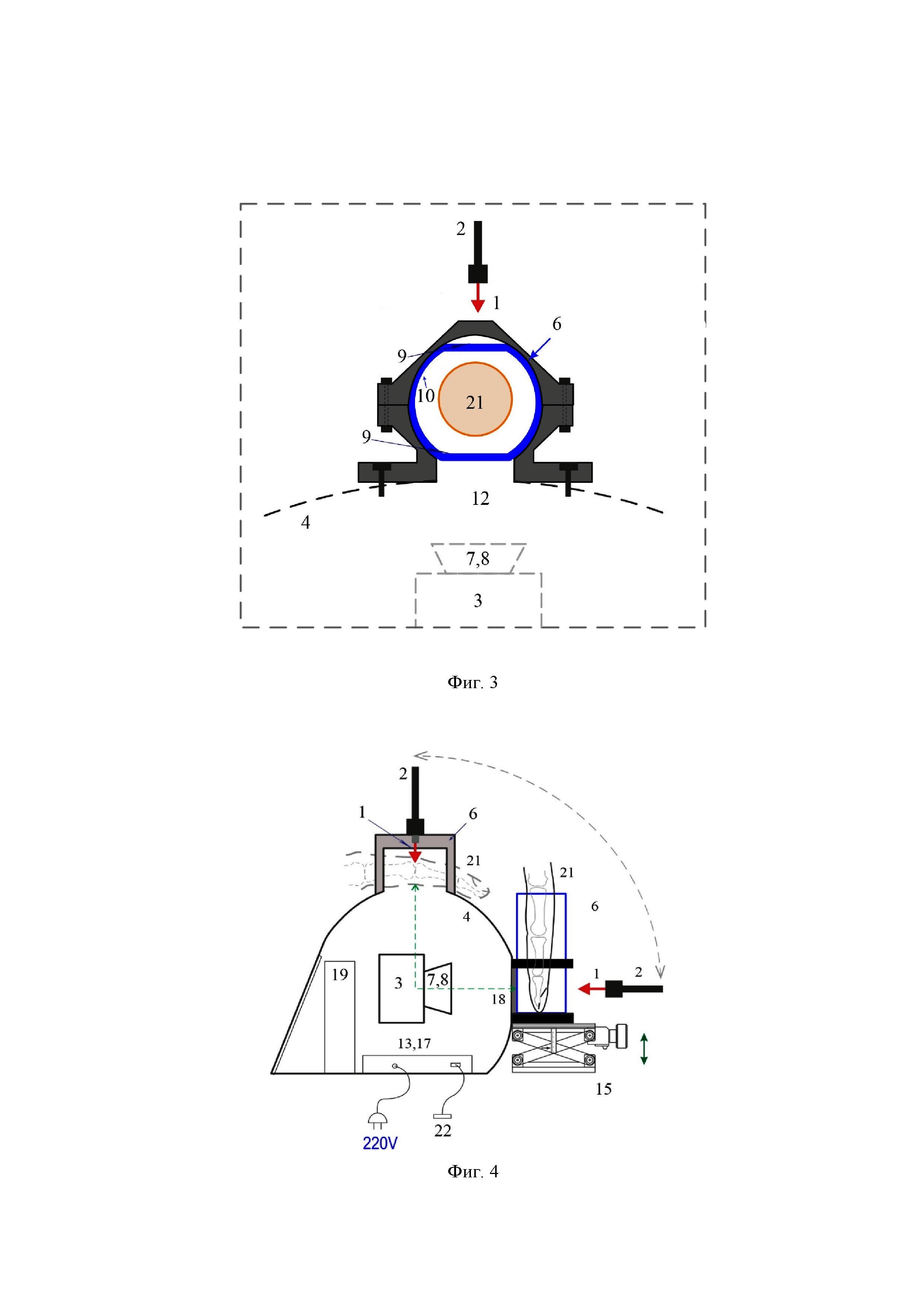
на фиг. 4–оптический сенсор с камерой- аппликатором на передвижном столике (вид сбоку);
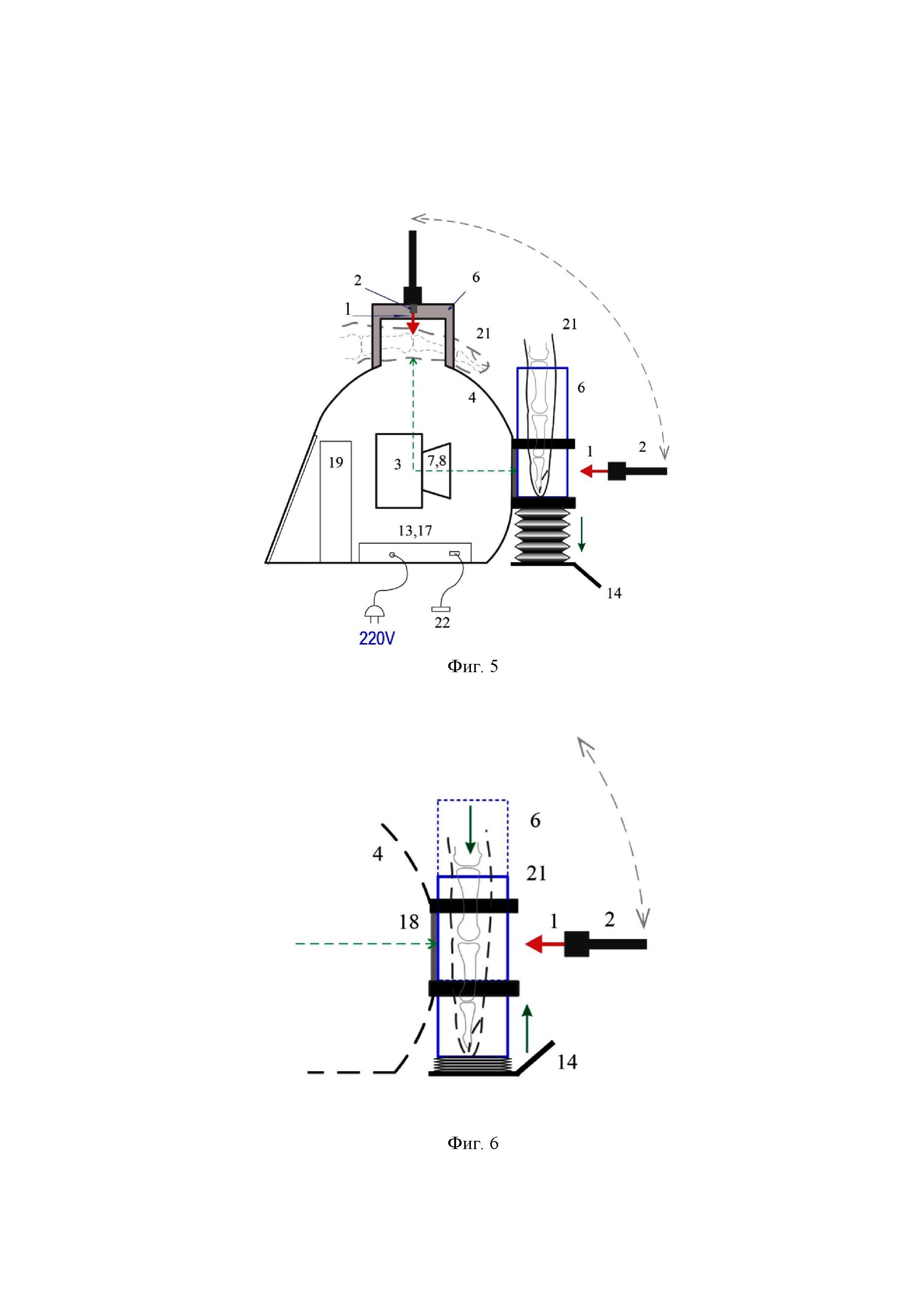
на фиг. 5 – оптический сенсор с камерой- аппликатором на сильфоне (вид сбоку);
на фиг. 6 – камера- аппликатор на сильфоне в сжатом состоянии;
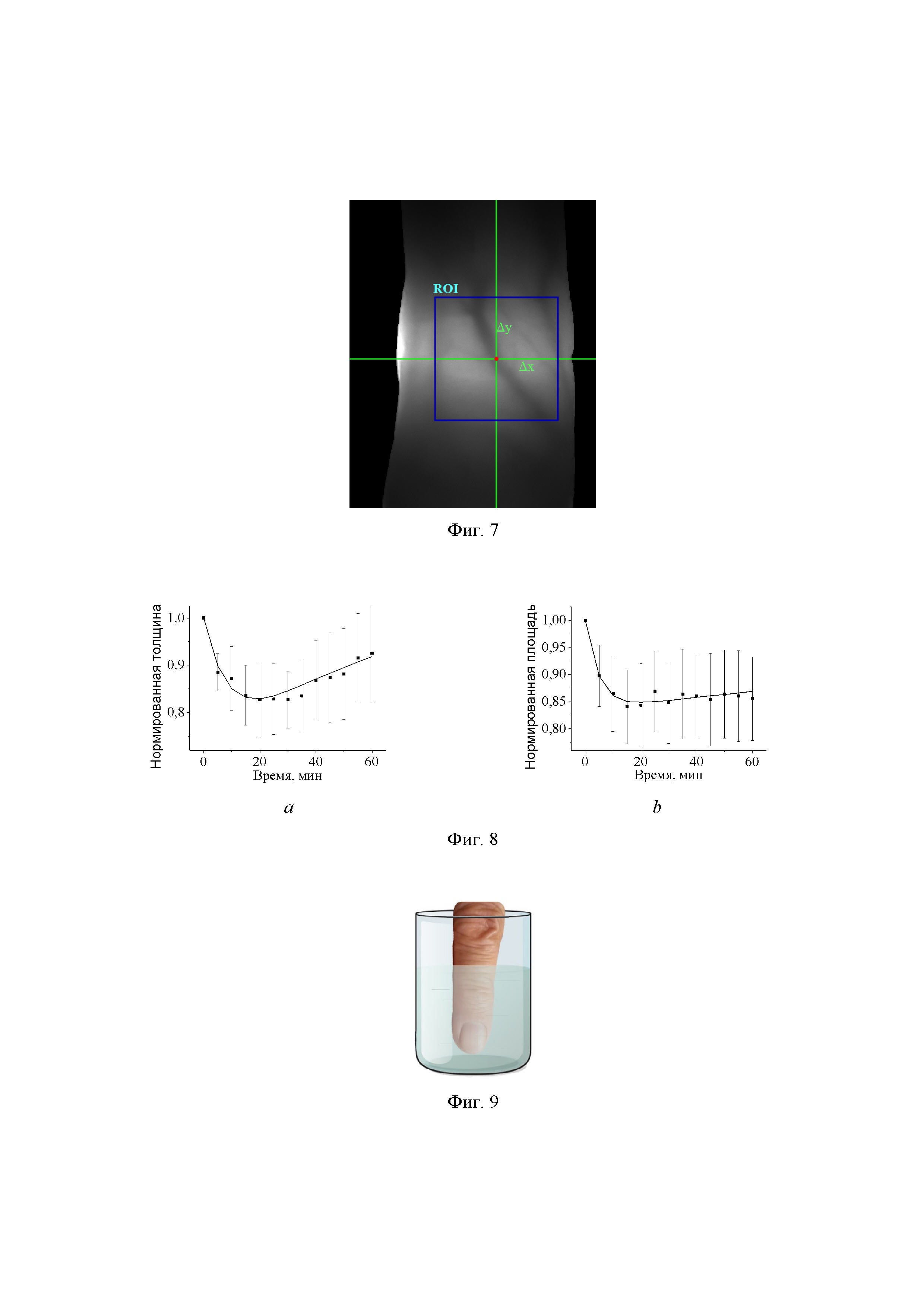
на фиг. 7 – изображение исследуемой области сустава (синий квадрат площадью 220x220 пикселей) для расчета контраста;
на фиг.8–кинетика изменения толщины (а) и площади (б) образцов кожи крыс под действием 40%-раствора глюкозы;
на фиг. 9 – схематическое представление иммерсии пальца просветляющим агентом в режиме полного погружения в агент;
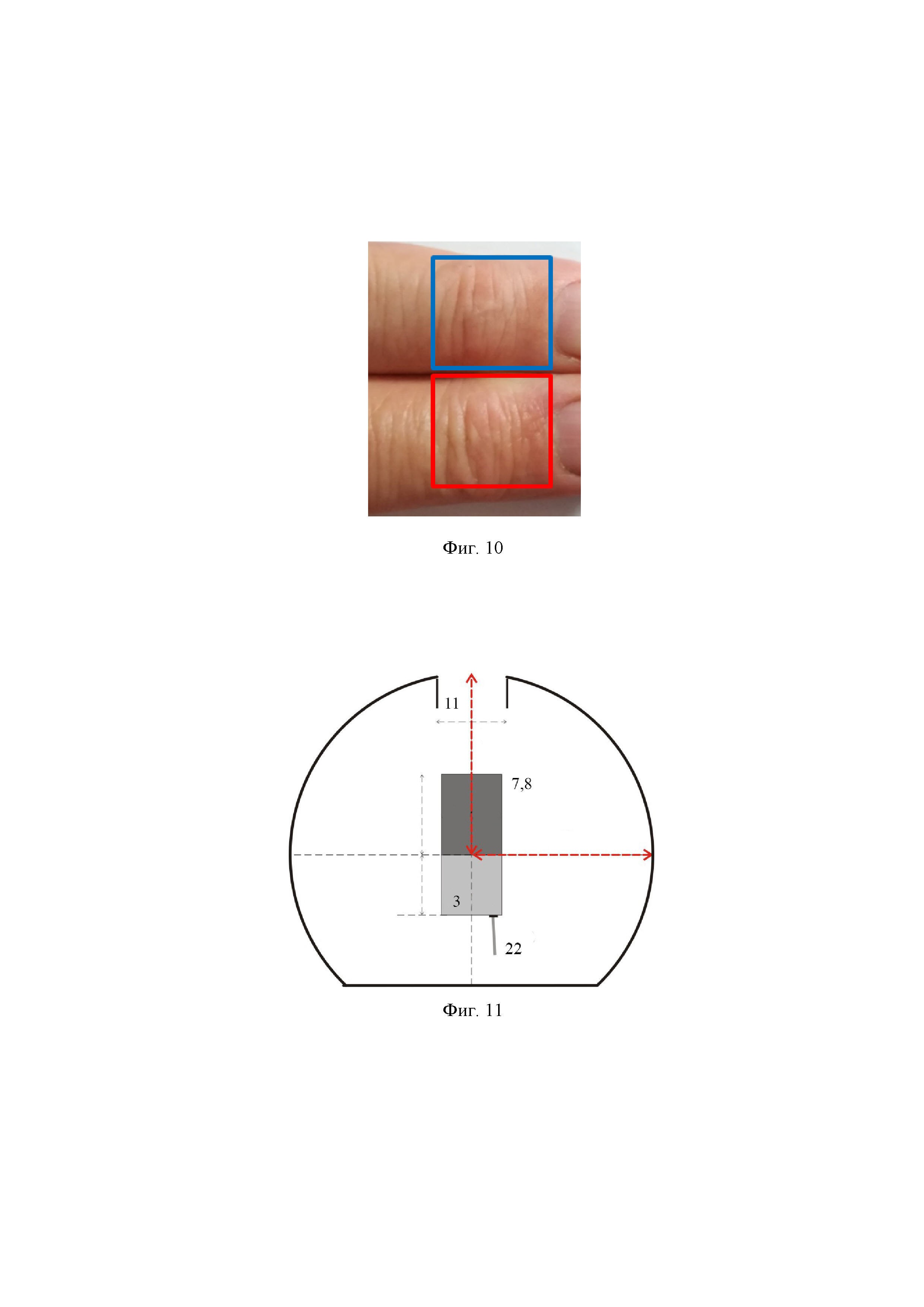
на фиг. 10– изображения, иллюстрирующие изменение натяжения кожи и размера пальца человека при его погружении в 85%-водный раствор глицерина на 20 минут (мужчина, 74 года указательные пальцы левой (сверху, синий квадрат, сразу после действия ОПА) и правой руки (снизу, красный квадрат, контроль). Хорошо видно, что под действием глицерина поверхность кожи стала более гладкой и поперечный размер пальца уменьшился;
на фиг. 11 – расположение цифровой монохромной камеры (вид спереди);
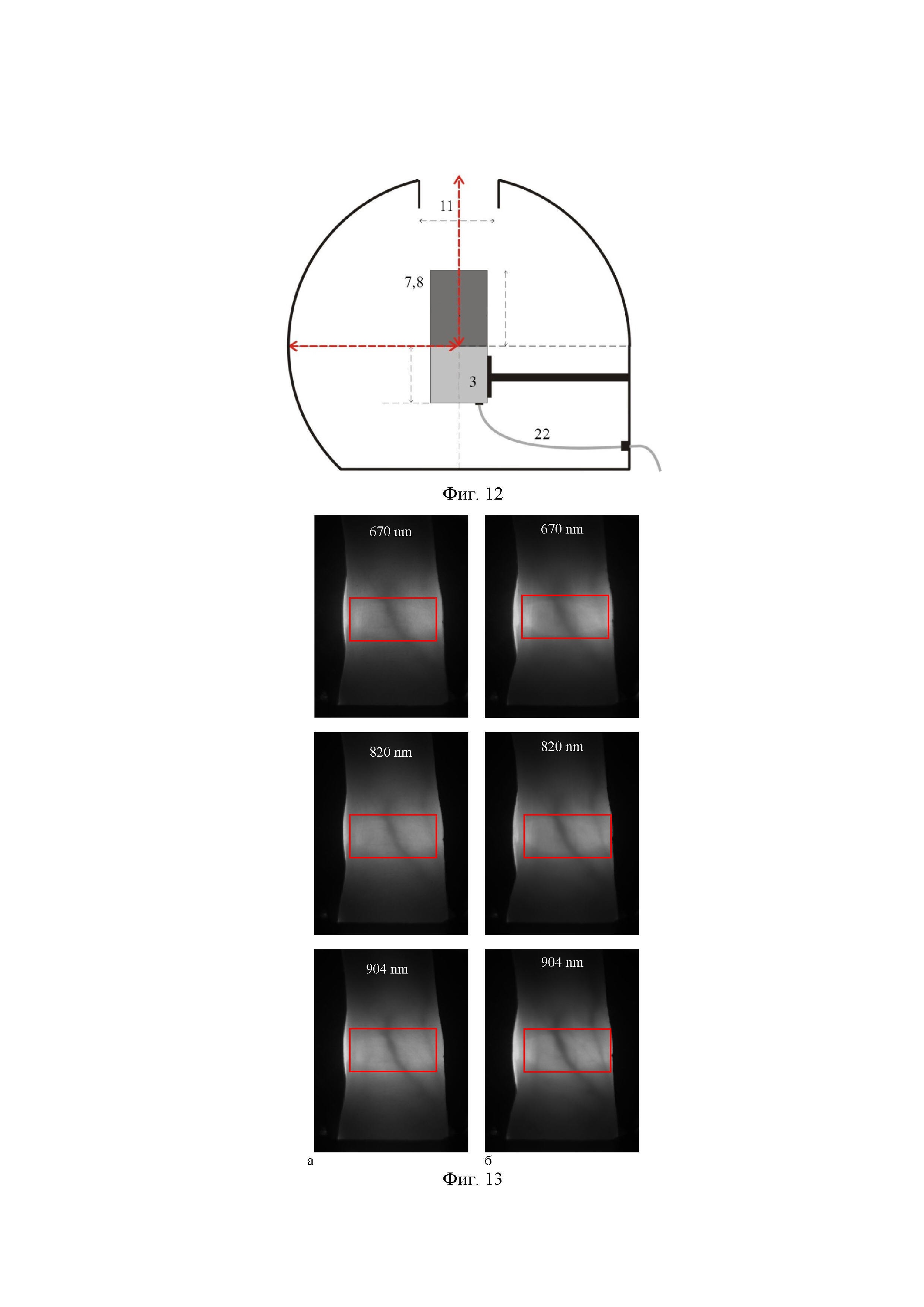
на фиг. 12 – расположение цифровой монохромной камеры (вид сбоку);
на фиг. 13 –изображения пальцевого сустава, полученные под действием иммерсии пальца в глицерине: до применения агента (а), через 60 мин после применения агента (б); изображения получены на трех длинах волн (670 нм, 820 нм и 904 нм).
Позициями на чертежах обозначено:
1 – лазерное излучение;
2 – световод со SMA разъемом;
3 – цифровая монохромная камера;
4 – корпус - опора для кисти руки;
5 –передняя панель программируемого блока управления;
6 – камера-аппликатор для иммерсионного (просветляющего) агента с пальцем внутри и ее крепление;
7 – объектив цифровой камеры;
8 – ИК-корректирующая линза;
9 – плоские стенки камеры-аппликатора;
10 – закругленные стенки камеры-аппликатора;
11 – окно в опоре - корпусе;
12 – отверстие;
13 – направляющие для цифровой монохромной камеры;
14 – сильфон;
15 – столик;
16 – шарнир;
17 – переключатель положения цифровой монохромной камеры;
18 – дополнительное отверстие в опоре – корпусе;
19–программируемый блок управления;
20 – кнопка «включено-выключено»;
21 – палец;
22 – USB-порт.
Сенсор состоит из освещающих источников лазерного излучения 1 (в частности, диодных лазеров с длинами волн 670, 820 и 904 нм), световода 2, монохромной цифровой камеры 3 (в частности, ПЗС/КМОП-камеры), опоры для кисти рук 4, выполненной в виде корпуса симметричной сферической формы. Форма корпуса эргономично адаптирована к форме ладонной поверхности руки, так что регистрация изображений суставов пальцев может быть проведена без нагрузки на руку. Сферическая форма корпуса позволяет захватывать сразу два сустава пальца - проксимальный и дистальный межфаланговые суставы путем перемещения пальца в нужное положение. Излучение от трёх лазерных диодов (на фиг. не показано), встроенных внутрь корпуса, передается через три отдельных волоконных жгута в единый световод 2, который может быть размещен на гибком держателе и установлен со стороны ладони. Один конец световода закреплен на корпусе 4 шарнирным соединением 16 с возможностью поворота на 90° в опоре - корпусе, а другой снабжен разъемом, например,SMA, и установлен напротив плоских стенок 9 камеры-аппликатора 6. Цифровая камера 3 выполнена с возможностью изменения положения по вертикали и горизонтали с помощью переключателя 17, при этом камера-аппликатор 6 расположена на корпусе 4 напротив окна 11 и выполнена с возможностью перемещения. Окно в опоре 11 служит для попадания света, прошедшего через камеру-аппликатор, содержащую иммерсионный (просветляющий) агент, и находящийся в ней палец, на цифровую камеру 3 для регистрации изображения в проходящем свете. Отверстие 12 в конструкции аппликатора определяет ширину пучка света для оптимальной засветки светочувствительной поверхности цифровой монохромной камеры 3.
Цифровая камера 3 связана с линзой 7 с фокальным расстоянием 12 мм посредством крепления, например CS-Mount.
Сенсор содержит программируемый блок управления 19источником лазерного изучения и цифровой монохромной камерой, выполненный с возможностью получения изображения пальца в режиме просвечивания в реальном времени на мониторе компьютера. Сенсор содержит камеру-аппликатор 6, заполненную иммерсионным агентом. Исследуемый палец размещается внутри камеры-аппликатора 6 таким образом, чтобы область сустава захватывалась камерой 3 и лазерное излучение было сфокусировано на верхнюю часть сустава.
Камера установлена на направляющих 13 в корпусе 4, так что положение камеры (вертикальное или горизонтальное) может быть изменено вручную при помощи переключателя 17. Благодаря симметричности сферической конструкции корпуса и центрального позиционирования камеры в корпусе можно обеспечить фиксированную дистанцию камеры от поверхности пальца (фиг. 4, 5).Для обеспечения естественного положения пальца держатель пальца должен быть съемным и крепиться с помощью четырех болтов (фиг. 3). На задней части корпуса размещено дополнительное отверстие 18 для обеспечения возможности вертикального размещения пальца в аппликаторе с просветляющим агентом, который выполнен из прозрачного стекла или пластика. Важно, что такой аппликатор с плоскими стенками обеспечивает иммерсию неоднородной границы кожи пальца, что существенно повышает эффективность ввода излучения в ткань пальца за счет минимизации рассеяния на входе лазерного пучка в кожу и на выходе из кожи.
В случае, когда палец расположен вертикально или лазерный пучок и камера расположены горизонтально, можно подсвечивать палец, находящийся в оптическом иммерсионном агенте (ОПА). Боковое положение держателя световода 2 (волоконного жгута) имеет механическое соединение (шарнир 16), аналогичное тому, что используют в хирургических микроскопах.
Камера-аппликатор для ОПА 6 имеет две плоские и две закругленные стенки (фиг. 3). Плоские стенки расположены со стороны корпуса и лазерного пучка. Аппликатор крепится к стенке корпуса с помощью двух монтажных колец и может быть быстро разобран. Снизу аппликатор устанавливается либо на передвижной столик15 с микрометрическим винтом(фиг. 4), либо на сильфон с фиксатором14 (фиг.5, 6). При помощи управления высотой стола положение аппликатора может быть изменено с точностью до микрометров. Вариант с сильфоном позволяет блокировать аппликатор после установки подходящего положения при помощи фиксатора. Таким образом, можно перемещать исследуемые суставы пальцев для просвечивания на необходимую высоту. Лазерный пучок перемещается путем поворота гибкого держателя световода 2 на 90 град в правильное положение позади аппликатора с помощью шарнира 16, установленного на стороне корпуса 4.
Управление диодными лазерами и монохромной цифровой ПЗС/КМОП-камерой с помощью специального программного обеспечения позволяет получить на мониторе компьютера изображение пальца в режиме просвечивания в реальном времени. «Живая» картинка снабжена перекрестием (фиг. 7) для контроля положения исследуемого сустава по центру, в оптимальном месте облучения, так, чтобы палец облучался симметрично относительно суставной щели. При получении последующих изображений на монитор выводится также и предыдущее сохраненное изображение того же сустава, которое можно наложить на текущую картинку и, изменяя прозрачность предыдущего изображения, совместить положение сустава в реальном времени. Таким образом, позиционирование пальца может быть воспроизведено в боковой плоскости с точностью 1 - 2 мм.
Камера-аппликатор 6 позволяет снабжать просветляющим агентом кожу вокруг исследуемого сустава со всех сторон в течение всего исследования.
Оптический сенсор позволяет проводить мультиспектральный анализ проксимальных и дистальных межфаланговых суставов за короткое время.
Способ осуществляется следующим образом.
В качестве иммерсионного агента используют, в частности, дегидратированный глицерин с концентрацией не ниже 99%, при этом иммерсионный агент заранее подогревают до физиологической температуры поверхности пальца и выше, вплоть до комфортного ощущения тепла, т.е. 33-39°С и наливают в камеру-аппликатор 6.
Располагают кисть руки, суставы пальцев которой необходимо исследовать, на корпусе-опоре 4. Погружают исследуемый сустав в иммерсионный агент на 8-10 минут до достижения эффекта «натяжения» кожи. Спустя 8-10 минут производят просвечивание сустава через плоские стенки 9 камеры-аппликатора 6 путём направления пучка от источника лазерного излучения в течение нескольких секунд, и фиксируют получаемое изображение с помощью цифровой камеры 3. ИК-корректирующая линза 8 цифровой камеры 3 фокусирует падающий свет в точке сбора изображения, что позволяет предотвратить сдвиг фокуса. Лазерное излучение 1 фокусируется на поверхности пальца, диаметр пятна составляет~ 12 мм. При использовании диодных лазеров с фиксированной мощностью время экспозиции зависит от диаметра пальца и состояния ревматоидного артрита.
Просвечивание лазерным излучением осуществляют последовательно на нескольких длинах волн. Для набора статистически достоверных результатов фиксирование изображения на всех длинах волн проводится каждые 1-5 мин в течение 10 минут или более в зависимости от диаметра пальца и состояния ревматоидного артрита.
Пример конкретного применения
Описанный способ применялся для исследования возможности повышения контраста изображения здоровых межфаланговых суставов указательного (толщина 1,6 см) и среднего (толщина 1,8 см) пальцев женщины-добровольца (возраст 25 лет).
В качестве просветляющего агента был взят дегидратированный глицерин. Показатель преломления глицерина был измерен на рефрактометре Аббе (Atago DR-M2 / 1550, Япония) на нескольких длинах волн (450, 589, 680, 1100, и 1550 нм), после чего результаты измерений были интерполированы для определения показателя преломления на длинах волн используемых светодиодов. Так, показатель преломления глицерина составил 1,469 для 670 нм, 1,466 для 820 нм и 1,465 для 904 нм. Агент наносился на исследуемый участок кожи методом погружения в агент, находящийся в кювете (фиг. 9),в течение первых 5 мин и затем дополнительно перед фиксированием изображения, которое проводилось каждые 5 мин в течение 15 минут.
В результате проведенных экспериментов был получен набор изображений, которые представляют собой двумерные карты распределения интенсивности рассеянного света на верхней поверхности пальца (фиг. 13), на основании которых рассчитывался контраст изображений в области максимальной яркости проходящего света (красный прямоугольник на фиг. 13). Хорошо видно, что контраст изображения растет на всех длинах волн при действии глицерина.
Для контроля и определения влияния иммерсионного агента на качество изображений можно применить несколько методов обработки изображений. Обычные методы обработки изображений для оценки эффективности агента основаны на том факте, что обработанная кожа с течением времени станет более прозрачной, при этом улучшится изображение крупных сосудистых сетей и возможность их использования в качестве контроля контраста изображения суставов. Методы, базирующиеся на измерении интенсивности, включают в себя такие алгоритмы, как расчет контраста, стандартного и среднеквадратического отклонения сигнала по полю изображения, а также градиентные фильтры. Все эти методы могут быть объединены под общим названием статистики первого порядка. Статистика первого порядка рассчитывается из вероятности наблюдения особого значения пикселя в случайно выбранном месте на изображении. Все функции, основанные на статистике первого порядка распределений значения серого, инвариантны при любой перестановке пикселей.
Контраст изображения в этом случае будет определяться по формуле
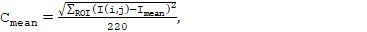 (1)
(1)
где, согласно фиг. 7,
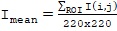
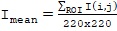 (2)
(2)
рассчитывается для визуализируемой области ROI (область интереса) площадью в 220×220 пикселей, или в общем случае площадью N×M пикселей; I(i, j) соответствует значению интенсивности в каждом пикселе из области ROI.
После повышения прозрачности поверхности кожи структуры, лежащие внутри, становятся более заметными. В основном это можно описать как улучшение четкости изображения. Для количественного описания этого процесса используется статистический подход к оценке резкости изображения с использованием собственных значений (Chong-YawW.; Paramesran, R., "Images harpness measureusing eigen values," in Signal Processing, 9thInternational Conference on Signal Processing (ICSP 2008),pp.840-843, 26-29 Oct. 2008DOI: 10.1109/ICOSP.2008.4697259). Алгоритм включает в себя: нормализацию изображения по энергии, расчета ковариантной матрицы средних отклонений и расчета уровня резкости, который определяется путем взятия следа первых k наибольших собственных чисел вырожденной матрицы из ковариационной матрицы.
Для обоснования достижения заявляемого результата, а именно оценки влияния иммерсионного агента на процесс сжатия кожи пальца, были проведены исследования по изучению кинетических параметров сжатия и набухания образцов кожи крыс под действием 40%-раствора глюкозы. Было показано, что в течение 10-15 мин происходит уменьшение толщины (поперечное сжатие) и уменьшение площади (продольное сжатие). Поперечное набухание образцов кожи наблюдалось после 15-20 мин иммерсии. На фиг. 8 представлена кинетика изменения толщины (а) и площади (б) образцов кожи крыс под действием 40%-раствора глюкозы. Кинетические коэффициенты обезвоживания и сжатия/набухания образцов кожи крыс под действием 40%-раствора глюкозы: максимум дегидратации (A) и степень набухания (B), константы, характеризующие время диффузии воды (τw) и глюкозы (τg), неизменная величина параметра(y0), получены путем аппроксимации экспериментальных результатов с помощью уравнения
|
где W (t) и W(t=0) - значения толщины или площади в момент времени t и t=0, соответственно, представлены в таблице:
Таблица. Кинетические параметры сжатия и набухания образцов кожи крыс под действием 40%-глюкозы
|
± - стандартное отклонение
Полученная кинетика изменения толщины и площади кожи была использована для количественной оценки сжатия кожи пальца человека. Если радиус интактного пальца rint=0.85 см, его окружность Lint=2πr=5.3 см. Площадь боковой поверхности центрального межфалангового сустава указательного пальца человека через 10-15 мин после погружения в 40% - раствор глюкозы уменьшается до S=2πrh=6.72 см2, где высота межфалангового сустава h=1.50 см. В норме окружность пальца немного больше Lint=5.34 см, чем длина окружности подлежащих тканей. Этот избыток легко определить экспериментально путем простого натягивания кожи в области межфалангового сустава и измерения микрометром длины избытка кожи. Типичное экспериментальное значение такого избытка в области проксимального межфалангового сустава ΔL = 1,1-1,2 см. Оценка возможной усадки кожи на основе измерений, представленных на фиг.8, дает уменьшение длины окружности кожи до Losm = 4.2 см, т.е. ΔL = (Lint – Losm) = 1,1 см. Это означает, что используемый иммерсионный раствор (в частности, раствор глюкозы) вполне может обеспечить полную компенсацию избытка кожного покрова вокруг пальца и обеспечить натяжение кожи и соответственно окклюзию. Таким образом, натяжение кожи вокруг пальца, вызванное поперечным и продольным сжатием, приводит к снижению рассеяния и увеличению контраста оптических изображений.
На фиг. 10 представлены результаты invivo демонстрации изменения натяжения кожи и размера пальца человека при его погружении в 85%-водный раствор глицерина на 20 минут. На цифровой фотографии представлены указательные пальцы левой (сверху, синий квадрат, сразу после действия ОПА) и правой руки (снизу, красный квадрат, контроль) мужчины возрастом 74 года. Хорошо видно, что в норме кожа в области межфаланговых суставов имеет сильную неоднородность в виде глубоких бороздок, однако под действием глицерина поверхность кожи становится более гладкой и поперечный размер пальца несколько уменьшается.
Действие оптического просветляющего агента на биоткань приводит к частичной замене внутритканевой жидкости иммерсионным раствором, согласованию показателей преломления рассеивателей и окружающей их среды и, следовательно, снижению рассеяния. Иммерсионный агент также вызывает локальную дегидратацию тканей из-за их осмотических свойств, что также приводит к согласованию показателей преломления компонентов ткани и их упорядочению.
Под действием иммерсионного агента с ярко выраженными гиперосмотическими свойствами распределение вещества происходит в поверхностных слоях эпидермиса. Пропитанные таким образом слои в течение некоторого времени выполняют двоякую роль – роль «окклюзионной пленки» и роль абсорбера воды, которая покидает верхние слои эпидермиса, устремляясь наружу.
Следует отметить, что этот вывод касается только одного из процессов, участвующих в повышении контраста, а именно уменьшения коэффициента рассеяния слоев кожи. Кроме иммерсионного просветления слоев кожи вклад в повышение контраста изображения дают: 1) плоская граница ввода излучения в держатель пальца при полном погружении пальца в иммерсионный агент, а также 2) натяжение кожи и ее поперечное сжатие.
В качестве биологически совместимых иммерсионных агентов могут быть использованы дегидратированный глицерин с концентрацией 99%;водный раствор глицерина 70-99 %; лосьон для рук с 5-30%-ным содержанием мочевины, в состав которого входит глицерин; водно-спиртовые растворы глюкозы, сахарозы, фруктозы, мальтозы с концентрациями 50% при содержании спирта на уровне 30%; водный раствор глюкозы с концентрацией 40-60%, водный раствор фруктозы с концентрацией 40-80%; водный раствор сахарозы с концентрацией 40-70%; водные растворы мальтозы и маннитола с концентрациями 40-50%. Верхние пределы концентраций водных растворов глюкозы, сахарозы и фруктозы соответствуют концентрациям насыщенных растворов данных сахаров.
Кроме того, важное значение имеет использование разнообразных физических и химических усилителей проницаемости кожи, что может существенно повысить скорость просветления ткани и уменьшить время аппликации ОПА. К физическим методам, например, относится ультразвуковое воздействие, нагрев, компрессия, а к химическим биосовместимые растворители липидного защитного слоя рогового слоя, такие как апротонный растворитель диметилсулфоксид (ДМСО), олеиновая кислота, тиазон и многие другие (V.V. Tuchin, OpticalClearingofTissuesandBlood, PM 154, SPIEPress, Bellingham, WA, 2006; Genina E.A., Bashkatov A.N., Sinichkin Yu.P., Yanina I.Yu., Tuchin V.V. Optical clearing of biological tissues: prospects of application in medical diagnostics and phototherapy, Journal of Biomedical Photonics & Engineering 1(1), P. 22-58, 2015; Clara Barba, Cristina Alonso, Meritxell Martí, Albert Manich, Luisa Coderch, Skin barrier modification with organic solvents Biochimica et Biophysica Acta 1858 1935–1943, 2016; Rong Yang, Tuo Wei, Hannah Goldberg, Weiping Wang, Kathleen Cullion, andDanielS. Kohane, GettingDrugsAcrossBiologicalBarriers, Adv. Mater. 29, 1606596, 2017).
Важно отметить, что ДМСО (Димексид) – это противовоспалительное, анальгетическое средство, применяемое в медицине, являющееся сильным антисептиком, обладающее заживляющими, противомикробными свойствами. Оно способно проникать вглубь кожи и эффективно работать в очаге воспаления, поэтому активно применяется для компрессов, в том числе и при лечении ревматоидных артритов (http://sovets.net/8659-kompressy-s-dimeksidom.html).
При лечении артрита можно применять и очень концентрированный ДМСО (http://pozvonochnikpro.ru/bolezni-sustavov/doa-kistey-ruk.html; http://www.listentoyourgut.com/symptoms/29/arthritis.html), вплоть до 50-80% в течение 30-60 минут. ДМСО при таких концентрациях является хорошим просветляющим агентом. Это означает возможность обеспечить диагностику и терапию заболевания одновременно.
Глицерин также широко используется при лечении суставов (https://www.ncbi.nlm.nih.gov/pubmed/29027137; https://www.medicinenet.com/glycerol/supplements-vitamins.htm; https://gocelery.zendesk.com/hc/en-us/community/posts/360006389023).
При лечении артрита применяются также низкомолекулярные и высокомолекулярные производные гиалуроновой кислоты, которые используются в комбинации с глицерином и другими агентами для оптического просветления кожи.
Таким образом,в качестве иммерсионного агента может быть использован состав, содержащий 45% глицерина, 45 % ДМСО и 10 % воды, который не только выполняет свойства иммерсионной жидкости для улучшения качества изображения межфаланговых суставов, но и обладает терапевтическими свойствами.
Заявляемая группа изобретений позволяет получить контрастное оптическое изображение за счёт нового свойства иммерсионного агента, помещённого в камеру-аппликатор, обеспечивающего процесс натяжения кожи в течение определённого времени и иммерсию неоднородной границы и подповерхностных структур кожи пальца, что существенно повышает эффективность ввода излучения в ткань пальца.