Результат интеллектуальной деятельности: КОМПОЗИЦИИ ФИНАФЛОКСАЦИНА В ВИДЕ СУСПЕНЗИИ
Вид РИД
Изобретение
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение в целом относится к композициям в виде суспензии, содержащим фторхинолон. Настоящее изобретение относится, в частности, к композициям в виде суспензии, содержащим финафлоксацин или производное финафлоксацина.
УРОВЕНЬ ТЕХНИКИ
Хинолоновые антибиотики, как известно, имеют требуемые антимикробные свойства широкого спектра. Например, хинолоновые соединения для применения в лечении патологических состояний глаз, ушей и носа раскрыты в патенте США № 6716830, полное содержание которого включено в данное описание посредством ссылки.
Для использования в качестве фармацевтических терапевтических средств, хинолоновые антибиотики должны быть приготовлены в виде стабильных эффективных композиций. В нестабильных композициях при хранении в течение некоторого периода времени твердые частицы могут выпадать в осадок или может происходить разложение активного фармацевтического ингредиента или вспомогательного вещества. Из-за проблемы безопасности и других ограничений такие композиции вряд ли будут одобрены регулирующими органами.
Финафлоксацин является фторхинолоном широкого спектра, который был ранее описан в заявке на патент США с серийным номером 12/829973 для лечения офтальмологических, ушных и назальных инфекций. Максимум антимикробной активности финафлоксацина наблюдается при рН в диапазоне от 5 до 6. Тем не менее в исследованиях стабильности было установлено, что в водных растворах финафлоксацина с этим уровнем рН наблюдается осаждение. Соответственно, необходимы новые составы финафлоксацина с лучшими характеристиками стабильности.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к композициям в виде суспензии, содержащим финафлоксацин или его фармацевтически приемлемую соль, производное, энантиомер или гидрат. Такие композиции финафлоксацина предназначены для лечения микробной инфекции, включая инфекции глаз, ушей и носа.
Как отмечалось выше, финафлоксацин имеет наибольшую антимикробную эффективность при низком уровне рН. Тем не менее композиции финафлоксацина в виде раствора страдают от низкой растворимости и стабильности при оптимальном значении рН, часто приводя к нежелательному образованию осадков. Настоящее изобретение относится к стабильным, эффективным композициям финафлоксацина в виде суспензии. В предпочтительных суспензиях финафлоксацина растворимая фракция финафлоксацина составляет больше, чем 0,05% мас./объем, а соотношение суспендированного и растворимого финафлоксацина находится в диапазоне от 18:1 до 1:1.
Вариант реализации настоящего изобретения представляет собой способ лечения инфицированной ткани, включающий обработку инфицированной ткани композицией для местного применения в виде суспензии, содержащей финафлоксацин. В предпочтительном варианте реализации для лечения инфицированной ткани используется местное применение дозы суспензии один раз в сутки. Составы в виде суспензии по настоящему изобретению особенно полезны в схемах дозирования с низкой частотой, поскольку фракции финафлоксацина с высокой растворимостью могут обеспечить немедленную антимикробную активность, а суспендированная фракция, которая растворяется со временем, обеспечивает пролонгированное действие.
Еще один вариант реализации настоящего изобретения относится к композициям в виде суспензии, содержащим свободное основание финафлоксацина. Особенно предпочтительная композиция в виде суспензии, содержащей свободное основание финафлоксацина, содержит финафлоксацин в форме А свободного основания, которая является стабильной при повышенных температурах, используемых для тепловой стерилизации таких композиций. Для того чтобы увеличить в композиции долю растворимого финафлоксацина, предпочтительные суспензии также содержат солюбилизатор, такой как виды двухвалентных катионов.
Вышеприведенное краткое описание в целом описывает признаки и технические преимущества некоторых вариантов реализации настоящего изобретения. Дополнительные признаки и технические преимущества будут описаны в нижеследующем подробном описании изобретения. Новые признаки, которые, как полагают, являются отличительными признаками настоящего изобретения, будут более понятны из подробного описания изобретения при рассмотрении в связи с любой из прилагаемых фигур. Тем не менее фигуры, приведенные в данном документе, предназначены для помощи в иллюстрации изобретения или для помощи в понимании настоящего изобретения и не предназначены для того, чтобы определить объем изобретения.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Более полное понимание настоящего изобретения и его преимуществ может быть получено со ссылкой на следующее описание, которое следует рассматривать совместно с фигурами на прилагаемых чертежах, на которых одинаковые номера ссылок указывают на подобные признаки, и где:
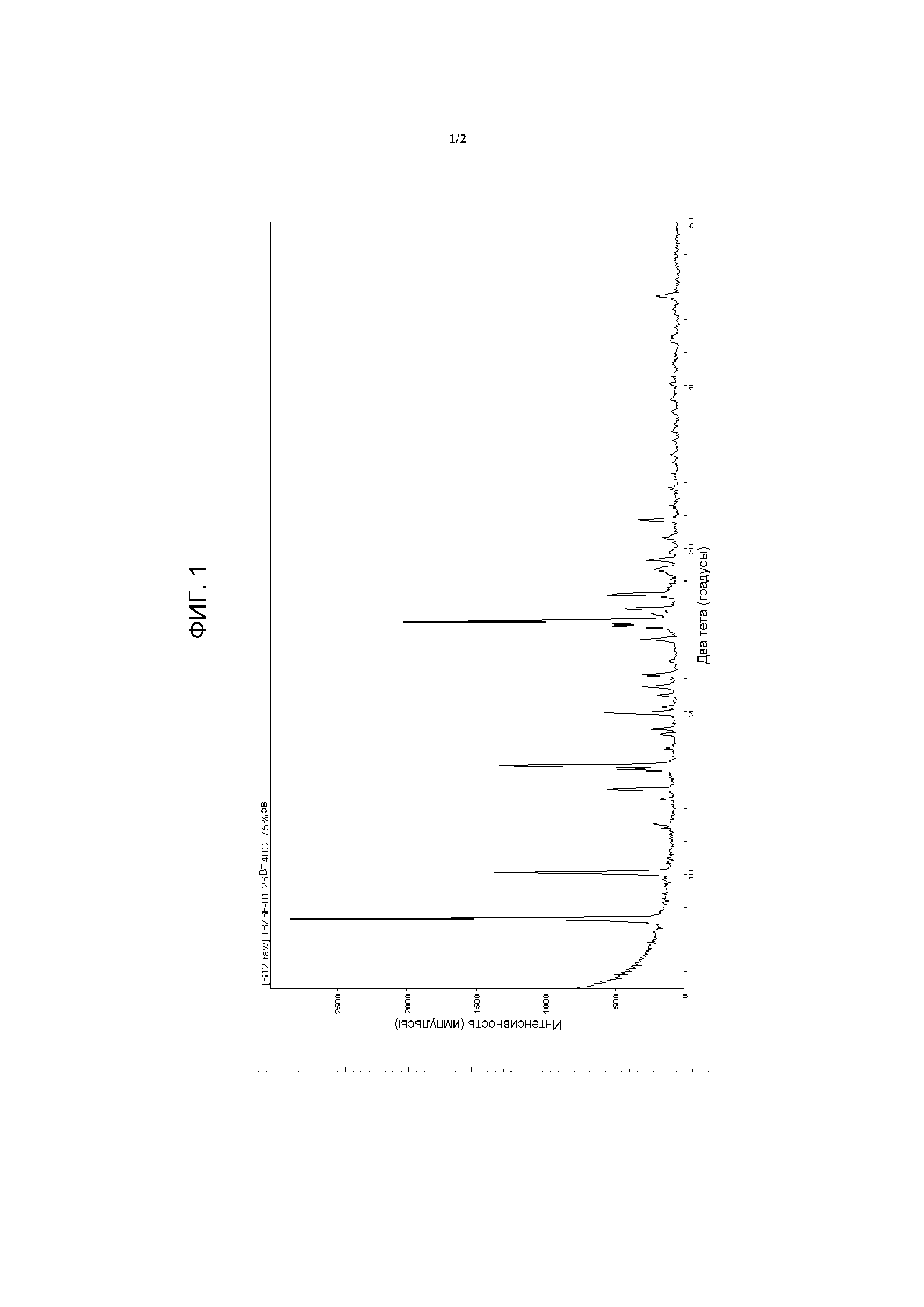
На ФИГУРЕ 1 проиллюстрирована диаграмма рентгеновской дифрактометрии формы А кристаллической формы свободного основания финафлоксацина; и
На ФИГУРЕ 2 проиллюстрирована диаграмма рентгеновской дифрактометрии формы В и формы С свободного основания финафлоксацина.
ПОДРОБНОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Композиции по настоящему изобретению особенно направлены на лечение субъектов-млекопитающих и людей, имеющих микробную инфекцию тканей или подверженных риску ее развития. Микробные инфекции тканей, которые можно лечить или предупреждать в соответствии со способом по настоящему изобретению, упоминаются в публикации J. P. Sanford et al., "The Sanford Guide to Antimicrobial Therapy 2007" 37th Edition (Antimicrobial Therapy, Inc.). Конкретные микробные инфекции тканей, которые можно лечить с помощью вариантов реализации настоящего изобретения, включают инфекции, вызванные бактериями, простейшими, грибами, дрожжами, спорами и паразитами. В частности, настоящее изобретение также относится к противомикробным композициям в виде суспензии и способам лечения инфекций глаз, ушей и носа/носовой пазухи.
Композиции в виде суспензии по настоящему изобретению содержат финафлоксацин или его фармацевтически приемлемую соль, производное, энантиомер или гидрат. Финафлоксацин (8-циано-1-циклопропил-6-фтор-7-[(4aS, 7aS)-гексагидропирроло[3,4-b]-1,4-оксазин-6(2H)-ил]-1,4-дигидро-4-оксо-3-хинолинкарбоновая кислота) имеет следующую структуру:
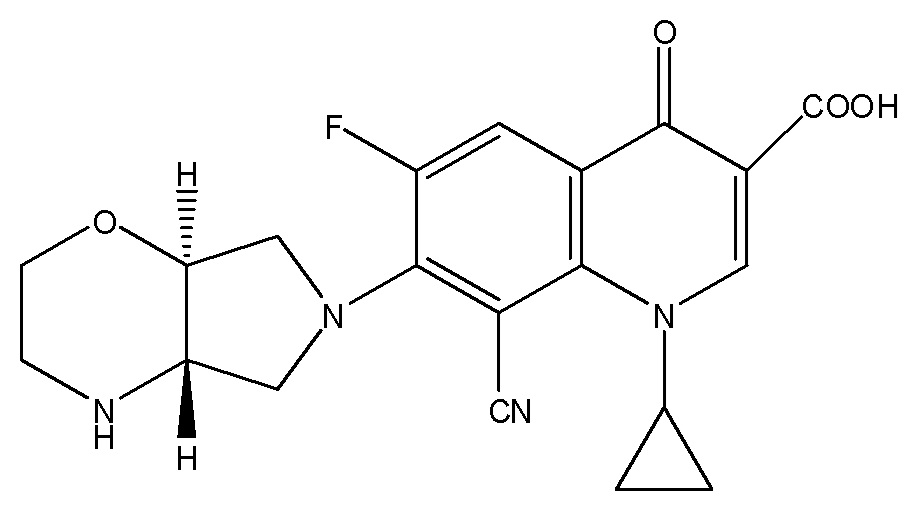
Предпочтительной формой финафлоксацина для использования в вариантах реализации настоящего изобретения является свободное основание финафлоксацина. Были идентифицированы по меньшей мере три полиморфа свободного основания финафлоксацина (формы А, В и С). По существу чистую форму А свободного основания финафлоксацина используют в предпочтительных вариантах реализации, поскольку было обнаружено, что она является наиболее стабильной при высоких температурах, таких как те, которые встречаются в процессе тепловой стерилизации. Кристаллическая форма формы А свободного основания финафлоксацина имеет по существу такой же спектр рентгеновской дифрактометрии, что и спектр рентгеновской порошковой дифрактометрии, показанный на ФИГУРЕ 1. Спектры рентгеновской порошковой дифрактометрии формы B и формы C свободного основания финафлоксацина показаны на ФИГУРЕ 2.
Как используется в настоящем описании, термин "по существу чистый" со ссылкой на конкретную полиморфную форму означает, что эта полиморфная форма содержит менее чем 10%, предпочтительно менее чем 5%, более предпочтительно менее чем 3%, наиболее предпочтительно менее чем 1% по массе любых других физических форм соединения.
Как используется в настоящем описании, термин "по существу такой же" со ссылкой на положения пиков рентгеновской дифрактометрии означает, что учитывается типичное положение пика и изменчивость интенсивности. Например, специалисту в данной области техники будет понятно, что положения пиков (2θ) будут показывать некоторую межаппаратурную вариабельность, как правило, на уровне 0,2°. Кроме того, специалистам в данной области техники будет понятно, что относительные интенсивности пиков покажут межаппаратурную вариабельность, а также вариабельность вследствие степени кристалличности, предпочтительной ориентации, подготовленной поверхности образца и других факторов, известных специалистам в данной области техники, и должны рассматриваться только как качественный показатель.
Диастереомерно и энантиомерно чистый финафлоксацин также предпочтителен для использования в вариантах реализации настоящего изобретения. Как используется в настоящем описании, термин “финафлоксацин” охватывает финафлоксацин и его фармацевтически приемлемые соли, производные, энантиомеры или гидраты. Фраза "фармацевтически приемлемый" является принятой в данной области техники и относится к композициям, полимерам и другим материалам и/или лекарственным формам, которые подходят для применения, включающего контакт с тканями человека или животного, при отсутствии чрезмерной токсичности, раздражения, аллергической реакции или другой проблемы или осложнения, соразмерных с разумным соотношением преимущество/риск, определенным специалистом в данной области техники.
Финафлоксацин и его производные могут быть синтезированы в соответствии со способами, описанными в патенте США № 6133260 авторов Matzke et al., полное содержание которого включено в настоящий документ в качестве ссылки. Форму А свободного основания финафлоксацина получают путем обработки гидрохлорида финафлоксацина гидроксосолью с последующим нагреванием в воде перед сушкой. Форму А финафлоксацина также можно получить в твердом состоянии из формы В свободного основания финафлоксацина при помощи тепловой и/или вакуумной сушки. Кроме того, в процессе составления композиции лекарственного продукта, форму А свободного основания финафлоксацина можно подобным образом получать из формы В свободного основания финафлоксацина путем нагревания в водной фазе.
Композиции в виде суспензии по настоящему изобретению обычно содержат финафлоксацин в концентрации 0,001% масс./об. или более. В предпочтительном варианте реализации композиция по настоящему изобретению содержит финафлоксацин в концентрации от 0,15 до 2,0% масс./об. В более предпочтительном варианте реализации композиция по настоящему изобретению содержит финафлоксацин в концентрации от 0,20 до 1,0% масс./об., а в другом предпочтительном варианте реализации содержит финафлоксацин в концентрации от 0,25 до 0,60% масс./об. Указанные концентрации относятся к общему количеству финафлоксацина по массе в композиции в виде суспензии и включают растворенный финафлоксацин во фракции раствора и частицы финафлоксацина в суспензионной фракции композиции.
Соотношение суспендированного финафлоксацина к растворенному финафлоксацину в композиции в виде суспензии может варьировать, но обычно находится в диапазоне от 18:1 до 1:1. В предпочтительном варианте реализации настоящего изобретения соотношение находится в диапазоне от 8:1 до 1:1. В более предпочтительном варианте реализации соотношение составляет от 4:1 до 2:1.
Концентрация растворимого финафлоксацина в суспензии может изменяться, но, как правило, составляет больше, чем 0,05% масс./об. В предпочтительном варианте реализации настоящего изобретения концентрация растворимого финафлоксацина составляет больше, чем 0,075% масс./об., а в наиболее предпочтительном варианте реализации концентрация растворимого финафлоксацина составляет больше, чем 0,1% масс./об. В конкретных предпочтительных вариантах реализации высокорастворимая фракция содержится в стабильной суспензии, имеющей предпочтительный уровень рН от 5,6 до 6,5, а наиболее предпочтительно уровень рН составляет от 5,8 до 6,2, а концентрация солюбилизатора (например, хлорида магния) составляет от 0,02 до 0,1% масс./об. Суспензии с рН за пределами этого диапазона, часто имеют нежелательные изменения полиморфа или рост частиц, как показано в примере 10 ниже. В предпочтительном варианте реализации настоящего изобретения суспензии финафлоксацина состоят по существу из формы А свободного основания финафлоксацина (например, предпочтительно содержание более 95% формы A; особенно предпочтительно содержание более 99% формы A), и сохраняют эту полиморфную форму при комнатной температуре (15-25°C) в течение периода времени, достаточного для удовлетворения стандартов устойчивости (например, 12 месяцев или больше, в предпочтительных вариантах реализации, от 12 месяцев до 18 месяцев в других вариантах реализации или от 6 месяцев до 18 месяцев еще в других вариантах).
Как правило, желательно максимально увеличить концентрацию растворимого финафлоксацина, поэтому для увеличения количества растворенного финафлоксацина в композиции в виде суспензии могут быть добавлены солюбилизаторы. В то время как могут быть использованы солюбилизаторы, известные в данной области техники, в предпочтительных вариантах реализации настоящего изобретения могут быть использованы двухвалентные катионы, такие как магний и кальций. Концентрация таких двухвалентных катионов может варьировать, но обычно составляет от 0,98 до 4,9 мМ. В предпочтительном варианте реализации настоящего изобретения концентрация двухвалентного катиона находится в диапазоне от 2,0 до 3,9 мМ, а в наиболее предпочтительном варианте реализации настоящего изобретения концентрация двухвалентных катионов составляет от 2,5 до 3,4 мМ. Особенно предпочтительным солюбилизатором является магниевая соль, такая как хлорид магния, ацетат магния и оксид магния. Особенно предпочтительной солью магния является хлорид магния. В то время как концентрация хлорида магния может изменяться, предпочтительной является концентрация от 0,02 до 0,10% масс./об., более предпочтительной является концентрация от 0,04 до 0,08% масс./об., и особенно предпочтительной является концентрация от 0,05 до 0,07.
Композиции в виде суспензий по настоящему изобретению получают с использованием буферной системы, которая поддерживает уровень рН композиции от около 5,6 до 7. Предпочтительные композиции финафлоксацина имеют уровень pH от 5,6 до 6,5, а особенно предпочтительные композиции имеют pH от 5,8 до 6,2.
Для получения однообразного размера частиц финафлоксацина в некоторых вариантах реализации настоящего изобретения также используются средства измельчения. В предпочтительном варианте реализации настоящего изобретения в качестве средства измельчения используют тилоксапол для получения среднего размера объема частиц финафлоксацина менее чем 10 мкм, а в наиболее предпочтительном варианте реализации менее чем 5 мкм.
Для того чтобы поддерживать однородность суспензии, в некоторых вариантах реализации настоящего изобретения могут быть также использованы суспендирующие агенты. Однородность суспензии может быть измерена путем заливки композиции в градуированный цилиндр объемом 50 мл при 25°С и измерения прозрачных и непрозрачных частей композиции с течением времени, по мере оседания композиции. Однородность представляет собой соотношение (выраженное в процентах) непрозрачной композиции в градуированном цилиндре. В предпочтительных вариантах реализации настоящего изобретения такие агенты могут поддерживать по существу однородную суспензию финафлоксацина (т.е. 95% или более непрозрачной суспендированной композиции) в течение периода более чем 4 часа, а в наиболее предпочтительном варианте реализации в течение периода более чем 8 часов. В предпочтительном варианте реализации настоящего изобретения суспендирующий агент представляет собой гидроксиэтилцеллюлозу (ГЭЦ) в концентрации от 0,1 до 0,3% масс./об., а наиболее предпочтительно ГЭЦ в концентрации 0,2 процента.
Суспензии финафлоксацина по настоящему изобретению могут быть повторно диспергированы при помощи встряхивания при 25°С в течение менее чем 30 с в предпочтительном варианте реализации, и в течение менее чем 15 с в наиболее предпочтительном варианте реализации.
Некоторые варианты реализации настоящего изобретения особенно полезны для лечения инфекций тканей глаза. Примеры патологических состояний глаз, которые можно лечить с помощью композиций и способов по настоящему изобретению, включают конъюнктивит, кератит, блефарит, дакриоцистит, ячмень и язвы роговицы. Способы и композиции по настоящему изобретению могут быть также использованы профилактически при различных офтальмологических хирургических процедурах, которые создают риск инфицирования.
Инфекции тканей ушей и носа/синусов также можно лечить посредством вариантов реализации настоящего изобретения. Примеры патологических состояний ушей, которые можно лечить композициями и способами по настоящему изобретению, включают острый наружный отит и средний отит и (там где имеется разрыв барабанной перепонки или были имплантированы тимпаностомические трубки). Примеры патологических состояний носа/синусов, которые можно лечить композициями и способами по настоящему изобретению, включают ринит, синусит, назальное носительство бактерий и ситуации, в которых ткани носа и синусов подвергаются хирургическому вмешательству.
Варианты реализации настоящего изобретения также могут быть использованы профилактически, чтобы предотвратить инфицирование ткани инфекционным агентом. В таких вариантах реализации настоящего изобретения ткань, которая подвергается риску инфицирования, вступает в контакт с композицией по настоящему изобретению.
В конкретных вариантах реализации настоящего изобретения композицию по настоящему изобретению вводят один раз в сутки. Однако композиции по настоящему изобретению также могут быть приготовлены для введения с любой частотой введения, в том числе один раз в неделю, один раз каждые 5 суток, каждые 3 суток, один раз каждые 2 суток, дважды в сутки, три раза в сутки, четыре раз в сутки, пять раз в сутки, шесть раз в сутки, восемь раз в сутки, каждый час, или с любой большей частотой. В зависимости от схемы лечения такую частоту введения дозы также поддерживают на протяжении различной продолжительности времени. Продолжительность конкретной схемы лечения может варьировать от однократного введения до схемы лечения продолжительностью в течение недель. Специалист в данной области техники будет хорошо знаком с определением схемы лечения для конкретного показания к назначению, которая включает фармацевтически эффективное количество финафлоксацина или его композиции. Фраза "фармацевтически эффективное количество" является признанным в данной области техники термином, применимым к любому медицинскому лечению, и относится к количеству агента, которое при введении в фармацевтическую композицию по настоящему изобретению, производит желаемый эффект с разумным соотношением преимущество/риск. Эффективное количество может изменяться в зависимости от таких факторов, как заболевание или инфекционный агент, подлежащие лечению, от конкретной композиции, которую вводят, или тяжести заболевания, или инфекционного агента.
В дополнение к финафлоксацину композиции по настоящему изобретению необязательно содержат одно или более вспомогательных веществ. Вспомогательные вещества, которые обычно используются в фармацевтических композициях, включают, но не ограничиваются веществами, регулирующими тоничность, консервантами, хелатирующими агентами, буферными агентами, поверхностно-активными веществами и антиоксидантами. Другие вспомогательные вещества включают солюбилизирующие агенты, стабилизирующие агенты, агенты, повышающие комфорт, полимеры, смягчающие вещества, агенты, регулирующие уровень рН и/или смазывающие вещества. В композициях по настоящему изобретению может быть использовано любое из множества вспомогательных веществ, в том числе вода, смеси воды и смешиваемых с водой растворителей, таких как С1-С7-алканолы, растительные масла или минеральные масла, содержащие от 0,5 до 5% нетоксичных водорастворимых полимеров, природные продукты, такие как альгинаты, пектины, трагакант, камедь карайи, ксантановая камедь, каррагенин, агар и смола акации, производные крахмала, такие как ацетат крахмала и гидроксипропилкрахмал, а также другие синтетические продукты, такие как поливиниловый спирт, поливинилпирролидон, поливинилметиловый эфир, полиэтиленоксид, предпочтительно поперечно-сшитая полиакриловая кислота и смеси этих продуктов. В предпочтительных вариантах реализации настоящего изобретения концентрация вспомогательного вещества(веществ) обычно составляет от 0,01 до 100-кратной концентрации финафлоксацина, и вспомогательное вещество(-ва) выбирают на основе его(их) инертности по отношению к финафлоксацину.
Подходящие средства, регулирующие тоничность, включают, но не ограничиваются маннитом, хлоридом натрия, глицерином, сорбитом и подобными им. Подходящие буферные агенты включают, но не ограничиваются фосфатами, боратами, ацетатами и подобными им. Подходящие поверхностно-активные вещества включают, но не ограничиваются ионными и неионными поверхностно-активными веществами, хотя предпочтительными являются неионные поверхностно-активные вещества, RLM 100, POE 20 цетилстеариловые эфиры, такие, как Procol® CS20 и полоксамеры, такие как Pluronic® F68. Подходящие антиоксиданты включают, но не ограничиваются сульфитами, аскорбатами, бутилированным гидроксианизолом (БГА) и бутилированным гидрокситолуолом (БГТ).
Композиции, приведенные в настоящем описании, могут содержать один или несколько консервантов. Примеры таких консервантов включают сложный эфир п-гидроксибензойной кислоты, алкилртутные соли тиосалициловой кислоты, такие как тиомерсал, фенилртутный нитрат, фенилртутный ацетат, фенилртутный борат, перборат натрия, хлорит натрия, парабены, такие как метилпарабен или пропилпарабен, спирты, такие как хлорбутанол, бензиловый спирт или фенилэтанол, производные гуанидина, такие как полигексаметиленбигуанид, перборат натрия или сорбиновая кислота. В некоторых вариантах реализации настоящего изобретения композиция может быть самоконсервирующейся, поэтому нет необходимости в консерванте. В предпочтительных вариантах реализации настоящего изобретения композиция в виде суспензии сохраняется в соответствии с критериями Европейской Фармакопеи (ЕФ) с использованием концентрации хлорида бензалкония (БАХ) от 0,004 до 0,012% масс./об., с наиболее предпочтительной концентрацией БАХ 0,005% масс./об.
Для использования при лечении синусовых пазух могут применяться композиции, которые включают вспомогательные вещества, пригодные для образования аэрозоля с помощью небулайзеров или других подобных устройств, хорошо известных специалистам в данной области техники.
Некоторые композиции по настоящему изобретению являются офтальмологически пригодными для глазного применения у субъекта. В предпочтительных аспектах композиции, которые включают финафлоксацин, будут введены в состав для местного применения для глаза в водной суспензии в форме капель. Термин "водный" обычно обозначает водную композицию, в которой вспомогательное вещество составляет >50%, более предпочтительно >75% и, в частности, >90% по массе воды. Эти капли можно вводить из ампулы с однократной дозой, которая может предпочтительно быть стерильной, что отменяет необходимость вводить в композицию бактериостатические компоненты. Кроме того, капли можно вводить из многодозового флакона, который предпочтительно может содержать устройство, извлекающее любой консервант из композиции при применении, такие устройства известны в данной области техники.
В других аспектах компоненты по изобретению могут вводиться в глаз в виде концентрированного геля или аналогичного носителя или в виде растворимых вставок, которые размещают под веками. В других аспектах компоненты по изобретению могут вводиться в глаз в виде мази, эмульсий вода-в-масле и масло-в-воде.
Что касается офтальмологических композиций для местного применения, такие композиции предпочтительно являются изотоническими или слегка гипотоническими в целях борьбы с любой гипертоничностью слез, вызванной испарением и/или заболеванием. В связи с этим может потребоваться введение средства, регулирующего тоничность, чтобы довести осмоляльность композиции до уровня равного или приблизительно равного 210-420 миллиосмолей на килограмм (мОсм/кг). Композиции по настоящему изобретению обычно имеют осмоляльность в диапазоне 220-420 мОсм/кг, и, предпочтительно, имеют осмоляльность в диапазоне 260-330 мОсм/кг.
В определенных вариантах реализации настоящего изобретения финафлоксацин вводят в состав композиции, которая содержит один или более заменителей слез. В данной области техники известно множество разнообразных заменителей слез, которые включают, но не ограничиваются перечисленным: мономерные полиолы, такие как глицерин, пропиленгликоль и этиленгликоль; полимерные полиолы, такие как полиэтиленгликоль; сложные эфиры целлюлозы, такие как гидроксипропилметилцеллюлоза, карбоксиметилцеллюлоза натрия и гидроксипропилцеллюлоза; декстраны, такие как декстран 70; виниловые полимеры, такие как поливиниловый спирт; и карбомеры, такие как карбомер 934Р, карбомер 941, карбомер 940 и карбомер 974Р. Некоторые композиции по настоящему изобретению могут быть использованы с контактными линзами или другими офтальмологическими продуктами.
В некоторых вариантах реализации настоящего изобретения композиции, указанные в данном описании, имеют вязкость 0,5-100 сП, предпочтительно 0,5-50 сП, и наиболее предпочтительно 1-20 сП. Такая относительно низкая вязкость гарантирует, что продукт является удобным, не вызывает помутнение зрения и легко обрабатывается во время операций производства, передачи и наполнения.
В способах, изложенных в данном документе, введение субъекту фармацевтически эффективного количества композиции, которая включает в себя финафлоксацин, может осуществляться любым способом, известным специалистам в данной области техники. Например, композицию можно вводить локально, местно, внутрикожно, в очаг поражения, интраназально, подкожно, перорально, путем ингаляции, путем инъекции, посредством локализованной перфузии с непосредственным омыванием клеток-мишеней, через катетер или с помощью лаважа.
В конкретных вариантах реализации настоящего изобретения композицию применяют местно на глазной поверхности. Что касается офтальмологического введения, предполагается, что могут быть использованы все локальные пути введения, относящиеся к глазу, в том числе местный, субконъюнктивальный, периокулярный, ретробульбарный, в субтеноновое пространство глаза, внутриглазной, субретинальный, задний околосклеральный и супрахориоидальный путь введения.
Композиции по настоящему изобретению могут также содержать противовоспалительный агент. Композиции по настоящему изобретению могут также содержать один или более противовоспалительных агентов. Противовоспалительные агенты, используемые в настоящем изобретении, широко классифицируются как стероидные или нестероидные. Предпочтительные стероидные противовоспалительные агенты представляют собой глюкокортикоиды. Глюкокортикоиды для офтальмологического, ушного или назального применения включают дексаметазон, лотепреднол, римексолон, преднизолон, фторметолон, гидрокортизон, мометазон, флутиказон, беклометазон, флунизолид, триамцинолон и будесонид.
Нестероидные противовоспалительные агенты включают, но не ограничиваются ингибиторами синтетазы простагландина H (ЦОГ-I или ЦОГ-II), также называемыми ингибиторами циклооксигеназы типа I и типа II, такими как диклофенак, флурбипрофен, кеторолак, супрофен, непафенак, амфенак, индометацин, напроксен, ибупрофен, бромфенак, кетопрофен, меклофенамат, пироксикам, сулиндак, мефенамовая кислота, дифлузинал, оксапрозин, толметин, фенопрофен, беноксапрофен, набуметом, этодолак, фенилбутазон, аспирин, оксифенбутазон, NCX-4016, HCT-1026, NCX-284, NCX-456, теноксикам и карпрофен; селективными ингибиторами циклооксигеназы типа II, такими как NS-398, виокс, целекоксиб, P54, этодолак, L-804600 и S-33516; антагонистами PAF, такими как SR-27417, A-137491, ABT-299, апафант, бепафант, минопафант, E-6123, BN-50727, нупафант и модипафант; ингибиторами PDE IV, такими как арифло, торбафиллин, ролипрам, филаминаст, пикламиласт, ципамфиллин, CG-1088, V-11294A, CT-2820, PD-168787, CP-293121, DWP-205297, CP-220629, SH-636, BAY-19-8004 и рофлумиласт; ингибиторами продукции цитокинов, такими как ингибиторы фактора транскрипции NF.каппа.B; или другими противовоспалительными средствами, известными специалисту в данной области техники.
Концентрации противовоспалительных агентов, содержащихся в композициях по настоящему изобретению будут изменяться в зависимости от выбранного агента или агентов и типа воспаления, которое подлежит лечению. Концентрации будут достаточными для уменьшения воспаления в целевых глазных, ушных или носовых тканях после местного применения композиций на эти ткани. Такое количество упоминается в данном описании как "противовоспалительное эффективное количество". Композиции по настоящему изобретению обычно содержат один или более противовоспалительных агентов в количестве от около 0,01 до около 2,0% масс./об., предпочтительно от 0,05 до 1,0% масс./об. и наиболее предпочтительно от 0,05 до 0,2% масс./об. В особенно предпочтительном варианте реализации настоящего изобретения противовоспалительное соединение является дексаметазоном в концентрации 0,1% масс./об.
Также предусмотрены различные техники введения в уши. В отдельных вариантах реализации настоящего изобретения, композиция может быть введена непосредственно в ушной канал (например: местные ушные капли или мази; устройства замедленного высвобождения в ухе или имплантированные рядом с ухом). Местные пути введения включают ушной внутримышечный, в барабанную полость и интракохлеарный пути инъекционного введения композиций. Кроме того, предполагается, что некоторые композиции по изобретению могут быть введены в состав внутриушных вставок или имплантируемых устройств. Например, введение композиций может осуществляться посредством инъекции в барабанную полость, которую осуществляют под эндоскопическим контролем (в том числе под контролем лазерной эндоскопии, чтобы сделать разрез в барабанной перепонке), как описано, например, в публикации Tsue et al., Amer. J. Otolaryngology, Vol. 16(3):158-164, 1995; Silverstein et al., Ear Nose Throat, Vol. 76:674-678, 1997; Silverstein et al., Otolaryngol Head Neck Surg, 120:649-655, 1999. Местное введение может быть также достигнуто путем введения через барабанную перепонку с помощью тонкой иглы (с регистрацией ЭМГ) посредством использования постоянного катетера, помещенного в рассечение барабанной перепонки (миринготомия), и инъекции или инфузии через евстахиеву трубу с помощью небольшого трубочного катетера. Кроме того, композиции могут вводиться с должной осторожностью и вниманием квалифицированным врачом во внутреннее ухо путем размещения Gelfoam или подобного абсорбента и клейкого продукта, смоченного композиций, напротив окна перепонки среднего/внутреннего уха или смежной структуры. Различные другие устройства могут быть использованы для доставки композиции в пораженный отдел уха; например, с помощью катетера или так, как проиллюстрировано в патенте США № 5476446, который предлагает многофункциональный аппарат, специально разработанный для использования в лечении и/или диагностике внутреннего уха субъекта-человека. Также см. патент США № 6653279 в отношении других устройств для этой цели.
Композиции по настоящему изобретению могут быть получены обычными способами приготовления водной фармацевтической суспензионной композиции, включая размерную обработку лекарственного препарата с использованием известных методик размерной обработки, например, измельчение в шаровой мельнице. Например, суспензию, содержащую финафлоксацин, средство измельчения, такое как тилоксопол и размалывающие шарики обрабатывают во вращающемся барабане в течение времени, достаточного для получения лекарственного средства с желаемыми размерами частиц. Размалывающие шарики затем отделяют от суспензии, и суспензию добавляют к оставшимся водным ингредиентам. Предпочтительно, однако, чтобы композиции по настоящему изобретению были получены определенным образом. В соответствии с предпочтительным способом, финафлоксацин сначала добавляют к смеси 1% тилоксопола в очищенной воде с гранулами. Смесь нагревают в автоклаве для стерилизации смеси (а также для того, чтобы обеспечить превращение финафлоксацина в полиморфную форму А). Суспензию измельчают в асептических условиях, чтобы произвести частицы финафлоксацина предпочтительно со средним объемом менее чем 10 мкм. После удаления размалывающих шариков, суспензию финафлоксацина смешивают с остатком компонентов суспензии и корректируют уровень рН.
Введение композиций, описанных в настоящем документе, для лечения инфекции носа может осуществляться с помощью ряда способов, известных специалистам в данной области техники. Например, такие композиции могут быть введены в форме капель или с помощью образования аэрозолей.
ПРИМЕРЫ
Примеры 1-7 ниже были приготовлены в соответствии с вариантами реализации настоящего изобретения.
|
|
|
|
|
|
|
ПРИМЕР 8 - Исследования антимикробной эффективности in Vitro
Композицию раствора финафлоксацина при рН 5,8 и 7,3 сравнивали с композициями ципрофлоксацина и офлоксацина с использованием стандартных тестов антимикробной чувствительности in vitro (M07-08 Methods for Dilution Antimicrobial Susceptibility Tests for Bacteria that Grow Aerobically; утвержденный стандарт - восьмое издание (январь 2009, Институт клинических и лабораторных стандартов), включен в данное описание в качестве ссылки). Минимальные ингибирующие концентрации (MIC50) были определены с использованием микроорганизмов, которые обычно встречаются при инфекциях ушей и глаз. MIC50 представляла собой наименьшую концентрацию антибиотика, которая предотвращала рост тестируемого организма, что было определено визуально по отсутствию мутности.
Результаты эксперимента представлены ниже в таблицах 1-5. При кислом рН, как правило, финафлоксацин имел большую активность в отношении грамположительных и грамотрицательных микроорганизмов, чем фторхинолоны ципрофлоксацин и офлоксацин, оба из которых используются для лечения ушных инфекций. Более высокая активность в кислой среде имеет важное значение для композиций, применяемых для лечения ушей, поскольку композиция с низким уровнем рН является предпочтительной для замедления роста бактерий и грибов, а также потому, что рН среды наружного слухового прохода составляет ~pH 6.
|
|
|
|
|
ПРИМЕР 9 - In vivo модель острого наружного отита (ОНО)
Тестируемые композиции финафлоксацина (от 0,045 до 0,3% общего финафлоксацина) оценивали в модели острого наружного отита (ОНО) у морской свинки с использованием Pseudomonas aeruginosa. Провели легкую экскориацию ушей морской свинки, и в каждое ухо закапали по 200 мкл бактериальной культуры (108КОЕ) P. aeruginosa. Уши подвергали лаважу солевым раствором, который высевали на среды для выделения Pseudomonas. В таблице 6 обобщены результаты этих исследований. Как правило, для достижения стерилизации всех ушей требовалась растворимая фракция 0,05% масс./об. финафлоксацина. В композициях 9, 17 и 18 растворимая фракция содержалась в концентрации более 0,05% масс./об., но общая концентрация финафлоксацина была ниже (0,075, 0,075 и 0,1% масс./об., соответственно).
|
|
ПРИМЕР 10 - Исследования стабильности
Поисковые исследования стабильности проводились с характеристиками физической и химической стабильности композиций по настоящему изобретению. Исследуемые композиции перечислены в таблице 7 ниже.
|
Было определено, что композиция 1, с рН 5,5, не отвечала требованиям стабильности в связи с образованием игольчатых частиц соли гидрохлорида финафлоксацина через 2 недели. Однако, композиции 2 и 3 с pH 6,0 и 6,2, соответственно, в ходе исследования не продемонстрировали образование частиц гидрохлорида финафлоксацина. Были протестированы другие композиции по настоящему изобретению (например, Пример 1 выше), которые не продемонстрировали образование частиц гидрохлорида финафлоксацина, обнаруживаемое при более низком уровне рН.
Настоящее изобретение и его варианты реализации были описаны подробно. Однако объем настоящего изобретения не ограничивается конкретными вариантами реализации любого процесса, производства, составом веществ, соединениями, средствами, способами и/или стадиями, описанными в настоящем описании. Различные модификации, замены и вариации могут быть сделаны в раскрытом материале без отхода от сущности и/или существенных характеристик настоящего изобретения. Соответственно, специалист в данной области техники легко поймет из настоящего раскрытия, что более поздние модификации, замены и/или варианты реализации, осуществляющие по существу, ту же самую функцию, или достижение, по существу, того же результата, что и варианты реализации настоящего изобретения, описанные в данном документе, могут быть использованы в соответствии с такими связанными вариантами реализации настоящего изобретения. Таким образом, нижеследующая формула изобретения охватывает в пределах объема формулы изобретения модификации, замены и вариации способов, производства, композиций вещества, соединений, средств, методов и/или стадий, описанных в данном документе.