Результат интеллектуальной деятельности: Способ очистки хондроитин сульфата
Вид РИД
Изобретение
Настоящее изобретение относится к промышленному способу очистки полученного из хрящей животных хондроитин сульфата (ХС), который предоставляет собой продукт, полностью соответствующий технологическим требованиям для использования указанного соединения в фармацевтической области. В частности, разработанный способ обеспечивает устранение кератана, гликозаминогликана, который, как показано с помощью современных технологий анализа, присутствует во всех препаратах ХС, полученных путем различных способов экстракции из различных типов животных источников.
Определения
Гликозаминогликаны (ГАГ) означают сложное семейство полисахаридов, которые являются основными составляющими внеклеточного матрикса соединительной ткани.
Термин [4)-β-D-GlcA-(1→3)-β-D-GalNAc-(1→] означает дисахарид, образованный D-глюкороновой кислотой (D-GlcA) и N-ацетил-D-галактозамином (D-GalNAc), связанных β-гликозидной связью (1-3).
Термин [4)-α-L-IduA-(1→3)-β-D-GalNAc-(1→] означает дисахарид, образованный L-идуроновой кислотой (L-IduA) и N-ацетил-D-галактозамином (D-GalNAc), связанных β-гликозидной связью (1-3).
Термин хондроитин сульфат (ХС) означает различным образом сульфатированные гликозаминогликаны различной молекулярной массы, которые присутствуют в различных животных тканях. Сахаридная главная цепь ХС состоит из дисахаридных звеньев [4)-β-D-GlcA-(1→3)-β-D-GalNAc-(1→], одно за другим связанными β-гликозидными связями (1→4). Сокращение ХС относится как к кислой форме, так и к образованной солью форме указанных полисахаридов.
Сокращение ХС-типА означает ХС, отличающийся преобладанием звеньев дисахарида типа ХС-А, [4)-β-D-GlcA-(1→3)-β-D-GalNAc4SO3--(1→].
Термин хондроитин/дерматан сульфат, сокращенно ХС/ДС, так же известный как ХС-типВ (не надо смешивать со структурным вариантом дисахарида СХ-В) означает различным образом сульфатированные гликозаминогликаны различной молекулярной массы, которые присутствуют в различных животных тканях, в которых сахаридная главная цепь состоит из различного количества дисахаридных звеньев [4)-β-D-GlcA-(1→3)-β-D-GalNAc-(1→] и [4-α-L-IduA-(1→3)-β-D-GalNAc-(1→], связанных β-(1→4) гликозидными связями. Сокращение ХС или ХС-типВ относится как к кислой форме, так и к образованной солью форме указанных полисахаридов.
Сокращение ХС-типС означает ХС, отличающийся преобладанием звеньев дисахарида типа ХС-С, [4)-β-D-GlcA-(1→3)-β-D-GalNAc6SO3--(1→].
Термин кератан сульфат (КС) означает различным образом сульфатированные гликозаминогликаны различной молекулярной массы, которые присутствуют в различных тканях животных и рыб. Сахаридная главная цепь КС состоит из дисахаридных звеньев [3)-β-D-Gal-(1→4)-β-D-GlcNAc-(1→]. Сокращение КС относится как к кислой форме, так и к образованной солью форме этих полисахаридов.
Сокращение ХС/КС означает загрязненные КС продукты ХС, продающиеся в настоящее время на рынке.
Уровень техники
Хондроитин сульфат (ХС) является гликозаминогликаном, состоящим из повторяющихся дисахаридных звеньев [4)-β-D-GlcA-(1→3)-β-D-GalNAc-(1→], связанных друг с другом β-гликозидными связями (1→4). Когда некоторые звенья -β-D-GlcA замещены на полисахаридной цепи -α-L-IduA-, используют термин ХС-типВ (не смешивать со структурным вариантом дисахарида ХС-В), также называемый дерматан сульфатом (сокращенно ХС/ДС).
В зависимости от центров сульфатирования, существуют различные типы структурных дисахаридов хондроитинов/дерматанов.
In vivo различные типы ХС в течение полимеризации сульфатируются конкретными сульфотрансферазами и затем, ковалентно связанные с конкретными белками, выделяются во внеклеточный матрикс в виде протеогликанов. Они являются универсальными составляющими различных соединительных тканей, таких как хрящи, кожа, кровеносные сосуды и кости (Abu K. & Seno N., The Basic of Carbohydrate Chemistry, 1993, 142-177, Japan: Kodansha).
ХС в изобилии распределяется в живых организмах, в которых он играет центральную роль в биологических процессах. В частности, ХС действует как регулятор факторов роста, цитокинов, хемокинов, адгезивных молекул и липопротеинов посредством взаимодействий с лигандами указанных белков посредством специальных сахаридных областей (Malavaki С., et al., Connect Tissue Res., 2008, 49, 133-139).
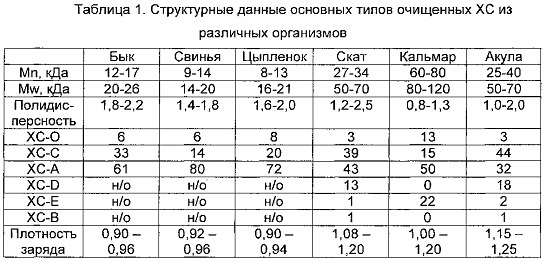
В таблице 1 показаны структурные параметры основных типов ХС, очищенных различными организмами. В частности, параметры молекулярной массы достаточно похожи для ХС из животных источников (бык, свинья, цыплята), однако сильно отличаются от ХС морского происхождения (акула, скат, кальмар), причем последний имеет большую молекулярную массу, чем первый. Образцы ХС морского происхождения также имеют плотность заряда более 1 из-за присутствия дисульфатированных дисахаридов, в то время как образцы ХС животного происхождения (бычьи, свиные, из цыплят) имеют плотность заряда менее 1.
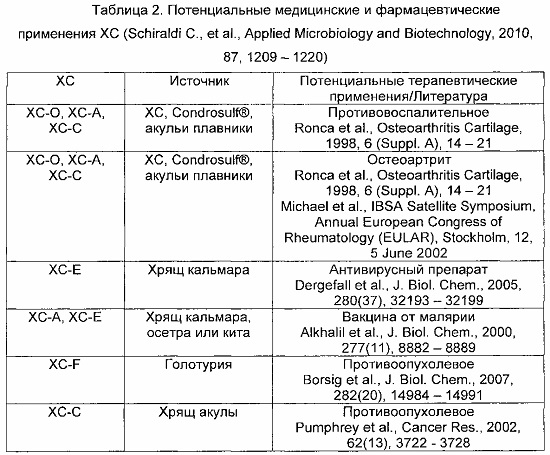
Принимая во внимание эти разнообразные функции, ХС использовали в фармацевтических, нутрицевтических и косметических продуктах (Коgа Т., New Food Industry, 1989, 31, 4-7; Park D.С. & Kim S.В., Fisheries Research, 1998, 12, 30-39; Cho S.Y., et al., Food Hydrocolloids, 2004, 18, 573-579; Cho S.Y., et al., Biological & Pharmaceutical Bulletin, 2004, 27, 47-51; Takuo N., et al., Recent Patents on Food, Nutrition & Agriculture, 2010, 2, 61-74).
ХС в настоящее время является активным ингредиентом множества противоартритных лекарств. ХС вносит значительный вклад в определение биомеханических свойств хряща, так как он смазывает суставы и обеспечивает механическую стойкость к сдавливающим напряжениям.
В последнее время было описано множество потенциальных фармацевтических применений ХС, частично зависящих от типа сульфатирования (Hiraoka et al., Glycobiology, 2001, 11(6), 495-594; Malavaki С., et al., Connect Tissue Res., 2008, 49, 133-139, Lauder R.M., Complement Ther. Med., 2009, 17, 56-62).
Недавние исследования показали, что ХС играет важную роль в развитии размеров опухоли и образовании метастазов. В опухолевых клетках, в частности, были обнаружены изменения длины цепи и положений сульфатирования молекулы ХС (Smetsers et al., J. Invest. Dermatol., 2004, 122(3), 701-716). Это позволяет использовать ХС в качестве биомаркера для ранней диагностики опухолей яичников (Pothacharoen et al., J. Cell Sci., 2006, 113, 193-205).
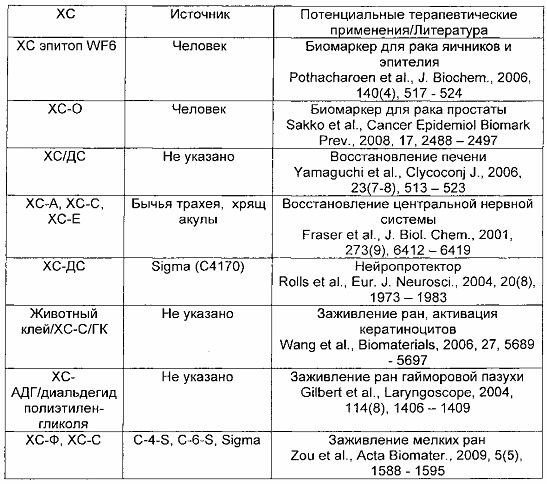
Эти характеристики на многие годы сделали ХС важными фармакологическими средствами, увеличивая интерес к их получению, которое в настоящее время основано на технологиях, включающих извлечение из различных тканей животных. В частности, ХС извлекают из хряща акулы, бычьей трахеи и некоторых побочных продуктов забоя свиней. Из-за требуемой высокой степени очистки этот способ является очень сложным и затратным, включая использование ферментов, антибиотиков и значительных объемов органических растворителей. Обработка также страдает от значительных эксплуатационных затруднений, связанных с неприятным запахом при обработке и получением сильно загрязняющих сточных вод, более того, использование тканей животных в качестве сырьевого материала в способе извлечения может привести к передаче вирусных и прионовых инфекций между видами (Schiraldi et al., 2010).
Получение ХС из хрящевых материалов животного происхождения подробно описывают в научной и патентной литературе. Все способы обычно включают следующие стадии: гомогенизация хряща, химическое разложение (щелочной гидролиз) и/или ферментативное разложение (трипсин, папаин, Alcalase и Neutrase, изготовленные Novozyme) протеогликанового матрикса для отделения белкового компонента от углеводного компонента, фильтрация для удаления нерастворимых остатков, множество способов осаждения с помощью растворителей, обычно этанола, для очистки/извлечения представляющих интерес полисахаридов, хроматографическое разделение с помощью ионообменных смол, обесцвечивание с помощью активированного угля, сушка и измельчение высушенного продукта, упаковка.
Использование ХС в качестве медикамента и нутрицевтика связано с конкретными критериями чистоты для сырьевого материала, определенных относительно похожими способами регулирующими органами различных стран. В настоящее время, согласно Фармакопеям США и ЕС, стандартным испытанием для определения содержания ХС является способ фотометрического титрования, проводимый с бромидом гексадецилтриметиламмония в качестве титрирующего раствора. Способ титрования показывает линейную зависимость между 0,5 и 7,5 мг стандарта ХС (Sigma), однако было показано, что в присутствии других ГАГ или нуклеиновых кислот существуют кривые титрования с завышенными точками эквивалентности (http://siqa.ufjf.br/Reeport Laboratorio de Analise de Glicoconjugados - UFJF). Эти результаты указывают, что способ титрования имеет низкую специфичность, потому что он может завышать количественную оценку ХС в присутствии других анионных соединений. Другие способы, указанные Фармакопеям США и ЕС, включают инфракрасную спектроскопию, определение удельного вращения плоскости поляризации и электрофорез на ацетате целлюлозы, причем все эти способы, как указано ниже, сейчас показывают их значительные ограничения при определении степени чистоты препаратов на основе ГАГ.
В последние несколько лет большой научный интерес к ГАГ и их возможным применениям, развитию новых и более усложненных подходов к определению характеристик этих полисахаридов и развитию новых стратегий для разделения различных типов ГАГ (Pomin V.Н. et al., Carbohydrate Polymers, 2012, 90, 839-846) продемонстрировал, что способы анализа, первоначально использованные регулирующими органами для определения чистоты промышленных препаратов ХС, предназначенных для фармацевтического и нутрицевтического применения, являются ненадлежащими, и что даже эталонные образцы, предложенные Фармакопеями США и ЕС, не являются чистыми, и значительно загрязнены кератан сульфатом (КС), смесью различным образом сульфатированных гликозаминогликанов с различными молекулярными массами, структура которых основана на дисахаридных звеньях [3)-β-D-Gal-(1→4)-(3-D-GlcNAc-(1→], связанных друг с другом 6-гликозидными связями (1→3).
Pomin V.Н. et al. (Carbohydrate Polymers, 2012, 90, 839-846) проанализировали 17 промышленных порций ХС для орального применения, 3 из которых были получены из бычьего хряща и 14 из хряща рыб, и стандартные образцы, указанные в качестве сравнительных продуктов Фармакопеями США и ЕС. Методологии анализа, принятые этими авторами, представляли собой электрофорез агарозного геля, ВЭЖХ на сильных анионообменных смолах (САО) и гельфильтрационных смолах (эксклюзионная хроматография, ЭксХ), перевариваемость с конкретными ГАГ лиазами, установленные уровни уроновой кислоты, одномерный и двумерный ЯМР. В частности, авторы (таблица 3) обнаружили, что в среднем КС представляет примерно 16% от всех ГАГ, обнаруженных в составах, полученных из хряща акулы, и получили похожие сведения со стандартом Фармакопеи ЕС, также полученным из хряща акулы.
Как показано в таблице 3, большое количество КС присутствует в ХС морского происхождения, что приводит к значительному уменьшению содержания ХС по сравнению с указанным количеством и означает, что данный продукт является несовместимым с применением, особенно в качестве медикамента, который требует высоких степеней чистоты (Volpi N., J. Pharm. Sci., 2007, 96, 3168-3180).
Pomin et al. показали, что разработанный ими электрофорез агарозного геля, аналогично электрофорезу ацетата целлюлозы, рекомендованному Фармакопеями США и ЕС, не способен показать загрязнение КС, потому что этот ГАГ совместно мигрирует с ХС. Более того, эксклюзионная высокоэффективная жидкостная хроматография, Экс-ВЭЖХ, неспособна показать присутствие КС в составах ХС, в то время как сильно анионообменная высокоэффективная жидкостная хроматография, САО-ВЭЖХ, оказалась наиболее соответствующим способом для определения загрязнений КС, так как ХС и КС имеют достаточно различные времена элюирования, но не настолько различные, чтобы препятствовать частичному перекрыванию пиков, что может вызвать неправильные количественные оценки загрязнения. Достаточно диагностическим, но не количественным, способом определения присутствия КС в составах ХС является одномерный 1Н-ЯМР, как указано с помощью изолированных групп с хорошим разрешением сигналов при 4,68 и 4,37-4,30 частей на млн., характерных для КС (Limtiaco J. et al., 2012, Analytical Methods, 4, 1168-1172, Pomin V.H. et al., 2010, Analytical Chemistry, 82, 4078-4088, Rudd T.R. et al., 2011, The Analyst, 136, 1390-1398, Zhang T. et al., 2009, J. Pharmaceutical Science, 98, 4017-4026).
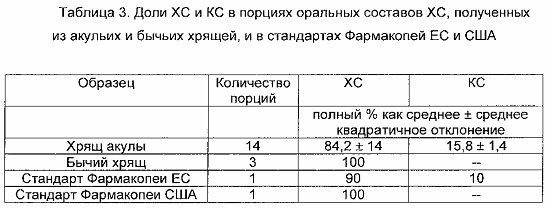
Доли были получены из интегралов профилей ВЭЖХ-САО (Pomin V.Н. et al., Carbohydrate Polymers, 2012, 90, 839-846).
На основе обнаруженных данных по загрязнению КС Pomin et al. указывают на необходимость пересмотра методологий, указанных Фармакопеями США и ЕС, для обеспечения более правильного определения количества биологически активного ингредиента, присутствующего в промышленных составах ХС.
Разработка новых способов анализа, способных определять загрязнение КС, очевидно требует существенного обзора способов получения ХС для уменьшения уровней загрязнения КС до пределов, совместимых с применением ХС в качестве медикамента и нутрицевтика.
Galeotti F. et al. (Analytical Biochem., 2013, YABIO 11579 26.12.13) определяют условия селективного осаждения ХС и КС из промышленных препаратов ХС/КС, полученных из хряща акулы, путем постепенного добавления этанола, насыщенного ацетатом натрия, в раствор, содержащий 33 мг/мл ХС/КС. Осаждение только хондроитина завершается с 1 объемом этанола. В том же исследовании авторы утверждают, что осаждение метанолом, пропанолом или ацетоном не обеспечивает селективного удаления КС. Ранее та же группа (Volpi N., J. Chromatography В, 1996, 685, 27-34) при описании осаждения 110 мг/мл смесей гликозаминогликанов с этанолом в присутствии 2% NaCl указывала, что полное осаждение ХС получают только при 1,2-1,6 объемов.
Все современные способы промышленного получения ХС основаны на критериях чистоты продукта, несоответствующих демонстрированию загрязнения КС. В ближайшее время, как только регулирующие органы, которые уже в курсе рассматриваемого вопроса, принявшие стандарты и способы определения характеристик, учтут новые возможности анализа, это сделает все продукты ХС, продаваемые сейчас на рынке, неподходящими для фармацевтического применения и подлежащими сильному титрованию для применения при получении нутрицевтиков и косметических средств.
Таким образом, несмотря на большое количество способов экстракции/очистки, разработанных до сих пор, в настоящее время проводят промышленное исследование новых способов, в которых получают ХС, особенно в отношении фармацевтического сорта, которые отвечают новым стандартам чистоты, в соответствии с которыми регулирующие органы устанавливают технические требования для ХС, особенно в связи с загрязнением КС, которые еще не включены в способы анализа современными Фармакопеями.
В этом контексте существующая в настоящее время разработка простого способа очистки, применимого в различных продуктах ХС, загрязненных КС (ХС/КС), представляется важной и актуальной промышленной целью.
Описание изобретения
Разработка более надлежащих методологий исследования показывает, что масштаб проблемы загрязнения КС препаратов ХС, продающихся в настоящее время на рынке, является даже еще большим и более широко распространенным, чем сообщали Pomin et al. (Carbohydrate Polymers, 2012, 90, 839-846), оказывая влияние не только на ХС продукты, полученные из сырьевых материалов морского происхождения, но также, хотя и в меньшей степени, на те, которые получены из других животных источников (крупный рогатый скот, свиньи, птица и т.п.).
Обнаружен способ, который при ограниченной стоимости и с уже существующими типами механического оборудования, исходя из существующих в настоящее время на рынке способов получений ХС/КС, обеспечивает удаление КС путем конечной обработки или целевых модификаций способов, разработанных в настоящее время на промышленном уровне, таким образом, возвращая технические требования к продукту ХС к значениям, которые в ближайшее время будут требоваться на международном уровне регулирующими органами, особенно для ХС фармацевтического сорта.
Данный способ, который совершенно отличен от современных технологий фракционного осаждения с помощью растворителя, отличается значительной эксплуатационной гибкостью и, будучи разработанным, является простым и не обладает значительными трудностями при увеличении масштаба производства до промышленного. Способ отличается следующими стадиями: 1) получение раствора ХС/КС в воде и измерение его проводимости, 2) добавление соли до тех пор, пока проводимость не достигнет критического значения, заданного в способе, при этом соль не добавляют, если присутствие только лишь ХС/КС уже гарантирует указанное значение на начальном этапе, 3) постепенное добавление к этому водному раствору расчетного количества органической фазы, состоящей из одного или более растворителей, смешиваемых друг с другом и с количеством воды, указанным на стадии 1, когда добавление органического растворителя завершено, изначально однофазная система становится двухфазной с концентрацией ХС в плотной фазе и концентрацией КС в легкой фазе, 4) извлечение путем осаждения 2-3 объемами этанола ХС из более плотной фазы и КС из менее плотной фазы.
Систематический подход для определения оптимальных условий очистки на промышленном уровне включает, для определенного типа ХС/КС («такой же тип» означает, что различия между уровнями загрязнения хондроитин сульфата кератан сульфатом должны попадать в интервал, не превышающий 2-3%) и для данного органического растворителя, построение диаграммы, на которой проводимость или концентрация водного раствора, содержащего ХС/КС и любые добавленные соли, показана в зависимости от количества органической фазы, требуемой чтобы вызвать образование двух жидких фаз, подходящих для способа очистки. Когда тип ХС/КС и природа выбранного органического растворителя установлены, таким образом возможно определить из построенного графика для данного типа органического растворителя пару значений (проводимость водного раствора и количество органического растворителя), которые приводят к образованию двух жидких фаз, образующих основу способа очистки. Значения, находящиеся ниже указанных параметров (более низкие значения проводимости или меньшее количество растворителя), приводят к низким извлечениям или отсутствию фазового разделения, при этом более высокие значения проводимости или большее количество органического растворителя превращает как ХС, так и КС в плотную фазу, вызывая потерю эффективности способа очистки.
Когда установлена концентрация ХС/КС, при которой требуется проводить способ очистки, определяют количество добавляемой соли (если она присутствует) для доведения проводимости до критического значения, которое вызывает образование двух жидких фаз.
Когда выбран тип используемого органического растворителя и экспериментально определены рабочие условия с помощью построения графика проводимости водного раствора, содержащего ХС/КС, в соответствии с количеством органической фазы, требуемой чтобы вызвать разделения двух жидких фаз, образующих основу способа очистки, его можно выполнить различными способами согласно промышленным возможностям.
Способ А). Когда установлены тип и количество используемого органического растворителя, значение проводимости, которое должен иметь водный раствор, можно найти на графике. Если этого значения достигают с помощью только лишь присутствия ХС/КС в растворе, органическую фазу добавляют в водную фазу при перемешивании. Изначально всегда существует однофазная система и только после добавления органического растворителя наблюдается образование двух жидких фаз, которое определяет разделение ХС в плотную фазу и КС в легкую фазу. Если критическое значение проводимости жидкой фазы не достигается только лишь присутствием ХС/КС в растворе, добавляют соль до тех пор, пока не достигнут требуемой проводимости, и затем добавляют органический растворитель, как описано ранее.
Способ В). Когда установлено значение проводимости водного раствора, содержащего ХС/КС и любые добавленные соли, количество используемого растворителя находят на графике и растворитель добавляют в водный раствор так, как описано для способа А).
Примерами органических растворителей, которые можно использовать в способе очистки ХС/КС по изобретению, являются метанол, этанол, 1-пропанол, 2-пропанол, ацетон, ацетонитрил и их смеси.
Способ по изобретению не только обеспечивает ХС с характеристиками, отвечающими наиболее строгим правилам, которые скоро введут регулирующие органы, но также обеспечивает большое количество КС - продукта, который до сих пор не был доступен на рынке, но для которого можно предположить важные применения, особенно в области офтальмологии (US 5141928, US 6159954) и в качестве соединения с иммуногенностью, до сих пор показанной in vitro (Meller et al., Clin. Chim. Acta, 1995, 236, 195-204, Nakano Т., Carbohydr. Polym., 2014, 99, 547-552).
В заявленных способах разделения получают извлечения, близкие к теоретическим значениям, и чистотой >98%.
Способ очистки ХС/КС предпочтительно выполняют при нейтральном рН, при котором получают наилучшие результаты в показателях как выхода, так и чистоты.
Время, когда две фазы поддерживают при перемешивании для обеспечения оптимального перераспределения двух растворов КС в легкой фазе и ХС в плотной фазе, не является критичным. Выходы и степень чистоты немного изменяются, если указанное время составляет только 1,5 часа или 18 часов.
Аналогично, температура, при которой выполняют способ, не является очень критичной, его можно проводить в широком интервале температур (например, от 4 до 25°С) без какого-либо существенного влияния на выходы или чистоту.
Заявленный способ очистки применим к ХС/КС, полученным различными способами и с использованием хрящей из различных источников.
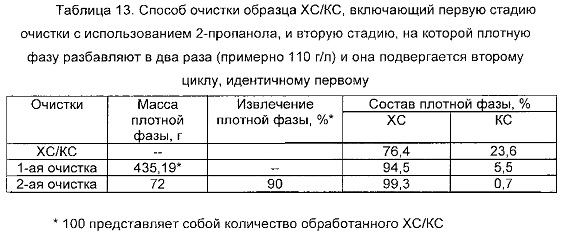
Действуя при особенно высоких концентрациях ХС/КС, лучшие очистки можно получить путем повторного подвергания плотной фазы следующему идентичному циклу очистки, после разбавления ее до концентрации первоначально обрабатываемого образца.
Неожиданно было обнаружено, что в способе очистки ХС/КС параллельно с отделением ХС от КС также значительно уменьшается содержание пирогена.
Заявитель заявленного способа впервые получил чистые стандарты ХС и КС, предпосылку для применения новых технических характеристик продукта, которые регулирующие органы подготавливают к выпуску.
В следующих примерах изобретение описано более подробно.
Пример 1. ЖЭХБ (жидкостная экспресс-хроматография белков) анализ образцов ХС/КС, ХС и КС
Аналитическая подготовительная методология хроматографии позволяет разделять образцы ХС/КС в масштабе сотых частей мг, делая доступными образцы с чистотой, превышающей 99%, в настоящее время не присутствующие на рынке, и подходящие в качестве стандартов для всех процессов валидации, которые регулирующие органы вероятно установят в ближайшем будущем. Приготовленные стандарты используют для всех используемых калибровок способов анализа для характеристики чистоты ХС и КС, описанных ниже.
В способе используют колонку HiLoad Q sepharose 26/10 HP GE Healthcare с сильным анионообменным фильтром, смонтированную на хроматографе Akta Explorer 100 Amersham (GE Healthcare), оборудованном детектором УФ/видимая область спектра. Линейный градиент двух буферных растворов используют в качестве системы элюента: буферный раствор А - 20 мМ ацетата натрия, рН 7,4, 0,5 М NaCl, буферный раствор В - 20 мМ ацетата натрия, рН 7,4, 3,0 М NaCl. Условиями для оптимального разделения ХС и КС являются: линейный градиент 0 - 100% B в А за 106 минут, расход 2 мл/мин, регистрация УФ 215 нм. Анализировали 300 мг образцы, растворенные в 5 мл буферного раствора А. При описанных условиях анализа время элюирования не удерживаемого анализируемого вещества составляет 50 мин, для ХС 193 мин и для КС 268 мин.
Используя образец ХС/КС морского происхождения, получают стандарты ХС и КС со степенью чистоты >99%, извлекая элюаты, соответствующие двум пикам ХС и КС, которые подвергают ультрафильтрации через мембраны с отсечкой при 3 кДа для удаления солей и лиофилизатов. Полученные таким образом образцы характеризуются тем, что указано в примерах 2-4 ниже.
Пример 2. Определение характеристик ХС и КС с помощью ЭксХ-ТДМ (эксклюзионная хроматография - тройная детекторная матрица)
Определение характеристик в показателях молекулярной массы, молекулярно-массового распределения, полидисперсности и характеристической вязкости промышленных ХС/КС продуктов и ХС и КС стандартов, полученных как описано в примере 1, проводили с помощью гельфильтрационного хроматографа (Viscotec, LabService Analytica, Italy), состоящего из двух модулей, и специально предназначенного управляющего программного обеспечения:
модуль GPCmax VE 2001 является объединенной системой, состоящей из специального насоса для эксклюзионной хроматографии (ЭксХ) (изократический насос, способный обеспечить постоянный, без пульсаций поток растворителя), дегазатора растворителя в режиме реального времени и автоматического дозатора,
модуль TDA302 (тройная детекторная матрица) является объединенной системой, образованной печью, термостатированной для колонки и тройного детектора, состоящего из детектора показателя преломления (ПП), вискозиметра (ВМ) с 4-мя капиллярными мостиками и детектора рассеяния света (PC), который, в свою очередь, состоит из двух частей, детектора прямоугольного рассеяния света (ДПРС), отличающегося превосходным отношением сигнала к шуму, и нового детектора рассеяния света под малым углом (РСМУ),
OmniSECTM является программным обеспечением GPCmax и TDA (операционная среда Windows), которое обеспечивает определение характеристик полимерного раствора в показателях концентрации, средней абсолютной молекулярной массы, показателя полидисперсности, молекулярного размера (гидродинамический и вращательный радиус) и характеристической вязкости полимера. Отношение dn/dc (отношение бесконечно малого изменения интенсивности сигнала, измеренного с помощью детектора показателя преломления, к бесконечно малому изменению концентрации анализируемого вещества) составляет 0,1466 мл/г для ХС и 0,1000 мл/г для КС (Swann D.A. et al., J. Biological Chemistry, 1984, 259, 12, 7693-7700).
Хроматографические колонки: хроматографическая система Viscotec оборудована предварительной колонкой TSK-gel CMPWXL (Tosoh Bioscience, Cat. No. 08033, 6,0×4,0 см, средний размер частиц 12 мкм) и 2-мя колонками TSK-gel CMPWXL, расположенными последовательно (Tosoh Bioscience, Italy, Cat. No. 8-08025, материал на основе гидроксилированного полиметакрилата, размер пор 100-1000 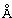 , средний размер частиц 13 мкм, 7,8×30,0 см).
, средний размер частиц 13 мкм, 7,8×30,0 см).
Колонка вискозиметра: предварительная колонка TOSOH08033 и колонка TOSOH08025, обе проданные Viscotek - LabService Analytica S.r.l., Via Emilia, 51/c, 40011, Anzola Emilia (BO, Italy).
Хроматографическими условиями, используемыми для аналитического определения характеристик образцов ХС и КС, являются: подвижная фаза 0,1 М NaNO3, температура 40°С, расход 0,6 мл/мин, продолжительность 50 мин.
Пример 3. Определение характеристик ХС/КС, ХС и КС с помощью кислотного гидролиза и ВЭЖХ - Dionex анализа моносахаридов
Для оценки состава промышленных продуктов ХС/КС и степени чистоты ХС и КС, полученных как описано в примере 1, был разработан аналитический протокол, основанный на кислотном гидролизе образца и хроматографическом анализе моносахаридов, составляющих дисахаридные звенья одиночной цепи гликозаминогликанов: ацетилированного галактозамина (GalNAc) и глюкороновой кислоты (GlcA) для ХС и глюкозамина (GlcN) и галактозы (Gal) для КС.
Предварительные испытания со стандартами указанных сахаров показывают, что в течение гидролиза данные аминосахара частично деацетилируются, каждый образуя два различных пика, при этом GlcA и Gal соответственно образуют один и три пика.
Аналитический протокол в целом обеспечивает гидролиз образца с эффективностью 95-100% и, соответственно, получение эквимолярного определения концентрации двух моносахаридов, составляющих дисахаридные звенья цепей ХС и КС. На основе мольных концентраций составляющих сахаров можно определить процентную массовую долю ХС и КС, присутствующих в образцах, исключая содержание воды, учитывая различные значения средних молекулярных масс дисахаридных звеньев, в соответствии с тканью животного происхождения и воздействием степени сульфатирования и натрификации (sodiation) отдельных молекул.
Кислотный гидролиз
Образцы ХС/КС, ХС и КС подвергают кислому гидролизу. В стандартной процедуре 50 мг образца растворяют в 0,5 мл 1М HCl, приготовленного с водой, очищенной с помощью ионообменной смолы (MQ water). Гидролиз проводят при 100°С в течение 18 часов при перемешивании, образцы затем нейтрализуют 5М NaOH и анализируют с помощью анионообменной хроматографии.
ВЭЖХ анализ моносахаридов с помощью ионообменной хроматографии
Продукты гидролиза анализируют с помощью высокоэффективной анионообменной хроматографии с импульсным амперометрическим детектированием (ВЭАОХ-ИАД), используя ионный хроматограф (ICS 3000, Dionex, Italy) с автоматическим дозатором и двойным насосом, оборудованным колонкой Carbopac РА 1 (4×287,5 мМ, Dionex, Italy) и предварительной колонкой. Хроматографическое разделение продолжается в течение 41 мин (0-12 мин от 1 до 4 мМ NaOH, 12-14 мин 4 мМ NaOH, 14-16 мин от 4 до 100 мМ NaOH, 16-30 мин 100 мМ NaOH, 30-39 мин 100-1 мМ NaOH, 30-41 мин 1 мМ NaOH).
Калибровку ХС и КС проводят с помощью очищенных стандартов для ЖЭХБ, содержащих остаточное загрязнение хондроитин сульфата кератан сульфатом и кератан сульфата хондроитин сульфатом ≤2%, которые гидролизуют так, как описано ранее.
В случае КС калибровочные отрезки, отсекаемые на оси, получают путем вычерчивания суммы областей пиков GlcN и Gal и их производных в зависимости от известного количества гидролизованного стандарта КС, при этом в случае ХС калибровочный отрезок, отсекаемый на оси, получают путем вычерчивания суммы областей пиков GalNAc и GlcA и их производных в зависимости от известного количества стандарта ХС.
Концентрацию (г/л) КС в образцах определяют путем добавления областей репрезентативных пиков для GlcN и Gal и их производных и вычисления концентрации по сравнению с отсекаемым на оси калибровочным отрезком гидролизованного стандарта КС, при этом концентрацию (г/л) ХС в образцах определяют путем добавления областей репрезентативных пиков для GalNAc и GlcA и их производных и вычисления концентрации по сравнению с отсекаемым на оси калибровочным отрезком гидролизованного стандарта ХС. Окончательно процентные доли КС и ХС обнаруживают путем вычисления отношений полученных концентраций к общей сумме процентных концентраций.
Пример 4. Определение характеристик ХС/КС, ХС и КС с помощью метанолиза ГАГ, ацетилирования метил гликозидов и ГХ-МС анализа полученных ацетилированных метил гликозидов
Для оценки состава промышленных продуктов ХС/КС и степени чистоты ХС и КС, полученных как описано в примере 1, был разработан аналитический протокол, включающий метанолиз ГАГ с помощью HCl, ацетилирование полученных метил гликозидов и их анализ с помощью ГХ-МС (газовой хроматографии - масс-спектрометрии). В стандартной процедуре 10 мг образцов подвергают метанолизу (1 мл MeOH/HCl 1.25М, 80°С, 20 часов) и полученные метил гликозиды ацетилируют ангидридом уксусной кислоты (50 мкл) и пиридином (50 мкл) при 100°С в течение 30 минут. Ацетилированные образцы метил гликозидов анализируют с помощью ГХ-МС (Agilent Technologies, GC 6850°, MS 5973N) на капиллярной колонке (Zebron ZB-5, Phenomenex, 30 м × 0,25 мм внутренний диаметр), используя расход 1 мл/мин гелия (газ-носитель) со следующей температурной программой: 150°С в течение 3 минут, 150°С → 240°С при 3°С/мин. Условиями МС детектирования являются: электронный источник ионизации при 70 эВ, квадрупольный анализатор, интервал сбора и обработки данных 40-450 Да.
Метанолиз определяет: полную деполимеризацию путем разрыва гликозидных связей, образование соответствующих метил гликозидов (в случае GlcA образуются как α, так и β метил гликозид), деацетилирование GalNAc и GlcNAc, удаление всех сульфатных групп.
Реакционные смеси анализируют с помощью ГХ-МС. Сахара определяют путем сравнения времени задержки и фрагментации ими известных стандартов.
Процентный молярный состав ХС, КС и ДС в образце вычисляют из отношения областей, лежащих под пиками, соответствующими одиночным метил гликозидам, нормализованными относительно аналитического сигнала стандартных образцов метил гликозидов. Таким образом, при правильном анализе мольные концентрации Gal и GlcN метил гликозидов равны и соответствуют мольной концентрации КС, сумма мольных концентраций GlcA метил гликозидов α и β соответствует мольной концентрации ХС, мольная концентрация IduA метил гликозида соответствует мольной концентрации ДС и мольная концентрация GalN метил гликозида соответствует сумме концентраций ХС + ДС.
Пример 5. Построение графика, на котором показана проводимость водного раствора ХС/КС в зависимости от объема 2-пропанола, требуемого для получения очистки ХС/КС
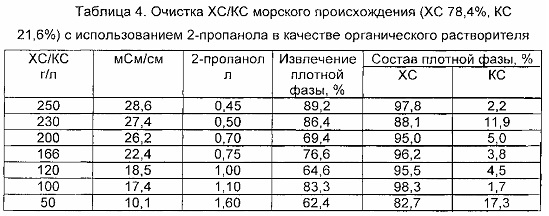
Используют образец ХС/КС морского происхождения, отличающийся содержанием ХС 78% и содержанием КС 22%, приготавливают следующие растворы (1 л) с концентрациями в интервале 50-250 г/л и измеряют их значение проводимости. 2-пропанол добавляют к каждому раствору до тех пор, пока они не разделяться на две жидкие фазы, давая % сухого остатка плотной фазы, который предпочтительно попадает в интервал ±8% от % ХС в смеси ХС/КС, образуя объект способа очистки (для анализируемого образца сухой остаток плотной фазы составляет от 70 до 86%). Как для образца ХС/КС, так и для сухого остатка плотной фазы содержание остаточной воды считают эквивалентным и оценивают в 12-15 масс. %.
Строят два графика, показывающих значения проводимости ХС/КС или значения концентрации, соответственно, в зависимости от объемов 2-пропанола, которые необходимы для получения фазового разделения с этими характеристиками плотной фазы. Все обнаруженные точки выстраиваются вдоль уравнения прямой в отрезках у=-0,0053х+1,7227 (R2=0,9491) для графика объемов 2-пропанола в зависимости от концентрации ХС/КС и уравнения прямой в отрезках у=-2х+0,0593 (R2=0,9743) для графика объемов 2-пропанола в зависимости от проводимости раствора.
При разработке рабочих условий на промышленном уровне для этого типа ХС/КС, когда было определено значение проводимости, вызванной ХС/КС, или концентрации ХС/КС, таким образом автоматически определяют объем 2-пропанола, добавляемого для получения разделения на две жидкие фазы, что приводит к ХС с чистотой >95%. Аналогично, когда был установлен объем используемого 2-пропанола, можно однозначно определить проводимость или концентрацию, которую доложен иметь раствор ХС/КС. В способе, если обрабатываемый раствор имеет концентрацию ХС/КС ниже той, которая необходима для достижения требуемого значения проводимости, указанного значения достигают путем добавления NaCl или других солей. В таблице 4 показаны экспериментальные данные. Полученные образцы ХС и КС анализируют так, как указано в примерах 1, 3 и 4.
Пример 6. Построение графика, на котором показана проводимость водного раствора ХС/КС в зависимости от объема этанола, требуемого для получения очистки ХС/КС
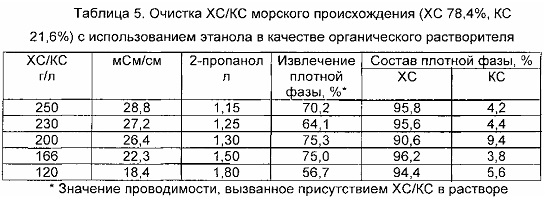
Используют образец ХС/КС морского происхождения, отличающийся содержанием ХС 78% и содержанием КС 22%, приготавливают растворы (1 л) с концентрациями в интервале 120-250 г/л и измеряют их значение проводимости. Этанол добавляют к каждому раствору до тех пор, пока они не разделяться на две жидкие фазы, давая % сухого остатка плотной фазы, ±8% от % ХС в смеси ХС/КС, образуя объект способа очистки (для анализируемого образца сухой остаток плотной фазы составляет от 70 до 86%). Как для образца ХС/КС, так и для сухого остатка плотной фазы содержание остаточной воды полагают эквивалентным и оценивают в 12-15 масс. %.
Строят два графика, показывающих значения проводимости ХС/КС или концентрации, соответственно, в зависимости от объемов этанола, которые необходимы для получения фазового разделения с этими характеристиками плотной фазы. Все обнаруженные точки выстраиваются вдоль уравнения прямой в отрезках у=-0,0049х+2,344 (R2=0,9661) для графика объемов этанола в зависимости от концентрации ХС/КС и уравнения прямой в отрезках у=-0,0658х+3,0284 (R2=0,9885) для графика объемов этанола в зависимости от проводимости раствора.
При разработке рабочих условий на промышленном уровне для этого типа ХС/КС, когда было определено значение проводимости, вызванной ХС/КС, или концентрации ХС/КС, таким образом автоматически определяют объем этанола, добавляемого для получения разделения на две жидкие фазы, что приводит к ХС с чистотой >95%. Аналогично, когда установлен объем используемого этанола, можно однозначно определить проводимость или концентрацию, которую доложен иметь раствор ХС/КС. В способе, если обрабатываемый раствор имеет концентрацию ХС/КС ниже той, которая необходима для достижения требуемого значения проводимости, указанного значения достигают путем добавления NaCl или других солей. В таблице 5 показаны экспериментальные данные. Полученные образцы ХС и КС анализируют так, как указано в примерах 1, 3 и 4.
Пример 7. Очистка ХС/КС с использованием различных смесей растворителей
ХС/КС морского происхождения (ХС 78,4%, КС 21,6%) очищают с помощью различных растворителей. NaCl добавляют к пяти образцам водного раствора объемом 1 л, причем каждый содержит 120 г/л ХС/КС (проводимость 18,8 мСм/см), до тех пор, пока конечная проводимость не составит 25,6 мСм/см (примерно 87,5 мМ NaCl) для растворителей, указанных ниже как А-С, и 37,1 мСм/см (примерно 290 мМ NaCl) для растворителей D-Е. Следующие растворители последовательно добавляют при сильном перемешивании в приготовленные таким образом растворы: А) 2-пропанол 0,75 л, В) 1-пропанол 0,75 л, С) 2-пропанол/2-бутанол 1,00/0,25 в объеме 0,75 л, D) этанол 1 л, Е) ацетон.
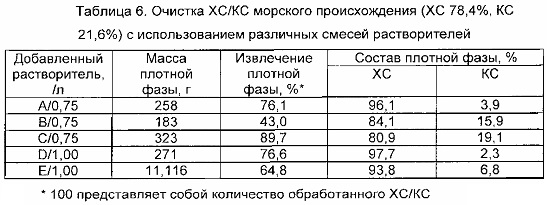
Добавление органического растворителя вызывает разделение изначально гомогенной системы на две жидкие фазы, в которых ХС селективно концентрируется в более плотной фазе, при этом КС аккумулируется в легкой фазе. Двухфазную систему поддерживают при перемешивании в течение 18 часов при комнатной температуре и затем оставляют расслаиваться. Две фазы осаждают при сильном перемешивании путем добавления 2-3 объемов этанола, осадок сушат в вакууме с получением ХС и КС соответственно в форме белых микрокристаллических порошков. В таблице 6 показаны экспериментальные результаты. Полученные образцы ХС и КС анализируют так, как указано в примерах 1, 3 и 4.
Как показывают данные таблицы 6, разработанный способ зависит от природы растворителя, однако универсальность способа всегда обеспечивает оптимизирование рабочих параметров (концентрация ХС/КС, природа растворителя, ионная сила).
Пример 8. Влияние химической природы соли на очистку образцов ХС/КС
ХС/КС морского происхождения (ХС 78,4%, КС 21,6%) очищают с использованием различных солей для достижения критического значения проводимости. Следующие соли добавляют соответственно в три образца водных растворов с объемом 1 л, содержащих 120 г/л ХС/КС (проводимость 18,8 мСм/см): A) NaCl, В) CaCl2, С) K2SO4, до тех пор, пока конечная проводимость не составит 25,6 мСм/см. 0,75 л 2-пропанола добавляют при сильном перемешивании в приготовленные таким образом три раствора. Добавление органического растворителя вызывает разделение изначально гомогенной системы на две жидкие фазы, в которых ХС селективно концентрируется в более плотной фазе, при этом КС аккумулируется в легкой фазе. Двухфазную систему поддерживают при перемешивании в течение 18 часов при комнатной температуре и затем оставляют расслаиваться. Две фазы осаждают при сильном перемешивании путем добавления 2-3 объемов этанола, осадок сушат в вакууме с получением ХС и КС соответственно в форме белых микрокристаллических порошков. В таблице 7 показаны экспериментальные результаты. Полученные образцы ХС и КС анализируют так, как указано в примерах 1, 3 и 4.
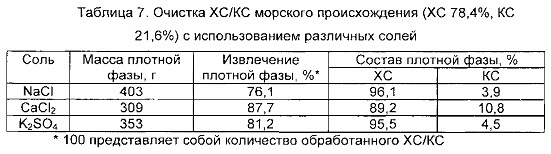
Как показывают данные таблицы 7, разработанный способ зависит от природы соли, используемой для достижения проводимости, необходимой для получения разделения на две жидкие фазы, однако универсальность способа всегда обеспечивает оптимизирование рабочих параметров (концентрация ХС/КС, природа растворителя, ионная сила).
Пример 9. Влияние рН на очистку образцов ХС/КС
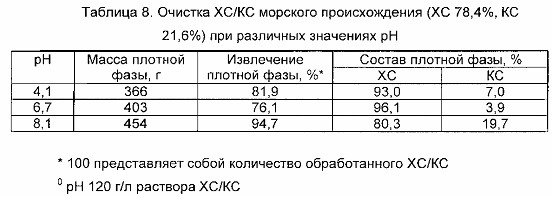
Очистка ХС/КС морского происхождения (ХС 78,4%, КС 21,6%) при различных значениях рН. Два образца ХС/КС (120 г/л) настраивают на рН 4,1 (19,6 мСм/см) и 8,1 (18,9 мСм/см), используя 1М водные растворы HCL и NaOH, соответственно. NaCl добавляют в водные растворы до тех пор, пока конечная проводимость не составит 25,6 мСм/см, затем добавляют 0,75 л 2-пропанола при сильном перемешивании до тех пор, пока раствор не разделится на две жидкие фазы. Добавление органического растворителя вызывает разделение изначально гомогенной системы на две жидкие фазы, в которых ХС селективно концентрируется в более плотной фазе, при этом КС аккумулируется в легкой фазе. Двухфазную систему поддерживают при перемешивании в течение 18 часов при комнатной температуре и затем оставляют расслаиваться. Две фазы осаждают при сильном перемешивании путем добавления 2-3 объемов этанола, осадок сушат в вакууме с получением ХС и КС соответственно в форме белых микрокристаллических порошков. В таблице 8 показаны экспериментальные результаты. Полученные образцы ХС и КС анализируют так, как указано в примерах 1, 3 и 4.
Как можно видеть из данных таблицы 8, способ очистки ХС/КС зависит от рН раствора, с результатами, которые являются наилучшими в показателях как выхода, так и чистоты при нейтральных значениях рН. Полученные образцы ХС и КС анализируют так, как указано в примерах 1, 3 и 4.
Пример 10. Влияние температуры на способ очистки образцов ХС/КС
Для подтверждения критического воздействия температуры на способ очистки ХС/КС приготавливают два образца ХС/КС морского происхождения (ХС 78,4%, КС 21,6%) (120 г/л, 18,8 мСм/см), растворенных в 1 л воды. NaCl добавляют в два раствора вплоть до конечной проводимости 25,6 мСм/см. Действуя при 4 и 25°С, затем добавляют 0,75 л 2-пропанола при сильном перемешивании. Добавление органического растворителя вызывает разделение изначально гомогенной системы на две жидкие фазы, в которых ХС селективно концентрируется в более плотной фазе, при этом КС аккумулируется в легкой фазе. Двухфазную систему поддерживают при перемешивании в течение 18 часов при 4 и 25°С, соответственно. Две фазы затем собирают и осаждают при сильном перемешивании путем добавления 2-3 объемов этанола, осадки сушат в вакууме с получением ХС и КС соответственно в форме белых микрокристаллических порошков. В таблице 9 показаны экспериментальные результаты. Полученные образцы ХС и КС анализируют так, как указано в примерах 1, 3 и 4.
Как показывают данные в таблице 9, разработанный способ в малой степени зависит от температуры, причем наилучшие результаты в показателях чистоты получают при работе при 25°С.

Пример 11. Влияние концентрации ХС/КС на способ очистки с использованием этанола в качестве органического растворителя
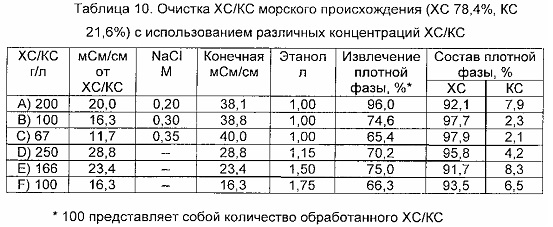
Для оценки критических факторов концентрации ХС/КС в способе очистки приготавливают шесть образцов объемом в 1 л ХС/КС с концентрацией, показанной в таблице 10. NaCl добавляют в образцы А-С, чтобы получить конечную проводимость в интервале от 38 до 40 мСм/см. Затем в раствор добавляют этанол при энергичном перемешивании в количестве, достаточном чтобы вызвать разделения на две жидкие фазы в первоначально гомогенном растворе воды в спирте с селективной концентрацией ХС в плотной фазе и КС в легкой фазе. Двухфазную систему поддерживают при перемешивании в течение 18 часов при комнатной температуре и затем оставляют расслаиваться. Две фазы каждого образца собирают и осаждают при сильном перемешивании путем добавления 2-3 объемов этанола и осадок сушат в вакууме, получая ХС и КС соответственно в форме белых микрокристаллических порошков. В таблице 10 показаны экспериментальные результаты. Полученные образцы ХС и КС анализируют так, как указано в примерах 1, 3 и 4. Как видно из данных таблицы 10, концентрация играет критическую роль, особенно в связи со степенью чистоты. Более низкие концентрации обеспечивают ХС с получаемой чистотой >96%.
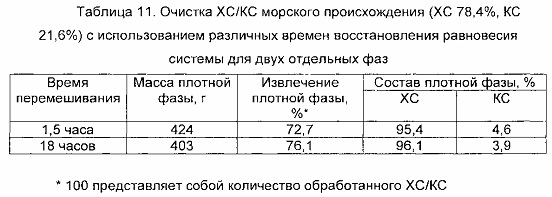
Пример 12. Влияние времени восстановления равновесия в способе очистки образца ХС/КС
Для оценки критических факторов в способе очистки образцов ХС/КС во время восстановления равновесия двухфазной системы, полученной путем поддерживания системы двух отдельных фаз при сильном перемешивании, приготавливают два образца ХС/КС морского происхождения (ХС 78,4%, КС 21,6%) (120 г/л, 18,8 мСм/см) и растворяют в 1 л воды. NaCl добавляют в два раствора вплоть до конечной проводимости 25,6 мСм/см. Действуя при 25°С, затем добавляют 0,75 л 2-пропанола при сильном перемешивании. Добавление органического растворителя вызывает разделение изначально гомогенной системы на две жидкие фазы, в которых ХС селективно концентрируется в более плотной фазе, при этом КС аккумулируется в легкой фазе. Двухфазную систему поддерживают при перемешивании при 25°С в течение 1,5 и 18 часов, соответственно. Две фазы затем собирают и осаждают при сильном перемешивании путем добавления 2-3 объемов этанола, осадки сушат в вакууме с получением ХС и КС соответственно в форме белых микрокристаллических порошков. В таблице 11 показаны экспериментальные результаты. Полученные образцы ХС и КС анализируют так, как указано в примерах 1, 3 и 4. Как выходит из данных в таблице 11, разработанный способ зависит в умеренной степени от времени восстановления равновесия двух фаз, с немного лучшими извлечениями и чистотой, получаемыми при более длительных временах.
Пример 13. Влияние источника извлечения ХС/КС на способ очистки
Для оценки критических факторов, присущих природе подлежащего очистке образца ХС/КС, анализировали три образца морского происхождения и два образца животного (из свиней) происхождения. Приготавливали растворы в воде пяти образцов объемом 1 л (120 г/л, 18,8 мСм/см). NaCl добавляют в растворы вплоть до конечной проводимости 25,6 мСм/см. Действуя при 25°С, затем добавляют 0,75 л 2-пропанола при сильном перемешивании. Добавление органического растворителя вызывает разделение изначально гомогенной системы на две жидкие фазы, в которых ХС селективно концентрируется в более плотной фазе, при этом КС аккумулируется в легкой фазе. Двухфазную систему поддерживают при перемешивании в течение 18 часов. Две фазы различных образцов затем собирают и осаждают при сильном перемешивании путем добавления 2-3 объемов этанола, осадки сушат в вакууме с получением ХС и КС соответственно в форме белых микрокристаллических порошков. В таблице 12 показаны экспериментальные результаты. Полученные образцы ХС и КС анализировали так, как указано в примерах 1, 3 и 4.
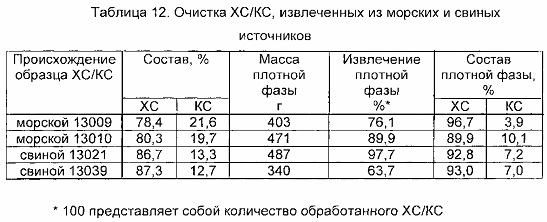
Данные показывают, что заявленный способ можно использовать независимо от типа применяемого в способе очистки ХС/КС. Очевидно, что чем меньше исходный продукт загрязнен КС, тем чище будет конечный очищенный ХС, как выясняется из данных по чистоте для образцов свиного происхождения, которые всегда изначально более чистые, чем образцы морского происхождения.
Пример 14. Повторная очистка ХС из легкой фазы
Для улучшения степени полученной чистоты, в частности когда используют очень высокие концентрации ХС/КС, плотную фазу можно снова непосредственно подвергнуть способу очистки. Ее сперва разбавляют водой для получения концентрации, первоначально используемой в первом способе очистки, и затем повторяют весь способ.