Результат интеллектуальной деятельности: Способ определения N-(бензимидазолил-2)-О-метилкарбамата в биологическом материале
Вид РИД
Изобретение
Изобретение относится к биологии, токсикологической и санитарной химии, а именно к способам определения N-(бензимидазолил-2)-O-метилкарбамата в биологическом материале, и может быть использовано в практике санэпидстанций, химико-токсикологических и ветеринарных лабораторий. Способ относится к числу массовых.
Известен способ определения производных карбаминовой кислоты (1-нафтил-N-метилкарбамата) в биологических объектах путем измельчения биологической ткани, ее обработки гексаном в присутствии безводного сульфата натрия в течение 2-3 часов, отделения гексанового извлечения, упаривания до сухого остатка, растворения остатка в смеси вода-метанол, взятых в объемном соотношении 3:2, прибавления к водно-метанольному раствору хлорида натрия, экстракции раствора хлороформом, отделения хлороформного экстракта, упаривания до сухого остатка, растворения остатка в гексане с последующим хроматографированием в тонком слое силикагеля на пластинах «Силуфол» с использованием подвижной фазы гексан-ацетон в объемном отношении 3:1 и проявлением хроматограмм путем последовательной обработки водно-этанольным раствором гидроксида калия и раствором соли диазония (Лабораторные исследования в ветеринарии. Химико-токсикологические методы. / Под ред. Б.И. Антонова. -М: Агропромиздат, 1989. - С. 160-162).
Способ характеризуется недостаточно высокой степенью извлечения N-(бензимидазолил-2)-O-метилкарбамата, относительно низкими точностью и чувствительностью определения.
Известен способ определения N-(бензимидазолил-2)-O-метилкарбамата в биологическом материале, заключающийся в том, что биологическую пробу измельчают, трехкратно настаивают с этилацетатом, этилацетатные извлечения объединяют, фильтруют, анализируемое вещество из этилацетата экстрагируют 0,1 н. раствором хлороводородной кислоты, полученный экстракт промывают гексаном, подщелачивают 4 н. раствором гидроксида натрия до рН 10, экстрагируют этилацетатом, экстракт обезвоживают, экстрагент испаряют, сухой остаток растворяют в ацетоне, хроматографируют в тонком слое силикагеля на пластинах «Силуфол» с использованием подвижной фазы этилацетат-хлороформ-уксусная кислота в объемном отношении 50:50:10, хроматограммы проявляют в УФ-свете и определяют анализируемое вещество визуально по интенсивности окраски и размеру пятна на хроматограмме (Методы определения микроколичеств пестицидов в продуктах питания, кормах и внешней среде. / Под ред. М.А. Клисенко. - Т. 1. - М.: ВО «Колос», 1992. - С. 477-480).
Способ характеризуется относительно низкой степенью извлечения анализируемого соединения, недостаточно высокими точностью и чувствительностью.
Наиболее близким является способ определения N-(бензимидазолил-2)-О-метилкарбамата в биологическом материале, который заключается в том, что биологическую ткань измельчают, трехкратно настаивают со смесью растворителей этилацетат-дихлорэтан-муравьиная кислота, взятых в отношении 5:5:1 по объему, каждый раз в течение 15 минут, полученные извлечения объединяют, объединенное извлечение фильтруют, фильтрат экстрагируют 0,1 н. раствором хлороводородной кислоты, полученный кислотный экстракт промывают этилацетатом, этилацетатный слой отбрасывают, водный слой подщелачивают 10% раствором гидроксида натрия до рН 8-9, экстрагируют этилацетатом, полученный экстракт отделяют, обезвоживают, экстрагент испаряют, остаток растворяют в органическом растворителе, которым является ледяная уксусная кислота, хроматографируют в тонком слое сорбента, которым является силикагель, обработанный вазелиновым маслом, с использованием подвижной фазы ацетонитрил-вода в отношении 6:4 по объему, хроматограммы проявляют в УФ-свете, анализируемое вещество элюируют из сорбента смесью растворителей этилацетат-дихлорэтан-муравьиная кислота, взятых в отношении 5:5:1 по объему, и проводят определение физико-химическим методом, которым является спектрофотометрия, измеряя оптическую плотность элюата при длине волны 282 нм (Патент 2300765 Российская Федерация, МПК G01N 30/90; G01N 31/22; G01N 235/32. Способ определения N-(бензилимидазолил-2)-O-метилкарбамата в биологическом материале / Шорманов В.К., Дурицын Е.П., Мехедова О.С., Баранов Ю.Н.; заявители и патентообладатели Шорманов В.К., Дурицын Е.П., Мехедова О.С., Баранов Ю.Н. (RU). - №2005132925/04; Заяв. 25.10.2005; Опуб. 10.06.2007 // Изобретения (Заявки и патенты). - 2007. - №16. - 8 с.).
Способ характеризуется недостаточно высокой чувствительностью определения.
Техническим результатом настоящего изобретения является повышение чувствительности определения.
Технический результат достигается тем, что биологическую ткань измельчают, трехкратно настаивают со смесью растворителей этилацетат-дихлорэтан-муравьиная кислота, взятых в отношении 5:5:1 по объему, каждый раз в течение 15 минут, полученные извлечения объединяют, объединенное извлечение фильтруют, фильтрат экстрагируют 0,1 н. раствором хлороводородной кислоты, полученный кислотный экстракт промывают этилацетатом, этилацетатный слой отбрасывают, водный слой подщелачивают 10% раствором гидроксида натрия до рН 8-9, экстрагируют этилацетатом, полученный экстракт отделяют, обезвоживают, экстрагент испаряют, остаток растворяют в органическом растворителе, которым является муравьиная кислота, хроматографируют в макроколонке сорбента, которым является «Сидасорб С-8» 15 μ, с использованием подвижной фазы ацетонитрил-вода в отношении 4:6 по объему, фракции элюата из макроколонки, содержащие анализируемое вещество, объединяют, обрабатывают раствором аммиака, испаряют до сухого остатка, остаток растворяют в смеси диоксан-пропанол-2 в отношении 5:1 по объему и проводят определение физико-химическим методом, которым является ВЭЖХ, с использованием аналитической колонки размерами 64×2 мм, заполненной сорбентом «Силасорб 600», подвижной фазы гексан-диоксан-пропанол-2 в отношении 15:5:1 по объему и УФ-детектора.
Способ осуществляется следующим образом: биологическую ткань, содержащую N-(бензимидазолил-2)-O-метилкарбамат, измельчают, трижды настаивают со смесью растворителей этилацетат-дихлорэтан-муравьиная кислота, взятых в отношении 5:5:1 по объему, каждый раз в течение 15 минут, полученные извлечения объединяют, объединенное извлечение фильтруют, фильтрат экстрагируют 0,1 н. раствором хлороводородной кислоты, полученный кислотный экстракт промывают этилацетатом, этилацетатный слой отбрасывают, водный слой подщелачивают 10% раствором гидроксида натрия до рН 8-9, экстрагируют этилацетатом, полученный экстракт отделяют, обезвоживают, экстрагент испаряют, остаток растворяют в органическом растворителе, которым является муравьиная кислота, хроматографируют в макроколонке сорбента, которым является «Силасорб С-8» 15 μ, с использованием подвижной фазы ацетонитрил-вода в отношении 4:6 по объему, фракции элюата из макроколонки, содержащие анализируемое вещество, объединяют, обрабатывают раствором аммиака, испаряют до сухого остатка, остаток растворяют в смеси диоксан-пропанол-2 в отношении 5:1 по объему и проводят определение физико-химическим методом, которым является ВЭЖХ, с использованием аналитической колонки размерами 64×2 мм, заполненной сорбентом «Силасорб 600», подвижной фазы гексан-диоксан-пропанол-2 в отношении 15:5:1 по объему и УФ-детектора.
Способ иллюстрируется следующими примерами.
Пример 1
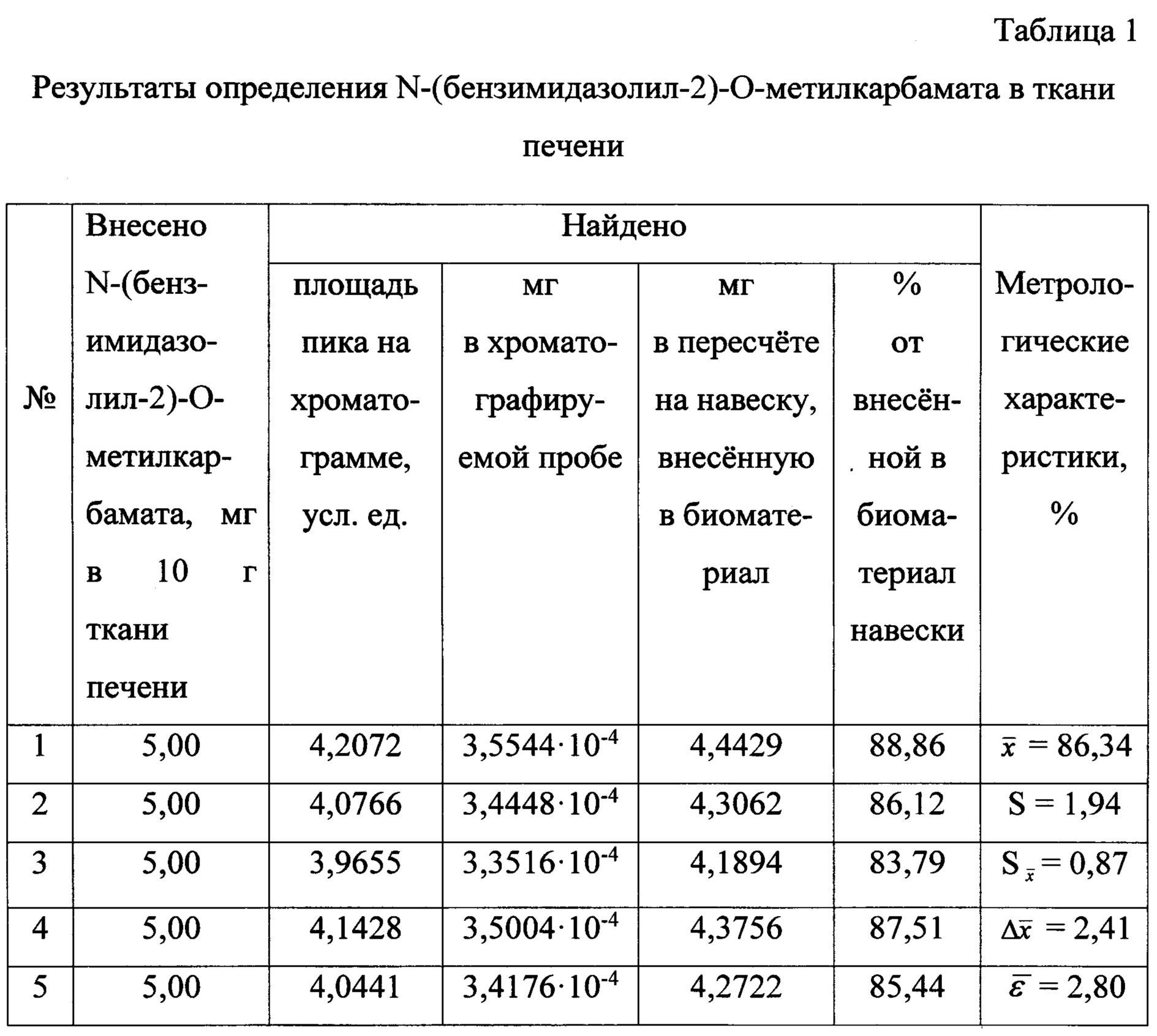
Определение N-(бензимидазолил-2)-O-метилкарбамата в ткани печени
К 10 г мелкоизмельченной ткани печени прибавляют 5 мг N-(бензимидазолил-2)-O-метилкарбамата, тщательно перемешивают биологическую ткань с веществом и оставляют на сутки при температуре 18-20°С. По истечении указанного времени биологическую ткань, содержащую анализируемое вещество, трижды настаивают со смесью растворителей этилацетат-дихлорэтан-муравьиная кислота, взятых в отношении 5:5:1 по объему. Для этого биологическую ткань заливают 20 мл смесью растворителей этилацетат-дихлорэтан-муравьиная кислота в отношении 5:5:1 по объему и настаивают 15 минут при перемешивании. Извлечение отделяют, операцию настаивания повторяют еще дважды в указанных условиях. Полученные извлечения объединяют, фильтруют через бумажный фильтр, фильтрат экстрагируют 0,1 н. раствором хлороводородной кислоты дважды порциями по 60 мл каждая. Отдельные экстракты объединяют, полученный объединенный кислотный экстракт промывают путем встряхивания в течение 4 минут с 120 мл этилацетата, этилацетатный слой отбрасывают, водный слой подщелачивают 10% раствором гидроксида натрия до рН 8-9, экстрагируют дважды порциями этилацетата по 150 мл каждая. Этилацетатные экстракты отделяют, объединяют, полученный объединенный этилацетатный экстракт обезвоживают, пропуская через стеклянный фильтр с 10 г безводного сульфата натрия, фильтр промывают 20 мл этилацетата. Отдельные фильтраты объединяют, экстрагент испаряют в токе воздуха при комнатной температуре, остаток растворяют в 3-4 мл органического растворителя, которым является муравьиная кислота, полученный раствор смешивают с 1 г сорбента «Силасорб С-8» 15 μ и испаряют остатки муравьиной кислоты из сорбента в токе воздуха.
В макроколонку размером 490×10 мм вносят вначале 6,5 г сорбента «Силасорб С-8» 15 μ, а затем, поверх образующегося слоя, - 1 г сорбента «Силасорб С-8» 15 μ, содержащего анализируемое вещество, предварительно введенное в виде раствора в муравьиной кислоте. Хроматографируют в мароколонке сорбента «Силасорб С-8» 15 μ с использованием подвижной фазы ацетонитрил-вода в отношении 4:6 по объему. Элюат, истекающий из макроколонки, собирают отдельными фракциями по 2 мл каждая.
Фракции элюата, истекающего из макроколонки, с 4 по 8 включительно, содержащие анализируемое вещество, объединяют, обрабатывают 0,2 мл 10% раствора аммиака, элюент испаряют в токе воздуха при температуре 18-22°С до сухого остатка. Остаток растворяют в 20 мл смеси растворителей диоксан-пропанол-2 в отношении 5:1 по объему, количественно перенося образующийся раствор в мерную колбу вместимостью 25 мл, при и доводят до метки смесью растворителей гексан-диоксан-пропанол-2 в отношении 15:5:1 по объему (раствор А). 2,5 мл раствора А вносят в мерную колбу вместимостью 20 мл и доводят до метки смесью растворителей гексан-диоксан-пропанол-2 в отношении 15:5:1 по объему (раствор Б).
16 мкл раствора Б вводят в жидкостный хроматограф типа «Милихром».
Проводят определение физико-химическим методом, которым является ВЭЖХ, хроматографируя с использованием аналитической колонки размерами 64×2 мм, заполненной сорбентом «Силасорб 600», подвижной фазы гексан-диоксан-пропанол-2 в отношении 15:5:1 по объему и УФ-детектора.
Скорость подачи элюента составляет 100 мкл/мин, масштаб регистрации - 0,8 единиц оптической плотности, время измерения - 0,6 сек. Оптическую плотность регистрируют при длине волны 282 нм.
Пик на хроматограмме с временем удерживания 4,71 мин (объемом удерживания 471 мкл соответствует N-(бензимидазолил-2)-O-метилкарбамату.
Количественное содержание N-(бензимидазолил-2)-O-метилкарбамата определяют, исходя из площади хроматографического пика, по уравнению градуировочного графика и пересчитывают на навеску вещества, внесенную в ткань печени.
Построение градуировочного графика
В ряд мерных колб вместимостью 20 мл вносят 0,125, 0,25; 0,5; 1,0; 1,5, 2,5, 4,0, 5,0 и 6,25 мл 0,02% раствора N-(бензимидазолил-2)-O-метилкарбамата в смеси растворителей гексан-диоксан-пропанол-2 в отношении 15:5:1 по объему и доводят до метки смесью растворителей гексан-диоксан-пропанол-2 в отношении 15:5:1 по объему. 16 мкл каждого из полученных растворов вводят в хроматограф типа «Милихром». В хроматографируемой пробе при этом содержится соответственно 0,02, 0,04, 0,08, 0,16, 0,24, 0,40, 0,64, 0,8 и 1,0 мкг анализируемого вещества.
Проводят определение, хроматографируя методом ВЭЖХ в аналитической колонке размерами 64×2 мм, заполненной сорбентом «Силасорб 600», с применением подвижной фазы гексан-диоксан-пропанол-2 в отношении 15:5:1 по объему и УФ-детектора.
Скорость подачи элюента составляет 100 мкл/мин, масштаб регистрации - 0,8 единиц оптической плотности, время измерения - 0,6 сек. Оптическую плотность регистрируют при длине волны 282 нм.
По результатам измерений на хроматографе строят график зависимости площади хроматографического пика от концентрации определяемого вещества. График линеен в интервале концентраций 0,02-1,00 мкг.
Методом наименьших квадратов рассчитывают уравнение градуировочного графика, которое в данном случае имеет вид:
11,918876⋅С-0,029267,
где S - площадь хроматографического пика, С - концентрация определяемого вещества в хроматографируемой пробе, мкг.
Результаты определения N-(бензимидазолил-2)-O-метилкарбамата в ткани печени представлены в таблице 1.
Пример 2
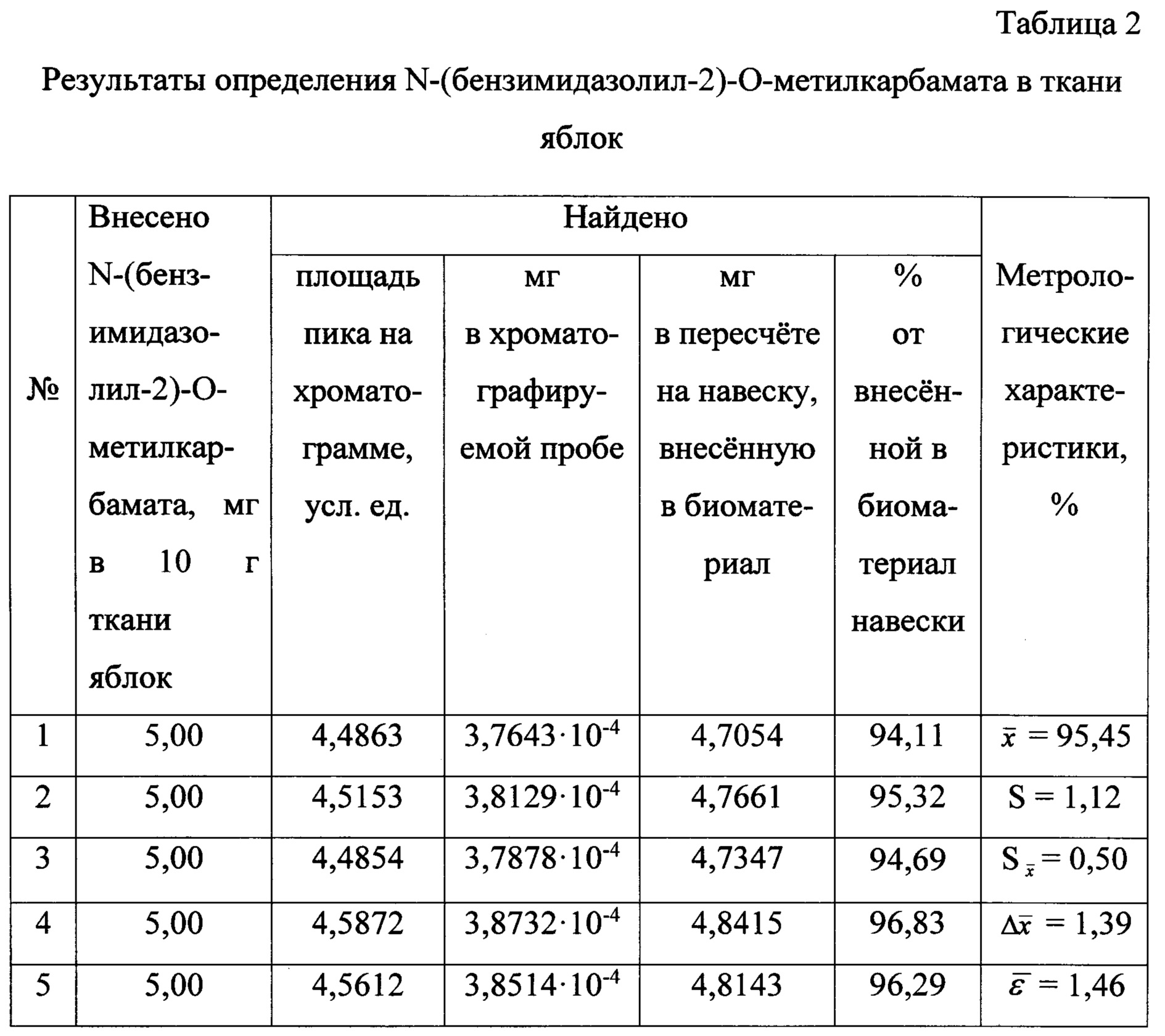
Определение N-(бензимидазолил-2)-O-метилкарбамата в ткани яблок
К 10 г мелкоизмельченной ткани яблок прибавляют 5 мг N-(бензимидазолил-2)-O-метилкарбамата, тщательно перемешивают биологическую ткань с веществом и оставляют на сутки при температуре 18-20°С. По истечении указанного времени биологическую ткань, содержащую анализируемое вещество, трижды настаивают со смесью растворителей этилацетат-дихлорэтан-муравьиная кислота, взятых в отношении 5:5:1 по объему. Для этого биологическую ткань заливают 20 мл смесью растворителей этилацетат-дихлорэтан-муравьиная кислота в отношении 5:5:1 по объему и настаивают 15 минут при перемешивании. Извлечение отделяют, операцию настаивания повторяют еще дважды в указанных условиях. Полученные извлечения объединяют, фильтруют через бумажный фильтр, фильтрат экстрагируют 0,1 н. раствором хлороводородной кислоты дважды порциями по 60 мл каждая. Отдельные экстракты объединяют, полученный объединенный кислотный экстракт промывают путем встряхивания в течение 4 минут с 120 мл этилацетата, этилацетатный слой отбрасывают, водный слой подщелачивают 10% раствором гидроксида натрия до рН 8-9, экстрагируют дважды порциями этилацетата по 150 мл каждая. Этилацетатные экстракты отделяют, объединяют, полученный объединенный этилацетатный экстракт обезвоживают, пропуская через стеклянный фильтр с 10 г безводного сульфата натрия, фильтр промывают 20 мл этилацетата. Отдельные фильтраты объединяют, экстрагент испаряют в токе воздуха при комнатной температуре, остаток растворяют в 3-4 мл органического растворителя, которым является муравьиная кислота, полученный раствор смешивают с 1 г сорбента «Силасорб С-8» 15 μ, и испаряют остатки муравьиной кислоты из сорбента в токе воздуха.
В макроколонку размером 490x10 мм вносят вначале 6,5 г сорбента «Силасорб С-8» 15 μ, а затем, поверх образующегося слоя, - 1 г сорбента «Силасорб С-8» 15 μ, содержащего анализируемое вещество, предварительно введенное в виде раствора в муравьиной кислоте. Хроматографируют в мароколонке сорбента «Силасорб С-8» 15 μ с использованием подвижной фазы ацетонитрил-вода в отношении 4:6 по объему. Элюат, истекающий из макроколонки, собирают отдельными фракциями по 2 мл каждая.
Фракции элюата, истекающего из макроколонки, с 4 по 8 включительно, содержащие анализируемое вещество, объединяют, обрабатывают 0,2 мл 10% раствора аммиака, элюент испаряют в токе воздуха при температуре 18-22°С до сухого остатка. Остаток растворяют в 20 мл смеси растворителей диоксан-пропанол-2 в отношении 5:1 по объему, количественно перенося образующийся раствор в мерную колбу вместимостью 25 мл, при и доводят до метки смесью растворителей гексан-диоксан-пропанол-2 в отношении 15:5:1 по объему (раствор А). 2,5 мл раствора А вносят в мерную колбу вместимостью 20 мл и доводят до метки смесью растворителей гексан-диоксан-пропанол-2 в отношении 15:5:1 по объему (раствор Б).
16 мкл раствора Б вводят в жидкостный хроматограф типа «Милихром».
Проводят определение физико-химическим методом, которым является ВЭЖХ, хроматографируя с использованием аналитической колонки размерами 64×2 мм, заполненной сорбентом «Силасорб 600», подвижной фазы гексан-диоксан-пропанол-2 в отношении 15:5:1 по объему и УФ-детектора.
Скорость подачи элюента составляет 100 мкл/мин, масштаб регистрации - 0,8 единиц оптической плотности, время измерения - 0,6 сек. Оптическую плотность регистрируют при длине волны 282 нм.
Пик на хроматограмме с временем удерживания 4,71 мин (объемом удерживания 471 мкл соответствует N-(бензимидазолил-2)-O-метилкарбамату.
Количественное содержание N-(бензимидазолил-2)-О-метилкарбамата определяют, исходя из площади хроматографического пика, по уравнению градуировочного графика и пересчитывают на навеску вещества, внесенную в ткань яблок.
Построение градуировочного графика и его уравнение приводятся в примере 1.
Результаты количественного определения N-(бензимидазолил-2)-O-метилкарбамата в ткани яблок представлены в таблице 2.
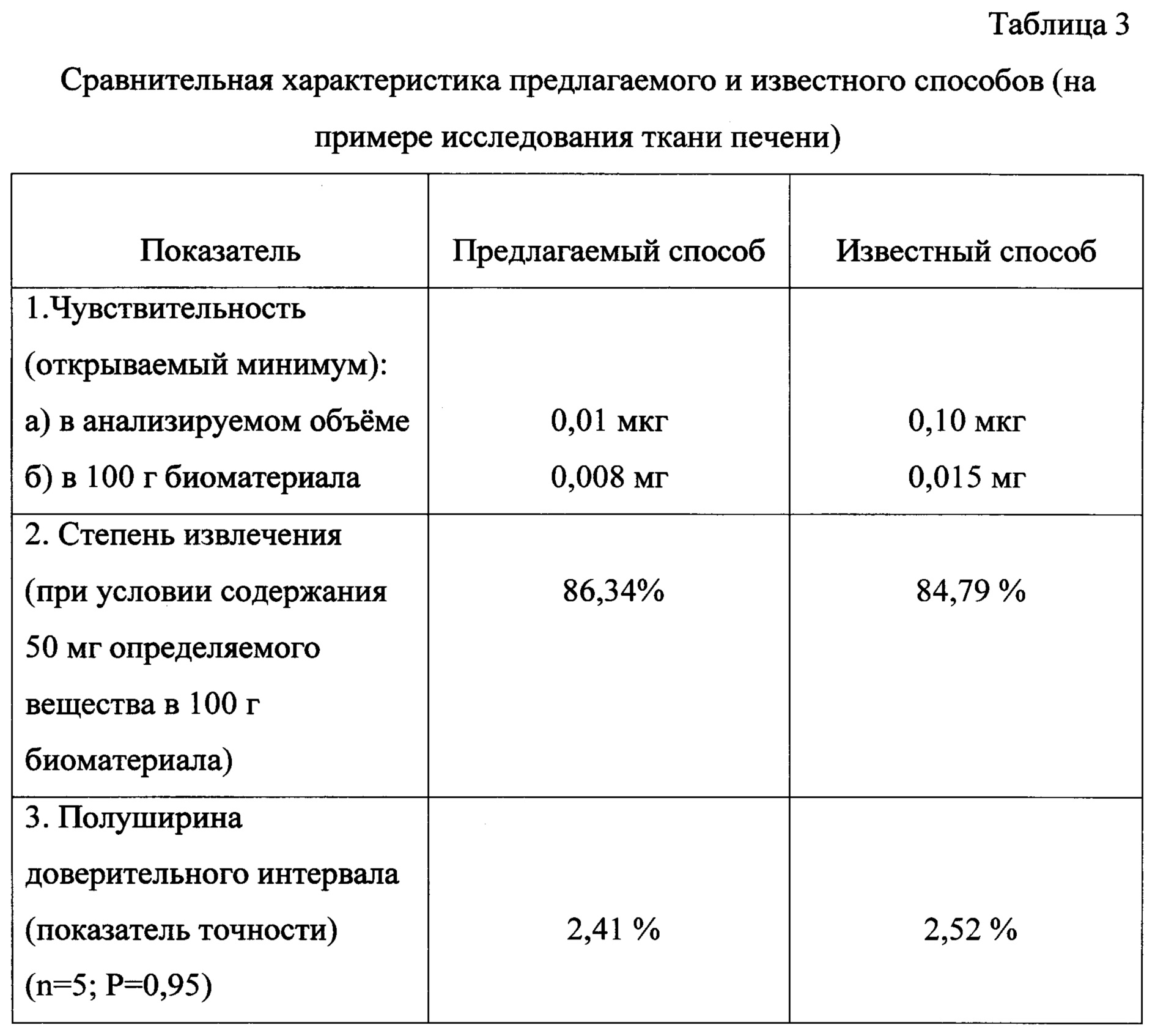
Предлагаемый способ по сравнению с прототипом в 1,8 раз повышает чувствительность определения в биологическом материале и в 10 раз в анализируемой пробе. Сравнительная характеристика предлагаемого и известного способов представлена в таблице 3.