Результат интеллектуальной деятельности: СПОСОБ ГЕРМЕТИЗАЦИИ ВЕЩЕСТВА
Вид РИД
Изобретение
[ОБЛАСТЬ ТЕХНИКИ]
[0001]
Настоящее изобретение относится к способу герметизации веществ и детекции целевой молекулы.
[ПРЕДПОСЫЛКИ ДЛЯ СОЗДАНИЯ ИЗОБРЕТЕНИЯ]
[0002]
Анализ единичных молекул известен как способ выполнения разных анализов посредством наблюдения за биомолекулами, такими как белки и нуклеиновые кислоты, таким образом, чтобы идентифицировать биомолекулы по отдельности. Известны несколько способов выполнения анализа единичных молекул.
[0003]
Источник 1 патентной литературы раскрывает микрокамеру для детекции ферментативной активности единичных молекул. Эта микрокамера включает контейнерную часть, в которой может быть герметизирована капля жидкости и которая способна хранить каплю жидкости объемом до 1000 фл (фемтолитров). Контейнерная часть изготовлена из выемки, выполненной по меньшей мере в одном из первого элемента и второго элемента, которые связаны друг с другом. Согласно Источнику 1 патентной литературы, ферментативную реакцию выполняют в капле жидкости. При такой конфигурации ферментативная реакция может быть выполнена с высокой концентрацией продуктов реакции, даже если число молекул продуктов реакции очень мало. Таким образом можно детектировать активность одной молекулы фермента.
[0004]
Источник 1 непатентной литературы раскрывает способ выполнения ферментного анализа единичных молекул посредством использования массива, где капля жидкости покрыта маслом, порядка нескольких фемтолитров, и прямо доступна снаружи. Этот массив включает паттерн гидрофильной области, изготовленный из гидрофильной поверхности, на которой расположена гидрофобная область, имеющая высоту 17 нм.
[0005]
Источник 2 непатентной литературы раскрывает способ детекции белка посредством иммуноферментного анализа (ИФА). Согласно этому способу, очень небольшое количество белков захватывается мельчайшими микробусинами, покрытыми специфичными к белку антителами, и комплексы микробусин и белков снабжены флуоресцентными метками. Затем микробусины, включающие эти комплексы, вводят в камеру реакции посредством центробежной силы. После этого подсчитывают число микробусин с захваченными белками. Таким образом выполняется количественный анализ белков.
[ЦИТИРУЕМЫЕ ССЫЛКИ]
[Патентная литература]
[0006]
[1] Опубликованная патентная заявка Японии, Tokukai, №2004-309405 А
[Непатентная литература]
[0007]
[1] С. Сакакихара и др.(S. Sakakihara et al.), Lab Chip, 2010, 10, 3355-3362
[2] Дэвид M. Риссин и др. (David М Rissin et al.), Nature Biotechnology: doi: 10.1038/nbt.1641
[РАСКРЫТИЕ ИЗОБРЕТЕНИЯ]
[Техническая задача]
[0008]
Для того, чтобы детектировать, например, маркеры заболевания в низкой концентрации для ранней детекции заболеваний, инфекционных заболеваний и т.д., есть спрос на биочувствительные способы, разработанные так, чтобы они имели повышенную чувствительность. Например, в случае, когда один миллион раковых клеток, содержащихся в опухоли объемом 1 мм3, секретируют маркерные белки (100 молекул на 1 клетку) в 5 литров крови, концентрация белков в крови составляет приблизительно 30 аттомоль (аМ). Необходим способ детекции целевых молекул в такой очень низкой концентрации.
[0009]
Одним из возможных способов детекции целевых молекул может быть способ детекции вышеупомянутым ферментативным анализом единичных молекул на уровне чувствительности одной молекулы. Более конкретно, такой способ осуществляют следующим образом: (i) специфично герметизируют целевую молекулу в капле жидкости объемом порядка нескольких фемтолитров (очень малая капля жидкости), (ii) связывают целевую молекулу с веществом, таким как антитело, помеченное ферментом, и (iii) детектируют активность ферментной метки антитела вышеуказанным образом. Специфичная герметизация целевой молекулы в очень малой капле жидкости может быть осуществлена способом, в котором используется, например, микробусина, помеченная веществом, таким как другое антитело, для специфичного связывания с целевой молекулой. Согласно этому способу, после того, как микробусина будет связана с целевой молекулой, микробусину герметизируют в очень малой капле раствора.
[0010]
В этой связи, чтобы эффективно детектировать целевые молекулы, которые содержатся в растворе только в очень малом количестве, например, приблизительно 30 аМ целевых молекул, как сказано выше, необходимо подготовить большое число пластин очень малых капель жидкости, приблизительно один миллион, и обеспечить захват микробусин этими пластинами.
[0011]
Однако согласно способу, раскрытому в Источнике 2 непатентной литературы, микробусины необходимо ввести в пластины посредством большой центробежной силы, поэтому требуется много времени и усилий. Кроме того, число пластин, используемых в способе из Источника 2 непатентной литературы, составлять приблизительно 50 тысяч. Поэтому способ из Источника 2 непатентной литературы очень трудно применить в случае, когда требуется приблизительно один миллион пластин. Таким образом, используя способ из Источника 2 непатентной литературы, трудно эффективно герметизировать большое число микробусин в пластинах. В этой связи, ни Источник 1 патентной литературы, ни Источник 1 непатентной литературы не раскрывают способ решения этой проблемы.
[0012]
В связи с этим настоящее изобретение имеет цель предложить способ эффективной герметизации большого числа веществ, таких как микробусины, нуклеиновая кислота, белок, вирус, клетки и липидно-мембранный комплекс, в пластине.
[Техническое решение]
[0013]
Для достижения вышеуказанной цели настоящее изобретение предлагает следующий способ герметизации вещества и т.д.
[1] Способ герметизации вещества, включающий: (i) этап введения первого растворителя, содержащего вещество, на субстрат, на котором выполнено некоторое множество ячеек, способных хранить вещество и отделенных одна от другой боковой стенкой; и (ii) этап введения второго растворителя, имеющего удельный вес больше чем удельный вес первого растворителя, на первый растворитель, причем этап (ii) выполняют после этапа (i).
[2] Способ по п. [1], отличающийся тем, что по меньшей мере один из первого растворителя и второго растворителя содержит поверхностно-активное вещество.
[3] Способ по п. [2], отличающийся тем, что поверхностно-активное вещество в первом растворителе имеет концентрацию от 0,01% до 1%.
[4] Способ по п. [2] или [3], отличающийся тем, что поверхностно-активным веществом является TWEEN 20 или Triton Х-100.
[5] Способ по любому из пл. [1]-[4], отличающийся тем, что вторым растворителем является по меньшей мере одно вещество, выбираемое из группы, состоящей из: насыщенного углеводорода, ненасыщенного углеводорода, ароматического углеводорода, силиконового масла, гексафторпропилен-эпоксидного полимера, полимера, имеющего структуру гидрофторэфира, перфторполиэфира, полимера хлортрифторэтилена и полимера, имеющего структуру перфторуглерода, или является смесью, включающей по меньшей мере одно вещество из упомянутых.
[6] Способ по любому из пп. [1]-[5], отличающийся тем, что первым растворителем является по меньшей мере одно вещество, выбираемое из группы, состоящей из: воды, гидрофильного спирта, гидрофильного эфира, кетона, нитрильных растворителей, ди-метилсульфоксида и N,N-диметилформамида, или является смесью, включающей по меньшей мере одно вещество из упомянутых.
[7] Способ по п. [5] или [6], отличающийся тем, что боковая стенка имеет гидрофобную верхнюю поверхность, включающую фторуглеродную полимерную смолу, и вторым растворителем является полимер, имеющий структуру перфторуглерода.
[8] Способ по п. [7], отличающийся тем, что фторуглеродная полимерная смола является аморфной фторуглеродной смолой.
[9] Способ по любому из пп. [1]-[8], отличающийся тем, что область, включающая ячейки субстрата открыта наружу.
[10] Способ по любому из пп. [1]-[9], отличающийся тем, что веществом является одно или несколько, выбираемых из микробусин, нуклеиновой кислоты, белка, вируса, клеток и липидного мембранного комплекса.
[11] Способ детекции целевой молекулы, включающий: (i) этап реагирования микробусин, специфично захватывающих целевые молекулы, с целевыми молекулами; этап осуществления, с использованием микробусин, способа, указанного в любом одном из пп. [1]-[9], причем этап (ii) выполняют после этапа (i); и этап определения, хранится ли любая одна из микробусин, захвативших целевую молекулу, в каждой из множества ячеек, причем этап (iii) выполняют после этапа (ii).
[12] Способ по п. [11], отличающийся тем, что микробусинами являются такие микробусины, с которыми связываются молекулы, способные специфично связываться с целевыми молекулами.
[13] Способ герметизации вещества в ячейках, выполненных на субстрате, посредством введения гидрофильного растворителя, содержащего вещество, в ячейки и покрытия гидрофильного растворителя, содержащего вещество, введенное в ячейки, гидрофобным растворителем, включающий: (i) этап введения гидрофильного растворителя, содержащего вещество, на субстрат, на котором выполнено некоторое множество ячеек, способных хранить вещество и отделенных одна от другой боковой стенкой; и (ii) этап введения гидрофобного растворителя, имеющего больший удельный вес чем удельный вес гидрофильного растворителя, на гидрофильный растворитель, причем этап (ii) выполняют после этапа (i).
[14] Способ по п. [13], отличающийся тем, что по меньшей мере один из гидрофильного растворителя и гидрофобного растворителя содержит поверхностно-активное вещество.
[15] Способ по п. [14], отличающийся тем, что поверхностно-активное вещество в гидрофильном растворителе имеет концентрацию от 0,01% до 1%.
[16] Способ по п. [14] или [15], отличающийся тем, что поверхностно-активным веществом является TWEEN 20 или Triton Х-100.
[17] Способ по любому из пп. [13]-[16], отличающийся тем, что гидрофобным растворителем является по меньшей мере одно вещество, выбираемое из группы, состоящей из насыщенного углеводорода, ненасыщенного углеводорода, ароматического углеводорода, силиконового масла, гексафторпропилен-эпоксидного полимера, полимера, имеющего структуру гидрофторэфира, перфторполиэфира, полимера хлортрифторэтилена и полимера, имеющего структуру перфторуглерода, или является смесью, включающей по меньшей мере одно вещество из упомянутых.
[18] Способ по любому из пп. [13]-[17], отличающийся тем, что гидрофильным растворителем является по меньшей мере одно вещество, выбираемое из группы, состоящей из воды, гидрофильного спирта, гидрофильного эфира, кетона, нитрильных растворителей, диметилсульфоксида и N,N-диметилформамида, или является смесью, включающей по меньшей мере одно вещество из упомянутых.
[19] Способ по п. [17] или [18], отличающийся тем, что боковая стенка имеет гидрофобную верхнюю поверхность, включающую фторуглеродную полимерную смолу, и гидрофобным растворителем является полимер, имеющий структуру перфторуглерода.
[20] Способ по п. [19], отличающийся тем, что фторуглеродная полимерная смола является аморфной фторуглеродной смолой.
[21] Способ по любому из пп. [13]-[20], отличающийся тем, что область, включающая ячейки субстрата, открыта наружу.
[22] Способ по любому из пп. [13]-[21], отличающийся тем, что веществом является одно или несколько, выбираемых из микробусины, нуклеиновой кислоты, белка, вируса, клеток и липидного мембранного комплекса.
[23] Способ детекции целевой молекулы, включающий: (i) этап реагирования микробусин, специфично захватывающих целевые молекулы с целевыми молекулами; (ii) этап осуществления, с использованием микробусин, способа, указанного в любом одном из пп. [13]-[21], причем этап (ii) выполняют после этапа (i); и (iii) этап определения, сохранена ли любая одна из микробусин, захвативших целевую молекулу, в каждой из множества ячеек, причем этап (iii) выполняют после этапа (ii).
[22] Способ по п. [21], отличающийся тем, что микробусинами являются такие микробусины, с которыми связываются молекулы, способные специфично связываться с целевыми молекулами.
[Полезные результаты изобретения]
[0014]
Использования способа герметизации вещества согласно настоящему изобретению дает возможность эффективно герметизировать многие вещества, такие как микробусины, нуклеиновая кислота, белок, вирус, клетки и липидный мембранный комплекс, в пластине, что способствует способу, посредством которого целевые молекулы в низкой концентрации могут быть детектированы с высокой чувствительностью.
[КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ]
[0015]
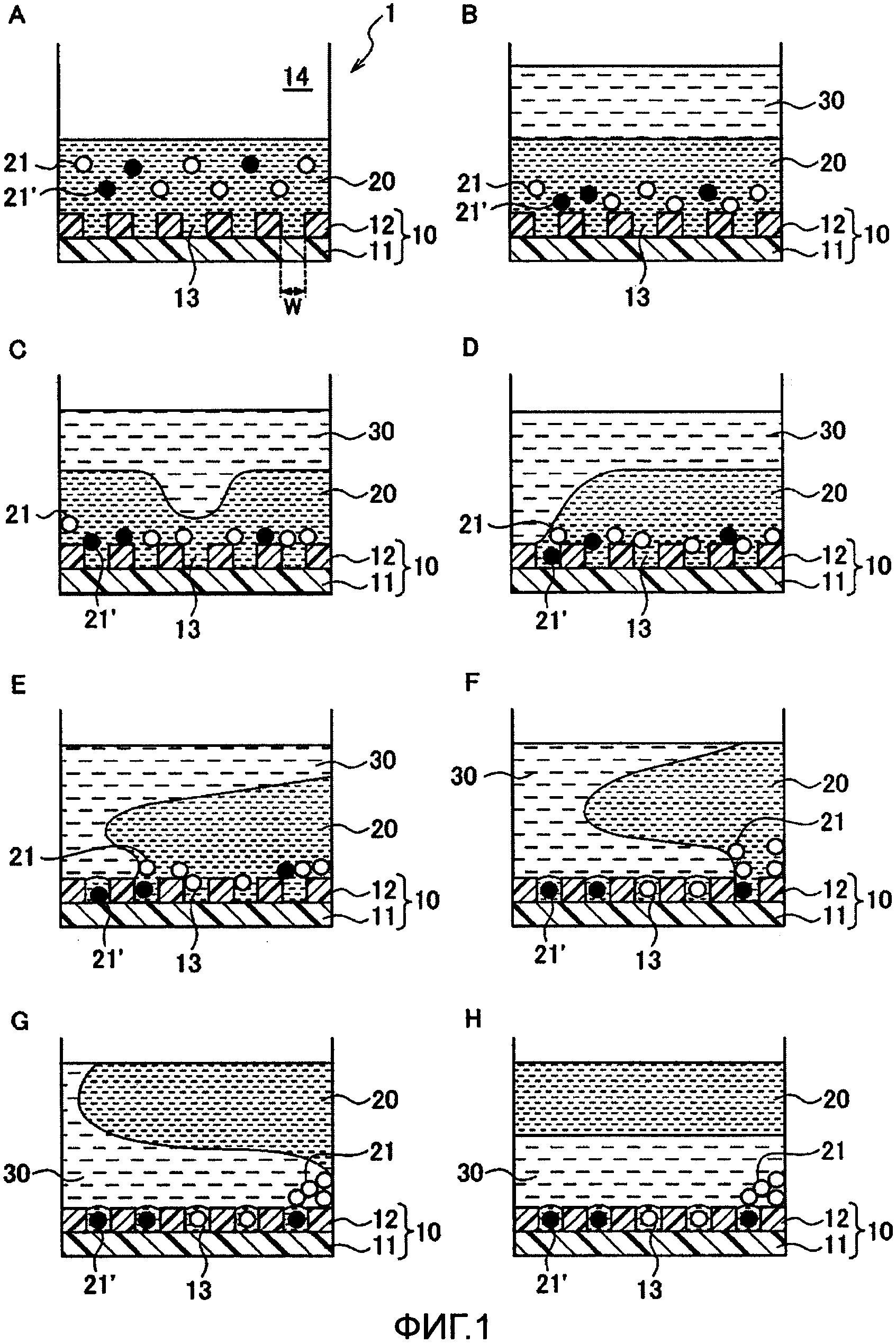
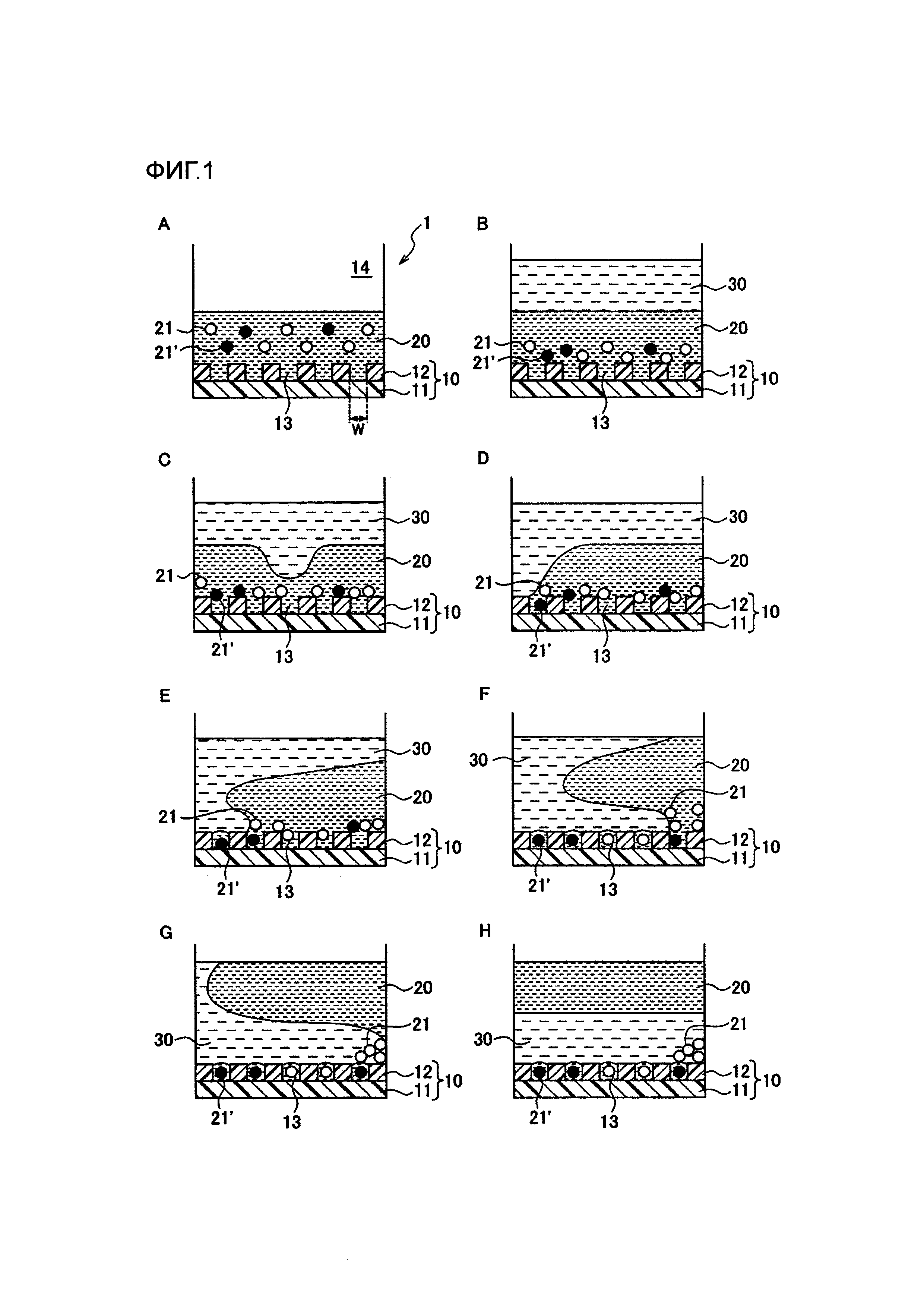
Фиг. 1 - последовательность видов, схематически иллюстрирующих порядок выполнения способа герметизации вещества согласно настоящему изобретению, которые показывают вид сбоку в разрезе пластины 1.
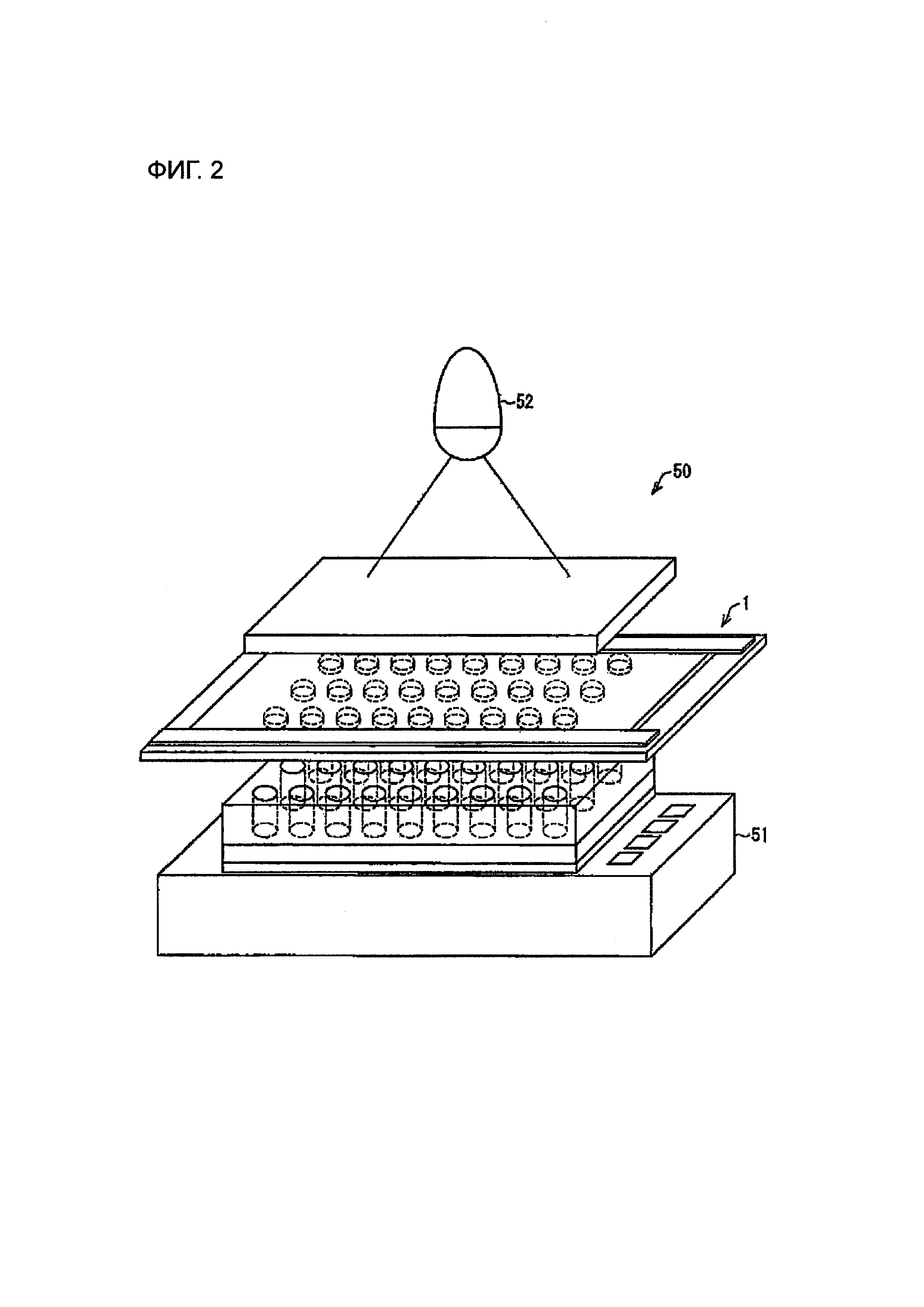
Фиг. 2 - вид, схематически иллюстрирующий один вариант осуществления устройства для детекции целевой молекулы согласно настоящему изобретению.
[ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ]
[0016]
Ниже будут описаны предпочтительные варианты осуществления настоящего изобретения со ссылками на чертежи. Описанные ниже варианты осуществления предназначены служить только в качестве примера варианта осуществления настоящего изобретения, но объем настоящего изобретения не должен истолковываться в ограничительном смысле.
[0017]
В способе герметизации вещества согласно настоящему изобретению веществом, герметизируемым в ячейках, выполненных на субстрате, могут быть микробусины, нуклеиновая кислота, белок, вирус, клетки, липидный мембранный комплекс и т.д.; однако ниже будет описан вариант осуществления с использованием микробусин в качестве примера.
[0018]
1. Способ герметизации микробусин
Со ссылкой на Фиг. 1, ниже описан способ герметизации микробусин согласно настоящему изобретению. На Фиг. 1 показана последовательность видов, схематически иллюстрирующих порядок осуществления способа герметизации микробусин согласно настоящему изобретению, которые показывают виды сбоку в разрезе пластины 1.
[0019]
Данный вариант осуществления относится к случаю, когда микробусины 21 и 21' герметизируют в пластине 1, включающей субстрат 10. Субстрат 10 включает множество ячеек 13, каждая из которых способна хранить только одну из микробусин 21 и 21' и которые отделены одна от другой боковой стенкой 12, имеющей гидрофобную верхнюю поверхность.
[0020]
Здесь термин "микробусина" используется как синоним термину "частица" и является техническим термином, широко используемым в данной области техники. Форма микробусины конкретно не ограничена; однако она обычно сферическая. Материал микробусины также конкретно не ограничен и может быть стеклом, силикагелем, полистиролом, полипропиленом, мембраной, магнитным материалом и т.д. Конкретные примеры материала включают целлюлозу, производные целлюлозы, акриловую смолу, стекло, силикагель, полистирол, желатин, поливинилпирролидон, сополимеры винила и акриламида, полистиролы, сшитые с дивинилбензолом и т.д., полиакриламид, латексный гель, полистирольный декстран, каучук, силикон, пластик, нитроцеллюлозу, природную губку, металлопластик, сшитый декстран (Sephadex (зарегистрированный товарный знак)) и агарозный гель (Sepharose (зарегистрированный товарный знак)). Микробусины могут быть пористыми. Микробусины предпочтительно имеют средний диаметр частиц 5 мкм или меньше, например, приблизительно 1 мкм - 4 мкм. При этом микробусины могут быть эффективно герметизированы в пластине, и пластина может иметь высокую плотность. Следует сказать, что термин "средний диаметр частицы" относится здесь к значению, полученному в результате измерений микробусин с помощью электронного микроскопа или посредством динамического рассеяния света.
[0021]
Данный вариант осуществления описывает, но без конкретного ограничения, случай использования микробусин, специфично захватывающих целевые молекулы. В данном варианте осуществления герметизируемыми микробусинами является смесь микробусин 21, которые еще не захватили целевые молекулы, и микробусин 21', которые захватили целевые молекулы.
[0022]
Например, в качестве микробусин, специфично захватывающих целевые молекулы, можно использовать микробусины, связанные с молекулой для специфичного захвата целевой молекулы. Молекула для специфичного захвата целевой молекулы может быть связана с модифицирующей группой на поверхности микробусины, например, посредством линкера. Например, настоящее изобретение может иметь такую форму, что молекула для специфичного захвата целевой молекулы ковалентно связана с аминогруппой на поверхности микробусины, модифицированной аминогруппой, посредством кросс-линкера, включающего N-гидроксисукцинимид и т.д.
[0023]
Термин "целевая молекула" относится к молекуле, которая должна быть детектирована (молекула-мишень). Более конкретно, термин "целевая молекула" здесь относится к молекуле, которая должна быть детектирована посредством захвата этой молекулы микробусиной. Примеры целевой молекулы включают (i) биомолекулы, такие как белок, нуклеиновая кислота, сахар, и (ii) сами частицы вируса.
[0024]
Молекула для специфичного захвата целевой молекулы (ниже такая молекула также именуется как "молекула, захватывающая мишень") может быть выбрана в соответствии с целевой молекулой. Примеры молекулы, захватывающей мишень, включают белок, антитело и нуклеиновую кислоту. Предпочтительно, одна микробусина связана со ста тысячами или больше молекул, захватывающих мишень. Например, в случае, когда молекула, захватывающая мишень, является антителом, молекула, захватывающая мишень, имеет константу диссоциации порядка нескольких наномоль (нМ). Однако при вышеупомянутой форме можно вызвать реакцию между микробусинами и целевыми молекулами с достаточно высокой концентрацией захвата мишени (например, в случае, когда концентрация микробусин составляет 8×106 частиц/мл, концентрация молекул, захватывающих мишени, составляет приблизительно 1 нМ).
[0025]
Способ герметизации микробусины согласно данному варианту осуществления включает этап введения микробусин, этап деаэрации и этап сохранения микробусин. Каждый из этих этапов подробно описан ниже.
[0026]
[Этап введения микробусин]
Далее описан этап введения микробусин со ссылкой на Фиг. 1А.
[0027]
Этап введения микробусин заключается в введении первого растворителя 20, содержащего микробусины 21 и 21', на субстрат 10. Способ введения первого растворителя 20 конкретно не ограничен; однако может быть применен способ, включающий использование области 14 с ячейками 13 на субстрате 10 в качестве открытой лунки, которая открыта наружу для введения первого растворителя 20 из отверстия в лунку.
[0028]
Первый растворитель 20 предпочтительно является гидрофильным, предпочтительно используется как таковой, например, является по меньшей мере одним веществом, выбираемым из группы, состоящей из воды, гидрофильного спирта, гидрофильного эфира, кетона, нитрильных растворителей, диметилсульфоксида (DMSO) и N,N-диметилформамида (DMF), или является смесью, включающей по меньшей мере одно вещество из упомянутых. Примеры гидрофильного спирта включают этанол, метанол, пропанол и глицерин. Примеры гидрофильного эфира включают тетрагидрофуран, оксид полиэтилена и 1,4-диоксан. Примеры кетонов включают ацетон и метилэфиркетон. Примеры нитрильных растворителей включают ацетонитрил.
[0029]
Первый растворитель 20 предпочтительно содержит поверхностно-активное вещество. На этапе сохранения микробусин, который описан ниже, второй растворитель 30, имеющий больший удельный вес чем удельный вес первого растворителя 20, вводят на первый растворитель 20 (см. Фиг. 1В), после чего выполняют замещение на основании разницы в удельном весе первого растворителя 20 и второго растворителя 30, чтобы сместить второй растворитель 30 в нижний слой первого растворителя 20 (см. Фиг. 1Н). В это время можно добавить ПАВ в первый растворитель 20 и/или второй растворитель 30, чтобы способствовать замещению между первым растворителем 20 и вторым растворителем 30.
Поверхностно-активное вещество (ПАВ) конкретно не ограничено; однако его примеры включают TWEEN 20 (CAS No. 9005-64-5, полиоксиэтилен сорбитанмонолаурат) и Triton Х-100 (CAS No. 9002-93-1, обычное название - полиэтиленгликоль-трет-октилфениловый эфир (n≈10)). Концентрация ПАВ, добавляемого в первый растворитель 20, конкретно не ограничена; однако она предпочтительно составляет от 0,01 до 1%.
[0030]
Помимо этого, анионное ПАВ, катионное ПАВ, неионное ПАВ, цвиттерионное ПАВ, природное ПАВ и т.д. могут широко использоваться в качестве поверхностно-активного вещества.
[0031]
Анионное ПАВ классифицируется, например, по карбоксильному типу, сульфатному типу, сульфоновому типу и фосфатному типу. Его конкретные примеры включают додецилсульфат натрия, лаурат натрия, метиловый эфир натрий альфа-сульфожирной кислоты, додецилбензолсульфонат натрия и додецил-этоксилат-сульфат натрия; из них предпочтительно использовать додецилбензолсульфонат.
[0032]
Катионное ПАВ классифицируется, например, по типу четвертичной соли аммония, типу алкиламина и типу гетероциклического амина. Его конкретные примеры включают стеарилтриметиламмонийхлорид, дистеарилдиметиламмоний хлорид, дидецилдиметиламмоний хлорид, цетилтрипиридиний хлорид и додецилдиметилбензоламмоний хлорид.
[0033]
Примеры неионного ПАВ включают полиоксиэтилен-алкиловые эфиры, полиоксиэтилен-гидрированные касторовые масла, эфиры полиоксиэтилен-моножирных кислот, эфиры полиглицерил-жирных кислот, алкилполигликозиды и N-метилалкилглюкамиды. Из них предпочтительными являются неионные ПАВ, предлагаемые под наименованиями Triton X (Triton Х-100 и т.д.), Pluronic (зарегистрированный товарный знак) (Pluronic F-123, F-68 и т.д.), Tween (Tween 20, 40, 60, 65, 80, 85 и т.д.), Brij (зарегистрированный товарный знак) (Brij 35, 58, 98 и т.д.) и Span (Span 20, 40, 60, 80, 83, и 85) в дополнение к этоксилату додецилового спирта, этоксилату нонифенола и лаурилдиэтаноламиду.
[0034]
Примеры амфотерного ПАВ включают бетаин лаурилдиметиламиноуксусной кислоты, бетаин додециламинометилдиметилсульфопропила и 3-(тетрадецилдиметиламинио)пропан-1-сульфонат; однако его предпочтительные примеры включают 3-[(3-холамидопропил)диметиламмонио]-1-пропансульфонат (CHAPS) и 3-[(3-холамидопропил)диметиламмонио]-2-гидрокси-1-пропансульфонат (CHAPSO).
[0035]
Природным ПАВ предпочтительно является, например, лецитин или сапонин. Из соединений, называемых лецитином, конкретно предпочтительными являются фосфатидилхолин, фосфатидиллетаноламин, фосфатидилинозитол, фосфатидилсерин, фосфатидная кислота и фосфатидилглицерол. В качестве сапонина предпочтителен сапонин коры квиллайи.
[0036]
В дополнение к микробусинам 21 и 21' первый растворитель 20 также может включать, например, вещество для специфичной детекции целевой молекулы, захваченной любой из микробусин 21'. Таким вещество может быть, например, флуоресцентный субстрат, который высвобождает флуоресцентный материал при разложении определенным ферментом, связанным с (i) целевой молекулой, захваченной любой из микробусин 21', или (ii) молекулой, специфично связанной с целевой молекулой. Примеры молекулы, специфично связанной с целевой молекулой, включают вторичное антитело и нуклеиновую кислоту. Примеры определенного фермента включают бета-галактозидазу и пероксидазу. Примеры флуоресцентного субстрата включают флуоресцеин-ди-бета-галактопиранозид (FDG) и Amplex Red (зарегистрированный товарный знак).
[0037]
[Этап сохранения микробусин]
Ниже описан этап сохранения микробусин со ссылкой на Фиг. 1B-1Н.
[0038]
Этап сохранения микробусин представляет собой этап введения второго растворителя 30, имеющего больший удельный вес чем удельный вес первого растворителя 20, на первый растворитель 20. Способ введения второго растворителя 30 конкретно не ограничен; однако может быть применен способ, который включает использование области 14 с ячейками 13 в субстрате 10 в качестве открытой лунки, которая открыта наружу, для введения второго растворителя 30 из отверстия в лунку. В это время второй растворитель 30 предпочтительно вводят так, чтобы слой второго растворителя 30 наслоился на слой первого растворителя 20, как показано на Фиг. 1В.
[0039]
Вторым растворителем 30 может быть растворитель, имеющий больший удельный вес чем удельный вес первого растворителя 20, используемого на этапе введения микробусин. Первый растворитель 20 и второй растворитель 30 предпочтительно взаимно амфифильны в степени, способной вызвать замещение слоя; однако они должны быть не совместимы друг с другом. Чрезмерно низкая амфифильность между первым растворителем 20 и вторым растворителем 30 не вызывает замещения слоя между первым растворителем 20 и вторым растворителем 30. Замещение слоя между первым растворителем 20 и вторым растворителем 30 также не происходит, когда первый растворитель 20 и второй растворитель 30 совместимы друг с другом. Для того, чтобы предотвратить смешивание первого растворителя 20 и второго растворителя 30, предпочтительно использовать гидрофильный растворитель в качестве первого растворителя 20 и гидрофобный растворитель в качестве второго растворителя 30. Как и первый растворитель 20, второй растворитель 30 может содержать ПАВ, чтобы способствовать замещению слоя.
[0040]
Вторым растворителем 30 предпочтительно является гидрофобный растворитель, предпочтительно используемый как таковой, например, по меньшей мере одно вещество, выбираемое из группы, состоящей из насыщенного углеводорода, ненасыщенного углеводорода, ароматического углеводорода, силиконового масла, гексафторпропилен-эпоксидного полимера, полимера, имеющего структуру гидрофторэфира, перфтор-полиэфира, полимера хлортрифторэтиленаи полимера, имеющего структуру перфторуглерода, или является смесью, включающей по меньшей мере одно вещество из упомянутых. Примеры насыщенных углеводородов включают алканы и циклоалканы. Примеры алканов включают декан и гексадекан. Примеры ненасыщенных углеводородов включают сквален. Примеры ароматических углеводородов включают бензол и толуол. Примеры гексафторпропилен-эпоксидных полимеров включают Krytox 143 (от компании DuPont Co., Ltd.) и Krytox GPL (от компании DuPont Co., Ltd.). Примеры полимера, имеющего структуру гидрофторэфира, включают Asahiklin АЕ3000 (от компании Asahi Glass Co., Ltd.) и Novec 7000 (от компании Sumitomo 3М Co., Ltd.). Примеры полимера, имеющего структуру перфторуглерода, включают Fluorinert FC-40 и Fluorinert FC-43 (от компании Sumitomo 3М Co., Ltd.).
[0041]
Второй растворитель 30, вводимый и наслаиваемый на первый растворитель 20, имеет больший удельный вес чем удельный вес первого растворителя 20 и, таким образом, смещается вниз под первый растворитель 20. Более конкретно, происходит замещение между первым растворителем 20 и вторым растворителем 30, в результате чего состояние, в котором верхним слоем является второй растворитель 30 и нижним слоем является первый растворитель 20 (см. Фиг. 1B), становится состоянием, в котором верхним слоем является первый растворитель 20 и нижним слоем является второй растворитель 30 (см. Фиг. 1Н). На Фиг. 1С-G схематически показано, как происходит замещение слоев. При этом замещении слоев микробусины 21 и 21', осаждающиеся на дно области 14, сохраняются в соответствующих ячейках 13, причем в этом случае они принудительно смещаются туда вторым растворителем 30, перемещающимся вниз под первый растворитель 20 (см. Фиг. 1D-F). В результате, микробусины могут герметизированы с высокой эффективностью в каждую из большого числа ячеек 13, которые выполнены на субстрате 10. В случае использования гидрофильного растворителя в качестве первого растворителя 20 и гидрофобного растворителя в качестве второго растворителя 30 капли (капли жидкости первого растворителя 20), покрытые вторым растворителем 30, эффективно формируются в соответствующих ячейках 13.
[0042]
Ниже предпочтительные примеры первого растворителя 20 и второго растворителя 30, используемых в способе герметизации микробусин согласно настоящему изобретению, показаны в "Таблице 1" и "Таблице 2".
[0043]
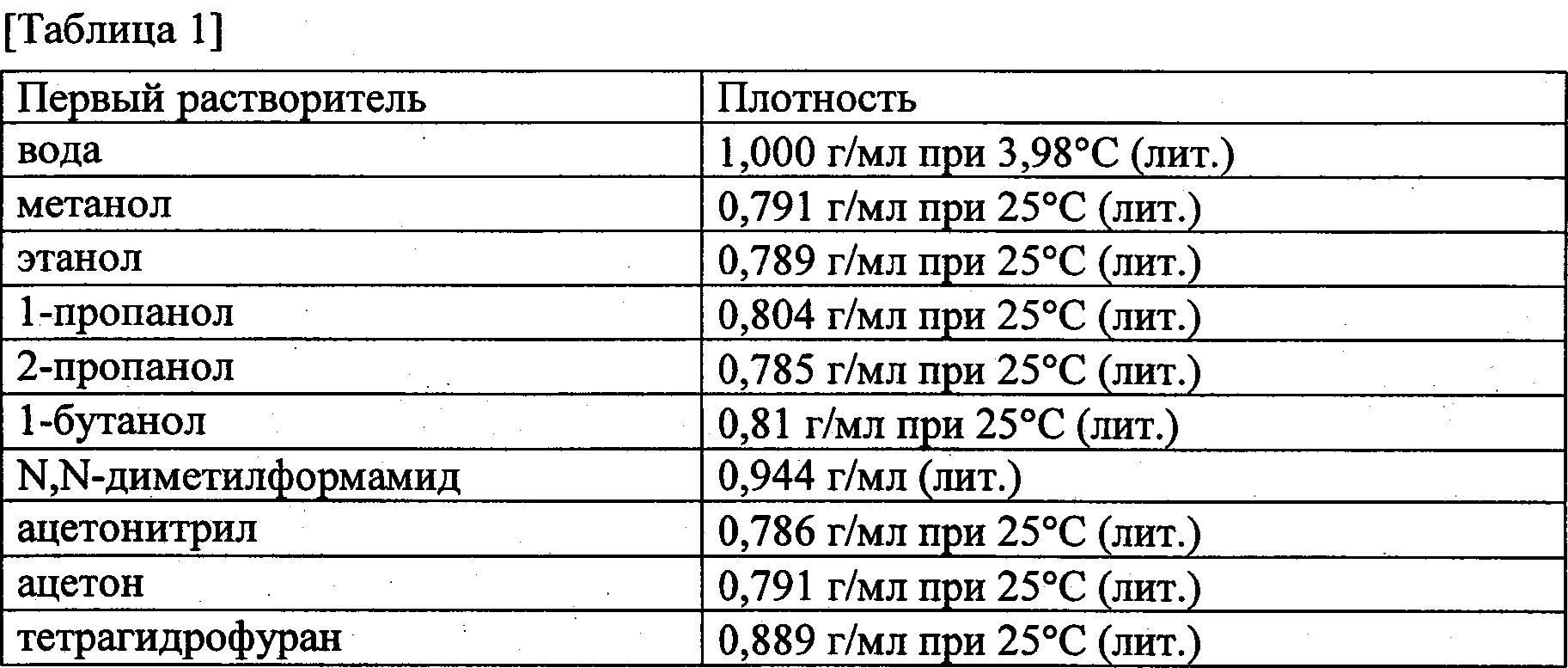
[0044]
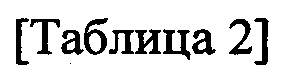
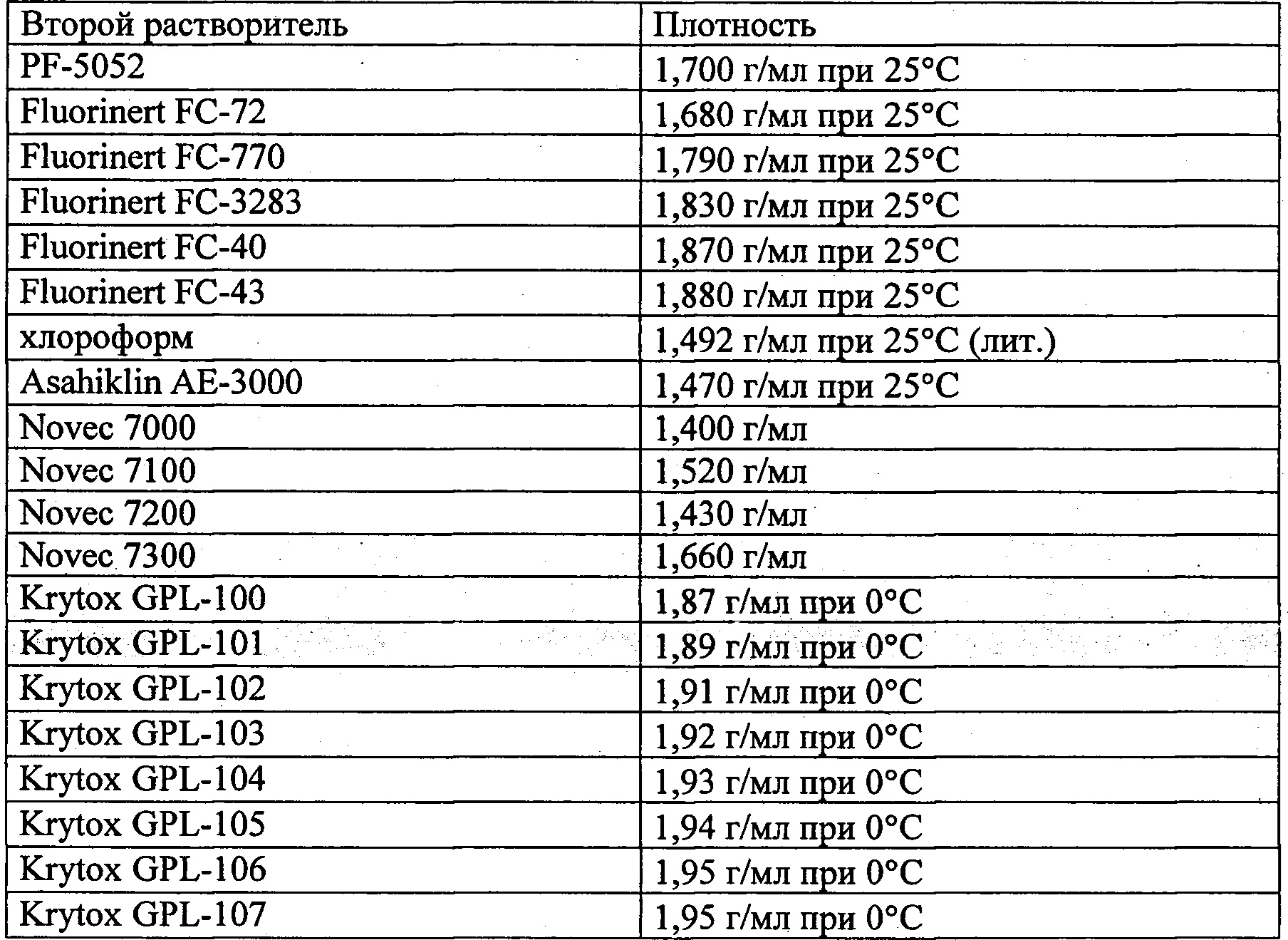
[0045]
На этапе сохранения микробусин, когда в качестве микробусин 21 и 21' используют магнитные микробусины, можно использовать магнитные средства для содействия перемещению микробусин в ячейки 13. Первый растворитель 20, содержащий микробусины 21 и 21', вводят в область 14, включающую ячейки 13 на этапе введения микробусин, после чего прилагают внешнее магнитное поле к микробусинам 21 и 21' до или после введения второго растворителя 30 на первый растворитель 20 на этом этапе. Это может содействовать перемещению микробусин 21 и 21' в ячейки 13 посредством силы, направленной в ячейки 13 и действующей на микробусины 21 и 21'. Приложение магнитного поля может быть осуществлено, например, посредством использования магнита рядом с со стороной, противоположной стороне, на которой выполнены ячейки 13 в субстрате 10 (нижняя лицевая сторона пластины 1).
[0046]
Данный вариант осуществления дает возможность получить пластину большой площади с большим числом ячеек. Например, даже с пластиной, включающей один миллион и больше ячеек, можно эффективно герметизировать микробусину 21 или 21' в ячейке, так что любая из микробусин 21 и 21' будет сохранена в каждой из ячеек. Таким образом, в данном варианте осуществления можно детектировать целевые молекулы с высокой чувствительностью, что позволяет детектировать целевые молекулы в такой очень низкой концентрации как приблизительно 10 аМ.
[0047]
[Этап деаэрации]
Область 14, включающая ячейки 13 в субстрате 10, может быть выполнена с открытым вверх пространством, как сказано выше; однако когда область 14 выполнена закрытой, этап деаэрации внутри области 14 может быть выполнен между этапом введения микробусин и этапом сохранения микробусин. Предпочтительно, деаэрацию выполняют, например, способом, позволяющим пластине 1 стоять неподвижно при пониженном давлении. Более конкретно, деаэрацию выполняют, например, способом, позволяющим пластине 1 стоять неподвижно в вакуумном десикаторе при давлении приблизительно 0,1 атм в течение приблизительно 30 секунд.
[0048]
Этап деаэрации не имеет существенного значения для настоящего изобретения. Однако выполнение этапа деаэрации удаляет воздух из ячеек 13, что позволяет эффективно вводить микробусины 21 и 21' в ячейки 13.
[0049]
2. Способ детекции целевой молекулы
Ниже описан способ детекции целевой молекулы согласно настоящему изобретению. Способ детекции целевой молекулы согласно настоящему изобретению включает этап реакции, этап герметизации микробусин и этап определения.
[0050]
Данный вариант осуществления в качестве микробусин использует микробусины, которые специфично захватывают целевые молекулы. Например, каждая из таких микробусин может быть связанной с молекулой для специфичного захвата целевой молекулы. Для способа герметизации микробусин подходящими являются любые микробусины, целевая молекула и молекула для специфичного захвата целевой молекулы из тех, примеры которых приведены выше.
[0051]
Этап реакции - это этап реакции микробусин с целевыми молекулами. Например, реакция между микробусинами и целевыми молекулами может быть осуществлена путем смешивания раствора, содержащего микробусины, с раствором, содержащим целевые молекулы.
[0052]
Этап герметизации микробусин - это этап осуществления вышеизложенного способа герметизации микробусин посредством использования микробусин, которые прореагировали с целевыми молекулами на этапе реакции. А именно, этап герметизации микробусины является этапом, включающим этап введения микробусин и этап сохранения микробусин, или этапом, включающим этап введения микробусин, этап деаэрации и этап сохранения микробусин. Следует сказать, что описания этапа введения микробусин, этапа деаэрации и этапа сохранения микробусин здесь не приведены, поскольку эти этапы могут быть выполнены так, как сказано выше в разделе "Способ герметизации микробусин".
[0053]
Этап определения - это этап, на котором после этапа герметизации микробусин определяют, содержит ли каждая из ячеек 13 любую одну из микробусин 21', захвативших целевые молекулы.
[0054]
Подходящими примерами способа определения, содержит ли каждая из ячеек 13 любую одну из микробусин 21', захвативших целевые молекулы, включают известные молекулярные реакции распознавания, такие как реакция антиген-антитело, реакция стрептавидин-биотин или комплементарное связывание нуклеиновых кислот. Например, этим способом может быть способ детекции флуоресцентного материала, высвобождающегося из флуоресцентного субстрата при разложении определенным ферментом, связанным с (i) целевой молекулой или (ii) молекулой, специфично связанной с целевой молекулой. Детекцию флуоресцентного материала выполняют, например, используя способ определения интенсивности флуоресценции каждой ячейки с помощью флуоресцентного микроскопа или датчик изображений.
[0055]
На этапе определения предпочтительно также определить, содержит ли каждая из ячеек 13 любую одну из микробусин 21 или любую одну из микробусин 21'. Определение, содержит ли каждая из ячеек 13 любую одну из микробусин 21 или любую одну из микробусин 21', может быть выполнено, например, путем наблюдения под микроскопом, чтобы определить наличие или отсутствие любой одной из микробусин 21 или любой одной из микробусин 21' в каждой из ячеек 13. Альтернативно, определение наличия или отсутствия любой одной из микробусин 21 или любой одной из микробусин 21' в каждой из ячеек 13 может быть выполнено способом детекции света, рассеиваемого микробусинами, или способом измерения электрического потенциала с помощью полевого транзистора (FET).
[0056]
После этапа определения на основании (i) числа ячеек 13, содержащих микробусины 21 или микробусины 21', и (ii) числа ячеек 13, содержащих микробусины 21', захвативших целевые молекулы, можно вычислить отношение числа микробусин, захвативших целевые молекулы, к общему числу микробусин. Таким образом можно количественно определить концентрацию целевых молекул.
[0057]
Согласно данному варианту осуществления, можно получить пластину большой площади, включающую большое число ячеек; кроме того, даже с пластиной, включающей один миллион или больше ячеек, можно эффективно герметизировать микробусины 21 или 21' в каждой из ячеек. Таким образом в данном варианте осуществления можно детектировать целевые молекулы с высокой чувствительностью, что позволяет детектировать целевые молекулы в такой низкой концентрации как приблизительно 10 аМ.
[0058]
3. Пластина
Далее описана конфигурация пластины 1 со ссылкой на Фиг. 1.
[0059]
В пластине 1 субстрат 10 включает пластинчатый элемент 11 и боковую стенку 12, имеющую гидрофобную верхнюю поверхность. Субстрат 10 включает множество ячеек 13, которые отделены одна от другой боковой стенкой 12.
[0060]
Предпочтительно, пластинчатый элемент 11 имеет гидрофильную поверхность. Термин "гидрофильная поверхность" относится к поверхности, аффинность которой к гидрофильному растворителю выше чем аффинность к гидрофобному растворителю. Пластинчатый элемент 11 должен быть выполнен только из твердого материала. Например, пластинчатый элемент 11 может быть изготовлен из стекла, кремния или полимерной смолы.
[0061]
Боковая стенка 12 выполнена на поверхности, предпочтительно на гидрофильной поверхности, пластинчатого элемента 11 и разделяет множество ячеек 13. Боковая стенка 12 имеет гидрофобную верхнюю поверхность. Термин "гидрофобная" здесь используется как синоним термина "липофильная" и обозначает тип, аффинность которого к гидрофобному растворителю выше чем аффинность к гидрофильному растворителю.
[0062]
Следует сказать, что верхняя поверхность боковой стенки 12 предпочтительно гидрофобная и ее боковая поверхность, т.е., внутренняя стенка каждой из ячеек 13, может быть или гидрофобной или гидрофильной.
[0063]
Например, боковая стенка 12 может быть изготовлена из гидрофильной структуры и гидрофобного слоя, который нанесен на ее верхнюю поверхность. Гидрофильная структура может быть изготовлена, например, из стекла, кремния или полимерной смолы. Гидрофобный слой может быть выполнен, например, из водоотталкивающей смолы или фторуглеродной полимерной смолы. Примеры фторуглеродной полимерной смолы включают аморфную фторуглеродную смолу. Предпочтительно использовать аморфную фторуглеродную смолу, поскольку она имеет высокое гидрофобное свойство и низкую токсичность для биологической пробы.
[0064]
В качестве второго растворителя 30 предпочтительно использовать растворитель имеющий аффинность к гидрофобному слою, формирующему верхнюю поверхность боковой стенки 12, в степени нерастворения гидрофобного слоя. Пониженная аффинность второго растворителя 30 к гидрофобному слою может препятствовать замещению слоев с первым растворителем 20. Чрезмерно высокая аффинность второго растворителя 30 к гидрофобному слою может привести к растворению гидрофобного слоя и не позволить сохранить форму боковой стенки 12. С этой точки зрения в качестве второго растворителя 30 предпочтительно использовать полимер, имеющий структуру перфторуглерода (Fluorinert FC-40, Fluorinert FC-43 и т.д.), если верхняя поверхность боковой стенки 12 выполнена из фторуглеродной полимерной смолы.
[0065]
Предпочтительные примеры аморфной фторуглеродной смолы включают по меньшей мере одну, выбираемую из CYTOP (зарегистрированный товарный знак), TEFLON (зарегистрированный товарный знак) AF2400, и TEFLON (зарегистрированный товарный знак) AF1600, Из них CYTOP (зарегистрированный товарный знак) наиболее предпочтителен, поскольку из него легче изготавливать микроскопические изделия.
[0066]
Альтернативно боковая стенка 12 может быть изготовлена из гидрофобного материала. Например, боковая стенка 12 может быть изготовлена из углеродной полимерной смолы или параксиленовой полимерной смолы. Примеры фторуглеродной полимерной смолы включают аморфную фторуглеродную смолу. В качестве аморфной фторуглеродной смолы предпочтительно использовать любую из упомянутых выше.
[0067]
Боковая стенка 12 должна иметь такую конфигурацию, чтобы множество ячеек 13 могли быть выполнена на пластинчатом элементе 11. Например, боковая стенка 12 может быть пластинчатой структурой, части которой, соответствующие ячейкам 13, представляют собой отверстия.
[0068]
Высота боковой стенки 12, измеренная от поверхности пластинчатого элемента 11 (т.е., толщина в вертикальном направлении) должна быть такой, чтобы ни одна из микробусин 21 и 21' после сохранения в ячейках 13 не была удалена из ячеек 13 на этапе сохранения микробусин. Например, высота боковой стенки 12 может быть такой, чтобы большая часть, предпочтительно вся часть, одной из микробусин 21 и 21', сохраненной в одной из ячеек 13, была расположена ниже верхней поверхности боковой стенки 12.
[0069]
Для того, чтобы эффективно хранить микробусины 21 и 21' в ячейках 13, высота боковой стенки 12 предпочтительно равна или больше среднего диаметра микробусин 21 и 21'. Кроме того, для того, чтобы хранить только одну из микробусин 21 и 21' в одной из ячеек 13, высота боковой стенки 12 предпочтительно равна или меньше чем 1,5 среднего диаметра микробусин 21 и 21'.
[0070]
Каждая из множества ячеек 13 представляет собой выемку, способную хранить только одну из микробусин 21 и 21', и множество ячеек 13 отделены одна от другой боковой стенкой 12. Каждая из ячеек 13 имеет нижнюю поверхность, которая является частью поверхности пластинчатого элемента 11, и нижняя поверхность гидрофильная.
[0071]
Ячейки 13 могут иметь любую форму и размер, если форма или размер позволяет каждой из ячеек 13 хранить только одну из микробусин 21 и 21'. Область, окруженная нижней поверхностью и боковой поверхностью каждой из ячеек 13, может иметь форму, например, круглой, цилиндрической или прямоугольной колонки.
[0072]
Ширина "w" каждой из ячеек 13 в горизонтальном направлении (например, в случае, когда поперечное сечение каждой ячейки 13, если смотреть в горизонтальном направлении, имеет форму круга, и ширина "w" является диаметром этого круга; в случае, когда поперечное сечение каждой ячейки 13, если смотреть в горизонтальном направлении, имеет форму квадрата, ширина "w" является длиной одной стороны этого квадрата) должна быть больше среднего диаметра микробусин 21 и 21'. Предпочтительно, ширина "w", например, в 1-2 раза больше чем средний диаметр 21 и 21'. В данном варианте осуществления каждая из ячеек 13 имеет глубину, равную высоте боковой стенки 12. Для того, чтобы эффективно хранить микробусины в ячейках, глубина каждой из ячеек в настоящем изобретении предпочтительно равна или больше чем средний диаметр микробусин. Кроме того, для того, чтобы хранить только одну микробусину в одной из ячеек, глубина каждой из ячеек в настоящем изобретении предпочтительно равна или в 1,5 раза меньше среднего диаметра микробусин.
[0073]
Способы изготовления пластины 1, такие как фотолитография, травление и ламинирование субстрата, такие же как способы изготовления микрочипов и пластин общего назначения.
[0074]
Согласно данному варианту осуществления, каждая из ячеек 13 имеет гидрофильную нижнюю поверхность, и боковая стенка 12 имеет гидрофобную верхнюю поверхность. Таким образом, первый растворитель 20, содержащий микробусины 21 и 21', может быть эффективно введен в ячейки 13, когда гидрофильный первый растворитель 20 используют на этапе введения микробусин. Помимо этого, поскольку можно предотвратить попадание гидрофобного второго растворителя 30, используемого на этапе сохранения микробусин, в ячейки 13, гидрофильный первый растворитель 20 в ячейках 13 может быть покрыт и герметизирован гидрофобным вторым растворителем 30, образовав капли (капли жидкости).
[0075]
Пластина 1 в данном варианте осуществления может быть, например, пластиной, включающей один миллион и больше ячеек. Даже с пластиной, имеющей такую большую площадь, использование способа герметизации микробусины данного варианта осуществления или способа детекции целевой молекулы данного варианта осуществления дает возможность эффективно герметизировать микробусины в ячейках, чтобы хранить одну из микробусин в каждой из ячеек. Таким образом, согласно данному варианту осуществления, можно детектировать целевые молекулы с высокой чувствительностью, что позволяет получить пластину, позволяющую детектировать целевые молекул в такой очень низкой концентрации как приблизительно 10 аМ.
[0076]
4. Набор
Пластина 1 и микробусины 21 могут быть представлены в форме набора. Каждая из ячеек 13 в пластине 1 способна хранить только одну из микробусин 21, включенных в этот набор.
[0077]
Каждая из микробусин 21, включенных в этот набор, может быть микробусиной, специфично захватывающей целевую молекулу. Например, каждая из микробусин 21, включенных в этот набор, может быть микробусиной, связанной с молекулой для специфичного связывания с целевой молекулой. Для использования в качестве целевой молекулы и молекулы для специфичного связывания с целевой молекулой может подходить любая из упомянутых выше.
[0078]
Этот набор может также включать вещество для специфичной детекции целевой молекулы. Веществом, предпочтительно используемым для специфичной детекции целевой молекулы может быть любое из упомянутых выше. Кроме того, набор может также включать, например, первый растворитель и второй растворитель.
[0079]
5. Устройство для детекции целевой молекулы
Далее будет описано устройство 50 для детекции целевой молекулы настоящего изобретения со ссылкой на Фиг. 2. На Фиг. 2 схематически показан один вариант осуществления устройства для детекции целевой молекулы согласно настоящему изобретению.
[0080]
Устройство 50 для детекции целевой молекулы согласно данному варианту осуществления включает пластину 1, датчик изображений 51 и источник света 52. Здесь пластина 1 показана как пластина с множеством лунок. Каждая лунка многолуночной пластины соответствует области 14 с Фиг. 1. Состав пластины 1 соответствует описанному выше, и поэтому описание пластины 1 здесь приведено не будет.
[0081]
Датчиком изображений 51 является датчик для детекции света, излучаемого каждой из ячеек 13, когда в них хранятся микробусины, захватившие целевые молекулы. Например, датчиком изображений 51 может быть датчик для детекции флуоресценции, излучаемой флуоресцентным субстратом при разложении определенным ферментом, связанным с (i) целевой молекулой или (ii) молекулой, специфично связанной с целевой молекулой. Подходящим датчиком изображений 51 может быть, например, КМОП-датчик изображений.
[0082]
Источником света 52 является источник света для излучения света на пластину 1. На Фиг. 2 источник света 52 расположен над пластиной 1. Однако настоящее изобретение конкретно этим не ограничено. Альтернативно, источником света 52 может быть источник, излучающий свет, например, на боковую сторону пластины 1.
[0083]
Между пластиной 1 и датчиком изображений 51 могут быть расположены, например, интерференционный светофильтр и/или светопроводящая матрица. Также, между источником света 52 и пластиной 1 может быть расположен, например, фильтр возбуждения.
[0084]
Согласно данному варианту осуществления, пластина 1 и датчик изображений 51 непосредственно соединены друг с другом. Это дает возможность легко определить без использования другого устройства, такого как микроскоп, хранится ли любая одна из микробусин, захвативших целевые молекулы, в каждой из ячеек 13. Это позволяет легко и с большой скоростью детектировать, хранится ли любая одна из микробусин, захвативших целевые молекулы в каждой из ячеек 13, и получить устройство для детекции целевой молекулы по приемлемой цене.
[0085]
6. Пример применения способа герметизации вещества согласно настоящему изобретению
В способе герметизации вещества согласно настоящему изобретению веществом, герметизируемым в ячейках, выполненных на субстрате, могут быть микробусины, нуклеиновая кислота, белок, вирус, клетки, липидный мембранный комплекс и т.д. В описанном выше варианте осуществления способ описан для микробусин в качестве примера.
[0086]
Согласно настоящему изобретению, нуклеиновая кислота включает ДНК и РНК. Белок и вирус включают их полимеры (олигомеры) и их комплексы с другими веществами. Клетки включают, в частности, бактериальные клетки, и липидный мембранный комплекс включает, в частности, липосому и экзосому, а также другую клеточную органеллу, такую как митохондрия.
[0087]
Когда предметом герметизации является нуклеиновая кислота, белок, вирус, клетки, липидный мембранный комплекс и т.д., способ герметизации вещества согласно настоящему изобретению можно использовать в таких применениях как ИФА-ПЦР.
[ПРОМЫШЛЕННАЯ ПРИМЕНИМОСТЬ]
[0088]
Настоящее изобретение подходит для применения как способ детекции целевых молекул в низкой концентрации, как пластина для этого и устройство для этого и т.д.
[ПЕРЕЧЕНЬ ССЫЛОЧНЫХ СИМВОЛОВ]
[0089]
1: Пластина
10: Субстрат
11: Пластинчатый элемент
12: Боковая стенка
13: Ячейка
14: Область
20: Первый растворитель
21, 21': Микробусины
30: Второй растворитель