Результат интеллектуальной деятельности: ВОДНЫЕ КОМПОЗИЦИИ АНАЛОГОВ LHRH С ЗАМЕДЛЕННЫМ ВЫСВОБОЖДЕНИЕМ
Вид РИД
Изобретение
Настоящее изобретение относится к водной фармацевтической композиции аналога LHRH для замедленного высвобождения, в частности, для замедленного высвобождения, совместимого с терапевтическим воздействием в течение, по меньшей мере, 2 недель.
Гормон, высвобождающий лютеинизирующий гормон, известный как LHRH или GnRH, представляет собой декапептид, имеющий следующую формулу: (pyro)Glu-His-Trp-Ser-Tyr-Gly-Leu-Arg-Pro-Gly-NH2.
LHRH высвобождается из гипоталамуса и связывается с рецептором гипофиза, вызывая высвобождение LH (лютеинизирующего гормона) и FSH (фолликулостимулирующего гормона). Затем LH и FSH действуют на гонады, стимулируя синтез стероидных половых гормонов. Пульсирующее высвобождение LHRH и обусловленное им высвобождение LH и FSH участвует в регуляции репродуктивного цикла у домашних животных и людей. Острые дозы агонистов LHRH повышают уровни LH и стероидных половых гормонов как у животных, так и у людей. Парадоксально, что хронические дозы указанных агонистов уменьшают уровни LH и стероидных гормонов. Следовательно, введение нескольких доз агонистов LHRH приводит к подавлению образования эстрогена у женщин и к подавлению образования тестостерона у мужчин. Такой же эффект наблюдается у животных и людей после введения острых или хронических доз антагонистов LHRH. Агонисты LHRH находятся на стадии клинических исследований, или используются для лечения нескольких гормонозависимых заболеваний, таких как рак простаты, гипертрофия простаты, эндометриоз, миома матки, преждевременное половое созревание и рак молочной железы. Они также используются в качестве противозачаточных средств. Обзор по аналогам LHRH можно найти в J. Sandow, et al. in "Hypothalamic Hormones. Chemistry, Physiology и Clinical Applications", edited by D. Gupta and W. Voeters, p. 307 (1978).
Лечение аналогами LHRH требует непрерывного и/или многократного введения пациенту лекарственного средства в течение продолжительного периода времени. Поскольку многократные инъекции вызывают у пациента ощущение неудобства и дискомфорта, желательно использовать препараты с замедленным высвобождением.
Как правило, высвобождения активного ингредиента достигают путем применения биологически совместимого и/или биоразлагаемого (со)полимера, такого как PLGA, в который заключена композиция, находящаяся в виде микроимплантата или микрочастиц в соответствующих наполнителях.
Настоящее изобретение относится к водной композиции аналога LHRH с замедленным высвобождением, которая имеет простой состав, в частности, не содержит каких-либо (со)полимеров или наполнителей, являющихся неводорастворимыми, биосовместимыми и/или биоразрушаемыми, и которую можно вводить с помощью классической иглы, такой как инсулиновая игла.
Таким образом, предметом настоящего изобретения является водная фармацевтическая композиция для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, которая содержит:
- аналог LHRH в качестве активного ингредиента,
- соль, и
- воду.
Если не указано иначе, в приведенном ниже описании границы диапазона значений включаются в указанный диапазон, особенно в выражении "варьирующий от".
Если не указано иначе, нижеследующие определения приведены для иллюстрации и указания значения и объема разных терминов, используемых для описания настоящего изобретения.
Термин "соль" в данном описании относится к моновалентной или поливалентной, органической или неорганической, анионной или катионной соли.
Термин "буфер" в данном описании относится к раствору, содержащему ионизируемое соединение, которое за счет изменения своего pH стабилизирует pH композиции в конкретном диапазоне. Как правило, буфер содержит либо слабую кислоту или ее соли, либо слабое основание или его соли, которые являются устойчивыми к изменениям pH.
Термин "способность проходить через иглу", которую можно определить путем измерения усилия, прикладываемого при инъекции, относится к пригодности композиции для парентерального введения с помощью устройства для инъекции, такого как шприц или инъектор.
Термин "стабилизатор" в данном описании относится к фармацевтически приемлемому соединению, способному предотвращать деградацию и увеличивать физическую или химическую стабильность активного вещества (например, к соединению, обладающему антиоксидантными свойствами, или к поверхностно-активным веществам).
Термин "поверхностно-активное вещество" в данном описании относится к соединению или наполнителю, обладающему поверхностно-активными свойствами. При применении в композициях настоящего изобретения поверхностно-активное вещество может повышать растворимость активного ингредиента в воде, обеспечивать защиту активного вещества от деградации и/или ограничивать осаждение активного ингредиента.
Термин "антиоксидант" в данном описании относится к соединению, обладающему антиоксидантными свойствами. При применении в композициях настоящего изобретения антиоксидант может ингибировать или предотвращать окислительную деградацию активного ингредиента и/или ингибировать или предотвращать окислительную деградацию наполнителей.
Термин "(со)полимер" обозначает полимер или сополимер, или их смесь.
Термин "не являющийся водорастворимым" относится к веществу, которое не растворяется в воде. Предпочтительно "не являющийся водорастворимым" (со)полимер или наполнитель имеет растворимость в воде, которая при 25°C составляет менее 1 мг/мл, предпочтительно менее 0,1 мг/мл.
Термин "биосовместимый" относится к веществу, которое является биологически совместимым, то есть, не вызывает значимые с медицинской точки зрения токсические, вредные или иммунологические ответы в живых тканях, биологических системах, или со стороны биологических функций.
Термин "биоразрушаемый" относится к веществу, которое может разрушаться под действием биологических агентов, биологических (микро)организмов, или при помещении в биологические жидкости.
Термин "в основном" при применении в выражении "композиция, в основном состоящая из" означает, что любые другие компоненты включают в себя только минорные примеси, содержание каждого из которых составляет менее 2, предпочтительно менее 1, более предпочтительно менее 0,5, 0,25% по отношению к общей массе композиции, а в совокупности их содержание составляет менее 3, 2, 1, 0,5% по отношению к общей массе композиции.
В предпочтительном варианте осуществления выражение "композиция, в основном состоящая из" означает, что любые другие компоненты включают в себя только минорные примеси, содержание каждого из которых составляет менее 2% по отношению к общей массе композиции, а в совокупности их содержание составляет менее 3% по отношению к общей массе композиции. В другом предпочтительном варианте осуществления выражение "композиция, в основном состоящая из" означает, что любые другие компоненты включают в себя только минорные примеси, содержание каждого из которых составляет менее 1% по отношению к общей массе композиции, а в совокупности их содержание составляет менее 2% по отношению к общей массе композиции. В более предпочтительном варианте осуществления выражение "композиция, в основном состоящая из" означает, что любые другие компоненты включают в себя только минорные примеси, содержание каждого из которых составляет менее 0,5% по отношению к общей массе композиции, а в совокупности их содержание составляет менее 1% по отношению к общей массе композиции. В другом более предпочтительном варианте осуществления выражение "композиция, в основном состоящая из" означает, что любые другие компоненты включают в себя только минорные примеси, содержание каждого из которых составляет менее 0,25% по отношению к общей массе композиции, а в совокупности их содержание составляет менее 0,5% по отношению к общей массе композиции. Если не указано иначе, все процентные значения, приведенные в настоящем изобретении, выражены в виде массовых (масс/масс) долей.
Аналог LHRH может быть выбран из группы, включающей в себя трипторелин, деслорелин, нафарелин, гистрелин, бусерелин, госерелин, гонадорелин и лейпрорелин, или их фармацевтически приемлемые соли. Активный ингредиент может находиться в виде соли или свободного основания.
Предпочтительно аналог LHRH представляет собой трипторелин или его фармацевтически приемлемую соль.
Водная фармацевтическая композиция настоящего изобретения в основном содержит активный ингредиент, или любые его фармацевтически приемлемые соли, соль и воду. Предпочтительно активный ингредиент, или его фармацевтически приемлемые соли, соль и вода составляют, по меньшей мере, 95% по массе по отношению к общей массе композиции, более предпочтительно, по меньшей мере, 97%.
Другим предметом настоящего изобретения является водная фармацевтическая композиция для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, которая содержит
- в качестве активного ингредиента аналог LHRH, выбранный из трипторелина, деслорелина, нафарелина, гистрелина, бусерелина, госерелина, гонадорелина и лейпрорелина, или любой их фармацевтически приемлемой соли,
- соль, и
- воду,
где активный ингредиент, или любые его фармацевтически приемлемые соли, соль и вода составляют, по меньшей мере, 95% по массе по отношению к общей массе композиции.
Предпочтительно водная фармацевтическая композиция для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, содержит:
- в качестве активного ингредиента трипторелин или любую его фармацевтически приемлемую соль,
- соль, и
- воду,
где активный ингредиент, или любые его фармацевтически приемлемые соли, соль и вода составляют, по меньшей мере, 95% по массе по отношению к общей массе композиции.
Соли аналога LHRH, подходящие для применения в настоящем изобретении, предпочтительно представляют собой фармацевтически приемлемые соли органических кислот, такие как соли уксусной, фенилуксусной, молочной, яблочной, памоевой, аскорбиновой, янтарной или бензойной кислот, или фармацевтически приемлемые соли неорганических кислот, такие как соли хлористоводородной, серной или фосфорной кислот.
В соответствии с одним предпочтительным вариантом осуществления аналог LHRH находится в форме соли.
Другим предметом настоящего изобретения является водная фармацевтическая композиция для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, которая содержит:
- в качестве активного ингредиента фармацевтически приемлемую соль аналога LHRH, выбранного из трипторелина, деслорелина, нафарелина, гистрелина, бусерелина, госерелина, гонадорелина и лейпрорелина,
- соль, и
- воду,
где фармацевтически приемлемая соль активного ингредиента, соль и вода составляют, по меньшей мере, 95% по массе по отношению к общей массе композиции.
В предпочтительном варианте осуществления аналог LHRH находится в форме фармацевтически приемлемой соли, выбранной из солей уксусной, фенилуксусной, молочной, яблочной, памоевой, аскорбиновой, янтарной, бензойной, серной и фосфорной кислот.
Предпочтительно аналог LHRH находится в форме памоата, ацетата или фосфата, более предпочтительно, в виде ацетата.
В предпочтительном варианте осуществления настоящего изобретения аналог LHRH представляет собой трипторелин, а его фармацевтически приемлемая соль представляет собой памоат, ацетат или фосфат, предпочтительно ацетат.
Другим предметом настоящего изобретения является водная фармацевтическая композиция для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, которая содержит
- в качестве активного ингредиента фармацевтически приемлемую памоатную, ацетатную или фосфатную соль аналога LHRH, выбранного из трипторелина,
- соль, и
- воду,
где активный ингредиент, или его фармацевтически приемлемая соль, соль и вода составляют, по меньшей мере, 95% по массе по отношению к общей массе композиции.
В соответствии с другим предпочтительным вариантом осуществления трипторелин представляет собой свободное основание.
Независимо от того, в каком виде находится аналог LHRH, т.е. в виде соли, или в виде свободного основания, в настоящем изобретении количество аналога LHRH, выраженное, например, в виде концентрации или процента, относится к аналогу LHRH, находящемуся в виде свободного основания.
Предпочтительно аналог LHRH присутствует в концентрации, варьирующей от 1 до 30% по массе, предпочтительно от 1 до 25% по массе, и более предпочтительно от 1,5 до 22% по массе по отношению к общей массе композиции.
Предпочтительно аналог LHRH представляет собой трипторелин и присутствует в концентрации, варьирующей от 1 до 30% по массе, предпочтительно от 1 до 25% по массе, и более предпочтительно от 1,5 до 22% по массе по отношению к общей массе композиции.
Другим предметом настоящего изобретения является водная фармацевтическая композиция для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, которая содержит:
- в качестве активного ингредиента аналог LHRH, выбранный из трипторелина, деслорелина, нафарелина, гистрелина, бусерелина, госерелина, гонадорелина и лейпрорелина, или любых их фармацевтически приемлемых солей,
- соль, и
- воду,
где активный ингредиент, или любая его фармацевтически приемлемая соль, соль и вода составляют, по меньшей мере, 95% по массе по отношению к общей массе композиции, а
аналог LHRH присутствует в концентрации, варьирующей от 1 до 30% по массе по отношению к общей массе композиции.
Предпочтительно водная фармацевтическая композиция для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, содержит:
- в качестве активного ингредиента трипторелин или любую его фармацевтически приемлемую соль,
- соль, и
- воду,
где активный ингредиент, или любые его фармацевтически приемлемые соли, соль и вода составляют, по меньшей мере, 95% по массе по отношению к общей массе композиции, а
аналог LHRH присутствует в концентрации, варьирующей от 1 до 30% по массе по отношению к общей массе композиции.
Композиция настоящего изобретения содержит соль. Соль может быть выбрана из группы, включающей в себя фосфаты, сульфаты, цитраты, ацетаты, сукцинаты, карбонаты или хлориды. Если соль представляет собой сульфат, она может быть выбрана из сульфата натрия или сульфата аммония.
В предпочтительном варианте осуществления соль выбрана из группы, включающей в себя фосфаты, сульфаты, цитраты, ацетаты, сукцинаты, карбонаты или хлориды.
Предпочтительно соль выбрана из фосфата или сульфата.
Другим предметом настоящего изобретения является водная фармацевтическая композиция для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, которая содержит:
- в качестве активного ингредиента аналог LHRH, выбранный из трипторелина, деслорелина, нафарелина, гистрелина, бусерелина, госерелина, гонадорелина и лейпрорелина, или любых их фармацевтически приемлемых солей,
- соль, выбранную из фосфатов, сульфатов, цитратов, ацетатов, сукцинатов, карбонатов и хлоридов, и
- воду,
где активный ингредиент, или любые его фармацевтически приемлемые соли, соль и вода составляют, по меньшей мере, 95% по массе по отношению к общей массе композиции,
и предпочтительно
- в качестве активного ингредиента аналог LHRH, выбранный из трипторелина, деслорелина, нафарелина, гистрелина, бусерелина, госерелина, гонадорелина и лейпрорелина, или любых их фармацевтически приемлемых солей,
- соль, выбранную из фосфатов и сульфатов, и
- воду,
где активный ингредиент, или любые его фармацевтически приемлемые соли, соль и вода составляют, по меньшей мере, 95% по массе по отношению к общей массе композиции.
Другим предметом настоящего изобретения является водная фармацевтическая композиция для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, где указанная композиция содержит:
- в качестве активного ингредиента трипторелин или любую его фармацевтически приемлемую соль,
- соль, выбранную из фосфатов, сульфатов, цитратов, ацетатов, сукцинатов, карбонатов и хлоридов, и
- воду,
где активный ингредиент, или любые его фармацевтически приемлемые соли, соль и вода составляют, по меньшей мере, 95% по массе по отношению к общей массе композиции,
и предпочтительно
- в качестве активного ингредиента трипторелин или любая его фармацевтически приемлемую соль,
- соль, выбранную из фосфатов и сульфатов, и
- воду,
где активный ингредиент, или любые его фармацевтически приемлемые соли, соль и вода составляют, по меньшей мере, 95% по массе по отношению к общей массе композиции.
В одном варианте осуществления настоящего изобретения соль представляет собой сульфат.
В другом предпочтительном варианте осуществления соль представляет собой сульфат, выбранный из сульфата натрия и сульфата аммония. Предпочтительно сульфат представляет собой сульфат натрия.
В другом варианте осуществления настоящего изобретения соль представляет собой фосфат.
В конкретном случае фосфатная соль может представлять собой фосфатный буфер. Фосфатный буфер можно получить путем растворения дигидрата дигидрофосфата натрия в воде и доведения pH до 7,5 гидроксидом натрия.
Предпочтительно фосфатная соль представляет собой фосфатный буфер.
В предпочтительном варианте осуществления настоящее изобретение предлагает водную фармацевтическую композицию для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, которая содержит:
- трипторелин в качестве активного ингредиента,
- соль, и
- воду,
причем трипторелин присутствует в концентрации, варьирующей от 1 до 30% по массе по отношению к общей массе композиции.
Другим предметом настоящего изобретения является водная фармацевтическая композиция для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, которая содержит:
- в качестве активного ингредиента аналог LHRH, выбранный из трипторелина, деслорелина, нафарелина, гистрелина, бусерелина, госерелина, гонадорелина и лейпрорелина, или любых их фармацевтически приемлемых солей,
- соль, выбранную из фосфатов, сульфатов, цитратов, ацетатов, сукцинатов, карбонатов и хлоридов, и
- воду,
где активный ингредиент, или любые его фармацевтически приемлемые соли, соль и вода составляютт, по меньшей мере, 97% по массе по отношению к общей массе композиции, а
аналог LHRH присутствует в концентрации, варьирующей от 1 до 30% по массе по отношению к общей массе композиции.
Предпочтительно водная фармацевтическая композиция для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, содержит:
- в качестве активного ингредиента аналог LHRH, выбранный из трипторелина, деслорелина, нафарелина, гистрелина, бусерелина, госерелина, гонадорелина и лейпрорелина, или любых их фармацевтически приемлемых солей,
- соль, выбранную из фосфатов и сульфатов, и
- воду,
где активный ингредиент, или любые его фармацевтически приемлемые соли, соль и вода составляют, по меньшей мере, 97% по массе по отношению к общей массе композиции, а
аналог LHRH присутствует в концентрации, варьирующей от 1 до 30% по массе по отношению к общей массе композиции.
Другим предметом настоящего изобретения является водная фармацевтическая композиция для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, которая содержит:
- в качестве активного ингредиента трипторелин или любую его фармацевтически приемлемую соль,
- соль, выбранную из фосфатов, сульфатов, цитратов, ацетатов, сукцинатов, карбонатов и хлоридов, и
- воду,
где активный ингредиент, или любые его фармацевтически приемлемые соли, соль и вода составляют, по меньшей мере, 97% по массе по отношению к общей массе композиции, а
аналог LHRH присутствует в концентрации, варьирующей от 1 до 22% по массе по отношению к общей массе композиции.
Предпочтительно водная фармацевтическая композиция для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, содержит:
- в качестве активного ингредиента трипторелин или любую его фармацевтически приемлемую соль,
- соль, выбранную из фосфатов и сульфатов, и
- воду,
где активный ингредиент, или любые его фармацевтически приемлемые соли, соль и вода составляют, по меньшей мере, 97% по массе по отношению к общей массе композиции, а
аналог LHRH присутствует в концентрации, варьирующей от 1 до 22% по массе по отношению к общей массе композиции.
В конкретном предпочтительном варианте осуществления pH конечной композиции варьирует от 4 до 9.
В другом варианте осуществления соль представляет собой сульфат, предпочтительно сульфат аммония. Предпочтительно соль представляет собой сульфат аммония, а pH раствора сульфата аммония варьирует от 4 до 8, более предпочтительно от 5 до 8.
В предпочтительном варианте осуществления соль представляет собой сульфат, предпочтительно сульфат натрия. Предпочтительно соль представляет собой сульфат натрия, а pH раствора сульфата натрия варьирует от 4 до 8, более предпочтительно от 4 до 7.
В другом предпочтительном варианте осуществления соль представляет собой фосфат. Предпочтительно соль представляет собой фосфат, а pH раствора фосфатной соли варьирует от 4 до 8, более предпочтительно от 6 до 8.
В предпочтительном варианте осуществления настоящего изобретения молярное отношение соли к аналогу LHRH варьирует примерно от 0,1:1 (что соответствует 0,1±0,01) до 2:1 (что соответствует 2±0,2).
Другим предметом настоящего изобретения является водная фармацевтическая композиция для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, которая содержит:
- в качестве активного ингредиента фармацевтически приемлемую соль аналога LHRH, выбранного из трипторелина, деслорелина, нафарелина, гистрелина, бусерелина, госерелина, гонадорелина и лейпрорелина,
- соль, выбранную из фосфатов, сульфатов, цитратов, ацетатов, сукцинатов, карбонатов и хлоридов, и
- воду,
где активный ингредиент, или любые его фармацевтически приемлемые соли, соль и вода составляют, по меньшей мере, 97% по массе по отношению к общей массе композиции, а
молярное отношение соли к аналогу LHRH варьирует примерно от 0,1:1 до 2:1.
Другим предметом настоящего изобретения является водная фармацевтическая композиция для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, которая содержит:
- в качестве активного ингредиента фармацевтически приемлемую соль аналога LHRH, выбранного из трипторелина, деслорелина, нафарелина, гистрелина, бусерелина, госерелина, гонадорелина и лейпрорелина,
- соль, выбранную из фосфатов и сульфатов, и
- воду,
где активный ингредиент, или любые его фармацевтически приемлемые соли, соль и вода составляют, по меньшей мере, 97% по массе по отношению к общей массе композиции, а
молярное отношение соли к аналогу LHRH варьирует примерно от 0,1:1 до 2:1.
Другим предметом настоящего изобретения является водная фармацевтическая композиция для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, которая содержит:
- в качестве активного ингредиента трипторелин или любую его фармацевтически приемлемую соль,
- соль, выбранную из фосфатов, сульфатов, цитратов, ацетатов, сукцинатов, карбонатов и хлоридов, и
- воду,
где активный ингредиент, или любые его фармацевтически приемлемые соли, соль и вода составляют, по меньшей мере, 97% по массе по отношению к общей массе композиции, а
молярное отношение соли к аналогу LHRH варьирует примерно от 0,1:1 до 2:1.
В более предпочтительном варианте осуществления настоящего изобретения активный ингредиент представляет собой трипторелин или его фармацевтически приемлемую соль, соль представляет собой фосфат, а молярное отношение фосфата к трипторелину варьирует примерно от 0,1:1 (что соответствует 0,1±0,01) до 2:1 (что соответствует 2±0,2).
Предпочтительно молярное отношение фосфата к трипторелину варьирует примерно от 0,15:1 (что соответствует 0,15±0,015) до 1,5:1 (что соответствует 1,5±0,15).
Одним из предметов настоящего изобретения является водная фармацевтическая композиция для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, которая содержит:
- от 1 до 30% (масс/масс) трипторелина в качестве активного ингредиента,
- фосфатную соль, и
- воду,
где молярное отношение фосфата к трипторелину варьирует примерно от 0,1:1 (0,1±0,01) до 2:1 (2±0,2), предпочтительно примерно от 0,15:1 (0,15±0,015) до 1,5:1 (1,5±0,15).
Предпочтительно водная фармацевтическая композиция для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, содержит:
- в качестве активного ингредиента трипторелин или любую его фармацевтически приемлемую соль,
- соль, выбранную из фосфатов, и
- воду,
где активный ингредиент, или любые его фармацевтически приемлемые соли, соль и вода составляют, по меньшей мере, 97% по массе по отношению к общей массе композиции,
трипторелин присутствует в концентрации, варьирующей от 1 до 30% по массе по отношению к общей массе композиции, а
молярное отношение фосфата к трипторелину варьирует примерно от 0,15:1 до 1,5:1.
В другом более предпочтительном варианте осуществления настоящего изобретения активный ингредиент представляет собой трипторелин, или его фармацевтически приемлемую соль, соль представляет собой сульфат натрия, а молярное отношение сульфата к трипторелину варьирует примерно от 0,1:1 (что соответствует 0,1±0,01) до 2:1 (что соответствует 2±0,2).
Предпочтительно молярное отношение сульфата к трипторелину варьирует примерно от 0,15:1 (что соответствует 0,15±0,015) до 1,5:1 (что соответствует 1,5±0,15).
Другим предметом настоящего изобретения является водная фармацевтическая композиция для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, которая содержит:
- от 1 до 30% (масс/масс) трипторелина в качестве активного ингредиента,
- сульфат натрия, и
- воду,
где молярное отношение сульфата к трипторелину варьирует примерно от 0,1:1 (0,1±0,01) до 2:1 (2±0,2), предпочтительно примерно от 0,15:1 (0,15±0,015) до 1,5:1 (1,5±0,15).
В другом более предпочтительном варианте осуществления настоящего изобретения активный ингредиент представляет собой трипторелин или его фармацевтически приемлемую соль, соль представляет собой сульфат аммония, а молярное отношение сульфата к трипторелину варьирует примерно от 0,1:1 (0,1±0,01) до 2:1 (2±0,2).
Предпочтительно молярное отношение сульфата к трипторелину варьирует примерно от 0,15:1 (0,15±0,015) до 1,5:1 (1,5±0,15).
Другим предметом настоящего изобретения является водная фармацевтическая композици для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, которая содержит:
- от 1 до 30% (масс/масс) трипторелина в качестве активного ингредиента,
- сульфат аммония, и
- воду,
где молярное отношение сульфаа к трипторелину варьирует примерно от 0,1:1 (0,1±0,01) до 2:1 (2±0,2), предпочтительно примерно от 0,15:1 (0,15±0,015) до 1,5:1 (1,5±0,15).
Предпочтительно водная фармацевтическая композиция для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, содержит:
- в качестве активного ингредиента трипторелин или любую его фармацевтически приемлемую соль,
- соль, выбранную из сульфата натрия или сульфата аммония, и
- воду,
где активный ингредиент, или любые его фармацевтически приемлемые соли, соль и вода составляют, по меньшей мере, 97% по массе по отношению к общей массе композиции,
трипторелин присутствует в концентрации, варьирующей от 1 до 30% по массе по отношению к общей массе композиции, а
молярное отношение фосфата к трипторелину варьирует примерно от 0,15:1 до 1,5:1.
В другом предпочтительном варианте осуществления водная фармацевтическая композиция настоящего изобретения не содержит каких-либо (со)полимеров или наполнителей, или их смесей, которые являются неводорастворимыми, биосовместимыми и/или биоразрушаемыми. Это означает, что содержание являющихся неводорастворимыми, биосовместимыми и/или биоразрушаемыми (со)полимеров или наполнителей в композиции составляет менее 0,1% по массе (масс/масс).
Классический и хорошо известный способ получения фармацевтической композиции с замедленным высвобождением активного фармацевтического ингредиента после введения включает в себя применение биосовместимых (со)полимеров, таких как полилактиды (PLA), полигликолиды (PLG), полилактид-согликолиды (PLGA), полиалкилцианоакрилаты, поликапролактоны, а также любые (со)полимерные средства, полученные путем сочетания или модификации указанных биосовместимых (со)полимеров. Такие (со)полимеры, которые являются неводорастворимыми, образуют биоразрушаемую матрицу из микрочастиц или твердых имплантатов, которая постепенно разрушается после введения в организм.
Другим предметом настоящего изобретения является водная фармацевтическая композиция для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, в которой отсутствуют являющиеся неводорастворимыми, биосовместимыми и/или биоразрушаемыми (со)полимеры, и которая содержит:
- в качестве активного ингредиента аналог LHRH, выбранный из трипторелина, деслорелина, нафарелина, гистрелина, бусерелина, госерелина, гонадорелина и лейпрорелина, или любых их фармацевтически приемлемых солей,
- соль, выбранную из фосфатов, сульфатов, цитратов, ацетатов, сукцинатов, карбонатов и хлоридов, и
- воду,
где активный ингредиент, или любые его фармацевтически приемлемые соли, соль и вода составляют, по меньшей мере, 95% по массе по отношению к общей массе композиции,
и предпочтительно содержит
- в качестве активного ингредиента аналог LHRH, выбранный из трипторелина, деслорелина, нафарелина, гистрелина, бусерелина, госерелина, гонадорелина и лейпрорелина, или любых их фармацевтически приемлемых солей,
- соль, выбранную из фосфатов и сульфатов, и
- воду,
где активный ингредиент, или любые его фармацевтически приемлемые соли, соль и вода составляют, по меньшей мере, 97% по массе по отношению к общей массе композиции.
Другим предметом настоящего изобретения является водная фармацевтическая композиция для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, в которой отсутствуют являющиеся неводорастворимыми, биосовместимыми и/или биоразрушаемыми (со)полимеры, и которая содержит:
- в качестве активного ингредиента аналог LHRH, выбранный из трипторелина, деслорелина, нафарелина, гистрелина, бусерелина, госерелина, гонадорелина и лейпрорелина, или любых их фармацевтически приемлемых солей,
- соль, выбранную из фосфатов, сульфатов, цитратов, ацетатов, сукцинатов, карбонатов и хлоридов, и
- воду,
где активный ингредиент, или любые его фармацевтически приемлемые соли, соль и вода составляют, по меньшей мере, 95% по массе по отношению к общей массе композиции, а
аналог LHRH присутствует в концентрации от 1 до 30% по массе по отношению к общей массе композиции.
В другом предпочтительном варианте осуществления водная фармацевтическая композиция настоящего изобретения для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, в которой отсутствуют водорастворимые, биосовместимые и/или биоразрушаемые (со)полимеры, содержит:
- трипторелин в качестве активного ингредиента,
- соль, и
- воду,
причем трипторелин присутствует в концентрации, варьирующей от 1 до 30% по массе по отношению к общей массе композиции.
Предпочтительно трипторелин присутствует в концентрации, варьирующей от 1 до 25% по массе, более предпочтительно от 1,5 до 22% по массе по отношению к общей массе композиции.
В конкретном варианте осуществления водная фармацевтическая композиция настоящего изобретения, в которой отсутствуют водорастворимые, биосовместимые и/или биоразрушаемые (со)полимеры, содержит:
- от 1 до 30% (масс/масс) трипторелина в качестве активного ингредиента,
- фосфатную соль, и
- воду,
где молярное отношение фосфата к трипторелину варьирует примерно от 0,1:1 (0,1±0,01) до 2:1 (2±0,2).
Предпочтительно молярное отношение фосфата к трипторелину варьирует примерно от 0,15:1 (0,15±0,015) до 1,5:1 (1,5±0,15).
В другом конкретном варианте осуществления водная фармацевтическая композиция настоящего изобретения, в которой отсутствуют водорастворимые, биосовместимые и/или биоразрушаемые (со)полимеры, содержит:
- от 1 до 30% (масс/масс) трипторелина в качестве активного ингредиента,
- сульфат натрия, и
- воду,
где молярное отношение сульфата к трипторелину варьирует примерно от 0,1:1 (0,1±0,01) до 2:1 (2±0,2).
Предпочтительно молярное отношение сульфата к трипторелину варьирует примерно от 0,15:1 (0,15±0,015) до 1,5:1 (1,5±0,15).
Предпочтительно водная фармацевтическая композиция для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, содержит:
- в качестве активного ингредиента трипторелин или любую его фармацевтически приемлемую соль,
- соль, выбранную из фосфатов, и
- воду,
где активный ингредиент, или любые его фармацевтически приемлемые соли, соль и вода составляют, по меньшей мере, 97% по массе по отношению к общей массе композиции,
трипторелин присутствует в концентрации, варьирующей от 1 до 25% по массе по отношению к общей массе композиции, а
молярное отношение фосфата к трипторелину варьирует примерно от 0,15:1 до 1,5:1.
В другом конкретном варианте осуществления водная фармацевтическая композиция настоящего изобретения, в которой отсутствуют водорастворимые, биосовместимые и/или биоразрушаемые (со)полимеры, содержит:
- от 1 до 30% (масс/масс) трипторелина в качестве активного ингредиента,
- сульфат аммония, и
- воду,
где молярное отношение сульфата к трипторелину варьирует примерно от 0,1:1 (0,1±0,01) до 2:1 (2±0,2).
Предпочтительно молярное отношение сульфата к трипторелину варьирует примерно от 0,15:1 (0,15±0,015) до 1,5:1 (1,5±0,15).
Предпочтительно водная фармацевтическая композиция, обеспечивающая замедленное высвобождение активного ингредиента в течение, по меньшей мере, 2 недель, содержит:
- в качестве активного ингредиента трипторелин или любую его фармацевтически приемлемую соль,
- соль, выбранную из сульфатов, и
- воду,
где активный ингредиент, или любые его фармацевтически приемлемые соли, соль и вода составляют, по меньшей мере, 97% по массе по отношению к общей массе композиции,
трипторелин присутствует в концентрации, варьирующей от 1 до 25% по массе по отношению к общей массе композиции, а
молярное отношение сульфата к трипторелину варьирует примерно от 0,15:1 до 1,5:1.
Композиция настоящего изобретения также может содержать другие водорастворимые добавки, традиционно используемые для получения подобных фармацевтических композиций, такие как, например, стабилизаторы, антиоксиданты или поверхностно-активные вещества.
Стабилизаторы или поверхностно-активные вещества могут быть выбраны из группы, включающей в себя ионы металлов, жирные кислоты и их соли, жирные спирты, простые полиоксиэфиры, полоксамеры, полиолы, такие как трегалоза, маннит, сахароза и декстроза, полисорбаты и эфиры полиоксиэтилена и жирных кислот.
Композиция настоящего изобретения может содержать один или несколько ионов поливалентных металлов в качестве стабилизатора.
В конкретном варианте осуществления композиция настоящего изобретения содержит один или несколько ионов поливалентных металлов, предпочтительно один или несколько катионов двухвалентных металлов.
В предпочтительном варианте осуществления ион поливалентного металла выбран из Zn2+, Cu2+, Mg2+, Fe2+ и Ca2+.
Антиоксиданты могут быть выбраны из группы, включающей в себя аминокислоты, такие как метионин, гистидин, триптофан; полиаминокислоты, такие как глутатион; хелатирующие средства, такие как динатрийэдитат и лимонная кислота; аскорбиновую кислоту; метабисульфит натрия; монотиоглицерин; бутилгидрокситолуол (ВНТ); бутилгидроксианизол; и их смеси.
В предпочтительном варианте осуществления водная фармацевтическая композиция настоящего изобретения содержит добавку, выбранную из стабилизаторов, поверхностно-активных веществ, антиоксидантов и их смесей.
В случае присутствия указанных добавок, выбранных из стабилизаторов, антиоксидантов, поверхностно-активных веществ и их смесей, их массовое количество (масс/масс) составляет менее 5,0% от массы фармацевтической композиции, предпочтительно менее 1,0%.
Другим предметом настоящего изобретения является водная фармацевтическая композиция для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, которая состоит из нижеследующих ингредиентов, или в основном содержит:
- в качестве активного ингредиента аналог LHRH, выбранный из трипторелина, деслорелина, нафарелина, гистрелина, бусерелина, госерелина, гонадорелина и лейпрорелина, или любых их фармацевтически приемлемых солей, в концентрации от 1 до 30% по массе по отношению к общей массе композиции,
- соль, выбранную из фосфатов, сульфатов, цитратов, ацетатов, сукцинатов, карбонатов и хлоридов,
- от 0 до 5% добавки, выбранной из стабилизаторов, антиоксидантов, поверхностно-активных веществ и их смесей, и
- воду (до 100%),
предпочтительно указанная композиция состоит из нижеследующих ингредиентов, или в основном содержит
- в качестве активного ингредиента аналог LHRH, выбранный из трипторелина, деслорелина, нафарелина, гистрелина, бусерелина, госерелина, гонадорелина и лейпрорелина, или любых их фармацевтически приемлемых солей, в концентрации от 1 до 30% по массе по отношению к общей массе композиции
- соль, выбранную из фосфатов и сульфатов,
- добавку, выбранную из стабилизаторов, антиоксидантов, поверхностно-активных веществ и их смесей, и
- воду (до 100%).
Другим предметом настоящего изобретения является водная фармацевтическая композиция для замедленного высвобождение активного ингредиента в течение, по меньшей мере, 2 недель, которая состоит из нижеследующих ингредиентов, или в основном содержит:
- в качестве активного ингредиента, трипторелин или любую его фармацевтически приемлемую соль, в концентрации от 1 до 22% по массе по отношению к общей массе композиции,
- соль, выбранную из фосфата, сульфата, цитрата, ацетата, сукцината, карбоната и хлорида,
- от 0 до 5% добавки, выбранной из стабилизаторов, антиоксидантов, поверхностно-активных веществ и их смесей, и
- воду (до 100%),
где pH водной фармацевтической композиции находится в диапазоне от 4 до 8.
Другим предметом настоящего изобретения является водная фармацевтическая композиция для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, которая состоит из нижеследующих ингредиентов, или в основном содержит:
- в качестве активного ингредиента трипторелин или любую его фармацевтически приемлемую соль, в концентрации от 1 до 22% по массе по отношению к общей массе композиции,
- соль, выбранную из сульфатов и фосфатов,
- от 0 до 1% добавки, выбранной из стабилизаторов, антиоксидантов, поверхностно-активных веществ и их смесей, где указанная добавка содержит, по меньшей мере, катион двухвалентного металла, выбранный из Zn2+, Cu2+, Mg2+, Fe2+ и Ca2+,
- воду (до 100%), а
pH водной фармацевтической композиции находится в диапазоне от 6 до 8,
и, более предпочтительно, композиция в основном содержит в качестве активного ингредиента трипторелин или любую его фармацевтически приемлемую соль, выбранную из памоата, ацетата и фосфата.
Другим предметом настоящего изобретения является водная фармацевтическая композиция для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, которая состоит из нижеследующих ингредиентов, или в основном содержит:
- в качестве активного ингредиента трипторелин или любую его фармацевтически приемлемую соль в концентрации от 1 до 22% по массе по отношению к общей массе композиции,
- соль, выбранную из фосфатов,
- от 0 до 1% добавки, выбранной из стабилизаторов, антиоксидантов, поверхностно-активных веществ и их смесей, и
- воду (до 100%),
где pH водной фармацевтической композиции находится в диапазоне от 6 до 8,
и, более предпочтительно, композиция в основном содержит в качестве активного ингредиента трипторелин или любую его фармацевтически приемлемую соль, выбранную из памоата, ацетата и фосфата.
Другим предметом настоящего изобретения является водная фармацевтическая композиция для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, которая состоит из нижеследующих ингредиентов, или в основном содержит:
- в качестве активного ингредиента трипторелин или любую его фармацевтически приемлемую соль, в концентрации от 1 до 22% по массе по отношению к общей массе композиции,
- соль, выбранную из сульфатов,
- от 0 до 1% добавки, выбранной из стабилизаторов, антиоксидантов, поверхностно-активных веществ и их смесей, и
- воду (до 100%),
где pH фармацевтической композиции находится в диапазоне от 6 до 8,
и, более предпочтительно, композиция в основном содержит в качестве активного ингредиента трипторелин или любую его фармацевтически приемлемую соль, выбранную из памоата, ацетата и фосфата.
Композиция настоящего изобретения также может содержать pH буфер.
В предпочтительном варианте осуществления фармацевтическая композиция, в соответствии с определением, приведенном в любом из описанных выше вариантов осуществления, представляет собой водный раствор.
Композицию настоящего изобретения можно получить путем смешивания активного ингредиента, соли и воды. Активный ингредиент можно заранее солюбилизировать в воде и затем добавить соль в виде раствора в воде для инъекции (WFI). В случае применения других добавок, их растворяют либо в растворе пептида, либо в растворе соли, перед их смешиванием.
Фармацевтическая композиция настоящего изобретения представляет собой готовую к применению композицию, герметически упакованную в устройство типа шприца.
Фармацевтическую композицию настоящего изобретения вводят парентеральным способом. В предпочтительном варианте осуществления композицию настоящего изобретения вводят путем подкожной, внутримышечной или глубокой подкожной инъекции, более предпочтительно, путем подкожной инъекции.
Фармацевтическая композиция настоящего изобретения обеспечивает замедленное высвобождение трипторелина у людей в течение, по меньшей мере, 2 недель. Такое высвобождение достигают в отсутствии какой-либо (со)полимерной матрицы в композиции, в частности, в отсутствии каких-либо (со)полимерных средств, являющихся неводорастворимыми, биосовместимыми и/или биоразрушаемыми, которые обычно используют для получения композиций с замедленным высвобождением, таких как полилактиды (PLA), полигликолиды (PLG), полилактид-согликолиды (PLGA), полиалкилцианоакрилаты, поликапролактоны, а также любые (со)полимерные средства, полученные в результате сочетания или модификации указанных биосовместимых (со)полимеров.
В предпочтительном варианте осуществления замедленное высвобождение аналога LHRH у людей продолжается в течение периода, составляющего, по меньшей мере, от 2 до 6 недель.
В предпочтительном варианте осуществления замедленное высвобождение аналога LHRH у людей продолжается в течение, по меньшей мере, 1 месяца.
Композиция настоящего изобретения обеспечивает замедленное высвобождение в течение, по меньшей мере, 14 дней, 21 дня, 28 дней, 35 дней или 42 дней.
В предпочтительном варианте осуществления композиция настоящего изобретения обеспечивает замедленное высвобождение в течение, по меньшей мере, 14 дней. В другом предпочтительном варианте осуществления композиция настоящего изобретения обеспечивает замедленное высвобождение в течение, по меньшей мере 21 дня. В другом предпочтительном варианте осуществления композиция настоящего изобретения обеспечивает замедленное высвобождение в течение, по меньшей мере, 28 дней. В более предпочтительном варианте осуществления композиция настоящего изобретения обеспечивает замедленное высвобождение в течение, по меньшей мере, 35 дней. В другом более предпочтительном варианте осуществления композиция настоящего изобретения обеспечивает замедленное высвобождение в течение, по меньшей мере, 42 дней.
Соединения настоящего изобретения, представляющие собой агонисты и антагонисты LHRH, можно использовать для лечения преждевременной половой зрелости, рака простаты, гипертрофии простаты, эндометриоза, миомы матки, рака молочной железы, угрей, предменструального синдрома, синдрома поликистозных яичников и заболеваний, возникающих в результате чрезмерной продукции половых гормонов у представителей обоих полов. Агонисты и антагонисты LHRH также могут использоваться для контролирования рождаемости как женщинами, так и мужчинами. При пульсирующем введении агонисты LHRH можно использовать в качестве стимуляторов детородной функции. Соединения настоящего изобретения, представляющие собой агонисты LHRH, также можно использовать для стимуляции роста у животных женского пола и икрометания у рыб.
Фармацевтическую композицию настоящего изобретения можно использовать для лечения преждевременной половой зрелости, рака простаты, гипертрофии простаты, эндометриоза, миомы матки, рака молочной железы, угрей, предменструального синдрома, синдрома поликистозных яичников и заболеваний, возникающих в результате чрезмерной продукции половых гормонов у представителей обоих полов. В предпочтительном варианте осуществления фармацевтическую композицию настоящего изобретения используют для лечения рака простаты.
Следовательно, изобретение также относится к способу лечения пациента, страдающего от преждевременной половой зрелости, рака простаты, гипертрофии простаты, эндометриоза, миомы матки, рака молочной железы, угрей, предменструального синдрома, синдрома поликистозных яичников и заболеваний, возникающих в результате чрезмерной продукции половых гормонов у представителей обоих полов, путем введения терапевтически активного количества фармацевтической композиции, описанной в любом из приведенных выше вариантов осуществления.
В другом варианте осуществления фармацевтическую композицию вводят путем однократной инъекции.
В одном варианте осуществления фармацевтическая композиция настоящего изобретения предназначена для лечения или профилактики преждевременной половой зрелости, рака простаты, гипертрофии простаты, эндометриоза, миомы матки, рака молочной железы, угрей, предменструального синдрома, синдрома поликистозных яичников и заболеваний, возникающих в результате чрезмерной продукции половых гормонов у представителей обоих полов.
В другом предпочтительном варианте осуществления настоящее изобретение также предлагает предварительно заполненный шприц, который содержит водную фармацевтическую композицию, описанную в одном из приведенных выше вариантов осуществления.
В другом предпочтительном варианте осуществления настоящее изобретение также предлагает предварительно заполненный шприц, содержащий водную фармацевтическую композицию для замедленного высвобождения активного ингредиента в течение, по меньшей мере, 2 недель, которая содержит:
- от 1 до 22% (масс/масс) трипторелина или любой его фармацевтически приемлемой соли,
- соль, выбранную из фосфатов и сульфатов,
- от 0 до 1% добавки, выбранной из стабилизаторов, антиоксидантов, поверхностно-активных веществ и их смесей, и
- воду для инъекций до 100%,
где pH композиции находится в диапазоне от 4 до 8.
Если не указано иначе, все технические и научные термины используются здесь в своем традиционном значении, известном специалисту в области, к которой относится настоящее изобретение.
Нижеследующие примеры приведены для иллюстрации описанных выше процедур и не должны рассматриваться как ограничивающие объем изобретения.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Пример 1: Способ получения
Разные композиции настоящего изобретения, содержащие аналог LHRH в качестве активного ингредиента, получают с помощью нижеследующего способа:
1. Получение сред
Разные среды, используемые для производства опытных образцов, получают следующим образом:
1.1. 200 мМ Фосфатный буфер pH 7,5
1,560 г NaH2PO4 2H2O отвешивают в колбу объемом 50 мл и растворяют в 45 мл воды для инъекций при перемешивании на магнитной мешалке. Затем pH доводят примерно до 7,5, используя 10N NaOH. Объем полученного раствора доводят до 50 мл водой для инъекций и измеряют pH.
1.2. 200 мМ Раствор сульфата натрия
1,420 г Na2SO4 отвешивают в колбу объемом 50 мл и растворяют в WFI при перемешивании на магнитной мешалке. Объем полученного раствора доводят до 50 мл.
1.3. 200 мМ Раствор сульфата аммония
1,321 г (NH4)2SO4 отвешивают в колбу объемом 50 мл и растворяют в WFI при перемешивании на магнитной мешалке. Объем полученного раствора доводят до 50 мл.
2. Получение опытных образцов
Гомогенизацию препарата осуществляют с помощью ручного двухтактного шприцевого устройства.
Пептид отвешивают в первый шприц. В первый шприц помещают либо 115,8 мг, либо 34,7 мг пептида, с получением конечной концентрации трипторелина соответственно 10% масс/масс или 3% масс/масс.
Указанный первый шприц, содержащий пептид, соединяют со вторым шприцем, содержащим 500 мкл воды для инъекций. Солюбилизацию пептида в воде достигают путем минимум пяти переливаний. Затем пустой шприц отсоединяют и заполняют 500 мкл одной из сред. После соединения со шприцем, содержащим раствор пептида, осуществляют однородное смешивание раствора со средой путем минимум десяти переливаний.
Опытные образцы хранят при комнатной температуре в защищенном от света месте.
Минимум десять переливаний осуществляют через 1 ч, 24 ч и 48 ч после получения образца.
Примеры составов композиций приведены в таблице 1:
|
Содержание аналога LHRH выражают в виде массового процента продукта по отношению к общей массе композиции.
Композиция 4 представляет собой разбавленную композицию 1.
3. Получение опытных образцов
3.1. Получение 20% масс/масс опытного образца при отношении фосфат/пептид 0,6
1,744 г ацетата трипторелина отвешивают в стеклянную бутыль объемом 25 мл и растворяют в 5,625 мл фосфатного буфера при перемешивании на магнитной мешалке. Медленно добавляют еще 1,875 мл фосфатного буфера при перемешивании на магнитной мешалке, чтобы обеспечить достаточную степень однородности опытного образца. pH конечной композиции составляет 5,7. Затем композицию, представляющую собой белое плотное полутвердое вещество, помещают в пластиковые шприцы объемом 1,2 мл, снабженные иглами 18G. Для введения такой композиции настоящего изобретения требуется максимальное усилие, соответствующее SIF 12 Н при скорости 200 мм/мин.
Фосфатный буфер получают путем растворения 1,43 г дигидрата дигидрофосфата натрия в 80 мл WFI, доведения pH до 7,5 5N раствором гидроксида натрия и доведения конечного объема до 100 мл.
3.2. Получение 20% масс/масс опытного образца при отношении сульфат/пептид 0,6
1,744 г ацетата трипторелина отвешивают в стеклянную бутыль объемом 25 мл и растворяют в 5,625 мл раствора сульфата натрия при перемешивании на магнитной мешалке. Медленно добавляют еще 1,875 мл раствора сульфата натрия при перемешивании на магнитной мешалке, чтобы обеспечить достаточную степень однородности опытного образца. pH конечной композиции составляет 5,4. Получают белое плотное полутвердое вещество.
Раствор сульфата натрия получают путем растворения 1,30 г сульфата натрия в 100 мл WFI.
3.3. Получение 10% масс/масс опытного образца при отношении фосфат/пептид 0,2
0,873 г ацетата трипторелина отвешивают в химический стакан объемом 10 мл и растворяют в 3,75 мл WFI при перемешивании на магнитной мешалке. Медленно добавляют 3,75 мл фосфатного буфера при перемешивании на магнитной мешалке, чтобы обеспечить достаточную степень однородности опытного образца. Получают белое полутвердое вещество.
Фосфатный буфер получают путем растворения 0,536 г дигидрата дигидрофосфата натрия в 80 мл WFI, доведения pH до 7,5 5N раствором гидроксида натрия и доведения конечного объема до 100 мл.
3.4. Получение 10% масс/масс опытного образца при отношении сульфат/пептид 0,2
0,873 г ацетата трипторелина отвешивают в стеклянную бутыль объемом 25 мл и растворяют в 3,75 мл WFI при перемешивании на магнитной мешалке. Медленно добавляют 3,75 мл раствора сульфата натрия при перемешивании на магнитной мешалке, чтобы обеспечить достаточную степень однородности опытного образца. pH конечной композиции составляет 5,2. Получают кремообразное и вязкое полутвердое вещество.
Раствор сульфата натрия получают путем растворения 0,2175 г сульфата натрия в 50 мл WFI.
Пример 2: Исследование стабильности
Опытные образцы хранят при комнатной температуре в защищенном от света месте и затем анализируют методом ВЭЖХ в разные моменты времени перед тестированием in vivo.
Результаты анализа стабильности приведены в таблицах 2 и 3.
|
Количество примесей не увеличивается после стояния в течение 38 дней при комнатной температуре.
|
Пример 3: Фармакокинетические (PK) исследования
Крысам вводят описанные в таблице 1 фармацевтические композиции, содержащие разные дозы соли трипторелина.
В таблице 4 указаны дозы, вводимые путем однократной внутримышечной инъекции:
|
В начале исследования для каждой композиции используют 6 самцов крыс Wistar.
Образцы крови берут у животных без анестезии из яремной вены путем непосредственной венопункции, до введения (момент времени 0) и через 2, 5, 9, 15 и 22 дней после введения.
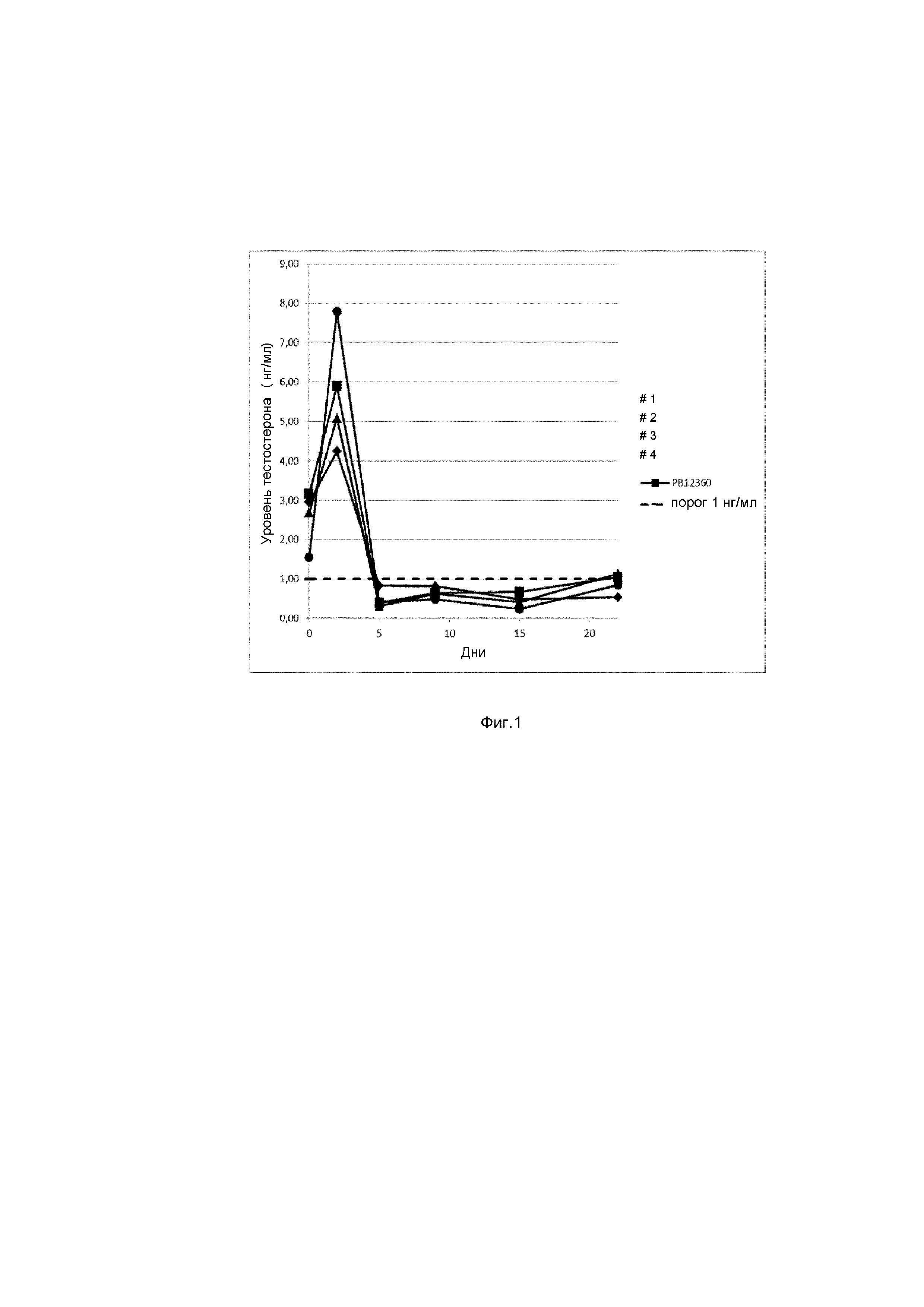
У крыс определяют уровни тестостерона после введения каждой композиции, полученные средние значения приведены на фигуре 1.
Результаты сравнивают с порогом 1 нг/мл, ниже которого происходит химическая кастрация.
Все композиции обеспечивают концентрации тестостерона ниже порога 1 нг/мл в течение периода от 5 до 15 дней после однократного внутримышечного введения композиции настоящего изобретения. Проведенное фармакокинетическое исследование демонстрирует эффективность указанных композиций.