Результат интеллектуальной деятельности: СПОСОБ ЛЕЧЕНИЯ ПЛОСКОКЛЕТОЧНОГО РАКА РОТОГЛОТКИ
Вид РИД
Изобретение
Изобретение относится к области медицины, а именно к онкологии, и может быть использовано при лечении плоскоклеточного рака полости рта и глотки путем сочетанного лучевого и лекарственного воздействия.
Известен способ повышения эффективности лучевой терапии опухолей различной локализации (RU 2088288 С1), включающий дистанционную γ-терапию в сочетании с химиотерапией, при которой больному вводят 5-фторурацил с 1 по 5 сутки ежедневно в суточной дозе 600 мг/м2, затем в течение 7-9-х суток ежедневно непосредственно перед облучением вводят платидиам в суточной дозе 20 мг/м2. Лучевую терапию терапию начинают на 7-е сутки в режиме динамического мультифракционирования: первые 3 дня фракции по 1,8 Гр два раза через 4-6 час, затем по 1,2 Гр два раза в день через 4-6 часов до суммарной очаговой дозы 30-32,4 Гр. После 10-12-дневного перерыва лечение повторяют по аналогичной схеме до суммарной очаговой дозы (далее - СОД) 60-64,8 Гр.
Недостатком этого способа является то, что в 40% случаев возникают лучевые реакции со стороны слизистых орофарингеальной области, требующие незапланированного перерыва в лечении, что негативно сказывается на его эффективности. С другой стороны, не менее 30% пациентов страдают от общих токсических явлений. Кроме того, такой метод химиолучевого лечения, достаточно эффективный в случае первичного очага (78,6% полной резорбции при опухолях ротоглотки), малоэффективен при воздействии на регионарные метастазы.
Также особый интерес представляет работа Sewit Teckie с соавторами 2016, в которой авторы ретроспективно оценили результаты и побочные эффекты лучевого лечения больных опухолями головы и шеи в режиме гипофракционирования, в том числе и ультрагипофракционирования с подведением 8 Гр за фракцию. В исследование включено 48 пациентов со средним сроком наблюдения от 6 до 54,3 мес. Средние дозы составили 30 Гр за 5 фракций, тогда как в 20 случаях разовая очаговая доза (далее - РОД) была 8 Гр. Общий ответ на лечение составил 79%. Одногодичный локорегионарный контроль достигал 50%. Многофакторный анализ показал, что локорегионарный контроль был выше при подведении доз ионизирующего излучения в РОД 6 Гр (р=0.04). Полный ответ на облучение также был достоверно связан с лучшей выживаемостью больных (р=0.01).
При этом побочные эффекты не были более выражены даже при облучении в РОД 8 Гр. Таким образом, исследователи подчеркивают положительную роль гипофракционирования (РОД 6 Гр и более) в лечении больных опухолями головы и шеи и предлагают проведение дальнейших научных изысканий в этом направлении.
За прототип принят способ химиолучевого лечения больных местнораспространенным раком головы и шеи, разработанный Pfister DG с соавторами (Concurrent cetuximab, cisplatin, and concomitant boost radiotherapy for locoregionally advanced, squamous cell head and neck cancer: A pilot phase II study of a new combined-modality paradigm. J Clin Oncol 2006).
Пробное исследование II фазы включило 22 больных, которым проводилось введение цисплатина (100 мг/м2 1 раз в неделю) и цетуксимаба (в стартовой дозе 400 мг/м2 с последующей дозой 250 мг/м2 1 раз в неделю) в сочетании с лучевой терапии с применением буста (локального наращивания дозы непосредственно на очаг опухолевого поражения с щажением нормальных тканей за счет исключения из объема облучения зон регионарного метастазирования). Дозы ионизирующего излучения подводили по 1,8 Гр в день в течение четырех недель и затем 1,8 Гр + 1,6 Гр бустом через 4-6 часов в течение двух недель до СОД 70 Гр. В итоге применения такой агрессивной схемы были получены хорошие отдаленные результаты лечения - 3-летняя общая выживаемость и локорегионарный контроль составили 76% и 71% соответственно.
Однако исследование было прервано на ранней стадии в связи с двумя летальными исходами в процессе его проведения (1 от пневмонии и 1 от невыясненных причин) и тяжелой переносимостью лечения у других больных, включая инфаркт миокарда, фибрилляцию предсердий, бактериемию и др.
Таким образом, предложенная схема лечения показала свою высокую эффективность за счет агрессивного воздействия трех агентов (цетуксимаб, цисплатин, ионизирующее излучение) на опухолевые клетки. В то же время однократные и суммарные дозы цисплатина и цетуксимаба в сочетании с разовыми дозами излучения и график их совместного воздействия оказались недопустимыми для жизнеспособности нормальных клеток.
Техническим результатом предлагаемого изобретения является разработка способа, увеличивающего темпы и степень регрессии первичной опухоли, подавление субклинических диссеминированных метастазов за счет оптимального режима сочетанного лучевого и лекарственного воздействия на опухоль.
Указанный технический результат при осуществлении изобретения достигается за счет того, что также как и в известном способе вводят цетуксимаб в стартовой дозе 400 мг/м2 с последующей дозой 250 мг/м2 1 раз в неделю в сочетании с лучевой терапией.
Особенностью заявляемого способа является то, что с 8 дня лечения цетуксимабом проводят лучевую терапию ежедневно по 5-дневной рабочей неделе на локорегионарную область, включая регионарные лимфоколлекторы: заглоточные лимфоузлы и лимфоколлекторы шеи до I-V групп с обеих сторон (CTV2/PTV2); при этом в течение последних 12 дней, после подведения СОД 32,4 Гр, дополнительно с интервалом, равным или более 6 часам, проводят облучение опухоли и метастатически измененных лимфоузлов (GTV/CTV1/PTV1) в РОД 1,5 Гр до СОД 72 Гр.
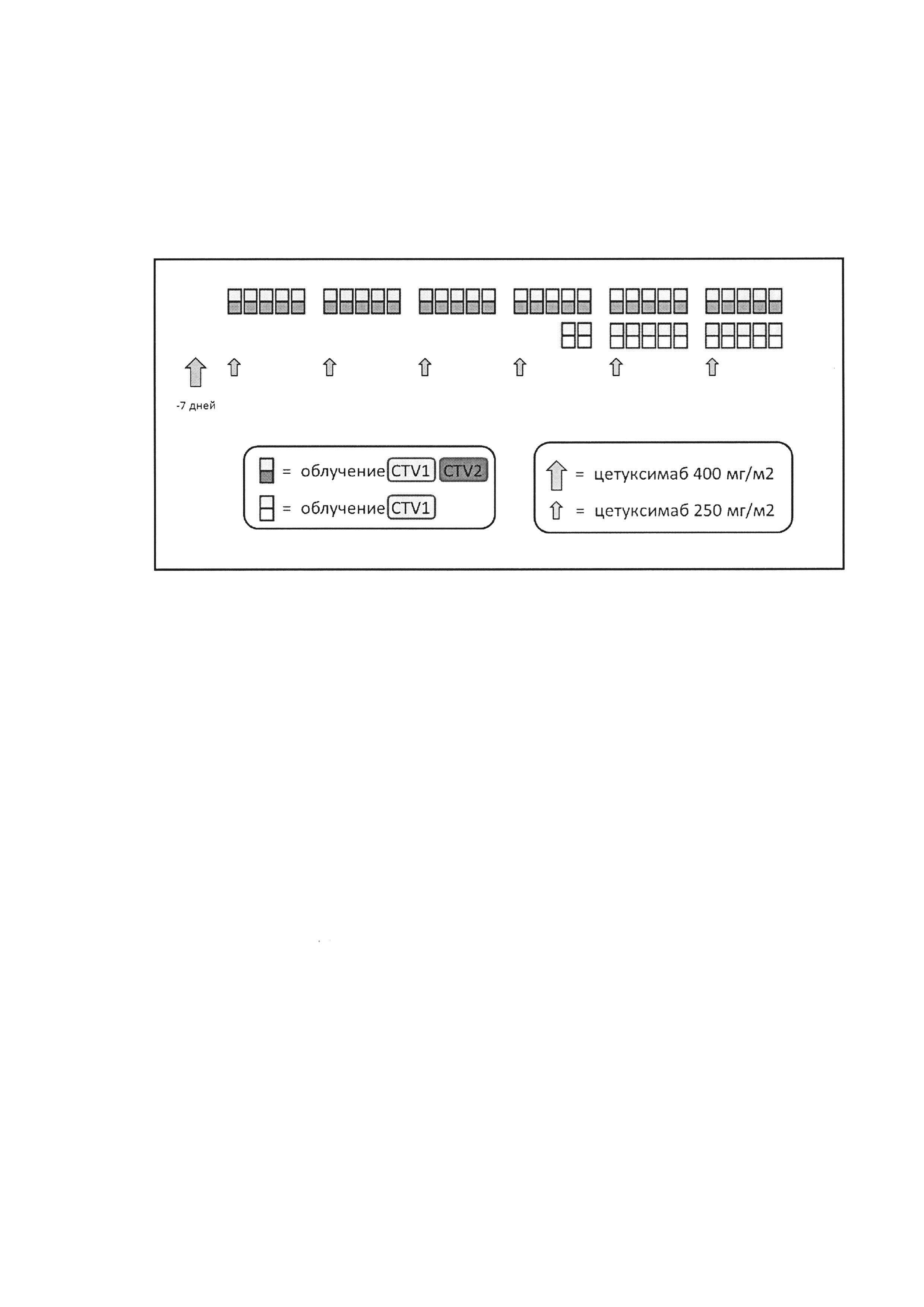
Изобретение поясняется подробным описанием, клиническими примерами и иллюстрацией, на которой изображена схема биолучевого лечения.
Способ осуществляют следующим образом (см. Фиг. ):
Цетуксимаб 1-й день. Внутривенное введение цетуксимаба в дозе 400 мг/м2 в течение 120 минут.
8-й день. Внутривенное введение цетуксимаба в дозе 250 мг/м2 в течение 60 минут.
15-й день. Внутривенное введение цетуксимаба в дозе 250 мг/м2 в течение 60 минут.
22-й день. Внутривенное введение цетуксимаба в дозе 250 мг/м2 в течение 60 минут.
29-й день. Внутривенное введение цетуксимаба в дозе 250 мг/м2 в течение 60 минут.
36-й день. Внутривенное введение цетуксимаба в дозе 250 мг/м2 в течение 60 минут.
43-й день. Внутривенное введение цетуксимаба в дозе 250 мг/м2 в течение 60 минут.
Лучевая терапия 8-й-47-й день. Лучевая терапия в РОД 1,8 Гр × 1 раз в сутки по 5-дневной рабочей неделе на локорегионарную область пораженных структур, включая регионарные лимфоколлекторы (CTV2/PTV2) до СОД 54 Гр.
32-й - 47-й день. Ежедневное дополнительное облучение (с ≥ 6-часовым интервалом) опухоли (GTV/CTV1/PTV1) в РОД 1,5 Гр (суммарно РОД 3,3 Гр) до СОД 72 Гр.
На первой неделе опухолевые клетки подвергают воздействию таргетного препарата цетуксимаба (400 мг/м2), который, связываясь с рецепторами эпидермального фактора роста (EGFR), блокирует процесс их фосфорилирования. Прекращается подача сигнала к ядру клетки, что приводит к подавлению пролиферации клеток, ангиогенеза, опухолевой инвазии, метастазирования с одновременной стимуляцией апоптоза и повышением чувствительности к лучевой терапии. Кроме того, цетуксимаб способствует выработке собственных Т-киллеров, которые вызывают лизис опухолевых клеток.
С восьмого дня опухолевые клетки подвергают воздействию дозы излучения, необходимой для их разрушения и гибели (1,8 Гр), с усилением противоопухолевого воздействия после подведения СОД 32,4 Гр за счет локального наращивания РОД до 3,3 Гр до СОД 72 Гр. Указанная доза облучения является допустимой для сохранения жизнеспособности нормальных клеток (с учетом предшествующего режима классического фракционирования по 1,8 Гр × 1 р/сут). Кроме того, смещение более агрессивного режима облучения на вторую половину курса лучевой терапии позволяет рассчитывать на меньшую выраженность лучевых реакций за счет частичной адаптации нормальных тканей. В результате подведения укрупненных фракций имеет место повреждение опухолевых клеток различной степени - летальное и сублетальное. При этом разрушающему лучевому воздействию подвергаются наиболее активные опухолевые клетки, способные к метастазированию. В то же время менее активные опухолевые клетки переходят в суб- и потенциально летальное состояние.
Радиомодифицирующее действие цетуксимаба выражается в блокировании восстановления суб- и потенциально летальных повреждений в опухоли, что, в конечном итоге, приводит к усилению лучевого разрушения опухоли. Не обладающий такими токсическими свойствами цетуксимаб, с учетом периода его полувыведения 70-100 час, продолжают вводить 1 раз в 7 дней в дозе 250 мг/м2 с целью поддержания эффективной его концентрации и сохранения вышеописанных эффектов в полном объеме. Дальнейшую эскалацию дозы препарата ограничивают возможные аллергические реакции и выраженные нарушения биологии кожных покровов и слизистых. Такое сочетание лучевого и лекарственного лечения с наращиванием СОД до 72 Гр с сокращением общей длительности лечения до 6 недель приводит к значительному повышению противоопухолевого эффекта.
Таким образом, в предложенном способе используется два взаимно дополняющих метода радиомодификации: цетуксимаб и нетрадиционное фракционирование дозы лучевого воздействия с интенсивным воздействием на массив опухоли.
Заявляемый способ с успехом апробирован для лечения больных с местнораспространенным опухолевым поражением орофарингеальной области: плоскоклеточным раком слизистой ротовой полости, глотки и языка.
Пример 1.
Больная Г., 60 лет. поступила с диагнозом: Рак ротоглотки (правая небная миндалина) IV ст., cT2N2bM0. В анамнезе 36 лет назад выполнена лимфаденэктомия на шее справа по поводу лимфаденита. Пациентка считает себя больной с ноября 2016 г., когда отметила боли в горле при глотании. Получала без эффекта симптоматическую терапию у ЛОР врача по месту жительства по поводу обострения тонзиллита. В январе 2017 г. при дополнительном обследовании было обнаружено новообразование ротоглотки и пациентка направлена к онкологу. Самостоятельно обратилась в МНИОИ им П.А. Герцена, где был установлен и морфологически подтвержден настоящий диагноз. Гистологическое исследование: биоптат из образования правой небной миндалины: частицы слизистой оболочки с покровом из многослойного плоского неороговевающего эпителия, в одной из частиц с картиной плоскоклеточной карциномы in situ и фокусами начала инвазивного роста. Гистологическое исследование: биоптат из образования подчелюстной области справа: фрагмент фиброзной ткани с лимфоцитарной инфильтрацией и комплексами плоскоклеточного неороговевающего рака. Цитологическое исследование материала из образования подчелюстной области справа - цитограмма плоскоклеточного рака с наклонностью к ороговению. ИГХ (экспрессия р16): обнаружена интенсивная положительная реакция во всех клетках плоскоклеточного рака.
Асимметрии лица нет. Тризма нет. Мимические пробы выполняет удовлетворительно. Речь не нарушена. В правой половине ротоглотки, по задней стенке, определяется опухоль, смешанной формы роста, плотно-эластичная при пальпации, размерами 2,5×3 см. В в/3 шеи справа определяется послеоперационный рубец без признаков воспаления. Отмечается рубцовая деформация в верхней трети шеи справа. На шее справа определяются единичные узлы, размерами до 1,5 см, плотные при пальпации, ограниченно подвижные. На шее слева без очаговой патологии.
Эндоскопия: В области правой миндаликовой ниши определяется мелкобугристая инфильтрация правой небной миндалины ярко-розового цвета, выбухает в просвет ротоглотки, размерами до 1,5 см. Задняя небная дужка визуально не изменена. Левые симметричные отделы без особенностей. Корень языка симметричен, анатомичен, эластичен, без признаков опухолевой инфильтрации. Надгортанник обычной формы и размеров. Все элементы гортани сохранены, четко визуализируются, слизистая гладкая. Обе гортани подвижны, фонации. Подскладочный отдел свободен. Заключение: сг ротоглотки с поражением правой небной миндалины.
МРТ с контрастным усилением: По задней стенке ротоглотки справа, суживая ее просвет справа и вызывая нерезко выраженную девиацию правой небной миндалины, определяется подслизистое многокамерное кистозное образование неправильно округлой формы, с четкими, ровными контурами, с MP-признаками псевдокапсулы, размерами около 13×23×35 мм, локализующееся по передней поверхности длинных мышц шеи и головы на уровне тел позвонков СЗ, С2 и частично смежных отделов зубовидного отростка позвонка С2, без убедительных MP-признаков распространения образования в проекцию симпатического ствола. В верхне-правых отделах области шеи по нижнемедиальному контуру, интимно прилежа к правой околоушной слюнной железе на уровне тела позвонка СЗ и смежных отделов тела С2, компримируя железу, определяется многокамерное кистозно-солидное образование неправильно округлой формы, с четкими, ровными контурами, с MP-признаками псевдокапсулы, размерами около 21×20×23 мм. Правая внутренняя сонная артерия и правая внутренняя яремная вена интимно прилежат к медиальному контуру образования в проекции хода правых подъязычного, добавочного и блуждающего нервов, без убедительных MP-признаков вовлечения в процесс вышеописанных нервов. Внутренняя яремная вена компримирована образованием. Увеличенных лимфатических узлов и деструкции костных структур на исследуемом уровне не выявлено. После введения контрастного препарата (Магневист 0,2 мл/кг массы тела) побочных реакций на введение не отмечено. Определяется интенсивное и неоднородное его накопление двумя вышеописанными образованиями. Других участков его патологического накопления не выявлено. Заключение: MP-картина под слизистого многокамерного кистозного образования по задней стенке ротоглотки справа без убедительных MP-признаков распространения образования (многокамерная киста?) в проекцию симпатического ствола, картина многокамерного кистозно-солидного образования в верхне-правых отделах области шеи по нижне-медиальному контуру правой околоушной слюнной железы (измененный лимфатический узел?, аденома правой околоушной слюнной железы?) без убедительных MP-признаков вовлечения в процесс правых подъязычного, добавочного и блуждающего нервов.
УЗИ: В правой подчелюстной области в зоне п\о рубца визуализируется не менее трех образований пониженной эхогенности до 24×14×24 мм. В левой подчелюстной области очаговой патологии не выявлено. В структуре заднего отростка правой околоушной слюнной железы визуализируется гиперплазированный л/узел до 8×4×7 мм. В области шеи визуализируется гиперплазированные л/узлы наибольших размеров: в верхней трети справа до 10×4×12 мм, в нижней трети слева до 12×3×5 мм.
Проведен 5-дневный курс биолучевой терапии с применением цетуксимаба по приведенной выше схеме до СОД72 Гр на область первичной опухоли и метастатически измененных лимфоузлов и до СОД54 Гр на локорегионарную область ротоглотки, включая заглоточные лимфоузлы и лимфоколлекторы шеи I-V групп с обеих сторон. На момент завершения лечения отмечена резорбция экзофитного компонента опухоли.
Лечение проведено с 7-дневным перерывом в лечении на пике лучевых реакций. По окончании лечения отмечены побочные эффекты в виде эпителиита II ст. СТС АЕ 4 версии выраженности со стороны слизистой глотки, акнеподобной сыпи I ст. СТС АЕ 4 версии и дерматита I ст. СТС АЕ 4 версии на шее с обеих сторон). Питание через рот в полном объеме. Согласно оценке качества жизни переносимость лечения удовлетворительная.
Больная выписана под наблюдение по месту жительства.
При контрольном обследовании через 2 месяца - без признаков рецидива, регионарного и отдаленного метастазирования, а также побочных эффектов проведенного ранее лечения за исключением ксеростомии I ст. СТС АЕ 4 версии. Оставлена под наблюдение. В настоящее время без признаков рецидива в течение 12 месяцев.
Пример 2.
Больная Ю., 47 лет, поступила с диагнозом: Рак ротоглотки (корень языка) III ст., cT3N0M0. Пациентка считает себя больной с ноября 2015 года, когда под контролем отоларинголога по месту жительства получала симптоматическую терапию по поводу хронического тонзиллита с временным положительным эффектом. Летом 2016 года появились боли ноющего характера в области корня языка, усиливающиеся при глотании. В ноябре 2016 года в связи с нарастанием жалоб, а также появлением помехи при глотании, самостоятельно обратилась к онкологу по месту жительства. Заподозрено злокачественное заболевание корня языка. Самостоятельно обратилась в МНИОИ им П.А. Герцена, где был установлен и морфологически подтвержден настоящий диагноз. Гистологическое исследование - биоптат из опухоли корня языка - частицы слизистой оболочки с покровом из плоского эпителия, лимфоидной основой, участками роста недифференцированного рака с высокой митотической активностью. Для уточнения гистогенеза новообразования необходимо иммуногистохимическое исследование. ИГХ от 21.12.2016 с CD 45, СК 5/6, CD 20, CD 3, BCL2, BCL 6, CD 10, PAX 5, MUMI, CD 4, CD 8, Ki67, Цитокератин (АЕ 1/АЕ3): В опухолевых клетках реакция с СК 5/6 негативная. В них выявлена положительная реакция с цитокератином. С остальными маркерами реакция в опухолевых клетках отрицательная. Имеется очень большая примесь CD 45 положительных лимфоидных клеток. Среди опухолевых клеток Ki 67 положительных определяются в очень большом количестве. Цитологическое исследование из опухоли ротоглотки - цитограмма плоскоклеточного неороговевающего рака. Цитологическое исследование пунктата л/у в/3 шеи справа - цитограмма гиперплазии лимфатического узла. Цитологическое исследование пунктата л/у в/3 шеи справа - клеточный состав лимфатического узла. ИГХ (экспрессия р16): обнаружена интенсивная положительная реакция во всех клетках опухоли.
Асимметрии лица и шеи нет. Мимические пробы выполняет удовлетворительно. Тризма нет. Речь не нарушена. Девиации языка нет. В области корня языка справа пальпаторно определяется опухоль плотной консистенции, размерами 4,0×3,5 см, с частичным переходом за среднюю линию и вовлечением левых отделов корня языка. Опухоль распространяется на латеральную стенку ротоглотки справа в области нижнего полюса небной миндалины. В верхней трети шеи слева и в подчелюстных областях с обеих сторон определяются единичные узлы плотно-эластической консистенции до 1,5 см в диаметре, подвижные относительно окружающих тканей. В остальных отделах шеи без очаговой патологии.
Эндоскопия: Корень языка эластичен, подвижен. При ретроградном осмотре в области задней 1/3 правой  корня языка определяется усиленный, извитый подслизистый сосудистый рисунок на фоне гладкой блестящей слизистой. Надгортанноглоточная складка не изменена. Левые симметричные отделы без особенностей. Надгортанник обычной формы и размеров. Грушевидные синусы свободны с обеих сторон. Гортань все три отдела сохранены, слизистая гладкая, обе
корня языка определяется усиленный, извитый подслизистый сосудистый рисунок на фоне гладкой блестящей слизистой. Надгортанноглоточная складка не изменена. Левые симметричные отделы без особенностей. Надгортанник обычной формы и размеров. Грушевидные синусы свободны с обеих сторон. Гортань все три отдела сохранены, слизистая гладкая, обе  подвижны. Трахея без особенностей. Заключение: cr правой 1/2 корня языка, эндофитная форма роста.
подвижны. Трахея без особенностей. Заключение: cr правой 1/2 корня языка, эндофитная форма роста.
МРТ головы и шеи с внутривенным контрастным усилением: Язычная справа и правая небная миндалины увеличена в размерах за счет участка измененного МР-сигнала (гиперинтенсивного на Т2 ВИ и STIR, гипоинтенсивного - на Т1 ВИ), распространяющегося на корень языка, размерами 30×28×45 мм, деформируя просвет ротоглотки. После введения контрастного препарата отмечается интенсивное и неравномерное накопление последнего, преимущественно периферическими отделами с визуализируемым гипоинтенсивным центральным образованием размерами 26×20×25 мм. Вдоль переднего и заднего края грудино-ключично-сосцевидных мышц, преимущественно справа, определяются увеличенные лимфоузлы размерами от 9 мм до 42×12 мм.
УЗИ шеи: В в/3 шеи справа (1/2) определяется лимфоузел с неровным контуром гетерогенной структуры размерами 19,5×16×27 мм (пункция). В ср/3 и в/3 шеи с обеих сторон определяются лимфоузлы с сохраненной структурой без признаков атипии размерами справа до 11×5 мм, слева до 10×4 мм.
Проведен курс биолучевой терапии с применением цетуксимаба по приведенной выше схеме до СОД 72 Гр на область первичной опухоли лимфоузлов и до СОД54 Гр на локорегионарную область ротоглотки, включая заглоточные лимфоузлы и лимфоколлекторы шеи Ib-IV групп с обеих сторон.
Лечение проведено с 7-дневным перерывом в лечении на пике лучевых реакций. По окончании лечения отмечены побочные эффекты в виде эпителиита III ст. СТС АЕ 4 версии выраженности со стороны слизистых полости рта и глотки, акнеподобной сыпи II ст. СТС АЕ 4 версии и дерматита II ст. СТС АЕ 4 версии на шее с обеих сторон. Питание через рот в полном объеме. Согласно оценке качества жизни переносимость лечения удовлетворительная.
Больная выписана под наблюдение по месту жительства.
При контрольном обследовании через 2 месяца - без признаков рецидива, регионарного и отдаленного метастазирования, а также побочных эффектов проведенного ранее лечения за исключением ксеростомии I ст. СТС АЕ 4 версии. Оставлена под наблюдение. В настоящее время без признаков рецидива в течение 14 месяцев.
Использование предложенного способа в клинике позволяет достичь излечения больного с минимальными побочными эффектами в отличие от известных схем химиолучевой терапии, а именно: регрессию первичной опухоли и подавление субклинических диссеминированных метастазов за счет оптимального режима сочетанного лучевого и лекарственного воздействия на опухоль.
Способ лечения плоскоклеточного рака полости рта и глотки, включающий введение цетуксимаба в стартовой дозе 400 мг/м с последующей дозой 250 мг/м 1 раз в неделю в сочетании с лучевой терапией, отличающийся тем, что с 8 дня лечения проводится лучевая терапия в РОД 1,8 Гр ежедневно по 5-дневной «рабочей неделе» до СОД 54 Гр на локорегионарную область, включая регионарные лимфоколлекторы (CTV2/PTV2), при этом в течение последних 12 дней, после подведения СОД 32,4 Гр дополнительно с ≥6-часовым интервалом ежедневно проводится дополнительное облучение опухоли (GTV/CTV1/PTV1) в РОД 1,5 Гр до СОД 72 Гр.