КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ПРОБИОТИЧЕСКИЕ БАКТЕРИИ, СПОСОБНАЯ ВОССТАНАВЛИВАТЬ БАРЬЕРНЫЙ ЭФФЕКТ ЖЕЛУДКА, УТРАЧЕННЫЙ В ПРОЦЕССЕ ФАРМАКОЛОГИЧЕСКОГО ЛЕЧЕНИЯ ПОВЫШЕННОЙ КИСЛОТНОСТИ ЖЕЛУДКА
Вид РИД
Изобретение
Настоящее изобретение относится к композиции, содержащей пробиотические бактерии, предназначенной для использования в фармакологическом лечении повышенной кислотности желудка. Данная композиция способна восстанавливать барьерный эффект желудка, утраченный в процессе фармакологического лечения повышенной кислотности желудка, и сводить к минимуму вторичные эффекты, обусловленные указанным фармакологическим лечением.
За последние десятилетия были разработаны различные фармакологические подходы для фармакологического лечения повышенной кислотности желудка, состояния, которое, в случае, если оно имеет место в выраженной форме в течение длительного времени, способно вызывать различные осложнения или патологии, такие как язвенная болезнь желудка и гастроэзофагеальная рефлюксная болезнь.
Среди наиболее широко используемых препаратов есть те, которые основаны на активных ингредиентах, способных ингибировать H2-гистаминовые рецепторы, такие как, например, циметидин, фамотидин, низатидин и ранитидин, или основаны на активных ингредиентах, способных ингибировать простагландины, такие как, например, мизопростол. В основе другой категории лекарственных средств лежат активные ингредиенты, которые выполняют функцию защиты слизистой оболочки желудка, такие как, например, соли висмута, сукральфат, либо антимускариновые или парасимпатолитические препараты на основе пирензепина и пипензолата. Наконец, существуют также антациды, такие как, например, натрия бикарбонат, алюминия гидроксид или магния гидроксид, и ингибиторы протонного насоса, лежащие в основе лансопразола, эзомепразола, рабепразола, пантопразола и омепразола.
Ингибиторы протонного насоса (PPI) представляют собой группу молекул, основное действие которых заключается в выраженном снижении кислотности желудочного сока в течение достаточно длительного периода времени (от 18 до 24 часов).
Лекарственные средства из группы PPI являются преемниками H2-антигистаминных препаратов, и ингибиторы PPI гораздо более распространены, чем последние, поскольку они более эффективны.
Вышеуказанные лекарственные средства используют для симптоматического и этиологического лечения различных синдромов, таких как (i) диспепсия и (ii) гастродуоденальная язва. PPI используют для лечения или профилактики язв желудка и двенадцатиперстной кишки. Их также используют в сочетании с некоторыми антибиотиками для лечения гастрита, вызванного Helicobacter pylori; (iii) синдрома Золлингера-Эллисона и (iv) гастроэзофагеальной рефлюксной болезни.
PPI также применяют в случаях, когда пациенты принимают ацетилсалициловую кислоту или другие НПВП продолжительного действия. Такие препараты, ингибируя функции фермента циклооксигеназы 1 (COX 1), имеют побочный эффект, выражающийся в снижении синтеза простагландинов, процесса, который зависит от данного конкретного фермента. Так как функции простагландинов включают защиту слизистой оболочки желудка от кислой среды, PPI используют для снижения кислотности среды и защиты слизистой оболочки желудка.
Данный тип лекарственных средств ингибирует желудочный фермент H+/K+-АТФазу (протонный насос), катализатор обмена ионов H+ и K+. Это приводит к эффективному ингибированию секреции кислоты.
В микроканалах, где значение pH является низким, близким к 2, эти ингибиторы ионизируются и превращаются в молекулы, способные образовывать ковалентные связи с тиольной группой (SH) цистеина из субъединицы насоса. Таким образом, насос необратимо ингибируется. Возобновление перекачивающей способности влечет за собой образование новых насосов, процесс, для которого требуется в среднем от 18 до 24 часов. Вследствие этого одна доза PPI позволяет ингибировать желудочную секрецию в течение примерно 24 часов.
Тот факт, что ингибиторы активны только в кислой среде, объясняет, почему они оказывают минимальное воздействие на внежелудочную H+/K+-АТФазу, действующую на уровне прямой кишки и толстой кишки.
В любом случае, если оставить за рамками их конкретный механизм действия, конечный эффект почти всех этих классов препаратов для лечения повышенной кислотности желудка или других патологических состояний, упомянутых выше, заключается в повышении значения pH в желудке, с кинетикой и интенсивностью, которые зависят от конкретной используемой фармакологической молекулы и ее дозировки. Исключением в этом отношении являются простагландины и препараты, защищающие слизистую оболочку желудка, которые вместо снижения концентрации водородных ионов в полости усиливают синтез слизи и бикарбонатных ионов клетками стенки желудка, увеличивая тем самым защиту слизистой оболочки от кислотной среды полости. В любом случае, препараты, способные снижать повышенную кислотность желудочного сока, представляют собой предпочтительный метод лечения в случае пептической язвы желудка и гастроэзофагеального рефлюкса, в то время как препараты, защищающие слизистую оболочку, представляют собой дополнительную терапию.
Хорошо известно, однако, что нормальная кислотность желудка представляет собой эффективный барьер против потенциально вредных или патогенных микроорганизмов, попадающих в обычную пищу. Действительно, многие из них являются особенно чувствительными к кислотности среды и не способны выживать более 5 минут, иногда даже меньше, при значениях рН ниже 3. Отсюда следует, что многие болезнетворные микроорганизмы, в том числе принадлежащие к роду Salmonella, не попадают в кишечник живыми и при отсутствии вредного воздействия на организм человека, опосредованного секретируемыми токсинами, уже присутствующими в пище, они не способны вызывать кишечную инфекцию и, следовательно, полномасштабную пищевую интоксикацию.
Следует отметить, однако, что повышение рН желудочного сока, обычно наблюдаемое у субъектов, которые принимают препараты для снижения или лечения повышенной кислотности желудка, делает этих людей более подверженными риску пищевых токсикоинфекций, вызванных, прежде всего, употреблением в пищу сырых продуктов, особенно рыбы, мяса и яиц.
У субъектов, принимающих такие лекарственные средства, как, например, ингибиторы протонного насоса, для снижения или лечения повышенной кислотности желудка, значение pH в желудке составляет примерно 5.
Такое значение pH позволяет энтеробактериям и, в частности, определенным штаммам E. coli, наделенным выраженной декарбоксилазной активностью, проходить невредимыми через ослабленный желудочный барьер. Белки, поступающие в организм с пищей, ферментативно расщепляются до аминокислот, которые в присутствии декарбоксилазной активности модифицируются в ряд биогенных аминов, таких как, например, гистамин, тирамин, путресцин и кадаверин, которые могут быть потенциально опасными или очень опасными. Наиболее распространенные симптомы, которые эти биогенные амины могут вызывать, полностью аналогичны вторичным эффектам, вызванным применением ингибиторов протонного насоса (PPI), и они представляют собой: диарею, головную боль, тошноту, боли в животе и метеоризм. Более того, когда определенные биогенные амины реагируют с нитритами, образуются N-нитрозамины. Эти нитрозамины вызывают генетические мутации путем алкилирования ДНК, и их присутствие связано с раком желудка, кишечника, поджелудочной железы и мочевого пузыря, а также с лейкемией.
Приостановка фармакологической терапии, очевидно, не является возможным решением для этих субъектов, поскольку это вновь подвергнет слизистую оболочку желудка и пищевода вредному воздействию, опосредованному желудочным соком. С другой стороны, немыслимо продолжать фармакологическую терапию и подвергать субъектов такому риску инфекции.
Таким образом, остается необходимость того, чтобы субъекты, нуждающиеся в этом, могли принимать лекарственные средства для снижения или лечения повышенной кислотности желудка, с одной стороны, и при этом не подвергаться воздействию особо опасных патогенных инфекций или риску рецидивов патогенных инфекций, с другой стороны.
Автор изобретения нашел решение вышеуказанной проблемы благодаря композиции, способной восстанавливать функциональность желудочного барьера, который оказывает защитное действие в отношении патогенных или вредных микроорганизмов.
Композиция по настоящему изобретению способна восстанавливать функцию желудочного барьера, которую обычно выполняет желудочный сок, и которая, в частности, снижена у субъектов, принимающих препараты для снижения или лечения повышенной кислотности желудка. Указанная композиция способна сводить к минимуму вторичные эффекты, связанные с фармакологической терапией, основанной на применении лекарственных средств, ингибирующих протонный насос (для краткости, PPI).
Композицию по настоящему изобретению можно успешно использовать для лечения пептической язвы или гастроэзофагеального рефлюкса.
После интенсивной научно-исследовательской деятельности автор изобретения неожиданно обнаружил, что подобранное сочетание пробиотических бактерий способно, с одной стороны, позволить субъектам, нуждающимся в этом, принимать препараты для снижения или лечения повышенной кислотности желудка, а с другой стороны, не подвергаться воздействию особо опасных патогенных инфекций или риску рецидивирующих патогенных инфекций.
Таким образом, предметом настоящего изобретения является композиция, обладающая признаками, описанными в прилагаемой независимой формуле изобретения.
Другие предпочтительные варианты осуществления настоящего изобретения описаны ниже и будут заявлены в прилагаемой независимой формуле изобретения.
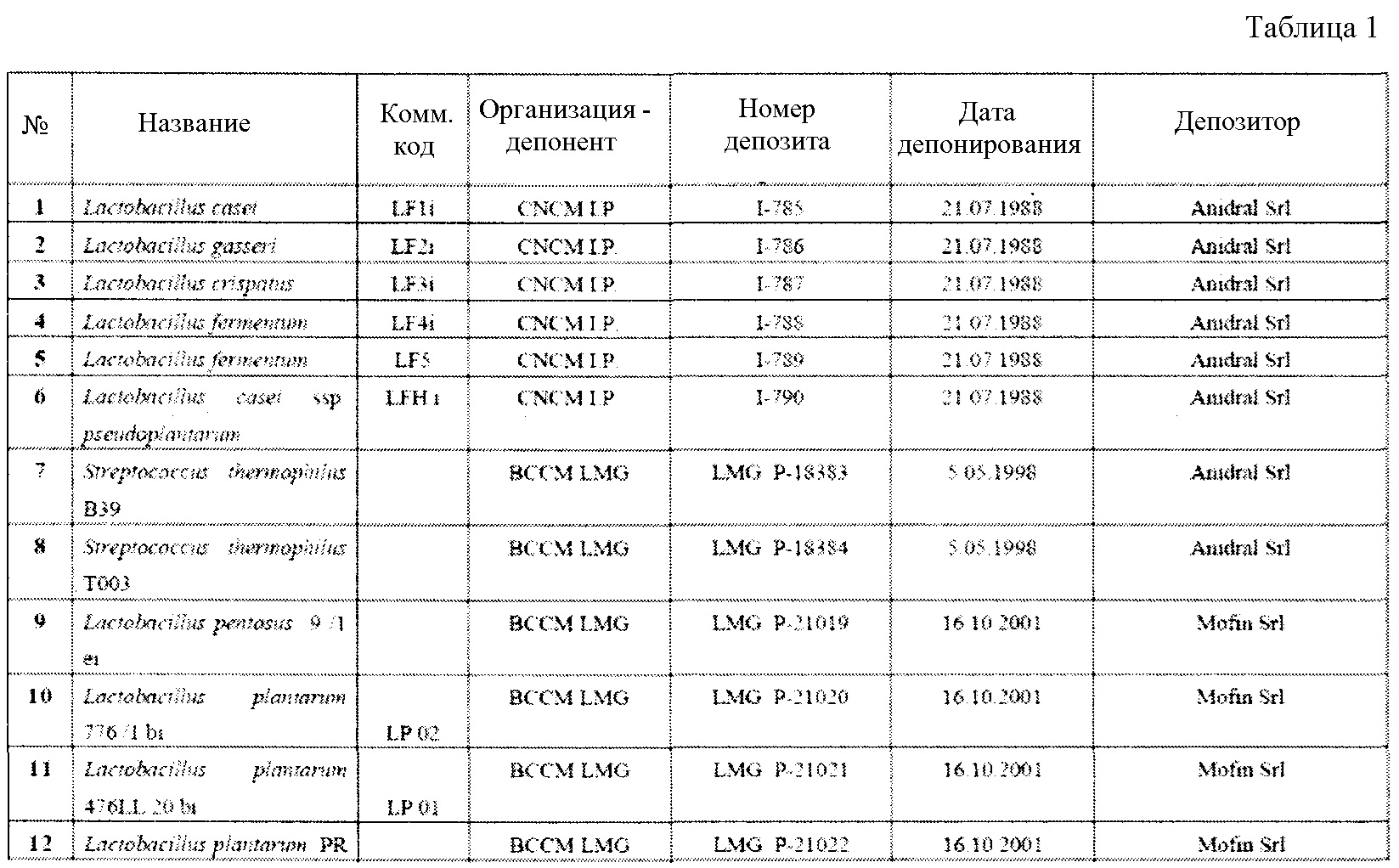
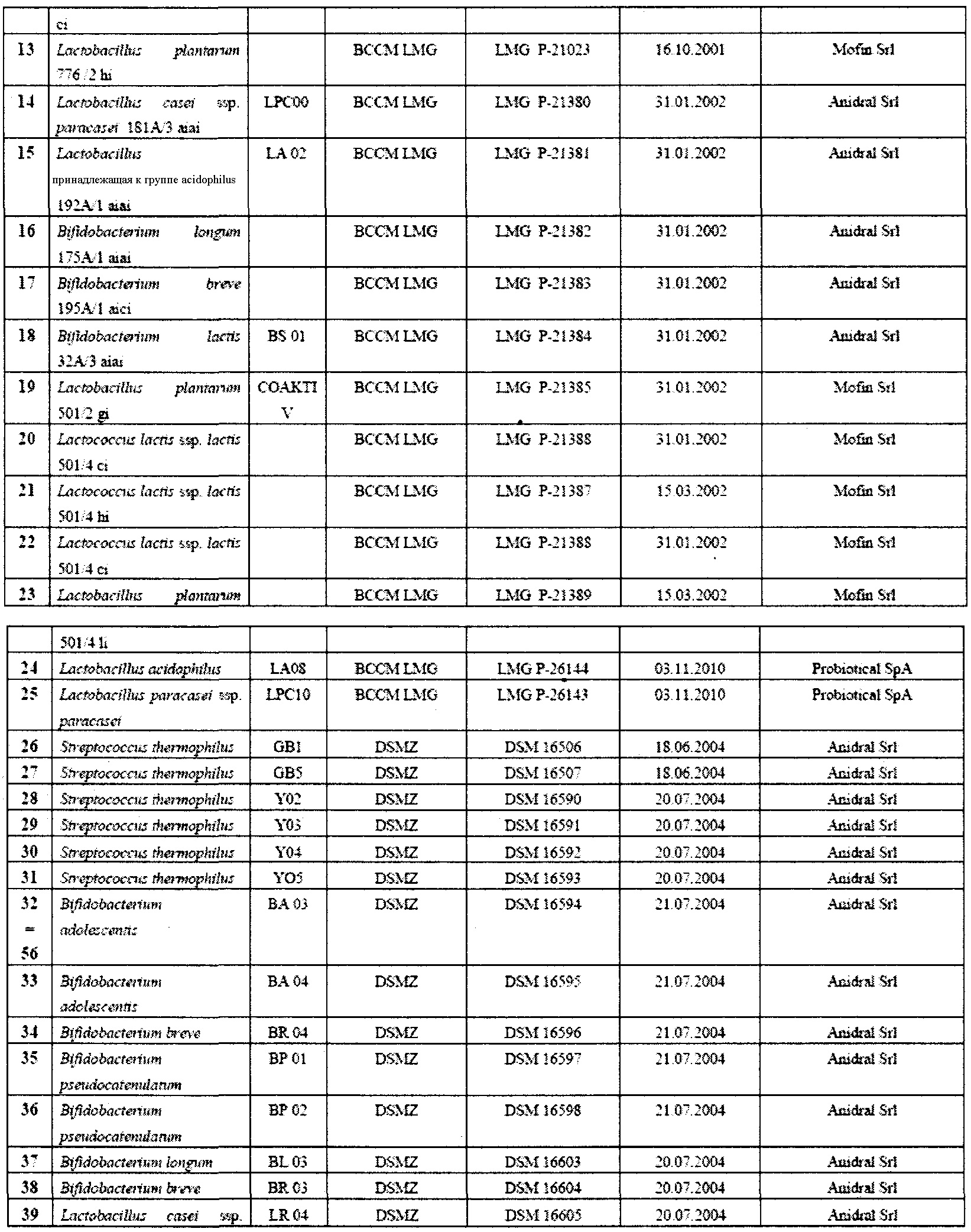
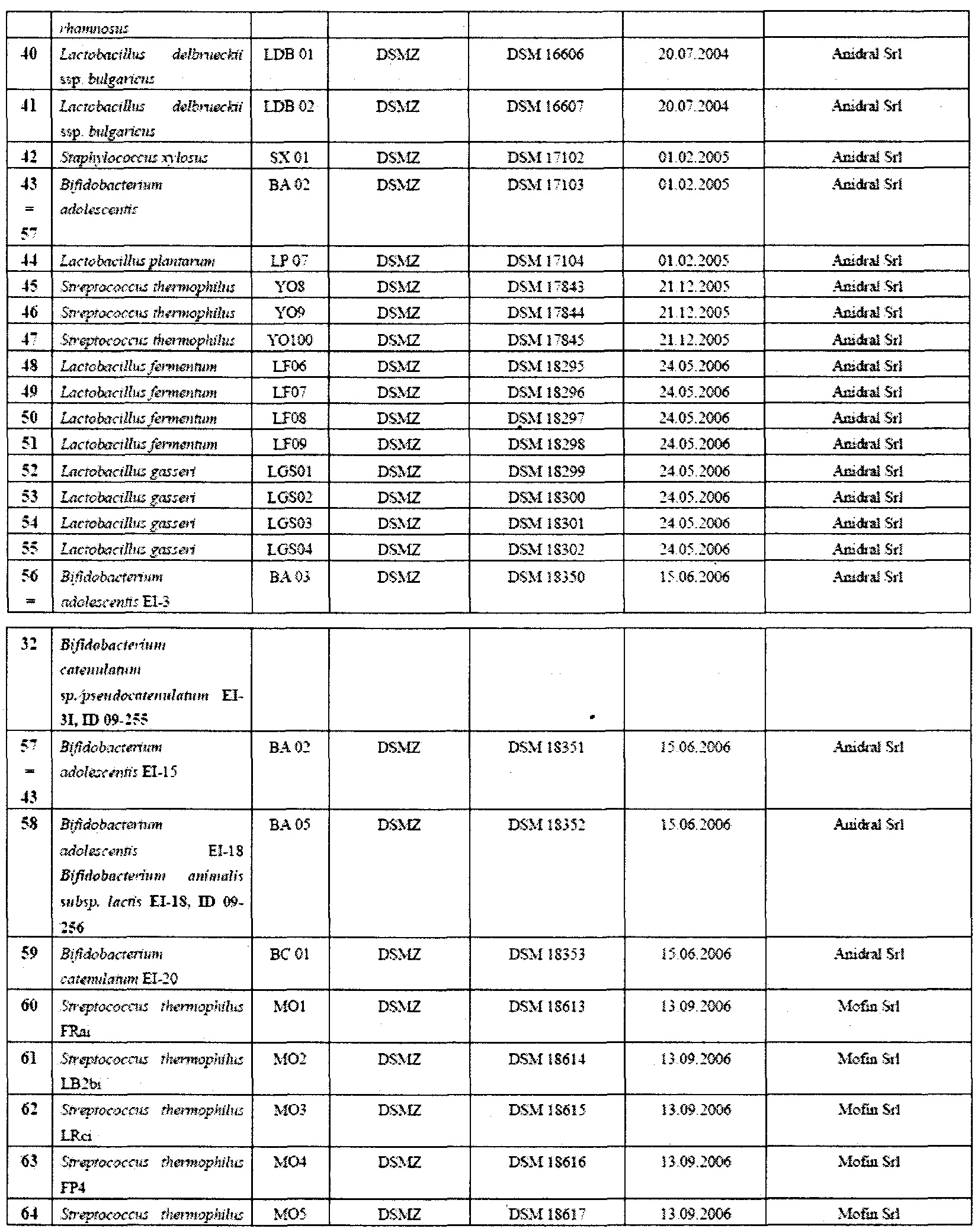
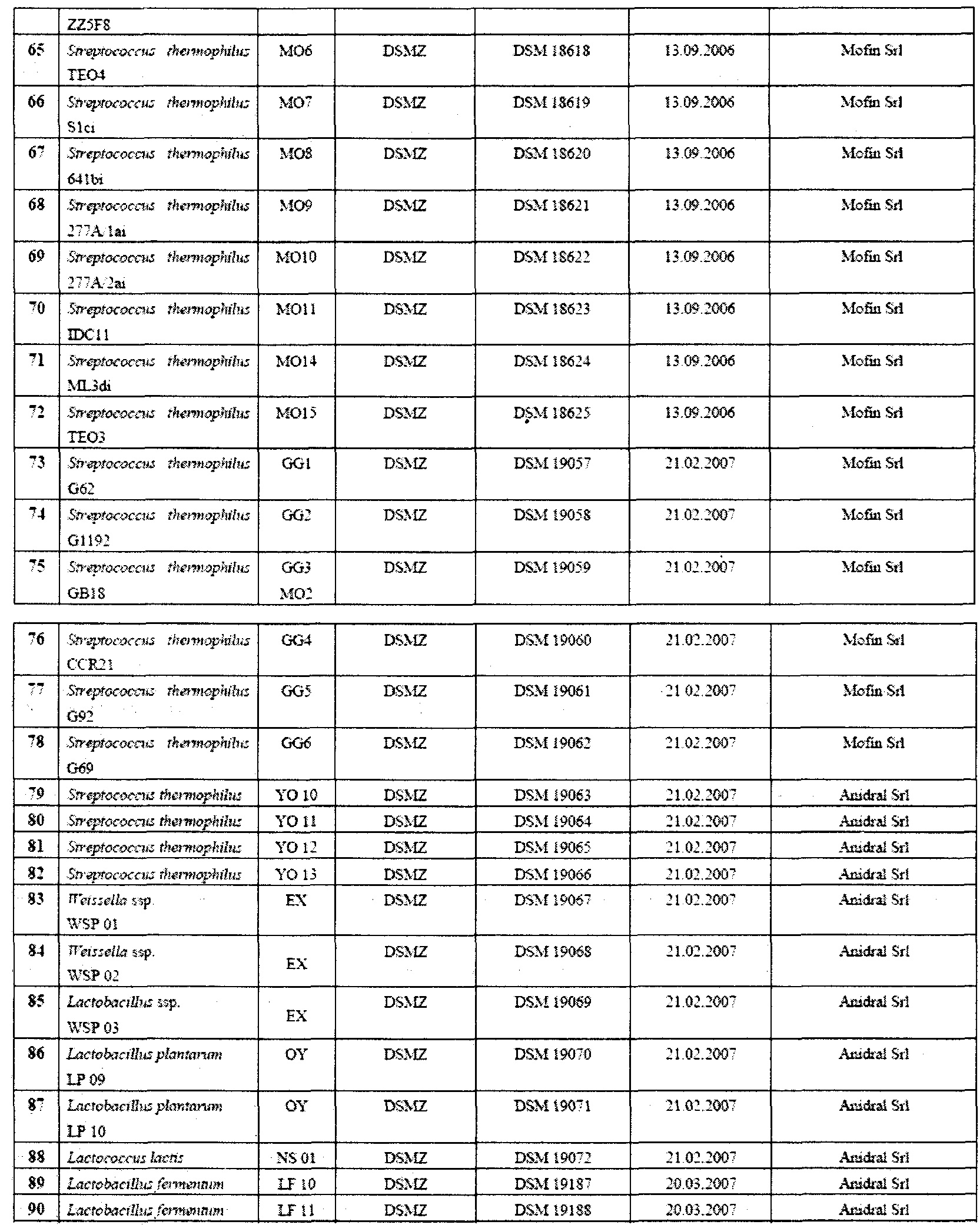
В таблице 1 приведена, в качестве примера, группа микроорганизмов, которые можно эффективно применять в контексте настоящего изобретения.
Автор изобретения проводил интенсивные исследования и отбор, по окончании которых было установлено, что штаммы пробиотических бактерий, принадлежащих к видам, выбранным из группы, включающей L. acidophilus, L. crispatus, L. gasseri, L. delbrueckii, L. salivarius, L. casei, L. paracasei, L. plantarum, L. rhamnosus, L. reuteri, L. brevis, L. buchneri, L. fermentum, L. lactis, L. pentosus, B. adolescentis, B. angulatum, B. bifidum, B. breve, B. catenulatum, B. infantis, B. lactis, B. longum, B. pseudocatenulatum и S. thermophilus, можно эффективно применять в лечении субъектов, принимающих препараты для снижения или лечения повышенной кислотности желудка.
Бактериальные штаммы были выбраны потому, что они способны колонизировать желудок при значении рН в диапазоне от 4,5 до 5. При этом значении рН выбранные штаммы действуют, продуцируя активные вещества, такие как бактериоцины, и/или метаболиты, и/или перекись водорода.
Композиция по настоящему изобретению может представлять собой пищевую композицию, например симбиотическую композицию или другую добавку, или фармацевтическую композицию, или медицинское устройство.
В предпочтительном варианте осуществления композиция может содержать один или более штаммов, выбранных из тех, которые перечислены в таблице 1.
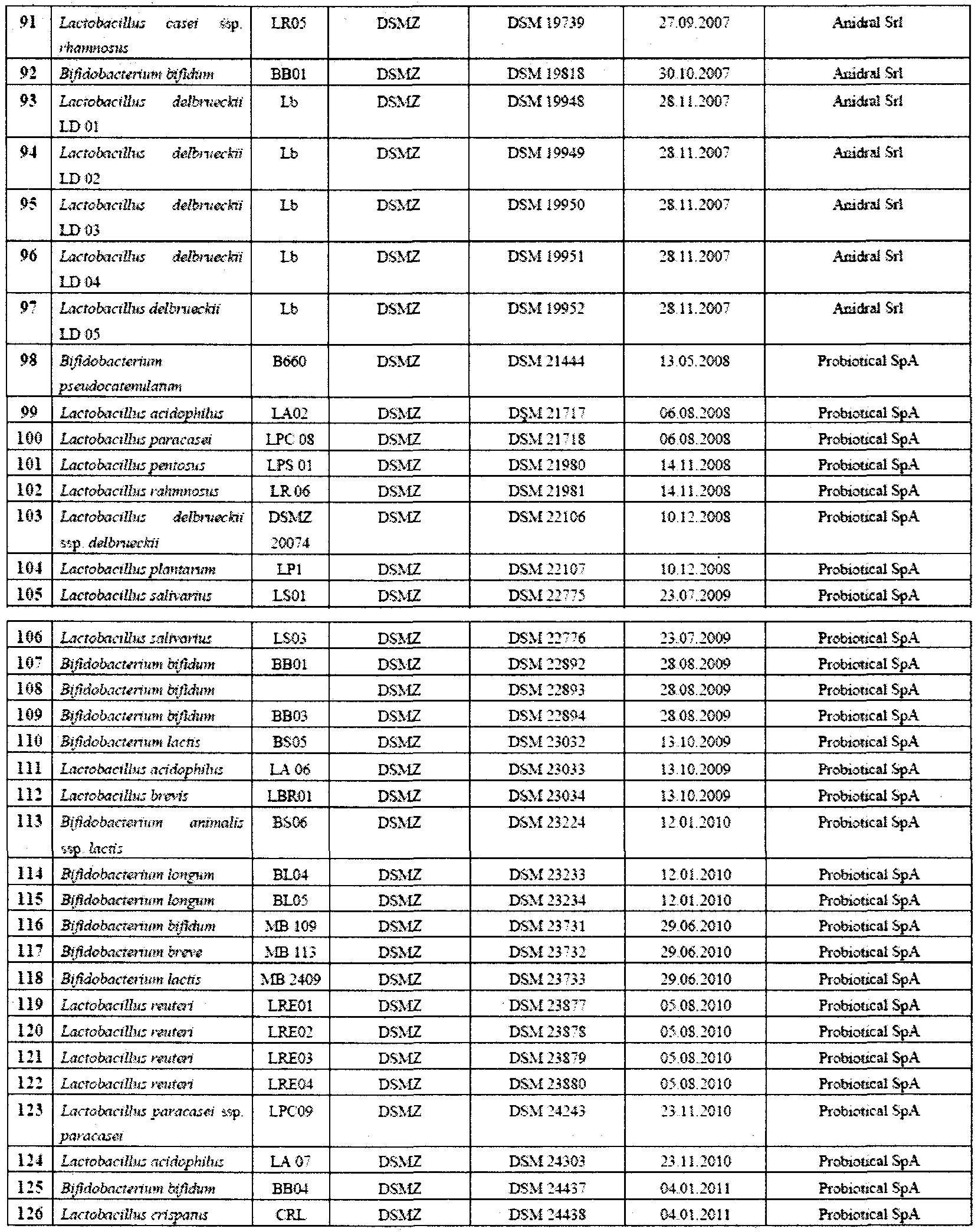
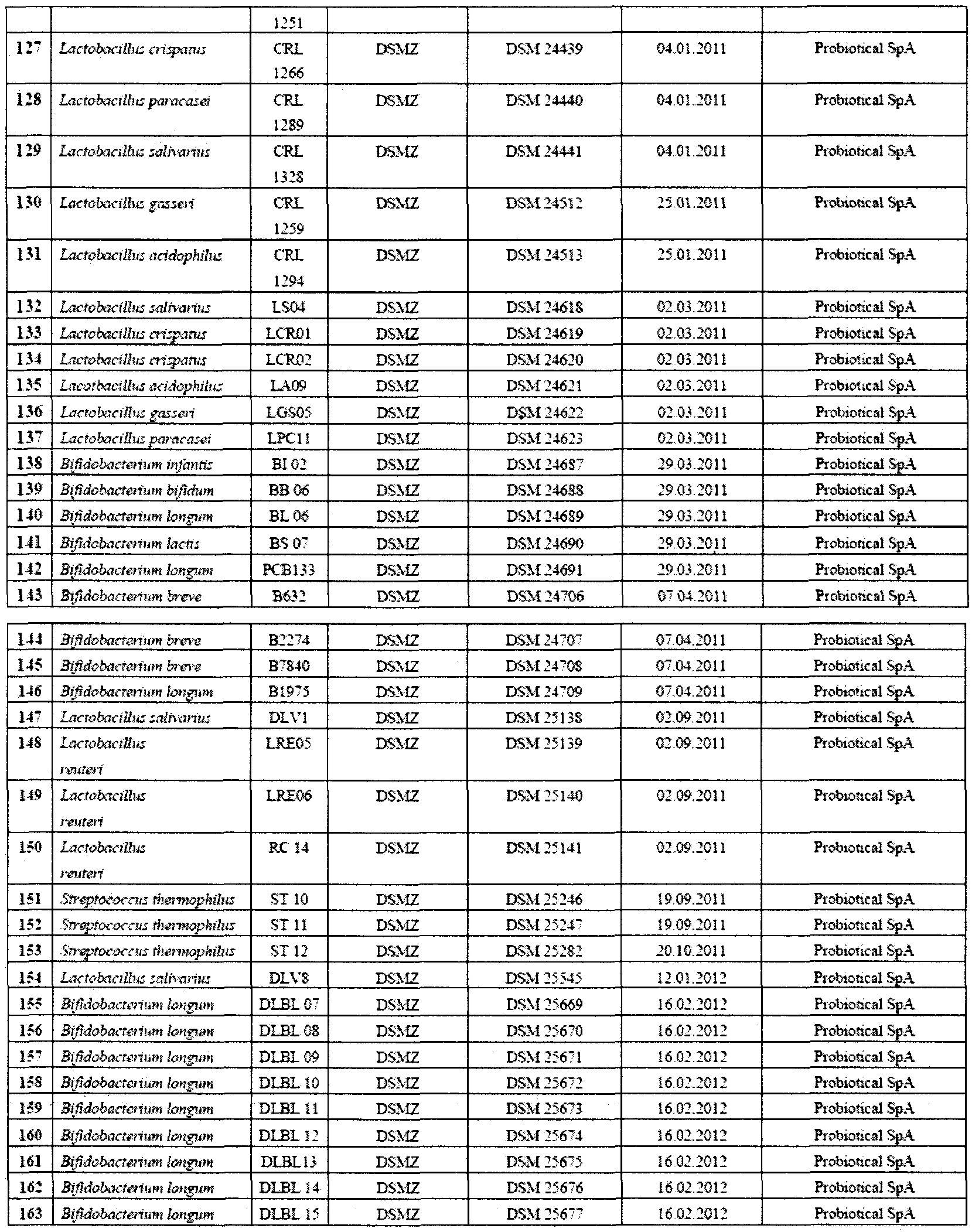
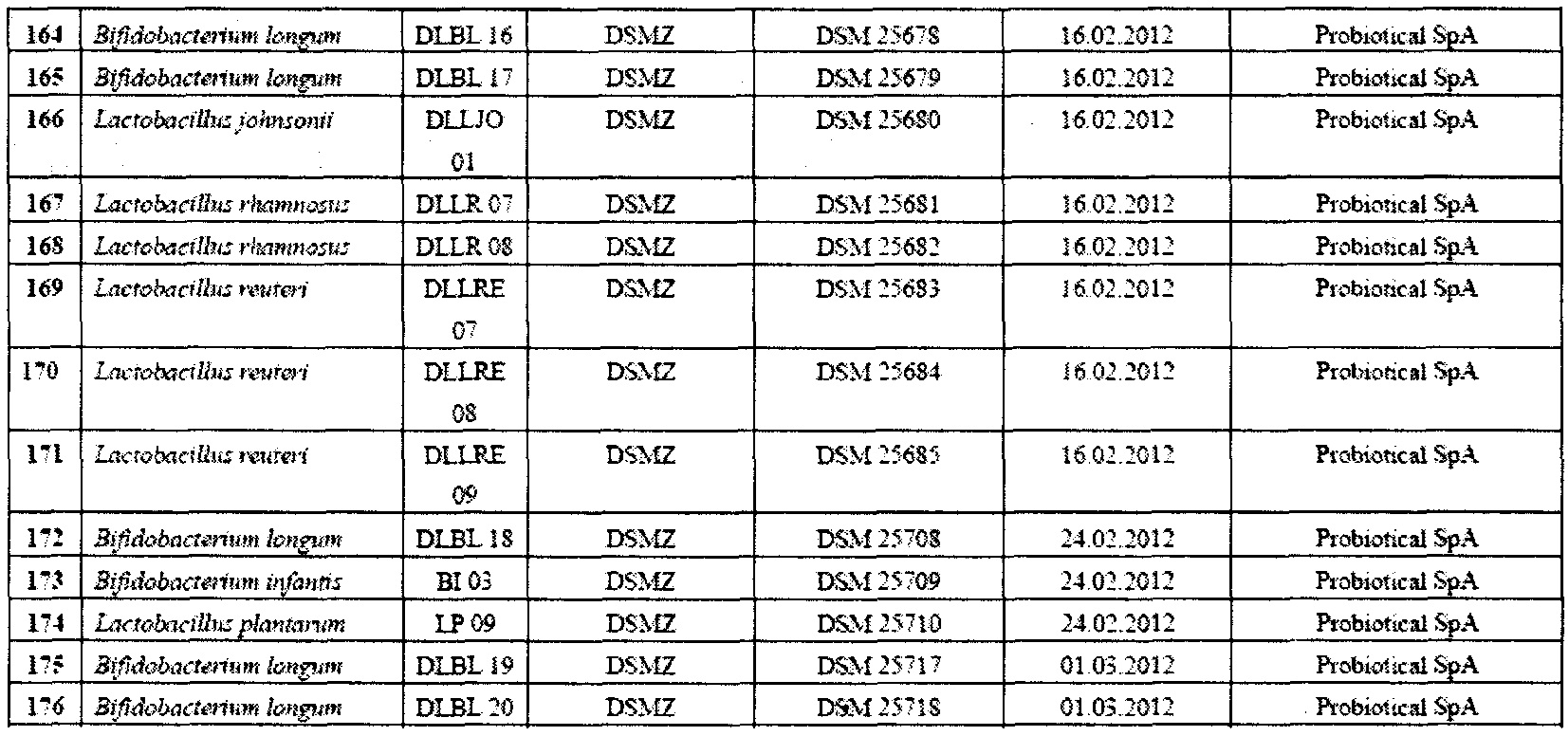
Предпочтительно композиция содержит от одного до шести штаммов, даже более предпочтительно от двух до пяти штаммов из тех, которые перечислены в таблице 1.
Особенно предпочтительные штаммы выбраны из тех, которые перечислены в таблице 2.
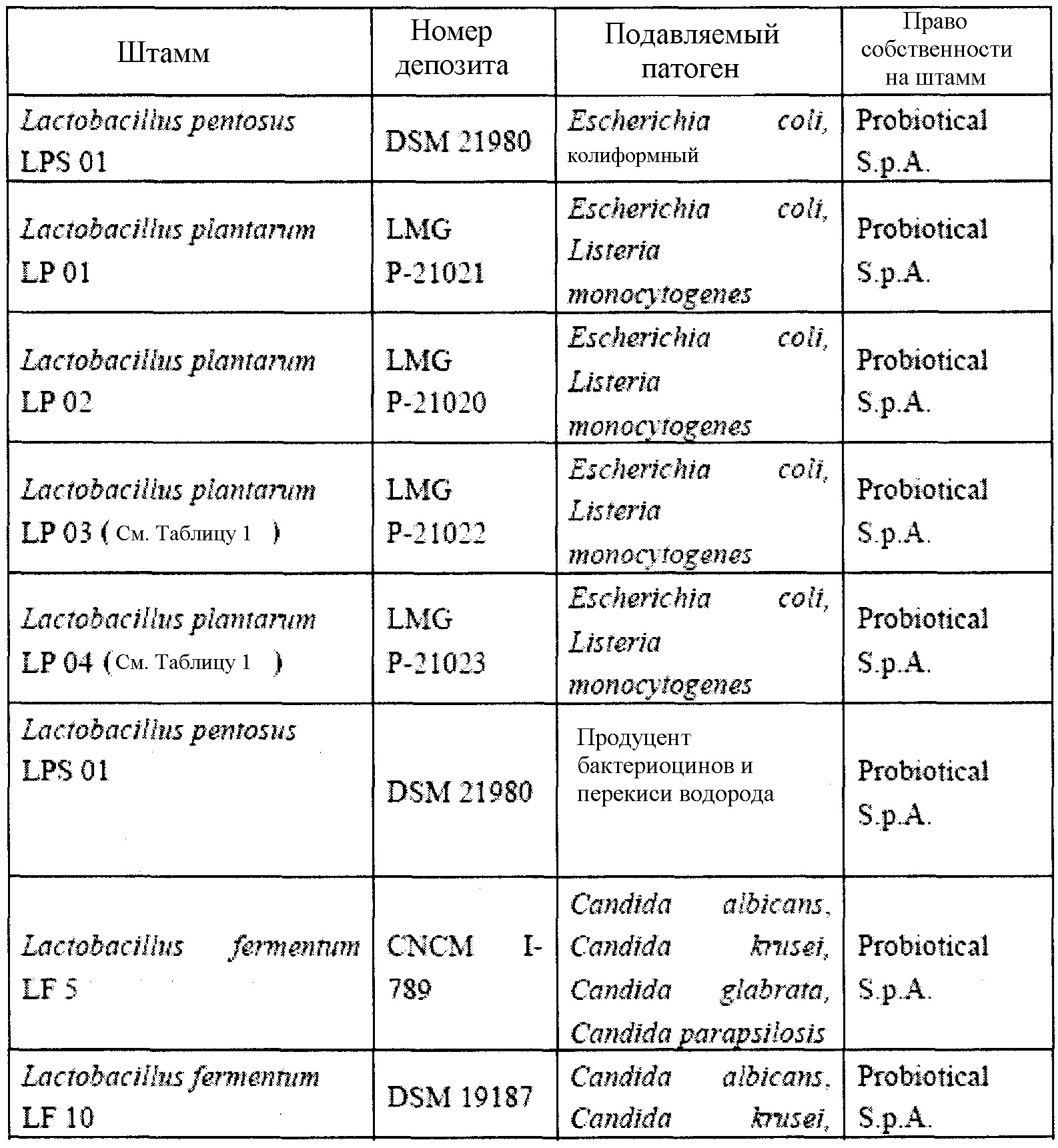
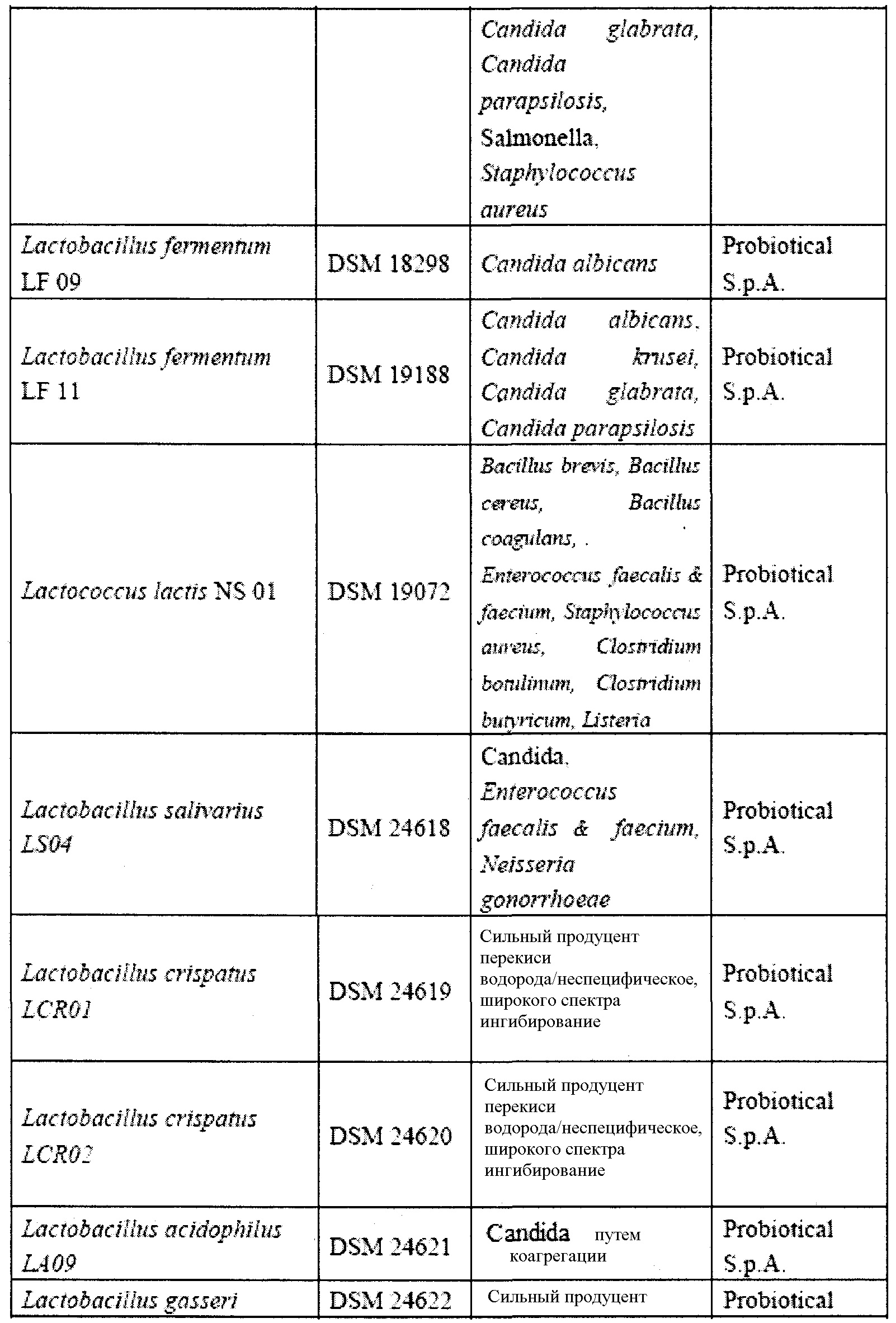
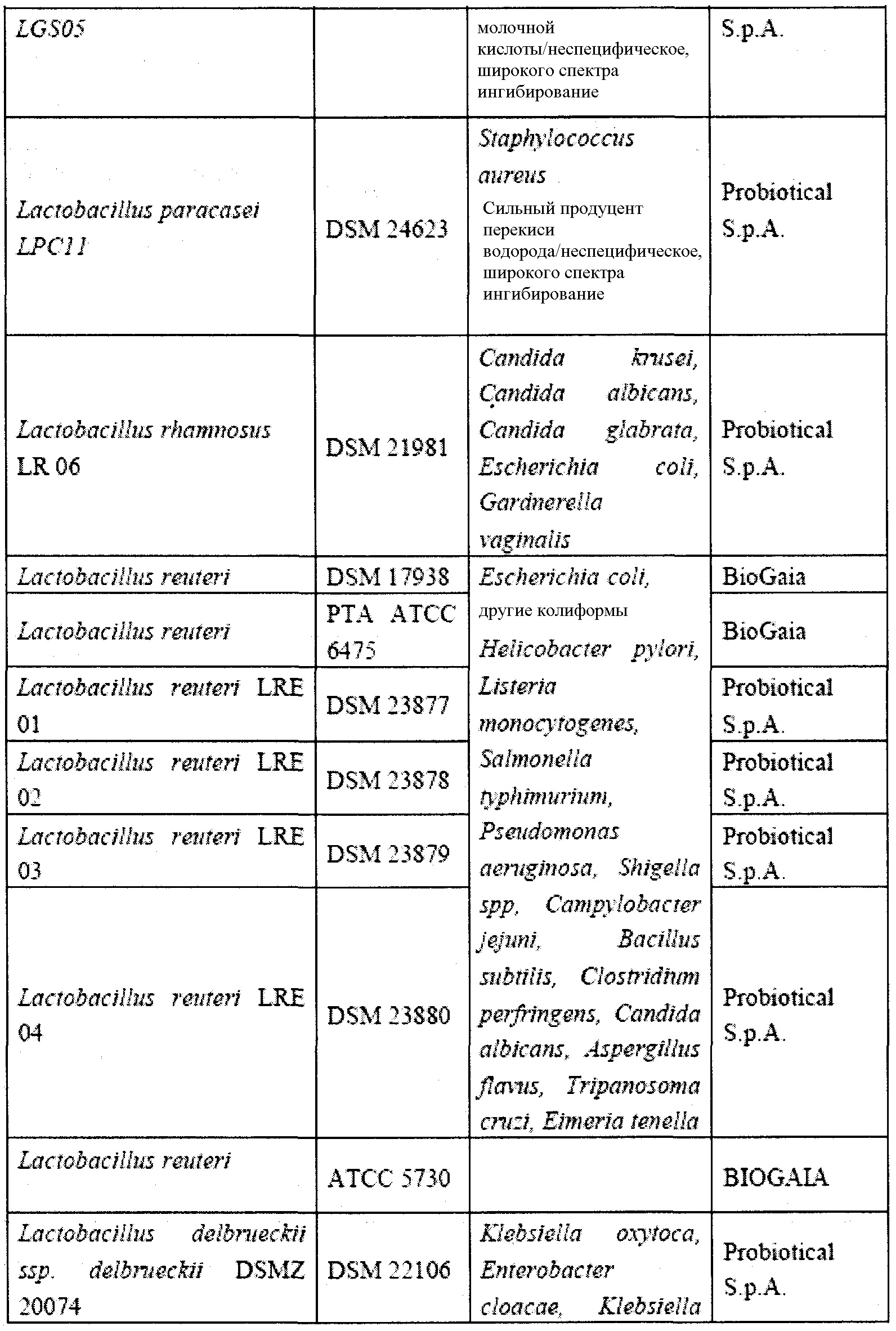
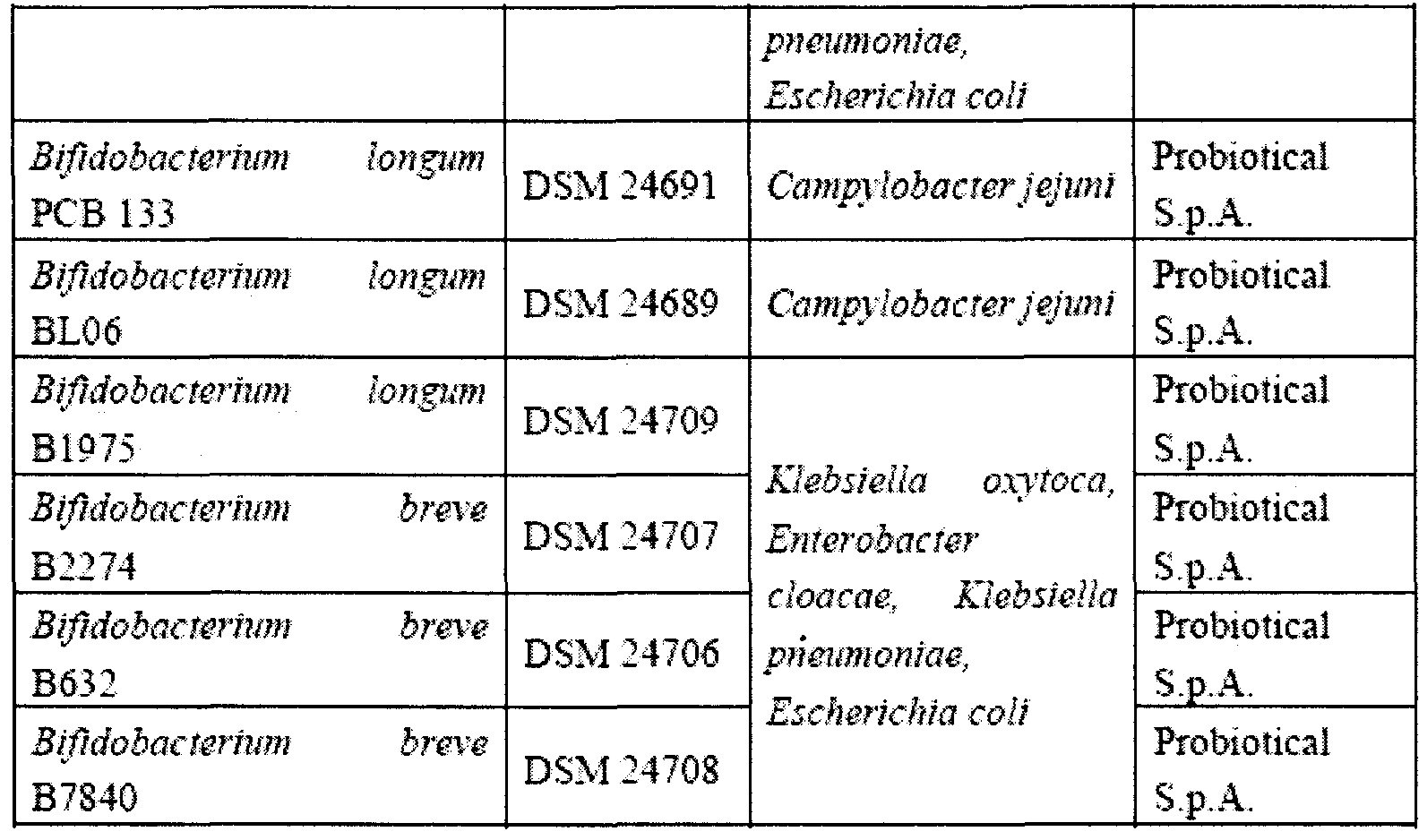
Штаммы из таблицы 2 изучали отдельно для определения патогена, которому они способны противодействовать (путем ингибирования роста или снижения численности одного или более видов/родов вредных или патогенных микроорганизмов), как показано в столбце 3 таблицы 2.
Таблица 2 демонстрирует, что бактерии способны продуцировать перекись водорода или по меньшей мере один бактериоцин с ингибирующей активностью в отношении одного или более видов/родов вредных или патогенных микроорганизмов.
Все штаммы, описанные и/или заявленные в настоящей патентной заявке, были депонированы в соответствии с Будапештским договором и сделаны доступными для общественности, по требованию, через уполномоченных ответственных лиц депозитария.
Композиции по настоящему изобретению можно эффективно применять как для лечения субъектов, принимающих препараты для снижения или лечения повышенной кислотности желудка, так и для лечения язв, вызванных нарушениями защитных механизмов слизистой оболочки (например, пониженная секреция или восприимчивость к простагландину Е, как в случае приема аспирина, или другим НПВП) или инфекцией H. pylori. Другими словами, композицию по настоящему изобретению могут применять также субъекты, которым прописаны PPI/другие антацидные препараты, хотя они и не страдают повышенной кислотностью желудка, но имеют повреждения слизистой оболочки желудка и/или двенадцатиперстной кишки, возникающие вследствие измененного соотношения между кислотностью желудочного сока и защитными механизмами слизистой оболочки.
В предпочтительном варианте осуществления композиция содержит от одного до шести штаммов, предпочтительно от двух до пяти штаммов, еще более предпочтительно три или четыре штамма, выбранных из группы, включающей или, альтернативно, состоящей из:
1. Lactobacillus pentosus LPS01 DSM 21980
2. Lactobacillus plantarum LP01 LMG P-21021
3. Lactobacillus plantarum LP02 LMG P-21020
4. Lactobacillus plantarum LP03 LMG P-21022
5. Lactobacillus plantarum LP04 LMG P-21023
6. Lactobacillus rhamnosus LR06 DSM 21981
7. Lactobacillus delbrueckii LDD 01 (MB386) DSM 20074
8. Bifidobacterium longum B1975 DSM 24709
9. Bifidobacterium breve B2274 DSM 24707
10. Bifidobacterium breve B632 DSM 24706
11. Bifidobacterium breve B7840 DSM 24708
12. Bifidobacterium longum PCB 133 DSM 24691
13. Bifidobacterium longum BL06 DSM 24689.
В другом предпочтительном варианте осуществления композиция по настоящему изобретению содержит от одного до шести штаммов, предпочтительно от двух до пяти штаммов, еще более предпочтительно три или четыре штамма, выбранных из тех, которые выше обозначены номерами от 1 до 13, в сочетании со штаммом Lactobacillus fermentum LF 09 DSM 18298 и/или штаммом Lactococcus lactis NS 01 DSM 19072.
В другом предпочтительном варианте осуществления композиция по настоящему изобретению содержит от одного до шести штаммов, предпочтительно от двух до пяти штаммов, еще более предпочтительно три или четыре штамма, выбранных из тех, которые выше обозначены номерами от 1 до 13, в сочетании с по меньшей мере одним штаммом, выбранным из группы, включающей или, альтернативно, состоящей из:
a. Lactobacillus reuteri LRE 01 DSM 23877
b. Lactobacillus reuteri LRE 02 DSM 23878
c. Lactobacillus reuteri LRE 03 DSM 23879
d. Lactobacillus reuteri LRE 04 DSM 23880
В композиции по настоящему изобретению смесь бактериальных штаммов присутствует в количестве, составляющем от 0,5 до 20% по массе относительно общей массы композиции, предпочтительно от 2,5 до 8%.
В предпочтительном варианте осуществления композиция может дополнительно содержать по меньшей мере одно пребиотическое волокно и/или углеводы с бифидогенным действием.
Пребиотическое волокно, которое находит применение в композиции по настоящему изобретению, представляет собой волокно, которое должно использоваться бактериальными штаммами, присутствующими в композиции, но не патогенами, которые они должны подавлять.
Если патоген, который следует подавлять, принадлежит к роду Candida, можно успешно использовать фруктоолигосахариды (ФОС) и галактоолигосахариды (ГОС), поскольку указанные волокна не используются Candida. При этом глюкоолигосахариды (ГОСα) способны непосредственно ингибировать E. coli посредством некоторых метаболитов.
Вследствие этого пребиотическое волокно можно выбирать в зависимости от обстоятельств и патогенов, которые предстоит подавлять, из: инулина, фруктоолигосахаридов (ФОС), галакто- и транс-галактоолигосахаридов (ГОС и ТОС), глюкоолигосахаридов (ГОСα), ксилоолигосахаридов (КОС), хитозанолигосахаридов (ХОС), соевых олигосахаридов (СОС), изомальтоолигосахаридов (ИМОС), стойкого крахмала, пектина, подорожника, арабиногалактанов, глюкоманнанов, галактоманнанов, ксиланов, лактосахарозы, лактулозы, лактитола и различных других типов камедей, гуммиарабика, волокон рожкового дерева, овса или бамбука, цитрусовых волокон и, в целом, волокон, имеющих растворимые и нерастворимые составляющие в различных соотношениях друг с другом.
В предпочтительном варианте осуществления изобретения композиция содержит по меньшей мере одно пребиотическое волокно, выбранное из числа упомянутых выше, и/или подходящие их смеси в любом относительном процентном содержании.
Количество пребиотических волокон и/или углеводов, имеющих бифидогенное действие, если они присутствуют в композиции, составляет от 0 до 60% по массе, предпочтительно от 5 до 45% и еще более предпочтительно от 10 до 30% относительно общей массы композиции. В этом случае композиция или добавка обладает симбиотической активностью и функциональными свойствами.
Кроме того, композиция может дополнительно содержать другие активные ингредиенты и/или компоненты, такие как витамины, минералы, биологически активные пептиды, вещества, обладающие антиоксидантной, снижающей уровень холестерина, снижающей уровень глюкозы, противовоспалительной или анти-подслащивающей активностью, в количестве по массе, как правило, составляющем от 0,001% до 20% по массе, предпочтительно от 0,01% до 5% относительно общей массы композиции, в любом случае в зависимости от типа активного компонента и его рекомендуемой суточной дозы, если таковая определена.
Пищевую композицию по настоящему изобретению, например, симбиотическую композицию или добавку, или фармацевтическую композицию, получают с использованием методов и оборудования, известных специалистам в данной области.
В предпочтительном варианте осуществления композиция содержит бактерии в концентрации, составляющей от 1×106 до 1×1011 КОЕ/г смеси, предпочтительно от 1×108 до 1×1010 КОЕ/г смеси.
В предпочтительном варианте осуществления композиция содержит бактерии в концентрации, составляющей от 1×106 до 1×1011 КОЕ/дозу, предпочтительно от 1×108 до 1×1010 КОЕ/дозу.
Доза может составлять от 0,2 до 10 г, например, она составляет 0,25 г, 1 г, 3 г, 5 г или 7 г.
Пробиотические бактерии, используемые в настоящем изобретении, могут быть в твердой форме, в частности в виде порошка, обезвоженного порошка, или в лиофилизированной форме. Все композиции по настоящему изобретению получают методами, известными специалистам в данной области, и с использованием известного оборудования.
В предпочтительном варианте осуществления композиция по настоящему изобретению дополнительно содержит лекарственное средство для снижения или лечения повышенной кислотности желудка.
В предпочтительном варианте осуществления указанное лекарственное средство выбирают из группы, включающей или, альтернативно, состоящей из:
- ингибиторов H2-рецепторов, предпочтительно циметидина, фамотидина, низатидина или ранитидина;
- простагландинов, предпочтительно мизопростола;
- протекторов слизистой оболочки желудка, предпочтительно солей висмута или сукральфата;
- мускариновых антагонистов или парасимпатолитических агентов, предпочтительно пирензепина или пипензолата;
- антацидов, предпочтительно натрия бикарбоната, алюминия гидроксида, магния гидроксида;
- ингибиторов протонного насоса, предпочтительно лансопразола, эзомепразола, рабепразола, пантопразола и омепразола.
Предпочтительно указанное лекарственное средство выбирают из группы, включающей или, альтернативно, состоящей из:
- ингибиторов H2-рецепторов, предпочтительно циметидина, фамотидина, низатидина или ранитидина;
- мускариновых антагонистов или парасимпатолитических агентов, предпочтительно пирензепина или пипензолата;
- антацидов, предпочтительно натрия бикарбоната, алюминия гидроксида, магния гидроксида;
- ингибиторов протонного насоса, предпочтительно выбранных из группы, включающей лансопразол, эзомепразол, рабепразол, пантопразол и омепразол.
Еще более предпочтительно указанное лекарственное средство выбирают из группы, включающей или, альтернативно, состоящей из:
- ингибиторов H2-рецепторов, предпочтительно циметидина, фамотидина, низатидина или ранитидина;
- ингибиторов протонного насоса, предпочтительно выбранных из группы, включающей лансопразол, эзомепразол, рабепразол, пантопразол и омепразол.
В предпочтительном варианте осуществления композиция по настоящему изобретению представляет собой фармацевтическую композицию, содержащую бактерии, приведенные в таблице 1 или таблице 2, или в предпочтительных вариантах осуществления, изложенных выше, указанные бактерии находятся в сочетании с препаратом, показанным для снижения или лечения повышенной кислотности желудка, указанным выше. Предпочтительно лекарственное средство представляет собой ингибитор протонного насоса, выбранный из группы, включающей лансопразол, эзомепразол, рабепразол, пантопразол и омепразол. Как бактерии, так и лекарственное средство непосредственно присутствуют в одной и той же композиции. Например, бактерии и лекарственное средство присутствуют вместе в таблетке, пастилке или гранулах в фармацевтической форме, подходящей для перорального введения.
Важно, чтобы бактерии и лекарственное средство были введены одновременно и действовали одновременно, так как необходимо восстанавливать барьерный эффект, утраченный из-за ингибиторов протонного насоса (PPI), при помощи активности пробиотичесих бактерий по настоящему изобретению, которые продуцируют бактериоцины и способны колонизировать желудок благодаря тому, что ингибиторы протонного насоса повысили рН до значения примерно 4,5-5,0.
В другом предпочтительном варианте осуществления композиция по настоящему изобретению находится в виде медицинского устройства. В этом случае бактерии присутствуют в композиции, подходящей для перорального введения, такой как, например, таблетка, пастилка или гранулы, отдельно, и лекарственное средство, показанное для снижения или лечения повышенной кислотности желудка, указанное выше, присутствует в другой композиции, подходящей для перорального введения. Предпочтительно лекарственное средство представляет собой ингибитор протонного насоса, выбранный из группы, включающей лансопразол, эзомепразол, рабепразол, пантопразол и омепразол.
Таким образом, например, вводят две таблетки, одну, содержащую бактерии, и другую, содержащую лекарственное средство.
В любом случае, две таблетки должны быть введены одновременно, учитывая, что необходимо, чтобы бактерии действовали одновременно с ингибиторами протонного насоса.
В случае медицинских устройств также важно, чтобы бактерии и лекарственное средство были введены друг за другом в течение короткого промежутка времени, так как необходимо восстанавливать барьерный эффект, утраченный из-за ингибиторов протонного насоса (PPI), при помощи активности пробиотичесих бактерий по настоящему изобретению, которые продуцируют бактериоцины и способны колонизировать желудок благодаря тому, что ингибиторы протонного насоса повысили рН до значения примерно 4,5-5,0.
Автор изобретения обнаружил, что бактерии, выбранные и перечисленные в таблице 1 или таблице 2, либо в предпочтительных вариантах осуществления, указанных выше, способны колонизировать желудок при значении рН около 5 таким образом, что восстанавливается барьерный эффект, сниженный или утраченный в результате повышения значения pH вследствие действия лекарственных средств, показанных для снижения или лечения повышенной кислотности желудка, таких как, например, препарат - ингибитор протонного насоса, выбранный из группы, включающей лансопразол, эзомепразол, рабепразол, пантопразол и омепразол.
В предпочтительном варианте осуществления композиция, содержащая пробиотические бактериальные штаммы по настоящему изобретению - указанные штаммы способны производить определенные бактериоцины - также полезна в качестве вспомогательного средства при лечении, направленном на окончательное избавление от Helicobacter pylori и на предотвращение ее повторного появления.
Таким образом, предметом настоящего изобретения является композиция, содержащая по меньшей мере один штамм бактерий, перечисленных в таблице 1 или в таблице 2, или в одном из вариантов осуществления, упомянутых выше, для применения в профилактическом и/или терапевтическом лечении инфекций, расстройств или заболеваний, вызванных присутствием Helicobacter pylori, в частности, в профилактическом и/или терапевтическом лечении рецидивов инфекций, вызванных Helicobacter pylori.
В самом широком смысле этого термина, антибиотики определяют как виды молекул, которые производятся микроорганизмами и активно противодействуют росту других микроорганизмов. На практике, однако, антибиотики обычно считаются вторичными метаболитами, которые активны при низких концентрациях для блокирования роста микроорганизмов. Вторичные продукты метаболизма, такие как органические кислоты, аммиак и перекись водорода, не следует включать в категорию антибиотиков. Антибиотики представляют собой молекулы, также пептидные молекулы (пенициллин), продуцируемые мультиферментными системами, биосинтез которых не блокируется ингибиторами белкового синтеза. Бактериоцины, с другой стороны, являются продуктами рибосомного синтеза.
Бактериоцины представляют собой пептидные молекулы, синтезируемые с помощью рибосомы, которые также могут быть связаны с липидами или углеводами. Хотя некоторые бактериоцины, продуцируемые грамположительными бактериями (Lactobacillus, Lactococcus), имеют спектр ингибирования, ограниченный некоторыми штаммами, принадлежащими к тем же видам, что и микроорганизм-продуцент, большинство из них демонстрирует широкий спектр действия против различных бактериальных видов, как грамположительных, так и грамотрицательных. Современная классификация бактериоцинов основана как на их химической природе, так и на спектре действия.

