Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ ПИРИМИДИН-1-ОЛОВОГО СОЕДИНЕНИЯ И ЕГО ПРОМЕЖУТОЧНОГО СОЕДИНЕНИЯ
Вид РИД
Изобретение
[Область техники, к которой относится изобретение]
[0001]
Настоящее изобретение относится к способу получения 2,4-дизамещенного пиримидин-5-ола, который является ключевым промежуточным соединением для получения соединения, которое обладает антагонистическим действием по отношению к рецептору орексина и является пригодным в качестве средства для лечения бессонницы, и промежуточного соединения для его получения.
[Уровень техники]
[0002]
Было обнаружено, что два типа интрацеребральных нейропептидов, орексин-A (OX-A, пептид, состоящий из 33 аминокислот) и орексин-B (OX-B, пептид, состоящий из 28 аминокислот), экспрессируемые в нейронах, локализованных в гипоталамусе головного мозга, являются эндогенными лигандами (источник 5 патентной литературы и источник 1 непатентной литературы) сопряженных с G-белком рецепторов, преимущественно находящихся в головном мозге, т. е., рецепторов орексина (источник 1 патентной литературы, источник 2 патентной литературы, источник 3 патентной литературы и источник 4 патентной литературы). Известно, что рецепторы орексина включают два подтипа, рецептор OX1 (OX1) в качестве типа 1 подтипа и рецептор OX2 (OX2) в качестве типа 2 подтипа. OX1 более селективно связывается с OX-A по сравнению с OX-B, и OX2 связывается с OX-A аналогично OX-B. Было обнаружено, что орексины стимулируют потребление пищи у крыс, и было предположено, что орексины будут выполнять физиологические функции в качестве медиаторов в центральном механизме обратной связи для контроля пищевого поведения (источник 1 непатентной литературы). С другой стороны, было отмечено, что орексины также регулируют состояния сна и бодрствования, и, следовательно, считают, что орексины могут привести к новому способу лечения нарколепсии, а также бессонницы и других нарушений сна (источник 2 непатентной литературы). Кроме того, было предположено, что орексиновые сигналы в вентральной тегментальной области, ассоциированные с наркоманией и никотиновой зависимостью, выполняют важную функцию в нейропластичности in vivo (источник 3 непатентной литературы и источник 4 непатентной литературы). Вместе с тем, сообщалось, что если OX2 селективно ингибируется в эксперименте с использованием крыс, то снижается зависимость от этанола (источник 5 непатентной литературы). Более того, сообщалось, что рилизинг-фактор кортикотропина (CRF), ассоциированный с депрессией и тревожным расстройством у крыс, вызывает орексин-индуцированную активность, и существует возможность того, что орексины выполняют важные функции в реакции на стресс (источник 6 непатентной литературы).
[0003]
5-Хлор-2-{(5R)-5-метил-4-[5-метил-2-(2H-1,2,3-триазол-2-ил)бензоил]-1,4-диазепан-1-ил}-1,3-бензоксазол (MK-4305; суворексант, источник 6 патентной литературы), обладающий двойным антагонистическим действием по отношению к рецепторам орексина для OX1 и OX2, недавно поступил в продажу в качестве терапевтического средства от бессонницы. Кроме того, E2006 (лемборексант) был клинически усовершенствован.
[0004]
В источнике 7 патентной литературы соединение, представленное следующей формулой, или его фармацевтически приемлемая соль в значительной степени описано в качестве соединения, которое характеризуется антагонистическим действием по отношению к рецептору орексина и, как ожидается, обладает эффектом в лечении бессонницы.
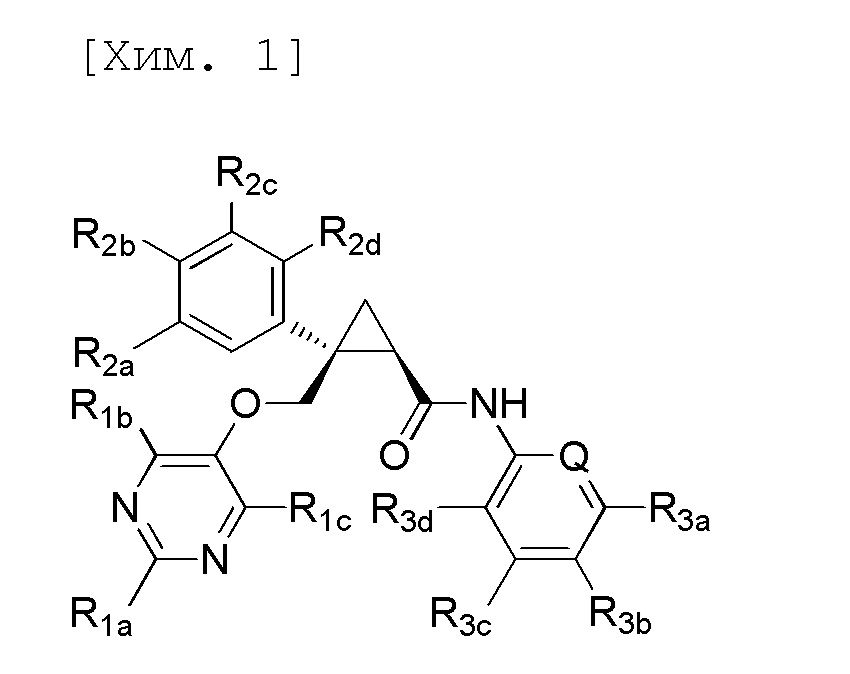
[В формуле Q представляет собой -CH- или атом азота, каждый из R1a и R1b независимо представляет собой, например, C1-6алкильную группу, R1c представляет собой атом водорода, каждый из R2a, R2b, R2c и R2d независимо представляет собой атом водорода или атом галогена, каждый из R3a, R3b и R3c независимо представляет собой атом водорода или атом галогена, и R3d представляет собой атом водорода].
[0005]
В том числе соединение, представленное следующей формулой (A), которое можно получать посредством следующего способа, описано в источнике 8 патентной литературы.
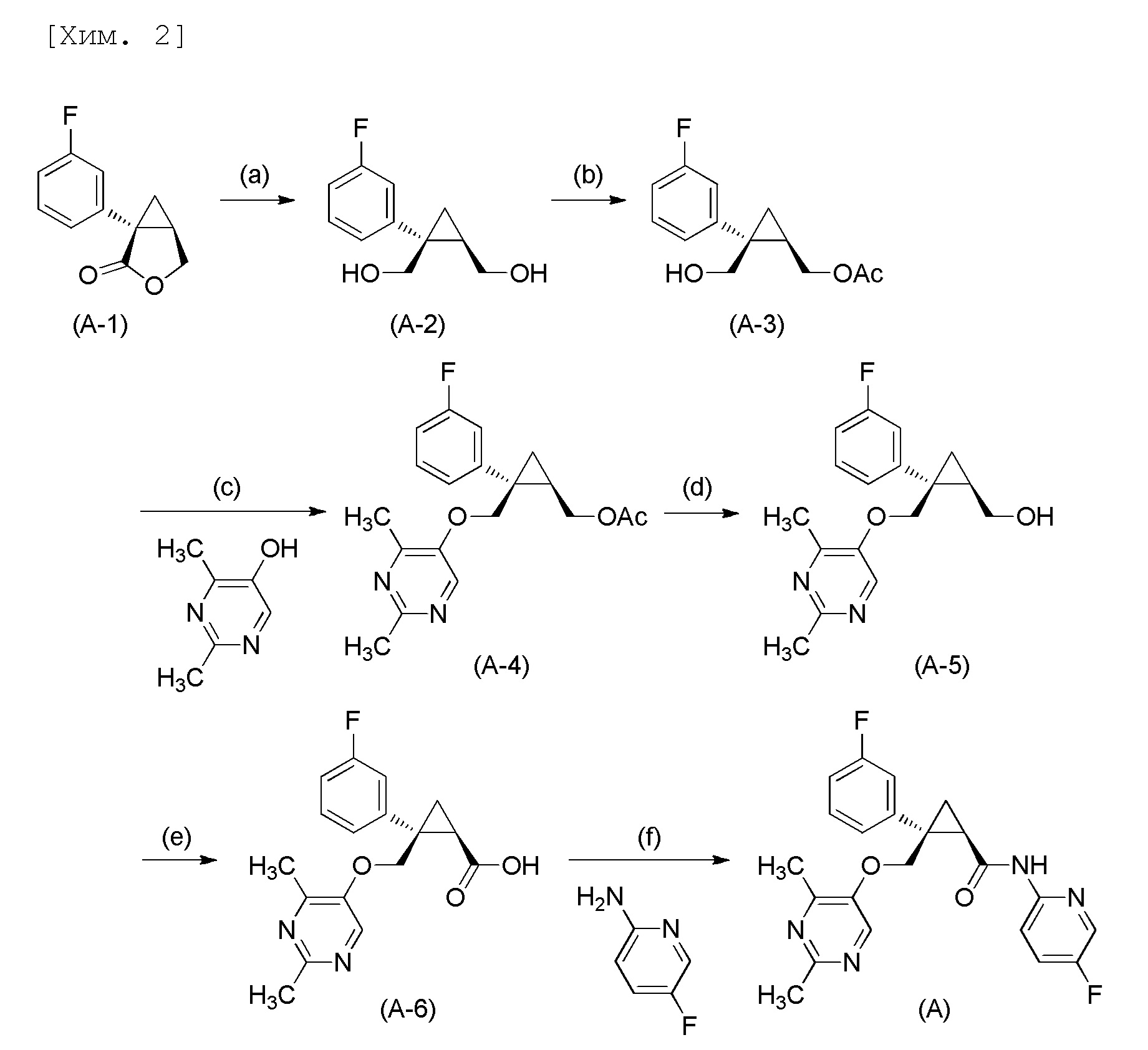
[В формулах Ac представляет собой ацетильную группу].
(1R,2S)-2-{[(2,4-диметилпиримидин-5-ил)окси]метил}-2-(3-фторфенил)циклопропилметанол (A-5), получаемый в вышеуказанном способе получения, можно получать посредством осуществления реакции {(1R, 2S)-2-(3-фторфенил)-2-[(тозилокси)метил]циклопропил}метилацетата, получаемого из соединения (A-3), с 2,4-диметилпиримидин-5-олом (стадия (g)) и последующего гидролиза (стадия (d)), как показано на следующих стадиях.
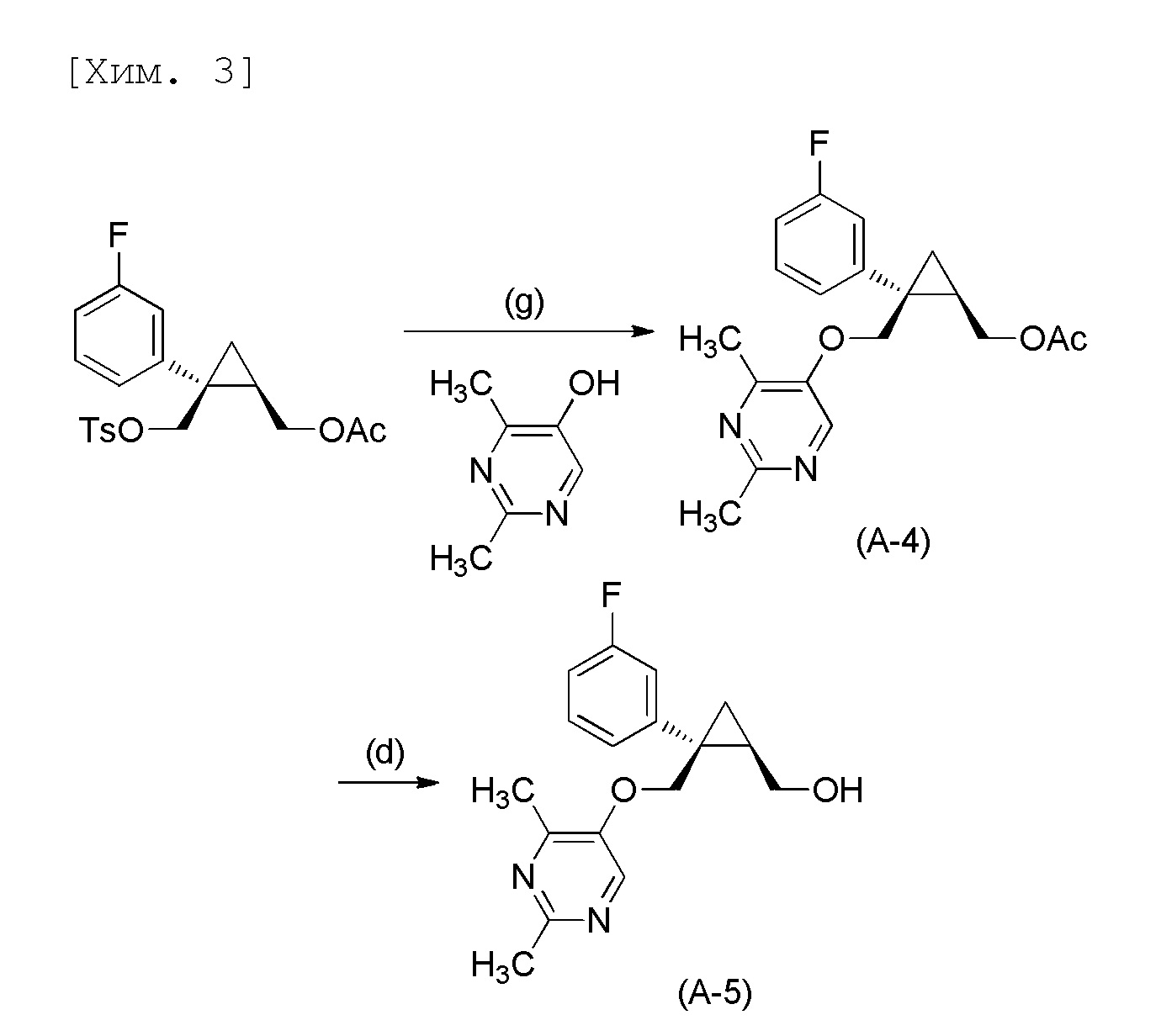
[В формулах Ac представляет собой ацетильную группу, и Ts представляет собой п-толуолсульфонильную группу].
[Перечень ссылок]
[Источник патентной литературы]
[0006]
[Источник 1 патентной литературы]
Международная публикация PCT № WO 1996/34877
[Источник 2 патентной литературы]
Нерассмотренная заявка на патент Японии, публикация № H10-327888
[Источник 3 патентной литературы]
Нерассмотренная заявка на патент Японии, публикация № H10-327889
[Источник 4 патентной литературы]
Нерассмотренная заявка на патент Японии, публикация № H11-178588
[Источник 5 патентной литературы]
Нерассмотренная заявка на патент Японии, публикация № H10-229887
[Источник 6 патентной литературы]
Международная публикация PCT № WO 2008/069997
[Источник 7 патентной литературы]
Международная публикация PCT № WO 2012/039371
[Источник 8 патентной литературы]
Международная публикация PCT № WO 2013/123240
[Непатентная литература]
[0007]
[Источник 1 непатентной литературы]
Sakurai T. et al., Cell, 1998, 92, 573-585
[Источник 2 непатентной литературы]
Chemelli R. M. et al., Cell, 1999, 98, 437-451
[Источник 3 непатентной литературы]
S.L. Borgland et al., Neuron, 2006, 49, 589-601
[Источник 4 непатентной литературы]
C.J. Winrow et al., Neuropharmacology, 2010, 58, 185-194
[Источник 5 непатентной литературы]
J.R. Shoblock et al., Psychopharmacology, 2010, 215:191-203
[Источник 6 непатентной литературы]
T. Ida et al., Biochemical and Biophysical Research Communications, 2000, 270, 318-323
[Краткое описание изобретения]
[Техническая задача]
[0008]
В примере получения 4 в источнике 7 патентной литературы описан способ получения 2,4-диметилпиримидин-5-ола с использованием 2,4-дихлор-5-метоксипиримидина в качестве исходного материала.
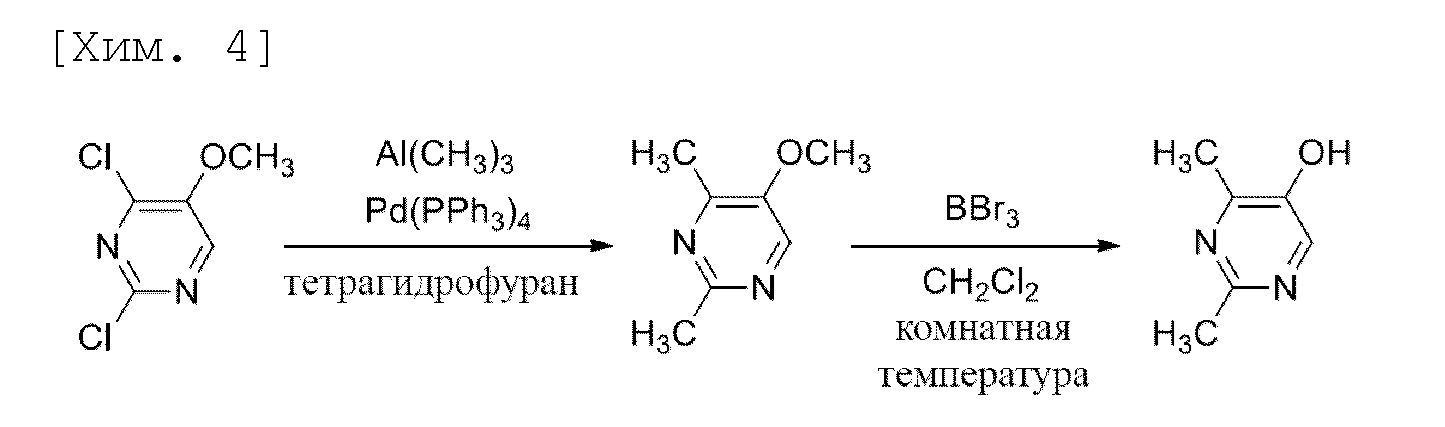
В способе получения 2,4-дихлор-5-метоксипиримидин, выступающий в качестве исходного материала, является дорогим, 2,4-диметил-5-метоксипиримидин, получаемый в качестве промежуточного соединения, является летучим, триметилалюминий, применяемый в качестве реагента, вызывает проблемы со здоровьем, такие как жжение и раздражение кожи, и обладает риском самовоспламенения, и трибромид бора также вызывает проблемы со здоровьем, такие как жжение и раздражение кожи, и требует аккуратного обращения. Следовательно, способ получения имеет проблемы при применении в промышленном производстве.
[0009]
На страницах 66-69 в источнике 8 патентной литературы описан способ получения 2,4-диметилпиримидин-5-ола с использованием 2,4-дихлор-5-метоксипиримидина в качестве исходного материала.
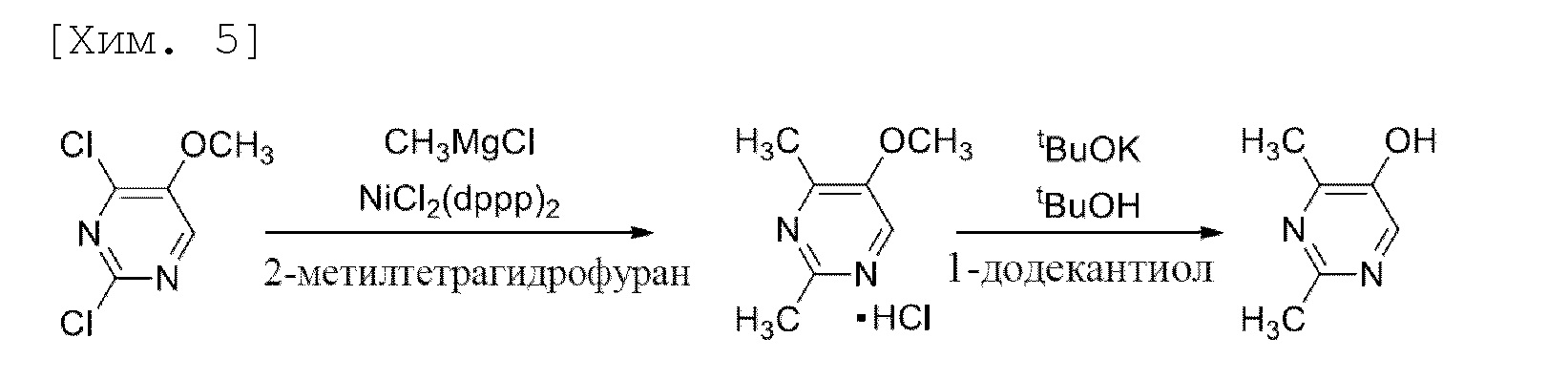
Способ получения также имеет проблемы, такие как дороговизна применяемого в качестве исходного материала 2,4-дихлор-5-метоксипиримидина, и то, что 2,4-диметил-5-метоксипиримидина гидрохлорид, получаемый в качестве промежуточного соединения, характеризуется гигроскопичностью. Кроме того, для применения способа получения в промышленном производстве существуют проблемы, например, трудно контролировать примеси, гидрогенизированные по 2- или 4-положению, при метилировании по 2-положению и 4-положению пиримидина, с использованием хлорида метилмагния.
[0010]
Следовательно, целью настоящего изобретения является создание способа получения 2,4-дизамещенного пиримидин-5-ола и, в частности, 2,4-диметилпиримидин-5-ола, применяемого в промышленном производстве.
[Решение задачи]
[0011]
Настоящее изобретение включает следующие аспекты.
[0012]
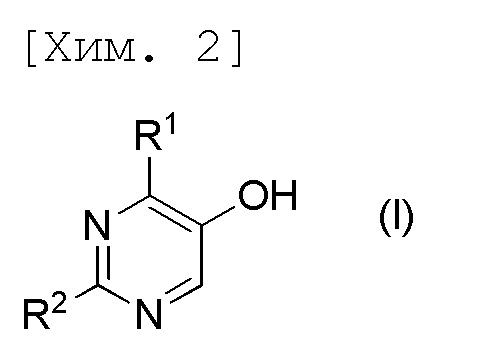
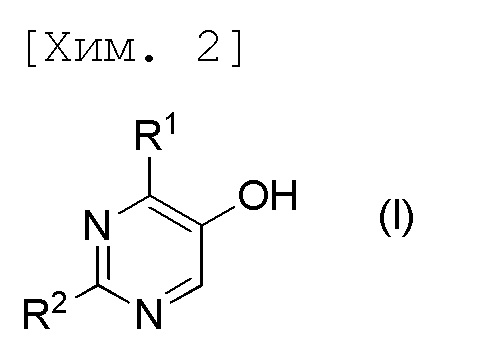
[1] Способ получения соединения формулы (I) или его соли,
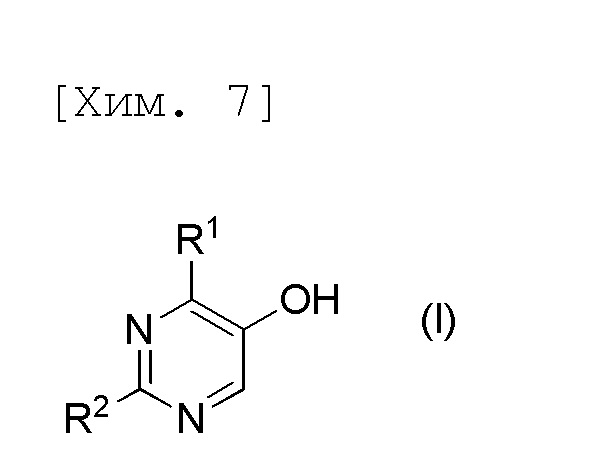
[причем в формуле R1 и R2 представляют собой C1-6алкильные группы, которые являются одинаковыми или отличаются друг от друга], включающий
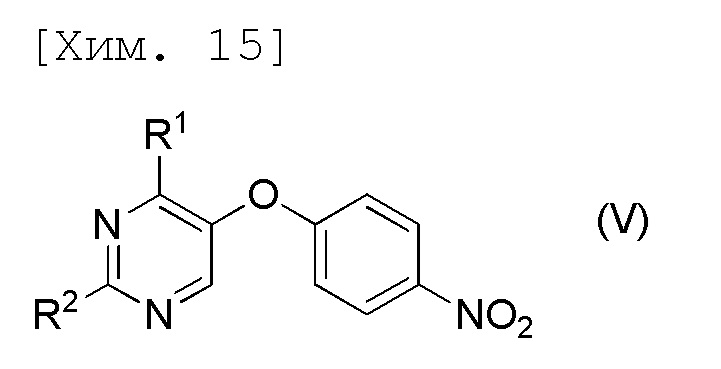
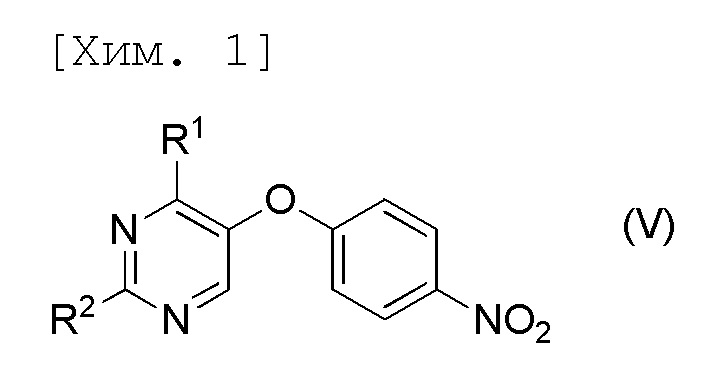
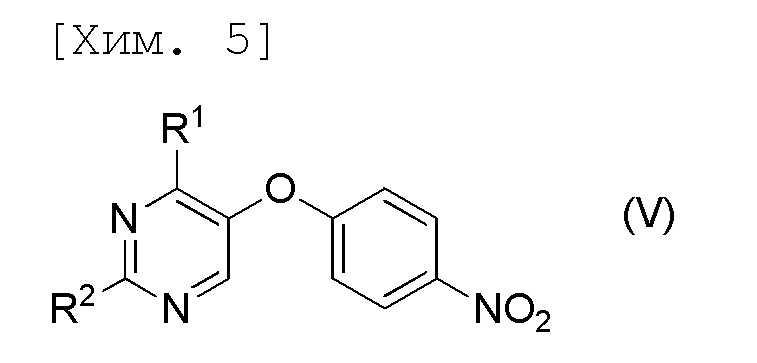
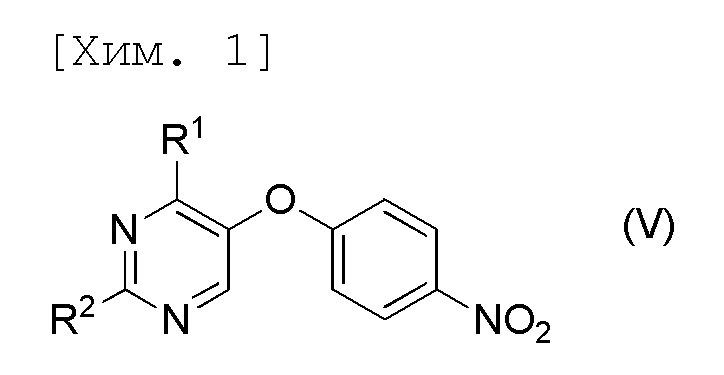
стадию осуществления гидролиза соединения формулы (V) или его соли,
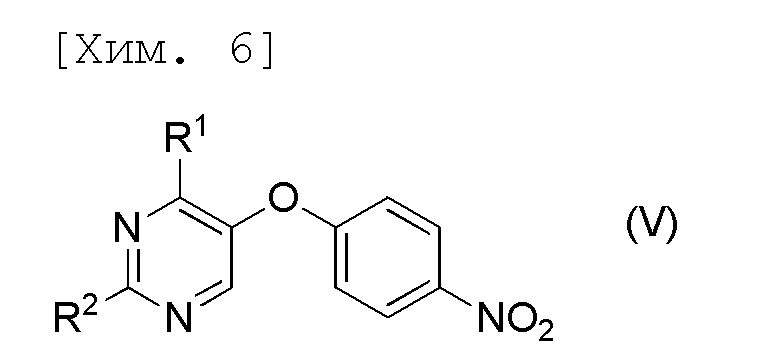
[причем в формуле R1 и R2 представляют собой C1-6алкильные группы, которые являются одинаковыми или отличными друг от друга].
[0013]
[2] Способ получения в соответствии с [1], включающий
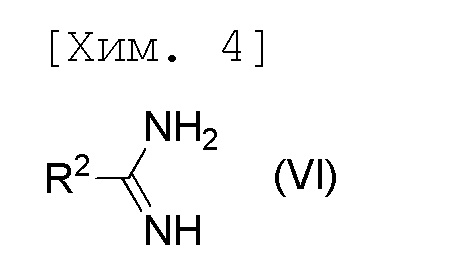
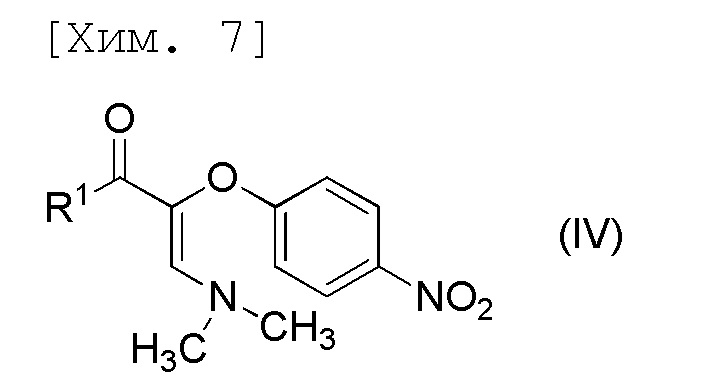
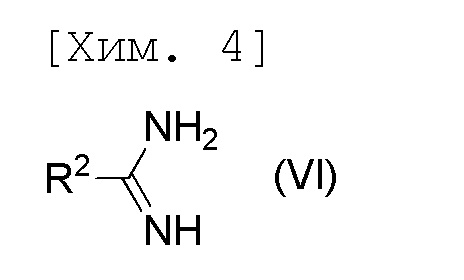
стадию получения соединения формулы (V) или его соли посредством осуществления реакции соединения формулы (IV) или его соли с соединением формулы (VI) или его солью,
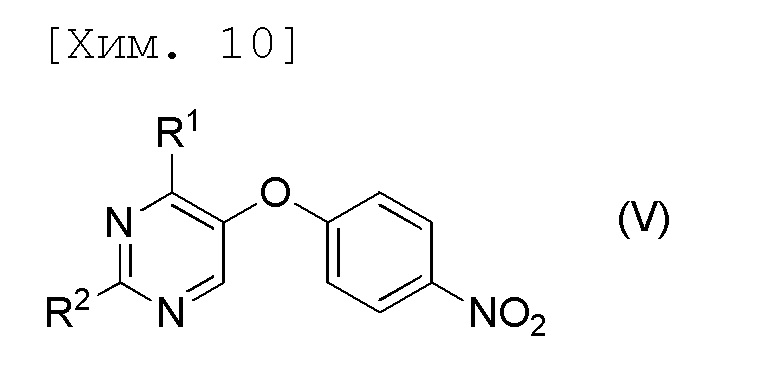
[причем в формуле R1 и R2 представляют собой C1-6алкильные группы, которые являются одинаковыми или отличными друг от друга].
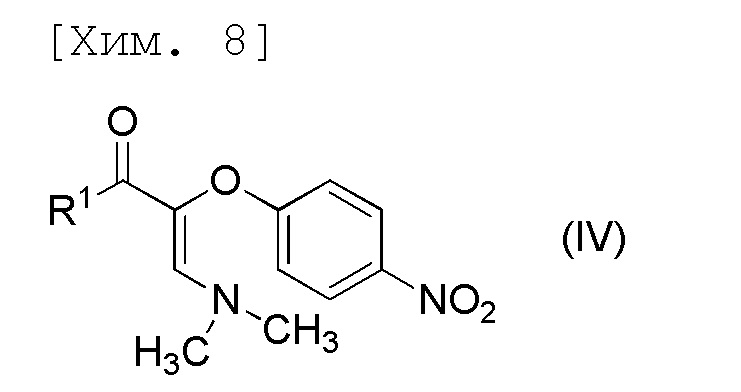
[причем в формуле R1 представляет собой C1-6алкильную группу],
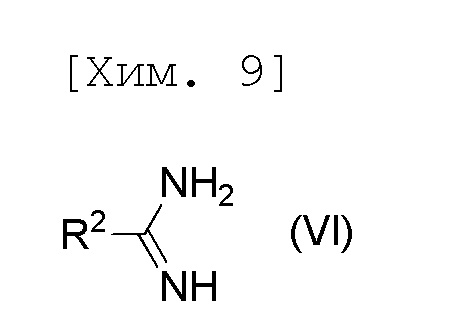
[причем в формуле R2 представляет собой C1-6алкильную группу], и
стадию осуществления гидролиза соединения формулы (V) или его соли.
[0014]
[3] Способ получения в соответствии с [1], включающий
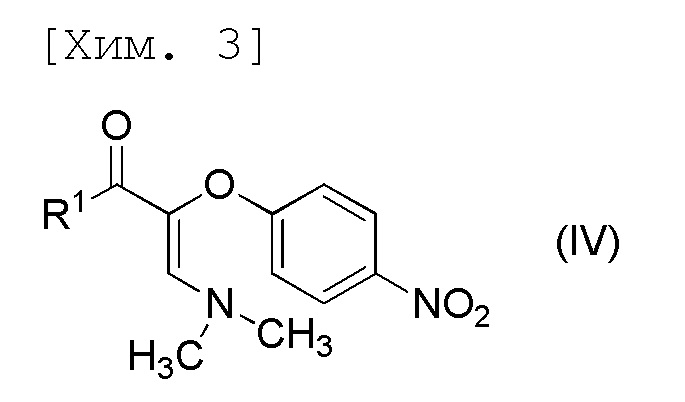
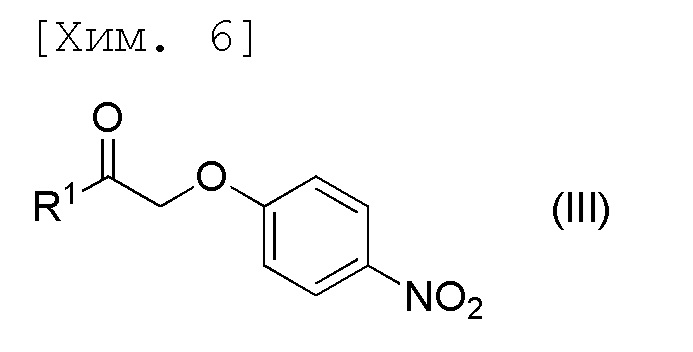
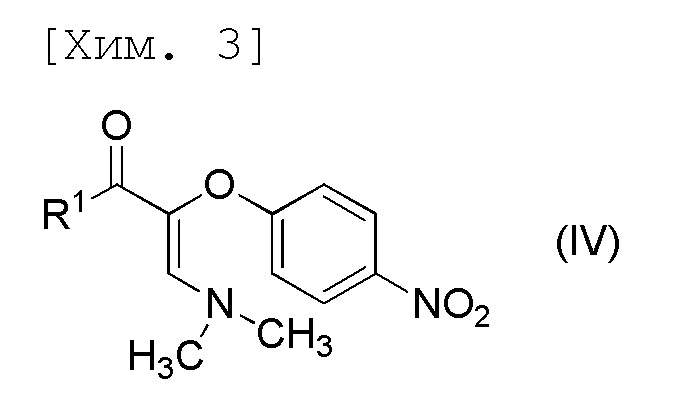
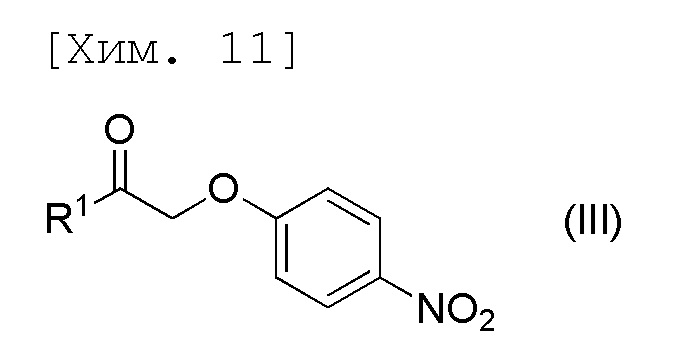
стадию получения соединения формулы (IV) или его соли посредством осуществления реакции соединения формулы (III) с N,N-диметилформамиддиметилацеталем,
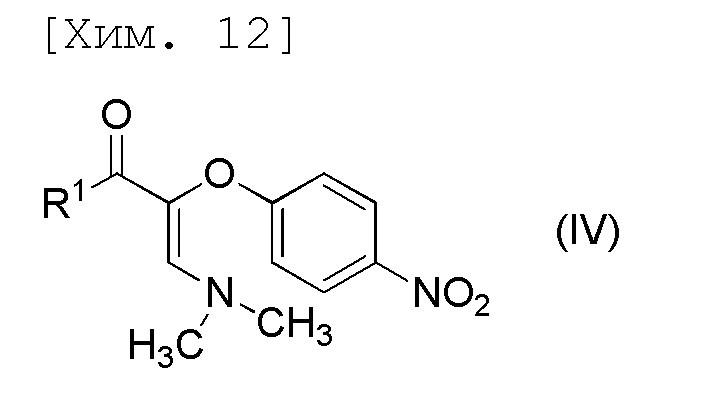
[причем в формуле R1 представляет собой C1-6алкильную группу],
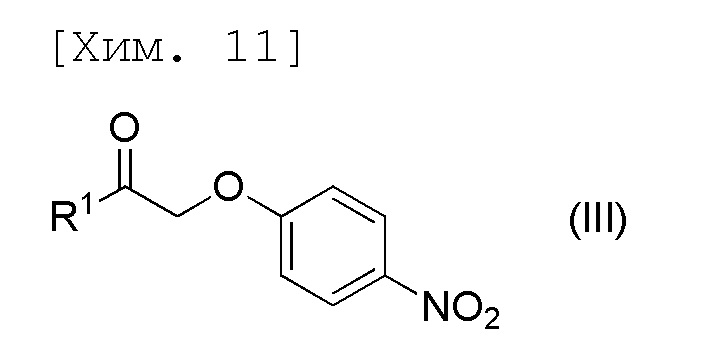
[причем в формуле R1 представляет собой C1-6алкильную группу],
стадию получения соединения формулы (V) или его соли посредством осуществления реакции соединения формулы (IV) или его соли с соединением формулы (VI) или его солью,
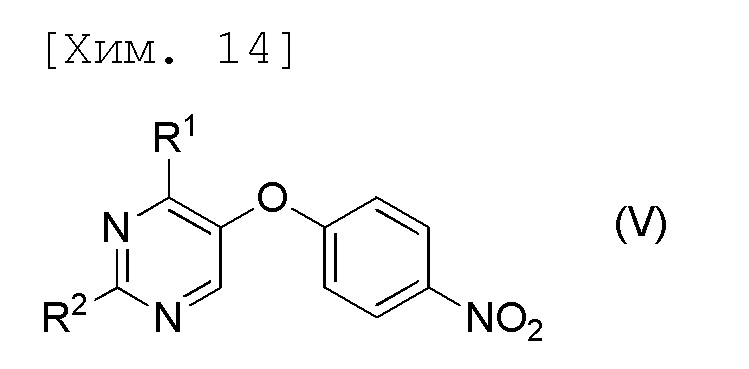
[причем в формуле R1 и R2 представляют собой C1-6алкильные группы, которые являются одинаковыми или отличными друг от друга].
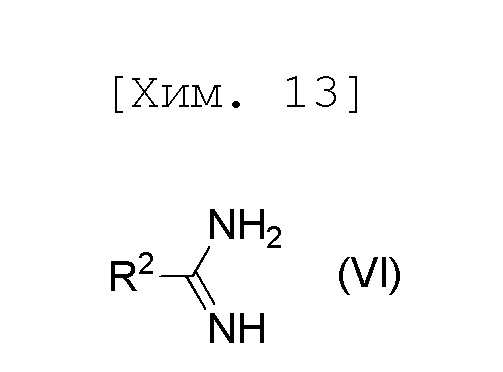
[причем в формуле R2 представляет собой C1-6алкильную группу], и
стадию осуществления гидролиза соединения формулы (V) или его соли.
[0015]
[4] Способ получения в соответствии с [1], включающий
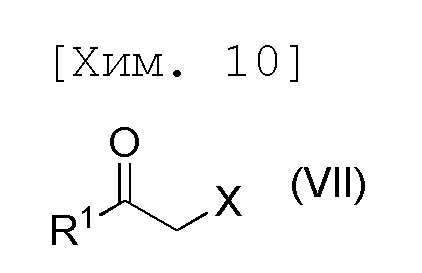
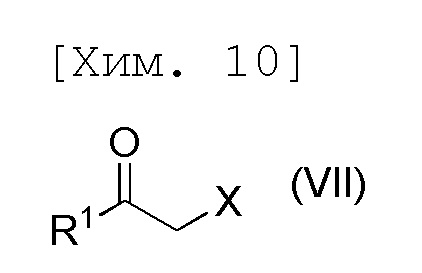
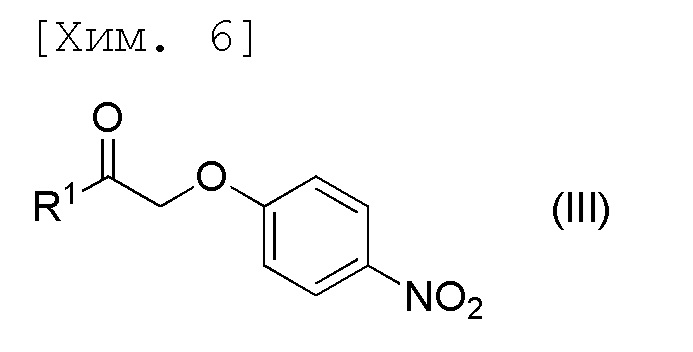
стадию получения соединения формулы (III) посредством осуществления реакции 4-нитрофенола с соединением формулы (VII),
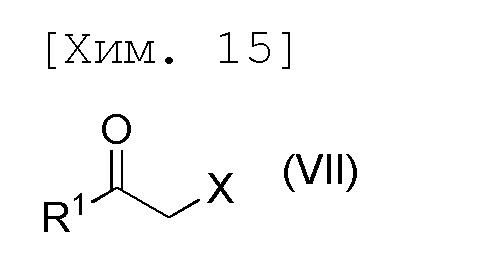
[причем в формуле X представляет собой хлор или бром, и R1 представляет собой C1-6алкильную группу],
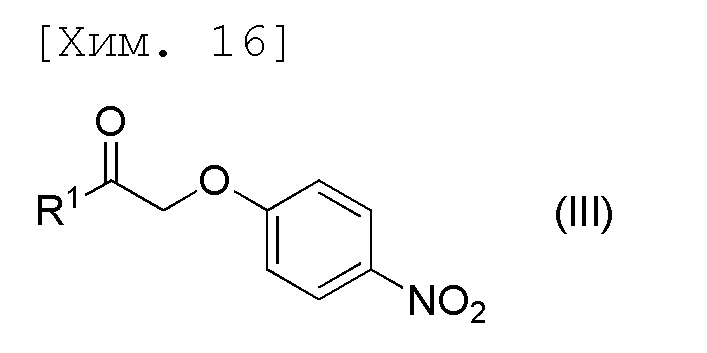
[причем в формуле R1 представляет собой C1-6алкильную группу],
стадию получения соединения формулы (IV) или его соли посредством осуществления реакции соединения формулы (III) с N,N-диметилформамиддиметилацеталем,
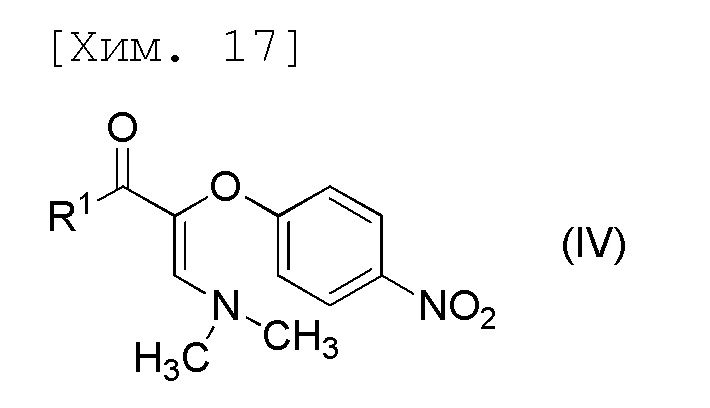
[причем в формуле R1 представляет собой C1-6алкильную группу],
стадию получения соединения формулы (V) или его соли посредством осуществления реакции соединения формулы (IV) или его соли с соединением формулы (VI) или его солью,
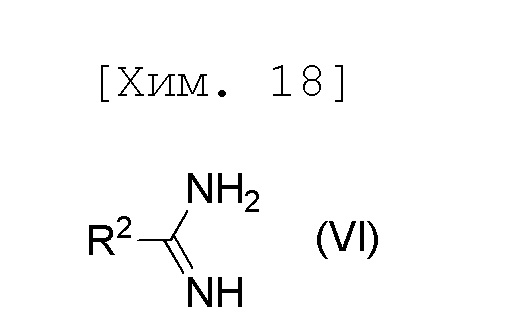
[причем в формуле R2 представляет собой C1-6алкильную группу],
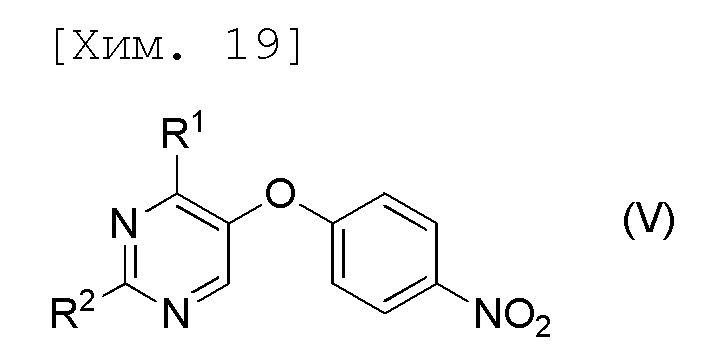
[причем в формуле R1 и R2 представляют собой C1-6алкильные группы, которые являются одинаковыми или отличными друг от друга], и
стадию осуществления гидролиза соединения формулы (V) или его соли.
[0016]
[5] Способ получения по любому из [1] - [4],
где как R1, так и R2 представляют собой метильные группы.
[0017]
[6] Соединение, представленное формулой (V), или его соль,
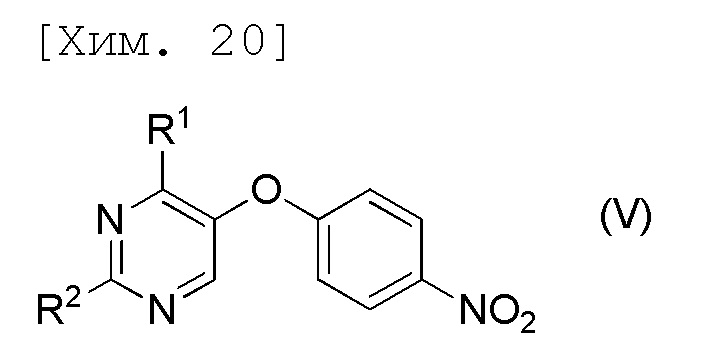
[причем в формуле R1 и R2 представляют собой C1-6алкильные группы, которые являются одинаковыми или отличными друг от друга].
[0018]
[7] Соединение или его соль в соответствии с [6],
где как R1, так и R2 представляют собой метильные группы.
[Предпочтительные эффекты настоящего изобретения]
[0019]
В настоящем изобретении предусматривают способ получения 2,4-дизамещенного пиримидин-5-ола, который является промежуточным соединением для получения соединения, которое обладает антагонистическим действием по отношению к рецептору орексина и является пригодным в качестве средства для лечения бессонницы, и его промежуточного соединения. В способе получения настоящего изобретения можно применять недорогой и легкодоступный исходный материал, при этом региоселективность замещающей группы легко контролируема, и примеси легко контролируемы, и 2,4-дизамещенный пиримидин-5-ол можно получать без применения реагентов и промежуточных соединений, вызывающих проблемы со здоровьем, риски и т. п. Следовательно, способ получения подходит для промышленного производства.
[Описание вариантов осуществления]
[0020]
Далее в данном документе будут описаны значения обозначений, терминов и т. п., описываемых в настоящем описании, и будет подробно описано настоящее изобретение.
[0021]
В настоящем описании структурные формулы соединений не ограничены формулами, описанными для удобства, и могут образовывать соли. Кроме того, может быть представлен, но не ограничен подобным образом, полиморфизм кристаллов и может быть обеспечена какая-либо отдельная кристаллическая форма или ее смесь. Может быть обеспечен гидрат или сольват, отличный от ангидрида, и все из них включены в настоящее изобретение.
[0022]
В настоящем описании, если не указано иное, конкретные примеры соли включают соли галогеноводородных кислот (например, гидрофторид, гидрохлорид, гидробромид и гидройодид) и соли неорганических кислот (например, сульфат, нитрат, перхлорат, фосфат, карбонат и бикарбонат).
[0023]
Настоящее изобретение включает изотопно-меченое соединение описанного в настоящем описании соединения и способ получения с его применением. Изотопно-меченое соединение является таким же, что и соединение, описанное в настоящем описании, за исключением того, что один или несколько атомов заменены атомами, атомная масса и массовое число которых отличаются от тех, что обычно обнаруживают в природе. Изотопы, которые могут быть включены в соединение в соответствии с настоящим изобретением, являются изотопами водорода, углерода, азота, кислорода и фтора соединения, и включают 2H, 3H, 11C, 13C, 14C, 13N, 15O и 18F.
[0024]
"C1-6алкильная группа" в R1 и R2 представляет собой линейную или разветвленную алкильную группу, содержащую 1-6 атомов углерода, и включает, например, линейные или разветвленные алкильные группы, такие как метильная группа, этильная группа, н-пропильная группа, изопропильная группа, н-бутильная группа, изобутильная группа, трет-бутильная группа, н-пентильная группа, изопентильная группа, неопентильная группа, н-гексильная группа, 1-метилпропильная группа, 1,2-диметилпропильная группа, 1-этилпропильная группа, 1-метил-2-этилпропильная группа, 1-этил-2-метилпропильная группа, 1,1,2-триметилпропильная группа, 1-метилбутильная группа, 2-метилбутильная группа, 1,1-диметилбутильная группа, 2,2-диметилбутильная группа, 2-этилбутильная группа, 1,3-диметилбутильная группа, 2-метилпентильная группа и 3-метилпентильная группа. В качестве другого аспекта, проиллюстрированы метильная группа, этильная группа, н-пропильная группа и т. п. В качестве еще одного аспекта, проиллюстрирована метильная группа.
[0025]
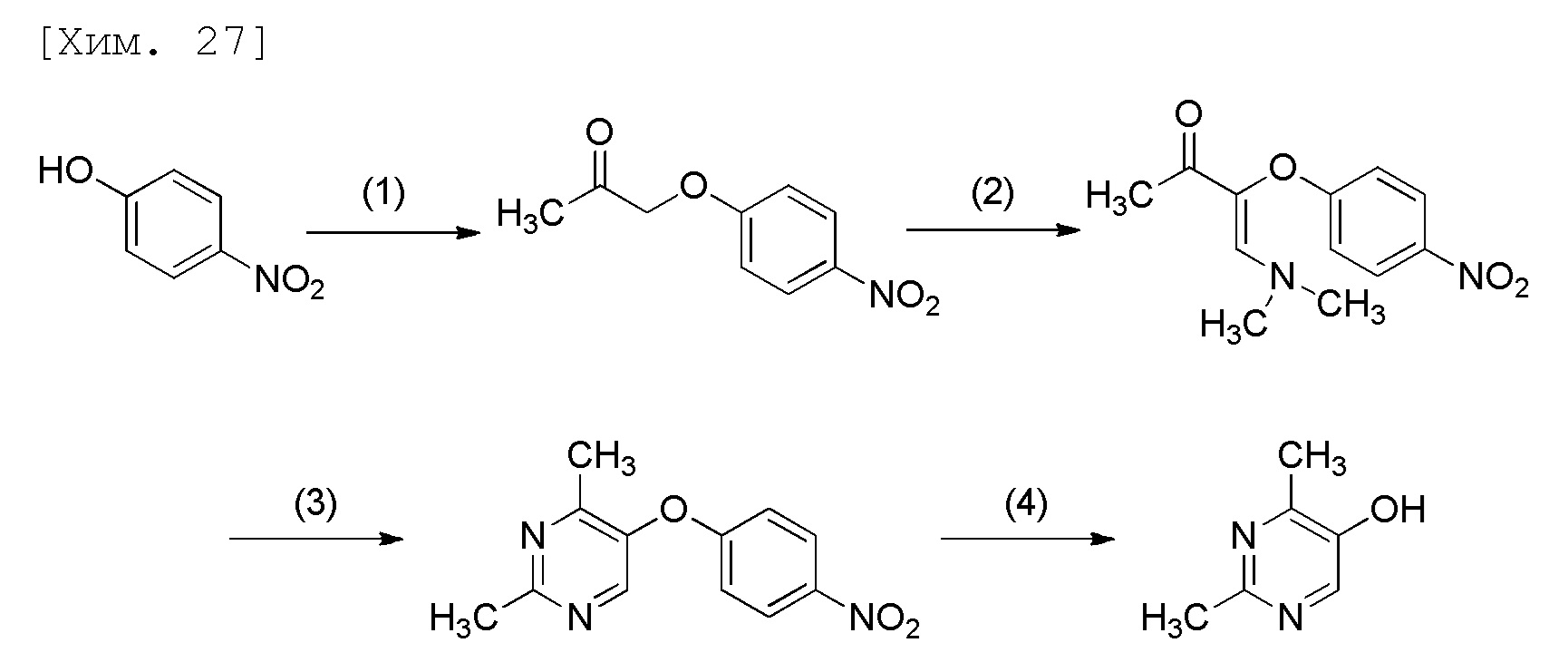
Способ получения 2,4-дизамещенного пиримидин-5-ола или его соли в соответствии с настоящим изобретением включает стадию осуществления гидролиза соединения (V) или его соли (четвертую стадию; стадию 4). Вместе с тем, в качестве другого аспекта, способ получения 2,4-дизамещенного пиримидин-5-ола в соответствии с настоящим изобретением включает стадию (третью стадию; стадию 3) получения соединения (V) или его соли посредством осуществления реакции соединения (IV) или его соли с производным амидина (VI) или его солью в присутствии основания и четвертую стадию. Вместе с тем, в качестве еще одного аспекта, способ получения 2,4-дизамещенного пиримидин-5-ола или его соли в соответствии с настоящим изобретением включает стадию (вторую стадию; стадию 2) получения соединения (IV) или его соли посредством реакции конденсации N,N-диметилформамиддиметилацеталя и соединения (III), третью стадию и четвертую стадию. Вместе с тем, в качестве еще одного аспекта, способ получения 2,4-дизамещенного пиримидин-5-ола или его соли в соответствии с настоящим изобретением включает стадию (первую стадию; стадию 1) получения 4-нитрофенилоксиметилкетонового соединения (III) посредством осуществления реакции галогенметилкетонового соединения (VII) с 4-нитрофенолом (II), вторую стадию, третью стадию и четвертую стадию.
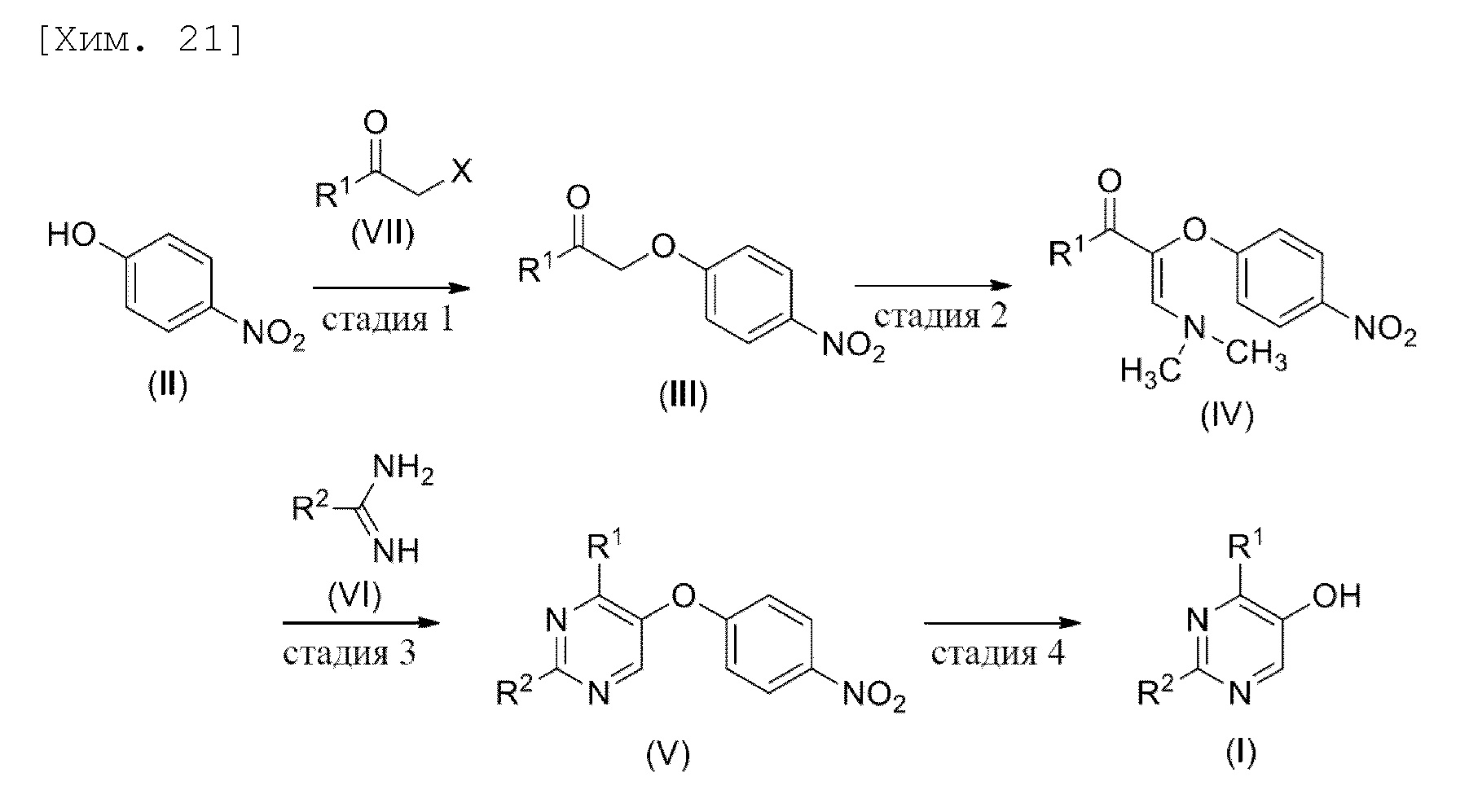
[В формулах R1 и R2 представляют собой C1-6алкильные группы, которые являются одинаковыми или отличными друг от друга].
[0026]
Далее в данном документе данные стадии будут подробно описаны.
[0027]
(Первая стадия)
Данная стадия является стадией получения 4-нитрофенилоксиметилкетонового соединения (III) в соответствии с реакцией алкилирования галогенметилкетонового соединения (VII) и фенольной гидроксильной группой 4-нитрофенола (II).
Для реакции алкилирования фенольной гидроксильной группы можно применять методики, которые хорошо известны специалистам в данной области. Например, соединение (VII) и соединение (II) применяют в эквивалентных количествах или одно из них применяют в большем количестве. Их смесь перемешивают, как правило, в течение периода от 0,1 часа до 5 суток в присутствии основания в растворителе, инертном по отношению к реакционной смеси, в каком-либо диапазоне от диапазона охлаждения до диапазона нагревания, но предпочтительно в диапазоне нагревания. Иллюстративные растворители, применяемые в данном случае, особым образом не ограничены и включают кетоны, такие как ацетон и метилэтилкетон, нитрилы, такие как ацетонитрил и пропионитрил, ароматические углеводороды, такие как бензол, толуол и ксилол, галогенированные углеводороды, такие как дихлорметан, 1,2-дихлорэтан и хлороформ, простые эфиры, такие как диэтиловый эфир, тетрагидрофуран, диоксан и диметоксиэтан, апротонные полярные растворители, такие как N,N-диметилформамид, диметилсульфоксид и N-метилпирролидон, и их смеси. Вместе с тем, иллюстративные основания, применяемые в данном случае, могут включать неорганические основания, такие как карбонат калия, карбонат натрия, карбонат цезия, гидрокарбонат натрия, гидроксид натрия и гидроксид калия, и органические основания, такие как триэтиламин, диизопропилэтиламин и пиридин.
[0028]
(Вторая стадия)
Данная стадия является стадией получения соединения (IV) или его соли в соответствии с реакцией конденсации 4-нитрофенилоксиметилкетонового соединения (III) и N,N-диметилформамиддиметилацеталя.
Для реакции конденсации можно применять методики, которые хорошо известны специалистам в данной области. Например, соединение (III) и N,N-диметилформамиддиметилацеталь применяют в эквивалентных количествах или одно из них применяют в большем количестве. Их смесь перемешивают, как правило, в течение периода от 0,1 часа до 5 суток в растворителе, инертном по отношению к реакционной смеси, в каком-либо диапазоне от диапазона охлаждения до диапазона нагревания, но предпочтительно в диапазоне нагревания. Иллюстративные растворители, применяемые в данном случае, особым образом не ограничены и включают ароматические углеводороды, простые эфиры и их смеси. Также для плавного протекания реакции можно добавлять каталитическое количество кислоты.
[0029]
(Третья стадия)
Данная стадия является стадией получения 2,4-дизамещенного-5-(4-(нитрофенил)окси)пиримидинового соединения (V), которое представляет собой соединение по настоящему изобретению или его соль, в соответствии с реакцией образования пиримидинового кольца соединения (IV) или его соли и производного амидина (VI) или его соли.
Для реакции образования пиримидинового кольца можно применять методики, которые хорошо известны специалистам в данной области. Например, соединение (IV) или его соль и соединение (VI) или его соль применяют в эквивалентных количествах или одно из них применяют в большем количестве. Их смесь перемешивают, как правило, в течение периода от 0,1 часа до 5 суток в присутствии основания в растворителе, инертном по отношению к реакционной смеси, в каком-либо диапазоне от диапазона охлаждения до диапазона нагревания, но предпочтительно в диапазоне нагревания. Иллюстративные растворители, применяемые в данном случае, особым образом не ограничены и включают кетоны, ароматические углеводороды, галогенированные углеводороды, простые эфиры, апротонные полярные растворители, нитрилы и их смеси. Также в качестве производного амидина можно применять соль присоединения кислоты. Иллюстративные основания, применяемые в данном случае, могут включать неорганические основания, такие как карбонат калия, карбонат натрия, карбонат цезия, гидрокарбонат натрия, гидроксид натрия и гидроксид калия, и органические основания, такие как триэтиламин, диизопропилэтиламин и пиридин.
[0030]
(Четвертая стадия)
Данная стадия является стадией получения 2,4-дизамещенного пиримидин-5-ола или его соли в соответствии с реакцией гидролиза 2,4-дизамещенного-5-(4-(нитрофенил)окси)пиримидинового соединения (V), которое представляет собой соединение по настоящему изобретению или его соль.
Для реакции гидролиза можно применять методики, которые хорошо известны специалистам в данной области. Например, применяют соединение (V) или его соль и эквивалентные количества или большее количество основания. Их смесь перемешивают, как правило, в течение периода от 0,1 часа до 5 суток в растворителе, инертном по отношению к реакционной смеси, в каком-либо диапазоне от диапазона охлаждения до диапазона нагревания, но предпочтительно в диапазоне нагревания. Иллюстративные растворители, применяемые в данном случае, особым образом не ограничены и включают ароматические углеводороды, простые эфиры, апротонные полярные растворители, нитрилы, спирты, такие как метанол, этанол, пропанол, изопропанол и бутанол, вода и их смеси. Иллюстративные основания, применяемые в данном случае, могут включать неорганические основания, такие как карбонат калия, карбонат натрия, карбонат цезия, гидрокарбонат натрия, гидроксид натрия, гидроксид калия, фосфат тринатрия и фосфат трикалия, и органические основания, такие как триэтиламин, диизопропилэтиламин и пиридин.
[0031]
Способ получения в соответствии с настоящим изобретением характеризуется следующими особенностями.
(1) В способах, описанных в источнике 7 патентной литературы и источнике 8 патентной литературы, в качестве исходного материала применяют дорогой 2,4-дихлор-5-метоксипиримидин. Тем не менее, в способе получения в соответствии с настоящим изобретением, 2,4-дизамещенный пиримидин-5-ол можно получать с применением недорогого и легкодоступного 4-нитрофенола в качестве исходного материала.
(2) В способах, описанных в источнике 7 патентной литературы и источнике 8 патентной литературы, трудно контролировать региоселективность, поскольку триметилалюминий или хлорид метилмагния применяют для введения метильной группы в дихлорпиримидин. Тем не менее, в способе получения в соответствии с настоящим изобретением посредством соответствующего выбора применяемого реагента в виде соединения (VI) или соединения (VII) можно вводить какой-либо из R1 и R2, и, таким образом, региоселективность легко контролируема и примеси также легко контролируемы.
(3) 2,4-Дизамещенный пиримидин-5-ол можно получать без применения реагентов и промежуточных соединений, вызывающих проблемы со здоровьем, такие как жжение и раздражение кожи, и характеризующихся риском самовоспламенения, летучестью и гигроскопичностью, и применять в способах, раскрытых в источнике 7 патентной литературы и источнике 8 патентной литературы.
Вместе с тем, в ходе конденсации N,N-диметилформамиддиметилацеталя и соединения (III) 4-нитрофенильная группа способствует региоселективной конденсации с получением соединения (IV) и дополнительно выполняет функцию удаляемой защитной группы в относительно мягких условиях на четвертой стадии.
[Примеры]
[0032]
Далее в данном документе настоящее изобретение будет подробно описано со ссылкой на примеры. Тем не менее, настоящее изобретение не ограничено следующими примерами. Вместе с тем, сокращения, используемые ниже, являются традиционными сокращениями, хорошо известными специалистам в данной области, и некоторые сокращения представляют собой следующие.
Химические сдвиги на спектрах протонного ядерного магнитного резонанса (1H-ЯМР) регистрировали в единицах δ (ppm) относительно тетраметилсилана, а константы взаимодействия регистрировали в герцах (Гц). На спектрограммах s обозначает синглет, d обозначает дублет, br обозначает широкий и m обозначает мультиплет.
1H-ЯМР измеряли с использованием спектрометра ядерного магнитного резонанса JNM-AL400 (400 МГц), коммерчески доступного от JEOL.
В следующих примерах термин "комнатная температура" обозначает, как правило, от приблизительно 10°C до приблизительно 35°C. Если не указано иное, % представляет собой процент по весу.
[0033]
Пример 1. Получение 2,4-диметилпиримидин-5-ола
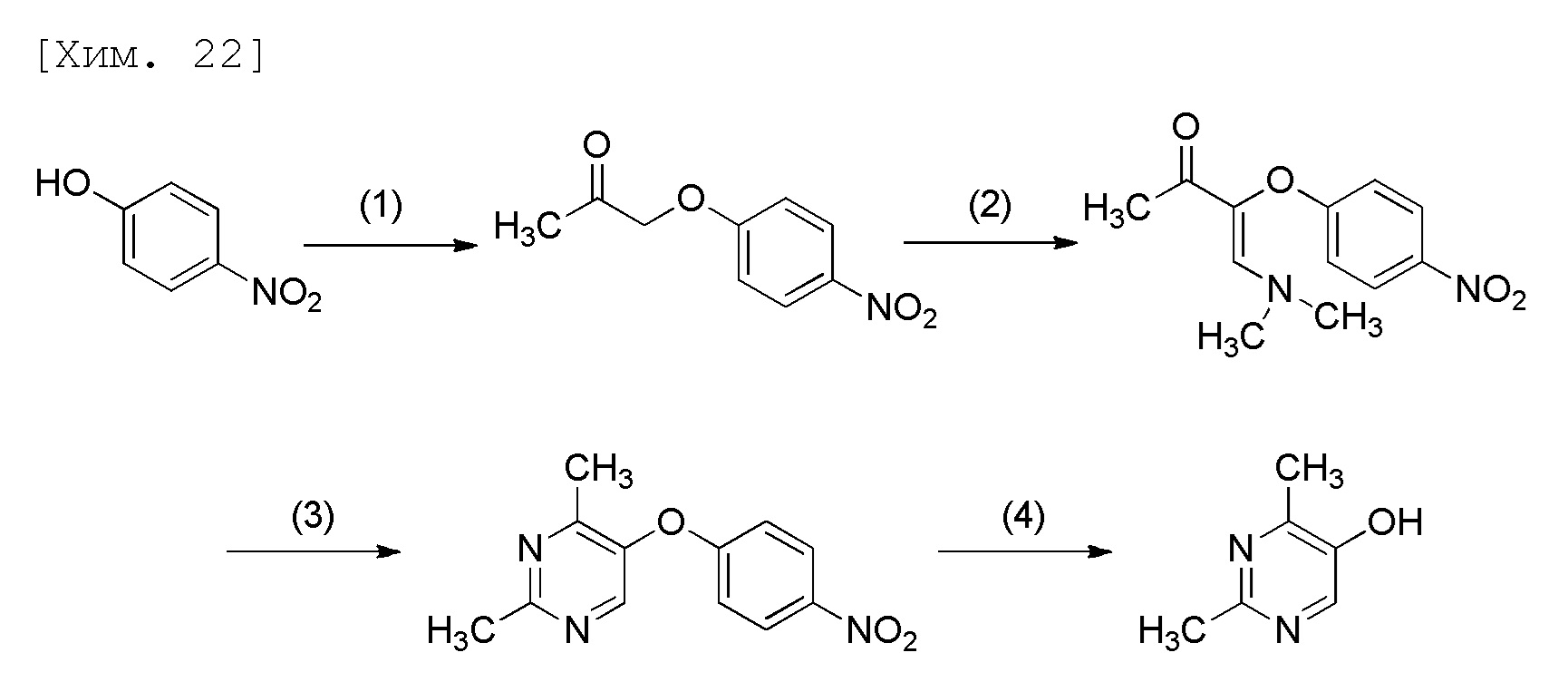
[0034]
(1) Получение 1-(4-нитрофенокси)пропан-2-она
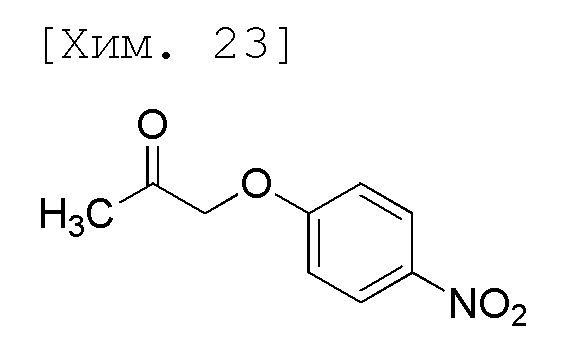
[0035]
Смесь 4-нитрофенола (10,0 г, 71,9 ммоль), карбоната калия (10,4 г, 75,5 ммоль) и ацетона (70 мл) перемешивали в течение 30 минут при 65°C (наружная температура). К реакционной смеси при 65°C (наружная температура) по каплям добавляли хлорацетон (степень чистоты 96%, 6,3 мл, 75,5 ммоль) и полученную смесь перемешивали в течение 9 часов при 65°C (наружная температура). Реакционную смесь охлаждали на ледяной бане и затем по каплям к реакционной смеси при такой же температуре добавляли воду (120 мл). Реакционную смесь перемешивали в течение 1 часа при такой же температуре и осажденное твердое вещество затем фильтровали. Полученное твердое вещество промывали водой (100 мл) и высушивали при пониженном давлении с получением целевого соединения (10,9 г, 77%).
1H-ЯМР (CD3Cl) δ (ppm): 2,31(3 H, s), 4,67 (2 H, s), 6,95 (2 H, d, J=9,3 Гц), 8,22 (2 H, d, J=9,3 Гц)
[0036]
(2) Получение (Z)-4-(диметиламино)-3-(4-нитрофенокси)бут-3-ен-2-она
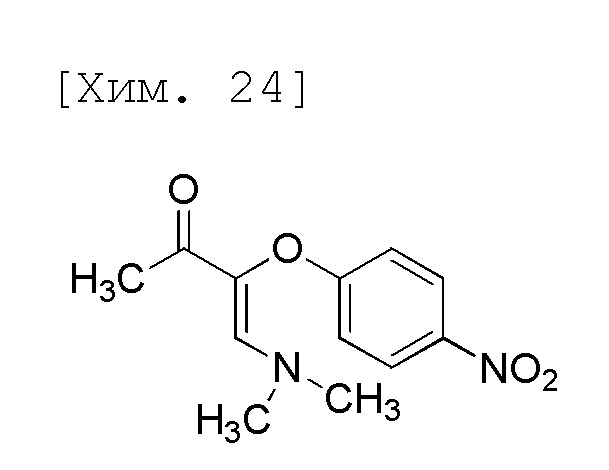
[0037]
Смесь 1-(4-нитрофенокси)пропан-2-она (4,20 г, 21,5 ммоль), толуола (12,6 мл) и N,N-диметилформамиддиметилацеталя (3,17 мл, 23,7 ммоль) перемешивали в течение 21 часа при 80°C (наружная температура). К реакционной смеси при такой же температуре добавляли толуол (8,4 мл) и перемешивали при комнатной температуре. Дополнительно реакционную смесь перемешивали в течение 1 часа при охлаждении на ледяной бане и осажденное твердое вещество затем фильтровали. Полученное твердое вещество промывали толуолом (4,2 мл) и затем высушивали при пониженном давлении с получением целевого соединения (2,95 г, 55%).
1H-ЯМР (CD3Cl) δ (ppm): 2,00 (3 H, brs), 3,01 (6 H, s), 6,90-7,16 (2 H, brm), 7,16-7,46 (1 H, brs), 8,22 (2 H, d, J=8,8 Гц)
[0038]
(3) Получение 2,4-диметил-5-(4-нитрофенокси)пиримидина
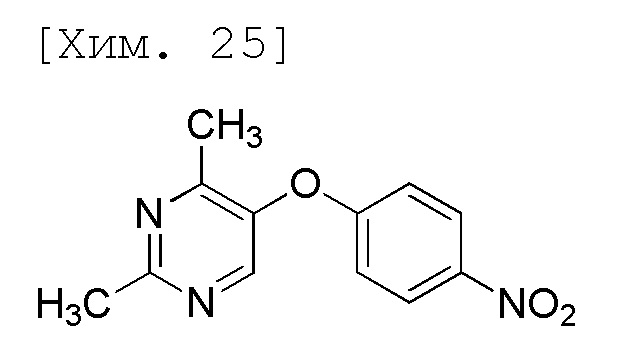
[0039]
Смесь (Z)-4-(диметиламино)-3-(4-нитрофенокси)бут-3-ен-2-она (3,00 г, 12,0 ммоль), ацетамидина гидрохлорида (степень чистоты 96%, 1,42 г, 14,4 ммоль), карбоната калия (2,00 г, 14,4 ммоль) и ацетонитрила (30 мл) перемешивали в течение 18 часов при 80°C (наружная температура) и затем к реакционной смеси добавляли ацетамидина гидрохлорид (степень чистоты 96%, 1,42 г, 14,4 ммоль) и карбонат калия (2,00 г, 14,4 ммоль) и перемешивали в течение 23 часов при 80°C (наружная температура). Реакционную смесь охлаждали на ледяной бане и к ней затем добавляли воду (15 мл) и этилацетат (30 мл). Полученную реакционную смесь перемешивали при комнатной температуре и органические слои затем разделяли и промывали с помощью 10% солевого раствора (6 мл). Полученные органические слои высушивали с применением безводного сульфата натрия и растворитель затем выпаривали при пониженном давлении. Обеспечивали затвердевание полученных остатков с применением смеси этилацетат-гептан (4,5 мл:9 мл) и их отфильтровывали. Полученное твердое вещество промывали смесью этилацетат-гептана (1 мл:2 мл) и затем высушивали при пониженном давлении с получением целевого соединения (2,51 г, 85%).
1H-ЯМР (CD3Cl) δ (ppm): 2,40 (3 H, s), 2,75 (3 H, s), 6,96 (2 H, d, J=9,0 Гц), 8,24 (2 H, d, J=9,0 Гц), 8,32 (1 H, s)
[0040]
(4) Получение 2,4-диметилпиримидин-5-ола
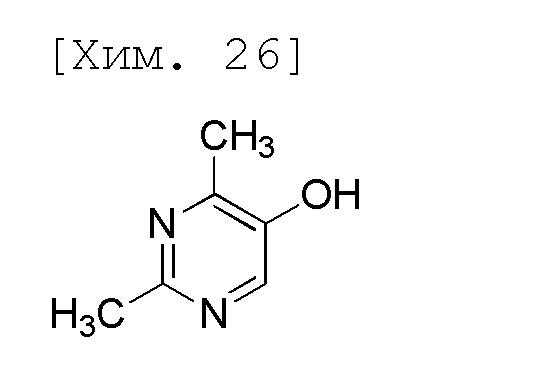
[0041]
Смесь 2,4-диметил-5-(4-нитрофенокси)пиримидина (2,50 г, 10,2 ммоль), метанола (12,5 мл) и 48% водного раствора гидроксида натрия (2,55 г, 30,6 ммоль) перемешивали в течение 20 часов при 60°C (наружная температура). Реакционную смесь охлаждали до комнатной температуры и затем к ней добавляли толуол (25 мл) и воду (10 мл). Полученную реакционную смесь перемешивали при комнатной температуре, затем разделяли водные слои и водные слои концентрировали до внутреннего объема 12,5 мл при пониженном давлении. К полученному концентрированному раствору на ледяной бане добавляли толуол (6,25 мл), концентрированную хлористоводородную кислоту (5,31 г, 51,0 ммоль) и этилацетат (6,25 мл). Полученную реакционную смесь перемешивали при комнатной температуре и водные слои затем разделяли и промывали смесью толуол-этилацетата (6,25 мл:6,25 мл). К полученным водным слоям добавляли 2-метилтетрагидрофуран (25 мл) и затем добавляли 5 моль/л водного раствора гидроксида натрия на ледяной бане для доведения pH до значения 6-7. Полученную реакционную смесь перемешивали при комнатной температуре, органические слои затем разделяли и водные слои повторно экстрагировали 2-метилтетрагидрофураном (25 мл). Полученные органические слои объединяли и затем промывали водой (2,5 мл) и растворитель выпаривали при пониженном давлении. К полученным остаткам добавляли толуол (6,25 мл), и суспендировали, и перемешивали при 50°C (наружная температура). Смесь перемешивали в течение 1,5 часа на ледяной бане и затем фильтровали. Полученное твердое вещество промывали толуолом (1,25 мл) и затем высушивали при пониженном давлении с получением целевого соединения (1,16 г, 91%).
1H-ЯМР (CD3Cl) δ (ppm): 2,51 (3 H, s), 2,65 (3 H, s), 8,03 (1 H, s), 9,87 (1 H, brs)
[0042]
Пример 2. Получение 2,4-диметилпиримидин-5-ола
[0043]
(1) Получение 1-(4-нитрофенокси)пропан-2-она
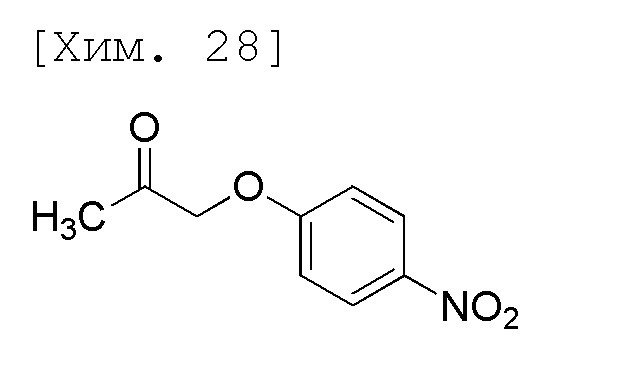
[0044]
Смесь 4-нитрофенола (100 г, 719 ммоль), карбоната калия (104 г, 755 ммоль) и ацетона (700 мл) перемешивали в течение 45 минут при 45°C (наружная температура). К реакционной смеси при 45°C (наружная температура) по каплям добавляли хлорацетон (степень чистоты 96,3%, 72,5 г, 755 ммоль) и полученную смесь перемешивали в течение 15 часов при 60°C (наружная температура). Реакционную смесь охлаждали на ледяной бане и затем к ней добавляли воду (800 мл) и этилацетат (1000 мл). Полученную реакционную смесь перемешивали при комнатной температуре, органические слои затем разделяли и к ней добавляли 0,5 моль/л водного раствора гидроксида натрия (500 мл) и хлорид натрия (50 г). Полученную реакционную смесь перемешивали при комнатной температуре и органические слои затем разделяли и промывали с помощью 10% солевого раствора (500 мл). Растворитель выпаривали при пониженном давлении, полученные остатки растворяли толуолом (500 мл) при 60°C (наружная температура) и затем охлаждали до 5°C (наружная температура) и осажденное твердое вещество отфильтровывали. Полученное твердое вещество промывали толуолом (50 мл) и высушивали при 40°C при пониженном давлении и затем получали целевое соединение (109 г, 78%).
1H-ЯМР (CD3Cl) δ (ppm): 2,31 (3 H, s), 4,67 (2 H, s), 6,95 (2 H, d, J=9,3 Гц), 8,22 (2 H, d, J=9,3 Гц)
[0045]
(2) Получение (Z)-4-(диметиламино)-3-(4-нитрофенокси)бут-3-ен-2-она
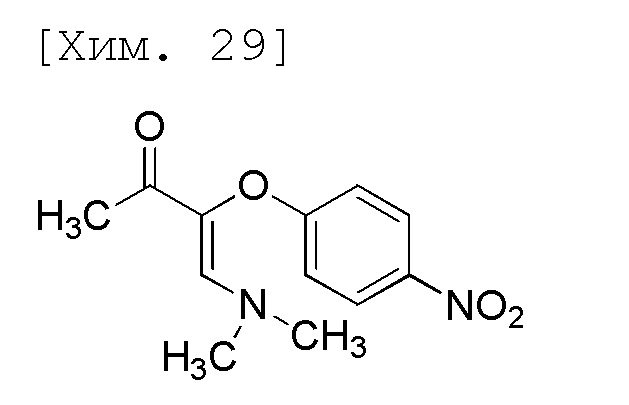
[0046]
Смесь 1-(4-нитрофенокси)пропан-2-она (109 г, 557 ммоль), толуола (326 мл) и N,N-диметилформамиддиметилацеталя (степень чистоты 98,3%, 82,9 мл, 613 ммоль) перемешивали в течение 21 часа при 80°C (наружная температура). К реакционной смеси при такой же температуре добавляли толуол (217 мл) и перемешивали при комнатной температуре. Дополнительно реакционную смесь перемешивали в течение 1,5 часа при охлаждении на ледяной бане и осажденное твердое вещество затем отфильтровывали. Полученное твердое вещество промывали толуолом (109 мл) и затем высушивали при пониженном давлении с получением целевого соединения (57,0 г, 41%).
1H-ЯМР (CD3Cl) δ (ppm): 2,00 (3 H, brs), 3,01 (6 H, s), 6,90-7,16 (2 H, brm), 7,16-7,46 (1 H, brs), 8,22 (2H, d, J=8,8 Гц)
[0047]
(3) Получение 2,4-диметил-5-(4-нитрофенокси)пиримидина
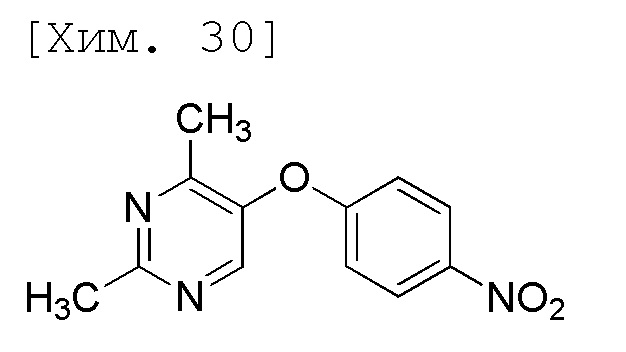
[0048]
Смесь (Z)-4-(диметиламино)-3-(4-нитрофенокси)бут-3-ен-2-она (56,8 г, 227 ммоль), ацетамидина гидрохлорида (степень чистоты 96,7%, 53,3 г, 545 ммоль), карбоната калия (степень чистоты 99,5%, 75,7 г, 545 ммоль) и ацетонитрила (568 мл) перемешивали в течение 20 часов при 80°C (наружная температура) и затем к реакционной смеси при 80°C (наружная температура) добавляли ацетамидина гидрохлорид (степень чистоты 96,7%, 2,22 г, 22,7 ммоль) и карбонат калия (степень чистоты 99,5%, 3,15 г, 22,7 ммоль) и перемешивали в течение 16 часов. Реакционную смесь охлаждали на ледяной бане и затем к ней добавляли воду (568 мл) и этилацетат (568 мл). Полученную реакционную смесь перемешивали при комнатной температуре и органические слои затем разделяли и промывали с помощью 10% солевого раствора (284 мл). Растворитель выпаривали при пониженном давлении, полученные остатки растворяли этилацетатом (85,2 мл) при 60°C (наружная температура), и затем охлаждали до комнатной температуры, и по каплям добавляли гептан (170 мл). Смесь охлаждали на ледяной бане и осажденное твердое вещество затем фильтровали. Полученное твердое вещество промывали смесью этилацетат-гептана (18,9 мл:37,9 мл) и высушивали при 50°C при пониженном давлении с получением целевого соединения (45,5 г, 82%).
1H-ЯМР (CD3Cl) δ (ppm): 2,40 (3 H, s), 2,75 (3 H, s), 6,96 (2H, d, J=9,0 Гц), 8,24 (2 H, d, J=9,0 Гц), 8,32 (1 H, s)
[0049]
(4) Получение 2,4-диметилпиримидин-5-ола
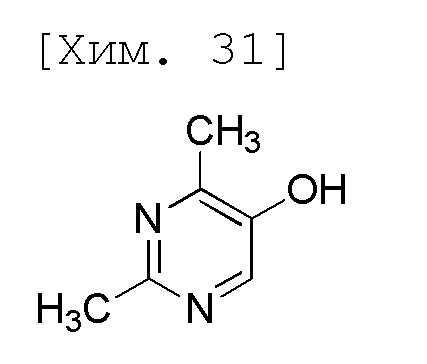
[0050]
Смесь 2,4-диметил-5-(4-нитрофенокси)пиримидина (39,8 г, 162 ммоль), метанола (199 мл) и 48% водного раствора гидроксида натрия (40,6 г, 487 ммоль) перемешивали в течение 18 часов при 60°C (наружная температура). Реакционную смесь охлаждали до комнатной температуры и затем добавляли толуол (398 мл) и воду (159 мл). Полученную реакционную смесь перемешивали при комнатной температуре, водные слои затем разделяли и водные слои концентрировали до внутреннего объема 199 мл при пониженном давлении. К полученному концентрированному раствору на ледяной бане добавляли толуол (99,5 мл), концентрированную хлористоводородную кислоту (84,5 г, 811 ммоль) и этилацетат (99,5 мл). Полученную реакционную смесь перемешивали при комнатной температуре и водные слои затем разделяли и промывали смесью толуол-этилацетата (99,5 мл:99,5 мл). К полученным водным слоям добавляли 2-метилтетрагидрофуран (398 мл) и затем добавляли 5 моль/л водного раствора гидроксида натрия на ледяной бане для доведения pH до значения 6-7. Полученную реакционную смесь перемешивали при комнатной температуре, органические слои затем разделяли и водные слои повторно экстрагировали 2-метилтетрагидрофураном (398 мл). Полученные органические слои объединяли и затем промывали водой (39,8 мл) и растворитель выпаривали при пониженном давлении. К полученным остаткам добавляли толуол (99,5 мл), и суспендировали, и перемешивали при 50°C (наружная температура). Смесь перемешивали в течение 1,5 часа на ледяной бане и затем фильтровали. Полученное твердое вещество промывали толуолом (19,9 мл) и затем высушивали при пониженном давлении, с получением целевого соединения (18,8 г, 93%).
1H-ЯМР (CD3Cl) δ (ppm): 2,51 (3 H, s), 2,65 (3 H, s), 8,02 (1 H, s), 10,1 (1 H, brs)
[0051]
Пример 3. Получение 2,4-диметилпиримидин-5-ола
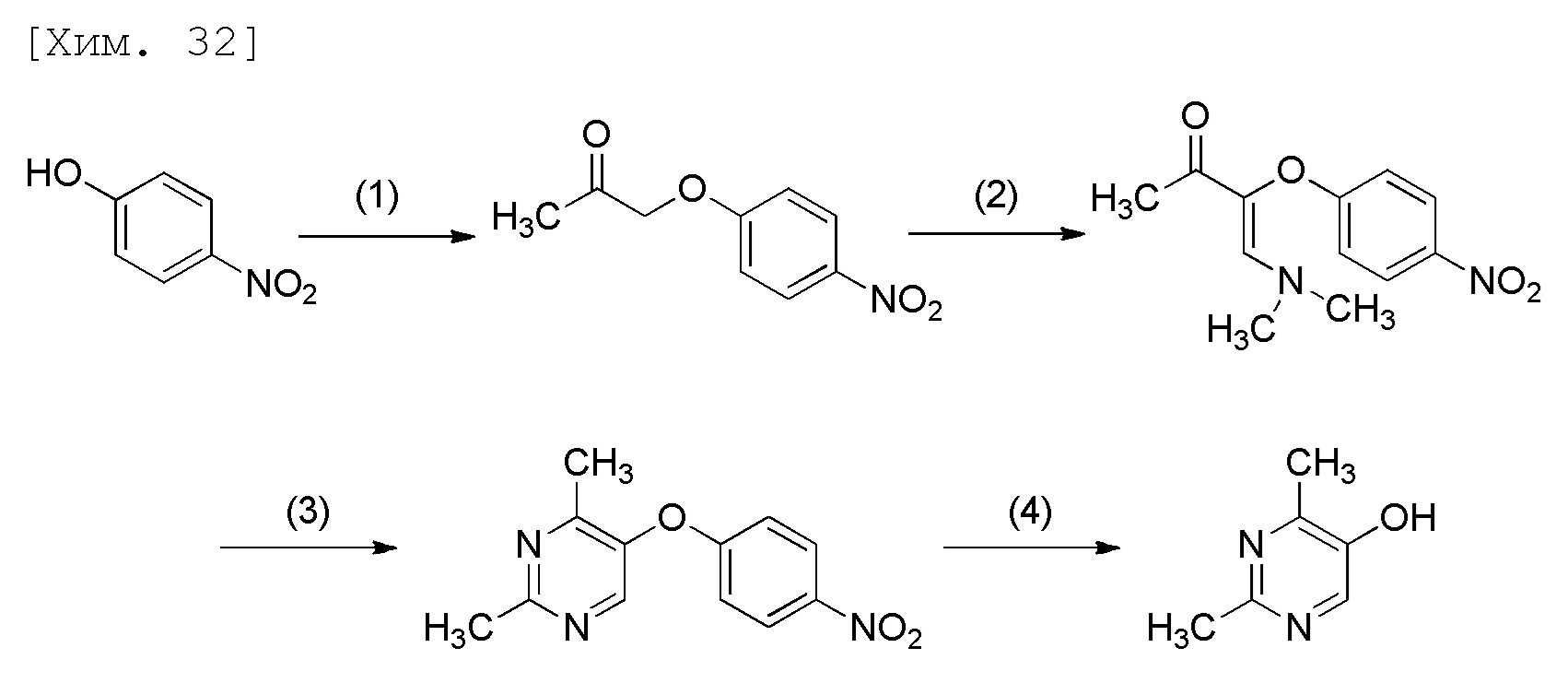
[0052]
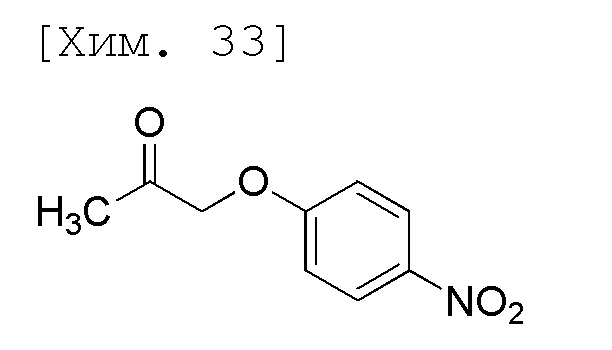
(1) Получение 1-(4-нитрофенокси)пропан-2-она
[0053]
Смесь 4-нитрофенола (10,0 г, 71,9 ммоль), карбоната калия (10,4 г, 75,5 ммоль) и ацетонитрила (70 мл) перемешивали в течение 30 минут при 60°C (наружная температура). К реакционной смеси при 60°C (наружная температура) по каплям добавляли хлорацетон (степень чистоты 96,3%, 6,29 мл, 75,5 ммоль) и полученную смесь перемешивали в течение 13,5 часов при 60°C (наружная температура). Реакционную смесь охлаждали на ледяной бане и затем к реакционной смеси при той же температуре добавляли воду (60 мл) и толуол (70 мл). Полученную реакционную смесь перемешивали при комнатной температуре и органические слои затем разделяли и промывали с помощью 10% солевого раствора (50 мл). Растворитель выпаривали при пониженном давлении, полученные остатки растворяли толуолом (50 мл) при 60°C (наружная температура) и затем охлаждали на ледяной бане и осажденное твердое вещество отфильтровывали. Полученное твердое вещество промывали толуолом (5 мл) и высушивали при пониженном давлении при 50°C и затем получали целевое соединение (12,1 г, 86%).
1H-ЯМР (CD3Cl) δ (ppm): 2,31 (3 H, s), 4,67 (2 H, s), 6,95 (2 H, d, J=9,3 Гц), 8,22 (2 H, d, J=9,3 Гц)
[0054]
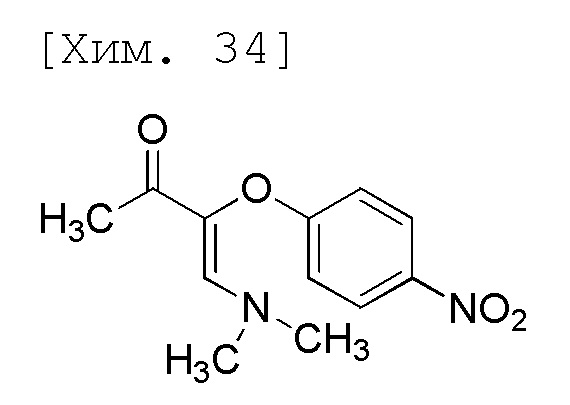
(2) Получение (Z)-4-(диметиламино)-3-(4-нитрофенокси)бут-3-ен-2-она
[0055]
Смесь 1-(4-нитрофенокси)пропан-2-она (12,1 г, 61,9 ммоль), толуола (36,3 мл) и N,N-диметилформамиддиметилацеталя (степень чистоты 98,3%, 9,22 мл, 68,1 ммоль) перемешивали в течение 21 часа при 80°C (наружная температура). К реакционной смеси при такой же температуре добавляли толуол (24,2 мл) и охлаждали до комнатной температуры. Дополнительно реакционную смесь перемешивали в течение 2 часов при охлаждении на ледяной бане и осажденное твердое вещество затем отфильтровывали. Полученное твердое вещество промывали толуолом (12,1 мл) и затем высушивали при комнатной температуре при пониженном давлении с получением неочищенной формы (7,76 г, 50%) целевого соединения. Смесь толуол-метанола (23,3 мл:3,88 мл) добавляли к неочищенной форме (7,76 г), и суспендировали, и перемешивали при 80°C (наружная температура), и при такой же температуре добавляли толуол (15,5 мл), и охлаждали до комнатной температуры. Дополнительно реакционную смесь перемешивали в течение 2 часов при охлаждении на ледяной бане и осажденное твердое вещество затем отфильтровывали. Полученное твердое вещество промывали толуолом (7,76 мл) и затем высушивали при комнатной температуре при пониженном давлении с получением целевого соединения (5,90 г, 38%).
1H-ЯМР (CD3Cl) δ (ppm): 2,00 (3 H, brs), 3,01 (6 H, s), 6,90-7,16 (2 H, brm), 7,16-7,46 (1 H, brs), 8,22 (2H, d, J=8,8 Гц)
[0056]
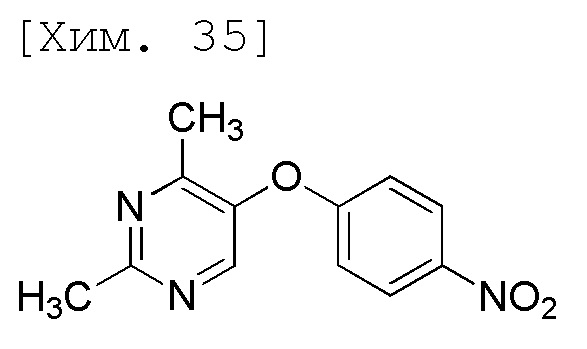
(3) Получение 2,4-диметил-5-(4-нитрофенокси)пиримидина
[0057]
Смесь (Z)-4-(диметиламино)-3-(4-нитрофенокси)бут-3-ен-2-она (3,00 г, 12,0 ммоль), ацетамидина гидрохлорида (степень чистоты 96%, 2,83 г, 28,8 ммоль), фосфата трикалия (степень чистоты 98%, 6,23 г, 28,8 ммоль) и ацетонитрила (21,0 мл) перемешивали в течение 22 часов при 80°C (наружная температура). Реакционную смесь охлаждали на ледяной бане и затем к ней добавляли воду (18,0 мл) и этилацетат (21,0 мл). Полученную реакционную смесь перемешивали при комнатной температуре, и органические слои затем разделяли и промывали с помощью 10% солевого раствора (15 мл). Растворитель выпаривали при пониженном давлении, полученные остатки растворяли метанолом (15,0 мл) при 50°C (наружная температура), и затем охлаждали на ледяной бане, и по каплям добавляли воду (45,0 мл). Смесь перемешивали в течение 2 часов на ледяной бане, и осажденное твердое вещество затем отфильтровывали. Полученное твердое вещество промывали водой (6,00 мл) и затем высушивали при комнатной температуре при пониженном давлении с получением целевого соединения (2,78 г, 95%).
1H-ЯМР (CD3Cl) δ (ppm): 2,40 (3 H, s), 2,75 (3 H, s), 6,96 (2 H, d, J=9,0 Гц), 8,24 (2 H, d, J=9,0 Гц), 8,32 (1 H, s)
[0058]
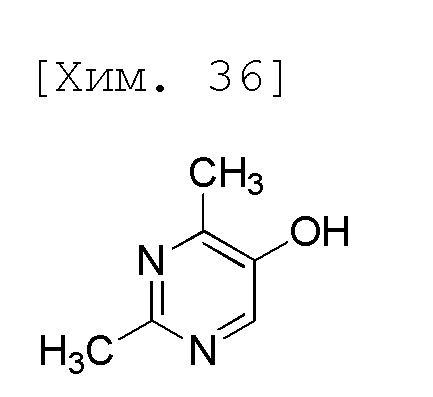
(4) Получение 2,4-диметилпиримидин-5-ола
[0059]
Смесь 2,4-диметил-5-(4-нитрофенокси)пиримидина (3,58 г, 14,6 ммоль), метанола (17,9 мл) и 48% водного раствора гидроксида натрия (3,65 г, 43,8 ммоль) перемешивали в течение 19 часов при 60°C (наружная температура). Реакционную смесь охлаждали до комнатной температуры и затем к ней добавляли толуол (35,8 мл) и воду (14,3 мл). Полученную реакционную смесь перемешивали при комнатной температуре, и водные слои затем разделяли, и водные слои концентрировали до внутреннего объема 17,9 мл при пониженном давлении. К полученному концентрированному раствору на ледяной бане добавляли толуол (8,95 мл), концентрированную хлористоводородную кислоту (7,60 г, 73,0 ммоль) и этилацетат (8,95 мл). Полученную реакционную смесь перемешивали при комнатной температуре, и водные слои затем разделяли и промывали смесью толуол-этилацетата (8,95 мл:8,95 мл). К полученным водным слоям добавляли этилацетат (35,8 мл) и добавляли 5 моль/л водного раствора гидроксида натрия на ледяной бане для доведения pH до значения 6-7. Полученную реакционную смесь перемешивали при комнатной температуре, и органические слои затем разделяли, и водные слои повторно экстрагировали этилацетатом (35,8 мл). Полученные органические слои объединяли и затем промывали водой (1,07 мл) и растворитель выпаривали при пониженном давлении. К полученным остаткам добавляли толуол (8,95 мл), и суспендировали, и перемешивали при 50°C (наружная температура). Смесь перемешивали в течение 2 часов на ледяной бане и затем фильтровали. Полученное твердое вещество промывали толуолом (1,79 мл) и затем высушивали при 50°C при пониженном давлении и затем получали целевое соединение (1,67 г, 92%).
1H-ЯМР (CD3Cl) δ (ppm): 2,51 (3 H, s), 2,65 (3 H, s), 8,02 (1 H, s), 10,01 (1 H, brs)
[Промышленная применимость]
[0060]
В настоящем изобретении предусматривают способ получения 2,4-дизамещенного пиримидин-5-ола, который является промежуточным соединением для получения соединения, которое обладает антагонистическим действием по отношению к рецептору орексина и является пригодным в качестве средства для лечения бессонницы, и его промежуточного соединения. В способе получения настоящего изобретения можно применять недорогой и легкодоступный исходный материал, при этом региоселективность замещающей группы легко контролируема, и примеси легко контролируемы, и 2,4-дизамещенный пиримидин-5-ол можно получать без применения реагентов и промежуточных соединений, вызывающих проблемы со здоровьем, риски и т. п. Следовательно, способ получения подходит для промышленного производства.