Результат интеллектуальной деятельности: Катализатор
Вид РИД
Изобретение
Область техники
Настоящее изобретение относится к области катализаторов полимеризации и, в частности, к гетерометаллическим катализаторам и их смесям, и системам, содержащим указанные катализаторы, для осуществления полимеризации диоксида углерода и эпоксида, лактида и/или лактона или эпоксида и ангидрида.
Предпосылки изобретения
Обеспокоенность, вызванная состоянием окружающей среды и экономическим фактором, обусловленная истощающимися запасами нефти, усилила растущий интерес к химическому превращению диоксида углерода (CO2), для обеспечения возможности его применения в качестве восстанавливаемого источника углерода. CO2, несмотря на его низкую реакционную способность, представляет собой весьма выгодный исходный материал углерода, так как он является недорогим, практически нетоксичным, доступным в большом количестве с высокой степенью чистоты и безопасным. Таким образом, CO2 может быть перспективным заменителем таких веществ, как монооксид углерода или фосген, во многих процессах. Одной из развивающихся сфер применения CO2 является сополимеризация с эпоксидами с получением алифатических поликарбонатов, впервые предложенная Inoue et al. более 40 лет назад (Inoue, S. et al, J. Polym. Sci., Part B: Polym. Lett. 1969, 7, pp 287).
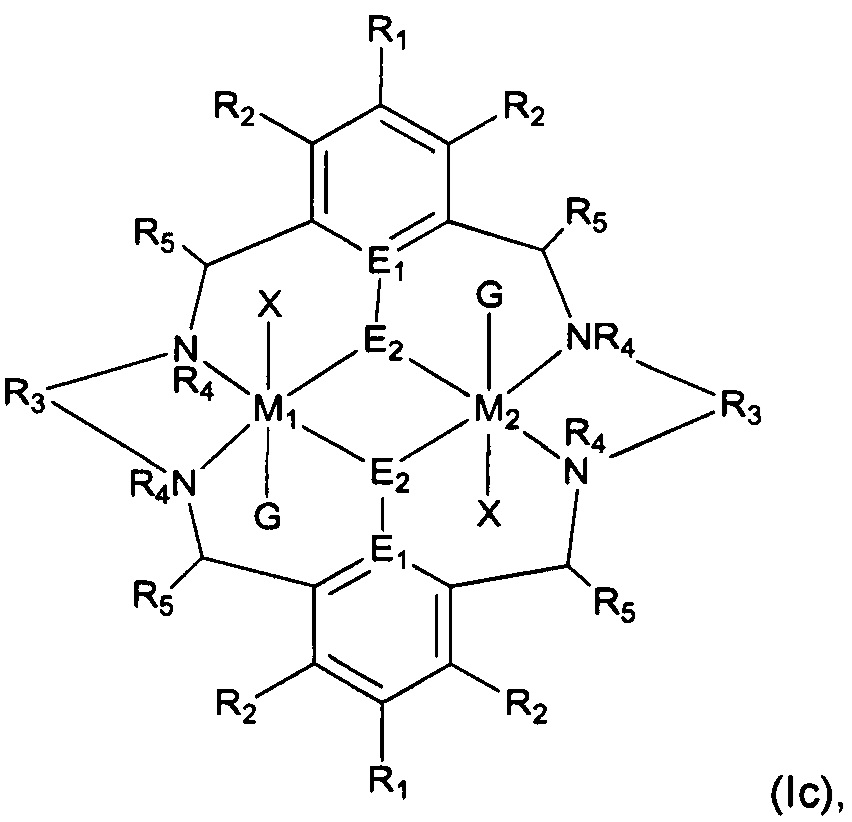
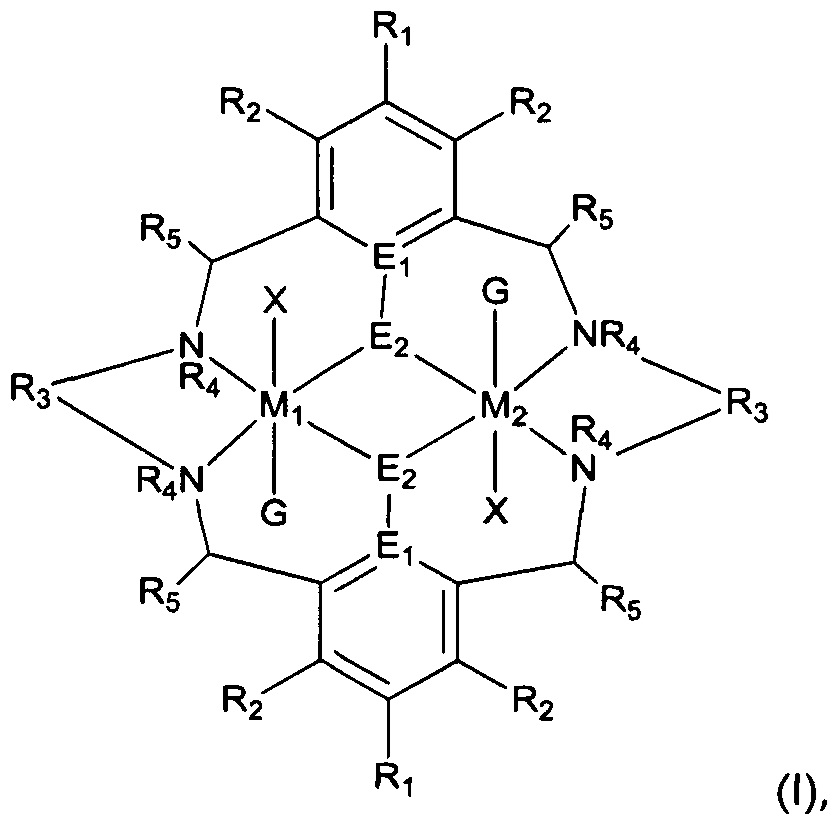
В WO 2009/130470, суть которой включена в данный документ посредством ссылки во всей своей полноте, описана сополимеризация эпоксида с CO2 с применением катализатора вида, представленного формулой (I):
Помимо эпоксидов, применяемых в сополимеризации, особый интерес получил оксид циклогексена (CHO) как продукт, поли(циклогексен карбонат) (PCHC) продемонстрировал высокую температуру стеклования и приемлемый предел прочности. Оксид пропилена также получил интерес, так как из него получают полимер (полипропилен карбонат, известный как PPC) с высокоэластичными свойствами, который применим в сфере пленок. Kember et al (Angew. Chem., Int. Ed., 2009, 48, pp 931 и Inorg. Chem., 2009, 48, pp 9535) сообщили о стабильном на воздухе дицинковом ацетатном комплексе, скоординированном с макроциклическим лигандом, соответствующем формуле (I), указанной выше, который демонстрирует высокую каталитическую активность даже при атмосферном давлении CO2. Катализатор проявляет отличную сополимеризационную селективность, обеспечивая высокие соотношения повторяющихся звеньев карбоната и низкие выходы побочного продукта - циклического циклогексенкарбоната (СНС). Дицинковый ацетатный комплекс представляет собой редкий пример катализатора, который способен к высокой активности в отношении CO2 при атмосферном давлении (1 Бар) с получением PCHC умеренного молекулярного веса с минимальным коэффициентом полидисперсности (PDI), и достигающий заметно высоких чисел оборотов (TON).
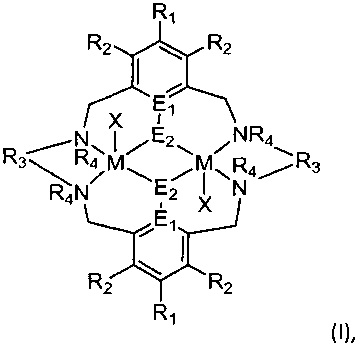
В WO 2013/034750, суть которой включена в данный документ посредством ссылки во всей своей полноте, раскрывают сополимеризацию эпоксида с CO2 в присутствии средства передачи цепи с применением катализатора вида, представленного формулой (I):
Различные соединения в соответствии с указанной выше формулой (I) испытывали относительно их способности катализировать реакцию между различными эпоксидами и диоксидом углерода. В каждом из данных испытываемых катализаторов M в обоих случаях были одинаковыми (обозначаемые далее в данном документе гомометаллическими катализаторами). Несмотря на то, что в WO 2013/034750 предполагают, что катализаторы, содержащие два различных металла (обозначаемые далее в данном документе гетерометаллическими катализаторами) могут быть применены, такие катализаторы не испытывали.
Авторами настоящего изобретения неожиданно было обнаружено, что гетерометаллические катализаторы также активны в качестве катализаторов и обладают активностью, которая сравнима или лучше таковой соответствующих гомометаллических катализаторов, взятых отдельно, или их смесей 50:50. Например, авторами настоящего изобретения было обнаружено, что катализатор, содержащий один металлический центр, включающий атом цинка и один металлический центр, включающий атом магния, неожиданно обладает активностью лучшей, чем соответствующий дицинковый или димагниевый катализаторы, или смесь 50:50 соответствующих дицинкового и димагниевого катализатора. Разработанные гетерометаллические катализаторы и системы, содержащие такой катализатор, также неожиданно сохраняют свою селективность и степень контроля над полученным полимером.
Таким образом, настоящее изобретение представляет собой новый и разработанный выбор в пределах известного уровня техники описания изобретения.
Краткое описание изобретения
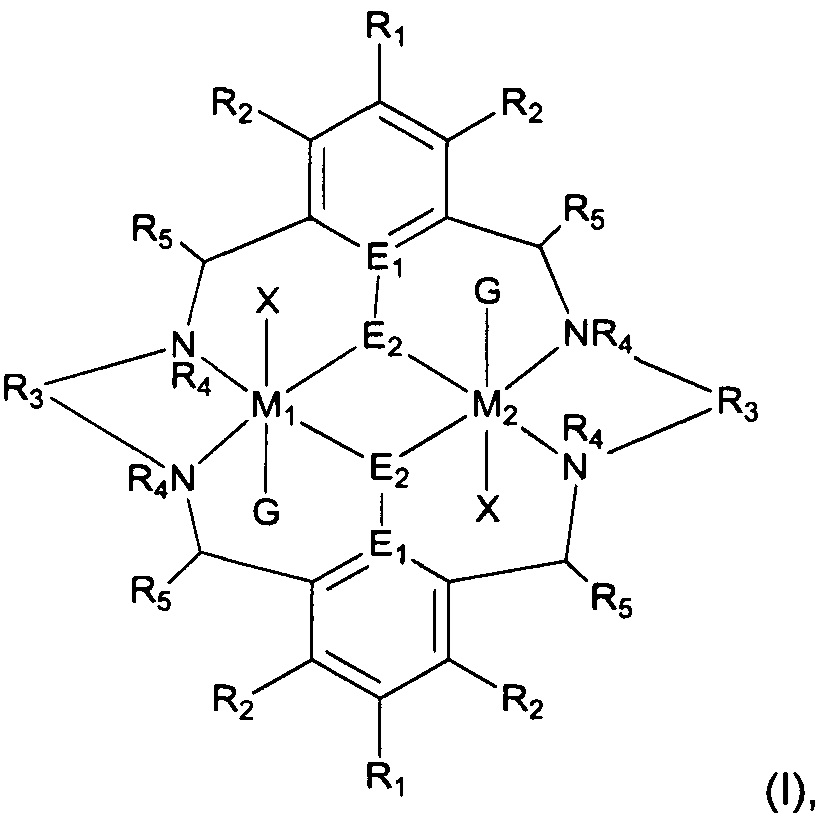
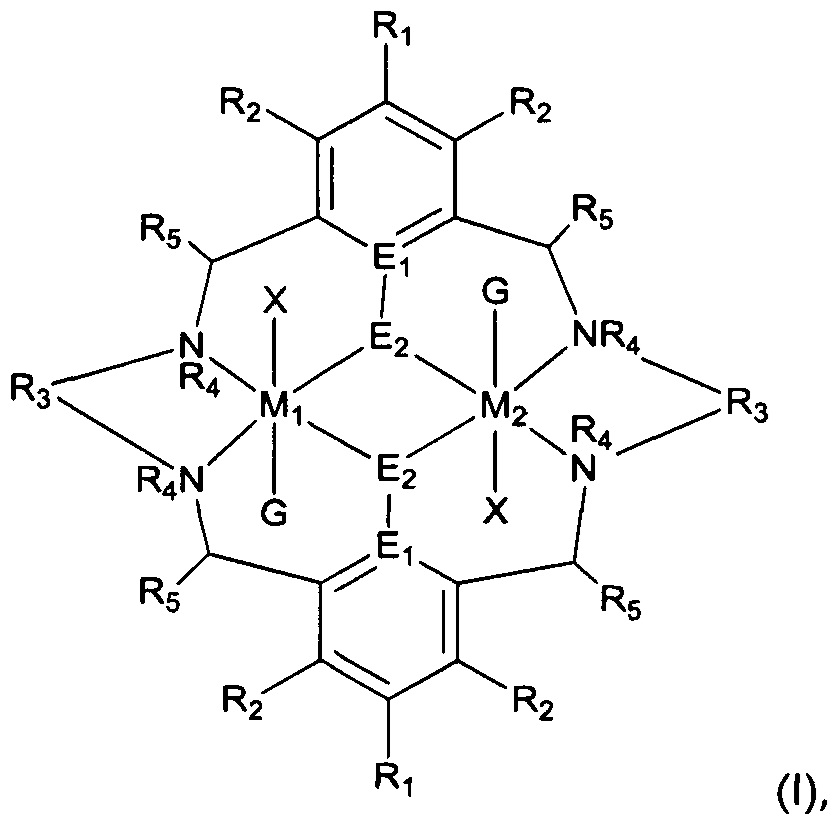
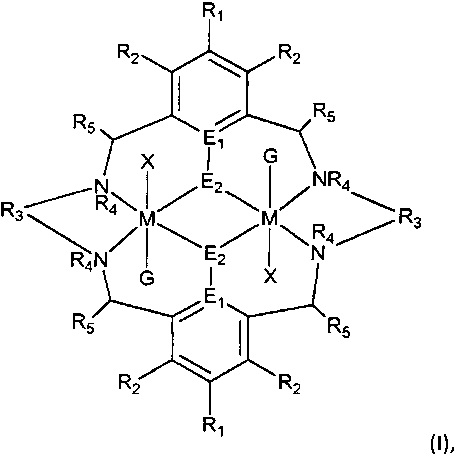
В первом аспекте настоящего изобретения представлен катализатор формулы (I):
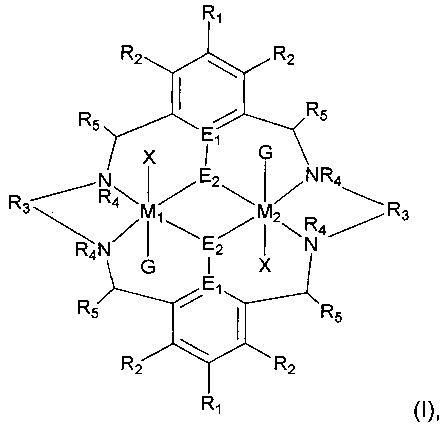
где
M1 и M2 являются различными и независимо выбраны из Mg, Zn, Fe, Co, Al и Cr;
R1 и R2 независимо выбраны из водорода, галогенида, нитрогруппы, нитрильной группы, имина, амина, простой эфирной группы, силильной группы, группы простого силилового эфира, сульфоксидной группы, сульфонильной группы, сульфинатной группы или ацетилидной группы или необязательно замещенной алкильной, алкенильной, алкинильной, галогеналкильной, арильной, гетероарильной, алкокси, арилокси, алкилтио, арилтио, алициклической или гетероалициклической группы;
R3 независимо выбран из необязательно замещенного алкилена, алкенилена, алкинилена, гетероалкилена, гетероалкенилена, гетероалкинилена, арилена, гетероарилена или циклоалкилена, где алкилен, алкенилен, алкинилен, гетероалкилен, гетероалкенилен и гетероалкинилен могут необязательно прерываться арилом, гетероарилом, алициклической или гетероалициклической группой;
R4 независимо выбран из H или необязательно замещенной алифатической, гетероалифатической, алициклической, гетероалициклической группой, арилом, гетероарилом, алкилгетероарилом или алкиларилом;
R5 представляет собой H или необязательно замещенную алифатическую, гетероалифатическую, алициклическую, гетероалициклическую группу, арил, гетероарил, алкилгетероарил или алкиларил;
E1 представляет собой C, E2 представляет собой O, S или NH, или E1 представляет собой N, а E2 представляет собой O;
X независимо выбран из OC(O)Rx, OSO2Rx, OSORx, OSO(Rx)2, S(O)Rx, ORx, фосфината, галогенида, нитрата, гидроксила, карбоната, амино, амидо или необязательно замещенной алифатической, гетероалифатической, алициклической, гетероалициклической группы, арила, гетероарила;
Rx независимо представляет собой водород, или необязательно замещенную алифатическую, галогеналифатическую, гетероалифатическую, алициклическую, гетероалициклическую, арильную, гетероарильную или алкиларильную группу; и
G отсутствует или независимо выбран из нейтрального или анионного донорного лиганда, который представляет собой основание Льюиса.
Во втором аспекте настоящего изобретения представлена каталитическая система, содержащая катализатор в соответствии с первым аспектом и необязательно дополнительный катализатор и/или сокатализатор.
В третьем аспекте настоящего изобретения представлен способ осуществления реакции (i) диоксида углерода с эпоксидом, (ii) ангидридом и эпоксидом или (iii) лактидом и/или лактоном в присутствии катализатора в соответствии с первым аспектом или каталитической системы в соответствии со вторым аспектом необязательно в присутствии средства передачи цепи.
В четвертом аспекте настоящего изобретения представлен продукт способа третьего аспекта настоящего изобретения.
В пятом аспекте настоящего изобретения представлен способ синтеза катализатора в соответствии с первым аспектом или каталитической системы в соответствии со вторым аспектом, причем способ включает
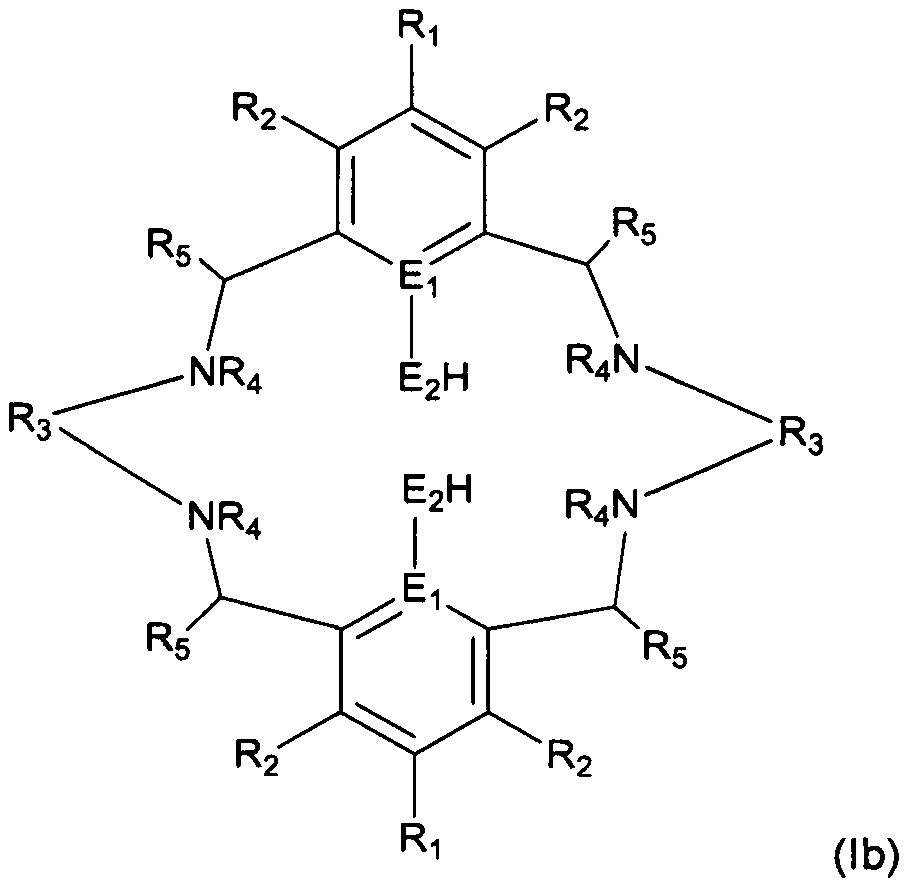
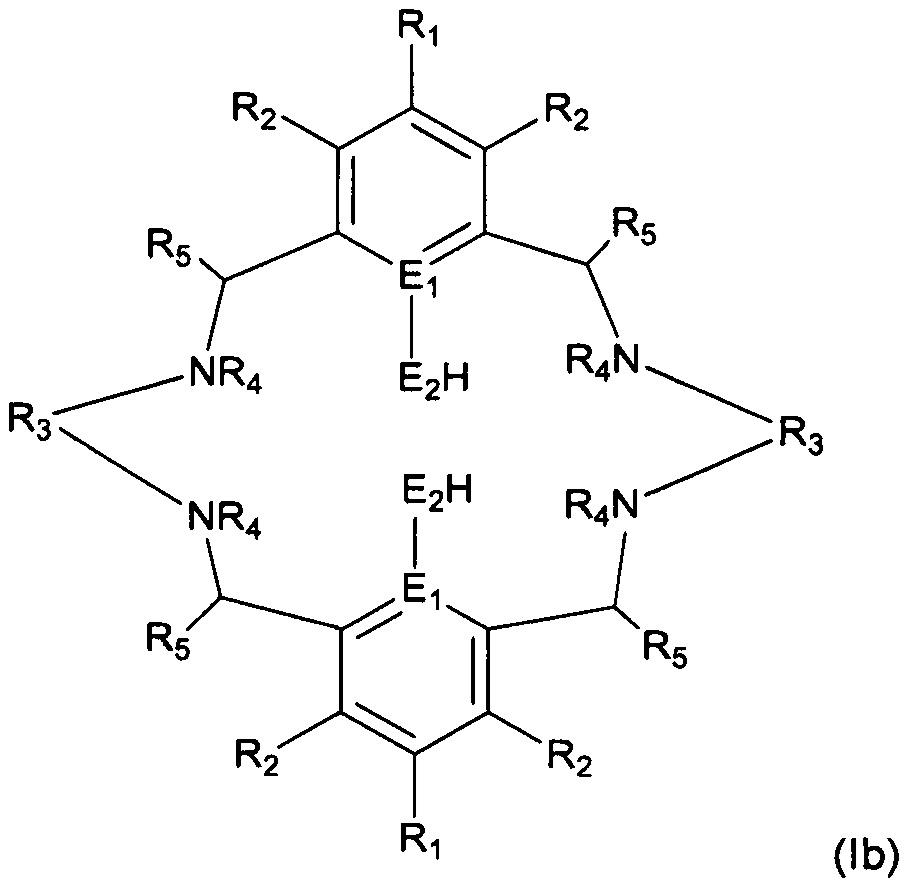
а) осуществление реакции лиганда формулы (Ib):
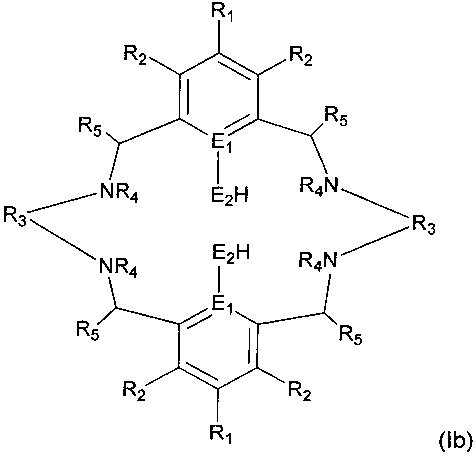
с соединением формулы (IV):

где n соответствует степени окисления M1;
RM1 независимо выбран из водорода и необязательно замещенного алкила, алкенила, алкинила, циклоалкила, циклоалкенила, циклоалкинила, арила, гетероарила, амино, алкокси, арилокси, алкилтио или алкиларила; и
b) осуществление реакции продукта стадии а) с соединением формулы (V):

где m соответствует степени окисления M2;
c) необязательно добавление соединения, содержащего G;
где R1-R5, E1, E2, M1, M2, X и G являются такими, как определено для катализатора по первому аспекту настоящего изобретения.
Краткое описание фигур
Варианты осуществления настоящего изобретения описаны ниже посредством примера и со ссылкой на прилагаемые рисунки, при этом
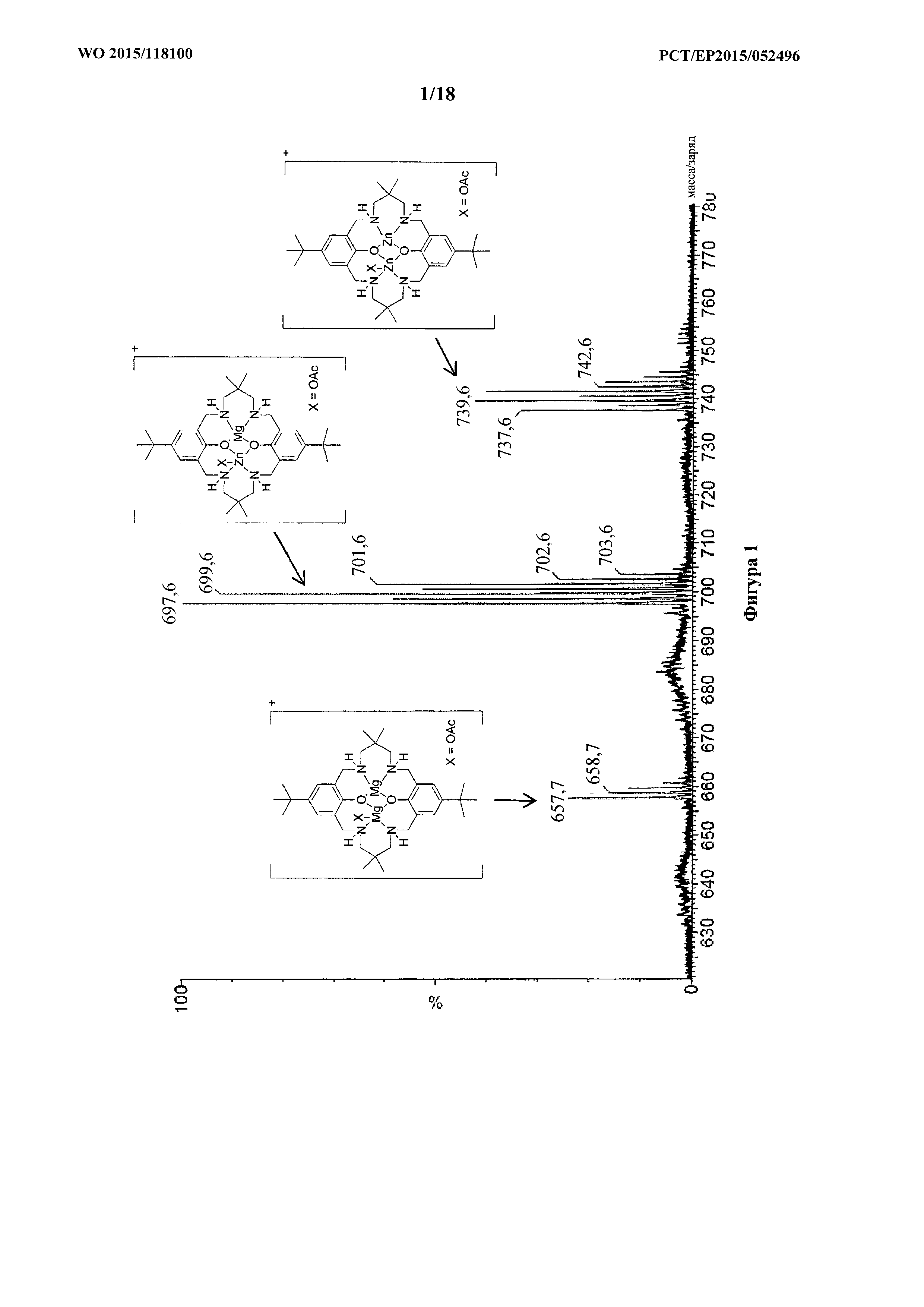
фигура 1: MALDI-ToF масс-спектр для продукта примера 1а, каталитической системы 1, с проиллюстрированной структурой молекулярных ионов.
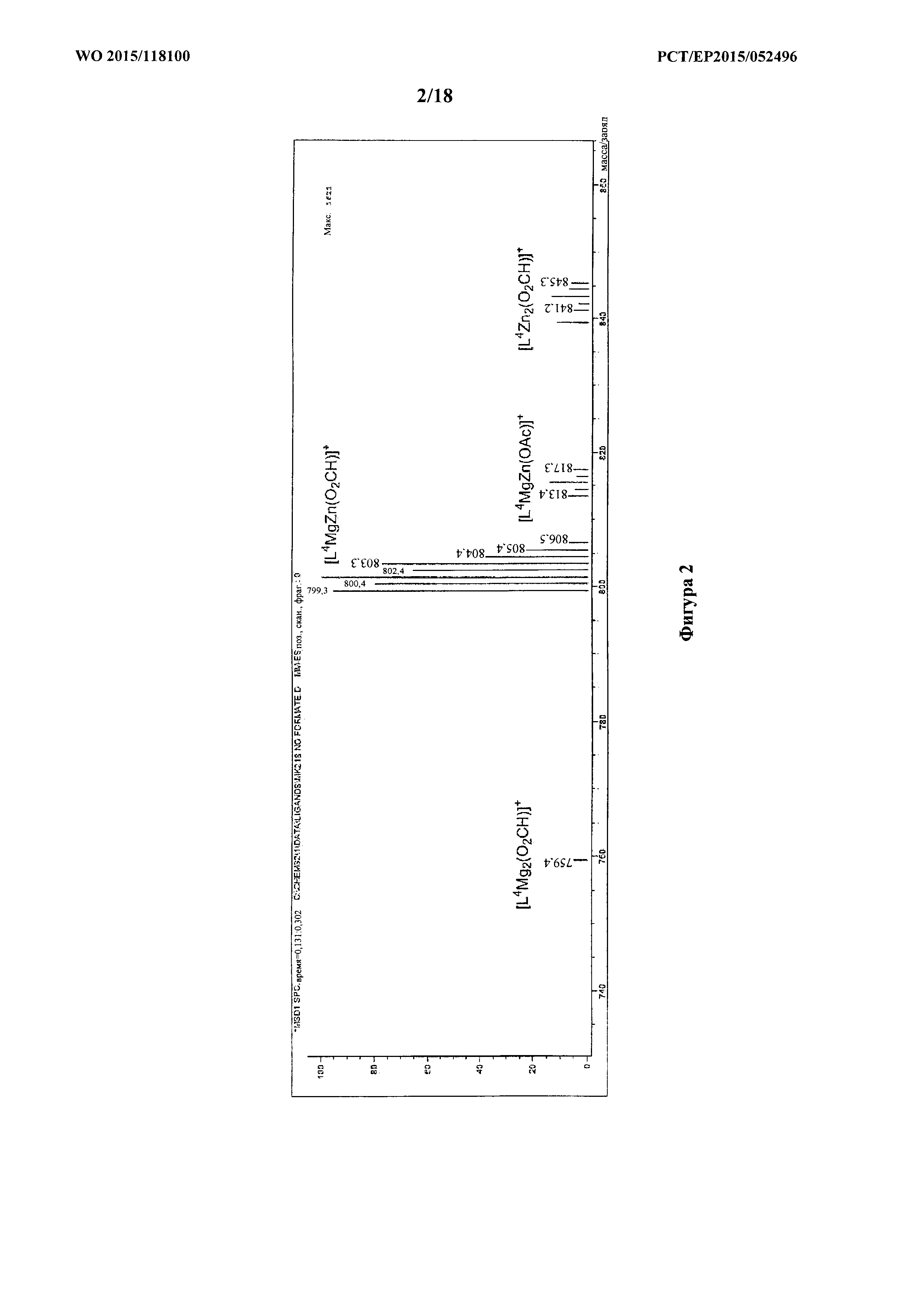
фигура 2: ESI-масс-спектр для продукта примера 1b, каталитической системы 2, с проиллюстрированной структурой молекулярных ионов.
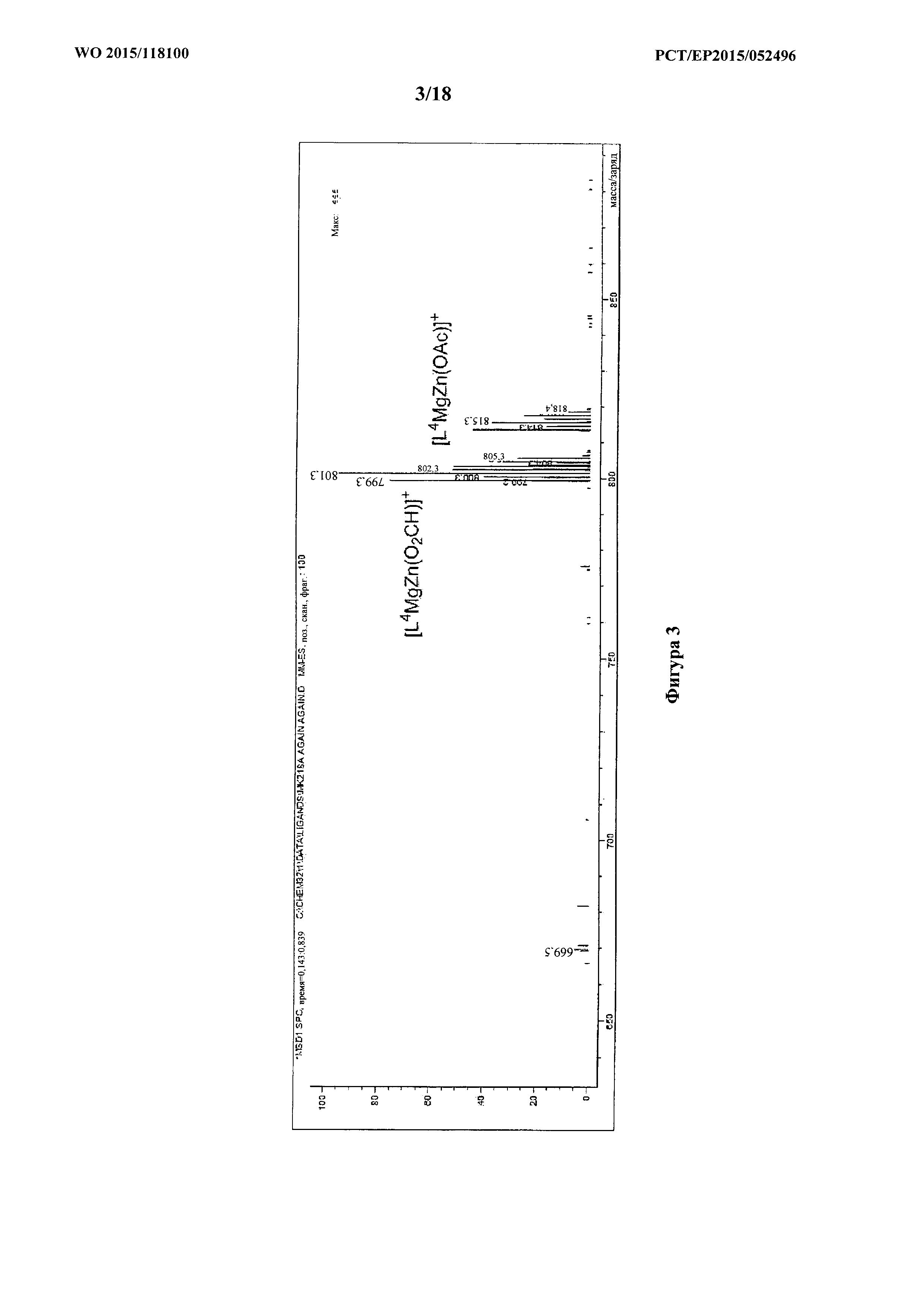
фигура 3: ESI-масс-спектр для продукта примера 1c, [L4ZnMg(OAc)2], кристаллизованный из каталитической системы 2, с проиллюстрированной структурой молекулярных ионов.
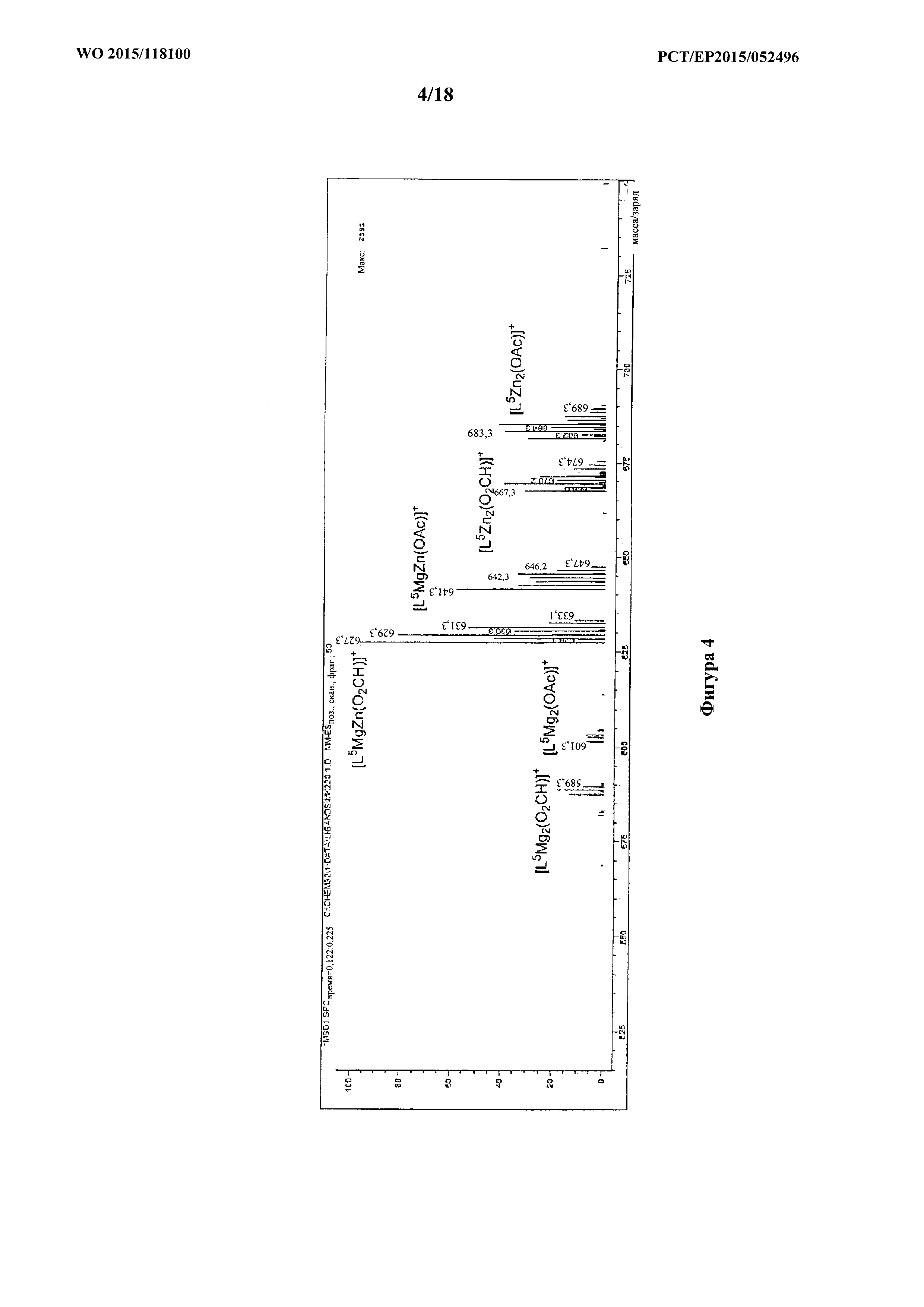
фигура 4: ESI-масс-спектр для продукта примера 1d, каталитической системы 3, с проиллюстрированной структурой молекулярных ионов.
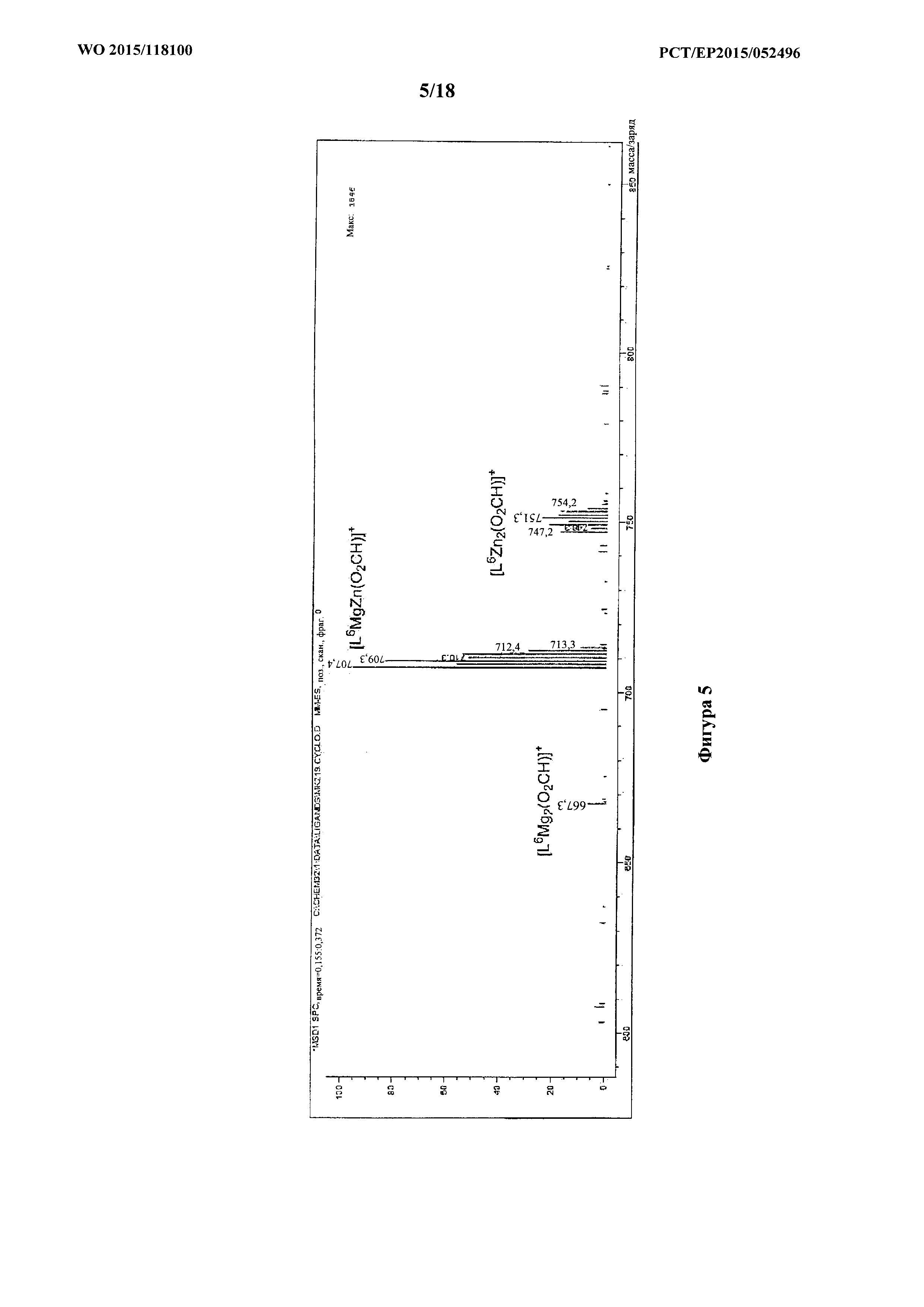
фигура 5: ESI-масс-спектр для продукта примера 1е, каталитической системы 4, с проиллюстрированной структурой молекулярных ионов.
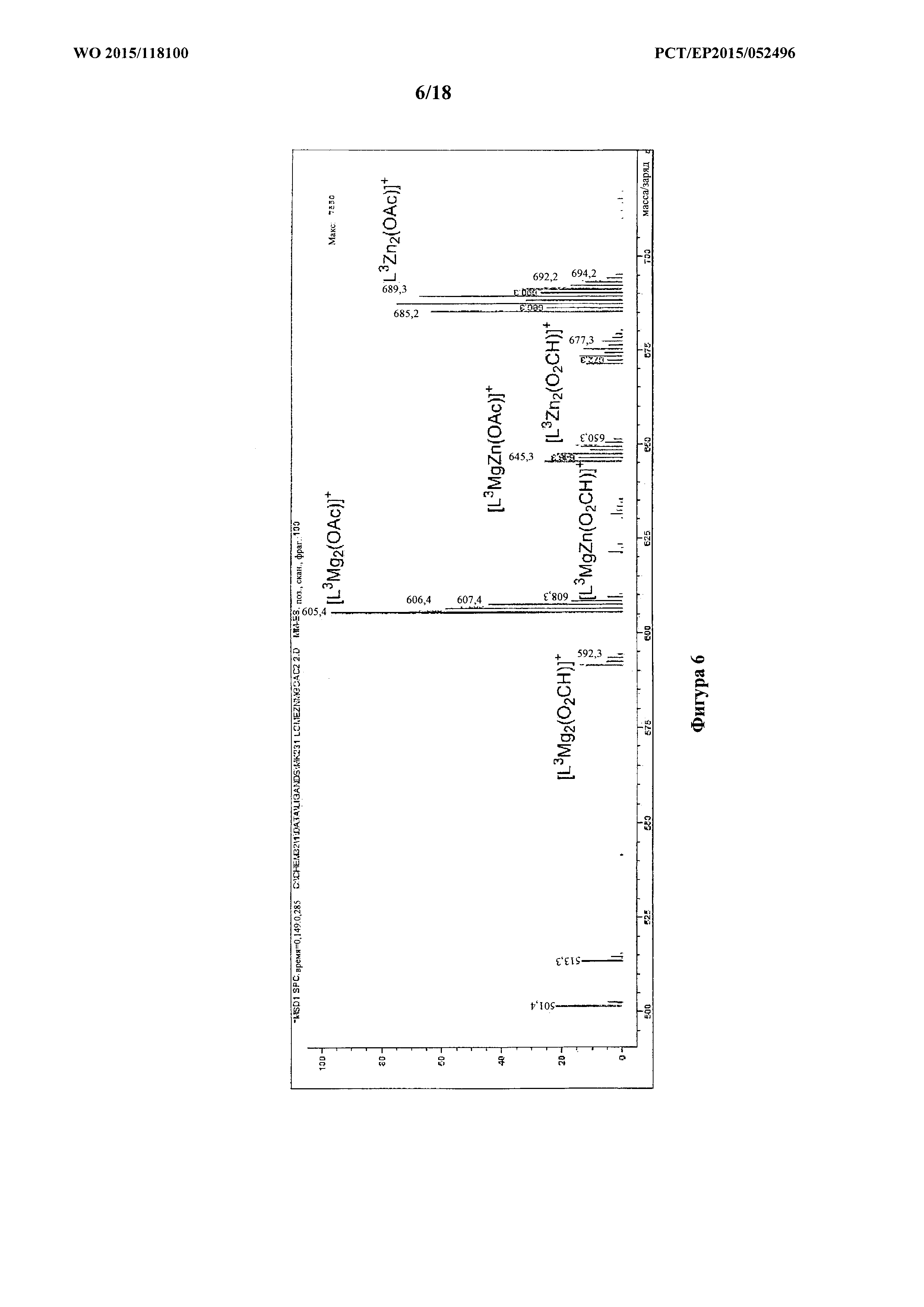
фигура 6: ESI-масс-спектр для продукта примера 1f, каталитической системы 5, с проиллюстрированной структурой молекулярных ионов.
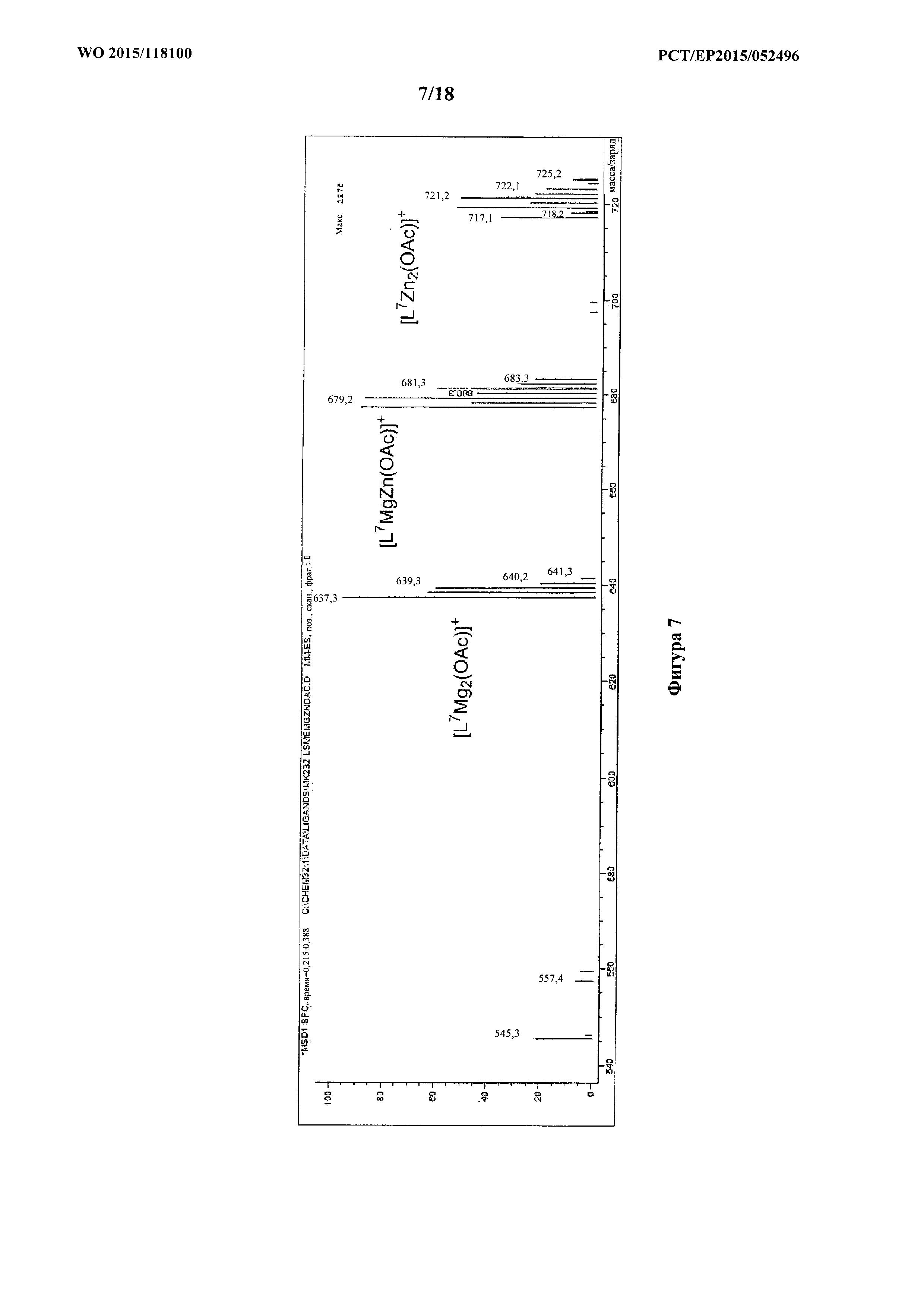
фигура 7: ESI-масс-спектр для продукта примера 1g, каталитической системы 6, с проиллюстрированной структурой молекулярных ионов.
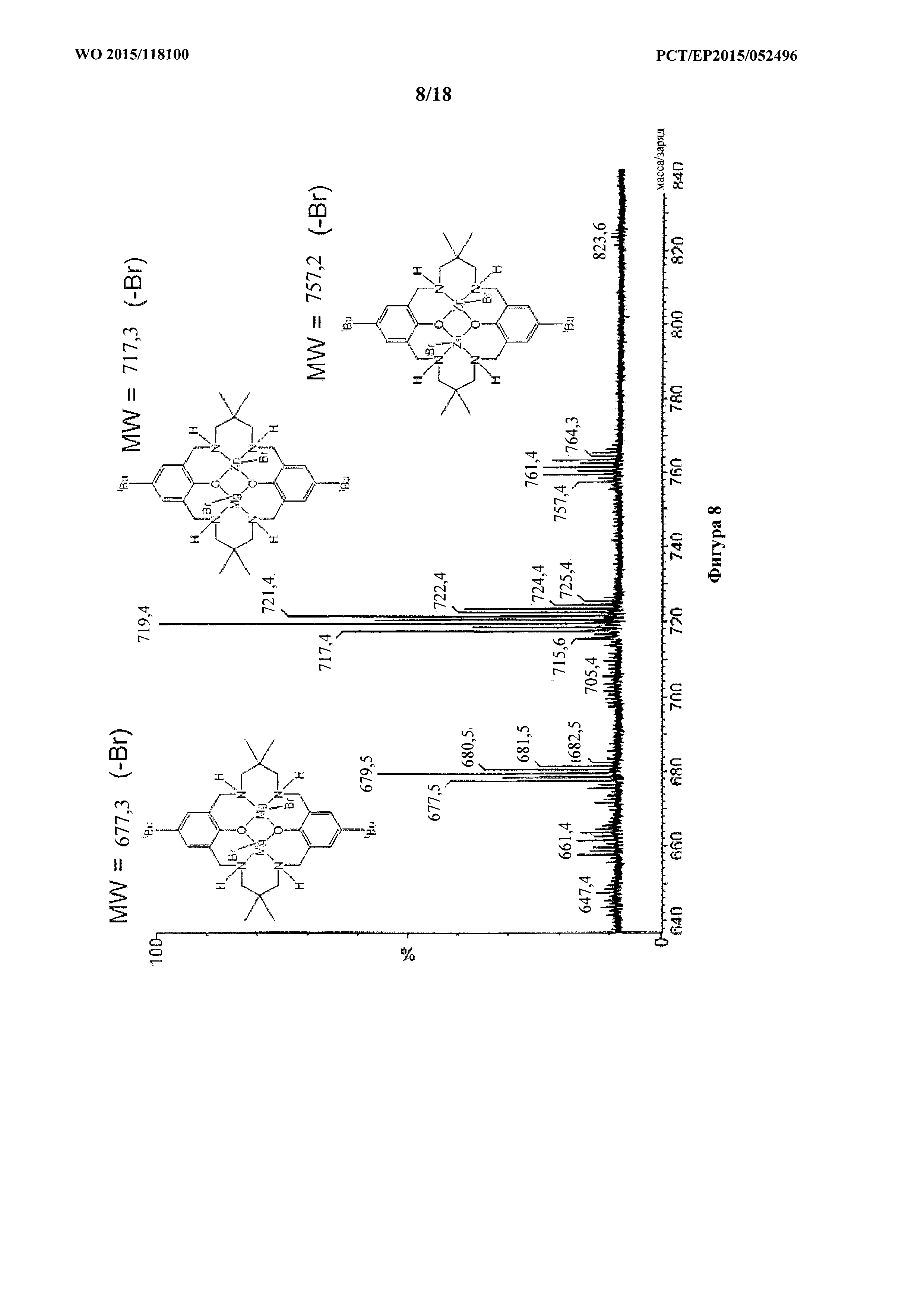
фигура 8: MALDI-ToF масс-спектр для продукта примера 1h, каталитической системы 7, с проиллюстрированной структурой молекулярных ионов.
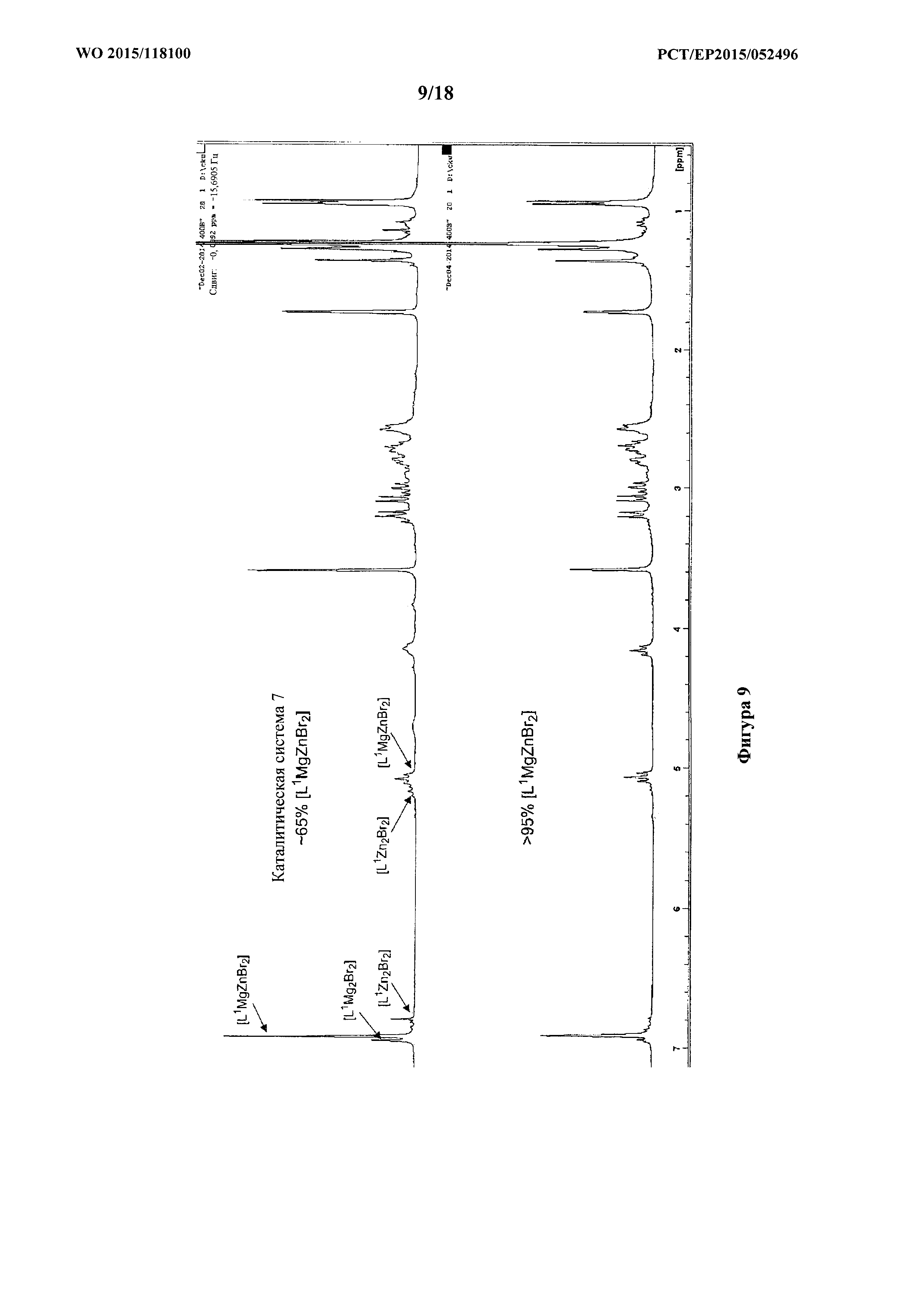
фигура 9: сравнение 1H NMR спектра каталитической системы 7 (верхняя часть) и продукта примера 1i, [L1MgZnBr2] (нижняя часть), указывающее на различие в степени чистоты.
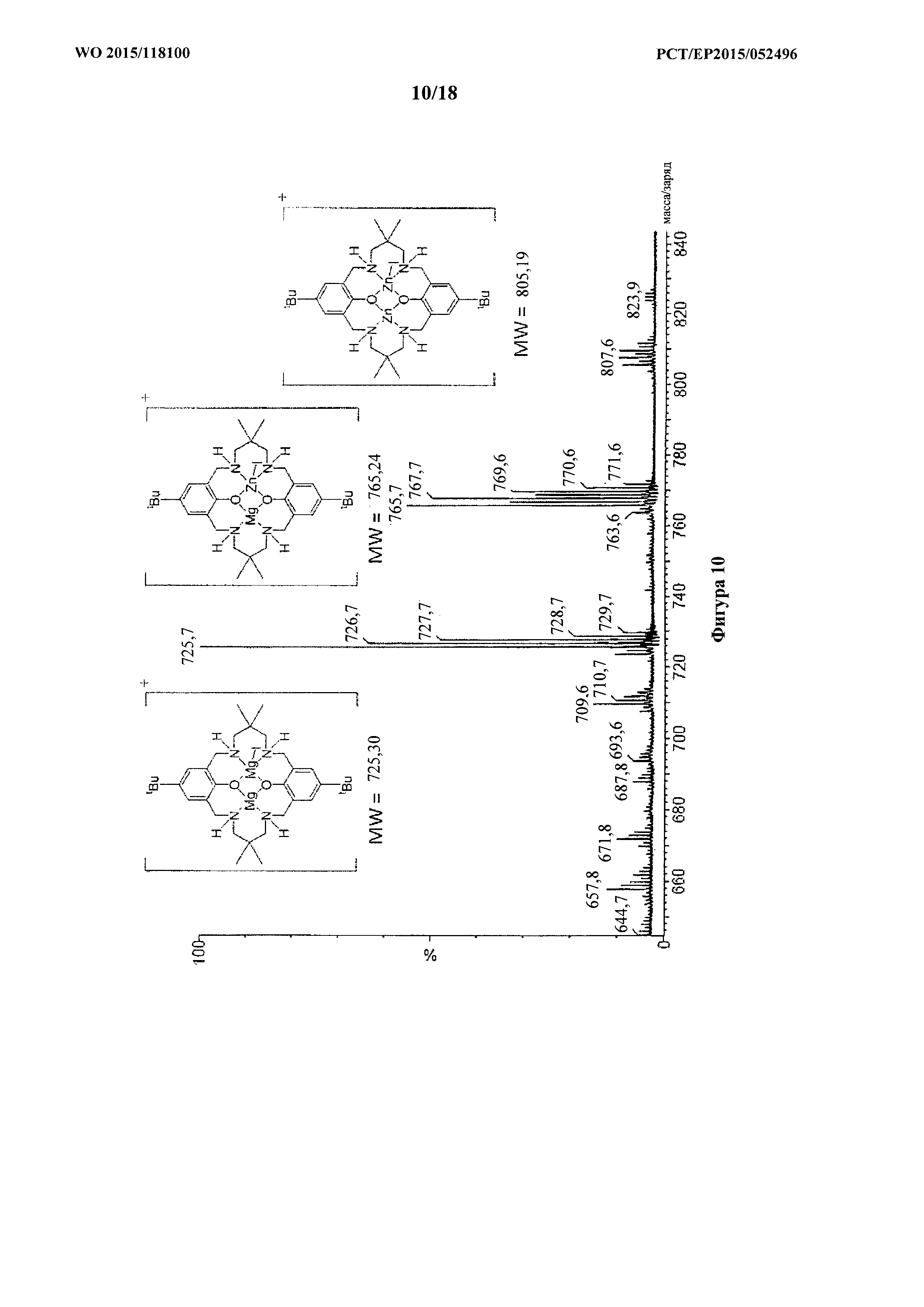
фигура 10: MALDI-ToF масс-спектр для продукта примера 1j, каталитической системы 8, с проиллюстрированной структурой молекулярных ионов.
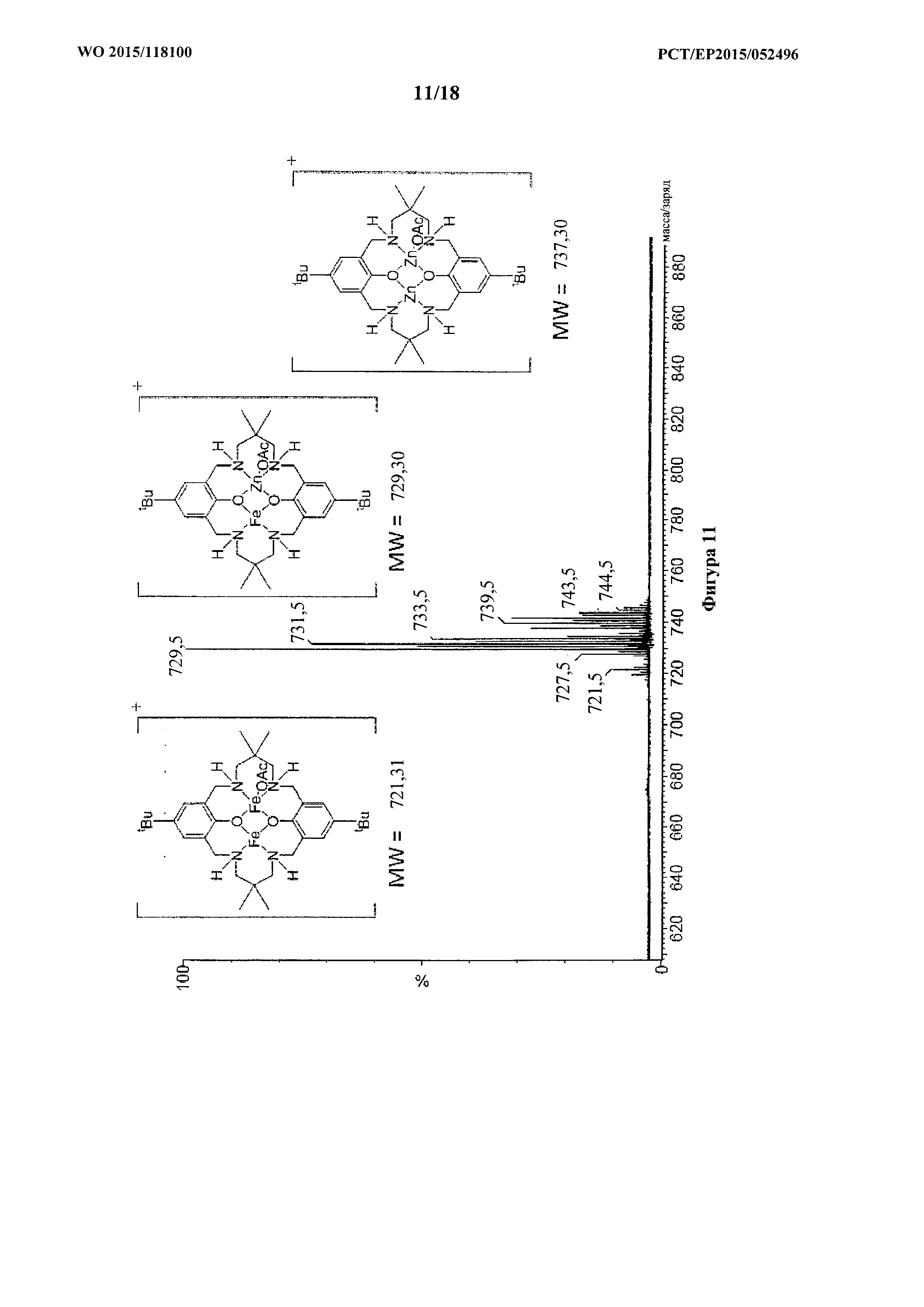
фигура 11: MALDI-ToF масс-спектр для продукта примера 1k, каталитической системы 9, с проиллюстрированной структурой молекулярных ионов.
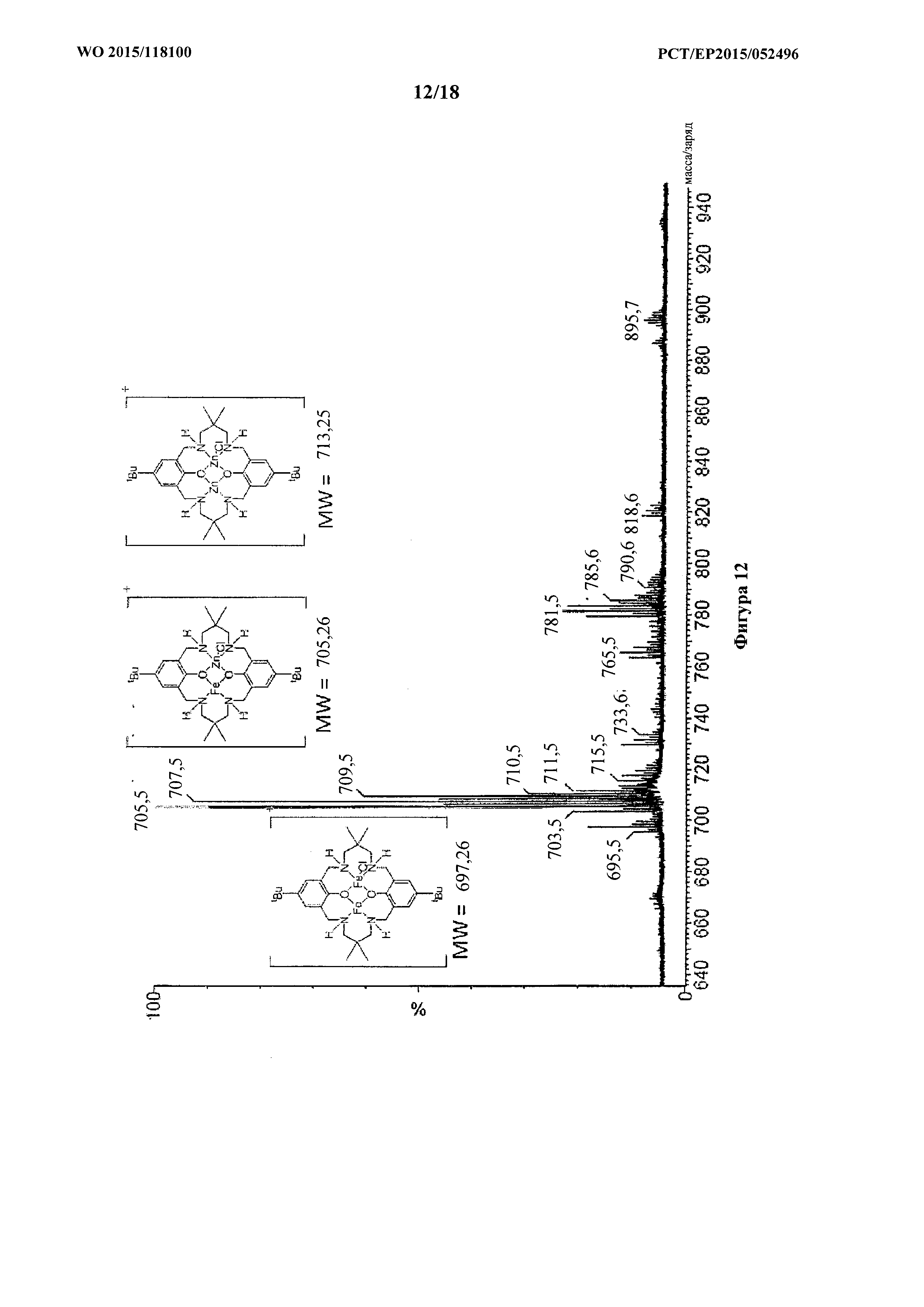
фигура 12: MALDI-ToF масс-спектр для продукта примера 1l, каталитической системы 10, с проиллюстрированной структурой молекулярных ионов.
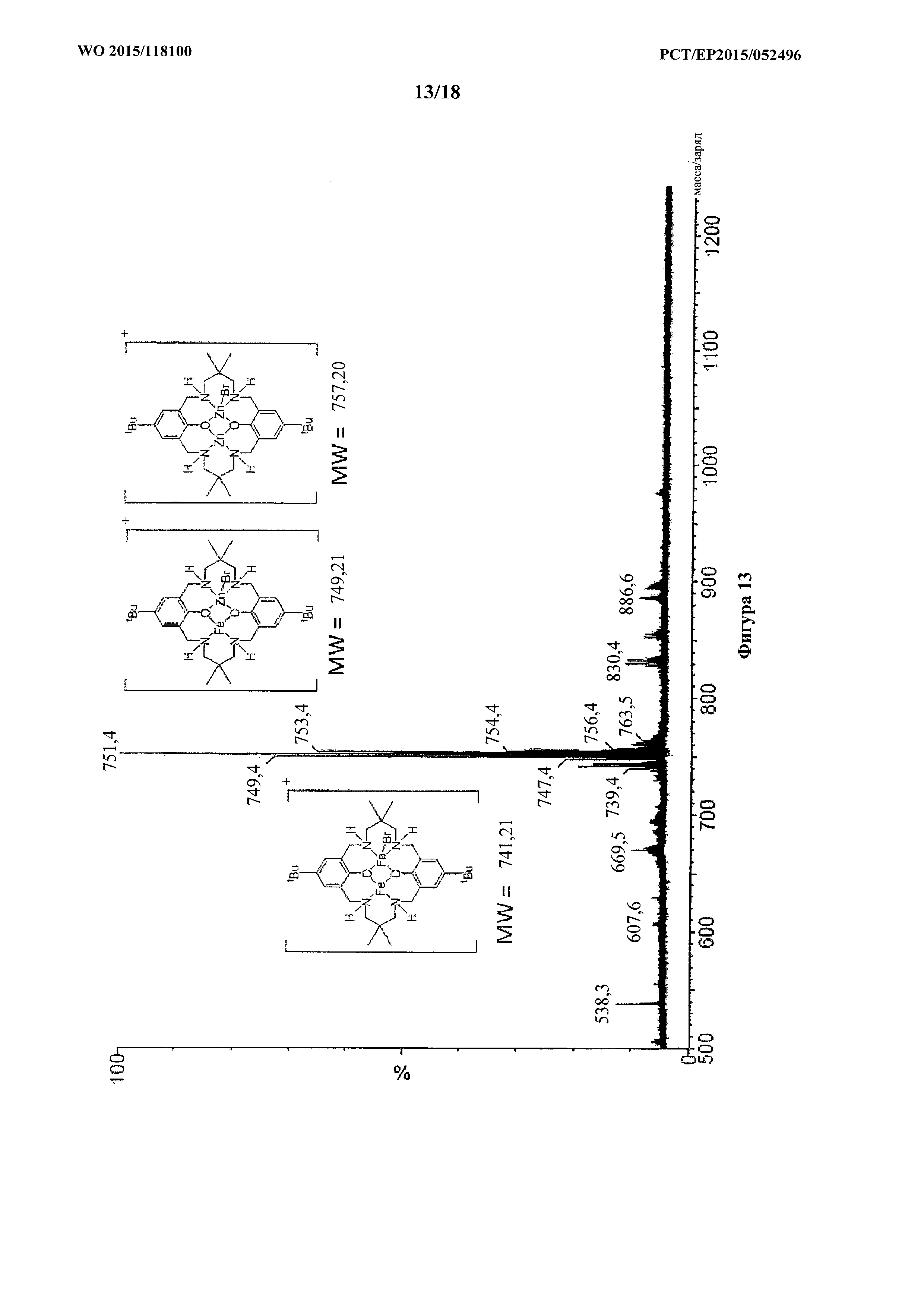
фигура 13: MALDI-ToF масс-спектр для продукта примера 1m, каталитической системы 11, с проиллюстрированной структурой молекулярных ионов.
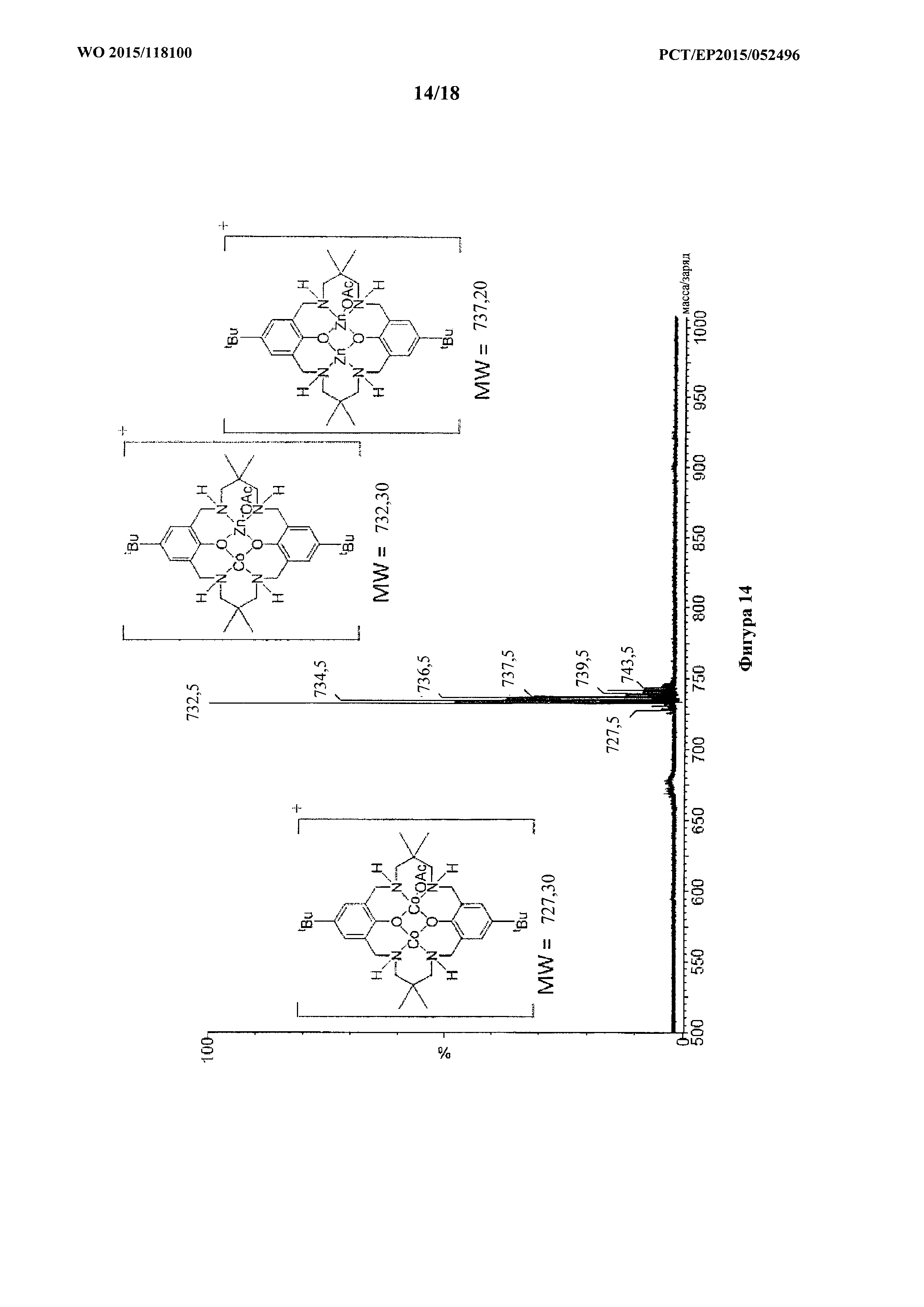
фигура 14: MALDI-ToF масс-спектр для продукта примера 1n, каталитической системы 12, с проиллюстрированной структурой молекулярных ионов.
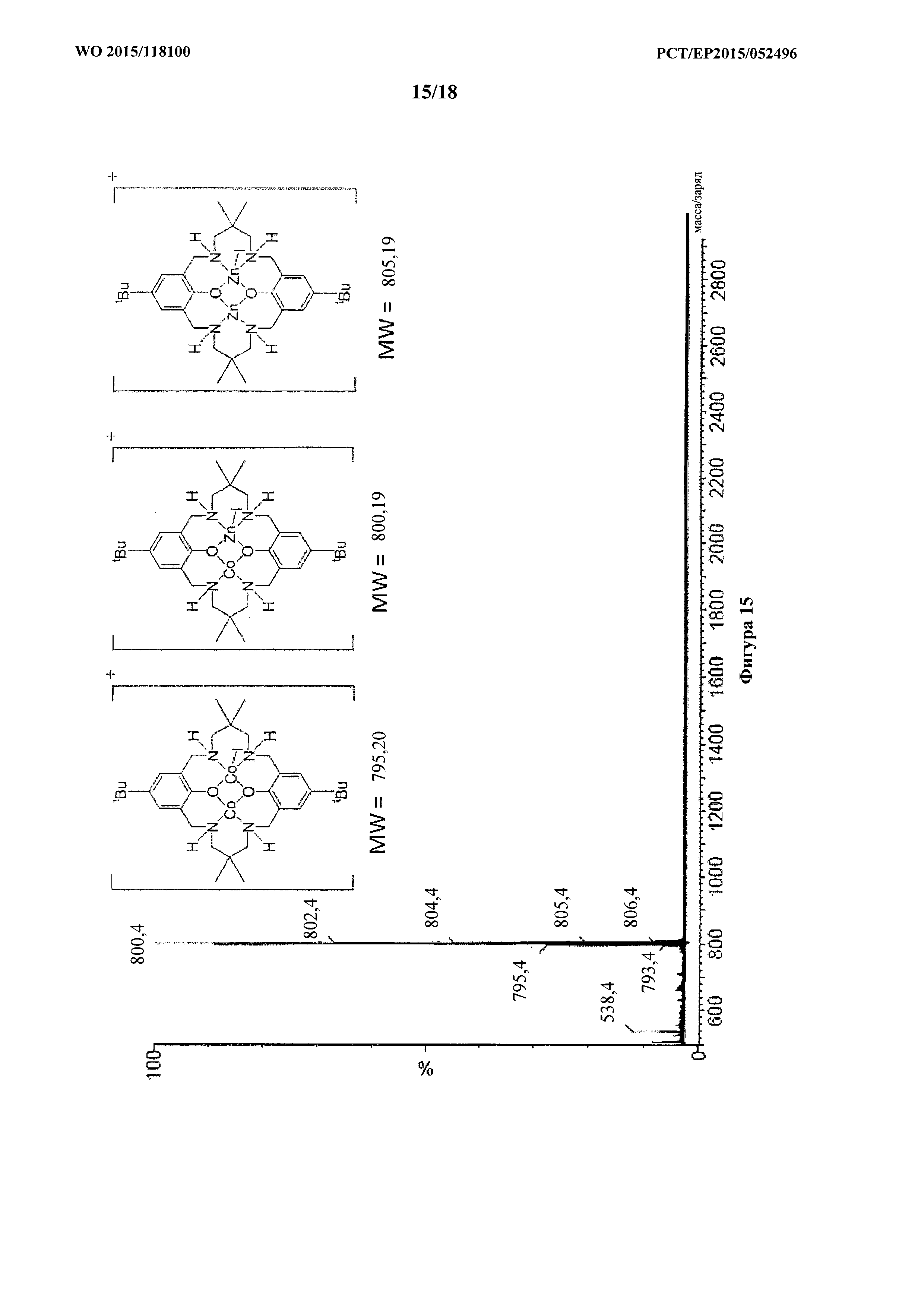
фигура 15: MALDI-ToF масс-спектр для продукта примера 1o, каталитической системы 13, с проиллюстрированной структурой молекулярных ионов.
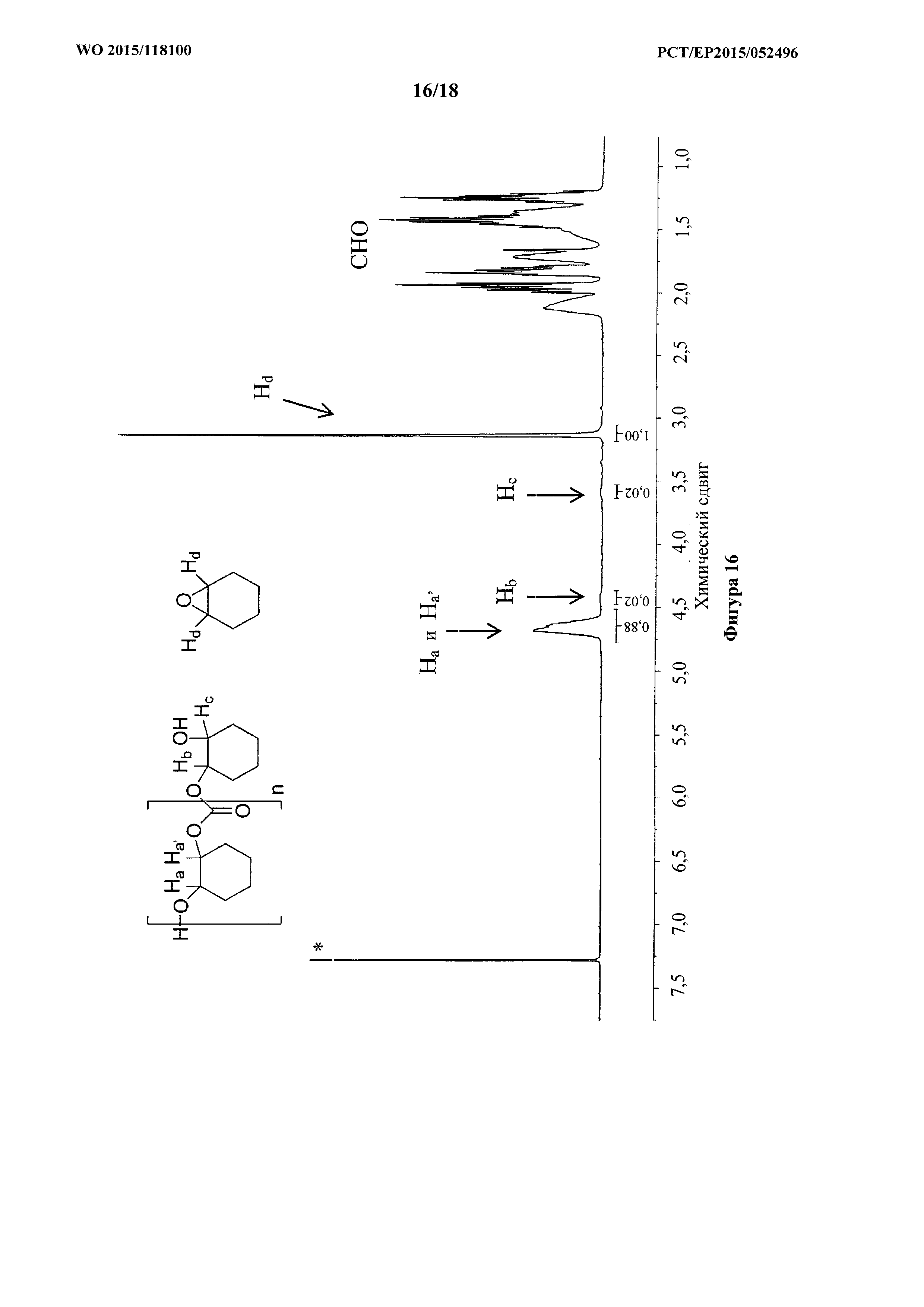
фигура 16: 1H NMR спектр непереработанной смеси CHO/CO2 для реакции сополимеризации, применяемый для расчета TON и TOF каталитической системы 1. Спектр подтверждает отсутствие сигналов, вызванных побочными продуктами - циклическим карбонатом (4 ppm) или простыми эфирными связями (3,4 ppm).
фигура 17: MALDI-ToF спектр поли(циклогексен карбоната), полученный вследствие применения каталитической системы 1.
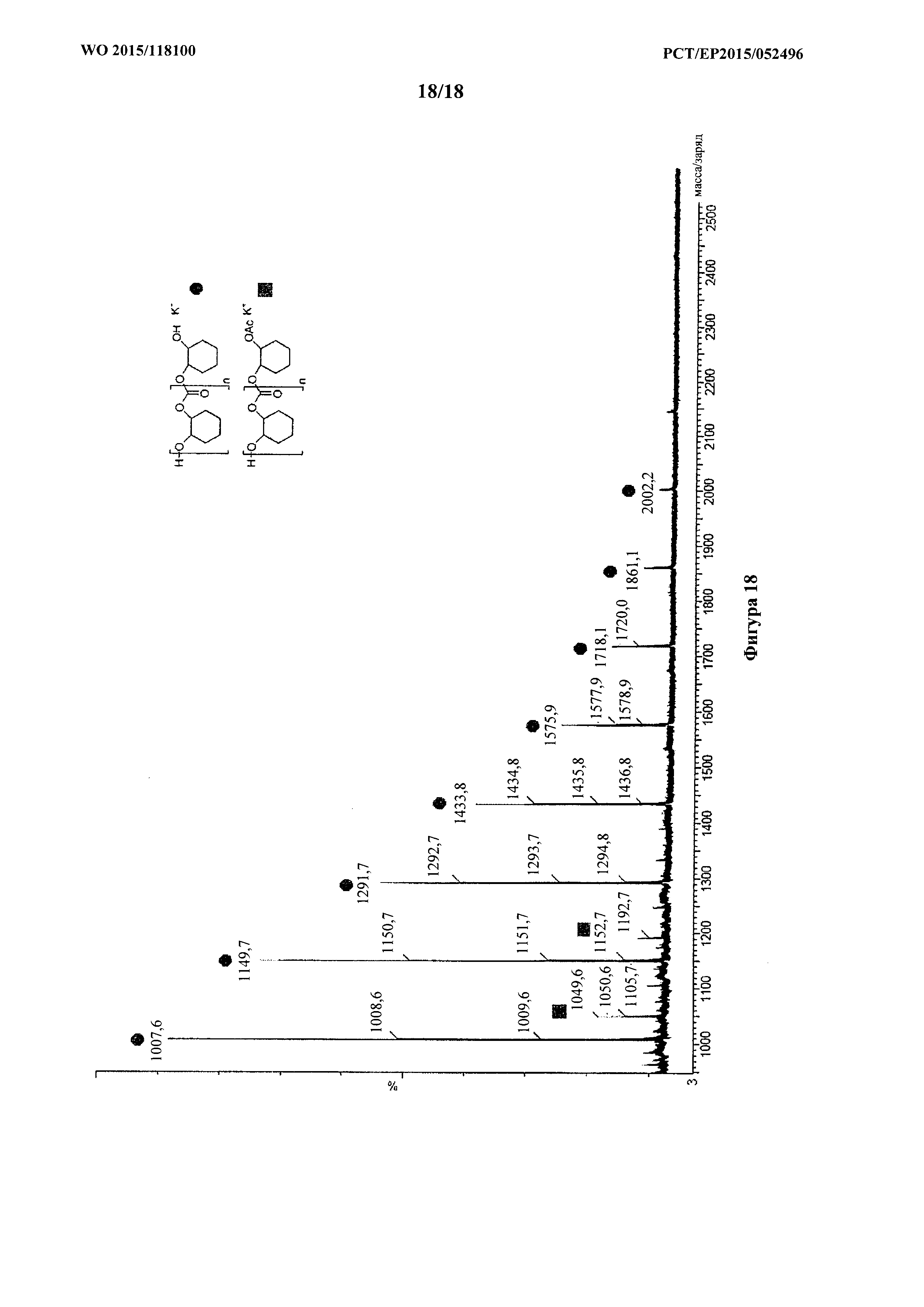
фигура 18: MALDI-ToF спектр поли(циклогексенкарбоната), полученный при применении каталитической системы 1, с 16 эквивалентами воды.
Определения
Для цели настоящего изобретения алифатическая группа представляет собой углеводородный фрагмент, который может представлять собой линейную или разветвленную цепь и может быть полностью насыщенным или содержать одно или несколько ненасыщенных звеньев, но который не является ароматическим. Термин "ненасыщенный" относится к фрагменту, который содержит одну или несколько двойных/или тройных связей. Таким образом, термин "алифатический" предназначен для охвата алкильных, алкенильных или алкинильных групп и их комбинаций. Алифатическая группа предпочтительно представляет собой C1-20алифатическую группу, то есть алифатическую группу с 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20 атомами углерода. Предпочтительно алифатическая группа представляет собой C1-15алифатическую, более предпочтительно C1-12алифатическую, более предпочтительно C1-10алифатическую, еще более предпочтительно C1-8алифатическую, а именно C1-6алифатическую группу.
Алкильная группа предпочтительно представляет собой "C1-20алкильную группу", то есть алкильную группу, представляющую собой линейную или разветвленную цепь с 1-20 углеродами. Таким образом, алкильная группа состоит из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20 атомов углерода. Предпочтительно алкильная группа представляет собой C1-15алкильную, предпочтительно C1-12алкильную, более предпочтительно C1-10алкильную, еще более предпочтительно C1-8алкильную, еще более предпочтительно C1-6алкильную группу. Более конкретно, примеры "C1-20алкильной группы" включают метильную группу, этильную группу, н-пропильную группу, изопропильную группу, н-бутильную группу, изобутильную группу, втор-бутильную группу, трет-бутильную группу, н-пентильную группу, н-гексильную группу, н-гептильную группу, н-октильную группу, н-нонильную группу, н-децильную группу, н-ундецильную группу, н-додецильную группу, н-тридецильную группу, н-тетрадецильную группу, н-пентадецильную группу, н-гексадецильную группу, н-гептадецильную группу, н-октадецильную группу, н-нонадецильную группу, н-эйкозильную группу, 1,1-диметилпропильную группу, 1,2-диметилпропильную группу, 2,2-диметилпропильную группу, 1-этилпропильную группу, н-гексильную группу, 1-этил-2-метилпропильную группу, 1,1,2-триметилпропильную группу, 1-этилбутильную группу, 1-метилбутильную группу, 2-метилбутильную группу, 1,1-диметилбутильную группу, 1,2-диметилбутильную группу, 2,2-диметилбутильную группу, 1,3-диметилбутильную группу, 2,3-диметилбутильную группу, 2-этилбутильную группу, 2-метилпентильную группу, 3-метилпентильную группу и им подобные.
Алкенильная и алкинильная группы представляют собой предпочтительно "C2-20алкенильную" и "C2-20алкинильную", более предпочтительно "C2-15алкенильную" и "C2-15алкинильную", еще более предпочтительно "C2-12алкенильную" и "C2-12алкинильную", еще более предпочтительно "C2-10алкенильную" и "C2-10алкинильную", еще более предпочтительно "C2-8алкенильную" и "C2-8алкинильную", наиболее предпочтительно "C2-6алкенильную" и "C2-6алкинильную" группы, соответственно.
Гетероалифатическая группа представляет собой описанную выше алифатическую группу, которая дополнительно содержит один или несколько гетероатомов. Таким образом, гетероалифатические группы предпочтительно содержат от 2 до 21 атомов, предпочтительно от 2 до 16 атомов, более предпочтительно от 2 до 13 атомов, более предпочтительно от 2 до 11 атомов, более предпочтительно от 2 до 9 атомов, еще более предпочтительно от 2 до 7 атомов, где по меньшей мере один атом представляет собой атом углерода. Особенно предпочтительные гетероатомы выбраны из O, S, N, P и Si. Если гетероалифатические группы содержат два или более гетероатомов, то гетероатомы могут быть одинаковыми или различными.
Алициклическая группа представляет собой насыщенную или частично ненасыщенную циклическую алифатическую моноциклическую или полицилическую (в том числе конденсированную, мостиковую и спиро-конденсированную) кольцевую систему, которая содержит от 3 до 20 атомов углерода, то есть алициклическую группу с 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20 атомами углерода. Предпочтительно алициклическая группа содержит от 3 до 15, более предпочтительно от 3 до 12, еще более предпочтительно от 3 до 10, еще более предпочтительно от 3 до 8, еще более предпочтительно от 3 до 6 атомов углерода. Термин "алициклическая" охватывает циклоалкильную, циклоалкенильную и циклоалкинильную группы. Следует понимать, что алициклическая группа может содержать алициклическое кольцо, несущее один или несколько связывающих или несвязывающих алкильных заместителей, таких как-CH2-циклогексил. В частности, примеры C3-20циклоалкильной группы включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, адамантил и циклооктил.
Гетероалициклическая группа представляет собой определенную выше алициклическую группу, которая помимо атомов углерода содержит один или несколько кольцевых гетероатомов, которые предпочтительно выбраны из O, S, N, P и Si. Гетероалициклические группы предпочтительно содержат от одного до четырех гетероатомов, которые могут быть одинаковыми или различными. Гетероциклические группы предпочтительно содержат от 5 до 20 атомов, более предпочтительно от 5 до 14 атомов, еще более предпочтительно от 5 до 12 атомов.
Арильная группа представляет собой моноциклическую или полициклическую кольцевую систему, содержащую от 5 до 20 атомов углерода. Арильная группа предпочтительно представляет собой "C6-12арильную группу" и представляет собой арильную группу, составленную из 6, 7, 8, 9, 10, 11 или 12 атомов углерода и включающую конденсированные кольцевые группы, такие как моноциклическая кольцевая группа или бициклическая кольцевая группа и им подобные. В частности, примеры "C6-10арильной группы" включают фенильную группу, бифенильную группу, инденильную группу, нафтильную группу или азуленильную группу и им подобные. Необходимо отметить, что конденсированные кольца, такие как индан и тетрагидронафталин, также включены в арильную группу.
Гетероарильная группа представляет собой арильную группу, которая помимо атомов углерода содержит от одного до четырех гетероатомов, которые предпочтительно выбраны из O, S, N, P и Si. Гетероарильная группа предпочтительно содержит от 5 до 20, более предпочтительно от 5 до 14 кольцевых атомов. В частности, примеры гетероарильной группы включают пиридин, имидазол, метилимидазол и диметиламинопиримидин.
Примеры алициклической, гетероалициклической, арильной и гетероарильной групп включают без ограничения циклогексил, фенил, акридин, бензимидазол, бензофуран, бензотиофен, бензоксазол, бензотиазол, карбазол, циннолин, диоксин, диоксан, диоксолан, дитиан, дитиазин, дитиазол, дитиолан, фуран, имидазол, имидазолин, имидазолидин, индол, индолин, индолизин, индазол, изоиндол, изохинолин, изоксазол, изотиазол, морфолин, нафтиридин, оксазол, оксадиазол, оксатиазол, оксатиазолидин, оксазин, оксадиазин, феназин, фенотиазин, феноксазин, фталазин, пиперазин, пиперидин, птеридин, пурин, пиран, пиразин, пиразол, пиразолин, пиразолидин, пиридазин, пиридин, пиримидин, пиррол, пирролидин, пирролин, хинолин, хиноксалин, хиназолин, хинолизин, тетрагидрофуран, тетразин, тетразол, тиофен, тиадиазин, тиадиазол, тиатриазол, тиазин, тиазол, тиоморфолин, тианафталин, тиопиран, триазин, триазол и тритиан.
Термин "галогенид" или "галоген" в данном документе применяются взаимозаменяемо и при использовании в данном документе означает атом фтора, атом хлора, атом брома, атом йода и им подобные, предпочтительно атом фтора, атом брома или атом хлора, и более предпочтительно атом фтора.
Галогеналкильная группа предпочтительно представляет собой "C1-20галогеналкильную группу", более предпочтительно "C1-15галогеналкильную группу", более предпочтительно "C1-12галогеналкильную группу", более предпочтительно "C1-10галогеналкильную группу", еще более предпочтительно "C1-8галогеналкильную группу", еще более предпочтительно "C1-6галогеналкильную группу, и представляет собой C1-20алкильную, C1-15алкильную, C1-12алкильную, C1-10алкильную, C1-8алкильную или C1-6алкильную группу соответственно, замещенную, как описано выше, по меньшей мере одним атомом галогена, предпочтительно 1, 2 или 3 атомом(ами) галогена. В частности, примеры "C1-20галогеналкильной группы" включают фторметильную группу, дифторметильную группу, трифторметильную группу, фторэтильную группу, дифторэтильную группу, трифторэтильную группу, хлорметильную группу, бромметильную группу, йодметильную группу и им подобные.
Алкоксигруппа предпочтительно представляет собой "C1-20алкоксигруппу", более предпочтительно "C1-15алкоксигруппу", более предпочтительно "C1-12алкоксигруппу", более предпочтительно "C1-10алкоксигруппу", еще более предпочтительно "C1-8алкоксигруппу", еще более предпочтительно "C1-6алкоксигруппу, и представляет собой оксигруппу, связанную с определенной выше C1-20алкильной, C1-15алкильной, C1-12алкильной, C1-10алкильной, C1-8алкильной или C1-6алкильной группой, соответственно. В частности, примеры "C1-20алкоксигруппы" включают метоксигруппу, этоксигруппу, н-пропоксигруппу, изопропоксигруппу, н-бутоксигруппу, изобутоксигруппу, втор-бутоксигруппу, трет-бутоксигруппу, н-пентилоксигруппу, изопентилоксигруппу, втор-пентилоксигруппу, н-гексилоксигруппу, изогексилоксигруппу, н-гексилоксигруппу, н-гептилоксигруппу, н-октилоксигруппу, н-нонилоксигруппу, н-децилоксигруппу, н-ундецилоксигруппу, н-додецилоксигруппу, н-тридецилоксигруппу, н-тетрадецилдоксигруппу, н-пентадецилоксигруппу, н-гекадецилоксигруппу, н-гептадецилоксигруппу, н-октадецилоксигруппу, н-нонадецилоксигруппу, н-эйкозилоксигруппу, 1,1-диметилпропоксигруппу, 1,2-диметилпропоксигруппу, 2,2-диметилпропоксигруппу, 2-метилбутоксигруппу, 1-этил-2-метилпропоксигруппу, 1,1,2-триметилпропоксигруппу, 1,1-диметилбутоксигруппу, 1,2-диметилбутоксигруппу, 2,2-диметилбутоксигруппу, 2,3-диметилбутоксигруппу, 1,3-диметилбутоксигруппу, 2-этилбутоксигруппу, 2-метилпентилоксигруппу, 3-метилпентилоксигруппу и им подобные.
Арилоксигруппа предпочтительно представляет собой "C5-20арилоксигруппу", более предпочтительно "C6-12арилоксигруппу", еще более предпочтительно "C6-10арилоксигруппу" и представляет собой оксигруппу, которая связана с определенной выше C5-20арильной, C6-12арильной или C6-10арильной группой, соответственно.
Алкилтиогруппа предпочтительно представляет собой "C1-20алкилтиогруппу", более предпочтительно "C1-15алкилтиогруппу", более предпочтительно "C1-12алкилтиогруппу", более предпочтительно "C1-10алкилтиогруппу", еще более предпочтительно "C1-8алкилтиогруппу", еще более предпочтительно "C1-6алкилтиогруппу" и представляет собой тио-(-S-)группу, которая связана с определенной выше C1-20алкильной, C1-15алкильной, C1-12алкильной, C1-10алкильной, C1-8алкильной или C1-6алкильной группой, соответственно.
Арилтиогруппа предпочтительно представляет собой "C5-20арилтиогруппу", более предпочтительно "C6-12арилтиогруппу", еще более предпочтительно "C6-10арилтиогруппу" и представляет собой тио-(-S-)группу, которая связана с определенной выше C5-20арильной, C6-12арильной или C6-10арильной группой, соответственно.
Алкиларильная группа предпочтительно представляет собой "C6-12арилC1-20алкильную группу", более предпочтительно предпочтительную "C6-12арилC1-16алкильную группу", еще более предпочтительно "C6-12арилC1-6алкильную группу" и представляет собой определенную выше арильную группу, которая в любом положении связана с определенной выше алкильной группой. Точка присоединения алкиларильной группы к молекуле может быть расположена в алкильной части и, таким образом, предпочтительно алкиларильная группа представляет собой -CH2-Ph или -CH2CH2-Ph. Алкиларильная группа может также обозначаться как "аралкил".
Силильная группа предпочтительно представляет собой группу -Si(Rs)3, где каждый Rs независимо может представлять собой водород, алифатическую, гетероалифатическую, алициклическую, гетероалициклическую, арильную или гетероарильную группу, определенную выше. В определенных вариантах осуществления каждый Rs может представлять собой водород или незамещенную алифатическую, алициклическую или арильную группу. Предпочтительно каждый Rs независимо выбран из водорода или алкильной группы, выбранной из метила, этила или пропила.
Группа простого силилового эфира предпочтительно представляет собой группу OSi(R6)3 где каждый R6 независимо может представлять собой водород или алифатическую, гетероалифатическую, алициклическую, гетероалициклическую, арильную или гетероарильную группу, определенную выше. В определенных вариантах осуществления каждый R6 независимо может представлять собой водород или незамещенную алифатическую, алициклическую или арильную группу. Предпочтительно каждый R6 представляет собой водород или алкильную группу, выбранную из метила, этила или пропила.
Нитрильная группа (также обозначаемая как цианогруппа) представляет собой группу CN.
Иминогруппа представляет собой группу -CRNR, предпочтительно группу -CHNR7, где R7 представляет собой алифатическую, гетероалифатическую, алициклическую, гетероалициклическую, арильную или гетероарильную группу, определенную выше. Согласно определенным вариантам осуществления R7 может представлять собой незамещенную алифатическую, алициклическую или арильную группу. Предпочтительно R7 представляет собой алкильную группу, выбранную из метила, этила или пропила.
Ацетилидная группа содержит тройную связь -C≡C-R9, где предпочтительно R9 может представлять собой алифатическую, гетероалифатическую, алициклическую, гетероалициклическую, арильную или гетероарильную группу, определенную выше. Для целей настоящего изобретения, если R9 представляет собой алкил, то тройная связь может присутствовать в любом положении вдоль алкильной цепи. В определенных вариантах осуществления R9 представляет собой незамещенную алифатическую, алициклическую или арильную группу. Предпочтительно R9 представляет собой метил, этил, пропил или фенил.
Аминогруппа группа предпочтительно представляет собой -NH2, -NHR10 или -N(R10)2, где R10 может представлять собой алифатическую, гетероалифатическую, алициклическую, гетероалициклическую, синильную, арильную или гетероарильную группу, определенную выше. Следует понимать, что аминогруппа представляет собой N(R10)2, каждая группа R10 может быть одинаковой или различной. В определенных вариантах осуществления каждый R10 независимо представляет собой незамещенную алифатическую, алициклическую синильную или арильную группу. Предпочтительно R10 представляет собой метил, этил, пропил, SiMe3 или фенил.
Амидогруппа предпочтительно представляет собой -NR11C(O)- или -C(O)-NR11-, где R11 может представлять собой водород, алифатическую, гетероалифатическую, алициклическую, гетероалициклическую, арильную или гетероарильную группу, определенную выше. В определенных вариантах осуществления R11 представляет собой незамещенную алифатическую, алициклическую или арильную группу. Предпочтительно R11 представляет собой водород, метил, этил, пропил или фенил. Амидогруппа может заканчиваться водородом, алифатической, гетероалифатической, алициклической, гетероалициклической, арильной или гетероарильной группой.
Сложноэфирная группа предпочтительно представляет собой -OC(O)R12- или -C(O)OR12-, где R12 может представлять собой водород, алифатическую, гетероалифатическую, алициклическую, гетероалициклическую, арильную или гетероарильную группу, определенную выше. Согласно определенным вариантам осуществления R12 может представлять собой незамещенную алифатическую, алициклическую или арильную группу. Предпочтительно R12 представляет собой водород, метил, этил, пропил или фенил. Сложноэфирная группа может заканчиваться водородом, алифатической, гетероалифатической, алициклической, гетероалициклической, арильной или гетероарильной группой.
Сульфоксид предпочтительно представляет собой -S(O)R13 и сульфонильная группа предпочтительно представляет собой -OS(O)2R13, где R13 может представлять собой водород, алифатическую, гетероалифатическую, алициклическую, гетероалициклическую, арильную или гетероарильную группу, определенную выше. В определенных вариантах осуществления R13 представляет собой незамещенную алифатическую, алициклическую или арильную группу. Предпочтительно R13 представляет собой водород, метил, этил, пропил или фенил.
Карбоксилатная группа предпочтительно представляет собой -OC(O)R14, где R14 может представлять собой водород, алифатическую, гетероалифатическую, алициклическую, гетероалициклическую, арильную или гетероарильную группу, определенную выше. В определенных вариантах осуществления R14 представляет собой незамещенную алифатическую, алициклическую или арильную группу. Предпочтительно R14 представляет собой водород, метил, этил, пропил, бутил (например, н-бутил, изобутил или трет-бутил), фенил, пентафторфенил, пентил, гексил, гептил, октил, нонил, децил, ундецил, додецил, тридецил, тетрадецил, пентадецил, гексадецил, гептадецил, октадецил, нонадецил, эйкозил, трифторметил или адамантил.
Ацетамид предпочтительно представляет собой MeC(O)N(R15)2, где R15 может представлять собой водород, алифатическую, гетероалифатическую, алициклическую, гетероалициклическую, арильную или гетероарильную группу, определенную выше. В определенных вариантах осуществления R15 представляет собой незамещенную алифатическую, алициклическую или арильную группу. Предпочтительно R15 представляет собой водород, метил, этил, пропил или фенил.
Фосфинатная группа предпочтительно представляет собой группу -OP(O)(R16)2 или -P(O)(OR16), где каждый R16 независимо выбран из водорода или алифатической, гетероалифатической, алициклической, гетероалициклической, арильной или гетероарильной группы, определенной выше. Согласно определенным вариантам осуществления R16 представляет собой алифатическую, алициклическую или арильную группу, которые необязательно замещены алифатической, алициклической, арильной или C1-6алкоксигруппой. Предпочтительно R16 представляет собой необязательно замещенный арил или C1-20алкил, более предпочтительно фенил, необязательно замещенный C1-6алкокси (предпочтительно метокси) или незамещенный C1-20алкил (такой как гексил, октил, децил, додецил, тетрадецил, гексадецил, стеарил).
Сильфинатная группа предпочтительно представляет собой -OSOR17, где R17 может представлять собой водород, алифатическую, гетероалифатическую, галогеналифатическую, алициклическую, гетероалициклическую, арильную или гетероарильную группу, определенную выше. В определенных вариантах осуществления R17 представляет собой незамещенную алифатическую, алициклическую или арильную группу. Предпочтительно R17 представляет собой водород, метил, этил, пропил или фенил.
Карбонатная группа предпочтительно представляет собой -OC(O)OR18, где R18 может представлять собой водород, алифатическую, гетероалифатическую, алициклическую, гетероалициклическую, арильную или гетероарильную группу, определенную выше. В определенных вариантах осуществления R18 представляет собой необязательно замещенную алифатическую, алициклическую или арильную группу. Предпочтительно R18 представляет собой водород, метил, этил, пропил, бутил (например, н-бутил, изобутил или трет-бутил), фенил, пентафторфенил, пентил, гексил, гептил, октил, нонил, децил, ундецил, додецил, тридецил, тетрадецил, пентадецил, гексадецил, гептадецил, октадецил, нонадецил, эйкозил, трифторметил, циклогексил, бензил или адамантил.
Следует понимать, если любая из перечисленных выше групп присутствует в основании Льюиса G, то могут присутствовать одна или несколько дополнительных групп R при необходимости заполнения валентной оболочки. Например, применительно к аминогруппе может присутствовать дополнительная группа R с получением RNHR10, где R представляет собой водород, необязательно замещенную алифатическую, гетероалифатическую, алициклическую, гетероалициклическую, арильную или гетероарильную группу, определенную выше. Предпочтительно R представляет собой водород или алифатическую, алициклическую или арильную группу.
Любая из алифатических, гетероалифатических, алициклических, гетероалициклических, арильных, гетероарильных, галогеналкильных, алкокси, арилокси, алкилтио, арилтио, алкиларильных, синильных групп, групп силилового простого эфира, сложноэфирных, сульфоксидных, сульфонильных, карбоксилатных, карбонатных, иминных, ацетилидных, амино, фосфинатных, сульфонатных или амидо групп, где бы не упоминалась в определениях выше, необязательно может быть замещена галогеном, гидрокси, нитро, карбоксилат, карбонат, алкокси, арилокси, алкилтио, арилтио, гетероарилокси, алкиларин, амино, амидо, иминной, нитрильной, силильной группой, группой силилового простого эфира, сложноэфирной, сульфоксидной, сульфонильной, ацетилидной, фосфинатной, сульфонатной или необязательно замещенной алифатической, гетероалифатической, алициклической, гетероалициклической, арильной или гетероарильной группой (например, необязательно замещенной галогеном, гидрокси, нитро, карбонатной, алкокси, арилокси, алкилтио, арилтио, амино, иминной, нитрильной, силильной, сульфоксидной, сульфонильной, фосфинатной, сульфонатной или ацетилидной группой).
Следует понимать, что хотя в формуле (I) группы X и G показаны как связанный с металлическим центром, содержащим один M1 или M2, одна или несколько X и/или G групп могут образовывать мостики между металлическими центрами, содержащими M1 и M2.
Для целей настоящего изобретения эпоксидная основа не ограничена. Таким образом, термин эпоксид относится к любому соединению, содержащему эпоксидный фрагмент. Предпочтительные примеры эпоксидов для целей настоящего изобретения включают оксид циклогексена, оксид стирола, оксид пропилена, замещенные оксиды циклогексена (такие как оксид лимонена, C10H16O или 2-(3,4-эпоксициклогексил)этилтриметоксисилан, C11H22O), оксиды алкилена (такие как оксид этилена и замещенные оксиды этилена) или незамещенные или замещенные оксираны (такие как эпихлоргидрин, 1,2-эпоксибутан, глицидиловые эфиры), 2-(2-метоксиэтокси)метилоксиран (MEMO), 2-(2-(2-метоксиэтокси)этокси)метилоксиран (ME2MO), 2-(2-(2-(2-метоксиэтокси)этокси)этокси)метилоксиран (ME3MO), 1,2-эпоксибутан, глицидиловые эфиры), винилоксид циклогексена, 3-фенил-1,2-эпоксипропан, 1,2- и 2,3-эпоксибутан, оксид изобутилена, оксид циклопертена, 2,3-эпокси-1,2,3,4-тетрагидронафталин, оксид индена, и функционализированные 3,5-диоксаэпоксиды. Примеры функционализированных 3,5-диоксаэпоксидов включают
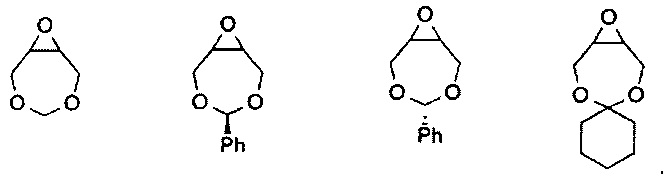
Эпоксидный фрагмент может представлять собой глицидиловый эфир или глицидиловый карбонат. Примеры глицидиловых эфиров и глицидиловых карбонатов включают
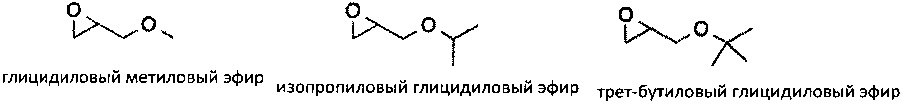
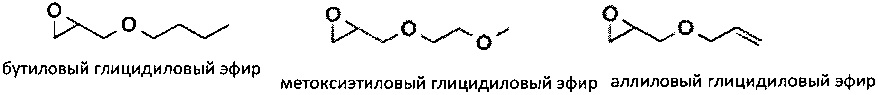
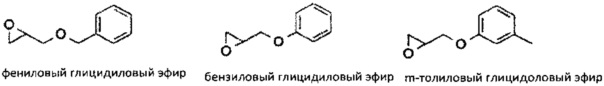
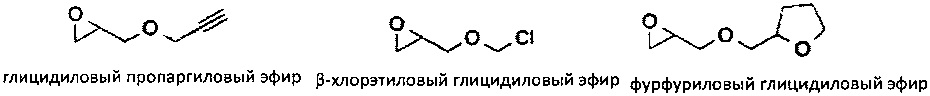

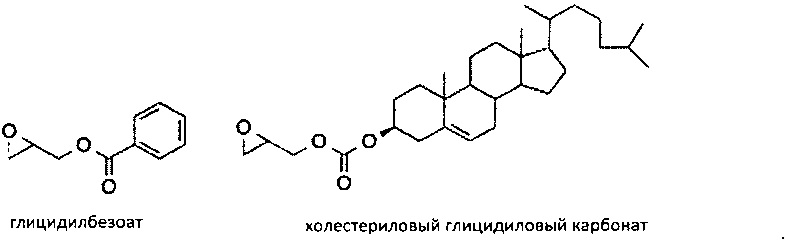
Эпоксидная основа может содержать более одного эпоксидного фрагмента, т.е. она может представлять собой бис-эпоксид, трис-эпоксид, или мульти-эпоксидсодержащий фрагмент. Примеры соединений, включающих более чем один эпоксидный фрагмент включает диглицидиловый простой эфир бисфенола А и 3,4-эпоксициклогексилметил-3,4-эпоксициклогексанкарбоксилат. Следует понимать, что реакции, осуществляемые в присутствии одного или нескольких соединений, содержащих более чем один эпоксидный фрагмент, могут приводить к образованию поперечных межмолекулярных связей в полученном в результате полимере.
Специалисту будет понятно, что эпоксид может быть получен из "зеленых" или возобновляемых ресурсов. Эпоксид может быть получен из (поли)ненасыщенного соединения, такого как выделенный из жирной кислоты и/или терпена, полученный с помощью общепринятых окислительных химических составов.
Эпоксидный фрагмент может содержать -OH функциональные группы или защищенные -OH функциональные группы. -OH функциональные группы могут быть защищены любой приемлемой защитной группой. Приемлемые защитные группы включают метил или другие алкильные группы, бензил, аллил, трет-бутил, тетрагидропиранил (ТНР), метоксиметил (MOM), ацетил (C(O)алкил), бензолил (C(O)Ph), диметокситритил (DMT), метоксиэтоксиметил (MEM), р-метоксибензил (PMB), тритил, силил (такой как триметилсилил (TMS), трет-бутилдиметилсилил (TBDMS), трет-бутилдифенилсилил (TBDPS), три-изо-пропилсилилохуметил (TOM), и триизопропилсилил (TIPS)), (4-метоксифенил)дифенилметил (MMT), тетрагидрофуранил (THF) и тетрагидропиранил (THP).
Предпочтительно эпоксид выбран из оксида пропилена, оксида циклогексена и оксида стирола.
Эпоксид предпочтительно имеет степень чистоты по меньшей мере 98%, более предпочтительно >99%.
Следует понимать, что термин "эпоксид" предназначен для охвата одного или нескольких эпоксидов. Другими словами, термин "эпоксид" относится к одному эпоксиду или смеси двух или более различных эпоксидов. Например, эпоксидная основа может представлять собой смесь оксида этилена и оксида пропилена, смесь оксида циклогексена и оксида пропилена, смесь оксида этилена и оксида циклогексена или смесь оксида этилена, оксида пропилена и оксида циклогексена.
Специалисту также будет понятно, что замещенные и незамещенные окситаны можно применять вместо и в дополнение к эпоксидам по второму аспекту настоящего изобретения. Приемлемые окситаны включают незамещенные или замещенные окситаны (предпочтительно замещенные в позиции 3 галогеном, алкилом (незамещенным или замещенным -OH или галогеном), амино, гидроксилом, арилом (например, фенилом), алкиларилом (например, бензилом)). Типичные окситаны включают окситан, 3-этил-3-окситанметанол, окситан-3-метанол, 3-метил-3-окситанметанол, 3-метилокситан, 3-этилокситан и т.п.
Термин ангидрид относится к любому соединению, содержащему ангидридный фрагмент в кольцевой системе (т.е циклический ангидрид). Предпочтительно ангидриды, применимые в настоящем изобретении, имеют следующую формулу:
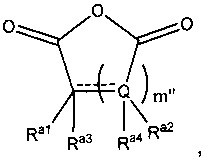
где mʺ равно 1, 2, 3, 4, 5, или 6 (предпочтительно 1 или 2), каждый Ra1, Ra2, Ra3 и Ra4 независимо выбран из водорода, галогена, гидроксила, нитро, алкокси, арилокси, гетероарилокси, амино, алкиламино, имино, нитрильной, ацетилидной, карбоксилатной или необязательно замещенной алифатической, гетероалифатической, алициклической, гетероалициклической, арильной, гетероарильной, алкиларильной или алкилгетероарильной группы; или два или более Ra1, Ra2, Ra3 и Ra4 могут быть взяты вместе с образованием насыщенной, частично насыщенной или ненасыщенной 3-12-членной, необязательно замещенной кольцевой системы, необязательно содержащей один или несколько гетероатомов, или могут быть взяты вместе с образованием двойной связи. Каждый Q независимо представляет собой C, O, N или S, предпочтительно C, где Ra3 и Ra4 либо присутствуют, либо отсутствуют, и 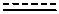 могут представлять собой либо
могут представлять собой либо  , либо
, либо  в соответствии с валентностью Q. Следует понимать, что если Q представляет собой C, а
в соответствии с валентностью Q. Следует понимать, что если Q представляет собой C, а  представляет собой
представляет собой  , Ra3 и Ra4 (или два Ra4 на смежных атомах углерода) отсутствуют. Предпочтительные ангидриды изложены ниже.
, Ra3 и Ra4 (или два Ra4 на смежных атомах углерода) отсутствуют. Предпочтительные ангидриды изложены ниже.

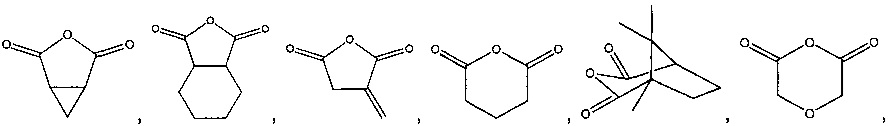
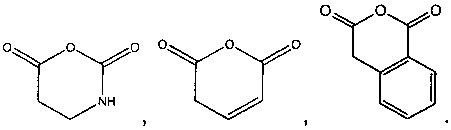
Термин лактон относится к любому циклическому соединению, содержащему в кольце фрагмент -C(O)O-. Предпочтительно лактоны, применимые в настоящем изобретении, имеют следующую формулу:
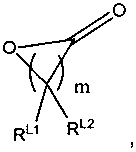
где m равняется 1-20 (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20), предпочтительно 2, 4 или 5; и RL1 и RL2 независимо выбраны из водорода, галогена, гидроксильной, нитро, алкокси, арилокси, гетероарилокси, амино, алкиламино, имино, нитрильной, ацетилидной, карбоксилатной или необязательно замещенной алифатической, гетероалифатической, алициклической, гетероалициклической, арильной, гетероарильной, алкиларильной или алкилгетероарильной группы. Два или более из RL1 и RL2 могут быть взяты вместе с образованием насыщенной, частично насыщенной или ненасыщенной 3-12-членной, необязательно замещенной кольцевой системы, необязательно содержащей один или несколько гетероатомов. Если m равняется 2 или более, RL1 и RL2 на каждом атоме углерода могут быть одинаковыми или различными. Предпочтительно RL1 и RL2 выбраны из водорода или алкила. Предпочтительно лактон имеет следующую структуру:
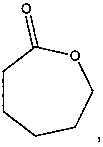
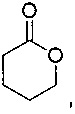
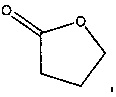
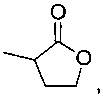
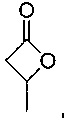
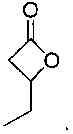
Термин лактид относится к циклическому соединению, содержащему две сложноэфирные группы. Предпочтительно лактиды, применимые в настоящем изобретении, имеют следующую формулу:
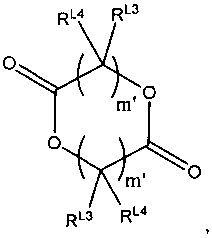
где m' равняется 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 (предпочтительно 1 или 2, более предпочтительно 1), a RL3 и RL4 независимо выбраны из водорода, галогеновой, гидроксильной, нитро, алкокси, арилокси, гетероарилокси, амино, алкиламино, имино, нитрильной, ацетилидной, карбоксилатной или необязательно замещенной алифатической, гетероалифатической, алициклической, гетероалициклической, арильной, гетероарильной, алкиларильной или алкилгетероарильной группы. Два или более RL3 и RL4 могут быть взяты вместе с образованием насыщенной, частично насыщенной или ненасыщенной 3-12-членной, необязательно замещенной кольцевой системы, необязательно содержащей один или несколько гетероатомов, если m' равняется 2 или более, RL3 и RL4 на каждом атоме углерода могут быть одинаковыми или различными, или один или несколько RL3 и RL4 на смежных атомах углерода могут отсутствовать, образуя таким образом двойную или тройную связь. Следует понимать, несмотря на то, что соединение имеет два фрагмента, представленных (-CRL3RL4)m', оба фрагмента могут быть идентичными. Предпочтительно m' равняется 1, RL4 представляет собой H, и RL3 представляет собой H, гидроксил или C1-6алкил, предпочтительно метил. Стереохимия фрагмента, представленного (-CRL3RL4)m', может быть либо одинаковой (например, RR-лактид или SS-лактид), либо отличающейся (например, мезо-лактид). Лактид может представлять собой смесь рацематов или может быть оптически чистым изомером. Предпочтительно лактид имеет следующую формулу:
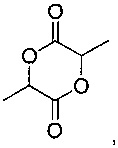
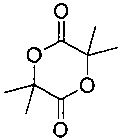 или
или 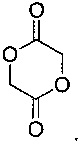
Термин "лактон и/или лактид", используемый в данном документе, охватывает лактон, лактид и комбинацию лактона и лактида. Предпочтительно термин "лактон и/или лактид" означает лактон или лактид.
Предпочтительные необязательные заместители групп Ra1, Ra2, Ra3, Ra4, RL1, RL2, RL3 и RL4 включают галоген, нитро, гидроксильную, незамещенную алифатическую, незамещенную гетероалифатическую, незамещенную арильную, незамещенную гетероарильную, алкокси, арилокси, гетероарилокси, амино, алкиламино, имино, нитрильную, ацетилидную и карбоксилатную группу.
Подробное описание
В первом аспекте настоящего изобретения, предусматривается катализатор формулы (I):
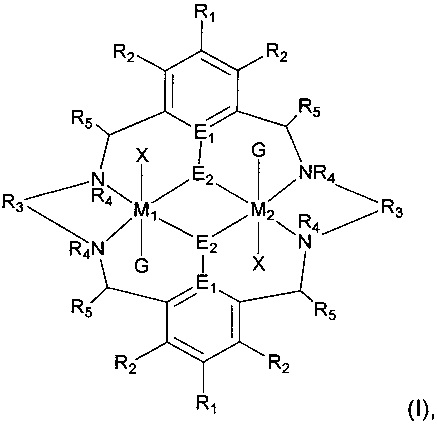
где
M1 и M2 являются различными и независимо выбраны из Mg, Zn, Fe, Co, Al и Cr;
R1 и R2 независимо выбраны из водорода, галогенида, нитрогруппы, нитрильной группы, имина, амина, простой эфирной группы, силильной группы, группы простого силилового эфира, сульфоксидной группы, сульфонильной группы, сульфинатной группы или ацетилидной группы или необязательно замещенной алкильной, алкенильной, алкинильной, галогеналкильной, арильной, гетероарильной, алкокси, арилокси, алкилтио, арилтио, алициклической или гетероалициклической группы;
R3 независимо выбран из необязательно замещенного алкилена, алкенилена, алкинилена, гетероалкилена, гетероалкенилена, гетероалкинилена, арилена, гетероарилена или циклоалкилена, где алкилен, алкенилен, алкинилен, гетероалкилен, гетероалкенилен и гетероалкинилен могут необязательно прерываться арильной, гетероарильной, алициклической или гетероалициклической группой;
R4 независимо выбран из H или необязательно замещенной алифатической, гетероалифатической, алициклической, гетероалициклической, арильной, гетероарильной, алкилгетероарильной или алкиларильной группы;
R5 представляет собой H или необязательно замещенную алифатическую, гетероалифатическую, алициклическую, гетероалициклическую, арильную, гетероарильную, алкилгетероарильную или алкиларильную группу;
E1 представляет собой C, E2 представляет собой O, S или NH, или E1 представляет собой N, а E2 представляет собой O;
X независимо выбран из OC(O)Rx, OSO2Rx, OSORx, OSO(Rx)2, S(O)Rx, ORx, фосфината, галогенида, нитрата, гидроксила, карбоната, амино, амидо или необязательно замещенной алифатической, гетероалифатической, алициклической, гетероалициклической, арильной, гетероарильной группы;
Rx независимо представляет собой водород, или необязательно замещенную алифатическую, галогеналифатическую, гетероалифатическую, алициклическую, гетероалициклическую, арильную, гетероарильную или алкиларильную группу; и
G отсутствует или независимо выбран из нейтрального или анионного донорного лиганда, который представляет собой основание Льюиса.
Специалисту будет понятно, что если M1 или M2 представляет собой Mg или Zn, металл(ы) будут находится в степени окисления +2, т.е. Mg представляет собой Mg(II) и Zn представляет собой Zn(II). Следует понимать, что если M1 или M2 представляет собой Co или Fe, металл(ы) могут находится в степень окисления или +2, или +3. Другими словами, Co может представлять собой или Co(II), или Co(III), и Fe может представлять собой или Fe(II), или Fe(III). Если Fe и/или Co находится в степени окисления +3, катализатор формулы (I) будет содержать дополнительную группу X, скоординированную с металлическим центром, где X является таким, как определено в данном документе. Если M1 или M2 представляет собой Al или Cr, металл(ы) будут находится в степени окисления +3, т.е Al представляет собой Al(III)-X и Cr представляет собой Cr(III)-X.
Предпочтительно M1 и M2 независимо выбраны из Mg, Zn, Fe и Co. Еще более предпочтительно M1 представляет собой или Mg или Zn. Другими словами, для предпочтительного катализатора по настоящему изобретению M1 представляет собой Zn и M2 представляет собой Mg, M1 представляет собой Zn и M2 представляет собой Co, M1 представляет собой Zn и M2 представляет собой Fe, M1 представляет собой Mg и M2 представляет собой Co, или M1 представляет собой Mg и M2 представляет собой Fe. В исключительно предпочтительных вариантах осуществления настоящего изобретения M1 представляет собой Zn и M2 представляет собой Mg.
В каждом случае группы R1 и R2 огу быть одинаковыми или различными. Предпочтительно R1 и R2 независимо выбраны из водорода, галогенида, амино, нитро, сульфоксида, силила, сульфонила, сильфината и необязательно замещенного алкила, алкенила, арила, гетероарила, алкокси, арилокси или алкилтио. Предпочтительно R2 представляет собой водород.
Еще более предпочтительно каждый R2 представляет собой водород и R1 независимо выбран из водорода, галогенида, амино, нитро, сульфоксида, силила, сульфонила, сильфината и необязательно замещенного алкила, алкенила, арила, гетероарила, алкокси, арилокси или алкилтио, таких как водород, C1-6алкил (например, галогеналкил), алкокси, арил, галогенид, нитро, силильная, сульфонил и алкилтио, например, tBu, iPr, Me, OMe, H, нитро, галоген, SiH2Me, SiEt3, SO2Me или фенил. Предпочтительно в каждом случае R2 является одинаковым, и в каждом случае R1 является одинаковым, и R1 и R2 могут быть одинаковыми или различными.
Следует понимать, что группа R3 представляет собой дизамещенную алкильную, алкенильную, алкинильную, гетероалкильную, гетероалкенильную или гетероалкинильную группу, которая необязательно может прерываться арильной, гетероарильной, алициклической или гетероалициклической группой, или может представлять собой дизамещенную арильную или циклоалкильную группу, которая выполняет функцию мостиковой группы между двумя центральными атомами азота в катализаторе формулы (I). Таким образом, если R3 представляет собой алкиленовую группу, такую как диметилпропилен, R3 группа имеет структуру -CH2-C(CH3)2-CH2-. Таким образом, определения алкильной, арильной, циклоалкильной и т.д. групп, изложенные выше, также соответственно относятся к алкиленовой, ариленовой, циклоалкиленовой и т.п. группам, изложенным для R3 и R3 и могут быть необязательно замещены. Типичные варианты R3 включают этилен, 2,2-диметилпропилен, пропилен, бутилен, фенилен, циклогексилен или бифенилен, более предпочтительно 2,2-диметилпропилен. Если R3 представляет собой циклогексилен, он может быть в виде рацемической, RR- или SS-форм. Предпочтительно R3 представляет собой замещенный пропилен, такой как 2,2-ди(алкил)пропилен.
Предпочтительно каждый R4 независимо выбран из водорода и необязательно замещенного алкила, алкенила, алкинила, арила, гетероалкила, гетероалкенила, гетероалкинила или гетероарила. Типичные варианты R4 включают H, Me, Et, Bn, iPr, tBu или Ph. Дополнительный типичный вариант представляет собой -CH2- (пиридин). В особенно предпочтительных вариантах осуществления каждый R4 представляет собой водород.
Предпочтительно каждый R5 независимо выбран из водорода и необязательно замещенной алифатической группы или арила. Более предпочтительно, R5 выбран из водорода и необязательно замещенного алкила или арила. Типичные R5 группы включают водород, метил, этил, фенил и трифторметил, предпочтительно водород, метил или трифторметил. В особенно предпочтительных вариантах осуществления каждый R5 представляет собой водород.
Предпочтительно E1 представляет собой C и E2 представляет собой O, S или NH. В особенно предпочтительных вариантах осуществления E1 представляет собой C и E2 представляет собой O.
Каждый X независимо выбран из OC(O)Rx, OSO2Rx, OS(O)Rx, OSO(Rx)2, S(O)Rx, ORx, фосфината, галогенида, нитро, гидроксила, карбоната, амино, амидо и необязательно замещенной алифатической, гетероалифатической (например, силильной), алициклической, гетероалициклической группы, арила или гетероарила. Предпочтительно каждый X независимо представляет собой OC(O)Rx, OSO2Rx, OS(O)Rx, OSO(Rx)2, S(O)Rx, ORx, галогенид, нитрат, гидроксил, карбонат, амино, нитро, амидо, алкил (например, разветвленный алкил), гетероалкил (например, силил) арил или гетероарил. В особенно предпочтительных вариантах осуществления каждый X независимо представляет собой OC(O)Rx, ORx, галогенид, карбонат, амино, нитро, алкил, арил, гетероарил, фосфинат или OSO2Rx. Предпочтительные варианты заместителей, когда X представляет собой алифатическую, гетероалифатическую, алициклическую, гетероалициклическую, арильную или гетероарильную группу, включают галоген, гидроксил, нитро, циано, амино или замещенную или незамещенную алифатическую, гетероалифатическую, алициклическую, гетероалициклическую группу, арил или гетероарил. Каждый X может быть одинаковым или различным и предпочтительно каждый X является одинаковым.
Rx независимо представляет собой водород, или необязательно замещенную алифатическую, галогеналифатическую, гетероалифатическую, алициклическую, гетероалициклическую группу, арил, алкиларил или гетероарил. Предпочтительно Rx необязательно представляет собой замещенный алкил, алкенильной, алкинил, гетероалкил, арил, гетероарил или алкиларил. Предпочтительные варианты заместителей для Rx включают галоген, гидроксил, циано, нитро, амино, алкокси, алкилтио или замещенную или незамещенную алифатическую, гетероалифатическую, алициклическую, гетероалициклическую группу, арил или гетероарил (например, необязательно замещенный алкил, арил, или гетероарил).
Типичные варианты X включают OAc, OCOEt, OC(O)CF3, галоген, OSO(CH3)2, Et, Me, OMe, OiPr, OtBu, Cl, Br, I, F, N(iPr)2 или N(SiMe3)2, OPh, OBn, силикат, дифенилфосфинат, бис-(4-метокси)фенилфосфинат, диоктилфосфинат, OCOBn, OCOCH2C6F5, OCO(CH2)5CH3, OCO(CH2)7CH3, ОСО(CH2)9CH3, O(CH2)5CH3, O(CH2)7CH3, O(CH2)9CH5 и т.п.
Если G не отсутствует, он представляет собой группу, способную отдавать неподеленную пару электронов (т.е основание Льюиса). В определенных вариантах осуществления G представляет собой азотсодержащее основание Льюиса. Каждый G может быть нейтральным или отрицательно заряженным. Если G отрицательно заряжен, тогда один или несколько положительных противоионов потребуются для компенсации заряда в комплексе. Подходящие положительные противоионы включают ионы металлов группы 1 (Na+, K+ и т.д.), ионы металлов группы 2 (Mg2+, Ca2+ и т.д.), ионы имидазолия, положительно заряженные необязательно замещенные гетероарил, гетероалифатическую или гетероалициклическую группу, ионы аммония (т.е. N(R12)4+), ионы иминия (т.е. (R12)2C=N(R12)2+, такие как ионы бис(трифенилфосфин)иминия) или ионы фосфония (P(R12)4+), где каждый R12 независимо выбран из водорода или необязательно замещенной алифатической, гетероалифатической, алициклической, гетероалициклической группы, арила или гетероарила. Типичные противоионы включают [H-B]+, где B выбран из триэтиламина, 1,8-диазабицикло[5.4.0]ундец-7-ена и 7-метил-1,5,7-триазабицикло[4.4.0]дец-5-ена.
G предпочтительно независимо выбран из необязательно замещенной гетероалифатической группы, необязательно замещенной гетероалициклической группы, необязательно замещенного гетероарила, галогенида, гидроксида, гидрида, карбоксилата и воды. Более предпочтительно G независимо выбран из воды, спирта, замещенного или незамещенного гетероарила (имидазола, метилимидазола (например, N-метилимидазола), пиридина, 4-диметиламинопиридина, пиррола, пиразола и т.д.), простого эфира (диметилового эфира, диэтилового эфира, циклических эфиров и т.д.), простого тиоэфира, карбена, фосфина, фосфиноксида, замещенной или незамещенной гетероалициклической группы (морфолина, пиперидина, тетрагидрофурана, тетрагидротиофена и т.д.), амина, алкиламина (триметиламина, триэтиламина и т.д.), ацетонитрила, сложного эфира (этилацетата и т.д.), ацетамида (диметилацетамида и т.д.), сульфоксида (диметилсульфоксида и т.д.), карбоксилата, гидроксида, гидрида, галогенида, нитрата, сульфоната и т.д. Согласно некоторым вариантам осуществления в одном или обоих примерах G независимо выбран из необязательно замещенного гетероарила, необязательно замещенной гетероалифатической, необязательно замещенной гетероалициклической группы, галогенида, гидроксида, гидрида, простого эфира, простого тиоэфира, карбена, фосфина, фосфиноксида, амина, алкиламина, ацетонитрила, сложного эфира, ацетамида, сульфоксида, карбоксилата, нитрата или сульфоната. Согласно определенным вариантам осуществления G может представлять собой галогенид; гидроксид; гидрид; воду; гетероарильную, гетероалициклическую или карбоксилатную группу, которая необязательно замещена алкилом, алкенилом, алкинилом, алкокси, галогеном, гидроксилом, нитро или нитрилом. Согласно предпочтительным вариантам осуществления G независимо выбран из галогенида; воды; гетероарила, необязательно замещенного алкилом (например, метилом, этилом и т.д.), алкенилом, алкинилом, алкокси (предпочтительно метокси), галогеном, гидроксилом, нитро или нитрилом. Согласно некоторым вариантам осуществления в одном или обоих примерах G является отрицательно заряженным (например, галогенидом). Согласно следующим вариантам осуществления в одном или обоих примерах G является необязательно замещенным гетероарилом. Типичные группы G включают хлорид, бромид, пиридин, метилимидазол (например, N-метилимидазол) и диметиламинопиридин (например, 4-метиламинопиридин).
Следует понимать, что если группа G присутствует, то группа G может ассоциироваться с единым M-активным металлический центром, как показано на формуле (I), или группа G может ассоциироваться с обоими металлическими центрами и образовывать мостик между двумя металлическими центрами, как показано ниже в формуле (Ia):
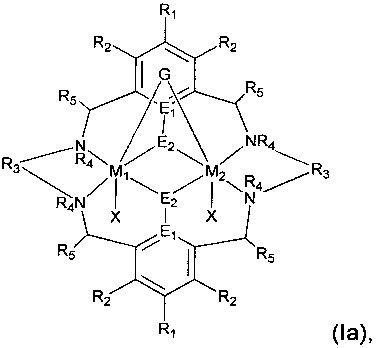
где R1, R2, R3, R4, R5, M, G, X, E1 и E2 являются такими, как определено для формулы (I).
Следует понимать, что предпочтительные характеристики, описанные выше для катализатора по первому аспекту, могут присутствовать в комбинации mutatis mutandis.
Например, в предпочтительных вариантах осуществления первого аспекта в каждом случае R2, R4 и R5 представляют собой H, R3 необязательно представляет собой замещенный пропилен, фенилен или циклогексилен, E1 представляет собой C и E2 представляет собой O, S или NH (предпочтительно E2 представляет собой O). Предпочтительно M1 представляет собой Mg и M2 представляет собой Zn (и vice versa).
Предпочтительно в каждом случае R2, R4 и R5 представляют собой H, R3 необязательно представляет собой замещенный пропилен, фенилен или циклогексилен, E1 представляет собой C и E2 представляет собой O, S или NH (предпочтительно E2 представляет собой O), каждый X независимо представляет собой OC(O)Rx, ORx, галогенид, карбонат, амино, нитро, алкил, арил, гетероарил, фосфинат или OSO2Rx, каждый R1 независимо представляет собой водород, алкил, алкенил, арил, гетероарил, алкокси, алкилтио, галогенид, амино, нитро, сульфоксид, сульфонил, сильфинат или силил, каждый G (в случаях, когда присутствует) независимо выбран из галогенида; воды; гетероарила, необязательно замещенного алкилом (например, метилом, этилом и т.д.), алкенилом, алкинилом, алкокси (предпочтительно метокси), галогеном, гидроксил, нитро или нитрилом и или M1, или M2 представляет собой Mg или Zn (еще более предпочтительно M1 представляет собой Zn и M2 представляет собой Mg).
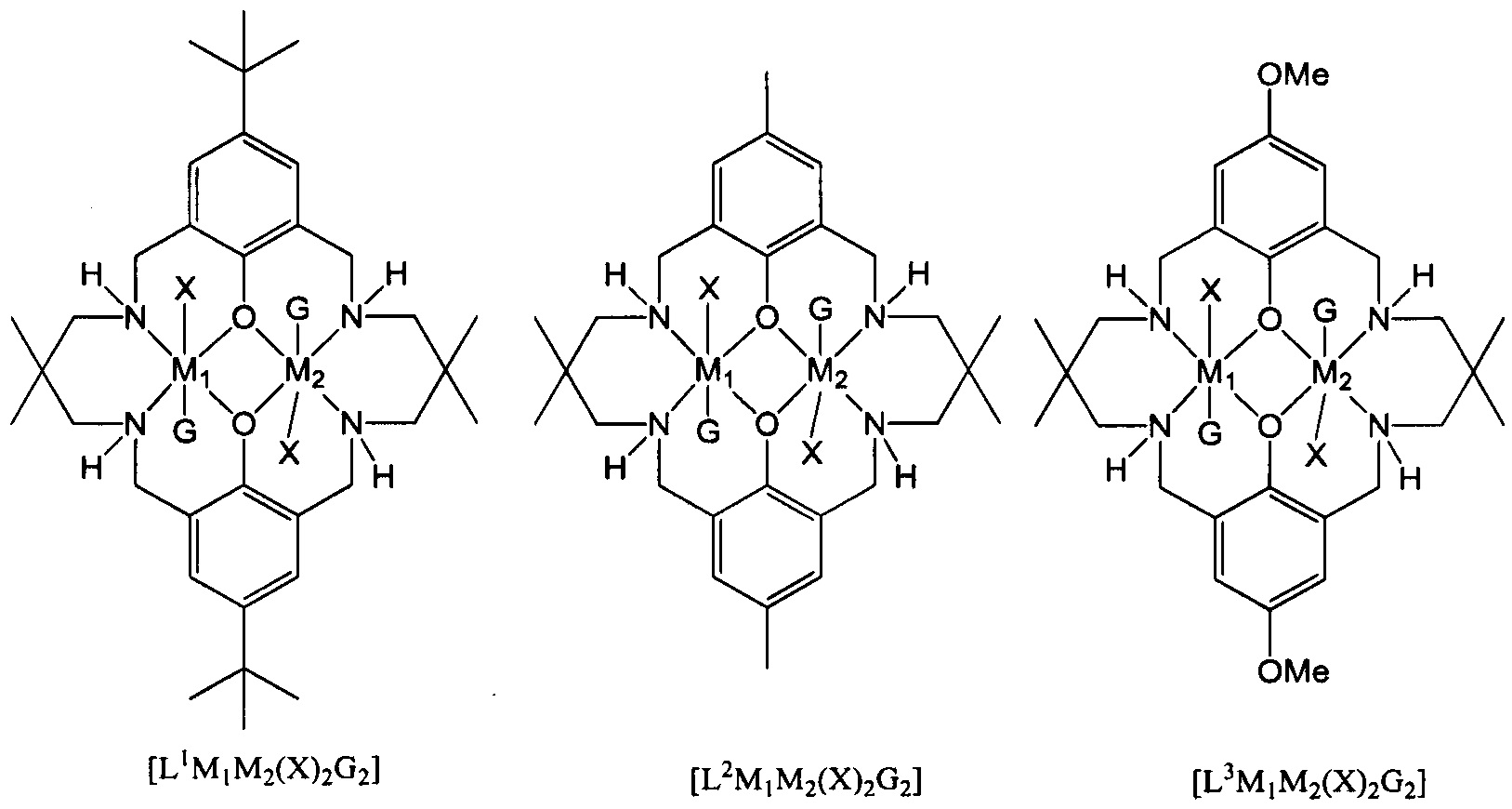
Типичные катализаторы по первому аспекту являются следующими:
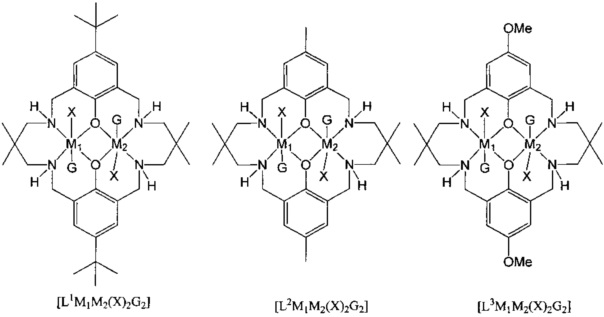
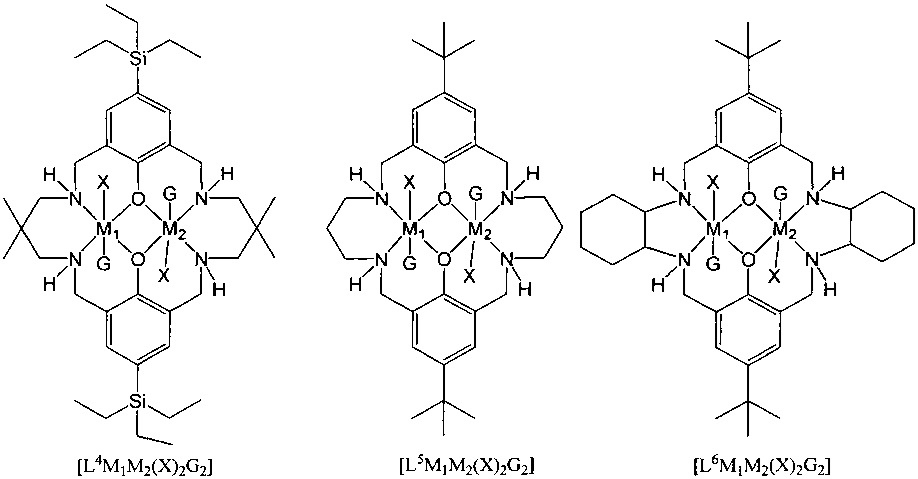
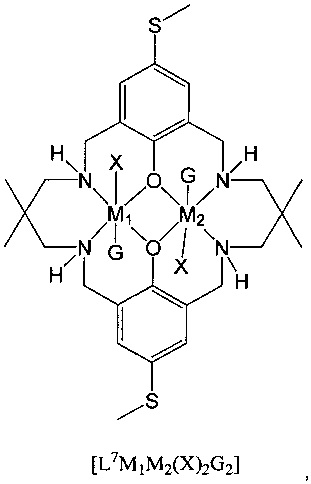
где в каждом случае G либо присутствует, либо отсутствует, и предпочтительно где X независимо представляет собой OC(O)Rx, ORx, галогенид, карбонат, амино, нитро, алкил, арил, гетероарил, фосфинат или OSO2Rx, еще более предпочтительно X представляет собой OAc. Предпочтительно M1 или M2 представляет собой Mg или Zn и еще более предпочтительно M1 представляет собой Zn и M2 представляет собой Mg (или vice versa).
Во втором аспекте настоящего изобретения представлена каталитическая система, содержащая катализатор в соответствии с первым аспектом.
Каталитическая система по второму аспекту может содержать один или несколько дополнительных катализаторов, которые способны катализировать реакцию между (i) диоксидом углерода и эпоксидом, (ii) эпоксидом и ангидридом или (iii) лактидом и/или лактоном, в зависимости от природы осуществляемой реакции. Приемлемые дополнительные катализаторы включают катализаторы формулы (I), как описано в WO 2009/130470, и катализаторы формул (I) или (III), как описано в WO 2013/034750, полное содержание которых включено в данный документ посредством ссылки. Другими словами, дополнительный катализатор может представлять собой один или несколько катализаторов формулы (Ic):
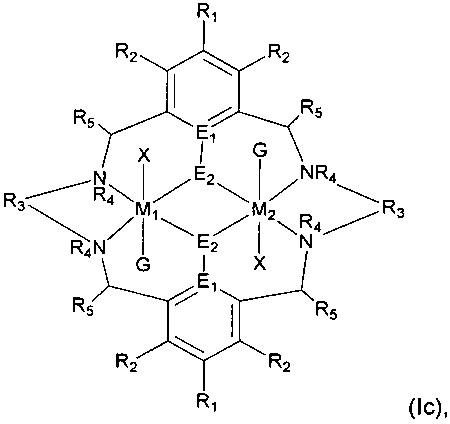
где R1-R5, E1 E2, G и X являются такими, как описано выше для первого аспекта, и где M1 и M2 могут быть одинаковыми или различными и выбраны из группы, состоящей из Zn(II), Cr(II), Co(II), Mn(II), Mg(II), Fe(II), Ti(II), Cr(III)-X, Co(III)-X, Mn(III)-X, Fe(III)-X, Ca(II), Ge(II), Al(III)-X, Ti(III)-X, V(III)-X, Ge(IV)-(X)2 и Ti(IV)-(X)2.
Специалисту будет понятно, что предпочтительные варианты для каждого из R1-R5, E1, E2, G и X, описанные для первого аспекта, в равной степени применимы к дополнительным катализаторам формулы (Ic) и что предпочтительные характеристики, описанные выше для каждого из R1-R5, E1, E2, G и X для первого аспекта могут присутствовать в комбинации mutatis mutandis для дополнительных катализаторов. Для дополнительных катализаторов X предпочтительно представляет собой карбоксилат такой как ацетат, бензоат и трифторацетат, или галогенид. Для дополнительных катализаторов M1 и M2 предпочтительно выбраны из Mg(II), Zn(II), Co(II), Cr(II), Fe(II), Al(III)-X, Co(III)-X, Fe(III)-X и Cr(III)-X, еще более предпочтительно M1 и M2 выбраны из Mg(II) и Zn(II).
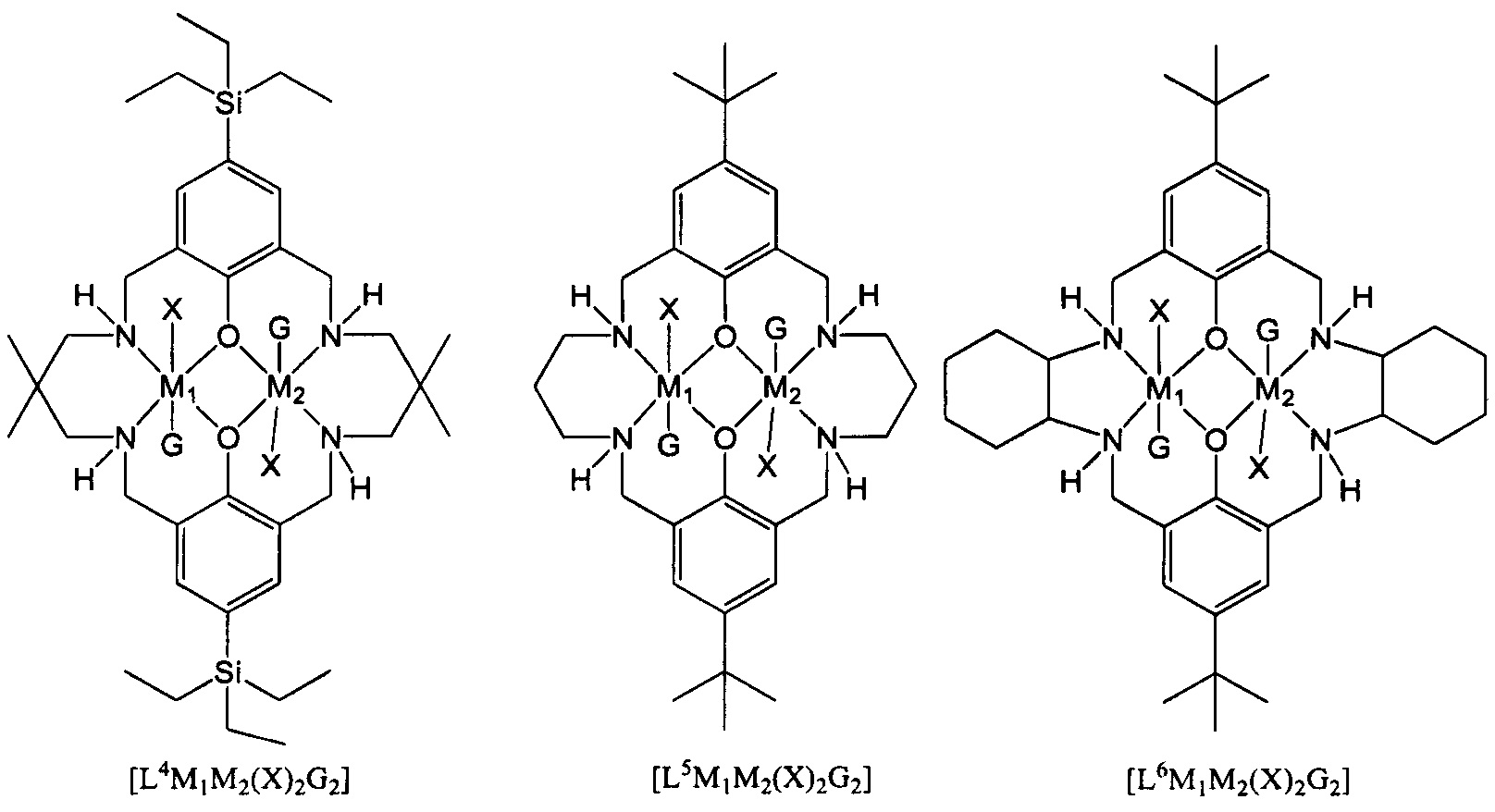
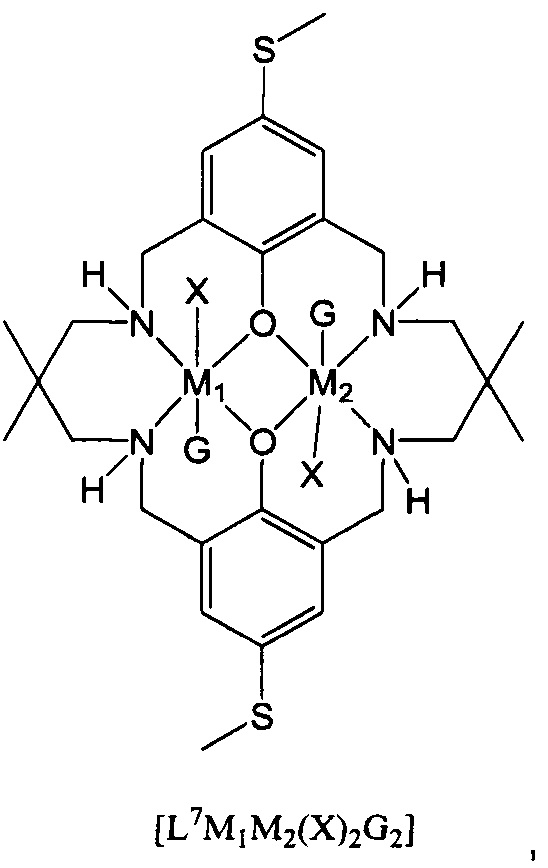
Типичные дополнительные катализаторы включают [L1Mg2(X)2] и [L1Zn2(X)2], где X является таким, как определено для первого аспекта настоящего изобретения и предпочтительно представляет собой OAc. Кроме того, типичные дополнительные катализаторы включают [L3Mg2(X)2], [L3Zn2(X)2], [L4Mg2(X)2], [L4Zn2(X2)], [L5Mg2(X)2], [L5Zn2(X)2], [L6Mg2(X)2], [L6Zn2(X)2], [L7Mg2(X)2], [L7Zn2(X)2], [L1Fe2(X)2] и [L1Co2(X)2].
Каталитическая система по второму аспекту может содержать сокатализатор. Приемлемые сокатализаторы включают соли, такие как соли аммония и соли фосфония, или основания Льюиса, такие как диметиламинопиридин (DMAP), метилимидазол и пиридин.
Каталитическая система может содержать по меньшей мере приблизительно 0,5% по весу, например, от приблизительно 0,5% по весу до приблизительно 99,5% по весу катализатора в соответствии с первым аспектом. Предпочтительно каталитическая система содержит катализатора по меньшей мере приблизительно 5% по весу, как например, по меньшей мере приблизительно 10% по весу, более предпочтительно по меньшей мере приблизительно 30% по весу, еще более предпочтительно по меньшей мере приблизительно 50% по весу и еще более предпочтительно по меньшей мере приблизительно 75% по весу, например, по меньшей мере приблизительно 95% по весу в соответствии с первым аспектом.
Дополнительный катализатор(ы) может присутствовать в количестве от приблизительно 0,5% по весу до приблизительно 99,5% по весу каталитической системы. Например, дополнительный катализатор может присутствовать в количестве от приблизительно 1% по весу до приблизительно 70% по весу, как например, приблизительно от 5% по весу до приблизительно 50% по весу, например, приблизительно от 10% по весу до приблизительно 30% по весу, например, приблизительно от 15% по весу до приблизительно 25% по весу каталитической системы.
Когда сокатализатор присутствует, он может присутствовать в каталитической системе в молярном соотношение сокатализатор : общее содержание катализатора (т.е. сумма катализатора по первому аспекту и дополнительного катализатора) от приблизительно 1:1 до приблизительно 1:100.
Катализаторы по первому аспекту и каталитическая система по второму аспекту способны осуществлять полимеризацию (i) диоксида углерода и эпоксида, (ii) эпоксида и ангидрида и (iii) лактида и/или лактона. Таким образом, в третьем аспекте настоящего изобретения представлен способ осуществления реакции диоксида углерода с эпоксидом, ангидрида с эпоксидом или лактидом и/или лактоном в присутствии катализатора в соответствии с первым аспектом или каталитической системы в соответствии со вторым аспектом.
Способ по третьему аспекту можно осуществлять в присутствии средства передачи цепи. Приемлемые средства передачи цепи включают, например, средства передачи цепи определенные формулой (II) в WO 2013/034750, полное содержание которой включено в данный документ посредством ссылки. Например, средство передачи цепи может представлять собой воду или может содержать по меньшей мере один аминный (-NHR), спиртовой (-OH) или тиольный (-SH) фрагмент, где R выбран из водорода или необязательно замещенной алифатической, гетероалифатической, алициклической, гетероалициклической, арильной или гетероарильной группы, например, выбран из водорода или необязательно замещенного алкила, гетероалкила, алкенила, гетероалкенила, циклоалкила, гетероциклоалкила, арила, или гетероарила.
Способ по третьему аспекту можно осуществлять в присутствии растворителя. Примеры растворителей, применимых в третьем аспекте, включают толуол, диэтилкарбонат, диметилкарбонат, диоксан, дихлорбензол, метиленхлорид, пропиленкарбонат, этиленкарбонат и т.д.
Если способ по третьему аспекту включает осуществление реакции эпоксида, эпоксид может представлять собой какое-либо соединение, содержащее эпоксидный фрагмент. Эпоксид можно очищать (например, посредством дистилляции, такой как через гидрид кальция) перед осуществлением реакции с диоксидом углерода или ангидридом. Например, эпоксид можно дистиллировать перед добавлением в реакционную смесь, содержащую катализатор или каталитическую систему.
Способ по третьему аспекту настоящего изобретения можно осуществлять при давлении 1-100 атмосфер, предпочтительно при давлении 1-40 атмосфер, как например, при давлении 1-10 атмосфер, более предпочтительно при давлении 1 или 2 атмосферы. Катализаторы и каталитические системы, применяемые в способе по третьему аспекту способны осуществлять реакцию при низких давлениях.
Катализаторы по первому аспекту или каталитические системы по второму аспекту могут действовать при температурах, достигающих 250°C. Способ по третьему аспекту настоящего изобретения можно осуществлять при температуре от приблизительно 0°C до приблизительно 250°C, как например, от приблизительно 0°C до приблизительно 120°C, предпочтительно от приблизительно 50°C до приблизительно 100°C. Продолжительность способа может достигать 168 часов, как например, от приблизительно 1 минуты до приблизительно 24 часов, например, от приблизительно 5 минут до приблизительно 12 часов, например, от приблизительно 1 до приблизительно 6 часов.
Способ по третьему аспекту настоящего изобретения можно осуществлять при низкой загрузке катализатора. Например, если осуществление реакции включает сополимеризацию диоксида углерода и эпоксида, загрузка катализатора для данного процесса предпочтительно находится в диапазоне 1:1000-100000 катализатор : эпоксид, более предпочтительно в диапазоне 1:1000-50000 катализатор : эпоксид, еще более предпочтительно в диапазоне 1:11000-10000 и наиболее предпочтительно в диапазоне 1:10000 катализатор : эпоксид. Если способ включает сополимеризацию эпоксида и ангидрида или осуществление реакции лактида и/или лактона, загрузка катализатора для данного процесса находится предпочтительно в диапазоне 1:1000-100000 катализатор : общее содержание мономера, более предпочтительно в диапазоне 1:1000-50000 катализатор : общее содержание мономера, еще более предпочтительно в диапазоне 1:11000-10000 и наиболее предпочтительно в диапазоне 1:10000 катализатор : общее содержание мономера. Указанные выше соотношения представляют собой молярные соотношения.
Следует понимать, что различные характеристики, описанные выше для способа по третьему аспекту, могут присутствовать в комбинации mutatis mutandis. Все предпочтительные характеристики по первому и второму аспектам в равной степени применимы к третьему аспекту и могут присутствовать в комбинации mutatis mutandis.
В четвертом аспекте настоящего изобретения представлен продукт способа третьего аспекта настоящего изобретения. Все предпочтительные характеристики третьего аспекта настоящего изобретения применимы к четвертому аспекту настоящего изобретения mutatis mutandis.
В пятом аспекте настоящего изобретения представлен способ синтеза катализатора в соответствии с первым аспектом или каталитической системы в соответствии со вторым аспектом, причем способ включает
а) осуществление реакции лиганда формулы (Ib):
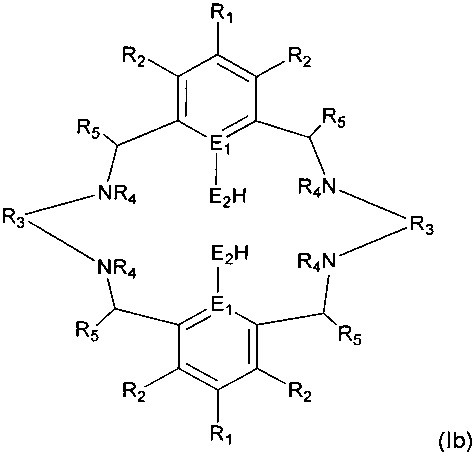
с соединением формулы (IV):

где n соответствует степени окисления M1;
RM1 независимо выбран из водород, алкил, алкенил, алкинил, циклоалкил, циклоалкенил, циклоалкинил, арил, гетероарил, амино, алкокси, арилокси, алкилтио и алкиларил; и
b) осуществление реакции продукта стадии а) с соединением формулы (V):

где m соответствует степени окисления M2;
c) необязательно добавление соединения, содержащего G;
где R1-R5, E1, E2, M1, M2, X и G являются такими, как определено для катализатора по первому аспекту настоящего изобретения.
Специалисту будет понятно, что определения групп R1-R5, E1, E2, X, G M1 и M2 в пятом аспекте настоящего изобретения соответствуют определениям групп R1-R5, E1, E2, X, M1 и M2 в катализаторе по первому аспекту, полученного с помощью данного способа.
Предпочтительно M1 представляет собой Zn или Mg и еще более предпочтительно M1 представляет собой Zn и M2 представляет собой Mg. Однако, специалисту будет понятно, что для способа по пятому аспекту, маркировка атома металла может быть изменена таким образом, что M2 предпочтительно представляет собой Zn или Mg и еще более предпочтительно М1 представляет собой Mg и M2 представляет собой Zn.
Соединение формулы (IV) может представлять собой какое-либо металлоорганическое соединение, содержащее M1. Термин "металлоорганическое" предназначен для охвата соединений, имеющих M1-C связь, а также соединений, имеющих M1-S связь, M1-N связь и/или M1-O связь. Предпочтительно RM1 может быть независимо выбран из необязательно замещенного алкила, алкенила, арила, гетероарила, алкокси, арилокси, амино, тиоалкила и алкиларила. RM1 могут быть одинаковыми или различными. Типичные варианты RM1 включают Me, Et, n-Pr, iPr, N-Bu, 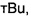 этилгексил, гексил, октил, циклогексил, бензил (Bn), адамантил, OEt, OPh, C(SiMe3)3, N(SiMe3)2, N(SiHMe2)2, N(SiH2Me)2 и N(SiH3)2. Например, если M1 представляет собой Zn, соединение формулы (IV) может представлять собой Et2Zn или EtZnOEt.
этилгексил, гексил, октил, циклогексил, бензил (Bn), адамантил, OEt, OPh, C(SiMe3)3, N(SiMe3)2, N(SiHMe2)2, N(SiH2Me)2 и N(SiH3)2. Например, если M1 представляет собой Zn, соединение формулы (IV) может представлять собой Et2Zn или EtZnOEt.
Соединение формулы (IV) можно добавлять в соотношении приблизительно от 1:0,01 до приблизительно 0,01:1, как например, приблизительно 1:1 по отношению к лиганду формулы (Ib). Соединение формулы (V) можно добавлять в соотношении приблизительно от 1:0,01 до приблизительно 0,01:1, как например, приблизительно 1:1 по отношению к лиганду формулы (Ib).
Способ по пятому аспекту можно осуществлять в присутствии растворителя. Примеры растворителей, применимых в пятом аспекте, включают толуол, диэтилкарбонат, диметилкарбонат, диоксан, дихлорбензол, метиленхлорид, пропиленкарбонат, этиленкарбонат, тетрагидрофуран (THF), пиридин, ацетонитрил и т.д.
Специалисту будет понятно, что если G присутствует, его можно добавлять в любой момент осуществления реакции. Если реакцию осуществляют в растворителе, G может присутствовать в применяемом растворителе (т.е. растворитель и G могут представлять собой THF, пиридин или ацетонитрил). Специалисту также будет понятно, что если G отрицательно заряжен, то один или несколько положительных противоионов потребуются для компенсации заряда в соединении, добавленном в способ. Приемлемые противоионы представляют собой такие, как описано выше для первого аспекта. Например, если G представляет собой Cl-, тогда соединение, добавляемое в способ, может представлять собой бис(трифенилфосфин)хлорид иминия (PPNCl), Et3NHCl или KCl.
Стадию а) способа по пятому аспекту настоящего изобретения можно осуществлять при температуре от приблизительно -80°C до приблизительно 100°C. Продолжительность стадии а) может достигать 24 часов, как например, от приблизительно 1 минуты до приблизительно 12 часов.
Стадию b) способа по пятому аспекту настоящего изобретения можно осуществлять при температуре от приблизительно -80°C до приблизительно 100°C. Продолжительность стадии b) может достигать 24 часов, как например, от приблизительно 1 минуты до приблизительно 12 часов.
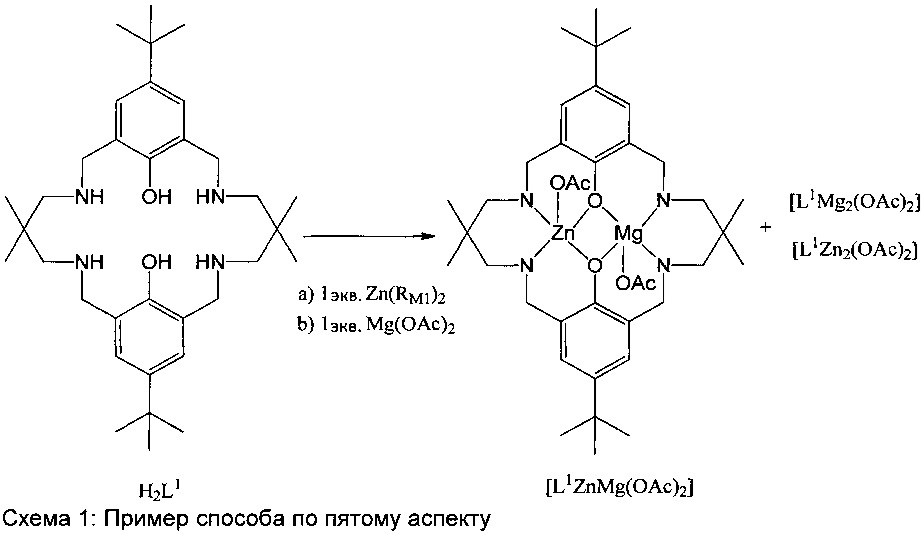
Исключительно в качестве примера способа по пятому аспекту, когда получаемый катализатор представляет собой [L1ZnMg(OAc)2], способ по пятому аспекту включает: а) осуществление реакции соединения H2L1 с соединением Zn(RM1)2 и затем b) последующее осуществление реакции продукта стадии а) с Mg(OAc)2.
Примеры
Пример 1
Материалы
Синтез макроциклических пролигандов H2Ln осуществляли, как сообщалось ранее (М.R. Kember et al, Angew. Chem. Int. Ed., 2009, 48, 931-933). Синтез металлических комплексов и каталитических систем осуществляли в безводных условиях с применением либо линии Шленка, либо заполненной азотом перчаточной камеры. Катализаторы A и B синтезировали в соответствии с описанным в литературе способом (М.R. Kember, P.D. Knight, Р.Т.R. Reung и C.K. Williams, Angew. Chem. Int. Ed., 2009, 48, 931-933, 1. M.R. Kember et al, Angew. Chem. Int. Ed., 2009, 48, 931-933, M.R. Kember и C.K. Williams, J. Am. Chem. Soc., 2012, 134, 15676-15679).
Все растворители и реагенты получали от Sigma Aldrich и Strem. THF высушивали посредством перегонки с обратным холодильником над натрием и бензофеноном и хранили в атмосфере азота. Оксид циклогексена (CHO) высушивали над MgSO4 и фракционно дистиллировали в атмосфере азота. Все высушенные растворители и реагенты хранили в атмосфере азота и дегазировали посредством нескольких циклов замораживания-нагнетания насосом-оттаивания. Для изучения сополимеризации применяли диоксид углерода исследовательской степени чистоты. Высокое давление реакции сополимеризации осуществляли в лабораторном реакторе Parr 5513 объемом 100 мл.
1H и 13C{1H} ЯМР спектры фиксировали на приборе Bruker AV-400, если не указано иное. Все масс-спектрометрические измерения осуществляли с помощью компактного прибора MALDI micro MX. Применяемая матрица представляла собой дитранол с KOA C в качестве ионизирующего средства и THF в качестве растворителя. Элементный анализ определяли Stephen Boyer (Лондонский Университет Метрополитен) и Alan Dickerson (Кембриджский университет). Эксклюзионную хроматографию фиксировали с помощью прибора Polymer labs PL GPC-50. THF применяли в качестве элюента при расходе газа 1 мл⋅мин.-1. Применяли две колонки Polymer Labs MIXED D и осуществляли калибровку с помощью точных стандартов полистирола Mw.
1. Получение катализаторов
а) Получение каталитической системы 1
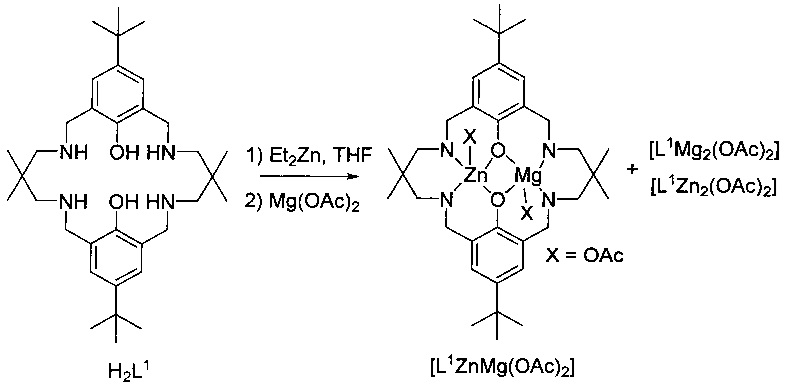
H2L1 (0,60 г, 1,09 ммоль) растворяли в безводном THF (30 мл) и охлаждали до -20°C. Et2Zn (0,14 г, 1,09 ммоль) растворяли в безводном THF (10 мл) и охлаждали до -20°C. Раствор Et2Zn по каплям добавляли в раствор пролиганда при -20°C и обеспечивали возможность в течение 4 ч. нагреться до 25°C. Затем Mg(OAc)2 (0,16 г, 1,09 ммоль) добавляли в реакционную смесь и оставляли ее перемешиваться в течение 16 ч. Растворитель удаляли под вакуумом с получением белого твердого вещества (0,70 г, 85%). Расч. для C38H60O2N2MgZn: C, 60,17; H, 7,97; N, 7,39; Обнаружено: C, 59,88; H, 7,87; N, 7,31%; MS (MALDI-TOF): масса/заряд 697 ([L1MgZn(OAc)]+, 100%), 657 ([L1Mg2(OAc)]+, 25%), 739 ([L1Zn2(OAc)]+, 45%); 13C ЯМР (400 МГц, C6D6): δ C=176,2, 163,5, 135,6, 125,9, 123,6, 62,3, 56,2, 34,2, 32,1, 27,9, 26,5, 24,4, 20,9 ppm.
b) Получение каталитической системы 2
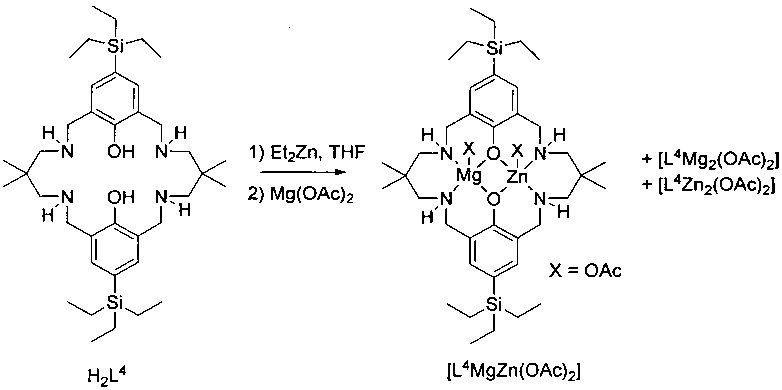
H2L4 (0,2 г, 0,3 ммоль) растворяли в безводном THF (5 мл) в атмосфере азота при 25°C. Et2Zn (0,037 г, 0,3 ммоль) растворяли в безводном THF (2 мл), добавляли в раствор лиганда и перемешивали в течение ночи. Добавляли Mg(OAc)2 (0,043 г, 0,3 ммоль) и перемешивали раствор в течение дополнительных 4 часов. Растворитель удаляли под вакуумом с получением белого твердого вещества (0,23 г, 0,27 ммоль, 90%). MS (ESI): масса/заряд 799,3 (100%, [L4MgZn(O2CH)]+), 813,4 (20%, [L4MgZn(OAc)]+), 759,4 (10%, [L4Mg2(O2CH)]+), 841,3 (15%, [L4Zn2(O2CH)]+).
Спектры ESI-MS полученные в MeCN, содержащем (0,1% NH4+O2CH-); см. фигуру 2.
с) Получение [L4ZnMg(OAc)2] из каталитической системы 2
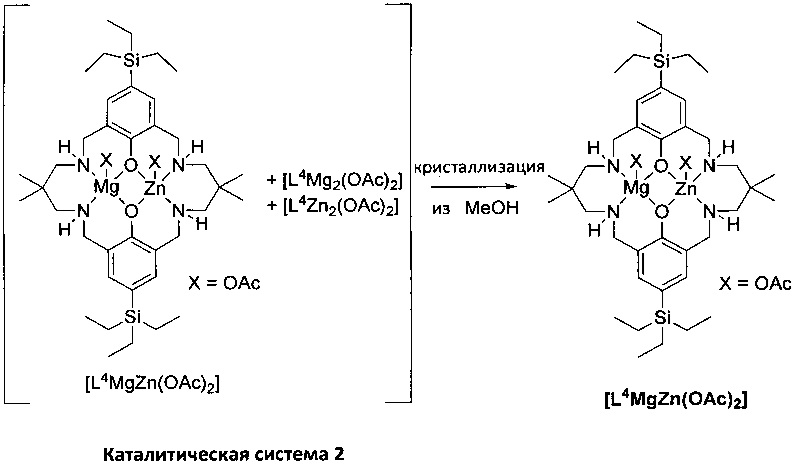
Каталитическую систему 2 (0,15 г) растворяли в 2 мл MeOH и помещали в трубку для ЯМР с пробкой. Фильтровали крупные бесцветные кристаллы, которые выросли в течение ночи. Кристаллы анализировали с помощью ESI-MS (в MeCN с 0,1% NH4+O2CH-); см. фигуру 3, на которой показано практически полное исчезновение пиков, соответствующих двум гомобиметаллическим соединениям, [L4Mg2(OAc)2] и [L4Zn2(OAc)2], указывающее на то, что соединение содержало практически чистое (>95%) гомобиметаллическое соединение [L4MgZn(OAc)2]. MS (ESI): масса/заряд 799,3 (100%, [L4MgZn(O2CH)]+), 813,4 (50%, [L4MgZn(OAc)]+), 759,4.
Спектры ESI-MS полученные в MeCN, содержащем (0,1% NH4+O2CH-); см. фигуру 3.
d) Получение каталитической системы 3
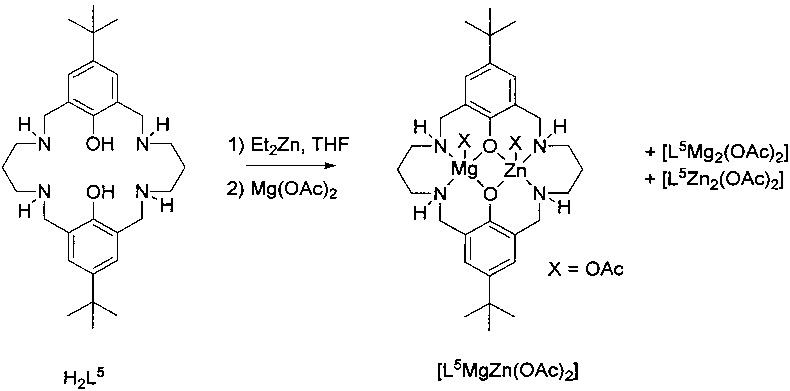
H2L5 (0,5 г, 1,01 ммоль) растворяли в безводном THF (10 мл) в атмосфере азота при 25°C. Et2Zn (0,124 г, 1,01 ммоль) растворяли в безводном THF (3 мл), добавляли в раствор лиганда и перемешивали в течение ночи. Mg(ОАс)2 (0,143 г, 1,01 ммоль) добавляли вместе с MeOH (5 мл) и перемешивали раствор в течение дополнительных 4 часов. Растворитель удаляли под вакуумом с получением белого твердого вещества (0,62 г, 0,88 ммоль, 89%). MS (ESI): масса/заряд 627,3 (100%, [L5MgZn(O2CH)]+), 641,3 (60%, [L5MgZn(OAc)]+), 587,3 (15%, [L5Mg2(O2CH)]+), 601,3 (10%, [L5Mg2(OAc)]+), 667,3 (40%, [L5Zn2(O2CH)]+), 681,2 (40%, [L5Zn2(OAc)]+).
Спектры ESI-MS полученные в MeCN, содержащем (0,1% NH4+O2CH-); см. фигуру 4.
e) Получение каталитической системы 4
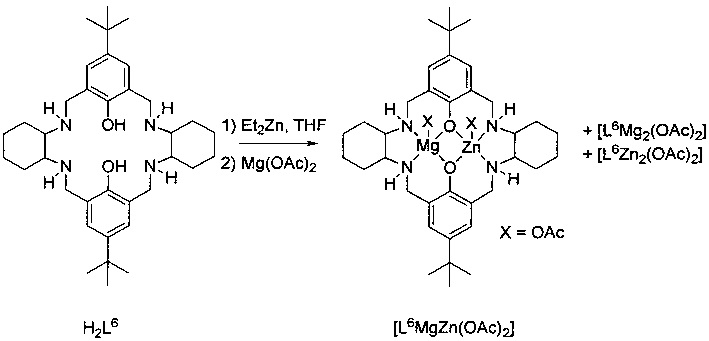
H2L6 (0,33 г, 0,58 ммоль) растворяли в безводном THF (5 мл) в атмосфере азота при 25°C. Et2Zn (0,071 г, 0,58 ммоль) растворяли в безводном THF (3 мл), добавляли в раствор лиганда и перемешивали в течение ночи. Mg(ОАс)2 (0,082 г, 0,58 ммоль) добавляли вместе с MeOH (5 мл) и перемешивали раствор в течение дополнительных 4 часов. Растворитель удаляли под вакуумом с получением белого твердого вещества (0,4 г, 0,52 ммоль, 89%). MS (ESI): масса/заряд 707,4 (100%, [L6MgZn(O2CH)]+), 667,3 (10%, [L6Mg2(O2CH)]+), 747,2 (30%, [L6Zn2(O2CH)]+).
Спектры ESI-MS полученные в MeCN, содержащем (0,1% NH4+O2CH-); см. фигуру 5.
f) Получение каталитической системы 5
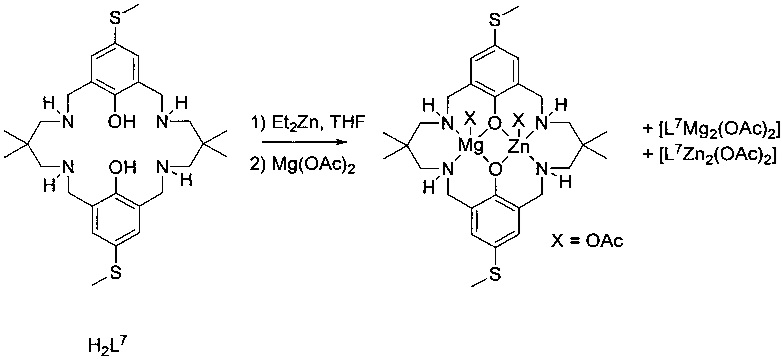
H2L7 (0,37 г, 0,70 ммоль) растворяли в безводном THF (5 мл) в атмосфере азота при 25°C. Et2Zn (0,087 г, 0,70 ммоль) растворяли в безводном THF (3 мл), добавляли в раствор лиганда и перемешивали в течение ночи. Mg(ОАс)2 (0,10 г, 0,70 ммоль) добавляли вместе с MeOH (1 мл) и перемешивали раствор дополнительно в течение 4 часов. Растворитель удаляли под вакуумом с получением белого твердого вещества (0,38 г, 0,52 ммоль, 74%). MS (ESI): масса/заряд 677,2 (90%, [L7MgZn(OAc)]+), 637,3 (100%, [L7Mg2(OAc)]+), 717,1 (50%, [L6Zn2(OAc)]+).
Спектры ESI-MS полученные в MeCN, содержащем (0,1% NH4+O2CH-); см. фигуру 6.
g) Получение каталитической системы 6
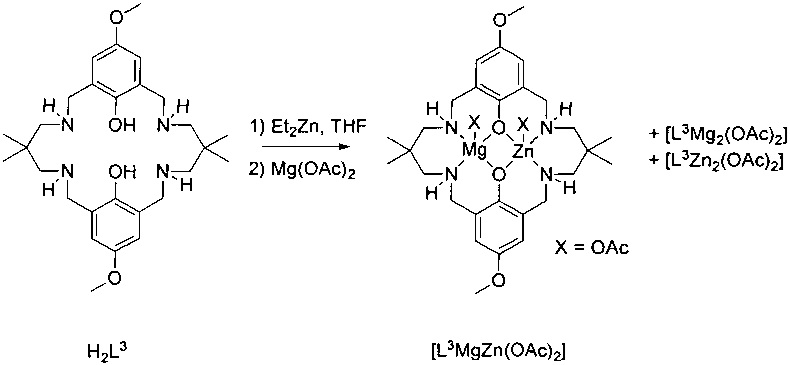
H2L3 (0,34 г, 0,67 ммоль) растворяли в безводном THF (5 мл) в атмосфере азота при 25°C. Et2Zn (0,083 г, 0,67 ммоль) растворяли в безводном THF (3 мл), добавляли в раствор лиганда и перемешивали в течение ночи. Mg(ОАс)2 (0,096 г, 0,67 ммоль) добавляли вместе с MeOH (1 мл) и перемешивали раствор дополнительно в течение 4 часов. Растворитель удаляли под вакуумом с получением белого твердого вещества (0,42 г, 0,60 ммоль, 90%). MS (ESI): масса/заряд 631,2 (5%, [L3MgZn(O2CH)]+), 645,3 (30%, [L3MgZn(OAc)]+), 591,3 (10%, [L3Mg2(O2CH)]+), 605,4 (100%, L3Mg2(OAc)]+), 673,2 (10%, L3Zn2(O2CH)]+), 685,2 (75%, L3Zn2(OAc)]+).
Спектры ESI-MS полученные в MeCN, содержащем (0,1% NH4+O2CH-); см. фигуру 7.
h) Получение каталитической системы 7 (~65% [L1MgZnBr2])
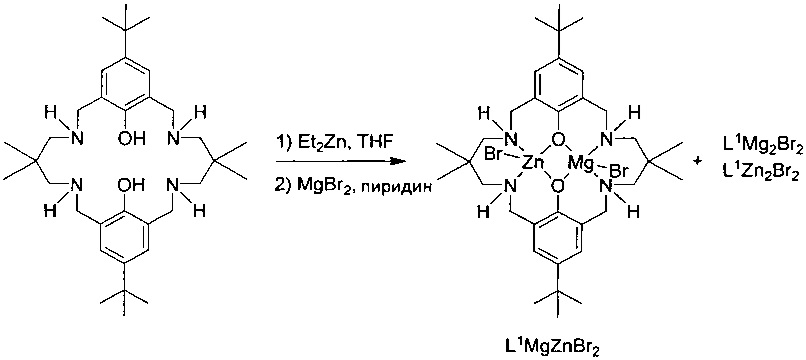
H2L1 (0,112 г, 0,2 ммоль) растворяли в безводном THF (10 мл) в атмосфере азота при 25°C. Et2Zn (20 мкл, 0,2 ммоль) добавляли в раствор лиганда и перемешивали в течение ночи. Вслед за раствором MgBr2 (0,038 г, 0,2 ммоль) в смешанную систему растворителей THF (15 мл)/пиридин (5 мл) добавляли растворитель пиридин (5 мл). Перемешивали раствор в течение 1 часа и затем удаляли растворитель под вакуумом с получением грязно-белого твердого вещества (0,158 г, 98%).
Спектры MALDI-ToF (фигура 8) получали с применением матрицы дитранола с KCl в качестве ионизирующего средства и THF в качестве растворителя: масса/заряд 677,5 [LMg2Br]+, 717,4 [LMgZnBr]+, 757,4 [LZn2Br]+.
В данном случае 1H ЯМР спектр (фигура 9, верхняя часть) можно было легко объяснять и сравнивать с теми двумя гомобиметаллическими соединениями [L1Mg2Br2] и [L1Zn2Br2]. Анализ составных частей 1H ЯМР подтверждали, что каталитическая система 7 содержит ~65% гетеробиметаллического [L1MgZnBr2].
i) Получение [L1MgZnBr2] (>95%)
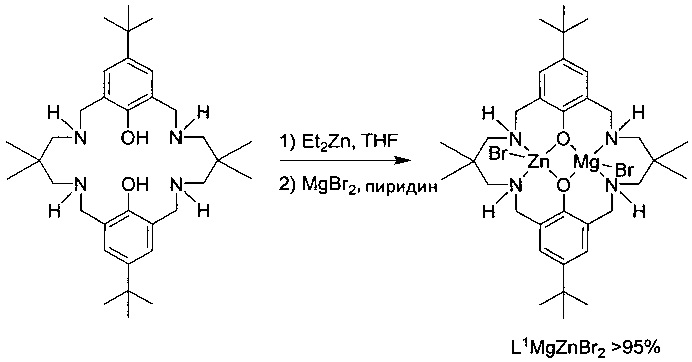
H2L1 (0,112 г, 0,2 ммоль) взвешивали в сосуде Шленка и растворяли в безводном THF (10 мл) с последующим добавлением Et2Zn (20 мкл, 0,2 ммоль) и перемешиванием реакционной смеси в течение ночи. Затем добавляли пиридин (5 мл) и охлаждали реакционную среду до -78°C. За этим по каплям добавляли раствор MgBr2 (0,0375 г, 0,204 ммоль) в пиридин (5 мл)/THF (15 мл) с течение 15 минут. Как только добавление было завершено реакционную смесь перемешивали в течение 15 минут и затем баню с сухим льдом убирали. После еще 30 минут все растворители удаляли in vacuo с получением бледно-желтого порошка. Продукт высушивали in vacuo в течение 2 часов с получением бледно-желтого твердого вещества (0,0910 г, 51%). Спектры MALDI-ToF получали с применением матрицы дитранола с KCl в качестве ионизирующего средства и THF в качестве растворителя: масса/заряд 677,5 [LMg2Br]+, 717,4 [LMgZnBr]+, 757,4 [LZn2Br]+.
Спектр 1H ЯМР (фигура 9, нижняя часть) демонстрировал практически полное исчезновение пиков, которые, как известно, соответствовали [L1Mg2Br2] и [L1Zn2Br2].
j) Получение каталитической системы 8
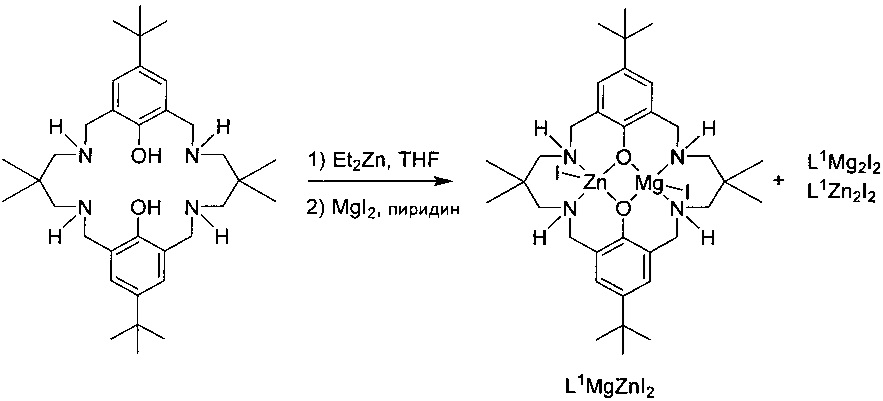
H2L1 (0,112 г, 0,2 ммоль) растворяли в безводном THF (5 мл) в атмосфере азота при 25°C. Затем Et2Zn (20 мкл, 0,2 ммоль) добавляли в раствор лиганда и перемешивали в течение ночи. Вслед за мутным раствором MgI2 (0,057 г, 0,2 ммоль) в смешанную систему растворителей THF (15 мл)/пиридин (5 мл) добавляли растворитель пиридин (5 мл). Перемешивали раствор в течение 90 минут и затем удаляли растворитель под вакуумом с получением бледно-желтого твердого вещества (0,046 г, 25%).
Спектры MALDI-ToF (фигура 10) получали с применением матрицы дитранола с KCl в качестве ионизирующего средства и THF в качестве растворителя: масса/заряд 725,7 [LMg2I]+, 765,7 [LMgZnI]+, 805,6 [LZn2I]+.
k) Получение каталитической системы 9
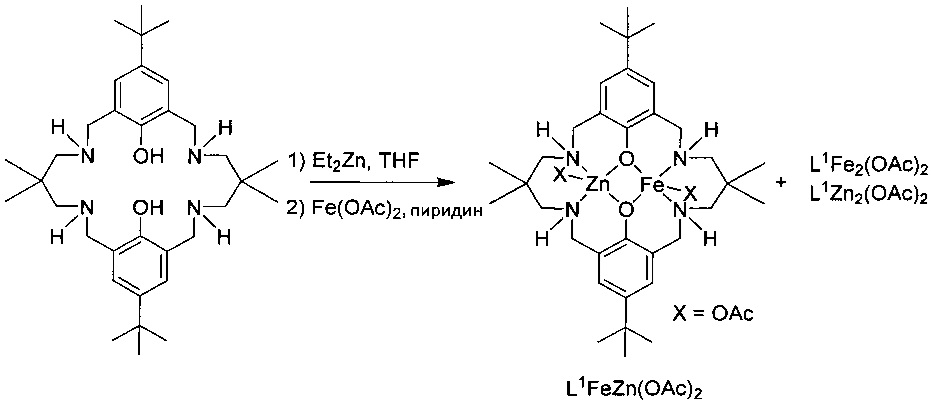
H2L1 (0,179 г, 0,3 ммоль) растворяли в безводном THF (12,5 мл) в атмосфере азота при 25°C. Затем Et2Zn (33 мкл, 0,3 ммоль) добавляли в раствор лиганда и перемешивали в течение ночи. Вслед за добавлением по каплям желтого/коричневого раствора Fe(OAc)2 (0,057 г, 0,3 ммоль) в смешанную систему растворителей THF (7,5 мл)/пиридин (1 мл) добавляли растворитель пиридин (2,5 мл). Перемешивали раствор в течение 1 часа, в течение которого происходило изменение цвета от желтого/коричневого до коричневого. Затем все растворители удаляли под вакуумом с получением коричневого порошка (0,142 г, 55%).
Спектры MALDI-ToF (фигура 11) получали с применением матрицы дитранола с KCl в качестве ионизирующего средства и THF в качестве растворителя: масса/заряд 721,5 [LFe2(OAc)]+, 729,5 [LFeZn(OAc)]+, 737,5 [LZn2(OAc)]+.
l) Получение каталитической системы 10
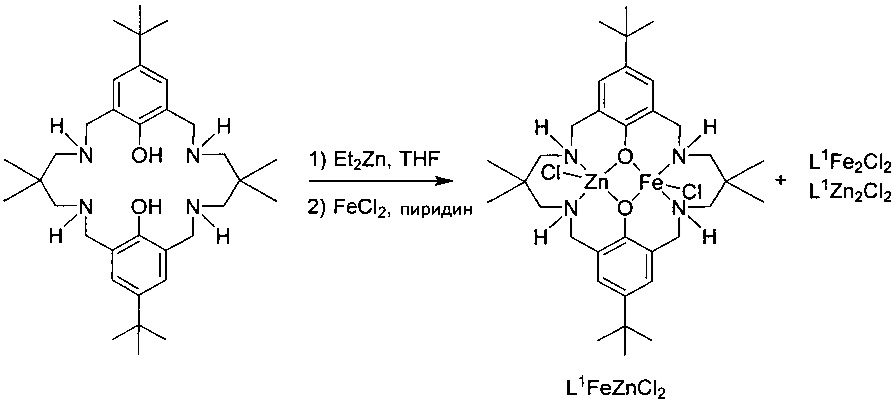
H2L1 (0,179 г, 0,3 ммоль) растворяли в безводном THF (10 мл) в атмосфере азота при 25°C. Затем Et2Zn (33 мкл, 0,3 ммоль) добавляли в раствор лиганда и перемешивали в течение ночи. Вслед за добавлением по каплям желтого раствора FeCl2 (0,041 г, 0,3 ммоль) в смешанную систему растворителей THF (7,5 мл)/пиридин (2,5 мл) добавляли растворитель пиридин (2,5 мл). Перемешивали раствор в течение 1 часа, в течение которого происходило изменение цвета от желтого до коричневого. Затем все растворители удаляли под вакуумом с получением коричневого порошка (0,181 г, 75%).
Спектры MALDI-ToF (фигура 12) получали с применением матрицы дитранола с KCl в качестве ионизирующего средства и THF в качестве растворителя: масса/заряд 697,5 [LFe2Cl]+, 705,5 [LFeZnCl]+, 713,5 [LZn2Cl]+.
m) Получение каталитической системы 11
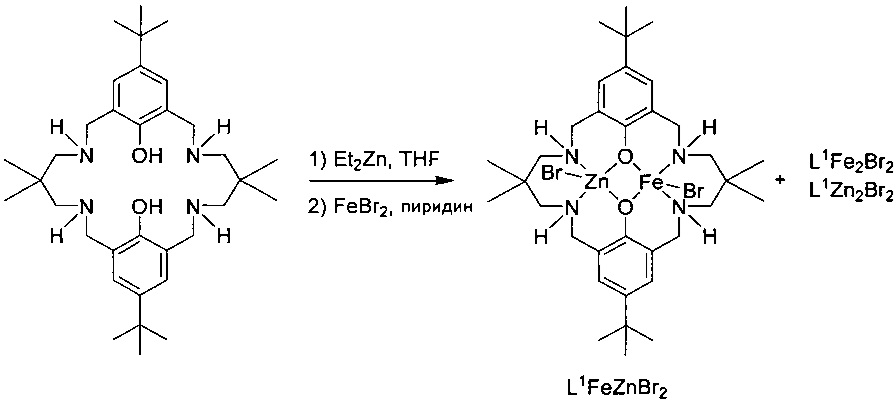
H2L1 (0,179 г, 0,3 ммоль) растворяли в безводном THF (12,5 мл) в атмосфере азота при 25°C. Затем Et2Zn (33 мкл, 0,3 ммоль) добавляли в раствор лиганда и перемешивали в течение ночи. Вслед за добавлением по каплям коричневой/желтой суспензии FeBr2 (0,070 г, 0,3 ммоль) в смешанную систему растворителей THF (9 мл)/пиридин (1 мл) добавляли растворитель пиридин (2,5 мл). Перемешивали раствор в течение 1 часа, в течение которого происходило изменение цвета суспензии до оранжевого/коричневого. Затем все растворители удаляли под вакуумом с получением коричневого порошка (0,157 г, 58%).
Спектры MALDI-ToF (фигура 13) получали с применением матрицы дитранола с KCl в качестве ионизирующего средства и THF в качестве растворителя: масса/заряд 741,4 [LFe2Br]+, 749,4 [LFeZnCl]+, 757,4 [LZn2Cl]+.
n) Получение каталитической системы 12
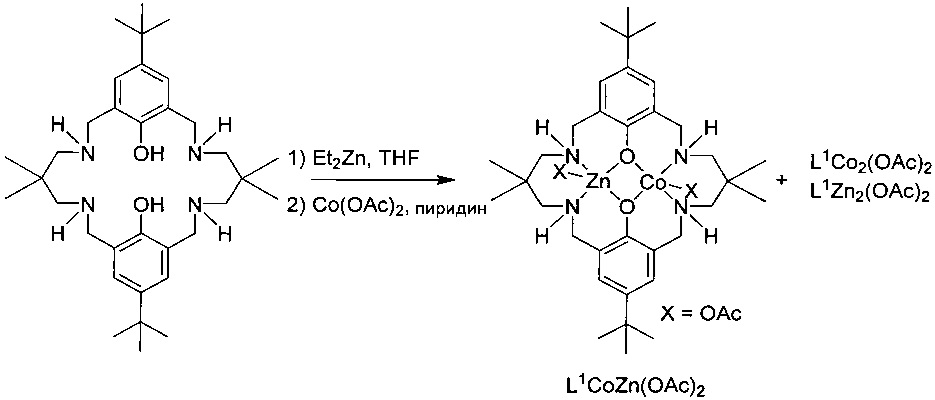
H2L1 (0,179 г, 0,3 ммоль) растворяли в безводном THF (10 мл) в атмосфере азота при 25°C. Затем Et2Zn (33 мкл, 0,3 ммоль) добавляли в раствор лиганда и перемешивали в течение ночи. Вслед за добавлением по каплям пурпурного раствора Co(ОАс)2 (0,057 г, 0,3 ммоль) в смешанную систему растворителей THF (10 мл)/пиридин (2,5 мл) добавляли растворитель пиридин (2,5 мл). Перемешивали раствор в течение 1 часа, в течение которого происходило изменение цвета от розового до коричневого. Затем все растворители удаляли под вакуумом с получением коричневого порошка (0,172 г, 67%).
Спектры MALDI-ToF (фигура 14) получали с применением матрицы дитранола с KCl в качестве ионизирующего средства и THF в качестве растворителя: масса/заряд 727,5 [LCo2(OAc)]+, 732,5 [LCoZn(OAc)]+, 737,5 [LZn2(OAc)]+.
o) Получение каталитической системы 13
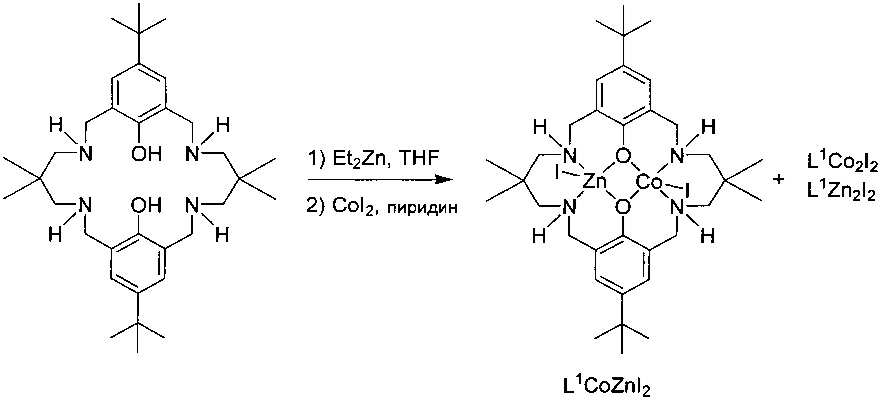
H2L1 (0,179 г, 0,3 ммоль) растворяли в безводном THF (12,5 мл) в атмосфере азота при 25°C. Затем Et2Zn (33 мкл, 0,3 ммоль) добавляли в раствор лиганда и перемешивали в течение ночи. Вслед за добавлением по каплям голубой/зеленой суспензии CoI2 (0,101 г, 0,3 ммоль) в смешанную систему растворителей THF (27,5 мл)/пиридин (2,5 мл) добавляли растворитель пиридин (2,5 мл). Перемешивали раствор в течение 1 часа, в течение которого образовывался пурпурный раствор. Затем все растворители удаляли под вакуумом с получением пурпурного порошка (0,234 г, 78%).
Спектры MALDI-ToF (фигура 15) получали с применением матрицы дитранола с KCl в качестве ионизирующего средства и THF в качестве растворителя: масса/заряд 795,4 [LCo2I]+, 800,4 [LCoZnI]+, 805,4 [LZn2I]+.
р) Получение каталитической системы 14
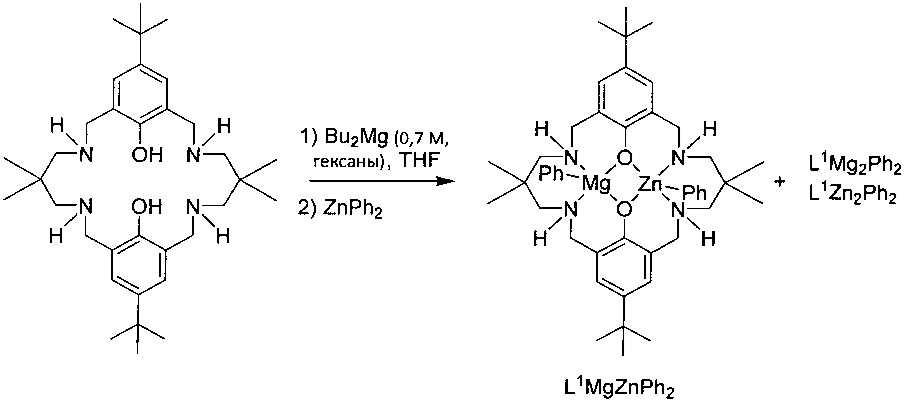
H2L1 (0,1 г, 0,181 ммоль) растворяли в безводном THF (10 мл) и помещали в перчаточный холодильник (-40°C). 0,26 мл n-бутил-втор-бутилмагниевый раствор (0,7 М в гексане) добавляли по каплям в раствор THF. Затем через четыре часа Ph2Zn (40 мг) добавляли в раствор и оставляли его перемешиваться в течение 16 ч. при 25°C в перчаточной камере. Затем испаряли растворитель с получением грязно-белого твердого вещества. (). Расч. для C46H64MgN4O2Zn: C, 69,52; H, 8,12; N, 7,05%. Обнаружено: C, 69,31; H, 7,85; N, 6,88%. MALDI-ToF MS масса/заряд: 675,4 (30%, [L1MgZnPh]+), 715,3 (60%, [L1MgZnPh]+), 755,3 (40%, [L1Zn2Ph]+). Вследствие чувствительный к воздушной среде природы этого соединения на масс-спектре также наблюдали множество продуктов распада.
Результаты
Характеристики смешанных металлических каталитических систем являлись отличными от каких-либо соответствующих гомобиметаллических соединений. Пример анализа производили для каталитической системы 1 по сравнению с L1Zn2(OAc)2 (катализатор A) и L1Mg2(OAc)2 (катализатор B).
На 1H ЯМР спектре каталитической системы 1 (фигура 16) показано полное расходование этильной группы, связанной с цинком, и образование увеличенных резонансов лиганда, которые находятся в соответствии с координацией металла. Эти явно выраженные сигналы не могли быть устранены как посредством изменения растворителя (например, бензола, толуола, тетрахлорэтана), так и посредством высоко-/низкотемпературных экспериментов (от -50 до 80°C). В отличие от гомобиядерных комплексов A и B, оба из которых демонстрировали явное устранение пиков при повышенной температуре. Элементный анализ, как и предполагалось, показал, что продукт содержал равное количество Zn и Mg. На спектре MALDI-ToF (фигура 1) показан пик в 697 а.е.м., который соответствует гетеробиядерному Zn/Mg комплексу катиона [LZnMg(OAc)]+. Ранее наблюдали, что этот класс комплексов ионизирован во время экспериментов MALDI-ToF с получением катионов в результате потери карбоксилата солигандом (М.R. Kember и C.K. Williams, J. Am. Chem. Soc., 2012, 134, 15676-15679, и M.R. Kember, P.D. Knight, P.T.R. Reung и C.K. Williams, Angew. Chem. - Int. Edit., 2009, 48, 931-933). Масс-спектр MALDI-ToF также указывал на присутствие гомобиядерных комплексов как A, так и B, о чем свидетельствуют пики в 657 и 739 а.е.м., приходящиеся на [LMg2(OAc)]+ и [LZn2(OAc)]+, соответственно.
С целью исключения вероятности смешанных металлических соединений, образованных только во время экспериментов MALDI-ToF, эквимолярную смесь A и B сравнивали. Эквимолярные смеси комплексов показали только ионы, ассоциированные с двумя гомобиядерными комплексами (т.е. A и B); подтверждения каких-либо катионов гетеробиядерных комплексов не было. Кроме того, когда эквимолярную смесь нагревали при 80°C в течение 16 ч. (условия, эквивалентные таковым при осуществлении полимеризации), спектр оставался таким же, демонстрируя только два гомобиядерных комплекса.
Определить состав смеси, приходящийся на явно выраженные сигналы ЯМР, было невозможно, хотя предполагаемый стехиометрический состав представлял собой 1:2:1 ([L1Zn2(OAc)2] : [L1MgZn(OAc)2] : L1Mg2(OAc)2]) наряду с результатами элементного анализа.
Каталитическую систему, полученную в примере 1а (каталитическая система 1), изучали относительно ее способности полимеризовать CO2 и эпоксид.
2. Полимеризация диоксида углерода и эпоксида
Реакции сополимеризации при низком давлении
Дистиллированный и обезвоженный оксид циклогексена (2,5 ммоль, 25 ммоль) и катализатор (0,025 ммоль) помещали в сосуд Шленка. Дегазировали реакционную, а затем нагревали до 80°C при давлении CO2 1 Бар. Через определенную постоянную времени смесь охлаждали с помощью выдержки на воздухе и фиксировали спектр 1H ЯМР неочищенной смеси. Затем удаляли оксид циклогексена под вакуумом с получением поликарбоната, который очищали посредством его растворения в THF и осаждения в присутствии MeOH.
Реакции сополимеризации при высоком давлении
Реактор Parr обезвоживали в течение 20 ч. при 140°C и продували CO2 трижды и обеспечивали возможность остыть до 25°C. Затем в реактор Parr добавляли катализатор (0,03 ммоль), растворенный в оксиде циклогексена (15 мл, 148 ммоль). После герметизации реактора добавляли 50 Бар CO2, в то время как реакционную смесь перемешивали с низкой частотой с целью обеспечения растворения CO2. Эту стадию повторяли несколько раз, прежде чем растворение CO2 достигало равновесия и давление паровой фазы над жидкостью оставалось неизменным. Сосуд нагревали до соответствующей температуры и перемешивали в течение определенного времени и затем фиксировали спектр 1H ЯМР непереработанной реакционной смеси. Затем смесь переносили в хлорид метилена и упаривали досуха. Белый порошок полимера очищали посредством его растворения в THF с последующим осаждением в присутствии MeOH.
а) Полимеризация эпоксида и диоксида углерода в присутствии каталитической системы 1
Активность каталитической системы 1 в отношении сополимеризации оксида циклогексена и диоксида углерода оценивали с помощью 0,1 мол. % катализатора (в сравнении с эпоксидом, при условии, что состав - 1:2:1), давления CO2 1 Бар, при 80°C и в течение 6 часов протекания, так как такие условия ранее были доказаны наиболее эффективными для A. Каталитическую систему 1 сравнивали с двумя гомобиядерными катализаторами (A, B) и с эквимолярной смесью (с молярным соотношением соединений А : В 1:1). Результаты показаны в таблице 1.
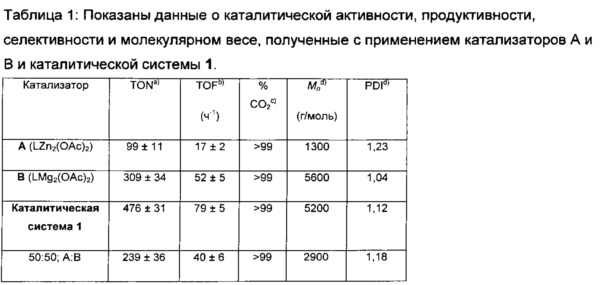
Все реакции сополимеризации проводили в сосуде Шленка при 0,1% загрузке катализатора (в сравнении с CHO), 80°C, 1 Бар CO2 в течение 6 ч. а) Число циклов каталитического превращения (TON)=количество молей потребляемого оксида циклогексена/количество молей катализатора. b) Частота циклов превращения (TOF)=TON/6. с) Выраженное в процентах потребление диоксида углерода в сравнении с теоретическим максимумом (100%). Его определяли посредством сравнения с относительными интегралами резонансов 1H ЯМР, которые приходятся на карбонатные (δ: 4,65 ppm) и простые эфирные (δ: 3,45 ppm) связи в основной цепи полимера. d) Определенные с помощью SEC в THF применяемые точные стандарты полистирола Mn в качестве калибрующего вещества.
Каталитическая система 1 явно значительно более активна, чем как катализатор A, так и катализатор B; более того, она обладала почти двойной активностью катализатора B, а именно его исключительно высокой каталитической активностью. Кроме того, она показывала значительно более высокую активность, чем эквимолярная смесь катализаторов A и B. Эквимолярная смесь имела величины продуктивности (TON) и активности (TOF), которые с большой точностью соответствовали предполагаемому составу на основе смеси: т.е. TONсмесь=(TON1+TON2)/2. Это полностью соответствовало масс-спектрометрическим исследованиям, которые указывали на то, что здесь, по сути, не присутствовал обмен металлами между двумя катализаторами. В противоположность этому, каталитическая система 1 проявляла значительно большую активность, чем сумма ее составляющих.
Каталитическая система 1 показала отличную селективность с близким теоретическим потреблением диоксида углерода в основной цепи полимера и достаточно низкое количество простых эфирных связей в полученном в результате полимере (таблица 1, фигура 16). Все катализаторы получали низкий Mn поликарбонатов (Mn<6000 г/моль), вследствие эффективной реакции передачи цепи с протонными примесями (спиртами); см., A. Cyriac, et al, Macromolecules, 2010, 43, 7398-7401, F. Jutz, et al, J. Am. Chem. Soc., 2011, 133, 17395-17405; W.J. van Meerendonk, et al, Macromolecules, 2005, 38, 7306-7313. Такие величины Mn весьма желательны для целевого компонента, как например, полиолы для высокомолекулярного полимерого синтеза. Кроме того, с помощью каталитической системы 1 коэффициент полидисперсности полученного в результате поликарбоната уменьшился, что указывало на высокую степень управления полимеризацией. На спектре MALDI-ToF показаны две группы цепей, обе с >99% карбонатными связями и отличающиеся по концевым группам цепи: одна группа представляет собой α-ацетил-ω-гидроксил, а другая представляет собой полициклогексен карбонат с α,ω-дигидроксильной концевой кэпированной группой (фигура 17).
С целью лучшего понимания и сравнения активности каталитической системы 1 с другими известными катализаторами эпоксид/CO2, эксперименты осуществляли в диапазоне условий; см. таблица 2.
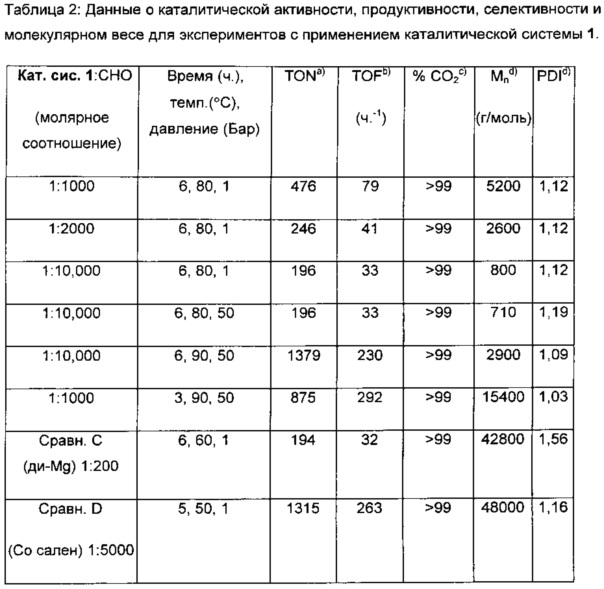
а) Число циклов каталитического превращения (TON)=количество молей потребляемого оксида циклогексена/количество молей катализатора. b) Частота циклов превращения (TOF)=TON/продолжительность реакции. с) Выраженное в процентах потребление диоксида углерода в сравнении с теоретическим максимумом (100%). Его определяли посредством сравнения с относительными интегралами резонансов 1H ЯМР, которые приходятся на карбонатные (δ: 4,65 ppm) и простые эфирные (δ: 3,45 ppm), присоединенные к основной цепи полимера. d) Определенные с помощью SEC в THF применяемые точные стандарты полистирола Mn.
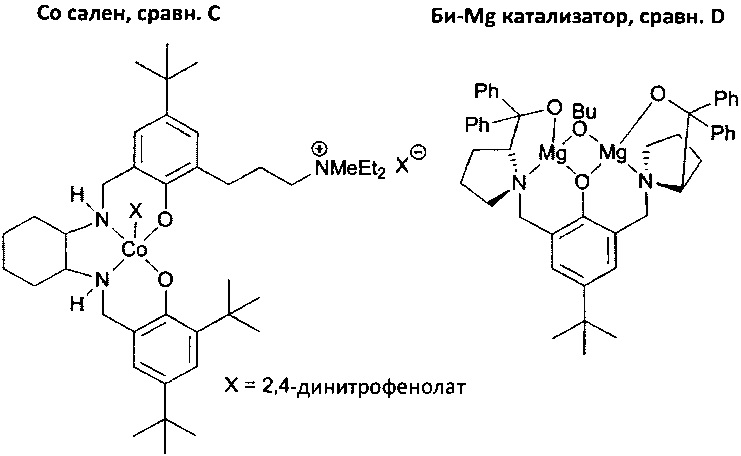
При любых условиях каталитическая система 1 демонстрировала достаточно высокую степень управления полимеризацией, о чем свидетельствует линейное увеличение молекулярного веса с уменьшением концентрации катализатора. Кроме того, нет различия в активности при постоянной концентрации катализатора и при изменении давления CO2, которое соответствует раннее обнаруженному с помощью цинкового катализатора, скорость которого не зависит от его давления (F. Jutz, et al, J. Am. Chem. Soc., 2011, 133, 17395-17405). С другой стороны, как и предполагалось, увеличение температуры значительно улучшало активность, в то время как сохранялась достаточно высокая селективность карбонатных связей. По сравнению с некоторыми приемлемыми катализаторами сополимеризации CHO/CO2, данная новая система продемонстрировала отличную активность, селективность и продуктивность. Например, она продемонстрировала аналогичную или более высокую продуктивность и активность по отношению к одному из наиболее эффективных кобальтовых катализаторов (W.-M. Ren, et al, Macromolecules, 2010, 43, 1396-1402). Кроме того, по сравнению с одним из некоторых других примеров ди-Mg катализатора, она в 2,5 раза быстрее, в то время как действует при загрузке в 5 раз меньше (Y.L. Xiao, et al, Macromolecules, 2006, 39, 128-137).
Поли(циклогексенкарбонат) (PCHC) показывал смещенные молекулярно-массовые распределения и малые коэффициенты полидисперсности. Неожиданно было показано, что в смеси присутствуют три различных катализатора. Однако предполагалось, что высокая в сравнении с ростом частота передачи цепи приводит к малому распределению по длине цепи и быстрому взаимному превращению между всеми цепями всех присутствующих катализаторов (S. Inoue, J. Polym. Sci, Part A: Polym. Chem., 2000, 38, 2861-2871). Это открытие является особенно важным как иллюстрация потенциала такой смешанной каталитической системы сополимеризации CO2/эпоксида. Подход согласно настоящему изобретению делает акцент на потенциал значительного усовершенствования каталитической активности посредством такого подхода смешанной системы. Таким образом, применение каталитической системы 1 создает возможность для сополимеров отличного качества, образованных в отношении молекулярный вес/PDI.
Реакции осуществляли для определения активности и стабильности каталитической системы 1 в присутствии воды; см. таблицу 3.
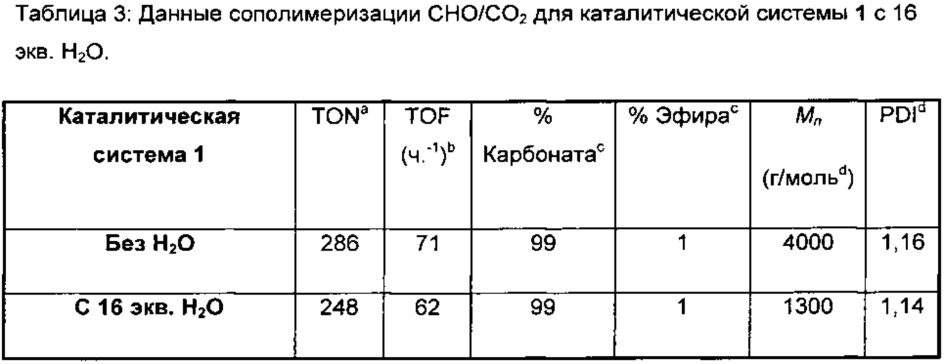
Все реакции сополимеризации осуществляли в сосуде Шленка в течение 4 ч. при 80°C и 1 Бар CO2 при CHO : загрузка катализатора 1:1000. а Число циклов каталитического превращения (TON)=количество молей потребляемого оксида циклогексена/количество молей катализатора. b Частота циклов превращения (TOF)=TON/продолжительность реакции. c Определенные посредством сравнения с относительными интегралами с 3,45 ppm (простые эфирные связи) и 4,65 ppm (поликарбонат) d Определенные с помощью SEC в THF применяемые точные стандарты полистирола Mn.
Важно то, что каталитическая система 1 сохраняла свою высокую активность даже тогда, когда в реакционную среду добавляли 16 эквивалентов H2O (в сравнении с катализатором) (таблица 3). Такая удивительная толерантность к воде является весьма выгодной, в частности, чтобы избегать сложного и проблематичного обезвоживания эпоксидов и CO2, в то время как селективность целевого продукта полиола улучшалась. Добавление протонных реагентов, таких как вода, приводило к передаче цепи посредством образования циклогександиола, из которого получали полимеры, заканчивающиеся телехелатным дигидроксилом (F. Jutz, et al, J. Am. Chem. Soc., 2011, 133, 17395-17405). Таким образом, когда в реакции полимеризации, катализируемые каталитической системой 1, добавляли 16 эквивалентов воды, Mn поликарбоната уменьшалось до 1300 г/моль, в то время как PDI оставался малым (1,14). Важно отметить, что цепи PCHC с α,ω-дигидроксильной концевой кэпированной группой получали как основной продукт, с практически полным подавлением цепей, заканчивающихся моногидроксилом (фигура 18). Такая селективность важна для цепей, заканчивающихся дигидроксилом, так как "полиолы" являются ключевыми реагентами для производства полиуретанов/сложных полиэфиров.
b) Полимеризация эпоксида и диоксида углерода в присутствии других каталитических систем
i) Сополимеризация оксида циклогексена/CO2 в присутствии каталитической системы 7 и [L1MgZnBr2]
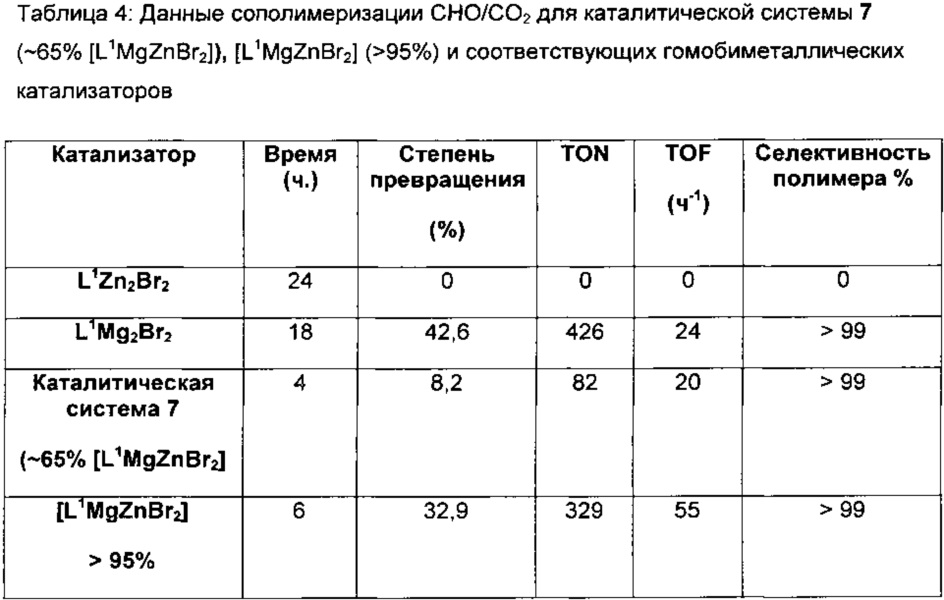
Все реакции сополимеризации осуществляли в сосуде Шленка при 80°C и 1 Бар CO2 при CHO : загрузка катализатора 1:1000.
ii) Сополимеризация оксида циклогексена/CO2 для каталитической системы 2, очищенного [L4ZnMg(OAc)2] и соответствующих гомобиметаллических катализаторов
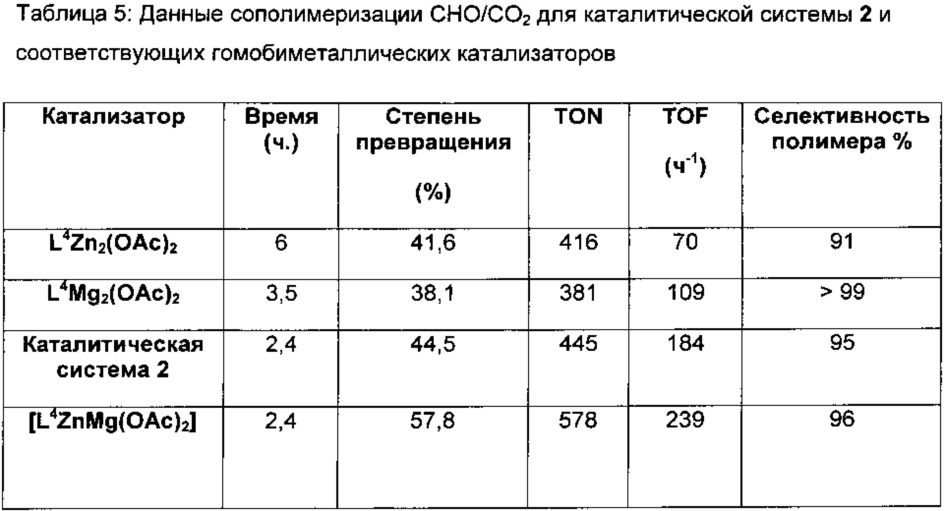
Все реакции сополимеризации осуществляли в сосуде Шленка при 100°C и 1 Бар CO2 при CHO : загрузка катализатора 1:1000.
iii) Сополимеризация оксида циклогексена/CO2 для каталитической системы 6 и соответствующего гомобиметаллического катализатора
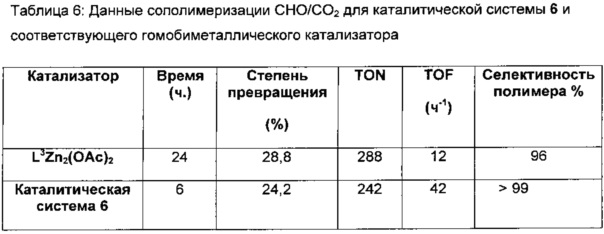
Все реакции сополимеризации осуществляли в сосуде Шленка при 80°C и 1 Бар CO2 при загрузке CHO : катализатор 1:1000.
iv) Сополимеризация оксида циклогексена/CO2 для каталитической системы 5 и соответствующего гомобиметаллического катализатора
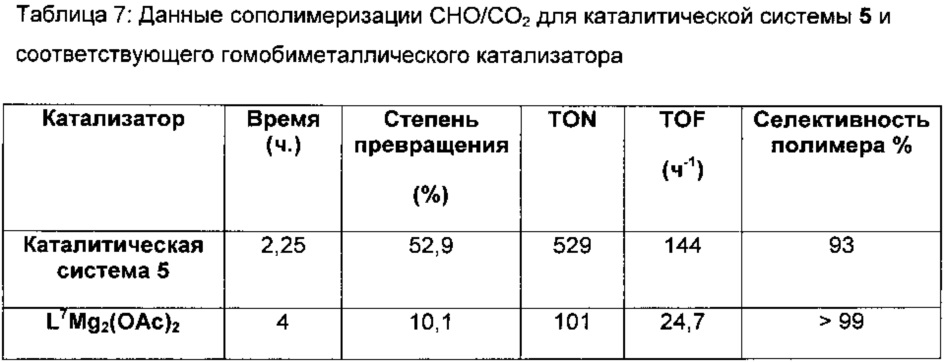
Все реакции сополимеризации осуществляли в сосуде Шленка при 100°C и 1 Бар CO2 при загрузке CHO : катализатор 1:1000.
v) Сополимеризация оксида циклогексена/CO2 для каталитической системы 14
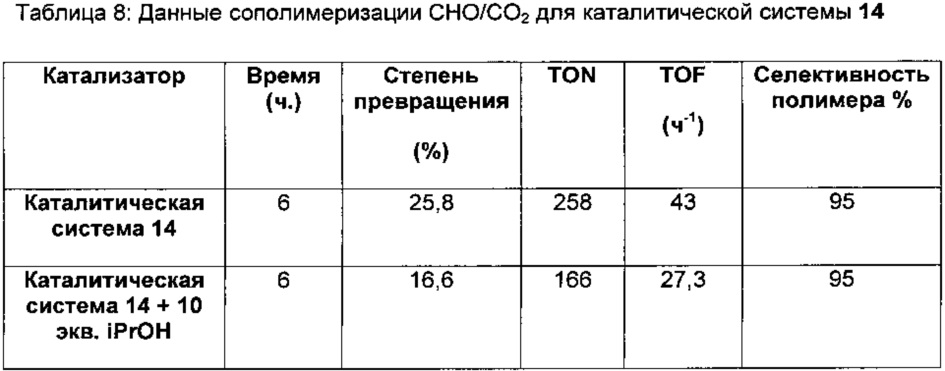
Все реакции сополимеризации осуществляли в сосуде Шленка при 80°C и 1 Бар CO2 при загрузке CHO : катализатор 1:1000.
В таблицах 4 и 5 сравнивают каталитическую активность гомобиметаллических комплексов и соответствующих им гетеробиметаллических каталитических систем, а также величину степени чистоты гетеробиметаллических комплексов. Из таблицы 4 можно явно заметить, что смешанная каталитическая система 7 (которая содержит ~65% [L1MgZnBr2] по 1H ЯМР) показала аналогичную активность по отношению к гомобиметаллическому Mg комплексу [L1MgZnBr2] и значительно большую активность, чем дицинковый аналог. Гетеробиметаллический [L1MgZnBr2] высокой степени чистоты проявлял значительно большую активность, чем каталитическая система 7 и любой их гомобиметаллических комплексов. В таблице 5 продемонстрировано, что смешанная каталитическая система 2 (уже содержащая значительное количество гетеробиметаллического комплекс [L4ZnMg(OAc)2]) проявляла значительно повышенную активность по сравнению с двумя гомобиметаллическими соединениями на основе одинаковой структуры лиганда. Очищенное гетеробиметаллическое соединение [L4ZnMg(OAc)2] показало даже большую активность, проявляя удивительную активность гетеробиметаллической системы, по сравнению с их гомометаллическими аналогами и смесями катализаторов, содержащими гомобиметаллические соединения.
В таблицах 6 и 7 продемонстрирована повышенная активность гетеробиметаллических каталитических систем по сравнению с одним из соответствующих гомобиметаллических катализаторов. В таблице 8 демонстрируется каталитическая активность каталитической системы 14 с добавлением средства передачи цепи (изопропанола) и без него.
vi) Сополимеризация оксида циклогексена/CO2 для других металлов
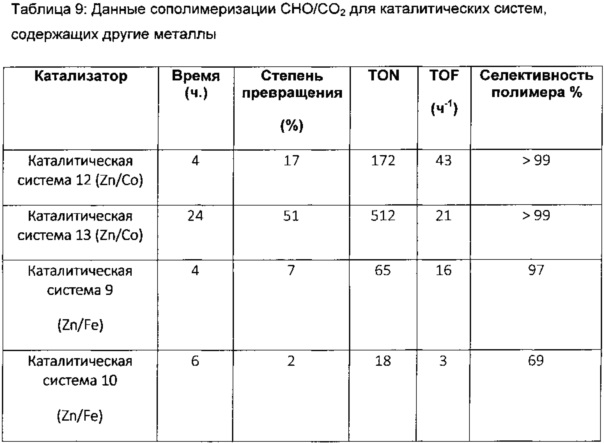
Все реакции сополимеризации осуществляли в сосуде Шленка при 80°C и 1 Бар CO2 при загрузке CHO : катализатор 1:1000.
В таблице 9 демонстрируется каталитическая активность следующих каталитических систем: 9, 10, 12 и 13, которые содержат другие смешанные металлические системы (Zn/Co и Zn/Fe). Все системы представляют собой эффективные катализаторы.