Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ БИМЕТАЛЛИЧЕСКИХ КАТАЛИЗАТОРОВ С ГРАДИЕНТНОЙ СТРУКТУРОЙ НА ОСНОВЕ ПЛАТИНЫ
Вид РИД
Изобретение
Изобретение относится к области электрохимической энергетики, а именно к способу изготовления катализаторов для топливных элементов, и может быть использовано для получения биметаллических катализаторов, применяемых в химических источниках тока, в частности, в низкотемпературных топливных элементах.
Наилучшими катализаторами для катода и анода низкотемпературных топливных элементов являются композиционные материалы, состоящие из наночастиц платины или ее сплавов, нанесенных на поверхность электропроводного носителя.
Одной из основных характеристик процесса гетерогенного катализа является эффективная удельная поверхность катализатора, то есть поверхность частиц катализатора, на которой протекают электрохимические процессы, отнесенная к массе нанесенного на носитель катализатора. В настоящее время получены катализаторы, содержащие наночастицы (НЧ), размер которых лежит в диапазоне 1-100 нм.
Эффективность работы электрокатализатора принято определять по таким параметрам, как активность в реакции восстановления кислорода (РВК), окисления метанола и окисления водорода, а также их стабильность в ходе эксплуатации. Все эти параметры катализаторов связаны с их структурно-морфологическими характеристиками.
Известно, что электрокатализаторы на основе биметаллических НЧ в сравнении с чистой платиной в ряде случаев характеризуются более высокой активностью в РВК.
Известен способ получения биметаллических наночастиц со структурой сплава (Min, М. Particle size and alloying effects of Pt-based alloy catalysts for fuel cell applications / M. Min, J. Cho, K. Cho, H. Kim // Electrochem. Acta. - 2000. - V. 45. - P. 4211-4217). Способ заключается в одновременном осаждении платины и второго металла, в роли которого выступают никель, кобальт и хром. Молярное соотношение платина : металл составило 3:1. Полученные в результате НЧ со структурой «сплав» характеризуются более высокими значениями удельной активности в сравнении с Pt/C материалами. Образование связи Pt-M оказывает влияние на повышение активности НЧ за счет изменения энергии свободных d-орбиталей. Наиболее каталитически активным отмечен материал, содержащий PtNi наночастицы.
Однако в подобных НЧ атомы платины располагаются во всем объеме, что приводит к уменьшению доли атомов платины, катализирующих реакцию восстановления кислорода. Атомы второго металла также будут располагаться не только внутри НЧ, но и на поверхности, что в процессе работы катализатора приведет к окислению поверхности НЧ и деградации каталитической активности платины.
Биметаллические НЧ со структурой оболочка-ядро, содержащие на поверхности атомы платины, а в ядре атомы неблагородного металла, являются более стабильными к окислительной деградации. Общепринятое обозначение данных наночастиц в мировой литературе - «core-shell».
Частицы со структурой «core-shell» были получены в способе, описанном в Zhang, J. Platinum monolayer on nonnoble metal-noble metal core-shell nanopar-ticle electrocatalysts for O2 reduction / J. Zhang, F.H.B. Lima, M.H. Shao, K. Sasaki, J.X. Wang, J. Hanson, R.R. Adzic // J. Phys. Chem. В. - 2005. - V. 109. - P. 22701-22704; Luo, M. Gram-level synthesis of core-shell structured catalysts for the oxygen reduction reaction in proton exchange membrane fuel cells / M. Luo, L. Wei, F. Wang, K. Han, H. Zhu // J. Power Sources. - 2014. - V. 270. - P. 34-41; патент CN104698165B, опубл. 02.12.2015. Способ состоит в восстановлении ионов меди на поверхности углеродного носителя, формировании ядра наночастиц и последующем восстановлении ионов платины на поверхности ядер за счет внесения в реакционную смесь прекурсора платины и добавления восстановителя.
Преимущественная локализация платины в поверхностном слое наночастиц позволяет не только снизить общее содержание драгоценного металла, но и повысить каталитическую активность в РВК, в том числе в результате промотирующего влияния металлического ядра.
К недостаткам следует отнести образование нестабильной структуры, приводящей к быстрой деградации активности подобных НЧ вследствие резкого перехода между атомами платины и меди.
Более устойчивой структурой является система, в которой присутствует плавный переход между атомами металла-ядра и платиной. При переходе от центра НЧ должно происходить уменьшение концентрации атомов металла ядра и увеличение концентрации платины. Таким образом, НЧ будут иметь «градиентную» структуру.
Подобным критериям отвечает способ, описанный в патенте CN104001521, опубликованном 27.08.2014. Способ заключается в формировании массива НЧ с градиентной структурой путем атомизации и последующего напыления атомов меди, затем медно-платиновой смеси, после которых напыляют атомы платины. Для получения катализатора с «градиентной» структурой на поверхность углеродного волокна размером 80x80 мм, помещенного в вакуумную камеру, направляют ионно-лучевой поток. Рабочее напряжение составляет 3,5 кВ. Атомы меди и платины напыляют, формируя тонкую пленку, толщиной около 48 нм. По результатам исследования, данные материалы имеют электрохимически активную площадь поверхности около 20-50 м2/г (Pt).
Значительная толщина общего слоя пленки, полученная данным способом, является существенным недостатком, так как при этом меньшее количество атомов платины будет работать в качестве катализатора вследствие большой толщины пленки относительно отдельных НЧ. Соответственно, площадь электрохимически активной поверхности значительно ниже, по сравнению с активной поверхностью наночастиц. Кроме того, данный способ сложно реализуем для создания отдельных НЧ с градиентной структурой.
Технической задачей, на решение которой направлено данное изобретение, является создание способа получения биметаллических катализаторов с градиентной структурой на основе платины на поверхности углеродного носителя, позволяющего значительно увеличить площадь электрохимически активной поверхности катализатора и уменьшить размер частиц, сохраняя при этом на поверхности высокую долю атомов платины.
Указанный технический результат достигается предложенным способом получения биметаллических катализаторов с градиентной структурой на основе платины и заключается в химическом восстановлении ионов d-металла на поверхности углеродного носителя и формировании ядра наночастиц, с последующим восстановлением ионов платины на поверхности ядер за счет внесения в реакционную смесь прекурсора платины и добавления восстановителя. Высокодисперсный углеродный носитель подвергают предварительной гомогенизации в ультразвуковом диспергаторе в водном растворе этиленгликоля до получения устойчивой суспензии с площадью поверхности частиц не менее 50 м2/г, с последующим четырехстадийным процессом восстановления d-металла из раствора солей с концентрацией 1-10 г/дм3 и ионов платины из гексахлорплатиновой кислоты, путем добавления на первой стадии 50%, на второй и третьей по 25% от общего объема раствора соли d-металла и гексахлорплатиновой кислоты в концентрации 11-30 г/дм3, путем добавления на второй и третьей стадии по 25%, а на четвертой 50% от общего объема раствора гексахлорплатиновой кислоты, при избытке восстановительного агента и значении рН среды 9-10 в условиях постоянного перемешивания и температуры 22-24°С с последующей фильтрацией и высушиванием.
Процесс образования биметаллических наночастиц в соответствии с предложенным способом состоит в последовательном осаждении прекурсоров металлов в определенном соотношении и позволяет получать частицы с более равномерной платиновой оболочкой. При этом содержание меди в ядре и плавный переход от медного ядра к платиновой оболочке, за счет градиентного распределения компонентов, позволяет повысить активность катализатора в реакции восстановления кислорода. Данное позитивное влияние легирующего компонента на функциональные характеристики электрокатализаторов связано с уменьшением межатомного расстояния Pt-Pt в наночастице и облегчением прохождения процесса адсорбции молекул кислорода в ходе РВК, а также с изменением энергии свободных d-орбиталей, которое также облегчает процесс адсорбции О2 на поверхности катализатора.
Отличительным признаком заявляемого способа является получение образцов на основе платинат-d-металлов наночастиц, в которых концентрация платины растет от ядра к поверхности, за счет внесения растворов прекурсоров металлов в четыре последовательные стадии путем добавления на первой стадии 50%, на второй и третьей по 25% от общего объема раствора соли d-металла и гексахлорплатиновой кислоты, в концентрации 11-30 г/дм3, путем добавления на второй и третьей стадии по 25%, а на четвертой 50% от общего объема раствора гексахлорплатиновой кислоты.
Изобретение обладает новизной, так как в мировой литературе не выявлено применение подобного способа.
Технический результат данного изобретения заключается в создании способа получения биметаллических катализаторов с градиентной структурой на основе платины на поверхности углеродного носителя, позволяющего значительно увеличить площадь электрохимически активной поверхности катализатора (≥80 м2/г) и уменьшить размер частиц (≤4 нм), сохраняя при этом на поверхности высокую долю атомов платины (13÷60% масс. Pt).
Сущность изобретения иллюстрируется следующими примерами, таблицей и иллюстрациями:
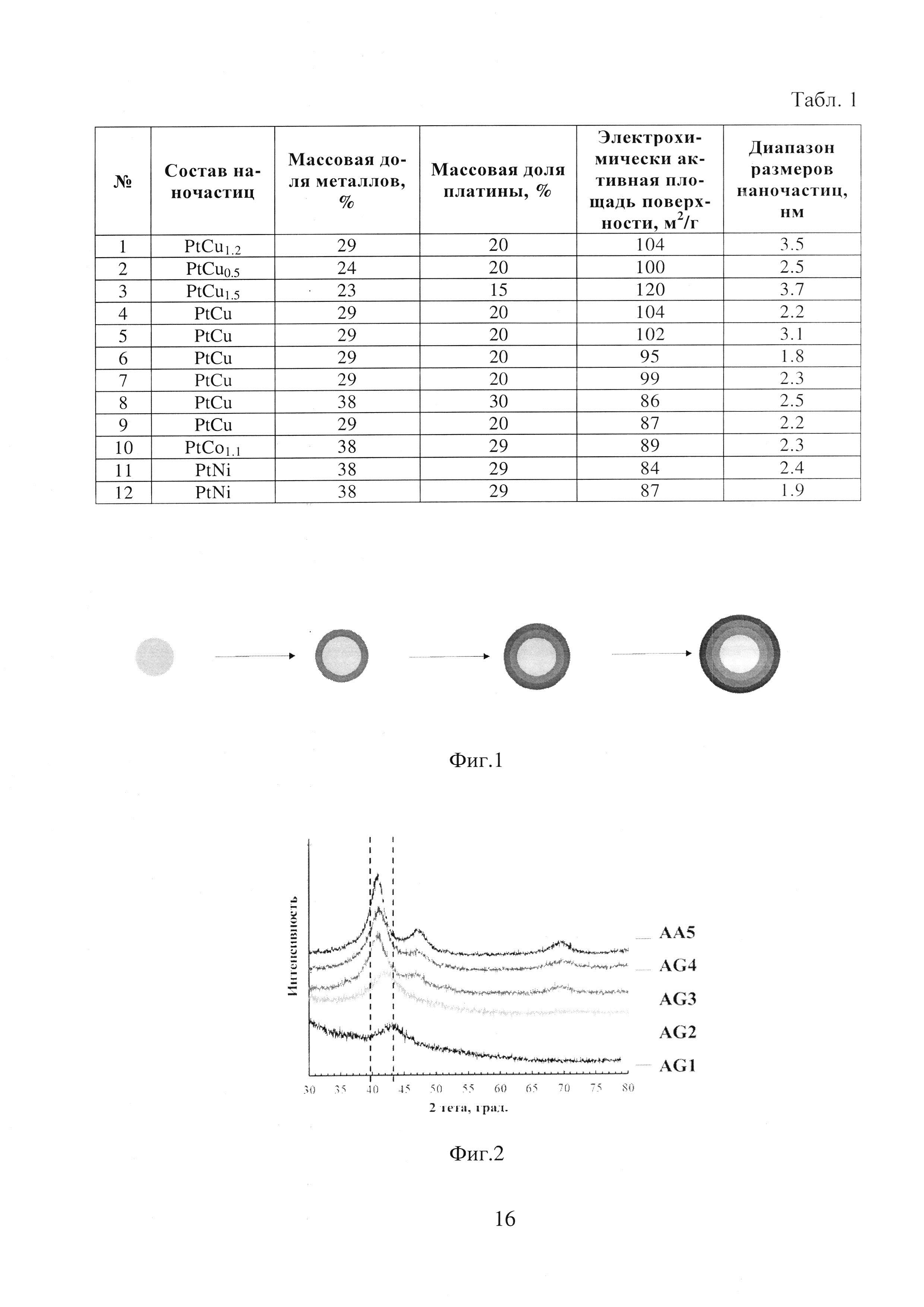
Табл. 1 - Функциональные характеристики полученных образцов.
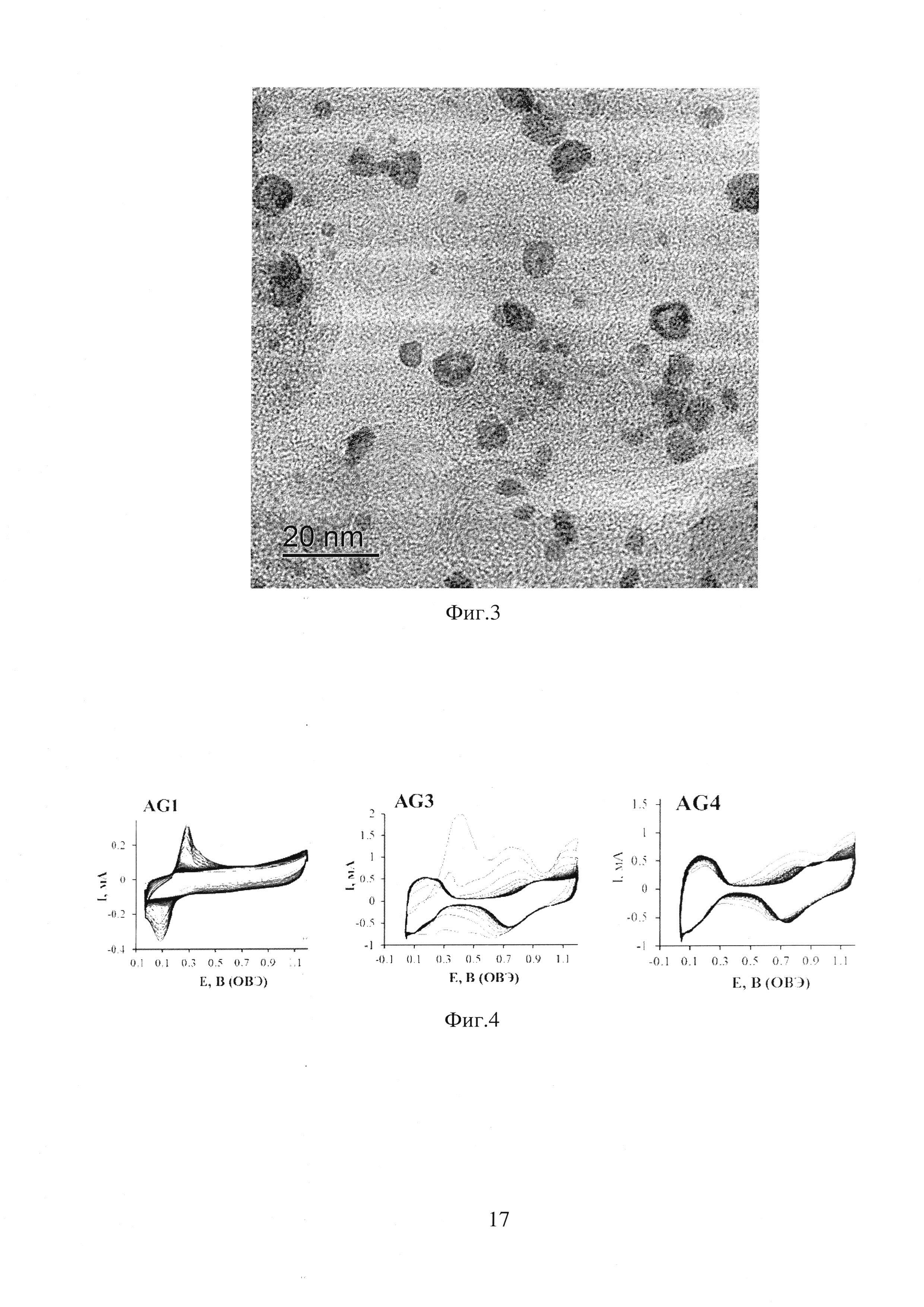
Фиг. 1 - Схема получения материалов заявляемым способом
Фиг. 2 - Рентгеновская дифрактограмма PtCu/C материала, полученного заявляемым способом.
Фиг. 3 - Фотографии микроструктуры, полученные методом просвечивающей электронной микроскопии, PtCu/C материалов.
Фиг.4 - Циклические вольтамперограммы промежуточных материалов (А-В) и конечного катализатора (Г).
Ниже приведены примеры реализации способа получения биметаллических катализаторов с градиентной структурой на основе платины.
Процесс химического восстановления ионов различных d-металлов на поверхности углеродного носителя и формирование ядра наночастиц, с последующим восстановлением ионов платины на поверхности ядер осуществлялся за счет внесения в реакционную смесь прекурсора платины и добавления восстановителя. Формирование наночастиц проводили в четыре стадии (Фиг. 1) путем последовательного добавления растворов соли d-металла и гексахлорплатиновой кислоты. Синтез Pt(d-металл)/С катализаторов проводили химическим восстановлением платины из раствора H2PtCl6⋅6H2O. В данном эксперименте использовали графитизированную углеродную сажу Vulcan ХС-72 (Cabot Corp., S(BET)=250-280 м2/г). В качестве восстановителей при проведении экспериментов использовали: боргидрид натрия в концентрации 1-6 г/дм3; гидразин в концентрации 5-20 г/дм3; муравьиную кислоту в концентрации 5-20 г/дм3; формальдегид в концентрации 5-20 г/дм3. В качестве солей d-металлов использовали: сульфат меди в концентрации 1-10 г/дм3; нитрат никеля в концентрации 1-10 г/дм3; нитрат кобальта в концентрации 1-10 г/дм3.
Пример 1.
Расчетный состав соотношения компонентов Pt : Cu - 1:1, массовая доля платины в образце 20%. На первой стадии высокодисперсный углеродный носитель (Vulcan ХС-72) в количестве 0,20 г помещают в химический стакан, к нему добавляют 70,0 мл этиленгликоля (ЭГ) и 40,0 мл бидистиллированной воды. Полученную смесь диспергируют ультразвуком в течение 5 минут. В полученную углеродную суспензию вносят заранее приготовленный раствор CuSO4⋅5H2O в количестве 24,7 мл, что составляет 50% от общего объема раствора сульфата меди (II) с концентрацией 0,00194 г соли в 1,0 мл данного раствора (соответствует 0,0078 М раствору). Далее путем добавления 6,0 мл раствора 0.5 М NaOH, приготовленного в смеси Н2О : ЭГ - 1:1, контролируя изменение по окраске индикаторной бумаги, доводят рН среды до значения 9 ч-10. Затем проводят восстановление ионов Cu2+, получая в результате суспензию Cu/С материала путем добавления к суспензии 0,20 М раствора боргидрида натрия в количестве 5,0 мл. Выдерживают суспензию в течение 30 минут на магнитной мешалке при температуре 22-24°С, полагая, что за это время происходит полное восстановление ионов меди (II).
На второй стадии, не прекращая перемешивание, вносят в раствор 1,8 мл H2PtCl6⋅6Н2О, что составляет 25% от общего объема раствора гексахлорплатиновой кислоты с концентрацией 0,0179 г соли в 1,0 мл данного раствора (соответствует 0,035 М раствору). Через 60 секунд добавляют к суспензии аликвоту раствора CuSO4⋅5Н2О в количестве 12,4 мл - 25% от общего объема раствора сульфата меди (II). Далее проводят восстановление ионов Cu(II) и Pt(IV), получая в результате суспензию PtCu/C материала путем добавления к суспензии 0,20 М раствора боргидрида натрия в количестве 3,5 мл. Выдерживают суспензию в течение 30 минут на магнитной мешалке при температуре 22-24°С, полагая, что за это время происходит полное восстановление ионов меди (II) и платины (IV).
На третьей стадии, не прекращая перемешивание, вносят в раствор 3,6 мл H2PtCl6⋅6Н2О, (25% от общего объема раствора гексахлорплатиновой кислоты) с концентрацией 0,0179 г соли в 1,0 мл данного раствора (соответствует 0,035М раствору). Через 60 секунд добавляют к реакционной смеси аликвоту раствора CuSO2⋅5H2O в количестве 12,4 мл - 25% от общего объема раствора сульфата меди (II). Далее проводят восстановление ионов Cu(II) и Pt(IV), получая в результате суспензию PtCu/C материала путем добавления к суспензии 0,20 М раствора боргидрида натрия в количестве 3,0 мл. Выдерживают суспензию в течение 30 минут на магнитной мешалке при температуре 22-24°С, полагая, что за это время происходит полное восстановление ионов меди (II) и платины (IV).
На четвертой стадии проводят формирование платиновой оболочки на наночастицах, сформированных на предыдущих стадиях. Для этого, не прекращая перемешивания, вносят в раствор 5,5 мл H2PtCl6⋅6H2O - 50% от общего объема раствора гексахлорплатиновой кислоты с концентрацией 0,0179 г соли в 1,0 мл данного раствора (соответствует 0,035 М раствору). Далее проводят восстановление ионов Pt(IV), путем добавления к суспензии 0,20 М раствора боргидрида натрия в количестве 4,0 мл. Выдерживают суспензию в течение 30 минут на магнитной мешалке при температуре 22-24°С, полагая, что за это время происходит полное восстановление ионов платины (IV). Далее отделяют, промывают и просушивают полученный материал в течение 12 часов в эксикаторе над окисью фосфора (V).
В ходе реализации представленного способа синтеза получаем PtCu/C материалы с составом металлической компоненты Pt : Cu. Массовая доля металлов в образце 29%, из которых 20% - массовая доля платины. Электрохимически активная площадь поверхности - 104 м2/г (Pt).
Пример 2. Процесс аналогичен приведенному в Примере 1, но отличается тем, что на первой стадии в суспензию добавляют прекурсор меди CuSO4⋅5H2O в количестве 12.5 мл с концентрацией 0.00194 г соли в 1.0 мл данного раствора, что соответствует 0.0078 М раствору. На второй и третьей стадиях добавляют 6,2 мл прекурсора меди. Таким образом получают образец с соотношением металлов Pt : 0.5Cu, с массовой долей металлов 24%, электрохимически активной площадью поверхности - 100 м2/г (Pt).
Пример 3. Аналогично Примеру 1, но отличается тем, что на второй, третьей и четвертой стадии добавляют к суспензии прекурсор платины в количестве 0.9, 1.8 и 2.7 мл соответственно. Таким образом, получаем PtCu/C материал с соотношение металлов 0.5 Pt : Cu, с массовой долей металлов 17%, электрохимически активной площадью поверхности - 120 м2/г (Pt).
Пример 4. Аналогично Примеру 1, но отличается тем, что уменьшают загрузку углеродного носителя до 0,1 г и всех вводимых веществ в два раза и таким образом получают образец с параметрами как в Примере 1.
Пример 5. Аналогично Примеру 1, но отличается тем, что в ходе приготовления суспензии на первой стадии синтеза добавляли этиленгликоль в количестве 50,0 мл, бидистиллированную воду в количестве 20,0 мл. Получают PtCu/C образец аналогичный, как в Примере 1 по составу, характеризующийся электрохимически активной площадью поверхности - 102 м2/г (Pt).
Пример 6. Аналогично Примеру 1, но отличается тем, что на каждой стадии после добавления восстановителя боргидрида натрия смесь выдерживают 20 минут, после этого приступают к проведению следующей стадии. Получают PtCu/C образец аналогичный, как в Примере 1 по составу, характеризующийся электрохимически активной площадью поверхности - 95 м2/г (Pt).
Пример 7. Аналогично Примеру 1, но отличается тем, что в ходе приготовления суспензии на первой стадии синтеза добавляли глицерин в количестве 60,0 мл, бидистиллированную воду в количестве 40,0 мл. Получают PtCu/C образец аналогичный, как в Примере 1 по составу, характеризующийся электрохимически активной площадью поверхности - 99 м2/г (Pt).
Пример 8. Аналогично Примеру 1, но отличается тем, что расчетная массовая доля платины в образце 30% и тем, что в ходе приготовления суспензии на первой стадии синтеза добавляли H2PtCl6⋅6H2O в количестве, необходимом для получения материала с расчетным составом Pt : Cu - 1:9. Получают PtCu/C образец аналогичный, как в Примере 1 по составу, характеризующийся электрохимически активной площадью поверхности - 86 м2/г (Pt).
Пример 9. Аналогично Примеру 7, но отличается тем, что на каждой стадии синтеза рН среды доводили до 10 насыщенным раствором аммиака. Получают PtCu/C образец аналогичный, как в Примере 1 по составу, характеризующийся электрохимически активной площадью поверхности - 87 м2/г (Pt).
Пример 10. Аналогично Примеру 1, но отличается тем, что вместо CuSO4⋅5H2O на каждой стадии использовали Со(NO3)2⋅6H2O, расчетный состав соотношения компонентов Pt : Co - 1:1, массовая доля платины в образце 30%. В ходе реализации представленного способа синтеза получаем PtCo/C материалы с составом металлической компоненты Pt : Co - 1:1,1. Массовая доля металлов в образце 38%, из которых 29% - массовая доля платины. Электрохимически активная площадь поверхности - 89 м2/г (Pt).
Пример 11. Аналогично Примеру 1, но отличается тем, что вместо CuSO4⋅5H2O на каждой стадии использовали Ni(NO3)2⋅6H2O, расчетный состав соотношения компонентов Pt : Ni - 1:1, массовая доля платины в образце 30%. В ходе реализации представленного способа синтеза получаем PtNi/C материалы с составом металлической компоненты Pt : Ni - 1:1. Массовая доля металлов в образце 38%, из которых 29% - массовая доля платины. Электрохимически активная площадь поверхности - 84 м2/г (Pt).
Пример 12. Аналогичен Примеру 11, но отличается тем, что на каждой стадии синтеза раствор непрерывно продували аргоном. Получают PtNi/C образец аналогичный, как в Примере 11 по составу, характеризующийся электрохимически активной площадью поверхности - 87 м2/г (Pt).
Приведенные выше примеры реализации предложенного способа подтверждают возможность получения биметаллических катализаторов с градиентной структурой на основе платины на поверхности углеродного носителя с заявленными характеристиками, а именно PtCu/C, PtCo/C и PtNi/C материалы с градиентной структурой, которые характеризуются массовой долей платины от 12 до 29%; массовой долей металлов от 17 до 38%; высокими значениями электрохимически активной площади поверхности от 84 до 120 м2/г (Pt) и небольшими размерами металлических наночастиц по данным РФА от 1,8 до 3,7 нанометров. Данный факт свидетельствует о высоком качестве получаемых катализаторов, которые характеризуются большей величиной активной площади поверхности и меньшим средним размером наночастиц, по сравнению с аналогами, что подтверждает эффективность предлагаемого подхода. Используемая методика позволяет получать биметаллические катализаторы, легированные различными d-металлами (Cu, Ni, Со), что показывает универсальность описанного подхода.
Результаты, полученные в приведенных примерах (Табл. 1), подтверждены исследованиями, выполненными на современном оборудовании по нижеприведенным методикам.
Массовую долю металлов в исследуемых образцах определяли методом гравиметрии.
Керамические тигли прокаливали до постоянной массы при 800-850°С и взвешивали после полного остывания 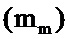 . Затем помещали в тигли 0,02 г Pt/C материала
. Затем помещали в тигли 0,02 г Pt/C материала  , сжигали навески в муфельной печи при 800-850°С в течении 40 минут. Взвешивали тигли с несгораемым остатком после полного остывания
, сжигали навески в муфельной печи при 800-850°С в течении 40 минут. Взвешивали тигли с несгораемым остатком после полного остывания 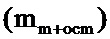 . По изменению массы определяли содержание металлов в образце, используя формулу:
. По изменению массы определяли содержание металлов в образце, используя формулу:
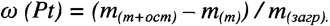
В материалах, содержащих биметаллические наночастицы, массовую долю металлов определяли методом термогравиметрии, с учетом окисления меди до оксида меди II.
Соотношение меди и платины в образцах определяли методом рентгенофлуоресцентного анализа на спектрометре РФС-001 с полным внешним отражением рентгеновского излучения. Диапазон определяемых химических элементов по периодической таблице Менделеева от А1 до U. Время экспозиции образцов - 300 сек. Регистрацию и обработку рентгеновских флуоресцентных спектров проводили с использованием программного обеспечения UniveRS.
Регистрацию рентгенограмм проводили на порошковом дифрактометре ARL X'TRA с геометрией по Бреггу-Брентано (θ-θ), CuKα - излучение (λ=0.15405618 нм) при комнатной температуре. Образцы тщательно перемешивали и помещали в кювету глубиной 1,5 мм или на бесфоновую подложку. Сьемку проводили в интервале углов 15-55 градусов с шагом 0,02 градуса и скоростью от 8 до 0,5 градусов в минуту, в зависимости от поставленной задачи. Средний размер кристаллитов металлической фазы рассчитывали по уравнению Шеррера для наиболее интенсивного пика (Фиг. 2). Отметим, что к размерам кристаллитов, рассчитанным по полуширине пика для PtCu/C материалов, следует относиться с осторожностью, поскольку этот пик фактически может представлять собой наложение отражений двух фаз на основе меди и платины, составляющих ядро и оболочку наночастиц.
Для изучения полученных материалов использовался метод порошковой дифракции. Для съемки ренгенограмм применялся порошковый дифрактометр ARL X'TRA с геометрией по Бреггу-Брентано (θ-θ), CuKα - излучение (λ=0.154056 нм) при комнатной температуре. Рентгенограммы исследуемых образцов записаны в интервале углов 5°≤20°≥90° методом пошагового сканирования с шагом перемещения детектора 0,02°.
Рентгенограммы обрабатывались программой SciDavis для корректного извлечения параметров пиков, что особенно важно при их перекрывании в случае малого размера частиц. Исходя из уравнения Вульфа-Брегга:
λ=2d⋅sinθ,
где d - межплоскостное расстояние (hk1), можно вывести формулу, в литературе известную как формулу Шеррера:
D=Kλ/(FWHM cosθ),
где λ - длина волны монохроматического излучения, 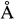 ; FWHM - полная ширина рефлекса на половине высоты (в радианах); K=0,89 - постоянная Шеррера; D - средняя толщина «стопки» отражающих плоскостей в области когерентного рассеяния,
; FWHM - полная ширина рефлекса на половине высоты (в радианах); K=0,89 - постоянная Шеррера; D - средняя толщина «стопки» отражающих плоскостей в области когерентного рассеяния, 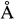 ; θ - угол падения пучка рентгеновского излучения (в радианах).
; θ - угол падения пучка рентгеновского излучения (в радианах).
Микроструктуру образцов изучали методом просвечивающей электронной микроскопии (Фиг. 3). Фотографии получали с помощью микроскопа JEM-2100 (JEOL, Japan) при напряжении 200 кВ и разрешении 0.2 нм. Для проведения измерений 0,5 мг катализатора помещали в 1 мл изопропанола и диспергировали ультразвуком, после чего наносили полученную суспензию на медную сетку, покрытую слоем аморфного углерода, и в течение 20 минут высушивали на воздухе при комнатной температуре.
При проведении цикловольтамперометрического исследования (Фиг. 4) использовали бипотенциостат AFCBP1 (PAIN). Для стандартизации поверхности платины и полного удаления примесей проводили 100 циклов развертки потенциала со скоростью 200 мВ/с в диапазоне потенциалов от 0 до 1 В (относительно СВЭ). Далее по площади пиков адсорбции и десорбции водорода проводили расчет количества электричества и оценку электрохимически активной площади поверхности платины, откуда следует, что количество электричества, затраченное на эти процессы, прямо пропорционально электрохимически активной площади поверхности платины.
При сравнении каталитической активности образцов в реакции восстановления кислорода, электролит насыщали кислородом в течении 40 минут, после чего снимали кислородные кривые при различных скоростях вращения электрода (400-2500 об/мин).
Используя зависимость Коутецкого - Левича для Pt/C катализаторов, находили значения кинетических параметров, полученных образцов:
1/i=l/iк+1/1д=1/iк+1/Bnω0,5,
В=0,62FD2/3υ-1/6c,
где i - ток на дисковом электроде, iк - кинетический ток, iд - диффузионный ток, ω - скорость вращения дискового электрода (рад/с), n - количество электронов, участвующих в электрохимической реакции, F - постоянная Фарадея (Кл/моль), D - коэффициент диффузии (см2/с), υ - кинематическая вязкость электролита (см2/с), с - концентрация кислорода в растворе.
Способ получения биметаллических катализаторов с градиентной структурой на основе платины, заключающийся в химическом восстановлении ионов d-металла на поверхности углеродного носителя и формировании ядра наночастиц, с последующим восстановлением ионов платины на поверхности ядер за счет внесения в реакционную смесь прекурсора платины и добавления восстановителя, отличающийся тем, что высокодисперсный углеродный носитель подвергают предварительной гомогенизации в ультразвуковом диспергаторе в вводном растворе этиленгликоля до получения устойчивой суспензии с площадью поверхности частиц не менее 50 м/г, с последующим четырехстадийным процессом восстановления d-металла из раствора солей с концентрацией 1-10 г/дм и ионов платины из гексахлорплатиновой кислоты, путем добавления на первой стадии 50%, на второй и третьей по 25% от общего объема раствора соли d-металла, и гексахлорплатиновой кислоты, в концентрации 11-30 г/дм, путем добавления на второй и третьей стадии по 25%, а на четвертой 50% от общего объема раствора гексахлорплатиновой кислоты, при избытке восстановительного агента и значении рН среды 9-10 в условиях постоянного перемешивания и температуры 22-24°С с последующей фильтрацией и высушиванием.